Изобретение представляет собой новый штамм Bacillus subtilis BN-135, относится к микробиологической отрасли и касается нового штамма - продуцента пектолитических ферментов, мацерирующих растительную ткань, а именно - пектат-лиазы и пектин-лиазы, и может быть использовано при получении ферментосодержащих лекарственных средств, применяемых для лечения и профилактики заболеваний, связанных с нарушениями процессов пищеварения, а также при получении препаратов, применяемых с целью увеличения выхода и улучшения качества овощных и фруктовых соков и пюре, плодово-ягодного осветленного вина, эфирных и растительных масел, чая, при обработке трудноусвояемых растительных кормов и получении биологических добавок для сельского хозяйства.
Современное направление диетологии основано на использовании в рационе человека свыше 2/3 растительных компонентов (овощи, фрукты, крупы) к общему объему потребляемой пищи. Это обуславливает создание лекарственных препаратов пищеварительного действия с включением ферментов, активно расщепляющих растительную ткань, не затрагивая при этом пищевых волокон и не образуя глюкозы.
Из литературных источников известно, что мацерирующий эффект растительной ткани максимально проявляется при сочетании комплекса ферментов пектолитического действия, таких как пектат-лиаза и пектин-лиаза, причем особая роль при мацерации растительной ткани отводится ферменту пектат-лиазе, который расщепляет негидролитическим путем пектиновые вещества, в том числе нерастворимый пектин - протопектин растительной ткани, составляющий основу межклеточных веществ и «цементирующий» растительную ткань, а фермент пектин-лиаза усиливает мацерирующее действие пектат-лиазы (Dean, M. Cell wall degradation by a pectate trans-eliminase / M. Dean, R.K.S. Wood // Natura. - 1967. - №214 - P. 408-410).
При этом растительная ткань распадается на отдельные клетки, образуя гомогенную легкоперевариваемую массу с сохранением пищевых волокон. При расщеплении протопектина увеличивается уровень растворимого пектина и образуются олигогалактурониды, которые так же, как и растворимый пектин, являются эффективными энтеросорбентами и выводят из организма соли тяжелых металлов и токсины. Кроме того, под действием фермента пектат-лиаза сохраняются микроцеллюлозные волокна, которые чрезвычайно полезны для нормализации перистальтики кишечника и очистки его от токсинов.
Потребность в данных ферментах вызвала необходимость изыскания сверхпродуктивных штаммов для получения высокоактивных препаратов мацерирующего действия, отличающихся не только высоким выходом целевого продукта, но и способностью к ферментации на недорогом и доступном сырье.
Для получения пектолитических ферментов в промышленности используют бактериальные и грибные продуценты.
Пектолитические ферменты, синтезируемые микроскопическими грибами, обладают оптимальной зоной действия в кислой среде при рН 3,0-5,5 и температуре 28-35°С и практически неактивны в щелочной среде.
Оптимум действия пищеварительных ферментов и получаемый на их основе лекарственный препарат должны проявлять свою активность в слабощелочной зоне рН, то есть при рН, характерном для тонкого кишечника, где происходят основные процессы переваривания пищевых нутриентов. К такой группе ферментов можно отнести пектат- и пектин-лиазы, синтезируемые бактериальными культурами и активно катализирующими деградацию пектина при рН 6,5-10,0 и температуре 35-45°С.
Кроме того, щелочные пектолитические ферменты мацерирующего действия бактериального происхождения могут применяться при обработке целлюлозы и в процессах переработки лубоволокнистых культур без нарушения механической прочности целлюлозы волокна в связи с тем, что ферментные препараты на их основе практически не содержат целлюлолитические ферменты. Нейтральные и слабощелочные пектолитические ферменты находят свое применение при обработке нейтральных овощей и фруктов с целью увеличения выхода и улучшения качества овощных и фруктовых соков и пюре, плодово-ягодного осветленного вина, для использования при обработке масличного сырья для повышения выхода эфирных и растительных масел, при обработке трудноусвояемых растительных кормов и получении биологических добавок для сельского хозяйства.
Для получения пектолитических ферментов известны аэробные и факультативно-анаэробные бактериальные продуценты.
Факультативно-анаэробные продуценты культивируют либо в условно-анаэробных условиях без перемешивания питательной среды, либо в аэробных условиях культивирования в погруженном состоянии при аэрации питательной среды. Аэробный процесс культивирования продуцентов является более технологичным.
Известен штамм факультативно-анаэробной бактерий Bacillus macerans ЦМПМ В-2692 - продуцент пектолитических ферментов (А.с. СССР №1162224. Штамм Bacillus macerans ЦМПМ В-2692 - продуцент пектолитических ферментов, 1984), который в условиях глубинного культивирования в аэробных условиях образует пектат-трансэлиминазу (по новой классификации ферментов - пектат-лиаза) с активностью 9000 ед./мл, эндополигалактуроназу с активностью 6,7 ед./мл, экзо-полигалактуроназу с активностью 5,3 ед./мл. Культивирование продуцента осуществляют на питательной среде, содержащей в качестве источника углерода свекловичный жом, при температуре 32-35°С, рН 6,8-7,2 в течение 18-20 ч.
Недостатками указанного штамма являются невысокая активность пектат-трансэлиминазы (пектат-лиазы) и отсутствие синтеза пектин-лиазы.
Известен штамм бактерий Bacillus macerans UV-21 (Патент РФ №2323974. Штамм бактерий Bacillus macerans bkm b-2419d - продуцент пектатлиазы, пектинлиазы и полигалактуроназы и комплекса щелочных карбогидраз, содержащих ксиланазу, бета-глюканазу, галактоманназу, арабиназу, ксилоглюканазу и амилазу, 2006) - который в аэробных условиях в погруженном состоянии при температуре 37-40°С, рН 7-8 в течение 24-48 часов на питательной среде, содержащей один или несколько субстратов - источников углерода, азота и других питательных веществ, в качестве которых могут быть использованы природные нерастворимые субстраты, например свекловичный жом, или частично растворимые субстраты - кукурузный экстракт или гидролизат крахмала, синтезирует через 36-48 часов культивирования пектат-лиазу с активностью 120-210 ед./мл, пектин-лиазу - с активность 12-18 ед./мл и комплекс щелочных карбогидраз - ксиланазу -10-18 ед./мл, глюканазу 12-15 ед./мл, арабиназу - 8-12 ед./мл, ксилоглюканазу 6-10 ед./мл и амилазу 15-25 ед./мл.
К недостаткам данного штамма следует отнести низкие активности мацерирующих ферментов - пектат-лиазы и пектин-лиазы в культуральной жидкости и длительный период культивирования продуцента.
Наиболее близким по технической сущности аналогом-прототипом к заявляемому штамму является аэробный штамм бактерий Bacillus subtilis ЦМПМ В-2691 - продуцент пектолитических ферментов (А.с СССР №1160742. Штамм Bacillus subtilis ЦМПМ В-2691 - продуцент пектолитических ферментов, 1985). Оптимальные условия культивирования: рН среды 8,1-8,3; температура 37-42°С. Продуцент синтезирует на питательной среде, содержащей свекловичный жом, пектолитические ферменты: пектат-трансэлиминазу (пектат-лиазу) - 7500 ед./мл, эндо-полигалактуроназу - 20 ед./мл, экзо-полигалактуроназу - 2,0 ед./мл за 18-20 часов культивирования.
Недостатками штамма являются низкая активность пектат-трансэлиминазы (пектат-лиазы) и отсутствие синтеза пектин-лиазы.
Целью изобретения является получение штамма бактерий Bacillus subtilis BN-135 - имеющего конститутивный характер синтеза мацерирующих ферментов и обладающего повышенным синтезом пектат-лиазы и пектин-лиазы на средах, содержащих в качестве источника углерода как пектиновые вещества, так и крахмалсодержащие субстраты, проявляющего высокие пектат-лиазную и пектин-лиазную активности по отношению к пектинам из разных источников.
Технический результат, который может быть получен при осуществлении изобретения, состоит в получении высокоактивного ферментного препарата мацерирующего действия, содержащего высокоактивные пектат-лиазу и пектин-лиазу, для применения в медицинской промышленности и других отраслях экономики.
Для достижения указанного технического результата предложено использовать штамм бактерий Bacillus subtilis BN-135 - высокоактивный продуцент пектолитических ферментов, мацерирующих растительную ткань - пектат-лиазы и пектин-лиазы, а для культивирования продуцента использовать доступное и дешевое сырье.
Заявляемый штамм Bacillus subtilis BN-135 выделен в результате многократного рассева на агаризованной среде при росте в аэробных условиях исходного штамма Bacillus subtilis ЦМПМ В-2691 и выделения моноспоровых вариантов. Варианты, отобранные на чашках, проверяли на продуктивность синтеза пектат-лиазы и пектин-лиазы при культивировании в жидкой среде в колбах в условиях активного аэрирования.
Штамм бактерий Bacillus subtilis BN-135 депонирован во Всероссийской Коллекции Промышленных Микроорганизмов ФГУПГосНИИГенетика под №ВКПМВ-11964.
Условия хранения. Штамм может храниться в лиофилизированном состоянии в течение нескольких лет и/или на косяках с картофельным агаром при +4°С при обязательных пересевах не реже одного раза в течение 3-6 месяцев.
Штамм бактерий Bacillus subtilis BN-135 имеет следующие культурально-морфологические и физиологические признаки.
Культурально-морфологические признаки.
Клетки прямые, палочковидные, 2,0-5,0×0,9-1,0 мкм, подвижные, грамположительные, встречаются в длинных и коротких цепочках. Споры эллипсоидальные, без экзоспориума, 2,0-2,4×1,0-1,2 мкм, расположены центрально или субтерминально.
На картофельном агаре: рост хороший, колонии светло-бежевые, круглые, блестящие, края ровные, размер колоний от 4 до 11 мм в диаметре. Пигмент в среду не диффундирует.
На сусле-агаре: колонии светло-бежевые, круглые, блестящие, с более светлой и плотной, чуть выпуклой серединой, края ровные, размер колоний от 2 до 6 мм.
На среде Чапека с глюкозой: колонии однородные, выпуклые молочно-белого цвета, блестящие, прозрачные, края ровные, рост обильный, размер колоний от 2 до 5 мм.
На мясопептонном агаре: рост слабый, колонии точечные, бежевые.
Физиолого-биохимическая характеристика штамма
Отношение к углеводам: усваивает глюкозу, сахарозу, ксилозу, арабинозу, мальтозу и маннит с образованием кислоты и газа, гидролизует крахмал.
Образует каталазу, ацетон, кристаллические декстрины. Нитраты редуцирует в нитриты. Фенилаланин не дезаминирует, тирозин не расщепляет. Аммиак и сероводород не образует. Гиппураты не гидролизует. Желатин разжижает на 1 см в верхней части. Молоко пептонизирует с образованием сгустка и газа. Растет на среде с 0,001% лизоцимом, не растет на среде с 5% хлористым натрием.
Хорошо растет на ломтиках моркови, картофеля, репы, капусты белокочанной, кабачка, тыквы, яблока (некислых сортов), груши с полной мацерацией субстрата; на гидролизованном крахмале, различных видах зерновой муки.
Отношение к кислороду - аэроб. Минимальная температура роста +10°С, максимальная +45°С, оптимальная 37-42°С, рН 6,8-7,6.
Данный вид бактерий не числится в качестве патогенного в санитарно-эпидемиологических правилах СП 1.3.2322-08/СП 1.3.2518-09 «Безопасность работы с микроорганизмами III-IV групп патогенности (опасности) и возбудителями паразитарных болезней».
Полученный штамм Bacillus subtilis BN-135 по своим морфологическим признакам при росте на картофельном агаре отличается от исходного штамма Bacillus subtilis ЦМПМ В-2691 большим размером колоний и более поздним вступлением в стадию спорообразования.
Полученный штамм по своим биохимическим свойствам в отличие от исходного штамма имеет конститутивный характер синтеза пектат-лиазы и пектин-лиазы, отличается от исходного повышенной потребностью к кислороду и повышенной способностью к биосинтезу ферментов при глубинном культивировании в аэробных условиях на жидких питательных средах, содержащих в качестве источника углеродного питания как пектиновые вещества, так и крахмалсодержащие субстраты.
Культивирование штамма Bacillus subtilis BN-135 проводят в аэробных условиях в погруженном состоянии при температуре 37-42°С, рН 6,8-7,6 в течение 18-24 часов.
Активность пектат-лиазы определяли по способности расщеплять пектины низкой степени этерификации: свекловичный - со степенью этерификации 35-37% и цитрусовый - со степенью этерификации 20-34%, пектин-лиазы - по способности расщеплять пектины высокой степени этерификации: яблочный - со степенью этерификации 70% и цитрусовый - со степенью этерификации 66%. За единицу активности принято такое количество фермента, которое за 1 час при 40°С и рН 8,4 вызывает образование ненасыщенных продуктов деградации пектина, увеличивающих оптическую плотность на 0,1. Метод основан на прямом спектрофотометрическом определении ненасыщенных продуктов распада пектина, имеющих максимальную оптическую плотность в спектре при длине волны 235 нм, в кварцевых кюветах с толщиной поглощающего слоя 10 мм.
Определение мацерирующей способности проводили по тесту, основанному на определении изменения массы растительного субстрата в результате действия ферментного препарата, полученного из культуральной жидкости заявляемого продуцента, в количестве 450 единиц пектат-лиазы на 1 г субстрата в течение 4 часов. В качестве растительного субстрата использовали измельченную морковь в трис-солянокислом буфере с рН-8,4. Степень мацерации моркови определяли по уменьшению массы обработанного ферментом субстрата по сравнению к контрольным вариантам и выражали в процентах.
Возможность использования изобретения иллюстрируется примерами, которые не ограничивают объем и сущность притязаний, связанных с ним.
Пример 1
Культуру Bacillus subtilis BN-135 выращивали в колбах на жидкой питательной среде следующего состава, г/л:
Питательную среду разливали по 50 мл в качалочные колбы вместимостью 750 мл и стерилизовали при давлении 0,1 МПа в течение 45 мин. В качестве посевного материала использовали водную суспензию спор штамма Bacillus subtilis BN-135, которые образуются на поверхности скошенного картофельного агара после инокулирования и выращивания в течение 48 ч при 40°С, в количестве 5% к объему питательной среды. рН среды перед культивированием устанавливали на уровне 7,0 с помощью растворов соляной кислоты или едкого калия. Культивирование проводили в аэробных условиях на качалке с частотой вращения 200-220 об/мин, температуре 40°С и в течение 18 ч.
Пример 2
Культуру Bacillus subtilis ЦМПМ В-2691 (прототип) выращивали на питательной среде и в условиях, соответствующих примеру 1.
Пример 3
Культуру Bacillus subtilis BN-135 выращивали в течение 20 часов в условиях, соответствующих условиям примера 1. Состав питательной среды отличался от состава примера 1 содержанием ржаной муки в количестве 25 г/л вместо свекловичного жома.
Пример 4
Культуру Bacillus subtilis ЦМПМ В-2691 (прототип) выращивали в течение 24 часов на питательной среде и в условиях, соответствующих примеру 3.
Пример 5
Культуру Bacillus subtilis BN-135 выращивали в течение 22 часов в условиях, соответствующих условиям примера 1. Состав питательной среды отличался от состава примера 1 содержанием ячменной муки в количестве 25 г/л вместо свекловичного жома.
Пример 6
Культуру Bacillus subtilis ЦМПМ В-2691 (прототип) выращивали в течение 24 часов на питательной среде и в условиях, соответствующих условиям примера 5.
По окончании культивирования продуцента проводили определение активности ферментов в центрифугате, полученном при центрифугировании культуральной жидкости при 10000 об/мин в течение 10 минут.
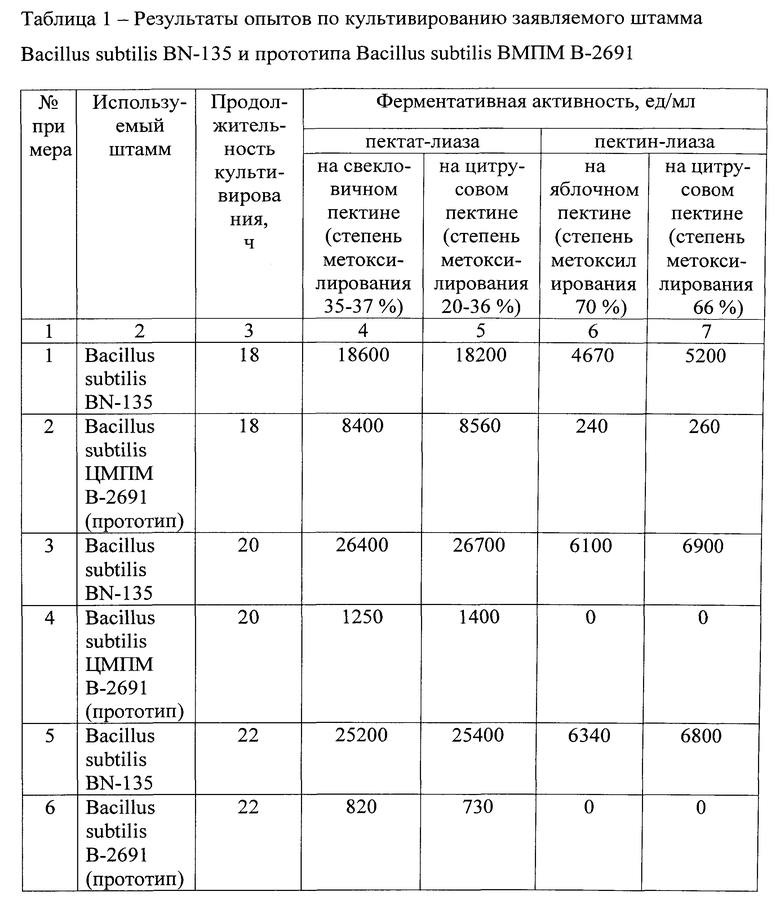
Данные результатов опытов по культивированию заявляемого штамма и прототипа представлены в таблице 1.
Для определения мацерирующей способности по окончании процесса ферментации получали сухие ферментные препараты из культуральных жидкостей заявляемого штамма и прототипа, полученных на питательной среде с использованием свекловичного жома (пример 1, 2), и препараты заявляемого штамма, полученные с использованием ржаной муки (пример 3) и ячменной муки (пример 5). Для этого культуральную жидкость отделяли от биомассы центрифугированием, а центрифугат концентрировали методом ультрафильтрации на мембране УПМ-50 с размером пор 50000 Да и сушили на лиофильной сушилке. Полученные препараты использовали для мацерации моркови.
Ферментативные активности полученных препаратов и мацерирующая способность моркови представлены в таблице 2.
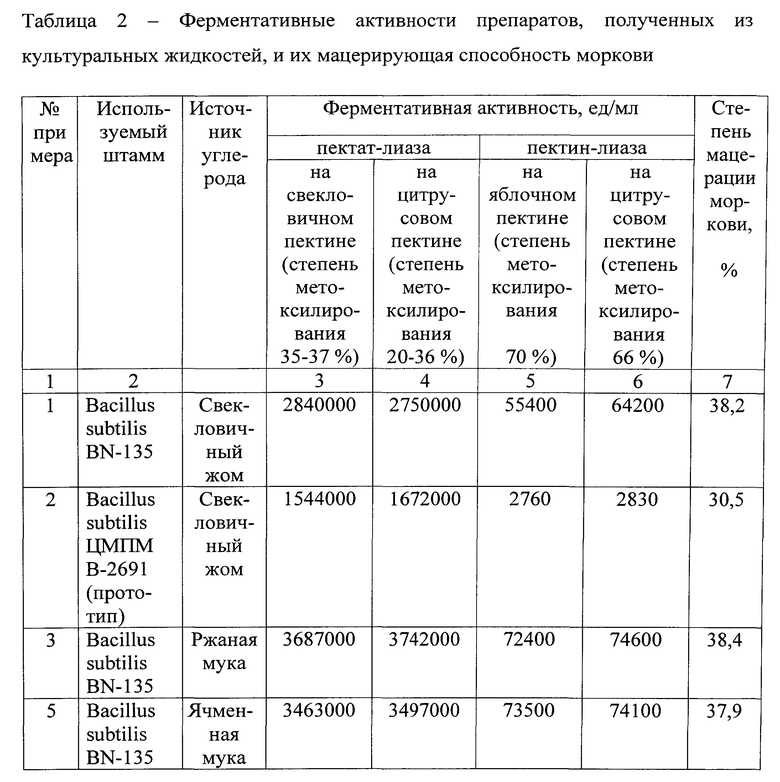
Степень мацерации моркови препаратами заявляемого штамма была близка и составила: с использованием свекловичного жома - 38,2%, с использованием ржаной муки - 38,4%, с использованием ячменной муки -37,9%. Степень мацерации моркови препаратом, полученным из культуральной жидкости прототипа с использованием свекловичного жома, была ниже и составила 30,5%.
Таким образом, использование заявляемого штамма Bacillus subtilis BN-135 по сравнению с прототипом имеет следующие преимущества:
1. Повышенный синтез пектат-лиазы - до 18600 ед./мл (в прототипе до 8560 ед./мл) на питательной среде, содержащей свекловичный жом, и до 26700 ед./мл на питательной среде, содержащей крахмалсодержащий субстрат (в прототипе до 1400 ед./мл).
2. Высокий синтез пектин-лиазы - до 5200 ед./мл (в прототипе -до 260 ед./мл) на питательной среде, содержащей свекловичный жом, и до 6900 ед./мл, на питательной среде, содержащей крахмалсодержащий субстрат (в прототипе - отсутствует).
3. Более высокую мацерирующую активность растительного сырья (моркови).
Заявляемый штамм Bacillus subtilis BN-135 в отличие от прототипа имеет конститутивный характер синтеза ферментов, мацерирующих растительную ткань - пектат-лиазы и пектин-лиазы, обладает способностью синтеза пектат-лиазы и пектин-лиазы на питательных средах, содержащих в качестве источника углерода как пектиновые вещества, так и крахмалсодержащие субстраты, имеет высокую активность по отношению к пектинам из разных источников, а препараты, полученные с использованием заявляемого штамма, обладают более высокой мацерирующей способностью.
Для достижения высокой активности штамма не требуется применения сложных и дорогих питательных сред, что позволит при его промышленном использовании получать высокоактивные препараты мацерирующего действия, содержащие пектат-лиазы и пектин-лиазы, для применения в медицинской промышленности, а также в пищевой промышленности и сельском хозяйстве.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ БАКТЕРИЙ BACILLUS SUBTILIS BN-135- ПРОДУЦЕНТА ПЕКТАТ-ЛИАЗЫ | 2014 |
|
RU2571945C1 |
| ШТАММ БАКТЕРИИ BACILLUS MACERANS BS-04 - ПРОДУЦЕНТ ПЕКТИНАЗ, ПРОТЕАЗЫ, КСИЛАНАЗЫ И АМИЛАЗЫ | 2004 |
|
RU2272838C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТНЫХ ПРЕПАРАТОВ МАЦЕРИРУЮЩЕГО ДЕЙСТВИЯ | 1991 |
|
RU2035506C1 |
| ШТАММ БАКТЕРИЙ BACILLUS MACERANS BKM B-2419D - ПРОДУЦЕНТ ПЕКТАТЛИАЗЫ, ПЕКТИНЛИАЗЫ И ПОЛИГАЛАКТУРОНАЗЫ И КОМПЛЕКСА ЩЕЛОЧНЫХ КАРБОГИДРАЗ, СОДЕРЖАЩЕГО КСИЛАНАЗУ, БЕТА-ГЛЮКАНАЗУ, ГАЛАКТОМАННАНАЗУ, АРАБИНАЗУ, КСИЛОГЛЮКАНАЗУ И АМИЛАЗУ | 2006 |
|
RU2323974C1 |
| Питательная среда для глубинного культивирования продуцентов пектолитических ферментов | 1981 |
|
SU1017728A1 |
| Питательная среда для культивирования продуцента мацерирующих ферментов @ @ -31 | 1983 |
|
SU1116058A1 |
| Штамм @ @ 2-82-продуцент пектат-лиазы | 1983 |
|
SU1161551A1 |
| Способ получения пектолитического ферментного препарата | 1977 |
|
SU622838A1 |
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОГО ФЕРМЕНТНОГО ПРЕПАРАТА ПЕКТИН-ЛИАЗЫ | 2002 |
|
RU2252959C2 |
| Штамм -67продуцент комплекса пектолитических ферментов | 1975 |
|
SU535347A1 |
Изобретение относится к микробиологической промышленности. Предложен штамм бактерии Bacillus subtilis ВКПМ B-11964 - высокоактивный продуцент пектолитических ферментов, мацерирующих растительную ткань. Данный штамм проявляет высокие пектат-лиазную и пектин-лиазную активности по отношению к пектинам из разных источников. 2 табл., 5 пр.
Штамм бактерии Bacillus subtilis ВКПМ B-11964 - высокоактивный продуцент пектолитических ферментов, мацерирующих растительную ткань.
| ШТАММ БАКТЕРИЙ BACILLUS MACERANS BKM B-2419D - ПРОДУЦЕНТ ПЕКТАТЛИАЗЫ, ПЕКТИНЛИАЗЫ И ПОЛИГАЛАКТУРОНАЗЫ И КОМПЛЕКСА ЩЕЛОЧНЫХ КАРБОГИДРАЗ, СОДЕРЖАЩЕГО КСИЛАНАЗУ, БЕТА-ГЛЮКАНАЗУ, ГАЛАКТОМАННАНАЗУ, АРАБИНАЗУ, КСИЛОГЛЮКАНАЗУ И АМИЛАЗУ | 2006 |
|
RU2323974C1 |
| Автоматическая масленка для крейцкопфов | 1928 |
|
SU10676A1 |
| ШТАММ БАКТЕРИИ BACILLUS MACERANS BS-04 - ПРОДУЦЕНТ ПЕКТИНАЗ, ПРОТЕАЗЫ, КСИЛАНАЗЫ И АМИЛАЗЫ | 2004 |
|
RU2272838C1 |
| CN 102660526 A, 12.09.2012 | |||
Авторы
Даты
2015-07-10—Публикация
2014-09-10—Подача