Предлагаемое изобретение относится к области органического синтеза, в частности к способу получения триамантана.
Полициклические каркасные углеводороды триамантанового ряда представляют большой интерес для получения фармацевтических препаратов [[1]. Патент EP №1994927 A1. Diamondoid derivatives possessing therapeutic activity in the treatment of viral disorders / Kong D., Lam F.W., Sciamanna S.F., Shelton E., Yu C.-Y., Carlton R.M., Liu S. Date of publication 26.11.2008; [2]. Fokin A.A., Merz A., Fokina N.A., Schwertfeger H., Liu S.L., Dahl J.E.P., Carlson R.K.M., Schreiner P.R. Synthetic Routes to Aminotriamantanes, Topological Analogues of the Neuroprotector Memantine // Synthesis. - 2009. - №6. - Р.909-912.], материалов для микроэлектроники [[3]. Заявка WO №2004010512 A2. Heteroatom-containing diamondoid transistors / Liu S., Dahl J.E., Carlson R.M. Int. Publication Date 29.01.2004.] и нелинейной оптики [[4]. Заявка WO №9511472 A1. Fiber optic cable and viscous filler material / Ashjian H., Shen D.-M., Wu M.M.-S. Int. Publication Date 27.04.1995.].
Основным способом синтеза триамантана (1) в лаборатории является скелетная изомеризация изосоставных (C18H24) углеводородов под действием кислотных катализаторов, в качестве которых используются кислоты Льюиса (AlCl3, AlBr3) и суперкислоты (B(OSO2CF3)3, CF3SO3H), а также Pt-содержащие катализаторы. Так, в работе [[5]. Williams V.Z., Schleyer Jr., P. v. R., Gleicher G.J., Rodewald L.B. Triamantane // J. Am. Chem. Soc. - 1966. - V.88. - №16. - P.3862-3863] приводится синтез триамантана (1) по следующей схеме:

Димер циклооктатетраена (2) циклопропанируют по Симмонсу-Смиту. Гидрогенолизом (3) получают углеводород, имеющий состав C18H24 (3а). Последующая изомеризация циклического углеводорода (3а) над бромидом алюминия в среде сероуглерода приводит к триамантану (1) с очень низким выходом (2-5%).
Недостатки метода:
1) циклооктатетраен и его димер (2) являются труднодоступными соединениями;
2) низкий выход триамантана;
3) продолжительность изомеризации составляет 4-6 дней;
4) необходимость использования избытка AlBr3;
5) реакция проводится в ядовитом и взрывоопасном сероуглероде;
6) высокое давление для гидрирования.
В литературе известен пример синтеза триамантана (1) из 1-диамантанкарбоновой кислоты (4) [[6]. Burns W., McKervey M.A., Rooney J.J. New Synthesis of Triamantane Involving a Novel Rearrangement of a Polycyclic Olefin in the Gas Phase on Platinum // J. Chem. Soc., Chem. Commun. - 1975. - V.24. - P.965-966]. Полный синтез (1) состоит из 6 стадий, наиболее сложной из них является шестая, суть которой заключается в перегруппировке и деметилировании олефина (5) в триамантан (1). Реакция проводится в атмосфере водорода в присутствии катализатора платины при 430°C. Выход триамантана (1) после перекристаллизации из ацетона составляет 30%.

Недостатки метода:
1) многостадийность (6 стадий);
2) требуются труднодоступные дорогостоящие реагенты;
3) на стадии этерификации применяется взрывоопасный диазометан;
4) жесткие условия гидрирования, изомеризации и деметилирования (430°C).
Наиболее удобный и эффективный способ синтеза триамантана (1) основан на скелетной изомеризации C18H24-углеводородов, полученных из [4π+4π]-димера норборнадиена бинора-S (6). Так, в работах [[7]. Hamilton R., McKervey М.А., Rooney J.J., Malone J.F. Gas-phase Reactions on Platinum. A Short Synthesis of Triamantane // J. Chem. Soc., Chem. Commun. - 1976. - V.24. - P.1027-1028; [8]. Hollowood F.S., McKervey М.А. Synthesis of Triamantane // J. Org. Chem. - 1980. - V.45. - №24. - P.4954-4958] был осуществлен синтез исходных соединений - углеводородов (7, 8) по следующей схеме:

Последующая изомеризация (7, 8) в присутствии AlCl3 приводит к триамантану (1) с выходом 60%.
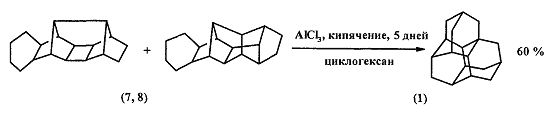
Недостатки метода:
1) значительная продолжительность реакции (5 дней);
2) в качестве катализатора используется чувствительный к влаге безводный AlCl3;
3) умеренный выход триамантана (1).
По другому способу изомеризацию полициклических углеводородов (7, 8) проводили под действием суперкислот, таких как: B(OSO2CF3)3 (0°C, фреон-113, 74 ч, выход (1) 70%), CF3SO3H-SbF5 (0°C, фреон-113, 74 ч, выход (1) 71%), CF3SO3H-B(OSO2CF3)3 (0°C, фреон-113, 74 ч, выход (1) 69%) [[9]. Farooq O., Farnia S.M.F., Stephenson M., Olah G.A. Superacid-Catalyzed Near-Quantitative Isomerization of C4n+6H4n+12 (n=1-3) Polycyclic Precursors to Diamondoid Cage Hydrocarbons Promoted by 1-Haloadamantanes and Sonication // J. Org. Chem. - 1988. - V.53. - №12. - P.2840-2843].
Недостатки метода:
1) изомеризация проводится при низкой температуре (0°C);
2) продолжительность реакции составляет 74 часа;
3) в качестве растворителя используется озоноразрушающий реагент - фреон-113.
В работе [[10]. Olah G.A., Wu A., Farooq O., Prakash G.K.S. Single-Step Reductive Isomerization of Unsaturated Polycyclics to C4n+6H4n+12 Diamondoid Cage Hydrocarbons with Sodium Borohydride / Triflic Acid1 // J. Org. Chem. - 1989. - V.54. - №6. - Р.1450-1451] разработан прямой метод синтеза триамантана (1) из олефинов (9, 10).
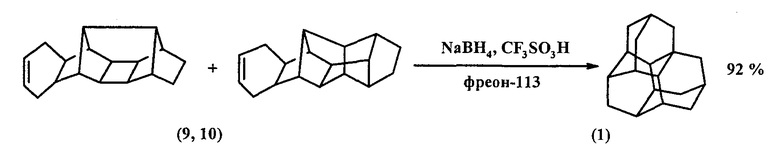
К охлажденной до -30°C смеси олефинов (9, 10) (7.6 ммоль) и NaBH4 (22.8 ммоль) в сухом фреоне-113 прикапывают в течение 30 мин в токе аргона или азота 12 мл CF3SO3H (137 ммоль). При этом реакционную массу охлаждают до -78°C. После добавления расчетного количества CF3SO3H температуру медленно доводят до комнатной (3-5 ч), после чего реакционную массу выдерживают еще 18 ч. По окончании синтеза реакционную массу охлаждают на ледяной бане, экстрагируют CH2Cl2 и сушат над безводным Na2SO4. Выход (1) 92%.
Недостатки метода:
1) реакция проводится при пониженной температуре (-78°C);
2) необходим большой избыток дорогостоящего, взрыво- и пожароопасного боргидрида натрия NaBH4;
3) продолжительность реакции составляет 18 ч;
4) в качестве растворителя используется озоноразрушающий реагент - фреон-113.
Авторами предлагается способ скелетной изомеризации C18H24 угеводородов (7, 8) в триамантан (1), не имеющий вышеперечисленных недостатков.
Задачей предлагаемого изобретения является удешевление себестоимости триамантана (1) за счет использования доступных катализаторов, увеличения выхода и упрощения технологии в целом.
Сущность предлагаемого способа заключается в изомеризации полициклических углеводородов состава C18H24, полученных из гептациклического димера норборнадиена - бинора-S, гептацикло[8.8.0.02,17.03,11.04,9.012,16.013,18]октадекан (7) и гептацикло[8.8.0.02,13.03,11.04,9.012,17.014,18]октадекан (8) (получены по методике [8]. Hollowood F.S., McKervey M.A. Synthesis of Triamantane // J. Org. Chem. - 1980. - V.45. - №24. - P.4954-4958.) под действием неорганических ионных жидкостей состава 2AlCl3+Et3N·HCl или 2.5AlCl3+Et3N·HCl при температуре 20-50°C в течение 2-72 ч при мольном соотношении реагентов (7, 8):[ионная жидкость]=1:2-4. Реакции проводили в реакторе под аргоном.
Установлено, что максимальный выход триамантана (1) (80%) в присутствии указанных ионных жидкостей наблюдается при T=50°C, за 8 ч при мольном соотношения реагентов: (7, 8):[2AlCl3+Et3N·HCl]=1:4.

Ионная жидкость состава 2.5AlCl3+Et3N·HCl проявляет меньшую каталитическую активность. В условиях: 50°C, 8 ч выход триамантана (1) в присутствии 2.5AlCl3+Et3N·HCl не превышает 40%.
Роль ионных жидкостей в данной реакции двоякая: они служат катализаторами и реакционной средой. Использование растворителей нежелательно, так как при добавлении растворителя (гексан, хлористый метилен) выход триамантана (1) снижается до 10%.
Преимущества предлагаемого метода:
1) высокий выход триамантана (1) - 80%;
2) мягкие условия реакции (50°C, 8 ч);
3) изомеризация проводится без растворителя;
4) доступность и дешевизна катализатора.
Предлагаемый способ поясняется примерами.
ПРИМЕР 1. В реактор (V=50 мл) под аргоном помещали 0.38 г (1,5 ммоль) смеси углеводородов C18H24 (7, 8) и 2.58 г (6 ммоль) ионной жидкости 2AlCl3+Et3N·HCl. Реакцию проводили при постоянном перемешивании в течение 8 ч при 50°C. Затем реактор охлаждали до комнатной температуры, реакционную массу экстрагировали петролейным эфиром и фильтровали через слой силикагеля (элюент - петролейный эфир). Растворитель отгоняли, остаток перекристаллизовывали из смеси этилацетат:циклогексан = 1:1. Выход триамантана (1) составляет 80%.
Выделенный триамантан (1) имел Тпл 221-221.5°C. (221°C [[11]. Гордадзе Г.Н., Геохимия углеводородов каркасного строения // Нефтехимия. - 2008. - Т.48. - №4. - С.243-255.]).
Спектр ЯМР 1H (CDCl3, δ, м.д., J/Гц) [[5]. Williams V.Z., Schleyer Jr., P. v. R., Gleicher G.J., Rodewald L.B. Triamantane // J. Am. Chem. Soc. - 1966. - V.88. - №16. - P.3862-3863]: 1.28 м, 1.49 м, 1.66 м, 1.68-1.75 м, 1.86 м.
Спектр ЯМР 13C (CDCl3, δ, м.д.) [[12]. Dheu M.-L., Gagnaire D., Duddeck H., Hollowood F., McKervey M.A. 13C Nuclear Magnetic Resonance Spectra. Part 9. Strain Effects on 13C Chemical Shifts of Triamantane // J. Chem. Soc. Perkin Trans II. - 1979. - P.357-359.]: 27.89, 33.62, 35.34, 38.19, 38.21, 38.65, 45.44, 47.01.
Масс-спектр (ЭУ, 70 эВ), m/z (Iотн (%)): 240.15 [M]+ (100.00), 239.15 (43.74), 143.10 (8.00), 131.10 (5.64), 129.10 (10.20), 128.10 (5.01), 117.10 (6.07), 115.10 (5.01), 105.10 (6.77), 91.05 (20.72), 79.05 (10.60), 77.05 (8.95).
Другие примеры, подтверждающие способ, приведены в таблице 1.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения диамантана (пентацикло [7.3.1.1 .0 .0]тетрадекана) | 2020 |
|
RU2771230C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАМАНТАНА (ПЕНТАЦИКЛО[7.3.1.1.0.0]ТЕТРАДЕКАНА) | 2017 |
|
RU2645914C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАМАНТАНА (ПЕНТАЦИКЛО[7.3.1.1.0.0]ТЕТРАДЕКАН) | 2011 |
|
RU2459794C1 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСИ ГЕКСАЦИКЛО[8.4.0.0.0.0.0]ТЕТРАДЕЦЕНА-5 И ГЕКСАЦИКЛО[6.6.0.0.0.0.0]ТЕТРАДЕЦЕНА-3 | 2008 |
|
RU2373177C2 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСИ ГЕКСАЦИКЛО[8.4.0.0.0.0.0]ТЕТРАДЕЦЕНА-5 И ГЕКСАЦИКЛО[6.6.0.0.0.0.0]ТЕТРАДЕЦЕНА-3 | 2008 |
|
RU2375341C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ДИМЕТИЛАДАМАНТАНА | 2012 |
|
RU2504533C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНТАЦИКЛО [8.2.1.1.0. 0] ТЕТРАДЕКАНДИОЛА-6,9 | 1998 |
|
RU2139847C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНТА- И ГЕКСАЦИКЛИЧЕСКИХ КАРКАСНЫХ УГЛЕВОДОРОДОВ | 1996 |
|
RU2151761C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОХЛОРЗАМЕЩЕННЫХ ПРОИЗВОДНЫХ АДАМАНТАНА И ДИАМАНТАНА | 1996 |
|
RU2125552C1 |
| СПОСОБ ПОЛУЧЕНИЯ 10-ГИДРОКСИГЕКСАЦИКЛО[9.2.1.0.0.0.0] ТЕТРАДЕКАНА(ГЕКСАЦИКЛОТЕТРАДЕКАНОЛА-10) | 1998 |
|
RU2135455C1 |
Изобретение относится к способу получения триамантана формулы I. Способ характеризуется тем, что полициклические углеводороды состава C18H24, полученные из гептациклического димера норборнадиена - бинора-S, гептацикло[8.8.0.02,17.03,11.04,9.012,16.013,18]октадекан и гептацикло[8.8.0.02,13.03,11.04,9.012,17.014,18]октадекан, подвергают скелетной изомеризации в присутствии ионных жидкостей состава 2AlCl3+Et3N·HCl или 2.5AlCl3+Et3N·HCl при температуре 20-50°C в течение 2-72 ч при мольном соотношении реагентов [углеводороды (C18H24)]:[ионная жидкость]=1:2-4, в атмосфере аргона. Способ использует доступные катализаторы и позволяет увеличить выход целевого соединения и упростить технологию в целом. 1 табл., 9 пр.
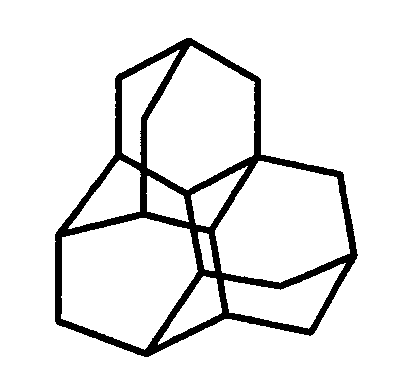 I.
I.
Способ получения триамантана формулы

отличающийся тем, что полициклические углеводороды состава C18H24, полученные из гептациклического димера норборнадиена - бинора-S, гептацикло[8.8.0.02,17.03,11.04,9.012,16.013,18]октадекан и гептацикло[8.8.0.02,13.03,11.04,9.012,17.014,18]октадекан, подвергают скелетной изомеризации в присутствии ионных жидкостей состава 2AlCl3+Et3N·HCl или 2.5AlCl3+Et3N·HCl при температуре 20-50°C в течение 2-72 ч при мольном соотношении реагентов [углеводороды (C18H24)]:[ионная жидкость]=1:2-4 в атмосфере аргона.
| HOLLOWOOD F.S., MCKERVEY М.А., SYNTHESIS OF TRIAMANTANE, J | |||
| ORG | |||
| CHEM., 1980, V.45, N24, P.4954-4958 | |||
| FAROOQ O | |||
| ET AL, SUPERACID-CATALYZED NEAR-QUANTITATIVE ISOMERIZATION OF C4N+6H4N+12 (N=1-3) POLYCYCLIC PRECURSORS TO DIAMONDOID CAGE HYDROCARBONS PROMOTED BY 1-HALOADAMANTANES AND SONICATION, J | |||
| ORG | |||
| CHEM., 1988, V.53, N12, P.2840-2843 | |||
| WO 1995006019 A1, 02.03.1995 | |||
| Способ получения адамантана | 1981 |
|
SU1032728A1 |
Авторы
Даты
2015-08-10—Публикация
2014-04-08—Подача