Изобретение относится к области нанотехнологий и может быть использовано в фармакологии, фармацевтике, медицине.
Из уровня техники известны различные способы получения микрокапсул.
Например, в патенте РФ №2173140 (МПК А61К 009/50, А61К 009/127, опубликован 10.09.2001) предложен способ получения кремнийорганолипидных микрокапсул с использованием роторно-кавитационной установки, обладающей высокими сдвиговыми усилиями и мощными гидроакустическими явлениями звукового и ультразвукового диапазона для диспергирования.
Недостатком данного способа является применение специального оборудования - роторно-кавитационной установки, которая обладает ультразвуковым действием, что оказывает влияние на образование микрокапсул и при этом может вызывать побочные реакции в связи с тем, что ультразвук разрушающе действует на полимеры белковой природы, поэтому предложенный способ применим при работе только с полимерами синтетического происхождения.
В патенте РФ №2359662 (МПК А61К 009/56, A61J 003/07, B01J 013/02, A23L 001/00, опубликован 27.06.2009) предложен способ получения микрокапсул хлорида натрия с использованием распылительного охлаждения в распылительной градирне Niro при следующих условиях: температура воздуха на входе 10°C, температура воздуха на выходе 28°C, скорость вращения распыляющего барабана 10000 оборотов/мин. Микрокапсулы по изобретению обладают улучшенной стабильностью и обеспечивают регулируемое и/или пролонгированное высвобождение активного ингредиента.
Недостатками предложенного способа являются длительность процесса и применение специального оборудования, комплекс определенных условий (температура воздуха на входе 10°C, температура воздуха на выходе 28°C, скорость вращения распыляющего барабана 10000 об/мин).
Наиболее близким методом является способ, предложенный в патенте РФ №2134967 (МПК A01N 53/00, A01N 25/28, опубликован 27.08.1999). Способ заключается в том, что в воде диспергируют раствор смеси природных липидов и пиретроидного инсектицида в весовом отношении 2-4: 1 в - этаноле, что приводит к упрощению способа микрокапсулирования.
Недостатком метода является диспергирование в водной среде, что делает предложенный способ неприменимым для получения микрокапсул водорастворимых препаратов в водорастворимых полимерах.
Техническая задача - устранение недостатка прототипа, т.е. создание способа получения микрокапсул водорастворимых аминокислот в альгинате натрия, который также является водорастворимым.
Технический результат - получение капсул с супрамолекулярными свойствами в водорастворимой оболочке.
Дополнительный технический результат - упрощение и ускорение процесса получения микрокапсул, уменьшение потерь при получении микрокапсул за счет увеличения выхода по массе.
Решение технической задачи достигается способом получения микрокапсул аминокислот с оболочкой из альгината натрия методом осаждения нерастворителем с применением этанола в качестве осадителя микрокапсул из альгината натрия без специального оборудования.
Аминокислоту растворяют в диметилсульфоксиде и диспергируют полученную смесь в суспензию альгината натрия в бутаноле, в присутствии ПАВ при перемешивании 1000 об/сек, затем приливают этанол и воду, полученную суспензию отфильтровывают и сушат при комнатной температуре.
В качестве ПАВ предпочтительно использование препарата E472c, являющегося сложным эфиром глицерина с одной - двумя молекулами пищевых жирных кислот и одной - двумя молекулами лимонной кислоты, причем лимонная кислота, как трехосновная, может быть этерифицирована другими глицеридами и как оксокислота - другими жирными кислотами. Свободные кислотные группы могут быть нейтрализованы натрием. E472c не обладает токсическим действием и не вызывает раздражения слизистых оболочек. Как эфир моно- и диглицеридов лимонной и жирных кислот относится к стабилизирующим веществам, применяемым для сохранения и улучшения вязкости и консистенции пищевых продуктов.
Отличительной особенностью предлагаемого способа является получение микрокапсул методом осаждения нерастворителем с использованием этанола в качестве осадителя, а также использование альгината натрия в качестве оболочки микрокапсул.
Изобретение характеризуется следующими изображениями:
На фиг. 1 Конфокальное изображение фрактальной композиции из раствора микрокапсул L-аргинина в оболочке альгината натрия, соотношение оболочка:ядро 3:1, в концентрации 0,25%: а) увеличение в 505 раз, б) увеличение в 930 раз, в) увеличение в 2830 раз.
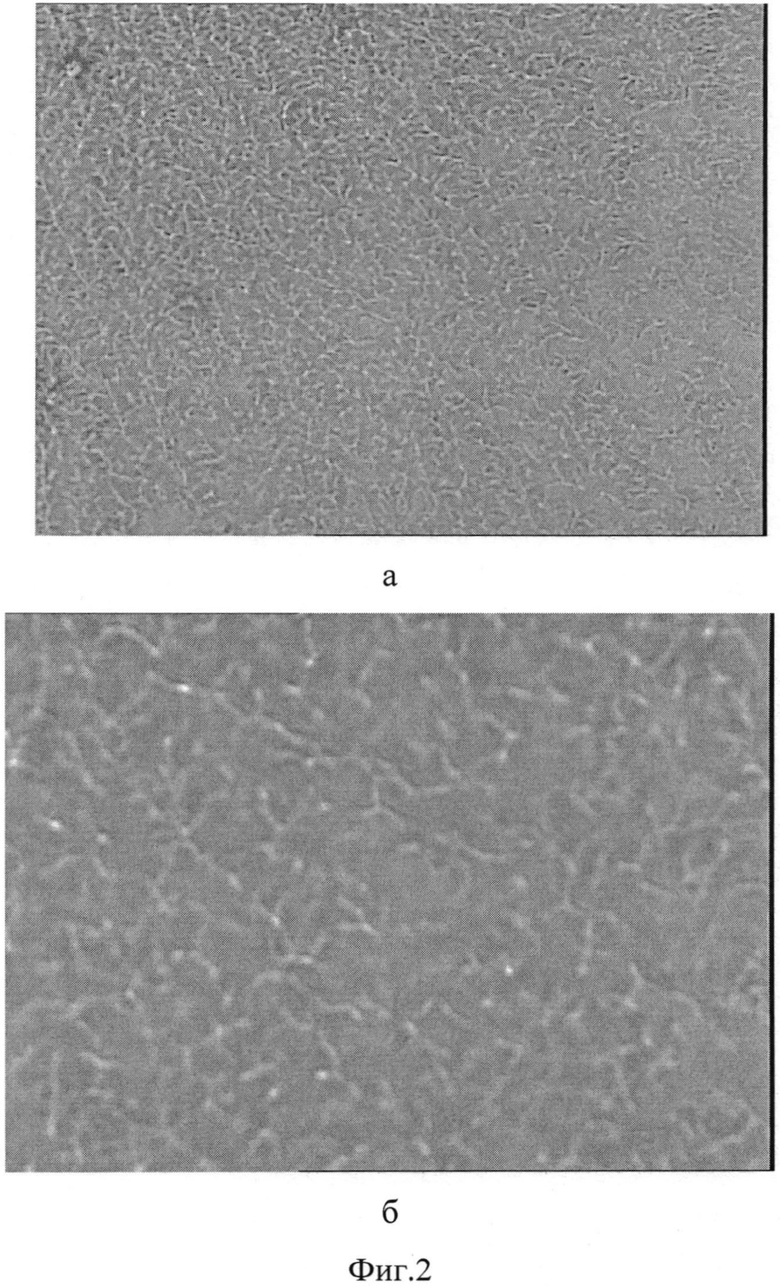
На фиг. 2 Конфокальное изображение фрактальной композиции из раствора микрокапсул L-аргинина в оболочке альгината натрия, соотношение оболочка:ядро 3:1, в концентрации 0,125%: а) увеличение в 930 раз, б) увеличение в 2830 раз.
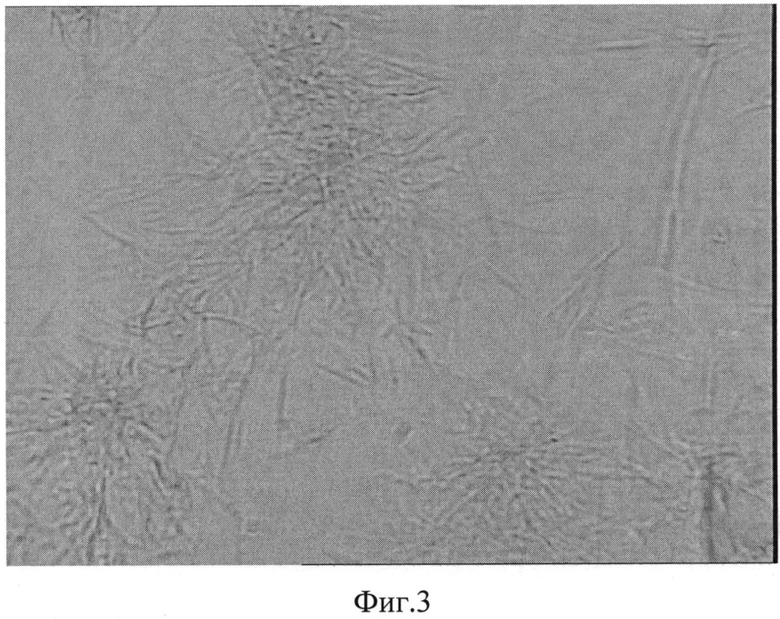
На фиг. 3 Конфокальное изображение фрактальной композиции из раствора микрокапсул L-аргинина в оболочке альгината натрия, соотношение оболочка:ядро 1:5, в концентрации 0,125% увеличение в 2830 раз.
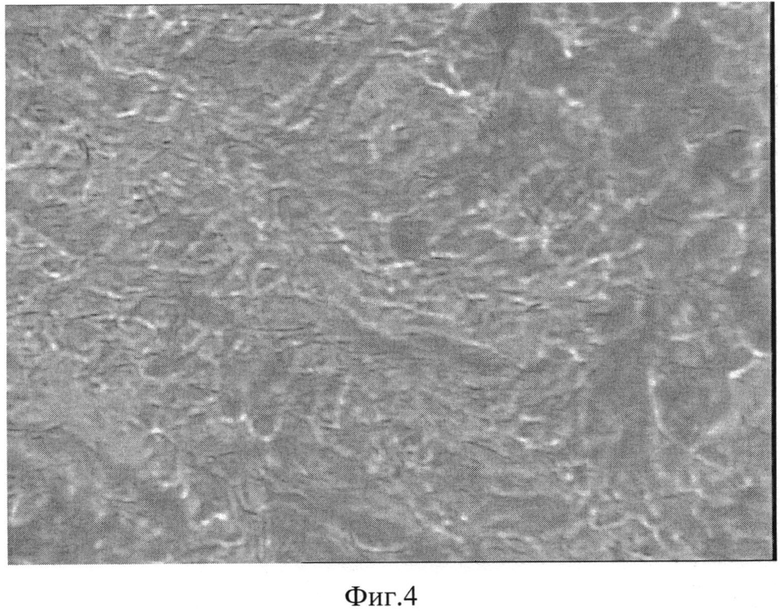
На фиг. 4 Конфокальное изображение фрактальной композиции из раствора микрокапсул норвалина в оболочке альгината натрия, соотношение оболочка:ядро 3:1, в концентрации 0,5% увеличение в 2830 раз.
На фиг. 5 Конфокальное изображение фрактальной композиции из раствора микрокапсул норвалина в оболочке альгината натрия, соотношение оболочка:ядро 3:1, в концентрации 0,125%: а) увеличение в 930 раз, б) увеличение в 2830 раз.
На фиг. 6 Конфокальное изображение фрактальной композиции из раствора микрокапсул норвалина в оболочке альгината натрия, соотношение оболочка:ядро 1:5, в концентрации 0,125%: а) увеличение в 930 раз, б) увеличение в 2830 раз.
Использование предлагаемого способа не ограничено аминокислотами, в приведенных ниже примерах.
ПРИМЕР 1. Получение микрокапсул L-аргинина в альгинате натрия с соотношением оболочка:ядро 1:5.
5 г L-аргинина растворяют в 10 мл диметилсульфоксида и диспергируют полученную смесь в суспензию альгината натрия в бутаноле, содержащего 1 г указанного полимера в присутствии 0,01 г препарата E472c при перемешивании 1000 об/сек. Далее приливают 5 мл этанола и 1 мл воды. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 6 г порошка микрокапсул. Выход составил 100%.
ПРИМЕР 2. Получение микрокапсул L-аргинина в альгинате натрия соотношение оболочка: ядро 3:1
1 г L-аргинина растворяют в 5 мл диметилсульфоксида и диспергируют полученную смесь в суспензию альгината натрия в бутаноле, содержащего 3 г указанного полимера в присутствии 0,01 г препарата E472c при перемешивании 1000 об/сек. Далее приливают 3 мл этанола и 1 мл воды. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 4 г порошка микрокапсул. Выход составил 100%.
ПРИМЕР 3. Получение микрокапсул норвалина в альгинате натрия, соотношение оболочка: ядро 1:5.
5 г норвалина растворяют в 10 мл диметилсульфоксида и диспергируют полученную смесь в суспензию альгината натрия в бутаноле, содержащий 1 г указанного полимера в присутствии 0,01 г препарата E472c при перемешивании 1000 об/сек. Далее приливают 5 мл этанола и 1 мл воды. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 6 г порошка микрокапсул. Выход составил 100%.
ПРИМЕР 4. Получение микрокапсул норвалина в альгинате натрия соотношение оболочка: ядро 3:1
1 г L-аргинина растворяют в 5 мл диметилсульфоксида и диспергируют полученную смесь в суспензию альгината натрия в бутаноле, содержащего 3 г указанного полимера в присутствии 0,01 г препарата E472c при перемешивании 1000 об/сек. Далее приливают 3 мл этанола и 1 мл воды. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 4 г порошка микрокапсул. Выход составил 100%.
ПРИМЕР 5. Исследование самоорганизации микрокапсул из растворов
Из порошка микрокапсул, полученных по примерам 1-4, были приготовлены водные растворы концентрациями 1%, 0,5%, 0,25%, 0,125% и т.д. путем разбавления раствора в два раза. Капля каждого из приготовленных растворов помещалась на предметное стекло до полного высушивания и по высушенной поверхности проводилась конфокальная сканирующая микроскопия. Представленные на фигурах 1-6 структуры являются упорядоченными, значит, они обладают самоорганизацией. Следовательно, микрокапсулы в альгинате натрия L-аргинина и норвалина обладают супрамолекулярными свойствами.
Таким образом, по предложенному способу получены микрокапсулы L-аргинина и норвалина с высоким выходом без специального оборудования в течение 10 мин. Образование микрокапсул происходит спонтанно за счет нековалентных взаимодействий и это говорит о том, что для них характерна самосборка.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛ АМИНОКИСЛОТ В КСАНТАНОВОЙ КАМЕДИ | 2014 |
|
RU2558859C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛ АМИНОКИСЛОТ В КОНЖАКОВОЙ КАМЕДИ | 2014 |
|
RU2558856C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛ ЛОЗАРТАНА КАЛИЯ В АЛЬГИНАТЕ НАТРИЯ | 2014 |
|
RU2558855C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛ АРОМАТИЗАТОРОВ "ВИШНЯ" И "ТОМАТ", ОБЛАДАЮЩИХ СУПРАМОЛЕКУЛЯРНЫМИ СВОЙСТВАМИ | 2013 |
|
RU2557939C2 |
| СПОСОБ ИНКАПСУЛЯЦИИ ФЕРРОЦЕНА | 2013 |
|
RU2545828C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОКАПСУЛ РЕЗВЕРАТРОЛА В КСАНТАНОВОЙ КАМЕДИ, ОБЛАДАЮЩИХ СУПРАМОЛЕКУЛЯРНЫМИ СВОЙСТВАМИ | 2014 |
|
RU2557942C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОКАПСУЛ СЕЛ-ПЛЕКСА, ОБЛАДАЮЩИХ СУПРАМОЛЕКУЛЯРНЫМИ СВОЙСТВАМИ | 2014 |
|
RU2556118C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛ АРОМАТИЗАТОРА "ЗЕЛЕНОЕ ЯБЛОКО" | 2013 |
|
RU2541814C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОКАПСУЛ АСПИРИНА В АЛЬГИНАТЕ НАТРИЯ | 2014 |
|
RU2565396C1 |
| СПОСОБ БИОИНКАПСУЛЯЦИИ БЕТАИНА, ОБЛАДАЮЩЕГО СУПРАМОЛЕКУЛЯРНЫМИ СВОЙСТВАМИ | 2013 |
|
RU2547559C2 |



Способ получения микрокапсул аминокислот в оболочке из альгината натрия может быть использован в фармакологии, фармацевтике, медицине. Согласно способу по изобретению аминокислоту растворяют в диметилсульфоксиде и диспергируют полученную смесь в суспензию альгината натрия в бутаноле в присутствии препарата E472c при перемешивании 1000 об/сек. Затем приливают этанол и воду, полученную суспензию отфильтровывают и сушат при комнатной температуре. Процесс осуществляют в течение 10 минут. Способ по изобретению обеспечивает упрощение и ускорение процесса получения микрокапсул, уменьшение потерь при получении микрокапсул за счет увеличения выхода по массе. 6 ил., 5 пр.
Способ получения микрокапсул аминокислот в оболочке из альгината натрия, характеризующийся тем, что аминокислоту растворяют в диметилсульфоксиде и диспергируют полученную смесь в суспензию альгината натрия в бутаноле в присутствии препарата Е472с при перемешивании 1000 об/сек, затем приливают этанол и воду, полученную суспензию отфильтровывают и сушат при комнатной температуре, а процесс осуществляют в течение 10 мин.
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛИРОВАННЫХ ПРЕПАРАТОВ, СОДЕРЖАЩИХ ПИРЕТРОИДНЫЕ ИНСЕКТИЦИДЫ | 1997 |
|
RU2134967C1 |
| Жан-Мари ЛЕН, Супрамолекулярная химия: Концепции и перспективы, - Новосибирск "Наука", Сибирское предприятие РАН, 1998, стр.210-211 | |||
| СОЛОДОВНИК В.Д | |||
| "Микрокапсулирование", - Москва, "Химия", 1980, стр.136-139 | |||
| Способ получения микрокапсул | 1978 |
|
SU676316A1 |
| Способ получения микрокапсул | 1976 |
|
SU707510A3 |
| МИКРОКАПСУЛА ДЛЯ ДЛИТЕЛЬНОГО ВЫСВОБОЖДЕНИЯ ФИЗИОЛОГИЧЕСКИ АКТИВНОГО ПЕПТИДА | 1993 |
|
RU2098121C1 |
| WO 1987001587 A1, 26.03.1987 | |||
Авторы
Даты
2015-10-20—Публикация
2014-04-02—Подача