Изобретение относится к органической химии, а именно к группе галогенацетатов, и непосредственно касается получения монохлорацетата серебра, применяемого, в частности, для получения полимерных материалов, используемых в медицине.
Так, известно, что монохлорацетат серебра используется для получения полимерного материала, применяемого в хирургии при изготовлении рассасывающихся в организме хирургических нитей. Такой материал получают сополимеризацией монохлорацетата серебра с гликолиевой кислотой методом фотоиндуцированной полимеризации в твердой фазе [K. Schwarz, М. Epple, «А detailed characterization of polyglycolide prepared by solid-state polycondensation reaction», Macromolecular Chemistry and Physics 200 (1999) 2221-2229; Pathiraja A Gunatillake; Raju Adhikari. «Biodegradable Synthetic Polymers for tissue engineering». European Cells and Materials 5 (2003): 1-16].
В качестве исходного продукта для получения монохлорацетата серебра обычно используются неорганические соли серебра и, в частности, нитрат серебра. Так, согласно известной публикации [The Thermally Induced Solid-state Polymerization Reaction in Halogenoacetates, Matthias Epple and Holger Kirschnick, Chem. Bev. 1996, 129, 1123-1129], исходный нитрат серебра на первой стадии процесса обрабатывают в этаноле гидроокисью калия до образования дисперсии гидроокиси серебра, а затем на второй стадии к полученной дисперсии гидроокиси серебра добавляют хлоруксусную кислоту. Полученную реакционную массу выдерживают в течение 1 часа при перемешивании и при температуре 50°С и выпавший целевой продукт отфильтровывают, перекристаллизовывают из воды и сушат в вакууме. Выход монохлорацетата серебра, полученного данным способом, составляет 50%. К основным недостаткам данного способа можно отнести и его неэкономичность, которая проявляется в довольно низком выходе получаемого продукта, и несоответствие его современным экологическим требованиям из-за использования гидроокиси калия, которая к тому же способствует нежелательному загрязнению конечного продукта неорганическими примесями.
В другом известном способе получения монохлорацетата серебра, [«Palladium nitrosyl carboxylate complexes X-ray structures of Pd4(m-NO)2(m-OCOCMe3)6 and Pd3(NO)2(m-OCOCF3)4-2C6H5Me», T.A. Stromnova et all, Inorganica Chimica Acta 350 (2003) 283-288], проводимом также в две стадии, предлагают на первой стадии процесса сначала получать монохлорацетат натрия, а затем из него получать монохлорацетат серебра. Для этого обрабатывают монохлоруксусную кислоту водным раствором гидроокиси натрия и подкисляют реакционную смесь уксусной кислотой, а затем полученный водный раствор монохлорацетата натрия приливают к водному раствору нитрата серебра и выпавший осадок полученного монохлорацетата серебра отфильтровывают, промывают водой и сушат в вакууме. Выход целевого продукта в данном случае составляет 80-95%. Недостаток данного способа, как и ранее рассмотренного аналога, также заключается в использовании в процессе синтеза агрессивных веществ, в частности едкого натра и уксусной кислоты, которые ухудшают экологические показатели процесса. Использование в способе едкого натра также приводит к загрязнению конечного продукта посторонними неорганическими примесями и необходимости введения дополнительных стадий очистки (перекристаллизации), что снижает интенсивность и экономичность процесса.
Для повышения интенсивности процесса и улучшения его экологических и экономических показателей предлагается новый способ получения монохлорацетата серебра, включающий использование в качестве исходных продуктов монохлоруксусной кислоты и нитрата серебра, осуществляемый перемешиванием водного раствора монохлоруксусной кислоты и водного раствора нитрата серебра, взятых в количествах, соответствующих мольному соотношению монохлоруксусной кислоты к нитрату серебра 1,0-1,4:1,0, выдерживанием полученной реакционной смеси при температуре 20-25°С и последующим выделением выпавшего осадка фильтрацией, промывкой его водой и этанолом и сушкой.
Основными отличиями нового способа от известных аналогов является проведение процесса в одну стадию, а не в две, как в аналогах, и исключение применения агрессивных жидкостей (щелочей и кислот), что повышает интенсивность процесса, улучшает его экологические и экономические показатели. Существенно на процесс синтеза влияют экспериментально подобранный температурный режим (20-25°С) и мольное соотношение исходных монохлоруксусной кислоты и нитрата серебра (1,0-1,4:1,0). Как показывают дополнительные экспериментальные исследования, при завышении и занижении температурного режима по сравнению с заявляемым режимом снижается выход конечного продукта (см. пример 3). Также на выход влияет и мольное соотношение исходных продуктов.
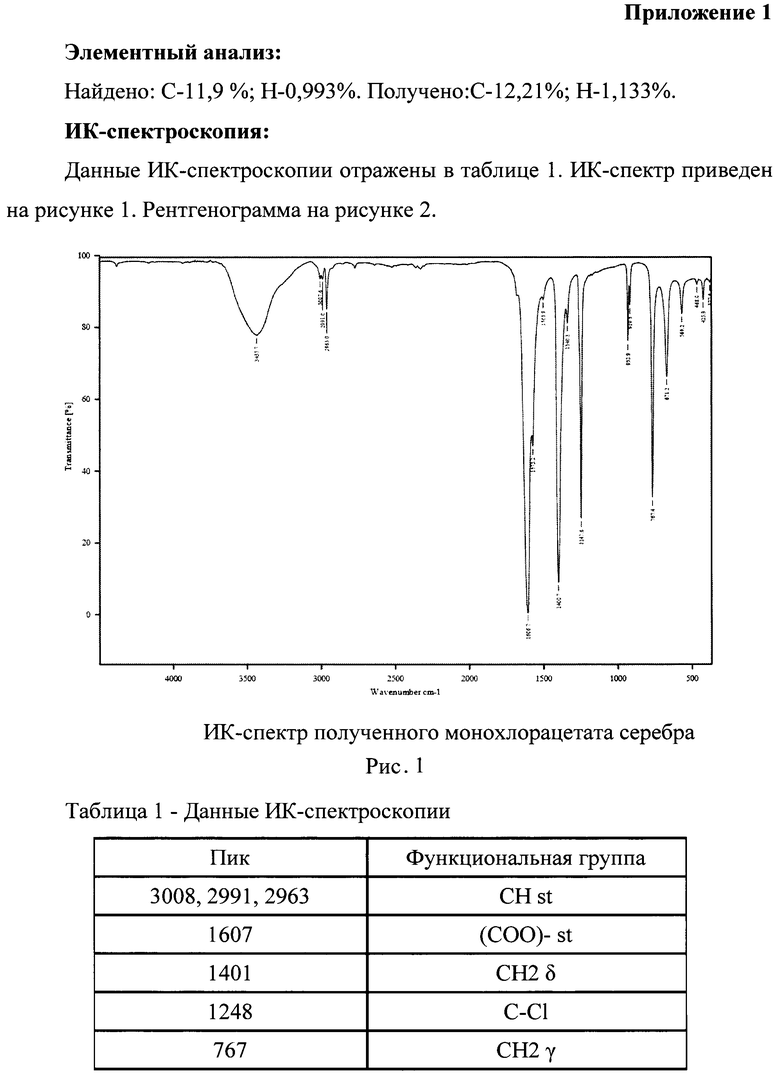
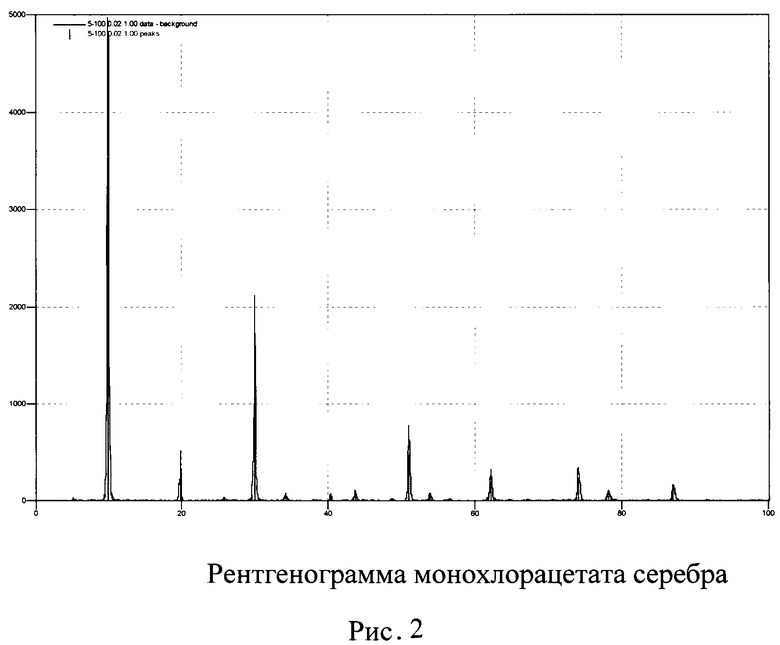
Достоинством нового способа являются и более мягкие условия его проведения (по сравнению с аналогами), поскольку процесс синтеза проводится в воде при комнатной температуре (20-25°С). Получают 1,2 г монохлорацетата серебра с выходом 93,5%. Получаемый продукт практически не содержит неорганических примесей, в отличие от монохлорацетата серебра, полученного согласно методикам синтеза, приведенным в способах-аналогах, что подтверждается методом элементного анализа (Найдено: С - 11,9%; Н - 0,993%. Получено: С - 12,21%; Н - 1,133%). Полученный продукт охарактеризован методами рентгенофазового анализа, ИК-спектроскопии (см. рис. 1, 2, таблица 1).
Получаемый таким способом монохлорацетат серебра по своему качеству соответствует требованиям, предъявляемым к химическим реактивам, применяемым в медицине, в частности для получения хирургических полимерных материалов.
Ниже изобретение иллюстрируется следующими примерами.
Пример 1
В колбе емкостью 25 см3 растворяют 0,66 г (0,007 м) монохлоруксусной кислоты в 10 см3 воды и при размешивании приливают к нему раствор 0,85 г (0,005 м) AgNO3 в 5 см3 воды, выдерживают при температуре 20°С. Выпавший осадок отфильтровывают, промывают водой и этанолом. Сушат до постоянного веса. Получают - 1,2 г монохлорацетата серебра. Выход 93,5%.
Пример 2
В колбе емкостью 25 см3 растворяют 0,47 г (0,005 м) монохлоруксусной кислоты в 10 см3 воды и при перемешивании приливают к нему раствор 0,85 г (0,005 м) AgNO3 в 5 см3 воды, выдерживают при 25°С. Выпавший осадок отфильтровывают, промывают водой и спиртом. Сушат до постоянного веса. Получают - 1,2 г монохлорацетата серебра. Выход 93,5%.
Пример 3
В колбе емкостью 25 см3 растворяют 0,66 г (0,007 м) монохлоруксусной кислоты в 10 см3 воды и при перемешивании приливают к нему раствор 0,85 г (0,005 м) AgNO3 в 5 см3 воды, выдерживает при 40°С. Выпавший осадок отфильтровывают, промывают водой и спиртом. Сушат до постоянного веса. Получают - 1,17 г монохлорацетата серебра. Выход 88,8%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИАЛКИЛЕНПОЛИАМИНПОЛИМЕТИЛФОСФОНОВЫХ КИСЛОТ | 2010 |
|
RU2434875C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА СВЕРХВЫСОКОМОЛЕКУЛЯРНОГО ПОЛИЭТИЛЕНА, МОДИФИЦИРОВАННОГО НАНОЧАСТИЦАМИ СЕРЕБРА | 2016 |
|
RU2631567C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИМИНОДИУКСУСНОЙ КИСЛОТЫ | 2014 |
|
RU2548573C1 |
| КОЛЛОИДНЫЙ РАСТВОР НАНОСЕРЕБРА В ЭТИЛЕНГЛИКОЛЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2610197C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИЭТИЛАММОНИЕВОЙ СОЛИ БИС(3-АМИНОФЕНИЛ)ФОСФИНОВОЙ КИСЛОТЫ | 2017 |
|
RU2659033C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,5-БИС(2-ГИДРОКСИФЕНОКСИ)-3-ОКСАПЕНТАНА МОНОГИДРАТА | 2012 |
|
RU2483055C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРИЛОТРИУКСУСНОЙ КИСЛОТЫ | 1990 |
|
SU1743148A1 |
| Способ получения карбоксиметилхитин-глюканового комплекса | 2023 |
|
RU2822043C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДНЫХ РАСТВОРОВ ПОЛИАКРИЛОВОЙ КИСЛОТЫ | 1987 |
|
SU1557982A1 |
| СПОСОБ ОЧИСТКИ СКАНДИЯ ОТ ТОРИЯ | 2014 |
|
RU2567167C2 |
Изобретение относится к органической химии, а именно к группе галогенацетатов, и непосредственно касается получения монохлорацетата серебра, применяемого, в частности, для получения полимерных материалов, используемых в медицине. Способ получения монохлорацетата серебра включает использование в качестве исходных продуктов монохлоруксусной кислоты и нитрата серебра. Его осуществляют перемешиванием водного раствора монохлоруксусной кислоты с водным раствором нитрата серебра, взятыми в количествах, соответствующих мольному соотношению монохлоруксусной кислоты к нитрату серебра 1,0-1,4:1,0, выдерживанием полученной реакционной смеси при температуре 20-25°C, последующим выделением выпавшего осадка фильтрацией, промывкой его водой и этанолом и сушкой. Получают 1,2 г монохлорацетата серебра с выходом 93,5%. Полученный продукт соответствует требованиям, предъявляемым к реактивам для медицины. 2 ил., 3 пр., 1 табл.
Способ получения монохлорацетата серебра, включающий использование в качестве исходных продуктов монохлоруксусной кислоты и нитрата серебра, отличающийся тем, что его осуществляют перемешиванием водного раствора монохлоруксусной кислоты с водным раствором нитрата серебра, взятыми в количествах, соответствующих мольному соотношению монохлоруксусной кислоты к нитрату серебра 1,0-1,4:1,0, выдерживанием полученной реакционной смеси при температуре 20-25°C, последующим выделением выпавшего осадка фильтрацией, промывкой его водой и этанолом и сушкой.
| Stromnova, Tatiana A | |||
| et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ получения солей щелочных металлов или аммония моно- или трихлоруксусных кислот | 1975 |
|
SU969151A3 |
| Matthias Epplev et al | |||
| "The Thermally Induced Solid-State Polymerization Reaction in Halogenoacetates" Chemische Berichte, Vol 129 | |||
Авторы
Даты
2015-10-27—Публикация
2014-12-11—Подача