Изобретение относится к области органической химии, а именно к области получения функционально замещенных фуро[3,4-с]пиридинов, конкретно алкилзамещенных 4-галоген-3-гидроксифуро[3,4-с]пиридин-1(3H)-онов
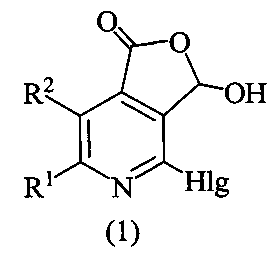
где R1=R2=CH3, Hlg=Cl; R1=СН3, R2=C2H5, Hlg=Cl; R1=CH3, R2=C3H7, Hlg=Cl; R1=R2=CH3, Hlg=Br; R1=CH3, R2=C2H5, Hlg=Br; R1=СН3, R2=C3H7, Hlg=Br, которые могут найти применение в качестве активатора калиевых каналов, ингибиторов киназы анапластической лимфомы (Anaplastic Lymphoma Kinase), ингибитора белка переноса холестерилового эфира (СЕТР), а также в качестве кардиопротекторных агентов.
Известен способ получения 3-гидрокси-1,3-дигидрофуро[3,4-с]пиридина путем окисления 1,3-дигидрофуро[3,4-с]пиридина кислородом воздуха [Parnell С.А., Peter V. Regioselective construction of the tetrasubstituted pyridine nucleus by cobalt-catalyzed alkyne-nitrile cooligomerizations // Tetrahedron. 1985, 24, 5791-5796]. Недостатком этого способа являются низкие (следовые) количества образующегося продукта реакции.
Известны способы получения 3-гидрокси-1,3-дигидрофуро[3,4-с]пиридина, заключающиеся в восстановлении карбонильной функции фуро[3,4-с]пиридин-3(1H)-она [Mukherjee P., Roy S.J.S., Sarkar Т.K. A diversity-oriented synthesis of bicycliccis-dihydroarenediols, cis-4-hydroxyscytalones, and bicyclic conduritol analogues // Org. Lett. 2010, 11, 2472-2475; EP 2072519 A61K 31/438; A61K 31/444; A61K 31/497 Diaryl ketimine derivative; Dormoy H. Tetrahedron. 1993, 14, 2915-2938; Desarbre E., Coudret S., Meheust C., Merour J.-Y. Synthesis of 2-substituted-1H-Pyrrolo[2,3-b]pyridines: preparation of 7-azaolivacine analogue and 7-azaindolopyridopyrimidine derivatives // Tetrahedron. 1997, 10, 3637-3648]. Недостатками данных способов являются труднодоступные исходные реагенты, использование безводных растворителей, необходимость обеспечения низких температур проведения синтеза и инертной атмосферы.
Авторами [WO 2009/146555 A61K 31/44; A61K 31/4427; А61Р 31/12; А61Р 31/18; C07D 213/81; C07D 405/12; C07D 493/04 HIV integrase inhibitors from pyridoxine; Dormoy H. Synthese industrielle en serie ellipticine II: Elaboration d'une nouvelle voie d′acces aux 6H-pyrido[4,3-b]carbazoles et analogues: B. Obtention des structures tétracycliques // Tetrahedron. 1993, 14, 2915-2938; Boa A.N., Canavan S.P., Hirst P.R., Ramsey C., Stead A.M.W., McConkey G.A. Synthesis of brequinar analogue inhibitors of malaria parasite dihydroorotate dehydrogenase // Bioorg. Med. Chem. 2005, 6, 1945-1967; Desarbre E., Coudret S., Meheust C., Merour J.-Y. Synthesis of 2-substimted-1H-Pyrrolo[2,3-b]pyridines: preparation of 7-azaolivacine analogue and 7-azaindolopyridopyrimidine derivatives // Tetrahedron. 1997, 10, 3637-3648; Pokhodylo N.T., Matiychuk V.S., Obushak P.M. A convenient method for the synthesis of thiopyrano[4,3-c]quinoline, a new heterocyclic system // Chem. Heterocycl. Compd. 2009, 1, 121-122; EP 503537 A61K 31/435; A61K 31/473; A61K 31/535 6,9-Bis(substituted-amino)benzo-[g]isoquinoline-5,10-diones] описан способ получения 1,3-дигидрофуро[3,4-с] пиридина построением фуранового цикла путем внутримолекулярной гетероциклизации функциональных групп пиридинового кольца. Недостатками данных способов являются их многостадийность, использование инертной атмосферы и низкая температура проведения синтеза.
В ряде источников описаны способы получения производных фуро[3,4-с]пиридина, которые используются в качестве интермедиатов для получения целевых продуктов, путем внутримолекулярной гетероциклизации функциональных групп пиридинового кольца [US 5519029 C07D 471/06; A61K 31/435; C07D 419/14 2-Aminoalkyl-5-aminoalkylamino substituted-isoquinoindazole-6(2H)-ones; US 5596097 C07D 471/06; C07D 487/06; A61K 31/47 Hetero-annulated indazoles; WO 2015/1348 A61K 31/502; A61K 31/5025; A61P 35/00 Pyridazine derivatives as hedgehog pathway inhibitors; US 5506232 A61K 31/47; A61K 31/473; A61P 35/00 6,9-Bis[(2-aminoethyl)amino]benzo[g]isoquinoline-5,10-dione and its dimaleate salt; WO 2014/191737 A61K 31/501; A61K 31/502; A61K 31/5025 Heterocyclic compounds as hedgehog signaling pathway inhibitors; US 4268513 A61K 31/47; A61K 31/535; A61P 25/04 Pyrrolo[3,4-c]quinoline compounds and pharmaceutical compositions, methods for their use and preparation]. Недостатками данных способов являются их многостадийность, использование инертной атмосферы и низкая температура проведения синтеза.
Известен способ получения 3-гидрокси-1,3-дигидрофуро[3,4-с]пиридина путем конденсации никотинальдегида с замещенными бензальдегидами [WO 2006/91800 A61K 31/44; А61Р 9/00; C07D 213/30 Novel pyridine derivatives as potassium ion channel openers]. Недостатком данного способа является низкая температура проведения синтеза.
Известен способ получения 3-гидрокси-1,3-дигидрофуро[3,4-с]пиридина взаимодействием индолин-2,3-диона с пентан-2,4-дионами [Godard A., Queguiner G. Polyazaphenanthrenes. Synthese de pyridazino[4,5-c]quinoleines // Chem. Heterocycl. Chem. 1984, 1, 27-32]. Недостатком данного способа является длительность процесса (6 часов).
Известен способ получения 3-гидрокси-1,3-дигидрофуро[3,4-с]пиридина в результате многостадийной реакции между 2-метоксипиридном, N1,N1,N2-триметил-N2-винилэтан-1,2-диамином и кетонами [Hong Н., Comins D.L. A Three-Step Synthesis of Cerpegin // J. Org. Chem. 1996, 1, 391-392]. Недостатком данного способа является многостадийность, а следовательно, длительность и трудоемкость процесса.
Наиболее близким к заявляемому является способ получения 3-гидроксифуро[3,4-с]пиридин-1(3H)-она, заключающийся в обработке 2,2,6,6-тетраметилпиперидина н-бутиллитием в среде сухого тетрагидрофурана и н-гексана с последующим добавлением раствора 2,6-дибромникотиновой и 2,6-дибромизоникотиновой кислот в тетрагидрофуране и N,N-диметилформамида при температуре минус 78°С в течение 15 часов [WO 2012/97682 A61K 31/435; A61K 31/495; A61K 31/551 Bicyclic inhibitors of alk; WO 2012/97479 A61K 31/4375; A61K 31/4985; A61P 35/00 Bicyclic inhibitors of anaplastic lymphoma kinase]. Недостатком данного способа являются длительность процесса и низкая температура проведения синтеза.
Основным недостатком всех описанных выше способов является то, что они не позволяют получить 4-галоген-3-гидроксифуро[3,4-с]пиридин-1(3H)-оны.
Задачей данного изобретения является разработка способа получения ранее неизвестных алкилзамещенных 4-галоген-3-гидроксифуро [3,4-с]пиридин-1(3H)-онов, которые могут найти применение в качестве активатора калиевых каналов, ингибиторов киназы анапластической лимфомы (Anaplastic Lymphoma Kinase), ингибитора белка переноса холестерилового эфира (СЕТР), а также в качестве кардиопротекторных агентов.
Техническим результатом является разработка способа получения ранее неописанных в литературе алкилзамещенных 4-галоген-3-гидроксифуро[3,4-с]пиридин-1(3H)-онов.
Технический результат достигается тем, что способ получения алкилзамещенных 4-галоген-3-гидроксифуро[3,4-с]пиридин-1(3H)-онов общей формулой (1)
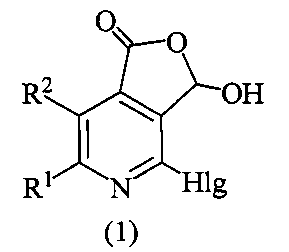
где R1=R2=CH3, Hlg=Cl; R1=CH3, R2=C2H5, Hlg=Cl; R1=CH3, R2=C3H7, Hlg=Cl; R1=R2=CH3, Hlg=Br; R1=CH3, R2=C2H5, Hlg=Br; R1=CH3, R2=C3H7, Hlg=Br, согласно изобретению характеризуется тем, что соответствующий 3-амино-8-гидрокси-1,6-диоксо-2,7-диазаспиро[4.4]нон-3-ен-4-карбонитрил растворяют в 2-5-кратном избытке концентрированной галогеноводородной кислоты и добавляют 5-7-кратный избыток галогенида фосфора (III), кипятят 40-50 минут, охлаждают, разбавляют водой и экстрагируют этилацетатом, экстракт упаривают, образовавшийся осадок перекристаллизовывают из пропан-2-ола.
Сопоставительный анализ заявляемого решения с известными показывает, что способы получения алкилзамещенных 4-галоген-3-гидроксифуро[3,4-с]пиридин-1(3Н)-онов в литературе не описаны. Важно отметить, что в качестве реагента и растворителя в предлагаемом способе используются дешевые и доступные водный раствор галогеноводорода и галогенид фосфора (III).
Сущность изобретения представлена в примерах:
Пример 1. Способ получения 3-гидрокси-6,7-диметил-4-хлорфуро[3,4-с]пиридин-1(3H)-она
0.47 г (0.002 моль) 3-амино-8-гидрокси-8,9-диметил-1,6-диоксо-2,7-диазаспиро[4.4]нон-3-ен-4-карбонитрила при интенсивном перемешивании растворяют в 3 мл концентрированной соляной кислоты, добавляют 1 мл PCl3. Кипят 40-50 минут, охлаждают, разбавляют водой и экстрагируют этилацетатом. Экстракт упаривают, образовавшийся осадок перекристаллизовывают из пропан-2-ола. Выход 0.16 г (38%), т.пл. 180-181°С. ИК-спектр ν, см-1: 3522 (ОН), 1771 (С=O). Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 2.53 с (3Н, СН3), 2.55 с (3Н, СН3), 6.65 с (1Н, ОН), 8.34 уш. с (1Н, СН). Найдено, %: С, 50.51; Н, 3.74; N, 6.66. C9H8ClNO3. Вычислено, %: С, 50.60; Н, 3.77; N, 6.56. Масс-спектр, m/z (Ioтн., %): 213 [М, 35Cl]+ (44%), 215 [М, 37Cl]+ (13%).
Пример 2. Способ получения 3-гидрокси-6-метил-4-хлор-7-этилфуро[3,4-с]пиридин-1(3Н)-она
Способ осуществляется аналогично способу 1, при этом вместо 3-амино-8-гидрокси-8,9-диметил-1,6-диоксо-2,7-диазаспиро[4.4]нон-3-ен-4-карбонитрила используется 3-амино-8-гидрокси-8-метил-1,6-диоксо-9-этил-2,7-диазаспиро[4.4]нон-3-ен-4-карбонитрил. Выход 0.19 г (42%), т.пл. 203-205°С (разл.). ИК-спектр ν, см-1: 3527 (ОН), 1769 (С=0). Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 1.13 т (3Н, J 7.5, СН2СН3), 2.59 с (3Н, СН3), 3.03 к (2Н, J7.3, СН2СН3),6.64 уш. с (1Н, ОН), 8.33 уш. с (1H, СН). Найдено, %: С С, 52.87; Н, 4.40; N, 6.09. C10H10ClNO3. Вычислено, %: С, 52.76; Н, 4.43; N, 6.15. Масс-спектр, m/z (Ioтн., %): 227 [М, 35Cl]+ (39%), 229 [М, 37Cl]+ (13%).
Пример 3. Способ получения 3-гидрокси-6-метил-7-пропил-4-хлорфуро[3,4-с]пиридин-1(377)-она
Способ осуществляется аналогично способу 1, при этом вместо 3-амино-8-гидрокси-8,9-диметил-1,6-диоксо-2,7-диазаспиро[4.4]нон-3-ен-4-карбонитрила используется 3-амино-8-гидрокси-8-метил-1,6-диоксо-9-пропил-2,7-диазаспиро[4.4]нон-3-ен-4-карбонитрил. Выход 0.20 г (41%), т.пл. 173-174°С (разд.). ИК-спектр ν, см-1: 3524 (ОН), 1770 (С=O). Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 0.95 т (3Н, J 7.3, СН2СН2СН3), 1.53 секстет (2Н, J 7.5, CH2CH2CH3), 2.59 с (3Н, СН3), 2.99 т (2Н, J 7.7, СН2СН2СН3), 6.65 с (1Н, ОН), 8.32 уш. с (1Н, СН). Найдено, %: С, 54.79; Н, 4.96; N, 5.87. C11H12ClNO3. Вычислено, %: С, 54.67; Н, 5.00; N, 5.80. Масс-спектр, m/z (Ioтн., %): 241 [М, 35Cl]+ (100%), 243 [М, 37Cl]+.
Пример 4. Способ получения 4-бром-3-гидрокси-6,7-диметилфуро[3,4-с]пиридин-1(3H)-она
Способ осуществляется аналогично способу 1, при этом вместо соляной кислоты используется бромоводородная кислота, вместо PCl3 используется PBr3. Выход 0.18 г (35%), т.пл. 186-187°С (разл.). ИК-спектр ν, см-1: 3527 (ОН), 1770 (С=O). Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 2.51 с (3Н, СН3), 2.55 с (3Н, СН3), 6.57 с (1H, ОН), 8.32 с (1H, СН). Найдено, %: С, 41.77; Н, 3.16; N, 5.48. C9H8BrNO3. Вычислено, %: С, 41.89; Н, 3.12; N, 5.43. Масс-спектр, m/z (Ioтн., %): 257 [М, 79Br]+ (14%), 259 [М, 81Br]+(13%).
Пример 5. Способ получения 4-бром-3-гидрокси-6-метил-7-этилфуро[3,4-с]пиридин-1(3H)-она
Способ осуществляется аналогично способу 1, при этом вместо 3-амино-8-гидрокси-8,9-диметил-1,6-диоксо-2,7-диазаспиро[4.4]нон-3-ен-4-карбонитрила используется 3-амино-8-гидрокси-8-метил-1,6-диоксо-9-этил-2,7-диазаспиро[4.4]нон-3-ен-4-карбонитрил, вместо соляной кислоты используется бромоводородная кислота, вместо РС13 используется PBr3. Выход 0.23 г (43%), т.пл. 211-212°С (разл.). ИК-спектр ν, см-1: 3525 (ОН), 1770 (С=O). Спектр ЯМР 1H (ДМСО-d6), δ, м.д.: 1.12 т (3Н, J 7.5, СН2СН3), 2.60 с (3Н, СН3), 3.00 к (2Н, J 7А, СН2СН3),6.61 уш. с (1Н, ОН), 8.31 уш. с (1Н, СН). Найдено, %: С, 44.03; Н, 3.67; N, 5.19. C10H10BrNO3. Вычислено, %: С, 44.14; Н, 3.70; N, 5.15. Масс-спектр, m/z (Ioтн., %): 271 [М, 79Br]+ (74%), 273 [М, 81Br]+ (72%).
Пример 6. Способ получения 4-бром-3-гидрокси-6-метил-7-пропилфуро[3,4-с]пиридин-1(3H)-она
Способ осуществляется аналогично способу 1, при этом вместо 3-амино-8-гидрокси-8,9-диметил-1,6-диоксо-2,7-диазаспиро[4.4]нон-3-ен-4-карбонитрила используется 3-амино-8-гидрокси-8-метил-1,6-диоксо-9-пропил-2,7-диазаспиро[4.4]нон-3- ен-4-карбонитрил, вместо соляной кислоты используется бромоводородная кислота, вместо PCl3 используется PBr3. Выход 0.25 г (44%), т.пл. 179-181°С (разл.). ИК-спектр ν, см-1: 3526 (ОН), 1767 (С=O). Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 0.95 т (3Н, J 7.3, СН2СН2СН3), 1-53 секстет (2Н, J 7.5, СН2СН2СН3), 2.59 с (3Н, СН3), 2.98 т (2Н, J 7.7, СН2СН2СН3), 6.57 с (1Н, ОН), 8.31 уш. с (1Н, СН). Найдено, %: С, 46.27; Н, 4.25; N, 4.94. C11H12BrNO3. Вычислено, %: С, 46.18; Н, 4.23; N, 4.90. Масс-спектр, m/z (Ioтн., %): 285 [М, 79Br]+(28%), 287 [М, 81Br]+ (26%).
Таким образом, предлагаемый способ позволяет получить неописанные в литературе алкилзамещенные 4-галоген-3-гидроксифуро[3,4-с]пиридин-1(3H)-оны, которые могут найти применение в качестве активатора калиевых каналов, ингибиторов киназы анапластической лимфомы (Anaplastic Lymphoma Kinase), ингибитора белка переноса холестерилового эфира (СЕТР), а также в качестве кардиопротекторных агентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения аммонийных солей 3-амино-8-гидрокси-1,6-диоксо-4-циано-2,7-диазаспиро[4.4]нон-3-ен-2-идов | 2016 |
|
RU2631856C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-АМИНО-8-ГИДРОКСИ-1,6-ДИОКСО-2,7-ДИАЗАСПИРО[4.4]НОН-3-ЕН-4-КАРБОНИТРИЛОВ | 2012 |
|
RU2495040C1 |
| Способ получения производных фуро[3,4-c]пиридин-1(3H)-онов | 2018 |
|
RU2680017C1 |
| Способ получения производных фуро[3,4-с]пиридин-1(3Н)-онов | 2020 |
|
RU2738707C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЗАМЕЩЕННЫХ 2-ОКСО-1,2-ДИГИДРОПИРИДИН-3,4-ДИКАРБОНИТРИЛОВ | 2015 |
|
RU2577526C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ОКСО-4-ЦИАНО-1,2-ДИГИДРОПИРИДИН-3-КАРБОКСАМИДОВ | 2011 |
|
RU2475480C1 |
| Способ получения производных 5-амино-3H-пиррол-4-карбонитрилов | 2018 |
|
RU2675600C1 |
| СПОСОБ ПОЛУЧЕНИЯ 8-АМИНО-1-ИМИНО-6-МОРФОЛИН-4-ИЛ-2-ОКСА-7-АЗАСПИРО[4,4]НОНА-3,6,8-ТРИЕН-9-КАРБОНИТРИЛОВ | 2011 |
|
RU2475489C1 |
| 1-имино-2,3,4,5-тетрагидро-1Н-пирроло[3,4-с]пиридин-3,4-дионов | 2016 |
|
RU2613967C1 |
| Применение 2-[(R-бензилиден)гидразоно]-8-гидрокси-6-(2-гидроксифенил)-9-ароил-1-тиа-3,6-диазаспиро[4.4]нона-8-ен-4,7-дионов в качестве средств, обладающих противовоспалительной активностью | 2022 |
|
RU2783241C1 |
Изобретение относится к способу получения новых алкилзамещенных 4-галоген-3-гидроксифуро[3,4-с]пиридин-1(3H)-онов общей формулы I, где R1=R2=CH3, Hlg=Cl; R1=СН3, R2=C2H5, Hlg=Cl; R1=CH3, R2=C3H7, Hlg=Cl; R1=R2=CH3, Hlg=Br; R1=CH3, R2=C2H5, Hlg=Br; R1=СН3, R2=C3H7, Hlg=Br, заключающемуся в том, что соответствующий 3-амино-8-гидрокси-1,6-диоксо-2,7-диазаспиро[4.4]нон-3-ен-4-карбонитрил растворяют в 2-5-кратном избытке концентрированной галогеноводородной кислоты, затем добавляют 5-7-кратный избыток галогенида фосфора (III), реакционную массу кипятят 40-50 минут, охлаждают, разбавляют водой и экстрагируют этилацетатом. Экстракт упаривают, образовавшийся осадок перекристаллизовывают из пропан-2-ола. Эти соединения могут найти применение в качестве активатора калиевых каналов, ингибиторов киназы анапластической лимфомы (Anaplastic Lymphoma Kinase), ингибитора белка переноса холестерилового эфира (СЕТР), а также в качестве кардиопротекторных агентов. 6 пр.
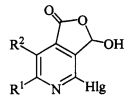
Способ получения алкилзамещенных 4-галоген-3-гидроксифуро[3,4-c]пиридин-1(3H)-онов общей формулы (1)
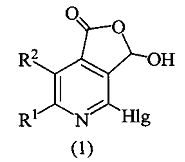
где R1=R2=CH3, Hlg=Cl; R1=CH3, R2=C2H5, Hlg=Cl; R1=CH3, R2=C3H7, Hlg=Cl; R1=R2=CH3, Hlg=Br; R1=СН3, R2=C2H5, Hlg=Br; R1=CH3, R2=C3H7, Hlg=Br, характеризующийся тем, что соответствующий 3-амино-8-гидрокси-1,6-диоксо-2,7-диазаспиро[4.4]нон-3-ен-4-карбонитрил растворяют в 2-5-кратном избытке концентрированной галогеноводородной кислоты и добавляют 5-7-кратный избыток галогенида фосфора (III), кипятят 40-50 минут, охлаждают, разбавляют водой и экстрагируют этилацетатом, экстракт упаривают, образовавшийся осадок перекристаллизовывают из пропан-2-ола.
| WO 2012097682 A 26.07.2012 | |||
| WO 2012097479 A1 26.07.2012 | |||
| СОЕДИНЕНИЯ КОНДЕНСИРОВАННОГО ФУРАНА | 2004 |
|
RU2302422C2 |
Авторы
Даты
2016-02-10—Публикация
2015-04-08—Подача