Настоящее изобретение предоставляет иммуноконъюгаты, включающие антитело или его фрагмент, специфичный к белку мезотелина, и лекарственное средство. Композиции таких иммуноконъюгатов могут быть использованы в лечении, профилактике или диагностировании расстройств, связанных с мезотелином, например рака.
ПРЕДПОСЫЛКИ К СОЗДАНИЮ ИЗОБРЕТЕНИЯ
Появление рака обычно ассоциируется со старением, в соответствии с чем 65% новых случаев рака зарегистрировано для пациентов в возрасте 65 лет и более. Рак стоит на втором месте после болезни сердца среди наиболее частых причин смерти в США. Действительно, Американское общество по борьбе с раком подсчитало, что один из четырех человек в США умрет от рака, при условии, что существующий уровень смертности останется неизменным. Только в США в 2008 году ожидается 1,437,180 новых случаев рака и 565,650 смертей от него.
Основанное на антителах лечение оказывается очень эффективным при различных видах рака, включая солидные опухоли. Например, HERCEPTIN® был успешно использован для лечения рака груди. Главной частью успешного развития лечения, основанного на антителах, является изоляция антител от белков клеточной поверхности, которые предпочтительно экспрессированы на опухолевых клетках. Полипептид - предшественник мезотелина - представляет собой глюкофосфатидилинозитол (ГФИ)-якорный, с глюкозилированной клеточной поверхностью белок, который расщепляется на 30 kDa N-конца скрытый полипептид и 40 kDa С-конца полипептид, принимая при этом ГФИ-якорную форму, связанную с мембраной (Chang, К. and I.Pastan, Proc. Natl. Acad. Sci. USA, (1996) 93(1):136), и который называется мезотелином. Мезотелин предпочтительно экспрессируют из определенных опухолевых клеток, в частности из мезотелиоматических клеток, опухолевых клеток поджелудочной железы и опухолевых клеток яичника, в то время как в нормальной ткани его экспрессия ограничена, что делает его целью изучения в развитии лечения опухолей (Argani, P. et al., Clin. Cancer Res. (2001) 7(12): 3862; Hassan, R., et al., dm. Cancer Res. (2004) 10(12 Pt 1):3937). Функция мезотелина не известна, также не было обнаружено никаких репродуктивных, гематологических или анатомических аномалий у мышей, у которых не хватало экспрессии гена мезотелина (Bera, Т.К. and I.Pastan, Mol. Cell. Biol. (2000) 20(8):2902).
Основанное на антителах целевое лечение экспрессирующих мезотелин раковых клеток было предложено для лечения рака легких, яичников и поджелудочной железы. Mab K1 было первым антителом полипептида мезотелина, связанного с мембраной, и было описано (Chang, К., et al., Int. J.Cancer, (1992) 50(3):373). Mab K1 было получено путем иммунизирования мышей. Вследствие малого сходства и низкого уровня поглощения антитела, иммунотоксин, состоящий из Mab K1, которое присоединено к химически укороченной модифицированной форме экзотоксина A Pseudomonas, не подходил для клинического развития. (2000) 23(4):473; Hassan, R., et al., Clin. Cancer Res. (2004) 10(12 Pt 1): 3937). Впоследствии были получены одноцепные антитела с более высоким уровнем сходства, включая SSl-(dsFv)-PE38, которые показали способность к уничтожению опухолевых клеток в искусственных условиях (Hassan, R., et al., Clin. Cancer Res. (2002) 8(11): 3520), а также эффективность в мышиной модели человеческих опухолей, экспрессирующих мезотелин (Fan, D., et al., Mol. Cancer Ther. (2002) 1(8): 595). Данные факты подтверждают, что изучение мезотелина поможет в развитии иммунотерапии для лечения различных видов рака. Было обнаружено, что SSl-(dsFv)-PE38 способно к быстрому очищению крови, и были совершены попытки увеличения молекулярного веса путем присоединения к гибридному белку полиэтиленгликоля (Filpula, D., et al., Bioconjugate Chem. (2007) 18(3): 773).
MS-1, MS-2 и MS-3 являются мезотелин-связывающими антителами, которые вызывают иммунную эффекторную активность на поверхности клеток благодаря их человеческому изотипу IgG1 и усваиваются клетками, экспрессирующими мезотелин (WO 2006/099141 А2). Одно из антител, неконъюгированное, химерическое (мышь/человек) IgG1 антимезотелиновое антитело MORAb 009, в настоящее время подвергается клиническому испытанию на выявление лечебных эффектов в лечении рака поджелудочной железы. Условием действия MORAb 009 является осуществление иммунных эффекторных функций, таких как ADCC (антителозависимая клеточная цитотоксичность) и функция блокирования.
Новые способы лечения с улучшенной способностью к борьбе с агрессивными видами рака, такими как рака яичников, поджелудочной железы и легких, необходимы и дадут преимущество в науке. Таким образом, настоящее изобретение предоставляет новые композиции конъюгатов, которые будут полезны в лечении, профилактике и/или диагностике расстройств, связанных с мезотелином, например рака.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к иммуноконъюгатам, включающим антитела, например моноклональные антитела или их мезотелин-связывающие фрагменты, которые присоединяются к цитотоксическим веществам, например майтансиноидам или их производным, и/или применяются с помощью одного или более дополнительных антираковых веществ. Иммуноконъюгаты изобретения могут быть использованы для лечения и/или диагностики и/или наблюдения за расстройствами, связанными с мезотелином, например раком.
Целью изобретения является создание иммуноконъюгатов, включающих антитела или антиген-связывающие фрагменты антител или их варианты, высокоселективных для 40 kDa, внеклеточной части предшественника полипептида мезотелина, и связывающих мезотелин в присутствии ракового антигена 125 (СА125; MUC16), и эффекторную часть. Особые характеристики антител мезотелина описаны в РСТ/ЕР2008/009756, а также в одном аспекте изобретения, сочетании их особой способности к специфичной иммунореакции с мезотелином в присутствии СА125 в комбинации с цитотоксическим веществом, например майтансиноидом, соединение способствует активности антител с функцией блокирования, которые соревнуются с СА125 за связывание с мезотелином.
В одном аспекте настоящего изобретения антитела или их фрагменты представляют собой IgG антитела или IgG фрагменты. Антитела или фрагменты могут также быть IgG1, IgG2a, IgG2b, IgG3, IgM, IgD, IgE, IgA, или IgM антителами. Fab фрагментами, F(ab')2 фрагментами, scFv фрагментами, Fv фрагментами, антителами двойных тел, линейными антителами, одноцепными антителами, биоспецифичными антителами, мультиспецифичными антителами или химерическими антителами (например, включающими каркас человеческого антитела, присоединенного к человеческому или нечеловеческому связывающему антитело участку, или каркас нечеловеческого антитела, присоединенного к человеческому или нечеловеческому связывающему антитело участку). Химерные антитела могут включать, например, участки каркаса антител из нечеловеческих источников, таких как, например, коровы, мыши, ламы, верблюда или кролика. Дальнейшую информацию о разработках антител можно найти в литературе, например, Holliger and Hudson, Nature Biotechnology, (Sep, 2005) 23: 1126-1136, на которую в настоящем документе есть ссылка. Указанные ранее фрагменты могут быть получены из иммуноглобулина или определенным способом, например, с помощью рекомбинантной экспрессии, в фрагментарной форме.
Антитела или их фрагменты настоящего изобретения можно сделать человеческими, отличающимися тем, что CDR последовательности или участки (например, CDR1, CDR2, CDR3) могут быть нечеловеческими, например мышиными.
Антитела или фрагменты антител настоящего изобретения или композиции, включающие антитела или фрагменты, могут включать цитотоксическое вещество, которое присоединено к антителу или его фрагменту. В одном аспекте цитотоксическое вещество представляет собой майтансиноид или его производное, тем не менее, имеются также другие цитотоксические вещества, которые могут включать, например, аплидин, ористатин, азарибин, анастрозол, азацитидин, блеомицин, бортезомид, бриостатин-1, бусульфан, калихеамицин, камптотецин, 10-гидроксикамптотецин, кармустин, целебрекс, хлорамбуцил, цисплатин, ириноцетан (CPT-I 1), SN-38, карбоплатин, кладрибин, циклофосфамид, цитарабин, дакарбазин, доцетаксил, дактиомицин, дауномицин глюкуронид, даунорубицин, дексаметазон. Любое из цитотоксических веществ может также включать их функциональные аналоги или производные.
В другом аспекте настоящее изобретение предоставляет иммуноконъюгаты, в которых цитотоксическое вещество не является иммунногенетическим, т.е. не увеличивает иммуногенетичность родительского антитела путем вовлечения клеточных эпитопов человека или млекопитающего, или Т клеточных эпитопов в технологию приготовления лекарственного средства. Композиции изобретения могут помимо антител и фрагментов (с указанным выше соединенным цитотоксическим веществом или без него) включать различные антираковые вещества, которые могут включать, например, блеомицин, доцетаксел (Таксотер), доксорубицин, эдатрексат, эрлотиниб (Тарцева), этопосид, финастерид (Проскар), флутамид (Эулексин), гемцитабин (Гемзар), гефитиниб (Ирреса), гозерелин ацетат (Золадекс), гранисетрон (Китрил), иматиниб (Гливек), ириноцетан (Кампто/Камптосар), ондансетрон (Зофран), паклитаксел (Таксол), пэгаспаргаза (Онкаспар), пилокарпин гидрохлорид (Саладжен), порфимер натрий (Фотофрин), интерлейкин-2 (Пролейкин), ритуксимаб (Ритуксан), топотецан (Гикамтин), трастузумаб (Герцептин), Триапин, винкристин, и винорелбин тартрат (Навельбин), или лечебные антитела или их фрагменты, или анти-ангиогенное вещество, такое как, например, ангиостатин, бевицизумаб (Avastin®), сорафениб (Nexavar®), бакулостатин, канстатин, маслин, анти-VEGF антитела или полипептиды, антитела с антиплацентарным фактором роста или пептиды, анти-Flk-l антитела, анти-Fit-l антитела или пептиды, ламинин пептиды, фибронектин пептиды, плазминогенные активаторные ингибиторы, тканевые металлопротеиназа ингибиторы, интерфероны, интерлейкин 12, IP-IO, Gro-β, тромбоспондин, 2-метоксиоэстрадиол, полифериновые белки, карбоксимидотриазол, CM1O1, маримастат, пентосан полисульфат, ангиопоэтин 2, интерферон-альфа, гербимицин A, PNU145156E, 16К пролактиновый фрагмент, линомид, талидомид, пентоксифилин, генистеин, TNP-470, эндостатин, паклитаксел, аккутин, цидофовир, винкристин, блеомицин, AGM-1470, тромбоцидный фактор 4 или миноциклин.
Настоящее изобретение далее предоставляет в другом аспекте метод лечения расстройства, связанного с мезотелином, путем регулирования эффективного для лечения количества иммуноконъюгатов изобретения или композиций изобретения, которые включают иммуноконъюгаты изобретения. Расстройство, связанное с мезотелином, может включать, например, рак, такой как рак с образованием солидной опухоли. Солидная опухоль может быть в яичниках, поджелудочной железе, респираторном тракте, легком, толстой кишке, желудке, пищеводе, шейке матки, печени, груди, голове и шее.
Эти и другие примеры осуществления изобретения раскрыты и наглядно показаны в следующем Подробном Описании.
ОПИСАНИЕ ФИГУР
Фигура 1 показывает противоопухолевую эффективность антимезотелинового иммуноконъюгата MF-T-SPDB-DM4 в клетках опухоли поджелудочной железы, трансфекцированной мезотелином, как в ксенотрансплантатной модели (А), трансфекцированной мезотелином, так и в контрольных нетрансфекцированных опухолях.
Фигура 2 показывает противоопухолевую эффективность антимезотелиновых иммуноконъюгатов со стойкими и расщепляемыми, полярными и неполярными линкерами в HeLaMATU ксенотрансплантатной модели с клетками раковой опухоли, экспрессирующими мезотелин внутренне.
Фигура 3 показывает противоопухолевую эффективность антимезотелиновых иммуноконъюгатов со стойкими и расщепляемыми, полярными и неполярными линкерами как в ксенотрансплантатной модели (А), трансфекцированной мезотелином, так и в нетрансфекцированных контрольных опухолях (В).
Фигура 4 показывает пример кривой зависимости от дозы токсичности MF-T-SPDP-DM4 на мезотелин-позитивных HelaMatu клетках.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение основано на открытии новых иммуноконъюгатов, которые являются мезотелин-специфичными или имеют сильное сходство с ним и могут принести пользу в описанном в изобретении лечении. Иммуноконъюгаты изобретения могут быть использованы в различных контекстах, которые наиболее полно описаны в настоящем документе. Необходимо понимать настоящее изобретение не ограничено особыми деталями, изложенными в настоящем документе, касательно аспектов изобретения, включая антимезотелиновые антитела, иммуноконъюгаты, методы лечения, протоколы, линии клеток, виды или семейства животных, конструкты и реагенты, которые могу изменяться. Также необходимо понимать, что терминология изобретения используется только для описания частных примеров осуществления изобретения и не ограничивает цель настоящего изобретения.
Определения
Если не оговорено иначе, все технические и научные термины в данном документе имеют значение, общепринятое в области, к которой принадлежит изобретение. Следующие ссылки могут, тем не менее, предлагать область, к которой принадлежит изобретение, с общим значением множества терминов, и могут использоваться, пока такие определения соответствуют значению, общепринятому в науке. Такие ссылки включают, но не ограничены. Singleton et ah, Dictionary of Microbiology and Molecular Biology (2d ed. 1994); The Cambridge Dictionary of Science and Technology (Walker ed., 1988); Hale & Marham, The Harper Collins Dictionary of Biology (1991); и Lackie et al., The Dictionary of Cell & Molecular Biology (3d ed. 1999); и Cellular and Molecular Immunology, Eds. Abbas, Lichtman and Pober, 2nd Edition, W.B.Saunders Company. Также можно обратиться за справкой касательно любых дополнительных технических ресурсов, доступных для научного лица, содержащих определения терминов, используемых в настоящем документе, имеющих значение, общепринятое в науке. Для целей настоящего изобретения далее даны определения следующих терминов. Дополнительные термины определены в другом месте описания. Используемые в настоящем документе и в приложенной формуле изобретения формы единственного числа подразумевают множественное число, если контекстом не подразумевается иное. Так, например, под «геном» подразумевается один или более генов, а также их эквиваленты, известные в науке.
В соответствии с документом термин «антитело» включает молекулы иммуноглобулина (например, любой вид, включающий IgG, IgE, IgM, IgD, IgA и IgY, и/или любой класс, включающий IgG1, IgG2, IgG3, IgG4, IgA1 и Ig A2), изолированные из естественной среды или полученные рекомбинантными средствами. Подразумевается, что антитела включают связывающие антиген фрагменты антител, такие как Fab, F(ab')2, scFv (одноценый Fvs), Fv, одноцепные антитела, двойные тела, дисульфид-связанный Fvs (sdFv), и фрагменты, включающие VL или VH домен, полученный из исходных иммуноглобулинов или с помощью рекомбинантных средств.
Антитела и/или связывающие антиген фрагменты антител настоящего изобретения могут быть моноспецифичными (например, моноклональными), биспецифичными, триспецифичными или более. Мультиспецифичные антитела могут быть специфичными для разных эпитопов антигена или для эпитопов более чем одного антигена. Смотрите, например, публикации WO 93/17715; WO 92/08802; WO 91/00360; WO 92/05793; Tutt, et al., 1991, J.Immunol. 147:60 69; U.S.Pat. Nos. 4,474,893; 4,714,681; 4,925,648; 5,573,920; 5,601,819; Kostelny et al., 1992, J.Immunol. 148:1547 1553, каждая из которых включена в данную заявку посредством ссылки.
Связывающие антиген фрагменты антител могут содержать различные области как отдельно, так и в сочетании с целым шарнирным участком, СН1, СН2, СН3 и CL доменом или их частями. Также в изобретение включены связывающие антиген фрагменты антител, также содержащие любую комбинацию различных участков с шарнирным участком, СН1, СН2, СН3 и CL доменом.
Предпочтительно, чтобы антитела или связывающие антиген фрагменты антител являлись гуманизированными, принадлежали человеку, мыши (например, мыши или крысе), ослу, овце, кролику, козлу, морской свинке, семейству верблюдов, лошади или цыпленку. В соответствии с документом «человеческие» антитела включают антитела, имеющие аминокислотную последовательность человеческого иммуноглобулина, и антитела, изолированные от библиотеки человеческого иммуноглобулина, от человеческих В-клеток или животных, трансгенных для одного или более человеческого иммуноглобулина, как описано ниже и, например, в Патенте США №5,939,598 Kucherlapati et al. Термин «антитело» также относится к другим белковым каркасам, которые способны направить CDR вставки антитела в ту же активную связывающую структуру, что и у естественных антител, таким образом, что связывание целевого антигена вместе с этими химерическими белками сохраняется относительно связывающей активности естественного антитела, из которого были получены CDR. В соответствии с настоящим документом термин «гуманизированные» формы нечеловеческих антител (например, мышей) означает химерические антитела, которые содержат минимальную последовательность, полученную из нечеловеческого иммуноглобулина. Большая часть гуманизированных антител представляет собой человеческие иммуноглобулины (антитело-реципиент), в которых гиперпеременные радикалы участков (например, определяющие комплементарность участки «CDR») реципиента заменены гиперпеременными радикалами участков (CDRs) из нечеловеческих видов (антитело-донор), таких как мышь, крыса, кролик, или нечеловеческих приматов, имеющих желаемую специфичность, сходство и активность. В некоторых случаях радикалы каркасного участка человеческого иммуноглобулина могут быть заменены соответствующими нечеловеческими радикалами. Более того, гуманизированные антитела могут содержать радикалы, которых не обнаружено в антителе-реципиенте или антителе-доноре. Такие модификации проводятся для дальнейшего улучшения активности антител. В целом, гуманизированное антитело может содержать почти все из, по меньшей мере, одного или обычно двух вариабельных доменов, в которых все или почти все гипервариабельные участки соответствуют участкам нечеловеческого иммуноглобулина и все или почти все каркасные участки принадлежат человеческой иммуноглобулиновой последовательности. Гуманизированное антитело может также содержать, по меньшей мере, часть иммуноглобулинового постоянного участка, присущего человеческому иммуноглобулину. Для справки, см. Jones, et al., (Nature 321:522-525, 1986); Reichmann, et al., (Nature 332:323-329, 1988); и Presta, (Curr. Op.Struct. Biol. 2:593-596, 1992). Создание гуманизированных антител можно найти в Патентах США №№.7,049,135, 6,828,422, 6,753,136, 6,706,484, 6,696,248, 6,692,935, 6,667,150, 6,653,068, 6,300,064, 6,294,353, и 5,514,548, которые включены в данную заявку во всей полноте посредством ссылки.
В соответствии с документом термин «одноцепные Fv» или «sFv» фрагменты антител включает VH и VL домены антитела, находящиеся в одной полипептидной цепи. Обычно Fv полипептид далее содержит полипептидный линкер между VH и VL доменами, который помогает sFv создать желаемую структуру для связывания антигена. Для справки смотрите Pluckthun (The Pharmacology of Monoclonal Antibodies. Vol.113, Rosenburg and Moore eds. Springer- Verlag, New York, pp.269-315, 1994), которая включена в данную заявку во всей полноте посредством ссылки.
Термин «двойные тела» относится к маленьким фрагментам антител с двумя антиген-связывающими участками, фрагменты которых содержат вариабельный домен с тяжелой цепью (VH), соединенного с вариабельным доменом с легкой цепью (VL) в одной и той же полипептидной цепи (VH-VL). С помощью линкера, слишком короткого для связывания двух доменов на одной и той же цепи, домены заставляют соединиться с дополнительными доменами на другой цепи и создать два антиген-связывающих участка. Двойные тела более подробно описаны, например, в ЕР 404,097; WO 93/11161; и Hollinger, et al., (Proc. Natl. Acad. Sci. USA 90: 6444-6448, 1993), каждая из которых включена в данную заявку во всей полноте посредством ссылки.
Выражение «линейные антитела» относится к антителам, описанным в науке, например, в Zapata, et al., (Protein Eng. 8(10): 1057-1062, 1995), которая включена посредством ссылки. Вкратце, такие антитела содержат пару соединенных Fd сегментов (VH-CHI-VH-CHI), которые формируют пару антиген-связывающих участков. Линейные антитела могут быть биспецифичными или моноспецифичными.
Термин «моноклональное антитело», используемый в данном документе, относится к антителу, полученному из совокупности достаточно гомогенных антител, то есть индивидуальных антител 10, содержащих идентичную совокупность, за исключением возможных естественных мутаций, которые могут наблюдаться в минимальных количествах. Моноклональные антитела высоко специфичны, то есть направлены на единичный антигенный участок. Более того, в отличие от традиционных (поликлональных) препаратов антител, которые обычно включают различные антитела, направленные на разные детерминанты (эпитопы), каждое моноклональное антитело направлено на единичный детерминант на антигене. Определение «моноклональный» указывает на характер антитела, полученного из достаточно гомогенной совокупности антител, и не подразумевает необходимость его наличия для создания антитела любым способом. Например, моноклональные антитела, используемые в соответствии с настоящим изобретением, могут быть созданы с помощью метода гидриомы, впервые описанном Kohler, et al., (Nature 256:495, 1975), или метода рекомбинантной ДНК (смотрите, например. Патент США №4,816,567). Моноклональные антитела могут быть также изолированы от фаговых библиотек антител с помощью методики, описанной, например, в Clackson, et al., (Nature 352:624-628, 1991) и Marks, et al., (J.MoI.Biol. 222: 581-597, 1991).
Моноклональные антитела также включают «химерические» антитела, в которых доля тяжелой и/или легкой цепи идентична или соответствует гомологически соответствующим последовательностям в антителах, полученных из определенного вида или принадлежащих определенному классу или подклассу антител, в то время как остаток цепи (цепей) идентичен или соответствует гомологически соответствующим последовательностям в антителах, полученных из другого вида или принадлежащих другому классу или подклассу антител, а также фрагменты таких антител, пока они проявляют описанную биологическую активность (смотрите, например, Патент США №4,816,567; и Morrison, et al., Proc. Natl. Acad. Sci. USA 81: 6851-6855, 1984, каждый из которых включен посредством ссылки).
В соответствии с документом термины «биологический образец» или «образец пациента», используемые в настоящем документе, относятся к образцу, полученному из организма или компонентов (например, клеток) организма. Образцы могут состоять из любой биологической ткани или жидкости. Образец может быть «клиническим», то есть полученным от пациента. Такие образцы включают, но не ограничиваются ими, слюну, кровь, серозную жидкость, плазму, клетки крови (например, белые тельца), образцы ткани, биопсии, мочу, жидкость брюшной полости и плевральную жидкость, сперму, грудной экссудат, спинномозговую жидкость, слезы, секретирующую слизь, лимфу, цитозоли, асциты, амниотическую жидкость, жидкость из мочевого пузыря, бронхиоальвеолярную жидкость или их клетки. Образец пациента может быть свежим или замороженным и обрабатываться гераримном, цетратом или этилендиаминтетрауксусной кислотой. Биологические образцы могут также включать части тканей, например замороженные части для гистологических целей.
Термин «рак» включает, но не ограничивается ими, солидные опухоли, такие как рак поджелудочной железы, груди, дыхательных путей, мозга, репродуктивных органов, пищеварительного тракта, мочевых путей, глаза, печени, кожи, головы и шеи, щитовидной железы, паращитовидной железы и их отдаленные метастазы. Термин также включает саркому, лимфому, лейкемию и миелому плазматической клетки.
Опухоли дыхательных путей включают, но не ограничиваются ими, мелкоклеточную и немелкоклеточную раковую опухоль легких, а также бронхиальную аденому и плевролегочную бластому. Опухоли груди включают, но не ограничиваются ими, инвазивную проточную раковую опухоль, инвазивную лобулярную раковую опухоль, проточный преинвазитивный рак и лобулярный преинвазитивный рак. Опухоли мозга включают, но не ограничиваются ими, глиому стволовой части мозга и гипофталмическую глиому, мозжечковую или мозговую астроцитому, медуллобластому, эпендиному, а также нейроэктодермальную и пинеальную опухоль. Опухоли мужских репродуктивных органов включают, но не ограничиваются ими, рак простаты и тестикулярный рак. Опухоли женских репродуктивных органов включают, но не ограничиваются ими, внутриматочный, шейный, яичниковый, вагинальный и относящийся к женским наружным половым органам рак, а также рак матки. Опухоли пищеварительного тракта включают, но не ограничиваются ими, рак анальный, толстой кишки, колоректальный, пищеводный, желчного пузыря, желудка, ректальный, тонкой кишки и слюнной железы. Опухоли мочевых путей включают, но не ограничиваются ими, рак мочевого пузыря, полового члена, почки, почечной лоханки, мочеточника и уретральный. Рак глаза включает, но не ограничивается ими, внутриглазную меланому и ретинобластому. Опухоли печени включают, но не ограничиваются ими, рак гепатоцеллюлярный (рак клеток печени с фиброламеллярным вариантом или без него), холангиоцеллюлярный (внутрипеченочный рак желчного протока) и смешанный гепатоцеллюлярный холангитный. Рак кожи включает, но не ограничивается ими, рак плоскоклеточный, саркома Калоши, злокачественная меланома, рак клеток кожи Меркеля и немеланомный рак кожи. Рак головы и шеи включает, но не ограничивается ими, рак гортанный/ ипофарингеальный/ осоглоточный/ рофарингеальный и рак губ и ротовой полости. Лимфомы включают, но не ограничиваются ими, лимфомы, связанные со СПИДом, не относящаяся к лимфоме Ходжкина, кожная Т-клеточная лимфома, болезнь Ходжкина и лимфома центральной нервной системы. Саркома включает, но не ограничивается ими, саркому мягкий тканей, остеогенную саркому, злокачественную фиброзную гистиоцитому, лимфосаркому и рабдомиосаркому. Лейкемия включает, но не ограничивается ими, лейкому острую миелоидную, острую лимфобластическую, хроническую лимфицитическую, хроническую миелогенную и лейкому клеток волос.
Термин «эпитоп», используемый в избретении, означает любой антигенный детерминант на антигене, например белок мезотелина, к которому антитело присоединяется через антиген-связывающий участок. Детерминанты или антигенные детерминанты обычно состоят из химически активных поверхностных групп молекул, таких как боковые цепи аминокислот или сахара, и обычно имеют специфические трехразмерные структурные характеристики, а также специфические зарядные характеристики.
Термин «специфически иммунореактивный» относится к связывающей реакции между антителом и белком, соединению или антигену с эпитопом, обнаруженным антиген-связывающим участком антитела. Связывающая реакция определяет присутствие белка, антигена или эпитопа с обнаруженным эпитопом среди 10 присутствия гетерогенной совокупности белков и других биологии. В контексте иммунологического анализа специфически иммунореактивные антитела могут присоединяться к белку с обнаруженным эпитопом и в меньшей степени к другим белкам без эпитопа, присутствующим в образце. При естественных условиях «специфически иммунореактивный» может относиться к условиям, в которых в животном формируется иммунная реакция на вакцину или антиген например гуморальная реакция на антиген (создание антигенов, вакцину, белок, соединение или антиген, находящийся в иммунологически реактивных условиях), или клеточно-опосредованная реакция (также «клеточная иммуная реакция», то есть реакция, опосредованная Т-лимфоцитами, на вакцину, белок, соединение или антиген). Термин «иммунологически реактивные условия», используемый в настоящем документе, употребляется в контексте иммунологического анализа или реакции в естественных условиях, причем физические условия реакции, включая, например, температуру, концентрацию соли, рН, реагенты и их концентрации, концентрации антигена и родственного антитела, специфически иммунореактивных по отношению к антигену, созданы таким образом, чтобы осуществить присоединение родственного антитела к антигену. Иммунологически реактивные условия зависят от характера антитело-связывающей реакции и обычно используются в протоколах иммунологических анализов. Смотрите Harlow and Lane (1988) Antibodies: A Laboratory Manual, Cold Spring Harbor Publications, New York, для описания характера и условий иммунологических анализов. Термин «пациент» или «объект», используемый в настоящем документе, включает млекопитающих (например, людей или животных).
Термин «инвариантное присоединение» определенного антитела к мезотелину, используемый в настоящем документе, относится к его способности присоединяться к мезотелину на различных раковых клеточных линиях, экспрессирующих мезотелин различной формы. Инвариантное связывание может быть вызвано, но не обязательно, тем, что антитела или антиген-связывающие фрагменты антител или их варианты обнаруживают эпитоп мезотелина, который не скрыт другим внеклеточным антителом, таким как раковый антиген 125 (СА125), взаимодействующий с мезотелином. Для инвариантно связывающих антител значение ЕС50, определяемое FACS-титрованием на двух отдельных раковых клеточных линиях, может отличаться не более чем на 10 свертываний или предпочтительно 5 свертываний, и наиболее предпочтительно от 1 до 3 свертываний.
В соответствии с документом термин «иммуноконъюгат» относится к соединенной молекуле, содержащей, по меньшей мере, одно антитело или его антиген-связывающий фрагмент, связанный с цитотоксическим веществом, например майтансиноидом или его производным, предпочтительно с помощью подходящей соединяющей группы или ее предшественника.
Иммуноконъюгаты
Изобретения
Настоящее изобретение относится к способам, замедляющим рост мезотелин-позитивных раковых клеток и развитие неопластической болезни с помощью антимезотелиновых иммуноконъюгатов. Часть антител предоставленных иммуноконъюгатов специфически иммунореактивна по отношению к 40 kDa, домену с С-концом мезотелинового предшествующего полипептида (SEQ ID NO 36), который в настоящем документе называется «мезотелином».
В одном аспекте изобретения антитела, связывающие антиген фрагментов антител и варианты антител и фрагментов изобретения описаны в РСТ/ЕР2008/009756 и состоят из вариабельного участка лепкой цепи и вариабельного участка тяжелой цепи. Варианты антител или связывающих антиген фрагментов антител, рассмотренных в изобретении, являются молекулами, в которых соединяющая активность антитела или связывающего антиген фрагмента антитела для мезотелина сохраняется.
Настоящее изобретение также относится к иммуноконъюгатам, состоящим из антимезотелиновых антител, связывающих антиген фрагментов антител и вариантов антител и фрагментов изобретения, отличающихся от описанных в (РСТ/ЕР2008/009756), и присоединяются к химиотерапевтическому агенту, например майтансиноидам или их производным.
Майтансиноиды, которые могут быть использованы в настоящем изобретении, хорошо известны в науке и могут быть получены из естественных источников с помощью известных методов или синтетически с помощью известных методов.
Примеры подходящих майтансиноидов включают майтансинол и аналоги майтансинола. Примеры подходящих аналогов майтансинола включают аналоги с модифицированным ароматическим ядром и модификациями на других позициях.
Конкретные примеры подходящих аналогов майтансинола с модифицированным ароматическим ядром включают:
(1) С-19-дехлоро (Патент США №4,256,746) (полученный в результате ЛАГ-восстановления ансамитоцина Р2);
(2) С-20-гидрокси (или С-20-дементил)+/-С-19-дехлоро (Патенты США №№4,361,650 и 4,361,650) (полученный в результате деметилирования с использованием Стрептомицитов или Актиномицитов или дехлорирования с использованием ЛАГ); и
(3) С-20-деметокси, С-20-ацилокси (-OCOR), +/-дехлоро (Патент США №4,294,757) (полученный в результате ацилирования с использованием хлористых ацилов).
Конкретные примеры подходящих аналогов майтансинола с модификациями на других позициях включают:
(1) C-9-SH (Патент США №4,424,219) (полученный в результате реакции майтансинола с H2S or P2S5);
(2) С-14-алкоксиметил (деметокси/CH2OR) (Патент США №4,331,598);
(3) С-14-гидроксиметил или ацилоксиметил (CH2OH или CH2OAc) (Патент США №4,450,254) (полученный из Nocardia);
(4) С-15-гидрокси/ацилокси (Патент США №4,364,866) (полученный в результате трансформации майтансинола Стрептомицитами);
(5) С-15-метокси (Патенты США №№.4,313,946 и 4,315,929) (полученный из Trewia nudiflora);
(6) С-18-N-деметил (Патенты США №№.4,362,663 и 4,322,348) (полученный в результате деметилирования майтансинола Стрептомицитами); и
(7) 4,5-деокси (Патент США №4,371,533) (полученный в результате восстановления майтансинола титан-трихлоридом/ЛАГ).
Синтез майтансиноидов, содержащих тиол, применяемых в настоящем изобретении, подробно описан в Патентах США №№.5,208,020, 5,416,064, и 7,276,497.
Предположительно применимы майтансиноиды с частью тиола на позициях С-3, С-14, С-15 или С-20. Позиция С-3 предпочтительна и позиция майтансинола С-3 наиболее предпочтительна. Также предпочтительны майтансиноид N-метил-аланин-содержащий с частью тиола С-3 и майтансиноид N-метил-цистеин-содержащий с частью тиола С-3, и их аналоги. Предпочтительные майтансиноиды описаны в Патентах США 5,208,020; 5,416,064; 6,333.410; 6,441,163; 6,716,821; RE39.151 и 7,276,497, на которые в настоящем документе есть ссылка. В предпочтительном варианте осуществления изобретения эстерифицированный майтансинол получают из N2'-деацетил-N2'-(3-меркапто-1-оксопрофил)-майтансин (DM1, CAS Reg. No 139504-50-0), N2'-деацетил-N2'-(4-меркапто-1-оксопентил)-майтансин (DM3, CAS Per. №796073-54-6), и N2'-деацетил-N2'-(4-метил-4-меркапто-1-оксопентил)-майтансин (DM4 CAS Per. №796073-69-3).
В настоящем документе имеется ссылка на следующие репрезентативные антитела изобретения: "MF-J", "MOR06640", "MF-226", и "MF-T". MF-J представляет собой антитело с вариабельным тяжелым участком, соответствующим SEQ ID NO: 28 (ДНК)/SEQ ID NO: 20 (белок), и вариабельным легким участком, соответствующим SEQ ID NO: 32 (ДНК)/SEQ ID NO: 24 (белок). MOR 06640 представляет собой антитело с вариабельным тяжелым участком, соответствующим SEQ ID NO: 29 (ДНК)/SEQ ID NO: 21 (белок), и вариабельным легким участком, соответствующим SEQ ID NO: 33 (ДНК)/SEQ ID NO: 25 (белок). MF-226 представляет собой антитело с вариабельным тяжелым участком, соответствующим SEQ ID NO: 30 (ДНК)/SEQ ID NO: 22 (белок) и вариабельным легким участком, соответствующим SEQ ID NO: 34 (ДНК)/SEQ ID NO: 26 (белок). MF-T представляет собой антитело с вариабельным тяжелым участком, соответствующим SEQ ID NO: 31 (ДНК)/SEQ ID NO: 23 (белок,) и вариабельным легким участком, соответствующим SEQ ID NO: 35 (ДНК)/seq ID NO: 27 (белок). Изобретение не ограничено этими антителами, которые используются в качестве примеров. Другие применимые антитела описаны, например, в РСТ/ЕР2008/009756.
В одном аспекте изобретение предоставляет иммуноконъюгаты, которые особенно иммунореактивны к мезотелину в присутствии ракового антигена 125 (CA 125/MUC 16) и тем самым эффективно воздействут на раковые клетки, экспрессирующими мезотелин и СА125, например клетки OVCAR-3.
В других аспектах изобретение предоставляет иммуноконъюгаты, которые особенно иммунореактивны к одной или более аминокислотам эпитопов антител MOR 06640 или MF-T. В определенных аспектах указанные иммуноконъюгаты особенно иммунореактивны, по меньшей мере, к двум, трем, четырем, пяти или шести аминокислотам эпитопов антител MOR 06640 или MF-T. В определенных аспектах иммуноконъюгаты настоящего изобретения особенно иммунореактивны к одной или более аминокислотам эпитопа, обнаруженного антителом MOR 06640. В альтернативных аспектах иммуноконъюгаты настоящего изобретения особенно иммунореактивны к одной или более аминокислотам эпитопа, обнаруженного антителом MF-T.
В другом аспекте изобретение предоставляет иммуноконъюгаты, имеющие антиген-связывающий участок, который особенно иммунореактивен или имеет высокое сходство по отношению к одному или более участкам мезотелина, аминокислотная последовательность которого описана SEQ ID NO: 36. Указано, что иммуноконъюгат имеет высокое сходство с антигеном, при условии, что сходство составляет, по меньшей мере, 100 нМ (одновалентное сходство Fab фрагмента). Иммуногонъюгат изобретения предпочтительно может быть особенно иммунореактивным к мезотелину со сходством приблизительно менее 100 нМ, более предпочтительно приблизительно менее 60 нМ, а также более предпочтительно приблизительно менее 30 нМ. Далее предпочтительны антитела, которые соединяются с мезотелином со сходством приблизительно менее 10 нМ, и более предпочтительно приблизительно менее 3 нМ. Например, сходство антитела изобретения с по отношению к мезотелину может быть около 9,1 нМ или 0,9 нМ (одновалентное сходство IgG1 характера).
Способы применения
Термин «лечение» включает любой процесс, действие, применение, терапию или тому подобное, при котором субъект (пациент), включая человека, получает медицинскую помощь с помощью объекта, улучшающего состояние субъекта, прямо или косвенно, или замедление развития болезни или расстройства субъекта, или улучшение по меньшей мере одного симптома болезни или расстройства в результате лечения.
Термин «комбинированное лечение» или «со-лечение» означает применение двух или более лечебных средств для лечения болезни, состояния и/или расстройства. Такое применение включает одновременное применение двух или более лечебных средств, например, в одной капсуле, содержащей фиксированное количество активных ингредиентов, или в нескольких отдельных капсулах для каждого вещества-ингибитора. Кроме того, такое применение включает последовательное использование каждого вида лечебного средства. Порядок применения двух или более последовательно применяемых лечебных средств не ограничен. Фраза «терапевтически эффективное количество» означает количество каждого применяемого вещества, необходимого для получения положительной динамики болезни, состояния и/или серьезности расстройства, и/или их симптомов, и одновременно избегая или сводя к минимуму побочные эффекты данного лечения.
Термин «фармацевтически приемлемый» означает, что рассматриваемый препарат подходит для использования в фармацевтическом продукте.
Иммуноконъюгаты настоящего изобретения предположительно полезны в качестве лечебных средств. Соответственно вариант осуществления настоящего изобретения включает метод лечения различного состояния пациента (включая млекопитающих), который подразумевает применение по отношению к указанному пациенту композиции, содержащей эффективной для лечения данного состояния количество иммуноконъюгатов.
Иммуноконъюгаты настоящего изобретения могут быть использованы в лечении или профилактике болезней и/или состояний, ассоциирующихся с белком мезотелина. Эти болезни и/или состояния включают, например, рак, такой как карцинома поджелудочной железы, яичников, желудка, пищевода, шейки матки, толстой кишки, печени, дыхательных путей и легких. Настоящее изобретение также относится к методам улучшения симптомов расстройства, при котором мезотелин повышается или экспрессируется другим атипичным способом. Такие расстройства включают, без ограничений, карциному поджелудочной железы, яичников, желудка, пищевода, шейки матки, толстой кишки, печени, дыхательных путей и легких (смотрите, например, (Liao, Cancer Res. 57: 2827-2831, 1997; Turner, Hum. Pathol. 28: 740-744, 1997; Liao, и др., Am. J.Pathol. 145:598-609, 1994; Saarnio, и др., Am. J.Pathol. 153: 279-285, 1998; Vermylen, и др., Eur. Respir. J. 14: 806-811, 1999). В одном варианте осуществления изобретения терапевтически эффективная доза иммуноконъюгатов изобретения применяется к пациенту с расстройством, в котором мезотелин повышается.
Иммуноконъюгаты настоящего изобретения можно применить отдельно или в сочетании с одним или более дополнительным веществом. Комбинированное лечение включает применение единичной фармацевтической дозы лекарственного средства, которая содержит иммуноконъюгат настоящего изобретения и дополнительные лечебные средства, а также применение иммуноконъюгата настоящего изобретения и каждого дополнительного лечебного средства с их собственной фармацевтической дозой лекарственного средства. Например, иммуноконъюгат настоящего изобретения и лечебное средство можно применить к пациенту одновременно в виде одной пероральной дозировочной композиции или каждый по отдельности.
При использовании отдельных дозированных препаративных форм иммуноконъюгат настоящего изобретения, а также одно или несколько дополнительных лечебных средств могут применяться фактически в одно и то же время (например, параллельно) или по отдельности в разное время (например, последовательно). Порядок применения агентов не ограничен.
Например, в одном случае использование антимезотелинового иммуноконъюгата данного изобретения вместе с одним или более противоопухолевым средством для усиления действия антимезотелинового иммуноконъюгата или противоопухолевого средства (средств), либо обоих предусмотрено при лечении болезней, связанных с мезотелином, таких как рак. Подобное комплексное лечение может также использоваться для предупреждения рака, предупреждения повторения рака, для предупреждения распространения или метастаза рака, либо для ослабления или улучшения симптомов, связанных с раком.
Одно или более противоопухолевое средство может содержать любое известное и подходящее в данной области соединение, такое как, например, химиоагенты, другие иммунотерапевтические средства, противоопухолевые вакцины, антиангиогенные средства, цитокины, гормональное лечение, генотерапию, а также лучевую терапию. Химиоагент (или «противоопухолевое средство» или «противоопухолевый агент» или «терапевтическое средство для лечения рака») относится к любой молекуле или соединению, помогающему в лечении рака. К примерам химиоагентов, предусмотренных настоящим изобретением, относятся цитозина арабинозид, таксоиды (например, паклитаксел, доцетаксел), антитубулиновые агенты (например, паклитаксел, доцетаксел, эпотилон В или его аналоги), макролиды (например, ризоксин), цисплатин, карбоплатин, адриамицин, тенопозид, митозантрон, дискодермолид, элетеробин, 2-кладрибин, алкилирующий агент (например, циклофосфамид, хлорметин, тиоепа, хлорамбуцил, мелфалан, кармустин (BSNU), ломустин (CCNU), циклотосфамид, бусульфан, дибромоманнитол, стрептозотоцин, митомицин С, цис- дихлородиамин платинум (II) (DDP) цисплатин, тио-тера), антибиотики (например, дактиномицин бывший актиномицин), блеомицин, митрамицин, антрамицины, антиметаболит (например, метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабин, флавопиридол, 5-флуороурацил, флударабин, гемцитабин, дакарбазин, термозоламид), аспарагиназа, бацилла кальметте и гуэрин, дифтерийный токсин, гексаметилмеламин, гидроксикарбамид, LYSODREN.RTM, аналоги нуклеозид, растительный алкалоид (например, таксол, паклитаксел камптотецин, топотекан, иринотекан (CAMPTOSAR, CPT-I 1), винкристин, алкалоиды барвинка, такие как винбластин), подофиллотоксин (включая производные, такие как эпидофиллотоксин, VP-16 (этопозид), VM-26 (тенипозид)), цитохалазин В, кольцин, грамицидин D, бромистый этидий, эметин, митомицин, прокарбазин, хлорметин, антрациклины (например, даунорубицин (бывший дауномидин), доксорубицин, липосомальный доксорубицин), дигидроксиантрациндион, митоксантрон, митрамицин, актиномицин D, прокаин, тетракаин, лидокаин, пропранолол, пуромицин, антимитотический агенты, абрин, рицин А, псевдомон экзотоксин, фактор роста нервов, тромбоцит, полученные из фактора роста, тканевой активатор плазминогена, альдеслейкин, аллютамин, анастрозол, бикалутамид, биомицин, бусульфан, капецитабин, карбоплатин, хлорабузил, кладрибин, циларабин, дактиномицин, эстрамузин, флоксурид, гамцитабин, гозерелин, идарубицин, итосфамид, лаупролид ацетат, левамизол, ломуслин, хлорметин, магестрол, ацетат, меркаптопурин, месна, митоланк, пэгаспаргаза, пентослатин, пикамин, риуксимаб, кампат-1, страплозоцин, тиогуанин, третиноин, винорелбин, или любые другие фрагменты, члены семейств или их производные, включая фармацевтически приемлемые соли. Композиции, содержащие один или несколько химиоагентов (например, FLAG, CHOP), также предусмотрены настоящим изобретением. FLAG содержит флударабин, цитозина арабинозид (цитарабин), а также Г-КСФ. CHOP содержит циклофосфамид, винкристин, доксорубицин и преднизон.
Химиоагент может быть антиангиогенное средством, таким как, например, ангиостатин, бевацизумаб (авастин®), сорафениб (нексавар®), бакулостатин, канстатин, маспин, антитела ингибитора фактора роста эндотелия сосудов или пептиды, антитела антиплацентного фактора роста или пептиды, антитела анти-Flk-1, антитела анти-Fit-l или пептиды, ламинин пептиды, фибронектин пептиды, ингибиторы активатора плазминогена, тканевые металлопротеиназовые ингибиторы, интерфероны, интерлейкин 12, IP-10, Gro-β, тромбоспондин, 2-метоксиэстрадиол, пролиферин связанный белок, карбоксиамидотриазол, СМ101, маримастат, пентозан полисульфат, ангиопоэтин-2, альфа-интерферон, гербимицин A, PNU145156E, 16К фрагмент пролактина, линомид, талидомид, пентоксифиллин, генистеин, NP-470, эндостатин, паклитаксел, аккутин, цидофовир, винкристин, блеомицин, AGM- 1470, тромбоцитарный фактор 4 или миноциклин.
В одном случае указанный химиоагент представляет собой гемцитабин дозой от 100 до 1000 мг/м2/цикл. В одном варианте изобретения указанный химиоагент представляет собой дакарбазин дозой от 200 до 4000 мг/м2/цикл. В противном случае указанная доза составляет от 700 до 100 мг/м2/цикл. Существует также вариант, где указанный химиоагент представляет собой флударабин дозой от 25 до 50 мг/м2/цикл. В противном случае указанный химиоагент представляет собой цитозина арабинозид (нитарабин) дозой от 200 до 2000 мг/м2/цикл. Существует также вариант, где указанный химиоагент представляет собой доцетаксел дозой от 1,5 до 7,5 мг/кг/цикл. В ином случае указанный химиоагент представляет собой паклитаксел дозой от 5 до 15 мг/кг/цикл. Существует также вариант, где указанный химиоагент представляет собой цисплатин дозой от 5 до 20 мг/кг/цикл. В ином случае указанный химиоагент представляет собой 5-флуороурапил дозой от 5 до 20 мг/кг/цикл. Существует также вариант, где указанный химиоагент представляет собой доксорубицин дозой от 2 до 8 мг/кг/цикл. В ином случае, указанный химиоагент представляет собой эпидофиллотоксин дозой от 40 до 160 мг/кг/цикл. Сущесвтует также вариант, где химиоагент представляет собой циклофосфамид дозой от 50 до 200 мг/кг/цикл. В ином случае, указанный химиоагент представляет собой иринотекан дозой от 50 до 150 мг/м2/цикл. Существует также вариант, где указанный химиоагент представляет собой винбластин дозой от 3,7 до 18,5 мг/м2/цикл. В противном случае, указанный химиоагент представляет собой винкристин дозой от 0,7 до 2 мг/м2/цикл. Существует также вариант, где указанный химиоагент представляет собой метотрексат дозой от 3,3 до 1000 мг/м2/цикл.
Существует вариант, при котором антимезотелиновые иммуноконъюгаты настоящего изобретения применяются в сочетании с одним или более иммунотерапевтическое средством, таким как антитела или иммуномодуляторы, которые включают Герцептин®, Ретуксан®, ОваРекс, Панорекс, ВЕС2, IMC-C225, Витаксин, Кампат I/H, Смарт MI95, ЛимфоЦид, Смарт ID 10, а также Онколим, ритуксан, ритуксимаб, гемтузумаб, либо трастузумаб.
Данное изобретение также предусматривает применение антимезотелиновых иммуноконъюгатов настоящего изобретения с одним или более антиангиогенным средством, которое включает ангиостатин, талидомид, домен «двойная петля» 5, эндостатин, серпин (ингибитор серин-протеаза) антитромбин, 29 kDa N-терминальные и 40 kDa С-терминальные расщепляющие белки фибронектина, 16 kDa расщепляющий белок пролактина, 7,8 kDa расщепляющий белок тромбоцитарного фактора 4, β-амино белок тромбоцитарного фактора 4 (Maione et al., 1990, Cancer Res. 51:2077), 14 пептид аминокислоты, соответствующий фрагменту коллагена I (Tolma et al., 1993, J.Cell Biol. 122:497), 19 пептид аминокислоты, соответствующий фрагменту тромбоспондина I (Tolsma et al., 1993, J.Cell Biol. 122:497), 20 пептид аминокислоты, соответствующий фрагменту SPARC (Sage et al., 1995, J.Cell. Biochem. 57: 1329-), или любой фрагмент, член семейства или его производные, включая фармацевтические приемлемые соли. Также были описаны другие пептиды, которые ингибируют ангиогенез и соответствуют фрагментам ламинина, фибронектина, проколлагена, а также EGF (См. обзор Сао, 1998, Prog. MoI. Subcell. Biol. 20:161). Было доказано, что моноклональные антитела и циклические пентапептиды, которые блокируют определенные интегрины, соединяющие RGD белки (например, имеют пептидный мотив Arg-Gly-Asp), имеют антиваскуляризационную активность (Brooks et al., 1994, Science 264:569; Hammes et al., 1996, Nature Medicine 2:529). Более того, ингибирование рецептора урокиназного активатора плазмогена антагонистами подавляет ангиогенез, рост опухоли и метастазы (Min et al., 1996, Cancer Res. 56: 2428-33; Crowley et aL, 1993, Proc Natl Acad. Sci. USA 90: 5021). Использование подобных антиангиогенных средств также предусмотрено настоящим изобретением.
В другом случае, антимезотелиновые иммуноконъюгаты настоящего изобретения применяют в сочетании со схемой лечения радиацией.
Антимезотелиновые иммуноконъюгаты настоящего изобретения также могут использоваться в сочетании с одним или более цитокинами, которые включают лимфокины, фактор некроза опухолей, цитокины типа фактор некроза опухолей, лимфотоксин-α, лимфотоксин-β, интерферон-β, макрофагальный белок воспаления, колониестимулирующие фактор гранулоцита моноцита, интерлейкины (включая интерлейкин-1, интерлейкин-2, интерлейкин-6, ннтерлейкин-12, интерлейкин-15, интерлейкин-18), 0Х40, CD27, CD30, CD40 или CD 137 лиганды, Fas-Pas лиганд, 4-IBBL, эндотелиальный моноцитный активирующий белок или любые фрагиенты, члены семейств или их производные, включая фармацевтически приемлемые соли.
Антимезотелиновые иммуноконъюгаты настоящего изобретения также могут использоваться в комбинации с противоопухолевой вакциной, например аутологичные клетки или ткани, неаутологичные клетки и ткани, карциноэмбриональный антиген, альфа-фетопротеин, хорионический гонадотропин человека, живая вакцина BCG, белки меланоцитного клеточной линии (например, gpIOO, MART-1/MelanA, TRP-I (gp75), тирозиназа, пшроко распространенный, связанный с опухолью, включая опухолеспецифический, антигены (например, BAGE, GAGE-I, GAGE-2, MAGE-I, MAGE-3, N-ацетилглюкозаминилтрансфераз-V, р15), трансформированные антигены, являющиеся опухолеассопиированными (β-катенин, MUM-I, CDK4), нонмеланомные антигены (например, HER-2/нейтрофилы (карцинома груди и яичника), папилломавирус 5 человека-Е6, Е7 (карцинома шейки матки), MUC-1 (карцинома груди, яичника и поджелудочной железы). Человеческие опухолевые антигены, признанные Т-клеткой, смотрите обычно Robbins and Kawakami, 1996, Curr. Opin. Immunol. 8:628. Противоопухолевые вакцины могут являться или не являться очищенными препаратами.
В другом варианте изобретения антимезотелиновые иммуноконъюгаты настоящего изобретения применяют вместе с гормональным лечением. Гормональное терапевтическое лечение включает гормональные агонисты, гормональные антагонисты (например, флутамид, тамоксифен, лейпрорелин ацетат (LUPRON), LH-RH антагонисты), ингибиторы гормонального биосинтеза и обработки, а также стероиды (например, дексаметазон, ретиноиды, бетаметазон, кортизол, кортизон, преднизон, дегидротестостерон, глюкокортикоид, минералокортикоид, эстроген, тестостерон, прогестин), антигестагены (например, мифепристон, онапристон), а также антиандрогены (например, ципротерон ацетат).
Антимезотелиновые иммуноконъюгаты данного изобретения могут использоваться в комбинации с анти-MDR (множественная лекарственная устойчивость) фенотипный агент. Многие виды человеческого рака в действительности выражают или спонтанно развивают устойчивость к нескольким классам противоопухолевых препаратов в одно и то же время, несмотря на то, что каждый класс препаратов имеет различные структуры и механизмы действия. Данный феномен, который может имитироваться в культивируемых клетках млекопитающего, обычно называется множественной лекарственной устойчивостью (MDR) или фенотипом множественной лекарственной устойчивости. Фенотип MDR представляет собой значительную преграду на пути к эффективному химиотерапевтическому лечению рака у пациентов-людей. Устойчивость злокачественных опухолей к многочисленным химиотерапевтическим агентам является основной причиной неудачного лечения (Wittes et al., Cancer Treat. Rep.70: 105 (1986); Bradley, G. et al., Biochim. Biophys. Acta 948:87 (1988); Griswald, D.P. et al., Cancer Treat Rep.65(S2): 51 (1981); Osteen, R.T. (ed.). Cancer Manual, (1990)). Изначально опухоли, которые чувствительны к цитотоксическим средствам, часто рецидивируют или развивают устойчивость к различным химиотерапевтическим препаратам (Riordan et al., Pharmacol. Ther. 28:51 (1985); Gottesman et al., Trends Pharmacol. Sci. Sci. 9:54 (1988); Moscow et al., J.Natl. Cancer Inst. 80:14 (1988); Croop, J.M. et al., J.Clin. Invest. 81:1303 (1988)). Клетки или ткани, полученные из опухолей и выращенные при наличии селективных цитотоксических средств, могут привести к перекрестной резистентности других препаратов данного класса, а также других классов препаратов, включая, но не ограничиваясь, антрациклинами, алкалоидами барвинка, а также эпидофиллотоксинами (Riordan et al., Pharmacol. Ther. 28:51 (1985); Gottesman et al., J.Biol. Chem. 263:12163 (1988)). Поэтому приобретенная устойчивость к результатам одного препарата при одновременной устойчивости к различным группам препаратов, структурно и функционально не связанных. Подобная устойчивость может стать проблемой как для опухолей твердой формы, так и опухолей жидкой формы (например, рак крови или лимфы). Один основной механизм множественной лекарственной устойчивости в клетках млекопитающих включает увеличенную экспрессию гликопротеиновой насосной системы клеточной мембраны (Juranka et al., FASEB J 3:2583 (1989); Bradley, G. et al., Blochem. Biophys. Acta 948:87 (1988)). Ген, кодирующий эту насосную систему, иногда называемый переносчиком многих лекарств, был клонирован из культивируемых клеток человека и обычно называется mdrl. Данный ген представлен в нескольких видах нормальных тканей, однако, физиологические субстраты, переносимые для генного продукта mdrl в данных тканях, не были определены. Продукт MDR1 представляет собой член суперсемейства АВС транспортного белка, группы белков, выполняющих функцию энергозависимого экспорта. Белковый продукт гена mdrl, обычно известный как Р-гликопротеин (Р-170, P-gp), является 170 kDa белком трансклеточной мембраны, содержащим вышеуказанный энергозависимый откачивающий насос. Экспрессии P-gp на поверхности клетки достаточно для представления клеток, устойчивых к многочисленным цитотоксическим средствам, включая многие противоопухолевые средства. P-gp-опосредованный MDR является важным клиническим компонентом опухолевой резистентности в опухолях различных типов, а mdrl генная экспрессия соответствует устойчивости к химиотерапии различных типов рака. Последовательность нуклеотидов гена mdrl (Gros, P. et al., Cell 47:371 (1986); Chen, С.et al., Cell 47:381 (1986)) указывает на то, что она кодирует полипептид, подобный или идентичный Р-гликопротеину, а также на то, что это члены высококонсервативного класса мембранных белков, которые подобны бактериальным переносчикам и участвуют в нормальных физиологических процессах переноса. Анализ последовательности гена mdrl указывает на то, что Pgp содержит 1280 аминокислот, распределенных между двумя гомологичными (43% идентичности) половинами. Каждая половина молекулы имеет шесть гидрофобных трансмембранных доменов, а также связывающий участок АТР внутри больших цитоплазматических петель. Только около 8% молекул являются внеклеточными, а углеводная часть (примерно 30 kDa) ограничена участками данной области.
Поэтому будет цениться то, что клетки млекопитающего, имеющие «множественную лекарственную устойчивость» или фенотип «множественной лекарственной устойчивости», характеризуются способностью отделять, вывозить или исключать множественность цитотоксических веществ (например, химиотерапевтические препараты) из внутриклеточной среды. Клетки могут приобретать данный фенотип в результате давления, выраженного воздействием отдельного химиотерапевтического препарата (селективный токсин). В противном случае клетки могут проявлять фенотип до воздействия токсина, так как перенос цитотоксических веществ включает механизм, действующий вместе с нормальным переносом продуктов клеточной секреции, метаболитов и им подобных. Множественная лекарственная устойчивость отличается от простой приобретенной устойчивости к селективному токсину тем, что клетка получает возможность переносить дополнительные цитотоксины (другие химиотерапевтические средства), которым клетка не была ранее подвержена. Например, Mirski et al. (1987), 47 Cancer Res. 2594-2598, описывает изоляцию устойчивой к множественным лекарствам клеточной популяции путем выращивания клеточной линии Н69, полученной из человеческой мелкоклеточной легочной раковой опухоли, в присутствии адриамицина (доксорубицина) в качестве селективного токсина. Было обнаружено, что сохранившиеся клетки препятствуют цитотоксическому эффекту антрациклинового аналога (например, дауномицин, эпирубицин, меногарил, а также митоксантрон), ацивицин, этопозид, грамицидин D, колхицин и производный от борвинок алкалоиды (винкристин и винбластин), а также адриамицин. Подобные техники селективного культивирования могут применяться для производства дополнительных резистентных ко многим лекарственным препаратам клеточных популяций. Следовательно, фармацевтические композиции данного изобретения могут дополнительно включать соединения, действующие для ингибирования фенотипа MDR и/или условий, связанных с фенотипом MDR. Подобные соединения могут включать любые известные в данной области ингибиторные соединения MDR, такие как антитела, специфические для компонентов MDR (например, анти- MDR транспортирующие антитела) или малые молекулярные ингибиторы транспортировщиков MDR, включая в особенности тамоксифен, верапамил, а также циклоспорин А, являющиеся агентами, которые изменяют или препятствуют множественной лекарственной устойчивости. (Lavie et al. J.Biol. Chem. 271: 19530-10536, 1996, которая указана в данном документе в ссылке). Подобные соединения можно найти в Патентах США №№5,773,280, 6,225,325, и 5,403,574, на каждую из которой в данном документе есть ссылка. Подобные ингибиторные соединения MDR могут использоваться вместе с антимезолиновыми иммуноконъюгатами для различных целей, включая изменение MDR фенотипа с последующим определением MDR фенотипа для ассестирования или усиления химиотерапевтического лечения. MDR ингибитор, такой как, например, тамоксифен, верапамил или циклоспорин А может использоваться вместе с соединениями данного изобретения для помощи в определении MDR фенотипа. Согласно данному аспекту MDR ингибитор может усиливать поглощение и накопление соединения данного изобретения в раковой клетке MDR, так как способность транспортной системы MDR переносить или «перекачивать» представленное соединение по сравнению с доменом субстрата ухудшится при наличии MDR ингибитора.
В другом варианте изобретения антимезотелиновые иммуноконъюгаты настоящего изобретения используются вместе с программой генотерапии при лечении рака. Генотерапия с рекомбинантными клетками, выделяющими интерлейкин-2, может применяться в сочетании с инвентивными иммуноконъюгатами для профилактики или лечения рака, в особенности рака молочной железы (см., например, Deshmukh et ah, 2001, J.Neurosurg. 94:287).
Для оценки терапевтической эффективности определенного иммуноконъюгата, например при лечения рака, он должен тестироваться в организме в ксенотрансплантной модели опухоли мыши. Примеры терапевтических моделей указаны в Примерах 1 и 2. Активность антител может также тестироваться с использованием зависимой от антитела клеточно-опосредованной цитотоксичности, как указано в Примере 3.
Фармацевтические композиции и дозировки
Иммуноконъюгаты, описанные в данном документе, могут быть представлены в фармацевтической композиции, содержащей фармацевтически приемлемый носитель. Фармацевтически приемлемый носитель может быть апирогенным. Данные композиции могут использоваться отдельно или вместе по меньшей мере с одним другим агентом, таким как стабилизирующее соединение, которое может использоваться в любом стерильном биологически совместимом фармацевтическом носителе, включая соль, забуференный раствор, декстрозу и воду. Может использоваться ряд водных носителей, включая соль, глицин и им подобные. Данные растворы являются стерильными и обычно не содержат твердых частиц. Данные растворы могут стерилизоваться обычными хорошо известными методами стерилизации (например, фильтрация).
Обычно выражение «фармацевтически приемлемый носитель» признан в данной области и включает фармацевтически приемлемый материал, композицию или проводник, подходящий для применения соединений настоящего изобретения для млекопитающих. Носители включают жидкий или твердый носитель, разбавитель, наполнитель, растворитель или герметик, участвующий в переносе или транспортировке необходимого агента из органа, или части тела к другому органу, или части тела. Каждый носитель должен быть «подходящим», то есть быть совместимым с другими ингредиентами композиции, а также не наносить вред пациенту. Некоторые примеры материалов, которые могут служить фармацевтически приемлемыми носителями, включают: сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлозу и ее производные, такие как натриевая карбоксиметилцеллюлоза, этилцеллюлоза и ацетатцеллюлоза; порошковый трагакант; солод; желатин; тальк; вспомогательные вещества, такие как какао-масло и суппозитарный воск; масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло, а также соевое масло; гликоли, такие как пропиленгликоль; полиолы, такие как глицерин, сорбитол, маннитол, а также полиэтиленгликоль; эфиры, такие как этилолеат и этиллаурат; агар; буферные вещества, такие как магний гидроксид и гидроксид алюминия; альгиновую кислоту; апирогенную воду; изотонический раствор; раствор Рингера; этиловый спирт; фосфатно-буферный раствор; а также другие нетоксичные совместимые вещества, использующиеся в фармацевтических композициях. Увлажняющие реагенты, эмульгаторы и лубриканты, такие как лаурилсульфат натрия и стеарат магния, а также красящие вещества, разделительные средства, покровные вещества, подсластители, ароматизаторы и ароматизирующие добавки, консерванты и антиоксиданты, могут также присутствовать в иммуноконъюгатных композициях данного изобретения.
Примеры фармацевтически приемлемых антиоксидантов включают: водорастворимые антиоксиданты, такие как аскорбиновая кислота, цистеин гидрохлорид, гидросульфат натрия, метабисульфит натрия, сульфит натрия и им подобные; маслорастворимые антиоксиданты, такие как аскорбилпальмитат, бутилированный гидроксианизол (ВНА), бутилированный гидрокситолуол (ВНТ), лецитин, пропилгаллат, альфа-токоферол и им подобные; хелатирующие металл агенты, такие как лимонная кислота, этилендиамин тетрауксусная кислота (EDTA), сорбитол, винная кислота, фосфорная кислота и им подобные.
Композиции могут содержать фармацевтически приемлемые вспомогательные вещества, как требуется для приближения к физиологическим условиям, такие как рН адаптирующийся и буферный агенты и им подобные. Концентрация иммуноконъюгата данного изобретения в подобных фармацевтических композициях может значительно различаться, а также может выбираться, в первую очередь, в зависимости от объема жидкости, вязкости и т.д., в соответствии с определенным выбранным способом применения. При желании, в фармацевтическую композицию можно включить более одного вида антител или иммуноконъюгата (например, антитело с различным Ка для мезотелинового соединения).
Композиции могут вводиться пациенту отдельно либо вместе с другими агентами, препаратами или гормонами. В дополнение к активным ингридиентам данные фармацевтические композиции могут содержать подходящие фармацевтически приемлемые носители, содержащие вспомогательные и дополнительные вещества, которые способствуют процессу перехода активных веществ в препараты, которые могут использоваться в фармацевтике. Фармацевтические композиции изобретения могут использоваться различными способами, включая, но не ограничиваясь, оральным, внутривенным, внутримышечным, внутриартериальным, интрамедулярным, интратекальным, интравентрикулярным, трансдермальным, подкожным, внутрибрюшным, интраназальным, парентальным, местным, подъязычным или ректальным способом.
Композиции изобретения дополнительно предполагают подходящие иммуноносители, такие как белки, полипептиды или пептиды, такие как альбумин, гемоцианин, тиреоглобулин и их производные, в особенности бычий сывороточный альбумин (BSA), а также гемоцианин фиссуреллы (KLH), полисахариды, карбогидраты, полимеры, твердые фазы. Специалистам хорошо известны другие белковые и небелковые вещества.
В случае вакцин, например противоопухолевые вакцины вместе с антителами изобретения, композиции изобретения могут применяться с или без адъюванта. Их применение может проводиться при отсутствии адъюванта, во избежание вызываемой им токсичности. Специалист данной области, к которой относится данное изобретение, например врач-онколог, оценит и поймет, как установить, должен ли использоваться адъювант, что может зависеть от истории болезни объекта, данных обследования семьи, данных о токсичности, результатов теста на аллергию т.д. В примерах осуществления изобретения, где используется адъювант, желательно, чтобы адъювант способствовал образованию защитных антител, таких как защитные антитела иммуноглобулина. Любой подходящий адъювант, известный специалисту данной области, предполагается настоящим изобретением и может быть легко адаптирован к нему. Подходящие адъюванты, использующиеся для вакцинации животных, могут включать, но не ограничиваются, гидроксидом алюминия, сапонином и его очищенными компонентами Quit А, полным адъювантом Фрейнда (CFA), а также неполным адъювантом Фрейнда (IFA). Было показано, что декстран сульфат является сильным стимулятором антитела иммуноглобулина 2 по сравнению со стафилококковыми поверхностными клеточными агентами, они также подходят в качестве адъюванта. Специалисты данной области оценят то, что некоторые адъюванты могут быть более предпочтительными для применения в ветеринарии, в то время как другие адъюванты больше подходят для людей, а также то, что токсичность адъюванта оценивается специалистам перед применением соединения для людей.
Композиции, подходящие для парентерального, подкожного, внутривенного, внутримышечного и подобных способов введения; подходящие фармацевтические носители; приготовление композиций и их применение может проводиться любыми известными специалисту способами (см., например, Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, Pa., 20 th edition, 2000). Жидкие лекарственные формы для орального применения соединения изобретения включают фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активному ингредиенту жидкие лекарственные формы могут содержать инертный разбавитель, обычно используемый в данной области, такой как, например, вода или другие, раствор как этиловый спирт, изопропиловый спирт, этиловый эфир угольной кислоты, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1, 3-бутиленгликоль, масла (в особенности, хлопковое, арахисовое, кукурузное, масло из проростков, оливковое, касторовое и кунжутное масло), глицерин, тетрагидрофурил спирт, полиэтиленгликоли и эфиры жирной кислоты сорбитана, а также смеси из них.
Выражения «парентеральное введение» и «применять парентерально», используемые в настоящем документе, обозначают способы введения, отличные от энтерального и местного введения, обычно при помощи инъекции, и включают, без ограничений, внутривенную, внутримышечную, внутриартериальную, субдуральную, интракапсулярную, внутриглазничную, интракардиальную, транстрахеальную, подкожную, внутрикожную, внутрибрюшную, подкапсулярную, субарахноидальную, интраспинальную, а также надчревную инъекцию и инфузию.
Специалист данной области может определить терапевтически эффективную дозу. Терапевтически эффективная доза означает количество иммуноконъюгата, который может использоваться для эффективного лечения болезни (например, рак), по сравнению с эффективностью, очевидной при отсутствии терапевтически эффективной дозы.
Первоначально терапевтически эффективная доза может оцениваться на животных моделях (например, крысах, мышах, кроликах, собаках или свиньях). Животные модели могут также использоваться для определения уровня концентрации и способа введения. Подобная информация может затем использоваться для определения эффективных доз и способов введения для людей. Терапевтическая эффективность и токсичность (например, ED50 - доза, терапевтически эффективная для 50% населения, a LD50 - летальная доза для 50% населения) иммуноконъюгата может быть определена с помощью стандартных фармацевтических процедур в клеточных культурах или у подопытных животных. Соотношение дозы и терапевтического эффекта является терапевтическим индексом, который может быть выражен отношением LD50/ED50. Данные, полученные при изучении животных, могут использоваться при определении пределов дозировки для человека. Дозировка, содержащаяся в подобных композициях, может находиться в пределах распространенной концентрации, которая включает ED50 с малой или нулевой токсичностью. Дозировка различается в данных пределах в зависимости от используемой дозировки, чувствительности пациента, способа введения.
Точная доза может определяться врачом ввиду факторов, связанных с пациентом, требующим лечения. Дозировка и введение могут меняться для предоставления достаточного уровня иммуноконъюгата или поддержания желаемого эффекта. Факторы, которые могут учитываться, включают тяжесть болезни, общее состояние здоровья объекта, возраст, рост, пол, диету, время и частоту применения, сочетание(я) препарата, чувствительность реакции, а также устойчивость/реакцию на лечение. Полинуклеотиды, кодирующие иммуноконъюгаты изобретения, могут быть сконструированы и введены в клетку либо вне организма, либо в живой организм, с использованием общепризнанных техник, включая, но не ограничиваясь, перемещением трансферин-поликатион-опосредованной ДНК, трансфекцией с лишенной оболочки или покрытой оболочкой нуклеиновой кислотой, липосомо опосредованным клеточным слиянием, внутриклеточным переносом покрытых ДНК латексных гранул, слиянием протопластов, вирусной инфекцией, электропорацией, «генной пушкой», а также DEAE- или фосфат кальция-опсредованной трансфекцией.
Эффективность в живом организме токсофорных компонентов иммуноконъюгата находится в пределах от примерно 5 мг до примерно 500 мг на 1 кг веса пациента. Способом применения иммуноконъюгата, содержащего фармацевтические композиции настоящего изобретения, могут быть любые подходящие способы, при которых антитело доставляется в хозяина. Например, фармацевтические композиции изобретения могут быть эффективными при парентеральном введении (например, подкожно, внутримышечно, внутривенно или интраназально). Все патенты и патентные заявки, указанные в данном раскрытии, целенаправленно включены в данный документ путем ссылки. Вышеуказанное раскрытие в общем описывает настоящее изобретение. Более полное понимание можно получить со ссылкой на следующие конкретные примеры, представленные только с целью иллюстрации и не расчитанные на ограничение сфер применения изобретения.
ПРИМЕРЫ
ПРИМЕР 1: Эффективность иммуноконъюгата в мезотелине, выражающем ксенографную мышиную модель человеческого рака поджелудочной железы
Для анализа того, смогли ли антимезотелиновые иммуноконъюгаты сократить развитие опухолей мезотелинозависимым способом, были ли клетки человеческого рака поджелудочной железы (MiaPaCa-2) успешно перенесены с мезотелином и использованы для образования подкожно растущей опухоли мышиной модели. Была использована клеточная линия человеческой карциномы толстой кишки НТ29 для установления мезотелин-негативных контрольных опухолей в рамках эффективности исследования. Клетки MiaPaCa поддерживались в качестве адгезивных культур в DMEM среде, дополненном 10% (объем к объему) FCS, 2,5% (объем к объему) лошадиной сыворотки, 1,5 г/л натрий биокарбоната, 4,5 г/л глюкозы, 4 ммоль глютамина и 0,4% (объем к объему) гигромицина. Клетки НТ29 были выращены в среде Мак-Коя 5а с 1,5 ммоль глютамина, 2,2 г/л натрий биокарбоната и 10% (объем к объему) FCS. Экспрессия мезотелина клеток MiaPaCa-2, а также отсутствие мезотелина в клетках НТ29 было подтверждено FACS (не показано). Для оценки роста в живом организме клеток опухоли особям женского пола NMRI безтимусных мышей были подкожно привиты в правый бок 3×106 степени MiaPaCa-2 клетки или 1×106 степени клетки НТ29, перерастворенные в 50% Matrigel™ или 50% среде. Антимезолиновые иммуноконъюгаты MF-J-SPDB-DM4, MF-T-SPDB-DM4, MF226-SPDB-DM4 и MOR6640-SPDB-DM4 были протестированы при лечебных дозах в 0,01 мг/кг, 0,03 мг/кг, 0,05 мг/кг и 0,2 мг/кг (связанный с количеством токсофора). MF-J-SPDB-DM4, MF-T-SPDB-DM4, MF226-SPDB-DM4 и MOR6640-SPDB-DM4 были образованы с помощью следующей процедуры: антимезотелиновые антитела были изменены с 4-[2-пиридилдитио] бутановой кислотой N-гидроксицинимидин эфира (SPDB) для введения дитиопиридиловых групп. При 8 мг/мл, ~6-кратный молярный избыток SPDB (~20 ммоль основного раствора в этаноле или этиловом спирте) был использован для модификации антител. Модифицированные антитела вступали в реакцию с 1,7-кратным молярным избытком свободной формы тиола матансиноида по сравнению с тиопиридилом. Реакция проводилась с 2,5 мг/мл антитела в присутствии 3% диметилацетамида (3% объем к объему) в течение 20 часов при комнатной температуре. Конъюгационная реагирующая смесь была очищена от непрореагировавшего препарата и побочных продуктов реакции с использованием деминерализирующей колонки Сефадекс G25. Число матансиноидных молекул в антителе было расчитано путем определения поглощения на 252 нанометра и 280 нанометров, с использованием коэффициента поглощения в 224000 М-1·см-1 для антитела и 5180 М-1·см-1 для DM4 в 280 нанометров. Отношение поглощения 252 нанометра/280 нанометров 0,37 для антитела и 5,05 для DM4.
Лечение начинали после установления опухоли на 5 день после внедрения опухолевой клетки, затем последовало два этапа лечения на 8 и 12 день после внедрения опухолевой клетки. Контрольных мышей лечили либо 0,2 мг/кг ненацеленного иммуноконъюгата (антилизоцим-SPDB-DM4) либо равными объемами самого переносчика (10 ммоль гистидина, 130 ммоль глицина, 5% (масса/объем) сахарозы, рН 5,5). Лечение проводили с дозировкой 100 мл/10 г массы тела путем внутривенного введения. В каждой группе было 6 животных. Состояние здоровья мышей проверяли каждый день. Длину и ширину подкожных опухолей измеряли электромагнитным методом два раза в неделю. Участок опухоли измеряли по формуле: участок опухоли [мм2] = длина [мм] × ширина [мм]. Все данные, полученные за время эксперимента, были задокументированы. Пример противоопухолевой эффективности антимезотелинового иммуноконъюгата MF-T-SPDB-DM4 в мезотелин-трансфектированных клетках человеческого рака поджелудочной железы при различных лечебных дозах указан на Фигуре 1. Особям женского пола NMRI безтимусных мышей привили 3×106 мезотелин-положительные клетки раковой опухоли (A) MiaPaCa-2 человеческой поджелудочной железы или 1×106 мезотелин-отрицательные НТ29 клетки раковой опухоли толстой кишки (В), перерастворенные в 50% Matrigel™/50% среды в их правый бок. На 5, 8 и 12 день после внедрения опухолевой клетки, мыши получили 0,01, 0,03, 0,05, 0,2 мг/кг MF-T-SPDB-DM4, (все концентрации относятся к количеству токсофора), или сам переносчик. Длину и ширину опухолей измеряли два раза в неделю, а участок опухоли расчитывали при умножении ширины на длину. Средние значения и стандартное отклонение каждой группы, а также измеряемый момент времени указаны на графике. Все n=6. Сноски обозначают Р-значения <0 05.
Лечение мышей с опухолями показало, что все протестированные антимезотелиновые иммуноконъюгаты были способны сдержать рост мезотелин-положительных MiaPaCa-2 опухолей в живом организме при дозах 0,03 мг/кг, 0,05 мг/кг и 0,2 мг/кг. При дозах в 0,05 мг/кг и 0,2 мг/кг MF-T-SPDB-DM4 происходило полное уничтожение опухоли без возобновления ее роста до конца периода наблюдения, длительностью 132 дня. 0,05 мг/кг ненацеленного контроля антилизоцима-SPDB-DM4 не имели эффекта на рост мезотелин-положительной MiaPaCa опухоли (Таблица 1). По сравнению с нелеченными и леченными переносчиком опухолями рост мезотелин-положительных НТ29 опухолей не был значительно остановлен самой большой дозой в 0,2 мг/кг MF-T-SPDB-DM4. Это говорит о том, что значительная эффективность, ингибирующая развитие опухоли, MF-T-SPDB-DM4 зависит от экспрессии мезотелина в опухоли.
ПРИМЕР 2: Эффективность в опухолях, эндогенно выражающих мезотелин, а также сравнение различных линкеров
Для того чтобы узнать, способны ли антимезотелиновые иммуноконъюгаты остановить развитие эндогенного мезотелина, выражающего опухолевые клетки в организме, использовали ксенографтную модель с подкожно растущими клетками рака шейки матки (HeLaMATU). Клетки HeLaMATU поддерживались в качестве адгезивных культур в DMEM/HAMS12 среде, дополненной 10% (объем к объему) FCS, 2,5% (объем к объему) лошадиной сыворотки, 1% пирувата натрия, 1% (объем к объему) глютамина. Мезотелиновая экспрессия была подтверждена анализом FACS в искусственных условиях. Особям женского пола NMRI безтимусных мышей подкожно привили в правый бок 1,5×106 клетки HeLaMATU, перерастворенные в 50% Matrigel™/50% среде. Дополнительно было рассмотрено, приводит ли обмен расщепляемого SPDB-линкер полярным (-сульфо-SPDB), стабильным линкером (-SMCC), либо полярным и стабильным линкером (-(PEG)4-mal) к изменению противораковой эффективности MOR6640-основанного иммуноконъюгата в организме. HeLaMATU мыши с опухолями получали внутривенно 0,2 мг/кг либо MOR6640-SPDB-DM4, MOR6640-SMCC-DM1, MOR6640-сульфо-SPDB-DM4, либо MOR6640-(PEG)4-mal-DMl (связанный с количеством токсофора) на 5, 8 и 12 день после внедрения опухолевой клетки. Контрольных мышей лечили либо 0,2 мг/кг ненацеленного иммуноконъюгата (антилизоцим-SPDB-DM4), либо равными объемами самого переносчика. В каждой группе было 6 животных. Состояние здоровья мышей проверяли каждый день. Длину и ширину подкожных опухолей измеряли электромагнитным методом два раза в неделю. Участок опухоли измеряли по формуле: участок опухоли [мм2] = длина [мм] × ширина[мм]. Полученные данные представлены на Фигуре 2. Лечение мышей с опухолями показало, что а) антимезотелиновые иммуноконъюгаты эффективно останавливали развитие опухолей, выражающих мезотелин эндогенно в организме, и b) что конъюгаты с расщепляемыми линкерами (MOR6640-SPDB-DM4 и MOR6640) показали более высокую противоопухолевую эффективность по сравнению с конъюгатами со стабильными линкерами (MOR6640-SMCC-DM1 и MOR6640-(PEG)4-mal-DMl). В частности, MOR6640-SPDB-DM4 и MOR6640-сульфо-SPDB-DM4 привели к уничтожению опухолей у всех подвергавшихся лечению животных одиннадцать дней спустя после лечения, в то время как лечение MOR6640-SMCC-DM1 и MOR6640-(PEG)4-mal-DMl только приостановило развитие опухоли. Тем не менее, спустя одиннадцать дней после последнего лечения участки опухолей, которые лечили MOR6640-SMCC-DM1 и MOR6640-(PEG)4-mal-DMl соответственно, стали значительно меньше по сравнению с опухолями, которые лечили переносчиком или антилизоцимом-SPDB-DM4.
Ненацеленный контрольный конъюгат не повлиял на рост опухоли. Для того чтобы сравнить противоопухолевую эффективность различных линкеров на второй ксенографтной модели, мы использовали модель с подкожно растущей векторными или мезотелин трансфецированными (#37) MiaPaCa-2 клетками (клетки человеческого рака поджелудочной железы). MiaPaCa-2-вектор и MiaPaCa-2#37 клетки поддерживались в качестве адгезивных культур в DMEM/HAMS12 среде, дополненной 10% (объем к объему) FCS, 1% (масса/объем) глютамина и 0,1 ммоль неосновных амонокислот. Мезотелиновая экспрессия была подтверждена анализом FACS, а также иммуногистохимическим анализом подкожных опухолей вне организма. Особям женского пола NMRI безтимусных мышей были подкожно привиты в правый бок 3×106 MiaPaCa-2-вектор и MiaPaCa-2#37 клетки, перерастворенные в 50% Matrigel™/50% среде соответственно. Мыши с опухолями получали 0,05 мг/кг либо MOR6640-SPDB-DM4, MOR6640-SMCC-DM1, MOR6640-sylfo-SPDB-DM4, либо MOR6640-(PEG)4-mal-DMl (связанный с количеством токсофора) на 5, 8 и 12 день после внедрения опухолевой клетки. Контрольных мышей лечили либо 0,05 мг/кг ненацеленного иммуноконъюгата (антилизоцим-SPDB-DM4), либо равными объемами самого переносчика. В каждой группе было 6 животных. Состояние здоровья мышей проверяли каждый день. Длину и ширину подкожных опухолей измеряли электромагнитным методом два раза в неделю. Участок опухоли измеряли по формуле: участок опухоли [мм2] = длина [мм] × ширина [мм]. Данные роста опухоли приведены на Фигуре 3. У мышей с мезотелин-выраженными опухолями лечение MOR6640-SPDB-DM4 и MOR6640-sulfo-SPDB-DM4 привело к уничтожению опухолей у всех подвергавшихся лечению животных спустя двенадцать дней после лечения. Тем не менее, возобновление роста данных опухолей происходило спустя десять дней (Фигура 3А). Лечение MOR6640-SMCC-DM1, MOR6640-(PEG)4-mal-DMl, а также антилизоцимом-SPDB-DM4 незначительно влияло на развитие опухоли. В отличие от мезотелин- выраженных опухолей, ни один из способов лечения не привел к изменению роста вектор трансфецированных клеток MiaPaCa-2 в организме (Фигура 3В).
ПРИМЕР 3: цитотоксичность антимезотелиновых иммуноконъюгатов в исскуственных условиях
Для оценки цитотоксичности антимезотелиновых иммуноконъюгатов были выращены на 80-90%, трипсинизированы и подсчитаны различные мезотелин-выраженные клеточные линии. Затем клетки были засеяны в 384 плоских блюдца в 800 с 25 мкл объема на ячейку в их среде роста для всех клеточных линий. Ячейки со средой были установлены для холостой субтракции. Спустя 24 часа после засева MF-J-SPDB-DM4, MF-226-SPDB-DM4, MOR6640-SPDP-DM4, MF226-SPDP-DM4, а также антилизоцим-SPDP-DM4 были разделены на дозы в пределах от 0,01 до 3,00 нмоль. Для каждого разбавления были установлены трипликаты. Конечные измерения проводили спустя 96 часов. Жизнеспособность клеток оценивали измерением проб WST-1 (Roche Cat# 1644807). IC50 значения указаны в Таблице 2. Кривая дозовой зависимости, указывающая в искусственных условиях цитотоксичность MF-T-SPDP-DM4 клеток HelaMatu, представлена на Фигуре 4.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОТИВООПУХОЛЕВЫЕ КОМБИНАЦИИ, ВКЛЮЧАЮЩИЕ КОНЪЮГАТЫ НА ОСНОВЕ АНТИТЕЛА К CEACAM5, ТРИФЛУРИДИН И ТИПИРАЦИЛ | 2021 |
|
RU2835019C1 |
| СХЕМЫ ПРИМЕНЕНИЯ ИММУНОКОНЪЮГАТА АНТИ-FOLR1 | 2014 |
|
RU2696579C2 |
| ИММУНОКОНЪЮГАТЫ, НАПРАВЛЕННЫЕ НА CD138, И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2547939C2 |
| СПОСОБЫ УЛУЧШЕНИЯ НАПРАВЛЕННОГО ВОЗДЕЙСТВИЯ НА CD138-ЭКСПРЕССИРУЮЩИЕ ОПУХОЛЕВЫЕ КЛЕТКИ И АГЕНТЫ ДЛЯ ИХ ОСУЩЕСТВЛЕНИЯ | 2008 |
|
RU2486203C2 |
| АНТИТЕЛА ПРОТИВ РЕЦЕПТОРА ФОЛИЕВОЙ КИСЛОТЫ 1, ИХ ИММУНОКОНЪЮГАТЫ И ИСПОЛЬЗОВАНИЕ | 2011 |
|
RU2610663C2 |
| АГЕНТЫ ПРОТИВ КЛЕТКИ-МИШЕНИ, НАЦЕЛЕННЫЕ НА CD138, И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2537265C2 |
| СХЕМЫ ПРИМЕНЕНИЯ ИММУНОКОНЪЮГАТА АНТИ-FOLR1 | 2014 |
|
RU2801307C1 |
| ПРИМЕНЕНИЕ ИММУНОКОНЪЮГАТОВ К CEACAM5 ДЛЯ ЛЕЧЕНИЯ РАКА ЛЕГКОГО | 2020 |
|
RU2828374C2 |
| ПРИМЕНЕНИЯ ИММУНОКОНЪЮГАТОВ, МИШЕНЬЮ КОТОРЫХ ЯВЛЯЕТСЯ CD138 | 2010 |
|
RU2561041C2 |
| БИПАРАТОПНЫЕ FR-АЛЬФА АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ | 2020 |
|
RU2832083C2 |













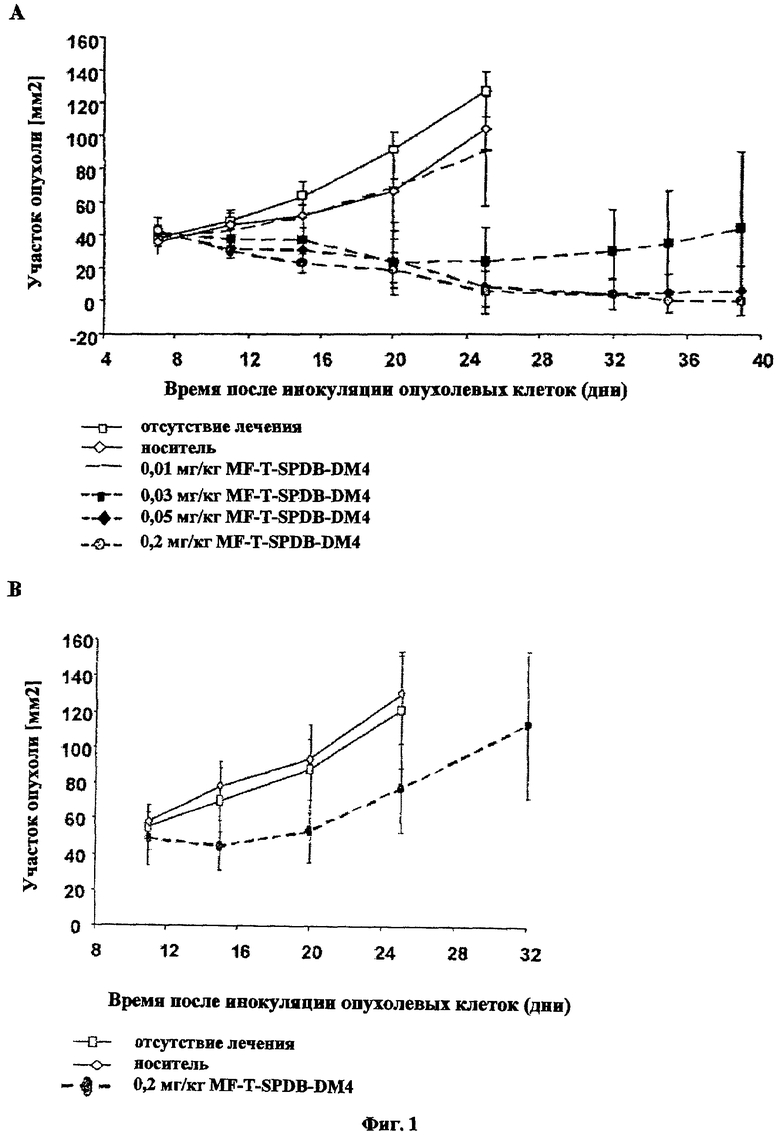



Изобретение относится к области иммунологии и биотехнологии. Описан иммуноконъюгат для лечения опухолевых расстройств, связанных с мезотелином. Конъюгат состоит из человеческого или гуманизированного антитела, или его функционального фрагмента, содержащего антигенсвязывающий участок, слитого с цитотоксическим средством DM4 через SPDB-линкер. Причем антитело или его функциональный вариант проявляют инвариантное связывание с мезотелином, то есть связывание с различными раковыми клетками, экспрессирующими мезотелин различной формы. Антигенсвязывающий участок содержит по 3 соответствующих CDR-участка лёгкой и 3 соответствующих CDR-участка тяжёлой цепи. Описана фармацевтическая композиция и способ лечения опухолевых расстройств, связанных с мезотелином, использующие иммуноконъюгат. Раскрыт также способ получения иммуноконъюгата, включающий присоединение цитотоксического средства DM4 к антителу через SPDB-линкер. Использование изобретения обеспечивает иммуноконъюгат на основе нового антитела, способного инвариантно связывать эпитоп мезотелина, не скрытый молекулой СА125, что может найти применение в терапии опухолей. 4 н. и 1 з.п. ф-лы, 4 ил., 3 табл., 3 пр.
1. Иммуноконъюгат, предназначенный для лечения опухолевых расстройств, связанных с мезотелином, содержащий цитотоксическое средство, представляющее собой N2′-деацетил-N2′-(4-метил-4-меркапто-1-оксопентил)-майтансин (DM4), и человеческое или гуманизированное антитело или его функциональный фрагмент, содержащий антигенсвязывающий участок, который является мезотелин-специфичным (SEQ ID NO: 36), причем указанное антитело или его функциональный фрагмент проявляет инвариантное связывание мезотелина, где антигенсвязывающий участок содержит:
HCDR1 согласно SEQ ID NO: 3,
HCDR2 согласно SEQ ID NO: 6,
HCDR3 согласно SEQ ID NO: 9,
LCDR1 согласно SEQ ID NO: 12,
LCDR2 согласно SEQ ID NO: 15,
LCDR3 согласно SEQ ID NO: 19,
причем цитотоксическое средство связано с антителом через SPDB-линкер, представляющий собой эфир 4-[2-пиридилдитио]бутановой кислоты и N-гидроксисукцинимида.
2. Иммуноконъюгат, определенный в п. 1, предназначенный для лечения рака, связанного с мезотелином.
3. Фармацевтическая композиция, предназначенная для лечения опухолевых расстройств, связанных с мезотелином, содержащая иммуноконъюгат по п. 1 или 2 в терапевтически эффективном количестве, и его фармацевтически приемлемый носитель или наполнитель.
4. Способ получения иммуноконъюгата по п. 1 или 2, включающий стадию присоединения цитотоксического средства, представляющего собой DM4, через SPDB-линкер с человеческим или гуманизированным антителом или его функциональным фрагментом, содержащим антигенсвязывающий участок, который является мезотелин-специфичным (SEQ ID NO: 36), причем указанное антитело или его функциональный фрагмент проявляет инвариантное связывание мезотелина, где антигенсвязывающий участок содержит:
HCDR1 согласно SEQ ID NO: 3,
HCDR2 согласно SEQ ID NO: 6,
HCDR3 согласно SEQ ID NO: 9,
LCDR1 согласно SEQ ID NO: 12,
LCDR2 согласно SEQ ID NO: 15,
LCDR3 согласно SEQ ID NO: 19.
5. Способ лечения опухолевого расстройства или состояния, связанного с нежелательным присутствием мезотелина, включающий введение нуждающемуся в таком лечении пациенту эффективного количества фармацевтической композиции по п. 3.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| US 2006182750 A1, 17.08.2006 | |||
| US 6809184 B1, 26.10.2004 | |||
| RU 2006147264 А, 20.07.2008 | |||
| РОЙТ и др., "Иммунология", М.: Мир, 2000, стр.110-111, 151. | |||
Авторы
Даты
2016-02-20—Публикация
2010-04-16—Подача