Изобретение относится к области аналитической химии, в частности к катодному инверсионно-вольтамперометрическому способу определения микотоксина Т-2 токсина, который представляет собой белое кристаллическое вещество, 8-(3-метилбутирилокси)-4,15-диацетокси-12,13-эпокситрихотец-9-ен-3-ол (известный также, как «Желтый Дождь») - не имеет максимумов поглощения в УФ-спектре при длине волны более 210 нм, не обладает флуоресценцией. Температура плавления Т-2 токсина 151-152°C. Данное изобретение может быть применено в анализе пищевых продуктов и продовольственном сырье и использовано в пищевой, медицинской, фармакологической промышленности и сельском хозяйстве.
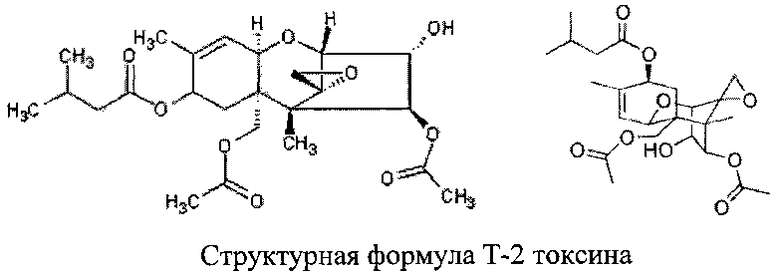
Т-2 токсин, брутто-формула (система Хилла) С24Н34О9, молекулярная масса 466,52 г/моль, трихотеценовый микотоксин, который был использован в качестве биологического оружия, продуцируемый плесневым грибом рода фузариум, высокотоксичен для эукариотических организмов. Т-2 токсин относится к семейству химических соединений, получивших название сесквитерпеноидов (sesquiterpenoids). Их отличительной чертой является трихотеценовое кольцо, содержащее олефиновую связь С-9 и эпоксидную группу С-12,13. Т-2 токсин является одним из наиболее токсичных представителей группы трихотеценовых микотоксинов, токсическое действие которых характеризуется поражением кроветворных и иммунокомпетентных органов, запуская стрессовые реакции эндоплазматического ретикулума, развитием геморрагического синдрома, лейкопенией, анемией, поражением функций желудочно-кишечного тракта. Т-2 токсин обладает высокой острой токсичностью (LD для различных видов млекопитающих от 3 до 10 мг/кг массы тела). В связи с этим установлена ПДК на содержание Т-2 токсина в пищевых продуктах на уровне 0,1 мг/кг.
Многие люди предпочитают лечиться фитопрепаратами и травяными сборами, полагая, что они полезнее для здоровья. Некоторые из них могут содержать плесневые грибки, продуцирующие опасные для человека токсины. Для исследования группа ученых Университета Пешавара в Пакистане выбрала 30 образцов наиболее используемых растительных средств, в 90% проб была обнаружена плесень, причем часто содержание микотоксинов превышал допустимые уровни нормы [Bashir Ahmad, Samina Ashiq, Arshad Hussain, Shumaila Bashir, Mubbashir Hussain /Evaluation of mycotoxins, mycobiota, and toxigenic fungi in selected medicinal plants of Khyber Pakhtunkhwa, Paristan // Fungal Biology, Volum 118, Issues 9-10, September-October 2014, Pages 776-784]. Идентификация трихотеценов и, в частности, Т-2 представляет определенные трудности, несмотря на то, что к настоящему времени уже разработана целая система подходов, обеспечивающая контроль за содержанием трихотеценов в продуктах сельскохозяйственного производства растительного происхождения. Официальные методы анализа микотоксинов обычно требуют сложное оборудование, как в случае тонкослойной хроматографии для определения Т-2 токсина, в сочетании с процедурами его извлечения при пробоподготовки проб. В течение примерно последних шестнадцати лет произошел переход к использованию более простых аналитических процедур, основанных на применении аффинных биосенсоров за счет своей простоты и чувствительности. Как правило, использование электрохимических биосенсоров для определения микотоксинов включает использование специфических антител или аптамер в качестве аффинных лигандов, так рекомбенантные антитела и искусстветные рецепторы проявили свою потенциальною значимость в этой области. Таким образом, в связи с высокой токсичностью Т-2 токсина и малыми МДУ к методу определения его в пищевых продуктах питания, кормах сельскохозяйственного производства, БАДах и лекарствах растительного происхождения предъявляются особые требования по чувствительности, селективности и воспроизводимости.
В прототипе описан способ определения Т-2 токсина методом амперометрического обнаружения с использованием электрохимического биосенсора на основе ферментативных продуктов реакции [D. Compagnone, К. Van Velzen, М. Del Carlo, Marcello Mascini, A. Visconti / Chapter 29 Rapid detection of organophosphates, Ochratoxin A, and Fusarium sp. In durum wheat via screen printed based electrochemical sensors // Comprehensive Analytical Chemistry. Volume 49, 2007, Pages 687-718]. В предлагаемом способе определение Т-2 токсина осложнено использованием модифицирующего агента, вследствие чего увеличивается суммарное время анализа.
В аналогичных работах описано определение Т-2 токсина электрохимическим методом с помощью электрохимического иммуносенсора с использованием композиционных материалов, таких как фуллерена С-60, ионной жидкости и ферроцена на хитозановой пленке на стеклоуглеродном электроде [Juan С. Vidal, Laura Bonel, Alba Ezquerra, Susana and others / Electrochemical affinity biosensors for detection of mycotoxins: A review // Biosensors and Bioelectronics. Volum 49, 15 November 2013, Pages 146-158] в продуктах детского питания. Те же авторы провели модифицирование золотого электрода screen-printed с использованием моноклонального антитела для определения Т-2 токсина в диапазоне концентраций от 1 до 1000 нг/мл. В предложенной работе золотой печатный электрод требует обновления и нанесения модификатора, что ограничивает применение данного метода с точки зрения трудоемкости и использования дополнительных химических реагентов.
Задачей заявленного изобретения является применение электродов из нетоксичного материала и определение Т-2 токсина методом дифференциальной вольтамперометрии в присутствии растворенного кислорода без дополнительного введения в фоновый электролит восстановителя, а также расширение диапазона определяемых концентраций и разработки экспресс-технологии оценки Т-2 токсина в течение 30-40 мин.
Поставленная задача достигается тем, что способ количественного определения Т-2 токсина включает перевод Т-2 токсина из пробы в раствор и вольтамперометрическое определение с использованием индикаторного стеклоуглеродного электрода. При этом накопление Т-2 токсина в перемешиваемом растворе проводят в течение 30 с при потенциале электролиза ЕЭ=(-0,5±0,05)В (табл.1) относительного насыщенного хлоридсеребряного электрода на фоне 0,1 М нитрата калия (KNO3) с последующей регистрацией катодных пиков в дифференциальном режиме съемки вольтамперограмм при скорости развертки потенциала 30 мВ/с и концентрацию Т-2 токсина определяют по высоте пика в диапазоне потенциалов Еп=(-1,25±0,35)В методом добавок аттестованных смесей.
В предлагаемом способе установлена способность Т-2 токсина восстанавливаться на углеродных электродах различных типов. Для выбора индикаторного электрода использовали графитовый электрод, пропитанный полиэтиленом с парафином в вакууме, стеклоуглеродный и углеситаловый электроды. Использование таких электродов обусловлено их высокой химической и электрохимической устойчивостью, отсутствием токсической ртути, широкой областью рабочих потенциалов, а также простотой механического обновления поверхности и требованиями техники безопасности. Использование в прототипах модифицированного стеклоуглеродного электрода/графитового печатного электрода с нанесением фермента на рабочую поверхность требует дополнительных химических реактивов и постоянного обновления поверхности электрода перед каждым анализом, что неудобно при проведении серийных анализов. Способность к электровосстановлению Т-2 токсина зависит от материала электрода и состояния его поверхности. Наибольшую величину аналитического сигнала, наименьшее значение остаточного тока и лучшую воспроизводимость сигналов на вольтамперограмме наблюдали на стеклоуглеродном электроде, который и был выбран в качестве рабочего (в аналоге в качестве индикаторного электрода использовали модифицированный СУ электрод с использованием композиционных материалов, таких как фуллерена С-60, ионной жидкости и ферроцена на хитозановой пленке).
Абсолютной новизной является разработка вольтамперометрического определения Т-2 токсина посредством измерения токов аналитического сигнала в приложенном напряжении, экспериментально установленный фоновый электролит - 0,1 М раствора нитрата калия (KNO3) с рН=4-5, который позволяет с хорошей воспроизводимостью проводить ИВ - измерения в присутствии растворенного кислорода без дополнительного введения восстановителя.
Другим отличительным признаком является использование трехэлектродной ячейки: индикаторный электрод - стеклоуглеродный; вспомогательный и сравнения - хлоридсеребряные электроды. Предварительный электролиз при потенциале (-0,5±0,05)В с последующим катодным растворением осадка позволяет регистрировать вольтамперограммы с четко выраженным максимумом при значении потенциала (-1,25±0,35) В.
Установленные условия проведения электродного процесса позволили количественно определять Т-2 токсин на основе реакции электровосстановления. Предлагаемый вольтамперометрический способ позволил сократить количество используемых реактивов, в частности, аптамеров для рекомбинантного моделирования поверхности индикаторных электродов, а также проводить измерения в присутствии растворенного кислорода и существенно улучшить метрологические характеристики анализа Т-2 токсина. Линейный диапазон определяемых концентраций 1-10-5÷6-10-3 мг/мл. Относительное стандартное отклонение (Sr) не более 20%.
Измерения проводили на компьютеризованных вольтамперометрических анализаторах СТА (ООО «ИТМ», г. Томск).
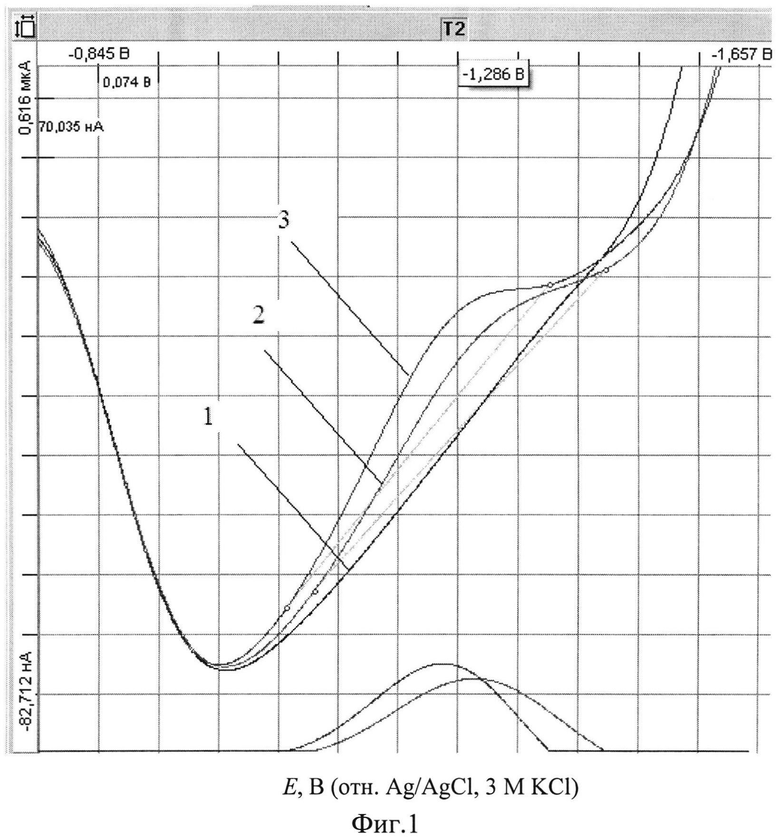
На Фиг. 1 представлено адсорбционное инверсионное вольтамперметрическое определение Т-2 токсина на стеклоуглеродном электроде. Концентрирование 30 сек при -0,5 В (метод добавок): 1-10 мл 0,1 М KNO3; 2-10 мл 0,1 М KNO3+0,02 мл Т-2 токсина; 3-10 мл 0,1 М KNO3+0,04 мл Т-2 токсина.
Пример 1. Определение содержания Т-2 токсина на уровне 0,0002 мг/мл.
В кварцевый стаканчик емкостью 20 мл наливают 10 мл 0,1 М раствора нитрата калия. Стаканчик с раствором помещают в электролитическую ячейку. Опускают в раствор электроды (индикаторный - стеклоуглеродный, вспомагательный и сравнения - хлоридсеребряные). Проводят электронакопление при потенциале (-0,5±0,05) В в течение 30 с при перемешивании раствора. По окончании электролиза начинают регистрацию вольтамперограммы в диапазоне потенциалов от -0,5 до -1,7 В (Фиг. 1, график 1). Отсутствие пиков свидетельствует о чистоте фона. Затем добавляют 0,02 мл стандартного раствора Т-2 токсина концентрации 10 мкг/см3 и проводят электронакопление при потенциале (-0,5±0,05) В в течение 30 с при перемешивании раствора с последующей регистрацией вольтамперограммы в диапазоне (-1,25±0,35) В (отн. ХСЭ) при чувствительности прибора (0,5÷1)·10-9 А/мм (Фиг. 1, график 2). Проводят разметку вольтамперограмм, средняя высота анодного пика составляет 54,45 нА. Далее в стаканчик с анализируемым раствором с помощью дозатора вносят добавку аттестованной смеси Т-2 токсина в объеме 0,02 мл концентрацией 0,01 мг/мл. Электронакопление и регистрацию аналитического сигнала проводят в тех же условиях (Фиг. 1, график 3). Пик регистрируют в диапазоне потенциалов от (-1,25±0,35)В (отн. ХСЭ), средняя высота пика составляет 87,83 нА.
Пример 2. Определение содержание Т-2 токсина в отрубях диетических пшеничных «Дивинка».
При отборе пробы для анализа Т-2 токсина следует руководствоваться требованиями ГОСТа 1243-66 «Сельскохозяйственная продукция. Методы отбора образцов при карантинном досмотре и экспертизе». Пробоподготовку для анализа Т-2 токсина проводят методом жидкостно-жидкостной экстракции с использованием соотношения CH3CN:KCl (9:1) и последующей очисткой гексаном и бензолом. Отобранную пробу измельчают в течение 1-2 минут в кофемолке или лабораторной мельнице. Навеску 20 г измельченного продукта помещают в плоскодонную коническу колбу на 250 мл, добавляют 10 мл 4% раствора хлористого калия и 90 мл ацетонитрила. Встряхивают на аппарате для встряхивания в течение 30 минут. Полученную смесь фильтруют через бумажный складчатый фильтр в мерный цилиндр, отбирают 70 мл фильтрата (аликвота соответствует 14 г исходного образца). В делительную воронку на 250 или 500 мл переносят 70 мл фильтрата, добавляют 50 мл гексана (или гептана). После встряхивания и разделения слоев верхний гексановый слой отбрасывают. Нижний ацетонитрильный слой еще дважды встряхивают с 40 мл гексана, каждый раз отбирая верхний гексановый слой. Ацетонитрильный слой разбавляют 17 мл дистиллированной воды и экстрагируют 50 и 25 мл бензола. Верхние бензольные слои отделяют и сушат безводным сернокислым натрием (10-15 г) в течение 30 минут. Раствор фильтруют через химическую воронку с кусочком ваты в кругло донную колбу на 250 мл. Сернокислый натрий промывают 10 мл бензола и отфильтровывают бензол в ту же круглодонную колбу. Упаривают бензольный раствор на ротационном испарителе при температуре водяной бани не выше 45-50°C досуха. Остаток растворяют в 200-300 мкл ацетонитрила. Полученный раствор является подготовленной пробой для вольтамперометрического измерения. Затем 0,02 мл полученного анализируемого раствора вносят в кварцевый стаканчик с фоновым раствором. Электронакопление и регистрацию аналитического сигнала проводят в тех же условиях. Катодный пик Т-2 токсина фиксируют в диапазоне (-1,25±0,35)В на стеклоуглеродном электроде при чувствительности прибора (1÷5) 10-8 А/мм в дифференциальном режиме съемки вольтамперограмм. Массовую концентрацию Т-2 токсина в пробе оценивают методом добавок аттестованных смесей, измеряя высоту катодных пиков по формуле (1):

где
X1 - содержание Т-2 токсина в анализируемой пробе, мг/мл;
Сд - концентрация аттестованной смеси /АС/ Т-2 токсина, из которой делается добавка к анализируемой пробе, мг/мл;
Vд - объем добавки АС Т-2 токсина, мл;
I1 - величина максимального тока компонента в анализируемой пробе, нА;
I2 - величина максимального тока компонента в пробе с добавкой АС, нА;
Vал - объем навески пробы, взятой для анализа, мл.
Время анализа одной пробы без учета времени пробоподготовки занимает около 20 минут.
Таким образом, впервые установлена способность количественного химического анализа Т-2 токсина по пикам электровостановления его на стеклоуглеродном электроде (в аналогах количественное определение Т-2 токсина проводят на золотом печатном электроде или модифицированном стеклоуглеродном электроде с использованием амперометрических биосенсоров или электрохимических иммунносенсоров).
Предложенный способ прост, не требует большого количества реактивов и трудозатрат и может быть приемлем в любой химической лаборатории, имеющей полярограф, особенно в настоящее время, когда налажен выпуск отечественной и зарубежной электроаппаратуры с контрольным управлением и обработкой данных (анализаторы типа СТА, ТА и др.). Предложенный способ может быть использован в медицине, фармакокинетических и фармацевтических исследованиях, сельскохозяйственной и пищевой промышленности, для разработки методик анализа Т-2 токсина и родственных ему соединений в сложных многокомпонентных биосистемах (кровь, моча). Определение концентраций в диапазоне 1·10-5÷6·10-3 мг/мл важно для пищевой и фармацевтической промышленности, в лекарственных растениях растительного происхождения.
Способ количественного определения Т-2 токсина методом дифференциальной вольтамперометрии

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АФЛАТОКСИНА В1 МЕТОДОМ ДИФФЕРЕНЦИАЛЬНОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2013 |
|
RU2534732C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ МОЛОЧНОЙ КИСЛОТЫ МЕТОДОМ ВОЛЬТАМПЕРОМЕТРИИ НА СТЕКЛОУГЛЕРОДНОМ ЭЛЕКТРОДЕ | 2013 |
|
RU2526821C1 |
| Вольтамперометрический способ определения дифениламина в продуктах выстрела | 2017 |
|
RU2657552C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СМЕСИ АФЛАТОКСИНОВ B1, B2, G1, G2 МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2015 |
|
RU2592049C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ГЕСПЕРИДИНА МЕТОДОМ ДИФФЕРЕНЦИАЛЬНОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2008 |
|
RU2381502C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БУТОПРОФИДА МЕТОДОМ ВОЛЬТАМПЕРОМЕТРИИ | 2005 |
|
RU2289127C1 |
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ 1-(2-ФТОРБЕНЗОИЛ)-5-ФЕНИЛ-5-ЭТИЛПИРИМИДИН-2,4,6(1Н,3Н,5Н)-ТРИОНА (ГАЛОНАЛА) | 2017 |
|
RU2659168C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СУРЬМЫ, ВИСМУТА, МЕДИ В ВОДНЫХ РАСТВОРАХ МЕТОДОМ АНОДНО-КАТОДНОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2010 |
|
RU2419786C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ НИКЕЛЯ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ НА ОРГАНО-МОДИФИЦИРОВАННОМ ЭЛЕКТРОДЕ | 2012 |
|
RU2504761C1 |
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ПРЕДНИЗОНА В СЫВОРОТКЕ КРОВИ | 2023 |
|
RU2815787C1 |
Изобретение относится к области аналитической химии и может быть использовано в фармакокинетических исследованиях, для контроля продуктов сельскохозяйственного производства растительного происхождения. Согласно изобретению Т-2 токсин переводят из пробы в раствор и проводят вольтамперометрическое накопление микотоксина в перемешиваемом растворе в течение 30 с при потенциале электролиза (-0,5±0,05) В относительно насыщенного хлоридсеребряного электрода на фоне нитрата калия (KNO3), рН 4,0÷5,0, с последующей регистрацией катодных пиков при скорости развертки 30 мВ/с. Концентрацию Т-2 токсина определяли по высоте пика в диапазоне Еn=(-1,25±0,35) В методом добавок аттестованных смесей. Изобретение обеспечивает расширение диапазона определяемых концентраций Т-2 токсина и разработки экспресс-технологии оценки Т-2 токсина в течение 30-40 мин и возможность использования электродов из нетоксичного материала. 1 ил., 2 табл., 2 пр.
Способ количественного определения Т-2 токсина, включающий перевод Т-2 токсина из пробы в раствор и вольтамперометрическое определение с использованием индикаторного стеклоуглеродного электрода, отличающийся тем, что используют дифференциальную вольтамперометрию, при этом накопление Т-2 токсина в перемешиваемом растворе проводят в течение 30 с при потенциале электролиза Eэ=(-0,5±0,05) В относительно насыщенного хлоридсеребряного электрода на фоне 0,1 М нитрата калия с последующей регистрацией катодных пиков в дифференциальном режиме съемки вольтамперограмм при скорости развертки потенциала 30 мВ/с и концентрацию Т-2 токсина определяют по высоте пика в диапазоне потенциалов Eп=(-1,25±0,35) В методом добавок аттестованных смесей.
| СПОСОБ ОПРЕДЕЛЕНИЯ МИКОТОКСИНОВ В ПРОДУКТАХ ЖИВОТНОГО И РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ | 2012 |
|
RU2514828C2 |
| CN203203997U, 18.09.2013 | |||
| US2011306508A, 15.12.2011 | |||
| ИЗМЕРИТЕЛЬ ДЕФОРМАЦИИ И СПОСОБЫ ИЗМЕРЕНИЯ ДЕФОРМАЦИИ (ВАРИАНТЫ) | 2006 |
|
RU2322649C1 |
| US5641632A, 24.06.1997 | |||
| Форсунка | 1931 |
|
SU26008A1 |
Авторы
Даты
2016-04-10—Публикация
2015-02-02—Подача