Изобретение относится к области молекулярной биологии и диагностической медицины и может быть использовано для выделения микроРНК из биологических жидкостей.
МикроРНК представляют собой класс коротких (19-24 нуклеотидов) некодирующих молекул рибонуклеиновых кислот (РНК), которые регулируют экспрессию генов млекопитающих на посттранскрипционном уровне. МикроРНК принимают участие в регуляции таких важнейших биологических процессов, как клеточный рост и дифференцировка, метаболизм и апоптоз, иммунный ответ. Изменение экспрессии микроРНК наблюдается при различных заболеваниях, включая онкологические, сердечно-сосудистые заболевания, неврологические, психические расстройства, аутоиммунные заболевания, сахарный диабет.
Клиническими исследованиями показано, что микроРНК могут выступать в качестве биомаркеров и изменение уровня их экспрессии может быть использовано для диагностики вышеперечисленных заболеваний, в том числе для раннего выявления опухолевого/патологического процесса, оценки прогноза заболевания и раннего выявления рецидивов, мониторинга эффективности терапии, включая лучевую и химиотерапию (1, 2, 3).
Показано, что микроРНК, характерные для разных тканей, в том числе и тканей опухолей, присутствуют в биологических жидкостях организма, таких как кровь, моча, спинномозговая жидкость, бронхоальвеолярные смывы и т.д. (4). В составе этих жидкостей микроРНК остаются стабильны в течение длительного времени благодаря тому, что формируют прочные комплексы с белками (5), липопротеинами (6) и/или находятся в составе окруженных мембранами частиц (экзосомы, апоптические тельца, микрочастицы) (7). Разрушение таких комплексов требует специальных условий и осложняет процесс выделения микроРНК из биологических жидкостей.
Основным препятствием в выделении высококачественных препаратов микроРНК из биологических жидкостей является высокое содержание в исходном материале биополимеров ненуклеотидной природы (белки, липопротеины, липиды и их комплексы), в том числе образующих прочные комплексы с микроРНК, присутствие в них ингибиторов ферментов, используемых в последующем анализе (например, ПЦР), а также высокое содержание ферментов, расщепляющих нуклеиновые кислоты.
Таким образом, получение высокоочищенных препаратов недеградированных микроРНК, пригодных для последующего анализа (ОТ-ПЦР, микрочиповый анализ, полногеномное секвенирование) является актуальной проблемой в молекулярной биологии и диагностической медицине.
В настоящее время для получения микроРНК из биологических жидкостей традиционно используются способы, основанные на фенольной экстракции.
Известен, например, способ выделения микроРНК, включающий смешивание образца, растворенного в 4М растворе гуанидин изотиоцианата с водонасыщенным фенолом в кислой среде, с последующим разделением фаз при помощи добавления хлороформа (8). При центрифугировании такой смеси суммарная РНК остается в верхней водной фазе, белки образуют интерфазу, а ДНК переходит в органическую фазу. Варианты последующей очистки включают переосаждение спиртами или дополнительную очистку РНК, например, на стекловолоконных сорбентах (9).
Способы фенольной экстракции используются также в ряде коммерческих наборов для выделения микроРНК, таких как TRIZOL LS. В ряде коммерческих наборов (miRVANA, miRNeasy и др.) для обогащения по микроРНК используется дополнительная стадия очистки на колонках со стекловолокнистыми сорбентами (9).
Основными недостатками вышеназванных способов являются многостадийность, низкая процессивность, трудоемкость процесса выделения, использование токсичных химических реагентов, зависимость от квалификации исполнителя и сложность автоматизации процесса выделения.
Наиболее близким к предлагаемому способу - прототипом является способ выделения микроРНК, включающий, согласно инструкции производителя, последовательное добавление к исследуемому образцу растворов для денатурации комплексов микроРНК с биополимерами и осаждения белков/гликолипопротеинов/протеогликанов с последующим инкубированием микроРНК-содержащего раствора (биологической жидкости) и осаждением преципитата центрифугированием. Далее к полученному супернатанту добавляют изопропиловый спирт и наносят полученный раствор на микроколонку со стекловолокнистым сорбентом (Exiqon A/S, Дания), связывающим микроРНК. Сорбент отмывают от несвязавшихся биополимеров и избытка химических агентов буферами для промывки, целевой продукт элюируют водой (10).
Недостатками прототипа являются недостаточный выход микроРНК из биологических жидкостей, а также высокая стоимость выделения целевого продукта.
Задачей изобретения является повышение эффективности выделения микроРНК из биологических жидкостей.
Технический результат: повышение выхода и снижение стоимости выделения целевого продукта.
Поставленная задача достигается предлагаемым способом, заключающимся в следующем.
К образцу биологической жидкости последовательно добавляют равный объем денатурирующего раствора, содержащего 0.3 М - 1.35 М гуанидин изотиоцианат и 1% 2-меркаптоэтанол (в конечной концентрации), затем добавляют равный объем буфера для осаждения, содержащего в конечных концентрациях 0.8 М натрия ацетат рН 4.0-6.0, и 0.5% - 2.5% октановую кислоту. Смесь перемешивают, инкубируют в течение 3-5 минут при комнатной температуре и центрифугируют при 16.200 g. В полученный супернатант добавляют равный объем 96% этанола и наносят на микроколонку производства ООО «БиоСилика» методом вакуумной фильтрации или центрифугированием. Сорбент промывают от примесей биополимеров ненуклеотидной природы сначала буферным раствором, содержащим 0.5 М гуанидин изотиоцианат, 10 мМ Трис-ацетат рН 6.5, 50%) этанол, 1% 2-меркаптоэтанол, а затем буферным раствором, содержащим 10 мМ Tris-HCl рН 7.5, 0,1 М NaCl, 75% этанол. Элюцию микроРНК с сорбента осуществляют раствором, содержащим 10 мМ ЭДТА рН 9.5.
Определяющими отличительными признаками предлагаемого способа, по сравнению с прототипом, являются:
1. МикроРНК-содержащие комплексы в составе образца биологической жидкости денатурируют раствором, содержащим 0.3 М - 1.35 М гуанидин изотиоцианат и 1%-ный 2-меркаптоэтанол, что позволяет эффективно ингибировать РНК-гидролизующие ферменты, создать условия для последующей эффективной диссоциации и повысить выход микроРНК из нуклеопротеиновых комплексов и сократить время выделения;
2. Осаждение нецелевых биополимеров осуществляют буферным раствором, содержащим 0.8 М натрия ацетат рН 4.0-6.0 и 0.5-2.5% октановую кислоту с последующим центрифугированием, что позволяет дополнительно выделить микроРНК из нуклеопротеиновых комплексов, осадить нецелевые биополимеры и, в результате, повысить выход целевого продукта;
3. К полученному супернатанту добавляют равный объем 96% этанола, что позволяет повысить эффективность связывания микроРНК с сорбентом, а также способствует денатурации оставшихся белков и липопротеинов, дополнительной диссоциации нуклеопротеиновых комплексов. Это способствует обогащению по содержанию микроРНК в препарате, увеличивает чистоту и выход продукта;
4. Отмывку сорбента от несвязавшихся биополимеров осуществляют последовательно сначала буферным раствором, содержащим 0.5 М гуанидин изотиоцианат, 10 мМ Трис-ацетат, рН 6.5, 50% этанол, 1% 2-меркаптоэтанол, а затем буферным раствором, содержащим 10 мМ Tris-HCl рН 7.5, 0,1 М NaCl, 75% этанол, что обеспечивает эффективное удаление примесей ненуклеотидной природы с поверхности сорбента и повышает чистоту получаемого препарата микроРНК.
Таким образом, предлагаемый способ позволяет быстро и эффективно выделять микроРНК из плазмы крови и мочи.
Изобретение иллюстрируется следующими примерами конкретного выполнения способа.
Пример 1. Выделение микроРНК из плазмы крови
В 200 мкл плазмы крови здоровых доноров вносили 100 мкл денатурирующего раствора с разной концентрацией гуанидин изотиоцианата и 5 мкл 100% 2-меркаптоэтанола, таким образом, чтобы получить конечную концентрацию гуанидин изотиоцианата в растворе 0.3 М, 0.6 М, 0.9 М или 1.35 М, а 2-меркаптоэтанола - 1%. Затем вносили 200 мкл буфера для осаждения, содержащего в конечной концентрации 0.8 М ацетат натрия рН 4.0, 5.0 или 6.0 и октановую кислоту, конечная концентрация которой составляла 0.5%, 1.5% и 2.5%. После добавления каждого реагента перемешивали раствор на встряхивателе в течение 3-5 секунд, полученный раствор инкубировали в течение 3 минут при комнатной температуре и осаждали получившийся преципитат центрифугированием при 16.000 g (Thermo Scientific, США) в течение 3-х минут. К полученному супернатанту добавляли равный объем 96% этанола.
Супернатант наносили на микроколонку производства ООО «БиоСилика», представляющую собой пластиковую емкость цилиндрической формы, закрывающуюся крышкой, с отверстием в конусном дне, на котором находится 10-15 мг стекловолокнистого сорбента, состоящего из волокон щелочного стекла, диаметр которых составляет 0,4-1 микрон. Для нанесения супернатанта использовали центрифугу (Thermo Scientific, США) при 400 g, в течение 30 секунд. Сорбент промывали 300 мкл буфера, содержащего 0.5 М гуанидин изотиоцианат, 10 мМ Трис-ацетат рН 6.5, 50% этанол, 1% 2-меркаптоэтанол. Затем сорбент промывали 300 мкл буфера, содержащего 10 мМ Tris-HCl рН 7.5, 0,1 М NaCl, 75% этанол и элюировали микроРНК добавлением 120 мкл буфера, содержащего 10 мМ ЭДТА, рН 9.5 (центрифугированием при 400 g, 1 мин, 20 с при 16.200 g).
МикроРНК переосаждали в присутствие гликогена (конечная концентрация 112 мкг/мл) 2-кратным объемом изопропанола (30 минут при -20°С, центрифугирование при 13000 g (Eppendorf 5810 r) в течение 15 мин при 4°С). Осадок последовательно промывали 75% и 96% этанолом, сушили на воздухе и растворяли в 30 мкл воды.
Далее, выделенные микроРНК анализировали методом ОТ-ПЦР в реальном времени (11), позволяющим селективно выявлять микроРНК с высокой чувствительностью и специфичностью. Метод ОТ-ПЦР включает в себя обратную транскрипцию микроРНК с помощью праймера со шпилькой, с последующей детекцией полученной кДНК с помощью ПЦР в реальном времени.
Для обратной транскрипции использовали праймеры RT:
5′GTCGTATCCAGTGCAGGGTCCGAGGTATTCGCACTGGATACGACCGCCAA-3′ (hsa-miR-16-5p), RT:
5′GTCGTATCCAGTGCAGGGTCCGAGGTATTCGCACTGGATACGACGCATTA-3′ (hsa-miR-126-3р) и ревертазу (Fermentas, Vilnius, Lithuania).
Условия обратной транскрипции: 16°С - 30 мин, 42°С - 30 мин, 70°С - 10 мин.
Для ПЦР использовали: Universal Reverse Primer 5′-GTGCAGGGTCCGAGGT-3′, Forward: 5′GCCCGTAGCAGCACGTAAATAT-3′, Probe: 5′-(FAM)-GCACTGGATACGACCGCCAA-(FQ)-3′ (hsa-miR-16-5p) и Universal Reverse Primer 5′-GTGCAGGGTCCGAGGT-3′, Forward: 5′-CCGCTCGTACCGTGAGTAAT-3′, Probe: 5′-(FAM)-GCACTGGATACGACGCATTA-(FQ)-3′ (hsa-miR-126-3р).
После первоначальной денатурации при 95°С в течение 3 мин, реакции проводили в течение 50 циклов при 95°С в течение 15 с и 60°С в течение 45 с. Праймеры и зонды для обратной транскрипции и TaqMan qPCR были синтезированы в лаборатории медицинской химии ИХБФМ СО РАН, Новосибирск.
Пример 2. Выделение микроРНК из мочи.
В 400 мкл мочи здоровых доноров вносили 200 мкл денатурирующего раствора с разной концентрацией гуанидин изотиоцианата и 10 мкл 100% 2-меркаптоэтанола, таким образом, чтобы получить конечную концентрацию гуанидин изотиоцианата в растворе 0.3 М, 0.6 М, 0.9 М или 1.35 М, а 2 меркаптоэтанола - 1%. Затем вносили 400 мкл буфера для осаждения, содержащего ацетат натрия рН 4.0, 5,0 или 6,0 и октановую кислоту, конечные концентрации которых составляли 0.8 М и 0.5%, 1.5% или 2.5%, соответственно. После добавления каждого реагента перемешивали раствор на встряхивателе в течение 3-5 секунд, полученный раствор инкубировали в течение 3 минут при комнатной температуре и осаждали получившийся преципитат центрифугированием при 16.200 g (Thermo Scientific, США) в течение 3 минут. К полученному супернатанту добавляли равный объем 96% этанола. Для выделения микроРНК, супернатант наносили на микроколонку производства ООО «БиоСилика» с использованием центрифуги (Thermo Scientific, США) при 400 g, в течение 30 секунд. Сорбент промывали 300 мкл буфера, содержащего 0.5 М гуанидин изотиоцианат, 10 мМ Трис-ацетат рН 6.5, 50% этанол, 1% 2-меркаптоэтанол. Затем сорбент промывали 300 мкл буфера, содержащего 10 мМ Tris-HCl рН 7.5, 0,1 М NaCl, 75% этанол и элюировали микроРНК добавлением 120 мкл буфера для элюции (центрифугированием при 400 g, 1 мин, 20 сек при 16.200 g). МикроРНК переосаждали в присутствие гликогена (конечная концентрация 112 мкг/мл) 2-х кратным объемом изопропанола (30 минут при -20°С, центрифугирование при 13000 g (Eppendorf 5810r) в течение 15 мин при 4°С). Осадок последовательно промывали 75%) и 96% этанолом, сушили на воздухе и растворяли в 30 мкл воды.
Далее проводили ОТ-ПЦР аналогично примеру 1.
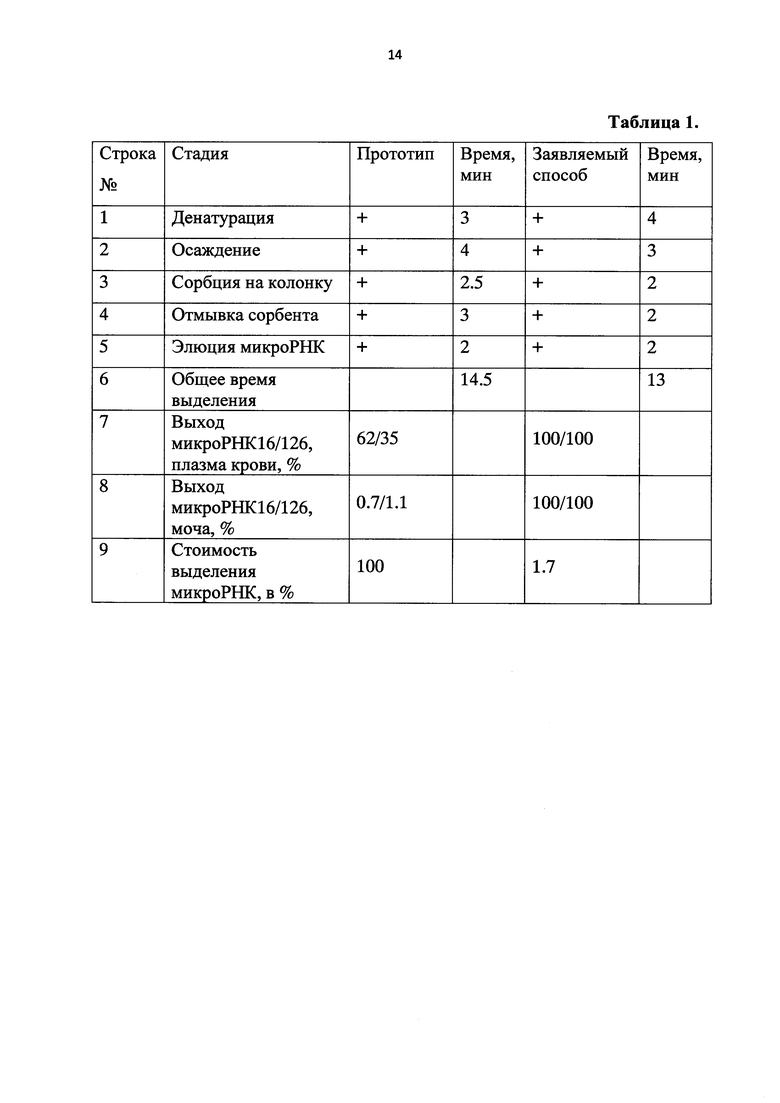
Сопоставительный анализ заявляемого способа, по сравнению с прототипом, представлен в таблице 1. Из таблицы 1 видно, что предлагаемый способ имеет следующие преимущества по сравнению с прототипом: позволяет выделять микроРНК из плазмы крови и мочи с большей эффективностью (строки 7, 8); позволяет сократить время выделения микроРНК на 10% (строки 1-6); позволяет сократить стоимость выделения микроРНК по меньшей мере в 58 раз (строка 9).
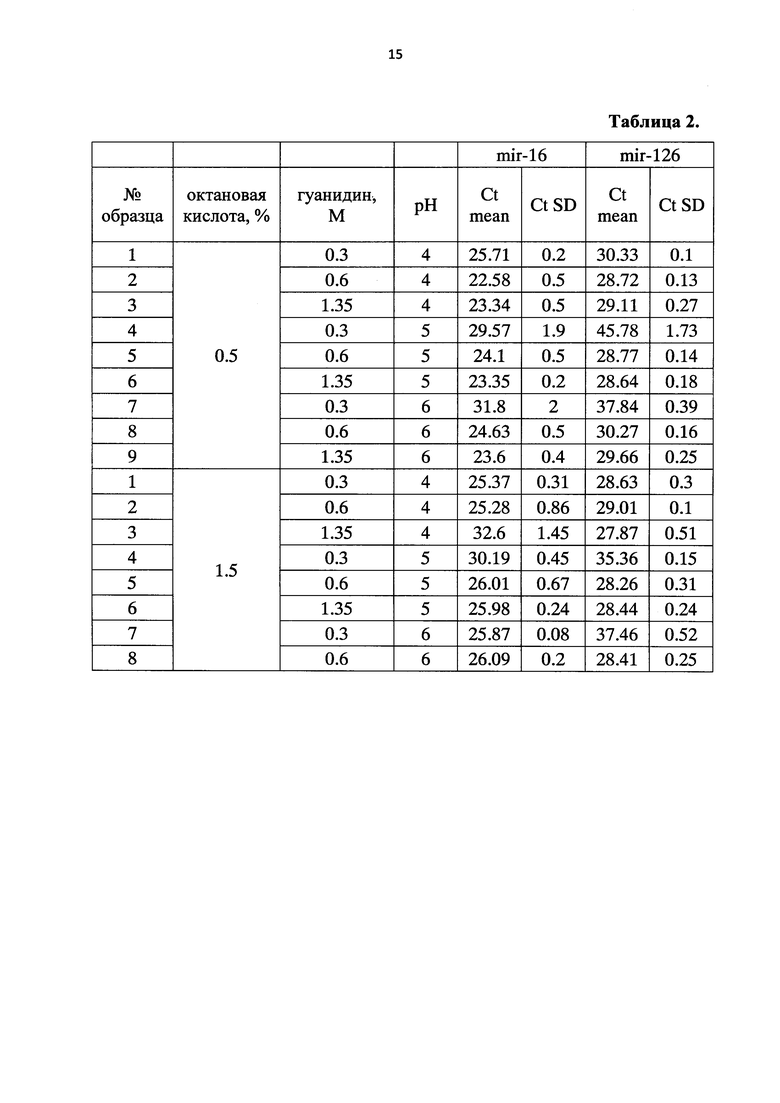
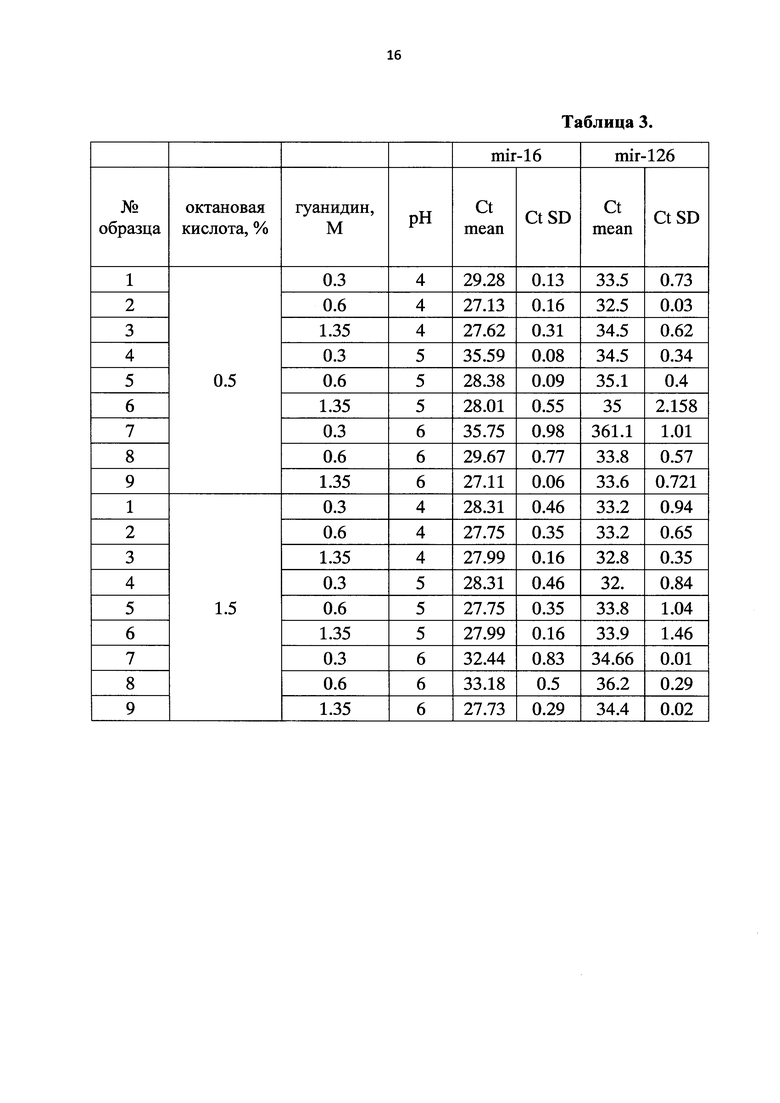
Эффективность выделения микроРНК из плазмы крови и мочи здоровых доноров (в зависимости от концентраций гуанидин изотиоцианата, октановой кислоты и рН раствора) представлена в таблицах 2, 3. Все выделения выполнены из одного сливного препарата плазмы крови. В таблице представлены средние значения порогового цикла (Ct mean) и стандартное отклонение значения порогового цикла (Ct SD), полученные в трех независимых экспериментах.
Из таблиц 2, 3 следует, что наиболее оптимально удаление полимеров ненуклеотидной природы и выделение микроРНК из плазмы крови происходит при рН 4,0, концентрации гуанидин изотиоцианата 0,6 М и концентрации октановой кислоты 0,5%, а из мочи - при рН 4,0, концентрации гуанидин изотиоцианата 1.35 М и концентрации октановой кислоты 1.5%.
В этих условиях наблюдается удаление 88% общего сывороточного белка из плазмы крови и 74% белка из мочи, при этом не наблюдается опалесценции раствора, то есть удаляются и липид-содержащие биополимеры и их комплексы, а микроРНК выделяются с максимальной эффективностью. При этом используется минимальное количество реагентов, что обеспечивает минимальную цену выделения препарата микроРНК (таблица 1, строка 9).
Пример 3.
Для оценки эффективности выделения микроРНК заявляемым способом и способом-прототипом из образцов плазмы и мочи здоровых доноров были выделены микроРНК 16 и микроРНК 126 и их концентрация определена методом количественной ПЦР. Все операции выделения микроРНК способом-прототипом выполняли, как рекомендовано производителем набора miRCURY™ RNA Isolation Kit-Biofluids (Exiqon A/S, Дания), а заявляемым способом так, как описано в примере 1.
Сравнение эффективности выделения микро РНК заявляемым способом и способом-прототипом из плазмы крови приведено в таблице 4.
Из таблицы 4 видно, что предлагаемый способ по количеству выделенной микроРНК из плазмы крови существенно превосходит прототип. Во всех случаях выделения микроРНК 16 и микроРНК 126 из плазмы крови, средние пороговые значения предложенного способа значительно больше пороговых значений прототипа. Эффективность выделения микроРНК 16 заявляемым способом из плазмы крови превышает таковую для способа-прототипа в 1.62 раза, а выделения микроРНК 126 - в 2,85 раз.
Сравнение эффективности выделения микроРНК из мочи 5 здоровых доноров представлено в таблице 5. В случае выделения микроРНК из мочи, предлагаемый способ так же существенно превосходит способ-прототип. Действительно, эффективность выделения микроРНК 16 заявляемым способом превышает таковую для прототипа в 142 раза, а эффективность выделения микроРНК 126 - в 90 раз.
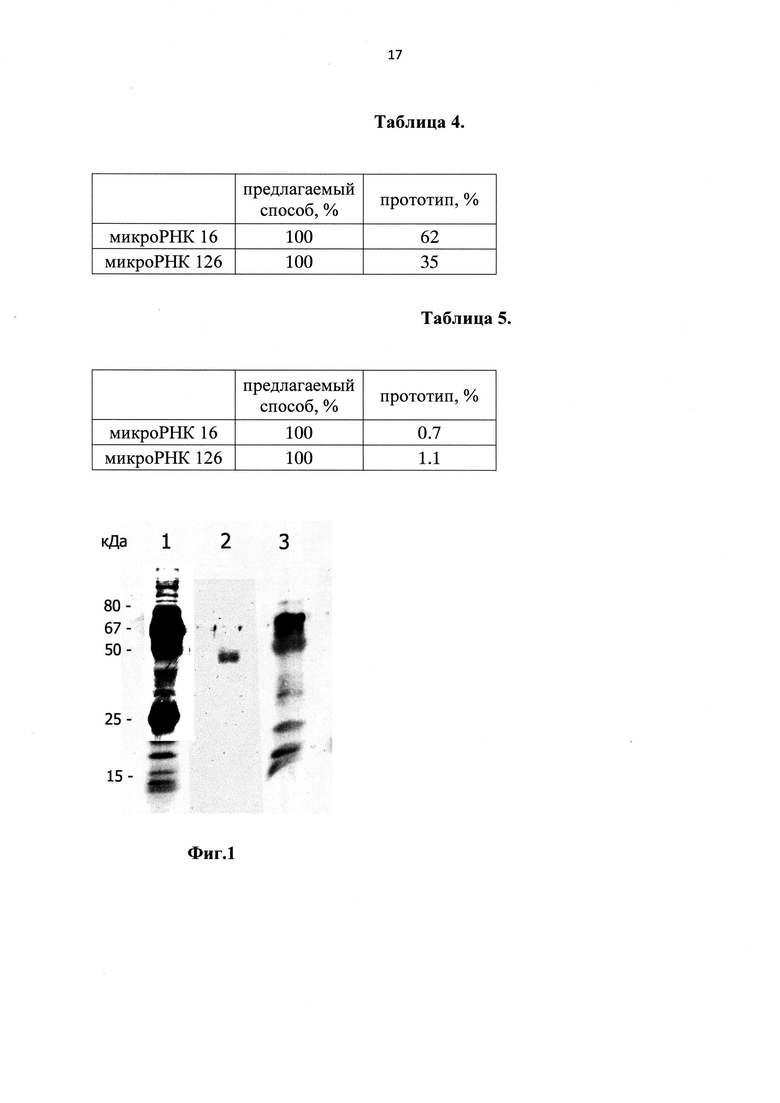
На фиг. 1 представлен электрофоретический анализ белков супернатантов из плазмы крови, полученных в результате выделения при помощи предлагаемого способа и прототипа, где дорожки: 1 - образец плазмы крови, 2 - супернатант плазмы крови при выделении способом-прототипом, 3 - супернатант плазмы крови при выделении предлагаемым способом.
Анализ набора белков супернатантов, полученных при выделении предлагаемым способом и прототипом, показывает, что при использовании способа-прототипа в супернатанте остается только один белок, в отличие от заявляемого способа, что может косвенно свидетельствовать об отличии осадителя, используемого в предлагаемом способе (октановой кислоты) от осадителя, используемого в прототипе (фиг. 1). Кроме того, очевидно, что при использовании способа-прототипа на стадии денатурации/осаждении одновременно с осаждением белков, осаждается и часть микроРНК (таблицы 2 и 3).
Использование предлагаемого способа позволит ускорить селективное выделение микроРНК, повысить суммарный выход микроРНК, а также снизить стоимость выделения целевого продукта. Способ может быть адаптирован для различных биологических жидкостей.
Источники информации
1. Colles Price, Jianjun Chen. MicroRNAs in Cancer Biology and Therapy: Current Status and Perspectives // Genes Dis. - 2014. - V. 1. - P. 53-63.
2. Wen-Tao Wang and Yue-Qin Chen. Circulating miRNAs in cancer: from detection to therapy // Wang and Chen Journal of Hematology & Oncology. - 2014. - V. 7. - P. 86.
3. Wen X., Deng F.M., Wang J. MicroRNAs as predictive biomarkers and therapeutic targets in prostate cancer // Am J ClinExp Urol - 2014. - V. 2. - P. 219-230.
4. Hanson E.K., Lubenow H., Ballantyne J. Identification of forensically relevant body fluids using a panel of differentially expressed microRNAs // Anal.
5. Arroyo J.D., Chevillet J.R., Kroh E.M., Ruf I.K., Pritchard C.C., Gibson D.F., Mitchell P.S., Bennett C.F., Pogosova-Agadjanyan E.L., Stirewalt D.L. et al. Argonaute2 complexes carry a population of circulating microRNAs independent of vesicles in human plasma // Proc. Natl. Acad. Sci. - 2011. - V. 108. - P. 5003-5008.
6. Vickers K.C., Palmisano B.T., Shoucri, B.M.; Shamburek R.D., Remaley A.T. MicroRNAs are transported in plasma and delivered to recipient cells by high-density lipoproteins // Nat. Cell. Biol. - 2011. - V. 13. - P. 423-433.
7. Raposo G.; Stoorvogel W. Extracellular vesicles: Exosomes, microvesicles, and friends // J. Cell Biol. - 2013. - V. 200. - P. 373-383.
8. Chomczynski P., Sacchi N. The single step method of RNA isolation by acid guanidiniumthiocyanate-phenol-chloroform extraction: twenty-something years on. // Nature Protocols. - 2006. - V. 1. - P. 581-585.
9. Eldh M., Lötvall J., Malmhäll C., Ekström K. Importance of RNA isolation methods for analysis of exosomal RNA: evaluation of differentmethods // Mol Immunol. - 2012. - V. 4. - P. 278-86.
10. McAlexander M.A., Phillips M.J., Witwer K.W. Comparison of Methods for miRNA Extraction from Plasma and Quantitative Recovery of RNAfrom Cerebrospinal Fluid // Front Genet. - 2013. - V. 4. - P. 1-8.
11. Kubista M., Andrade J.M., Bengtsson M., Forootan A., Jonák J., Lind K., Sindelka R., Sjöback R., Sjögreen В., Strömbom L., Ståhlberg A., Zoric N. The real-time polymerase chain reaction // Mol Aspects Med. - 2006. - V. 27. - P. 95-125.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫДЕЛЕНИЯ КОРОТКИХ РНК ИЗ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ | 2014 |
|
RU2558292C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ЦИРКУЛИРУЮЩИХ ДНК ИЗ ПЛАЗМЫ ИЛИ СЫВОРОТКИ КРОВИ | 2015 |
|
RU2603098C1 |
| Способ выделения внеклеточных везикул из биологических жидкостей | 2018 |
|
RU2678988C1 |
| Способ выделения ДНК из парафиновых блоков с гистологическим биоматериалом | 2016 |
|
RU2637360C1 |
| СПОСОБ ВЫДЕЛЕНИЯ НУКЛЕИНОВЫХ КИСЛОТ | 2004 |
|
RU2272072C1 |
| Способ выделения ДНК из почвы | 2018 |
|
RU2696052C1 |
| СПОСОБ ВЫДЕЛЕНИЯ РИБОНУКЛЕИНОВЫХ КИСЛОТ | 2002 |
|
RU2232810C1 |
| Способ выделения целевых фрагментов ДНК из многокомпонентной смеси | 2024 |
|
RU2832884C1 |
| Аналитическая система для диагностики рака лёгкого при помощи свободных и ассоциированных с клетками крови циркулирующих микроРНК | 2020 |
|
RU2755651C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ДНК ИЗ КОСТНОГО МАТЕРИАЛА | 2019 |
|
RU2724506C1 |
Изобретение относится к области молекулярной биологии и диагностической медицины. Предложен способ выделения микроРНК из биологических жидкостей. Способ включает обработку образца биологической жидкости равным объемом денатурирующего буферного раствора, содержащего 0.3÷1.35 М гуанидин изотиоцианат, 1% 2-меркаптоэтанол, осаждение нецелевых биополимеров добавлением равного объема буферного раствора, содержащего 0.8 М натрия ацетат, рН 4.0-6.0 и 0.5-2.5% октановую кислоту и центрифугированием. К полученному супернатанту добавляют равный объема 96% этанола, отмывку сорбента от несвязавшихся биополимеров осуществляют сначала буферным раствором, содержащим 0.5 М гуанидин изотиоцианат, 10 мМ Трис-ацетат рН 6.5, 50% этанол, 1% 2-меркаптоэтанол, затем буферным раствором, содержащим 10 мМ Tris-HCl рН 7.5, 0,1 М NaCl, 75% этанол. Изобретение обеспечивает повышение выхода микроРНК. 2 з.п. ф-лы, 1 ил., 5 табл., 3 пр.
1. Способ выделения микроРНК из биологических жидкостей, включающий обработку образца денатурирующим буферным раствором, осаждение нецелевых биополимеров с последующим центрифугированием и отделением супернатанта, добавление к последнему спирта и сорбцию микроРНК на стекловолокнистом сорбенте в присутствии хаотропного агента с последующей отмывкой сорбента от несвязавшихся биополимеров и химических реагентов и элюцией целевого продукта, отличающийся тем, что образец биологической жидкости обрабатывают равным объемом денатурирующего буферного раствора, содержащего 0.3÷1.35 М гуанидин изотиоцианат, 1% 2-меркаптоэтанол, осаждение нецелевых биополимеров осуществляют добавлением равного объема буферного раствора, содержащего 0.8 М натрия ацетат, рН 4.0-6.0 и 0.5-2.5% октановую кислоту и центрифугированием, к полученному супернататанту добавляют равный объема 96% этанола, а отмывку сорбента от несвязавшихся биополимеров осуществляют сначала буферным раствором, содержащим 0.5 М гуанидин изотиоцианат, 10 мМ Трис-ацетат рН 6.5, 50% этанол, 1% 2-меркаптоэтанол, а затем буферным раствором, содержащим 10 мМ Tris-HCl рН 7.5, 0,1 М NaCl, 75% этанол.
2. Способ по п. 1, отличающийся тем, что для выделения микроРНК используют микроколонки со стекловолокнистым сорбентом производства ООО «БиоСилика».
3. Способ по п. 1, отличающийся тем, что элюцию микроРНК с сорбента проводят раствором, содержащим 10 мМ ЭДТА, рН 9.5.
| СПОСОБ ВЫДЕЛЕНИЯ ВНЕКЛЕТОЧНЫХ НУКЛЕИНОВЫХ КИСЛОТ ИЗ МОЧИ | 2006 |
|
RU2311640C1 |
| СПОСОБ ВЫДЕЛЕНИЯ НУКЛЕИНОВЫХ КИСЛОТ | 2004 |
|
RU2272072C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ВНЕКЛЕТОЧНЫХ ДЕЗОКСИРИБОНУКЛЕИНОВЫХ КИСЛОТ ИЗ КРОВИ | 2008 |
|
RU2372405C1 |
| СПОСОБ ВЫДЕЛЕНИЯ РИБОНУКЛЕИНОВЫХ КИСЛОТ | 2002 |
|
RU2232810C1 |
Авторы
Даты
2016-05-27—Публикация
2015-05-06—Подача