Изобретение относится к фармакологии и медицине, а именно к синтетическому гепатопротекторному средству пиримидинового ряда L-аскорбату 1-(2-гидроксиэтил)-4,6-диметил-1,2-дигидропиримидин-2-она формулы
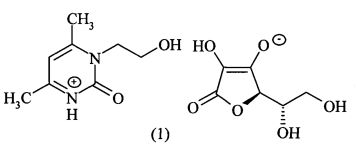
Среди гепатопротекторов пиримидины используются в качестве средств, стимулирующих белковый синтез и восстановление клеток печени при ее повреждениях токсической и инфекционной этиологии. Калия оротат - один из предшественников пиримидиновых нуклеотидов (урацил, тимин, цитозин), входящих в состав нуклеиновых кислот. Калия оротат усиливает репаративные и регенеративные процессы в тканях, увеличивает синтез альбуминов в печени и применяется как регенерант и нестероидный анаболик при нарушениях белкового обмена. Установлен гепатозащитный эффект для аддуктов оротовой кислоты с аминокислотами и диаминами [Патент РФ №2047606, опубл. 10.11.1995].
При экспериментальном токсическом гепатите обнаружена гепатопротекторная активность некоторых производных пиримидина [Новиков В.Е., Климкина Е.И. Фармакология гепатопротекторов // Обзоры по клинической фармакологии и лекарственной терапии. - 2005. - Т. 4. - №1. - С. 2-20]. Установлено, что аналоги пиримидиновых нуклеотидов - препараты Метилурацил и Пентоксил - оказывают слабо выраженное гепатопротективное действие [Тауки А.Н., Федоров В.Н., Куница З.А., Смирнов Н.А., Кочнева Н.В. Сравнительная эффективность лекарственных средств разных фармакотерапевтических групп при экспериментальном токсическом гепатите // Российский медико-биологический вестник им. академика И.П. Павлова. - 2010. Вып. 1]. Выявлено гепатопротекторное действие Оксиметилурацила [Мышкин В. А., Еникеев Д. А. Оксиметилурацил и патология печени. Экспериментальный аспект // Медицинский вестник Башкортостана. - Т. 4. - Вып. 2. - С. 147-151].
Широким спектром биологической активности, в том числе гепатопротекторными свойствами, обладают 2,4-диоксо-5-арилиденимино-1,3-пиримидины [Патент US 6730787, опубл. 04.05.2004].
Известен способ лечения заболеваний печени различного генеза с применением производных бис (2-тио-4,6-диоксо-1,2,3,4,5,6-гексагидропиримидин-5-ил)арилметанов [Патент РФ №2400233, опубл. 27.09.2010].
Наиболее близким (по структуре химического соединения) техническим решением является применение в качестве гепатопротектора лекарственного средства Ксимедон. Препарат Ксимедон (1-(β-оксиэтил)-4,6-диметил-1,2-дигидро-2-оксопиримидин) предназначен для лечения и профилактики осложнений гнойно-септических заболеваний [Патент РФ 2195283, опубл. 27.12.2002]. Показано, что применение Ксимедона приводит к увеличению активности микросомальных оксидаз печени человека [Патент РФ 2316327, опубл. 10.02.2008]. Ксимедон обладает широким спектром фармакологических эффектов [Измайлов С.Г. и др. Ксимедон в клинической практике. Нижний Новгород: Изд-во НГМА 2001]. Недостатком Ксимедона является невысокая гепатопротекторная активность.
Заявляемое соединение - L-аскорбат 1-(2-гидроксиэтил)-4,6-диметил-1,2-дигидропиримидин-2-она известно только как средство, оказывающее стимулирующее влияние на физическую работоспособность [Патент РФ 2515247 С1, опубл. 10.05.2014].
Задачей, на решение которой направлено изобретение, является расширение арсенала гепатопротекторных средств пиримидинового ряда, а также расширение сферы применения L-аскорбата 1-(2-гидроксиэтил)-4,6-диметил-1,2-дигидропиримидин-2-она.
Технический результат - новое синтетическое гепатопротекторное средство, обладающее способностью уменьшать функциональные и структурные нарушения гепатоцитов и ускорять восстановление структуры и функции печени при токсическом гепатите.
Технический результат достигается применением L-аскорбата 1-(2-гидроксиэтил)-4,6-диметил-1,2-дигидропиримидин-2-она в качестве средства гепатопротекторного действия.
Синтез заявляемого средства - L-аскорбата 1-(2-гидроксиэтил)-4,6-диметил-1,2-дигидропиримидин-2-она формулы (1) осуществляли по способу, изложенному нами ранее [Патент РФ 2515247, опубл. 10.05.2014], кипячением 1-(2-гидроксиэтил)-4,6-диметил-1,2-дигидропиримидин-2-она с L-аскорбиновой кислотой в метиловом спирте.
Токсичность заявляемого средства определяли при внутрибрюшинном введении белым мышам с последующей оценкой падежа животных. Расчет ЛД50 проводили в программе «R» version 2.13.0 (2011-04-13).
Исследование гепатопротекторных свойств L-аскорбата 1-(2-гидроксиэтил)-4,6-диметил-1,2-дигидропиримидин-2-она формулы (1) осуществляли в соответствии с методикой, изложенной в [Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. - М.: Минздрав РФ ЗАО «ИИА «Ремедиум». - 2005. - С.685]. Для изучения гепатопротекторных свойств заявляемого соединения использованы терапевтическая и профилактическая схемы воздействия.
По окончании введения препаратов животных умерщвляли под эфирным наркозом, отбирали кровь для биохимических исследований и печень для гистологических и иммуногистохимических исследований. Биохимические показатели определяли в сыворотке крови на биохимическом анализаторе Daytona Randox с использованием набора реактивов Randox. Измеряли общепринятые биомаркеры токсического повреждения клеток печени (ферменты цитолиза): аланинаминотрансфераза (АлАТ), аспартатаминотрансфераза (АсАТ), отношение АсАТ к АлАТ, или коэффициент де Ритиса (КдР). Синтетическую функцию печени контролировали по содержанию общего белка в сыворотке крови. Статистическую обработку проводили по ранговому непараметрическому U-критерию Манна-Уитни для сравнения двух независмых групп. Распределение переменных величин в вариационных рядах выражали через медиану и нижний и верхний квартили.
Изобретение иллюстрируется примерами конкретного осуществления.
Пример 1. Токсикологическая оценка заявляемого средства. В соответствии с данными, изложенными в [патент РФ 2515247, опубл. 10.05.2014], острая токсичность ЛД50 заявляемого средства на лабораторных крысах в условиях внутрибрюшинного введения больше 3000 мг/кг. Для более точной оценки токсикологических показателей средство вводили белым мышам массой 15-25 г внутрибрюшинно в дозах 2000, 4000, 6000 и 8000 мг/кг. Оценивали случаи гибели животных. На основании полученных результатов ЛД50 заявляемого средства составляет 5430 мг/кг, что позволяет его отнести к категории «относительно безвредных веществ» (VI класс токсичности) по способности вызывать острое отравление [Измеров Н.Ф., Саноцкий И.В., Сидоров К.К. Параметры токсикометрии промышленных ядов при однократном введении (справочник). - М.: Медицина, - 1977. - С. 196-197].
Показатели острой токсичности для препаратов сравнения: ЛД50 Ксимедона при внутрибрюшинном введении превосходит 6500 мг/кг [Измайлов С.Г. и др. Ксимедон в клинической практике. Нижний Новгород: Изд-во НГМА 2001]. ЛД50 Тиотриазолина выше 3000 мг/кг (внутрибрюшинно, мыши, собственные экспериментальные данные). Таким образом, гепатопротектор Тиотриазолин и лекарственный препарат Ксимедон также относятся к IV классу токсичности.
Полученные результаты позволяют заключить, что по параметрам острой токсичности заявляемое средство соответствует требованиям к гепатопротекторам и стимуляторам метаболизма.
Пример 2. Дизайн терапевтической схемы воздействия: в течение 3 суток моделировали токсическое повреждение печени белых крыс подкожным введением четыреххлористого углерода (ЧХУ) в смеси с растительным маслом в пропорции 1:1 в дозе 2 мл/кг (в расчете на ЧХУ). После этого в течение 5 дней животным с токсическим повреждением печени вводили перорально заявляемое средство или препараты сравнения (Ксимедон и Тиотриазолин) в дозе 20 мг/кг. Контрольная группа животных (позитивный контроль) подвергалась аналогичному воздействию ЧХУ, но в течение последующих 5 дней содержалась без введения каких-либо препаратов. По окончании введения тестируемых соединений исследовали биохимические показатели крови и проводили гистологическое исследование ткани печени. Значения биомаркеров группы интактных животных использовали для вычисления референтных (нормативных) интервалов.
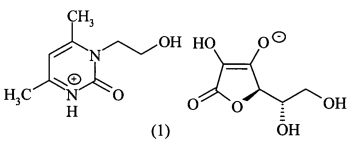
Результаты исследования биомаркеров повреждения гепатоцитов приведены в таблице 1. В контрольной ЧХУ-группе наблюдали отклонение биохимических показателей от референтных величин интактных животных: значения АлАТ повышены в 1.9 раза (Р=0,00002), АсАТ повышены на 23.2% (Р>0.05). Коэффициент де Ритиса был снижен вдвое (Р=0,001385), уровень белка сыворотки крови снижен на 8.4% (Р=0,000046). В группах, получавших в течение 5 дней исследуемые препараты, наблюдали улучшение биохимических показателей, однако в зависимости от исследованных препаратов эффекты были различны.
Под влиянием Ксимедона активность ферментов АлАт и АсАТ имела тенденцию к снижению по сравнению с ЧХУ-контролем (Р>0,05), коэффициент де Ритиса при этом изменился несущественно. Полученные результаты свидетельствуют об отсутствии значимого гепатопротекторного эффекта Ксимедона в условиях данной экспериментальной схемы.
При применении лекарственного средства Тиотриазолина ближе всего к референтным значениям интактных животных приближался коэффициент де Ритиса. При этом уровень трансаминаз оставался повышенным, а более высокое по сравнению с другими опытными группами животных значение коэффициента де Ритиса объясняется повышением активности АсАТ. Таким образом, Тиотриазолин также проявил слабо выраженную гепатопротекторную тенденцию.
При применении заявляемого средства после затравки ЧХУ активность трансаминаз соответствовала референтным интервалам интактных животных, причем активность АлАТ была в 1,73 раза ниже в сравнении с ЧХУ-контролем (Р=0,005).
Исследуемые средства улучшили показатели, связанные с общим метаболизмом. Заявляемое средство и Ксимедон увеличивали концентрации общего белка сыворотки крови по сравнению с ЧХУ-контрольной группой (Р=0,0033 и Р=0,0047, соответственно). Полученные результаты свидетельствуют о нормализации белкового обмена и восстановлении белоксинтезирующей функции печени.
Для гистологического исследования образцы ткани печени размером 0.5×0.5×0.5 см фиксировали в 10% забуференном формалине, заливали в парафин, изготавливали срезы толщиной 5-7 мкм и окрашивали гематоксилин-эозином.
В группе интактных животных выявлено гистологическое строение печени, характерное для здоровых животных. Заметна хорошо выраженная структурная организация печени в виде долек. Границы между клетками хорошо дифференцируются. Клетки имеют форму многоугольника, края хорошо выражены. Ядра расположены по центру клеток, цитоплазма равномерная, умеренной плотности, с тонкой сетчатой базофильной структурой.
В результате воздействия ЧХУ в контрольной группе животных констатировали морфологические изменения, свидетельствующие о развитии патологического процесса токсического повреждения печеночной ткани - цитолиза гепатоцитов и некроза. У части животных (33%) наблюдали выраженный стеатоз, обусловленный жировым перерождением и некротическими изменениями. У другой части животных (67%) изменения морфологии соответствовали состоянию белковой и гидропической дистрофии гепатоцитов, охватывающей все клетки. Обнаруживали утолщение клеточных мембран с приобретением ими эозинофильной окраски, нарушение дольчатой структуры органа, увеличение объема клеток и изменение их формы (клетки становятся более округлыми), ядра смещены к периферии, цитоплазма разрежена, в некоторых клетках выявляется крупная зернистость и участки без содержимого, заполненные жиром, щелевидные пространства между клетками исчезают из-за отечности ткани. Выявляются отдельные некротизированные клетки, умеренная инфильтрация ткани лимфоидными клетками.
Во всех группах, получавших препараты, отмечается заметное улучшение морфологического строения печени по сравнению с ЧХУ группой. Эффективность используемых препаратов оценивали по уменьшению степени патологических изменений.
У крыс, получавших Ксимедон, из патологических изменений сохраняется некоторая разреженность цитоплазмы, межклеточные пространства уменьшены по сравнению с интактными животными, объем клеток выше нормы, имеются жировые инфильтраты и сохраняются локальные очаги некроза и стеатоза.
В группе, получавшей Тиотриазолин, из патологических изменений выявляется сужение межклеточных пространств, отмечены инфильтраты в клетках в виде жировых капель, отдельные очаги некроза, изменение формы гепатоцитов, уплотнение цитоплазмы, ее повышенная однородность, слабая выраженность характерной сетчатой структуры, что свидетельствует о сохранении белковой дистрофии.
В группе, получавшей заявляемое средство, в гепатоцитах наблюдали капельные жировые включения, отдельные некротизированные клетки, остаточные дистрофические изменения. Выраженность стеатоза и дистрофических нарушений гепатоцитов при этом была меньше по сравнению с контролем и группой, получавшей Ксимедон.
Таким образом, заявляемое средство противодействует ЧХУ-индуцированному некрозу (цитолизу гепатоцитов) и жировому перерождению печеночной ткани и нормализует белоксинтезирующую функцию печени. Гепатопротекторный эффект заявляемого средства превосходит гепатопротекторный эффект Ксимедона и Тиотриазолина.
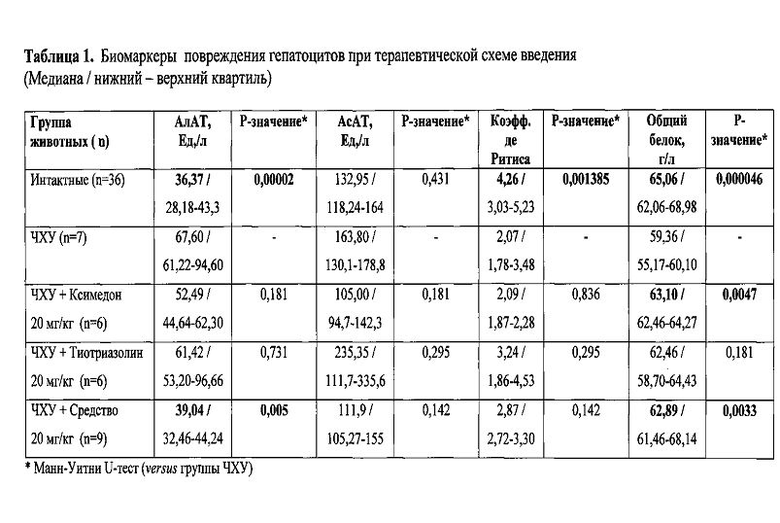
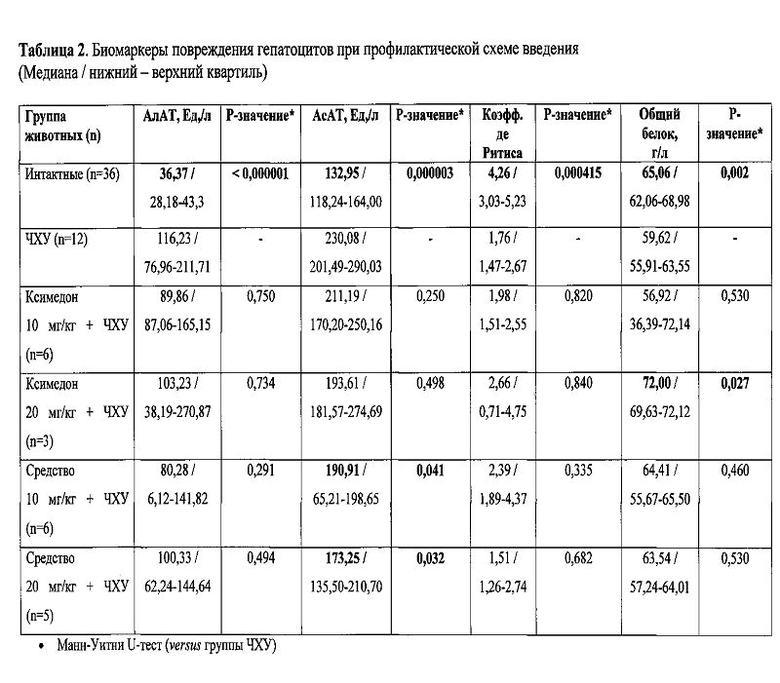
Пример 3. Дизайн профилактической схемы воздействия: в течение 4 суток животным вводили заявляемое средство или Ксимедон перорально в дозах 10 и 20 мг/кг. В течение этих же 4-х суток через 1-1.5 часа после введения препаратов вводили ЧХУ в смеси с растительным маслом в пропорции 1:1 в дозе 2 мл/кг (в расчете на ЧХУ). Животным контрольной группы (позитивный контроль) вводили ЧХУ в смеси с растительным маслом в пропорции 1:1 в дозе 2 мл/кг в течение 4 суток без гепатопротекторов. На следующий день после последнего введения ЧХУ и исследуемых соединений изучали сывороточные биомаркеры печеночного метаболизма и проводили гистологический анализ печени. Результаты эксперимента приведены в таблице 2.
Установлено, что в контрольной группе воздействие ЧХУ приводит к повышению активности АлАТ в 3.2 раза (Р<0,000001), АсАТ в 1.7 раза (Р=0,000003) и снижению коэффициента де Ритиса в 2.4 раза (Р=0,000415). Это свидетельствует о токсическом повреждении печени и цитолизе гепатоцитов.
В группах, которым вводили Ксимедон или заявляемое средство, повышение АлАТ было менее выраженным, однако достоверных различий между опытными группами и ЧХУ-контролем не выявлено (Р>0,05). Уровень АсАТ в группах, получавших исследуемые препараты по профилактической схеме, был ниже, чем в контроле. При этом достоверные различия активности АсАТ в сравнении с ЧХУ-группой выявлены лишь для заявляемого средства в дозах 10 и 20 мг/кг (Р=0,041 и Р=0,032, соответственно). Таким образом, заявляемое средство оказывает более эффективное профилактическое гепатоцитопротекторное действие по сравнению с Ксимедоном.
Затравка ЧХУ вызывала снижение концентрации общего белка сыворотки крови на 8.7% (Р=0,002). При профилактическом введении Ксимедона в дозе 20 мг/кг общий белок крови превышал значение этого параметра для группы ЧХУ на 20.8% (Р=0,027). При введении 10 мг/кг Ксимедона уровень общего белка не отличался от группы ЧХУ (таблица 2). При введении заявляемого средства в дозах 10 и 20 мг/кг различия концентраций общего белка сыворотки крови с группой ЧХУ не были статистическими значимыми (Р>0,05), однако в этих группах уровень общего белка ближе всего приближался к референтным значениям интактных животных. Таким образом, при введении по профилактической схеме заявляемое средство оказывает сопоставимый с ксимедоном положительный эффект на белоксинтезирующую функцию печени, подавленную ЧХУ.
Гистологические исследования структуры печени при профилактической схеме воздействия: при окрашивании гематоксилин-эозином срезов печени крыс, затравленных ЧХУ, выявляется умеренная жировая инфильтрация паренхимы и некрозы гепатоцитов с преимущественной локализацией в перицентральной зоне. На фоне введения заявляемого средства в дозах 10 и 20 мг/кг отмечается менее выраженная жировая дистрофия печени по сравнению с ЧХУ группой животных и по сравнению с группами, получавшими аналогичные дозы Ксимедона.
Иммуногистохимические исследования проводили с использованием нескольких маркеров: десмина, ядерного антигена пролиферирующих клеток (PCNA, Proliferative Cell Nuclear Antigen) и альфа-гладкомышечного актина (А-ГМА). Экспрессия десмина характерна для звездчатых клеток печени, играющих важную роль в накоплении ретиноидов и синтезе компонентов межклеточного матрикса. Увеличение количества десмин-позитивных клеток является адаптивной реакцией, направленной на восстановление паренхимы печени при ее повреждении. У животных, затравленных ЧХУ, выявлены десмин-позитивные отростчатые клетки в очагах жировой дистрофии преимущественно вокруг центральной вены. Профилактическое введение заявляемого средства сопровождалось менее выраженным увеличением числа десмин-позитивных клеток, локализующихся в участках жировой дистрофии, что согласуется с меньшим повреждением печеночной ткани.
В случае хронического действия повреждающего фактора звездчатые клетки печени способны трансдифференцироваться в миофибробласты, вырабатывающие компоненты соединительной ткани и способствующие фиброгенезу в печени. Окрашивание с использованием антител против альфа-гладкомышечного актина (А-ГМА) позволяет оценить выраженность трансдифференцировки звездчатых клеток печени в миофибробласты. У животных, которым вводили заявляемое средство в дозах 10 и 20 мг/кг, не выявлены признаки трансдифференцировки звездчатых клеток печени в миофибробласты, что свидетельствует об отсутствии развития фиброза при токсическом повреждении печени под воздействием ЧХУ на фоне введения заявляемого средства.
Иммуногистохимическое окрашивание с использованием антител против ядерного антигена пролиферирующих клеток (PCNA, Proliferative Cell Nuclear Antigen) позволяет выявлять клетки, находящиеся в синтетической фазе клеточного цикла. Уровень пролиферативного ответа гепатоцитов положительно коррелирует с интенсивностью повреждения печени. При введении заявляемого средства регистрировали менее выраженную пролиферацию гепатоцитов по сравнению с группой ЧХУ.
Результаты гистологических и иммуногистохимических исследований при профилактической схеме введения свидетельствуют о гепатопротекторном эффекте заявляемого средства.
Таким образом, учитывая значительное улучшение общего состояния животных при ЧХУ-индуцированном токсическом гепатите, нормализацию биомаркеров печеночного метаболизма, улучшение структурно-морфологической организации печени, низкую токсичность, а также очевидные преимущества по эффективности по сравнению с препаратами Ксимедон и Тиотриазолин, заявляемый L-аскорбат 1-(2-гидроксиэтил)-4,6-диметил-1,2-дигидропиримидин-2-она является перспективным гепатопротекторным средством.
Заявляемое техническое решение создано при поддержке гранта Российского научного фонда №14-50-00014.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕПАТОПРОТЕКТОРНОЕ СРЕДСТВО ИЗ МОРСКИХ ВОДОРОСЛЕЙ | 2013 |
|
RU2528898C1 |
| Гепатопротекторное средство из морских водорослей | 2017 |
|
RU2667472C1 |
| СРЕДСТВО, СТИМУЛИРУЮЩЕЕ ФИЗИЧЕСКУЮ РАБОТОСПОСОБНОСТЬ | 2013 |
|
RU2515247C1 |
| Гепатопротекторное средство для профилактики тетрациклиновых поражений печени | 1987 |
|
SU1822772A1 |
| Способ лечения животных при лучевой болезни | 2024 |
|
RU2836843C1 |
| ВОДНЫЙ РАСТВОР, ОБЛАДАЮЩИЙ ГЕПАТОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 1996 |
|
RU2111746C1 |
| Гепатопротекторное средство | 2015 |
|
RU2614691C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИАРИТМИЧЕСКИМИ И ГЕПАТОПРОТЕКТОРНЫМИ СВОЙСТВАМИ | 2011 |
|
RU2469720C1 |
| ГЕПАТОПРОТЕКТОРНОЕ СРЕДСТВО | 2010 |
|
RU2444569C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ГЕПАТОЗАЩИТНЫМ ДЕЙСТВИЕМ, И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2003 |
|
RU2257208C1 |
Изобретение относится к фармакологии и медицине. Предложено синтетическое гепатопротекторное средство пиримидинового ряда. В этом качестве предложено применение L-аскорбата 1-(2-гидроксиэтил)-4,6-диметил-1,2-дигидропиримидин-2-она формулы I. Технический результат: соединение обладает способностью уменьшать функциональные и структурные нарушения гепатоцитов и ускорять восстановление структуры и функции печени при токсическом гепатите; его эффективность по показателям АлАТ и АсАТ выше, чем у ксимедона. 2 табл.
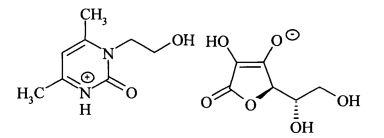 формула I
формула I
Применение L-аскорбата 1-(2-гидроксиэтил)-4,6-диметил-1,2-дигидропиримидин-2-она формулы
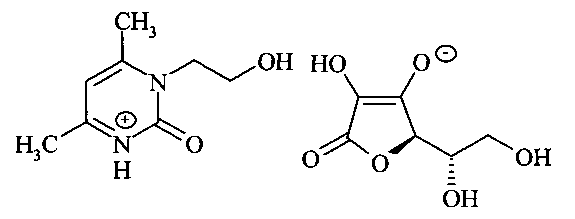
в качестве гепатопротекторного средства.
| ГЕПАТОПРОТЕКТОРНОЕ И ДЕТОКСИКАЦИОННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ОСЛОЖНЕНИЙ ГНОЙНО-СЕПТИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2001 |
|
RU2195283C1 |
| СРЕДСТВО, СТИМУЛИРУЮЩЕЕ ФИЗИЧЕСКУЮ РАБОТОСПОСОБНОСТЬ | 2013 |
|
RU2515247C1 |
| БУСЫГИН Д.В | |||
| Исследование гепатопротекторных свойств лекарственного препарата ксимедон | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Выпускная квалификационная работа, выводы | |||
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| КСИМЕДОН В КАЧЕСТВЕ ИНДУКТОРА АКТИВНОСТИ МИКРОСОМАЛЬНЫХ ОКСИДАЗ ПЕЧЕНИ ЧЕЛОВЕКА | 2006 |
|
RU2316327C1 |
| СПОСОБ ЭКСПЛУАТАЦИИ ПИРОВИДИКОНА | 1999 |
|
RU2141172C1 |
| US8415351 B2 09.04.2013. | |||
Авторы
Даты
2016-07-10—Публикация
2015-05-26—Подача