Изобретение относится к медицине, а именно к фармакологии.
Цель - повышение гепатопротекторной активности при снижении токсичности.
Указанная цель достигается применением дихлор-бис-М-М-диметилкарбодецок- симетил-М-этиленаммония сульфида для профилактики тетрациклиновых поражений печени.
Пример 1. Дистрофию печени воспроизводят на 80 белых крысах обоего пола массой 180-200 г,которых подразделяют на 4 группы: по 20 животных в каждой группе.
Животным первой группы ежедневно в течение 5 дн вводят в желудок тетрациклин в токсической дозе (0.5 г/кг) в 1 %-ном растворе крахмального клейстера. Животным второй группы - тетрациклин в токсической дозе (0,5 г/кг) в сочетании с дихлор-бис-М- N-диметилкарбодецоксиметил-М-этиленам- мония сульфидом в дозе 30 мг/кг. Животным третьей группы - тетрациклин в токсической дозе (0,5 г/кг) в сочетании с дихлор-бис-М-.М-диметилкарбодецоксиме- тил-М-этиленаммония сульфидом в дозе 5 мг/кг; животным четвертой группы (контроль) - 1 %-ный раствор крахмального клейстера.
Через 24 ч после последнего введения препаратов белых крыс выводят из опыта методом декаптации. О степени поражения печени судят по активности аланинаминот- расфераэы (АлАТ), аспартатиминотрасфера- зы (АсАТ). интенсивности переписного окисления липидов (ПОЛ) в гомогенатах печени и морфологическим изменениям в ткани печени. Активность трансаминаз определяют по Рейтману и Френкелю интенсивность ПОЛ - по скорости образования малонового диальдегида. Для излучения морфологического строения ткани печени участки органа помещают в 10- 12%-ный раствор нейтрального формалина, проводят через спирт этиловый возрастающий крепости, заключают в парафин, готовят срезы и окрашивают их классическими гистологическими методами.
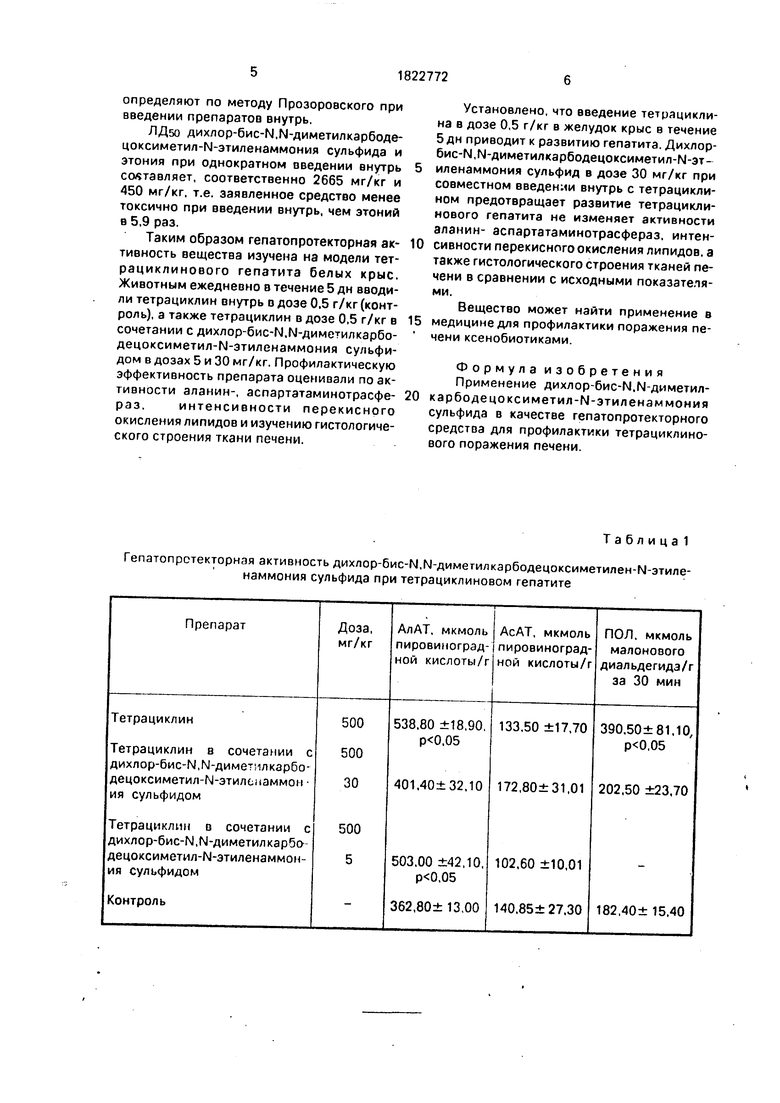
Результаты проведенных исследований представлены в табл. 1.
Как видно из табл.1, повторное введение в желудок крыс тетрациклина в токсической дозе (0,5 г/кг) приводит к развитию
(Л
С
00
ю ю VI
XI
го
дистрофических процессов в печени и нарушению ее функционального состояния, о чем свидетельствует достоверное повышение активности АлАТ и интенсивности ПОЛ в гомогенатах печени. При микроскопии гистологических препаратов отмечается вакуольная и зернистая дистрофия цитоплазмы гепатоцитов. По периферии долек в участках с наиболее выраженной вакуольной дистрофией нарастает содержание липидов и заметно уменьшается количество гликогена, вплоть до полного его исчезновения. Часть дистрофически измененных клеток содержат пикнотические ядра. Наряду с этим, преимущественно, по периферии долек обнаруживаются очаги некробиоза, являющиеся свидетельством глубокого повреждения клеток печени. Помимо дистрофических изменений паренхимы печени обнаруживаются повсеместные расширения вокруг синусоидных пространств, а также очаговый периваскулярный отек в районе триад, десквамация эндотелиоци- тов и наличие нитей фибрина в центральных венах.
В группе животных, получавших в течение 5 дн тетрациклин в токсической дозе (0,5 г/кг) в сочетании с дихлор-бис-М-,М-ди- метилкарбодецоксиметил-Н-этиленаммон - ия сульфидом в дозе 5 мг/кг токсическое поражение печени менее выражено, чем у животных первой группы. При микроскопии гистологических срезов печени животных этой группы определяются небольшие очаги вакуольной и зернистой дистрофии цитоплазмы гепатоцитов, расположенных в периферических отделах долек. Значительно реже, чем у животных с тетрациклиновым поражением печени, обнаруживаются гепа- тоциты с признаками некробиоза. У гепатоцитов с дистрофическими изменениями цитоплазмы ядра имеют обычные контуры, умеренно окрашиваются гематоксилином. Функциональное состояние печени нормализуется медленно. Через 24 ч после отмены препаратов активность АлАТ достоверно, чем у контрольных крыс.
При выполнении дозы дихлор-бис-N.N- диметилкарбодецоксиметил-М-этиленамм- ония сульфида до 30 мг/кг гепатопротектор- ная активность препарата возрастает. В группе животных, получавших в течение 5 дн тетрациклин в токсической дозе (0,5 г/кг) в сочетании с дихлор-бис М,М-диметилкар- бодецоксиметил-М-этиленаммония сульфидом в дозе 3 мг/кг через 24 ч и после последнего введения препаратов отмечается нормализация функционального состояния печени. Активность АлАТи интенсивность ПОЛ в гомогенатах печени у
животных этой группы соответствуют аналогичным показателям у животных контрольных групп и достоверно ниже, чем в группе животных с тетрациклиновым поражением печени. Гепатопротекторное действие дихлор-бис-М,М-диметилкарбоде- цоксиметил-М-эти лен аммония сульфида подтверждается и при изучении гистологических срезов печени. Выявленные изменения в структуре ткани печени у крыс этой группы не превышают таковые у животных контрольной группы. Сопоставление сроков нормализации функционального состояния печени у крыс этой группы (24 ч после отме5 ны ксенобиотика) с таковыми при применении этония (15-21 сут) позволяет считать, что заявленный препарат обладает более выраженной гепатопротекторной активностью, чем этоний.
0 П р и м е р 2. Комбинированное действие тетрациклина и дихлор-бис-Ы,М-диметил- карбодецоксиметил-М-этиленаммония сульфида изучают в опытах in vitro в отношении культур кишечной палочки, сине5 гнойной палочки и золотистого стафилококка методом последовательных серийных разведений в жидкой питательной среде. В пробирки с серийными разведениями тетрациклина вносят
0 суббактеристатические для каждого штамма микроорганизмов концентрации дихлор- бис-,М-диметилкарбодецоксиметил-М-эти ленаммония сульфида и культуру микроорганизмов (250000 колониеобразующих
5 ед/мл). Результат комбинированного действия препаратов оценивают как синергид- ный, если минимальная ингибирующая концентрация (МПК) антибиотика снижается в 4 и более раз, аддитивный - в 2 раза,
0 индифферентный - не изменяется, антагонистический - снижается в 2 и более раз.
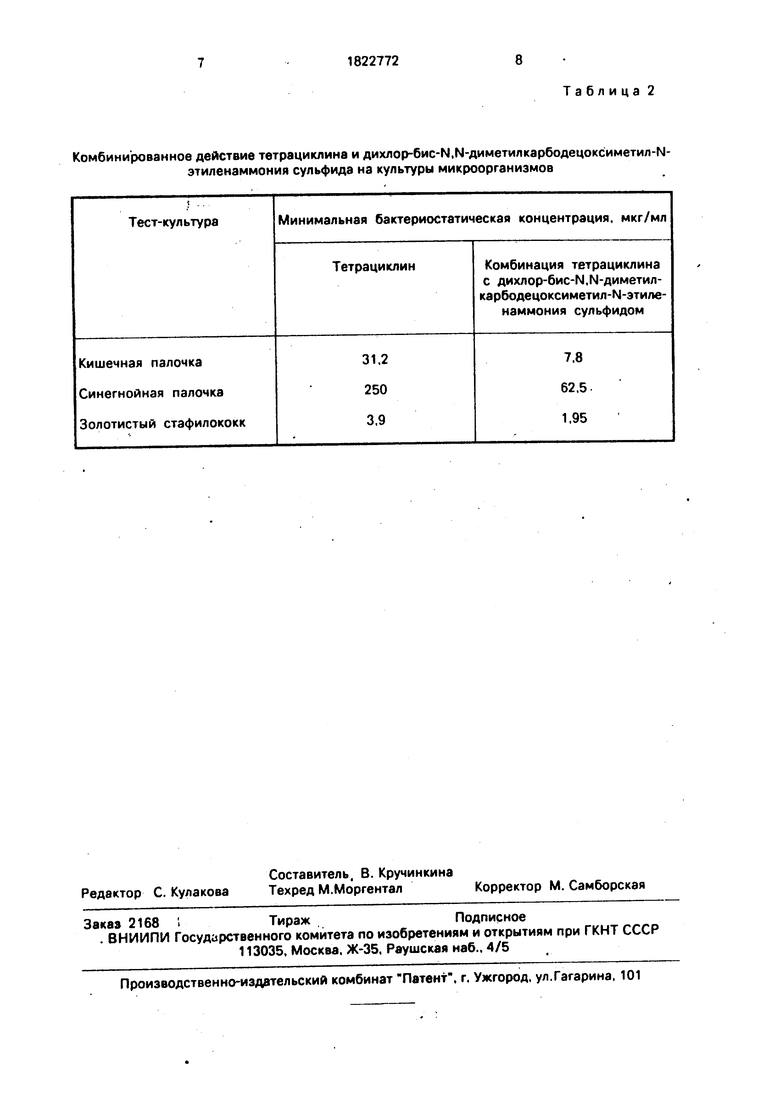
Результаты проведенных исследований представлены в табл.2.
Как видно из табл.2 тетрациклин в соче5 тании дихлор-бис-М,М-диметилкарбодецок- симетил-го-этиленаммония сульфидом оказывает синергидное действие на культуры кишечной и синегнойной палочек, а также аддитивное действие на культуру
0 золотистого стафилококка. Это свидетельствует о сохранении тетрациклином, выраженным противомикробных свойств при совместном применении с дихлор-бис-N.N- диметилкарбодецоксиметил-М-этиленамм5 ония сульфидом.
П р и м е р 3. Острую токсичность дих- лор-бис-М,М-диметилкарбодецоксиметил- N-этиленаммония сульфида и отония изучают на белых крысах массой 180-200 г. Сред- несмертельную дозу (ЛДбо) препаратов
определяют по методу Прозоровского при введении препаратов внутрь,
ЛДво дихлор-бис-Ы.Ы-диметилкарбоде- цоксиметил-М-этиленаммония сульфида и этония при однократном введении внутрь составляет, соответственно 2665 мг/кг и 450 мг/кг, т.е. заявленное средство менее токсично при введении внутрь, чем этоний в 5,9 раз.
Таким образом гепатопротекторная ак- тивность вещества изучена на модели тет- рациклинового гепатита белых крыс. Животным ежедневно в течение 5 дн вводили тетрациклин внутрь о дозе 0,5 г/кг (контроль), а также тетрациклин в дозе 0,5 г/кг в сочетании с дихлор-бис-М.М-диметилкарбо- децоксиметил-М-этиленаммония сульфидом в дозах 5 и 30 мг/кг. Профилактическую эффективность препарата оценивали по активности аланин-, аспартатаминотрасфе- раз, интенсивности перекисного окисления липидов и изучению гистологического строения ткани печени.
Установлено, что введение тетрациклина в дозе 0,5 г/кг в желудок крыс в течение 5 дн приводит к развитию гепатита. Дихлор- бис-М,М-диметилкарбодецоксиметил-М-эт- иленаммония сульфид в дозе 30 мг/кг при совместном введении внутрь с тетрациклином предотвращает развитие тетрацикли- нового гепатита не изменяет активности аланин- аспартатаминотрасфераз. интенсивности перекисного окисления липидов. а также гистологического строения тканей печени в сравнении с исходными показателями.
Вещество может найти применение в медицине для профилактики поражения печени ксенобиотиками.
Формула изобретения Применение дихлор-бис-М.М-диметил- карбодецоксиметил-г 1-этиленаммония сульфида в качестве гепатопротекторного средства для профилактики тетрациклино- вого поражения печени.

| название | год | авторы | номер документа |
|---|---|---|---|
| Гепатопротекторное средство | 2015 |
|
RU2614691C2 |
| СРЕДСТВО ГЕПАТОПРОТЕКТОРНОГО ДЕЙСТВИЯ | 2015 |
|
RU2590952C1 |
| СПОСОБ КОРРЕКЦИИ ГЕПАТОТОКСИЧЕСКИХ РЕАКЦИЙ, ИНДУЦИРОВАННЫХ ИЗОНИАЗИДОМ | 2015 |
|
RU2601919C1 |
| СПОСОБ ПРОФИЛАКТИКИ ОСЛОЖНЕНИЙ, ИНДУЦИРОВАННЫХ ИЗОНИАЗИДОМ | 2015 |
|
RU2597788C1 |
| СПОСОБ ЗАЩИТЫ ПЕЧЕНИ ОТ КСЕНОБИОТИКОВ В ЭКСПЕРИМЕНТЕ | 2000 |
|
RU2195936C2 |
| Способ получения средства, обладающего гепатопротекторным и антигепатотоксическим действием | 2020 |
|
RU2771028C1 |
| СПОСОБ ТЕРАПИИ ЭКСПЕРИМЕНТАЛЬНОГО ХРОНИЧЕСКОГО ТОКСИЧЕСКОГО ГЕПАТИТА | 2009 |
|
RU2392000C1 |
| ГЕПАТОПРОТЕКТОР | 2007 |
|
RU2325158C1 |
| ВОДНЫЙ РАСТВОР, ОБЛАДАЮЩИЙ ГЕПАТОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 1996 |
|
RU2111746C1 |
| ПРИМЕНЕНИЕ АЦИЗОЛА В КАЧЕСТВЕ ГЕПАТОПРОТЕКТОРА | 2004 |
|
RU2260427C1 |
Изобретение относится к медицине, а именно к фармакологии и гепатологии Цель - повышение гепатопротекторной активности при снижении токсичности. В качестве такого средства используют дихлор-бис-N-, N-диметилкарбодецокси- метин-М-этиленаммония сульфид 2 табл.
Таблица
Гепатопрстекторная активность дихлор-бис-Н.М-диметилкарбодецоксиметилен-М-этиле- наммония сульфида при тетрациклиновом гепатите
Комбинированное действие тетрациклина и дихлор-бис-Ы,М-диметилкарбодецоксиметил-Ы- этиленаммония сульфида на культуры микроорганизмов
Тест-культура
Минимальная бактериостатическая концентрация, мкг/мл
Тетрациклин
Кишечная палочка Синегнойная палочка Золотистый стафилококк
Таблица 2
Комбинация тетрациклина
с дихлор-бис-М,М-диметилкарбодецоксиметил-М-этиленаммония сульфидом
62,5

| И.Х.Пасечник и др | |||
| Влияние этония на функции печени при экспериментальном гепатите// -- в сб | |||
| Актуальные вопросы фармакологии и токсикологии Тернополь, 1981 | |||
| с | |||
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
Авторы
Даты
1993-06-23—Публикация
1987-03-25—Подача