Изобретение относится к области фармацевтической химии и касается фармацевтического препарата тровентол, который используют в качестве бронхолитического средства, применяемого для купирования приступа бронхоспазма.
Изобретение относится к промышленному способу получения фармакопейного тровентола в виде химического соединения йодметилата тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты.
В патенте SU 1532047 впервые описан препарат тровентол в качестве бронхолитического средства, применяемого в виде аэрозольной лекарственной формы. Корецкой Н.И. с соавторами приведен способ получения кристаллического тровентола из тропинового эфира 2-оксиметил-2-фенилмасляной кислоты методом кватернизации йодистым метилом в растворе ацетона.
Недостатком способа является качество получаемого тровентола, чистота которого охарактеризована только температурой плавления 258-260°С (перекристаллизация из воды) и результатами хроматографии на бумаге. В патенте также приведен исходный продукт для получения тровентола - тропиновый эфир 2-оксиметил-2-фенилмасляной кислоты с температурой плавления 99-101°C, полученный из гептана. В результате исследования установлено, что применение в качестве растворителя гептана, температура кипения которого близка к температуре плавления эфира, приводит к образованию плава, который осаждается на стенках реакционного сосуда в виде трудноудаляемой корки. Кроме того, в патенте отсутствует описание способа синтеза тропинового эфира 2-оксиметил-2-фенилмасляной кислоты. Но в статье, опубликованной в ХФЖ №2, 1977, с. 3-8, те же авторы описывают способ получения гидрохлорида тропинового эфира 2-оксиметил-2-фенилмасляной кислоты (соединение XIV), методом оксиметилирования тропиновых эфиров 2-замещенных фенилуксусных кислот параформом в диметилформамиде в присутствии каталитических количеств этилата натрия, с последующим переводом продуктов оксиметилирования в солянокислый раствор.
Недостатком способа получения гидрохлорида тропинового эфира 2-оксиметил-2-фенилмасляной кислоты является многостадийность технологического процесса и использование разнообразных реагентов, что затрудняет применение его в промышленных масштабах. На стадии синтеза тропинового эфира 2-оксиметил-2-фенилмасляной кислоты выявлен следующий ряд недостатков:
- используемый растворитель - товарный диметилформамид предварительно необходимо очищать - перегонять над щелочью для удаления воды и муравьиной кислоты, которые могут приводить к разложению катализатора и гидролизу тропинового эфира 2-фенилмасляной кислоты и получаемого продукта реакции; кроме того, в процессе используют пятикратное количество диметилформамида, что экономически нецелесообразно и приводит к увеличению объема промышленных реакторов;
- проведение синтеза при температуре 38-40°C, снижение температуры приводит к уменьшению выхода продукта до 50%;
- использование в качестве катализатора раствора этилата натрия в спирте приводит к переэтерификации за счет побочных реакций этилового спирта с тропиновыми эфирами исходного соединения и получаемого продукта реакции; при этом степень конверсии тропинового эфира 2-фенилмасляной кислоты достигает только 93%, а не прореагировавший исходный эфир (до 7-8%), значительно затрудняет очистку конечного тровентола.
На стадии очистки и выделения гидрохлорида тропинового эфира 2-оксиметил-2-фенилмасляной кислоты к недостаткам можно отнести:
- обязательное удаление из реакционной смеси диметилформамида, что приводит к дополнительным энергозатратам и удлиняет технологический процесс;
- растворение остатка продуктов реакции в соляной кислоте и удаление из раствора побочных продуктов реакции экстракцией диэтиловым эфиром, имеющим низкую температуру кипения, в промышленных условиях может привести к взрыво- и пожароопасной ситуации;
- подщелачивание очищенного солянокислого раствора 10% раствором аммиака, что приводит к образованию эмульсии, которую экстрагируют хлороформом, из экстракта отгоняют хлороформ и выделяют маслянистый остаток, который растворяют в подходящем растворителе и кристаллизуют гидрохлорид тропинового эфира 2-оксиметил-2-фенилмасляной кислоты.
Таким образом, в открытой публикации отсутствует описание всего технологического процесса получения тровентола из тропинового эфира 2-фенилмасляной кислоты, позволяющего получать фармакопейный тровентол в промышленных масштабах.
Задачей изобретения является разработка простого в технологическом исполнении и удобного для промышленного использования способа получения фармакопейного тровентола с чистотой свыше 99,5%.
Поставленная задача решена тем, что тропиновый эфир 2-фенилмасляной кислоты обрабатывают параформом в диметилацетамиде при мольном соотношении 1:1 - 1:1,5, температуре 20-25°С в присутствии трет-бутилата калия, затем реакционную массу подкисляют 3% (масс.) раствором соляной кислоты, экстрагируют образовавшиеся побочные продукты сложными эфирами, или углеводородами и осаждают карбонатом щелочного металла тропиновый эфир 2-гидроксиметил-2-фенилмасляной кислоты, затем перекристаллизовывают его из ацетонитрила и кватернизируют йодистым метилом в растворе ацетонитрила. Получают кристаллы тровентола с температурой плавления 263°С (разл.) и хроматографической чистотой свыше 99,5%.
На фиг. 1 приведен ИК-спектр тровентола.
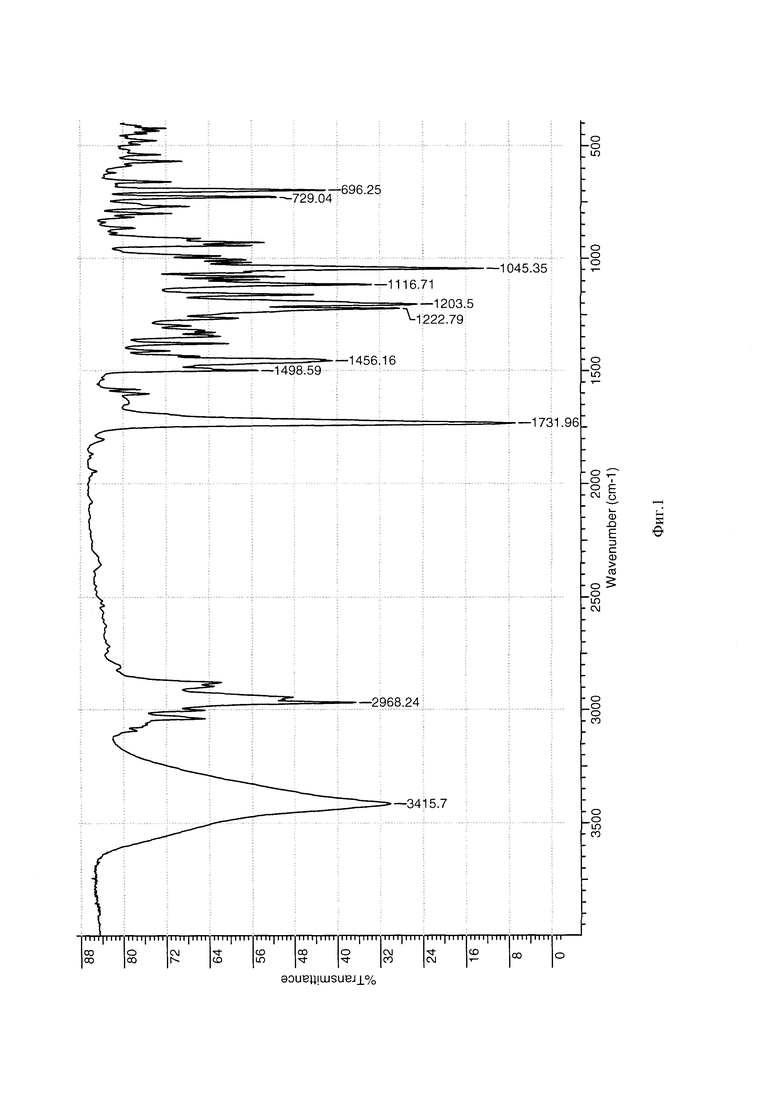
На фиг. 2 приведен спектр ПМР тровентола.
На фиг. 3 приведена хроматограмма ВЭЖХ тровентола.
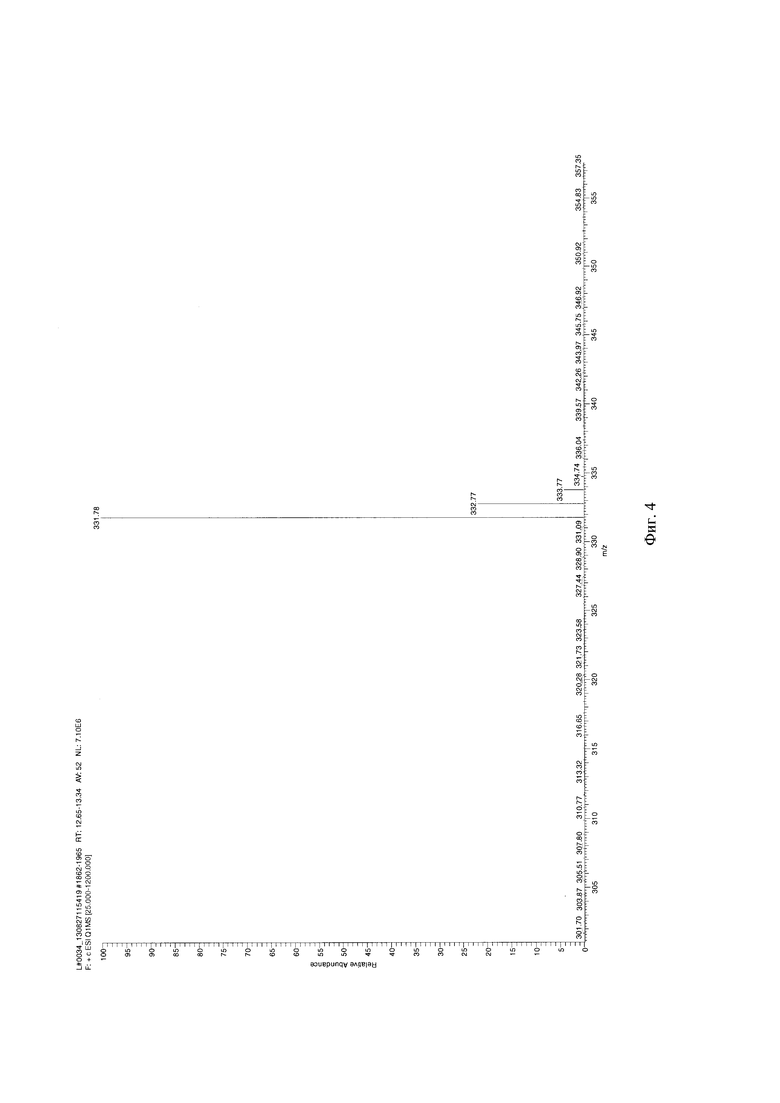
На фиг. 4 приведен масс-спектр тровентола.
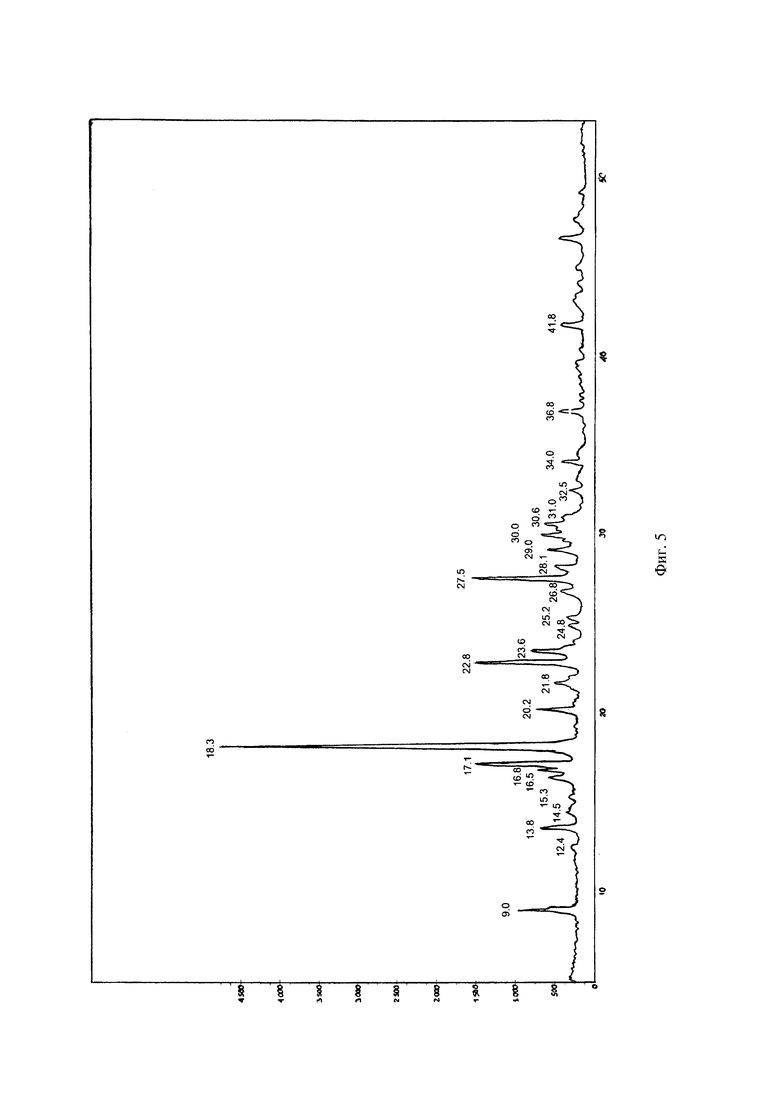
На фиг. 5 приведен ПДРЛ спектр тровентола.
Изобретение относится к промышленному способу получения тровентола с температурой плавления 263°С (разл.) и чистотой свыше 99,5%.
Способ получения тровентола осуществляют обработкой тропинового эфира 2-фенилмасляной кислоты параформом в растворе диметилацетамиде при мольном соотношении 1:1 - 1:1,5 и температуре 20-25°С в присутствии трет-бутилата калия в течение 1 час. Затем в реакционную смесь добавляют 3% (масс.) раствор соляной кислоты, удаляют экстракцией сложными эфирами или углеводородами побочные продукты реакции оксиметилирования и осаждают карбонатом щелочного металла кристаллы тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты. Кристаллы отделяют от маточного раствора, перекристаллизовывают из ацетонитрила, а затем кватернизируют йодистым метилом в растворе ацетонитрила и получают кристаллы тровентола с температурой плавления 263°С (разл.) и чистотой свыше 99,5%.
Использование товарного диметилацетамида, имеющего высокую степень очистки и сравнительно высокую стабильность, позволяет избежать дополнительной подготовки растворителя.
Использование в качестве катализатора трет-бутилата калия дает возможность уменьшить количество растворителя и осуществить синтез при нормальные температурных условиях. В результате исследования кинетики реакции оксиметилирования было установлено, что при использовании в качестве катализатора трет-бутилата калия в начальный момент времени образуется до 70% конечного продукта. Через 1 час при катализе трет-бутилатом калия при комнатной температуре степень конверсии исходного тропинового эфира 2-фенилмасляной кислоты достигает 99,2%, а выход целевого соединения составляет 98%.
Использование в качестве экстрагента сложных эфиров или углеводородов обеспечивает сравнительно высокую безопасность процесса.
Использование при осаждении тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты карбоната щелочного металла позволяет уменьшить потери целевого продукта, за счет уменьшения степени гидролиза эфира.
Использование ацетонитрила на стадиях перекристаллизации тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты и кватернизации позволяет получить тровентол высокой степени очистки и избежать использования двух различных растворителей на этих стадиях технологического процесса.
Строение полученного, предлагаемым способом, тровентола доказано методами ИК-спектроскопии, ПМР-спектроскопии и масс-спектроскопии. Кроме того, было установлено, что данным способом получается тровентол в стабильной кристаллической форме, которая была охарактеризована методом порошковой рентгеновской дифракции. Содержание основного вещества определено методом ВЭЖХ.
ИК-спектр (спектр поглощения в инфракрасной области) регистрировали на спектрометре Shimadzu FTIR-8400S:
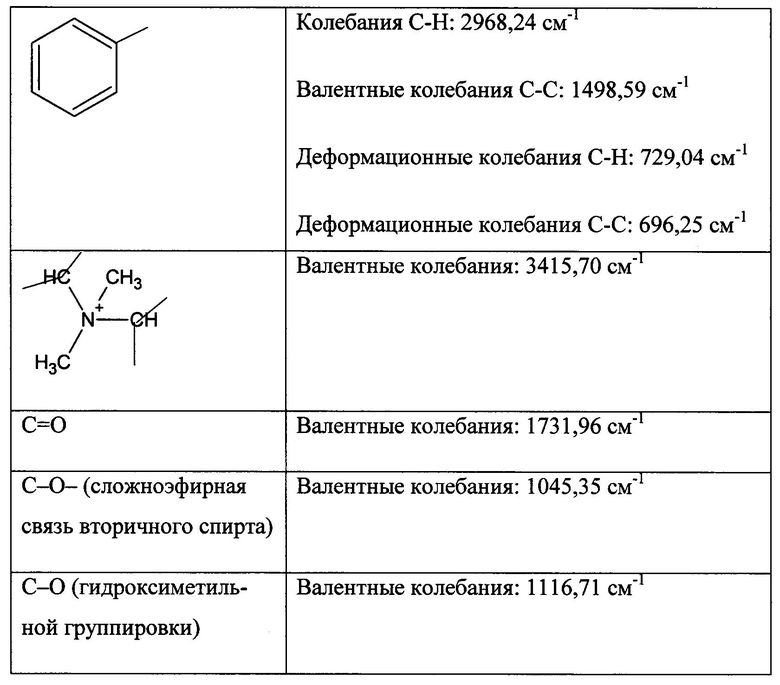
ПМР-спектр (протонный магнитный резонанс) раствора образца в ДМСО d6 (диметилсульфоксид) регистрировали на спектрометре Bruker AM 500 с рабочей частотой 500 Mhz, δ м.д.: 0,65 т (3Н, СН3), 1,40-1,47 м (1Н, СН2), 1,56-1,60 д (1Н, СН2), 1,76-1,84 м (2Н, СН2), 2,00-2,10 м (4Н, 2СН2), 2,50-2,52 к (2Н, СН2; J=1,75 MHz), 2,95 с (3Н, СН3), 3,08 с (3Н, СН3), 3.71-3.73 м (1H, СН); 3,78-3,79 м (1H, СН); 3,95-3,97 д (1Н, СН2), 4,07-4,09 д (1Н, СН2); 5,00-5,02 м (1Н, СН); 7,19-7,21 м (2Н, Наром.); 7,24-7,28 м (1Н, Наром.), 7,34-7,37 м (2Н, Наром.)
Масс-спектр регистрировали на спектрометре Orbitrap LTQ Velos: m/z [M-I]+=331,78.
Хроматографическая чистота тровентола определена методом высокоэффективной жидкостной хроматографии (ВЭЖХ) на жидкостном хроматографе высокого давления Waters Alliance е2695 с фотодиодноматричным детектором Waters 2998 (Waters, США) на колонке Intertsil® ODS-3 С18 размером 3,0×150 мм, размер частиц 3 мкм (GL Sciences, Япония). Подвижная фаза: раствор А: смесь ацетонитрила и раствора 0,005 М октансульфоната натрия и 0,07 М триэтиламина, доведенного до значения рН 2,5 фосфорной кислотой в объемном соотношении 23:77; раствор Б: ацетонитрил. Градиентный режим элюирования: 100% раствора А - 4 мин; от 100% до 83% раствора А за 24 мин, от 83% до 45 раствора А за 20 мин. Скорость потока подвижной фазы 0,4 мл/мин. Объем анализируемой пробы - 10 мкл. Детектирование - 210 нм. Температура колонки 35°С. Концентрация испытуемого раствора - 1,5 мг/мл. Полученный образец тровентола имеет чистоту 99,95% (Фиг. 3).
Результаты исследований свидетельствуют о том, что предлагаемый способ позволяет получать фармакопейный тровентол с чистотой свыше 99,5%, отвечающий требованиям, предъявляемым к фармацевтическим субстанциям.
ПДРЛ (порошковая дифракция рентгеновского луча) спектр регистрировали при комнатной температуре на рентгеновском дифрактометре Seifert XRD 3003 ТТ, снабженным первичным монохроматором, источник излучения CuKα1, геометрия съемки «на отражение». ПДРЛ спектр характеризуется значимыми дифракционными пиками на порошковой рентгеновской дифрактограмме при значениях угла 2θ: 9,0°; 12,4°; 13,8°; 14,5°; 15,3°; 16,5°; 16,8°; 17,1°; 18,3°; 20,2°; 21,8°; 22,8°; 23,6°; 24,8°; 25,2°; 26,8°; 27,5°; 28,1°; 29,0°; 30,0°; 30,6°; 31,0°; 32,5°; 34,0°; 36,8°; 41,8°
Приведенные ниже примеры иллюстрируют данное изобретение, но не ограничивают его и показывают возможность осуществления способа в промышленных условиях.
Пример 1
В реактор загружают 2,28 кг тропинового эфира 2-фенилмасляной кислоты, 3,4 л диметилацетамида и 3,58 кг параформа. Смесь охлаждают до 10-15°С и добавляют при интенсивном перемешивании 0,097 кг трет-бутилата калия. Реакционную массу перемешивают при 25°С в течение 1 ч и выливают в 3% (масс.) раствор соляной кислоты, охлажденный до 0°С. Полученный раствор промывают толуолом и нейтрализуют 15% (масс.) раствором карбоната натрия. Выпавший осадок отделяют от раствора, промывают водой и сушат. Получают 2,0 кг технического тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты.
Пример 2
2,0 кг технического тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты растворяют в 8 л ацетонитрила, раствор фильтруют, собранный фильтрат охлаждают до 0-5°С, выпавший осадок отделяют, промывают ацетонитрилом и сушат. Получают 1,8 кг тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты, белый кристаллический порошок, содержание основного вещества 99,5%.
Пример 3
1,8 кг тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты растворяют при перемешивании в 18 л ацетонитрила и постепенно добавляют раствор 1,214 кг йодистого метила в 2 л ацетонитрила. После добавления всего раствора йодистого метила, реакционную массу нагревают до кипения и перемешивают 1 ч. Затем охлаждают до 10-15°С, при этом выпадает осадок, который отделяют, промывают ацетонитрилом и сушат. Получают 2,4 кг йодметилата тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты (тровентола) с чистотой не менее 99,5% с температурой плавления 263°С (разл.).
Пример 4
В реактор загружают 22,8 кг тропинового эфира 2-фенилмасляной кислоты, 22,8 л диметилацетамида и 35,8 кг параформа. Смесь охлаждают до 10-15°С и добавляют при интенсивном перемешивании 0,76 кг трет-бутилата натрия. Реакционную массу перемешивают при 20°С в течение 1 ч и выливают в 3% (масс.) раствор соляной кислоты, охлажденный до 0°С. Полученный раствор промывают этилацетатом и нейтрализуют 15% (масс.) раствором карбоната калия. Выпавший осадок отделяют от раствора, промывают водой и сушат. Получают 19,5 кг технического тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты.
Пример 5
В реактор загружают 22,8 кг тропинового эфира 2-фенилмасляной кислоты, 22,8 л диметилацетамида и 35,8 кг параформа. Смесь охлаждают до 10-15°С и добавляют при интенсивном перемешивании 0,76 кг трет-бутилата натрия. Реакционную массу перемешивают при 20°С в течение 1 ч и выливают в 3% (масс.) раствор соляной кислоты, охлажденный до 0°С. Полученный раствор промывают гептаном и нейтрализуют 15% (масс.) раствором карбоната калия. Выпавший осадок отделяют от раствора, промывают водой и сушат. Получают 18,7 кг технического тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты.
| название | год | авторы | номер документа |
|---|---|---|---|
| Иодметилат тропинового эфира @ -оксиметил- @ - @ фенилмасляной кислоты в качестве бронхолитического средства | 1977 |
|
SU1532047A1 |
| ПРОИЗВОДНОЕ УРАЦИЛА | 1992 |
|
RU2040523C1 |
| ПРОИЗВОДНЫЕ ЭФИРОВ ФОСФОНОВЫХ КИСЛОТ И СПОСОБЫ ИХ СИНТЕЗА | 2011 |
|
RU2581045C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕЛМИСАРТАНА | 2004 |
|
RU2430092C2 |
| УЛУЧШЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ НАЛМЕФЕНА ИЗ НАЛТРЕКСОНА | 2018 |
|
RU2712232C1 |
| Способ получения эритродиол-5-ил-алкеновой кислоты | 1984 |
|
SU1480760A3 |
| Способ получения производных имидазолаили иХ СОлЕй, или ОпТичЕСКиХ изОМЕРОВ | 1976 |
|
SU850006A3 |
| СПОСОБ ПОЛУЧЕНИЯ 2-(ФТОРМЕТОКСИ)-1,1,1,3,3,3-ГЕКСАФТОРИЗОПРОПАНА (СЕВОФЛУРАНА) | 2024 |
|
RU2830201C1 |
| ЭПОКСИСОЕДИНЕНИЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2459822C2 |
| СТАБИЛИЗИРОВАННАЯ ФАРМАЦЕВТИЧЕСКИ ЭФФЕКТИВНАЯ КОМПОЗИЦИЯ И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, ЕЕ СОДЕРЖАЩИЙ | 2000 |
|
RU2246943C2 |

Изобретение относится к фармацевтике. Описан способ получения тровентола, который заключается в оксиметилировании тропинового эфира 2-фенилмасляной кислоты в растворе диметилацетамида в присутствии трет-бутилата калия. Затем следует экстракция побочных продуктов этилацетатом, или толуолом, или гептаном, осаждение тропинового эфира 2-гидроксиметил-2-фенилмасляной кислоты карбонатом щелочного металла с последующей перекристаллизацией из ацетонитрила и кватернизацией в растворе ацетонитрила. Далее выделяют кристаллы тровентола. Изобретение обеспечивает простой в технологическом исполнении и удобный для промышленного использования способ получения тровентола с чистотой свыше 99,5%. 4 з.п. ф-лы, 5 ил., 5 пр.
1. Способ получения тровентола, заключающийся в том, что проводят оксиметилирование тропинового эфира 2-фенилмасляной кислоты параформом в растворе диметилацетамида при мольном соотношении 1:1 - 1:1,5, соответственно, и температуре 20-25°С в присутствии трет-бутилата калия, добавляют в реакционную массу 3% раствор соляной кислоты, экстрагируют образующиеся побочные продукты этилацетатом, или толуолом, или гептаном, проводят выделение тропинового эфира 2-гидроксиметил-2-фенил-масляной кислоты осаждением раствором карбоната щелочного металла с последующей перекристаллизацией из ацетонитрила, затем проводят его кватернизацию йодистым метилом в растворе ацетонитрила, при нагревании до кипения, затем выделяют кристаллы тровентола с температурой плавления 263°С (разл.) и чистотой свыше 99,5%.
2. Способ по п. 1, в котором в качестве карбоната щелочного металла используют карбонат натрия.
3. Способ по п. 1, в котором в качестве карбоната щелочного металла используют карбонат калия.
4. Способ по любому из пп. 1-3, который является промышленным.
5. Способ по любому из пп. 1-3, согласно которому получают фармакопейный тровентол.
| Иодметилат тропинового эфира @ -оксиметил- @ - @ фенилмасляной кислоты в качестве бронхолитического средства | 1977 |
|
SU1532047A1 |
| КОРЕЦКАЯ Н.И | |||
| и др | |||
| Синтез и фармакологическое исследование тропиновых эфиров альфа-замещенных троповых кислот | |||
| Химико-фармацевтический журнал, М.:"Медицина", 1972г (7), Т6, с.3-8 | |||
| ГЛУШКОВ Р.Г | |||
| и др | |||
| Фармакологическая активность тропинового эфира фенилглиоксиловой кислоты и его производных | |||
| Новый метод получения | |||
Авторы
Даты
2016-08-10—Публикация
2014-12-24—Подача