(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИМИДАЗОЛА ИЛИ ИХ СОЛЕЙ, ИЛИ ОПТИЧЕСКИХ
1
Изобретение относится к способу получения новых производных имидаэола формулы I
О
чAn (i)
сн,
J хМ
и
где Ар - фенил, замещенный фенил, тиенил, хлортиенил или нафтил, и в которой указанный замещенный фенил является фенилом, имеющим от 1 до 3 заместителей, независимо выбираемых из группы, состоящей из ггшоида, метила, метокси-нитро- и циано-группы; а R является алкилом, имеющим от 2 до 10 атомов углерода, алкоксиметилом, где алкильная группа имеет от 1 до 10 атомов углерода,этенилом, 2-пропенилоксиметилом, 2-пропенилоксиметилом, оксиметилом, галоидметилом, арилметилом, арилэтилом, арилоксиметилом, арилтиометилом или арилметоксиметилом, в которых указанный арил является заместителем, выбираемым из группы, состоящей из феИЗОМЕРОВ
нила, замещенного фенила, нафтила или моно- и ди-галоиднафтила, и в которой указанный замещенный фенил
5 является фенилом/ имеющим от 1 до 3 заместителей, независимо выбираемых из группы, состоящей из галоида, алкила , алкилокси с С, , циано-, Нитрогрупп, фенила, фенилметила,
)0 бензоила, хлорбензоила, алкилкарбонила с , алкилоксикарбонила с хлорбензоила, алкилкарбонила с С. , , ал1-А
килоксикарбонила с С. или. трифтор f-Aметила, при условии, что когда боЛее,
и чем один заместитель присутствует, то только один из них может быть выбран из группы, состоящей из фенила, бензила, феиилметила или хлорбензоила. Обладающих биологической активностью.
Известен способ получения 1-(2-арил-1,З-диоксолан-2-илметил) имидазолов взаимодействием имидазола или его соли с металлом с соответствующим
галоидом tl
25
Цель изобретения - синтез новых производных имидазола, обладающих биологической активностью.
Поставленная цель достигается тем, 30 что согласно способу получения производных имидазола формулы I, соединение формулы или его соли с металлом подвергают взаимодействию с соединением формулы Ч- LJ R где W представляет собой реакционноспособную сложноэфирную группу, в органическом растворителе, с выделением целевого продукта в свободном виде, в виде соли или оптических изо меров. Процесс проводят при кипячении реакционной массы в присутствии йоди того металла и в случае, когда в ка честве исходного продукта используют соединение формулы II, процесс ведут с использованием избытка имид азола или в присутствии основания такого, как карбонат или бикарбонат натрия или калия. Цис- и транс- диастереомерные ра цематы можно в дальнейшем разделить на их оптические изомеры, цис {+), ЦИС (-), транс (+) и транс (-) путе применения общеизвестных методик. Соединения формулы (I) и их соли при добавлении кислот являются полезными при борьбе с плесенью и бак терЯями. Сами по себе они являются ценными при лечении людей, животных и растений, страдающих от болезнетворных микроорганизмов, и при разрушении микроорганизмов на материалах. Пример 1. Смесь из 1,1 ч. имидазола, 1 ч. 2-(бромметил)-2,4-бис(4-хлорфенил)-1,3-диоксолана, 0,4 ч. йодистого калия и 20 ч. диметилформамида перемешивают и кипятят в течение 12 ч. Воду прибавляют и продукт экстрагируют диэтиловым эфиром. Экстракт промывают дважды водой, высушивают, фильтруют и выпаривают. Остаток ,4-бис(4-хлорфенил) -1 ,З-диоксолан-2-илметилЗ-имидазола превращают в соль азотной кислоты. Неочищенную соль фильтруют и кристаллизуют из смеси изопропанола и диизопропилового эфира, получая 1-(2,4-бис (4-хлорфенил)-1,3-диоксолан-2-илметил) -ими;С1азол нитрат, т.пл. 192,3С. Пример 2. Смесь из 7ч. имидазола, 7,5 ч. 2-(бромметил)-2- (4-хлорфенил) -4-фенил-1,3-диоксолана, 2 ч. йодистого натрия и 100 ч. диметилформамида перемешивают и кипятят в течение 48 ч. Реакционную смесь оставляют охладиться до комнатной температуры и к ней приливают воду. Продукт экстрагируют дважды бензолом. Экстракт промывают дважды водой и растворитель удаляют под вакуумом. Остаток из (4-хлорфенил) -4-фенил-1,3-диоксолан-2-илметилЗ-имидазола превращают в соль азотной кислоты в 4-метил-2-пентаноле и диизопропиловом эфире. Неочищенную соль отфильтровывают и кристаллизуют из 4-метил-2-пентанола, получая (4-хлорфенил)-4-фенил-1,3-диоксолан-2-илметилЗ-имидазол нитрат, т.пл. 153,20С. Пример 3. По примеру 2 получают следующие соли имидазола при добавлении кислот






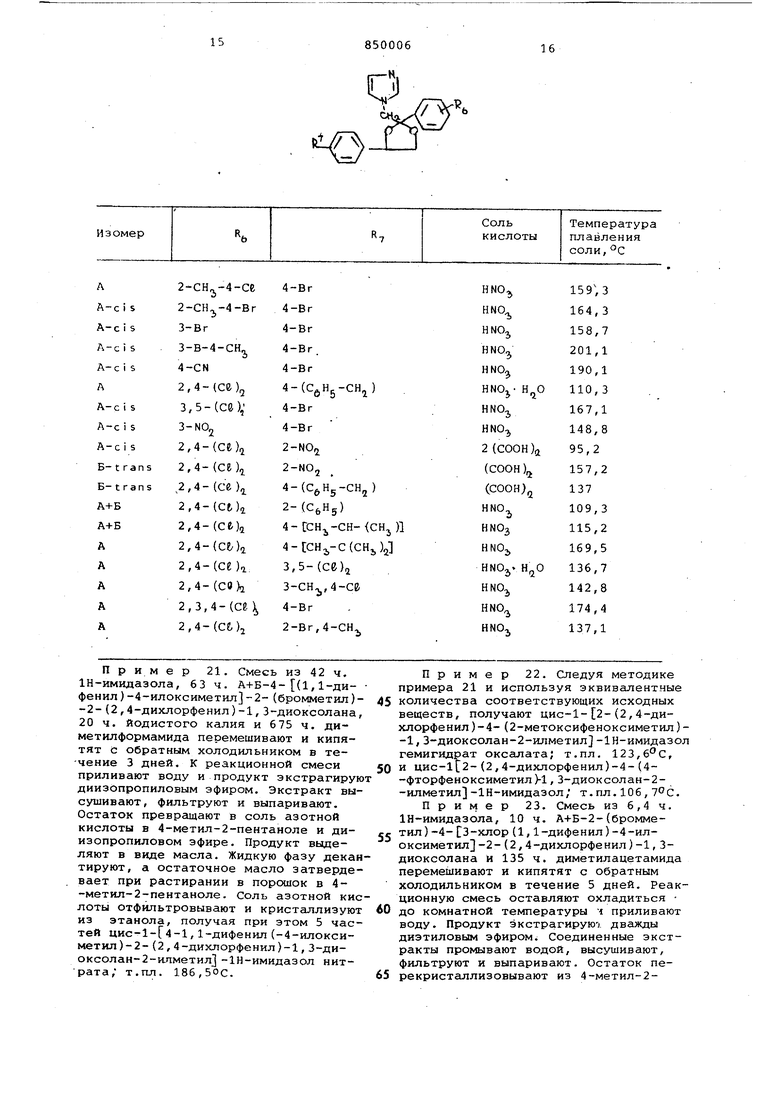






гЗ
ыI СИ,
е )
4-се
4-се
2-се
2,4-(ce)i
2-се
fc
2-се
ei)
2,4-(се)2
4-В
2,4- (Cfc )2 4-В
4-се
4-В
4-В
2,4-(СН),
4-В
2-СЕ
4-СН5
4-СН
4-F
4-F Пример 4. Смесь из 13,6 ч. имидазола, 18,5 ч. 2(-бpoммeтил)-2- (ортохлорфенил)-4- (п-хлорфенил)-1, диоксолана, 4 ч, йодистого натрия и 150 ч. диметилформамида перемешивают и кипятят с обратным холодильником в течение 72 ч. Прибавляют воду и пр дукт экстрагируют дважды диизопропиловым эфиром. Соединенные экстракты промывают дважды водой, высушивают, фильтруют и выпаривают. Остаток очищают с помощью колоночной хроматографии над силикагелем, используя .хлороформ в качестве элюента. Чистые фракции собирают и элюёнт выпаривают Остаток из (о-хлорфенил)-4-(п-хлорфенил)-1,З-диоксолан-2-илметилЗ -имидазола превращают в соль азотной кислоты в изопропаноле и диизопропиловом эфире. Соль отфильтровывают и кристаллизуют из смеси этанола и диизопропилового эфира, получая при этом (о-хлорфенил)-4-(п-хлорфенил)-1,З-диоксолан-2-илметилЗ-имидазол нитрат; т.пл. 183,1°С. Пример 5-. По примеру 4 и используя эквивалентное количество 2-(бромметил)-4-(4-бpюмфeнил)-2(2.4-лиxлopфeнил)-l, 3-диоксолана, ис пользуемого там,получают (4-6pOM фенил)-2-(3,4-дихлорфенил)-1,3-диПродсхлжение таблицу
(соон :
119,9
134,7
183,8
164,2
151
194,7
161,2
156,5
131,1
193,6
144,3
200,8
145,2
210,5
165,4
184,1
207,5
144,3
140,2
163,2
179,3 oкcoлaн-2-илмeтилJ-имидазол нитрат; т.пл. 141,90с. Пример 6. К перемешиваемому раствору из 2,3 ч. натрия в 80 ч. метанола прибавляют 6,8 ч. имидазола, за которым следует прибавление 100 ч. диметилформамида, а метанол удаляют при атмосферном давлении до тех пор, пока внутренняя температура не достигнет 130ОС. Затем к смеси добавляют 7 ч. A-2-(бpoммeтил)-2-(п-xлopфeнил)-4- (4-хлор-о- толилоксиметил)-1,3-диоксолана и смесь перемешивают и кипятят с обратным холодильником в течение 3 ч. К реакционной смеси приливают воду и продукт экстрагируют бензолом. Экстракт высушивают и выпаривают под вакуумом. Остаток из А-1-Г2- (п-хлорфенил)-4- (4-хлор-о-толилоксиметил)-,3-диoкcoлaн-2-илмeтилJ -имидазола превращают в соль азотной кислоты в изопропаноле. При добавлении диизопропилового эфира соль выпадает в осадок. Ее отфильтровывают и кристаллизуют из смеси метанола и диизопропилового эфира, получая при этом цис-1-Г2(п-хлорфенил)-4- (4-хлор-О-толилоксиметил)-1,З-диоксолан-2-илметилЗимидазол нитрат; т.пл. 164,.
Пример 7. Следуя методике примера 6 и используя эквивалентные количества соответствующих исходных
Пример 8. К перемешиваемому раствору из 4,6 ч. натрия в 160 ч. метанола последовательно прибавляют 13,6 ч. имидазола, 300 ч, диметилформамида и 4 ч. йодистого натрия. Метанол отгоняют при атмосферном давлении до тех пор, пока внутренняя температура не достигнет 130°С. Затем к смеси добавляют 25,9 ч. А+Б-2-(бромметил)-2-(парахлорфенил)-4-(2,6-дихлорфенилоксиметил)-1,3-диоксолана и содержимое перемешивают при температуре кипения с обратным холодильником в течение 2 ч. Реакционную смесь оставляют охладиться до комнатной температуры и к ней приливают воду. Продукт экстрагируют дважды бензолом. Соединенные экстракты промывают дважды водой, высушивают и выпаривают под вакуумом. Остаток, содержащий А и Б-изомеры, хроматографируют над силикагелем,с помощью хлороформа в качестве элюента. . А-изомер собирают в виде маслянистого свободного основания и превращают
веществ, получгиот следующие имидазолы и соли имидазола при добавлении кислот
О iwO
psj O-Ofe
в соль азотной кислоты в изопропаноле. Неочищенную соль кристаллизуют из изопропанола, получая при этом
5 3,8 ч. А-1Г2-(п-хлорфенил)-4-(2,6-дихлорфеноксиметил)-1,3-диоксолан-2-илметил -имидазол нитрата; т.пл. 145,80с.
Б-изомер также собирают в виде маслянистого свободного основания и превращают в соль азотной кислоты в изопропаноле и диизопропиловом эфире. Неочищенную соль кристаллизуют из изопропанола, получая при этом 2,2 ч. Б-1 2-(п-хлорфенил)-4- (2,6-дихлорфеноксиметил)-1,3-диоксолан-2-илметил -имидазол нитрата,V т.пл. 197200,50с.
Пример 9. По примеру 8 получают следующие имидазолы и соли имидазолов при добавлении кислот: А-1- 2-(2,4-дихлорфенил)-4- (о-толилг оксиметил) -1, З-диоксолан-2- илметил -имидазол нитрат; т.пл. 156,2ОС, ,4-дихлорфенил-4-(о-толил5 оксиметил)-, З-диоксолан-2-илметил -имидазол сесквиоксалат; т.пл.138,З . (2,4-дихлорфенил)-4- (2,6-диметилфеноксиметил)1,З-диоксолан-2-илметилЗ-1Н-имидаэол нитрат т.пл. 155,бОс,и А+Б-1-1:2-(2,4-дихлор фенил)-4- (2,6-диметилфеноксиметил)-1,3-диоксолан-2-илметил}-1Н-ймидазол нитрат: т.пл. 134,. Пример 10. Смесь из 6,8 ч. имидазола, 7,8 ч. А-2-(бромметил)-2- (2, 4-дихлорфенил )-4- (феноксиметил)-1,3-диоксолана, 4 ч. йодистого наТрия и 150 ч. диметилформамида перемешивают и кипятят с обратным холодильником в течение 3 дней. Реакцион ной смеси позволяют охладиться до комнатной температуры, приливают к ней воду и продукт экстрагируют дваж
d
ды диизопропиловым эфиром. Соединенные экстракты, содержащие А-1р- (2,4-дихлорфенил)-4-{феноксиметил)-1,З-диоксолан-2-илметил -имидазол, промывают дважды водой и подкисляют избытком концентрированного раствора азотной кислоты. Соль отфильтровывают и кристаллизуют из смеси этанола и диизопропилового эфира, получая при этом 5,6 ч. (2,4-дихлорфенил;-4-(феноксиметил)-1,З-диоксолан-2-илметил -имидазол нитрата; т.пл. 180,50с. Пример 11. Следуя методике примера 10 и используя эквивалентные количества соответствующих исходных веществ, получают следующие имидаэолы и соли имидазолов при добавлении кислот
Пример 12. Смесь из 13,6 ч. имидазола, 22,2 ч. Л+Б-2-(бромметил)-4-(о-хлорфеноксиметил)-2-(2,4-дихлорфенил)-1,3-диоксолана, 4 ч. йодистого калия и 150 ч. диметилформамида перемешивают и кипятят с обратным холодильником в течение 3 дней Реакционной смеси позволяют охладиться до комнатной температуры, приливают воду и продукт экстрагируют дважды диизопропиловым эфиром. Соединенные экстракты промывают дважды водой, высушивают, фильтруют и выпаривают. Остаток очищают с помощью колоночной хроматографии над силикагелем, используя хлороформ в качестве элюента, получая при этом две фракции. Первую фракцию выпаривают и остаток с A-1-L4-(о-хлорфеноксиметил )-2-(2,4-дихлорфенил)-1,3-диоксолан-2-илметил -имидазолом растворяют в смеси 4-метил-2-пента«ола и диизопропилового эфира. Раствор подкисляют избытком концентрированного раствора азотной кислоты. Соль азотной кислоты отфильтровывают и кристаллизуют из смеси 4-метнл-2-пентанола и диизопропилового эфира, получая при этом (о-хлорфеноксиметил ) -2- (2,4-дихлорфенил)-1,3диоксолан-2-илметил имидазол нитрат, т.пл. 136,2Рс.
Вторую фракцию выпаривают и остаток с Б-1-f4-(о-хлорфеноксиметил)-2-(2,4-дихлорфенил)-1,3-диоксолан-2-илметилЗ имидазолом растворяют в смеси из 4-метил-2-пентанола и диизопропилового эфира. Раствор подO кисляют избытком щавелевой кислоты. Оксалатную соль отфильтровывают и кристаллизуют из 4-метил-2-пентанола, получая при этом 4 ч. B-l-f4-(о-хлорфеноксиметил)-2-(2,4-дихлор5 фенил)-,З-диоксолан-2-илметил -имидазол диоксалата т.пл. 103,5С.
Пример 13.. Следуя методике примера 12 и используя эквивалентные количества соответствующих исходных веществ, получают следующие имидазолы и соли имидазолов при добавлении кислот. Здесь представлен только один изомер, вторая фракция не получается при хроматографии. Пример 14, Смесь из 9,7 ч. . 1Н-имидазола, 12,5 ч. А+Б-2-(бромметил (-4-(4-бромфеноксиметил)-2-(4-метилфенил )-1, 3-диоксолана, 3 ч. й дистого калия и 135 ч, диметилформ амида перемешивают и кипятят q обратным холодильником в течение 72 ч К реакционной смеси приливают воду и продукт экстрагируют дважды диэти лс зым эфиром. Экстракт, содержащий (4-бромфеноксиметил)-2-(4-метилфенил)-, З-диоксолан-2-илметил -1Н-имидазол, промывают дважды водо и прибавляют избыток раствора концентрированной азотной кислоты и ди изопропиловый эфир. Образующуюся со отфильтровывают и кристаллизуют из смеси этанола и диизопропилового эф ра, получая при этом 5,6 ч. (4-бромфеноксиметил)-2-(4-метилфенил)-1,З-диоксолан-2-илметил -1Н-имидазол нитрата; т.пл. 175,. Пример 15. Следуя методике примера 14, но заменяя используемый там А+Б-2-(бромметил)-4-(4-бромфеноксиметил ) -2- (4-метилфенил)-1,3-диоксолан эквивалентными количествами А+Б-2-(бромметил)-4-(4-бромфеноксиметил) -2- (4-хлорфенил)-1,3-диоксола на и А+Б-2-(бромметил)-4-(4-бромфеноксиметил) -2- (4-бромфенил)-1,3диоксолана, получают (4-бром феноксиметил)-2- (4-хлорфенил)-1;3-диоксолан-2-илметил}-1Н-имид азол и его соль азотной кислоты (т.пл. 158°С) и (4-бромфеноксиметил) -2- (4-бромфенил)-1,3-диоксолан-2-илметил -1Н-имидазол и его соль азотной кислоты (т.пл. 170,3С) . Пример 16. Смесь из 7,9 ч. 1Н-имидазола, 11,5 ч, А+Б-2-.(бромме тил )-2- (2,4-дихлорфенил)-4-(4-фенил феноксиметил)-1,3-диоксолана, 4ч. йодистого калия и 135 ч. диметилформамида перемешивают и кипятят с обратным холодильником в течение 3 дней. К реакционной смеси приливают воду и продукт экс-трагируют дважды диэтиловь эфиром. Соединенные экстракты проплавают водой, высушивают, фильтруют и выпаривают. Остаток очищают с помощью колоночной хроматографии над силикагелем, ис.т пользуя хлороформ в качестве элюента Первую фракцию собирают и элюент выпаривают. Остаток превращают в соль азотной кислоты в 4-метил-2-пентанола и диизопропиловом эфире. Соль отфильтровывают и кристаллизуют из смеси этанола и диизопропилового эфира, получая при этом А+5-1- 2- (2,4-дихлорфенил)-4- (4-фенилфенокси метил)-,3-диоксолан-2-илметил -1Н-имидазол нитрат; т.пл. 187,9С. Вторую фракцию собирают и элюент выпаривают. Остаток кристаллизуют из 4-метил-2-пентанола, получая при это транс-1- С2- U 4-дихлорфенил )-4-(4-фенилфеноксиметил)-1,3-диоксолаи-2-илметил -1Н-имидазол ;т.пл. 155, . Пример 17. Смесь из 6,8 ч имидазола, 8,5 ч. Б-2-(бромметил)-4-п-хлорфеноксиметил)-2-(2,4-дихлорфенил )-1, 3-диоксолана, 2 ч. йодида натрия и 100 ч. диметилформамида перемешивают и кипятят с обратным холодильником в течение 36 ч. Реакционную смесь оставляют охладиться до комнатной температуры и приливают воду. Продукт экстрагируют дважды бензолом. Соединенные органические соли промывают дважды водой, высушивают и растворитель удаляют под вакуумом. Остаток очищают с помощью колоночной хроматографии над силикагелем используя хлороформ в качестве элюента. Чистые фракции собирают и элюент выпаривают. Остаток с (п-хлорфеноксиметил)-2- (2,4-дихлорфенил)-1,3-диоксолан-2-илметил -имидазолом превращают в оксалатную соль в 4-метил-2-пентанол; при добавлении диизопропилового эфира соль выпадает в осадок. Ее отфильтровывают и кристаллизуют из 4-метил-2-пентанола, получая при этом 3,1 ч. транс-1- 4 -п-хлорфеноксиметил )-2-(2,4-дихлорфенил )-1,З-диоксолан-2-илметил -имидазол сесквиоксалата; т. пл, . Пример 18. По примеру 17 получают (2, 4-дихлорфеноксиметил)-2-(2,4-дихлорфенил)-1,3-диоксолан-2-илметил -имидазол сесквиоксалат; т. пл. 121,2°С, реакцией взаимодействия Б-2-(бромметил)-4-(2, 4-дихлорфеноксиметил)-2-(2,4-дихлорфенил ) -1, 3-диоксолана с имидазолом. Пример .19, Смесь из 8,6 ч. 1Н-имидазола, 11,3 ч. А-2-(брог метил )-2- (2, 4-дихлорфенил) -4- (3,-5-диметилфеноксиметил)-1,3-диоксолана, 4 ч. йодистого калия и 135 ч. диметилацетамида перемешивают и кипятят с обратным холодильником в течение 3 дней. К реакционной смеси приливают воду и продукт экстрагируют дважды диизопропиловым эфиром. Соединенные экстракты промывают дважды водой и добавляют избыток концентрированного раствора азотной кислоты. Образующуюся соль азотной кислоты отфильтровывают и кристаллизуют из смеси изопропанола и диизопропилового эфира. Продукт снова отфильтровывают и перекристаллизовывают из 4-метил-2- пентанола, получая при этом гидрат (2,4-дихлорфенил)-4-(3,5-диметилфеноксиметил)-1,3-диоксолан-2-илметил -1Н-имидазолнитрата; т.пл. 122,6°С. Пример 20. Следуя методике римера 19 и используя эквивалентные оличества соответствующих исходных еществ, получают следующие имидзолы и соли .имидазолов при добавлеии кислот Пример 21. Смесь из 42 ч. 1Н-имидазола, 63 ч. А+Б-4-(1,1-дифенил)-4-илоксиметил -2- (брог далетил)-2- (2,4-дихлорфенил)-1,3-диоксолана, 20 ч, йодистого калия и 675 ч. диметилформамида перемешивают и кипятят с обратным холодильником в течение 3 дней. К реакционной смеси приливают воду и продукт экстрагирую диизопропиловым эфиром. Экстракт высушивают, фильтруют и выпаривают. Остаток превращают в соль азотной кислоты в 4-метил-2-пентаноле и диизопропиловом эфире. Продукт выделяют в виде масла. Жидкую фазу декан тируют, а остаточное масло затвердевает при растирании в порошок в 4-метил-2-пентаноле. Соль азотной кис лоты отфильтровывают и кристаллизуют из этанола, получая при этом 5 частей ЦИС-1-Г4-1,1-дифенил(-4-илоксиметил )- 2- (2,4-дихлорфенил)-1,3-диоксолан-2-апметил -1Н-имидазол нитрата, т.пл. 186,5ос. Пример 22. Следуя методике примера 21 и используя эквивалентные количества соответствующих исходных веществ, получают цис-1- 2-(2,4-дихлорфенил)-4- (2-метоксифеноксиметил)-1,З-диоксолан-2-илметил -1Н-имидазол гемигидрат оксалата; т.пл. 123,, и цис-1 2-(2,4-дихлорфенил)-4-(4-фторфеноксиметилН,З-диоксолан-2-илметил -1Н-имидазол; т.пл.106,. Пример 23. Смесь из 6,4 ч. 1Н-имидазола, 10 ч. А+Б-2-(бромметил)-4- 3-хлор(1,1-дифенил)-4-илоксиметил -2- (2,4-дихлорфенил)-1,3диоксолана и 135 ч. диметилацетамида перемешивают и кипятят с обратным холодильником в течение 5 дней. Реакционную смесь оставляют охладиться до комнатной температуры ч приливают воду. Продукт экстрагирую дважды диэтиловым эфиром Соединенные экстракты промывают водой, высушивают, фильтруют и выпаривают. Остаток перекристаллизовывают из 4-метил-2-пентанола, получая при этом 2,2 ч. . (22%) транс-1-1 4- З-хлор-(1,1-дифенил)-4-илоксиметил -2- (2,4-дихлор фенил )-1, 3-диоксолан-2-илметил -1Н-имидазола; т.пл. 140,. Пример 24. Смесь из 10,2 ч 1Н-имидазола и 26,8 ч. 30%-ного рас вора метилата натрия перемешивают и кипятят, с обратным холодильником в течение 15 мин. Затем к смеси прибавляют 90 ч. диметилформамида. Метанол отгоняют до тех пор, пока вну ренняя температура не достигнет при мерно 130°С. После добавления допол нительного количества 90 ч. диметил формамида, прибавляют по частям при мерно при 100°С 50 ч, А+Б-4- (1,1-дифенил)-4-илоксиметил -2-(бромметил-2-2,4-дихлорфенил)-1,3-диоксола на. По завершении прибавления перемешивание продолжают в течение 5 ч при температуре кипения с обратным холодильником. К реакционной смеси приливают смесь из воды и толуола. Органическую фазу разделяют и переме шивают с активированным древесным углем. Последний отфильтровывают и фильтр1ат выпаривают. Остаток очищают дважды с помощью колоночной.хроматографии над силикагелем, используя смесь из хлороформа и 1% метанола в качестве элюента. Чистые фракции собирают и элюент выпаривают. Остаток кристаллизуют из изопропанола, получая при этом 9,3 ч. цис-1- 4-(1,1-дифенил) -4-илоксиметил)-2-(2,4-дихлорфенил)-1,3-диоксолан-2-илметил1-1Н-имидазола; т.пл. 150,. Пример 25. Смесь из 17 ч 1Н-имидазола, 27,4 ч. А+Б-4-(1,1-дифенил)-4-илоксиметил}-2- (бромметил)-2-(3,4,5-т&ихлорфенил)-1,3-диоксола на и 135 ч. диметилгцетамида перемешивают и кипятят с обратным холодильником в течение 5 дней. Реакционную смесь охлаждают и к ней приливают воду. Продукт экстрагируют дважды диэтиловым эфиром. Соединенные экстракты промывают водой, высушивают, фильтруют и выпаривают. Оста ток очищают с помощью колоночной хроматографии над силикагелем, используя хлороформ в качестве элюента Первую фракцию собирают и элюент выпаривают. Остаток превращают в соль азотной кислоты в 4-метил-2-пентаноле и диизопропиловом эфире. Соль отфильтровывают и кристаллизуют из смеси ацетонитрила и диизопропилового эфира, получая при этом 3 ч. цис-1- 4-(1,1-дифенил-4-илоксиметил)-2-(3,4 ,5-трихлорфег1ил )-1, 3-диоксолан-2-илметил -1Н-имидазол нитрата; т.пл. 212,20с. Вторую фракцию собирают и выпаривают элюент. Остаток превращают в соль азотной кислоты в 4-метил-2-пентаноле и диизопропиловом эфире. Соль отфильтровывают.и кристаллизуют из смеси ацетонитрила и диизопропилового эфира, получая при этом 1,9 ч. транс-1- 4- 1(1,1-дифенил)-4-илоксиметил -2- (3,4,5-трихлорфенил) -1,З-диоксолан-2-илметил -1Н-имидазол нитрата; т.пл. 1580С. Пример 26. Следуя методике примера 25 и используя эквивалентные количества соответствующих исходных веществ, получают следующие имидазолы и соли имидазолов при добавлении кислот: цис-1- 4- (1,4-дифенил)-4-илоксиметил -2- (4-бром-2-хлорфенил) -1,З-диоксолан-2-илметил -1Н-имидазол, т. пл. 161,8°С; транс-1- 4- (1,1-дифенил-)-4-илоксиметил -2-(4-бром-2-хлорфенил)-1,3-диоксолан-2-илметилЗ-1Н-имидазол;т.пл.164,6°С; цис-1- (1,1-дифенил)-4-илоксиметил) -2- (2-нафталенил)-1,З-диоксолан-2-илметил -1Н-имидазол;т.пл. 15 2,60 С; транс-1- (1,1-дифенил)-4-илоксиметил)-2-(2-нафталенил )-1, 3-диоксолан-2-илметил -1Н-имидазол нитрат; т. пл. 230,6°С; цис-1- 4-(1,1-дифенил)-4-илоксиметил -2-(2,4,5-трихлорфенил)-1,З-диоксолан-2-илметил -1Н-имидазол нитрат; т.пл.199, и транс-1- 4-(1,1-дифенил)-4-илоксиметилД-2- (2,4,5-трихлорфенил)-1,3-диоксолан-2-илметил - Н-имидазол;т.пл. 139,20с. Пример 27. Смесь из 11,5 ч. 1Н-имидазола, 17,5 ч. Л+Б-2-(бромметил) -2- (2,4-дихлорфенил)-4-(3,4,5трихлорфеноксиметил)-1,3-диоксолана, 3ч. йодистого калия и 180 ч. диметилацетамида перемешивают и кипятят с обратным холодильником в течение 3 дней. К-реакционной смеси приливают воду и продукт экстрагируют 4раза диэтиловым эфиром. Соединенные экстракты промывают 5 раз водой, высушивают, фильтруют и выпаривают. аслянистый остаток очищают с поощью колоночной хроматографии над иликагелем, используя хлороформ в ачестве элюента. Первую фракцию (А-изомер) собирают и элюент выпариают. Маслянистый остаток превращают соль азотной кислоты в 4-метил-2пентаноле. Соль отфильтровывают и ристаллизуют из смеси 4-метил-2пентанола и диизопропилового эфиа, получая после осушки 7,5 ч.(40%) ис-гидрата-1- 2-(2,4-дихлорфенил)4-(3,4,5-трихлорфеноксиметил)-1,3диоксолан-2-илметил -1Н-имидазол итрата; т.пл. 149,. Вторую фракцию (Б-изомер) собиают и элюент выпаривают. Маслянистый статок превращают в соль азотной ислоты в 4-метил-2-пентанола. Соль тфильтровывают и кристаллизуют из меси 4-метил-2-пентанола. Соль отильтровывают и кристаллизуют из меси 4-метил-2-пентанола и диизоропилового эфира, получая после осуши 6,2 ч. (27%) транс-1-1.2-(2, 4-дихлорфенил)-4-(3,4,5-трихлорфеноксиметил)-1,З-диоксолан-2-илметил -1Н-имидазол нитрата; т.пл. 169,. Пример 28. Следуя методике примера 25 и используя эквивалентные количества соответствующих исходных веществ, получают следующие имидазолы и соли имидазолов при добавлении кислот. Когда представляют только один изомер, это означает, что из хроматографии не получают вторую фракцию. Цис-1- Г4-(2-хлор-5-метилфеноксиметил)-2-(2,4-дихлорфенил)-1,3-диоксолана-2-илметил -1Н-имидазол;т.пл. 131, 7ОС, транс-1-С4-(2-ХЛОР-5-метилфеноксиметил)-2-(2,4-дихпорфенил)-1,3-диоксолан-2-илметилЗ-1Н-имидазол сесквй-окссшат,т.пл. 148; Т. (1,6-дибром-2-нафталенилоксй -метил -2-U,4-дихлорфенил;-1,3-диоксолан-2-илметил-1Н-имидазол нитрат; т.пл. 179,4°С; (2,3-дихлорфеноксиметил)-2- (2,4-дихлорфенил -1,З-диоксолан-2-илметил -1Н-ИМИДазол оксалат; т.пл. 151,1°С и Б-1- 4-(2, 3-дихлорфеноксиметил)-2- (2,4 -дихлорфенил )-1, 3-диоксо/1ан-2-илметил -1Н-имидазол сесквиоксалат, т.пл. 156,. Пример 29. Следуя методике примера 10, используя эквивалентные количества соответствующих исходных вещестю, получают следующие соедине ния: А+Б-1- 4-(4-бромфенилтиометил) -2-(2,4-дихлорфенил)-1,3-диоксолан-2-илметил -1Н-имидазол нитрат, А+Б -1- 2- (2,4-дихлорфенил)-4-(фенилтиометил)-, З-диоксолан-2-илметкл -1Н-имидазол нитрат;т.пл. 122,. Пример 30. Смесь из 4,5 ч. 1Н-имидазола, 6,5 ч. А-2-(бромметил -4- {4-бромфеноксиметил)-2-(2,3-дихлорфенил)-1,3-диоксолана и 125 ч. диметилацетамида перемешивают и кипятят с обратным холодильником в те чение двух дней. Реакционную смесь оставляют охладиться до комнатной температуры, приливают воду и проду экстрагируют дважды диэтиловым эфиром. Соединенные экстракты промываю двс1Жды водой и прибавляют избыток раствора концентрированной азотной кислоты. Образующуюся соль азотной кислоты отфильтровывают и кристалли зуют из 4-метил-2-пентанола, получа при этом 5 ч. (68%) цис-1- 4-(4-бро феноксиметил ) -2- (2,3-дихлорфенил)-1,З-диоксолан-2-илметил -1Н-имидаэол нитрата; т.пл. 138,9°С. Пример 31. Следуя методике примера 25 и используя эквивгшентны количества соответствующих исходных веществ, получают следующие соли имидазолов при добавлении кислот: цис-1- 4- СЗ-хлор-(1,1-дифенил-4-илоксиметил)-2- (2,4-дихлорфенил)-1,3-диоксолан-2-илметил -1Н-имидазол нитрат; т.пл. 171, цис-1-Г -(1, -(ифенил) -4-илоксиметил)-2- (2-хлор-4-метоксифенил)-1,З-диоксолан-2-илметил -1Н-имидазол нитрат; т.пл. 172,9С, А+Б-1-р-(2,4-дихлорфенил)-4- (фенилметил)-1,3-диоксолан-2-илметил -1Н-имидазоя оксалат; т.пл. 117, А+Б-1- 2-(2,4-дихлорфенил) -4- (4-фторфенил)тиометил -1,З-диоксолан-2-илметилЗ-1Н-имидаэол оксалат;.т.пл. 129,ВОС; A+B-l-4f-(4-хлорбензил)-2- (2,4-дихлс рфенил)-1,З-диоксолан-2-илметил -1Н-имидазол сесквиоксалат, т.пл. 141,6°С; А+Б-1-Г2- (2;4-дихлорфенил)-4-(4-метоксибензил)-,З-диоксолан-2-илметил1 -1Н-имидазол диоксалат/ т.пл. 94,, цис-2-2-(2, 4-дихлорфенил )-2-(1Н-имидазол-1-илметил)-1,3-диоксолан-4-илметоксибензонитрилнитрат; т.пл. 162,1С и цис-бутил (2,4-дихлррфенил)-2-(1Н-имИдазол-1-илметил)-, З-диоксолан-4-илгметоксиЗ-бензоат нитрат;т.пл. 90,. Пример 32. Смесь из 14,4 ч. 1Н-имидазола, 18,5 ч. А+Б-2-(бромметил) -2- (2,4-диклорфенил)(4-метоксифенил)-этил -1,3-диоксолана, 5 ч. йодистого калия и 135 ч. диметилацетамида перемешивают и кипятят с обратным холодильником в течение двух дней. Реакционную смесь оставляют охладиться до комнатной температуры и к ней приливают воду. Продукт экстрагируют дважды диизопропиловым эфиром. Соединенные экстракты промывают водой,высушивают, фильтруют и выпаривают. Остаток превращают в соль щавелевой кислоты в 4-метил-2-пентаноле и диизопропиловом эфире. Соль отфильтровывают и кристаллизуют ИЗ смеси диизопропилового эфира и этанола, получая при этом А+Б-1- 2-(2, 4-дихлорфенил)-4- 2-(4-метоксифенил)-этил}-1, 3-диоксолан-2-илметил -1Н-имидазол сесквиоксалат; т.пл. 130,70с. - . Пример 33. Следуя методике примера 25 и используя эквивгшентные количества соответствующих исходных веществ, получают следующие имидазолы и соли имидазолов при добавлении, кислот: (4-хлорфенил )-этил)-2-(2,4-дихлорфенил -1, 3-диоксолан-2-нлметил -1Н-имидаэол диоксалат/ т.пл. 131,90с, (2,4-дихлорфенил)-4-(2-фенилэтил)-1,3-диоксолан-2-нлметил -1Н-имидазолсесквиоксалат ; т.пл. 117,8с и А+В-1-С2-(2,4 ДИХлорфенил)-4- (2- (4-метилфенил)-этил)-1,3-диоксолан-2-илметил -1Н-имид аз ол сесквиоксалат, и гидрат; т.пл. 123,. (2-хлорфенил )-этил -2- / -(2,4-дихлОрфенил)-1,З-диоксолан-2-илметил}-1Н-имидазол нитрат; т.пл. 98,8°С, (2,4-лихлорфенил-1- (2- (2,4-дихлорфенил)-этил -1, 3-диоксолан-2-илметилJ-1Н-имидазолнитрат; т.пл. 158,1°С и А+Б-1-С2- (2,4-дихлорфенил)-4- (2- 12,4-дихлорфенил) -этил -1, 3-диоксолан -2-илметил -1Н- имидазол нитрату т.пл. 140,1С. Пример 34. К перемешиваемом раствору метилата натрия, полученному исходя из 3,8 ч натрия в 40i ч метанола, добавляют 11 ч. 1Н-имидазола и 225 ч. диметилформамида. Метанол отгоняют до тех пор, пока внутренняя температура не достигнет . Затем к смеси прибавляют 19 ч. А+Б-2-(бромметил)-2-(2,4-дихлорфенил)-4-этил-1,3-диоксолана и содержимое перемешивают и кипятят с обратным хо лодильником в течение 1 ч. Реакционную смесь оставляют охладиться до комнатной температуры и к смеси приливают воду. Продукт экстрагируют трижды диэтиловым эфиром. Соединенны экстракты пр01«|1вают водой, высушиваю фильтруют и выпаривают. Остаток очищают с помощью колоночной хроматогра фии над силикагелем, используя смесь из хлороформа и 1% метанола в качест ве элюенха. Первую фракцию собирают и элюент выпаривают. Остаток превращают в соль азотной кислоты в диизопропиловом эфире. Соль отфильтровывают и кристаллизуют из смеси изопропанола и диизопропилового эфира, получая при этом 12 ч. (56%) А+Б-1- 2,4-дихлорфенил1-4-ЭТИЛ-1,3-диоксо л ан-2-ил метил -Дн-имидазол нитрата; т.пл. 149,100. Пример 35. К перемешиваемом раствору метилата натрия, полученно2-се-С(,н,
2-СН,-С Н
4-сн,-с,н
2,3,4-(ce), 2-В,
2,3-(ce),j, з-сг-с н
4-OCH,-CgH
2-CH2 -4-Ce-C Hj
2-Се-4-ОСН,-СйН
з,4,5-(сг),, 2-Нафтил
гз
Ni5
МБ
147,6 117,5 172,7 176,4 135,3 140,3 151,6 157,1 126,8 117,7 195,8 195,1 му, исходя из 2,7 ч. натрия в 40 ч. метанола, добавляют 8 ч. 1Н-имидазола и 225 ч. диметилформамида. Метанол отгоняют до тех пор, пока внутренняя температура не достигнет . Затем к смеси прибавляют 30 ч. А+Б-2-(4-бром-2-хлорфенил)-2-(бромметил)-4-ЭТИЛ-1,3-диоксолана и перемешивание продолжают в течение 1 ч. при температуре кипения с обратным холодильником. Реакционную смесь охлаждают и нашивают воду. Продукт экстрагируют дважды диизопропиловым эфиром. Соединенные экстракты промывают водой, высушивают, фильтруют и выпари-, вают. Остаток очищают с помощью колоночной хроматографии над силикагелем, используя смесь из хлороформа и 2% метанола в качестве элюента. Чистые фракции собирают и элюент выпаривают. Остаток превращают в соль азотной кислоты в диизопропиловом эфире. Соль отфильтровывают и кристаллизуют из смеси 4-метил-2-пентанола и диизопропилового эфира, получая при этом 8,5 ч. (26%) А+Б-1- 2-(4-бром-2-хлорфенил)-4-этил-1,3-диоксолан-2-илметил -1Н-имидазолнитрат; т.пл. 162,2-С. Пример 36. Следуя методике примера 25 и используя эквивалентные количества соответствующих исходных веществ, получают следующие соли имидазблов при добавлении кислот
23
Пример 37. Смесь из 7,7 ч. 1Н-имидазола, 8 частей цис-2-(бромметил) -2- (2,4-дихлорфенил)-1,3-диоксолан-4-метанола, 1 ч. йодистого калия и 180 ч, диметилацетамида перемешивают и кипятят с обратным холодильником в течение 3 дней. Реакционную смесь охлаждают и выпаривают Затем к остатку прибавляют 50 ч.-воды и 300 ч. хлороформа. Содержимое промывают три раза водой, высушивают фильтруют и выпаривают. Остаток очищают с помощью колоночной хроматографии над силикагелем, используя смесь из хлороформа и 2% метанола в качестве элюента. Чистые фракции собирают в элюент выпаривают, получают при этом 9,2 ч. дис-2-(2,4-дихлорфенил)-2-(1Н-имидазол-1-илметил) -1, З-диоксолан-4-метанола; т.пл. 140С.
Пример 38. Следуя методике примера 37 и используя эквивалентное количество транс-2-(бромметнл)-2-(2,4-дихлорфенил)-1,З-диоксолан-4-метанола в качестве исходного вещества, - получают транс-2-(2,4-дихлорфенил)-2-(1Н-имидаз ол-1-нлметил)-1, 3-диоксгшан-4-метанол;т.пл, 129с,
Пример 39. Смесь из 13,8 ч. 1-(2-хлор-4-фторфенил)-2-(1Н-имидазол-1-ил)-этанол хлоргидрата,14,6 ч 3- (1,1-дифенил) -4-илокси -1,2-пропандиола, 16 ч. п-толуолсульфоновой кислоты, 40 ч. бутанола и 225 ч. ксилола перемешивают и кипятят с Ъбратиым холодильником в течение 1 недели с водоотделителем. После охлаждения, прибавляют диэтиловый эфир и содержимое промывают последовательно разбавленным раствором гидроокиси натрия и водой, высушивают, фильтруют и выпаривают. Остаток очищают с помощью колоночной хроматографии над силикагелем, используя хлороформ в качестве элюента. Первую фракцию (А-изомер) собирают и элюент выпаривают. Остаток превращают в соль азотной кислоты в 4-метнл-285000624
Продолжение таблицы
-пентаноле и диизопропиловом эфире. Продукт отфильтровывают и кристаллизуют из смеси ацетонитрила и диизо0пропилового эфира, получая при этом 5 ч. цис-1-| 4-(1,1-дифенил)-4-илоксиметил -2-(2-хлор-4-фторфенил)-1,3-диоксолан-2-илметилТ{-1Н-имид-. азол нитрата; т.пл. 185,.
Вторую фракцию (Б-изомар) соби5рают и элюент выпаривают. Остаток превращают в соль азотной кислоты в 4-метил-2-пентаноле и дииэопропиловом эфире, получая при этом 5,9 ч. транс-1-{4-(1,1-дифенил)-4-илоксиDметил}-2-(2-хлор-4-фторфенил)-1,3-диоксолаи-2-илметил -1Н-имидазапНитрата, т.пл. 156,.
Пример 40. Следуя методике примера 39 и используя эквивалентные
5 количества соответствующих исходных веществ, получают следующие имидазолы и соли имидазолов при добавлении кислот. Когда представляется только Один изомер/ то из хроматографии не получается вторая фракция.
0
Цис-1-54- (1,1-дифенил)-4-илокси,метилХ-2- (2-тиенил)-1,3-диоксолан-2-илметил1-1Н-имидазол;т.пл. 149,5С, транс-1- 4- С(1 Д-ДИфенил)-4-илоксиметил -2- (2-тиенил)-1,З-диоксолан-25-илметил -1Н-имидазол;- т.пл. цис-1-(4- (1,1-дифеннл)-4-илоксиметил -2-(2,4-либромфенил)-1,3-диоксолан-2-илметил}-1Н-имидазол нитрат, т.пл. 174,40с, TpaHc-l-U-(l,l -ди0фенил)-4-илоксиметилЗ-2-(2,4-дибромфенил-1,3-диоксолан-2-илметил5-1Н-имидазол нитрат,т.пл. 141,850 и цис-l-i4- Г(1,1 -дифенил),)-4-илоксиметш1} -2- Г5-хлор-2-тиенил)-1,3-диоксолан5-2-илметил}-1Н-имидазол нитрат, т.пл. 1700с.
Формула изобретения
О
х
S где А - фенил, 3ah4emeHHbin фенил, тиенил, хлортиенил или нафтил, и в которой указанный замешенный, фенил имеет значения фенильной группы, имеющей от 1 до 3 заместителей, независимо состоящих из галоида, метила, метокси, нитро- или циаНогруппы;R - апкил, имеющий от 2 до 10 атомов углерода, алкоксиметил, в котором алкильнс1я группа имеет от 1 до 10 атомов углерода, этенил, 2-пропенилоксиметил, 2-пропинилоксиметил, оксиметил, галоидметил, арил метил, арилэтил, арилоксиметил, арилтиометил или арилметоксиметил, в которых указанный арил является фенилом, замещенным фенилом/ нафтил или моно- и ди-галоиднафтилом, ив которых указанный замещенный фенил означает фенильную группу, имеющую .от 1 до 3 заместителей, независимо состоящих из галоида, низшего гшкинизшего ашкилокси с С, ла с С. циано, нитро-групп, фенила, фенилметила, бёнзоила, хлорбензоила, низ шего алкилкарбонила с С, низшего ёшкилоксикарбонила с С. или трифторметила, при условии, что когда более, чем один заместитель присутствует, то только один заместит.елъ может быть выбран из группы, состоящей из фенила, бензила, фрнил метила или хлорбензоила, отличающийся тем, что соединени формулы II или его соль с металлом подвергают взаимодействию с соединением формулы I I I. в которой W представляет собой реакционноспособную сложноэфирную группу в органическом растворителе, с выделением целевого продукта в свободном виде, в виде соли или оптических изомеров . 2.Способ по п. 1, отличаю«ц и и с я тем, что процесс проводят при кипячении реакционной массы. 3.Способ по пп. 1-2, отличающийся тем, что процесс проводят в присутствии йодистого металла. 4.Способ по пп. 1-3, отличающийся тем, что в случае, когда в качестве исходного продукта используют соединение формулы II, процесс ведут с использованием избытка имидазола или в присутствии основания такого, как карбонат или бикарбонат натрия или калия. Приор по признакам: 27.01.75 Ар - фенил, моно- ди- или триГсшоидфенил, низший алкилфенил, низший алкоксифенил; R - фенил, замещенный фенил, нафтил или галоиднафтил, где замещенный фенил означает фенил, имеющий от 1 до 3 за1местителей, независимо выбранных из группы, состоящий из галоида, низшего алкила, низшей алкокси-группы, цианогруппы, фенила или бензила. 06.10.75 А,, - имеет все остальные значения; R - имеет все остальные значения. Источники информации, принятые во внимание при экспертизе , 1. Патент США 3575999, кл. 260-309, опублик. 1971.
Авторы
Даты
1981-07-23—Публикация
1976-01-21—Подача