Изобретение относится к методам измерения или испытания, использующим жизнеспособные микроорганизмы, и касается способа определения микробиологической чистоты лекарственных средств для таргетной терапии.
Наиболее близким к заявленному является способ определения микробиологической чистоты отдельных биотехнологических лекарственных средств [1], который позволяет количественно определять жизнеспособные клетки бактерий и грибов по их способности размножаться и образовывать колонии на плотной питательной среде. При этом каждая колония является результатом размножения одной клетки. Для выявления отдельных видов патогенных микроорганизмов используют комплекс жидких и плотных питательных сред, соответствующих специфическим потребностям определяемых микроорганизмов, а также биохимические тесты для их идентификации.
Способ включает стадии:
- пробоподготовку образца лекарственного средства (не менее 10 г);
- добавление измельченного образца к 100 мл фосфатно-буферного раствора и посев в 4 чашки Петри, а также в жидкую неселективную накопительную среду для определения патогенных бактерий;
- инкубацию посевов с питательными средами для выделения бактерий при температуре (32,5±±2,5)°С, для выращивания дрожжевых и плесневых грибов - при температуре (22,5±2,5)°С;
- пересев на жидкую селективную питательную среду;
- пересев на диагностические питательные среды;
- микроскопическое исследование;
- биохимическую идентификацию выделенных микроорганизмов;
- количественный и качественный учет результатов.
К недостаткам известного способа определения микробиологической чистоты лекарственных средств следует отнести значительное количество образца для анализа, разведение которого не полностью используется при испытании.
Между совокупностью существенных признаков заявляемого способа и достигаемым техническим результатом существует причинно-следственная связь, а именно: использование триптиказо-соевого бульона или питательной среды №8 в качестве универсального разбавителя (растворителя) и среды для культивирования позволяет сократить объем образца для анализа в 7 раз.
Предлагаемое техническое решение отличается от известного [1] тем, что на стадии пробоподготовки используется уменьшенное количество образца, разведение которого полностью используется для анализа. В качестве универсального разбавителя применяется триптиказо-соевый бульон или питательная среда №8.
Задачей изобретения является сокращение количества образца для оценки качества по показателю «Микробиологическая чистота», времени пробоподготовки и минимизация потерь лекарственного средства при анализе.
Поставленная задача решается благодаря применению неселективной питательной среды в качестве разбавителя уменьшенного количества образца при определении отдельных видов патогенных бактерий.
Питательные среды, описанные в [1], являются универсальными, свободными от ингибиторов и индикаторов, предназначенными для широкого спектра микробиологических задач. Богатая питательная основа данных сред подходит для культивирования большинства микроорганизмов, в том числе требовательных к условиям роста.
Предложенное изменение позволяет в 7 раз сократить количество образца для анализа таргетных препаратов по показателю «Микробиологическая чистота».
Сущность предложенного изобретения заключается в следующем:
- образец в количестве 1,4 г разбавляют 14 мл триптиказо-соевого бульона или среды №8;
- 4 мл полученного разведения используют для количественного определения аэробных бактерий и грибов, производя посев в 4 стерильные чашки Петри (по 1 мл в каждую), 2 из которых заливают плотной питательной средой для выращивания бактерий, 2 другие - средой для выращивания дрожжевых и плесневых грибов;
- оставшиеся 10 мл разведения используют для выделения E.coli.
Стадию инкубации и последующие операции выполняют так же, как в известном способе.
Техническим результатом заявляемого изобретения является уменьшение объема пробы, минимизация потерь лекарственного средства при анализе, расширение арсенала способов оценки микробиологической чистоты лекарственных препаратов таргетной терапии.
Возможность осуществления заявляемого изобретения показана следующими примерами.
Средства и методы
При доказательстве возможности определения микробиологической чистоты лекарственных средств для таргетной терапии использовали:
1. Тест-штаммы микроорганизмов:
- Candida albicans АТСС 10231,
- Escherichia coli АТСС 8739,
- Bacillus subtilis ATCC 6633,
- Aspergillus brasiliensis ATCC 16404.
2. Питательные среды:
2.1. производства фирмы «Биомерье», Франция
- триптиказо-соевый агар;
- триптиказо-соевый бульон;
- агар Сабуро;
- бульон Мак-Конки;
- агар Мак-Конки.
2.2. производства ФБУН Государственный научный центр прикладной микробиологии и биотехнологии (п. Оболенск, Россия):
- среда №1 ГРМ;
- среда №2 ГРМ (Сабуро);
- среда для выделения энтеробактерий (агар Эндо ГРМ);
- среда №8 ГРМ;
- среда №3 ГРМ.
3. Реактивы: раствор натрия хлорида 0,9%.
4. Расходные материалы: стерильные пробирки биологические; пипетки серологические 1, 5, 10 мл; флаконы стерильные одноразовые 125 мл; чашки Петри 90 мм стерильные одноразовые.
5. Аттестованное и поверенное оборудование: инкубаторы фирмы Binder (Германия), ламинарный шкаф класс II тип А2 фирмы Labconco (США), счетчик колоний Scan 100 фирмы Interscience (Франция).
При доказательстве возможности применения заявляемого изобретения проводили расчет коэффициента восстановления (R) микроорганизмов по формуле (1):
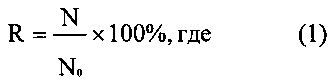
N - количество колоний, выделенных в ходе анализа (КОЕ);
N0 - количество внесенных клеток микроорганизмов (КОЕ).
Приемлемым считали коэффициент восстановления не ниже 50%.
Пример 1. Определение микробиологической чистоты лекарственного средства эрлотиниб таблетки 100 мг.
Отбирали 1 г вещества. Образец растворяли в 10 мл триптиказо-соевого бульона. Вносили тест-штаммы в количестве 50 КОЕ/г каждого микроорганизма.
По 1 мл подготовленного образца вносили в 4 чашки Петри, 2 из которых заливали 10-15 мл триптиказо-соевого агара - для определения содержания аэробных микроорганизмов, а 2 оставшихся - 10-15 мл агара Сабуро для выделения дрожжевых и плесневых грибов.
6 мл раствора образца инкубировали при температуре (32,5±2.5)°С в течение 48 ч. Чашки Петри, залитые триптиказо-соевым агаром и агаром Сабуро, инкубировали в течение 120 ч при температурах (32,5±2.5)°С и (22,5±2.5)°С соответственно.
После инкубации на агаризованных питательных средах подсчитывали количество колоний микроорганизмов и по формуле (1) рассчитывали коэффициент восстановления выделенных бактерий, дрожжевых и плесневых грибов.
По истечении периода инкубации 1 мл раствора образца вносили в 9 мл бульона Мак-Конки, инкубировали в течение 48 ч при температуре (32,5±2.5)°С, производили пересев бактериологической петлей на агар Мак-Конки, инкубировали в течение 24 ч при температуре (32,5±2.5)°С, после чего наблюдали типичный рост колоний Escherichia coli.
Результат: в процессе испытания было проведено количественное определение бактерий, дрожжевых и плесневых грибов, которыми был инокулирован образец лекарственного средства эрлотиниб, таблетки 100 мг. Коэффициент восстановления аэробных микроорганизмов составил 75%, дрожжевых и плесневых грибов - 101%. С применением предлагаемого способа из контаминированного лекарственного средства были выделены бактерии Escherichia coli.
Пример 2. Определение микробиологической чистоты лекарственного средства траметиниб таблетки 1 мг.
Отбирали 1 г вещества. Образец растворяли в 10 мл среды №8 ГРМ. Вносили тест-штаммы в количестве 50 КОЕ/г каждого микроорганизма.
По 1 мл подготовленного образца вносили в 4 чашки Петри, 2 из которых заливали 10-15 мл среды №1 ГРМ - для определения содержания аэробных микроорганизмов, а 2 оставшихся - 10-15 мл среды №2 ГРМ для выделения дрожжевых и плесневых грибов.
6 мл раствора образца инкубировали при температуре (32,5±2.5)°С в течение 48 ч. Чашки Петри, залитые средами №1 ГРМ и №2 ГРМ, инкубировали в течение 120 ч при температурах (32,5±2.5)°С и (22,5±2.5)°С соответственно.
После инкубации на агаризованных питательных средах подсчитывали количество колоний микроорганизмов и по формуле (1) рассчитывали коэффициент восстановления выделенных бактерий, дрожжевых и плесневых грибов.
По истечении периода инкубации 1 мл раствора образца вносили в 9 мл среды №3, инкубировали в течение 48 ч при температуре (32,5±2.5)°С, производили пересев бактериологической петлей на агар Эндо, инкубировали в течение 24 ч при температуре (32,5±2.5)°С, после чего наблюдали типичный рост колоний Escherichia coli.
Результат: в процессе испытания было проведено количественное определение бактерий, дрожжевых и плесневых грибов, которыми был инокулирован образец лекарственного средства тарметиниб, таблетки 1 мг. Коэффициент восстановления аэробных микроорганизмов составил 71%, дрожжевых и плесневых грибов - 91%. С применением предлагаемого способа из контаминированного лекарственного средства были выделены бактерии Escherichia coli.
Пример 3. Определение микробиологической чистоты лекарственного средства акситиниб таблетки 7 мг.
Отбирали 1 г вещества. Образец растворяли в 10 мл среды №8 ГРМ. Вносили тест-штаммы в количестве 5 КОЕ/г каждого микроорганизма.
По 1 мл подготовленного образца вносили в 4 чашки Петри, 2 из которых заливали 10-15 мл среды №1 ГРМ - для определения содержания аэробных микроорганизмов, а 2 оставшихся - 10-15 мл среды №2 ГРМ для выделения дрожжевых и плесневых грибов.
6 мл раствора образца инкубировали при температуре (32,5±2.5)°С в течение 48 ч. Чашки Петри, залитые средами №1 ГРМ и №2 ГРМ, инкубировали в течение 120 ч при температурах (32,5±2.5)°С и (22,5±2.5)°С соответственно.
После инкубации на агаризованных питательных средах подсчитывали количество колоний микроорганизмов и по формуле (1) рассчитывали коэффициент восстановления выделенных бактерий, дрожжевых и плесневых грибов.
По истечении периода инкубации 1 мл раствора образца вносили в 9 мл среды №3, инкубировали в течение 48 ч при температуре (32,5±2.5)°С, производили пересев бактериологической петлей на агар Эндо, инкубировали в течение 24 ч при температуре (32,5±2.5)°С, после чего наблюдали типичный рост колоний Escherichia coli.
Результат: в процессе испытания было проведено количественное определение бактерий, дрожжевых и плесневых грибов, которыми был инокулирован образец лекарственного средства акситиниб, таблетки 7 мг. Коэффициент восстановления аэробных микроорганизмов составил 93%, дрожжевых и плесневых грибов - 78%. С применением предлагаемого способа из контаминированного лекарственного средства были выделены бактерии Escherichia coli.
Пример 4. Определение микробиологической чистоты лекарственного средства ибрутиниб капсулы 4 мг.
Отбирали 1 г вещества. Образец растворяли в 10 мл триптиказо-соевого бульона. Вносили тест-штаммы в количестве 5 КОЕ/г каждого микроорганизма.
По 1 мл подготовленного образца вносили в 4 чашки Петри, 2 из которых заливали 10-15 мл триптиказо-соевого агара - для определения содержания аэробных микроорганизмов, а 2 оставшихся - 10-15 мл агара Сабуро для выделения дрожжевых и плесневых грибов.
6 мл раствора образца инкубировали при температуре (32,5±2.5)°С в течение 48 ч. Чашки Петри, залитые триптиказо-соевым агаром и агаром Сабуро, инкубировали в течение 120 ч при температурах (32,5±2.5)°С и (22,5±2.5)°С соответственно.
После инкубации на агаризованных питательных средах подсчитывали количество колоний микроорганизмов и по формуле (1) рассчитывали коэффициент восстановления выделенных бактерий, дрожжевых и плесневых грибов.
По истечении периода инкубации 1 мл раствора образца вносили в 9 мл бульона Мак-Конки, инкубировали в течение 48 ч при температуре (32,5±2.5)°С, производили пересев бактериологической петлей на агар Мак-Конки, инкубировали в течение 24 ч при температуре (32,5±2.5)°С, после чего наблюдали типичный рост колоний Escherichia coli.
Результат: в процессе испытания было проведено количественное определение бактерий, дрожжевых и плесневых грибов, которыми был инокулирован образец лекарственного средства ибрутиниб, капсулы 4 мг. Коэффициент восстановления аэробных микроорганизмов составил 93%, дрожжевых и плесневых грибов - 87%. С применением предлагаемого способа из контаминированного лекарственного средства были выделены бактерии Escherichia coli.
Пример 5. Определение микробиологической чистоты субстанции иматиниба мезилат.
Отбирали 1 г вещества. Образец растворяли в 10 мл триптиказо-соевого бульона. Вносили тест-штаммы в количестве 50 КОЕ/г каждого микроорганизма.
По 1 мл подготовленного образца вносили в 4 чашки Петри, 2 из которых заливали 10-15 мл триптиказо-соевого агара - для определения содержания аэробных микроорганизмов, а 2 оставшихся - 10-15 мл агара Сабуро для выделения дрожжевых и плесневых грибов.
6 мл раствора образца инкубировали при температуре (32,5±2.5)°С в течение 48 ч. Чашки Петри, залитые триптиказо-соевым агаром и агаром Сабуро, инкубировали в течение 120 ч при температурах (32,5±2.5)°С и (22,5±2.5)°С соответственно.
После инкубации на агаризованных питательных средах подсчитывали количество колоний микроорганизмов и по формуле (1) рассчитывали коэффициент восстановления выделенных бактерий, дрожжевых и плесневых грибов.
По истечении периода инкубации 1 мл раствора образца вносили в 9 мл бульона Мак-Конки, инкубировали в течение 48 ч при температуре (32,5±2.5)°С, производили пересев бактериологической петлей на агар Мак-Конки, инкубировали в течение 24 ч при температуре (32,5±2.5)°С, после чего наблюдали типичный рост колоний Escherichia coli.
Результат: в процессе испытания было проведено количественное определение бактерий, дрожжевых и плесневых грибов, которыми был инокулирован образец фармацевтической субстанции иматиниба мезилат. Коэффициент восстановления аэробных микроорганизмов составил 91%, дрожжевых и плесневых грибов - 88%. С применением предлагаемого способа из контаминированного лекарственного средства были выделены бактерии Escherichia coli.
Литература.
1. Государственная фармакопея РФ XII изд. Часть 1. М.: Медицина, 2007: 704.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ МИКРОБИОЛОГИЧЕСКОЙ ЧИСТОТЫ ФАРМАЦЕВТИЧЕСКОЙ СУБСТАНЦИИ, ПРОИЗВЕДЕННОЙ БИОТЕХНОЛОГИЧЕСКИМ ПУТЕМ | 2015 |
|
RU2596399C1 |
| Штамм бактерий Bacillus megaterium, обладающий способностью продуцировать пробиотические и антимикробные вещества класса органических кислот | 2021 |
|
RU2757086C1 |
| Способ идентификации дрожжеподобного гриба Candida auris | 2022 |
|
RU2791911C1 |
| Идентификация дрожжеподобного гриба Candida auris | 2022 |
|
RU2791966C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ БАКТЕРИЙ | 2008 |
|
RU2399660C2 |
| Способ определения чувствительности кампилобактерий к пробиотикам и аутопробиотикам | 2022 |
|
RU2816763C1 |
| КОРМОВАЯ ДОБАВКА ПРОБИОТИЧЕСКАЯ | 2024 |
|
RU2833079C1 |
| Способ получения питательной среды для селективного выявления Candida auris | 2022 |
|
RU2788607C1 |
| Средство для продуцирования органических соединений, обладающих антибактериальной и антигрибковой активностью | 2021 |
|
RU2774192C2 |
| Штамм микромицета Penicillium vulpinum F-1523, обладающий антибактериальной активностью в отношении возбудителя сибирской язвы Bacillus anthracis | 2015 |
|
RU2612150C2 |
Изобретение относится к фармацевтике и микробиологии. Способ определения микробиологической чистоты лекарственных средств предусматривает подготовку образца лекарственного средства путем разбавления его в триптиказо-соевом бульоне или среде №8. Проводят посев образца на жидкую накопительную селективную среду с последующим инкубированием на ней. Затем проводят пересев на диагностические питательные среды с последующей биохимической идентификацией выделенных микроорганизмов. Изобретение позволяет сократить количество используемого образца и минимизировать потери образца при анализе. 5 пр.
Способ определения микробиологической чистоты препаратов таргетной терапии, включающий пробоподготовку образца лекарственного средства; пересев и инкубирование на жидкой накопительной селективной среде, пересев на диагностические питательные среды с последующей биохимической идентификацией выделенных микроорганизмов, отличающийся тем, что при пробоподготовке образца лекарственного средства в качестве разбавителя используют триптиказо-соевый бульон или среду № 8.
| Государственная фармакопея РФ, М., 2007, ч.1, стр | |||
| Упругое экипажное колесо | 1918 |
|
SU156A1 |
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| Способ получения молочной кислоты | 1922 |
|
SU60A1 |
| САХНО Н.Г., Применение микробиологических методов для стандартизации и контроля качества некоторых | |||
Авторы
Даты
2016-09-10—Публикация
2015-09-09—Подача