Приоритет и перекрестная ссылка на родственную заявку
Данная заявка имеет приоритет Предварительной заявки США серийный №61/566,655, поданной 4 декабря 2011 года, полное содержание которой включено в данное описание посредством ссылки на нее.
Техническая область изобретения
Изобретение относится к фармацевтической композиции уникального состава и к новому способу лечения посредством внутриопухолевой инъекции. Фармацевтическая композиция по изобретению представляет собой насыщенный ионный раствор ионов натрия и ионов кальция ("лекарственную ионную бомбу"). Изобретение внутриопухолевой инъекции "лекарственной ионной бомбы" можно использовать в качестве терапии первой линии для лечения рака и опухолей по меньшей мере в девяти органах человека (например карциномы и опухоли кожи и подкожной ткани, молочной железы, предстательной железы, щитовидной железы, легкого, печени, генитального органа, головного мозга и поджелудочной железы) и по меньшей мере четырех категорий доброкачественных заболеваний (например кожного и подкожного новообразования, кистозно-фиброзного изменения молочной железы, доброкачественной гиперплазии предстательной железы и узлов щитовидной железы).
Предшествующий уровень техники
Рак представляет собой неконтролируемый рост аномальных клеток в организме. Рак часто способен проникать в другие ткани из его первоначального местонахождения и может распространяться в другие части тела через кровеносную систему и лимфатическую систему. Существует множество типов рака, которые можно классифицировать по патологии и клиническому диагнозу на карциному, саркому, лейкоз, лимфому и миелому, а также злокачественные опухоли центральной нервной системы.
Лечение рака требует усилий и от пациента, и от лечащего врача. Существующие в настоящее время методы лечения включают хирургию, химиотерапию, радиотерапию, иммунотерапию, биотерапию, лазерную терапию, криотерапию, термотерапию и т.д. Хотя в последние десятилетия были получены значительные результаты в предупреждении и лечении рака, выживаемость больных раком все еще низкая для многих типов рака. По оценкам, только в США насчитывается свыше 1,5 миллионов новых случаев рака и более чем полмиллиона связанных с раком смертельных случаев в 2011 году. Таким образом, рак остается главной угрозой для здоровья людей.
В двух опубликованных сообщениях для лечения опухолей использовали единственный компонент высококонцентрированный хлорид натрия. В одном сообщении Siegle et al. использовали гипертонический физиологический раствор для лечения одного пациента с многогломусными опухолями, редким доброкачественным новообразованием, возникающим из гломусного тельца под ногтями пальцев и барабанной перепонкой (Siegle, et al. 1994 J. Dermatologic Surgery & Oncology 20:347-348). Использовали единственный компонент, 23,4%-ный раствор хлорида натрия, который не привел к успешному лечению пациента. Этот пациент получил 4 сеанса внутрипросветной инъекции 23,4%-ного гипертонического физиологического раствора с интервалом в 6 месяцев. В другом сообщении Lin et al. использовали 36,5%-ный гипертонический физиологический раствор для лечения опухоли печени у кроликов, и ни одна из опухолей не была успешно вылечена (Lin, et al. 2005 Am. J. Roentgenology 184: 212-219).
Таким образом, остается безотлагательная потребность в новых и эффективных средствах для лечения рака.
Краткое изложение сущности изобретения
Изобретение основано, частично, на открытии уникальных фармацевтических композиций, пригодных для лечения различных типов рака, злокачественной опухоли, доброкачественной опухоли и незлокачественного заболевания, и относится к способам их использования. Настоящее изобретение реагирует на назревшую необходимость создания быстрых и эффективных терапевтических средств, которые являются доступными.
В частности, изобретение относится к разработке новых фармацевтических композиций для лечения рака, злокачественной опухоли, доброкачественной опухоли и незлокачественного заболевания. Эта фармацевтическая композиция по изобретению названа "лекарственной ионной бомбой." В предпочтительном воплощении композиция "лекарственной ионной бомбы" содержит 5,0479 М ионов натрия (Na+) (например из хлорида натрия (NaCl)), и 250 мМ ионов кальция (Ca2+) (например из хлорида кальция (CaCl2)) в стерильной дистиллированной воде (1 М=1 моль/л; 1 мМ = 1×10-3 М). В некоторых воплощениях композиция содержит два дополнительных компонента: 10 миллилитров (мл) Ultravist 370 и 20 миллиграммов (мг) адреналина, которые смешивают с литром раствора "лекарственной ионной бомбы" перед тем, как осуществлять внутриопухолевую инъекцию. Здесь Na+ и Ca2+ в композиции используются для уничтожения раковых клеток.
Комбинация Na+ и Ca2+ в композиции "лекарственной ионной бомбы" оказывает синергетический эффект, комплементарный эффект и эффект двойной волны в уничтожении раковых клеток. Стерильная дистиллированная вода является растворителем. Ultravist 370 представляет собой рентгеноконтрастную среду для отслеживания диффузии раствора "лекарственной ионной бомбы" внутри обрабатываемой раковой или злокачественной опухоли под контролем сканирования методом компьютерной томографии (СТ). Адреналин является сосудосуживающим лекарственным средством для усиления уничтожающего рак эффекта посредством задержки высвобождения композиций "лекарственной ионной бомбы" в кровоток. Без связи с теорией, полагают, что адреналин может вызывать сужение кровеносных сосудов, создавая кратковременную "искусственную опухолевую капсулу" в обрабатываемой опухоли для предотвращения вымывания раствора "лекарственной ионной бомбы" из некапсулированной опухолевой массы.
В данном документе демонстрируется, что "лекарственная ионная бомба" способна уничтожать 18 типов линий раковых клеток человека в тканевой культуре за минуты. "Лекарственная ионная бомба" также уничтожала модели рака человека у бестимусных мышей за несколько суток. Мышиные опухоли, равные примерно 2-3% массы тела, были уничтожены одной однократной внутриопухолевой инъекцией 0,12 мл "лекарственной ионной бомбы". У выбранных пациентов-людей доброкачественная опухоль или раковое образование размером 50 миллиметров (мм) × 70 мм была(о) уничтожена(о) одной однократной внутриопухолевой инъекцией "лекарственной ионной бомбы". Данное изобретение было успешно использовано у 78 пациентов-людей, страдавших 6 типами злокачественной опухоли или рака и 10 типами доброкачественных новообразований или незлокачественных состояний.
В одном аспекте данное изобретение в общем относится к фармацевтической композиции, пригодной для лечения рака, злокачественной опухоли, доброкачественной опухоли и незлокачественного заболевания путем введения посредством внутриопухолевой инъекции. Композиция содержит, в водном растворе, источник Na+ обеспечивающий концентрацию Na+ от примерно 2,0 М до примерно 5,5 М, и источник Са2+, обеспечивающий концентрацию Са2+ от примерно 50 мМ до примерно 6,0 М в водном растворе. В некоторых предпочтительных воплощениях источником Na+ является NaCl, и источником Са2+ является CaCl2.
В другом аспекте данное изобретение в общем относится к композиции, пригодной для приготовления фармацевтической композиции для лечения опухоли, содержащей Na+ и Са2+ в таких количествах, чтобы при добавлении к ним подходящего количества воды получить фармацевтическую композицию (насыщенный ионный раствор), содержащую примерно 5,0479 М Na+ и примерно 250 мМ Са2+, при комнатной температуре.
В еще одном аспекте данное изобретение в общем относится к способу лечения опухоли у пациента, включающему внутриопухолевую инъекцию или прямую инъекцию в опухолевое образование фармацевтически эффективного количества композиции, содержащей примерно 5,0479 М Na+ и примерно 250 мМ Са2+, при комнатной температуре.
Краткое описание графических материалов
На Фиг. 1 показана мышиная модель саркомы МСА207 у мыши C57BL6. Фиг. 1А. Опухоль до лечения размером 8 мм × 8 мм. Фиг. 1В. Стандартная процедура внутриопухолевой инъекции "лекарственной ионной бомбы" у мыши. Фиг. 1C. Мышиная саркома уничтожена однократной инъекцией 0,10 мл "лекарственной ионной бомбы".
На Фиг. 2 показана модель рака молочной железы человека MCF7 у бестимусной мыши. Фиг. 2А. Опухоль до лечения размером 13 мм × 13 мм, которая равна 3%± массы тела мыши. Фиг. 2В. Стандартная процедура внутриопухолевой инъекции "лекарственной ионной бомбы" у мыши. Фиг. 2С.
Модель большого рака молочной железы человека у бестимусной мыши была уничтожена однократной инъекцией 0,14 мл "лекарственной ионной бомбы".
Фиг. 3 объясняет использование флуоресцентного Са2+ зонда в определении ex vivo притока Са2+ из внеклеточной жидкости во внутриклеточную жидкость в клетках рака молочной железы человека MCF7. Фиг. 3А. Семь раковых клеток до обработки, меченных флуоресцентным Са2+ зондом. Фиг. 3В. Две из 7 раковых клеток уничтожены "лекарственной ионной бомбой" через 14± секунд после начала обработки. Фиг. 3С. Все 7 раковых клеток уничтожены через 18± секунд после начала обработки. Процедура измерения притока Na+ была такой же, как упомянуто выше, но с использованием флуоресцентного Na+ зонда.
На Фиг. 4 представлены фотоснимки видеоизображения из инвертированного микроскопа Nikon Diaphot. Фиг. 4А. Клетки рака молочной железы человека MCF7 до обработки. На Фиг. 4В обработанные раковые клетки подвергнуты вихреподобному вращению в среде для тканевой культуры через 5-7 секунд после добавления "лекарственной ионной бомбы". Фиг. 4С. Все раковые клетки уничтожены через 16±секунд после начала обработки. Клетки на этих 3 микроснимках были из одного и того же поля. Увеличение × 400.
На Фиг. 5 представлена группа микроснимков, изображающих патологические признаки in vivo мышиной саркомы МСА207, которую лечили "лекарственной ионной бомбой". Фиг. 5А. Белые линии, окружающие раковые клетки, представляют собой ионы натрия (соли) и ионы кальция (соли) в раковой ткани у мыши. Увеличение × 1000. Фиг, 5В. Подвергнутые обработке раковые ткани омертвели там, куда достигла "лекарственная ионная бомба". Увеличение × 400. Фиг. 5С. Множественные тромбозы в срезе обработанной опухоли. Увеличение × 400.
На Фиг. 6 представлена группа фотоснимков со сканирующего электронного микроскопа (SEM) моделей рака молочной железы человека MCF7 у бестимусных мышей. На SEM1 показаны контрольные раковые клетки. SEM2. Мембраны клеток рака молочной железы человека распались на кусочки и дебрис. На SEM3 показаны сильно поврежденные кровеносные сосуды опухоли, особенно повреждения наружного покрова артериол или венул в ткани опухоли. Многие сосуды опухоли разорваны в поперечном направлении.
На Фиг. 7 представлена группа снимков с трансмиссионного электронного микроскопа (ТЕМ) моделей рака молочной железы человека MCF7 у бестимусных мышей. На ТЕМ1 показаны контрольные раковые клетки. ТЕМ2 демонстрирует сильно поврежденную клеточную мембрану, ядро, митохондрию и цитоплазматические органеллы раковой клетки. ТЕМЗ демонстрирует полностью разрушенные внешний слой, средний слой и внутренний слой сосуда опухоли. Эндотелиальная клетка отошла от внутреннего слоя венулы. Увеличения × 5000.
На Фиг. 8 показан врач-клиницист, выполняющий внутриопухолевую инъекцию "лекарственной ионной бомбы" у пациента с большой опухолью. Фиг. 8А. Опухоль до лечения размером 40 мм × 60 мм в правом плече пациента. Фиг. 8В демонстрирует инъекцию под давлением 3 мл "лекарственной ионной бомбы" для уничтожения опухоли. ФИГ. 8С показывает, что отверстие иглы направлено вверх, а на Фиг. 8D отверстие иглы направлено вниз.
На Фиг. 9 показан случай 82-летней леди, страдающей огромной плоскоклеточной карциномой в нижней части спины в течение 3 лет. Фиг. 9.1. Карцинома до лечения размером 70 мм × 70 мм. Фиг. 9.2. Однократную внутриопухолевую инъекцию 26 мл раствора "лекарственной ионной бомбы" вводят в раковое образование. Фиг. 9.3. Аналог фотоснимка видеоизображения с телевизионной аппаратуры через 5 суток после лечения. Макроскопически, обработанное все раковое образование полностью уничтожено. Микроскопически, вся обработанная раковая ткань омертвела.
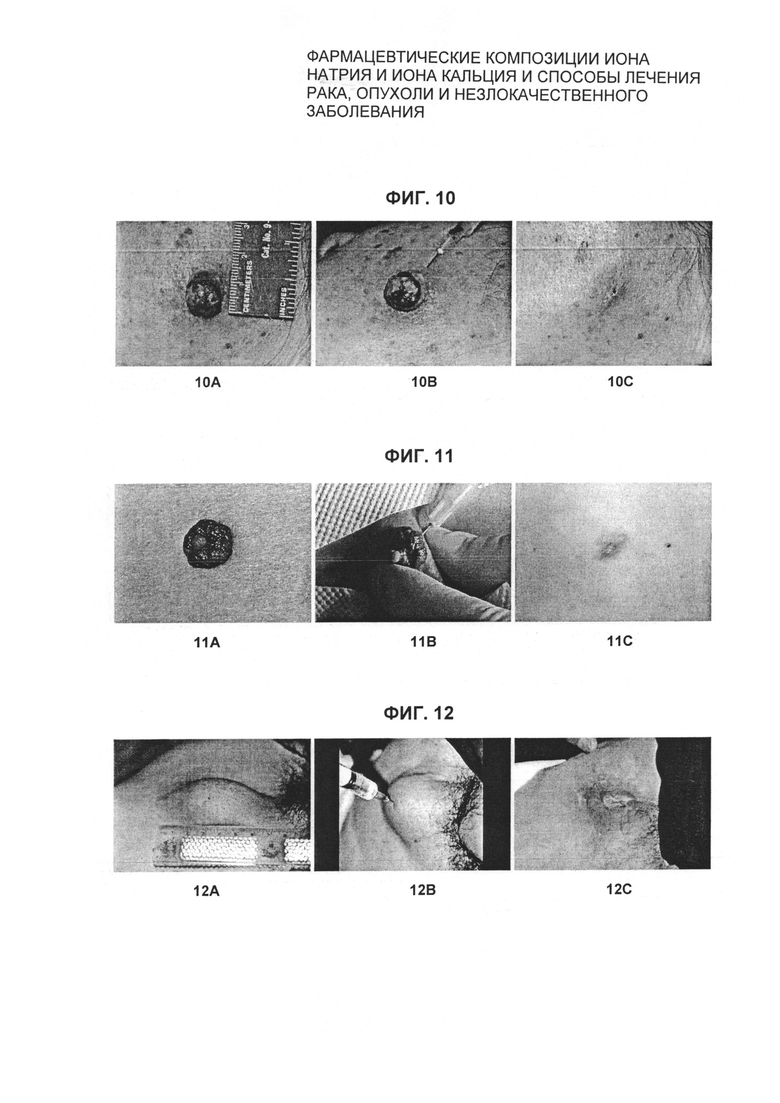
На Фиг. 10 показан случай 70-летней леди с плоскоклеточной карциномой в левой части лица. Фиг. 10А. Раковая опухоль до лечения размером 15 мм × 15 мм. Этот рак уничтожен одной однократной внутриопухолевой инъекцией 1,0 мл раствора "лекарственной ионной бомбы". Фиг. 10В. Стандартная процедура внутриопухолевой инъекции "лекарственной ионной бомбы" у пациента-человека. Фиг. 10С. Через семь суток после обработки опухоль подверглась коагулирующему некрозу и выглядела как обуглившаяся мертвая опухоль. Рана зажила без дефекта через 2 недели. При последующем обследовании через 3 года возврат рака не выявлен.
На Фиг. 11 показан случай 52-летней леди со злокачественной опухолью кожи. Эта опухоль является редко встречающейся опухолью, которая имеет вторую опухоль (опухоль-потомок, коричневая), растущую из ее родительской опухоли (черная). Фиг. 11А. Опухоль до лечения размером 20 мм × 20 мм. Фиг. 11 В. Стандартная процедура внутриопухолевой инъекции "лекарственной ионной бомбы" у пациента-человека. Фиг. 11С. Две опухоли уничтожены однократной внутриопухолевой инъекцией 0,5 мл "лекарственной ионной бомбы" через 3 суток, и рана зажила через 2 недели после лечения. Последующее обследование через 3 года показало отсутствие рецидива опухоли.
На Фиг. 12 показан случай 74-летнего мужчины, страдающего раком в левой паховой области, метастазирующим из пениса. Фиг. 12А. Раковая опухоль до лечения размером 50 мм × 70 мм. Фиг. 12 В. Раковое образование лечили одной однократной внутриопухолевой инъекцией 3,5 мл раствора "лекарственной ионной бомбы". Фиг. 12С. Большая раковая опухоль у пациента-человека была уничтожена за 4 суток, и рана зажила через 3 недели.
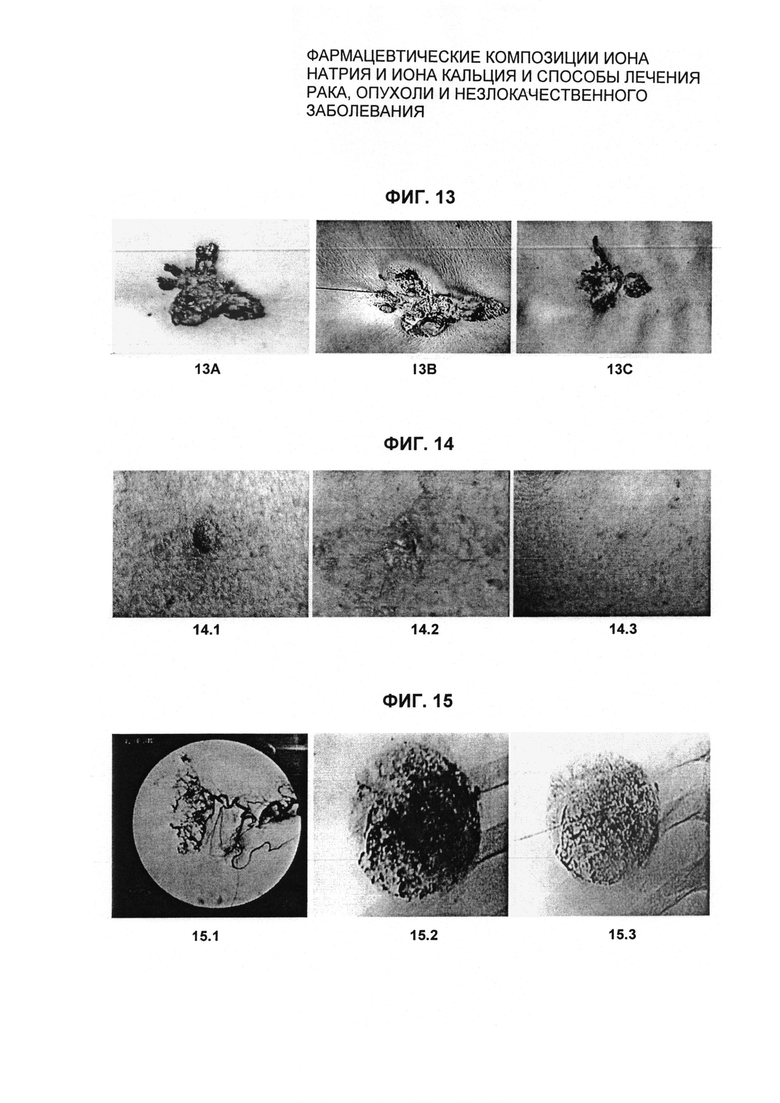
На Фиг. 13 показан случай 82-летнего мужчины, страдающего меланомой в передней части грудной клетки в течение 2 лет. Фиг. 13А. Типичная меланома в форме бабочки у пациента-человека до лечения. Фиг. 13 В. Аналог фотоснимка видеоизображения, демонстрирующий однократную внутриопухолевую инъекцию 1,2 мл "лекарственной ионной бомбы" с целью уничтожения этой меланомы. Фиг. 13С. Меланома была уничтожена за сутки, и рана зажила через 3 недели после лечения. Последующее обследование через 9 лет продемонстрировало отсутствие рецидива меланомы.
На Фиг. 14 показан 58-летний мужчина с базальноклеточной карциномой в передней части грудной клетки. Фиг. 14.1. Базальноклеточная карцинома до лечения размером 12 мм × 12 мм. Фиг. 14.2. Базальноклеточная карцинома регрессировала через одну неделю после однократной внутриопухолевой инъекции 0,5 мл "лекарственной ионной бомбы". Фиг. 14.3. Место регрессированной карциномы зажило через 3 недели после лечения. Последующее обследование через 8 лет показало отсутствие рецидива подвергнутой лечению базальноклеточной карциномы.
Фиг. 15. На Фиг. 15.1 представлено изображение, полученное в результате ангиографии через печеночную артерию, которое показывает наличие большой раковой опухоли в правой доле печени у 62-летнего мужчины. Фиг. 15.2. Изображение большой карциномы печени до лечения у того же пациента. Длинную иглу катетера помещали в центр этой большой раковой опухоли печени и инъецировали 20 мл раствора "лекарственной ионной бомбы". Фиг. 15.3. Размер раковой опухоли уменьшился в размерах с 67 мм × 67 мм × 80 мм до лечения до 45 мм × 45 мм × 60 мм после лечения через 7 суток после лечения.
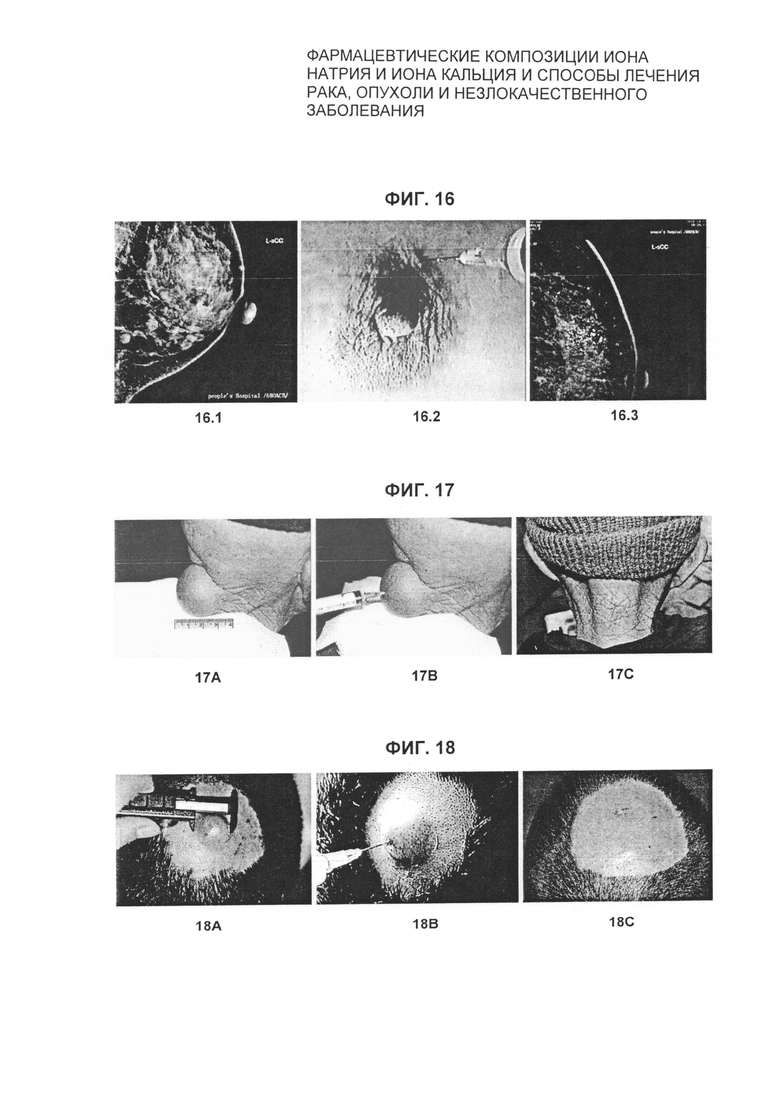
На Фиг. 16 показан случай леди с кистозно-фиброзным изменением молочной железы в группе клинического исследования автора изобретения. Фиг. 16.1. Изображение, полученное в результате маммографии до лечения, показывает большую кисту размером 40 мм × 40 мм, которая расположена позади левого соска, и несколько небольших фиброзно-кистозных образований, окружающих большую кисту. Фиг. 16.2. Слизеподобную жидкость внутри кисты откачивали, а затем большую кисту повторно промывали и откачивали. Затем выполняли однократную инъекцию внутрь кисты 3,5 мл "лекарственной ионной бомбы". Фиг. 16.3. Изображение, полученное в результате маммографии после лечения, показывает, что фиброзно-кистозное заболевание молочной железы вылечено через 3 месяца после лечения.
На Фиг. 17 показан случай 78-летнего мужчины с липомой. Эта опухоль находилась на задней стороне его шеи в течение 18 лет. Фиг. 17А. Опухоль до лечения размером 40 мм × 40 мм. Фиг. 17В. В опухоль однократной внутриопухолевой инъекцией вводили 2,0 мл "лекарственной ионной бомбы". Фиг. 17С. Эта большая опухоль была вылечена через 8 недель. Последующее обследование через 9 лет показало отсутствие рецидива подвергнутой лечению опухоли.
На Фиг. 18 показан случай пациента с атеромой. Фиг. 18А. Атерома в верхней части головы до лечения размером 18 мм × 18 мм. Фиг. 18В. Аналог фотоснимка видеоизображения, который демонстрирует однократную внутриопухолевую инъекцию 0,5 мл "лекарственной ионной бомбы". Фиг. 18С. Атерома была вылечена в 2001 году. Этот фотоснимок был сделан при проведении обследования через 9 лет.
На Фиг. 19 показан случай 66-летнего мужчины с большой атеромой размером 22 мм × 28 мм. Опухоль лечили однократной внутриопухолевой инъекцией 1,5 мл "лекарственной ионной бомбы" в 2001 году. Через 9 лет обследование показало отсутствие рецидива подвергнутой лечению опухоли.
На Фиг. 20 показано применение инъекции "лекарственной ионной бомбы" в косметическое образование. На Фиг. 20.1 показан кожный невус на лице пациента. Фиг. 20.2. Однократная инъекция в образование 0,2 мл "лекарственной ионной бомбы". Фиг. 20.3. Невус подвергся коагулирующему некрозу через 7 суток после лечения. Фиг. 20.4. Кожный невус удален без шрама.
Подробное описание изобретения
К созданию изобретения привела случайность. Ранее автор изобретения использовал внутриопухолевую инъекцию мышьяка в экспериментальном лечении опухолей у мышей, которая не дала хорошего результата. Однажды автор изобретения пошел за покупками в китайский супермаркет и купил дюжину соленых утиных яиц. По дороге домой он стал размышлять, почему эти соленые утиные яйца могут храниться при комнатной температуре в течение нескольких лет без гниения. Ответ в том, что белки и желтки в соленых утиных яйцах коагулируются или свертываются при высокой концентрации соли (хлорида натрия), в частности при высокой концентрации ионов натрия. Автор изобретения связал этот явление с биологией клетки, физиологией клетки, мембранным потенциалом, ионной наукой и лечением рака и предположил, что высокие концентрации хлорида натрия могут коагулировать или сворачивать белки в раковых клетках подобно тому, как это происходит в соленых утиных яйцах.
Была проведена серия экспериментов с использованием различных растворов с высокими концентрациями хлорида натрия, хлорида кальция и раствора "лекарственной ионной бомбы", содержащего ионы натрия и ионы кальция. Три животных модели опухолей, мышиной саркомы МСА207, мышиного колоректального рака МС38 и мышиной меланомы B16F1, были созданы у мышей C57BL6. Лечение внутриопухолевой инъекцией начинали, когда опухоль достигала размера 8 мм × 8 мм.
Тридцать шесть мышей C57BL6 с опухолями случайным образом были разделены на три группы согласно типам опухолей (12 животных в каждой группе). Затем животные в каждой группе дополнительно были разделены на 4 подгруппы (3 мыши с опухолями в каждой подгруппе). Животных с опухолями в подгруппе 1, в качестве контроля, лечили внутриопухолевой инъекцией 0,1 мл нормального физиологического раствора. Животных с опухолями в подгруппе 2 лечили внутриопухолевой инъекцией 0,1 мл раствора хлорида натрия в различных концентрациях. Животных с опухолями в подгруппе 3 лечили внутриопухолевой инъекцией 0,1 мл раствора хлорида кальция в различных концентрациях. Животных с опухолями в подгруппе 4 лечили раствором "лекарственной ионной бомбы".
Через двадцать четыре, 48 и 72 часа после лечения результаты экспериментов оценивали путем измерения размеров некротической области обработанных опухолей с использованием линейки. В контрольной группе не наблюдалось никакого некроза опухолей. Однако некроз происходил во всех опухолях, обработанных раствором хлорида натрия в высоких концентрациях, раствором хлорида кальция и раствором "лекарственной ионной бомбы". В репрезентативных примерах одна однократная внутриопухолевая инъекция 0,1 мл 5,0479 М раствора хлорида натрия вызывала в среднем 90% ±5 некроз всех обработанных опухолей через 48 часов после лечения. Одна однократная внутриопухолевая инъекция 0,1 мл 250 мМ, 1,0 М, 1,5 М, 2,0 М и 3,0 М растворов хлорида кальция вызывала коагулирующий некроз всех обработанных опухолей через 48 часов после лечения. Одна однократная внутриопухолевая инъекция 0,1 мл раствора "лекарственной ионной бомбы" приводила к 100%-ному некрозу всех обработанных опухолей через 48 часов после лечения.
Автор изобретения также изучал терапевтический эффект "лекарственной ионной бомбы" на 3 моделях рака человека у бестимусных мышей, включая глиобластому человека U87, рак молочной железы человека MCF7 и рак предстательной железы человека РСЗ. Количество бестимусных мышей, группирование животных и все экспериментальные методы и инъекционные дозы в каждой подгруппе были такими же, как в моделях мышиной опухоли C57BL6. Данные показали, что однократная внутриопухолевая инъекция 0,1 мл "лекарственной ионной бомбы" успешно уничтожала опухоль в каждой модели всех 3 типов рака человека у бестимусных мышей.
Внутриопухолевая инъекция "лекарственная ионной бомбы" была успешно применена в лечении 78 пациентов-людей с опухолями, включая 6 типов злокачественных опухолей или карциномы (базальноклеточная карцинома, плоскоклеточная карцинома, максиллярная карцинома, меланома, карцинома, метастазирующая из рака пениса и печени) и 10 типов доброкачественных опухолей (атерома, липома, новообразование, киста, кистозно-фиброзное изменение молочной железы, лимфаденопатия, узел щитовидной железы, генитальная опухоль, кожный невус и косметические образования). "Лекарственная ионная бомба" содержит два активных компонента Na+ и Са2+ или два активных соединения хлорид натрия и хлорид кальция. В предпочтительном воплощении "лекарственная ионная бомба" содержит 5,0479 М хлорида натрия и 250 мМ хлорида кальция в стерильной дистиллированной воде.
В предпочтительном воплощении путь введения "лекарственной ионной бомбы" представляет собой путь посредством внутриопухолевой инъекции (например прямой инъекции) "лекарственной ионной бомбы" в опухоль или рак у субъекта.
При использовании только ионов натрия (например NaCl) для внутриопухолевой инъекции эффективная лечебная концентрация Na+ составляет от примерно 2,0 М до примерно 5,4414 М при комнатной температуре. При использовании только ионов кальция (например CaCl2 для внутриопухолевой инъекции эффективная лечебная концентрация Са2+ составляет от примерно 50 мМ до 6,0 М при комнатной температуре.
Отмечается, что источник Na4+ не ограничивается NaCl, и источник Са2+ не ограничивается CaCl2. Другие примеры источников Na+ включают неорганические или органические соли, например бикарбонат натрия, карбонат натрия и хлорат натрия и др. Другие источники Са2+ включают неорганические или органические соли, например глюконат кальция, карбонат кальция и ацетат кальция и др.
Имеется несколько отличий композиций "лекарственной ионной бомбы", описанных в данном документе, от двух композиций, о которых сообщалось ранее, в которых использован единственный компонент хлорид натрия. (1) Данное изобретение предусматривает использование в лечении рака ионов Na+ и Са2+. Однако в предшествующих сообщениях описано использование гипертонического физиологического раствора. (2) Композиции "лекарственной ионной бомбы" содержат вплоть до пяти компонентов в конкретных количествах. Автор изобретения обнаружил, что когда Na+ и Са2+ объединены в фармацевтической композиции, тогда новая "лекарственная ионная бомба" оказывает уничтожающие рак синергетический эффект, комплементарный эффект и эффект двойной волны. (3) В данном изобретении ион кальция использован в качестве "усилителя" лечения рака, поскольку ион кальция является одним из вторичных мессенджеров в биологии клеточной сигнальной трансдукции. Ионы кальция также вовлечены в метаболизм многих ферментов, активируя протеинкиназу С и способствуя активации другого вторичного мессенджера сАМР. Ионы кальция осуществляют регуляцию белка кальмодулина с образованием альфа спиральной структуры. Следовательно, небольшое увеличение количества ионов кальция во внутриклеточной жидкости вызывает огромные патофизиологические изменения во внутренней среде клеток и большие биологические трансформации в молекулярных регуляциях клеток, которые вызывают либо болезнь, либо апоптоз, либо гибель обработанных раковых клеток. (4) Концентрации ионов в "лекарственной ионной бомбе", раскрытой здесь, основаны на большом количестве экспериментальных данных. (5) В данном изобретении механизмы воздействия высокой концентрации Na+ и Са2+ с целью уничтожения раковых клеток были проверены, основываясь на аспектах физиологии клетки, молекулярной биологии, биологии клеточной мембраны, мембранного потенциала, ионных каналов, патологии, сканирующей электронной микроскопии (SEM) и трансмиссионной электронной микроскопии (ТЕМ). (6) Данное изобретение впервые выдвинуло показания внутриопухолевой инъекции "лекарственной ионной бомбы", и точно направленная внутриопухолевая инъекция "лекарственной ионной бомбы" показана для лечения рака, злокачественной опухоли, доброкачественной опухоли и незлокачественного заболевания примерно в девяти органах человека (карциномы и опухоли кожи и подкожной ткани, молочной железы, предстательной железы, щитовидной железы, легкого, печени, генитальных органов, головного мозга и поджелудочной железы) и четырех категорий доброкачественных заболеваний (кожных и подкожных новообразований, кистозно-фиброзных изменений молочной железы, доброкачественной гиперплазии предстательной железы и узлов щитовидной железы). (7) Предпочтительным путем введения "лекарственной ионной бомбы" является внутриопухолевая инъекция или прямая инъекция "лекарственной ионной бомбы" в раковое образование или опухоль. (8) Впервые предложено использовать идею и определение точно направленной внутриопухолевой инъекции "лекарственной ионной бомбы" в лечении рака и других, доброкачественных заболеваний под контролем СТ сканирования или ультразвуковой визуализации. (9) Концентрация Na+ в предпочтительном растворе "лекарственной ионной бомбы" отличается от концентрации, указанной в двух предшествующих сообщениях (например, композиция по заявленному изобретению содержит 5,0479 М Na+ (NaCl) и 250 мМ Са2+ (CaCl2) в стерильной дистиллированной воде с получением насыщенного ионного раствора. (10) Изобретение внутриопухолевой инъекции "лекарственной ионной бомбы" успешно использовано в лечении 78 пациентов-людей, страдающих 6 типами рака и 10 типами доброкачественных опухолей и незлокачественных заболеваний. Следовательно, клиническое применение изобретения в лечении типов заболеваний отличается от опубликованных ранее сведений.
Использованный в данном описании термин "доброкачественная опухоль" относится ко всем единичным или множественным солидным опухолям или новообразованиям в патологической классификации, включая, без ограничения, аденому, ангиому, атерому, фиброму, липому, тератому, тирому, кисту, полип, кожный невус, нарост и бородавку и другие состояния с новообразованиями у пациентов-людей.
Использованный в данном описании термин "злокачественная опухоль" относится ко всем единичным или множественным солидным злокачественным образованиям в патологической классификации, включая, без ограничения, рак, карциному, лимфому, меланому, миелому, саркому, опухоли головного мозга и другие злокачественные опухоли у пациентов-людей.
Физиология клетки в разработке "лекарственной ионной бомбы"
В физиологии клетки жизнеспособность нормальных клеток, опухолевых клеток или раковых клеток зависит от равновесия осмотического давления внутри и вне клеток. Нормальное осмотическое давление в клетках зависит от равновесия концентраций ионов между внеклеточной и внутриклеточной жидкостями. Физиологически Na+, K+ и Са2+ играют важную роль в поддержании жизнеспособности клеток. Когда концентрации ионов во внеклеточной и внутриклеточной жидкостях идентичны, тогда такое состояние называется изотоническим. Поскольку клетка находится в равновесии, градиент ионной концентрации отсутствует, и приток воды равен оттоку воды. Это не приводи к заболеванию или гибели клетки. Когда клетка имеет более высокую ионную концентрацию внутри клетки, чем снаружи, тогда это состояние называется гипертоническим. Это состояние характеризуется результирующим притоком воды в клетку. Когда клетка имеет более низкую ионную концентрацию внутри клетки, чем снаружи, тогда она гипотоническая, то есть вода вытекает из клетки (Costanzo LS, 2010 Costanzo Physiology, 4th edition, Saunders, Philadelphia).
He предполагая ограничения этого принципа, считается, что значительное изменение концентраций Na+ и Са2+ между внеклеточной и внутриклеточной жидкостями вызывает огромные трансформации в физиологии клеток, которые приводят к заболеванию, апоптозу или гибели клеток. "Лекарственная ионная бомба" умышленно разработана для того, чтобы иметь высокие концентрации Na+ и Са2+, которые уничтожают раковые клеточные линии в культуре ткани, моделях рака на животных и больших карцином у пациентов-людей.
Одна стратегия заключается в том, чтобы доставлять высокие концентрации Na+ и Са2+ во внеклеточную жидкость или во внутриопухолевую ткань, где оба иона могут быстро проходить через мембраны клеток во внутриклеточную жидкость.
Во-первых, была протестирована потенциальная роль Na+, K+, Са2+ и Mg2+ в лечении опухоли и рака. Были выполнены эксперименты in vivo на мышах BALB/c. Растворы с высокими концентрациями Na+, K+, Са2+ и Mg2+ инъецировали внутримышечно. Однако растворы с высокими концентрациями К+ и Mg2+ токсичны и вызывали паралич ног, недостаточность сердечнососудистой системы и дыхательной системы и гибель животных. Эксперименты фокусировались на растворах с высокими концентрациями Na+ и Са2+.
Готовили растворы с разными концентрациями хлорида натрия, и тестирование начинали с 1,0 М, затем 1,5 М, 1,711 М, 3,0 М, 4,28 М, 4,449 М, 5,0479 М, 5,133 М и 5,4414 М. Готовили растворы с разными концентрациями хлорида кальция, и тестирование начинали с 25 мМ, затем 50 мМ, 100 мМ, 150 мМ, 200 мМ, 250 мМ, 300 мМ, 400 мМ, 500 мМ, 901 мМ и 1,0 М, 1,5 М, 2,0 М, 3,0 М, 4,0 М, 5,0 М, 5,5 М и 6,0 М.
После сравнительных исследований было установлено, что композиция предпочтительной "лекарственной ионной бомбы" содержит 5,0479 М Na+ и 250 мМ Са2+ в примерно 890 мл в стерильной воде и представляет собой насыщенный ионный раствор комбинации Na+ и Са2+ при комнатной температуре.
Существует по меньшей мере три логических обоснования для выбора Na+, который является первым активным компонентом "лекарственной ионной бомбы". (1) Na+ является важным и безопасным ионом, и его концентрация в организме очень гибкая. Медицинские растворы хлорида натрия давно применяются для внутривенной инфузии пациентам-людям. Не существует доказательств, свидетельствующих о том, что Na+ является токсичным или мутагенными агентом, когда его используют в надлежащих концентрациях. (2) Na+ имеет уникальное свойство быстрой диффузии в живую ткань и ткань опухоли. Как показано под контролем рентгеновской визуализации в реальном времени в этом изобретении, диффузия 5,0479 М раствора хлорида натрия приблизительно в 25 раз быстрее, чем 1,0 М и 2,0 М раствора хлорида кальция, в модели рака у бестимусных мышей. (3) Как указано, высококонцентрированные растворы хлорида натрия способны уничтожать множество типов опухолей животных у мышей C57BL6 и моделей рака человека у бестимусных мышей.
В этом исследовании Са2+ используют в качестве второго активного компонента "лекарственной ионной бомбы". Са2+ является одним из вторичных мессенджеров в биологии клеточной сигнальной трансдукции и его внутриклеточная концентрация составляет менее 0,0001 мМ. Исследователи подтвердили, что среда для культуры ткани, содержащая 250 мМ Са2+, индуцировала заболевание, апоптоз и гибель 18 типов раковых клеточных линий человека. Флуоресцентная микроскопия с использованием флуоресцентного Са2+ зонда продемонстрировала, что 250 мМ, 1,0 М, 1,5 М, 2,0 М и 3,0 М растворы Са2+ вызывали немедленную болезнь или гибель раковых клеток.
Тест ex vivo на цитотоксическую активность "лекарственной ионной бомбы"
Были протестированы растворы с различными концентрациями Na+ и Са2+ и предпочтительный раствор "лекарственной ионной бомбы". Опухолевые клетки выращивали в среде DMEM или RPMI1640, дополненной 10% сыворотки плода коровы (FCS). Среда в контрольной группе не содержала раствор "лекарственной ионной бомбы". Раствор "лекарственной ионной бомбы" добавляли во всех 18 экспериментальных группах рака. Гибель раковых клеток оценивали по результатам теста с вытеснением красителя трипанового синего или проточной цитометрии. Данные показали, что "лекарственная ионная бомба" уничтожала все 18 типов человеческих раковых клеточных линий в тканевой культуре через 3-30 минут, включая линии клеток рака легкого человека А549, рака щитовидной железы человека ARO, рака предстательной железы человека CWR-22, рака шейки матки человека HeLa, лейкоза человека HL60, колоректального рака человека НТ-29, Т-клеточного лейкоза человека Jurkat, лейкоза человека К562, лимфомы человека М2, меланомы человека М24, рака молочной железы человека MCF7, аденокарциномы молочной железы человека MDA-MB-231, рака яичника человека OVCAR3, рака предстательной железы человека РС3, рака почки человека SK-RC-52, эпителиальной опухоли молочной железы человека T-47D, рака предстательной железы человека LNCap и глиобластомы человека U87.
Минимальная и максимальная эффективные терапевтические концентрации Na+ и Са2+
Терапевтический эффект in vivo "лекарственной ионной бомбы" тестировали в 3 мышиных моделях опухолей. Высококонцентрированный раствор хлорида натрия, высококонцентрированный раствор хлорида кальция и предпочтительный раствор "лекарственной ионной бомбы" инъецировали в мышиную саркому МСА207, мышиный колоректальный рак МС38 и мышиную меланому B16F1 у мышей C57BL6. Данные показали, что при использовании только раствора Na+ для внутриопухолевой инъекции его минимальная эффективная терапевтическая концентрация составляет 2,0 М при комнатной температуре. 3 М концентрация раствора Na+ вызывала в среднем 30% ±10 некроз всех обработанных опухолей через 48 часов. Одна однократная внутриопухолевая инъекция 5,0479 М раствора Na+ вызывала в среднем 90% ±5 некроз всех обработанных опухолей через 48 часов. Максимальная эффективная терапевтическая концентрация Na+ (например хлорида натрия) раствор составляла 5,4414 М при комнатной температуре, которая вызывала в среднем 92% ±5 некроз всех обработанных опухолей через 48 часов. Для внутриопухолевой инъекции или прямой инъекции в опухоль минимальная эффективная терапевтическая концентрация Са2+ (например хлорида кальция) раствора составляла 50 мМ при комнатной температуре, и максимальная эффективная терапевтическая концентрация составляла 6,0 М при комнатной температуре, когда его использовали один для внутриопухолевой инъекции. Однако высококонцентрированный раствор хлорида кальция является токсичным и является причиной незаживающей раны в месте инъекции.
Диффузия "лекарственной ионной бомбы" в ткани опухоли
Эксперименты по диффузии ex vivo выполняли на свежей говяжьей печени при комнатной температуре. Тридцать частей раствора "лекарственной ионной бомбы" смешивали с одной частью черной туши (India ink). Смешанный раствор "лекарственной ионной бомбы" инъецировали в говяжью печень, начиная с 1,0 мл, затем 2,0 мл и 3,0 мл. Через шестьдесят минут после инъекции говяжьи печени разрезали, и размеры областей диффузии измеряли линейкой.
Эксперименты по диффузии in vivo проводили на мышах под контролем рентгеновской визуализации. Девяносто девять мл раствора "лекарственной ионной бомбы" смешивали с одним мл рентгеноконтрастного усилителя Ultravist 370, и 0,12 мл смешанного раствора "лекарственной ионной бомбы" инъецировали в человеческую модель рака у бестимусной мыши. Как правило, мышиная опухоль или человеческая модель рака размером от 8 мм × 8 мм до 10 мм × 10 мм полностью заполнялась 0,12 мл смешанного раствора "лекарственной ионной бомбы" через 3-5 минут. Данные продемонстрировали, что по времени и скорости диффузия 5,0479 М раствора хлорида натрия была приблизительно в 25 раз быстрее, чем диффузия 1,0 М и 2,0 М раствора хлорида кальция, в ткани опухоли у живой мыши.
Полученные данные по разному времени диффузии, разной скорости диффузии и разному объему диффузии растворов Na+ и Ca2+ побудили автора изобретения к созданию композиции "лекарственной ионной бомбы". Ключевым замыслом данного изобретения является разработка мощной "лекарственной ионной бомбы" для лечения рака, злокачественной опухоли, доброкачественной опухоли и незлокачественного заболевания комбинацией Na+ и Ca2+. Поскольку диффузия Na+ быстрая, а диффузия Са2+ медленная в ткани опухоли, и поскольку оба типа ионов способны уничтожать рак, когда их используют по отдельности, было выдвинуто предположение, что комбинация Na+ и Ca2+ в композиции "лекарственной ионной бомбы" будет оказывать синергетический эффект, комплементарный эффект и эффект двойной волны в уничтожении рака. Первая волна уничтожающего рак эффекта in vivo (раннее цитотоксическое действие) опосредована Na+, и она происходит через 1-12 часов после лечения. Вторая волна уничтожающего рак действия in vivo (поздний цитотоксический эффект) опосредована Ca2+, и она происходит через 6-24 часов после лечения. Эта гипотеза теперь доказана полученными данными, раскрытыми в данном описании.
Взаимосвязь между притоком Na+-Ca2+ и гибелью раковых клеток
Для выяснения взаимосвязи между притоком Na+ и Са2+ из внеклеточной жидкости во внутриклеточную жидкость и гибелью раковых клеток использовали три метода отслеживания ионных каналов. Метод локальной фиксации потенциала (пэтч-кламп) широко используется для измерения мембранного потенциала кардиомиоцитов. Здесь метод пэтч-кламп использовали, чтобы продемонстрировать взаимосвязь между изменениями мембранного потенциала и гибелью мышиных кардиомиоцитов. Нормальные мышиные кардиомиоциты предварительно культивировали в пэтч-кламп камере, и мембранные потенциалы измеряли до и после добавления раствора "лекарственной ионной бомбы". Мембранный потенциал мышиных кардиомиоцитов регистрировали автоматически. При добавлении 5% и 10% среды "лекарственной ионной бомбы" в пэтч-кламп камере мышиные кардиомиоциты погибали через 5 и 3 минуты соответственно. При добавлении 100% раствора "лекарственной ионной бомбы" в пэтч-кламп камеру мышиные кардиомиоциты погибали через двенадцать секунд. Данные показали, что цитотоксическое действие "лекарственной ионной бомбы" является дозо- и время-зависимым.
Метод с использованием флуоресцентного ионного зонда использовали в исследовании притока Na+ и Са2+ из внеклеточной жидкости во внутриклеточную жидкость раковых клеток. Флуоресценцию и время притока Na+ или Са2+ зонда в раковые клетки регистрировали в реальном времени до и после добавления раствора "лекарственной ионной бомбы" в клеточную камеру. Если раковая клетка погибла, флуоресцентное изображение раковой клетки, меченой Na+ или Са2+ зондом, исчезает с экрана компьютера, что указывает на то, что либо мембрана раковой клетки разрушена, либо вся раковая клетка убита. Видеоданные с использованием флуоресцентного Na+ зонда показали, что при использовании 5,0479 М раствора Na+ одного для уничтожения клеток рака молочной железы человека MCF7 требовалось 20±4 секунд. При использовании предпочтительного раствора "лекарственной ионной бомбы" для уничтожения того же типа раковых клеток требовалось только 18±4 секунд, что свидетельствует о том, что Са2+ оказывает усиливающий эффект в лечении рака, и что композиция комбинации Na+ и Са2+ оказывает синергетический и комплементарный эффект в уничтожении рака.
Инвертированный микроскоп Nikon Diaphot является системой визуализации в реальной времени для исследования живых клеток. Он оснащен видеоаппаратурой и фотоаппаратом. Видеоданные выявили 5 патологических фаз уничтожения раковых клеток "лекарственной ионной бомбой": (1) быстрый разрыв клеточной мембраны раковых клеток; (2) резкая дегидратация раковых клеток из-за высоких концентраций Na+ и Са2+ во внеклеточной жидкости после добавления "лекарственной ионной бомбы"; (3) набухание раковых клеток вследствие притока большого количества Na+ и Са2+ из внеклеточной жидкости во внутриклеточную жидкость; (4) уничтожение раковых клеток, вызванное чрезмерным набуханием раковых клеток; и (5) немедленная гибель раковых клеток. Весь процесс 5 патологических повреждений раковых клеток происходил за двенадцать секунд, и каждая патологическая фаза происходила только за 3-4 секунды.
В физиологических условиях концентрация Na+ во внеклеточной жидкости составляет 140 мМ, а во внутриклеточной жидкости 14 мМ. Поскольку предпочтительный раствор "лекарственной ионной бомбы" имеет концентрацию Na+ 5,0479 М, концентрация Na+ во внеклеточной жидкости раковых клеток в 36 раз выше нормального уровня, а концентрация Na+ во внутриклеточной жидкости примерно в 360 раз выше нормальной концентрации. В результате, раковые клетки уничтожатся за двенадцать секунд благодаря чрезвычайно высокой концентрации Na+ в "лекарственной ионной бомбе".
С другой стороны, нормальная концентрация Са2+ во внеклеточной жидкости составляет 2,5 мМ, а во внутриклеточной жидкости 0,0001 мМ в клетках млекопитающего. "Лекарственная ионная бомба" содержит 250 мМ Са2+, т.е. в концентрации в 100 раз выше физиологического уровня во внеклеточной жидкости и приблизительно в 2,5 миллиона раз выше физиологической концентрации во внутриклеточной жидкости. Поскольку Са2+ является одним из вторичных мессенджеров в биологии клеточной сигнальной трансдукции, высокая концентрация Са2+ во внутриклеточной жидкости не только вызывает огромные физиологические повреждения, но и вызывает также огромные биологические повреждения раковых клеток. Следовательно, высокая концентрация Са2+ в "лекарственной ионной бомбе" является уничтожающим рак усилителем и может ускорять гибель раковых клеток. Патологические и ультраструктурные исследования Через двадцать четыре часа после лечения "лекарственной ионной бомбой" образцы для микроскопии, SEM и ТЕМ брали у бестимусной мыши, несущей рак молочной железы человека MCF7, или пациентов, чей рак лечили "лекарственной ионной бомбой." Микроскопические препараты для изучения патологии окрашивали гематоксилином и эозином, и образцы для SEM и ТЕМ готовили согласно соответствующим инструкциям.
Репрезентативные патологические признаки рака человека, который лечили "лекарственной ионной бомбой", включают (1) ионы натрия (соли) и ионы кальция (соли), проникшие в окружающую ткань раковых клеток; (2) некроз опухолевых тканей и раковых клеток, куда достигал раствор "лекарственной ионной бомбы", свидетельствующий о том, что полное заполнение опухоли раствором "лекарственной ионной бомбы" является необходимым условием уничтожения или излечения рака; (3) тромбозы в кровеносных сосудах опухоли; и (4) сильное кровотечение в некротических участках в результате повреждения сосудистой сети опухоли.
SEM продемонстрировала, что модели рака молочной железы человека, обработанные "лекарственной ионной бомбой", показали разрушенные мембраны раковых клеток с бесчисленными микроответствиями. Мембраны раковых клеток распались на куски или дебрис. Ткани внешнего слоя кровеносных сосудов опухоли оторвались. Видны поперечные разрывы атериол или венул в опухолевой ткани. ТЕМ показала деструктивные клеточные мембраны, митохондрию, лизосому и ядро раковых клеток. Эндотелиальные клетки во внутренней выстилке сосудов опухоли отщепились от сосудистого русла. Большинство раковых клеток были разорваны на несколько частей, и интерстициальная ткань подвергнутого лечению рака была раскрошена. Все эти патологические и ультраструктурные признаки подвергнутых лечению мышиных опухолей и моделей рака выглядели как место после ядерной бомбардировки.
Применение "лекарственной ионной бомбы" у пациентов-людей
Из 78 пациентов-людей 11 пациентов страдали злокачественными опухолями или раком, включая 2 случая базальноклеточной карциномы кожи, 3 случая плоскоклеточной карциномы кожи, 2 случая меланомы, 1 случай максиллярной аденокарциномы, 1 случай рака, метастазирующего из пениса, и 2 случая рака печени. За исключением одного пациента с максиллярной карциномой в последней стадии, который умер через 3 месяца после лечения, остальные 10 раковых пациентов успешно прошли лечение одной однократной внутриопухолевой инъекцией "лекарственной ионной бомбы." Остальные 67 пациентов с 10 типами доброкачественных опухолей и незлокачественных заболеваний (1 случай генитального новообразования, 1 случай узла щитовидной железы, 2 случая лимфаденопатии, 3 случая кожного невуса, 4 случая кисты, 4 случая кистозно-фиброзного изменения молочной железы, 6 случаев косметических состояний, 10 случаев новообразования, 15 случаев атеромы и 21 случаев липомы) успешно прошли лечение.
Когда доброкачественная опухоль или раковое состояние локализовано на поверхности тела или в подкожной ткани, тогда опухоль можно лечить под визуальным контролем и без анестезии. Пациента укладывают на процедурный стол. После обеззараживания участка опухоли 70%-ным спиртом иглу 19 размера вводят в центр опухоли. Опухоль или раковое образование лечат внутриопухолевой инъекцией предпочтительного раствора "лекарственной ионной бомбы". Особое предостережение: нельзя протыкать противоположную сторону капсулы опухоли. Надлежащее нагнетание при инъекции поддерживают в течение 3-5 минут, чтобы вся опухоль была полностью заполнена раствором "лекарственной ионной бомбы". Как правило, пациент спокойно переносит лечение. Последующие обследования выполняют через 7, 14, 21 и 28 суток после лечения.
Если злокачественная опухоль или раковое образование локализована(о) в глубокой ткани организма, например опухоль головного мозга или рак поджелудочной железы, применяют общую анестезию. Точно направленную внутриопухолевую инъекцию предпочтительной "лекарственной ионной бомбы" выполняют под контролем СТ, чтобы контролировать, заполнена ли полностью вся опухоль "лекарственной ионной бомбой", смешанной с Ultravist 370. После лечения пациента госпитализируют на несколько суток, и последующие обследования проводят через 7, 14, 21 и 28 суток путем СТ-сканирования для определения, сократилось ли в размерах или полностью уничтожено обработанное раковое образование.
Для внутриопухолевой инъекции используют иглы размера от 19 до 26, и экстрадлинные иглы используют для опухолей, локализованных в глубокой ткани, в зависимости от размера и локализации опухоли. Иглы и экстрадлинные иглы могут быть изогнуты под углом для достижения опухоли или ракового образования, если хирургический доступ невозможен или раковое состояние является неоперабельным.
Уникальное преимущество данного изобретения заключается в том, что внутриопухолевая инъекция "лекарственной ионной бомбы" может быть использована в качестве терапии первой линии у раковых пациентов, которых можно излечить или эффективно лечить без необходимости проведения хирургического вмешательства, химиотерапии и/или радиотерапии. С другой стороны, предложенный способ лечения можно комбинировать с хирургическим вмешательством, химиотерапией, радиотерапией, иммунотерапией, биотерапией и другими терапиями рака для повышения терапевтического результата лечения рака.
Фармацевтические композиции Na+ и Са2+ и способы, раскрытые в данном документе, можно назначать раковым пациентам для уничтожения ракового образования in situ перед хирургическим вмешательством. Затем "мертвый рак" безопасно удаляют хирургической операцией. Преимущества этой стратегии заключаются в снижении риска распространения ятрогенных раковых метастазов или неоперабельной раковой ткани в результате хирургической операции и, соответственно, в увеличении выживаемости пациентов и излечиваемости опухолей.
Считается, что фармацевтические композиции Na+ и Са2+ по изобретению при надлежащем введении, как раскрыто в данном документе, не вызывают побочных эффектов, таких как воспаление, развитие гипертермии, канцерогенез и мутагенез.
Фармацевтические композиции Na+ и Са2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих кожными и подкожными видами рака и злокачественными опухолями, включая, без ограничения, базальноклеточную карциному, меланому, саркому, рак кожи и другие злокачественные состояния кожи. Их можно также применять в качестве терапии первой линии у пациентов, страдающих кожными и подкожными доброкачественными опухолями, включая, без ограничения, аденому, атерому, гемангиому, липому, кожный невус, нарост и бородавку, а также другие новообразования.
Фармацевтические композиции Na+ и Са2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих опухолями головного мозга, включая, без ограничения, глиому, аденому и другие опухоли головного мозга. У выбранных пациентов с опухолями головного мозга фармацевтические композиции и способы лечения по данному изобретению дают пациентам шанс возможного излечения, не подвергая их высокорискованной хирургической операции на головном мозге по удалению опухоли головного мозга. Пациенты с глиомой и другими типами опухолей головного мозга подвергаются только незначительной хирургической операции, при которой делают небольшое отверстие в черепной кости для введения иглы в опухоль головного мозга под контролем СТ-сканирования. Этот способ лечения может значительно снизить смертность пациентов и увеличить выживаемость и излечимость опухоли.
Фармацевтические композиции Na+ и Са2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих раком щитовидной железы. Такие пациенты могут избежать высокорискованного хирургического вмешательства или изотопной радиотерапии. Это лечение может защитить пациента от повреждения паращитовидных желез в результате хирургической операции. Кроме того, оно может быть использовано в качестве превентивного лечения рака у пациентов, которым планировалось проведение общей тиреоидэктомии или промежуточной тиреоидэктомии. Например, перед хирургической операцией рак щитовидной железы может быть уничтожен in situ посредством внутриопухолевой инъекции "лекарственной ионной бомбы", а затем "мертвый рак щитовидной железы" безопасно может быть удален хирургическим путем. Эта стратегия защищает пациента от ятрогенного метастазирования или распространения неоперабельной раковой ткани и увеличивает выживаемость и излечимость опухоли.
Фармацевтические композиции Na+ и Са2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих доброкачественными опухолями щитовидной железы, включая, например, аденому, тирому, кисту и узлы в щитовидной железе.
Фармацевтические композиции Na+ и Са2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих первичным или рекуррентным гипертиреозом, и пациенты могут избежать высокорискованной изотопной радиотерапии и хирургического вмешательства. Перед лечением пациент принимает йод через рот. Когда доли щитовидной железы пациента станут маленькими, выполняют инъекцию в щитовидную железу "лекарственной ионной бомбы" в обе доли щитоводной железы. Пациента лечат просто путем инъекции в продольном направлении в каждую долю щитовидной железы под контролем ультразвуковой визуализации или СТ-сканирования. Механизм использования "лекарственной ионной бомбы" в лечении гипертиреоза состоит в сокращении количества клеток, продуцирующих тиреоидные гормоны, как и в результате хирургического вмешательства и изотопной радиотерапии.
Фармацевтические композиции Na+ и Са2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих раком молочной железы. У выбранных пациентов, страдающих раком молочной железы, данное изобретение обеспечивает возможное излечение без хирургического вмешательства. Такие пациенты могут избежать деструктивного хирургического вмешательства. Внутриопухолевую инъекцию "лекарственной ионной бомбы" в данном изобретении можно также использовать в качестве превентивного лечения рака у пациентов, страдающих первичным раком молочной железы, при котором, как считается, требуется удаление опухоли молочной железы или мастэктомия или радикальная мастэктомия. За два-три дня до хирургической операции рак молочной железы пациента уничтожают in situ посредством внутриопухолевой инъекции "лекарственной ионной бомбы," затем "мертвый рак молочной железы" безопасно удаляют хирургической операцией. Важно то, что это может защитить пациента от ятрогенного метастазирования в результате хирургического вмешательства и увеличить выживаемость пациента и излечимость рака. Пациента укладывают на процедурный стол и дают ему местную анестезию. Девяносто девять мл раствора "лекарственной ионной бомбы" смешивают с одним мл среды Ultravist 370, и затем смешанный раствор "лекарственной ионной бомбы" инъецируют прямо в раковое образование молочной железы под контролем СТ-сканирования или ультразвуковой визуализации.
Фармацевтические композиции Na+ и Са2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих доброкачественными заболеваниями молочной железы, включая, без ограничения, аденому, фиброму, фиброзно-кистозное изменение и гиперплазию молочной железы.
Фармацевтические композиции Na+ и Ca2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих первичным раком предстательной железы. У выбранных пациентов, страдающих раком предстательной железы, данное изобретение обеспечивает возможное излечение без традиционной гормонотерапии, брахитерапии, хирургического вмешательства или химиотерапии, которые имеют серьезные последствия, особенно эректильную дисфункцию и рецидив рака. Нормальная предстательная железа весит примерно от 17 граммов до 25 граммов. Точно направленная инъекция в предстательную железу "лекарственной ионной бомбы" является минимально инвазивным способом лечения, который не вызывает вышеуказанные осложнения или побочные эффекты. Пациентов можно безопасно лечить посредством трансуретральной инъекции под контролем СТ-сканирования, ультразвука или цистоскопа. Опираясь на клинический опыт в лечении других раковых состояний у пациентов-людей, необходимо лишь примерно от 1,0 мл до 2,0 мл раствора "лекарственной ионной бомбы", чтобы уничтожить раковое образование предстательной железы у пациента-человека.
Фармацевтические композиции Na+ и Ca2+ и способы лечения по изобретению особенно показаны для пациентов, страдающих доброкачественной гиперплазией предстательной железы (ВРН). У выбранных пациентов данное изобретение обеспечивает уникальную возможность излечивать ВРН без хирургического вмешательства или гормонотерапии. В клиническом исследовании изобретения состояние одного пациента с ВРН значительно улучшилось в результате использования инъекции "лекарственной ионной бомбы" в предстательную железу.
Фармацевтические композиции Na+ и Са2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих первичным раком поджелудочной железы. У выбранных пациентов, страдающих раком поджелудочной железы, изобретение обеспечивает возможность излечения рака поджелудочной железы, не прибегая к хирургическому вмешательству. Поджелудочная железа представляет собой вытянутый, клиновидный орган, расположенный поперек задней части брюшного отдела позади желудка. Органы брюшной полости пациента не поражаются, если доступ инъекции выбран в задней части спины. Пациента помещают в положение лицом вниз и внутриопухолевую инъекцию "лекарственной ионной бомбы" выполняют под контролем СТ-сканирования. Девяносто девять мл раствора "лекарственной ионной бомбы" смешивают с одним мл среды Ultravist 370, и затем смешанный раствор "лекарственной ионной бомбы" инъецируют прямо в рак поджелудочной железы с помощью более длинной иглы или экстрадлинной иглы под контролем СТ-сканирования.
Фармацевтические композиции Na+ и Са+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве превентивного лечения рака у пациентов, страдающих раком поджелудочной железы, которым назначена хирургическая операция. За 2-3 суток до хирургической операции раковое образование поджелудочной железы уничтожают in situ посредством внутриопухолевой инъекции "лекарственной ионной бомбы", затем "мертвый рак поджелудочной железы" безопасно удаляют хирургической операцией. Эта стратегия может защитить пациента от ятрогенного метастазирования и увеличивает выживаемость пациента и излечимость рака.
Фармацевтические композиции Na+ и Са2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих доброкачественными опухолями поджелудочной железы, такими как инсулинома, киста, аденома и другие опухоли поджелудочной железы.
Фармацевтические композиции Na+ и Ca2+ и способы лечения по изобретению можно применять в качестве паллиативного лечения рака поджелудочной железы во время хирургической операции, когда распространенный рак поджелудочной железы является неудаляемым. Во время лапаротомии раствор "лекарственной ионной бомбы" инъецируют в рак поджелудочной железы под визуальным контролем. Это лечение может облегчить состояние ракового пациента и улучшить качество жизни пациента.
Фармацевтические композиции Na+ и Ca2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих первичным раком легкого, раком печени и раком почки. Лечение осуществляют под контролем СТ-сканирования или под визуальным контролем во время хирургической операции.
Фармацевтические композиции Na+ и Ca2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих колоректальной карциномой и в сочетании с большой кишечной обструкцией. Под контролем эндоскопа "лекарственную ионную бомбу" инъецируют в раковое образование под визуальным контролем для облегчения обструктивных симптомов в экстренном порядке.
Фармацевтические композиции Na+ и Ca2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, страдающих раком шейки матки. Пациента лечат простой внутриопухолевой инъекцией "лекарственной ионной бомбы" под визуальным контролем.
Фармацевтические композиции Na+ и Ca2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов, имеющих предзлокачественную и доброкачественную опухоль в женских и мужских генитальных органах, под визуальным контролем.
Фармацевтические композиции Na+ и Ca2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов с лейомиомой или лейомиосаркомой в матке, которые можно лечить трансвагинально или под контролем перитонеальной эндоскопии или минимальной неинвазивной хирургической операции.
Фармацевтические композиции Na+ и Ca2+ и способы лечения путем внутриопухолевой инъекции "лекарственной ионной бомбы" в данном изобретении могут быть использованы в качестве терапии первой линии у пациентов с доброкачественными и злокачественными опухолями яичника, включая, без ограничения, карциному яичника, тератому и фиброидные состояния. Пациента лечат, вводя более длинную иглу в опухоль под контролем лапароскопии или минимальной неинвазивной хирургической операции.
Фармацевтические композиции Na+ и Ca2+ способы лечения по изобретению можно использовать в косметической терапии для удаления кожного невуса, нароста, бородавки и новообразования на поверхности тела.
Взятое в совокупности, изобретение внутриопухолевой инъекции "лекарственной ионной бомбы" можно использовать в качестве терапии первой линии в лечении рака и опухоли по меньшей мере в девяти органах человека (карциномы и опухоли кожи и подкожной ткани, молочной железы, предстательной железы, щитовидной железы, легкого, печени, генитального органа, головного мозга и поджелудочной железы) и доброкачественных заболеваний четырех категорий (кожного и подкожного новообразования, кистозно-фиброзного изменения молочной железы, доброкачественной гиперплазии предстательной железы и узлов щитовидной железы). Примеры
Данное изобретение более конкретно иллюстрируется приведенными ниже репрезентативными примерами процедуры внутриопухолевой инъекции "лекарственной ионной бомбы" при опухолях животных и раковых состояниях человека.
Композиция "лекарственной ионной бомбы" для лечения рака содержит 5,0479 М Na+ и 250 мМ Са2+ плюс примерно 890 мл стерильной дистиллированной воды, чтобы конечный объем составлял один литр раствора "лекарственной ионной бомбы". Две дополнительные композиции содержат 20 микрограммов (мкг)/мл адреналина и 10 микролитров (мкл)/мл рентгеноконтрастной среды Ultravist 370.
Na+ и Ca2+ в этой композиции оказывают цитотоксическое действие, дистиллированная вода является растворителем, Ultravist 370 является рентгеноконтрастной средой, и адреналин является сосудосуживающим агентом. Исследования подтвердили, что композиция раствора "лекарственной ионной бомбы", содержащая 5,0479 М NaCl и 250 мМ CaCl2, при комнатной температуре представляет собой полностью растворенный и насыщенный ионный раствор с максимально эффективным уничтожающим рак действием.
Согласно изобретению заявлен способ лечения путем внутриопухолевой инъекции раствора "лекарственной ионной бомбы", при котором путь введения раствора "лекарственной ионной бомбы" представляет собой внутриопухолевую инъекцию (прямую инъекцию) раствора "лекарственной ионной бомбы" в опухоль или рак у субъекта.
Кроме того, заявлены минимальная и максимальная эффективные терапевтические концентрации Na+ и Са2+ для внутриопухолевой инъекции. Когда для внутриопухолевой инъекции используют только Na+ (например NaCl), тогда эффективная терапевтическая концентрация Na+ колеблется в пределах от примерно 2,0 М до примерно 5,4414 М при комнатной температуре. Когда для внутриопухолевой инъекции используют только Са2+ (например CaCl2, тогда эффективная терапевтическая концентрация Са2+ колеблется в пределах от примерно 50 мМ до 6,0 М при комнатной температуре.
ПРИМЕР 1
На Фиг. 1 представлена модель мышиной саркомы МСА207 у мыши C57BL6. Фиг. 1А. До лечения опухоль имела размер 8 мм × 8 мм. Фиг. 1 В. Стандартная процедура внутриопухолевой инъекции "лекарственной ионной бомбы" у мыши. Фиг. 1C. Мышиная саркома уничтожена однократной инъекцией 0,10 мл "лекарственной ионной бомбы".
ПРИМЕР 2
На Фиг. 2 представлена модель рака молочной железы человека MCF7 у бестимусной мыши. Фиг. 2А. До лечения опухоль имела размер 13 мм × 13 мм, что составляет 3%± массы тела мыши. Фиг. 2В. Стандартная процедура внутриопухолевой инъекции "лекарственной ионной бомбы" у мыши. Фиг. 2С. Модель большой раковой опухоли молочной железы человека у бестимусной мыши уничтожена однократной инъекцией 0,14 мл "лекарственной ионной бомбы".
ПРИМЕР 3
На Фиг. 3 показано применение метода с использованием флуоресцентного Са2+ зонда для определения ex vivo притока Ca2+ из внеклеточной жидкости во внутриклеточную жидкость в клетках рака молочной железы человека MCF7. Фиг. 3А. Семь раковых клеток, меченных флуоресцентным Са2+ зондом, до обработки. Фиг. 3В. Две из 7 раковых клеток были уничтожены "лекарственной ионной бомбой" через 14± секунд после начала обработки. Фиг. 3С. Все 7 раковых клеток были уничтожены через 18± секунд после начала обработки. Процедура измерения притока Na+ была такой же, как указано выше, но с использованием флуоресцентного Na+ зонда.
ПРИМЕР 4
На Фиг. 4 представлен групповой фотоснимок видеоизображения с инвертированного микроскопа Nikon Diaphot. Фиг. 4А. Клетки рака молочной железы человека MCF7 до обработки. На Фиг. 4В показаны обработанные раковые клетки, подвергнутые вихреподобному вращению в среде для культуры ткани, через 5-7 секунд после добавления "лекарственной ионной бомбы". Фиг. 4С. Все раковые клетки были уничтожены через 16± секунд после начала обработки. Клетки на этих 3 микроснимках были из одного и того же участка. Увеличение × 400.
ПРИМЕР 5
На Фиг. 5 представлена группа микроснимков, на которых изображены признаки in vivo мышиной саркомы МСА207, обработанной "лекарственной ионной бомбой". Фиг. 5А. Белые линии, окружающие раковые клетки, представляют собой ионы натрия (соли) и ионы кальция (соли) в раковой ткани у мыши. Увеличение × 1000. Фиг. 5В. Обработанные раковые ткани омертвели там, куда достигла "лекарственная ионная бомба". Увеличение × 400. Фиг. 5С. Множественные тромбозы в срезе обработанной опухоли. Увеличение × 400.
ПРИМЕР 6
На Фиг. 6 показана группа SEM моделей рака молочной железы человека MCF7 у бестимусных мышей. SEM1 демонстрирует контрольные раковые клетки. SEM2. Мембраны клеток рака молочной железы человека распались на кусочки и дебрис. На SEM3 изображены сильно поврежденные кровеносные сосуды опухоли, в частности повреждения внешнего покрова артериол или венул в ткани опухоли. Многие сосуды опухоли разорваны поперек.
ПРИМЕР 7
На Фиг. 7 показана группа ТЕМ моделей рака молочной железы человека MCF7 у бестимусных мышей. На ТЕМ1 изображены контрольные раковые клетки. ТЕМ2 выявляет тяжело поврежденную клеточную мембрану, ядро, митохондрию и цитоплазматические органеллы раковой клетки. На ТЕМЗ изображены полностью разрушенные внешний слой, средний слой и внутренний слой сосуда опухоли. Эндотелиальная клетка во внутреннем слое венулы оторвалась. Увеличения × 5000.
ПРИМЕР 8
На Фиг. 8 показан врач-клиницист, выполняющий внутриопухолевую инъекцию "лекарственной ионной бомбы" у пациента с большой опухолью. Фиг. 8А. Опухоль до лечения размером 40 мм × 60 мм в правом плече пациента. Фиг. 8В демонстрирует инъекцию под давлением 3 мл "лекарственной ионной бомбы" для уничтожения опухоли. Фиг. 8С показывает, что отверстие иглы направлено вверх, а на Фиг. 8D отверстие иглы направлено вниз.
ПРИМЕР 9
На Фиг. 9 показан случай 82-летней леди, страдающей огромной плоскоклеточной карциномой в нижней части спины в течение 3 лет. Фиг. 9.1. Карцинома до лечения размером 70 мм × 70 мм. Фиг. 9.2. Однократную внутриопухолевую инъекцию 26 мл раствора "лекарственной ионной бомбы" вводят в раковое образование. Фиг. 9.3. Аналог фотоснимка видеоизображения с телевизионной аппаратуры через 5 суток после лечения. Макроскопически, обработанное все раковое образование полностью уничтожено. Микроскопически, вся обработанная раковая ткань омертвела.
ПРИМЕР 10
На Фиг. 10 показан случай 70-летней леди с плоскоклеточной карциномой в левой части лица. Фиг. 10А. Раковая опухоль до лечения размером 15 мм × 15 мм. Этот рак уничтожен одной однократной внутриопухолевой инъекцией 1,0 мл раствора "лекарственной ионной бомбы". Фиг. 10В. Стандартная процедура внутриопухолевой инъекции "лекарственной ионной бомбы" у пациента-человека. Фиг. 10С. Через семь суток после обработки опухоль подверглась коагулирующему некрозу и выглядела как обуглившаяся мертвая опухоль. Рана зажила без дефекта через 2 недели. При последующем обследовании через 3 года возврат рака не выявлен.
ПРИМЕР 11
На Фиг. 11 показан случай 52-летней леди со злокачественной опухолью кожи. Эта опухоль является редко встречающейся опухолью, которая имеет вторую опухоль (опухоль-потомок, коричневая), растущую из ее родительской опухоли (черная). Фиг. 11А. Опухоль до лечения размером 20 мм × 20 мм. Фиг. 11В. Стандартная процедура внутриопухолевой инъекции "лекарственной ионной бомбы" у пациента-человека. Фиг. 11С. Две опухоли уничтожены однократной внутриопухолевой инъекцией 0,5 мл "лекарственной ионной бомбы" через 3 суток, и рана зажила через 2 недели после лечения. Последующее обследование через 3 года показало отсутствие рецидива опухоли.
ПРИМЕР 11
На Фиг. 12 показан случай 74-летнего мужчины, страдающего раком в левой паховой области, метастазирующим из пениса. Фиг. 12А. Раковая опухоль до лечения размером 50 мм × 70 мм. Фиг. 12В. Раковое образование лечили одной однократной внутриопухолевой инъекцией 3,5 мл раствора "лекарственной ионной бомбы". Фиг. 12С. Большая раковая опухоль у пациента-человека была уничтожена за 4 суток, и рана зажила через 3 недели.
ПРИМЕР 13
На Фиг. 13 показан случай 82-летнего мужчины, страдающего меланомой в передней части грудной клетки в течение 2 лет. Фиг. 13А. Типичная меланома в форме бабочки у пациента-человека до лечения. Фиг. 13В. Аналог фотоснимка видеоизображения, демонстрирующий однократную внутриопухолевую инъекцию 1,2 мл "лекарственной ионной бомбы" с целью уничтожения этой меланомы. Фиг. 13С. Меланома была уничтожена за сутки, и рана зажила через 3 недели после лечения. Последующее обследование через 9 лет продемонстрировало отсутствие рецидива меланомы.
ПРИМЕР 14
На Фиг. 14 показан случай 58-летнего мужчины с базальноклеточной карциномой в передней части грудной клетки. Фиг. 14.1. Базальноклеточная карцинома до лечения размером 12 мм × 12 мм. Фиг. 14.2. Базальноклеточная карцинома регрессировала через одну неделю после однократной внутриопухолевой инъекции 0,5 мл "лекарственной ионной бомбы". Фиг. 14.3. Место регрессированной карциномы зажило через 3 недели после лечения. Последующее обследование через 8 лет показало отсутствие рецидива подвергнутой лечению базальноклеточной карциномы.
ПРИМЕР 15
На Фиг. 15.1 представлено изображение, полученное в результате ангиографии через печеночную артерию, которое показывает наличие большой раковой опухоли в правой доле печени у 62-летнего мужчины. Фиг. 15.2. Изображение большой карциномы печени до лечения у того же пациента. Длинную иглу катетера помещали в центр этой большой раковой опухоли печени и инъецировали 20 мл раствора "лекарственной ионной бомбы". Фиг. 15.3. Размер раковой опухоли уменьшился в размерах с 67 мм × 67 мм × 80 мм до лечения до 45 мм × 45 мм × 60 мм после лечения через 7 суток после лечения.
ПРИМЕР 16
На Фиг. 16 показан случай леди с кистозно-фиброзным изменением молочной железы в группе клинического исследования автора изобретения. Фиг. 16.1. Изображение, полученное в результате маммографии до лечения, показывает большую кисту размером 40 мм × 40 мм, которая расположена позади левого соска, и несколько небольших фиброзно-кистозных образований, окружающих большую кисту. Фиг. 16.2. Слизеподобную жидкость внутри кисты откачивали, а затем большую кисту повторно промывали и откачивали. Затем выполняли однократную инъекцию внутрь кисты 3,5 мл "лекарственной ионной бомбы". Фиг. 16.3. Изображение, полученное в результате маммографии после лечения, показывает, что фиброзно-кистозное заболевание молочной железы вылечено через 3 месяца после лечения.
ПРИМЕР 17
На Фиг. 17 показан случай 78-летнего мужчины с липомой. Эта опухоль находилась на задней стороне его шеи в течение 18 лет. Фиг. 17А. Опухоль до лечения размером 40 мм × 40 мм. Фиг. 17В. В опухоль однократной внутриопухолевой инъекцией вводили 2,0 мл "лекарственной ионной бомбы". Фиг. 17С. Эта большая опухоль была вылечена через 8 недель. Последующее обследование через 9 лет показало отсутствие рецидива подвергнутой лечению опухоли.
ПРИМЕР 18
На Фиг. 18 показан случай пациента с атеромой. Фиг. 18А. Атерома в верхней части головы до лечения размером 18 мм × 18 мм. Фиг. 18В. Аналог фотоснимка видеоизображения, который демонстрирует однократную внутриопухолевую инъекцию 0,5 мл "лекарственной ионной бомбы". Фиг. 18С. Атерома была вылечена в 2001 году. Этот фотоснимок был сделан при проведении обследования через 9 лет.
ПРИМЕР 19
На Фиг. 19 показан случай 66-летнего мужчины с большой атеромой размером 22 мм × 28 мм. Опухоль лечили однократной внутриопухолевой инъекцией 1,5 мл "лекарственной ионной бомбы" в 2001 году. Через 9 лет обследование показало отсутствие рецидива подвергнутой лечению опухоли.
ПРИМЕР 20
На Фиг. 20 показано применение инъекции "лекарственной ионной бомбы" в косметическое образование. На Фиг. 20.1 показан кожный невус на лице пациента. Фиг. 20.2. Однократная инъекция в образование 0,2 мл "лекарственной ионной бомбы". Фиг. 20.3. Невус подвергся коагулирующему некрозу через 7 суток после лечения. Фиг. 20.4. Кожный невус удален без шрама.
Включение посредством ссылки
В данном описании имеются упоминания и ссылки на другие документы, такие как патенты, патентные заявки, патентные публикации, журналы, книги, статьи, web-контенты. Все такие документы во всей их полноте включены в данное описание посредством ссылки. Любые материалы, или их части, которые, как сказано, включены в данное описание посредством ссылки, но которые находятся в противоречии с существующими определениями, утверждениями или другими раскрывающими материалами, в прямой форме изложенными здесь, включены только в той степени, в которой не возникает никаких противоречий между этим включенным материалом и материалом настоящего описания. В случае противоречия, противоречие разрешается в пользу настоящего описания как предпочтительного описания.
Эквиваленты
Репрезентативные примеры предназначены для иллюстрации изобретения, но не предназначены для ограничения объема изобретения и не должны толковаться как ограничивающие объем изобретения. Более того, различные модификации изобретения и многие его дополнительные воплощения, помимо тех, которые представлены и описаны в данном документе, станут очевидными для специалистов в данной области из полного содержания этого документа, включая примеры и ссылки на научную и патентную литературу, включенные в данное описание. Примеры содержат важную дополнительную информацию, пояснения примерами и рекомендации, которые могут быть адаптированы к практическому использованию данного изобретения в его различных воплощениях и эквивалентах.




Изобретение относится к химико-фармацевтической промышленности и представляет собой фармацевтическую композицию для внутриопухолевой инъекции, содержащую эффективное для лечения количество Na+ от 2,0 М до 5,5 М и эффективное для лечения количество Са2+ от 250 мМ до 3,0 М в водном растворе при комнатной температуре. Также представлено лекарственное средство для лечения злокачественной опухоли и рака, доброкачественной опухоли и незлокачественной гиперплазии посредством внутриопухолевой инъекции, содержащее 5,0479 М Na+, 250 мМ Са2+, 890 мл дистиллированной воды, 10 мл Ultravist 370, 20 мг адреналина при комнатной температуре. Изобретение обеспечивает создание эффективной противоопухолевой композиции на основе насыщенного ионного раствора ионов натрия и кальция, инъекцию которой можно использовать в лечении рака и опухоли в девяти органах человека (карциномы и опухоли кожи и подкожной ткани, молочной железы, предстательной железы, щитовидной железы, легкого, печени, генитального органа, головного мозга и поджелудочной железы) и некоторых других доброкачественных заболеваний (кожного и подкожного новообразования, кистозно-фиброзного изменения молочной железы, доброкачественной гиперплазии предстательной железы и узлов щитовидной железы). 2 н. и 4 з.п. ф-лы, 20 пр., 20 ил.
1. Фармацевтическая композиция для внутриопухолевой инъекции, содержащая эффективное для лечения количество Na+ от 2,0 М до 5,5 М и эффективное для лечения количество Са2+ от 250 мМ до 3,0 М в водном растворе при комнатной температуре.
2. Фармацевтическая композиция по п. 1, где источником Na+ является неорганическая соль натрия, такая как NaCl, и органическая соль натрия.
3. Фармацевтическая композиция по п. 1, где источником Са2+ является неорганическая соль кальция, такая как CaCl2, и органическая соль кальция.
4. Лекарственное средство для лечения злокачественной опухоли и рака, доброкачественной опухоли и незлокачественной гиперплазии посредством внутриопухолевой инъекции, содержащее 5,0479 М Na+, 250 мМ Са2+, 890 мл дистиллированной воды, 10 мл Ultravist 370, 20 мг адреналина при комнатной температуре.
5. Лекарственное средство по п. 4 для применения в лечении рака и злокачественной опухоли, включающих, без ограничения ими, рак головного мозга, щитовидной железы, молочной железы, легкого, печени, поджелудочной железы, почки, толстой и прямой кишки, яичника и предстательной железы, матки и шейки матки, кожи и подкожной ткани.
6. Лекарственное средство по п. 4 для применения в лечении доброкачественной опухоли и незлокачественной гиперплазии, включающих, без ограничения ими, аденому, ангиому, атерому, фиброму, липому, тератому, тирому, кисту, полип, новообразование кожи, кистозно-фиброзное изменение молочной железы, доброкачественную гиперплазию предстательной железы, узел щитовидной железы и гипертиреоз.
| Yung-Chang Lin et al | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Насос | 1917 |
|
SU13A1 |
| Кард-машина для обработки льняных очесов | 1924 |
|
SU1155A1 |
| Yousif A | |||
| Asiri. | |||
Авторы
Даты
2016-10-20—Публикация
2012-12-04—Подача