РОДСТВЕННЫЕ ПАТЕНТНЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет согласно предварительной заявке на патент США №61/437244, поданной 28 января 2011, содержание которой полностью включено в настоящую заявку посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к способам, тест-системам и наборам, которые помогают обнаруживать и диагностировать проницаемость кишечного барьера и гематоэнцефалического барьера.
УРОВЕНЬ ТЕХНИКИ
По сравнению с другими клеточными органами в теле человека эпителиальные клетки кишечника подвергаются воздействию огромного количества антигенов, которые происходят из употребленной пищи, дрожжей, бактерий и вирусов. Некоторые из этих бактериальных антигенов не представляют угрозы для иммунной системы слизистой оболочки, в то время как другие могут быть вредными для хозяина. Иммунная система кишечника контролирует бактериальные антигены в просвете кишечника, допуская проникновение небольшого количества молекул в эпителий, где они взаимодействуют с иммунной системой слизистой оболочки и системным иммунитетом для выработки регуляторной функции Т-клеток или толерантности к этим антигенам. Тем не менее, недопустимое или чрезмерное воздействие бактериальных антигенов на иммунную систему кишечника может вызвать разрушение этого регуляторного механизма и привести к желудочно-кишечным заболеваниям (1). Таким образом, понимание физиологии поглощения антигена играет основную роль в оценке патогенеза заболевания, включая воспалительные и аутоиммунные реакции (2).
Эти и другие внешние материалы, описанные в настоящей заявке, полностью включены в настоящее описание посредством ссылки. В тех случаях, когда определение или использование термина во включенной ссылке не соответствует или противоречит определению этого термина, приведенному в настоящей заявке, применяют определение этого термина, приведенное в настоящей заявке, а определение этого термина в указанной ссылке не применяется.
Повышенная проницаемость кишечника считается ранней стадией, которая предшествует развитию некоторых аутоиммунных заболеваний (3-6). По этой причине в последнее время отмечается повышенный интерес к роли дисфункции кишечного барьера в патогенезе многих патологических состояний, затрагивающих желудочно-кишечный тракт, а также внекишечные органы, включая нервную систему (7). Нарушение регуляции барьерной функции кишечника, в качестве биологического пути для воспаления, аутоиммунных и онкологических заболеваний, обсуждалось в обзорной статье Fasano (7). В этой обзорной статье, а также более ранней статье Fasano (4), автор подчеркнул, что согласно традиционному представлению, основные функции желудочно-кишечного тракта ограничиваются перевариванием и всасыванием питательных веществ и поддержанием водно-электролитного гомеостаза. Однако более внимательный анализ анатомической и функциональной структуры желудочно-кишечного тракта показывает, что другой чрезвычайно важной функцией этого органа является его способность регулировать транспорт макромолекул между окружающей средой и хозяином посредством барьерного механизма. Вместе с лимфоидной тканью кишечника и нейроэндокринной сетью эпителиальный барьер кишечника, при участи межклеточных плотных контактов, контролирует равновесие между толерантностью и иммунностью к чужеродным антигенам.
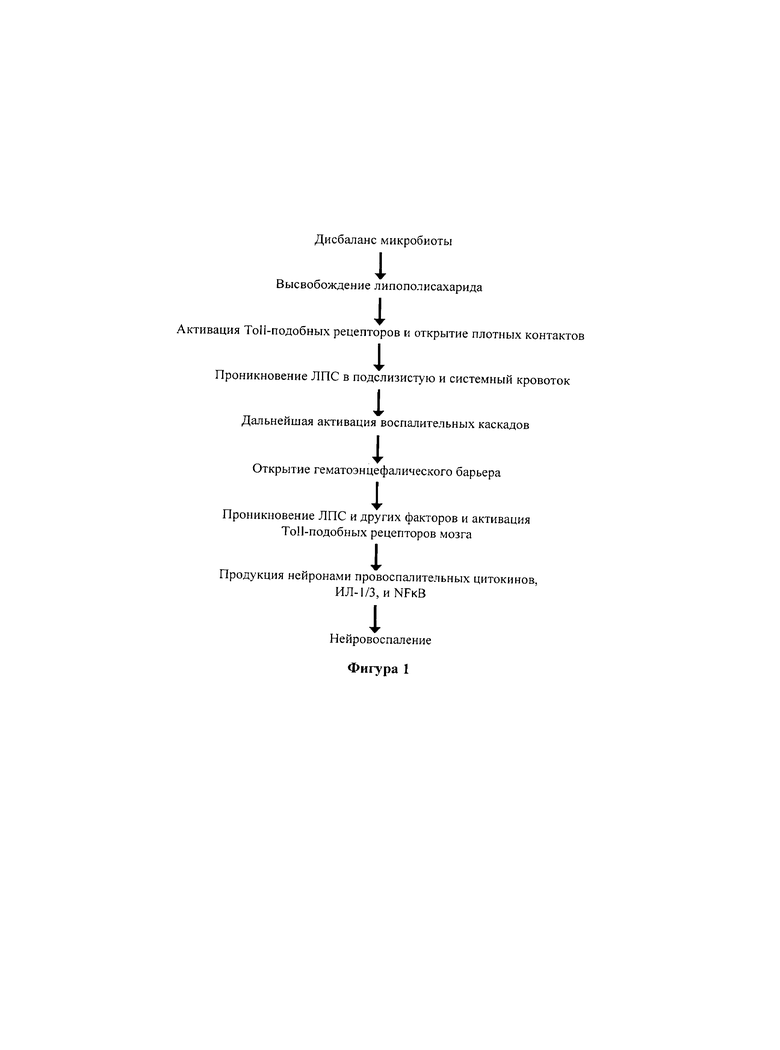
Зонулин/окклюдин являются физиологическими модуляторами параклеточных плотных контактов, которые участвуют в транспорте макромолекул и, следовательно, поддержании баланса между иммунным ответом и толерантностью (7). Когда у лиц, генетически чувствительных к факторам окружающей среды, нарушается регуляция тонко настроенных белков кишечного барьера, возникает возможность развития как кишечных заболеваний, таких как целиакия, болезнь Крона и язвенный колит, так и внекишечных аутоиммунных заболеваний, таких как артрит, волчанка, тиреоидит, диабет и даже рассеянный склероз (PC), злокачественных опухолей и большого депрессивного расстройства (8-14). Бактериальные липополисахариды (ЛПС) являются одним из основных факторов окружающей среды, которые могут лежать в основе патофизиологической дисфункции кишечника и гематоэнцефалического барьера, и, следовательно, принимать участие в кишечной и внекишечной автоиммунной активности. Вследствие дисбактериоза микробиоты кишечника и транслокации бактерий ЛПС, по-видимому, вызывают активацию Toll-подобных рецепторов на эпителиальных клетках и активацию воспалительного каскада, что сначала приводит к дисфункции кишечного барьера, а затем и гематоэнцефалического барьера (14). Роль ЛПС в индукции синдрома повышенной проницаемости кишечника и повышенной проницаемости мозга показана на Фигуре 1.
На Фигуре 1 особое значение придается тому факту, что нарушение функции желудочно-кишечного тракта может поставить под угрозу целостность кишечного барьера и увеличивает поступление непереваренных антигенов в системный кровоток, провоцируя тем самым иммунную систему. Реакция на эти антигены активирует иммунные и воспалительные каскады, что приводит к выработке провоспалительных цитокинов, панели антител и повышенной проницаемости кишечного барьера (или синдрому повышенной проницаемости кишечного барьера). При отсутствии лечения дисфункция кишечного барьера может привести к нейровоспалению, нейроинвазии и нейродегенерации.
В этой связи существует потребность в неинвазивном способе, устройстве и анализах для измерения кишечной проницаемости в отношении больших антигенных молекул, которые могут провоцировать иммунную систему, вызывая воспаление, которое может вначале привести к проницаемости гематоэнцефалического барьера, а затем к нейровоспалению и нейродегенерации (15-25). Эти и другие потребности удовлетворяются настоящим изобретением.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В качестве объекта настоящего изобретения предложено устройство, системы, анализы и способы, с помощью которых полученный от человека образец может быть протестирован, что поможет при обнаружении и диагностике проницаемости кишечного и/или гематоэнцефалического барьера.
Согласно некоторым аспектам настоящего изобретения одну или более фракций образца тестируют в отношении связывания: (1) с бактериальным токсином, и (2) связывания с нативным антигеном, выбранным по меньшей мере из одного из: (а) относящегося к кишечнику антигена и (б) относящегося к гематоэнцефалическому барьеру антигена. Согласно некоторым аспектам настоящего изобретения бактериальный токсин может преимущественно содержать липополисахарид.
При тестировании кишечной проницаемости нативный антиген, относящийся к кишечнику, предпочтительно выбирают из списка, состоящего из: (1) кишечного структурного белка, (2) белка плотных контактов, (3) рецептора, связывающегося с белком плотных контактов, и (4) белка межклеточных контактов. В примерах некоторых аспектов настоящего изобретения тестирование происходит в отношении антител к одному или нескольким белкам, таким как актин/актомиозин, окклюдин и/или зонулин, кишечный ZOT-рецептор и матриксная металлопротеиназа-3 (ММР-3).
При тестировании проницаемости гематоэнцефалического барьера антиген, относящийся к гематоэнцефалическому барьеру, предпочтительно выбирают из группы, состоящей из: (1) белка гематоэнцефалического барьера; (2) глиального фибриллярного кислого белка (ГФКБ); (3) матриксной металлопротеиназы (ММР); (4) ZOT-связывающего белка мозга; (5) ZOT-рецептора мозга; (6) кальпротектина; и (7) основного белка миелина. В примерах некоторых аспектов настоящего изобретения тестирование происходит в отношении антител к одному или более из (1) белка гематоэнцефалического барьера, (2) глиального фибриллярного кислого белка (ГФКБ) и (3) матриксной металлопротеиназы (ММР).
С диагностической точки зрения анализ результатов тестирования с помощью одного или более из описанных выше способов можно применять для помощи при обнаружении и/или диагностике заболеваний, связанных с синдромом повышенной проницаемости кишечника и/или чрезмерной проницаемости гематоэнцефалического барьера. Согласно некоторым аспектам настоящего изобретения детектирование связывания образцов с соответствующими компонентами может быть выполнено с помощью иммунологического анализа, включая, но не ограничиваясь перечисленными: ИФА, РИА, латексную агглютинацию, анализ с использованием гранул, протеомный анализ, а также другие иммунологические анализы, известные специалисту в данной области.
Согласно некоторым аспектам настоящего изобретения также могут быть предложены тестовые планшеты и наборы для проведения иммунологического анализа, включая, например, улучшенные тестовые планшеты, имеющие в качестве связанных пептидов: (1) бактериальный токсин, и (2) нативный антиген, содержащий по меньшей мере одно из (а) относящегося к кишечнику антигена и (б) нативного относящегося к гематоэнцефалическому барьеру антигена.
В наиболее предпочтительных тестовых планшетах, которые применяют для помощи при обнаружении и диагностировании или иному способу определения заболевания, связанного с синдромом повышенной проницаемости кишечника, относящиеся к кишечнику антигены могут быть преимущественно выбраны из группы, состоящей из: (1) кишечного структурного белка; (2) белка плотных контактов; (3) рецептора, связывающегося с белком плотных контактов; и (4) белка межклеточных контактов.
В наиболее предпочтительных тестовых планшетах, которые применяют для обнаружения и диагностики или иного способа идентификации заболевания, связанного с синдромом повышенной проницаемости гематоэнцефалического барьера, относящиеся к гематоэнцефалическому барьеру антигены могут быть преимущественно выбраны из группы, состоящей из: (1) белка гематоэнцефалического барьера; (2) глиального фибриллярного кислого белка (ГФКБ); (3) матриксной металлопротеиназы (ММР); (4) ZOT-связывающего белка мозга; (5) ZOT-рецептора мозга; (6) кальпротектина; и (7) основного белка миелина.
В область настоящего изобретения также включены тестовые наборы, которые могут состоять из одного или более планшетов, в которых можно провести совместное тестирование как первого набора антигенов, связанных с синдромом повышенной проницаемости кишечника, так и второго набора антигенов, связанных с увеличенной проницаемостью гематоэнцефалического барьера.
С более общей точки зрения в область настоящего изобретения включены способы и устройства, которые помогают обнаруживать и диагностировать заболевание, связанное с чрезмерной проницаемостью анатомического барьера, которые включают: получение и анализ результатов теста с использованием панели антител, которая производит сигналы при связывании образца пациента с бактериальным токсином, и нативным антигеном, выбранным по меньшей мере из одного из (а) относящегося к кишечнику антигена и (б) нативного относящегося к гематоэнцефалическому барьеру антигена.
Во всех включенных в область настоящего изобретения способах и устройствах образцы могут содержать любой подходящий образец организма, включая, например, образец цельной крови, образец сыворотки/сывороток крови, образец слюны, или образец других жидкостей организма.
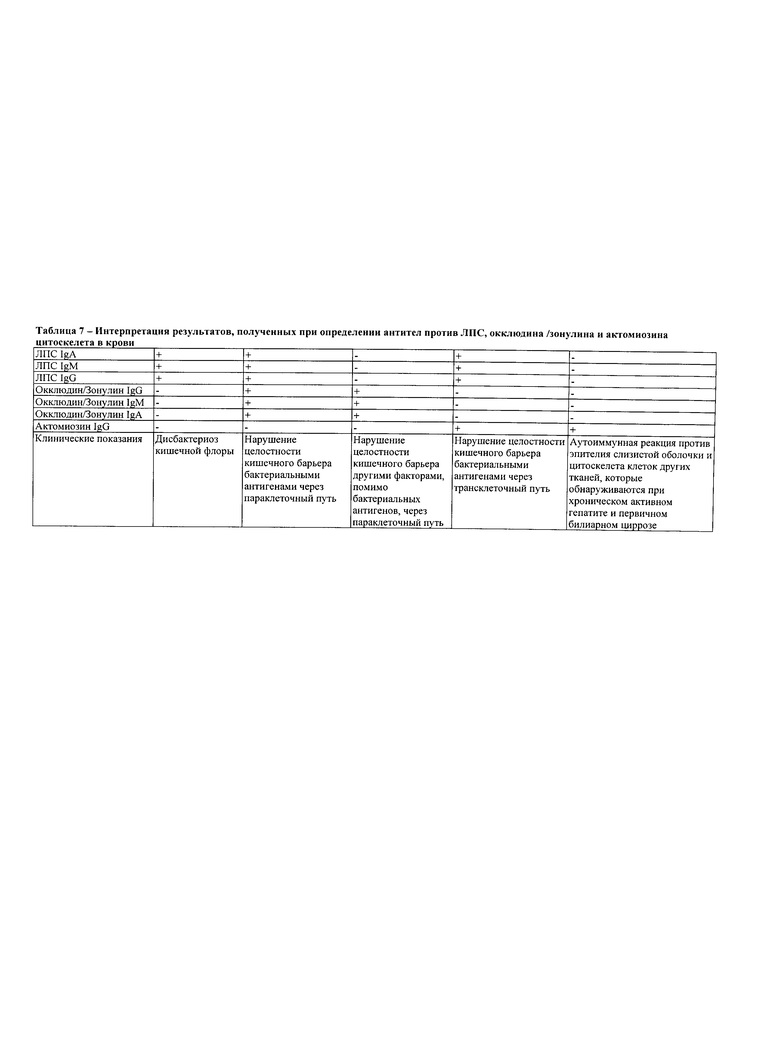
В настоящем изобретении далее предусмотрено, что способы и устройства, включенные в область настоящего изобретения, можно применять для помощи при дифференциальной диагностике заболеваний, связанных с (1) дисбактериозом кишечной флоры, и (2) нарушением целостности кишечного барьера. Например, в настоящем изобретении предусмотрено, что диагноз, относящийся к дисбактериозу кишечной флоры, как правило, может быть установлен, когда результаты тестов включают положительный результат для любого из IgA, IgM и IgG против бактериального токсина липополисахарида, и отрицательные результаты для всех IgA, IgM и IgG против окклюдина и зонулина, а также отрицательный результат для IgG против актомиозина.
В настоящем изобретении также предусмотрено, что постановка дифференциального диагноза будет облегчаться за счет установления различия между нарушением кишечного барьера через параклеточный путь и трансклеточный путь.
В отношении нарушения целостности кишечного барьера через параклеточный путь диагноз, относящийся к нарушению кишечного барьера бактериальными антигенами, как правило, может быть установлен, когда результаты тестов включают положительный результат для любого из IgA, IgM и IgG против бактериального токсина липополисахарида, и положительные результаты для любого из IgA, IgM и IgG против окклюдина или зонулина, а также отрицательный результат для IgG против актомиозина. Напротив, диагноз, относящийся к нарушению целостности кишечного барьера, не вызванному бактериальными антигенами, как правило, может быть установлен, когда результаты тестов включают отрицательный результат для всех IgA, IgM и IgG против бактериального токсина липополисахарида, и положительные результаты для любого из IgA, IgM и IgG против окклюдина или зонулина, а также отрицательный результат для IgG против актомиозина.
В отношении нарушения целостности кишечного барьера через трансклеточный путь диагноз, относящийся к нарушению кишечного барьера бактериальными антигенами, как правило, может быть установлен, когда результаты тестов включают положительный результат для любого из IgA, IgM и IgG против бактериального токсина липополисахарида, и отрицательные результаты для всех из IgA, IgM и IgG против окклюдина или зонулина, а также положительный результат для IgG против актомиозина. Также в соответствии с обсуждаемым в настоящей заявке открытием диагноз, относящийся к нарушению целостности кишечного и гематоэнцефалического барьера, индуцированному бактериальным токсином, как правило, может быть установлен, когда результаты тестов включают положительный результат для любого из IgA, IgM и IgG против бактериального токсина липополисахарида, и положительные результаты для любого из IgA, IgM и IgG против окклюдина и зонулина, а также положительный результат для любого из IgA, IgM и IgG против белков гематоэнцефалического барьера, и положительный результат для любого из IgA, IgM и IgG против нейрональных антигенов. Напротив, диагноз, относящийся к одновременному нарушению целостности кишечного и гематоэнцефалического барьеров, индуцированному другими факторами, которые отличаются от бактериального токсина, вероятно, может быть установлен, когда результаты тестов включают отрицательный результат для каждого из IgA, IgM и IgG против бактериального токсина липополисахарида, а также положительные результаты для любого из IgA, IgM и IgG против окклюдина и зонулина, положительный результат для любого из IgA, IgM и IgG против белков гематоэнцефалического барьера, и положительный результат для любого из IgA, IgM и IgG против нейрональных антигенов. В настоящем изобретении также предусмотрено, что дисбактериоз кишечной флоры может развиваться без нарушения целостности кишечного барьера, но с нарушением целостности гематоэнцефалического барьера. Например, в этой ситуации диагноз, относящийся к дисбактериозу кишечной флоры, как правило, может быть установлен, когда результаты тестов включают положительный результат для любого из IgA, IgM и IgG против бактериального токсина липополисахарида, а также отрицательные результаты для каждого из IgA, IgM и IgG против окклюдина и зонулина, положительный результат для любого из IgA, IgM и IgG против белков гематоэнцефалического барьера, и положительный результат для любого из IgA, IgM и IgG против нейрональных антигенов. Аналогичным образом, диагноз, относящийся к нарушению целостности гематоэнцефалического барьера, нейровоспалению и нейроавтоиммунному процессу и не связанный с кишечным барьером или дисбактериозом кишечной флоры, вероятно, может быть установлен, когда результаты тестов включают отрицательный результат для каждого из IgA, IgM и IgG против бактериального токсина липополисахарида, а также отрицательные результаты для каждого из IgA, IgM и IgG против окклюдина и зонулина, положительный результат для любого из IgA, IgM и IgG против белков гематоэнцефалического барьера, и положительный результат для любого из IgA, IgM и IgG против нейрональных антигенов.
В отношении конкретных заболеваний анализ результатов теста, описанного в данном документе, можно применять для помощи вобнаружении и диагностировании бокового амиотрофического склероза, болезни Паркинсона, рассеянного склероза, болезни Альцгеймера, или периферической невропатии, и большого депрессивного расстройства. Как полагают, такие состояния, вероятно, развиваются, когда результаты тестов включают положительный результат для любого из IgA, IgM и IgG против белков гематоэнцефалического барьера, и положительный результат для любого из IgA, IgM и IgG против нейрональных антигенов.
Различные объекты, признаки, аспекты и преимущества предмета настоящего изобретения станут более очевидными из следующего подробного описания предпочтительных вариантов реализации изобретения в совокупности с прилагаемыми чертежами и таблицами.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На Фигуре 1 приведена схема, относящаяся к предшествующему уровню техники, на которой показана известная в настоящее время роль ЛПС в индукции синдрома повышенной проницаемости кишечника и синдрома повышенной проницаемости гематоэнцефалического барьера.
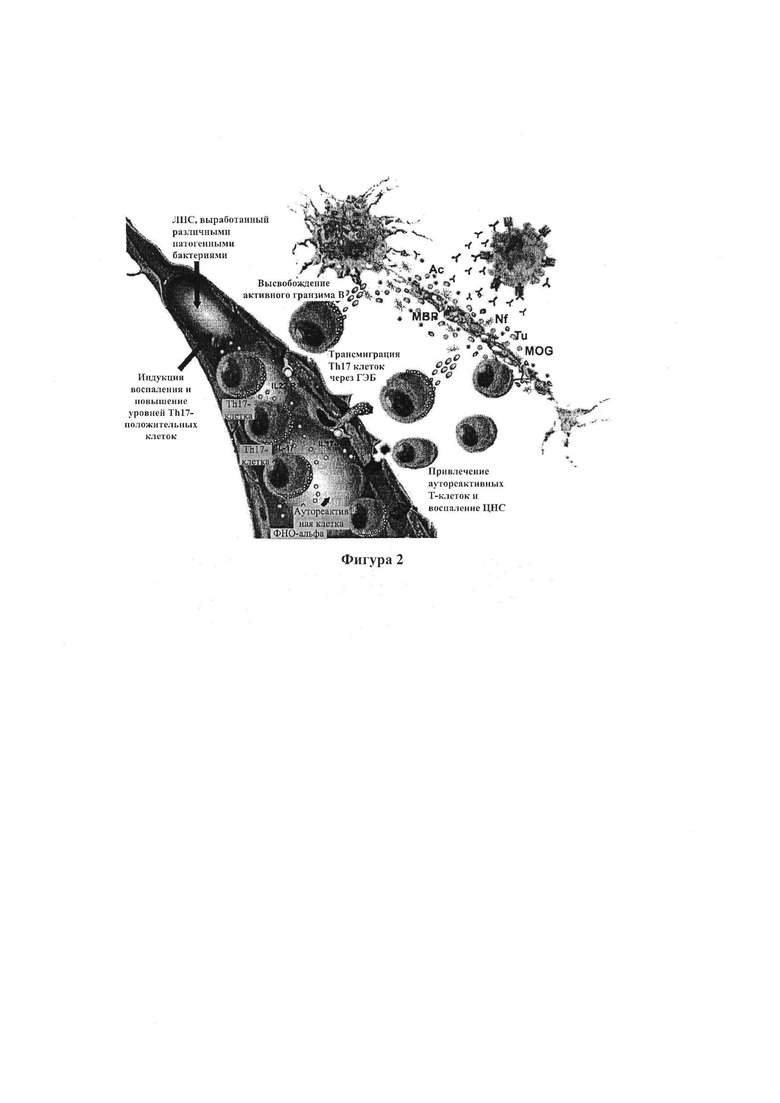
На Фигуре 2 приведена схема, относящаяся к предшествующему уровню техники, на которой показана известная в настоящее время роль ЛПС в индукции воспаления и активации ТЫ7-лимфоцитов в патогенезе воспалительных и нейроиммунных заболеваний: индукция липополисахаридами воспалительного ответа, продукции цитокинов, а также увеличения количества Th17-положительных клеток в системном кровотоке.
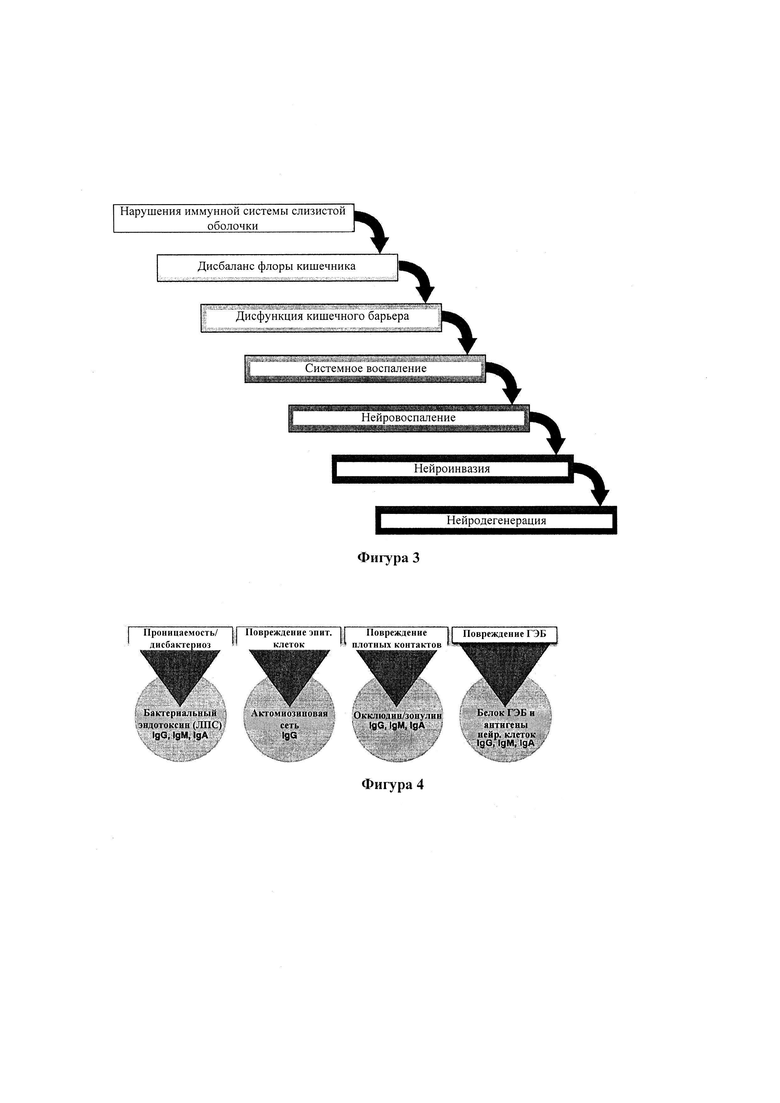
На Фигуре 3 приведена схема, относящаяся к предшествующему уровню техники, на которой показана известная в настоящее время этиология дисфункции кишечника и мозга - как потеря толерантности слизистой оболочки, при отсутствии лечения, может вызвать каскад, который индуцирует дисфункцию кишечного барьера, системное воспаление, нейровоспаление, нейроинвазию и нейродегенерацию.
На Фигуре 4 приведена схема, которая иллюстрирует предлагаемый сценарий реализации настоящего изобретения, в котором пусковые факторы и механизмы, вовлеченные в развитие патологической проницаемости кишечного барьера и проницаемости гематоэнцефалического барьера, могут быть использованы для следующего поколения подходов к тестированию, предназначенных установления проницаемости кишечного барьера (IPI) и/или установления проницаемости гематоэнцефалического барьера (BBPI).
На Фигуре 5 приведена схема, которая иллюстрирует предлагаемую роль нарушения проницаемости кишечного барьера в патогенезе аутоиммунных заболеваний согласно некоторым аспектам настоящего изобретения.
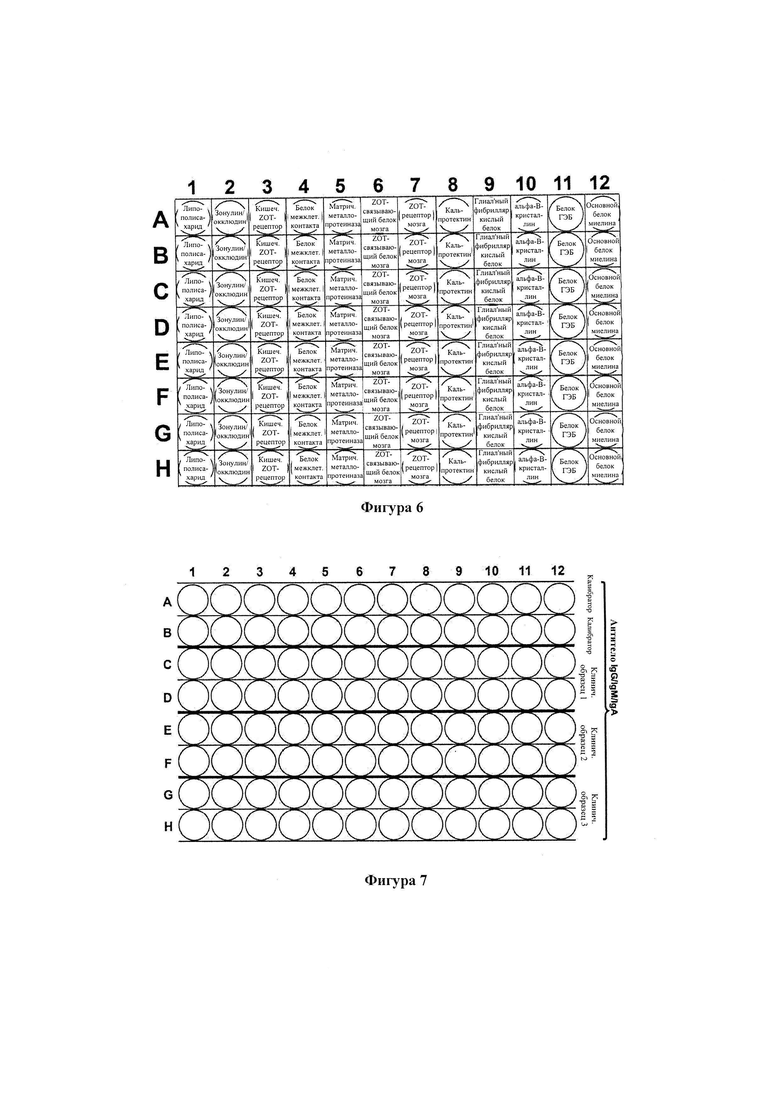
На Фигуре 6 приведена схема, которая иллюстрирует компоновку планшета для микротитрования с образцом для проведения иммунологического анализа, где планшет для микротитрования имеет 12 различных рядов с 12 различными антигенами и пептидами согласно некоторым аспектам настоящего изобретения.
На Фигуре 7 приведена схема, которая иллюстрирует компоновку планшета для микротитрования с образцом в соответствии с некоторыми аспектами настоящего изобретения, в котором IgG/IgM/IgA измеряют в отношении 12 различных антигенов или пептидов, выбранных из белков кишечного барьера и гематоэнцефалического барьера (ГЭБ) и относящихся к ним тканевых антигенов (связанные антигены и пептиды показаны как прозрачные).
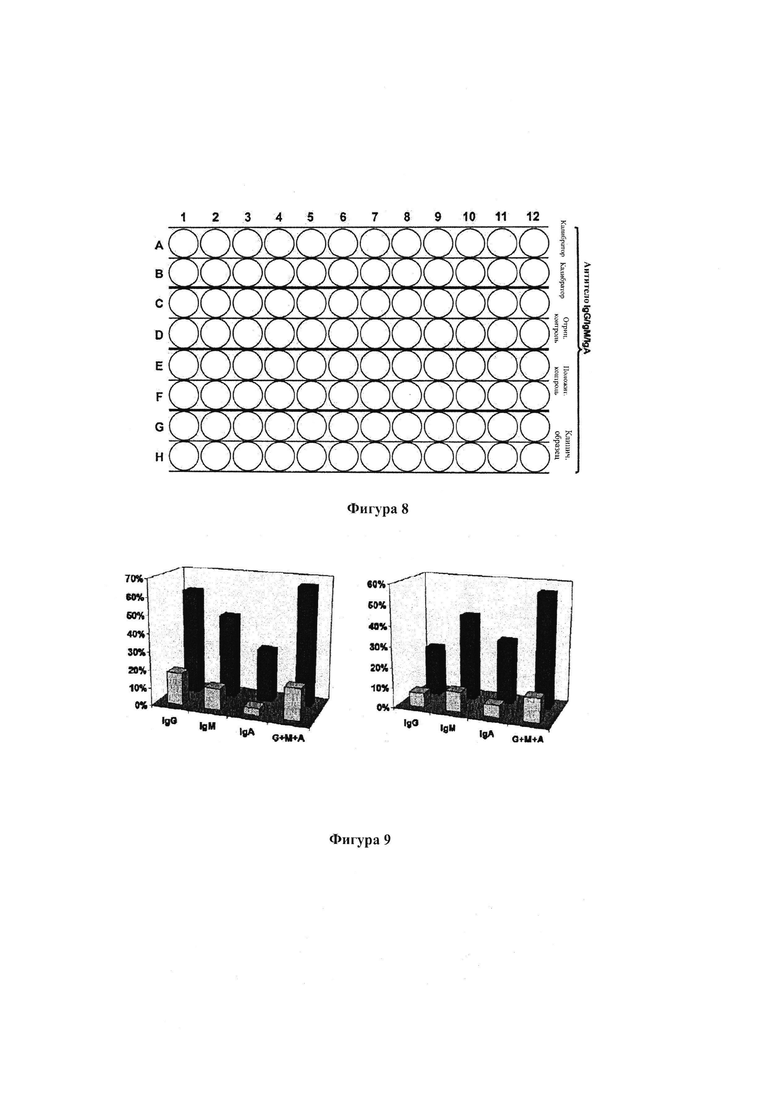
На Фигуре 8 приведена схема, которая иллюстрирует компоновку планшета для микротитрования с образцом в соответствии с некоторыми аспектами настоящего изобретения, в котором IgG/IgM/IgA измеряют с еженедельным использованием отрицательных и положительных контролей с целью контроля качества (связанные антигены и пептиды показаны как прозрачные).
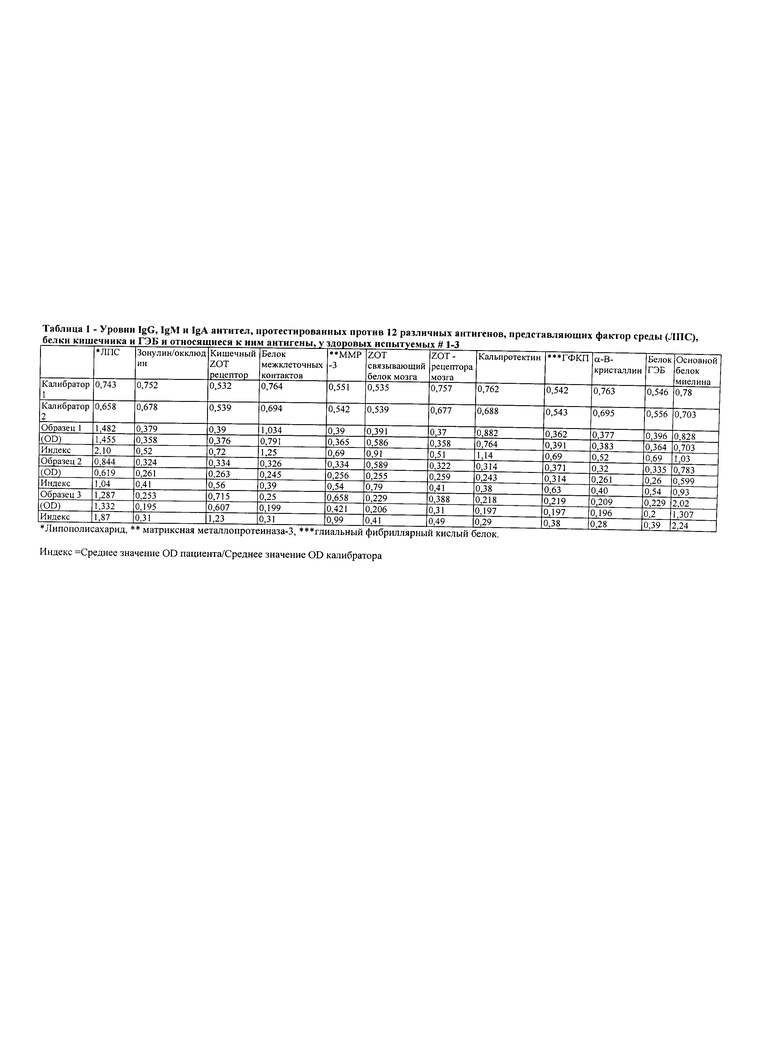
На Фигуре 9 приведена схема, которая иллюстрирует сравнение уровней IgG, IgM и IgA против бактериального липополисахарида и окклюдина/зонулина у здоровых доноров и пациентов с аутоиммунными заболеваниями желудка. Процентное повышение IgG, IgM, IgA и IgG+IgM+IgG против бактериального липополисахарида у здоровых доноров показано в виде светлых столбцов на графике слева, а результаты пациентов с аутоиммунными заболеваниями желудка с двумя стандартными отклонениями выше среднего значения показаны в виде темных столбцов на графике слева. Процентное повышение уровней IgG, IgM, IgA и IgG+IgM+IgG против окклюдина/зонулина у здоровых доноров показано в виде светлых столбцов на графике справа, а результаты пациентов с аутоиммунными заболеваниями желудка с двумя стандартными отклонениями выше среднего значения в виде темных столбцов на графике справа.
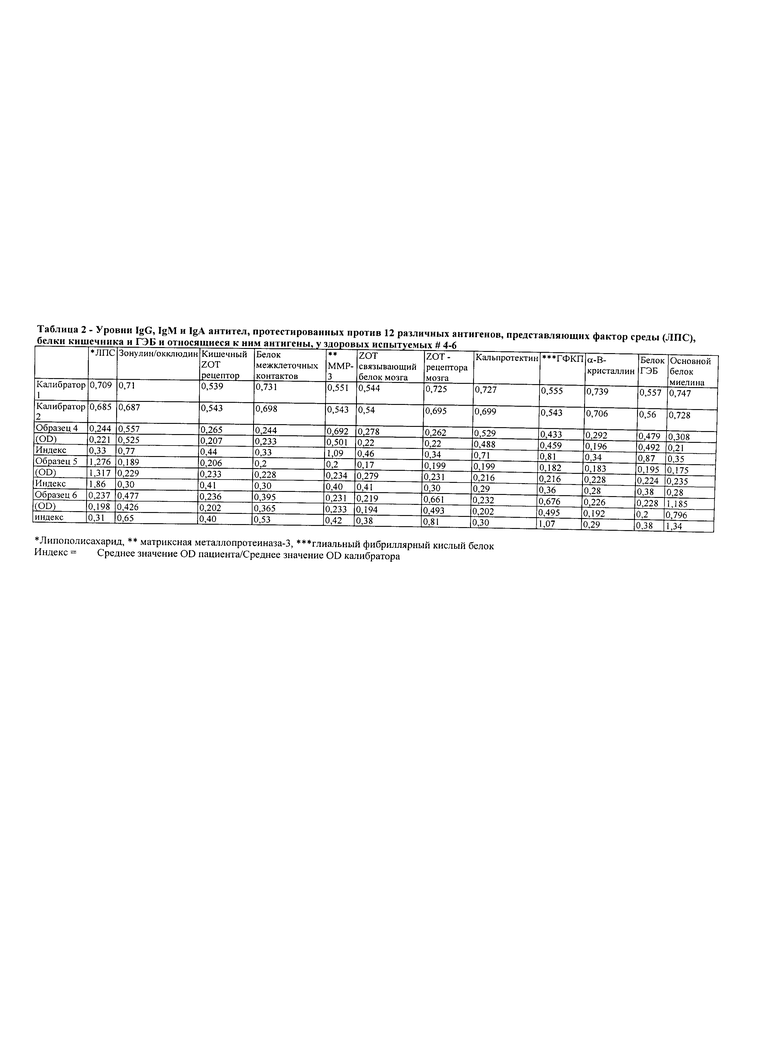
В Таблице 1 приведены уровни IgG, IgM и IgA антител, протестированных в отношении 12 различных антигенов, представляющих факторы окружающей среды (ЛПС), белки кишечного барьера и ГЭБ и относящиеся к ним антигены, у первой группы из трех здоровых испытуемых (образцы 1-3) в соответствии с некоторыми аспектами настоящего изобретения.
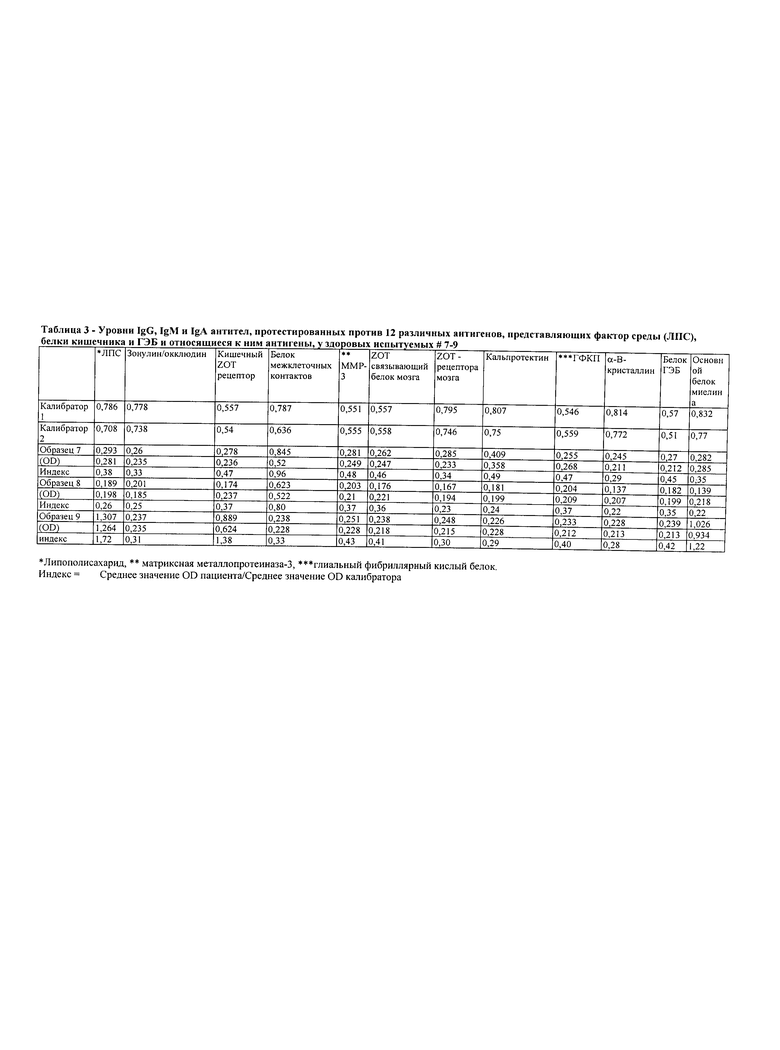
В Таблице 2 приведены уровни IgG, IgM и IgA антител, протестированных в отношении 12 различных антигенов, представляющих факторы окружающей среды (ЛПС), белки кишечного барьера и ГЭБ и относящиеся к ним антигены, у второй группы из трех здоровых испытуемых (образцы 4-6) в соответствии с некоторыми аспектами настоящего изобретения.
В Таблице 3 приведены уровни IgG, IgM и IgA антител, протестированных в отношении 12 различных антигенов, представляющих факторы окружающей среды (ЛПС), белки кишечного барьера и ГЭБ и относящиеся к ним антигены, у третьей группы из трех здоровых испытуемых (образцы 7-9) в соответствии с некоторыми аспектами настоящего изобретения.
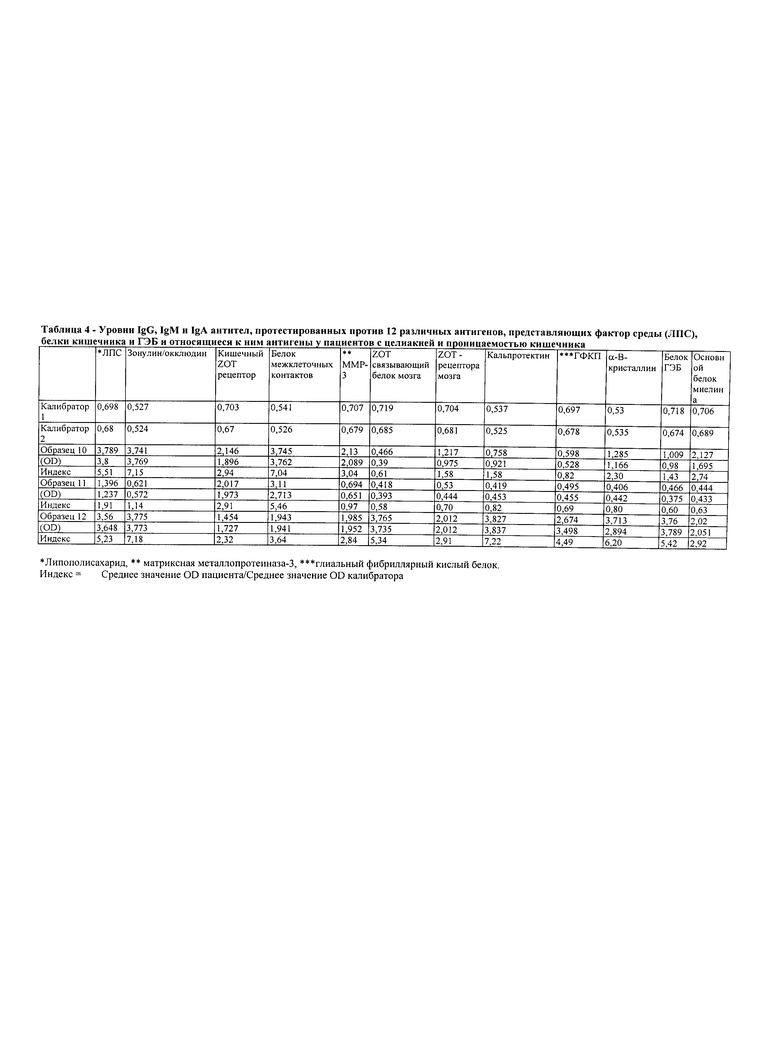
В Таблице 4 приведены уровни IgG, IgM и IgA антител, протестированных в отношении 12 различных антигенов, представляющих факторы окружающей среды (ЛПС), белки кишечного барьера и ГЭБ и относящиеся к ним антигены, у трех пациентов (образцы 10-12) с целиакией и повышенной проницаемостью кишечника в соответствии с некоторыми аспектами настоящего изобретения.
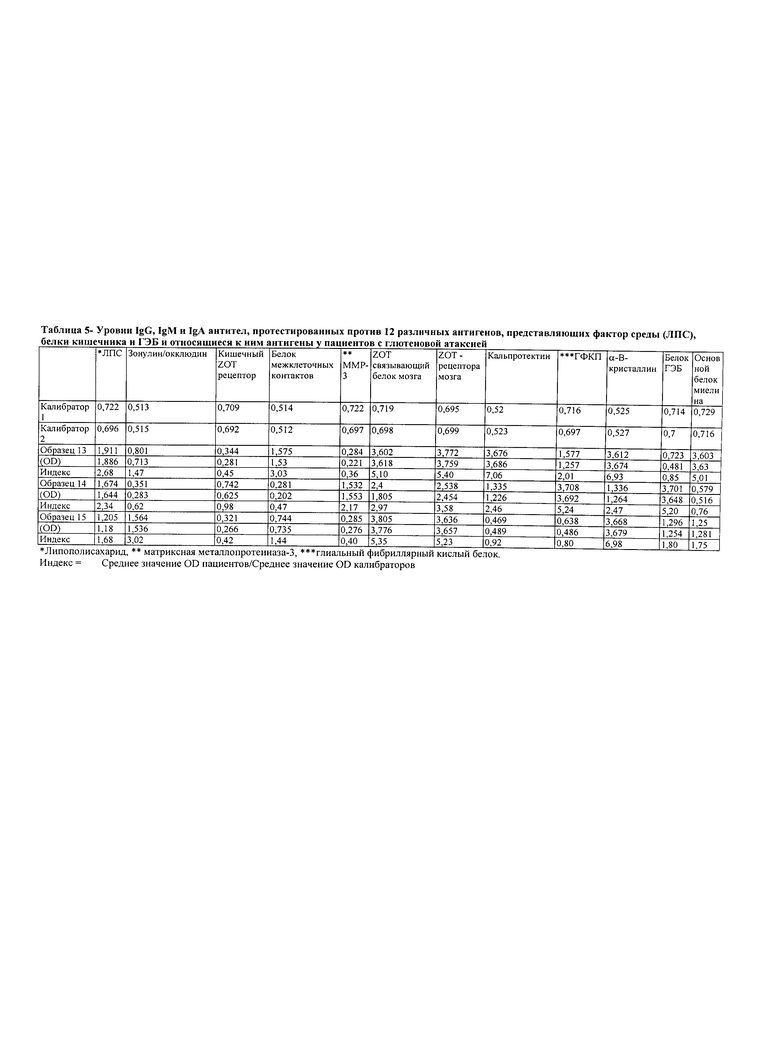
В Таблице 5 приведены уровни IgG, IgM и IgA антител, протестированных против 12 различных антигенов, представляющих факторы окружающей среды (ЛПС), белки кишечного барьера и ГЭБ и относящиеся к ним антигены, у трех пациентов (образцы 13-15) с глютеновой атаксией в соответствии с некоторыми аспектами настоящего изобретения.
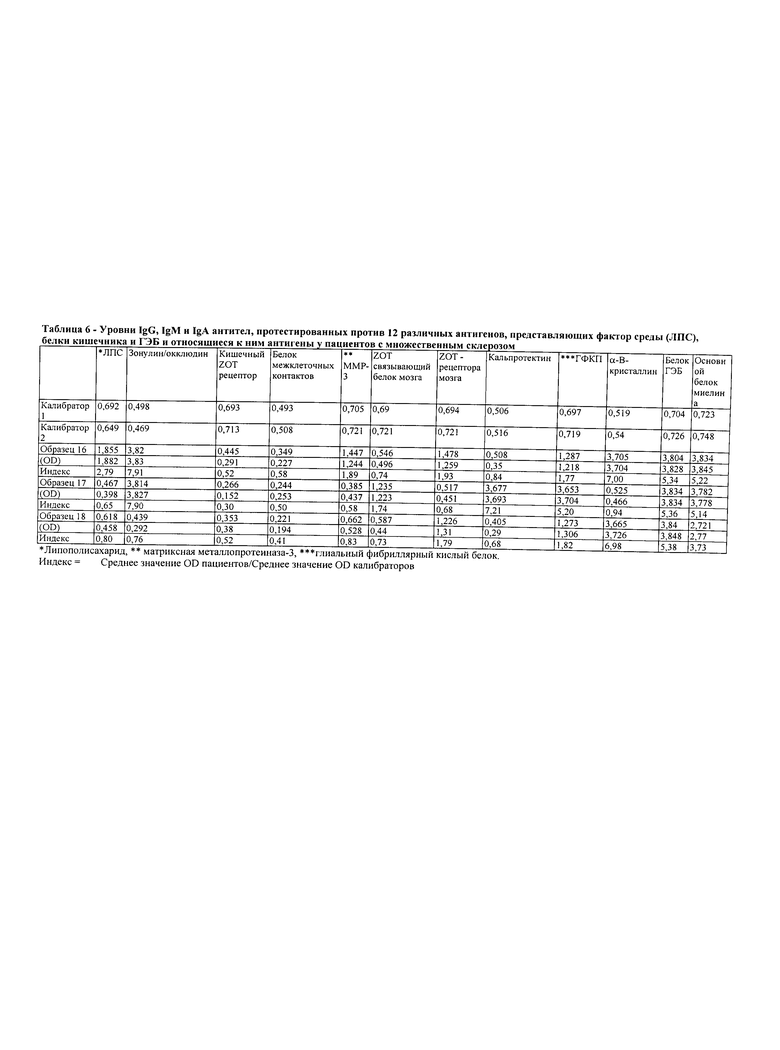
В Таблице 6 приведены уровни IgG, IgM и IgA антител, протестированных против 12 различных антигенов, представляющих факторы окружающей среды (ЛПС), белки кишечного барьера и ГЭБ и относящиеся к ним антигены, у трех пациентов (образцы 16-18) с рассеянным склерозом (MS) в соответствии с некоторыми аспектами настоящего изобретения.
В Таблице 7 представлена клиническая интерпретация уровней определенных антител против ЛПС, окклюдина/зонулина и актомиозиновой сети в крови в соответствии с некоторыми аспектами настоящего изобретения.
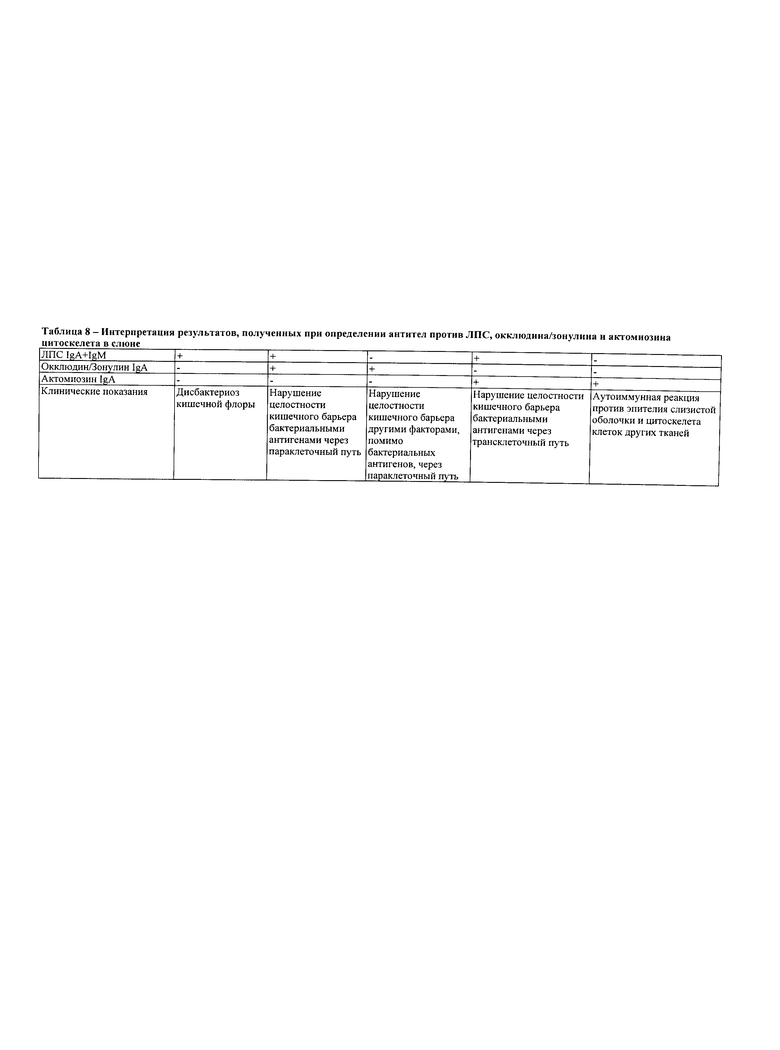
В Таблице 8 приведена клиническая интерпретация повышенных уровней определенных антител против ЛПС, окклюдина/зонулина и актомиозина в ротовой жидкости в соответствии с некоторыми аспектами настоящего изобретения.
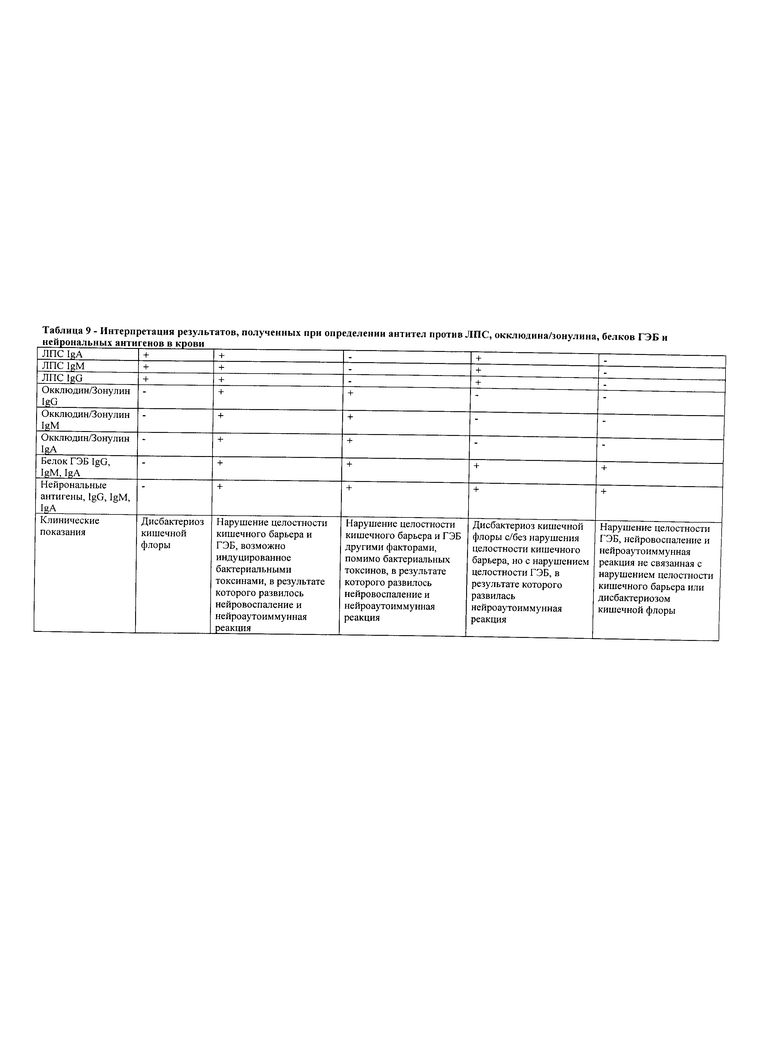
В Таблице 9 приведена клиническая интерпретация повышенных уровней определенных антител против ЛПС, окклюдина/зонулина, белка гематоэнцефалического барьера и нейрональных антигенов в крови в соответствии с некоторыми аспектами настоящего изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Повышенное поглощение антигенов является предпосылкой для развития заболевания. Известно, что ряд состояний увеличивает проницаемость кишечника и, следовательно, увеличивает поглощение антигенов. Вполне вероятно, что поглощение иммуногенных молекул или антигенов из просвета кишечника может привести к иммунологически-опосредованной активности как в кишечнике в виде IgA и IgM, так и вне его с выработкой антиген-специфических IgA, IgM, IgG и иммунных комплексов (26, 27).
I. Влияние бактериальных токсинов и воспалительных цитокинов на индукцию разрушения гематоэнцефалического барьера и нейровоспаление
Гематоэнцефалический барьер (ГЭБ) поддерживает внутреннюю среду и стабильность центральной нервной системы. Структурные и функциональные изменения ГЭБ могут привести к аутоиммунным заболеваниям, в частности нейроаутоиммунным заболеваниям, таким как рассеянный склероз (28).
ГЭБ отделяет лейкоциты крови, которые обычно реагируют на некротическое повреждение, от паренхимы головного мозга, где некротическая гибель клеток может происходить в ответ на факторы окружающей среды, такие как инфекции, токсины, эксайтотоксичность или травмы (23). ГЭБ состоит из двух слоев. Первый слой состоит из микрососудистых эндотелиальных клеток, которые имеют многочисленные плотные контакты, структурно сходные с таковыми в эпителиальных клетках кишечника (24, 28). Второй слой состоит из пограничной глиальной мембраны, которая образована отростками глиальных клеток (29). Периваскулярное пространство между эндотелиальными клетками и астроцитами заселено макрофагами, которые ведут себя как незрелые дендритные клетки (29). Таким образом, факторы, способные нарушать барьер из плотных контактов эпителиальных клеток, могут разрушать как ГЭБ, так и нервную ткань (30-33). Эти факторы включают бактериальные эндотоксины, провоспалительные цитокины, ферменты и эффекторные клетки Th1, Th17, которые играют ключевую роль в воспалении центральной нервной системы (29, 34-35).
Хорошо установлено, что нарушение ГЭБ эндотоксинами, цитокинами, хемокинами, молекулами адгезии и другими факторами, а также перемещение аутореактивных Т-клеток из системного компартмента в центральную нервную систему, играет важную роль в развитии повреждений, вызванных множественным склерозом (36-38). Однако при сравнении человеческих Th1 и Th17 лимфоцитов было установлено, что Th17 лимфоциты человека мигрировали через ГЭБ быстрее, чем Th1 лимфоциты. Действительно, значительное количество лимфоцитов памяти CD4+CD45RO+, экспрессирующих ИЛ-17 и ИЛ-22, при их миграции через ГЭБ экспрессировали ИЛ-17+ и ИЛ-22+ маркеры, которые подтвердили способность Th17 лимфоцитов проникать через ГЭБ in vitro и in vivo (35). Эндотелиальные клетки ГЭБ экспрессируют рецепторы ИЛ-17R и ИЛ-22R, которые используются Th17 лимфоцитами для инфильтрации через эндотелиальные клетки ГЭБ (ЭК). Подобная диффузия через ГЭБ клеток или антигенов, таких как бычий сывороточный альбумин (БСА), который является макромолекулой, была существенно повышена при добавлении ИЛ-17 и ИЛ-22 к монослоям ГЭБ-ЭК человека. Повышенная проницаемость ГЭБ-ЭК коррелирует со снижением экспрессии окклюдина и зонулина - двух важных белков плотных контактов (39).
Эти результаты убедительно показывают, что воспаление, индуцированное ЛПС и другими бактериальными токсинами, вызывающими активацию Th17 лимфоцитов и экспрессию рецепторов ИЛ-17 и ИЛ-22 на эндотелиальных клетках гематоэнцефалического барьера, приводит к связыванию Th17 на плотных контактах ГЭБ. Этот процесс разрушает плотные контакты, приводя к трансмиграции ТЫ 7 и аутореактивных Т-клеток через ГЭБ, в свою очередь высвобождение гранзима-В под действием ТЫ 7 лимфоцитов и высвобождение интерферона-гамма под действием CD4-клеток, вызывающее разрушение нервных клеток, высвобождение нейрональных антигенов и белков ГЭБ в системный кровоток (клетки одновременно экспрессирующие ИЛ-17, ИЛ-22 и гранзим-В под действием ИЛ-17 и ИЛ-22) играет важную роль в индукции и нарушении целостности ГЭБ, а также проницаемости ГЭБ для циркулирующих CD4+ лимфоцитов и растворимых молекул, вызывая воспаление ЦНС (40-44). Роль Th17 лимфоцитов в патогенезе воспалительных и нейроиммунологических заболеваний показана на Фигуре 2. На основании этого механизма действия индукция бактериальным токсином проницаемости кишечника и нарушения белковой структуры ГЭБ может привести к продукции антител не только против ЛПС, но также против белков плотных контактов и белков ГЭБ. Таким образом, этапы блокирования нейровоспаления согласно некоторым аспектам настоящего изобретения начинаются с тестирования ЛПС, окклюдина, клаудинов, белков ГЭБ, белков плотных контактов, ферментов, таких как матриксная металлопротеиназа, и антител против связанных рецепторов, на основании которых врач может планировать восстановление дисфункции желудочно-кишечного барьера с последующим уменьшением системного воспаления и заканчивая восстановлением гематоэнцефалического барьера.
Экспрессия рецепторов ИЛ-17 и ИЛ-22 на эндотелиальных клетках гематоэнцефалического барьера приводит к связыванию Th17 клеток с плотными контактами ГЭБ. Это нарушает плотные контакты, вызывая выработку аутореактивных CD4 и нейродегенерацию. Th17 клетки затем трансмигрируют через ГЭБ, создавая предпосылки для гибели нейронов за счет высвобождения гранзима В. Высвобождение антигенов нервных клеток приводит к порочному кругу нейроаутоиммунного воспаления и нейродегенерации.
На основании информации, представленной здесь, было выдвинуто предположение, что кишечник является отправной точкой для многих нейродегенеративных расстройств. Начальной стадией является дисбаланс микрофлоры, которая высвобождает большие количества липополисахарида (ЛПС). Большое количество ЛПС эндотоксинов индуцирует положительную регуляцию провоспалительных цитокинов ФНО-альфа и ИЛ-1β, что приводит к деградации или диссоциации плотных контактов и их белков, включая окклюдин и зонулин. Этот процесс сопровождается воспалением в кровотоке, которое распространяется на ГЭБ. Воспаление открывает ГЭБ, вызывая нейроинфильтрацию, нейровоспаление, нейроаутоиммунное поражение и, наконец, нейродегенерацию. На Фигуре 3 схематически представлены патофизиологические процессы, ведущие к нейродегенерации. При отсутствии лечения дисфункции кишечного барьера у человека может развиваться нейровоспаление, и с течением времени возможна нейродегенерация. Многие аутоиммунные заболевания имеют множественные пусковые механизмы, симптомы и системные дисфункции. В случае нейроаутоиммунных поражений, когда у многих людей вырабатываются высокие уровни антител к ЛПС, белкам плотных контактов, а также белкам ГЭБ, в процесс вовлечены иммунная и нервная системы. Общей основой для этих двух систем является желудочно-кишечный тракт, важность которого была изучена (43).
Таким образом, согласно некоторым аспектам настоящего изобретения детектирование и измерение антител против белков плотных контактов, таких как окклюдин, бактериальных эндотоксинов, таких как ЛПС, и белков ГЭБ является лучшим способом не только для оценки целостности ЖКТ и кишечного барьера, но также для определения и/или диагностики причины системного воспаления, нейровоспаления, нейроинвазии и нейродегенерации. Любые повреждения кишечного эпителия также должны быть быстро восстановлены. В противном случае повреждения позволят белкам пищи, синантропным и патогенным бактериям проникнуть в системный кровоток, вызывая запуск воспалительного каскада, который приведет к сложным аутоиммунным и нейроиммунным заболеваниям.
II. Измерение проницаемости для небольших Сахаров по сравнению с крупными антигенными молекулами
В имеющейся в настоящий момент методологии оценки кишечной проницаемости используют лактулоза и манит. На протяжении последних 40 лет это был полезный клинический инструмент. Поглощение лактулозы указывает на разрыв кишечного барьера, и тем самым на кишечную проницаемость. Вопреки распространенному мнению, поглощение этой небольшой молекулы на самом деле скорее указывает на кратковременную негерметичность, а не разрыв. Лактулоза имеет относительно низкую молекулярную массу, и перенос этого вещества через мембрану кишечника не отражает ситуацию для переноса белков пищи или других белков и иммунный ответ на них. Кроме того, тест на основе лактулозы/маннитола позволяет измерять перенос небольших молекул только посредством параклеточного, но не трансклеточного пути.
Таким образом, идентификация кишечной проницаемости для больших молекул (LMIPI) должна оцениваться с использованием больших молекул, таких как бактериальные эндотоксины (сравнимые по размеру с белками пищи), которые являются антигенными и провоцируют иммунную систему. Кроме того, в отношении проницаемости ГЭБ следует отметить, что, хотя несколько линий доказательств выявили, что изменения в проницаемости ГЭБ являются основным инициирующим фактором в патогенезе множественного склероза и экспериментального аутоиммунного энцефаломиелита (ЕАЕ) (45-50), в настоящее время нет признанного способа анализа крови для измерения проницаемости ГЭБ. Тем не менее, морфологические и функциональные изменения ГЭБ были продемонстрированы на животных моделях с использованием зонулина/окклюдина для измерения повреждений барьера (7, 11, 28).
Как показано на Фигуре 4, основной упор в методологии согласно настоящему изобретению делается на большие молекулы, которые являются антигенными, и после их высвобождения из барьеров обладают способностью провоцировать иммунную систему, приводя к выработке специфических IgG, IgM и/или IgA антител против них, которые обнаруживают в крови, сыворотке крови, и/или слюне.
Оценка проницаемости кишечного барьера для больших антигенных молекул, таких как бактериальные эндотоксины и белки пищи, становится важной для понимания патогенеза заболеваний желудочно-кишечного тракта и аутоиммунных заболеваний. Научные данные свидетельствуют о том, что многие желудочно-кишечные и аутоиммунные заболевания сопровождаются повышенной транслокацией эндотоксинов и других бактериальных токсинов аэробных и анаэробных бактерий через стенку кишечника (7, 51-55). Повышенная транслокация и связанное с ней воспаление могут вызвать деградацию белков плотных контактов и последующий иммунный ответ против белков плотных контактов, таких как окклюдин/зонулин и бактериальных эндотоксинов, таких как ЛПС. Действительно, эпителиальные клетки крысы и человека, подвергнутые воздействию бактериальных токсинов или глиадина, секретируют значительное количество зонулина. Высвобождение зонулина сопровождается отсоединением белка ZO-1 от комплекса плотного контакта, что приводит к кишечной проницаемости через трансклеточный путь (7, 51). Многие хронические состояния сопровождаются повышением сывороточных уровней IgA и IgM против ЛПС и других антигенов патогенных бактерий (24, 25). Эти состояния вызывают воспаление кишечника и повышение проницаемости барьерной слизистой оболочки, в результате чего увеличенные промежутки между клетками стенки кишечника и диссоциация белков плотных контактов могут индуцировать потерю актомиозиновой сети и защитного барьера. Потеря защитного барьера может увеличить транслокацию бактерий и тем самым повысить концентрацию в сыворотке эндотоксинов, белков плотных контактов и актомиозина.
В соответствии с некоторыми аспектами настоящего изобретения повышенные сывороточные уровни IgA и IgM против ЛПС, белков плотных контактов (окклюдина/зонулина) и актомиозина указывают на наличие проницаемости кишечного барьера и передвижение макромолекул через барьеры. Эндотоксины бактерий могут вызывать аутоиммунные поражения за счет бактериального токсина, который действует как суперантиген для Т-лимфоцитов, или при помощи механизма, называемого молекулярная мимикрия. Многие бактерии имеют антигенные сайты, которые очень похожи на тканевые антигены человека, включая нервную ткань. Если проницаемость кишечного барьера не контролируется, то воспалительный каскад антигенов и антител, выработанных против них, направится, в свою очередь, в различные ткани, где вначале вызовет воспаление, а затем аутоиммунные поражения, включая нейроаутоиммунные поражения. Поэтому при естественном течении нарушения проницаемости кишечного барьера, вызванного антигенами, продолжающаяся дегенерация может вызвать системное воспаление с последующей индукцией антигенной и клеточной проницаемости гематоэнцефалического барьера, которая приводит к сопутствующим дополнительным иммунным реакциям, вызывающим нейровоспаление, нейроинвазию и нейродегенерацию. Таким образом, согласно некоторым аспектам настоящего изобретения пациентов с хроническими воспалительными и аутоиммунными состояниями следует проверить на наличие повышенной проницаемости кишечника в отношении больших антигенных молекул путем измерения уровней IgA, IgG и/или IgM против бактериального ЛПС, белков плотных контактов и актомиозина. Наконец, у пациентов с нейроиммунными заболеваниями помимо измерений уровней IgA, IgG и/или IgM антител против ЛПС и окклюдина/зонулина, также следует измерить уровни этих антител против белков ГЭБ, ферментов, связанных рецепторов и нейрональных антигенов. Многоступенчатый процесс деградации плотных контактов при действии бактериальных токсинов и выработки антител против высвободившихся белков плотных контактов, ЛПС и других бактериальных антигенов, что приводит к повреждению ткани и аутоиммунным реакциям, показан на Фигуре 5.
В соответствии с некоторыми аспектами настоящего изобретения детектирование и измерение IgA и IgM в слюне и IgG, IgM и IgA в крови против белков плотных контактов и ЛПС будет представлять собой лучший тест для оценки барьерной функции кишечника, в то время детектирование и измерение в крови антител (IgG, IgM и IgA) против ЛПС, окклюдина/зонулина и других белков плотных контактов, а также белков ГЭБ и нервных клеток, будет представлять собой лучший способ оценки кишечной/ГЭБ проницаемости и нейроаутоиммунных реакций.
Бактериальные антигены (ЛПС) индуцируют деградацию плотных контактов и высвобождение зонулина, вызывая открытие плотных контактов и прохождение окклюдина и ЛПС через плотные контакты с последующей миграцией в подслизистую, где окклюдин и ЛПС презентируются макрофагам и дендритным клеткам. Макрофаги представляют эти антигены Т- и В-клеткам, это сопровождается аберрантным иммунным ответом, как гуморальным (IgA, IgM и IgG антитела против окклюдина и ЛПС), так и клеточно-опосредованным. Взаимодействие между гуморальным и клеточным иммунитетом несет полную ответственность за аутоиммунный процесс, нацеленный на кишечный эпителий и другие тканевые антигены, что приводит к типичному для аутоиммунных заболеваний повреждению тканей.
Ниже приведены примерные описания тестов, а также их применения и анализа результатов в отношении некоторых испытуемых пациентов. Хотя другие материалы и методы, аналогичные или эквивалентные описанным в настоящей заявке, могут быть использованы в практике или тестировании согласно настоящему изобретению, предпочтительный способ и материалы далее описываются с помощью приблизительного описания количественных анализов с целью дополнительной иллюстрации настоящего изобретения в соответствии с определенными аспектами.
Твердофазный иммуноферментный анализ (ИФА)
A. Материалы и методы - планшеты и подготовка образцов:
Липополисахариды штаммов Е.coli 055:85; Е.coli K-235, Pseudomonas aeruginosa, Pseudomonas putida, Salmonella enteritidis, Salmonella typhimurium, Klebsiella pneumonia, Morganella morganii, Hafnia alvei, Citrobacter koseri, актин, актомиозин, основной белок миелина и α-В-кристаллин были приобретены у Sigma-Aldrich, Сент-Луис, Миссури, США. Глиальный фибриллярный кислый белок (ГФКБ) был приобретен у Boehringer Mannheim, Индианаролис, Индиана, США. Также были использованы пептиды зонулина 1, 2, 3, кишечный ZOT-рецептор, пептид основного белка миелина 87-106, белок межклеточных контактов, матриксная металлопротеиназа-3, кальций-связывающий участок S100-B, названный в данном исследовании ВВВ-1 MSELEKAMVA LIDVFHQYSG REGDKHKLKK, BBB-2 SELKELINNE LSHFLEEIKE QEVVDKVMET, ВВВ-3 LDNDGDGECD FQEFMAFVAM VTTACHEFFE НЕ, ZOT-связывающий белок-1 и -2 мозга, кальпротектин (MRP-8) и ZOT-рецептор мозга.
Все пептиды класса ВЭЖХ с чистотой выше 90% были синтезированы EZ Biolab, Кармел, Индиана, США. В настоящей заявке, если из контекста не следует обратное, все диапазоны, указанные в настоящем описании, следует интерпретировать как включающие их конечные точки, и открытые диапазоны следует интерпретировать как включающие значения, которые применимы в коммерческой практике. Также все списки значений следует рассматривать как включающие промежуточные значения, если из контекста не следует обратное.
Антигены и пептиды растворяли в метаноле до концентрации 1,0 мг/мл, затем разбавляли в соотношении 1:100 в 0,1 М карбонат-бикарбонатном буфере, pH 9,5 и добавляли по 50 мкл в каждую лунку полистироловых планшетов для ИФА с плоским дном, как показано на Фигуре 6.
Планшеты инкубировали в течение ночи при 4°C и затем трижды промывали 200 мкл буферного солевого раствора на основе буфера TRIS (TBS), содержащим 0,05% Tween 20 (рН 7,4). Неспецифическое связывание иммуноглобулинов предотвращали путем добавления 200 мл 2% бычьего сывороточного альбумина (БСА) к TBS, и инкубировали в течение ночи при 4°C. Планшеты промывали и после центрального контроля качества (КК) хранили при 4°C до использования.
Конъюгаты фермента включали: очищенные аффинным способом и меченные фосфатазой антитела козы против IgG человека (Jackson ImmunoResearch, каталожный номер 109-055-008); очищенные аффинным способом и меченные фосфатазой антитела kos против IgA человека (Jackson ImmunoResearch, каталожный номер 109-055-011); и очищенные аффинным способом и меченные фосфатазой антитела коз$ против IgM человека (Jackson ImmunoResearch, каталожный номер 109-055-043).
Другие дополнительные реагенты и материалы, включенные в способ, как описано далее в настоящей заявке, включают: порошок забуференного фосфатом физиологического солевого раствора (PBS, Sigma, каталожный номер Р3813-10РАК), бычий сывороточный альбумин (Biocell, каталожный номер 3203-00), азид натрия (Sigma, каталожный номер S-2002), Tween 20 (Sigma, каталожный номер P1379-1000ML), глицерин (Sigma, каталожный номер G5516-500ML), гидроксид натрия (Sigma, каталожный номер S-5881), хлорид магния (Sigma, каталожный номер 8266), диэтаноламин (Sigma, каталожный номер D-8885), 1,0 н. раствор соляной кислоты (Sigma, каталожный номер Н3162-IGA), 5 мг таблетки субстрата p-NPP (пара-нитрофенилфосфат) (Sigma, каталожный номер S-0942) и дистиллированную воду (D. H2O).
Микролуночные планшеты готовили и покрывали 12-ю различными антигенами или пептидами, относящимися к кишечнику или мозгу, как показано на Фигуре 6. Калибратор, положительные контроли и разбавленные образцы пациентов добавляли в лунки, и аутоантитела, распознающие различные антигены, связывались при первой инкубации. После промывки лунок для удаления несвязанных белков с помощью дополнительной стадии промывки удаляли несвязанные конъюгаты очищенных, меченых щелочной фосфатазой кроличьих антител против IgG/IgM/IgA человека. Связанные конъюгаты визуализировали с помощью субстрата пара-нитрофенилфосфата (PNPP), дающего желтый продукт реакции, интенсивность которого пропорциональна концентрации аутоантител в образце. Для остановки реакции в каждую лунку добавляли гидроксид натрия. Интенсивность окрашивания регистрировали при длине волны 405 нм. Для сбора образцов использовали пробирки с плоскими красными крышками или крышками тигровой окраски (SST пробирки), хотя согласно некоторым аспектам настоящего изобретения другие устройства для сбора образцов включены в область изобретения для проведения этого анализа.
Образцы крови собирали с использованием асептических способов из вены, сыворотку получали с использованием стандартных методик. Согласно некоторым аспектам настоящего изобретения для анализа предпочтительно использовать не менее 100 мкл сыворотки, что, следовательно, соответствует приблизительно одному или более миллилитров крови.
B. Методика проведения тестового анализа
В данном разделе обсуждается аналитическая методика детектирования IgG, IgM, и/или IgA антител против ЛПС, белков кишечника и/или ГЭБ. Согласно некоторым аспектам настоящего изобретения перед началом тестового количественного анализа температура всех реагентов была доведена до комнатной. Процедура тестового анализа включает приготовление нужного количества лунок или планшетов с желаемым числом и типом антигенов и/или пептидов. После приготовления всех лунок планшета для микротитрования приблизительно 100 мкл контрольного калибратора, разбавленного в соотношении 1:100, добавляют в ряды A и B планшета для микротитрования, как показано на Фигуре 7, эту процедуру можно выполнять с помощью многоканальной пипетки. Приблизительно 100 мкл образца пациента для тестирования, разбавленного в соотношении 1:100, в данном случае сыворотки крови, добавляли, чтобы дублировать лунки рядов C и D для первого клинического образца, рядов E и F для второго клинического образца и рядов G и Н для третьего клинического образца, как показано на Фигуре 7.
Анализы периодических (например, еженедельных) отрицательных и положительных контролей, которые аналогичны клиническим образцам, проводили в двух повторах в отдельном планшете, как показано на Фигуре 8.
Планшеты затем инкубировали в течение 60 мин при комнатной температуре. После инкубации содержимое лунок выливали и промывали четыре раза фосфатно-солевым буфером с использованием промывочного раствора ELISA Washer. Приблизительно 100 мкл оптимально разбавленных и меченных щелочной фосфатазой козьих антител против IgA человека добавляли к планшету с IgA или приблизительно 100 мкл меченного ферментом IgG добавляли к планшету с IgG, а антитела против IgM добавляли к планшету с IgM при оптимальном разбавлений.
Соответствующие планшеты затем инкубировали в течение приблизительно от 30 до приблизительно 60 минут при комнатной температуре. За десять минут до конца инкубации, предназначенной для образования конъюгатов, готовили раствор субстрата путем смешивания приблизительно 5 мг пара-нитрофенилфосфата в форме таблетки с приблизительно 5 мл субстратного буфера, который хорошо перемешивали до полного растворения таблетки. Промывали четыре раза фосфатно-солевым буфером с использованием ELISA Washer. После этого добавляли по 100 мкл раствора субстрата в каждую лунку. Затем планшет инкубировали в течение 30 минут при комнатной температуре, избегая любого воздействия прямого солнечного света. Реакцию останавливали добавлением приблизительно 50 мкл 3 н. NaOH. Интенсивность окрашивания смеси в лунке регистрировали с помощью ридера для микропланшетов при длине волны 405 нм в сравнении с окрашиванием в контрольной лунке, регистрировали оптическую плотность калибраторов, контролей и неизвестных образцов.
C. Подсчет результатов
После регистрации интенсивности окрашивания в планшете при 405 нм для получения значений оптической плотности (OD405) средние значения OD для отрицательных контролей, средние значения OD для положительных контролей и средние значения OD каждого клинического образца делили на среднее значение OD калибраторов в рядах A и B для того чтобы получить соответствующее индексное значение (IV).
Индексное значение (IV) для каждого антитела рассчитывали по отношению к 12 различным антигенам путем деления средней оптической плотности каждого дублирующегося образца на среднее значение оптической плотности контрольного значения калибратора (например, делили среднее значение OD лунок C1 и D1 на среднее OD лунок A1 и В1, среднее значение OD лунок C2 и D2 на среднее значение OD лунок A2 и B2, среднее значение OD лунок C3 и D3 на среднее значение OD лунок A3 и B3, и т.д.). Результаты сопоставляли с установленными диапазонами нормальных значений.
Индекс = (среднее значение OD для пациентов)/(среднее значение OD калибраторов)
D. Интерпретация результатов
L. Панель IgG/IgM/IgA антител у пациентов с целиакией. иммунной реактивностью и чувствительностью к глютену и болезнью Крона:
В Таблицах 1-6 приведены примеры уровней панели антител IgG, IgM и IgA у 9 здоровых испытуемых (Табл.1-3) и их сравнение с панелью у 3 пациентов с целиакией и кишечной проницаемостью (Табл.4), 3 пациентов с глютеновой атаксией (Табл.5) и 3 пациентов с рассеянным склерозом (Табл.6), соответственно.
В Таблицах 7-9 представлена интерпретация данных и лабораторные различия между целиакией и иммунной реактивностью/чувствительностью/аутоиммунной реакцией на глютен.
II. Панель антител IgG, IgM и IgA против белков кишечника и ГЭБ, а также относящихся к ним антигенов у пациентов с целиакией и проницаемостью кишечника, глютеновой атаксией и пациентов с множественным склерозом.
На основании расчета индексов в Таблицах 1 -6 приведены уровни панели IgG, IgM и IgA антител у девяти здоровых испытуемых в контрольной группе (Табл.1-3), 3 пациентов с целиакией и проницаемостью кишечника (Табл.4), 3 пациентов с глютеновой атаксией (Табл.5) и 3 пациентов с рассеянным склерозом (Табл.6), соответственно. Следует отметить, что за исключением антител к ЛПС и основному белку миелина, для которых индексы могут быть выше 1,5, но незначительно больше, чем 2,0, у всех здоровых испытуемых индексы антител к другим антигенам ниже или значительно ниже 1,5 (Табл.1-3).
У пациентов с целиакией, которая подтверждается наличием IgG и IgA против деамидированного 33-mer пептида α-глиадина, тканевой трансглутаминазы (ТТГ) и комплекса глиадин-ТТГ, уровни панели антител варьируют от пациента к пациенту.
Например, в образце 10 из Таблицы 4 уровни антител против ЛПС, зонулина/окклюдина, кишечного ZOT-рецептора, белка межклеточных контактов, ММР-3, α-В-кристаллина и основного белка миелина значительно повышены, это указывает на то, что помимо повышенной проницаемости кишечника пациент может страдать от проницаемости ГЭБ. Пример 11 в Таблице 4 показывает значительное повышение антител против белка межклеточных контактов и кишечного ZOT-рецептора и умеренное повышение уровней антител против ЛПС, но не против белков ГЭБ и нейрональных антигенов, это указывает на то, что помимо целиакии пациент может страдать от кишечной проницаемости, проницаемости ГЭБ, нейроаутоиммунной реакции, и, возможно, других аутоиммунных реакций.
Уровни IgG, IgM и IgA антител против 12 различных антигенов, представляющих антигены кишечника и мозга, у 3 пациентов (образцы 13-15) с глютеновой атаксией приведены в Таблице 5. Глютеновую атаксию у этих пациентов подтверждали присутствием IgG и IgA антител против деамидированного 33-mer пептида α-глиадина, ТТГ-2, комплекса глиадин-ТТГ, ТТГ-6 и антигенов мозжечка. У этих пациентов уровни панели антител были значительно выше против ZOT-связывающего белка, ZOT-рецептора мозга, α-В-кристаллина, кальпротектина, ГФКБ и белка межклеточных контактов, что подтверждает ухудшение повреждений барьера.
Уровни этих антител против 12 протестированных антигенов у 3 пациентов (образцы 16-18) с множественным склерозом представлены в Таблице 6. Помимо отклонений показателей МРТ диагноз множественного склероза ставили на основании обнаружения антител против основного белка миелина, гликопротеина миелина олигодендроцитов (МОГ), α-В-кристаллина, протеолипидного белка, активации лимфоцитов и выработке провоспалительных цитокинов (44). Значительное повышение уровня антител было обнаружено в отношении нейрональных антигенов, белков ГЭБ и зонулина/окклюдина. Это свидетельствует о том, что пациенты с множественным склерозом действительно страдают от дисфункции ГЭБ.
III. Измерение уровней IgG. IgM и IgA антител против бактериального липополисахарида и окклюдина/зонулина у пациентов с аутоиммунными заболеваниями желудка.
Кишечная проницаемость играет важную роль в развитии желудочно-кишечных аутоиммунных заболеваний (4). На Фигуре 9 приведены схемы, в которых проводится сопоставление повышенных уровней антител против бактериальных эндотоксинов (липополисахариды) и структуры плотных контактов (окклюдин/зонулин) у здоровых контрольных испытуемых и у пациентов с аутоиммунными заболеваниями желудка.
Чрезмерное проникновение антигенных макромолекул через эпителий кишечника может инициировать выработку множества воспалительных цитокинов и закрепить текущее увеличение системного хронического воспаления (56). По-видимому, это необходимый компонент для трех факторов, которые приводят к последующему развитию аутоиммунного заболевания (генетическая предрасположенность, воздействие окружающей среды и проницаемость кишечника).
В соответствии с некоторыми аспектами настоящего изобретения выдвинуто предположение, что повышенные уровни антител к ЛПС, окклюдину/зонулину и актомиозиновой сети являются биологическими маркерами, которые позволяют идентифицировать нарушение целостности здорового кишечного барьера, и что повышенные уровни антител к ЛПС, окклюдину/зонулину, другим белкам плотных контактов, белкам ГЭБ и нейрональным антигенам (например, основному белку миелина, α-В-кристаллину, ГФКБ, кальпротектину и ZOT-белку мозга) указывают не только на нарушение целостности здорового кишечного барьера, но также на нарушение целостности ГЭБ.
В Таблице 8 представлена клиническая интерпретация повышенного уровня антител против ЛПС, окклюдина/зонулина и актомиозина в ротовой жидкости в соответствии с некоторыми аспектами настоящего изобретения.
В Таблице 9 представлена клиническая интерпретация повышенного уровня антител против ЛПС, окклюдина/зонулина, белка гематоэнцефалического барьера и нейрональных антигенов в соответствии с некоторыми аспектами настоящего изобретения.
ПРИМЕРЫ ИССЛЕДОВАНИЙ ОТДЕЛЬНЫХ КЛИНИЧЕСКИХ СЛУЧАЕВ
Два различных описания клинических случаев, первый пациента с целиакией и второй пациента с множественным склерозом, представлены в следующем виде.
A. Описание клинического случая №1: Пациент с целиакией и дисфункцией кишечного барьера.
Женщина в возрасте 38 лет, рост 5'4” фута (164,5 см) и вес 106 фунтов (48 кг) с заболеванием ЖКТ, включая запор, диарею и боль во всем теле, с напоминающим фибромиалгию синдромом и потерей веса (1-2 фунта в месяц в течение последних шести месяцев) была осмотрена терапевтом. Результаты лабораторных исследований показали отклонения показателей общего анализа крови, уровень гемоглобина составил 9,9 г/дл, средний объем эритроцита 77 фл, скорость оседания эритроцитов 54 мм/1-й ч, с низким содержанием фолиевой кислоты и витамина В-12, но высоким уровнем печеночных ферментов и C-реактивным белком высокой чувствительности. Были получены подробные биохимические и иммунологические профили, включая антинуклеарные антитела, ревматоидный фактор, Т3, Т4 и ТТГ, показатели во всех тестах были в пределах нормы. После неоднократных жалоб на дискомфорт со стороны ЖКТ, субфебрильную температуру и головную боль пациентка была направлена для обследования ЖКТ. Была проведена колоноскопия и биопсия двенадцатиперстной кишки, иммуногистологическое исследование выявило полную атрофию кишечных ворсинок по классификации Марш III. В этой временной точке были проверены концентрации IgG и IgA против глиадина и трансглутаминазы. Уровни как IgG, так и IgA против глиадина и трансглутаминазы в 3-5 раз превышали контрольные значения.
В связи с наличием атрофии ворсинок диагноз целиакии был установлен на основании положительных результатов анализа антител против глиадина и трансглутаминазы. Пациентке было сделано переливание крови, и она начала терапию противовоспалительными препаратами и безглютеновую диету. Через три месяца, несмотря на улучшение общего дискомфорта со стороны ЖКТ и прибавку в весе 4 фунта, уровень C-реактивного белка у пациентки был все еще повышен и сохранялась боль в теле и субфебрильная температура. С учетом этих факторов, а также чтобы определить причину воспаления и субфебрильной температуры исследовали антитела к ЛПС, зонулину/окклюдину и белки межклеточных контактов. Результаты представлены в Таблице 4, образец 10 показал, что по сравнению со здоровыми испытуемыми пациентка (образец 10) имела 3-6 кратное увеличение уровней IgG, IgM и IgA антител против ЛПС, зонулина/окклюдина и белков межклеточных контактов, это указывает на то, что помимо целиакии пациентка страдала от бактериальной транслокации, повреждения плотных контактов и синдрома повышенной кишечной проницаемости для больших антигенных молекул.
В этой связи помимо безглютеновой диеты пациентка прошла лечение синдрома повышенной кишечной проницаемости с применением безлектиновой диеты плюс пробиотики, такие как глутамин, N-ацетилцистеин, EPA/DHA, витамин D, лактоферрин, ксилит и босвеллиевая кислота. Через тридцать дней после начала применения указанной пробиотической схемы лечения в комбинации с безлектиновой и безглютеновой диетой клиническое состояние пациентки значительно улучшилось: лихорадка снизилась до 37°C и она прибавила еще 6 фунтов. Через шестьдесят дней лечение повышенной кишечной проницаемости было сокращено только до приема пробиотиков, однако безглютеновая диета была продолжена. Через год все лабораторные тесты повторили и результаты повторных тестов глиадина, трансглутаминазы, CRO, ЛПС и зонулина/окклюдина были в пределах нормы, это являлось дополнительным свидетельством того, что лечение повышенной кишечной проницаемости с одновременным применением безглютеновой диеты было эффективным для терапии пациентки, страдающей от целиакии и синдрома повышенной кишечной проницаемости.
Обсуждение: Из литературных данных было известно, что помимо атрофии ворсинок кишечника большинство пациентов с целиакией также страдает от синдрома повышенной кишечной проницаемости. По этой причине приблизительно только у 50% пациентов с целиакией происходит улучшение при использовании безглютеновой диеты, когда структура ворсинок возвращается к норме после шести месяцев указанного лечения. Механизм, посредством которого при целиакии происходит индукция синдрома повышенной кишечной проницаемости, обусловлен тем фактом, что у некоторых людей специфические пептиды глиадина связываются с эпителиальными клетками и вызывают повреждение белков плотных контактов, что приводит к высвобождению зонулина/окклюдина и клаудинов из подслизистой в кровь. В данном конкретном случае некоторые симптомы пациентки улучшились при применении безглютеновой диеты, но безглютеновая диета не ослабила воспалительный каскад, индуцированный транслокацией ЛПС и повышенной проницаемостью кишечника. Тем не менее, через 30-90 дней после применения безглютеновой диеты с одновременным лечением, направленным на восстановление белков плотных контактов с использованием натуральных средств (57-61), как клинические, так и симптоматические результаты лабораторных исследований вернулись к норме. Таким образом, можно сделать вывод, что пациенты с целиакией должны быть обследованы на наличие повышенной кишечной проницаемости для крупных молекул, которые являются антигенными, и получить лечение, направленное не только на целиакию, но также на восстановление кишечного барьера. Предмет настоящего изобретения обеспечивает такую возможность.
Б. Описание клинического случая №2: пациент с рассеянным склерозом, проницаемостью кишечного и гематоэнцефалического барьеров
Мужчина в возрасте 58 лет, высота 5'8” (176,7 см) футов и вес 182 фунта (82,5 кг) после 3-недельной истории прогрессирующей боли в шее, спине и мышцах со слабостью конечностей был направлен к невропатологу. В день, предшествующий его направлению, у него возникли трудности при мочеиспускании с покалыванием и сенсорными нарушениями в торсе и ногах до степени, когда он был не в состоянии подняться по лестнице. Чуть более двух лет до поступления у пациента были семейные проблемы и развилось депрессивное состояние, в отношении которого он не предпринимал попыток лечения. Общая история болезни пациента была обычной за исключением необъяснимой микроцитарной анемии легкой степени тяжести, которую лечили с помощью витамина B-12 и добавок препаратов железа.
Чтобы выяснить, мог ли пациент страдать от малого инсульта или страдал от некоторых неврологических или аутоиммунных расстройств, был начат ряд исследований для установления иммунологического и неврологического профиля.
Лабораторное исследование показало нормальные значения показателей биохимического и общего анализа крови с уровнем гемоглобина 10,8 г/дл. Иммунологический профиль, включая антинуклеарные антитела, ревматоидный фактор, иммунные комплексы, общий иммуноглобулин, антитела к кардиолипиду, и функции щитовидной железы были в пределах нормы.
При дальнейшем исследовании образцы спинномозговой жидкости и крови собирали и исследовали на микобактерии, Borrelia, цитомегаловирус, вирус Эпштейна-Барр, вирус герпеса 6 типа, лимфотропный Т-клеточный вирус 1 и 2 типа и сифилис, все образцы были отрицательными. Содержание белка в спинномозговой жидкости составляло 0,7 г/л, глюкозы - 2,3 мМоль/л.
Неврологическое обследование выявило сниженную скорректированную остроту зрения 6/48 в правом глазу и 6/36 в левом глазу при нормальном движении глаз. Пациент имел пирамидальную слабость в обеих ногах и походку со средней базой. Точечное обследование выявило полусенсорный уровень ниже D10 с обеих сторон. МРТ сканирование головного мозга показало нарушения строения белого вещества легкой степени тяжести с генерализованной атрофией легкой степени тяжести, которая наблюдалась у пациентов с множественным склерозом.
Однако для того чтобы исключить вероятность чувствительности к глютену, целиакии, а также синдрома повышенной кишечной проницаемости проводили тесты на наличие антител против глиадина, ТТГ и тесты с лактулозой/маннитолом. Исследование на наличие целиакии выявило, что уровни IgG и IgA антител против глиадина в 3-6 раза выше нормального диапазона, но результаты теста на IgG и IgA против трансглутаминазы были полностью отрицательными. Кроме того, результаты теста с лактулозой/маннитолом имели сильные отклонения. В этой связи проводили следующие дополнительные тесты: определение IgG, IgM и IgA антител к ЛПС, зонулину/окклюдину, кишечному ZOT-рецептору, белку межклеточных контактов, ММР-3, ZOT-связывающему белку мозга, ZOT-рецептору мозга, кальпротектину, ГФКБ, α-В-кристаллину, белку ГЭБ и основному белку миелина. Результаты кратко обобщены в Таблице 6, где образец 17 показывает значительное повышение уровня антител против основного белка миелина и ГФКБ, подтверждающее отклонения показателей на МРТ и диагноз множественного склероза. Кроме того, значительное повышение уровней антител против зонулина/окклюдина, кальпротектина и белка ГЭБ указывало на участие желудочно-кишечного тракта с повышенной проницаемостью кишечника и ГЭБ у данного пациента (Табл.6). На основании результатов этих тестов пациент получал 1 г метилпреднизолона внутривенно в течение пяти дней, что в результате привело к некоторым клиническим улучшениям. В этот момент времени пациент начал получать β-серон и демонстрировал значительное улучшение через пятнадцать дней. Также для восстановления поврежденного ГЭБ и кишечного барьера пациент получал 200 мг миноциклин IV глутатиона, а также пробиотики, такие как глутамин, N-ацетилцистеин, EPA/DHA, витамин D, лактоферрин, ксилит и босвеллиевую кислоту. Через три месяца после этой схемы лечения общее состояние здоровья пациента значительно улучшилось.
Для специалиста в данной области техники должно быть очевидным, что возможны многие другие варианты, помимо уже описанных, которые не выходят за пределы сущности изобретения. Таким образом, предмет изобретения не ограничивается описанными примерами, за исключением объема прилагаемой формулы изобретения. Более того, при интерпретации описания и формулы изобретения все термины должны интерпретироваться в широком смысле в соответствии с контекстом. В частности, термины «содержит» и «содержащий» следует интерпретировать как относящиеся к элементам, компонентам или стадиям неисключающим образом, указывая, что упомянутые элементы, компоненты или этапы могут присутствовать, или применяться, или сочетаться с другими элементами, компонентами или этапами, на которые нет явной ссылки. Если формула изобретения настоящего описания относится по крайней мере к одному из элементов, выбранных из группы, состоящей из A, B, C … и N, то текст следует интерпретировать как требующий только одного элемента из группы, а не A плюс N, или B плюс N, и т.д.
СПИСОК ЛИТЕРАТУРНЫХ ИСТОЧНИКОВ
1. Walker WA, Sanderson IR. Epithelial barrier function to antigens. Ann NY Acad Sci. 664:10-17, 1992.
2. Walker WA, Isselbacher KJ. Uptake and transfer of macromolecules by the intestine. Gastroenterol. 67:531-550, 1974.
3. Arrieta MC, Bistritz L, Meddings JB. Alterations in intestinal permeability. Gut. 55:1512-1520, 2006.
4. Fasano A, Shea-Donohue Т. Mechanisms of disease: the role of intestinal barrier function in the pathogenesis of gastrointestinal autoimmune diseases. Nat Clin Prac Gastroenterol Hepatol. 2(9):416-422, 2005.
5. Sapone A, Lammers KM, Mazzarella G, et al. Differential mucosal IL-17 expression in two gliadin-induced disorders: gluten sensitivity and the autoimmune enteropathy celiac disease. Int Arch Allergy Immunol. 152:75-80, 2010.
6. Sapone A, Lammers KM, Casolaro V, et al. Divergence of gut permeability and mucosal immune gene expression in two gluten-associated conditions: celiac disease and gluten sensitivity. BMC Med. 9: 23, 2011.
7. Fasano A. Zonulin and its regulation of intestinal barrier function: the biological door to inflammation, auto immunity and cancer. Physiol Rev, 91:151-175, 2011.
8. Shor DB, Barzilai O, Ram M, et al. Gluten sensitivity in multiple sclerosis: experimental myth or clinical truth? Ann NY Acad Sci, 1 173:343-349, 2009.
9. Vojdani A, O'Bryan T, Green JA, et al. Immune response to dietary proteins, gliadin and cerebellar peptides in children with autism. Nutr Neurosci. 7(3): 151-161, 2004.
10. Correale J, Villa A. The blood-brain-barrier in multiple sclerosis: functional roles and therapeutic targeting. Autoimmunity. 40:148-160, 2007.
11. Morgan L, Shah В, Rivers LE, et al. Inflammation and dephosphorylation of the tight junction protein occludin in an experimental model of multiple sclerosis. Neurosci. 147:664-673, 2007.
12. Skardelly M, Armbruster FP, Meixensberger J, et al. Expression of zonulin, c-kit, glial fibrillary acidic protein in human gliomas. Transl Oncol. 2:117-120, 2009.
13. Yacyshyn В, Meddings J, Sadowski D, et al. Multiple sclerosis patients have peripheral blood CD45RO + В cells and increased intestinal permeability. Dig Dis Sci. 41(12); 2493-2498, 1996.
14. Garate I, Garcia-Bueno В, Madrigal, JLM et al. Origin and consequences of brain toll-like receptor 4 pathway stimulation in an experimental model of depression. J Neuroinflamm. 8:151, 1-31, 2011.
15. Al-Sadi RM, Ma TY. IL-Iβ causes an increase in intestinal epithelial tight junction permeability. J Immunol. 178:4641-4649, 2007.
16. Matysiak-Budnik T, Thomas-Collignon A, Megraud F, Heyman M. Alterations of epithelial permeability by Helicobacter and IL-lbeta in vitro: protective effect of rebamipide. Dig Dis Sci, 2001; 46:1558-1566.
17. Turner JR. “Putting the squeeze” on the tight junction: understanding cytoskeletal regulation. Semin Cell Dev Biol, 2000; 11:301-308.
18. Ma TY, Hoa NT, Tran DD, Bui V, Pedram A, Mills S, Merryfield M. Cytochalasin В modulation of Caco-2 tight junction barrier: role of myosin light chain kinase. Am J Physiol, 2000; 279:G875-G885.
19. Ma TY, Tran D, Hoa N, Nguyen D, Merryfield M, Tarnawski A. Mechanism of extracellular calcium regulation of intestinal epithelial tight junction permeability: role of cytoskeletal involvement. Microsc Res Tech, 2000; 51:156-168.
20. Al-Sadi R, Ye D, Dokladny K, Ma TY. Mechanism of IL-1β-induced increase in intestinal epithelial tight junction permeability. J Immunol. 2008; 180:5653-5661.
21. Shen L, Black ED, Witkowski ED, Lencer WI, Guerriero V, Schneebrger ЕЕ, Turner JR. Myosin light chain phosphorylation regulates barrier function by remodeling tight junction structure. J Cell Sci, 2006; 119:2095-2106.
22. Hecht G, Pestic L, Nikcevic G, Koutsouris A, Tripuraneni J, Lorimer Dd, Nowak G, Guerriero, Jr V, Elson El, Lanerolle PD. Expression of the catalytic domain of myosin light chain kinase increases paracellular permeability. Am J Physiol, 1996; 271:C1678-1684.
23. Ma TY, Boivin MA, Ye E, Pedram A, Said HM. Mechanism of TNF-a modulation ofCaco-2 intestinal epithelial tight junction barrier: role of myosin light-chain kinase protein expression. Am J Physiol, 2005; 288:G422-G430.
24. Мае M, Kudera M, Leunis JC. The gut-brain barrier in major depression: intestinal mucosal dysfunction with an increased translocation of LPS from gram negative bacteria (leaky gut) plays a role in the inflammatory pathophysiology of depression. Euro Endocrinol Lett, 2008; 29:117-124.
25. Мае M, Coucke F, Ategis JC. Normalization of the increased translocation of endotoxin from gram negative enterobacteria (leaky gut) is accompanied by a remission of chronic fatigue syndrome. Neuro Endocrinol Lett, 2007; 28(6):101-116.
26. Walker-Smith JA, Ford RP, Phillips AD. The spectrum of gastrointestinal allergies to food. Ann Allergy, 1984; 53:629-636.
27. Juvonen P, Jakobsson I, Lindberg T. Macromolecular absorption and cow's milk allergy. Arch Dis Child, 1990; 65:300-303.
28. Huang XN, FuJ, Wang WZ. The effects of Fasudil on the permeability of the rat blood-brain barrier and blood-spinal cord barrier following experimental autoimmune encephalomyelitis. J Neuroimmunol. 239:61-67, 2011.
29. Lassmann H, Zimprich F, Vass K, Hickey WF. Microglial cells are a component of the perivascular glia limitans. J Neurosci Res, 1991; 28:236-243.
30. Schneeberger ЕЕ, Lynch RD. The tight junction: a multifunctional complex. Am J Physiol Cell Physiol, 2004; 286: C1213-C1228.
31. Chen ML, et al. Disruption of tight junctions and induction of proinflammatory cytokine responses in colonic epithelial cells by Campylobacter jejuni. Infect Immun, 2006; 74:6581-6589.
32. LaPierre LA. The molecular structure of the tight junction. Adv Drug Deliv, 2000; 41:255-264.
33. Wong V, Gumbiner BM. A synthetic peptide corresponding to the extracellular domain of occludin perturbs the tight junction permeability barrier. J Cell Biol, 1997; 136(2):399-409.
34. Engelhardt B, Rasohoff RM. The ins and outs of the T-lymphocyte trafficking to the CNS: anatomical sites and molecular mechanisms. Trends Immunol, 2005; 26(9):485-495.
35. Aloisi F, Ria F, Adorini L. Regulation of T-cell responses by CNS antigen-presenting cells: different roles for microglia and astrocytes. Immunol Today, 2000; 21(3):141-147.
36. Ghimikar RS, Lee YL, Eng LF. Inflammation in traumatic brain injury: role of cytokines and chemokines. Neurochem Res, 1998; 23(3):329-340.
37. Kebir H, Kreymborg K, Ifergan I, Dodelet-Devillers A, Cayrol R, Bernard M, Biuliani F, Arbour N, Becher B, Prat A. Human TH17 lymphocytes promote blood-brain barrier disruption and central nervous system inflammation. Nat Med, 2007; 13:1173-1176.
38. Sospedra M, Martin R. Immunology of multiple sclerosis. Annu Rev Immunol, 2005; 23:683-747.
39. Biernacki K, Prat A, Blain M, Antel JP. Regulation of Th1 and Th2 lymphocyte migration by human adult brain endothelial cells. J Neuropathol Exp Neurol, 2001; 60(12):1127-1136.
40. Wosik K, Cayrol R, Dodelet-Devillers A, Berthelet F, Bernard M, Moumdjian R, Bouthillier A, Reudelhuber TL, Prat A. Angiotensin II controls occluding function and is required for blood-brain barrier maintenance: relevance to multiple sclerosis. J Neurosci, 2007; 27(34):9032-9042.
41. Kawanokuchi J, Shimizu K, Nitta A, Yamada K, Mizuno T, Takeuchi H, Suzumura A. Production and function of IL-17 in microglia. J Neuroimmunol, 2008; 194:54-61.
42. Ganor Y, Teichberg VI, Levite M. TCR activation eliminate glutamate receptor GLUR3 from the cell surface of normal human Т cells via an autocrine/paracrine granzyme B-mediated proteolytic cleavage. J Immunol, 2007; 178:683-692.
43. Vojdani A, Lambert J. A gut feeling for immune dysregulation and neuroinflammation. The Autism File USA, 2009; 31:56-64.
44. Vojdani A, Vojdani E, Cooper EL. Antibodies to myelin basic protein, myelin oligodendrocytes peptides, α-β-crystallin, lymphocyte activation and cytokine production in patients with multiple sclerosis. J Internal Med, 2003; 254:363-74.
45. Kirk J, Plumb J, Mirakhur M, et al. Tight junctional abnormality in multiple sclerosis white matter affects all calibers of vessel and is associated with blood-brain barrier leakage and active demyelination. J Pathol. 2003; 201:319-327.
46. Hawkins ВТ, Davis ТР. The blood-brain barrier/neurovascular unit in health and disease. Pharmacol Rev, 2005; 57:173-185.
47. Leech S, Kirk J, Plumb J, et al. Persistent endothelial abnormalities and blood-brain barrier leak in primary and secondary progressive multiple sclerosis. Neuropathol Appl Neurobiol, 2007; 33:86-98.
48. Persidsky Y, Ramirez SH, Haorah J, et al. Bllod-brain barrier: structural components and function under physiologic and pathologic conditions. J Neuroimmune Pharmacol, 2006, 1:223-236.
49. Reijerkerk A, Kooij G, van der Pol SM, et al. Tissue-type plasminogen activator is a regulator of monocyte diapedesis through the brain endothelial barrier. J Immunol, 2008; 181:3567-3574.
50. Wosik K, Cayrol R, Dodelet-Devillers A, et al. Angiotension II controls occluding function and is required for blood-brain barrier maintenance: relevance to multiple sclerosis. J Neurosci, 2007; 27:9032-9042.
51. El Asmar, Panigrahi P, Bamford P, et al. Host-dependent zonulin secretion causes the impairment of the small intestine barrier function after bacterial exposure. Gastroenterol, 2002; 123:1607-1615.
52. Balkovetz DF, Katz J. Bacterial invasion of paracellular route: divide and conquer. Microbes Infect, 2003; 5:613-619.
53. Kuula H et al. Local systemic responses in matrix metalloproteinase 8-deficient mice during Porphyromonas gingivalis-induced periodontitis. Infect Immun, 2009; 77(2):850-859.
54. 54. Cywes С, Wessels M.R. Group A Streptococcus tissue invasion by CD44-mediated cell signalling. Nature, 2001; 414:648-652.
55. Y Xu, Q Yu. E-cadherin negatively regulated CD44-hyaluronan interaction and CD44-mediated tumor invasion and branching morphogenesis. J Biol Chem, 2003; 278:8661-8668.
56. Garrote J, Gomez-Gonzalez E, Bemardo D, Arranz E, Chirdo F. Celiac disease pathogenesis: the proinflammatory cytokine network. J Pediatr Gastroenterol Nutr, 2008; 47 (Suppl 1).
57. Maldonado Galdeano C, Perdigon G. The probiotic bacillum Lactobacillus casei induces activation of the mucosal immune system through innate immunity. Clin Vaccine Immunol, 2006, 13(2):219-226.
58. Wakabayashi H, Takakura N, Yamauchi K, et al. Modulation of immunity-related gene expression in small intestine of mice by oral administration of lactoferrin. Clin Vaccine Immunol, 2006; 13(2):239-245.
59. Han S, Jeong SY, Nam YJ, et al. Xylitol inhibits inflammatory cytokine expression induced by lipopolysaccharides from Porphyromonas gingivalis. Clin Diag Lab Immunol, 2005; 12(11):1285-1291.
60. Chevrier MR, Ryan AE, Lee DY-W, et al. Boswellia carterii extract inhibits the cytokines and promotes Th2 cytokines in vitro. Clin Diag Lab Immunol, 2005; 575-580.
61. Syrovets Т, Buchele В, Krauss С, et al. Acetyl-boswellic acids inhibit lipopolysaccharide-mediated TNF-alpha induction in monocytes by direct interaction with IκB kinases. J Immunol, 2005; 174:498-506.

Группа изобретений относится к медицине и может быть использована для тестирования образца, полученного от человека. Для этого проводят измерение первого сигнала, полученного вследствие связывания первой части указанного образца с бактериальным липополисахаридом, и измерение второго сигнала, полученного вследствие связывания второй части указанного образца с нативным антигеном, выбранным по меньшей мере из одного из: (а) относящегося к кишечнику антигена и (б) относящегося к гематоэнцефалическому барьеру антигена. Также предложена диагностика заболевания, связанного с синдромом повышенной кишечной проницаемости у субъекта, способ диагностики заболевания, связанного с проницаемостью гематоэнцефалического барьера у субъекта, и тестовый планшет. Группа изобретений обеспечивает диагностику заболеваний, связанных с синдромом повышенной кишечной проницаемости (независимо от того, развился он посредством парацеллюлярного или трансцеллюлярного пути, и независимо от того, был ли он вызван бактериальными токсинами или другими причинами), и/или заболеваний, связанных с чрезмерной проницаемостью гематоэнцефалического барьера, таких как: нейровоспаление и/или нейроаутоиммуннные реакции, боковой амиотрофический склероз, болезнь Паркинсона, рассеянный склероз, болезнь Альцгеймера или периферическая невропатия и большое депрессивное расстройство. 5 н. и 21 з.п. ф-лы, 9 ил., 9 табл.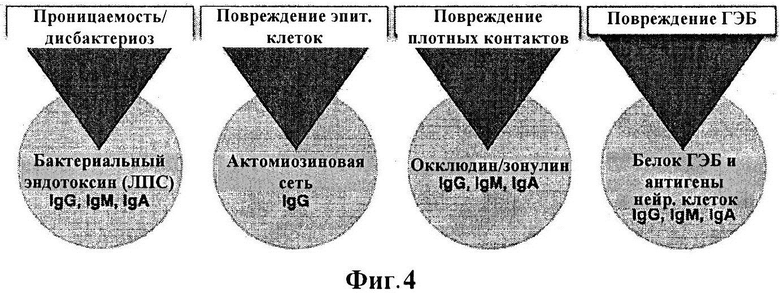
1. Способ тестирования образца, полученного от человека, включающий:
- измерение первого сигнала, полученного вследствие связывания первой части указанного образца с бактериальным липополисахаридом; и
- измерение второго сигнала, полученного вследствие связывания второй части указанного образца с нативным антигеном, выбранным по меньшей мере из одного из: (а) относящегося к кишечнику антигена и (б) относящегося к гематоэнцефалическому барьеру антигена.
2. Способ по п. 1, отличающийся тем, что указанный нативный относящийся к кишечнику антиген выбран из группы, состоящей из: (1) кишечного структурного белка; (2) белка плотных контактов; (3) рецептора, связывающегося с белком плотных контактов; и (4) белка межклеточных контактов.
3. Способ по п. 2, отличающийся тем, что относящийся к гематоэнцефалическому барьеру антиген выбран из группы, состоящей из: (1) белка гематоэнцефалического барьера; (2) глиального фибриллярного кислого белка (ГФКБ); (3) матриксной металлопротеиназы (ММР); (4) ZOT-связывающего белка мозга; (5) ZOT-рецептора мозга; (6) кальпротектина и (7) основного белка миелина.
4. Способ по п. 1, отличающийся тем, что кишечный структурный антиген включает актин/актомиозин.
5. Способ по п. 1, отличающийся тем, что антиген плотных контактов выбран из группы, состоящей из окклюдина и зонулина.
6. Способ по п. 1, отличающийся тем, что связывающийся рецептор включает кишечный ZOT-рецептор.
7. Способ по п. 1, отличающийся тем, что структурный белок включает матриксную металлопротеиназу-3 (ММР-3).
8. Способ по п. 1, отличающийся тем, что относящийся к гематоэнцефалическому барьеру антиген выбран из группы, состоящей из: (1) белка гематоэнцефалического барьера; (2) глиального фибриллярного кислого белка (ГФКБ) и (3) матриксной металлопротеиназы (ММР).
9. Способ диагностики заболевания, связанного с синдромом повышенной кишечной проницаемости, у субъекта, включающий:
- получение образца от указанного субъекта;
- получение результата тестирования указанного образца, при этом указанный результат тестирования получают с применением способа по п. 1; и
- анализ результатов указанного теста.
10. Способ диагностики заболевания, связанного с проницаемостью гематоэнцефалического барьера, у субъекта, включающий:
- получение образца от указанного субъекта;
- получение результата тестирования указанного образца, при этом указанный результат тестирования получают с применением способа по п. 1; и
- анализ результатов указанного теста.
11. Тестовый планшет, имеющий в качестве связанных антигенов: (1) бактериальный липополисахарид и (2) нативный антиген, включающий по меньшей мере одно из (а) относящегося к кишечнику антигена и (б) относящегося к гематоэнцефалическому барьеру антигена.
12. Тестовый планшет по п. 11, отличающийся тем, что указанный относящийся к кишечнику антиген выбран из группы, состоящей из: (1) кишечного структурного белка; (2) белка плотных контактов; (3) рецептора, связывающегося с белком плотных контактов; и (4) белка межклеточных контактов.
13. Тестовый планшет по п. 12, отличающийся тем, что указанный относящийся к гематоэнцефалическому барьеру антиген выбран из группы, состоящей из: (1) белка гематоэнцефалического барьера; (2) глиального фибриллярного кислого белка (ГФКБ); (3) матриксной металлопротеиназы (ММР); (4) ZOT-связывающего белка мозга; (5) ZOT-рецептора мозга; (6) кальпротектина и (7) основного белка миелина.
14. Тестовый планшет по п. 11, отличающийся тем, что указанный относящийся к гематоэнцефалическому барьеру антиген выбран из группы, состоящей из: (1) белка гематоэнцефалического барьера; (2) глиального фибриллярного кислого белка (ГФКБ); (3) матриксной металлопротеиназы (ММР); (4) ZOT-связывающего белка мозга; (5) ZOT-рецептора мозга; (6) кальпротектина и (7) основного белка миелина.
15. Способ диагностики заболевания, связанного с чрезмерной проницаемостью анатомического барьера, у субъекта, включающий:
- получение образца от указанного субъекта;
- осуществление тестирования указанного образца посредством использования тестовой панели антител, которая производит сигналы при связывании образца из организма пациента с бактериальным липополисахаридом и нативным антигеном, выбранным по меньшей мере из одного из: (а) относящегося к кишечнику антигена и (б) относящегося к гематоэнцефалическому барьеру антигена; и
- анализ результатов указанного теста, при этом указанный анатомический барьер представляет собой кишечный барьер или гематоэнцефалический барьер.
16. Способ по п. 15, отличающийся тем, что указанный образец представляет собой образец крови.
17. Способ по п. 15, отличающийся тем, что указанный образец представляет собой образец слюны.
18. Способ по п. 15, отличающийся тем, что указанный этап анализа результатов теста включает вывод о том, что диагноз, относящийся к дисбактериозу кишечной флоры, является вероятным, если результаты указанного теста включают положительный результат для любого из IgA, IgM и IgG против бактериального липополисахарида и отрицательные результаты для всех IgA, IgM и IgG против окклюдина и зонулина, а также отрицательный результат для IgG против актомиозина.
19. Способ по п. 15, отличающийся тем, что указанный этап анализа результатов теста включает вывод о том, что диагноз, относящийся к нарушению целостности кишечного барьера бактериальными антигенами через параклеточный путь, является вероятным, если результаты указанного теста включают положительный результат для любого из IgA, IgM и IgG против бактериального липополисахарида и положительные результаты для любого из IgA, IgM и IgG против окклюдина или зонулина, а также отрицательный результат для IgG против актомиозина.
20. Способ по п. 15, отличающийся тем, что указанный этап анализа результатов теста включает вывод о том, что диагноз, относящийся к нарушению целостности кишечного барьера через параклеточный путь факторами, отличными от бактериальных антигенов, является вероятным, если результаты указанного теста включают отрицательный результат для всех IgA, IgM и IgG против бактериального липополисахарида и положительные результаты для любого из IgA, IgM и IgG против окклюдина или зонулина, а также отрицательный результат для IgA против актомиозина.
21. Способ по п. 15, отличающийся тем, что указанный этап анализа результатов тестов включает вывод о том, что диагноз, относящийся к нарушению целостности кишечного барьера бактериальными антигенами через трансклеточный путь, является вероятным, если результаты указанного теста включают положительный результат для любого из IgA, IgM и IgG против бактериального липополисахарида и отрицательные результаты для всех IgA, IgM и IgG против окклюдина или зонулина, а также положительный результат для IgA против актомиозина.
22. Способ по п. 15, отличающийся тем, что указанный этап анализа результатов теста включает вывод о том, что диагноз, относящийся к нарушению целостности кишечного и гематоэнцефалического барьеров, индуцированному бактериальным липополисахаридом, является вероятным, если результаты указанного теста включают положительный результат для любого из IgA, IgM и IgG против бактериального липополисахарида и положительные результаты для любого из IgA, IgM и IgG против окклюдина и зонулина, положительный результат для любого из IgA, IgM и IgG против белков гематоэнцефалического барьера, а также положительный результат для любого из IgA, IgM и IgG против нейрональных антигенов.
23. Способ по п. 15, отличающийся тем, что указанный этап анализа результатов теста включает вывод о том, что диагноз, относящийся к нарушению целостности кишечного и гематоэнцефалического барьеров факторами, отличными от бактериального липополисахарида, является вероятным, если результаты указанного теста включают отрицательный результат для каждого из IgA, IgM и IgG против бактериального липополисахарида и положительные результаты для любого из IgA, IgM и IgG против окклюдина и зонулина, положительный результат для любого из IgA, IgM и IgG против белков гематоэнцефалического барьера, а также положительный результат для любого из IgA, IgM и IgG против нейрональных антигенов.
24. Способ по п. 15, отличающийся тем, что указанный этап анализа результатов тестов включает вывод о том, что диагноз, относящийся к дисбактериозу кишечной флоры без нарушения целостности кишечного барьера и с нарушением целостности гематоэнцефалического барьера, является вероятным, если результаты указанного теста включают положительный результат для любого из IgA, IgM и IgG против бактериального липополисахарида и отрицательные результаты для каждого из IgA, IgM и IgG против окклюдина и зонулина, положительный результат для любого из IgA, IgM и IgG против белков гематоэнцефалического барьера, а также положительный результат для любого из IgA, IgM и IgG против нейрональных антигенов.
25. Способ по п. 15, отличающийся тем, что указанный этап анализа результатов теста включает вывод о том, что диагноз, относящийся к нарушению целостности гематоэнцефалического барьера, нейровоспалению и нейроаутоиммунной реакции без взаимосвязи с кишечным барьером или дисбактериозом кишечной флоры, является вероятным, если результаты указанного теста включают отрицательный результат для каждого из IgA, IgM и IgG против бактериального липополисахарида и отрицательные результаты для каждого из IgA, IgM и IgG против окклюдина и зонулина, положительный результат для любого из IgA, IgM и IgG против белка гематоэнцефалического барьера, а также положительный результат для любого из IgA, IgM и IgG против нейрональных антигенов.
26. Способ по п. 15, отличающийся тем, что указанный этап анализа результатов теста включает вывод о том, что диагноз заболевания, выбранного из бокового амиотрофического склероза, болезни Паркинсона, рассеянного склероза, болезни Альцгеймера или периферической невропатии и большого депрессивного расстройства, является вероятным, если результаты указанного теста включают положительный результат для любого из IgA, IgM и IgG против белков гематоэнцефалического барьера, а также положительный результат для любого из IgA, IgM и IgG против нейрональных антигенов.
| BLIXT O et al | |||
| Pathogen specific carbohydrate antigen microarrays: a chip for detection of Salmonella O-antigen specific antibodies.Glycoconj J | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| US 20100190191 A1, 29.07.2010 | |||
| US 20030170747 A1, 11.09.2003 | |||
| MEAS M et al | |||
| The gut-brain barrier in major depression: intestinal mucosal dysfunction with an increased translocation of LPS from gram negative enterobacteria (leaky gut) plays a role in the inflammatory pathophysiology of depression.// Neuro Endocrinol Lett | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
Авторы
Даты
2017-01-10—Публикация
2012-01-26—Подача