Изобретение относится к области медицины, конкретно к способу диагностики аллоиммунной тромбоцитопении новорожденного (АТПН). Способ включает типирование генов системы НРА у матери и ребенка, исследование антитромбоцитарных антител классов IgG и IgM в сыворотке крови матери к собственным тромбоцитам и тромбоцитам ребенка. Способ обеспечивает раннюю и точную диагностику аллоиммунной тромбоцитопении новорожденного.
Изобретение относится к медицине, а именно лабораторной диагностике, основанной на генетическом и проточно-цитометрическом методах выявления критериев, свидетельствующих об аллоиммунном характере разрушения тромбоцитов плода и новорожденного.
Тромбоцитопения, снижение уровня тромбоцитов в периферической крови менее 150×109/л, встречается у 1-5% новорожденных [3, 11]. Тромбоцитопения может возникнуть вследствие действия антитромбоцитарных антител; плацентарной недостаточности; внутриутробных инфекций (цитомегаловирусной инфекции, токсоплазмоза, краснухи); сепсиса; ДВС-синдрома; хромосомных нарушений (трисомии 18, 13, 21, триплодии); наследственных заболеваний (анемии Фанкони, TAR-синдрома); гемобластоза; аплазии мегокариоцитарного ростка кроветворения; тромбоза; гиперспленизма [4, 9]. Дифференциальная диагностика причин, вызвавших снижение числа тромбоцитов, является основой для назначения терапии, определения прогноза для жизни и здоровья ребенка, установления риска развития подобной патологии у сибсов [5, 17].
В патогенезе иммунной тромбоцитопении лежит реакция взаимодействия антител - иммуноглобулинов класса G с антигенами поверхности тромбоцитов, приводящая к разрушению клеток в ретикуло-эндотелиальной системе [9, 16, 19]. Кроме прямой деструкции тромбоцитов происходит также снижение их продукции мегакариоцитами [6, 8]. Во внутриутробном периоде и периоде новорожденности могут наблюдаться следующие варианты иммунной тромбоцитопении:
1) аллоиммунная тромбоцитопения, возникающая при несовместимости матери и плода по специфическим антигенам тромбоцитов системы НРА (Human Platelet Antigens) и сенсибилизации матери к данным антигенам;
2) трансиммунная тромбоцитопения, при которой разрушение тромбоцитов ребенка происходит аутоантителами матери, страдающей иммунной тромбоцитопенией (ИТП) или системными заболеваниями, сопровождающимися аутосенсибилизацией;
3) аутоиммунная тромбоцитопения, развивающаяся вследствие срыва иммунологической толерантности и выработкой антител к собственным тромбоцитам у ребенка.
Частота случаев возникновения аллоиммунной тромбоцитопении составляет от 1/800 до 1/1000 новорожденных [12, 15]. Наиболее опасным осложнением АТПН являются внутричерепные кровоизлияния во внутриутробном или раннем постнатальном периодах. Тяжелые нарушения, приводящие к инвалидности, регистрируются в 20% случаев АТПН, смертность составляет 15%. Установлено, что в 75% случаев АТПН возникает при несовместимости по гену НРА-1а, когда генотип матери - HPA-1bb, ребенка - HPA-1ab [10, 14]. Причиной АТПН в 15,5% случаев являются антитела к антигену НРА-5b, когда генотип матери - НРА-5аа, ребенка - НРА-5ab, и в 4% случаев - анти-15b антитела, когда генотип матери - НРА-15аа, ребенка - НРА-15ab. Сочетание антител указанных специфичностей выявляется в 5,5% случаев АТПН [18, 20].
При установлении диагноза АТПН учитывают данные акушерского анамнеза, состояния здоровья матери, клинической картины и результатов лабораторных тестов. Для решения вопроса об аллоиммунном характере разрушения тромбоцитов необходимо выявить различия генотипов системы НРА у матери и ребенка, установить наличие антител классов IgG, М в сыворотке крови матери, взаимодействующих с тромбоцитами ребенка, исключить присутствие антитромбоцитарных аутоантител у матери и новорожденного [11, 22]. Результаты исследования применимы для установления тактики ведения пациента, определения риска развития тромбоцитопении у сибсов ребенка [21].
Известен способ определения антитромбоцитарных аутоантител методом проточной цитометрии (Бутина Е.В. и соавт. Пат. №2488114 РФ. Опубл. 20.07.2013; Бюл. №20), который выявляет фиксированные и циркулирующие в плазме крови антитела классов G и М к собственным тромбоцитам. Представленный способ разработан для диагностики и контроля лечения аутоиммунной тромбоцитопении и может быть использован как один из составляющих тестов при исследовании причин тромбоцитопении новорожденного.
Наиболее близким к предлагаемому изобретению является алгоритм диагностики АТПН, включающий генетические (НРА-типирование) и иммунологические тесты (Kaplan С, 2008). Однако имеющийся алгоритм не предусматривает исследование аутосенсибилизации у матери и новорожденного, кроме того, при выявлении антител используются другие методы диагностики - MAIPA (monoclonal antibody specific immobilization of platelet antigens) и MACE (modified antigen capture enzyme-linked immunosorbent assay).
Техническим результатом заявляемого изобретения является создание способа диагностики аллоиммунной тромбоцитопении новорожденного, что необходимо для назначения ребенку адекватной медикаментозной терапии, определения возможности грудного вскармливания, тактики выбора компонентов крови при трансфузиях, установления риска развития тромбоцитопении у детей в данной семье.
Для достижения указанного результата в соответствии с прототипом исследуют НРА-генотипы матери и ребенка, изучают наличие антитромбоцитарных аллоантител в сыворотке крови матери. Отличительными особенностями предлагаемого способа от уже имеющегося являются обязательный скрининг аутоантител как у матери, так и ребенка, и применение метода проточной цитометрии вместо технологии MAIPA и МАСЕ. Данная замена проведена на основании проведенного ранее исследования, подтверждающего высокую специфичность и чувствительность метода проточной цитометрии при исследовании антител к тромбоцитам (Бутина Е.В., 2014).
Способ предусматривает следующую последовательность исследований:
1. Получение препаратов геномной ДНК из образцов периферической крови матери и ребенка. Предпочтение отдается методикам, использующим автоматические станции для выделения и очистки нуклеиновых кислот. Проведение процедуры НРА-типирования ДНК матери и ребенка. Анализ заключается в определении а- и b-форм генов локусов НРА-1, -2, -3, -4, -5, -15 методом полимеразной цепной реакции (ПЦР) с флуориметрической регистрацией продуктов в ходе процесса (ПЦР в реальном времени) с помощью наборов реагентов ТромбоГенТест (Рег. удост. Росздравнадзора №ФСР 2011/12472).
2. Скрининг аутоантител к тромбоцитам в крови матери и ребенка. Исследование осуществляют в соответствии со способом, описанным в патенте на изобретение Российской Федерации №2488114. Способ заключается в определении методом проточной цитометрии процентного содержания тромбоцитов, покрытых иммуноглобулинами классов G и М. Для анализа исследуют собственные тромбоциты и сыворотку крови пациента, причем в качестве маркеров аутоиммунного процесса используют антитела, относящиеся к иммуноглобулинам классов G и М, при этом коэффициент аутосенсибилизции тромбоцитов рассчитывают как отношение количества Anti-Human IgG-позитивных клеток к числу клеток, адсорбирующих анти-СБ41 моноклональные антитела. Значение коэффициента аутосенсибилизции тромбоцитов более 2% без инкубации с аутосывороткой и более 5% после инкубации с аутосывороткой расценивают как наличие у пациента антитромбоцитарных аутоантител, фиксированных на клетках и/или циркулирующих в плазме крови.
3. Скрининг в сыворотке крови матери антител к антигенам тромбоцитов ребенка осуществляется следующим образом: выделение тромбоцитов из периферической крови (а), инкубацию тромбоцитов с аутосывороткой пациента (b), окрашивание моноклональными антителами (с), лазерную проточную цитометрию, анализ и интерпретацию полученных данных (d).
a) Выделение тромбоцитов проводят на градиенте плотности с использованием растворов Хенкса (НПО «Микроген» ТУ 9385-088-1423783-08) и фиколл-урографина (плотность 1,078) (Фиколл 400 NPS400, Урографин 76% N ЛС-001850) с центрифугированием 15 мин при 1200g. Клетки, находящиеся в интерфазном кольце, переносят в пластиковую пробирку и добавляют 4 мл раствора Хенкса, центрифугируют 5 мин при 700g. После удаления супернатанта осадок ресуспензируют в растворе Хенкса, доводя концентрацию тромбоцитов до 5×105/мкл.
b) В две пробирки для проточной цитофлуориметрии вносят по 100 мкл суспензии тромбоцитов ребенка. Затем в одну из пробирок добавляют 100 мкл сыворотки крови матери. Инкубируют 30 мин при комнатной температуре. Далее в обе пробы вносят 2 мл фосфатно-солевого буфера (ФСБ) (БиолоТ), содержащего 0,1% бычьего сывороточного альбумина (БСА) (Sigma). Центрифугируют 5 мин при 3000 g. Надосадочную жидкость удаляют. Процедуру «отмывания» тромбоцитов повторяют 2 раза. Осадок клеток ресуспензируют в 100 мкл ФСБ.
c) В первую пробу вносят 10 мкл моноклональных антител CD41-FITC (Beckman Coulter IOTest pN IM0649V), во вторую - 100 мкл моноклональных антител Goat F(ab')2 Anti-Human IgG-FITC, предварительно разведенных в PBS в соотношении 1:20, в третью - 100 мкл моноклональных антител Anti-Human IgM heavy chain-FITC, предварительно разведенных в PBS в соотношении 1:20. Пробы инкубируют в темноте 20 минут. Затем добавляют по 5 мл буфера ФСБ+БСА и центрифугируют 5 мин при 3000g. Последнюю процедуру повторяют.
d) Образцы исследуют на проточном цитофлуориметре, оснащенном двумя или более флуоресцентными каналами и лазером (длина волны 488 нм). Анализ клеток в образце проводят по трем параметрам: интенсивности прямого и бокового (бидиректного) светорассеяния (линейная шкала), флуоресценции FITC. При анализе первой пробы на графике выбирают регион неповрежденных тромбоцитов и определяют количество клеток, окрашенных моноклональными антителами к CD41. Далее анализируют тот же регион, но во второй пробе. В каждом образце просматривают не менее 2×105 тромбоцитов.
Для определения уровня адсорбции антител на тромбоцитах в норме были исследованы сыворотки крови и тромбоциты 165 здоровых мужчин - доноров крови и/или ее компонентов. Установлено, что в 95,8% случаев относительное содержание тромбоцитов, адсорбировавших на себе аллоантитела IgG, к общему количеству тромбоцитов не превышает 3%. Также менее 3% от общего числа тромбоцитов у 95,1% здоровых лиц фиксируют IgM антитела. Данный показатель был принят за значение нормы. Следовательно, фиксация IgG и/или IgM антител более чем 3% тромбоцитов расценивается как критерий аллосенсибилизации.
Диагностика АТПН в соответствии с предлагаемым способом основана на анализе результатов проведенных исследований:
1. Определение степени совпадения НРА-генотипов матери и ребенка. Генотипы расцениваются как несовместимые при выявлении одного или нескольких сочетаний генов НРА у матери и ребенка: НРА-1bb/HPA-1ab; НРА-5аа/HPA-5ab; НРА-15аа/HPA-1ab.
2. Исследование наличия антитромбоцитарных аутоантител в крови матери. Данный анализ позволяет сделать заключение о возможном влиянии материнских аутоантител на число тромбоцитов у ребенка.
3. Выявление антитромбоцитарных аутоантител в крови ребенка. Диагностируется аутоиммунный механизм разрушения тромбоцитов как причина тромбоцитопении у ребенка.
4. Определение антител в сыворотке крови матери к тромбоцитам ребенка является диагностическим критерием АТПН.
Оценка результатов исследования представлена в таблице 1.
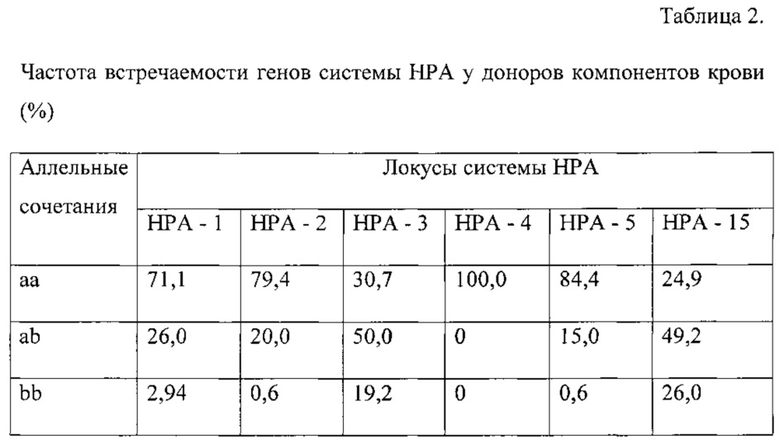
Полиморфизм генов системы НРА исследован у 320 доноров компонентов крови Кировского НИИ гематологии и переливания крови в 2013-2015 годах (Таблица 2). Диагностика иммунных причин тромбоцитопении проведена у 40 детей с числом тромбоцитов в периферической крови менее 150×109/л (от 39 до 133×109/л, медиана - 70×109/л), родившихся в Кировском областном клиническом перинатальном центре в 2015 году. Генетические и иммунологические исследования проведены также у их матерей (40 женщин). При установлении диагноза АТПН учитывались данные акушерского анамнеза, течения настоящей беременности, состояния здоровья женщины, клинической картины заболевания, динамики тромбоцитопении, результатов
При обследовании женщин, дети которых родились с тромбоцитопенией, «генотипы риска» выявлены у 18 из них: генотип HPA-1bb определен у 6 женщин, генотип НРА-5аа - у 8 и генотип НРА-15аа - у 4 женщин. Аллосенсибилизация к антигенам тромбоцитов установлена у восьми матерей: Аллоантитела к тромбоцитам ребенка выявлены у всех женщин с генотипом HPA-1bb и у двух - с генотипом НРА-5аа. Трансиммунный генез тромбоцитопении определен у 8 детей. Проведенный анализ выявил у матерей этих новорожденных наличие аутоантител к тромбоцитам и снижение у них числа тромбоцитов в периферической крови (от 44 до 105×109/л). В остальных случаях лабораторные данные, свидетельствующие об иммунном характере тромбоцитопении, получены не были. Таким образом, иммунный генез тромбоцитопении установлен у 40% детей с низким числом тромбоцитов при рождении. В 50% случаев причиной явились антитромбоцитарные аллоантитела, был поставлен диагноз АТПН. Также в 50% случаев снижение числа тромбоцитов у детей произошло в результате действия материнских аутоантител, был выставлен диагноз - трансиммунная тромбоцитопения.
Ниже приводятся клинические примеры.
Пример 1.
Новорожденный С, 6 день жизни, родился от 3 беременности, 1 родов. Срок гестации 39 недель. Вес при рождении 3440. Число тромбоцитов в периферической крови при рождении 100×109/л,
на 3 день жизни - 80×109/л, на 6 день жизни - 50×109/л. Уровень гемоглобина, эритроцитов и лейкоцитов в норме. Признаки инфекционного процесса отсутствуют. Наследственных заболеваний не выявлено. Геморрагических признаков тромбоцитопении не обнаружено. Число тромбоцитов в периферической крови матери - 250×109/л. Клинический диагноз новорожденного: тромбоцитопения неясной этиологии. Образцы крови матери и ребенка направлены в лабораторию для проведения иммуногематологического и молекулярно-генетического анализа. Исследование осуществлялось в соответствии с предлагаемым способом диагностики аллоиммунной тромбоцитопении новорожденного. Результаты исследований:
НРА-генотип матери: HPA-1bb, 2аа, 3ab, 4аа, 5ab, 15ab.
НРА-генотип ребенка: HPA-1ab, 2ab, 3ab, 4аа, 5ab, 15аа.
Коэффициент аутосенсибилизации к тромбоцитам у матери - 2,6%, у ребенка - 0,8% (оба значения в пределах нормы).
Методом проточной цитометрии в сыворотке крови матери выявлены антитела, адсорбирующиеся на 58,8% тромбоцитов ребенка (в норме не более 3%).
Заключение: Установлен высокий генетически обусловленный риск развития АТПН по антигену НРА-1а (генотип матери HPA-1bb). В сыворотке крови матери выявлены аллоантитела к тромбоцитам ребенка. Лабораторный диагноз: Аллоиммунная тромбоцитопения новорожденного.
Пример 2.
Новорожденный М., 4 день жизни, родился от 3 беременности, 2 родов. Срок гестации 35 недель. Вес при рождении 2440. Число тромбоцитов в периферической крови при рождении 80×109/л, на 4 день жизни - 85×109/л. Уровень гемоглобина, эритроцитов и лейкоцитов в норме. При объективном осмотре клинических проявлений тромбоцитопении нет, очагов инфекции не выявлено, стигмы дизэмбриогенеза отсутствуют. Число тромбоцитов в периферической крови матери 85×109/л. Клинический диагноз новорожденного: тромбоцитопения неясной этиологии.
Образцы крови матери и ребенка направлены в лабораторию для проведения иммуногематологического и молекулярно-генетического анализа. Результаты исследований:
НРА-генотип матери: HPA-1aa, 2аа, 3bb, 4аа, 5ab, 15ab.
НРА-генотип ребенка: HPA-1aa, 2аа, 3bb, 4аа, 5аа, 15аа.
Коэффициент аутосенсибилизации к тромбоцитам у матери - 6,3%, у ребенка - 1,8% (в норме не более 5%).
Методом проточной цитометрии в сыворотке крови матери выявлены антитела, адсорбирующиеся на 10,3%) тромбоцитов ребенка (в норме не более 3%).
Заключение: НРА-генотипы матери и ребенка иммунологически совместимы. В сыворотке крови матери выявлены антитела, реагирующие как с собственными тромбоцитами, так и с тромбоцитами ребенка.
Лабораторный диагноз: Трансиммунная тромбоцитопения новорожденного.
Пример 3.
Новорожденный С., 3 день жизни, родился от 1 беременности, 1 родов. Срок гестации 34 недель. Вес при рождении 2020. Число тромбоцитов в периферической крови при рождении 70×109/л, на 4 день жизни - 55×109/л. Уровень гемоглобина и эритроцитов ниже нормы, лейкоцитов - в норме. При объективном осмотре выявляется петехиальная сыпь на нижних конечностях, очагов инфекции не выявлено. Число тромбоцитов в периферической крови матери 145×109/л. Клинический диагноз новорожденного: тромбоцитопения неясной этиологии.
Образцы крови матери и ребенка направлены в лабораторию для проведения иммуногематологического и молекулярно-генетического анализа. Результаты исследований:
НРА-генотип матери: HPA-1ab, 2аа, 3bb, 4аа, 5ab, 15ab.
НРА-генотип ребенка: HPA-1ab, 2аа, 3ab, 4аа, 5аа, 15аа.
Коэффициент аутосенсибилизации к тромбоцитам у матери - 0,3%, у ребенка - 0,8% (в норме не более 5%).
Методом проточной цитометрии в сыворотке крови матери антитела к тромбоцитам ребенка не выявлены - 0,3% (в норме не более 3%).
Заключение: НРА-генотипы матери и ребенка иммунологически совместимы. Антитромбоцитарные ауто- и аллоантитела не выявлены.
Лабораторный диагноз: Данных за иммунную тромбоцитопению не получено.
Список литературы:
1. Бутина Е.В., Ёлов А.А., Зайцева Г.А., Шерстнев Ф.С. Типирование генов системы НРА у доноров компонентов крови // Клинич. лаб. диагн. - 2011. - №9. - С. 30.
2. Бутина Е.В., Зайцева Г.А., Исаева Н.В. Определение IgG, связанного с тромбоцитами, у пациентов с тромбоцитопенией // Клинич. лаб. диагн. - 2014. - №10. - С. 23-25.
3. Головко O.К., Линчевский Г.Л., Воробьева О.В. Клинические аспекты иммунных тромбоцитопений в неонатологии // Здоровье ребенка. - 2006. - №2. - С. 115-122.
4. Закиров И.И., Сафина А.И. Тромбоцитопении новорожденных // Вестник современной клинической медицины. - 2013. - Т. 6, вып. 6. - С. 102-107.
5. Масчан А.А., Румянцев А.Г. Иммуно-опосредованные тромбоцитопении новорожденных: дифференциальный диагноз и принципы терапии // Вопросы гематологии/онкологии и иммунопатологии в педиатрии. - 2010. - Т. 9, №3. С. 13-18.
6. Масчан А.А., Румянцев А.Г. Иммунная тромбоцитопения у детей: от консенсуса в терминологии к консенсусу в лечении // Вопросы гематологии/онкологии и иммунопатологии в педиатрии - 2010. - Т. 9.- №1. - С. 5-13.
7. Патент №2488114 РФ. Опубл. 20.07.2013; Бюл. №20. «Способ определения аутоантител к тромбоцитам» ФГБУН КНИИГиПК ФМБА России. Авторы: Бутина Е.В., Зайцева Г.А., Исаева Н.В., Васкина Е.А., Докшина И.А.
8. Bassler D, Greinacher A, Okascharoen С, et al. А systematic review and survey of the management of unexpected neonatal alloimmune thrombocytopenia // Transfusion. 2008. - №48. - P. 92-98.
9. Espinoza J.P., Caradeux J., Errol R. Norwitz, Illanes S.E. Fetal and Neonatal Alloimmune Thrombocytopenia // Rev Obstet Gynecol. - 2013. - №6 (1). - P. 15-21.
10. Ghevaert C, Campbell K, Walton J, et al. Management and outcome of 200 cases of fetomaternal alloimmune thrombocytopenia // Transfusion. - 2007. №47. - P. 901-910.
11. Kaplan C. Neonatal alloimmune thrombocytopenia // Haematologica. - 2008. - №93. P. 805-807.
12. Kaplan C. Foetal and neonatal alloimmune thrombocytopaenia // Orphanet J Rare Dis. - 2006. - №1. - P.36-39.
13. Kiefel V, Bassler D, Kroll H, et al. Antigen-positive platelet transfusion in neonatal alloimmune thrombocytopenia (NAIT) // Blood. - 2006. - №107. - P. 3761-3763.
14. Killie MK, Husebekk A, Kjeldsen-Kragh J, Skogen В. A prospective study of maternal anti-HPA la antibody level as a potential predictor of alloimmune thrombocytopenia in the newborn // Haematologica. - 2008. - №93. - P. 870-877.
15. Knight M, Pierce M, Allen D, et al. The incidence and outcomes of fetomaternal alloimmune thrombocytopenia: a UK national study using three data sources // Br J Haematol. - 2011. №152. - P. 460-468.
16. Porcelijn L, Van den Akker ES, Oepkes D. Fetal thrombocytopenia // Semin Fetal Neonatal Med. - 2008. - №13. - P. 223-230. Arnold DM, Smith JW, Kelton JG. Diagnosis and management of neonatal alloimmune thrombocytopenia // Transfus Med Rev. - 2008. - №22. - P. 255-267.
17. Roberts I, Stanworth S, Murray NA. Thrombocytopenia in the neonate // Blood Rev. - 2008. - P. 22. - P. 173-186.
18. Scheffer P, Ait Soussan A, Verhagen O, et al. Noninvasive fetal genotyping of human platelet antigen-la // BJOG. 2011. - №118 - P. 1392-1395.
19. Serrarens-Janssen VM, Semmekrot В A, Novotny VM, et al. Fetal/neonatal alloimmune thrombocytopenia (FMAIT): past, present and future // Obstet Gynecol Surv. - 2008. №63. - P. 239-252.
20. Skogen B, Killie MK, Kjeldsen-Kragh J, et al. Reconsidering fetal and neonatal alloimmune thrombocytopenia with a focus on screening and prevention // Expert Rev Hematol. - 2010. - №3. - P. 559-566.
21. Vinograd CA, Bussel JB. Antenatal treatment of fetal alloimmune thrombocytopenia: a current perspective // Haematologica. - 2010. - №95. - P. 1807-1811.
22. Wu GG, Kaplan C, Curtis BR, Pearson HA. Report of the 14th international society of blood transfusion platelet immunology workshop // Vox Sang. - 2010. - №99. - P. 375-381.
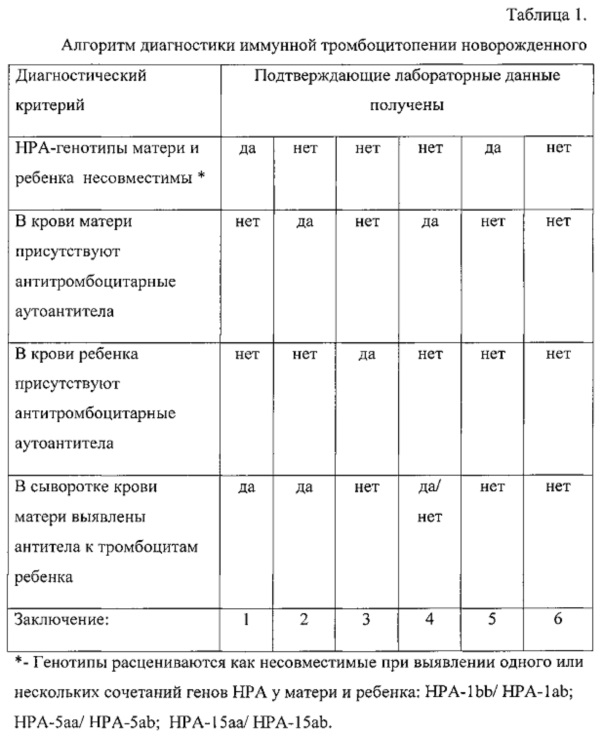
Заключение:
1. Диагностирована аллоиммунная тромбоцитопения новорожденного.
2. Диагностирована трансиммунная тромбоцитопения новорожденного.
3. Диагностирована аутоиммунная тромбоцитопения у ребенка.
4. Диагностирована аутосенсибилизация к антигенам тромбоцитов у матери.
5. Диагностирован генетически обусловленный риск развития АИТН без выявленных антитромбоцитарных антител. Исследование антител следует повторить через 2-6 недели.
6. Данных за иммунную тромбоцитопению новорожденного не получено.
Другие, кроме представленных, сочетания диагностических критериев свидетельствуют о комплексе иммунных процессов, приводящих к тромбоцитопении.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ диагностики аллоиммунной тромбоцитопении новорожденных | 2022 |
|
RU2817215C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АУТОАНТИТЕЛ К ТРОМБОЦИТАМ | 2012 |
|
RU2488114C1 |
| Способ диагностики иммунной нейтропении новорожденного | 2021 |
|
RU2781474C1 |
| АНТИТЕЛА К HPA-1a | 2015 |
|
RU2688627C2 |
| СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, ПРОИСХОДЯЩИЕ ОТ ИММУНОГЛОБУЛИНОВ, КОТОРЫЕ НЕ СТИМУЛИРУЮТ ЛИЗИС, ОПОСРЕДОВАННЫЙ КОМПЛЕМЕНТОМ | 1999 |
|
RU2226196C2 |
| Способ лечения иммунной тромбоцитопении | 2018 |
|
RU2703458C1 |
| СПОСОБ ДИАГНОСТИКИ АУТОИММУННОЙ ТРОМБОЦИТОПЕНИИ | 1993 |
|
RU2036474C1 |
| Способ морфометрической оценки прогноза течения иммунной тромбоцитопении после спленэктомии по индексу соотношения масс CD4+/CD8+ T-лимфоцитов селезенки | 2016 |
|
RU2621627C1 |
| СПОСОБ ПРОФИЛАКТИКИ РАЗВИТИЯ ТРОМБОЦИТОПЕНИИ У БОЛЬНЫХ ХГС В СОЧЕТАНИИ С ИНФЕКЦИЕЙ Helicobacter pylori, ПОЛУЧАЮЩИХ КПВТ | 2013 |
|
RU2536285C1 |
| УСТРОЙСТВО, СОДЕРЖАЩЕЕ ШАРИКИ, ДЛЯ ДИАГНОСТИКИ IN VITRO И ЕГО ПРИМЕНЕНИЯ | 2019 |
|
RU2818259C2 |
Изобретение относится к области медицины, а именно к гематологии, и может быть использовано для диагностики аллоиммунной тромбоцитопении новорожденного. Способ включает в себя типирование генов системы НРА и исследование антитромбоцитарных ауто- и аллоантител. Исследование генов НРА проводится методом ПЦР в режиме реального времени, определение антител к тромбоцитам - методом проточной цитометрии. При выявлении несовместимых сочетаний генов НРА у матери и ребенка НРА-1bb/HPA-1ab; НРА-5аа/HPA-5ab; НРА-15аа/HPA-1ab, выявлении в сыворотке крови матери IgG антител, адсорбирующихся более чем на 3% тромбоцитов ребенка, и при коэффициенте аутосенсибилизации тромбоцитов менее 5% диагностируют аллоиммунную тромбоцитопению новорожденного. Использование данного способа обеспечивает раннюю и точную диагностику аллоиммунной тромбоцитопении новорожденного, что необходимо для назначения адекватной медикаментозной терапии, выбора компонентов крови при трансфузиях. 2 табл., 3 пр.
Способ диагностики аллоиммунной тромбоцитопении новорожденного, включающий в себя типирование генов системы НРА и исследование антитромбоцитарных ауто- и аллоантител, отличающийся тем, что исследование генов НРА проводится методом ПЦР в режиме реального времени, определение антител к тромбоцитам - методом проточной цитометрии, и при выявлении несовместимых сочетаний генов НРА у матери и ребенка НРА-1bb/HPA-1ab; НРА-5аа/HPA-5ab; НРА-15аа/HPA-1ab, выявлении в сыворотке крови матери IgG антител, адсорбирующихся более чем на 3% тромбоцитов ребенка, и при коэффициенте аутосенсибилизации тромбоцитов менее 5% диагностируют аллоиммунную тромбоцитопению новорожденного.
| СПОСОБ ОПРЕДЕЛЕНИЯ АУТОАНТИТЕЛ К ТРОМБОЦИТАМ | 2012 |
|
RU2488114C1 |
| СПОСОБ ДИАГНОСТИКИ АУТОИММУННОЙ ТРОМБОЦИТОПЕНИИ | 1993 |
|
RU2036474C1 |
| US 2005208596 A1, 22.09.2005 | |||
| БУТИНА Е.В | |||
| и др | |||
| Определение IgG, связанного с тромбоцитами, у пациентов с тромбоцитопенией // Клиническая лабораторная диагностика, 2014, N10, стр.23-25 | |||
| МИНЕЕВА Н.В | |||
| и др | |||
| Антигены и антитела к тромбоцитам // Онкогематология, 2013, N3, стр.60-68. | |||
Авторы
Даты
2017-02-21—Публикация
2015-10-12—Подача