Изобретение относится к способу получения N-(5-гидроксиникотиноил)-L-глутаминовой кислоты (I) - перспективного лекарственного средства, которое обладает противогипоксической, антиамнестической активностью и может найти применение в медицине в качестве средства с ноотропным типом действия для лечения патологических состояний, связанных с нарушением памяти, мозгового кровообращения, последствий черепно-мозговых травм, а также в гериатрической практике.
До настоящего времени были известны два способа получения N-(5-гидроксиникотиноил)-L-глутаминовой кислоты (I).
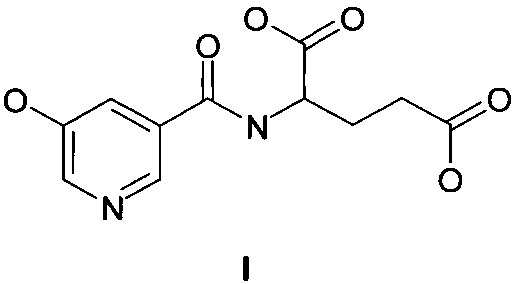
По первому способу (SU 1368314 А1, опубл. 23.01.1988) I получают действием глутаминовой кислоты (II) на азид 5-оксиникотиновой кислоты (III) в присутствии гидроксида натрия в водной среде при 20-23°C.
Способ заключается в том, что 5-оксиникотиновую кислоту (IV) переводят в этиловый эфир кипячением в этиловом спирте в присутствии серной кислоты, который обработкой водным гидразингидратом переводят в гидразид 5-оксиникотиновой кислоты. Из последнего действием нитрита натрия в присутствии водной соляной кислоты получают III, конденсацией которого с II в водно-щелочной среде (pH 8-10) получают I с выходом 35%, считая на IV.
Недостатками данного метода являются низкий выход I, считая на IV, а также необходимость использования неустойчивого, взрывоопасного III, который даже при сушке (40°C) осмоляется и не приемлем в промышленном применении.
Наиболее близким к предложенному является второй способ (RU 2051908 С1, опубл. 10.01.1996), по которому для синтеза I применяют взаимодействие II со смешанным ангидридом 5-оксиникотиновой кислоты. IV обрабатывают метиловым (этиловым, бутиловым или изобутиловым) эфиром хлормуравьиной кислоты для защиты оксигруппы. Полученную 5-метоксикарбонилоксиникотиновую кислоту в присутствии триэтиламина и при температуре от -8 до -16°C обрабатывают бутиловым или изобутиловым эфирами хлормуравьиной кислоты. К полученному смешанному ангидриду добавляют хлоргидрат диэтилового эфира L-глутаминовой кислоты. По окончании реакции снимают защиту с гидроксильной и карбоксильной групп, выделяют целевой продукт и после перекристаллизации из водного спирта получают I с выходом 56-62%, считая на IV.
Недостатками данного способа являются необходимость поддержания низкой температуры от -8 до -16°C на стадии получения смешанного ангидрида 5-оксиникотиновой кислоты, необходимость защиты оксигруппы 5-гидроксиникотиновой кислоты, сложность контроля полноты его образования, а также использование в синтезе дорогостоящих хлорформиатов.
Задачей изобретения является создание более простого способа получения N-(5-гидроксиникотиноил)-L-глутаминовой кислоты (I) без предварительной стадии защиты оксигруппы 5-гидроксиникотиновой кислоты
Задача решается способом получения N-(5-гидроксиникотиноил)-L-глутаминовой кислоты путем взаимодействия производного 5-оксиникотиновой кислоты с производным L-глутаминовой кислоты, в котором в качестве производного 5-оксиникотиновой кислоты используют ее имидазолид, который получают взаимодействием 5-оксиникотиновой кислоты с 1,1'-карбонилдиимидазолом в среде органического растворителя при температуре от 45 до 65°C, в качестве производного L-глутаминовой кислоты используют ее диэтиловый эфир, их взаимодействие проводят в той же среде органического растворителя при температуре от 55 до 85°C и при избытке производного L-глутаминовой кислоты по отношению к производному 5-оксиникотиновой кислоты, выбранном из молярного соотношения от 1,2:1 до 1,5:1, полученный полупродукт гидролизуют щелочным агентом при pH 8-9, подкисляют реакционную массу до pH 3-5 и выделяют целевой продукт.
Кроме того, после гидролиза проводят очистку раствора с помощью сорбента, а выделение целевого продукта осуществляют путем отделения осадка от реакционной массы фильтрацией, суспендирования осадка в воде, подкисления суспензии до pH 3-5, добавления в нее щелочного агента до pH 8-9, очистки полученного раствора с помощью сорбента, подкисления раствора до pH 3-5 и отделения осадка фильтрацией.
Кроме того, используют органический растворитель, выбранный из ряда: диметилформамид, тетрагидрофуран, дихлорметан, толуол.
Кроме того, используют щелочной агент, выбранный из ряда: гидроокись лития, гидроокись натрия, гидроокись калия.
Кроме того, в качестве сорбента используют активированный уголь.
Техническим результатом изобретения является сокращение числа стадий (исключение стадии защиты оксигруппы 5-гидроксиникотиновой кислоты) и исключение необходимости использования низких температур (все стадии проводятся при температурах от +20°C до +85°C)
Предлагается способ получения I, при котором 5-гидроксиникотиновая кислота (IV) переводится в имидазолид 5-гидроксиникотиновой кислоты действием 1,1'-карбонилдиимидазола в подходящем растворителе (ДМФА, тетрагидрофуран, дихлорметан, толуол). Имидазолид 5-гидроксиникотиновой кислоты далее без выделения реагирует с диэтиловым эфиром L-глутаминовой кислоты (V). На заключительной стадии снимают защиту с карбоксильных групп и целевой продукт VI получают после очистки с выходом 70%.
В отличие от предыдущих способов получения I в данном случае не требуется защита оксигруппы 5-гидроксиникотиновой кислоты. Тем самым убирается соответствующая стадия.
Первая и вторая стадии проходят друг за другом в одном реакционном сосуде без выделения промежуточного имидазолида 5-гидроксиникотиновой кислоты. Первую стадию проводят предпочтительно при 45-65°C. Более предпочтительно при 60-65°C.
Предпочтительно проводить вторую стадию при 60-85°C. Более предпочтительно при 80-85°C.
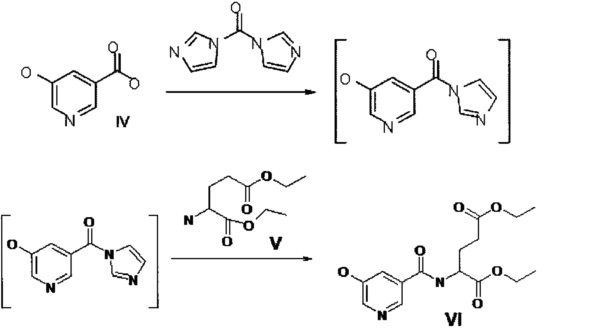
Реакционную массу после завершения второй стадии подвергают концентрированию.
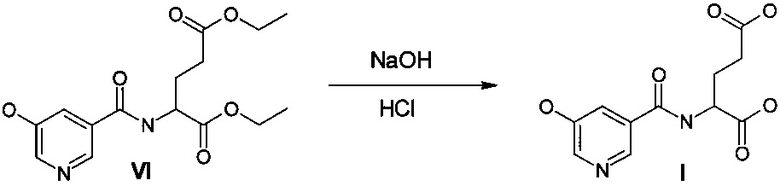
На третьей стадии осуществляют гидролиз сложноэфирных групп с одновременной двухкратной очисткой продукта с использованием активированного угля. Для выделения целевого продукта используют подкисление реакционной массы концентрированной соляной кислотой до pH 3-5. Более предпочтительно подкислять до pH 4.
Стадия получения диэтилового эфира 5-гидрокси-3-карбоксипиридин-L-глутаминовой кислоты проходит ступенчато. Первоначально в реакционной массе параллельно образуются и целевой диэтиловый эфир 5-гидрокси-3-карбоксипиридин-L-глутаминовой кислоты VI (м.в. 324,34) и побочный продукт, содержащий в своей структуре второй фрагмент гидроксиникотиновой кислоты VII (м.в. 445,43):
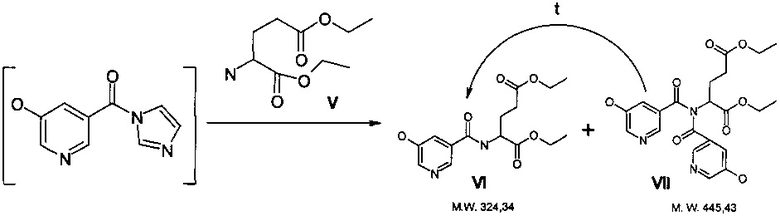
Побочный продукт VII в ходе нагревания до 70-80°C самопроизвольно переходит в целевой продукт VI. Избыток эфира аминокислоты (V) способствует этому процессу. Варьированием соотношения эфира аминокислоты : исходная кислота от 1,1:1 до 1,5:1 было установлено, что соотношение 1,5:1 является оптимальным для прохождения целевой реакции. Длительность выдержки при 80°C составляет от 1 до 2 часов (контроль ВЭЖХ-МС).
Для проведения синтеза предпочтительными растворителями являются ДМФА и толуол. Более предпочтительным является толуол.
Преимуществами предлагаемого способа получения 5-гидрокси-3-карбоксипиридин-L-глутаминовой кислоты I являются:
1) исключение стадии защиты оксигруппы в 5-оксиникотиновой кислоте;
2) увеличение выхода 5-гидрокси-3-карбоксипиридин-L-глутаминовой кислоты I в трехстадийном синтезе по данному способу по сравнению с представленным в RU 2051908 на 8-10% (с 60-62% до 70%);
3) технологичность нового способа получения и возможность масштабирования для промышленного производства;
4) снижение себестоимости производства 5-гидрокси-3-карбоксипиридин-L-глутаминовой кислоты I за счет использования более дешевого реагента (замена дорогостоящих хлорформиатов на дешевый 1,1'-карбонилдиимидазол).
Пример 1
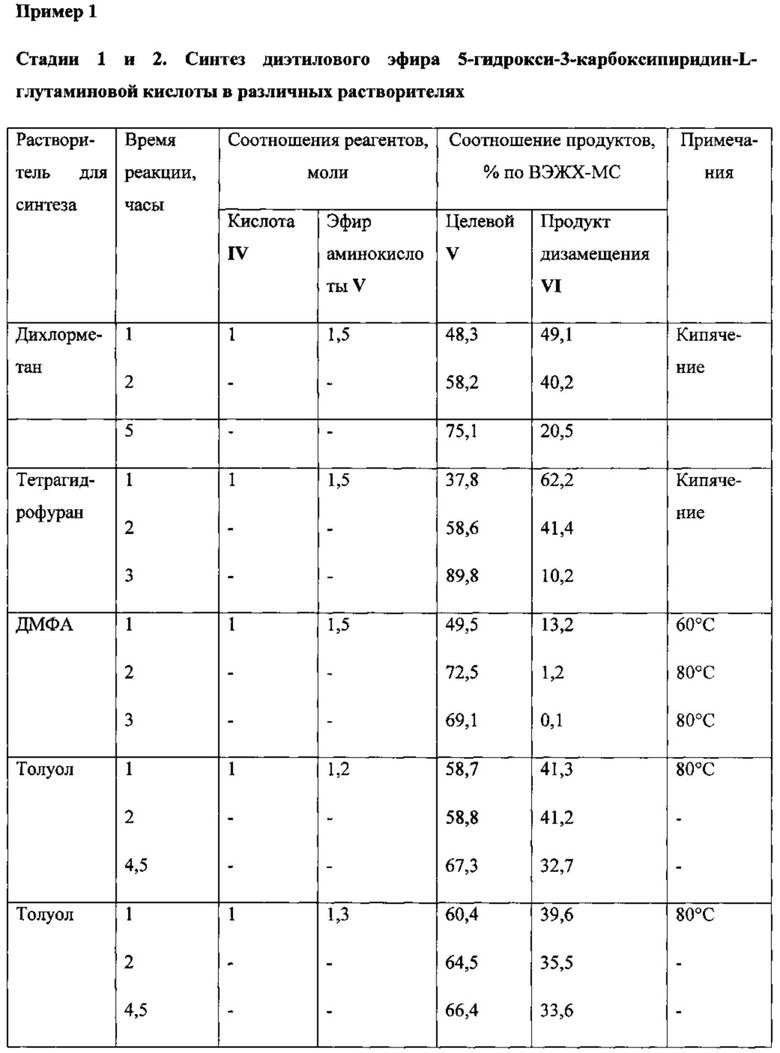
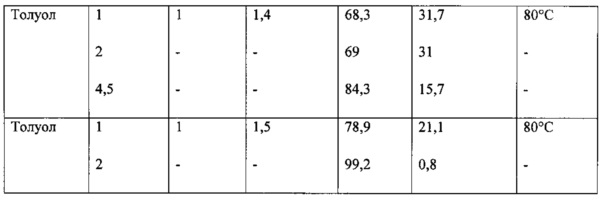
Пример 2
Стадии 1 и 2. Синтез диэтилового эфира 5-гидрокси-3-карбоксипиридин-L-глутаминовой кислоты в ДМФА
В колбе на 500 мл при перемешивании на магнитной мешалке приготовили суспензию 20 г (0,144 м) 5-гидроксиникотиновой кислоты в 300 мл ДМФА и прибавили 29,3 г (0,137 м) 1,1'-карбонилдиимидазола (содержание основного вещества 75,5%). Нагревали до 60-65°C (температура бани) и перемешивали при этой температуре 30 минут. Прилили одной порцией раствор 43,8 г (0,216 м) диэтилового эфира L-глутаминовой кислоты в 50 мл ДМФА, подогрели до 80-85°C (температура бани) и перемешивали при этой температуре 4 часа. Растворитель отогнали при 80°C и 20 мм рт.ст. Вес после концентрирования 95,6 г.
Стадия 3. Гидролиз диэтилового эфира 5-гидрокси-3-карбоксипиридин-L-глутаминовой кислоты
В 0,5 л стакане при охлаждении на водяной бане и магнитном перемешивании приготовили раствор 57,6 г (1,44 м) гидроксида натрия в 230 мл воды. Раствор охладили до комнатной температуры и вылили в 1 л одногорлую колбу с 95,6 г сырца диэтилового эфира 5-гидрокси-3-карбоксипиридин-L-глутаминовой кислоты. Перемешивали на магнитной мешалке при комнатной температуре в течение 2 часов, добавили 8 г активированного угля марки ОУ-А и перемешивали еще 30 минут. Профильтровали от угля на воронке Бюхнера (3 слоя фильтровальной бумаги). Перелили фильтрат в 1 л стакан и при перемешивании механической мешалкой и охлаждении водой со льдом прикапывали концентрированную соляную кислоту до pH 4 (пошло 175 мл). Перемешивали еще 1 час. Осадок отфильтровали на Шотте №3, промыли 3×200 мл водой. Сушили при 55°C и 40 мм рт.ст. в течение 12 часов. Вес 43,2 г (содержание основного вещества 82%, воды 18%). Продукт суспендировали в 0,43 л воды, подкислили при механическом перемешивании до pH 4 (19 мл конц. соляной кислоты). Приготовили раствор 12 г гидроксида натрия в 30 мл воды и подщелочили до pH 8 (пошло 26 мл раствора). К раствору добавили 4 г угля ОУ-А и перемешивали 30 минут. Отфильтровали от угля, промыли водой. Маточник перенесли в стакан с механическим перемешиванием и подкислили конц. соляной кислотой до pH 4. Осадок отфильтровали и промыли на фильтре водой (3×100 мл). Сушили в вакуум-сушильном шкафу при 55°C и 40 мм рт.ст. 24 часов. Вес 31,9 г. Чистота по ВЭЖХ (единичная примесь 0,27%, сумма примесей 0,35%). Тпл. 224,1-224,5°C (лит. 224-226°C).
Суммарный выход на три стадии 66%.
Пример 3
Стадии 1 и 2. Синтез диэтилового эфира 5-гидрокси-3-карбоксипиридин-L-глутаминовой кислоты в толуоле
В 2 л колбе, снабженной механическим перемешиванием, термометром, обратным холодильником с хлоркальциевой трубкой, приготовили суспензию 81 г (0,583 м) 5-гидроксиникотиновой кислоты и 118 г (0,550 м) 1,1'-карбонилдиимидазола (содержание основного вещества 75,5%) в 600 мл толуола. Нагревали до 60-65°C (температура бани) и перемешивали при этой температуре 30 минут. Прилили одной порцией раствор 176 г (0,867 м) диэтилового эфира L-глутаминовой кислоты в 200 мл толуола, подогрели до 80-85°C (температура бани) и перемешивали при этой температуре 1 час. Реакционную массу концентрировали при 60°C и 20 мм рт.ст. Вес после концентрирования 345 г.
Стадия 3. Гидролиз диэтилового эфира 5-гидрокси-3-карбоксипиридин-L-глутаминовой кислоты
В 2 л стакане при охлаждении на водяной бане и магнитном перемешивании приготовили раствор 233 г (5,83 м) гидроксида натрия в 930 мл воды. Раствор охладили до комнатной температуры и вылили в 3 л одногорлую колбу с 345 г сырца диэтилового эфира 5-гидрокси-3-карбоксипиридин-L-глутаминовой кислоты. Перемешивали на магнитной мешалке при комнатной температуре в течение 2 часов, добавили 30 г активированного угля марки ОУ-А и перемешивали еще 30 минут. Профильтровали от угля на воронке Бюхнера (3 слоя фильтровальной бумаги). Перелили фильтрат в 2 л стакан и при перемешивании механической мешалкой и охлаждении водой со льдом прикапывали концентрированную соляную кислоту до pH 4 (пошло 545 мл). Перемешивали еще 1 час. Осадок отфильтровали на Шотте №3, промыли 3×600 мл водой. Сушили при 55°C и 40 мм рт.ст. в течение 12 часов. Вес 143 г (содержание основного вещества 80%, воды 21%). Продукт суспендировали в 0,75 л воды, подкислили при механическом перемешивании до pH 4 (65 мл конц. соляной кислоты). Приготовили раствор 40 г гидроксида натрия в 100 мл воды и подщелочили до pH 8 (пошло 90 мл раствора). К раствору добавили 13 г угля ОУ-А и перемешивали 30 минут. Отфильтровали от угля, промыли водой. Маточник перенесли в стакан с механическим перемешиванием и подкислили конц. соляной кислотой до pH 4. Осадок отфильтровали и промыли на фильтре водой (3×500 мл). Сушили в вакуум-сушильном шкафу при 55°C и 40 мм рт.ст. 24 часов. Вес 103 г. Чистота по ВЭЖХ (единичная примесь 0,19%, сумма примесей 0,39%). Тпл.. 224,4-224,8°C (лит. 224-226°C).
Суммарный выход на три стадии 70%.
Изобретение относится к способу получения N-(5-гидроксиникотиноил)-L-глутаминовой кислоты, которая обладает противогипоксической, антиамнестической активностью и может найти применение в медицине в качестве средства с ноотропным типом действия для лечения патологических состояний, связанных с нарушением памяти, мозгового кровообращения, последствий черепно-мозговых травм, а также в гериатрической практике. Способ заключается во взаимодействии производного 5-оксиникотиновой кислоты с производным L-глутаминовой кислоты. При этом в качестве производного 5-оксиникотиновой кислоты используют ее имидазолид, который получают взаимодействием 5-оксиникотиновой кислоты с 1,1'-карбонилдиимидазолом в среде органического растворителя при температуре от 45 до 65°C, а в качестве производного L-глутаминовой кислоты - ее диэтиловый эфир. Их взаимодействие проводят в той же среде органического растворителя при температуре от 55 до 85°C и при избытке производного L-глутаминовой кислоты по отношению к производному 5-оксиникотиновой кислоты, выбранном из молярного соотношения от 1,2:1 до 1,5:1. Полученный полупродукт гидролизуют щелочным агентом при рН 8-9, подкисляют реакционную массу до рН 3-5 и выделяют целевой продукт. Предлагаемый способ позволяет сократить количество стадий и повысить выход целевого продукта. 4 з.п. ф-лы, 1 табл., 3 пр.
1. Способ получения N-(5-гидроксиникотиноил)-L-глутаминовой кислоты путем взаимодействия производного 5-оксиникотиновой кислоты с производным L-глутаминовой кислоты, отличающийся тем, что в качестве производного 5-оксиникотиновой кислоты используют ее имидазолид, который получают взаимодействием 5-оксиникотиновой кислоты с 1,1'-карбонилдиимидазолом в среде органического растворителя при температуре от 45 до 65°C, в качестве производного L-глутаминовой кислоты используют ее диэтиловый эфир, их взаимодействие проводят в той же среде органического растворителя при температуре от 55 до 85°C и при избытке производного L-глутаминовой кислоты по отношению к производному 5-оксиникотиновой кислоты, выбранном из молярного соотношения от 1,2:1 до 1,5:1, полученный полупродукт гидролизуют щелочным агентом при рН 8-9, подкисляют реакционную массу до рН 3-5 и выделяют целевой продукт.
2. Способ по п.1, отличающийся тем, что после гидролиза проводят очистку раствора с помощью сорбента, а выделение целевого продукта осуществляют путем отделения осадка от реакционной массы фильтрацией, суспендирования осадка в воде, подкисления суспензии до рН 3-5, добавления в нее щелочного агента до рН 8-9, очистки полученного раствора с помощью сорбента, подкисления раствора до рН 3-5 и отделения осадка фильтрацией.
3. Способ по п.1, отличающийся тем, что используют органический растворитель, выбранный из ряда диметилформамид, тетрагидрофуран, дихлорметан, толуол.
4. Способ по п.1, отличающийся тем, что используют щелочной агент, выбранный из ряда гидроокись лития, гидроокись натрия, гидроокись калия.
5. Способ по п.2, отличающийся тем, что в качестве сорбента используют активированный уголь.
| RU 2051908 C1, 10.01.1996 | |||
| @ -Никотиноиламинокислоты, обладающие противогипоксической и антиамнестической активностью | 1984 |
|
SU1368314A1 |
| Устройство для транспортирования материалов | 1976 |
|
SU905154A1 |
Авторы
Даты
2017-03-03—Публикация
2016-03-23—Подача