Изобретение относится к области фармацевтики и медицины, в частности онкологии, и касается новых препаратов, механизм действия которых заключается в том, что они разрушают уже существующие сосуды внутри опухоли, предотвращая тем самым доступ крови и кислорода, жизненно необходимые для выживания солидных опухолей размером более 1 мм3.
Онкология представляет собой область медицины, в которой лечение больных раком пациентов главным образом проводят парентерально (внутривенно), в то время как в пероральной лекарственной терапии имеется только небольшой прогресс.
Пероральная лекарственная терапия является преимущественной с точки зрения удобства и простоты введения. При ускорении разработки пероральных лекарственных средств ожидается, что пероральная лекарственная терапия также будет развиваться быстро.
Хотя для клинического использования были одобрены десятки противораковых соединений, сохраняется постоянная потребность в новых лекарственных средствах, более избирательных, более эффективных и менее токсичных.
Известна фармацевтическая композиция для лечения рака, содержащая гексахлорофен, его производные или их фармацевтически приемлемые соли, состав которой формулируется как таблетки, гранулы, пилюли, порошка, эмульсии, сиропы, растворы, суспензии, аэрозоли или мягкие и твердые желатиновые капсулы. Дозировка композиции при лечении составляет 10-1000 мг/кг в сутки. (KR 20060124031 (А), МПК А61К 31/02; А61К 31/055, опубл. 2006-12-05).
Существенным недостатком известной композиции являются ограниченный спектр цитотоксического действия, направленный только против опухолевых клеток толстой кишки или злокачественной меланомы.
Известна применяемая в виде капсул фармацевтическая композиция на основе дииндолилметана и рыбьего жира, полисорбата-80 и токоферола ацетата, применяемая в течение не менее 12 месяцев в дозировке 400 мг/сут дииндолилметана (RU 2564438, МПК А61К 31/404, А61Р 35/00, опубл. 2015.09.27).
Однако и эта композиция обладает тем же существенным недостатком - ограниченным спектром цитотоксического действия, направленным на лечение онкоурологии, в частности на лечение простатической интраэпителиальной неоплазии (ПИН).
Настоящее изобретение решает задачу создания нового перорального противоопухолевого средства для профилактики или лечения доброкачественных или злокачественных опухолей, каким бы ни было их происхождение или размер, в рамках лечения млекопитающих, в частности человека, резистентных к традиционному лечению.
Данная задача решается тем. что в качестве лекарственного средства предложена желатиновая капсула избирательного разрушения сосудов в опухолях, содержащая в желатиновой оболочке примерно 250-900 мг фармацевтического состава, содержащего противоопухолевого соединения 7-метокси-4-нитро-3-(п-метоксифенил)изохинолинона 16-18 мас.%, кросповидона 5-8 мас.%, гипромелозы 2-3 мас.%, полисорбата 80 1-2 мас.%, натрия лаурилсульфата 0,7-1,2 мас.%, остальное - маннитол.
При создании изобретения было установлено, что сочетание в качестве противоопухолевого соединения 7-метокси-4-нитро-3-(п-метоксифенил)изохинолинона с набором вспомогательных компонентов в комбинации в соответствии с изобретением позволяет осуществлять пероральную лекарственную терапию с максимальным эффектом за счет обеспечения высокой биодоступности, стабильности препарата при хранении и низком уровне побочных эффектов терапии.
Наиболее оптимальным является применение желатиновых капсул, содержащих противоопухолевого соединения 7-метокси-4-нитро-3-(п-метоксифенил)изохинолинона 16,13 мас.%, кросповидона 5,8 мас.%, гипромелозы 2,58 мас.%, полисорбата 80 1,61 мас.%, натрия лаурилсульфата 0,97 мас.%, остальное - маннитол.
Дополнительно желатиновая капсула по любому из перечисленных составов может содержать коллоидный диоксид кремния, в соотношении 1 мас.% от первоначального состава капсулы.
Противоопухолевый компонент, входящий в комбинацию по изобретению, известен из предшествующего уровня техники
Соединение 7-метокси-4-нитро-3-(п-метоксифенил)изохинолинона (далее ЭТИДИН) было описано в международной заявке WO 2011107709 (A1) USE OF ISOQUINOLONES FOR PREPARING DRUGS, NOVEL ISOQUINOLONES AND METHOD FOR SYNTHESISING SAME.
ЭТИДИН - физиологически активное вещество изохинолинового ряда, обладающее противоопухолевой активностью, действие которой связано с разрушением капилляров и угнетением деления клеток, тем самым достигается разрушение уже существующих сосудов внутри опухоли, предотвращающее доступ крови и кислорода, жизненно необходимые для выживания солидных опухолей, в том числе, размером более 1 мм3, при этом не влияя на сосуды окружающих тканей и образование новых сосудов в этих тканях.
Структурная формула ЭТИДИНа
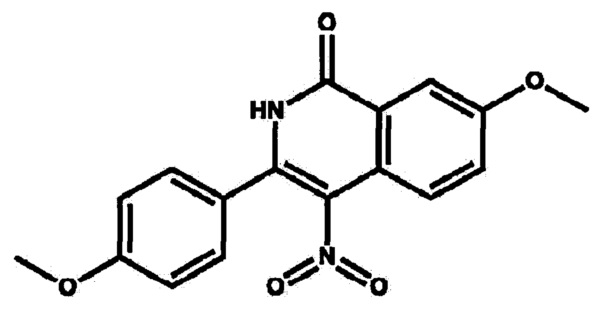
Однако из уровня техники не известна готовая лекарственная форма этого соединения.
Фармацевтическая субстанция ЭТИДИН - мелкокристаллический порошок желтого цвета, практически не растворим в воде и других органических растворителях, обладающий следующими технологическими характеристиками (данные проведенных нами измерений 5 образцов): свободная насыпная плотность 0,42±0,02 г/см3; предельная насыпная плотность 0,63±0,02 г/см3, сыпучесть 1,8±0,06 г/с, угол естественного откоса 47±2 град.
Анализируя представленные данные, можно отметить, что технологические характеристики ЭТИДИН не являются удовлетворительными, непосредственное дозирование в желатиновые капсулы невозможно, поэтому необходимо введение вспомогательных компонентов в состав лекарственной формы с целью придания порошку ЭТИДИН удовлетворительных для получения готовой лекарственной формы технологических характеристик.
Отсутствие источников информации, содержащих ту же совокупность признаков, что и в предлагаемых в изобретении объектах, сообщает им соответствие критерию «новизна».
Та же совокупность признаков позволяет получить новый непредсказуемый эффект - разработка высокоэффективного нового перорального лекарственного средства - Желатиновая капсула, избирательного разрушения сосудов в опухолях, и, таким образом, сообщает ей соответствие критерию «изобретательский уровень».
Получение нового лекарственного средства с использованием известного оборудования с помощью известных компонентов сообщает разработанному изобретению соответствие критерию «промышленная применимость».
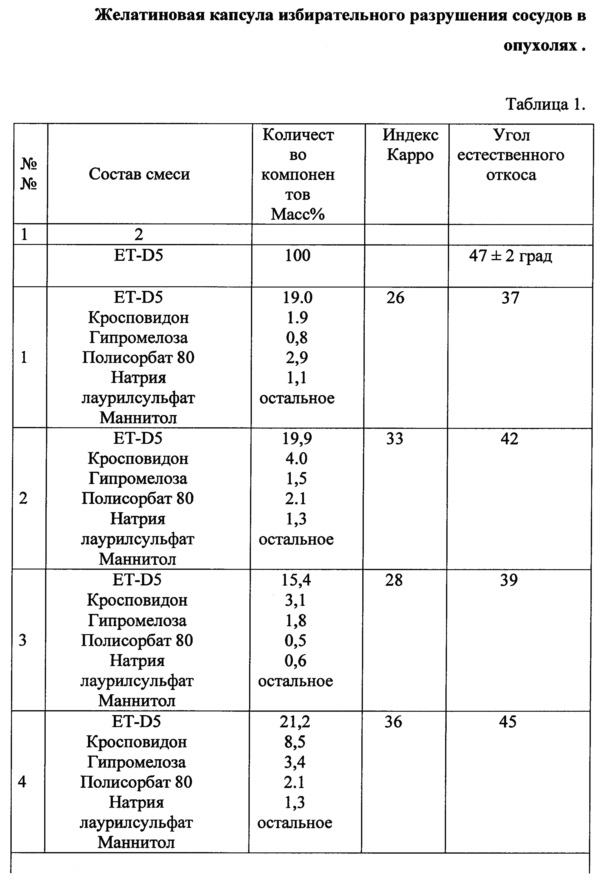
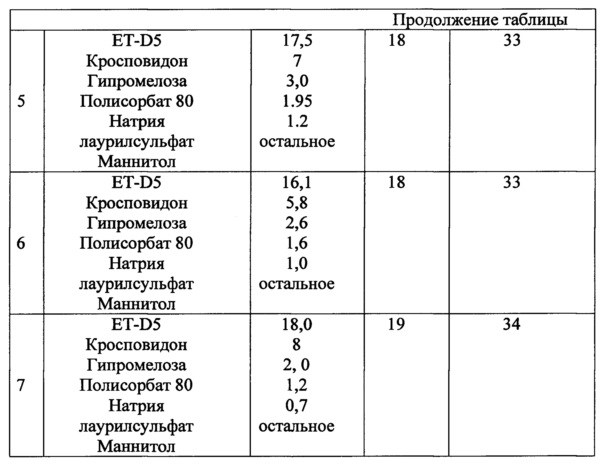
В таблице 1 приведены технологические характеристики вариантов фармацевтического состава избирательного разрушения сосудов в опухолях для наполнения желатиновых капсул.
Приведенные ниже примеры подтверждают, но не ограничивают применение изобретения.
Пример 1. Выбор фармацевтического состава смеси для капсулирования.
На основании изучения научной, научно-технической и патентной литературы в качестве вспомогательных веществ выбраны следующие вещества:
Маннитол (EurPh, JP, USP)
Кросповидон (EurPh, JP, USP)
Гипромелоза (EurPh, USP, BP)
Полисорбат 80 (EurPh, USP, BP)
Натрия лаурилсульфат (EurPh, USP, BP)
Анализ размера частиц ЭТИДИН на лазерном анализаторе SimatsuPH 201, показал, что 90% частиц субстанции имеют размер менее 50 мкм, что позволяет использовать ЭТИДИН без предварительной микронизации.
Учитывая свойства ЭТИДИН, в качестве солюбилизатора в состав смеси вводили натрия лаурилсульфат и полисорбат 80. Для улучшения распадаемости в состав смеси вводили гипромелозу и кросповидон. В качестве наполнителя использовали маннитол, как наиболее оптимальное вспомогательное вещество, заменитель лактозы.
Все компоненты смеси просеивали на вибросите для получения однородного порошка. Смешивание компонентов проводили на Y-образном смесителе фирмы «Эрвека» Германия (рабочий объем 1,5 л), фиксировали крышку с помощью зажимного устройства. С помощью сенсорной панели устанавливали режим смешивания порошка: скорость, время смешивания. Запускали процесс смешивания. Время перемешивания и скорость вращения не оказывали существенного влияния на качество порошковой смеси. Поэтому для дальнейших опытов был выбран режим перемешивания, предлагаемый предприятием-производителем 18 об/мин, 40 мин.
Количество вспомогательных веществ варьировалось в зависимости от состава смеси до получения однородной массы, сохраняющей свойства сыпучести. Технологические характеристики вариантов
фармацевтического состава избирательного разрушения сосудов в опухолях для наполнения желатиновых капсул приведены в таблице 1.
Как видно из приведенной таблицы введение вспомогательных компонентов по изобретению (составы 5-7) позволяет существенно уменьшить склонность ЭТИДИН к слеживанию, уменьшает ее гигроскопичность, повышает сыпучесть.
Таким образом, можно констатировать, что предлагаемый состав порошковой смеси для капсулирования имеет в значительной степени улучшенные технологические характеристики, чем основное действующее вещество, что, в свою очередь, может быть использовано для получения пероральной формы - твердых желатиновых капсул.
Дополнительные испытания показали, что введение указанных вспомогательных компонентов в заявляемых пределах устраняет также пылеобразование, повышает смачиваемость и растворимость активной субстанции, что дает возможность гомогенизировать структуру порошковой смеси и улучшить связанные с этим технологические свойства, в частности улучшить абсорбции в желудочно-кишечном тракте и распределить вещества в организме. В составе новой лекарственной формуляции, созданной нами на основе современного технологического решения, ЭТИДИН быстро проникает в кровоток и попадает в органы-мишени, где достигает концентраций, многократно превышающих таковые для кристаллического вещества.
Введение вспомогательных веществ также обеспечивает высокую точность дозирования препаратов, уменьшая отклонение от средней массы, снижает влияние температуры и влажности окружающей среды на качество порошка, а следовательно, и на качество готового продукта.
Пример 2. Получение фармацевтического состава для капсулирования с улучшенными фармакологическими свойствами.
То же, что и примере 1, кроме того, для вывода токсинов из желудочно-кишечного тракта с сохранением нормальных компонентов флоры и полезных веществ в фармацевтический состав, содержащий противоопухолевого соединения 7-метокси-4-нитро-3-(п-метоксифенил)изохинолинона 16-18 мас.%, кросповидона 5-8 мас.%, гипромелозы 2-3 мас.%, полисорбата 80 1-2 мас.%, натрия лаурилсульфата 0,7-1,2 мас.%, остальное - маннитол, дополнительно на стадии перемешивания вводили коллоидный диоксид кремния в виде препарата аэросил Aeroperl® 300 pharma (Evoniklndustries, ФРГ) в соотношении 1:100 к первоначальному составу.
Aeroperl® 300 pharma представляет собой гранулы сферической формы. Средний размер гранул около 30 мкм. Обладает высокой удельной поверхностью (300 м2/г), развитой системой мезо и макропор, которые обладают удельным объемом порядка 2,5 мл/г.
Пример 3. Получение желатиновых капсул.
Для получения капсулированного продукта был взят фармацевтический состав 6, содержащий:
Получение твердых желатиновых капсул осуществляли на ручной капсулонаполняющей машине MF-30. Наполнение вели в твердые желатиновые капсулы №0.
Всего было получено три серии твердых желатиновых капсул, содержащих по 50, 100 и 150 мг ЭТИДИН в количестве по 1000 штук.
Оценку качества полученных капсул осуществляли в соответствии с требованиями общей фармакопейной статьи ГФ XI «Капсулы».
Показатели качества твердых желатиновых капсул с продуктом
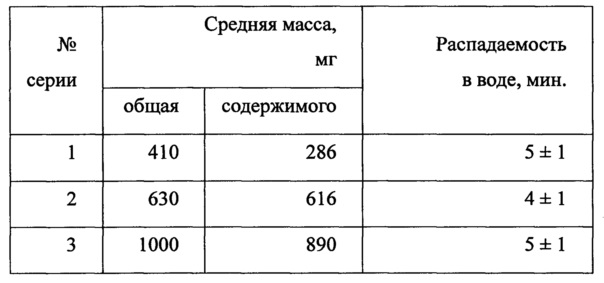
Как следует из приведенных данных, растворимость активной субстанции не превышает допустимые нормы.
Пример 4. Оценка специфической противоопухолевой активности лекарственной формы ЭТИДИН в отношении первичных злокачественных опухолей головного мозга на модели глиобластомы крысы 101/8.
Для решения поставленных задач исследуемый препарат вводили трехкратно крысам Вистар с привитой интракраниальной опухолью глиобластомой 101/8 перорально. Контроль был представлен группой крыс с глиобластомой, без лечения. На первом этапе исследования животные получали исследуемый препарат трехкратно (на 2, 5 и 8 день после имплантации опухоли). Из каждой группы 50% животных выведены из эксперимента на 14-е сутки после имплантации опухоли для проведения морфологической оценки. Показателями эффективности препарата служили увеличение средней продолжительности жизни животных (УПЖ), количество выживших животных в группе, результаты морфометрического анализа неоангиогенеза, индекс обновления клеток опухоли, показатель выраженности лекарственного патоморфоза опухоли. Оставшиеся 50% животных находились под наблюдением на протяжении срока жизни, но не более 60 дней после интракраниальной имплантации опухоли.
Для оценки дозо-зависимого эффекта животные с привитой глиобластомой 101/8 получили интенсивный режим введения: 4-кратное введение по 100 мг/кг перорально на 2, 5, 8 и 14 день ЭТИДИН. По вышеописанному протоколу проводили оценку специфической активности препаратов и сравнивали с соответствующими значениями, полученными при режиме введения на 2, 5 и 8 день. Статистическая обработка материала была проведена с использованием пакета STATSOFT STATISTICA 6.1. Все полученные данные были проверены на соответствие нормальному распределению методом Колмогорова-Смирнова, последующий сравнительный статистический анализ проводили непараметрическими методами с подсчетом среднего значения, медианы и квартального разброса. Достоверности различия между группами оценивали по U-критерию Манна-Уитни. Для сравнения экспериментальных групп был применен однофакторный дисперсионный анализ ANOVA, для множественного сравнения - метод Коновера.
Результаты проведенного исследования влияния терапии разработанными лекарственными формами ЭТИДИН на увеличение продолжительности жизни крыс «Вистар» показали статистически значимое увеличение продолжительности жизни животных опытных групп по сравнению с группой Контроля (глиобластома крысы 101/8 без лечения). Наилучшие результаты показаны в группах животных, получавших желатиновые капсулы, содержащие ЭТИДИН в дозировке 100 мг/кг.
Препарат может выпускаться в трех дозировках по 50, 100 или 150 мг противоопухолевого соединения 7-метокси-4-нитро-3-(п-метоксифенил)изохинолинона в капсуле. Конкретный уровень терапевтически эффективной дозы для конкретного пациента может варьировать в обеспечивающем эффективность диапазоне в зависимости от возраста, веса тела пациента, тяжести заболевания, вида опухоли, способа введения и других известных факторов. Кроме того, более выраженный противоопухолевый эффект лекарственного средства по изобретению сопровождается более низким уровнем токсичности, что позволит исключить возможность проявления отрицательных побочных эффектов у пациента.
Как видно из приведенных примеров, предлагаемый состав желатиновых капсул позволяет получить пероральную лекарственную форму, обладающую избирательным разрушением сосудов в опухолях.
Желатиновая капсула избирательного разрушения сосудов в опухолях относится к области фармацевтики и медицины, в частности онкологии, и касается новых препаратов, механизм действия которых заключается в том, что они разрушают уже существующие сосуды внутри опухоли, предотвращая тем самым доступ крови и кислорода, жизненно необходимые для выживания солидных опухолей размером более 1 мм. Капсула содержит в желатиновой оболочке примерно 250-900 мг фармацевтического состава, содержащего противоопухолевого соединения 7-метокси-4-нитро-3-(п-метоксифенил)изохинолинона 16-18 мас.%, кросповидона 5-8 мас.%, гипромелозы 2-3 мас.%, полисорбата 80 - 1-2 мас.%, натрия лаурилсульфата 0,7-1,2 мас.%, остальное - маннитол. Настоящее изобретение решает задачу создания нового перорального противоопухолевого средства для профилактики или лечения доброкачественных или злокачественных опухолей, каким бы ни было их происхождение или размер, в рамках лечения млекопитающих, в частности человека, резистентных к традиционному лечению. 2 з.п. ф-лы, 1 табл.
1. Желатиновая капсула избирательного разрушения сосудов в опухолях, содержащая в желатиновой оболочке примерно 250-900 мг фармацевтического состава, содержащего противоопухолевого соединения 7-метокси-4-нитро-3-(п-метоксифенил)изохинолинона 16-18 мас.%, кросповидона 5-8 мас.%, гипромелозы 2-3 мас.%, полисорбата 80 1-2 мас.%, натрия лаурилсульфата 0,7-1,2 мас.%, остальное – маннитол.
2. Желатиновая капсула по п. 1, отличающаяся тем, что она содержит противоопухолевого соединения 7-метокси-3-(4-метоксифенил)нитроизохинолинона-1(2н) 16,1 мас.%, кросповидона - 5,8 мас.%, гипромелозы 2,6 мас.%, полисорбата 80 1,6 мас.%, натрия лаурилсульфата 0,97 мас.%, остальное - маннитол.
3. Желатиновая капсула по любому из пп. 1,2, отличающаяся тем, что она дополнительно содержит коллоидный диоксид кремния в соотношении 1:100 к первоначальному составу.
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| СПОСОБ ЛЕЧЕНИЯ ПРОСТАТИЧЕСКОЙ ИНТРАЭПИТЕЛИАЛЬНОЙ НЕОПЛАЗИИ (ПИН) | 2014 |
|
RU2564438C1 |
Авторы
Даты
2017-03-15—Публикация
2015-11-17—Подача