Настоящее изобретение относится к фармацевтической композиции, содержащей комплекс полимерного носителя и переносимого вещества и по меньшей мере один антиген. Комплекс полимерного носителя и переносимого вещества предпочтительно содержит носитель и переносимое вещество, при этом носитель представляет собой поперечно сшитый дисульфидом катионный компонент, а переносимое вещество - по меньшей мере одну молекулу нуклеиновой кислоты. По меньшей мере один антиген предпочтительно выбран из антигена, полученного из патогена, ассоциированного с инфекционной болезнью, антигена, ассоциированного с аллергией или аллергическим заболеванием, антигена, ассоциированного с аутоиммунным заболеванием, или антигена, ассоциированного с раком или опухолевым заболеванием, или в каждом случае из фрагмента, варианта и/или производного указанного антигена. Такая фармацевтическая композиция согласно изобретению может представлять собой, например, вакцину, в которой комплекс полимерного носителя и переносимого вещества может служить в качестве адъюванта для поддержания иммунного ответа на антиген. Соответственно, такая фармацевтическая композиция позволяет эффективно индуцировать адаптивный иммунный ответ, направленный против по меньшей мере одного антигена, входящего в состав такой композиции, в частности, иммунного ответа со сдвигом в сторону Th1.
Настоящее изобретение, кроме того, относится к наборам или наборам частей, содержащим компоненты фармацевтической композиции согласно изобретению, а также к применению фармацевтической композиции согласно изобретению или набора или набора частей согласно изобретению в качестве вакцины, в частности, для лечения инфекционных болезней, аллергии, аутоиммунных заболеваний и опухолевых или раковых заболеваний. Кроме того, изобретение относится к: (a) комплексу полимерного носителя и переносимого вещества для применения в терапии в сочетании с по меньшей мере одним антигеном или его фрагментом, вариантом и/или производным; и (b) по меньшей мере одному антигену или его фрагменту, варианту и/или производному для применения в терапии в сочетании с комплексом полимерного носителя и переносимого вещества, при этом в каждом случае (a) и (b), в частности, для применения в терапии инфекционных болезней, аллергий, аутоиммунных заболеваний и опухолевых или раковых заболеваний.
В настоящее время в случае множества заболеваний требуется введение адъювантов, чтобы обеспечить поддержание на основе врожденного иммунного ответа адаптивного иммунного ответа, в частности, в контексте вакцинаций. Некоторые, но не обязательно все, такие заболевания дополнительно или альтернативно требуют введения лекарственных средств, основанных на пептидах, белках и нуклеиновых кислотах, например, трансфекции нуклеиновых кислот в клетки или ткани. Такие требования обычно означают разные аспекты лечения таких заболеваний и обычно их трудно рассматривать в одном подходе. Как следствие, в предшествующем уровне техники такие аспекты обычно рассматривали, используя отдельные подходы.
В указанном выше контексте, в общем, полагают, что вакцинация является одним из наиболее эффективных и экономичных путей профилактики или лечения заболеваний. Тем не менее, оказалось, что несколько проблем в разработке вакцины трудно решить: вакцины часто бывают неэффективными в случае очень молодых и очень пожилых людей; в случае многих вакцин требуется введение несколько раз, и защита, которую они придают, ослабевает с течением времени, что требует ревакцинации, и в случае некоторых заболеваний, таких как ВИЧ-инфекция, разработка эффективных вакцин является экстренной необходимостью. Общепринято, что многие такие вакцины могут быть разрешены или усовершенствованы, если они могут вызывать более сильный и более продолжительный иммунный ответ.
Соответственно, разработка новых эффективных и безопасных фармацевтических композиций, которые содержат адъюванты, в целях вакцинации, которая поддерживает индукцию и сохранение адаптивного иммунного ответа за счет инициации или стимуляции параллельного врожденного иммунного ответа, представляет собой основную сложную проблему.
Адъюванты обычно определяют как соединения, которые могут повышать и/или модулировать иммуногенность, присущую антигену. Чтобы уменьшить негативные побочные эффекты, новые вакцины имеют более определенный состав, что часто приводит к более низкой иммуногенности по сравнению с предыдущими вакцинами, основанными на целых клетках или вирусах. Таким образом, адъюванты необходимы для того, чтобы они помогали новым вакцинам индуцировать сильные и устойчивые иммунные ответы с дополнительным преимуществом, которое заключается в том, что требуется меньше антигена и меньше инъекций. В настоящее время ясно, что адаптивный иммунный ответ зависит, главным образом, от уровня и специфичности начальных сигналов опасности, распознаваемых присущими организму иммунными клетками после инфекции или вакцинации (Guy, B. (2007), Nat. Rev. Microbiol. 5(7): 505-17). В частности, в случае кандидатов, которые могут стать вакцинами нового поколения, которые будут содержать все больше и больше высоко очищенных рекомбинантных белков и, несмотря на высокую степень безопасности, будут слабо иммуногенными, эффективные адъюванты будут становиться все более необходимыми.
К сожалению, до сих пор доступно только несколько разрешенных к применению адъювантов. Наиболее известными являются квасцы, которые, как известно, являются безопасными, но также представляют собой очень слабый адъювант. Было разработано много дополнительных адъювантов, например, включая введение патогенов, CpG-нуклеотидов и т.д. Однако большинство таких новых или «разработанных» адъювантов еще не удовлетворяют указанным выше требованиям, так как необходимо рассмотреть и решить множество новых возникающих проблем. Такие проблемы, наряду с прочими, включают новые и вновь возникающие инфекционные болезни, многократные введения, угрозу пандемии гриппа и т.д.
Кроме того, новые мишени для вакцин обычно труднее разработать и - вследствие специально заданных иммунных ответов - они требуют более сильных адъювантов для обеспечения успеха. Кроме того, существует значительное количество важных патогенов, для которых в настоящее время у нас даже нет эффективных вакцин. Это является очень сложной целью в будущем. Чтобы обеспечить возможность разработки вакцин против таких мишеней, будут необходимы более эффективные фармацевтические композиции, которые включают в себя адъюванты и такие мишени. Таким образом, в таких композициях будут необходимы новые адъюванты, обеспечивающие определенные преимущества, включая более гетерологичные гуморальные ответы, охватывающие разнообразные патогены, индукцию эффективных функциональных гуморальных ответов, обеспечение гибели или нейтрализации патогенов и индукцию более эффективных T-клеточных ответов для того, чтобы прямо и опосредованно вызвать гибель патогенов, в частности, индукцию цитотоксических T-клеток, которые являются частью иммунного Th1-ответа. Кроме того, адъюванты могут быть необходимы для достижения более прагматичных эффектов, включая снижение дозы антигена и преодоление конкуренции между антигенами в комбинированных вакцинах. Кроме того, на фоне старения популяции, которая становится все более чувствительной к инфекционным болезням, новые адъюванты будут необходимы для преодоления естественного ухудшения иммунного ответа с возрастом (O'Hagan, D. T. and E. De Gregorio (2009), Drug Discov. Today 14(11-12): 541-51).
В обзоре O'Hagan (2009; выше) суммированы некоторые причины острой необходимости в новых эффективных адъювантах, например, необходимость в более низкой дозе антигена в вакцинах, необходимость увеличения широты иммунного ответа и гетерологичной активности, получения сложных комбинированных вакцин и преодоления конкуренции между антигенами, преодоления ограниченного иммунного ответа у некоторых групп населения, таких как пожилые люди, маленькие дети и дети грудного возраста, пациенты с хроническими заболеваниями и нарушенным иммунитетом, повышения ответа эффекторных T-клеток и титра антител, более быстрой индукции защитных ответов, а также увеличения продолжительности ответа за счет усиления ответов B- и T-клеток памяти.
Суммируя вышесказанное, следует отметить, что требуются новые эффективные и безопасные фармацевтические композиции, которые включают в себя иммуностимулирующие средства или адъюванты, которые предпочтительно являются эффективными в индукции врожденного иммунного ответа, в частности, в индукции противовирусного цитокина IFN-альфа; и которые также эффективны в поддержании адаптивного иммунного ответа; безопасны, т.е. не ассоциированы с какими-либо длительными эффектами; которые хорошо переносимы; которые могут быть получены путем простого синтеза; которым нужны недорогие условия хранения (в частности, возможная лиофилизация); которые требуют простых и недорогих компонентов; которые являются биологически разрушаемыми; которые совместимы со многими разными видами вакцинных антигенов; которые можно доставлять совместно с антигеном и иммуностимулятором, и т.д.
Как уже объяснялось выше, адъюванты или иммуностимуляторы обычно действуют благодаря их способности индуцировать врожденный иммунный ответ. Врожденная иммунная система образует преобладающую систему защиты хозяина в большинстве организмов и включает в себя такие барьеры, как гуморальный и химические барьеры, включая, например, воспаление, систему комплемента и клеточные барьеры. Врожденная иммунная система обычно основана на небольшом количестве рецепторов, называемых рецепторами распознавания картины. Они распознают консервативные молекулярные картины, которые позволяют отличать чужеродные организмы, подобные вирусам, бактериям, грибам и паразитам, от клеток хозяина. Такие ассоциированные с патогенами молекулярные картины (PAMP) включают вирусные нуклеиновые кислоты, компоненты бактериальных стенок и стенок грибов, флагеллярные белки и другое. Первым подробно исследованным семейством рецепторов распознавания картины (PAMP-рецепторов) было семейство Toll-подобных рецепторов (TLR). TLR являются трансмембранными белками, которые распознают лиганды во внеклеточной среде или в просвете эндосом. После связывания лиганда они трансдуцируют сигнал через цитоплазматические адаптерные белки, что приводит к запуску защитной реакции хозяина и влечет за собой продуцирование противомикробных пептидов, провоспалительных хемокинов и цитокинов, противовирусных цитокинов и т.д. (смотри, например, Meylan, E., J. Tschopp, et al. (2006), Nature 442 (7098): 39-44). Дальнейшие соответствующие компоненты иммунной системы включают, например, TLR эндосом, цитоплазматические рецепторы, интерфероны типа I и цитоплазматические рецепторы. Таким образом, иммуностимулирующие средства или адъюванты предпочтительно определяют в настоящем описании как индукторы врожденного иммунного ответа, которые активируют рецепторы распознавания картины (PAMP-рецепторы). Таким образом, запускается каскад сигналов, который, например, может приводить к высвобождению цитокинов (например, IFN-альфа), поддерживающих врожденный иммунный ответ. Соответственно, предпочтительным признаком иммуностимулирующего средства или адъюванта является связывание с такими рецепторами и активация таких PAMP-рецепторов. В идеале, такое средство или адъювант дополнительно поддерживает адаптивный иммунный ответ, например, в результате сдвига иммунного ответа таким образом, чтобы был активирован предпочтительный класс Th-клеток. В зависимости от заболевания или расстройства, подвергаемого лечению, может быть предпочтительным сдвиг в сторону иммунного ответа, основанного на Th1, или в других случаях может быть предпочтительным сдвиг в сторону Th2-иммунного ответа.
В известном уровне техники существуют некоторые многообещающие кандидаты для использования в качестве адъювантов, которые удовлетворяют по меньшей мере некоторым, но не всем, определенным выше необходимым характеристикам.
В качестве примера, среди указанных выше новых разработанных адъювантов можно назвать некоторые нуклеиновые кислоты, подобные CpG-ДНК-олигонуклеотидам или исРНК (иммуностимулирующие РНК), которые оказались многообещающими кандидатами для новых иммуностимулирующих средств или адъювантов, так как они позволяют осуществлять терапевтическую или профилактическую индукцию врожденного иммунного ответа. Понятно, что такие основанные на нуклеиновых кислотах адъюванты обычно требуется эффективно доставлять к месту действия, чтобы обеспечить индукцию эффективного врожденного иммунного ответа без излишней потери активности адъюванта и, в некоторых случаях, без необходимости увеличивать вводимый объем выше переносимых системой уровней.
Одним из способов решить такую проблему может быть трансфекция клеток, которые являются частью врожденной иммунной системы (например, дендритных клеток, плазмацитоидных дендритных клеток (pDC)) иммуностимулирующими нуклеиновыми кислотами, которые являются лигандами PAMP-рецепторов (например, Toll-подобных рецепторов (TLR)), что таким образом может привести к иммуностимуляции лигандами, представляющими собой нуклеиновые кислоты. Дополнительным способом может быть прямая трансфекция основанными на нуклеиновых кислотах адъювантами. Однако все указанные способы обычно ухудшаются в результате неэффективной доставки нуклеиновой кислоты и в связи с этим пониженной активности адъюванта, в частности, при местном введении.
Однако одним из основных недостатков таких основанных на нуклеиновых кислотах способов до настоящего времени является их ограниченная способность проходит через плазматическую мембрану клеток млекопитающих, что приводить к плохому доступу в клетки и неадекватной терапевтической эффективности. До настоящего времени такое затруднение является главной проблемой для применений, основанных на трансфекции нуклеиновыми кислотами, например, биомедицинских разработок и, соответственно, коммерческой успешности многих биофармацевтических средств (смотри, например, Foerg, C. and Merkle, H.P., J. Pharm. Sci. 97, 144-62 (2008).
Трансфекцию нуклеиновых кислот или генов в клетки или ткани исследовали вплоть до настоящего времени в контексте целей трансфекции in vitro и в контексте способов, основанных на генной терапии. Однако в настоящее время нет доступных адъювантов, которые основаны на такой методике доставки генов, которые были бы эффективными и безопасными, в частности, нет лицензированных адъювантов. По-видимому, это обусловлено сложными требованиями для адъювантов в целом в сочетании с проблемами, связанными со стабильностью, которые необходимо решать в случае основанных на нуклеиновых кислотах адъювантах.
Тем не менее, трансфекция нуклеиновых кислот или генов в клетки или ткани, для того чтобы вызвать (врожденный и/или адаптивный) иммунный ответ, по-видимому, обеспечивает многообещающий способ получения новых адъювантов.
Однако во многих из таких способов используют трансфекцию нуклеиновых кислот или генов в клетки или ткани, не имея намерения индуцировать врожденный иммунный ответ. Существуют даже некоторые способы генной терапии, при которых необходимо строго избегать индукции врожденного иммунного ответа. Даже в редких случаях, когда осуществляют вакцинацию с целью индукции адаптивного антигенспецифичного иммунного ответа с использованием введения нуклеиновых кислот, например, в случае противоопухолевых вакцинаций с использованием кодируемых ДНК или мРНК антигенов, индукцию адаптивного иммунного ответа обычно осуществляют в виде активной иммунизации против кодируемого антигена, но не в виде сопутствующей адъювантной терапии, и при этом может требоваться дополнительное введение отдельного адъюванта, чтобы индуцировать врожденный иммунный ответ.
Несмотря на то, что в данной области известно множество способов трансфекции, в настоящее время перенос или встраивание нуклеиновых кислот или генов в клетки индивидуума все еще представляет собой серьезную проблему и еще не найдено удовлетворительное решение. Для решения указанной сложной проблемы в последнее десятилетие разработаны разнообразные способы. Такие способы включают трансфекцию с использованием фосфата кальция, катионных липидов, катионных полимеров и липосом. Другими способами трансфекции являются электропорация и вирусная трансдукция.
Однако, как известно специалисту, системы для переноса или встраивания нуклеиновых кислот или генов должны удовлетворять нескольким требованиям для применений in vivo, которые включают эффективную доставку нуклеиновой кислоты в клетки индивидуума с высокой функциональностью, защиту нуклеиновой кислоты от повсеместно встречающихся нуклеаз, высвобождение нуклеиновой кислоты в клетку, отсутствие проблем, связанных с безопасностью, возможное производство в коммерчески приемлемой форме, масштаб которого можно наращивать, и стабильность при хранении при небольших затратах (например, возможная лиофилизация). Такие требования необходимо добавить к комплексу требований, предъявляемых к адъюванту, особенно когда он находится в форме нуклеиновой кислоты, которая описана выше.
Несколько успешных методик переноса или встраивания нуклеиновых кислот или генов, доступных в настоящее время, основаны на использовании вирусных векторов, таких как аденовирусы, аденоассоциированные вирусы, ретровирусы и вирусы герпеса. Вирусные векторы способны опосредовать перенос генов с высокой эффективностью и возможностью длительной экспрессии генов. Однако острая иммунная реакция («цитокиновая буря»), иммуногенность и основанный на инсерциях мутагенез, обнаруженные в клинических испытаниях генной терапии, вызвали серьезные опасения в отношении безопасности некоторых широко используемых вирусных векторов.
Другое решение проблемы переноса или встраивания нуклеиновых кислот или генов можно найти, используя невирусные векторы. Хотя невирусные векторы не столь эффективны, как вирусные векторы, было разработано множество невирусных векторов для обеспечения безопасной альтернативы. Методики доставки невирусных нуклеиновых кислот были проанализированы с использованием физических (доставка нуклеиновых кислот без носителя) и химических способов (доставка нуклеиновых кислот на основе синтетических векторов). Физические способы обычно включают доставку с помощью инъекции через иглу, электропорации, генной пушки, обработки ультразвуком и гидродинамической доставки, с использованием физической силы, которая приводит к пермеабилизации клеточной мембраны и облегчает перенос генов внутрь клеток. В химических способах обычно используют синтетические или встречающиеся в природе соединения (например, катионные липиды, катионные полимеры, гибридные системы липид-полимер) в качестве носителей для доставки нуклеиновой кислоты в клетки. Хотя был достигнут значительный прогресс в фундаментальной науке и применениях различных невирусных систем доставки нуклеиновых кислот, большинство из способов, не основанных на использовании вирусов, все еще менее эффективны, чем вирусные векторы, особенно для доставки генов in vivo (смотри, например, Gao, X., Kim, K. and Liu, D., AAPSJ9, E92-104 (2007)).
Такие средства для трансфекции, которые определены выше, обычно были успешно использованы по отдельности в реакциях in vitro. Однако в случае применения нуклеиновых кислот in vivo, должны быть удовлетворены дополнительные требования. Например, комплексы, образованные между нуклеиновыми кислотами и средствами для трансфекции, должны быть стабильными в физиологических растворах соли в отношении агломерации. Кроме того, такие комплексы обычно не должны взаимодействовать с частями системы комплемента хозяина и, следовательно, не должны быть иммуногенными сами по себе, так как носитель сам по себе не должен индуцировать адаптивный иммунный ответ у индивидуума. Кроме того, комплекс должен защищать нуклеиновую кислоту от раннего внеклеточного разрушения повсеместно встречающимися нуклеазами.
В данной области доступно много реагентов для трансфекции, в частности катионные липиды, которые проявляют превосходную активность при трансфекции в культуре клеток. Однако большинство таких реагентов для трансфекции не могут хорошо работать в присутствии сыворотки, и только немногие активны in vivo. Происходит сильное изменение размера, поверхностного заряда и липидного состава в том случае, когда липоплексы подвергаются воздействию огромного количества отрицательно заряженных и часто амфипатических белков и полисахаридов, которые присутствуют в крови, слизистой, жидкости эпителиальной выстилки или тканевом матриксе. После введения in vivo липоплексы склонны взаимодействовать с отрицательно заряженными компонентами крови и образовывать крупные агрегаты, которые могут абсорбироваться на поверхности циркулирующих эритроцитов, улавливаться в густом слизистом слое или накапливаться в просветах микрососудов, что препятствует достижению ими целевых клеток в отдаленных местах. Некоторые даже подвергаются растворению после того, как они поступают в кровообращение (смотри, например, Gao, X., Kim, K. and Liu, D., AAPSJ9, E92-104 (2007)).
В одном из многообещающих способов используют катионные полимеры. Катионные полимеры оказались эффективными при трансфекции нуклеиновых кислот, так как они могут образовать прочные комплексы и конденсировать отрицательно заряженную нуклеиновую кислоту. Таким образом, был исследован ряд катионных полимеров в качестве носителей для доставки генов in vitro и in vivo. Такие катионные полимеры включают полиэтиленимин (PEI), полиамидоамин и дендримеры полипропиламина, полиаллиламин, катионный декстран, хитозан, катионные белки и катионные пептиды. Хотя большинство катионных полимеров обладают функцией конденсации ДНК в небольшие частицы и способствуют захвату клетками в результате эндоцитоза посредством взаимодействия зарядов с анионными участками на клеточной поверхности, их активность в трансфекции и токсичность сильно отличаются.
Только в одном способе, известном в данной области, описанном Fotin-Mleczek с соавторами (WO 2009/030481), было показано иммуностимулирующее действие РНК в комплексе с короткими катионными пептидами. Такие препараты, по-видимому, эффективно индуцируют продукцию цитокинов в иммунокомпетентных клетках. К сожалению, Fotin-Mleczek с соавторами не оценивали индукцию такими комплексами предпочтительного противовирусного цитокина IFN-α. Кроме того, такие комплексы оказались нестабильными во время лиофилизации.
В указанном выше контексте катионные полимеры проявляют повышенную эффективность в трансфекции по мере увеличения молекулярной массы. Однако увеличение молекулярной массы также приводит к повышению токсичности катионного полимера. В указанном выше контексте (высокомолекулярный) PEI является, пожалуй, наиболее активным и наиболее изученным полимером для трансфекции нуклеиновых кислот, в частности, в целях доставки генов. К сожалению, он имеет такой же недостаток вследствие его биологически не разрушаемой природы и токсичности. Кроме того, даже несмотря на то, что полиплексы, образованные высокомолекулярными полимерами, имеют улучшенную стабильность в физиологических условиях, полученные данные показали, что такие полимеры могут препятствовать распаковыванию вектора. Чтобы преодолеть такое негативное влияние, Read с соавторами (смотри Read, M.L. с соавторами, J. Gene Med. 5, 232-245 (2003); и Read, M.L. с соавторами, Nucleic Acids Res. 33, e86 (2005)) разработали новый тип синтетического вектора, основанного на линейном восстанавливаемом катионе (RPC), получаемом в результате окислительной поликонденсации пептида Cys-Lys10-Cys. Такой пептид Cys-Lys10-Cys может быть расщеплен во внутриклеточной среде, что способствует высвобождению нуклеиновых кислот. В данном контексте Read с соавторами (2003, выше) смогли показать, что полиплексы, образованные такими RPC, подвергаются дестабилизации в восстанавливающих условиях, обеспечивая эффективное высвобождение ДНК и мРНК. Однако исследование эффективности трансфекции in vitro, проведенное Read с соавторами (2003, выше), также показало, что отношения N/P (атомов азота к атомам фосфора), равные 2, были неудовлетворительными, и были необходимы более высокие отношения N/P для улучшения эффективности трансфекции. Кроме того, Read с соавторами (2003, выше) обнаружили, что дополнительно были необходимы хлорохин или катионный липид DOTAP для повышения эффективности трансфекции до адекватных уровней. В результате Read с соавторами (2005, выше) включили остатки гистидина в RPC, которые обладают известной буферной способностью в эндосомах, и показали, что такие обогащенные гистидином RPC могут расщепляться во внутриклеточной восстанавливающей среде. Такой способ позволил осуществить эффективную доставку в цитоплазму широкого диапазона нуклеиновых кислот, включая плазмидную ДНК, мРНК и молекулы миРНК, без необходимости в эндосомолитическом агенте хлорохине.
К сожалению, ни Read с соавторами (2003, выше), ни Read с соавторами (2005, выше) не оценивали, могут ли RPC непосредственно быть использованы в применениях in vivo. В их исследовании, проведенном в 2005 году, трансфекцию осуществляли в отсутствие сыворотки, чтобы избежать маскировки способности остатков гистидина усиливать перенос генов, которая могла возникнуть в результате связывания белков сыворотки с полиплексами, ограничивающего захват клетками. Однако предварительные эксперименты показали, что на трансфицирующие свойства полиплексов обогащенных гистидином RPC может влиять присутствие сывороточных белков, при этом происходит снижение на 50% количества GFP-позитивных клеток, наблюдаемое в случае 10% FCS. Для применения in vivo Read с соавторами (2005, выше) предложили модификации гидрофильным полимером поли-[N-(2-гидроксипропил)метакриламид]. К сожалению, они не смогли предотвратить агрегацию полиплексов и связывание поликатионных комплексов с сывороточными белками. Кроме того, образуются сильно заряженные катионные комплексы (положительный дзета-потенциал) при образовании комплексов нуклеиновой кислоты вследствие большого избытка катионного полимера, для которого характерно высокое соотношение N/P. Соответственно, такие комплексы имеют только ограниченное применение in vivo из-за их сильной тенденции к индуцируемой солью агломерации и взаимодействиям с содержимым сыворотки (опсонизации). Кроме того, такие (положительно заряженные) комплексы могут вызывать активацию комплемента при использовании в целях генной терапии. Также оказалось, что в случае таких положительно заряженных основанных на RPC комплексах наблюдается плохая трансляция переносимой нуклеиновой кислоты после местного введения в дерму.
В одном способе, подобном способу Read с соавторами, McKenzie с соавторами (McKenzie, D. L, K. Y. Kwok, et al. (2000), J. Biol. Chem. 275(14): 9970-7 и McKenzie, D. L, E. Smiley, et al. (2000), Bioconjug. Chem. 11(6): 901-9), разработали поперечно сшивающие пептиды в качестве средств доставки путем встраивания множества цистеинов в короткие синтетические пептиды. В своих исследованиях они изучали оптимальное образование комплексов с ДНК, и в результате они смогли показать, что соотношение N/P, составляющее по меньшей мере 2, необходимо для полностью образованных конденсатов пептид-ДНК. Таким образом, только положительно заряженные комплексы, по-видимому, демонстрируют оптимальную конденсацию ДНК. В противоположность таким данным они предложили разработку отрицательно заряженных комплексов для доставки генов in vivo, так как в предыдущих исследованиях было показано, что внутривенное применение электроположительных конденсатов ДНК приводит к быстрой опсонизации и неспецифичному биораспределению в легкие и печень (Collard, W. T., Evers, D. L, McKenzie, D. L, and Rice, K. G. (2000), Carbohydr. Res. 323, 176-184). Таким образом, McKenzie с соавторами (2000; выше) предложили дериватизацию носителей полиэтиленгликолем и направленными к мишени лигандами. Следует отметить, что способ McKenzie с соавторами (2000, выше) является дополнительным объектом патента (US 6770740 B1), в котором, в частности, раскрыта трансфекция кодирующих нуклеиновых кислот, антисмысловых нуклеиновых кислот и рибозимов.
Таким образом, применение нуклеиновых кислот in vivo, по-видимому, остается до сих пор одной из наиболее сложных проблем, так как белки плазмы с анионными зарядами могут неспецифично связываться с положительно заряженными комплексами и быстро удалять их, например, через ретикулоэндотелиальную систему. Опсонизация и активация системы комплемента катионными комплексами является дополнительным физиологическим явлением, которое может участвовать в снижении эффективности вводимых in vivo катионных комплексов. Это особенно применимо к введению основанных на нуклеиновых кислотах лекарственных средств, например, к трансфекции нуклеиновых кислот в клетки и ткани, особенно если предполагается экспрессия кодируемого белка или пептида или транскрипция РНК с трансфицируемой нуклеиновой кислоты.
Суммируя вышесказанное, следует сказать, что известный уровень техники не обеспечил возможные средства или способы, которые позволяют получить эффективные и безопасные фармацевтические композиции, которые содержат адъюванты, для целей вакцинации, особенно если требуется сдвинутый в сторону Th1 иммунный ответ.
Соответственно, целью настоящего изобретения является предоставление таких средств или способов, которые решают одну из нескольких указанных проблем.
Основополагающая цель настоящего изобретения решается за счет объекта настоящего изобретения, предпочтительно объекта, указанного в прилагаемой формуле изобретения.
Для ясности и четкости приведены следующие определения. Любые технические признаки, раскрываемые таким образом, могут быть частью всех без исключения вариантов осуществления изобретения. Дополнительные определения и пояснения могут быть приведены в контексте настоящего описания.
Нуклеиновая кислота: Термин «нуклеиновая кислота» обычно означает любую ДНК- или РНК-молекулу и используется как синоним термина «полинуклеотид». Кроме того, модификации или производные нуклеиновой кислоты, которая определена в настоящем описании, однозначно включены в общий термин «нуклеиновая кислота». Например, PNA также включена в термин «нуклеиновая кислота».
Моноцистронная РНК: Моноцистронная РНК обычно может представлять собой РНК, предпочтительно мРНК, которая кодирует только одну открытую рамку считывания. Открытая рамка считывания в данном контексте представляет собой последовательность нескольких нуклеотидных триплетов (кодонов), которые могут быть транслированы в пептид или белок.
Би-/полицистронная РНК: РНК, предпочтительно мРНК, которая обычно может иметь две (бицистронная) или более (полицистронная) открытых рамок считывания (ORF). Открытая рамка считывания в данном контексте представляет собой последовательность нескольких нуклеотидных триплетов (кодонов), которая может быть транслирована в пептид или белок.
5'-кэп-структура: 5'-кэп обычно представляет собой модифицированный нуклеотид, в частности, гуаниновый нуклеотид, добавляемый к 5'-концу РНК-молекулы. Предпочтительно 5'-кэп добавляют, используя 5'-5'-трифосфатную связь.
Поли(C)-последовательность: Поли(C)-последовательность обычно представляет собой длинную последовательность цитозиновых нуклеотидов, обычно от примерно 10 до примерно 200 цитидиновых нуклеотидов, предпочтительно от примерно 10 до примерно 100 цитидиновых нуклеотидов, более предпочтительно от примерно 10 до примерно 70 цитидиновых нуклеотидов или еще более предпочтительно от примерно 20 до примерно 50 или даже от примерно 20 до примерно 30 цитидиновых нуклеотидов. Поли(C)-последовательность предпочтительно может быть локализована с 3'-стороны от кодирующей области, входящей в состав нуклеиновой кислоты.
Поли(A)-хвост: Поли(A)-хвост, также называемый «3'-поли(A)-хвостом», обычно представляет собой длинную последовательность адениновых нуклеотидов длиной примерно до 400 аденозиновых нуклеотидов, например, от примерно 25 до примерно 400, предпочтительно от примерно 50 до примерно 400, более предпочтительно от примерно 50 до примерно 300, еще более предпочтительно от примерно 50 до примерно 250, наиболее предпочтительно от примерно 60 до примерно 250 аденозиновых нуклеотидов, добавляемых к 3'-концу РНК.
Стабилизированная нуклеиновая кислота: Стабилизированная нуклеиновая кислота обычно может быть по существу резистентной к разрушению in vivo (например, разрушению экзо- или эндонуклеазой) и/или разрушению ex vivo (например, в процессе производства перед введением вакцины, например, в ходе приготовления раствора вакцины, который необходимо ввести). Стабилизация мРНК может быть достигнута, например, добавлением 5'-кэп-структуры, поли(A)-хвоста, поли(C)-хвоста или любой другой модификации UTR. Стабилизация также может быть достигнута за счет модификации остова или модификации G/C-содержания в нуклеиновой кислоте. В контексте изобретения допустимы различные другие способы.
Модификация нуклеиновой кислоты (модифицированная нуклеиновая кислота): Модификация молекулы нуклеиновой кислоты обычно может включать модификации остова, модификации сахара или модификации оснований. Модификация остова применительно к настоящему изобретению обычно представляет собой модификацию, при которой фосфаты остова из нуклеотидов, входящих в молекулу нуклеиновой кислоты, могут быть химически модифицированы. Модификация сахара применительно к настоящему изобретению обычно может представлять собой химическую модификацию сахара нуклеотидов в нуклеиновой кислоте. Кроме того, модификация оснований применительно к настоящему изобретению обычно может представлять собой химическую модификацию остатка основания нуклеотидов в молекуле нуклеиновой кислоты. Таким образом, модифицированная нуклеиновая кислота также может быть определена в настоящем описании как молекула нуклеиновой кислоты, которая может содержать аналоги нуклеотидов. Кроме того, модификация молекулы нуклеиновой кислоты может включать модификацию липидами. Такая модифицированная липидами нуклеиновая кислота обычно может включать нуклеиновую кислоту, которая определена в настоящем описании. Такая модифицированная липидами молекула нуклеиновой кислоты обычно может дополнительно содержать по меньшей мере один линкер, ковалентно связанный с такой молекулой нуклеиновой кислоты, и по меньшей мере один липид, ковалентно связанный с соответствующим линкером. Альтернативно, модифицированная липидами молекула нуклеиновой кислоты может содержать по меньшей мере одну молекулу нуклеиновой кислоты, которая определена в настоящем описании, и по меньшей мере один (бифункциональный) липид, ковалентно связанный (без линкера) с такой молекулой нуклеиновой кислоты. Согласно третьему альтернативному варианту модифицированная липидом молекула нуклеиновой кислоты может содержать молекулу нуклеиновой кислоты, которая определена в настоящем описании, по меньшей мере один линкер, ковалентно связанный с такой молекулой нуклеиновой кислоты, и по меньшей мере один липид, ковалентно связанный с соответствующим линкером, а также по меньшей мере один (бифункциональный) липид, ковалентно связанный (без линкера) с такой молекулой нуклеиновой кислоты.
Модификация нуклеиновой кислоты также может включать модификацию содержания G/C в кодирующей области молекулы нуклеиновой кислоты, особенно если молекула нуклеиновой кислоты находится в форме мРНК. В данном контексте особенно предпочтительно, чтобы содержание G/C в кодирующей области молекулы нуклеиновой кислоты было увеличено по сравнению с содержанием G/C в кодирующей области конкретной кодирующей последовательности дикого типа, т.е. немодифицированной мРНК. Аминокислотная последовательность, кодируемая последовательностью нуклеиновой кислоты, предпочтительно не модифицирована по сравнению с аминокислотной последовательностью, кодируемой конкретной мРНК дикого типа. Модификация G/C-содержания в молекуле нуклеиновой кислоты, особенно если молекула нуклеиновой кислоты находится в форме мРНК или кодирует мРНК, основана на том факте, что последовательность любой области транслируемой мРНК важна для эффективной трансляции такой мРНК. Таким образом, важны состав и последовательность различных нуклеотидов. В частности, последовательности, имеющие повышенное содержание G (гуанозина)/C (цитозина), более стабильны, чем последовательности, имеющие повышенное содержание A (аденозина)/U (урацила). Таким образом, кодоны кодирующей последовательности или мРНК изменяют по сравнению с кодирующей последовательностью или мРНК дикого типа, при этом сохраняя транслируемую аминокислотную последовательность, так чтобы они содержали повышенное количество G/C-нуклеотидов. Что касается того факта, что несколько кодонов кодируют одну и ту же аминокислоту (так называемая вырожденность генетического кода), то могут быть определены наиболее предпочтительные для стабильности кодоны (так называемое использование альтернативных кодонов). Предпочтительно содержание G/C в кодирующей области молекулы нуклеиновой кислоты, особенно если нуклеиновая кислота находится в форме мРНК или кодирует мРНК, увеличивают по меньшей мере на 7%, более предпочтительно по меньшей мере на 15%, особенно предпочтительно по меньшей мере на 20% по сравнению с содержанием G/C в кодируемой области мРНК дикого типа. Согласно конкретному варианту заменяют по меньшей мере 5%, 10%, 20%, 30%, 40%, 50%, 60%, более предпочтительно по меньшей мере 70%, еще более предпочтительно по меньшей мере 80% и наиболее предпочтительно по меньшей мере 90%, 95% или даже 100% заменяемых кодонов в области, кодирующей белок или пептид, который определен в настоящем описании, или его фрагмент, вариант и/или производное или полную последовательность мРНК дикого типа или кодирующую последовательность, при этом увеличивая содержание G/C в указанной последовательности. В данном контексте особенно предпочтительно увеличение содержания G/C в молекуле нуклеиновой кислоты, особенно если нуклеиновая кислота находится в форме мРНК или кодирует мРНК, до максимума (т.е. 100% заменяемых кодонов), в частности, в области, кодирующей белок, по сравнению с последовательностью дикого типа. Кроме того, модификация нуклеиновой кислоты, особенно если нуклеиновая кислота находится в форме мРНК или кодирует мРНК, основана на данных о том, что эффективность трансляции также определяется разной частотой встречаемости тРНК в клетках. Частота встречаемости тРНК в клетке и, следовательно, использование кодонов в указанной клетке зависит от вида, из которого получена клетка. Соответственно, в дрожжевой клетке обычно наблюдают использование кодонов, которое отличается от использования кодонов в клетке млекопитающего, такой как клетка человека. Таким образом, если так называемые «редкие кодоны» присутствуют в молекуле нуклеиновой кислоты (по отношению к соответствующей системе экспрессии), особенно если нуклеиновая кислота находится в форме мРНК или кодирует мРНК, в повышенной степени, то соответствующая модифицированная молекула нуклеиновой кислоты транслируется в значительно более низкой степени, чем в том случае, когда кодоны присутствуют кодоны кодируют относительно «частые» тРНК. Таким образом, особенно если модифицированная молекула нуклеиновой кислоты находится в форме мРНК или кодирует мРНК, кодирующая область модифицированной нуклеиновой кислоты предпочтительно модифицирована по сравнению с соответствующей областью мРНК дикого типа или кодирующей последовательностью так, что по меньшей мере один кодон последовательности дикого типа, который кодирует тРНК, которая является относительно редкой в клетке, заменяют кодоном, который кодирует тРНК, которая относительно часто встречается в клетке и несет такую же аминокислоту, что и относительно редкая тРНК. При такой модификации последовательности молекулы нуклеиновой кислоты, особенно если нуклеиновая кислота находится в форме мРНК или кодирует мРНК, модифицируют так, чтобы были встроены кодоны, для которых имеются относительно часто встречающиеся тРНК. Другими словами, при такой модификации все кодоны последовательности дикого типа, которые кодируют тРНК, которая является относительно редкой в клетке, может быть в каждом случае заменена на кодон, который кодирует тРНК, которая является относительно частой в клетке и которая в каждом случае несет такую же аминокислоту, что и относительно редкая тРНК. Какие тРНК встречаются относительно часто в клетке и какие наоборот встречаются относительно редко, известно специалисту в данной области; см., например, Akashi, Curr. Opin. Genet. Dev. 2001, 11(6): 660-666. Особенно предпочтительно, чтобы последовательность нуклеиновой кислоты, кодирующая белок, используемый в настоящем изобретении, была оптимизирована по кодонам в соответствии с использованием кодонов у человека. Особенно предпочтительны кодоны, которые используются для конкретной аминокислоты, тРНК для которой встречается наиболее часто, например кодон Gly, в случае которого используется тРНК, которая встречается наиболее часто в (человеческой) клетке. В данном контексте особенно предпочтительно связать содержание G/C в последовательности, которое повышено, в частности максимизировано в модифицированной молекуле нуклеиновой кислоты, особенно если нуклеиновая кислота находится в форме мРНК или кодирует мРНК, с «частыми» кодонами без модификации аминокислотной последовательности белка, кодируемого кодирующей областью молекулы нуклеиновой кислоты. Такой предпочтительный вариант позволяет обеспечивать особенно эффективно транслируемую и стабилизированную (модифицированную) нуклеиновую кислоту, особенно если нуклеиновая кислота находится в форме мРНК или кодирует мРНК.
Производное молекулы нуклеиновой кислоты: Производное молекулы нуклеиновой кислоты обычно означает в настоящем описании модифицированную нуклеиновую кислоту, которая определена выше.
Аналоги нуклеотидов: Аналоги нуклеотидов обычно представляют собой нуклеотиды, структурно сходные (аналогичные) встречающимся в природе нуклеотидам, которые содержат модификации остова, модификации сахара или модификации оснований нуклеотидов.
Модификация UTR: Модификация UTR обычно представляет собой модификацию 5'- и/или 3'-области молекулы нуклеиновой кислоты, особенно кодирующей молекулы нуклеиновой кислоты. В настоящем описании «UTR» обычно означает «нетранслируемую область». UTR может, например, содержать или состоять из стабилизирующей последовательности (UTR-модификация). Такие стабилизирующие последовательности в 5'- и/или 3'-нетранслируемых областях могут оказывать влияние, увеличивая время полужизни нуклеиновой кислоты в цитозоле. Такие стабилизирующие последовательности могут иметь 100% идентичность последовательности с встречающимися в природе последовательностями, которые встречаются в вирусах, бактериях и эукариотах, но также могут быть частично или полностью синтетическими. Нетранслируемые последовательности (UTR) гена (альфа-)глобина, например, из Homo sapiens или Xenopus laevis, могут быть приведены в качестве примера стабилизирующих последовательностей, которые можно использовать для стабилизированной нуклеиновой кислоты. Другой пример стабилизирующей последовательности имеет общую формулу (C/U)CCANxCCC(U/A)PyxUC(C/U)CC, которая входит в 3'UTR очень стабильной РНК, которая кодирует (альфа-)глобин, коллаген типа (I), 15-липоксигеназу или тирозингидроксилазу (см. Holcik et al., Proc. Natl. Acad. Sci. USA 1997, 94: 2410-2414). Такие стабилизирующие последовательности, конечно, можно использовать отдельно или в сочетании с одной другой, а также в сочетании с другими стабилизирующими последовательностями известными специалисту в данной области. В контексте настоящего изобретения модификация UTR предпочтительно означает модификацию кодирующей нуклеиновой кислоты, такой как ген или мРНК, добавлением или заменой 5'- и/или 3'-UTR, предпочтительно добавлением или заменой на стабилизирующую 5'- и/или 3'-UTR, например, такую, которая описана выше.
Синтез нуклеиновой кислоты: Молекулы нуклеиновой кислоты, используемые согласно изобретению, которые определены в настоящем описании, могут быть получены с применением любого способа, известного в данной области, включая способы синтеза, такие как, например, твердофазный синтез, а также способы in vitro, такие как реакции транскрипции in vitro.
Для получения молекулы нуклеиновой кислоты, особенно если нуклеиновая кислота находится в форме мРНК, соответствующая молекула ДНК может быть, например, транскрибирована in vitro. Такая ДНК-матрица предпочтительно содержит подходящий промотор, например, промотор T7 или SP6, для транскрипции in vitro, за которым следует требуемая нуклеотидная последовательность, кодирующая молекулу нуклеиновой кислоты, например, мРНК, которую необходимо получить, и сигнал терминации для транскрипции in vitro. Молекула ДНК, которая образует матрицу для по меньшей мере одной представляющей интерес РНК, может быть получена в результате пролиферации при ферментации и последующего выделения в виде части плазмиды, которая может реплицироваться в бактериях. Плазмидами, которые можно назвать в качестве подходящих для настоящего изобретения, являются, например, плазмиды pT7T (GenBank, номер доступа U26404; Lai et al., Development 1995, 121: 2349-2360), серии pGEM®, например, pGEM®-1 (GenBank, номер доступа X65300; из Promega) и pSP64 (GenBank, номер доступа X65327); см. также Mezei and Storts, Purification of PCR Products, в: Griffin and Griffin (ed.), PCR Technology: Current Innovation, CRC Press, Boca Raton, FL, 2001.
Белок: Белок обычно состоит из одного или нескольких полипептидов, подвергнутых укладке в 3-мерную форму, способствующую осуществлению биологической функции.
Пептид: Пептид обычно представляет собой короткий полимер, состоящий из аминокислотных мономеров, связанных пептидными связями. Обычно он состоит менее чем из 50 мономерных единиц. Тем не менее, термин пептид не исключен в случае молекул, имеющих более 50 мономерных единиц. Длинные пептиды также называют полипептидами, которые обычно имеют от 50 до 600 мономерных единиц, более конкретно от 50 до 300 мономерных единиц. Кроме того, в настоящем описании определение «пептид» также включает любую пептидильную молекулу, включая аналоги пептидов.
Аналоги пептидов: Аналог пептида обычно может содержать встречающиеся в природе или не встречающиеся в природе аминокислоты, которые могут быть использованы в целях изобретения. Например, они могут содержать аминокислоты, выбранные из изостерических или хиральных аналогов (D-аминокислота или L-аминокислота) аминокислоты. Кроме того, аналог может содержать одну или несколько аминокислот, предпочтительно выбранных из гидроксипролина, β-аланина, 2,3-диаминопропионовой кислоты, α-аминоизомасляной кислоты, N-метилглицина (саркозина), орнитина, цитруллина, трет-бутилаланина, трет-бутилглицина, N-метилизолейцина, фенилглицина, циклогексилаланина, норлейцина, нафтилаланина, пиридилаланина, 3-бензотиенилаланина, 4-хлорфенилаланина, 2-фторфенилаланина, 3-фторфенилаланина, 4-фторфенилаланина, пеницилламина, 1,2,3,4-тетрагидроизохинолин-3-карбоновой кислоты, β-2-тиенилаланина, метионинсульфоксида, гомоаргинина, N-ацетиллизина, 2,4-диаминомасляной кислоты, п-аминофенилаланина, N-метилвалина, гомоцистеина, гомосерина, ε-аминогексановой кислоты, δ-аминовалериановой кислоты, 2,3-диаминомасляной кислоты. Аналог пептида, который определен в настоящем описании, может дополнительно включать модифицированные пептиды. Термин специально охватывает модификации пептидного остова (т.е. миметики амидной связи), известные специалистам в данной области. Такие модификации включают модификации по азоту амида, α-углероду, карбонилу амида, полную замену амидной связи, удлинения, делеции или поперечные сшивки остова. Известно несколько модификаций пептидного остова, включая ψ[CH2S], ψ[CH2NH], ψ[CSNH2], ψ[NHCO], ψ[COCH2] и ψ[(E) или (Z)CH=CH]. В использованной выше номенклатуре ψ указывает на отсутствие амидной связи. Структура, которая заменяет амидную группу, указана в скобках. Другие модификации включают, например, N-алкильную (или арильную) замену (ψ[CONR]), или поперечные сшивки остова с образованием лактамов и других циклических структур, C-концевые модификации гидроксиметилом, O-модификации (например, C-концевой гидроксиметилбензиловый эфир), N-концевые модификации, включая замещенные амиды, такие как алкиланилиды и гидразиды.
Синтез пептидов: Пептид, аналог пептида или его производное предпочтительно синтезируют, используя химический способ, известный специалисту в данной области. Например, синтетические пептиды получают, используя известные способы твердофазного синтеза, жидкофазного синтеза или конденсации пептидов или любое их сочетание, и они могут содержать природные и/или неприродные аминокислоты. В общем, способы химического синтеза включают последовательное добавление одной или нескольких аминокислот к растущей пептидной цепи. Обычно либо аминогруппу, либо карбоксильную группу первой аминокислоты защищают подходящей защитной группой. Защищенная или дериватизованная аминокислота затем может быть либо связана с инертной твердой подложкой, либо использована в растворе при добавлении следующей аминокислоты к последовательности, имеющей комплементарную (амино- или карбоксильную) группу, соответствующим образом защищенную, в условиях, которые обеспечивают возможность образования амидной связи. Затем защитную группу удаляют из вновь добавленного аминокислотного остатка и затем добавляют следующую аминокислоту (соответствующим образом защищенную) и так далее. После того, как требуемые аминокислоты связаны в правильной последовательности, любые оставшиеся защитные группы (и любую твердую подложку, если использовали методику твердофазного синтеза) удаляют последовательно или одновременно, чтобы получить конечный полипептид. Такие способы подходят для синтеза пептида, применяемого в целях настоящего изобретения (такого как аналог пептида), или его производного. Типичные защитные группы включают трет-бутилоксикарбонил (Boc), 9-флуоренилметоксикарбонил (Fmoc) бензилоксикарбонил (Cbz); п-толуолсульфонил (Tx); 2,4-динитрофенил; бензил (Bzl); бифенилизопропилоксикарбоксикарбонил, трет-амилоксикарбонил, изоборнилоксикарбонил, о-бромбензилоксикарбонил, циклогексил, изопропил, ацетил, о-нитрофенилсульфонил и тому подобные. Типичные твердые подложки представляют собой поперечно сшитые полимерные подложки. Такие подложки могут включать полимеры на основе дивинилбензола, поперечно сшитого со стиролом, например, сополимеры дивинилбензола-гидроксиметилстирола, сополимеры дивинилбензола-хлорметилстирола и сополимеры дивинилбензола-бензгидриламинополистирола.
Получение рекомбинантного пептида или белка: Пептид, или белок, или его производное могут быть получены с использованием способа получения рекомбинантного белка или пептида. Чтобы обеспечить возможность получения рекомбинантного пептида или белка, предпочтительно выделяют или синтезируют по меньшей мере одну кодирующую их нуклеиновую кислоту. Обычно нуклеиновую кислоту, кодирующую рекомбинантный белок или пептид, выделяют, используя известный способ, такой как, например, амплификация (например, с использованием ПЦР), или выделяют из нуклеиновой кислоты из организма, используя один или несколько ферментов рестрикции, или выделяют из библиотеки нуклеиновых кислот. Для экспрессии белка или пептида способами рекомбинации нуклеиновую кислоту, кодирующую белок/пептид, помещают в функциональной связи с промотором или другой регуляторной последовательностью, способной регулировать экспрессию в бесклеточной системе или в клеточной системе. Например, нуклеиновую кислоту, содержащую последовательность, которая кодирует пептид или белок, помещают в функциональной взаимосвязи с подходящим промотором и поддерживают в подходящей клетке в течение времени и в условиях, достаточных для протекания экспрессии. Типичные экспрессирующие векторы для экспрессии in vitro, бесклеточная экспрессия или основанная на клетках экспрессия были описаны и хорошо известны специалисту. В данном контексте бесклеточные системы экспрессии могут включать фракцию S30 E. coli, лизат ретикулоцитов кролика и экстракт зародышей пшеницы, а клеточная система может быть выбрана из бактериальных клеток (например, E. coli), клеток насекомых, растений или млекопитающих (например, клеток 293, COS, CHO, 1OT, 293T).
Сигнальный пептид секреции: Такие сигнальные пептиды представляют собой последовательности, которые обычно имеют длину примерно от 15 до 30 аминокислот и предпочтительно расположены на N-конце кодируемого пептида, но не ограничены указанным. Сигнальные пептиды, которые определены в настоящем описании, предпочтительно обеспечивают возможность транспорта белка или пептида в определенный клеточный компартмент, предпочтительно на клеточную поверхность, в эндоплазматическую сеть (ER) или компартмент эндосом-лизосом.
Носитель/полимерный носитель: Носитель в контексте изобретения обычно может представлять собой соединение, которое способствует транспорту и/или образованию комплекса с другим соединением. Полимерный носитель обычно представляет собой носитель, который образован из полимера. Носитель в контексте настоящего изобретения предпочтительно подходит в качестве носителя для молекул нуклеиновой кислоты, например, для опосредования растворения в физиологически приемлемых жидкостях, транспорта и захвата клетками молекул нуклеиновой кислоты или вектора. Соответственно, носитель в контексте настоящего изобретения может представлять собой компонент, который может подходить для депонирования и доставки молекулы нуклеиновой кислоты или вектора. Такие носители могут представлять собой, например, катионные или поликатионные носители или соединения, которые могут служить в качестве средства для трансфекции или комплексообразования. Особенно предпочтительными носителями или полимерными носителями в данном контексте являются катионные или поликатионные соединения, включая протамин, нуклеолин, спермин или спермидин или другие катионные пептиды или белки, такие как поли-L-лизин (PLL), полиаргинин, основные полипептиды, проникающие в клетку пептиды (CPP), включая ВИЧ-связывающие пептиды, Tat ВИЧ-1 (ВИЧ), Tat-производные пептиды, пенетратин, производные из VP22 или аналогичные пептиды, VP22 HSV (Herpes simplex), MAP, KALA или домены трансдукции белка (PTD), PpT620, богатые пролином пептиды, богатые аргинином пептиды, богатые лизином пептиды, MPG-пептид(ды), Pep-1, L-олигомеры, пептид(ды) кальцитонина, полученные из Antennapedia пептиды (особенно из Drosophila antennapedia), pAntp, plsI, FGF, лактоферрин, транспортан, буфорин-2, Bac715-24, SynB, SynB(1), pVEC, полученные из hCT пептиды, SAP или гистоны. В контексте настоящего изобретения такие катионные или поликатионные носители предпочтительно представляют собой катионные или поликатионные пептиды или белки, которые предпочтительно содержат или дополнительно модифицированы так, чтобы они содержали по меньшей мере один остаток, который способен образовывать дисульфидную связь, предпочтительно остаток -SH.
Катионный компонент: Термин «катионный компонент» обычно относится к заряженной молекуле, которая положительно заряжена (катион) при значении pH обычно примерно от 1 до 9, предпочтительно при значении pH, равном или ниже 9 (например, 5-9), равном или ниже 8 (например, 5-8), равном или ниже 7 (например, 5-7), наиболее предпочтительно при физиологических значениях pH, например примерно от 7,3 до 7,4. Соответственно, катионный пептид, белок или полимер согласно настоящему изобретению положительно заряжен в физиологических условиях, в частности, в условиях физиологической концентрации солей в клетке in vivo. Катионные пептид или белок содержит большее количество катионных аминокислот, например, большее количество Arg, His, Lys или Orn, чем отрицательно заряженные или нейтральные аминокислоты. В предпочтительном варианте катионный пептид или белок в контексте настоящего изобретения содержит большее количество катионных аминокислот, например, большее количество Arg, His, Lys или Orn, чем других остатков. Определение «катионный» также может относиться к «поликатионным» компонентам.
Заряд соединения, комплекса или компонента, такого как катионный компонент или комплекс полимерного носителя и переносимого вещества (A), который определен в настоящем описании, предпочтительно определяют или оценивают в физиологических условиях, например, при pH примерно от 5,5 до 7,5, предпочтительно при pH примерно от 6,0 до 7,4, таком как примерно 7,0, при температуре примерно от 25°C до 40°C, предпочтительно при температуре примерно от 35 до 38°C, такой как примерно 37°C, при физиологической концентрации соли, например, примерно от 130 до 160 мМ, предпочтительно примерно от 137 мМ до 150 мМ, такой как примерно 137 мМ. Особенно предпочтительными условиями для определения или оценки заряда соединения, комплекса или компонента, которые определены в настоящем описании, являются условия, имеющиеся в случае 100% раствора лактата Рингера при 25°C.
Дзета-потенциал: «Дзета-потенциал» является широко используемым параметром поверхностного электрического заряда частицы. Обычно его определяют по движению заряженной частицы через электрическое поле. В контексте настоящего изобретения дзета-потенциал является предпочтительным параметром для характеристики заряда частицы, например, комплекса (A) фармацевтических композиций согласно настоящему изобретению. Таким образом, в контексте настоящего изобретения заряд частицы предпочтительно определяют посредством определения дзета-потенциала способом электрофореза с лазерным допплеровским анализом, используя устройство Zetasizer Nano (Malvern Instruments, Malvern, UK), при 25°C и угле рассеяния 173°. Поверхностный заряд данной частицы также зависит от ионной силы используемого матрикса (например, содержащего соль буфера) и pH раствора. Таким образом, фактический дзета-потенциал данного комплекса (A) при определенном соотношении зарядов (N/P) может слегка отличаться в случае разных буферов, используемых для инъекции. Для измерения частицы, такой как комплекс (A), фармацевтических композиций согласно настоящему изобретению предпочтительно суспендируют в растворе лактата Рингера. Таким образом, в настоящем изобретении раскрыто применение отрицательно заряженного комплекса (A) в условиях, обеспечиваемых данным буфером для инъекций, предпочтительно в условиях раствора лактата Рингера, оцениваемых по его дзета-потенциалу. Раствор лактата Рингера согласно настоящему изобретению предпочтительно содержит 130 ммоль/л ионов натрия, 109 ммоль/л ионов хлорида, 28 ммоль/л лактата, 4 ммоль/л ионов калия и 1,5 ммоль/л ионов кальция. Натрий, хлорид, калий и лактат обычно происходят из NaCl (хлорида натрия), NaC3H5O3 (лактата натрия), CaCl2 (хлорида кальция) и KCl (хлорида калия). Осмолярность раствора лактата Рингера составляет 273 мОсм/л, и pH доводят до 6,5.
Фармацевтически эффективное количество: Фармацевтически эффективное количество в контексте изобретения обычно понимают как количество, которое достаточно для индукции иммунного ответа.
Иммунная система: Иммунная система может защищать организмы, например, от инфекции. Если патоген прорывается через физический барьер организма и проникает в такой организм, врожденная иммунная система обеспечивает немедленную, но неспецифичную реакцию. Если патогены ускользают от такого врожденного ответа, позвоночные обладают вторым уровнем защиты - адаптивной иммунной системой. В данном случае иммунная система адаптирует свой ответ во время инфекции, чтобы улучшить распознавание патогена. Такой улучшенный ответ затем сохраняется после удаления патогена в форме иммунологической памяти и позволяет адаптивной иммунной системе осуществлять более быстрые и более сильные атаки каждый раз, когда она сталкивается с патогеном. Соответственно, иммунная система включает в себя врожденную и адаптивную иммунные системы. Каждая из таких двух частей содержит так называемые гуморальные и клеточные компоненты.
Иммунный ответ: Иммунный ответ обычно может представлять собой специфичную реакцию адаптивной иммунной системы на конкретный антиген (так называемый специфичный или адаптивный иммунный ответ) или неспецифичную реакцию врожденной иммунной системы (так называемый неспецифичный или врожденный иммунный ответ). По существу изобретение связано со специфичными реакциями (адаптивными иммунными ответами) адаптивной иммунной системы. Однако такой специфичный ответ может поддерживаться дополнительной неспецифичной реакцией (врожденным иммунным ответом). Таким образом, изобретение также относится к соединению или композиции для одновременной стимуляции врожденной и адаптивной иммунных систем, чтобы вызвать эффективный адаптивный иммунный ответ.
Адаптивный иммунный ответ: Адаптивный иммунный ответ обычно понимают как антигенспецифичный ответ. Специфичность по отношению к антигену позволяет генерировать ответы, которые специально предназначены для конкретных антигенов, экспрессирующих антигены клеток, патогенов или инфицированных патогенами клеток. Способность формировать такие специально предназначенные ответы поддерживается в организме «клетками памяти». Стоит патогену инфицировать организм более одного раза, такие специфичные клетки памяти используются для их быстрой элиминации. В данном контексте первой стадией адаптивного иммунного ответа является активация наивных антигенспецифичных T-клеток или других иммунных клеток, способных индуцировать антигенспецифичный иммунный ответ антигенпрезентирующими клетками. Это происходит в лимфоидных тканях и органах, через которые постоянно проходят наивные T-клетки. К типам клеток, которые могут служить в качестве антигенпрезентирующих клеток, наряду с прочими относятся дендритные клетки, макрофаги и B-клетки. Каждая из таких клеток имеет отличную от других функцию в процессе вызова иммунных ответов. Дендритные клетки захватывают антигены посредством фагоцитоза и макропиноцитоза и стимулируются, например, при контакте с чужеродным антигеном, мигрируя в местную лимфоидную ткань, где они дифференцируются в зрелые дендритные клетки. Макрофаги пожирают антигенные частицы, такие как бактерии, и индуцируются инфекционными агентами или другими соответствующими стимулами, экспрессируя молекулы MHC. Уникальная способность B-клеток связывать и интернализовать растворимые белковые антигены посредством своих рецепторов также может быть важна для индукции T-клеток. Презентация антигена на молекулах MHC приводит к активации T-клеток, что приводит к индукции их пролиферации и дифференцировки в вооруженные эффекторные T-клетки. Наиболее важной функцией эффекторных T-клеток является убийство инфицированных клеток цитотоксическими T-клетками CD8+ и активация макрофагов Th1-клетками, которые вместе формируют опосредованный клетками иммунитет, и активация B-клеток Th2- и Th1-клетками для получения разных классов антител, таким образом происходит запуск гуморального иммунного ответа. T-клетки распознают антиген своими T-клеточными рецепторами, которые непосредственно не узнают и не связывают антиген, но вместо этого распознают короткие пептидные фрагменты, например, белковых антигенов, происходящих из патогенов, которые связаны с молекулами MHC на поверхности других клеток.
Адаптивная иммунная система: Адаптивная иммунная система обычно состоит из высоко системных клеток и процессов, которые исключают или специализированных предотвращают рост патогенов. Адаптивный иммунный ответ придает иммунной системе позвоночных способность узнавать и запоминать конкретные патогены (чтобы создавать иммунитет), и осуществлять более сильные атаки каждый раз, когда они сталкиваются с патогеном. Система обладает высокой способностью к адаптации вследствие соматической гипермутабельности (процесса ускоренных соматических мутаций) и рекомбинации V(D)J (необратимой генетической рекомбинации участков рецептора антигена). Такой механизм позволяет небольшому числу генов образовывать огромное количество разных рецепторов антигенов, которые затем уникальным образом экспрессируются на каждом отдельном лимфоците. Так как реаранжировка генов приводит к необратимому изменению в ДНК каждой клетки, все потомство (потомки) такой клетки затем будет наследовать гены, кодирующие такую же специфичность рецепторов, включая B-клетки памяти и T-клетки памяти, которые являются ключевыми для долговременного специфичного иммунитета. Теория иммунной сети является теорией о том, как работает адаптивная иммунная система, которая основана на взаимодействиях между вариабельными областями рецепторов T-клеток, B-клеток и молекулами, производимыми T-клетками и B-клетками, которые имеют вариабельные области.
Врожденная иммунная система: Обычно подразумевают, что врожденная иммунная система, также известная как неспецифичная иммунная система, включает в себя клетки и механизмы, которые защищают хозяина от инфекции другими организмами неспецифичным образом. Это значит, что клетки врожденной системы узнают и отвечают на патогены общим способом, но в отличие от адаптивной иммунной системы, она не придает хозяину длительный или защитный иммунитет. Врожденная иммунная система может быть, например, активирована лигандами рецепторов ассоциированных с патогенами картин молекул (PAMP), например, Toll-подобных рецепторов (TLR), или другими вспомогательными веществами, такими как липополисахариды, TNF-альфа, лиганд CD40 или цитокины, монокины, лимфокины, интерлейкины или хемокины, IL-1, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-12, IL-13, IL-14, IL-15, IL-16, IL-17, IL-18, IL-19, IL-20, IL-21, IL-22, IL-23, IL-24, IL-25, IL-26, IL-27, IL-28, IL-29, IL-30, IL-31, IL-32, IL-33, IFN-альфа, IFN-бета, IFN-гамма, GM-CSF, G-CSF, M-CSF, LT-бета, TNF-альфа, факторы роста и hGH, лиганд Toll-подобного рецептора человека TLR1, TLR2, TLR3, TLR4, TLR5, TLR6, TLR7, TLR8, TLR9, TLR10, лиганд мышиного Toll-подобного рецептора TLR1, TLR2, TLR3, TLR4, TLR5, TLR6, TLR7, TLR8, TLR9, TLR10, TLR11, TLR12 или TLR13, лиганд NOD-подобного рецептора, лиганд RIG-I-подобного рецептора, иммуностимулирующая нуклеиновая кислота, иммуностимулирующая РНК (исРНК), CpG-ДНК, антибактериальное средство или противовирусное средство. Обычно ответ врожденной иммунной системы включает в себя рекрутинг иммунных клеток к местам инфекции посредством продуцирования химических факторов, включая специализированные химические медиаторы, называемые цитокинами; активацию каскада комплемента; идентификацию и удаление чужеродных веществ, присутствующих в органах, тканях, крови и лимфе, специализированными лейкоцитами; активацию адаптивной иммунной системы в результате процесса, известного как презентация антигенов; и/или действие в качестве физического и химического барьера для инфекционных агентов.
Клеточный иммунитет/клеточный иммунный ответ: Клеточный иммунитет обычно относится к активации макрофагов, клеток природных киллеров (NK), антигенспецифичных цитотоксических T-лимфоцитов и высвобождению различных цитокинов в ответ на антиген. В более общем виде клеточный иммунитет не связан с антителами, а связан с активацией клеток иммунной системы. Клеточный иммунный ответ характеризуется, например, активацией антигенспецифичных цитотоксических T-лимфоцитов, которые способны индуцировать в организме апоптоз клеток, представляющих эпитопы антигена на своей поверхности, таких как инфицированные вирусом клетки, клетки с внутриклеточными бактериями и злокачественные клетки, представляющие опухолевые антигены; активацией макрофагов и клеток природных киллеров, делающей их способными разрушать патогены; и стимуляцией клеток, приводящей к секреции различных цитокинов, которые влияют на функцию других клеток, вовлеченных в адаптивные иммунные ответы и врожденные иммунные ответы.
Гуморальный иммунитет/гуморальный иммунный ответ: Гуморальный иммунитет обычно относится к продукции антител и вспомогательным процессам, которые могут ее сопровождать. Гуморальный иммунный ответ обычно может характеризоваться, например, активацией Th2 и продукции цитокинов, образованием зародышевых центров и переключением изотипов, созреванием аффинности и образованием клеток памяти. Гуморальный иммунитет также обычно может относиться к эффекторным функциям антител, которые включают нейтрализацию патогенов и токсинов, активацию классического пути комплемента и стимуляцию фагоцитоза опсонинами и элиминацию патогенов.
Антиген: Согласно настоящему изобретению термин «антиген» обычно относится к веществу, которое может узнаваться иммунной системой и может обладать способностью запускать антигенспецифичный иммунный ответ, например, за счет образования антител или антигенспецифичных T-клеток в качестве части адаптивного иммунного ответа. Обычно антиген представляет собой белок или пептид, но также может представлять собой сахар, липид, нуклеиновую кислоту и другую структуру. В данном контексте первой стадией адаптивного иммунного ответа является активация наивных антигенспецифичных T-клеток антигенпрезентирующими клетками. Это происходит к лимфоидных тканях и органах, через которые наивные T-клетки постоянно проходят. Три типа клеток, которые могут служить в качестве антигенпрезентирующих клеток, представлены дендритными клетками, макрофагами и B-клетками. Каждая из таких клеток имеет отличную от других функцию в процессе вызова иммунных ответов. Тканевые дендритные клетки захватывают антигены в ходе фагоцитоза и макропиноцитоза и при инфекции подвергаются стимуляции, приводящей к миграции в местную лимфоидную ткань, где они дифференцируются в зрелые дендритные клетки. Макрофаги поглощают антигенные частицы, такие как бактерии, и индуцируются инфекционными агентами, экспрессируя молекулы MHC класса II. Уникальная способность B-клеток связывать и интернализовать растворимые белковые антигены посредством своих рецепторов, также может быть важна для индукции T-клеток. Презентация антигена на молекулах MHC приводит к активации T-клеток, что приводит к индукции их пролиферации и дифференцировки в вооруженные эффекторные T-клетки. Наиболее важной функцией эффекторных T-клеток является уничтожение инфицированных клеток цитотоксическими T-клетками CD8+ и активация макрофагов Th1-клетками, которые вместе формируют опосредованный клетками иммунитет, и активация B-клеток Th2- и Th1-клетками для получения разных классов антител, таким образом происходит запуск гуморального иммунного ответа. T-клетки распознают антиген своими T-клеточными рецепторами, которые непосредственно не узнают и не связывают антиген, но вместо этого распознают короткие пептидные фрагменты, например, белковых антигенов патогенов, которые связаны с молекулами MHC на поверхности других клеток.
T-клетки относятся к двум основным классам, которые обладают разными эффекторными функциями. Два класса различают по экспрессии белков клеточной поверхности CD4 и CD8. Указанные два типа T-клеток отличаются классом молекулы MHC, которую они узнают. Существует два класса молекул MHC - молекулы MHC класса I и MHC класса II, которые отличаются по своей структуре и картине экспрессии в тканях организма. T-клетки CD4+ связываются с молекулой MHC класса II, а T-клетки CD8+ связываются с молекулой MHC класса I. Молекулы MHC класса I и молекулы MHC класса II по-разному распределены среди клеток, что отражает разные эффекторные функции T-клеток, которые их узнают. Молекулы MHC класса I презентируют пептиды из патогенов, обычно вирусов, T-клеткам CD8+, которые дифференцируются в цитотоксические T-клетки, которые специализируются на уничтожении любой клетки, которую они специфично распознают. Почти все клетки экспрессируют молекулы MHC класса I, хотя уровень конститутивной экспрессии варьирует от одного типа клеток к другому. Но молекулы MHC класса I презентируют не только патогенные пептиды вирусов, ими презентируются также аутоантигены, подобные опухолевым антигенам. Молекулы MHC класса I связывают пептиды из белков, разрушаемых в цитозоле и транспортируемых в эндоплазматический ретикулум. При этом молекулы MHC класса I на поверхности клеток, инфицированных вирусами или другими цитозольными патогенами, представляют в виде дисплея пептиды из таких патогенов. T-клетки CD8+, которые узнают комплексы молекул MHC класса I с пептидами, специализируются на уничтожении любых клеток, представляющих чужеродные пептиды, и таким образом освобождают организм от клеток, инфицированных вирусами и другими цитозольными патогенами. Основной функцией T-клеток CD4+ (T-хелперных клеток CD4+), которые узнают молекулы MHC класса II, является активация других эффекторных клеток иммунной системы. Таким образом, молекулы MHC класса II обычно находятся на B-лимфоцитах, дендритных клетках и макрофагах, клетках, которые принимают участие в иммунных ответах, а не на других клетках ткани. Макрофаги, например, при активации уничтожают внутривезикулярные патогены, которые они несут, а B-клетки секретируют иммуноглобулины против чужеродных молекул. Связывание молекул MHC класса II с пептидами в эндоплазматическом ретикулуме предотвращено, и, таким образом, молекулы MHC класса II связывают пептиды, образованные из белков, которые разрушаются в эндосомах. Они могут улавливать пептиды, полученные из патогенов, которые проникли в везикулярную систему макрофагов, или из антигенов, интернализованных незрелыми дендритными клетками, или рецепторами иммуноглобулинов B-клеток. Патогены, которые накапливаются в больших количествах внутри везикул макрофагов и дендритных клеток, как правило, стимулируют дифференцировку клеток TH1, тогда как внеклеточные антигены обычно стимулируют продуцирование клеток TH2. Клетки TH1 активируют бактерицидные свойства макрофагов и индуцируют B-клетки к продуцированию IgG-антител, которые очень эффективны в опсонизации внеклеточных патогенов для поглощения фагоцитирующими клетками, тогда как клетки TH2 инициируют гуморальный ответ посредством активации наивных B-клеток к секреции IgM, и индуцируют продукцию слабо опсонизирующих антител, таких как IgG1 и IgG3 (мышиные) и IgG2 и IgG4 (человеческие), а также IgA и IgE (мышиные и человеческие).
Вакцина: Вакциной обычно считают профилактический или терапевтический материал, обеспечивающий по меньшей мере один антиген или антигенную функцию. Антиген или антигенная функция может стимулировать адаптивную иммунную систему организма, обеспечивая адаптивный иммунный ответ.
Иммуностимулирующее средство: Обычно подразумевают, что термин «иммуностимулирующее средство» не включает такие средства, как, например, антигены (с любой химической структурой), которые вызывают адаптивный/цитотоксический иммунный ответ, например, «гуморальный» или «клеточный» иммунный ответ, другими словами вызывают иммунные ответы (и придают иммунитет сами по себе), которые характеризуются специфичным ответом на структурные свойства антигена, распознаваемого иммунокомпетентными клетками как чужеродный. Вернее, обычно подразумевают, что термин «иммуностимулирующее средство» означает средства/соединения/комплексы, которые не запускают какой-либо адаптивный/цитотоксический иммунный ответ сами по себе, но которые могут исключительно усиливать такой адаптивный/цитотоксический иммунный ответ неспецифичным образом, например, активируя рецепторы «PAMP» и тем самым запуская высвобождение цитокинов, которые поддерживают реальный адаптивный/цитотоксический иммунный ответ. Соответственно, любую иммуностимуляцию средствами (например, антигенами), которые вызывают адаптивный и/или цитотоксический иммунный ответ сами по себе (сами по себе придают иммунитет прямо или опосредованно), обычно не описывают фразой «иммуностимулирующее средство».
Адъювант: Обычно подразумевают, что термин «адъювант» не включает средства, которые придают иммунитет сами по себе. Соответственно, адъюванты обычно не могут придавать иммунитет сами по себе, но помогают иммунной системе различными путями усиливать иммунный ответ на антигены, например, стимулируя презентацию антигена иммунной системе. При этом адъювант предпочтительно может, например, модулировать антигенспецифичный иммунный ответ, например, сдвигая преобладающий основанный на Th1 антигенспецифичный ответ в сторону антигенспецифичного ответа, основанного больше на Th2, или наоборот. Соответственно, обычно подразумевают, что термины «иммуностимулирующее средство» и «адъювант» в контексте настоящего изобретения означают средства, соединения или комплексы, которые не придают иммунитета сами по себе, а только поддерживают иммунный ответ неспецифичным образом (в отличие от антигенспецифичного иммунного ответа) за счет эффектов, которые модулируют антигенспецифичный (адаптивный клеточный и/или гуморальный иммунный ответ) неспецифичными мерами, например, экспрессией/секрецией цитокинов, улучшенной презентацией антигенов, сдвигом природы плеч иммунного ответа и т.д. Соответственно, любое средство, само по себе вызывающее иммунитет, обычно не описывают терминами «адъювант» или «иммуностимулирующее средство».
Иммуностимулирующие РНК: Иммуностимулирующая РНК (исРНК) в контексте изобретения обычно может представлять собой РНК, которая сама способна индуцировать врожденный иммунный ответ. Обычно такая РНК не имеет открытой рамки считывания и таким образом не дает пептидный антиген, но вызывает врожденный иммунный ответ, например, посредством связывания с конкретным видом рецепторов ассоциированных с патогенами молекулярных картин (PAMP) (например, Toll-подобным рецептором (TLR) или другими подходящими рецепторами). Однако, конечно, и мРНК, имеющие открытую рамку считывания и кодирующие пептид/белок (например, антигенную функцию) могут индуцировать врожденный иммунный ответ.
Фрагмент последовательности: Фрагмент последовательности обычно представляет собой более короткую часть полноразмерной последовательности, например, последовательности нуклеиновой кислоты или аминокислотной последовательности. Соответственно, фрагмент последовательности обычно состоит из последовательности, которая идентична соответствующему участку или соответствующим участкам в полноразмерной последовательности. Предпочтительный фрагмент последовательности в контексте настоящего изобретения состоит из участка непрерывно следующих друг за другом структурных единиц, таких как нуклеотиды или аминокислоты, соответствующего участку непрерывно следующих друг за другом структурных единиц в молекуле, из которой получен фрагмент, который составляет по меньшей мере 5%, предпочтительно по меньшей мере 20%, предпочтительно по меньшей мере 30%, более предпочтительно по меньшей мере 40%, более предпочтительно по меньшей мере 50%, еще более предпочтительно по меньшей мере 60%, еще более предпочтительно по меньшей мере 70%, и наиболее предпочтительно по меньшей мере 80% от общей (т.е. полноразмерной) молекулы, из которой получен фрагмент. Таким образом, например, фрагмент белкового или пептидного антигена предпочтительно соответствует участку непрерывно следующих друг за другом структурных единиц в белковом или пептидном антигене, из которого получен фрагмент, который соответствует, по меньшей мере 5%, предпочтительно по меньшей мере 20%, предпочтительно по меньшей мере 30%, более предпочтительно по меньшей мере 40%, более предпочтительно по меньшей мере 50%, еще более предпочтительно по меньшей мере 60%, еще более предпочтительно по меньшей мере 70%, и наиболее предпочтительно по меньшей мере 80% общего (т.е. полноразмерного) белкового или пептидного антигена. Особенно предпочтительно, чтобы фрагмент последовательности представлял собой функциональный фрагмент, т.е. чтобы фрагмент выполнял одну или несколько функций, выполняемых последовательностью, из которой фрагмент получен. Например, фрагмент белкового или пептидного антигена предпочтительно выполняет по меньшей мере одну антигенную функцию (например, способен вызывать специфичную иммунную реакцию против по меньшей мере одной антигенной детерминанты в указанном белковом или пептидном антигене) белкового или пептидного антигена, из которого получен фрагмент.
Фрагменты белков: «Фрагменты» белков или пептидов, т.е. фрагменты аминокислотных последовательностей, в контексте настоящего изобретения обычно могут содержать последовательность белка или пептида, который определен в настоящем описании, который в отношении его аминокислотной последовательности (или кодирующей его молекулы нуклеиновой кислоты) укорочен на N-конце, C-конце и/или внутри последовательности по сравнению с аминокислотной последовательностью исходного (природного) белка (или кодирующей его молекулы нуклеиновой кислоты). Таким образом, такое укорочение может иметь место либо на уровне аминокислот, либо соответственно на уровне нуклеиновой кислоты. Следовательно, идентичность последовательностей в отношении такого фрагмента, который определен в настоящем описании, предпочтительно может относиться к полному белку или пептиду, который определен в настоящем описании, или к полной (кодирующей) молекуле нуклеиновой кислоты для такого белка или пептида.
Подобным образом, «фрагменты» последовательностей нуклеиновой кислоты в контексте настоящего изобретения могут содержать последовательность нуклеиновой кислоты, которая определена в настоящем описании, которая в отношении молекулы нуклеиновой кислоты укорочена на 5'-конце, 3'-конце и/или внутри последовательности по сравнению с молекулой нуклеиновой кислоты исходной (нативной) молекулы нуклеиновой кислоты. Поэтому идентичность последовательности в отношении такого фрагмента, который определен в настоящем описании, предпочтительно может относиться к полной нуклеиновой кислоте, которая определена в настоящем описании.
Предпочтительные фрагменты белков или пептидов в контексте настоящего изобретения, кроме того, могут содержать последовательность белка или пептида, который определен в настоящем описании, которая имеет длину от примерно 6 до примерно 20 или более аминокислот, например, фрагменты, которые процессированы и презентированы молекулами MHC класса I, предпочтительно имеющие длину от примерно 8 до примерно 10 аминокислот, например 8, 9 или 10 (или даже 6, 7, 11 или 12 аминокислот), или фрагменты, которые процессированы и презентированы молекулами MHC класса II, предпочтительно имеющие длину примерно 13 или более аминокислот, например, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот, при этом такие фрагменты могут быть выбраны из любой части аминокислотной последовательности. Такие предпочтительные фрагменты обычно узнаются T-клетками в форме комплекса, состоящего из пептидного фрагмента и молекулы MHC, т.е. обычно фрагменты не распознаются в их нативной форме. Фрагменты белков или пептидов могут содержать по меньшей мере один эпитоп таких белков или пептидов. Кроме того, также может подразумеваться, что домены белка, подобные внеклеточному домену, внутриклеточному домену или трансмембранному домену, и укороченные варианты белка содержат фрагмент белка.
Эпитоп (также называемый «антигенной детерминантой»): T-клеточные эпитопы или части белков в контексте настоящего изобретения могут содержать фрагменты, предпочтительно имеющие длину от примерно 6 до примерно 20 или еще более аминокислот, например, фрагменты, которые процессированы и презентированы молекулами MHC класса I, предпочтительно имеющие длину от примерно 8 до примерно 10 аминокислот, например, 8, 9 или 10 (или даже 11 или 12 аминокислот), или фрагменты, которые процессированы и презентированы молекулами MHC класса II, предпочтительно имеющими длину примерно 13 или более аминокислот, например, 13, 14, 15, 16, 17, 18, 19, 20 или еще больше аминокислот, при этом такие фрагменты могут быть выбраны из любой части аминокислотной последовательности. Такие фрагменты обычно распознаются T-клетками в форме комплекса, состоящего из пептидного фрагмента и молекулы MHC, т.е. фрагменты обычно не распознаются в их нативной форме.
B-клеточные эпитопы обычно представляют собой фрагменты, расположенные на внешней поверхности (нативного) белковых или пептидных антигенов, которые определены в настоящем описании, предпочтительно имеющие длину от 5 до 15 аминокислот, более предпочтительно имеющие длину от 5 до 12 аминокислот, еще более предпочтительно имеющие длину от 6 до 9 аминокислот, которые могут узнаваться антителами, т.е. в их нативной форме.
Такие эпитопы белков или пептидов, кроме того, могут быть выбраны из любых упоминаемых в настоящем описании вариантов таких белков или пептидов. В данном контексте антигенные детерминанты могут быть конформационными или прерывистыми эпитопами, которые состоят из участков белков или пептидов, которые определены в настоящем описании, которые являются прерывистыми по аминокислотной последовательности белков или пептидов, которые определены в настоящем описании, но сближаются в трехмерной структуре, или могут быть непрерывными или линейными эпитопами, которые состоят из одной полипептидной цепи.
Вариант: Вариант объекта, такой как вариант последовательности, например нуклеотидной или аминокислотной последовательности, относится к модифицированному объекту, такому как модифицированная последовательность, например, модифицированная нуклеотидная или аминокислотная последовательность. Например, вариант последовательности может иметь одну или несколько нуклеотидных или аминокислотных делеций, инсерций, добавлений и/или замен по сравнению с последовательностью, из которой вариант получен. Предпочтительно, вариант последовательности в контексте настоящего изобретения по меньшей мере на 40%, предпочтительно по меньшей мере на 50%, более предпочтительно по меньшей мере на 60%, более предпочтительно по меньшей мере на 70%, еще более предпочтительно по меньшей мере на 80%, еще более предпочтительно по меньшей мере на 90%, наиболее предпочтительно по меньшей мере на 95% идентичен последовательности, из которой вариант получен. Соответственно, вариант пептидного или белкового антигена в контексте настоящего изобретения предпочтительно по меньшей мере на 40%, предпочтительно по меньшей мере на 50%, более предпочтительно по меньшей мере на 60%, более предпочтительно по меньшей мере на 70%, еще более предпочтительно по меньшей мере на 80%, еще более предпочтительно по меньшей мере на 90%, наиболее предпочтительно по меньшей мере на 95% идентичен последовательности белкового или пептидного антигена, из которого вариант получен. Предпочтительно, вариант является функциональным вариантом, т.е. такой вариант выполняет одну или несколько функций, выполняемых последовательностью, из которой вариант получен. Например, вариант белкового или пептидного антигена предпочтительно выполняет по меньшей мере одну антигенную функцию (например, способен вызывать специфичную иммунную реакцию против по меньшей мере одной антигенной детерминанты в указанном белковом или пептидном антигене) белкового или пептидного антигена, из которого вариант получен.
Могут быть созданы «варианты» белков или пептидов, которые определены в контексте настоящего изобретения, имеющие аминокислотную последовательность, которая отличается от исходной последовательности одной или несколькими мутациями, такими как одна или несколько замененных, встроенных и/или делетированных аминокислот. Предпочтительно, такие фрагменты и/или варианты имеют такую же биологическую функцию или специфичную активность, как и полноразмерный нативный белок, например обладает специфичным антигенным свойством. «Варианты» белков или пептидов, которые определены в контексте настоящего изобретения, могут, например, содержать консервативную аминокислотную замену(ны) по сравнению с их нативной, т.е. немутантной физиологической, последовательностью. Такие аминокислотные последовательности, а также кодирующие их нуклеотидные последовательности, в частности, подпадают под термин варианты, который определен в настоящем описании. Замены, при которых аминокислоты, которые относятся к одному и тому же классу, заменяют друг на друга, называют консервативными заменами. В частности, к таким аминокислотам относятся аминокислоты, имеющие алифатические боковые цепи, положительно или отрицательно заряженные боковые цепи, ароматические группы в боковых цепях, или аминокислоты, боковые цепи которых могут вступать в образование водородных мостиков, например, боковые цепи которых имеют гидроксильную функцию. Это означает, например, что аминокислота, имеющая полярную боковую цепь, заменена другой аминокислотой, имеющей подобную полярную боковую цепь, или, например, аминокислота, характеризуемая гидрофобной боковой цепью, заменена другой аминокислотой, имеющей подобную гидрофобную боковую цепь (например, серин (треонин) заменен треонином (серином) или лейцин (изолейцин) заменен изолейцином (лейцином)). Инсерции и замены возможны, в частности, в таких положениях в последовательности, которые не вызывают модификации в трехмерной структуре или не влияют на область связывания. Модификации трехмерной структуры в результате инсерции(ий) или делеции(ий) легко можно определить, например, используя спектры CD (спектры кругового дихроизма) (Urey, 1985, Absorption, Circular Dichroism and ORD of Peptides, в: Modern Physical Methods in Biochemistry, Neuberger et al., (ed.), Elsevier, Amsterdam).
Кроме того, варианты белков или пептидов могут включать аналоги пептидов, которые определены в настоящем описании. Кроме того, варианты белков или пептидов, которые определены в настоящем описании, которые могут кодироваться молекулой нуклеиновой кислоты, также могут содержать такие последовательности, в случае которых нуклеотиды нуклеиновой кислоты заменены согласно вырожденности генетического кода, при этом не приводя к изменению соответствующей аминокислотной последовательности белка или пептида, т.е. аминокислотная последовательность или по меньшей мере ее часть могут не отличаться от исходной последовательности одной или несколькими мутациями в указанном выше смысле.
Идентичность последовательностей: Чтобы определить процент идентичности двух последовательностей, например, последовательностей нуклеиновых кислот или аминокислотных последовательностей, которые определены в настоящем описании, таких как аминокислотные последовательности, кодируемые последовательностью нуклеиновой кислоты из комплекса полимерного носителя и переносимого вещества, или последовательность нуклеиновой кислоты или аминокислотная последовательность антигена, который определен в настоящем описании, последовательности переносимой нуклеиновой кислоты или аминокислотные последовательности как таковые, последовательности могут быть подвергнуты выравниванию, чтобы затем их сравнить друг с другом. Таким образом, например, положение в первой последовательности можно сравнить с соответствующим положением во второй последовательности. Если положение в первой последовательности занято таким же компонентом, что и в случае положения во второй последовательности, две последовательности являются идентичными в данном положении. Если это не так, то последовательности отличаются в данном положении. Если встречаются инсерции во второй последовательности по сравнению с первой последовательностью, могут быть вставлены пробелы в первой последовательности, чтобы обеспечить возможность дальнейшего выравнивания. Если встречаются делеции во второй последовательности по сравнению с первой последовательностью, то пробелы могут быть вставлены во вторую последовательность, чтобы обеспечить возможность дальнейшего выравнивания. Затем вычисляют процент идентичности двух последовательностей как функцию количества идентичных положений, деленного на общее количество положений, включая такие положения, которые заняты только в одной последовательности. Процент идентичности двух последовательностей можно определить, используя математический алгоритм. Предпочтительно, но без ограничения, примером математического алгоритма, который можно использовать, является алгоритм, описанный в публикации Karlin с соавторами (1993), PNAS USA, 90: 5873-5877, или Altschul с соавторами (1997), Nucleic Acids Res., 25: 3389-3402. Такой алгоритм включен в программу BLAST. Последовательности, которые в определенной степени идентичны последовательностям согласно настоящему изобретению, могут быть идентифицированы с использованием такой программы. «Вариант» белка или пептида может иметь, например, по меньшей мере 70%, 75%, 80%, 85%, 90%, 95%, 98% или 99% идентичность аминокислот на участке длиной 10, 20, 30, 50, 75 или 100 аминокислот, предпочтительно на протяжении всей длины последовательности такого белка или пептида. Аналогично «вариант» последовательности нуклеиновой кислоты может иметь, например, по меньшей мере 70%, 75%, 80%, 85%, 90%, 95%, 98% или 99% идентичность нуклеотидов на участке длиной 10, 20, 30, 50, 75 или 100 нуклеотидов, предпочтительно на протяжении всей длины последовательности такой последовательности нуклеиновой кислоты.
Производное белка или пептида: Обычно подразумевают, что производное пептида или белка представляет собой молекулу, которая получена из другой молекулы, такой как указанный пептид или белок. Термин «производное» пептида или белка также охватывает слияния, содержащие пептид или белок, используемый в настоящем изобретении. Например, слияние содержит метку, такую как, например, эпитоп, например FLAG-эпитоп, или эпитоп V5, или эпитоп HA. Например, эпитоп представляет собой FLAG-эпитоп. Такая метка применима, например, для очистки слитого белка. Термин «производное» пептида или белка также охватывает дериватизованный пептид или белок, такой как, например, пептид или белок, модифицированный так, чтобы он содержал один или несколько химических остатков, отличных от аминокислоты. Химический остаток может быть связан ковалентно с пептидом или белком, например, через амино-концевой остаток аминокислоты, через остаток аминокислоты на карбоксильном конце или с внутренним остатком аминокислоты. Такие модификации включают добавление защитной или кэпирующей группы к реакционно-способному остатку в пептиде или белке, добавление регистрируемой метки и другие изменения, которые неблагоприятным образом не нарушают активность пептидного или белкового соединения. Например, производное может содержать остаток ПЭГ, радионуклид, цветной латекс и т.д. Производное обычно обладает или проявляет улучшенные характеристики в отношении, например, повышенной резистентности к протеазам и/или более длительного времени полужизни и/или улучшенной транспортабельности между клетками или тканями организма человека или животного и/или уменьшенных неблагоприятных эффектов и/или повышенной аффинности или иммуногенности. В WO 2010/003193 описаны различные методики получения производных пептидов или белков, которые можно использовать отдельно или в сочетании, применяя стандартные способы, известные специалисту, включая дериватизацию белка или пептида, например, пегилированием, модификацией гидроксиэтилкрахмалом или гликозилированием.
Согласно первому аспекту, одна или несколько целей, лежащих в основе настоящего изобретения, достигаются благодаря фармацевтической композиции, включающей:
(A) комплекс полимерного носителя и переносимого вещества, содержащий:
a) полимерный носитель, содержащий поперечно сшитые дисульфидной связью катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидной связью катионными компонентами; и
b) по меньшей мере одну молекулу нуклеиновой кислоты, и
(B) по меньшей мере один антиген, который выбран из группы, состоящей из:
(i) антигена из патогена, ассоциированного с инфекционной болезнью;
(ii) антигена, ассоциированного с аллергией или аллергическим заболеванием;
(iii) антигена, ассоциированного с аутоиммунным заболеванием; и
(iv) антигена, ассоциированного с раком или опухолевым заболеванием,
или фрагмент, вариант и/или производное указанного антигена.
Предпочтительно, компонент (B) не связан ковалентно, в частности, не связан дисульфидной связью с компонентом (A). Таким образом, компонент (B) предпочтительно не связан ковалентно, например, не связан дисульфидной связью с полимерным носителем и/или по меньшей мере одной молекулой нуклеиновой кислоты. Предпочтительно, по меньшей мере один антиген не связан ковалентно с комплексом полимерного носителя и переносимого вещества, в частности, не связан ковалентно с полимерным носителем комплекса полимерного носителя и переносимого вещества. Например, предпочтительно, по меньшей мере один антиген, такой как белковый или пептидный антиген, не связан ковалентно с комплексом полимерного носителя и переносимого вещества, например, с полимерным носителем, дисульфидной связью. Однако в одном варианте, в котором компонент (A) и компонент (B) связаны дисульфидными связями, такая связь предпочтительно не осуществляется посредством поперечно сшивающего агента, такого как поперечно сшивающий агент 3,6-диокса-1,8-октандитиол (DODT). Кроме того, в одном варианте, в котором компонент (A) и компонент (B) связаны дисульфидными связями, компонент (B) предпочтительно не является овальбумином или фрагментом овальбумина.
Преимущество компонента (B), например, белкового антигена, не связанного ковалентно с полимерным носителем, заключается в том, что структура антигена, например, белкового антигена, не будет нарушена и его иммуногенность будет сохранена. Если антиген, например белковый антиген, ковалентно связан с полимерным носителем, например, дисульфидными связями, третичная структура антигена может быть изменена или даже денатурирована, что может нарушить структуру конформационных эпитопов и может сделать белок менее иммуногенным или неиммуногенным. Эпитопы, которые распознаются иммунной системой, могут быть линейными эпитопами, состоящими из участков непрерывно следующих друг за другом аминокислот, или конформационными эпитопами, которые имеют конкретную трехмерную форму, состоящими из аминокислот, происходящих из разных частей белка.
Кроме того, предпочтительно, полимерный носитель, в частности катионные компоненты полимерного носителя, и по меньшей мере одна молекула нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества не связаны ковалентно, но предпочтительно ассоциированы посредством других связей, отличных от ковалентных связей, таких как ионные связи и/или ван-дер-ваальсовы связи. Таким образом, предпочтительно, чтобы в комплексе полимерного носителя и переносимого вещества только катионные компоненты были ковалентно связаны друг с другом, но чтобы молекулы нуклеиновых кислот были нековалентно ассоциированы с полимерным носителем.
Кроме того, в предпочтительном варианте компоненты (A) и (B) не образовывали вместе мицеллярную структуру, в частности, полимерный носитель предпочтительно не образует мицеллярную структуру.
В некоторых вариантах всех аспектов изобретения комплекс полимерного носителя и переносимого вещества предназначен для применения в качестве адъюванта. Например, его применяют в качестве адъюванта, и/или он обладает адъювантными свойствами, которые может легко определить специалист, используя обычные методики, включая методики, которые описаны в настоящей публикации.
В качестве первого ингредиента фармацевтическая композиция согласно изобретению включает (например, в качестве адъюванта) по меньшей мере один комплекс полимерного носителя и переносимого вещества, содержащий
a) (в качестве носителя) полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами, и
b) (в качестве переносимого вещества) по меньшей мере одну молекулу нуклеиновой кислоты.
Комплекс полимерного носителя и переносимого вещества, входящий в состав фармацевтической композиции согласно изобретению, позволяет получать более эффективный и/или более безопасный адъювант в целях вакцинации. Преимущественно, комплекс полимерного носителя и переносимого вещества подходит для доставки нуклеиновых кислот in vivo, в частности, для упаковки и стабилизации нуклеиновой кислоты в целях трансфекции нуклеиновой кислоты, например, проявляет один или несколько пониженных негативных побочных эффектов высокомолекулярных полимеров, которые обсуждаются выше, таких как плохая способность к биологическому разрушению или высокая токсичность, агломерация, низкая активность при трансфекции in vivo и т.д. Комплекс полимерного носителя и переносимого вещества также обеспечивает улучшенный перенос нуклеиновой кислоты in vivo, особенно интрадермальным или внутримышечным путями, включая стабильность в сыворотке, стабильность в присутствии соли, эффективность захвата, пониженная активация комплемента, высвобождение нуклеиновой кислоты и т.д. Такой комплекс полимерного носителя и переносимого вещества, кроме того, может поддерживать индукцию и сохранять адаптивный иммунный ответ посредством инициации или усиления параллельного врожденного иммунного ответа. Кроме того, комплекс полимерного носителя и переносимого вещества может иметь улучшенную стабильность при хранении, особенно во время лиофилизации.
Комплекс полимерного носителя и переносимого вещества, который определен выше, содержит в качестве одного компонента полимерный носитель, образованный поперечно сшитыми дисульфидными связями катионными компонентами. Термин «катионный компонент» обычно относится к заряженной молекуле, которая положительно заряжена (катион) при значении pH примерно от 1 до 9, предпочтительно при значении pH равном или ниже 9, равном или ниже 8, равном или ниже 7, наиболее предпочтительно при физиологических значениях pH, например, примерно от 7,3 до 7,4. Соответственно, катионный пептид, белок или полимер согласно настоящему изобретению положительно заряжен в физиологических условиях, в частности, в условиях физиологической концентрации соли в клетке in vivo. Определение «катионный» также может относиться к «поликатионным» компонентам.
В данном контексте катионные компоненты, которые образуют основу полимерного носителя комплекса полимерного носителя и переносимого вещества посредством поперечного сшивания дисульфидными связями, обычно выбраны из любого подходящего катионного или поликатионного пептида, белка или полимера, подходящего для такой цели, в частности, любого катионного или поликатионного пептида, белка или полимера, способного образовывать комплекс с нуклеиновой кислотой, который определен согласно настоящему изобретению, и тем самым предпочтительно конденсирующего нуклеиновую кислоту. Катионный или поликатионный пептид, белок или полимер предпочтительно представляет собой линейную молекулу, однако, также можно использовать разветвленные катионные или поликатионные пептиды, белки или полимеры.
Каждый катионный или поликатионный белок, пептид или полимер полимерного носителя содержит по меньшей мере один остаток -SH, наиболее предпочтительно по меньшей мере один остаток цистеина или любую другую химическую группу, имеющую остаток -SH, способную образовывать дисульфидную связь при конденсации по меньшей мере с одним другим катионным или поликатионным белком, пептидом или полимером в качестве катионного компонента полимерного носителя, который описан в настоящей публикации.
Каждый катионный или поликатионный белок, пептид или полимер или любой другой компонент полимерного носителя предпочтительно связан с соседним компонентом(ами) (катионными белками, пептидами, полимерами или другими компонентами) поперечными сшивками дисульфидными связями. Предпочтительно, поперечно сшивающая дисульфидная связь представляет собой (обратимую) дисульфидную связь (-S-S-) между по меньшей мере одним катионным или поликатионным белком, пептидом или полимером и по меньшей мере одним другим катионным или поликатионным белком, пептидом или полимером или другим компонентом полимерного носителя. Поперечная сшивка дисульфидной связью обычно образуется при конденсации -SH-остатков компонентов полимерного носителя, в частности, катионных компонентов. Такой -SH-остаток может быть частью структуры катионного или поликатионного белка, пептида или полимера или любого другого компонента полимерного носителя до поперечного сшивания дисульфидной связью или может быть добавлен перед образованием поперечной сшивки дисульфидной связью в результате модификации, которая определена ниже. В данном контексте атомы серы, близлежащие по отношению к одному компоненту полимерного носителя, необходимые для образования дисульфидной связи, могут быть обеспечены за счет самого компонента, например, за счет остатка -SH, который определен в настоящем описании или может быть обеспечен за счет модификации компонента соответствующим образом, чтобы получить остаток -SH. Такие остатки -SH обычно обеспечиваются за счет каждого компонента, например, посредством цистеина или любой другой (модифицированной) аминокислоты или соединения в компоненте, который несет остаток -SH. В том случае, когда катионный компонент или любой другой компонент полимерного носителя представляет собой пептид или белок, предпочтительно, чтобы остаток -SH присутствовал за счет по меньшей мере одного остатка цистеина. Альтернативно, компонент полимерного носителя может быть соответствующим образом модифицирован остатком -SH, предпочтительно в результате химической реакции с соединением, несущим остаток -SH, так что каждый из компонентов полимерного носителя несет по меньшей мере один такой остаток -SH. Таким соединением, несущим остаток -SH, может быть, например, (дополнительный) цистеин или любая другая (модифицированная) аминокислота или соединение компонента полимерного носителя, которое несет остаток -SH. Таким соединением также может быть любое соединение, не являющееся амино-соединением или остатком, такое как соединение или остаток, не являющийся аминокислотой, который содержит или позволяет ввести остаток -SH в компонент, который определен в настоящем описании. Такие соединения, не являющиеся амино-соединениями, например соединения, не являющиеся аминокислотами, могут быть связаны с компонентом полимерного носителя согласно настоящему изобретению в результате химических реакций или связывания соединений, например, посредством связывания 3-тиопропионовой кислоты или 2-иминотиолана (реагента Траута), образования амида (например, карбоновые кислоты, сульфокислоты, амины и т.д.), присоединения по Михаэлю (например, остатки малеинимида, α,β-ненасыщенные карбонилы и т.д.), посредством клик-химии (например, азиды или алкины), метатезиса алкена/алкина (например, алкены или алкины), образования имина или гидрозона (альдегиды или кетоны, гидразины, гидроксиламины, амины), реакций комплексообразования (авидин, биотин, белок G) или компоненты, которые обеспечивают возможность реакций замещения Sn-типа (например, галогеналканы, тиолы, спирты, амины, гидразины, гидразиды, сложные эфиры сульфоновой кислоты, соли оксифосфония), или других химических остатков, которые можно использовать при связывании других компонентов. В некоторых случаях остаток -SH может быть маскирован защитными группами во время химического связывания с компонентом. Такие защитные группы известны в данной области и могут быть удалены после химического связывания. В каждом случае остаток -SH, например, цистеина или любой другой (модифицированной) аминокислоты или соединения, может присутствовать на концах или внутри в любом положении компонента полимерного носителя. Как определено в настоящем описании, каждый из компонентов полимерного носителя, предпочтительно каждый из катионных компонентов полимерного носителя, обычно имеет по меньшей мере один остаток -SH, но также может содержать два, три, четыре, пять или еще больше остатков -SH.
В предпочтительном варианте полимерный носитель, переносимая молекула нуклеиновой кислоты и/или антиген, такой как белковый или пептидный антиген, не модифицированы введением новых участков связывания для образования дисульфидных связей, таким как введение новых остатков -SH, в частности, полимерный носитель, переносимая молекула нуклеиновой кислоты и/или антиген, такой как белковый или пептидный антиген, предпочтительно не модифицированы дитиопиридином. Таким образом, в конкретном предпочтительном варианте полимерный носитель, переносимая молекула нуклеиновой кислоты и/или антиген не содержат дитиопиридин.
В следующем предпочтительном варианте полимерный носитель не содержит остатка полиэтиленгликоля (ПЭГ), в частности, предпочтительно катионные компоненты полимерного носителя предпочтительно не содержат остатка ПЭГ. Однако если полимерный носитель содержит остаток ПЭГ, катионный компонент предпочтительно не является поли-L-лизином.
В дополнение к связыванию катионных компонентов остаток -SH можно использовать для связывания дополнительных компонентов с полимерным носителем, которые определены в настоящем описании, в частности, аминокислотного компонента, например, антигенных эпитопов, антигенов, антител, проникающих в клетки пептидов (например, TAT), лигандов и т.д. Если полимерный носитель содержит дополнительные компоненты в дополнение к катионным компонентам, предпочтительно, чтобы дополнительный компонент не являлся овальбумином или фрагментом овальбумина, в частности, если дополнительный компонент представляет собой аминокислотный компонент.
Как определено выше, полимерный носитель комплекса полимерного носителя и переносимого вещества образован поперечно сшитыми дисульфидными связями катионными (или поликатионными) компонентами.
Согласно одному первому альтернативному варианту по меньшей мере один катионный (или поликатионный) компонент полимерного носителя может быть выбран из катионных или поликатионных пептидов или белков. Такие катионные или поликатионные пептиды или белки предпочтительно имеют длину примерно от 3 до 100 аминокислот, предпочтительно имеют длину примерно от 3 до 50 аминокислот, более предпочтительно имеют длину примерно от 3 до 25 аминокислот, например, длину примерно от 3 до 10; от 5 до 20; от 5 до 15; от 8 до 15, 16 или 17; от 10 до 15, 16, 17, 18, 19 или 20; или от 15 до 25 аминокислот. Альтернативно или дополнительно, такие катионные или поликатионные пептиды или белки могут иметь молекулярную массу от примерно 0,01 кДа до примерно 100 кДа, включая молекулярную массу от примерно 0,5 кДа до примерно 100 кДа, предпочтительно от примерно 10 кДа до примерно 50 кДа, еще более предпочтительно от примерно 10 кДа до примерно 30 кДа. В данном контексте также специально включены аналоги и производные белков или пептидов, которые определены в настоящем описании.
В конкретном случае такой катионный компонент полимерного носителя содержит или состоит из катионного или поликатионного пептида или белка, при этом катионные свойства катионного или поликатионного пептида или белка или полимерного носителя полностью, если полимерный носитель состоит из катионных или поликатионных пептидов или белков, могут быть определены на основе содержания в них катионных аминокислот, в частности, на основе содержания в них катионных аминокислот в избытке по отношению к анионным или нейтральным аминокислотам, и следовательно, на основе их общего положительного заряда. Предпочтительно, содержание катионных аминокислот в катионном или поликатионном пептиде или белке и/или полимерном носителе составляет по меньшей мере 10%, 20% или 30%, предпочтительно по меньшей мере 40%, более предпочтительно по меньшей мере 50%, 60% или 70%, но также предпочтительно по меньшей мере 80%, 90% или даже 95%, 96%, 97%, 98%, 99% или 100%, наиболее предпочтительно по меньшей мере 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98%, 99% или 100%, или может быть в диапазоне примерно от 10% до 90%, более предпочтительно в диапазоне примерно от 15% до 75%, еще более предпочтительно в диапазоне примерно от 20% до 50%, например, 20%, 30%, 40% или 50%, или в диапазоне, образованном любыми двумя вышеуказанными значениями, при условии, что содержание всех аминокислот, например, катионных, липофильных, гидрофильных, ароматических и других аминокислот в катионном или поликатионном пептиде или белке или в полном полимерном носителе, если полимерный носитель полностью состоит из катионных или поликатионных пептидов или белков, составляет 100%.
В данном контексте катионные аминокислоты предпочтительно представляют собой встречающиеся в природе аминокислоты Arg (аргинин), Lys (лизин), His (гистидин) и Orn (орнитин). Однако в более широком смысле любая (неприродная) аминокислота, несущая катионный заряд на своей боковой цепи, также может быть рассмотрена для осуществления изобретения. Однако такие катионные аминокислоты предпочтительно представляют собой аминокислоты, которые содержат боковые цепи, которые положительно заряжены в физиологических условиях pH. В более предпочтительном варианте такими аминокислотами являются Arg, Lys и Orn.
Предпочтительно, такие катионные или поликатионные пептиды или белки полимерного носителя, которые содержат или дополнительно модифицированы так, чтобы они содержали по меньшей мере один остаток -SH, выбраны без ограничения из катионных пептидов или белков, таких как протамин, нуклеолин, спермин или спермидин, олиго- или поли-L-лизин (PLL), основные полипептиды, олиго- или полиаргинин, проникающие в клетки пептиды (CPP), химерные CPP, такие как транспортан, или MPG-пептиды, ВИЧ-связывающие пептиды, Tat, Tat ВИЧ-1 (ВИЧ), полученные из Tat пептиды, представители семейства пенетратина, например пенетратин, полученные из Antennapedia пептиды (в частности, из Drosophila antennapedia), pAntp, plsI и т.д., производные противомикробных CPP, например, буфорин-2, Bac715-24, SynB, SynB(1), pVEC, полученные из hCT пептиды, SAP, MAP, KALA, PpTG20, L-олигомер, FGF, лактоферрин, гистоны, VP22-производные или аналогичные пептиды, HSV, VP22 (Herpes simplex), MAP, KALA или домены трансдукции белков (PTD, PpT620, богатые пролином пептиды, богатые аргинином пептиды, богатые лизином пептиды, Pep-1, L-олигомеры, пептид(ды) кальцитонина и т.д.
Альтернативно или дополнительно, такие катионные или поликатионные пептиды или белки полимерного носителя, которые содержат или дополнительно модифицированы так, чтобы они содержали по меньшей мере один остаток -SH, выбраны без ограничения из катионных пептидов, имеющих общую формулу (I):
{(Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x};
где l+m+n+o+x=3-100, и каждый из l, m, n или o независимо друг от друга является любым числом, выбранным из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21-30, 31-40, 41-50, 51-60, 61-70, 71-80, 81-90 и 91-100, при условии, что общее содержание Arg (аргинина), Lys (лизина), His (гистидина) и Orn (орнитина) составляет по меньшей мере 10% от всех аминокислот олигопептида; и Xaa означает любую аминокислоту, выбранную из нативных (= встречающихся в природе) или ненативных аминокислот, за исключением Arg, Lys, His или Orn; и x означает любое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21-30, 31-40, 41-50, 51-60, 61-70, 71-80, 81-90, при условии, что общее содержание Xaa не превышает 90% от всех аминокислот олигопептида. Любая из аминокислот Arg, Lys, His, Orn и Xaa может быть расположена в любом месте пептида. В данном контексте катионные пептиды или белки длиной в диапазоне 7-30 аминокислот являются особенно предпочтительными. Еще более предпочтительными пептидами, имеющими такую формулу, являются олигоаргинины, такие как, например, Arg7, Arg8, Arg9, Arg12, His3Arg9, Arg9His3, His3Arg9His3, His6Arg9His6, His3Arg4His3, His6Arg4His6, TyrSer2Arg9Ser2Tyr, (ArgLysHis)4, Tyr(ArgLysHis)2Arg и т.д.
Согласно конкретному предпочтительному варианту такие катионные или поликатионные пептиды или белки полимерного носителя, имеющие эмпирическую общую формулу (I), которая показана выше, могут без ограничения иметь по меньшей мере одну из следующих подгрупп формул:
Arg7, Arg8, Arg9, Arg10, Arg11, Arg12, Arg13, Arg14, Arg15-30;
Lys7, Lys8, Lys9, Lys10, Lys11, Lys12, Lys13, Lys14, Lys15-30;
His7, His8, His9, His10, His11, His12, His13, His14, His15-30;
Orn7, Orn8, Orn9, Orn10, Orn11, Orn12, Orn13, Orn14, Orn15-30.
Согласно следующему конкретному предпочтительному варианту катионные или поликатионные пептиды или белки полимерного носителя, имеющие эмпирическую общую формулу (I), которая показана выше, и которые содержат или дополнительно модифицированы так, чтобы они содержали по меньшей мере один остаток -SH, могут быть предпочтительно выбраны без ограничения из по меньшей мере одной из следующих подгрупп формул. Следующие формулы (как и в случае с эмпирической формулой (I)) конкретно не указывают какой-либо порядок аминокислот, а предназначены для отражения эмпирических формул исключительно путем конкретного указания (количества) аминокислот в качестве компонентов соответствующего пептида. Соответственно, в качестве примера, подразумевается, что эмпирическая формула Arg(7-29)Lys1 означает, что пептиды, подпадающие под такую формулу, содержат от 7 до 19 остатков Arg и 1 остаток Lys в любом порядке. Если пептиды содержат 7 остатков Arg и 1 остаток Lys, то все варианты, имеющие 7 остатков Arg и 1 остаток Lys, охвачены формулой. Следовательно, остаток Lys может быть расположен в любом месте последовательности, например, длиной 8 аминокислот, состоящей из 7 остатков Arg и 1 остатка Lys. Подгруппа предпочтительно содержит:


Согласно следующему конкретному предпочтительному варианту катионные или поликатионные пептиды или белки полимерного носителя, имеющие эмпирическую общую формулу (I), которая показана выше, которые содержат или дополнительно модифицированы так, чтобы они содержали по меньшей мере один остаток -SH, могут быть выбраны без ограничения из подгруппы, состоящей из соединений общих формул Arg7 (также называемых R7), Arg9 (также называемых R9), Arg12 (также называемых R12).
Согласно одному следующему конкретному предпочтительному варианту катионный или поликатионный пептид или белок полимерного носителя в том случае, когда он определен согласно формуле {(Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x}; (формула (I)), которая показана выше, который содержит или дополнительно модифицирован так, чтобы он содержал по меньшей мере один остаток -SH, может быть выбран, без ограничения, из соединений подформулы (Ia):
{(Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa')x(Cys)y}
где (Arg)l;(Lys)m;(His)n;(Orn)o и x имеют значения, которые определены в настоящем описании, Xaa' означает любую аминокислоту, выбранную из нативных (= встречающихся в природе) или ненативных аминокислот, за исключением Arg, Lys, His, Orn или Cys, и y означает любое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21-30, 31-40, 41-50, 51-60, 61-70, 71-80 и 81-90, при условии, что общее содержание Arg (аргинина), Lys (лизина), His (гистидина) и Orn (орнитина) составляет по меньшей мере 10% от всех аминокислот олигопептида.
Такой вариант можно применять в ситуациях, когда катионный или поликатионный пептид или белок полимерного носителя, например, в том случае, когда он определен согласно эмпирической формуле (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x (формула (I)), которая показана выше, содержит или был модифицирован по меньшей мере одним цистеином в качестве остатка -SH в указанном выше значении, так что катионный или поликатионный пептид в качестве катионного компонента несет по меньшей мере один цистеин, который способен образовывать дисульфидную связь с другими компонентами полимерного носителя.
Согласно другому конкретному предпочтительному варианту катионный или поликатионный пептид или белок полимерного носителя, в том случае, когда он определен согласно формуле {(Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x} (формула (I)), которая показана выше, без ограничения может быть выбран из соединений подформулы (Ib):
Cys1{(Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x}Cys2
где эмпирическая формула (формула (I)) представляет собой формулу, которая определена в настоящем описании, образует кор аминокислотной последовательности согласно (полуэмпирической) формуле (I), и при этом Cys1 и Cys2 представляют собой цистеины, расположенные проксимально или терминально по отношению к {(Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x}. Иллюстративные примеры могут содержать любую из указанных выше последовательностей, фланкированную двумя Cys и следующие последовательности:



Данный вариант можно применять в ситуациях, в которых катионный или поликатионный пептид или белок полимерного носителя, например, в том случае, когда он определен согласно эмпирической формуле (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x (формула (I)), которая показана выше, был модифицирован по меньшей мере двумя цистеинами в качестве остатков -SH в указанном выше значении, так что катионный или поликатионный пептид комплекса полимерного носителя и переносимого вещества в качестве катионного компонента несет по меньшей мере два (концевых) цистеина, которые способны образовывать дисульфидную связь с другими компонентами полимерного носителя.
Согласно второму альтернативному варианту, по меньшей мере один катионный (или поликатионный) компонент полимерного носителя может быть выбран, например, из любого (непептидного) катионного или поликатионного полимера, подходящего в данном контексте, при условии, что такой (непептидный) катионный или поликатионный полимер содержит или модифицирован так, чтобы он содержал по меньшей мере один остаток -SH, который обеспечивает образование дисульфидной связи катионного или поликатионного полимера с другим компонентом полимерного носителя, который определен в настоящем описании. Таким образом, подобно тому, как определено в настоящем описании, полимерный носитель может содержать одинаковые или разные катионные или поликатионные полимеры.
В конкретном случае, когда катионный компонент полимерного носителя содержит (непептидный) катионный или поликатионный полимер, катионные свойства (непептидного) катионного или поликатионного полимера могут быть определены на основании содержания катионных зарядов по сравнению с общими зарядами компонентов катионного полимера. Предпочтительно, содержание катионных зарядов, предпочтительно фактических катионных зарядов (т.е. после вычитания анионных и нейтральных зарядов), в катионном полимера при (физиологическим) pH, который определен в настоящем описании, составляет по меньшей мере 10%, 20% или 30%, предпочтительно по меньшей мере 40%, более предпочтительно по меньшей мере 50%, 60% или 70%, а также предпочтительно по меньшей мере 80%, 90% или даже 95%, 96%, 97%, 98%, 99% или 100%, наиболее предпочтительно по меньшей мере 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98%, 99% или 100%, или может быть в диапазоне примерно от 10% до 90%, более предпочтительно в диапазоне примерно от 30% до 100%, еще более предпочтительно в диапазоне примерно от 50% до 100%, например, 50, 60, 70, 80%, 90% или 100%, или в диапазоне, образованном любыми двумя из указанных выше значений, при условии, что содержание всех зарядов, например, положительных и отрицательных зарядов при (физиологическом) pH, который определен в настоящем описании, в полном катионном полимере составляет 100%.
Предпочтительно, (непептидный) катионный компонент полимерного носителя представляет собой катионный или поликатионный полимер, обычно имеющий молекулярную массу от примерно 0,1 или 0,5 кДа до примерно 100 кДа, предпочтительно от примерно 1 кДа до примерно 75 кДа, более предпочтительно от примерно 5 кДа до примерно 50 кДа, еще более предпочтительно от примерно 5 кДа до примерно 30 кДа или молекулярную массу от примерно 10 кДа до примерно 50 кДа, еще более предпочтительно от примерно 10 кДа до примерно 30 кД. Кроме того, (непептидный) катионный или поликатионный полимер обычно содержит по меньшей мере один остаток -SH, который способен образовывать дисульфидную связь при конденсации с любыми другими катионными компонентами или другими компонентами полимерного носителя, который определен в настоящем описании.
Указанные катионные или поликатионные пептиды или белки могут быть получена всеми способами, известными специалисту, или посредством получения рекомбинантного пептида или белка или в результате синтеза пептидов, который описан в настоящей публикации.
В указанном выше контексте (непептидный) катионный компонент полимерного носителя может быть выбран из акрилатов, модифицированных акрилатов, таких как pDMAEMA (поли(диметиламиноэтилметилакрилат)), хитозанов, азиридинов или 2-этил-2-оксазолина (образующего олигоэтиленимины или модифицированные олигоэтиленимины), полимеров, получаемых при взаимодействии бисакрилатов с аминами с образованием сложных олиго-бета-аминоэфиров или полиамидоаминов, или других полимеров, подобных сложным полиэфирам, поликарбонатам, и т.д. Каждая молекула таких (непептидных) катионных или поликатионных полимеров обычно содержит по меньшей мере один остаток -SH, при этом такой по меньшей мере один остаток -SH может быть введен в (непептидный) катионный или поликатионный полимер посредством химических модификаций, например, с использованием иминотиолана, 3-тиопропионовой кислоты или введением аминокислот, содержащих -SH-остатки, таких как цистеин или любая другая (модифицированная) аминокислота. Такие остатки -SH предпочтительно представляют собой остатки, которые уже определены выше.
В контексте полимерного носителя катионные компоненты, которые образуют основу для полимерного носителя поперечным сшиванием дисульфидными связями, могут быть одинаковыми или могут отличаться друг от друга. Также особенно предпочтительно, чтобы полимерный носитель согласно настоящему изобретению содержал смеси катионных пептидов, белков или полимеров и необязательно дополнительных компонентов, которые определены в настоящем описании, которые поперечно сшиты дисульфидными связями, описанными в настоящей публикации. Особенно предпочтительными катионными компонентами полимерного носителя в контексте настоящего изобретения являются катионные пептиды или белки.
В данном контексте комплекс полимерного носителя и переносимого вещества благодаря тому, что полимерный носитель можно варьировать, преимущественно позволяет комбинировать требуемые свойства разных (коротких) катионных или поликатионных пептидов, белков или полимеров или других компонентов. Полимерный носитель, например, позволяет эффективно осуществлять компактизацию нуклеиновой кислоты в целях эффективной трансфекции нуклеиновых кислот, для адъювантной терапии, в целях генной терапии, для нокдауна генов или других методик без потери активности, в частности, обеспечивая эффективную трансфекцию нуклеиновой кислоты в разные клеточные линии in vitro, но особенно трансфекцию in vivo. Полимерный носитель и, следовательно, комплекс полимерного носителя и переносимого вещества, кроме того, является нетоксичным для клеток, обеспечивает высвобождение переносимой нуклеиновой кислоты, является стабильным при лиофилизации и применим в качестве иммуностимулирующего средства или адъюванта. Предпочтительно, комплекс полимерного носителя и переносимого вещества может индуцировать противовирусный цитокин IFN-альфа.
В частности, полимерный носитель, образованный связанными дисульфидной связью катионными компонентами, позволяет в значительной степени варьировать его пептидным или полимерным содержимым и таким образом модулировать его биофизические/биохимические свойства, в частности катионные свойства полимерного носителя, довольно легко и быстро, например, за свет введения в качестве катионных компонентов одинаковых или разных катионных пептидов или полимеров и необязательно добавления других компонентов в полимерный носитель. Даже притом, что полимерный носитель состоит из довольно небольших нетоксичных мономерных единиц, он образует длинную катионную связывающую последовательность, обеспечивающую сильную конденсацию переносимой нуклеиновой кислоты и стабильность комплекса. В восстанавливающих условиях в цитозоле (например, цитозольный GSH), комплекс быстро распадается на (катионные) компоненты, которые затем разрушаются (например, олигопептиды). Это обеспечивает высвобождение переносимой нуклеиновой кислоты в цитозоль. Вследствие распада на небольшие олигопептиды или полимеры в цитозоле не наблюдается токсичности, которая, как известно, имеет место в случае высокомолекулярных олигопептидов или полимеров, например, в случае высокомолекулярного полиаргинина.
Соответственно, полимерный носитель комплекса полимерного носителя и переносимого вещества может содержать разные (короткие) катионные или поликатионные пептиды, белки или полимеры, выбранные из катионных или поликатионных пептидов, белков или (непептидных) полимеров, которые определены выше, необязательно вместе с дополнительными компонентами, которые определены в настоящем описании.
Кроме того, полимерный носитель комплекса полимерного носителя и переносимого вещества, который определен выше, более предпочтительно по меньшей мере один из разных (коротких) катионных или поликатионных пептидов или (непептидных) полимеров, образующих основу для полимерного носителя посредством поперечного сшивания дисульфидными связями, предпочтительно может быть модифицирован перед поперечным сшиванием дисульфидными связями по меньшей мере одним дополнительным компонентом. Альтернативно, полимерный носитель, как таковой, может быть модифицирован по меньшей мере одним дополнительным компонентом. Также необязательно он может содержать по меньшей мере один дополнительный компонент, который обычно образует дисульфид полимерного носителя вместе с другими (короткими) катионными или поликатионными пептидами, которые определены выше, посредством образования поперечных сшивок дисульфидными связями.
Чтобы обеспечить возможность модификации катионного или поликатионного пептида или (непептидного) полимера, которые определены выше, каждый из компонентов полимерного носителя также может (предпочтительно уже до поперечного сшивания дисульфидными связями) содержать по меньшей мере один дополнительный функциональный остаток, который позволяет связывать такие дополнительные компоненты, которые определены в настоящем описании. Такие функциональные остатки могут быть выбраны из функциональных групп, которые позволяют связывать дополнительные компоненты, например, из функциональностей, которые определены в настоящем описании, например, посредством образования амидов (например, карбоновые кислоты, сульфокислоты, амины и т.д.), присоединения по Михаэлю (например, остатки малеинимида, α,β-ненасыщенные карбонилы и т.д.), посредством клик-химии (например, азиды или алкины), метатезиса алкена/алкина (например, алкены или алкины), образования имина или гидрозона (альдегиды или кетоны, гидразин, гидроксиламины, амины), реакций комплексообразования (авидин, биотин, белок G) или компонентов, которые обеспечивают возможность реакций замещения Sn-типа (например, галогеналканы, тиолы, спирты, амины, гидразины, гидразиды, сложные эфиры сульфоновой кислоты, соли оксифосфония), или других химических остатков, которые можно использовать при связывании других компонентов.
Согласно особенно предпочтительному варианту дополнительным компонентом, который может входить в состав полимерного носителя или который можно использовать для того, чтобы модифицировать разные (короткие) катионные или поликатионные пептиды или (непептидные) полимеры, образующие основу для полимерного носителя комплекса полимерного носителя и переносимого вещества, является аминокислотный компонент (AA), который, например, может модифицировать биофизические/биохимические свойства полимерного носителя, который определен в настоящем описании. Согласно настоящему изобретению аминокислотный компонент (AA) содержит определенное количество аминокислот, предпочтительно в диапазоне примерно от 1 до 100, предпочтительно в диапазоне примерно от 1 до 50, более предпочтительно, выбранное из количества, включающего 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15-20, или может быть выбран из диапазона, образованного любыми двумя из вышеуказанных значений. В данном контексте аминокислоты из аминокислотного компонента (AA) могут быть выбраны независимо друг от друга. Например, если в полимерном носителе присутствуют два или более (AA) компонентов, они могут быть одинаковыми или могут отличаться друг от друга.
Аминокислотный компонент (AA) может содержать или может быть фланкирован (например, на концах) -SH-содержащим остатком, который позволяет вводить такой компонент (AA) посредством дисульфидной связи с полимерным носителем, который определен в настоящем описании. В конкретном случае, когда -SH-содержащий остаток представляет собой цистеин, аминокислотный компонент (AA) также можно записать как -Cys-(AA)-Cys-, где Cys означает цистеин, и обеспечивает необходимый -SH-остаток для дисульфидной связи. -SH-содержащий остаток также может быть введен в аминокислотный компонент (AA) с использованием любых модификаций или реакций, которые указаны выше для катионного компонента или любых его компонентов.
Кроме того, аминокислотный компонент (AA) может иметь два остатка -SH (или еще больше), например, в форме, представленной формулой HS-(AA)-SH, обеспечивая связывание двух функциональностей посредством дисульфидных связей, например, если аминокислотный компонент (AA) используют в качестве линкера между двумя дополнительными компонентами (например, в качестве линкера между двумя катионными полимерами). В таком случае один -SH-остаток предпочтительно защищен на первой стадии с использованием защитной группы, которая известна в данной области, с получением аминокислотного компонента (AA) формулы HS-(AA)-S-защитная группа. Затем аминокислотный компонент (AA) может быть связан со следующим компонентом полимерного носителя с образованием первой дисульфидной связи через незащищенный остаток -SH. Затем обычно удаляют защиту с защищенного -SH-остатка и связывают со следующим свободным -SH-остатком следующего компонента полимерного носителя с образованием второй дисульфидной связи.
Альтернативно, аминокислотный компонент (AA) может быть снабжен другими функциональными группами, которые уже описаны выше для других компонентов полимерного носителя, которые позволяют связывать аминокислотный компонент (AA) с любыми компонентами полимерного носителя.
В некоторых вариантах, в которых аминокислотный компонент (AA) связан посредством дисульфидных связей с полимерным носителем, предпочтительно, чтобы дисульфидная связь не была осуществлена через поперечный линкер, такой как поперечный линкер 3,6-диокса-1,8-октандитиол (DODT).
Таким образом, аминокислотный компонент (AA) может быть связан со следующими компонентами полимерного носителя с использованием или без использования дисульфидной связи. Связывание без использования дисульфидной связи может быть осуществлено посредством любой из реакций, описанных выше, предпочтительно в результате связывания аминокислотного компонента (AA) с другим компонентом полимерного носителя с использованием химии амидов, как определено в настоящем описании. При желании или необходимости другой конец аминокислотного компонента (AA), например, N- или C-конец, можно использовать для связывания с другим компонентом, например лигандом L. С указанной целью другой конец аминокислотного компонента (AA) предпочтительно содержит или модифицирован так, чтобы он содержал дополнительную функциональную группу, например вид алкина (смотри выше), которую можно использовать для добавления других компонентов, например, посредством клик-химии. Если лиганд связан через кислотолабильную связь, такая связь предпочтительно расщепляется в эндосоме, и полимерный носитель презентирует аминокислотный компонент (AA) на своей поверхности.
Аминокислотный компонент (AA) может встречаться в качестве дополнительного компонента полимерного носителя, который определен выше, например, в качестве линкера между катионными компонентами, например, в качестве линкера между одним катионным пептидом и следующим катионным пептидом, в качестве линкера между одним катионным полимером и следующим катионным полимером, в качестве линкера между одним катионным пептидом и катионным полимером, которые все предпочтительно представляют собой катионные пептиды и катионные полимеры, которые определены в настоящем описании, или в качестве дополнительного компонента полимерного носителя, например, при связывании аминокислотного компонента (AA) с полимерным носителем или его компонентом, например, посредством боковых цепей, SH-остатков или через дополнительные остатки, которые определены в настоящем описании, при этом аминокислотный компонент (AA) предпочтительно соответствующим образом модифицирован.
Согласно следующему и особенно предпочтительному альтернативному варианту аминокислотный компонент (AA) может быть использован для модификации полимерного носителя, особенно содержания катионных компонентов в полимерном носителе, который определен выше.
В данном контексте предпочтительно, чтобы содержание катионных компонентов в полимерном носителе составляло по меньшей мере 10%, 20% или 30%, предпочтительно по меньшей мере 40%, более предпочтительно по меньшей мере 50%, 60% или 70%, а также предпочтительно по меньшей мере 80%, 90% или даже 95%, 96%, 97%, 98%, 99% или 100%, наиболее предпочтительно по меньшей мере 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98%, 99% или 100%, или может быть в диапазоне примерно от 30% до 100%, более предпочтительно в диапазоне примерно от 50% до 100%, еще более предпочтительно в диапазоне примерно от 70% до 100%, например 70, 80, 90 или 100%, или в диапазоне, образованном любыми двумя из указанных выше значений, при условии, что содержание всех компонентов в полимерном носителе составляет 100%.
В контексте настоящего изобретения аминокислотный компонент (AA) может быть выбран из следующих альтернативных вариантов.
Согласно первому альтернативному варианту аминокислотный компонент (AA) может представлять собой ароматический аминокислотный компонент (AA). Включение ароматической аминокислоты или последовательностей в качестве ароматического аминокислотного компонента (AA) в полимерный носитель согласно настоящему изобретению позволяет осуществлять другое (второе) связывание полимерного носителя с нуклеиновой кислотой в результате взаимодействий ароматических аминокислот с основаниями переносимой нуклеиновой кислоты в отличие от ее связывания посредством катионных заряженных последовательностей молекулы полимерного носителя с фосфатным остовом. Такое взаимодействие может происходить, например, посредством интеркаляций или посредством связывания в малой или большой бороздках. Такой вид взаимодействия не склонен в декомпактизации анионными комплексообразующими партнерами (например, гепарином, гиалуроновыми кислотами), которые встречаются, главным образом, во внеклеточном матриксе in vivo, а также менее чувствителен к действию солей.
Для указанной цели аминокислоты в ароматическом аминокислотном компоненте (AA) могут быть выбраны из любых одинаковых или разных ароматических аминокислот, например, выбраны из Trp, Tyr или Phe.
Кроме того, ароматический аминокислотный компонент (AA) может содержать или может быть фланкирован -SH-содержащим остатком, который позволяет вводить такой компонент посредством дисульфидной связи в качестве следующей части полимерного носителя, который определен выше, например, в качестве линкера. Такой -SH-содержащий остаток может представлять собой любой остаток, который определен в настоящем описании, подходящий для связывания одного компонента, который определен в настоящем описании, со следующим компонентом, который определен в настоящем описании. В качестве примера таким -SH-содержащим остатком может быть цистеин.
Кроме того, ароматический аминокислотный компонент (AA) может содержать или представлять по меньшей мере один пролин, который может служить в качестве компонента, нарушающего структуру более длинных последовательностей Trp, Tyr и Phe в ароматическом аминокислотном компоненте (AA), предпочтительно два, три или более пролинов.
Согласно второму альтернативному варианту аминокислотный компонент (AA) может представлять собой гидрофильный (и предпочтительно незаряженный полярный) аминокислотный компонент (AA). Введение гидрофильных (и предпочтительно незаряженных полярных) аминокислот или последовательностей в качестве гидрофильного (и предпочтительно незаряженного полярного) аминокислотного компонента (AA) в полимерный носитель согласно настоящему изобретению обеспечивает возможность более гибкого связывания с переносимой нуклеиновой кислотой. Это приводит к более эффективной компактизации переносимой нуклеиновой кислоты и, следовательно, лучшей защите от нуклеаз и нежелательной декомпактизации. Это также позволяет получить (длинный) полимерный носитель, который имеет уменьшенный катионный заряд по сравнению с полным носителем, и в данном контексте позволяет при желании или необходимости лучше корректировать связывающие свойства.
С указанной целью аминокислоты в гидрофильном (и предпочтительно незаряженном полярном) аминокислотном компоненте (AA) могут быть выбраны из любых одинаковых или разных гидрофильных (и предпочтительно незаряженных полярных) аминокислот, например, выбраны из Thr, Ser, Asn или Gln.
Кроме того, гидрофильный (и предпочтительно незаряженный полярный) аминокислотный компонент (AA) может содержать или может быть фланкирован -SH-содержащим остатком, который позволяет вводить такой компонент посредством дисульфидной связи в качестве следующей части соединения общей формулы (I), описанной выше, например, в качестве линкера. Такой -SH-содержащий остаток может представлять собой любой остаток, который определен в настоящем описании, подходящий для связывания одного компонента, который определен в настоящем описании, со следующим компонентом, который определен в настоящем описании. В качестве примера таким -SH-содержащим остатком может быть цистеин.
Кроме того, гидрофильный (и предпочтительно незаряженный полярный) аминокислотный компонент (AA) может содержать по меньшей мере один пролин, который может служить в качестве компонента, нарушающего структуру более длинных последовательностей Ser, Thr и Asn в гидрофильном (и предпочтительно незаряженном полярном) аминокислотном компоненте (AA), предпочтительно два, три или более пролинов.
Согласно третьему альтернативному варианту аминокислотный компонент (AA) может представлять собой липофильный аминокислотный компонент (AA). Введение липофильных аминокислот или последовательностей в качестве липофильного аминокислотного компонента (AA) в полимерный носитель согласно настоящему изобретению обеспечивает возможность более сильной компактизации переносимой нуклеиновой кислоты и/или полимерного носителя и переносимой им нуклеиновой кислоты при образовании комплекса. Это, в частности, является следствием взаимодействий одной или нескольких нитей полимера полимерного носителя, в частности, липофильных участков липофильного аминокислотного компонента (AA), и переносимой нуклеиновой кислоты. Такое взаимодействие предпочтительно будет придавать дополнительную стабильность комплексу, образованному между полимерным носителем и переносимой им нуклеиновой кислотой. Такая стабилизация определенным образом может быть сравнима с определенным видом нековалентного поперечного сшивания между разными полимерными нитями. Особенно в водной среде такое взаимодействие обычно является сильным и обеспечивает значимый эффект.
Для указанной цели аминокислоты в липофильном аминокислотном компоненте (AA) могут быть выбраны из любых одинаковых или разных липофильных аминокислот, например, выбраны из Leu, Val, Ile, Ala, Met.
Кроме того, липофильный аминокислотный компонент (AA) может содержать или может быть фланкирован -SH-содержащим остатком, который позволяет вводить такой компонент посредством дисульфидной связи в качестве следующей части полимерного носителя, описанного выше, например, в качестве линкера. Такой -SH-содержащий остаток может представлять собой любой остаток, который определен в настоящем описании, подходящий для связывания одного компонента, который определен в настоящем описании, со следующим компонентом, который определен в настоящем описании. В качестве примера таким -SH-содержащим остатком может быть цистеин.
Кроме того, липофильный аминокислотный компонент (AA) может содержать по меньшей мере один пролин, который может служить в качестве компонента, нарушающего структуру более длинных последовательностей Leu, Val, Ile, Ala и Met в липофильном аминокислотном компоненте (AA), предпочтительно два, три или больше пролинов.
Наконец, согласно четвертому альтернативному варианту аминокислотный компонент (AA) может представлять слабо основный аминокислотный компонент (AA). Введение слабо основных аминокислот или последовательностей в качестве слабо основного аминокислотного компонента (AA) в полимерный носитель согласно настоящему изобретению может служить в качестве протонной губки и облегчает избегание эндосом (также называемое высвобождением из эндосом) (эффект протонной губки). Введение такого слабо основного аминокислотного компонента (AA) предпочтительно усиливает эффективность трансфекции.
С указанной целью аминокислоты в слабо основном аминокислотном компоненте (AA) могут быть выбраны из любых одинаковых или разных слабо основных аминокислот, например, выбраны из гистидина или аспартата (аспарагиновой кислоты).
Кроме того, слабо основный аминокислотный компонент (AA) может содержать или может быть фланкирован -SH-содержащим остатком, который обеспечивает возможность введения такого компонента посредством дисульфидной связи в качестве следующей части соединения общей формулы (I), описанной выше, например, в качестве линкера. Таким -SH-содержащим остатком может быть любой остаток, который определен в настоящем описании, подходящий для связывания одного компонента, который определен в настоящем описании, со следующим компонентом, который определен в настоящем описании.
Кроме того, слабо основный аминокислотный компонент (AA) может содержать по меньшей мере один пролин, который может служить в качестве компонента, нарушающего структуру более длинных последовательностей гистидина или аспартата (аспарагиновой кислоты) в слабо основном аминокислотном компоненте (AA), предпочтительно два, три или более пролинов.
Согласно пятому альтернативному варианте аминокислотный компонент (AA) может представлять собой сигнальный пептид или сигнальную последовательность, сигнал или последовательность локализации, сигнал или последовательность ядерной локализации (NLS), антитело, проникающий в клетку пептид (например, TAT) и т.д. Предпочтительно такой аминокислотный компонент (AA) связан с полимерным носителем или другим компонентом полимерного носителя посредством (обратимой) дисульфидной связи. В данном контексте сигнальный пептид или сигнальная последовательность, сигнал или последовательность локализации, сигнал или последовательность ядерной локализации (NLS), антитело, проникающий в клетку пептид (например, TAT) и т.д. дополнительно содержит по меньшей мере один -SH-остаток. В данном контексте сигнальный пептид, сигнал или последовательность локализации или сигнал или последовательность ядерной локализации (NLS) можно использовать для направления комплекса полимерного носителя и переносимого вещества согласно изобретению в конкретные клетки-мишени (например, гепатоциты или антигенпрезентирующие клетки), и предпочтительно он позволяет осуществлять транслокацию полимерного носителя в конкретную мишень, например, в клетку, в ядро, в эндосомальный компартмент, последовательности для митохондриального матрикса, последовательности локализации в плазматической мембране, последовательности локализации в аппарате Гольджи, ядре, цитоплазме и цитоскелете и т.д. Такой сигнальный пептид, сигнал или последовательность локализации или сигнал ядерной локализации можно использовать для транспорта любой из определенных в настоящем описании нуклеиновых кислот, предпочтительно РНК или ДНК, более предпочтительно кшРНК или пДНК, например, в ядро. Без ограничения, такой сигнальный пептид, сигнал или последовательность локализации или сигнал ядерной локализации может содержать, например, последовательности локализации в эндоплазматическом ретикулуме. Примеры сигнальных пептидов секреции, которые определены в настоящем описании, включают без ограничения сигнальные пептиды классических или неклассических молекул MHC (например, сигнальные последовательности молекул MHC I и II, например, молекулы MHC класса I HLA-A*0201), сигнальные пептиды цитокинов или иммуноглобулинов, которые определены в настоящем описании, сигнальные пептиды инвариантной цепи иммуноглобулинов или антител, который определены в настоящем описании, сигнальные пептиды Lamp1, таразина, Erp57, кальретикулина, кальнексина и других ассоциированных с мембранами белков или белков, ассоциированных с эндоплазматическим ретикулумом (ER) или компартментом эндосом-лизосом. Особенно предпочтительно, согласно настоящему изобретению могут быть использованы сигнальные пептиды молекулы MHC класса I HLA-A*0201. Такой дополнительный компонент может быть связан, например, с катионным полимером или любым другим компонентом полимерного носителя, который определен в настоящем описании. Предпочтительно, такой сигнальный пептид, сигнал или последовательность локализации или сигнал или последовательность ядерной локализации (NLS) связаны с полимерным носителем или с другим компонентом полимерного носителя посредством (обратимой) дисульфидной связи. Для указанной цели компонент (AA) дополнительно содержит по меньшей мере один -SH-остаток, который определен в настоящем описании. Связывание с любым из компонентов полимерного носителя также может быть осуществлено с использованием кислотолабильной связи, предпочтительно посредством боковой цепи любого из компонентов полимерного носителя, которая позволяет откреплять или высвобождать дополнительный компонент при более низких значениях pH, например, при физиологических значениях pH, которые определены в настоящем описании.
Кроме того, согласно другому альтернативному варианту аминокислотный компонент (AA) может представлять собой функциональный пептид или белок, который, соответственно, может модулировать функциональность полимерного носителя. Такие функциональные пептиды или белки в качестве аминокислотного компонента (AA) предпочтительно содержат любые пептиды или белки, которые определены в настоящем описании, например, которые определены ниже в качестве терапевтически активных белков. Согласно одному альтернативному варианту такие дополнительные функциональные пептиды или белки могут содержать так называемые проникающие в клетку пептиды (CPP) или катионные пептиды для транспортировки. Особенно предпочтительными являются CPP, которые индуцируют pH-опосредованное конформационное изменение в эндосоме и приводят к улучшенному высвобождению полимерного носителя (в комплексе с нуклеиновой кислотой) из эндосомы за счет встраивания в липидный слой липосомы. Такие проникающие в клетку пептиды (CPP) или катионные пептиды для транспортировки могут включать без ограничения протамин, нуклеолин, спермин или спермидин, олиго- или поли-L-лизин (PLL), основные полипептиды, олиго- или полиаргинин, проникающие в клетку пептиды (CPP), химерные CPP, такие как транспортан, или MPG-пептиды, ВИЧ-связывающие пептиды, Tat, Tat ВИЧ-1 (ВИЧ), полученные из Tat пептиды, представители семейства пенетратина, например, пенетратин, полученные из Antennapedia пептиды (в частности, из Drosophila antennapedia), pAntp, plsI и т.д., производные противомикробных CPP, например, буфорин-2, Bac715-24, SynB, SynB(1), pVEC, полученные из hCT пептиды, SAP, MAP, KALA, PpTG20, L-олигомер, FGF, лактоферрин, гистоны, VP22-производные или аналогичные пептиды, HSV, VP22 (Herpes simplex), MAP, KALA или домены трансдукции белков (PTD, PpT620, богатые пролином пептиды, богатые аргинином пептиды, богатые лизином пептиды, Pep-1, L-олигомеры, пептид(ды) кальцитонина и т.д.). Такой аминокислотный компонент (AA) также может быть связан с любым компонентом полимерного носителя, который определен в настоящем описании. Предпочтительно, он связан с полимерным носителем или другим компонентом полимерного носителя через (обратимую) дисульфидную связь. Для указанной выше цели аминокислотный компонент (AA) предпочтительно содержит по меньшей мере один -SH-остаток, который определен в настоящем описании. Связывание с любым из компонентов полимерного носителя также может быть осуществлено с использованием SH-остатка или кислотолабильной связи, предпочтительно через боковую цепь любого из компонентов полимерного носителя, которая позволяет откреплять или высвобождать дополнительный компонент при более низких значениях pH, например, при физиологических значениях pH, которые определены в настоящем описании.
Согласно последнему альтернативному варианту аминокислотный компонент (AA) может состоять из любого пептида или белка, который может выполнять любую предпочтительную функцию в клетке. Особенно предпочтительными являются пептиды или белки, выбранные из терапевтически активных белков или пептидов, из антигенов, например опухолевых антигенов, антигенов патогенов (животных антигенов, вирусных антигенов, антигенов простейших, бактериальных антигенов, аллергенных антигенов), аутоиммунных антигенов, или других антигенов, из аллергенов, из антител, из иммуностимулирующих белков или пептидов, из антигенспецифичных T-клеточных рецепторов или из любых других белков или пептидов, подходящих для конкретного (терапевтического) применения, которое определено ниже для кодирующих нуклеиновых кислот. Особенно предпочтительными являются пептидные эпитопы по меньшей мере из одного антигена (антигена, полученного из патогена, ассоциированного с инфекционной болезнью; антигена, ассоциированного с аллергией или аллергическим заболеванием; антигена, ассоциированного с аутоиммунным заболеванием; или антигена, ассоциированного с раком или опухолевым заболеванием), который определен в настоящем описании.
В случае, когда аминокислотный компонент (AA) ковалентно связан с комплексом полимерного носителя и переносимого вещества, в частности с полимерным носителем, аминокислотный компонент (AA) предпочтительно не является овальбумином или фрагментом овальбумина. Предпочтительно, аминокислотный компонент не является овальбумином или фрагментом овальбумина.
Вследствие пептидной природы аминокислотного компонента соответственно применимо определение пептида, белка или его фрагмента, варианта и производного и специально включено в настоящее описание.
Кроме того, указанные компоненты (AA) могут быть получены любыми способами, известными специалисту, либо путем получения рекомбинантного пептида или белка, либо путем синтеза пептидов, как описано в настоящей публикации.
Полимерный носитель может содержать по меньшей мере один из указанных выше катионных или поликатионных пептидов, белков или полимеров или других компонентов, например, (AA), при этом любые из указанных выше альтернативных вариантов можно сочетать друг с другом, и он может быть образован полимеризацией указанных компонентов в реакции конденсационной полимеризации с использованием их -SH-остатков.
Согласно другому варианту полимерный носитель комплекса полимерного носителя и переносимого вещества или его отдельные компоненты, например, указанные выше катионные или поликатионные пептиды, белки или полимеры или другие компоненты, например, (AA), могут быть дополнительно модифицированы лигандом, предпочтительно углеводом, более предпочтительно сахаром, еще более предпочтительно маннозой. Предпочтительно, такой лиганд связан с полимерный носителем или с компонентом полимерного носителя (обратимой) дисульфидной связью или посредством присоединения по Михаэлю. В случае, когда лиганд связан дисульфидной связью, лиганд дополнительно содержит по меньшей мере один -SH-остаток. Такие лиганды можно использовать для направления комплекса полимерного носителя и переносимого вещества в конкретные клетки-мишени (например, гепатоциты или антигенпрезентирующие клетки). В данном контексте манноза является особенно предпочтительной в качестве лиганда в случае, когда мишенью являются дендритные клетки, особенно в целях вакцинации или для адъюванта.
Согласно следующему варианту изобретения комплекс полимерного носителя и переносимого вещества может содержать компоненты (AA), которые определены выше, которые не содержат -SH-остатков. Такие компоненты (AA) могут быть добавлены до или во время реакции образования комплекса по меньшей мере с одной молекулой нуклеиновой кислоты. При этом компонент(ты) (нековалентно) включают в комплекс полимерного носителя и переносимого вещества без включения компонента(ов) (AA) в сам полимерный носитель в результате (ковалентной) полимеризации.
Согласно одному конкретному варианту полный комплекс полимерного носителя и переносимого вещества может быть образован в результате конденсационной полимеризации (по меньшей мере одного) из указанных выше катионных или поликатионных пептидов, белков или полимеров или дополнительных компонентов, например, (AA), посредством их -SH-остатков на первой стадии и образования комплекса нуклеиновой кислоты с таким полимерным носителем на второй стадии. Таким образом, полимерный носитель может содержать определенное количество по меньшей мере одного или более одинаковых или разных определенных выше катионных или поликатионных пептидов, белков или полимеров или дополнительных компонентов, например, (AA), при этом количество предпочтительно находится в указанном выше диапазоне.
Согласно одному альтернативному конкретному варианту комплекс полимерного носителя и переносимого вещества образуют, осуществляя конденсационную полимеризацию по меньшей мере одного из указанных выше катионных или поликатионных пептидов, белков или полимеров или дополнительных компонентов, например, (AA), посредством их -SH-остатков одновременно с образованием комплекса переносимой нуклеиновой кислоты с (полученным in situ) полимерным носителем. Подобным образом, полимерный носитель также может содержать определенное количество по меньшей мере одного или нескольких одинаковых или разных определенных выше катионных или поликатионных пептидов, белков или полимеров или дополнительных компонентов, например, (AA), при этом количество предпочтительно находится в указанном выше диапазоне.
Комплекс полимерного носителя и переносимого вещества дополнительно содержит в качестве переносимого вещества по меньшей мере одну нуклеиновую кислоту (молекулу). В контексте настоящего изобретения такая молекула нуклеиновой кислоты может представлять собой любую подходящую нуклеиновую кислоту, выбранную, например, из любой (однонитевой или двунитевой) ДНК, предпочтительно, например и без ограничения, геномную ДНК, однонитевые молекулы ДНК, двунитевые молекулы ДНК, кодирующую ДНК, ДНК-праймеры, ДНК-зонды, иммуностимулирующие ДНК, (короткие) олигонуклеотиды ДНК ((короткие) олигодезоксирибонуклеотиды), или может быть выбрана, например, из любой PNA (пептидонуклеиновой кислоты) или может быть выбрана, например, из любой (однонитевой или двунитевой) РНК, предпочтительно, без ограничения ими, (короткого) олигонуклеотида РНК ((короткого) олигорибонуклеотида), кодирующей РНК, матричной РНК (мРНК), иммуностимулирующей РНК, малой интерферирующей РНК (миРНК), антисмысловой РНК, микро-РНК, малой ядерной РНК (мяРНК), короткой шпилечной (кш)РНК или рибопереключателей (рибосвитчей), рибозимов или аптамеров; и т.д. Молекула нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества также может представлять собой рибосомную РНК (рРНК), транспортную РНК (тРНК), матричную РНК (мРНК) или вирусную РНК (вРНК). Предпочтительно, молекула нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества представляет собой РНК. Более предпочтительно, молекула нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества представляет собой (линейную) однонитевую РНК, еще более предпочтительно мРНК или иммуностимулирующую РНК. В контексте настоящего изобретения мРНК обычно представляет собой РНК, которая состоит из нескольких структурных элементов, например, необязательной 5'-кэп-структуры, необязательной 5'-UTR-области, вышерасположенного участка связывания с рибосомой с последующей кодирующей областью, необязательной 3'-UTR-области, за который может следовать поли-A хвост (и/или поли-C-хвост). мРНК может встречаться в виде моно-, ди- или даже полицистронной РНК, т.е. РНК, которая несет кодирующие последовательности одного, двух или более белков или пептидов. Такие кодирующие последовательности в ди- или даже полицистронной мРНК могут быть разделены по меньшей мере одной последовательностью IRES, например, как определено в настоящем описании.
Кроме того, нуклеиновая кислота комплекса полимерного носителя и переносимого вещества может представлять собой одно- или двунитевую нуклеиновую кислоту (молекулу) (которую также можно рассматривать как нуклеиновую кислоту (молекулу), полученную благодаря нековалентной ассоциации двух однонитевых нуклеиновых кислот (молекул)) или частично двунитевую или частично однонитевую нуклеиновую кислоту, которые по меньшей мере частично являются самокомплементарными (обе такие частично двунитевые или частично однонитевые молекулы нуклеиновых кислот обычно образованы более длинной и более короткой однонитевыми молекулами нуклеиновых кислот или двумя однонитевыми молекулами нуклеиновых кислот, которые примерно равны по длине, но при этом одна однонитевая молекула нуклеиновой кислоты частично комплементарна другой однонитевой молекуле нуклеиновой кислоты, и, следовательно, обе образуют двунитевую молекулу нуклеиновой кислоты в такой области, т.е. частично двунитевую или частично однонитевую нуклеиновую кислоту (молекулу). Предпочтительно, нуклеиновая кислота (молекула) может быть однонитевой молекулой нуклеиновой кислоты. Кроме того, нуклеиновая кислота (молекула) может быть кольцевой или линейной молекулой нуклеиновой кислоты, предпочтительно линейной молекулой нуклеиновой кислоты.
Согласно одному альтернативному варианту молекула нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества может представлять собой кодирующую нуклеиновую кислоту, например, ДНК или РНК. Такая кодирующая ДНК или РНК может представлять собой любую ДНК или РНК, которая определена в настоящем описании. Предпочтительно, такая кодирующая ДНК или РНК может представлять собой одно- или двунитевую ДНК или РНК, более предпочтительно однонитевую ДНК или РНК, и/или кольцевую или линейную ДНК или РНК, более предпочтительно линейную ДНК или РНК. Еще более предпочтительно, кодирующая ДНК или РНК может представлять собой (линейную) однонитевую ДНК или РНК. Наиболее предпочтительно, молекула нуклеиновой кислоты согласно настоящему изобретению может представлять собой ((линейную) однонитевую) матричную РНК (мРНК). Такая мРНК может быть в виде моно-, ди- или даже полицистронной РНК, т.е. РНК, которая несет кодирующие последовательности одного, двух или более белков или пептидов. Такие кодирующие последовательности в ди- или даже полицистронной мРНК могут быть разделены по меньшей мере одной последовательностью IRES, например, как определено в настоящем описании.
Кодирующие нуклеиновые кислоты
Молекула нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества может кодировать белок или пептид, который может быть выбран без ограничения, например, из терапевтически активных белков или пептидов, включая адъювантные белки, из антигенов, например, опухолевых антигенов, антигенов патогенов (например, выбранных из животных антигенов, из вирусных антигенов, из антигенов простейших, из бактериальных антигенов), аллергенных антигенов, аутоиммунных антигенов или других антигенов, из аллергенов, из антител, из иммуностимулирующих белков или пептидов, из антигенспецифичных T-клеточных рецепторов или из любого другого белка или пептида, подходящего для конкретного (терапевтического) применения, при этом кодирующая нуклеиновая кислота может быть транспортирована в клетку, ткань или организм, и затем белок может быть экспрессирован в такой клетке, ткани или организме. В данном контексте кодирующая нуклеиновая кислота может дополнительно кодировать сигнальный пептид, который определен в настоящем описании.
a) Терапевтически активные белки
В контексте настоящего изобретения терапевтически активные белки или пептиды могут кодироваться молекулой нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества. Терапевтически активные белки определяют в настоящем описании как белки, которые оказывают влияние на выздоровление, профилактически предотвращают или терапевтически лечат заболевание, предпочтительно, которое определено в настоящем описании, как белки, в которых нуждается индивидуум. Такие белки могут быть выбраны из любых встречающихся в природе или синтетически сконструированных рекомбинантных или изолированных белков, известных специалисту в данной области. Без ограничения, терапевтически активные белки могут включать белки, способные стимулировать или ингибировать сигнальную трансдукцию в клетке, например, цитокины, лимфокины, монокины, факторы роста, рецепторы, молекулы сигнальной трансдукции, факторы транскрипции и т.д.; антикоагулянты; антитромбины; противоаллергические белки; факторы апоптоза или связанные с апоптозом белки, терапевтически активные ферменты и любой белок или пептид, связанный с любым приобретенным заболеванием или любым наследственным заболеванием, или подходящий для лечения любого приобретенного заболевания или любого наследственного заболевания.
Терапевтически активный белок, который может кодироваться молекулой нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества, также может быть адъювантным белком. В данном контексте адъювантный белок предпочтительно следует понимать как любой белок, который способен вызывать врожденный иммунный ответ, который определен в настоящем описании. Предпочтительно, такой врожденный иммунный ответ включает в себя активацию рецептора распознавания картины, такого как, например, рецептор, выбранный из семейства Toll-подобных рецепторов (TLR), включая, например, Toll-подобный рецептор, выбранный из TLR1-TLR10 человека или из мышиных Toll-подобных рецепторов TLR1-TLR13. Более предпочтительно, адъювантный белок выбран из адъювантных белков человека или из патогенных адъювантных белков, выбранных из группы, состоящей без ограничения из бактериальных белков, белков простейших, вирусных белков или белков грибов, животных белков, в частности, из бактериальных адъювантных белков. Кроме того, также можно использовать нуклеиновые кислоты, кодирующие человеческие белки, вовлеченные в адъювантные эффекты (например, лиганды рецепторов распознавания картины, рецепторы распознавания картины, белки сигнальных путей трансдукции, факторы транскрипции или цитокины).
b) Антигены
Молекула нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества альтернативно может кодировать антиген. В контексте настоящего изобретения антигены, которые кодируются молекулой нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества, обычно включают любой антиген, антигенный эпитоп или антигенный пептид, подпадающий под приведенное выше определение, более предпочтительно белковые и пептидный антигены, например, опухолевые антигены, аллергенные антигены, аутоиммунные аутоантигены, антигены патогенов и т.д. В частности, антигены, которые кодируются молекулой нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества, могут представлять собой антигены, образованные вне клетки, чаще всего антигены, не полученные из организма самого хозяина (например, человека) (т.е. не являющиеся аутоантигенами), а полученные из клеток-хозяев вне организма хозяина, например, вирусные антигены, бактериальные антигены, антигены грибов, антигены простейших, животные антигены, аллергенные антигены и т.д. Аллергенными антигенами (антигенами аллергии) обычно являются антигены, которые вызывают аллергию у человека, и могут быть получены либо от человека, либо из других источников. Кроме того, антигены, которые кодируются молекулой нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества, могут представлять собой антигены, образованные внутри клетки, ткани или организма. Такие антигены включают антигены, полученные из самого организма хозяина (например, человека), например, опухолевые антигены, собственные антигены или аутоантигены, такие как аутоиммунные собственные антигены, и т.д., а также (не собственные) антигены, которые определены в настоящем описании, которые были исходно получены из клеток-хозяев вне организма хозяина, но которые подвергаются фрагментации или распадаются внутри организма, ткани или клетки, например, в результате (протеазного) расщепления, метаболизма и т.д. В данном контексте антиген, который кодируется переносимой нуклеиновой кислотой, входящей в состав комплекса полимерного носителя и переносимого вещества, определяют так, как описано ниже, по меньшей мере для одного антигена, второго ингредиента фармацевтической композиции согласно изобретению.
Особенно предпочтительно в данном контексте, чтобы антиген или его фрагмент, вариант и/или производное, кодируемый переносимой нуклеиновой кислотой, представлял собой такой же антиген, как по меньшей мере один антиген, который определен в настоящем описании, который входит в состав фармацевтической композиции согласно изобретению в качестве второго ингредиента. Однако в альтернативных вариантах антиген или его фрагмент, вариант и/или производное, кодируемый переносимой нуклеиновой кислотой, представляет собой другой антиген, отличный от по меньшей мере одного антигена, который определен в настоящем описании, который входит в состав фармацевтической композиции согласно изобретению в качестве второго ингредиента. В конкретном случае, когда антиген кодируется переносимой нуклеиновой кислотой, молекула нуклеиновой кислоты вместе с полимерным носителем служит в качестве адъюванта или иммуностимулирующего средства для индукции неспецифичного врожденного иммунного ответа, тогда как кодируемый белковый или пептидный антиген, который экспрессируется переносимой нуклеиновой кислотой, служит в качестве антигена, индуцируя антигенспецифичный адаптивный иммунный ответ.
Антитела
Согласно следующему альтернативному варианту молекула нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества может кодировать антитело или фрагмент антитела. Согласно настоящему изобретению такое антитело может быть выбрано из любого антитела, например, любых рекомбинантно полученных или встречающихся в природе антител, известных в данной области, в частности, антител, подходящих для терапевтических, диагностических или научных целей, или антител, которые были идентифицированы в связи с конкретными злокачественными заболеваниями. В настоящем описании термин «антитело» используют в наиболее широком смысле и он, в частности, охватывает моноклональные и поликлональные антитела (включая агонистические, антагонистические и блокирующие или нейтрализующие антитела) и виды антител с полиэпитопной специфичностью. Согласно изобретению термин «антитело» обычно включает любое антитело, известное в данной области (например, антитела IgM, IgD, IgG, IgA и IgE), такое как встречающиеся в природе антитела, антитела, образованные при иммунизации в организме-хозяине, антитела, которые были выделены и идентифицированы из встречающихся в природе антител или антител, созданных при иммунизации в организме-хозяине, и рекомбинантно полученные способами молекулярной биологии, известными в данной области, а также химерные антитела, человеческие антитела, гуманизированные антитела, биспецифичные антитела, интраантитела, т.е. антитела, экспрессированные в клетках и необязательно локализованные в конкретных компартментах клетки, и фрагменты и варианты указанных выше антител. В общем, антитело состоит из легкой цепи и тяжелой цепи, которые обе имеют вариабельные и константные домены. Легкая цепь состоит из N-концевого вариабельного домена, VL, и C-концевого константного домена, CL. Напротив, тяжелая цепь IgG-антитела, например, состоит из N-концевого вариабельного домена, VH, и трех константных доменов, CH1, CH2 и CH3.
В контексте настоящего изобретения антитела, которые кодируются молекулой нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества, предпочтительно могут включать полноразмерные антитела, т.е. антитела, состоящие из полной тяжелой и полной легкой цепей, как описано выше. Однако производные антител, такие как фрагменты, варианты или аддукты антител, также могут кодироваться молекулой нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества. Фрагменты антител предпочтительно выбраны из фрагментов Fab, Fab', F(ab')2, Fc, Facb, pFc', Fd и Fv указанных выше (полноразмерных) антител. В общем, фрагменты антител известны в данной области. Например, Fab-фрагмент («фрагмент, антигенсвязывающий») состоит из одного константного и одного вариабельного домена каждой из тяжелой и легкой цепей. Два вариабельных домена связывают эпитоп на конкретных антигенах. Две цепи связаны дисульфидной связью. Фрагмент scFv («одноцепочечный вариабельный фрагмент»), например, обычно состоит из вариабельных доменов легкой и тяжелой цепей. Домены связаны искусственной связью, обычно полипептидной связью, такой как пептид, состоящий из 15-25 остатков глицина, пролина и/или серина.
В данном контексте предпочтительно, чтобы разные цепи антитела или фрагмента антитела кодировались полицистронной молекулой нуклеиновой кислоты. Альтернативно, разные нити антитела или фрагмента антитела кодируются несколькими моноцистронными нуклеиновыми кислотами (последовательностями).
миРНК
Согласно следующему альтернативному варианту молекула нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества может быть в форме днРНК, предпочтительно миРНК. днРНК или миРНК представляет интерес особенно в связи с явлением интерференции РНК. Способ интерференции РНК (РНК-и) in vitro основан на двунитевых молекулах РНК (днРНК), которые запускают специфичную для последовательности супрессию генной экспрессии (Zamore (2001) Nat. Struct. Biol. 9: 746-750; Sharp (2001) Genes Dev. 5: 485-490; Hannon (2002) Nature 41: 244-251). При трансфекции клеток млекопитающих длинной днРНК активация протеинкиназы R и РНКазы L приводит к неспецифичным эффектам, таким как, например, интерфероновый ответ (Stark et al. (1998) Annu. Rev. Biochem. 67: 227-264; He and Katze (2002) Viral Immunol. 15: 95-119). Такие неспецифичные эффекты можно избежать в случае использования более коротких, например 21-23-мерных, так называемых миРНК (малые интерферирующие РНК), поскольку неспецифичные эффекты не запускаются под влиянием миРНК, которые короче 30 п.н. (Elbashir et al. (2001) Nature 411: 494-498).
Таким образом, молекула нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества может представлять собой двунитевую РНК (днРНК), имеющую длину от 17 до 29, предпочтительно от 19 до 25, и предпочтительно по меньшей мере на 90%, более предпочтительно на 95% и особенно предпочтительно на 100% (нуклеотидов днРНК) комплементарную участку молекулы нуклеиновой кислоты (терапевтически активного) белка или антигена, описанного в настоящей публикации выше (в качестве активного ингредиента), или любого дополнительного белка, который описан в настоящей публикации, либо кодирующему, либо некодирующему участку, предпочтительно кодирующему участку. Такая молекула нуклеиновой кислоты (участок) может быть названа в настоящем описании «последовательностью-мишенью» и может представлять собой любую молекулу нуклеиновой кислоты, которая определена в настоящем описании, предпочтительно геномную ДНК, кДНК, РНК, например, мРНК, и т.д. «Комплементарная на 90%» означает, что при длине днРНК, описанной в настоящей публикации, например, 20 нуклеотидов днРНК содержит не более 2 нуклеотидов, не являющихся комплементарными соответствующему участку последовательности-мишени. Однако последовательность двунитевой РНК, используемой согласно изобретению, предпочтительно полностью комплементарна по своей общей структуре участку последовательности-мишени. В данном контексте молекула нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества может представлять собой днРНК, имеющую общую структуру 5'-(N17-29)-3', предпочтительно имеющую общую структуру 5'-(N19-25)-3', более предпочтительно имеющую общую структуру 5'-(N19-24)-3', или еще более предпочтительно имеющую общую структуру 5'-(N21-23)-3', при этом в случае каждой общей структуры каждый N означает нуклеотид (предпочтительно разные нуклеотиды) участка последовательности-мишени, предпочтительно выбранный из числа непрерывно следующих друг за другом 17-29 нуклеотидов участка последовательности-мишени, и присутствующий в общей структуре 5'-(N17-29)-3' в природном порядке. В принципе, все участки, имеющие длину от 17 до 29, предпочтительно от 19 до 25 пар оснований, которые имеются в последовательности-мишени, могут служить для получения днРНК, которая определена в настоящем описании. В равной мере, днРНК, используемые в качестве молекулы нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества, также может быть направлена против нуклеотидных последовательностей (терапевтически применимого) белка или антигена, описанного в настоящей публикации ранее (в качестве активного ингредиента), которые не лежат в кодирующей области, в частности, в 5'-некодирующей области последовательности-мишени, следовательно, например, против некодирующих областей последовательности-мишени, выполняющих регуляторную функцию. Таким образом, последовательность-мишень днРНК, используемой в качестве молекулы нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества, может лежать в транслируемой и нетранслируемой области последовательности-мишени и/или в области регуляторных элементов белка или антигена, описанных выше. Последовательность-мишень для днРНК, используемой в качестве молекулы нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества, также может лежать в перекрывающейся области нетранслируемой и транслируемой последовательностей; в частности, последовательность-мишень может содержать по меньшей мере один нуклеотид выше стартового триплета кодирующей области, например, геномной ДНК, кДНК, РНК или мРНК и т.д.
Иммуностимулирующие нуклеиновые кислоты:
a) Иммуностимулирующие CpG-нуклеиновые кислоты
Согласно другому альтернативному варианту молекула нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества может быть в форме (иммуностимулирующей) CpG-нуклеиновой кислоты, в частности CpG-РНК или CpG-ДНК, которая предпочтительно индуцирует врожденный иммунный ответ. CpG-РНК или CpG-ДНК, используемые согласно изобретению, могут представлять собой однонитевую CpG-ДНК (он-CpG-ДНК), двунитевую CpG-ДНК (днДНК), однонитевую CpG-РНК (он-CpG-РНК) или двунитевую CpG-РНК (дн-CpG-РНК). CpG-нуклеиновая кислота, используемая согласно изобретению, предпочтительно находится в форме CpG-РНК, более предпочтительно в форме однонитевой CpG-РНК (он-CpG-РНК). Также предпочтительно, такие CpG-нуклеиновые кислоты имеют длину, которая описана выше. Предпочтительно CpG-мотивы не метилированы. В предпочтительном варианте CpG-нуклеиновая кислота не является CpG-ДНК, состоящей из последовательности 5'-TCCATGACGTTCCTGACGTT-3' (SEQ ID NO: 123), в частности, если белковый или пептидный антиген является овальбумином или фрагментом овальбумина. В следующем предпочтительном варианте CpG-нуклеиновая кислота не является последовательностью, содержащей последовательность SEQ ID NO: 123. Предпочтительно, CpG-нуклеиновая кислота не является CpG-ДНК. В некоторых вариантах осуществления настоящего изобретения комплекс полимерного носителя и переносимого вещества не содержит CpG-ДНК, предпочтительно не содержит CpG-нуклеиновой кислоты. В некоторых вариантах осуществления настоящего изобретения фармацевтическая композиция не содержит CpG-ДНК, предпочтительно не содержит CpG-нуклеиновой кислоты.
Иммуностимулирующие РНК (исРНК)
Подобным образом, согласно следующему альтернативному варианту, (иммуностимулирующая) молекула нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества может быть в форме иммуностимулирующей РНК (исРНК), которая предпочтительно вызывает врожденный иммунный ответ. Такая иммуностимулирующая РНК может представлять собой любую (двунитевую или однонитевую) РНК, например, кодирующую РНК, которая определена в настоящем описании. Предпочтительно, иммуностимулирующая РНК может представлять собой однонитевую, двунитевую или частично двунитевую РНК, более предпочтительно однонитевую РНК и/или кольцевую или линейную РНК, более предпочтительно линейную РНК. Более предпочтительно, иммуностимулирующая РНК может представлять собой (линейную) однонитевую РНК. Еще более предпочтительно, иммуностимулирующая РНК может представлять собой (длинную) (линейную) (однонитевую) некодирующую РНК. В данном контексте особенно предпочтительно, чтобы исРНК несла трифосфат на своем 5'-конце, что имеет место в случае транскрибируемой in vitro РНК. Иммуностимулирующая РНК также может присутствовать в виде короткого олигонуклеотида РНК, который определен в настоящем описании. Иммуностимулирующая РНК, применяемая в изобретении, кроме того, может быть выбрана из любого класса молекул РНК, встречающихся в природе или получаемых синтетически, которые могут индуцировать врожденный иммунный ответ и могут поддерживать адаптивный иммунный ответ, индуцированный антигеном. В данном контексте иммунный ответ может быть осуществлен различными путями. Значимым фактором для соответствующего (адаптивного) иммунного ответа является стимуляция разных субпопуляций T-клеток. T-лимфоциты обычно подразделяют на две субпопуляции, клетки T-хелперы 1 (Th1) и клетки T-хелперы 2 (Th2), с помощью которых иммунная система способна разрушать внутриклеточные (Th1) и внеклеточные (Th2) патогены (например, антигены). Две популяции Th-клеток отличаются по картине эффекторных белков (цитокинов), продуцируемых ими. Таким образом, клетки Th1 способствуют клеточному иммунному ответу за счет активации макрофагов и цитотоксических T-клеток. С другой стороны, клетки Th2 стимулируют гуморальный иммунный ответ за счет стимуляции превращения B-клеток в плазматические клетки и за счет образования антител (например, против антигенов). Таким образом, соотношение Th1/Th2 имеет большое значение для индукции и поддержания адаптивного иммунного ответа. Применительно к настоящему изобретению соотношение Th1/Th2 при (адаптивном) иммунном ответе предпочтительно сдвинуто в направлении к клеточному ответу (Th1-ответу) и, следовательно, индуцируется клеточный иммунный ответ. Согласно одному примеру врожденная иммунная система, которая может поддерживать адаптивный иммунный ответ, может быть активирована лигандами Toll-подобных рецепторов (TLR). TLR представляют собой семейство высоко консервативных полипептидов рецепторов распознавания картины (PRR), которые узнают ассоциированные с патогенами молекулярные картины (PAMP), и играют ключевую роль во врожденном иммунитете у млекопитающих. В настоящее время идентифицировано по меньшей мере тринадцать представителей семейства, названных TLR1-TLR13 (Toll-подобные рецепторы: TLR1, TLR2, TLR3, TLR4, TLR5, TLR6, TLR7, TLR8, TLR9, TLR10, TLR11, TLR12 или TLR13). Кроме того, был идентифицирован ряд специфичных лигандов TLR. Например, обнаружено, что неметилированная бактериальная ДНК и ее синтетические аналоги (CpG-ДНК) являются лигандами для TLR9 (Hemmi H. с соавторами (2000) Nature 408: 740-5; Bauer S. с соавторами (2001) Proc. Natl. Acad. Sci. USA 98, 9237-42). Кроме того, сообщалось, что лиганды для некоторых TLR включают некоторые молекулы нуклеиновых кислот, и что некоторые типы РНК являются иммуностимулирующими независимым от последовательности или зависимым от последовательности образом, при этом такие различные иммуностимулирующие РНК могут, например, стимулировать TLR3, TLR7 или TLR8 или внутриклеточные рецепторы, такие как RIG-I, MDA-5, и т.д. Например, Lipford с соавторами определили, что некоторые G,U-содержащие олигорибонуклеотиды являются иммуностимулирующими, действующими через TLR7 и TLR8 (смотри WO 03/086280). Предположили, что иммуностимулирующие G,U-содержащие олигорибонуклеотиды, описанные Lipford с соавторами, могут быть получены из РНК-источников, включая рибосомную РНК, транспортную РНК, матричную РНК и вирусную РНК.
Таким образом, иммуностимулирующая РНК (исРНК), применяемая в качестве молекулы нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества, может содержать любую последовательность РНК, которая, как известно, является иммуностимулирующей, включая без ограничения последовательности РНК, представляющие собой и/или кодирующие лиганды TLR, предпочтительно выбранные из представителей семейства человека TLR1-TLR10 или представителей мышиного семейства TLR1-TLR13, более предпочтительно выбранные из представителей семейства (человека) TLR1-TLR10, еще более предпочтительно из TLR7 и TLR8, лигандов внутриклеточных рецепторов для РНК (таких как RIG-I или MDA-5, и т.д.) (смотри, например, Meylan, E., Tschopp, J. (2006). Toll-like receptors and RNA helicases: two parallel ways to trigger antiviral responses. Mol. Cell 22, 561-569), или любую другую иммуностимулирующую последовательность РНК. Кроме того, (классы) иммуностимулирующих молекул РНК, применяемых в качестве молекулы нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества, могут включать любую другую РНК, способную вызывать врожденный иммунный ответ. Без ограничения ими, такие иммуностимулирующие РНК могут включать рибосомную РНК (рРНК), транспортную РНК (тРНК), матричную РНК (мРНК) и вирусную РНК (вРНК), предпочтительно иммуностимулирующая РНК является некодирующей РНК. Такая иммуностимулирующая РНК может иметь длину от 1000 до 5000, от 500 до 5000, от 5 до 5000 или от 5 до 1000, от 5 до 500, от 5 до 250, от 5 до 100, от 5 до 50 или от 5 до 30 нуклеотидов.
Согласно особенно предпочтительному варианту такая последовательность иммуностимулирующей нуклеиновой кислоты предпочтительно представляет собой РНК, предпочтительно состоящую или содержащую последовательность нуклеиновой кислоты формулы (II) или (III):
GlXmGn
где:
G означает гуанозин, урацил или аналог гуанозина или урацила;
X означает гуанозин, урацил, аденозин, тимидин, цитозин или аналог указанных выше нуклеотидов;
l означает целое число от 1 до 40,
при этом,
когда l=1, G означает гуанозин или его аналог,
когда l>1, по меньшей мере 50% нуклеотидов представляют собой гуанозин или его аналог;
m означает целое число и равно по меньшей мере 3;
при этом,
когда m=3, X означает урацил или его аналог,
когда m>3, встречаются по меньшей мере 3 следующих друг за другом урацила или аналога урацила;
n означает целое число от 1 до 40,
при этом,
когда n=1, G означает гуанозин или его аналог,
когда n>1, по меньшей мере 50% нуклеотидов представляют собой гуанозин или его аналог.
ClXmCn
где:
C означает цитозин, урацил или аналог цитозина или урацила;
X означает гуанозин, урацил, аденозин, тимидин, цитозин или аналог указанных выше нуклеотидов;
l означает целое число от 1 до 40,
при этом,
когда l=1, C означает цитозин или его аналог,
когда l>1, по меньшей мере 50% нуклеотидов представляют собой цитозин или его аналог;
m означает целое число и равно по меньшей мере 3;
при этом,
когда m=3, X означает урацил или его аналог,
когда m>3, встречаются по меньшей мере 3 следующих друг за другом урацила или аналога урацила;
n означает целое число от 1 до 40,
при этом,
когда n=1, C означает цитозин или его аналог,
когда n>1, по меньшей мере 50% нуклеотидов представляют собой цитозин или его аналог.
Нуклеиновые кислоты формулы (II) или (III), которые можно применять в качестве переносимой нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества, могут представлять собой относительно короткие молекулы нуклеиновых кислот, имеющие типичную длину приблизительно от 5 до 100 (но также могут быть длиннее 100 нуклеотидов в случае конкретных вариантов, например, до 200 нуклеотидов), от 5 до 90 или от 5 до 80 нуклеотидов, предпочтительно длину приблизительно от 5 до 70, более предпочтительно длину приблизительно от 8 до 60 и более предпочтительно длину приблизительно от 15 до 60 нуклеотидов, более предпочтительно от 20 до 60, наиболее предпочтительно от 30 до 60 нуклеотидов. Если нуклеиновая кислота комплекса переносимой нуклеиновой кислоты имеет максимальную длину, например, 100 нуклеотидов, m обычно будет <=98. Количество нуклеотидов G в нуклеиновой кислоте формулы (II) определяют по l или n. Символы l и n независимо друг от друга означают целое число от 1 до 40, при этом, когда l или n=1, G означает гуанозин или его аналог, и когда l или n>1, по меньшей мере 50% нуклеотидов представляют собой гуанозин или его аналог. Например, не налагая никаких ограничений, когда l или n=4, Gl или Gn могут представлять собой, например, GUGU, GGUU, UGUG, UUGG, GUUG, GGGU, GGUG, GUGG, UGGG или GGGG, и т.д.; когда l или n=5, Gl или Gn могут представлять собой, например, GGGUU, GGUGU, GUGGU, UGGGU, UGGUG, UGUGG, UUGGG, GUGUG, GGGGU, GGGUG, GGUGG, GUGGG, UGGGG или GGGGG, и т.д.; и т.д. Нуклеотид, который является соседним с Xm в нуклеиновой кислоте формулы (II) согласно изобретению, предпочтительно не является урацилом. Подобным образом, количество нуклеотидов C в нуклеиновой кислоте формулы (III) согласно изобретению определяют по l или n. Символы l и n независимо друг от друга означают целое число от 1 до 40, при этом, когда l или n=1, C означает цитозин или его аналог, и когда l или n>1, по меньшей мере 50% нуклеотидов представляют собой цитозин или его аналог. Например, не налагая никаких ограничений, когда l или n=4, Cl или Cn могут представлять собой, например, CUCU, CCUU, UCUC, UUCC, CUUC, CCCU, CCUC, CUCC, UCCC или CCCC, и т.д.; когда l или n=5, Cl или Cn могут представлять собой, например, CCCUU, CCUCU, CUCCU, UCCCU, UCCUC, UCUCC, UUCCC, CUCUC, CCCCU, CCCUC, CCUCC, CUCCC, UCCCC, или CCCCC, и т.д.; и т.д. Нуклеотид, который является соседним с Xm в нуклеиновой кислоте формулы (V) согласно изобретению, предпочтительно не является урацилом. Предпочтительно, в случае формулы (II), когда l или n>1, по меньшей мере 60%, 70%, 80%, 90% или даже 100% нуклеотидов представляют собой гуанозин или его аналог, как определено выше. Остальные нуклеотиды до 100% (когда гуанозин составляет менее 100% нуклеотидов) во фланкирующих последовательностях Gl и/или Gn представляют собой урацил или его аналог, как определено в настоящем описании ранее. Также предпочтительно, l и n независимо друг от друга означают целое число от 2 до 30, более предпочтительно целое число от 2 до 20 и еще более предпочтительно целое число от 2 до 15. Нижний предел l или n можно при необходимости варьировать, и он равен по меньшей мере 1, предпочтительно по меньшей мере 2, более предпочтительно по меньшей мере 3, 4, 5, 6, 7, 8, 9 или 10. Такое определение применимо соответствующим образом к формуле (III).
Согласно особенно предпочтительному варианту нуклеиновая кислота, соответствующая любой из формул (II) или (III), указанных выше, которая может быть применима в качестве нуклеиновой кислоты комплекса полимерного носителя и переносимого вещества, может быть выбрана из последовательности, состоящей или содержащей любую из следующих последовательностей:


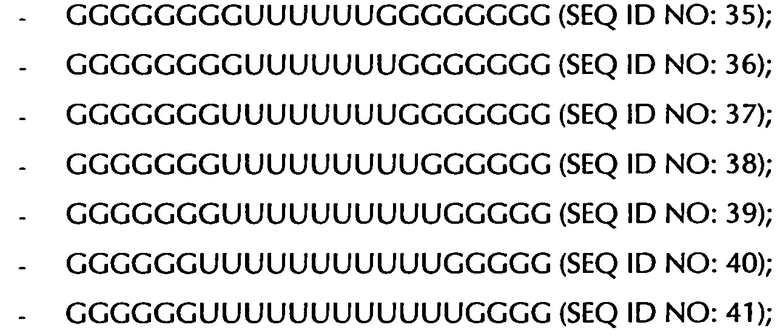
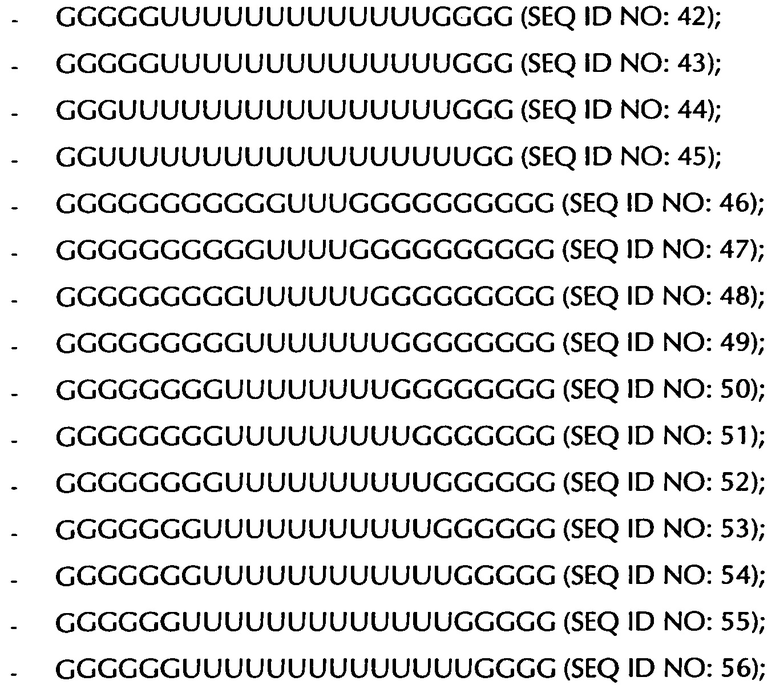

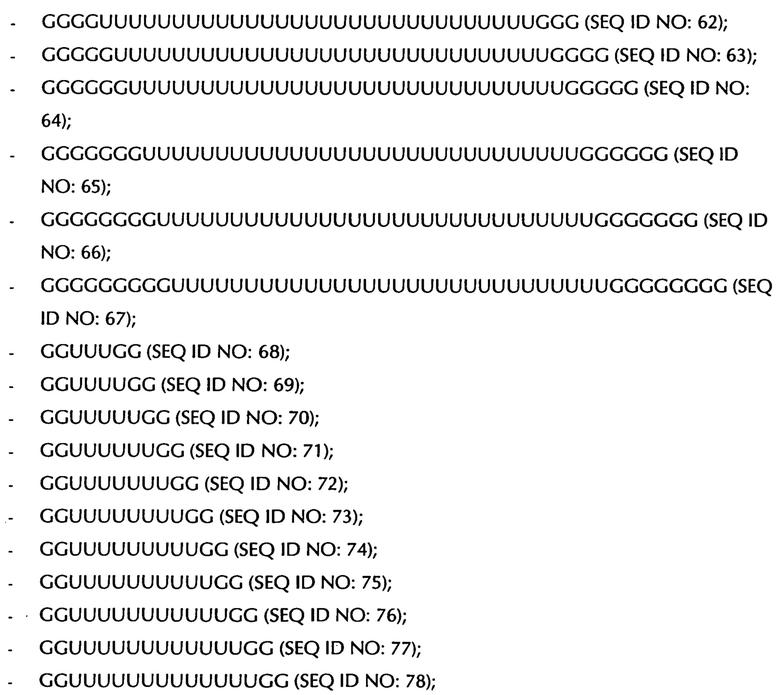



или из последовательности, имеющей по меньшей мере 60%, 70%, 80%, 90% или даже 95% идентичность последовательности с любой из таких последовательностей.
Согласно следующему особенно предпочтительному варианту такие иммуностимулирующие последовательности нуклеиновых кислот, в частности исРНК, состоят или содержат нуклеиновую кислоту формулы (IV) или (V):
(NuGlXmGnNv)a
где:
G означает гуанозин (гуанин), уридин (урацил) или аналог гуанозина (гуанина) или уридина (урацила), предпочтительно гуанозин (гуанин) или его аналог;
X означает гуанозин (гуанин), уридин (урацил), аденозин (аденин), тимидин (тимин), цитидин (цитозин) или аналог таких нуклеотидов (нуклеозидов), предпочтительно уридин (урацил) или его аналог;
N означает последовательность нуклеиновой кислоты, имеющую длину примерно от 4 до 50, предпочтительно примерно от 4 до 40, более предпочтительно примерно от 4 до 30 или от 4 до 20 нуклеотидов, при этом каждый N независимо выбран из гуанозина (гуанина), уридина (урацила), аденозина (аденина), тимидина (тимина), цитидина (цитозина) или аналога таких нуклеотидов (нуклеозидов);
a означает целое число от 1 до 20, предпочтительно от 1 до 15, наиболее предпочтительно от 1 до 10;
l означает целое число от 1 до 40,
при этом, когда l=1, G означает гуанозин (гуанин) или его аналог,
когда l>1, по меньшей мере 50% таких нуклеотидов (нуклеозидов) представляют собой гуанозин (гуанин) или его аналог;
m означает целое число и равно по меньшей мере 3;
при этом, когда m=3, X означает уридин (урацил) или его аналог, и
когда m>3, встречаются по меньшей мере 3 следующих друг за другом уридина (урацила) или аналогов уридина (урацила);
n означает целое число от 1 до 40,
при этом, когда n=1, G означает гуанозин (гуанин) или его аналог,
когда n>1, по меньшей мере 50% таких нуклеотидов (нуклеозидов) представляют собой гуанозин (гуанин) или его аналог;
u, v могут независимо друг от друга означать целое число от 0 до 50,
при этом предпочтительно когда u=0, v≥1, или
когда v=0, u≥1;
при этом молекула нуклеиновой кислоты формулы (IV) имеет длину по меньшей мере 50 нуклеотидов, предпочтительно по меньшей мере 100 нуклеотидов, более предпочтительно по меньшей мере 150 нуклеотидов, еще более предпочтительно по меньшей мере 200 нуклеотидов и наиболее предпочтительно по меньшей мере 250 нуклеотидов.
(NuСlXmCnNv)a
где:
C означает цитидин (цитозин), уридин (урацил) или аналог цитидина (цитозина) или уридина (урацила), предпочтительно цитидин (цитозин) или его аналог;
X означает гуанозин (гуанин), уридин (урацил), аденозин (аденин), тимидин (тимин), цитидин (цитозин) или аналог указанных выше нуклеотидов (нуклеозидов), предпочтительно уридин (урацил) или его аналог;
каждый N означает последовательность нуклеиновой кислоты, имеющую независимо друг от друга длину примерно от 4 до 50, предпочтительно примерно от 4 до 40, более предпочтительно примерно от 4 до 30 или от 4 до 20 нуклеотидов, при каждый N независимо выбран из гуанозина (гуанина), уридина (урацила), аденозина (аденина), тимидина (тимина), цитидина (цитозина) или аналога таких нуклеотидов (нуклеозидов);
a означает целое число от 1 до 20, предпочтительно от 1 до 15, наиболее предпочтительно от 1 до 10;
l означает целое число от 1 до 40,
при этом, когда l=1, C означает цитидин (цитозин) или его аналог,
когда l>1, по меньшей мере 50% таких нуклеотидов (нуклеозидов) представляют собой цитидин (цитозин) или его аналог;
m означает целое число и равно по меньшей мере 3;
при этом, когда m=3, X означает уридин (урацил) или его аналог,
когда m>3, встречаются по меньшей мере 3 следующих друг за другом уридина (урацила) или аналогов уридина (урацила);
n означает целое число от 1 до 40,
при этом, когда n=1, C означает цитидин (цитозин) или его аналог,
когда n>1, по меньшей мере 50% таких нуклеотидов (нуклеозидов) представляют собой цитидин (цитозин) или его аналог;
u, v могут независимо друг от друга означать целое число от 0 до 50,
при этом предпочтительно когда u=0, v≥1, или
когда v=0, u≥1;
при этом молекула нуклеиновой кислоты формулы (V) согласно изобретению имеет длину по меньшей мере 50 нуклеотидов, предпочтительно по меньшей мере 100 нуклеотидов, более предпочтительно по меньшей мере 150 нуклеотидов, еще более предпочтительно по меньшей мере 200 нуклеотидов и наиболее предпочтительно по меньшей мере 250 нуклеотидов.
В случае формулы (V) любое из определений, приведенных выше для элементов N (т.е. Nu и Nv) и X (Xm), в частности коровой структуры, которая определена выше, а также для целых чисел a, l, m, n, u и v, подобным образом соответственно применимо к элементам формулы (IV), при этом в формуле (V) коровая структура определена как ClXmCn. Определение пограничных элементов Nu и Nv идентично определениям, приведенным выше для Nu и Nv.
Согласно особенно предпочтительному варианту молекула нуклеиновой кислоты согласно формуле (IV) содержит, предпочтительно состоит, например, любой из следующих последовательностей:
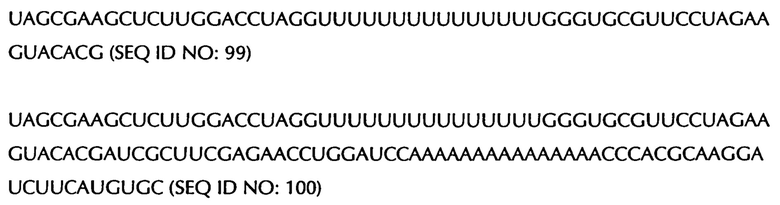


или последовательности нуклеиновой кислоты, имеющей по меньшей мере 60%, предпочтительно по меньшей мере 70%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 90% и наиболее предпочтительно по меньшей мере 95% идентичность с любой из определенных выше последовательностей.
Согласно другому особенно предпочтительному варианту молекула нуклеиновой кислоты согласно формуле (V) содержит, предпочтительно состоит, например, из любой из следующих последовательностей:
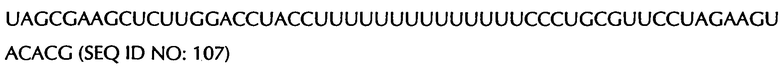
или
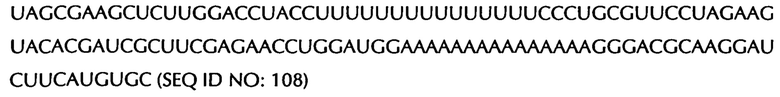
или последовательность нуклеиновой кислоты, имеющей по меньшей мере 60%, предпочтительно по меньшей мере 70%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 90% и наиболее предпочтительно по меньшей мере 95% идентичность с любой из определенных выше последовательностей.
В следующем предпочтительном варианте молекула нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества также может быть в форме модифицированной нуклеиновой кислоты.
Согласно первому варианту молекула нуклеиновой кислоты определенного в настоящем описании комплекса полимерного носителя и переносимого вещества может быть представлена в виде «стабилизированной нуклеиновой кислоты», предпочтительно в виде стабилизированной РНК или ДНК, более предпочтительно в виде РНК, которая по существу резистентна к распаду in vivo (например, под действием экзо- или эндонуклеаз), как определено выше.
Согласно другому варианту переносимая нуклеиновая кислота определенного в настоящем описании комплекса полимерного носителя и переносимого вещества может быть модифицирована, как определено в настоящем описании, и/или стабилизирована, особенно если молекула нуклеиновой кислоты имеет форму кодирующей нуклеиновой кислоты, например, мРНК, путем модификации содержания G/C в молекуле нуклеиновой кислоты, в частности, в мРНК, предпочтительно в ее кодирующей области, которая определена в настоящем описании.
Молекулы нуклеиновых кислот, применяемые в настоящем изобретении в качестве переносимого вещества, входящего в состав комплекса полимерного носителя и переносимого вещества, который определен в настоящем описании, могут быть получены с использованием любого способа, известного в данной области, включая способы синтеза нуклеиновых кислот, которые определены в настоящем описании.
Кроме того, настоящее изобретение специально охватывает варианты и фрагменты молекул нуклеиновых кислот, которые определены в настоящем описании, входящие в качестве переносимой нуклеиновой кислоты в комплекс полимерного носителя и переносимого вещества.
Особенно предпочтительными молекулами переносимой нуклеиновой кислоты в контексте настоящего изобретения являются молекулы нуклеиновых кислот, содержащие, предпочтительно состоящие из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательностям SEQ ID NO: 105 или 122.
В комплексе полимерного носителя и переносимого вещества катионный компонент полимерного носителя, который определен в настоящем описании, и переносимая нуклеиновая кислота обычно представлены в молярном соотношении примерно от 1 до 10000, предпочтительно в молярном соотношении примерно от 5 до 5000, более предпочтительно в молярном соотношении примерно от 10 до 2500, еще более предпочтительно в молярном соотношении примерно от 25 до 2000 и наиболее предпочтительно в молярном соотношении примерно от 25 до 1000 полимерного носителя к нуклеиновой кислоте.
Кроме того, в комплексе полимерного носителя и переносимого вещества катионный компонент полимерного носителя, который определен в настоящем описании, и переносимая нуклеиновая кислота предпочтительно представлены в N/P-соотношении по меньшей мере 0,1, 0,2, 0,3, 0,4, 0,5, 0,75, 1, 1,5 или 2. Предпочтительно N/P-соотношение лежит в диапазоне примерно от 0,1, 0,3, 0,4, 0,5, 0,75, 1,0, 1,5 или 2 до 20, предпочтительно в диапазоне примерно от 0,2 (0,5 или 0,75 или 1,0) до 12, более предпочтительно в диапазоне N/P-соотношения примерно от 0,4 (0,75 или 1,0) до 10 и еще более предпочтительно в диапазоне N/P-соотношения примерно от 0,4 (0,75 или 1,0) до 5. Наиболее предпочтительно N/P-соотношение лежит в диапазоне от 0,1 до 0,9. В данном контексте N/P-соотношение является мерой ионного заряда катионного (боковой цепи) компонента полимерного носителя или полимерного носителя как такового. В частности, если катионные свойства катионного компонента генерируются за счет атомов азота (например, боковых цепей аминокислот), то N/P-соотношение выражает отношение основных атомов азота к фосфатным остаткам в нуклеотидном остове, если считать, что атомы азота (боковых цепей) в катионном компоненте полимерного носителя вносят вклад в положительные заряды, а фосфаты фосфатного остова нуклеиновой кислоты вносят вклад в отрицательный заряд. В общем, один фосфат дает один отрицательный заряд, например, один нуклеотид в переносимой вещество молекуле нуклеиновой кислоты дает один отрицательный заряд. Формула приведена в примерах. N/P-соотношение определяют как отношение азот/фосфат (N/P-соотношение) полного комплекса полимерного носителя и переносимого вещества согласно изобретению. Такое соотношение обычно является показателем содержания/количества катионных компонентов в полимерном носителе и характеристикой содержания/количества нуклеиновых кислот, связанных или входящих в комплекс полимерного носителя и переносимого вещества согласно изобретению. Его можно вычислить на основе того, что, например, 1 мкг РНК обычно содержит примерно 3 нмоль фосфатных остатков, при условии, что в РНК имеет место статистическое распределение оснований. Кроме того, 1 нмоль пептида обычно содержит примерно x нмоль остатков азота, в зависимости от молекулярной массы и количества его (катионных) аминокислот.
В данном контексте предпочтительно, чтобы в комплексе полимерного носителя и переносимого вещества катионный компонент полимерного носителя, который определен в настоящем описании, и переносимая нуклеиновая кислота были представлены в N/P-соотношении, составляющем по меньшей мере примерно 1 или предпочтительно в диапазоне примерно от 1 до 20 в случае применений in vitro (например, в случае, когда клетки, выделенные из организма пациента, могут быть обработаны in vitro фармацевтической композицией согласно изобретению и затем введены пациенту).
В случае применений фармацевтической композиции согласно изобретению in vivo N/P-соотношение составляет по меньшей мере 0,1 (0,2, 0,3, 0,4, 0,5, 0,6), предпочтительно в диапазоне примерно от 0,1 (0,2, 0,3, 0,4, 0,5 или 0,6) до 1,5. Еще более предпочтительным является диапазон N/P-соотношений от 0,1 или 0,2 до 0,9 или диапазон N/P-соотношений от 0,5 до 0,9.
В конкретном случае, когда предполагается индукция IFN-α, N/P-соотношение составляет по меньшей мере 0,1 (0,2, 0,3, 0,4, 0,5 или 0,6), или предпочтительным является диапазон N/P-соотношений от 0,1 до 1 или более предпочтительным является диапазон N/P-соотношений от 0,1 или 0,2 до 0,9 или диапазон N/P-соотношений от 0,5 до 0,9. В других случаях, если может предполагаться индукция TNFα, особенно предпочтительным является N/P-соотношение от 1 до 20.
N/P-соотношение в значительной степени влияет на поверхностный заряд получаемого в результате комплекса полимерного носителя и переносимого вещества. Таким образом, предпочтительно, чтобы получаемый в результате комплекс полимерного носителя и переносимого вещества был положительно заряжен в случае применений in vitro и отрицательно или нейтрально заряжен в случае применений in vivo. Поверхностный заряд получаемого в результате комплекса полимерного носителя и переносимого вещества может быть указан в виде дзета-потенциала, который может быть измерен способом электрофореза с допплеровским анализом с использованием Zetasizer Nano (Malvern Instruments, Malvern, UK). В общем, N/P-соотношение ниже 1 приводит к отрицательному дзета-потенциалу, а N/P-соотношение выше 1 приводит к положительному дзета-потенциалу (в рамках типичных ошибок измерения).
В некоторых вариантах поверхностный заряд комплекса полимерного носителя и переносимого вещества, предпочтительно дзета-потенциал, является положительным, т.е. выше 0 мВ, таким как выше 1 мВ, выше 2 мВ, выше 4 мВ, выше 5 мВ или выше 10 мВ. В альтернативных вариантах поверхностный заряд комплекса полимерного носителя и переносимого вещества, предпочтительно дзета-потенциал, является отрицательным, т.е. ниже 0 мВ, таким как ниже -1 мВ, ниже -2 мВ, ниже -4 мВ, ниже -5 мВ или ниже -10 мВ, таким как примерно от -1 мВ до -50 мВ, примерно от -2 мВ до -40 мВ или примерно от -5 мВ до -30 мВ.
Комплекс полимерного носителя и переносимого вещества, который применим в настоящем изобретении, например, для применения в качестве адъюванта, предпочтительно способен запускать неспецифичную для антигена (врожденную) иммунную реакцию (которая обеспечивается врожденной иммунной системой), предпочтительно иммуностимулирующим образом. Обычно иммунная реакция может быть осуществлена различными путями. Важным фактором для подходящего иммунного ответа является стимуляция разных субпопуляций T-клеток. T-лимфоциты обычно подразделяют на две субпопуляции, клетки T-хелперы 1 (Th1) и клетки T-хелперы 2 (Th2), с помощью которых иммунная система способна разрушать внутриклеточные (Th1) и внеклеточные (Th2) патогены (например, антигены). Две популяции Th-клеток отличаются по картине эффекторных белков (цитокинов), продуцируемых ими. Таким образом, клетки Th1 способствуют клеточному иммунному ответу за счет активации макрофагов и цитотоксических T-клеток. С другой стороны, клетки Th2 стимулируют гуморальный иммунный ответ за счет стимуляции превращения B-клеток в плазматические клетки и за счет образования антител (например, против антигенов). Таким образом, соотношение Th1/Th2 имеет большое значение в иммунном ответе. Применительно к настоящему изобретению соотношение Th1/Th2 при иммунном ответе предпочтительно сдвигается иммуностимулирующим средством, в частности, комплексом полимерного носителя и переносимого вещества, в направлении к клеточному ответу, который, как говорят, является Th1-ответом, и при этом преимущественно индуцируется клеточный иммунный ответ. Как описано выше, комплекс полимерного носителя и переносимого вещества может индуцировать неспецифичный врожденный иммунный ответ, который может позволять поддерживать специфичный адаптивный иммунный ответ, вызванный антигеном.
Определение иммуностимулирующей (врожденный иммунитет) или адъювантной способности компонента в фармацевтической композиции согласно изобретению:
Для определения иммуностимулирующей способности иммуностимулирующего средства или адъюванта (в частности, комплекса полимерного носителя и переносимого вещества, который применяют в настоящем изобретении) в данной области известно несколько способов, которые могут быть использованы. Например, преимущественно используют способы анализа соединений in vitro в отношении их способности индуцировать цитокины, которые являются (исключительно или по меньшей мере обычно) частью врожденной иммунной системы, и тем самым (в качестве дополнительного рычага иммунной системы) обычно улучшают индукцию антигенспецифичного иммунного ответа, вызываемого антигеном. С указанной целью могут быть выделены, например, PBMC из образцов крови и подвергнуты стимуляции конкретным иммуностимулирующим средством или адъювантом. После инкубации определяют секрецию требуемых цитокинов (например, в виде реакции активации PAMP-рецепторов), обычно являющихся частью врожденной иммунной системы (а не антигенспецифичной иммунной системы), используя ELISA. Такие выбранные цитокины могут быть использованы в данной области в качестве определителей индукции врожденного иммунного ответа в организме. В данном контексте предпочтительно измеряют секрецию TNF-альфа и IFN-альфа, чтобы определить неспецифичный (врожденный иммунный ответ), вызываемый соединением или комплексом. В частности, IFN-альфа играет важную роль в индукции неспецифичного иммунного ответа после вирусной инфекции и может быть использован в качестве показателя индукции сдвинутого в сторону Th1 адаптивного иммунного ответа, который является особенно предпочтительным в контексте лечения злокачественной опухоли или опухолевых заболеваний. Соответственно, особенно предпочтительно, чтобы иммуностимулирующие соединение или комплекс, тестируемый в скрининговом анализе, индуцировал, например, секрецию IFN-альфа. Такое соединение или комплекс затем используют, например, в применениях в качестве иммуностимулирующего средства (запускающего неспецифичный (врожденный) иммунный ответ) при основанной на вакцинации терапии.
IFN-альфа является частью семейства интерферонов типа I. Интерфероны типа I (IFN) являются плейотропными цитокинами, которые важны для поддержания противовирусных иммунных ответов. Они индуцируют апоптоз инфицированных вирусами клеток и резистентность клеток к вирусной инфекции, в добавление к активации природных киллеров (NK) и T-клеток. Интерфероны типа I оказывают влияние на большую группу цитокинов и хемокинов, которые между прочим влияют на созревание иммуноцитов, хоминг, эффекторные функции и апоптоз. Обычно основной ролью IFN-альфа является индукция состояния праймирования, влияющего на продукцию и регулирование других медиаторов, включая цитокины. Например, передача сигнала IFN-альфаβ приводит к повышающей регуляции продукции IFN-альфаγ дендритными клетками (DC) и T-клетками, и тем самым способствует индукции и поддержанию Th1-клеток. Сдвиг иммунного ответа в направлении иммунного ответа Th1 может стать особенно важным после использования белковых или пептидных вакцин, поскольку такие вакцины обычно индуцируют основанный на Th2 иммунный ответ, который в результате предотвращает или снижает индукцию цитотоксических T-клеток.
Таким образом, предпочтительно, чтобы соединение или комплекс, используемый в качестве адъюванта в контексте настоящего изобретения, предпочтительно могло обладать свойством, приводящим к сдвигу антигенспецифичного иммунного ответа, вызванного антигеном, в сторону основанного на Th1 иммунного ответа. Направление иммунного ответа, индуцированного антигеном, обычно измеряют на основе определения индукции нескольких подтипов антигенспецифичных антител и индукции антигенспецифичных цитотоксических T-клеток CD8+. В данном контексте подтип антитела IgG1 отражает индукцию основанного на Th2 иммунного ответа, а индукция подтипа антитела IgG2a и индукция цитотоксических T-клеток отражает индукцию основанного на Th1 иммунного ответа. Индукцию антигенспецифичных антител обычно определяют, измеряя титр антител в крови после введения вакцины, используя ELISA. Индукцию антигенспецифичных цитотоксических T-клеток обычно определяют, измеряя секрецию IFN-гамма в спленоцитах после стимуляции антигенспецифичными пептидами в ELISPOT. В данном контексте индукция секреции IFN-гамма является доказательством того, что в селезенке присутствуют антигенспецифичные цитотоксические T-клетки, которые могут специфично атаковать клетки, которые презентируют эпитопы антигена на молекулах MHC I на своей поверхности.
Для определения полезных свойств адъюванта обычно проводят вакцинации in vivo. При этом можно исследовать, улучшает ли адъювант или иммуностимулирующее соединение или комплекс антигенспецифичный иммунный ответ, вызванный вакциной и, кроме того, может ли он сдвигать антигенспецифичный иммунный ответ в требуемом направлении, проявляя адъювантные свойства. В частности, полагают, что при индукции противоопухолевого иммунного ответа индукция сдвинутого в сторону Th1 иммунного ответа, особенно индукция цитотоксических T-клеток, играет основную роль, поскольку индукция антигенспецифичных цитотоксических T-клеток, как полагают, представляет собой необходимую предпосылку для успешной борьбы с опухолью.
Соответственно, способы скрининга, тестирования и/или исследования соединения или комплекса, которые проявляют адъювантные свойства, хорошо известны в данной области и легко могут быть применены, например, тесты ELISA, в которых измеряют иммунный ответ, вызванный тестируемыми соединениями/комплексами.
В другом аспекте настоящее изобретение относится к способу получения фармацевтической композиции согласно изобретению, при этом указанный способ включает стадии: (i) получения по меньшей мере одного комплекса полимерного носителя и переносимого вещества, который определен в настоящем описании; (ii) получения антигена, который определен в настоящем описании; и (iii) объединения указанного комплекса полимерного носителя и переносимого вещества и указанного антигена. Стадия объединения (iii) может быть осуществлена непосредственно перед введением пациенту (например, примерно за 1, 5, 15, 30 или 60 минут перед указанным введением и до 72 часов до указанного введения), или может быть осуществлена во время производства указанной фармацевтической композиции. Соответствующий специалист (например, врач или медицинский работник или производитель) будет с обычными методиками, подходящими для такой стадии объединения.
В контексте настоящего изобретения способ получения комплекса полимерного носителя и переносимого вещества, который определен в настоящем описании, может включать следующие стадии:
a) получения по меньшей мере одного катионного белка или пептида, который определен в настоящем описании, и/или по меньшей мере одного катионного или поликатионного полимера и необязательно по меньшей мере одного аминокислотного компонента (AA), который определен в настоящем описании, каждый из которых содержит по меньшей мере один -SH-остаток,
b) получения по меньшей мере одной молекулы нуклеиновой кислоты, которая определена в настоящем описании, предпочтительно в указанных выше соотношениях,
c) смешивания компонентов, полученных на стадиях a) и b), предпочтительно в основной или нейтральной среде, которая определена в настоящем описании, предпочтительно в присутствии кислорода или дополнительного инициатора, который определен в настоящем описании, предпочтительно при pH, при температуре и в момент времени, которые определены в настоящем описании, и осуществления при этом конденсации и, следовательно, полимеризации катионных компонентов, полученных на стадии a), друг с другом посредством дисульфидных связей (в ходе конденсационной полимеризации или поликонденсации) с получением полимерного носителя и образования комплекса молекулы нуклеиновой кислоты, полученной на стадии b), с катионными компонентами, полученными на стадии a),
d) необязательно очистки комплекса полимерного носителя и переносимого вещества, полученного согласно стадии c), предпочтительно с использованием способа, который определен в настоящем описании,
e) необязательно лиофилизации комплекса полимерного носителя и переносимого вещества, полученного согласно стадии c) или d).
Способ получения комплекса полимерного носителя и переносимого вещества, который описан в настоящей публикации, может включать многостадийную реакцию конденсационной полимеризации или поликонденсации посредством -SH-остатков полученных веществ, например катионных пептидов или полимеров, которые определены в настоящем описании, и необязательно дополнительных аминокислотных компонентов (AA) на стадии c). Реакция конденсационной полимеризации или поликонденсации, которую осуществляют одновременно с комплексообразованием или электростатическим связыванием молекулы нуклеиновой кислоты, предпочтительно приводит к получения комплекса полимерного носителя и переносимого вещества, в котором полимерным носителем является конденсационный полимер, в котором отдельные компоненты связаны дисульфидными связями.
Как описано в настоящей публикации, на стадии a) способа получения комплекса полимерного носителя и переносимого вещества получают по меньшей мере один катионный или поликатионный белок или пептид, который определен в настоящем описании, и/или по меньшей мере один катионный или поликатионный полимер, который определен в настоящем описании, предпочтительно в указанных выше соотношениях. Такие компоненты смешивают на стадии c) с молекулой нуклеиновой кислоты, полученной на стадии b), предпочтительно в основной или нейтральной среде, которая определена в настоящем описании, предпочтительно в присутствии кислорода или другого инициатора, который определен в настоящем описании, предпочтительно при pH, при температуре и в момент времени, которые определены в настоящем описании, и при этом осуществляя конденсацию и, следовательно, полимеризацию таких компонентов друг с другом посредством дисульфидных связей (в ходе конденсационной полимеризации или поликонденсации) с получением полимерного носителя в комплексе с молекулой нуклеиновой кислоты, которая определена в настоящем описании.
Согласно альтернативному варианту на стадии a) способа получения комплекса полимерного носителя и переносимого вещества получают по меньшей мере один катионный или поликатионный белок или пептид и/или по меньшей мере один катионный или поликатионный полимер, которые определены в настоящем описании, и необязательно на стадии a) получают по меньшей мере один аминокислотный компонент (AA), который определен в настоящем описании, и используют для реакции конденсационной полимеризации или поликонденсации и комплексообразования перед добавлением нуклеиновой кислоты, полученной на стадии b), но используя такие же условия полимеризации, которые описаны для стадии c). Полимеризованный полимерный носитель и нуклеиновую кислоту со стадии b) затем смешивают на стадии c). Предпочтительно, все компоненты получают в указанных выше соотношениях и смешивают, предпочтительно в основной или нейтральной среде, которая определена в настоящем описании, предпочтительно в присутствии кислорода или другого инициатора, который определен в настоящем описании, предпочтительно при pH, при температуре и в момент времени, которые определены в настоящем описании. При смешивании и начале реакции компоненты конденсируются и таким образом полимеризуются друг с другом посредством дисульфидных связей (в ходе конденсационной полимеризации или поликонденсации) с получением полимерного носителя в комплексе с молекулой нуклеиновой кислоты, которая определена в настоящем описании.
В обоих указанных выше альтернативных вариантах могут быть выбраны разные полимерные носители, в частности, разные пептиды и/или разные полимеры, для конденсационной полимеризации, которая указана выше. В данном контексте выбор разных компонентов полимерного носителя обычно зависит от требуемых свойств конечного полимерного носителя и требуемой катионной силы конечного полимерного носителя. Соответственно, содержание катионных компонентов может быть дополнительно «разбавлено» или модифицировано в указанном выше альтернативном варианте осуществления стадии a), например, за счет введения аминокислотного компонента (AA), который определен в настоящем описании, предпочтительно в определенных выше диапазонах. При этом может быть получен модифицированный полимерный носитель, в котором катионный характер немодифицированного полимерного носителя обычно сохраняется в тех пределах, которые определены в настоящем описании. Таким образом, свойства конечного полимерного носителя можно по желанию корректировать с использованием свойств компонентов (AA) за счет встраивания аминокислотного компонента (AA), который определен в настоящем описании, на стадии a).
На стадии c) по меньшей мере один катионный или поликатионный белок или пептид, который определен в настоящем описании, и/или по меньшей мере один катионный или поликатионный полимер, который определен в настоящем описании, и необязательно по меньшей мере один аминокислотный компонент (AA) и по меньшей мере одна нуклеиновая кислота, которая определена в настоящем описании, предпочтительно находятся в основной или нейтральной среде со стадии a) способа получения комплекса полимерного носителя и переносимого вещества согласно изобретению. Такая основная или нейтральная среда обычно имеет pH в диапазоне от примерно 5 до примерно 10, предпочтительно в диапазоне pH от примерно от примерно 6 до примерно 9, более предпочтительно в диапазоне pH от примерно 7 до примерно 8, например примерно 6,5, 7, 7,5, 8, 8,5 или 9 или любой диапазон, выбранный из любых двух таких или вышеуказанных значений.
Кроме того, температура раствора на стадии c) предпочтительно находится в диапазоне от примерно 5°C до примерно 60°C, более предпочтительно в диапазоне от примерно 15°C до примерно 40°C, еще более предпочтительно в диапазоне от примерно 20°C до примерно 30°C и наиболее предпочтительно в диапазоне от примерно 20°C до примерно 25°C, например примерно 25°C.
На стадии c) способа получения комплекса полимерного носителя и переносимого вещества, который описан в настоящей публикации, можно использовать подходящие буферы. Предпочтительные буферы могут включать без ограничения буферы, которые предпочтительно выбраны из карбонатных буферов, боратных буферов, буфера на основе бицина, CHES-буфера, CAPS-буфера, буферов, содержащих этаноламин, HEPES, MOPS-буфера, фосфатного буфера, PIPES-буфера, трис-буфера, трицинового буфера, TAPS-буфера и/или TES-буфера в качестве буферных средств. Особенно предпочтительным является карбонатный буфер.
При смешивании компонентов, предпочтительно в присутствии кислорода, предпочтительно в присутствии основной или нейтральной среды, которая определена в настоящем описании, начинается реакция конденсационной полимеризации или поликонденсации и образование комплекса по меньшей мере с одной молекулой нуклеиновой кислоты. С указанной целью на смесь на стадии c) предпочтительно действуют кислородом или могут инициировать, используя дополнительный инициатор, например каталитическое количество окислителя, например ДМСО и т.д. После начала реакции конденсационной полимеризации или поликонденсации, по меньшей мере один катионный или поликатионный белок или пептид и/или по меньшей мере один катионный или поликатионный полимер и, необязательно, по меньшей мере один аминокислотный компонент (AA), которые определены в настоящем описании, конденсируются и таким образом полимеризуются друг с другом посредством дисульфидных связей (конденсационная полимеризация или поликонденсация). На данной стадии реакции a) предпочтительно создают линейные полимеры, используя мономеры, по меньшей мере с одним реакционно-способным -SH-остатком, т.е. по меньшей мере один катионный или поликатионный белок или пептид и/или по меньшей мере один катионный или поликатионный полимер и, необязательно, по меньшей мере один аминокислотный компонент (AA), которые определены в настоящем описании, при этом каждый компонент имеет по меньшей мере один свободный -SH-остаток, который определен в настоящем описании, например, на своих концах. Однако могут быть использованы компоненты с более чем одним, предпочтительно с двумя свободными -SH-остатками, что может привести к получению разветвленных полимеров. Одновременно с реакцией полимеризации катионные полимеры связываются с по меньшей мере одной молекулой нуклеиновой кислоты и при этом образуют с ней комплекс.
Согласно одному альтернативному варианту комплекс полимерного носителя и переносимого вещества дополнительно может быть модифицирован компонентом (AA), который определен в настоящем описании.
Согласно первому примеру компонент (AA) (например, лиганд) связывают с катионным компонентом перед получением катионного компонента на стадии a) посредством любой функциональной группы, которая определена в настоящем описании, например, -SH-остатка. Такой компонент (AA) или (например, лиганд) предпочтительно связывают с катионным компонентом на одном конце таких компонентов. Если связывание осуществляют посредством -SH-связей, предпочтительно используют катионные компоненты с двумя (или еще больше) -SH-остатками. Компонент (AA) или (например, лиганд) предпочтительно несет только один -SH-остаток. В данном случае один -SH-остаток катионного компонента предпочтительно защищен на первой стадии с использованием защитной группы, которая известна в данной области. Затем катионный компонент может быть связан с компонентом L с образованием первой дисульфидной связи через незащищенный -SH-остаток. Затем обычно удаляют защиту защищенного -SH-остатка катионного компонента для следующих реакций.
Альтернативно, упомянутый выше компонент (AA) или (например, лиганд) можно использовать на стадии c) для связывания с катионными компонентами, полученными на стадии a), описанной выше, например, посредством дисульфидных связей без блокирования свободных -SH-остатков. Но в данном контексте можно применять все способы, известные специалисту или описанные в настоящей публикации, для связывания компонента (AA) с катионным компонентом или с полимерным носителем.
Альтернативно, компонент (AA) или (например, лиганд) может быть связан с комплексом полимерного носителя и переносимого вещества после стадии c) посредством функциональной группы, которая определена в настоящем описании, например, -SH-остаток. В данном контексте предпочтительно, чтобы компонент (AA) (например, лиганд) был связан через свободные -SH-остатки полимерных компонентов носителя.
Согласно стадии c) способа получения комплекса полимерного носителя и переносимого вещества, который описан в настоящей публикации, по меньшей мере одну молекулу нуклеиновой кислоты, которая определена в настоящем описании, смешивают с катионными компонентами, полученными на стадии b), предпочтительно в указанных выше соотношениях. Обычно в комплексе полимерного носителя и переносимого вещества катионные компоненты, которые определены в настоящем описании, и по меньшей мере одна молекула нуклеиновой кислоты находятся в молярном соотношении примерно от 5 до 10000, предпочтительно в молярном соотношении примерно от 5 до 5000, более предпочтительно в молярном соотношении примерно от 10 до 2500, еще более предпочтительно в молярном соотношении примерно от 10 до 1000 катионного полимера к нуклеиновой кислоте. N/P-соотношения предпочтительно представляют собой соотношения, указанные выше. В данном контексте особенно предпочтительным является случай, когда N/P-соотношения выбраны так, чтобы избежать агломерации и токсичности in vivo.
В конкретном варианте компоненты (AA), которые определены выше, которые не содержат -SH-остатков, могут быть добавлены на стадии c), и такие компоненты при этом включают в комплекс полимерного носителя и переносимого вещества без полимеризации посредством (концевых) -SH-остатков. При этом такие компоненты (AA) обычно нековалентно связаны и включены нековалентно в комплекс в качестве дополнительного компонента. Особенно предпочтительным в данном контексте является включение по меньшей мере одного антигена или его фрагмента, варианта и/или производного, представленного в виде белка или пептида, в комплекс полимерного носителя и переносимого вещества в качестве компонента (AA). Такой вариант является особенно предпочтительным, если AA является овальбумином или фрагментом овальбумина. Таким образом, в особенно предпочтительном варианте, если AA является овальбумином или его фрагментом, AA ковалентно не связан с комплексом полимерного носителя и переносимого вещества, например, AA ковалентно не связан с комплексом полимерного носителя и переносимого вещества дисульфидными связями.
Согласно следующей стадии d) способа получения комплекса полимерного носителя и переносимого вещества, который описан в настоящей публикации, комплекс полимерного носителя и переносимого вещества, полученный согласно стадии c), необязательно очищают. Очистку можно осуществлять, используя хроматографические способы, такие как ВЭЖХ, FPLC, GPS, диализ и т.д.
Согласно следующей стадии e) способа получения комплекса полимерного носителя и переносимого вещества, который описан в настоящей публикации, комплекс полимерного носителя и переносимого вещества, полученный согласно стадии c) или d), необязательно подвергают лиофилизации. С указанной целью можно добавлять подходящий криопротектор или лиопротектор к комплексу полимерного носителя и переносимого вещества, полученному на стадии c) или d).
Способ получения комплекса полимерного носителя и переносимого вещества, который определен в настоящем описании, особенно подходит для адаптации химических свойств требуемого комплекса полимерного носителя и переносимого вещества благодаря специфичному подбору компонентов полимерного носителя и тем самым возможности избежать агломерации и токсичности in vivo.
В качестве второго ингредиента фармацевтическая композиция согласно изобретению содержит по меньшей мере один антиген, выбранный из антигена, полученного из патогена, ассоциированного с инфекционной болезнью; антигена, ассоциированного с аллергией или аллергическим заболеванием; антигена, ассоциированного с аутоиммунным заболеванием; или антигена, ассоциированного с раком или опухолевым заболеванием, или в каждом случае фрагмента, варианта и/или производного указанного антигена.
Такой по меньшей мере один антиген может быть представлен в виде белка или пептида, в виде нуклеиновой кислоты, кодирующей по меньшей мере один антиген, или в виде антигенных клеток, антигенных клеточных фрагментов, клеточных фракций; компонентов клеточной стенки, модифицированных, ослабленных или инактивированных (например, химически или посредством облучения) патогенов (вирусов, бактерий и т.д.), содержащих по меньшей мере один антиген.
В некоторых вариантах антиген, включенный в качестве второго ингредиента в фармацевтическую композицию, представляет собой пептидный или белковый антиген или фрагмент, вариант и/или производное указанного пептидного или белкового антигена.
a) Антигены из патогена, ассоциированного с инфекционной болезнью
Антигены из патогена, ассоциированного с инфекционной болезнью, получают из патогена, который ассоциирован с индукцией инфекционной болезни. В некоторых вариантах указанный антиген представляет собой пептидный или белковый антиген или фрагмент, вариант и/или производное указанного пептидного или белкового антигена, и/или находится, представлен в виде и/или получен из (например, препарат) инактивированного или ослабленного указанного патогена (например, вируса, такого как любой вирус, описанный в настоящей публикации). В данном контексте (например, пептидный или белковый) антиген может находиться, представлен в виде и/или получен из (например, препарат) ослабленного или инактивированного патогена (например, вируса, такого как любой вирус, описанный в настоящей публикации), ассоциированного с инфекционной болезнью.
В альтернативных вариантах всех аспектов изобретения антиген (например, пептидный или белковый антиген), используемый в настоящем изобретении, не является антигеном, находящимся в (например, препарате) инактивированном или ослабленном вирусе (таком как любой вирус, описанный в настоящей публикации, или любой патоген, описанный в настоящей публикации); и/или является антигеном, которые не представлен в виде (например, в виде препарата) указанного инактивированного или ослабленного вируса или патогена; и/или является антигеном, который не получен из (например, препарат) указанного инактивированного или ослабленного вируса или патогена. Например, антиген, используемый в любом аспекте настоящего изобретения, может представлять собой или может быть представлен в виде изолированного и/или очищенного белкового или пептидного антигена. Как будет понятно специалисту, изолированный (и/или очищенный) антиген включает такие антигены, которые присутствуют (или представлены) в (исходной) композиции, которая содержит менее чем примерно 40%, 30%, 20%, 10%, 5%, 2% или 1% нежелательных или других конкретных компонентов, таких как другие белки/пептиды или примеси.
В конкретных вариантах (например, белковый или пептидный) антиген, используемый в настоящем изобретении, представляет собой рекомбинантный антиген, например, рекомбинантный антиген, который получен с использованием основанной на рекомбинации продукции, например, с использованием методик, описанных в настоящей публикации. В альтернативных вариантах (например, белковый или пептидный) антиген, используемый в настоящем изобретении, представляет собой синтетический антиген, например, антиген, который получен с использованием синтеза пептидов, например, с использованием методик, описанных в настоящей публикации.
Антигены из патогена, ассоциированного с инфекционной болезнью, выбраны из антигенов из патогенов Acinetobacter baumannii, рода Anaplasma, Anaplasma phagocytophilum, Ancylostoma braziliense, Ancylostoma duodenale, Arcanobacterium haemolyticum, Ascaris lumbricoides, рода Aspergillus, Astroviridae, рода Babesia, Bacillus anthracis, Bacillus cereus, Bartonella henselae, вируса BK, Blastocystis hominis, Blastomyces dermatitidis, Bordetella pertussis, Borrelia burgdorferi, рода Borrelia, видов Borrelia, рода Brucella, Brugia malayi, семейства Bunyaviridae, Burkholderia cepacia и других видов Burkholderia, Burkholderia mallei, Burkholderia pseudomallei, семейства Caliciviridae, рода Campylobacter, Candida albicans, видов Candida, Chlamydia trachomatis, Chlamydophila pneumoniae, Chlamydophila psittaci, приона CJD, Clonorchis sinensis, Clostridium botulinum, Clostridium difficile, Clostridium perfringens, Clostridium perfringens, видов Clostridium, Clostridium tetani, видов Coccidioides, коронавирусов, Corynebacterium diphtheriae, Coxiella burnetii, вируса геморрагической лихорадки Крым-Конго, Cryptococcus neoformans, рода Cryptosporidium, цитомегаловируса, вирусов денге (DEN-1, DEN-2, DEN-3 и DEN-4), Dientamoeba fragilis, вируса Эбола (EBOV), рода Echinococcus, Ehrlichia chaffeensis, Ehrlichia ewingii, рода Ehrlichia, Entamoeba histolytica, рода Enterococcus, рода энтеровирусов, энтеровирусов, главным образом вируса Коксаки A и энтеровируса 71 (EV71), Epidermophyton spp, вируса Эпштейн-Барр (EBV), Escherichia coli O157:H7, O111 и O104:H4, Fasciola hepatica и Fasciola gigantica, приона FFI, надсемейства Filarioidea, флавивирусов, Francisella tularensis, рода Fusobacterium, Geotrichum candidum, Giardia intestinalis, Gnathostoma spp, приона GSS, вируса Гуанарито, Haemophilus ducreyi, Haemophilus influenzae, Helicobacter pylori, хенипавируса (вируса Хендра, вируса Нипах), вируса гепатита A, вируса гепатита B, вируса гепатита C, вируса гепатита D, вируса гепатита E, вируса простого герпеса 1 и 2 (HSV-1 и HSV-2), Histoplasma capsulatum, ВИЧ (вируса иммунодефицита человека), Hortaea werneckii, бокавируса человека (HBoV), герпесвируса 6 человека (HHV-6) и герпесвируса 7 человека (HHV-7), метапневмовируса человека (hMPV), вируса папилломы человека (HPV), вирусов парагриппа человека (HPIV), вируса японского энцефалита, вируса JC, вируса Хунин, Kingella kingae, Klebsiella granulomatis, приона куру, вируса Ласса, Legionella pneumophila, рода Leishmania, рода Leptospira, Listeria monocytogenes, вируса лимфоцитарного хориоменингита (LCMV), вируса Мачупо, видов Malassezia, вируса Марбург, вируса кори, Metagonimus yokagawai, Microsporidia phylum, вируса контагиозного моллюска (MCV), вируса эпидемического паротита, Mycobacterium leprae и Mycobacterium lepromatosis, Mycobacterium tuberculosis, Mycobacterium ulcerans, Mycoplasma pneumoniae, Naegleria fowleri, Necator americanus, Neisseria gonorrhoeae, Neisseria meningitidis, Nocardia asteroides, видов Nocardia, Onchocerca volvulus, Orientia tsutsugamushi, семейства Orthomyxoviridae, Paracoccidioides brasiliensis, Paragonimus spp, Paragonimus westermani, парвовируса B19, рода Pasteurella, рода Plasmodium, Pneumocystis jirovecii, вируса полиомилита, вируса бешенства, респираторно-синцитиального вируса (RSV), риновируса, риновирусов, Rickettsia akari, рода Rickettsia, Rickettsia prowazekii, Rickettsia rickettsii, Rickettsia typhi, вируса лихорадки долины Рифт, ротавируса, вируса краснухи, вируса Сабиа, рода Salmonella, Sarcoptes scabiei, коронавируса SARS, рода Schistosoma, рода Shigella, вируса Син Номбре, хантавируса, Sporothrix schenckii, рода Staphylococcus, рода Staphylococcus, Streptococcus agalactiae, Streptococcus pneumoniae, Streptococcus pyogenes, Strongyloides stercoralis, рода Taenia, Taenia solium, вируса клещевого энцефалита (TBEV), Toxocara canis или Toxocara cati, Toxoplasma gondii, Treponema pallidum, Trichinella spiralis, Trichomonas vaginalis, видов Trichophyton, Trichuris trichiura, Trypanosoma brucei, Trypanosoma cruzi, Ureaplasma urealyticum, вируса ветряной оспы (VZV), вируса ветряной оспы (VZV), Variola major или Variola minor, приона vCJD, вируса венесуэльского энцефалита лошадей, Vibrio cholerae, вируса Западного Нила, вируса западного энцефалита лошадей, Wuchereria bancrofti, вируса желтой лихорадки, Yersinia enterocolitica, Yersinia pestis и Yersinia pseudotuberculosis.
В данном контексте особенно предпочтительными являются антигены из патогенов, выбранных из вируса бешенства, вируса гепатита B, вируса папилломы человека (hPV), Bacillus anthracis, респираторно-синцитиального вируса (RSV), вируса простого герпеса (HSV), вируса гриппа и Mycobacterium tuberculosis.
Кроме того, антиген из патогена, ассоциированного с инфекционной болезнью, может быть выбран из следующих антигенов: белок наружной мембраны A OmpA, ассоциированный с биопленкой белок Bap, транспортный белок MucK (Acinetobacter baumannii, Acinetobacter infections); вариабельный поверхностный гликопротеин VSG, ассоциированный с микротрубочками белок MAPP15, транссиалидаза TSA (Trypanosoma brucei, африканская сонная болезнь (африканский трипаносомоз)); антиген p24 ВИЧ, белки оболочки ВИЧ (Gp120, Gp41, Gp160), полибелок GAG, белок негативного регуляторного фактора Nef, трансактиватор транскрипции Tat (ВИЧ (вирус иммунодефицита человека)), СПИД (синдром приобретенного иммунодефицита)); белок ингибируемой галактозой адгезии GIAP, антиген Eh29 29 кДа, Gal/GalNAc-лектин, белок CRT, иммунодоминантный антиген 125 кДа, белок M17, адгезин ADH112, белок STIRP (Entamoeba histolytica, амебиаз); главные поверхностные белки 1-5 (MSP1a, MSP1b, MSP2, MSP3, MSP4, MSP5), белки системы секреотина типа IV (VirB2, VirB7, VirB11, VirD4) (род Anaplasma, анаплазмоз); защитный антиген PA, вызывающий отек фактор EF, летальный фактор LF, гомологичные белки S-слоя SLH (Bacillus anthracis, сибирская язва); акранолизин, фосфолипаза D, коллагенсвязывающий белок CbpA (Arcanobacterium haemolyticum, инфекция Arcanobacterium haemolyticum); белок нуклеокапсида NP, гликопротеиновый предшественник GPC, гликопротеин GP1, гликопротеин GP2 (вирус Хунин, аргентинская геморрагическая лихорадка); белки хитин-белкового слоя, поверхностный антиген A14, 14 кДа, основной белок спермы MSP, организующий полимеризацию MSP белок MPOP, MSP-фибриллярный белок 2 MFP2, активирующая полимеризацию MSP киназа MPAK, ABA-1-подобный белок ALB, белок ABA-1, кутикулин CUT-1 (Ascaris lumbricoides, аскаридоз); аллерген 41 кДа Asp v13, аллерген Asp f3, основной конидиальный поверхностный белок rodlet A, протеаза Pep1p, GPI-заякоренный белок Gel1p, GPI-заякоренный белок Crf1p (род Aspergillus, аспергиллез); семейство белка VP26, белок VP29 (Astroviridae, астровирусная инфекция); ассоциированный с роптириями белок 1 RAP-1, поверхностные антигены мерозоитов MSA-1, MSA-2 (a1, a2, b, c), 12D3, 11C5, 21B4, P29, вариант поверхностного антигена эритроцитов VESA1, антиген-1 апикальной мембраны 1 AMA-1 (род Babesia, бабезиоз); гемолизин, энтеротоксин C, PX01-51, гликолатоксидаза, ABC-переносчик, пенициллин-связывающий белок, белок семейства переносчиков цинка, псевдоуридинсинтаза Rsu, белок репликации плазмиды RepX, олигоэндопептидаза F, мембранный белок профага, белок HemK, флагеллярный антиген H, антиген клеточной поверхности 28,5 кДа (Bacillus cereus, инфекция Bacillus cereus); большой T-антиген LT, малый T-антиген, капсидный белок VP1, капсидный белок VP2 (вирус BK, инфекция вирусом BK); 29 кДа-белок, каспаза-3-подобные антигены, гликопротеины (Blastocystis hominis, инфекция Blastocystis hominis); дрожжевой поверхностный адгезин WI-1 (Blastomyces dermatitidis, бластомикоз); нуклеопротеин N, полимераза L, белок матрикса Z, гликопротеин GP (вирус Мачупо, боливийская геморрагическая лихорадка); наружный поверхностный белок A OspA, наружный поверхностный белок OspB, наружный поверхностный белок OspC, декорин-связывающий белок A DbpA, декорин-связывающий белок B DbpB, коровый белок флагеллярного филамента 41 кДа Fla, предшественник основного мембранного белка A BmpA (иммунодоминантный антиген P39), предшественник липопротеина наружной поверхности 22 кДа (антиген IPLA7), вариабельный поверхностный липопротеин vlsE (род Borrelia, инфекция Borrelia); нейротоксины Botulinum BoNT/A1, BoNT/A2, BoNT/A3, BoNT/B, BoNT/C, BoNT/D, BoNT/E, BoNT/F, BoNT/G, рекомбинантный Hc-домен токсина ботулизма F FHc (Clostridium botulinum, ботулизм (и ботулизм у новорожденных)); нуклеокапсид, предшественник гликопротеина (вирус Сабиа, бразильская геморрагическая лихорадка); медь/цинк-суперкосиддисмутаза SodC, бактериоферритин Bfr, рибосомный белок 50S RplL, OmpA-подобный содержащий трансмембранный домен белок Omp31, иммуногенный белок M5 P39, 39 кДа, ABC-переносчик цинка периплазматический цинксвязывающий белок znuA, периплазматический иммуногенный белок Bp26, рибосомный 30S-белок S12 RpsL, глицеральдегид-3-фосфатдегидрогеназа Gap, предшественник иммуногенного белка наружной мембраны 25 кДа Omp25, белок инвазии B lalB, запускающий фактор Tig, молекулярный шаперон DnaK, предполагаемая пептидил-пролил-цис-транс-изомераза SurA, липопротеин Omp19, белок наружной мембраны MotY Omp16, консервативный белок наружной мембраны D15, малатдегидрогеназа Mdh, компонент системы секреции типа IV (T4SS) VirJ, липопротеин с неизвестной функцией BAB1_0187 (род Brucella, бруцеллез); представители семейства ABC-переносчиков (LolC, OppA и PotF), предполагаемый трансмембранный белок системы высвобождения липопротеинов LolC/E, флагеллин FliC, белок внутриклеточной подвижности Burkholderia A BimA, бактериальный фактор элонгации Tu EF-Tu, OmpA-подобный белок 17 кДа, boaA-кодирующий белок, boaB-кодирующий белок (Burkholderia cepacia и другие виды Burkholderia, инфекция Burkholderia); миколилтрансфераза Ag85A, белок теплового шока Hsp65, белок TB10.4, антиген 19 кДа, белок PstS3, белок теплового шока Hsp70 (Mycobacterium ulcerans, язва Бурули); основной и минорный капсидные вирусные белки норовируса VP1 и VP2, геномный полипротеин, капсидный белок саповируса VP1, белок Vp3, геномный полипротеин (семейство Caliciviridae, инфекция калицивируса (норовирус и саповирус)); основной белок наружной мембраны PorA, флагеллин FlaA, поверхностный антиген CjaA, фибронектин-связывающий белок CadF, аспартат/глутамат-связывающий белок ABC-переносчик Peb1A, белок FspA1, белок FspA2 (род Campylobacter, кампилобактериоз); гликолитический фермент енолаза, секретируемые аспартилпротеазы SAP1-10, гликофосфатидилинозитол (GPI)-связанный белок клеточной стенки, белок Hyr1, родственный рецептору комплемента 3 белок CR3-RP, адгезин Als3p, белок теплового шока 90 кДа hsp90, гидрофобный белок клеточной поверхности CSH (обычно Candida albicans и другие виды Candida, кандидоз); антиген 17-кДа, белок P26, тримерные аутопереносчики адгезины TAA, адгезин A Bartonella BadA, вариабельно экспрессируемые белки наружной мембраны Vomp, белок Pap3, белок HbpA, ассоциированная с оболочкой протеза HtrA, белок OMP89, белок GroEL, белок LalB, белок OMP43, дигидролипоамидсукцинилтрансфераза SucB (Bartonella henselae, болезнь кошачьих царапин); поверхностный белок амастигот 2, специфичный для амастигот поверхностный белок SSP4, круципаин, транссиалидаза TS, поверхностный гликопротеин трипомастигот TSA-1, регулирующий комплемент белок CRP-10, белок G4, белок G2, пароксонемальный палочковый белок PAR2, парафлагеллярный палочковый компонент Par1, муцин-ассоциированные поверхностные белки MPSP (Trypanosoma cruzi, болезнь Шагаса (американский трипаносомоз)); гликопротеины оболочки (gB, gC, gE, gH, gI, gK, gL) (вирус ветряной оспы (VZV), ветряная оспа); основной белок наружной мембраны MOMP, предполагаемый белок наружной мембраны PMPC, белок комплекса наружной мембраны B OmcB, белки теплового шока Hsp60 HSP10, белок IncA, белки системы секреции типа III, белок малой цепи рибонуклеотидредуктазы NrdB, плазмидный белок Pgp3, наружный хламидиальный белок N CopN, антиген CT521, антиген CT425, антиген CT043, антиген TC0052, антиген TC0189, антиген TC0582, антиген TC0660, антиген TC0726, антиген TC0816, антиген TC0828 (Chlamydia trachomatis, хламидия); белок низкой отвечаемости на кальций E LCrE, наружный хламидиальный белок N CopN, сериновая/треониновая протеинкиназа PknD, переносящий ацил белок S-малонилтрансфераза FabD, связывающий однонитевую ДНК белок Ssb, основной белок наружной мембраны MOMP, белок наружной мембраны 2 Omp2, семейство полиморфных мембранных белков (Pmp1, Pmp2, Pmp3, Pmp4, Pmp5, Pmp6, Pmp7, Pmp8, Pmp9, Pmp10, Pmp11, Pmp12, Pmp13, Pmp14, Pmp15, Pmp16, Pmp17, Pmp18, Pmp19, Pmp20, Pmp21) (Chlamydophila pneumoniae, инфекция Chlamydophila pneumoniae); холерный токсин B CTB, токсин-корегулируемый пилин A TcpA, токсин-корегулируемый пилин TcpF, белок F биосинтеза токсин-корегулируемых пилей TcpF, субъединица A холерного энтеротоксина, субъединица B холерного энтеротоксина, термостабильный энтеротоксин ST, чувствительный к маннозе гемагглютинин MSHA, белок наружной мембраны U порин ompU, порирующий белок B, полиморфный мембранный белок D (Vibrio cholerae, холера); пропионил-CoA-карбоксилаза PCC, белок 14-3-3, прогибитин, цистеинпротеазы, глутатионтрансферазы, гельзолин, катепсин-L-протеаза CatL, белок тегумента 20,8 кДа TP20.8, белок тегумента 31,8 кДа TP31.8, фосфатаза лизофосфатидиловой кислоты LPAP, (Clonorchis sinensis, клонорхоз); белки поверхностного слоя SLP, антиген глутаматдегидрогеназы GDH, токсин A, токсин B, цистеинпротеаза Cwp84, цистеинпротеаза Cwp13, цистеинпротеаза Cwp19, белок клеточной стенки CwpV, флагеллярный белок FliC, флагеллярный белок FliD (Clostridium difficile, инфекция Clostridium difficile); риновирусы: капсидные белки VP1, VP2, VP3, VP4; коронавирусы: белки sprike S, белки оболочки E, мембранные белки M, нуклеокапсидные белки N (обычно риновирусы и коронавирусы, насморк (острый вирусный ринофарингит; острая инфекция верхних дыхательных путей)); прионный белок Prp (прион CJD, болезнь Крейтцфельдта-Якоба (CJD)); белок оболочки Gc, белок оболочки Gn, нуклеокапсидные белки (вирус геморрагической лихорадки Крым-Конго, геморрагическая лихорадка Крым-Конго (CCHF)); ассоциированная с вирулентностью DEAD-бокс-РНК-геликаза VAD1, галактоксилдоманнан-белок GalXM, глюкуроноксиломаннан GXM, маннопротеин MP (Cryptococcus neoformans, криптококкоз); кислый рибосомный белок P2 CpP2, антигены муцина Muc1, Muc2, Muc3, Muc4, Muc5, Muc6, Muc7, белок поверхностной адгезии CP20, белок поверхностной адгезии CP23, поверхностный белок CP12, поверхностный белок CP21, поверхностный белок CP40, поверхностный белок CP60, поверхностный белок CP15, ассоциированные с поверхностью гликопептиды gp40, ассоциированные с поверхностью гликопептиды gp15, белок стенки ооцисты AB, профилин PRF, апираза (род Cryptosporidium, криптоспоридиоз); связывающий жирные кислоты и ретинол белок-1 FAR-1, тканевой ингибитор металлопротеазы TIMP (TMP), цистеинпротеиназа ACEY-1, цистеинпротеиназа ACCP-1, поверхностный антиген Ac-16, секретируемый белок 2 ASP-2, металлопротеаза 1 MTP-1, ингибитор аспартилпротеазы API-1, ассоциированный с поверхностью антиген SAA-1, специфичный для взрослых секретируемый фактор Xa, ингибитор сериновой протеазы антикоагулянт AP, катепсин D-подобная аспарагиновая протеаза ARR-1 (обычно Ancylostoma braziliense; множество других паразитов, кожная мигрирующая личинка (CLM)); катепсин L-подобные протеазы, антиген 53/25-кДа, представители семейства 8 кДа, белок цистицерка с подобной маргинальному трипсину активностью TsAg5, белок онкосферы TSOL18, белок онкосферы TSOL45-1A, лактатдегидрогеназа A LDHA, лактатдегидрогеназа B LDHB (Taenia solium, цистицеркоз); антиген pp65, мембранный белок pp15, белок капсида-проксимального тегумента pp150, белок M45, ДНК-полимераза UL54, геликаза UL105, гликопротеин gM, гликопротеин gN, гликопротеин H, гликопротеин B gB, белок UL83, белок UL94, белок UL99 (цитомегаловирус, цитомегаловирусная инфекция); капсидный белок C, премембранный белок prM, мембранный белок M, белок оболочки E (домен I, домен II, домен II), белок NS1, белок NS2A, белок NS2B, белок NS3, белок NS4A, белок 2K, белок NS4B, белок NS5 (вирусы денге (DEN-1, DEN-2, DEN-3 и DEN-4)-флавивирусы, лихорадка денге); белок 39 кДа (Dientamoeba fragilis, диентаамебиаз; предшественник дифтерийного токсина Tox, дифтерийный токсин DT, пилин-специфичная сортаза SrtA, белок осевого пилина SpaA, белок пилина кончика SpaC, белок минорного пилина SpaB, ассоциированный с поверхностью белок DIP1281 (Corynebacterium diphtheriae, дифтерия); гликопротеин GP, нуклеопротеин NP, минорный белок матрикса VP24, основной белок матрикса VP40, активатор транскрипции VP30, кофактор полимеразы VP35, РНК-полимераза L (вирус Эбола (EBOV), геморрагическая лихорадка Эбола); прионный белок (прион vCJD, вариант болезни Крейтцфельдта-Якоба (vCJD, nvCJD)); белок системы UvrABC B, белок Flp1, белок Flp2, белок Flp3, белок TadA, рецептор гемоглобина HgbA, наружный мембранный белок TdhA, белок CpsRA, регулятор CpxR, белок SapA, антиген 18 кДа, наружный мембранный белок NcaA, белок LspA, белок LspA1, белок LspA2, белок LspB, компонент наружной мембраны DsrA, лектин DltA, липопротеин Hlp, основной белок наружной мембраны OMP, белок наружной мембраны OmpA2 (Haemophilus ducreyi, шанкроид); аспартилпротеаза 1 Pep1, фосфолипаза B PLB, альфа-маннозидаза 1 AMN1, глюканозилтрансфераза GEL1, уреаза URE, белок матрикса пероксисом Pmp1, богатый пролином антиген Pra, реактивный белок T-клеток человека TcrP (Coccidioides immitis и Coccidioides posadasii, кокцидиоидомикоз); аллерген Tri r2, белок теплового шока 60 Hsp60, катин грибов Act, антиген Tri r2, антиген Tri r4, антиген Tri t1, белок IV, глицерол-3-фосфатдегидрогеназа Gpd1, осмосенсор HwShol A, осмосенсор HwShol B, гистидинкиназа HwHhk7B, аллерген Mala s 1, аллерген Mala s 11, тиоредоксин Trx Mala s 13, аллерген Mala f, аллерген Mala s (обычно виды Trichophyton, виды Epidermophyton, виды Malassezia, Hortaea werneckii, дерматофитоз); белок EG95, белок EG10, белок EG18, белок EgA31, белок EM18, антиген EPC1, антиген B, антиген 5, белок P29, белок 14-3-3, 8-кДа белок, миофилин, белок теплового шока 20 HSP20, гликопротеин GP-89, связывающий жирные кислоты белок FAPB (род Echinococcus, эхинококкоз); основной поверхностный белок 2 MSP2, основной поверхностный белок 4 MSP4, MSP вариант SGV1, MSP вариант SGV2, белок наружной мембраны OMP, белок наружной мембраны 19 OMP-1 9, основной антигенный белок MAP1, основной антигенный белок MAP1-2, основной антигенный белок MAP1B, основной антигенный белок MAP1-3, Erum2510-кодирующий белок, белок GroEL, белок GroES, 30-кДа основной белок наружной мембраны, GE 100-кДа белок, GE 130-кДа белок, GE 160-кДа белок (род Ehrlichia, эрлихиоз); секретируемый антиген SagA, sagA-подобные белки SalA и SalB, адгезин коллагена Scm, поверхностные белки Fms1 (EbpA(fm), Fms5 (EbpB(fm), Fms9 (EpbC(fm) и Fms10, белок EbpC(fm), 96-кДа иммунозащитный гликопротеин G1 (род Enterococcus, энтерококковая инфекция); геномный полипротеин, полимераза 3D, вирусный капсидный белок VP1, вирусный капсидный белок VP2, вирусный капсидный белок VP3, вирусный капсидный белок VP4, протеаза 2A, протеаза 3C (род Enterovirus, энтеровирусная инфекция); белки наружной мембраны OM, 60-кДа белок наружной мембраны, антиген клеточной поверхности OmpA, антиген клеточной поверхности OmpB (sca5), 134-кДа белок наружной мембраны, 31-кДа белок наружной мембраны, 29,5-кДа белок наружной мембраны, белок клеточной поверхности SCA4, белок клеточной поверхности Adr1 (RP827), белок клеточной поверхности Adr2 (RP828), белок клеточной поверхности SCA1, белок инвазии invA, белок клеточного деления fts, семейство sec 0 белков секреции, белки вирулентности virB, tlyA, tlyC, парвулинподобный белок Pip, транслоказа пребелка SecA, 120-кДа поверхностный белковый антиген SPA, антиген комплекса 138-кДа, основной 100-кДа белок (белок I), внутрицитоплазматический белок D, защитный поверхностный белковый антиген SPA (Rickettsia prowazekii, эпидемический сыпной тиф); ядерные антигены Эпштейн-Барр (EBNA-1, EBNA-2, EBNA-3A, EBNA-3B, EBNA-3C, EBNA-лидерный белок (EBNA-LP)), латентные мембранные белки (LMP-1, LMP-2A, LMP-2B), ранний антиген EBV-EA, мембранный антиген EBV-MA, вирусный капсидный антиген EBV-VCA, щелочная нуклеаза EBV-AN, гликопротеин H, гликопротеин gp350, гликопротеин gp110, гликопротеин gp42, гликопротеин gHgL, гликопротеин gB (вирус Эпштейн-Барр (EBV), (инфекционный мононуклеоз вирусом Эпштейн-Барр); капсидный белок VP2, капсидный белок VP1, основной белок NS1 (парвовирус B19, инфекционная эритема (пятая болезнь)); антиген pp65, гликопротеин 105, основной капсидный белок, гликопротеин оболочки H, белок U51 (герпесвирус человека 6 (HHV-6) и герпесвирус человека 7 (HHV-7), внезапная экзантема); тиоредоксин-глутатионредуктаза TGR, катепсины L1 и L2, белок типа Кунитца KTM, лейцинаминопептидаза LAP, цистеинпротеиназа Fas2, сапонинподобный белок-2 SAP-2, тиоредоксинпероксидазы TPx, Prx-1, Prx-2, катепсин I, цистеинпротеиназа CL3, протеаза катепсин L CL1, фосфоглицераткиназа PGK, 27-кДа секреторный белок, 60-кДа белок HSP35альфа, глутатионтрансфераза GST, 28,5-кДа антиген тегумента, 28,5 кДа TA, катепсин B3 протеаза CatB3, цистатин типа I стефин-1, катепсин L5, катепсин L1g и катепсин B, связывающий жирные кислоты белок FABP, лейцинаминопептидазы LAP (Fasciola hepatica и Fasciola gigantica, фасциолез); прионный белок (прион FFI, спорадическая фатальная инсомния (FFI)); подобный гомологу аллергена яда белок VAL-1, преобладающий транскрипт личинок ALT-1, преобладающий транскрипт личинок ALT-2, тиоредоксинпероксидаза TPX, гомолог аллергена веспид VAH, тиоредоксинпероксидаза 2 TPX-2, антигенный белок SXP (пептиды N, N1, N2 и N3), ассоциированный с активацией белок-1 ASP-1, тиоредоксин TRX, трансглутаминаза BmTGA, глутатион-S-трансферазы GST, миозин, гомолог аллергена веспид VAH, 175-кДа коллагеназа, глицеральдегид-3-фосфатдегидрогеназа GAPDH, кутикулярный коллаген Col-4, секретируемые личиночные кислые белки SLAP, хитиназа CHI-1, связывающий мальтозу белок MBP, гликолитический фермент фруктоза-1,6-бисфосфатальдолаза Fba, тропомиозин TMY-1, специфичный для нематод генный продукт OvB20, онхоцистатин CPI-2, Cox-2 (надсемейство Filarioidea, филяриоз); фосфолипаза C PLC, термолабильный энтеротоксин B, компонент токсина лота 1b, белок CPE1281, пируватферредоксиноксидоредуктаза, фактор элонгации G EF-G, перфринголизин O Pfo, глицеральдегид-3-фосфатдегидрогеназа GapC, фруктоза-бисфосфатальдолаза Alf2, энтеротоксин Clostridium perfringens CPE, альфа-токсин AT, альфа-токсоид ATd, эпсилон-токсоид ETd, белок HP, большой цитотоксин TpeL, эндо-бета-N-ацетилглюкозаминидаза Naglu, фосфоглицеромутаза Pgm (Clostridium perfringens, пищевое отравление Clostridium perfringens); лейкотоксин IktA, адгезионный FadA, белок наружной мембраны RadD, высокомолекулярный аргининсвязывающий белок (род Fusobacterium, инфекция Fusobacterium); фосфолипаза C PLC, термолабильный энтеротоксин B, компонент токсина лота Ib, белок CPE1281, пируватферредоксиноксидоредуктаза, фактор элонгации G EF-G, перфринголизин O Pfo, глицеральдегид-3-фосфатдегидрогеназа GapC, фруктоза-бисфосфатальдолаза Alf2, энтероксин Clostridium perfringens CPE, альфа-токсин AT, альфа-токсоид ATd, эпсилон-токсоид ETd, белок HP, крупный цитотоксин TpeL, эндо-бета-N-ацетилглюкозаминидаза Naglu, фосфоглицеромутаза Pgm (обычно Clostridium perfringens; другие виды Clostridium, газовая гангрена (Clostridial myonecrosis)); липаза A, липаза B, пероксидаза Dec1 (Geotrichum candidum, геотрихоз); прионный белок (прион GSS, синдром Герстманна-Штреусслера-Шейнкера (GSS)); белки стенки цист CWP1, CWP2, CWP3, вариант поверхностного белка VSP, VSP1, VSP2, VSP3, VSP4, VSP5, VSP6, 56-кДа антиген, пируватферредоксиноксидоредуктаза PFOR, алкогольдегидрогеназа E ADHE, альфа-жиардин, альфа8-жиардин, альфа1-жиардин, бета-жиардин, цистеинпротеазы, глутатион-S-трансфераза GST, аргининдеиминаза ADI, фруктоза-1,6-бисфосфатальдолаза FBA, антигены трофозоита Giardia GTA (GTA1, GTA2), орнитинкарбоксилтрансфераза OCT, белок, подобный ассеблину исчерченных фибрилл SALP, уридинфосфорил-подобный белок UPL, альфа-тубулин, бета-тубулин (Giardia intestinalis, жиардиаз); представители семейства ABC-переносчика (LolC, OppA, и PotF), предполагаемый трансмембранный белок системы высвобождения липопротеинов LolC/E, флагеллин FliC, белок внутриклеточной подвижности Burkholderia A BimA, бактериальный фактор элонгации-Tu EF-Tu, 17-кДа OmpA-подобный белок, boaА-кодирующий белок (Burkholderia mallei, сап); циклофилин CyP, 24 кДа белок личинок третьей стадии GS24, продукты экскреции-секреции ESP (40, 80, 120 и 208 кДа) (Gnathostoma spinigerum и Gnathostoma hispidum, гнатостомиаз); белки пилины, минорная ассоциированная с пилином субъединица pilC, основная субъединица пилина и варианты pilE, pilS, белок вариации фаз porA, порин B PorB, белок TraD, антиген наружной мембраны Neisseria H.8, 70-кДа антиген, основной белок наружной мембраны PI, белки наружной мембраны PIA и PIB, W-антиген, поверхностный белок A NspA, трансферрин-связывающий белок TbpA, трансферрин-связывающий белок TbpB, PBP2, mtrR-кодирующий белок, ponA-кодирующий белок, пермеаза мембраны FbpBC, система белков FbpABC, белки LbpAB, белок наружной мембраны Opa, переносчик наружной мембраны FetA, подавляемый железом регулятор MpeR (Neisseria gonorrhoeae, гонорея); белок наружной мембраны A OmpA, белок наружной мембраны C OmpC, белок наружной мембраны K17 OmpK17 (Klebsiella granulomatis, паховая гранулема (донованоз)); фибронектин-связывающий белок Sfb, фибронектин/фибриноген-связывающий белок FBP54, фибронектин-связывающий белок FbaA, M-белок типа 1 Emm1, M-белок типа 6 Emm6, иммуноглобулин-связывающий белок 35 Sib35, поверхностный белок R28 Spr28, супероксиддисмутаза SOD, C5a-пептидаза ScpA, антиген I/II Agl/II, адгезин AspA, G-родственный альфа2-макроглобулин-связывающий белок GRAB, поверхностный фибриллярный белок M5 (Streptococcus pyogenes, стрептококковая инфекция, группа A); β-антиген C-белка, белки аргининдеиминазы, адгезин BibA, 105-кДа белок BPS, поверхностные антигены c, поверхностные антигены R, поверхностные антигены X, резистентный к трипсину белок R1, резистентный к трипсину белок R3, резистентный к трипсину белок R4, поверхностный иммуногенный белок Sip, поверхностный белок Rib, белок с богатыми лейцином повторами LrrG, белок с богатыми серином повторами Srr-2, альфа-антиген C-белка Bca, бета-антиген Bag, поверхностный антиген эпсилон, альфа-подобный белок ALP1, альфа-подобный белок ALP5, поверхностный антиген дельта, альфа-подобный белок ALP2, альфа-подобный белок ALP3, альфа-подобный белок ALP4, белок C-бета Bac (Streptococcus agalactiae, стрептококковая инфекция группы B); трансферрин-связывающий белок 2 Tbp2, фосфатаза P4, белок наружной мембраны P6, пептидогликан-ассоциированный липопротеин PaI, белок D, белок E, белок адгезии и проницаемости Hap, белок наружной мембраны 26 Omp26, белок наружной мембраны P5 (фимбрин), белок наружной мембраны D15, белок наружной мембраны OmpP2, 5'-нуклеотидаза NucA, белок наружной мембраны P1, белок наружной мембраны P2, липопротеин наружной мембраны Pep, липопротеин E, белок наружной мембраны P4, фукулокиназа FucK, [Cu,Zn]-супероксиддисмутаза SodC, протеаза HtrA, белок О145, альфа-галактозилцерамид (Haemophilus influenzae, инфекция Haemophilus influenzae); полимерaза 3D, вирусный капсидный белок VP1, вирусный капсидный белок VP2, вирусный капсидный белок VP3, вирусный капсидный белок VP4, протеаза 2A, протеаза 3C (энтеровирусы, главным образом вирус Коксаки A и энтеровирус 71 (EV71), болезнь рук, стоп и полости рта (HFMD)); РНК-полимераза L, белок L, гликопротеин Gn, гликопротеин Gc, нуклеокапсидный белок S, гликопротеин оболочки G1, нуклеопротеин NP, белок N, полибелок M (вирус Син Номбре, хантавирус, хантавирусный легочный синдром (HPS)); белок теплового шока HspA, белок теплового шока HspB, цитратсинтаза GltA, белок UreB, белок теплового шока Hsp60, активирующий нейтрофилы белок NAP, каталаза KatA, вакуолизирующий цитотоксин VacA, уреаза альфа UreA, уреаза бета Ureb, белок Cpn10, белок groES, белок теплового шока Hsp10, белок MopB, ассоциированный с цитотоксичностью 10-кДа белок CAG, 36-кДа антиген, бета-лактамаза HcpA, бета-лактамаза HcpB (Helicobacter pylori, инфекция Helicobacter pylori); интегральные мембранные белки, склонные к агрегации белки, O-антиген, токсин-антигены Stx2B, токсин-антиген Stx1B, фрагмент антигена адгезии Int28, белок EspA, белок EspB, интимин, белок Tir, белок IntC300, белок Eae (Escherichia coli O157:H7, O111 и O104:H4, гемолитико-уремический синдром (HUS)); РНК-полимераза L, белок L, гликопротеин Gn, гликопротеин Gc, нуклеокапсидный белок S, гликопротеин оболочки G1, нуклеопротеин NP, белок N, полибелок M (семейство Bunyaviridae, геморрагическая лихорадка с почечным синдромом (HFRS)); гликопротеин G, белок матрикса M, нуклеопротеин N, белок слияния F, полимераза L, белок W, белок C, фосфопротеин p, неструктурный белок V (хенипавирус (вирус Хендра и вирус Нипах), хенипавирусные инфекции); полибелок, гликопротеин Gp2, поверхностный антиген гепатита A HBAg, белок 2A, вирусный белок VP1, вирусный белок VP2, вирусный белок VP3, вирусный белок VP4, белок P1B, белок P2A, белок P3AB, белок P3D (вирус гепатита A, гепатит A); поверхностный антиген гепатита B HBsAg, коровый антиген гепатита B HbcAg, полимераза, белок Hbx, средний поверхностный белок preS2, поверхностный белок L, большой S-белок, вирусный белок VP1, вирусный белок VP2, вирусный белок VP3, вирусный белок VP4 (вирус гепатита B, гепатит B); гликопротеин оболочки E1 gp32 gp35, гликопротеин оболочки E2 NS1 gp68 gp70, капсидный белок C, коровый белок Core, полибелок, вирусный белок VP1, вирусный белок VP2, вирусный белок VP3, вирусный белок VP4, антиген G, белок NS3, белок NS5A, (вирус гепатита C, гепатит C); вирусный белок VP1, вирусный белок VP2, вирусный белок VP3, вирусный белок VP4, большой антиген гепатита дельта, малый антиген гепатита дельта (вирус гепатита D, гепатит D); вирусный белок VP1, вирусный белок VP2, вирусный белок VP3, вирусный белок VP4, капсидный белок E2 (вирус гепатита E, гепатит E); гликопротеин L UL1, урацил-ДНК-гликозилаза UL2, белок UL3, белок UL4, белок ДНК-репликации UL5, портальный белок UL6, белок созревания вириона UL7, ДНК-геликаза UL8, связывающий начало репликации белок UL9, гликопротеин M UL10, белок UL11, щелочная экзонуклеаза UL12, сериновая-треониновая протеинкиназа UL13, белок тегумента UL14, терминаза UL15, белок тегумента UL16, белок UL17, капсидный белок VP23 UL18, основной капсидный белок VP5 UL19, мембранный белок UL20, белок тегумента UL21, гликопротеин H (UL22), тимидинкиназа UL23, белок UL24, белок UL25, капсидный белок P40 (UL26, VP24, VP22A), гликопротеин B (UL27), белок ICP18.5 (UL28), основной ДНК-связывающий белок ICP8 (UL29), ДНК-полимераза UL30, белок ядерного матрикса UL31, гликопротеин оболочки UL32, белок UL33, белок внутренней ядерной мембраны UL34, капсидный белок VP26 (UL35), большой белок тегумента UL36, белок сборки капсида UL37, белок VP19C (UL38), рибонуклеотидредуктаза (большая субъединица) UL39, рибонуклеотидредуктаза (малая субъединица) UL40, белок тегумента/белок выключения генов хозяина вирионом VHS (UL41), фактор процессивности ДНК-полимеразы UL42, мембранный белок UL43, гликопротеин C (UL44), мембранный белок UL45, белки тегумента VP11/12 (UL46), белок тегумента VP13/14 (UL47), белок созревания вириона VP16 (UL48, альфа-TIF), белок оболочки UL49, dUTP-дифосфатаза UL50, белок тегумента UL51, белок комплекса ДНК-геликаза/праймаза UL52, гликопротеин K (UL53), белок регуляции транскрипции IE63 (ICP27, UL54), белок UL55, белок UL56, белок репликации вируса ICP22 (IE68, US1), белок US2, сериновая/треониновая протеинкиназа US3, гликопротеин G (US4), гликопротеин J (US5), гликопротеин D (US6), гликопротеин I (US7), гликопротеин E (US8), белок тегумента US9, белок капсида/тегумента US10, белок Vmw21 (US11), белок ICP47 (IE12, US12), основной активатор транскрипции ICP4 (IE175, RS1), убиквитинлигаза E3 ICPO (IE1 10), связанный с латентностью белок 1 LRP1, связанный с латентностью белок 2 LRP2, фактор нейровирулентности RL1 (ICP34.5), ассоциированный с латентностью транскрипт LAT (вирус простого герпеса 1 и 2 (HSV-1 и HSV-2), простой герпес); белок теплового шока Hsp60, белок клеточной поверхности H1C, дипептидилпептидаза типа IV DppIV, M-антиген, 70-кДа белок, 17-кДа гистон-подобный белок (Histoplasma capsulatum, гистоплазмоз); связывающий жирные кислоты и ретинол белок-1 FAR-1, тканевой ингибитор металлопротеиназы TIMP (TMP), цистеинпротеиназа ACEY-1, цистеинпротеиназа ACCP-1, поверхностный антиген Ac-16, секретируемый белок 2 ASP-2, металлопротеаза 1 MTP-1, ингибитор аспартилпротеазы API-1, ассоциированный с поверхностью антиген SAA-1, ассоциированный с поверхностью антиген SAA-2, специфичный для взрослых секретируемый фактор Xa, ингибирующий сериновую протеазу антикоагулянт AP, катепсин D-подобная аспарагиновая протеаза ARR-1, глутатион S-трансфераза GST, аспарагиновая протеаза APR-1, ацетилхолинэстераза AChE (Ancylostoma duodenale и Necator americanus, анкилостомоз); белок NS1, белок NP1, белок VP1, белок VP2, белок VP3 (бокавирус человека (HBoV), инфекция бокавирусом человека); основной поверхностный белок 2 MSP2, основной поверхностный белок 4 MSP4, MSP вариант SGV1, MSP вариант SGV2, белок наружной мембраны OMP, белок наружной мембраны 19 OMP-19, основной антигенный белок MAP1, основной антигенный белок MAP1-2, основной антигенный белок MAP1B, основной антигенный белок MAP1-3, Erum2510-кодирующий белок, белок GroEL, белок GroES, 30-кДа основные белки наружной мембраны, белок GE 100 кДа, белок GE 130 кДа, белок GE 160 кДа (Ehrlichia ewingii, эрлихиоз человека, вызванный ewingii); основные поверхностные белки 1-5 (MSP1a, MSP1b, MSP2, MSP3, MSP4, MSP5), белки системы секреотина типа IV VirB2, VirB7, VirB11, VirD4 (Anaplasma phagocytophilum, гранулоцитарный анаплазмоз человека (HGA)); белок NS1, малый гидрофобный белок NS2, SH-белок, белок слияния F, гликопротеин G, белок матрикса M, белок матрикса M2-1, белок матрикса M2-2, фосфопротеин P, нуклеопротеин N, полимераза L (метапневмовирус человека (hMPV), инфекция метапневмовирусом человека); основной поверхностный белок 2 MSP2, основной поверхностный белок 4 MSP4, MSP вариант SGV1, MSP вариант SGV2, белок наружной мембраны OMP, белок наружной мембраны 19 OMP-19, основной антигенный белок MAP1, основной антигенный белок MAP1-2, основной антигенный белок MAP1B, основной антигенный белок MAP1-3, Erum2510-кодирующий белок, белок GroEL, белок GroES, 30-кДа основные белки наружной мембраны, GE 100-кДа белок, GE 130-кДа белок, GE 160-кДа белок (Ehrlichia chaffeensis, моноцитарный эрлихиоз человека); белок репликации E1, регуляторный белок E2, белок E3, белок E4, белок E5, белок E6, белок E7, белок E8, основной капсидный белок L1, минорный капсидный белок L2 (вирус папилломы человека (HPV), инфекция вирусом папилломы человека (HPV)); белок слияния F, гемагглютинин-нейраминидаза HN, гликопротеин G, белок матрикса M, фосфопротеин P, нуклеопротеин N, полимераза L (вирусы парагриппа человека (HPIV), инфекция вирусом парагриппа человека); гемагглютинин HA, нейраминидаза NA, нуклеопротеин NP, белок матрикса M1, белок матрикса M2, белок NS1, комплекс полимеразы PA, PB1 PB2, белок ядерного экспорта NEP (семейство Orthomyxoviridae, грипп (острое респираторное заболевание)); геномный полибелок, белок E, белок M, капсидный белок C (вирус японского энцефалита, японский энцефалит); токсин RTX, пили типа IV, основная субъединица пилуса PilA, факторы регуляции транскрипции PilS и PilR, белок сигма54, белки наружной мембраны (Kingella kingae, инфекция Kingella kingae); прионный белок (прион куру, куру); нуклеопротеин N, полимераза L, белок матрикса Z, гликопротеин CP (вирус Ласса, лихорадка Ласса); пептидогликан-ассоциированный липопротеин PAL, 60-кДа шаперон Cpn60 (groEL, HspB), пилин типа IV PilE, белок наружной мембраны MIP, основной белок наружной мембраны MompS, цинковая металлопротеиназа MSP (Legionella pneumophila, легионеллез (болезнь легионеров, лихорадка Понтиак)); нуклеаза P4, белок WD, рибонуклеотидредуктаза M2, поверхностный мембранный гликопротеин Pg46, цистеинпротеиназа CP, регулируемый глюкозой белок 78 GRP-78, специфичный для стадии S антиген-подобный белок A2, АТФаза F1, бета-тубулин, белок теплового шока 70 Hsp70, KMP-11, гликопротеин GP63, белок BT1, нуклеозидгидролаза NH, белок клеточной поверхности B1, рибосомный белок P1-подобный белок P1, стерол-24-c-метилтрансфераза SMT, LACK-белок, гистон H1, белок SPB1, тиолспецифичный антиоксидант TSA, белковый антиген STI1, сигнальная пептидаза SP, гистон H2B, поверхностный антиген PSA-2, цистеинпротеиназа b Cpb (род Leishmania, лейшманиоз); основной мембранный белок I, богатый серином антиген 45 кДа, 10-кДа шаперонин GroES, HSP-антиген, аминооксононаноатсинтаза AONS, белковая рекомбиназа A RecA, ацетил/пропионил-кофермент A-карбоксилаза альфа, аланинрацемаза, 60-кДа шаперонин 2, ESAT-6-подобный белок EcxB (L-ESAT-6), белок Lsr2, белок ML0276, гепарин-связывающий гемагглютинин HBHA, белок теплового шока 65 Hsp65, mycP1- или ML0041-кодирующий белок, htrA2- или ML0176-кодирующий белок, htrA4- или ML2659-кодирующий белок, gcp- или ML0379-кодирующий белок, clpC- или ML0235-кодирующий белок (Mycobacterium leprae и Mycobacterium lepromatosis, лепра); белок наружной мембраны LipL32, мембранный белок LIC10258, мембранный белок LP30, мембранный белок LIC12238, Ompa-подобный белок Lsa66, поверхностный белок LigA, поверхностный белок LigB, основной белок наружной мембраны OmpL1, белок наружной мембраны LipL41, белок LigAni, поверхностный белок LcpA, белок адгезии LipL53, белок наружной мембраны UpL32, поверхностный белок Lsa63, флагеллин FlaB1, мембранный липопротеин LipL21, мембранный белок pL40, поверхностный адгезин лептоспиры Lsa27, белок наружной мембраны OmpL36, белок наружной мембраны OmpL37, белок наружной мембраны OmpL47, белок наружной мембраны OmpL54, ацилтрансфераза LpxA (род Leptospira, лептоспироз); предшественник листериолизина O Hly (LLO), ассоциированный с инвазией белок lap (P60), листериолизин-регулирующий белок PrfA, цинковая металлопротеиназа MpI, фосфатидилинозитол-специфичная фосфолипаза C PLC (PlcA, PlcB), O-ацетилтрансфераза Oat, пермеаза ABC-переносчика lm.G_1771, белок адгезии LAP, рецептор LAP Hsp60, адгезин LapB, гемолизин листериолизин O LLO, белок ActA, интерналин A InlA, белок InlB (Listeria monocytogenes, листериоз); наружный поверхностный белок A OspA, наружный поверхностный белок OspB, наружный поверхностный белок OspC, декорин-связывающий белок A DbpA, декорин-связывающий белок B DbpB, коровый белок флагеллярного филамента 41 кДа Fla, основный мембранный белок A BmpA (иммунодоминантный антиген P39), предшественник липопротеина наружной поверхности 22 кДа (антиген IPLA7), вариабельный липопротеин поверхности vlsE (обычно Borrelia burgdorferi и другие виды Borrelia, болезнь Лайма (боррелиоз Лайма)); подобный гомологу аллергена яда белок VAL-1, преобладающий личиночный транскрипт ALT-1, преобладающий личиночный транскрипт ALT-2, тиоредоксинпероксидаза TPX, гомолог аллергена веспид VAH, тиоредоксинпероксидаза 2 TPX-2, антигенный белок SXP (пептиды N, N1, N2 и N3), ассоциированный с активацией белок-1 ASP-1, тиоредоксин TRX, трансглутаминаза BmTGA, глутатион-S-трансферазы GST, миозин, гомолог аллергена веспид VAH, коллагеназа 175 кДа, глицеральдегид-3-фосфатдегидрогеназа GAPDH, кутикулярный коллаген Col-4, секретируемые кислые личиночные белки SLAP, хитиназа CHI-1, связывающий мальтозу белок MBP, гликолитический фермент фруктоза-1,6-бисфосфатальдолаза Fba, тропомиозин TMY-1, специфичный для нематод генный продукт OvB20, онхоцистатин CPI-2, белок Cox-2 (Wuchereria bancrofti и Brugia malayi, лимфатический филяриотоз (элефантиаз)); гликопротеин GP, белок матрикса Z, полимераза L, нуклеопротеин N (вирус лимфоцитарного хориоменингита (LCMV), лимфоцитарный хориоменингит); тромбоспондин-родственный безымянный белок TRAP, поверхностный белок 2 спорозоита SSP2, антиген 1 апикальной мембраны AMA1, мембранный антиген роптрии RMA1, антиген с кислыми и основными повторами ABRA, проходящий в клетку белок PF, белок Pvs25, поверхностный белок 1 мерозоита MSP-1, поверхностный белок 2 мерозоита MSP-2, поверхностный антиген инфицированных кольцевыми формами эритроцитов RESA, антиген печеночной стадии 3 LSA-3, белок Eba-175, антиген 5 с сериновыми повторами SERA-5, белок CS циркумспорозоита, поверхностный белок 3 мерозоита MSP3, поверхностный белок 8 мерозоита MSP8, енолаза PF10, белок гепатоцитов и эритроцитов 17 кДа HEP17, мембранный белок 1 эритроцитов EMP1, белок Кбета, поверхностный белок мерозоита 4/5 MSP 4/5, белок теплового шока Hsp90, глутамат-богатый белок GLURP, поверхностный белок мерозоита 4 MSP-4, белок STARP, предшественник антигена, родственного белка циркумспорозоита CRA (род Plasmodium, малярия); нуклеопротеин N, ассоциированный с мембраной белок VP24, минорный нуклеопротеин VP30, кофактор полимеразы VP35, полимераза L, белок матрикса VP40, гликопротеин оболочки GP (вирус Марбург, геморрагическая лихорадка Марбург (MHF)); белок C, белок матрикса M, фосфопротеин P, неструктурный белок V, гликопротеин гемагглютинина H, полимераза L, нуклеопротеин N, белок слияния F (вирус кори, корь); представители семейства ABC-переносчиков (LolC, OppA и PotF), предполагаемый трансмембранный белок системы высвобождения липопротеинов LolC E, флагеллин FliC, белок A внутриклеточной подвижности Burkholderia A BimA, бактериальный фактор элонгации-Tu EF-Tu, 17 кДа OmpA-подобный белок, boaA-кодирующий белок, boaB-кодирующий белок (Burkholderia pseudomallei, мелиоидоз (болезнь Уитмора)); белки пилины, минорная ассоциированная с пилином субъединица pilC, основная субъединица пилина и варианты pilE, pilS, белок вариации фаз porA, порин B PorB, белок TraD, антиген наружной мембраны Neisseria H.8, 70-кДа антиген, основной белок наружной мембраны PI, белки наружной мембраны PIA и PIB, W-антиген, поверхностный белок A NspA, трансферрин-связывающий белок TbpA, трансферрин-связывающий белок TbpB, PBP2, mtrR-кодирующий белок, ponA-кодирующий белок, пермеаза мембраны FbpBC, система белков FbpABC, белки LbpAB, белок наружной мембраны Opa, переносчик наружной мембраны FetA, подавляемый железом регулятор MpeR, фактор H-связывающий белок fHbp, адгезин NadA, белок NhbA, репрессор FarR (Neisseria meningitidis, менингококковое заболевание); 66 кДа белок, 22 кДа белок (обычно Metagonimus yokagawai, метагонимоз); полярные белки трубочек (34, 75 и 170 кДа у Glugea, 35, 55 и 150 кДа у Encephalitozoon), кинезин-родственный белок, наибольшая субъединица РНК-полимеразы II, сходная с интегральным мембранным белком YIPA, белок 1 против сайленсинга, фактор транскрипции теплового шока HSF, протеинкиназа, тимидинкиназа, NOP-2-подобный ядрышковый белок (Microsporidia phylum, микроспоридиоз); CASP8 и FADD-подобный регулятор апоптоза, глутатионпероксидаза GPX1, РНК-геликаза NPH-II NPH2, каталитическая субъединица поли(A)-полимеразы PAPL, основной белок оболочки P43K, субъединица 70 кДа раннего фактора транскрипции VETFS, субъединица 82 кДа раннего фактора транскрипции VETFL, металлоэндопептидаза G1-типа, нуклеозидтрифосфатаза I NPH1, подобный белку репликации A28 MC134L, субъединица 7 кДа РНК-полимеразы RPО7 (вирус контагиозного моллюска (MCV), контагиозный моллюск (MC)); белок матрикса M, фосфопротеин P/V, малый гидрофобный белок SH, нуклеопротеин N, белок V, гликопротеин слияния F, гемагглютинин-нейраминидаза HN, РНК-полимераза L (вирус эпидемического паротита, эпидемический паротит); белки наружной мембраны OM, антиген клеточной поверхности OmpA, антиген клеточной поверхности OmpB (sca5), белок клеточной поверхности SCA4, белок клеточной поверхности SCA1, внутрицитоплазматический белок D, белок поверхностного слоя кристаллина SLP, защитный поверхностный белок антиген SPA (Rickettsia typhi, мышиный тиф (эндемический тиф)); адгезин P1, адгезин P30, белок p116, белок P40, белок цитоскелета HMW1, белок цитоскелета HMW2, белок цитоскелета HMW3, MPN152-кодирующий белок, MPN426-кодирующий белок, MPN456-кодирующий белок, MPN-500-кодирующий белок (Mycoplasma pneumoniae, Mycoplasma pneumonia); NocA, зависимый от железа регуляторный белок, VapA, VapD, VapF, VapG, казеинолитическая протеаза, ассоциированный с кончиком филамента 43-кДа белок, белок P24, белок P61, 15-кДа белок, 56-кДа белок (обычно Nocardia asteroides и другие виды Nocardia species, нокардиоз); белок, подобный гомологу аллергена яда VAL-1, преобладающий личиночный транскрипт ALT-1, преобладающий личиночный транскрипт ALT-2, тиоредоксинпероксидаза TPX, гомолог аллергена веспид VAH, тиоредоксинпероксидаза 2 TPX-2, антигенный белок SXP (пептиды N, N1, N2 и N3), ассоциированный с активацией белок-1 ASP-1, тиоредоксин TRX, трансглутаминаза BmTGA, глутатион-S-трансферазы GST, миозин, гомолог аллергена веспид VAH, коллагеназа 175 кДа, глицеральдегид-3-фосфатдегидрогеназа GAPDH, кутикулярный коллаген Col-4, секретируемые личиночные кислые белки SLAP, хитиназа CHI-1, связывающий мальтозу белок MBP, гликолитический фермент фруктоза-1,6-бисфосфатальдолаза Fba, тропомиозин TMY-1, специфичный для нематод генный продукт OvB20, онхоцистатин CPI-2, ЦОГ-2 (Onchocerca volvulus, онхоцеркоз (речная слепота)); секретируемый гликопротеин 43 кДа гликопротеин gp0, гликопротеин gp75, антиген Pb27, антиген Pb40, белок теплового шока Hsp65, белок теплового шока Hsp70, белок теплового шока Hsp90, белок P10, триозафосфатизомераза TPI, N-ацетилглюкозамин-связывающий лектин паракокцин, 28 кДа белок Pb28 (Paracoccidioides brasiliensis, паракокцидиоидомикоз (южно-американский бластомикоз)); 28-кДа круципаин-подобная цистеиновая протеаза Pw28CCP (обычно Paragonimus westermani и другие виды Paragonimus, парагонимоз); белок наружной мембраны OmpH, белок наружной мембраны Omp28, белок PM1539, белок PM0355, белок PM1417, репарационный белок MutL, белок BcbC, белок PM0305, формиатдегидрогеназа-N, белок PM0698, белок PM1422, ДНК-гираза, липопротеин PlpE, адгезивный белок Cp39, рецептор системы захвата гема HasR, капсулярный белок 39 кДа, регулируемый железом OMP IROMP, белок наружной мембраны OmpA87, белок фимбрий Ptf, белок субъединицы фимбрий PtfA, трансферрин-связывающий белок TbpI, фермент эстераза MesA, токсин Pasteurella multocida PMT, адгезивный белок Cp39 (род Pasteurella, пастереллез); филаментный гемагглютинин FhaB, аденилатциклаза CyaA, предшественник субъединицы 4 коклюшного токсина PtxD, предшественник пертактина Prn, субъединица 1 токсина PtxA, белок Cpn60, белок brkA, предшественник субъединицы 2 коклюшного токсина PtxB, предшественник субъединицы 3 коклюшного токсина PtxC, предшественник субъединицы 5 коклюшного токсина PtxE, пертактин Prn, белок Fim2, белок Fim3 (Bordetella pertussis, коклюш (судорожный кашель)); «F1 капсульный антиген, ассоциированный с вирулентностью антиген V, секретируемый эффекторный белок LcrV, V-антиген, протеаза наружной мембраны Pla, секретируемый эффекторный белок YopD, предполагаемый секретируемый протеинтирозинфосфатаза YopH, основная субъединица комплекса иглы YscF, протеинкиназа YopO, предполагаемый белок аутопереносчик YapF, ABC-переносчик внутренней мембраны YbtQ (Irp7), предполагаемый сахар-связывающий белок YPO0612, белок теплового шока 90 HtpG, предполагаемый белок сульфатазы YdeN, белок-носитель липопротеина наружной мембраны LolA, шаперон секреции YerA, предполагаемый липопротеин YPO0420, белок активатор гемолизина HpmB, рецептор наружной мембраны пестицина/иерсиниябактина Psn, секретируемый эффекторный белок YopE, секретируемый эффекторный белок YopF, секретируемый эффекторный белок YopK, белок наружной мембраны YopN, белок наружной мембраны YopM, предшественник коагулазы/фибринолизина Pla; (Yersinia pestis, чума); белок PhpA, поверхностный адгезин PsaA, пневмолизин Ply, АТФ-зависимая протеаза Clp, липоат-протеинлигаза LplA, заякоренный на поверхности клеточной стенки белок psrP, сортаза SrtA, глутамил-тРНК-синтетаза GltX, холин-связывающий белок A CbpA, пневмококковый поверхностный белок A PspA, пневмококковый поверхностный белок C PspC, 6-фосфоглюконатдегидрогеназа Gnd, связывающий железо белок PiaA, муреингидролаза LytB, протеон LytC, протеаза A1 (Streptococcus pneumoniae, пневмококковая инфекция); основной поверхностный белок B, кексин-подобная протеаза KEX1, белок A12, 55 кДа-антиген P55, основной поверхностный гликопротеин Msg (Pneumocystis jirovecii, плазмаклеточная пневмония (PCP)); геномный полибелок, полимераза 3D, вирусный капсидный белок VP1, вирусный капсидный белок VP2, вирусный капсидный белок VP3, вирусный капсидный белок VP4, протеаза 2A, протеаза 3C (вирус полиомиелита, полиомиелит); белок Nfa1, эксендин-3, секреторная липаза, катепсин B-подобная протеаза, цистеинпротеаза, катепсин, пероксиредоксин, белок Cry1Ac (обычно Naegleria fowleri, первичный амебный менингоэнцефалит (PAM)); агнопротеин, большой T-антиген, малый T-антиген, основной капсидный белок VP1, минорный капсидный белок Vp2 (вирус JC, прогрессирующая мультифокальная лейкоэнцефалопатия); белок низкой отвечаемости на кальций E LCrE, наружный хламидиальный белок N CopN, сериновая/треониновая протеинкиназа PknD, S-малонилтрансфераза ацил-переносящего белка FabD, связывающий однонитевую ДНК белок Ssb, основной белок наружной мембраны MOMP, белок наружной мембраны 2 Omp2, семейство полиморфных мембранных белков (Pmp1, Pmp2, Pmp3, Pmp4, Pmp5, Pmp6, Pmp7, Pmp8, Pmp9, Pmp10, Pmp11, Pmp12, Pmp13, Pmp14, Pmp15, Pmp16, Pmp17, Pmp18, Pmp19, Pmp20, Pmp21) (Chlamydophila psittaci, орнитоз); белок наружной мембраны P1, белок теплового шока B HspB, пептидный ABC-переносчик, GTP-связывающий белок, белок IcmB, рибонуклеаза R, фосфатаза SixA, белок DsbD, белок наружной мембраны TolC, ДНК-связывающий белок PhoB, АТФаза DotB, белок теплового шока B HspB, мембранный белок Com1, белок 28 кДа, ДНК-3-метиладенингликозидаза I, белок наружной мембраны OmpH, белок наружной мембраны AdaA, T-белок системы отщепления глицина (Coxiella burnetii, Q-риккетсиоз); нуклеопротеин N, большой структурный белок L, фосфобелок P, белок матрикса M, гликопротеин G (вирус бешенства, бешенство); белок слияния F, нуклеопротеин N, белок матрикса M, белок матрикса M2-1, белок матрикса M2-2, фосфопротеин P, малый гидрофобный белок SH, основной поверхностный гликопротеин G, полимераза L, неструктурный белок 1 NS1, неструктурный белок 2 NS2 (респираторно-синцитиальный вирус (RSV), инфекция респираторно-синцитиальным вирусом); геномный полибелок, полимераза 3D, вирусный капсидный белок VP1, вирусный капсидный белок VP2, вирусный капсидный белок VP3, вирусный капсидный белок VP4, протеаза 2A, протеаза 3C (риновирус, риновирусная инфекция); белок наружной мембраны OM, антиген клеточной поверхности OmpA, антиген клеточной поверхности OmpB (sca5), белок клеточной поверхности SCA4, белок клеточной поверхности SCA1, белок PS120, внутрицитоплазматический белок D, антиген защитного поверхностного белка SPA (род Rickettsia, риккетсиозная инфекция); белки наружной мембраны OM, антиген клеточной поверхности OmpA, антиген клеточной поверхности OmpB (sca5), белок клеточной поверхности SCA4, белок клеточной поверхности SCA1, внутрицитоплазматический белок D (Rickettsia akari, риккетсиоз); гликопротеин оболочки GP, полимераза L, нуклеопротеин N, неструктурный белок NSS (вирус лихорадки долины Рифт, лихорадка долины Рифт (RVF)); белки наружной мембраны OM, антиген клеточной поверхности OmpA, антиген клеточной поверхности OmpB (sca5), белок клеточной поверхности SCA4, белок клеточной поверхности SCAT, внутрицитоплазматический белок D (Rickettsia rickettsii, пятнистая лихорадка Скалистых гор (RMSF)); неструктурный белок 6 NS6, неструктурный белок 2 NS2, промежуточный капсидный белок VP6, внутренний капсидный белок VP2, неструктурный белок 3 NS3, РНК-зависимая РНК-полимераза L, белок VP3, неструктурный белок 1 NS1, неструктурный белок 5 NS5, наружный капсидный гликопротеин VP7, неструктурный гликопротеин 4 NS4, наружный капсидный белок VP4; (ротавирус, ротавирусная инфекция); полибелок P200, гликопротеин E1, гликопротеин E2, белок NS2, капсидный белок C (вирус краснухи, краснуха); шаперонин GroEL (MopA), инозитолфосфатфосфатаза SopB, белок теплового шока HsIU, шаперонный белок DNAJ, белок TviB, белок IroN, флагеллин FliC, белок инвазии SipC, гликопротеин gp43, белок наружной мембраны LamB, белок наружной мембраны PagC, белок наружной мембраны TolC, белок наружной мембраны NmpC, белок наружной мембраны FadL, транспортный белок SadA, трансфераза WgaP, эффекторные белки SifA, SteC, SseL, SseJ и SseF (род Salmonella, сальмонеллез); белок 14, неструктурный белок NS7b, неструктурный белок NS8a, белок 9b, белок 3a, нуклеопротеин N, неструктурный белок NS3b, неструктурный белок NS6, белок 7a, неструктурный белок NS8b, мембранный белок M, малый мембранный белок оболочки EsM, полибелок репликазы 1a, гликопротеин шиповидных отростков S, полибелок репликазы 1 ab; (коронавирус SARS, SARS (тяжелый острый респираторный синдром)); сериновая протеаза, антиген 1 атипичного саркоптеса 1 ASA1, глутатион-S-трансферазы GST, цистеиновая протеаза, сериновая протеаза, aпoлипопротеин (Sarcoptes scabiei, чесотка); глутатион-S-трансферазы GST, парамиозин, гемоглобиназа SM32, основной антиген яйцеклеток, связывающий жирные кислоты белок 14 кДа Sm14, основной личиночный поверхностный антиген P37, 22,6 кДа-антиген тегумента, калпаин CANP, трифосфатизомераза Tim, поверхностный белок 9B, наружный капсидный белок VP2, интегральный мембранный белок 23 кДа Sm23, Cu,Zn-супероксиддисмутаза, гликопротеин Gp, миозин (род Schistosoma, шистосоматоз (бильгарциоз)); 60 кДа шаперонин, специфичный для типа антиген 56 кДа, пируватфосфатдикиназа, 4-гидроксибензоатоктапренилтрансфераза (Orientia tsutsugamushi, клещевой тропический тиф); дегидрогеназа GuaB, белок инвазии Spa32, инвазин IpaA, инвазин IpaB, инвазин IpaC, инвазин IpaD, инвазин IpaH, инвазин IpaJ (род Shigella, шигеллез (бактериальная дизентерия)); белок P53, гомолог белка вириона US10, регулятор транскрипции IE63, трансактиватор транскрипции IE62, протеаза P33, белок альфа-трансиндуцирующего фактора 74 кДа, дезоксиуридин-5'-трифосфатнуклеотидгидролаза, трансактиватор транскрипции IE4, гомолог мембранного белка UL43, гомолог ядерного фосфопротеина UL3, гомолог ядерного белка UL4, связывающий начало репликации белок, мембранный белок 2, фосфопротеин 32, белок 57, фактор процессивности ДНК-полимеразы, портальный белок 54, ДНК-праймаза, гомолог белка тегумента UL14, гомолог белка тегумента UL21, гомолог белка тегумента UL55, гомолог субъединицы тройной терминазы UL33, гомолог субъединицы тройной терминазы UL15, капсид-связывающий белок 44, белок упаковки вириона 43 (вирус ветряной оспы (VZV), Shingles (Herpes zoster)); укороченный гомолог 3-бета-гидрокси-5-енстероиддегидрогеназы, мембранный белок вириона A13, белок A19, белок A31, укороченный гомолог белка A35, гомолог белка A37.5, белок A47, белок A49, белок A51, семафорин-подобный белок A43, ингибитор сериновой протеиназы 1, ингибитор сериновой протеиназы 2, ингибитор сериновой протеиназы 3, белок A6, белок B15, белок C1, белок C5, белок C6, белок F7, белок F8, белок F9, белок F11, белок F14, белок F15, белок F16 (Variola major или Variola minor, натуральная оспа (оспа)); адгезин/гликопротеин gp70, протеазы (Sporothrix schenckii, споротрихоз); связывающий железо гема белок IsdB, коллаген адгезин Cna, фактор агглютинации A ClfA, белок MecA, фибронектин-связывающий белок A FnbA, энтеротоксин типа A EntA, энтеротоксин типа B EntB, энтеротоксин типа C EntС1, энтеротоксин типа C EntC2, энтеротоксин типа D EntD, энтеротоксин типа E EntE, токсин-1 синдрома токсического шока TSST-1, стафилокиназа, пенициллин-связывающий 2a-белок PBP2a (MecA), секреторный антиген SssA (род Staphylococcus, стафилококковое пищевое отравление); гема-железо-связывающий белок IsdB, коллаген-адгезин Cna, фактор агглютинации A ClfA, белок MecA, фибронектин-связывающий белок A FnbA, энтеротоксин типа A EntA, энтеротоксин типа B EntB, энтеротоксин типа C EntC1, энтеротоксин типа C EntC2, энтеротоксин типа D EntD, энтеротоксин типа E EntE, токсин-1 синдрома токсического шока TSST-1, стафилокиназа, пенициллин-связывающий 2a-белок PBP2a (MecA), секреторный антиген SssA (род Staphylococcus, стафилококковая инфекция); антиген Ss-IR, антиген NIE, стронгиластацин, Na+-K+-АТФаза Sseat-6, тропомизин SsTmy-1, белок LEC-5, 41 кДа-антиген P5, 41-кДа личиночный белок, 31-кДа личиночный белок, 28-кДа личиночный белок (Strongyloides stercoralis, стронгилоидоз); глицерофосфодиэфирфосфодиэстераза GlpQ (Gpd), белок наружной мембраны TmpB, белок Tp92, антиген TpF1, содержащий повторы белок Tpr, содержащий повторы белок F TprF, содержащий повторы белок G TprG, содержащий повторы белок I TprI, содержащий повторы белок J TprJ, содержащий повторы белок K TprK, мембранный белок трепонем A TmpA, липопротеин, 15-кДа Tpp15, 47-кДа мембранный антиген, миниферритин TpF1, адгезин Tp0751, липопротеин TP0136, белок TpN17, белок TpN47, белок наружной мембраны TP0136, белок наружной мембраны TP0155, белок наружной мембраны TP0326, белок наружной мембраны TP0483, белок наружной мембраны TP0956 (Treponema pallidum, сифилис); катепсин L-подобные протеазы, 53/25-кДа антиген, представители семейства 8 кДа, белок цистицерка с подобной маргинальному трипсину активностью TsAg5, белок онкосфер TSOL18, белок онкосфер TSOL45-1A, лактатдегидрогеназа A LDHA, лактатдегидрогеназа B LDHB (род Taenia, тениоз); столбнячный токсин TetX, столбнячный токсин C TTC, 140 кДа белок S-слоя, бета-субъединица флавопротеина CT3, фосфолипаза (лецитиназа), белок переносчик фосфора HPr (Clostridium tetani, столбняк); геномный полибелок, белок E, белок M, капсидный белок C (вирус клещевого энцефалита (TBEV), клещевой энцефалит); 58-кДа антиген, 68-кДа антигены, экскреторный-секреторный антиген личинок Toxocara TES, 32-кДа гликопротеин, гликопротеин TES-70, гликопротеин GP31, экскреторный-секреторный антиген TcES-57, антиген околокишечной жидкости Pe, растворимые антигены экстракта Ex, экскреторные/секреторные личиночные антигены ES, антиген TES-120, полибелковый аллерген TBA-1, катепсин L-подобная цистеиновая протеаза c-cpl-1, белок 26 кДа (Toxocara canis или Toxocara cati, токсокароз (глазная форма синдрома мигрирующей личинки (OLM) и висцеральная форма синдрома мигрирующей личинки (VLM))); белки микронем (MIC1, MIC2, MIC3, MIC4, MIC5, MIC6, MIC7, MIC8), белок роптрии Rop2, белки роптрии (Rop1, Rop2, Rop3, Rop4, Rop5, Rop6, Rop7, Rop16, Rop17), белок SR1, поверхностный антиген P22, основной антиген p24, основной поверхностный антиген p30, белки плотных гранул (GRA1, GRA2, GRA3, GRA4, GRA5, GRA6, GRA7, GRA8, GRA9, GRA10), антиген 28 кДа, поверхностный антиген SAG1, SAG2-родственный антиген, нуклеозидтрифосфатаза 1, нуклеозидтрифосфатаза 2, белок Stt3, белок, содержащий HesB-подобный домен, ромбоид-подобная протеаза 5, токсомепсин 1 (Toxoplasma gondii, токсоплазмоз); секретируемый гликопротеин 43 кДа, секретируемый гликопротеин 53 кДа, парамиозин, антиген Ts21, антиген Ts87, антиген p46000, TSL-1-антигены, кавеолин-1 CAV-1, личиночный антиген у новорожденных 49 кДа, гомолог просапозина, сериновая протеаза, ингибитор сериновой протеиназы, 45-кДа гликопротеин Gp45 (Trichinella spiralis, трихинеллез); Myb-подобные факторы транскрипции (Myb1, Myb2, Myb3), белок адгезии AP23, белок адгезии AP33, адгезиновый белок AP33-3, адгезины AP51, адгезин AP65, белок адгезии AP65-1, альфа-актинин, кинезин-ассоциированный белок, тенеурин, протеиназа 62 кДа, субтилизин-подобная сериновая протеаза SUB1, ген 3 цистеиновой протеиназы 3 CP3, альфа-енолаза Eno1, цистеиновая протеиназа CP30, белки теплового шока (Hsp70, Hsp60), иммуногенный белок P270, (Trichomonas vaginalis, трихомоноз); бета-тубулин, 47-кДа белок, секреторная лейкоцитарно-подобная протеиназа-1 SLP-1, 50-кДа белок TT50, 17 кДа антиген, 43/47 кДа белок (Trichuris trichiura, трихоуроз (инфекция власоглавом)); белок ESAT-6 (EsxA), 10 кДа фильтрующийся антиген EsxB, секретируемый антиген 85-B FBPB, фибронектин-связывающий белок A FbpA (Ag85A), сериновая протеаза PepA, белок PPE-семейства PPE18, фибронектин-связывающий белок D FbpD, иммуногенный белок MPT64, секретируемый белок MPT51, каталаза-пероксидаза-пероксинитритаза T KATG, периплазматический фосфат-связывающий липопротеин PSTS3 (PBP-3, Phos-1), регулируемый железом гепарин-связывающий гемагглютинин Hbha, белок PPE-семейства PPE14, белок PPE-семейства PPE68, белок Mtb72F, белок Apa, иммуногенный белок MPT63, периплазматический фосфат-связывающий липопротеин PSTS1 (PBP-1), молекулярный шаперон DnaK, липопротеин клеточной поверхности Mpt83, липопротеин P23, белок пермеазы системы транспорта фосфата pstA, 14 кДа антиген, фибронектин-связывающий белок C FbpC1, аланиндегидрогеназа TB43, глутаминсинтетаза 1, белок ESX-1, белок CFP10, белок TB10.4, белок MPT83, белок MTB12, белок MTB8, Rpf-подобные белки, белок MTB32, белок MTB39, кристаллин, белок теплового шока HSP65, белок PST-S (обычно Mycobacterium tuberculosis, туберкулез); белок наружной мембраны FobA, белок наружной мембраны FobB, локус внутриклеточного роста IgIC1, локус внутриклеточного роста IgIC2, аминотрансфераза Wbt1, шаперонин GroEL, 17 кДа основной мембранный белок TUL4, липопротеин LpnA, белок семейства хитиназы 18, изоцитратдегидрогеназа, белок семейства Nif3, белок гликозилирования пилей типа IV, белок наружной мембраны tolC, белок FAD-связывающего семейства, мультимерный белок наружной мембраны пилей типа IV, двукомпонентный сенсорный белок KdpD, белок шаперон DnaK, белок TolQ (Francisella tularensis, туляремия); MB-антиген, уреаза, белок GyrA, белок GyrB, белок ParC, белок ParE, липид-ассоциированные мембранные белки LAMP, тимидинкиназа TK, фосфолипаза PL-A1, фосфолипаза PL-A2, фосфолипаза PL-C, экспрессируемый на поверхности антиген 96 кДа; (Ureaplasma urealyticum, инфекция Ureaplasma urealyticum); неструктурный полибелок, структурный полибелок, капсидный белок CP, белок E1, белок E2, белок E3, протеаза P1, протеаза P2, протеаза P3 (вирус венесуэльского энцефалита лошадей, венесуэльский энцефалит лошадей); гликопротеин GP, белок матрикса Z, полимераза L, нуклеопротеин N (вирус Гуанарито, венесуэльская геморрагическая лихорадка); полибелок, белок E, белок M, капсидный белок C, протеаза NS3, белок NS1, белок NS2A, белок AS2B, белок NS4A, белок NS4B, белок NS5 (вирус Западного Нила, лихорадка Западного Нила); капсидный белок CP, белок E1, белок E2, белок E3, протеаза P2 (вирус западного энцефалита лошадей, западный энцефалит лошадей); геномный полибелок, белок E, белок M, капсидный белок C, протеаза NS3, белок NS1, белок NS2A, белок AS2B, белок NS4A, белок NS4B, белок NS5 (вирус желтой лихорадки, желтая лихорадка); предполагаемый Yop-таргетирующий белок YobB, эффекторный белок YopD, эффекторный белок YopE, белок YopH, эффекторный белок YopJ, белок транслокации YopK, эффекторный белок YopT, белок YpkA, белок биосинтеза жгутиков FlhA, пептидаза M48, система выкачивания калия KefA, регулятор транскрипции RovA, адгезин lfp, белок транслокации LcrV, белок PcrV, инвазин Inv, белок наружной мембраны OmpF-подобный порин, адгезин YadA, протеинкиназа C, фосфолипаза C1, белок PsaA, маннозилтрансфераза-подобный белок WbyK, белок YscU, антиген YPMa (Yersinia pseudotuberculosis, инфекция Yersinia pseudotuberculosis); эффекторный белок YopB, 60 кДа шаперонин, белок WbcP, тирозиновая протеинфосфатаза YopH, белок YopQ, энтеротоксин, галактозидаза пермеаза, редуктаза NrdE, белок YasN, инвазин Inv, адгезин YadA, порин наружной мембраны F OmpF, белок UspA1, белок EibA, белок Hia, белок клеточной поверхности AiI, шаперон SycD, белок LcrD, белок LcrG, белок LcrV, белок SycE, белок YopE, регуляторный белок TyeA, белок YopM, белок YopN, белок YopO, белок YopT, белок YopD, протеаза ClpP, белок MyfA, белок FilA и белок PsaA (Yersinia enterocolitica, иерсиниоз),
(в скобках указан конкретный патоген, из которого антиген(ы) получен, и инфекционная болезнь, с которой антиген ассоциирован).
В конкретных вариантах осуществления настоящего изобретения особенно предпочтительными являются следующие антигены патогенов, ассоциированных с инфекционной болезнью:
- нуклеопротеин (N), фосфопротеин (P), белок матрикса (M), гликопротеин (G) и вирусная РНК-полимераза (L), в каждом случае вируса бешенства;
- поверхностный антиген гепатита B (HBsAg), коровый антиген гепатита B (HbcAg), ДНК-полимераза вируса гепатита B, белок HBx, средний поверхностный белок preS2, большой S-белок, вирусный белок VP1, вирусный белок VP2, вирусный белок VP3 и вирусный белок VP4, в каждом случае вируса гепатита B;
- белок E1, белок E2, белок E3, белок E4, белок E5, белок E6, белок E7, белок E8, белок L1 и белок L2, в каждом случае вируса папилломы человека (hPV);
- защитный антиген (PA), фактор отека (EF), летальный фактор (LF) и гомологичные белки S-слоя (SLH), в каждом случае Bacillus anthracis;
- белок слияния (F), нуклеокапсидный (N) белок, фосфопротеин (P), белок матрикса (M), гликопротеин (G), большой белок (L; РНК-полимераза), неструктурный белок 1 (NS1), неструктурный белок 2 (NS2), малый гидрофобный (SH) белок, фактор элонгации M2-1 и белок регуляции транскрипции M2-2, в каждом случае респираторно-синцитиальный вирус (RSV);
- гликопротеин L (UL1), урацил-ДНК-гликозилаза UL2, белок UL3, белок UL4, белок репликации ДНК UL5, портальный белок UL6, белок созревания вириона UL7, ДНК-геликаза UL8, связывающий начало репликации белок UL9, гликопротеин M (UL10), белок UL11, щелочная экзонуклеаза UL12, сериновая-треониновая протеинкиназа UL13, белок тегумента UL14, терминаза (UL15), белок тегумента UL16, белок UL17, капсидный белок VP23 (UL18), основной капсидный белок VPS (UL19), мембранный белок UL20, белок тегумента UL21, гликопротеин H (UL22), тимидинкиназа UL23, белок UL24, белок UL25, капсидный белок P40 (UL26, VP24, VP22A), гликопротеин B (UL27), белок ICP18.5 белок (UL28), основной ДНК-связывающий белок ICP8 (UL29), ДНК-полимераза UL30, белок ядерного матрикса UL31, гликопротеин оболочки UL32, белок UL33, белок внутренней ядерной мембраны UL34, капсидный белок VP26 (UL35), большой белок тегумента UL36, белок сборки капсида UL37, белок VP19C (UL38), рибонуклеотидредуктаза (большая субъединица) UL39, рибонуклеотидредуктаза (малая субъединица) UL40, белок тегумента/белок выключения генов хозяина вирионом VHS (UL41), фактор процессивности ДНК-полимеразы UL42, мембранный белок UL43, гликопротеин C (UL44), мембранный белок UL45, белки тегумента VP1 1/12 (UL46), белок тегумента VP13/14 (UL47), белок созревания вириона VP1 6 (UL48, альфа-TIF), белок оболочки UL49, dUTP-дифосфатаза UL50, белок тегумента UL51, белок комплекса ДНК-геликазы/праймазы UL52, гликопротеин K (UL53), белок регуляции транскрипции IE63 (ICP27, UL54), белок UL55, белок UL56, белок вирусной репликации ICP22 (IE68, US1), белок US2, сериновая/треониновая протеинкиназа US3, гликопротеин G (US4), гликопротеин J (US5), гликопротеин D (US6), гликопротеин I (US7), гликопротеин E (US8), белок тегумента US9, белок капсида/тегумента US10, белок Vmw21 (US11), белок ICP47 (IE12, US12), основной активатор транскрипции ICP4 (IE175, RS1), E3 убиквитинлигаза ICPO (IE110), связанный с латентностью белок 1 (LRP1), связанный с латентностью белок 2 (LRP2), фактор нейровирулентности RL1 (ICP34.5) и ассоциированный с латентностью транскрипт (LAT), в каждом случае вирус Herpes simplex (HSV); или
- белок ESAT-6, белок ESX-1, белок CFP10, белок TB10.4, белок MPT63, белок MPT64, белок MPT83, белок MTB12, белок MTB8, белок AG85A, белок AG85B, Rpf-подобные белки, белок KATG, белок PPE18, белок MTB32, белок MTB39, кристаллин, белок HSP65, белок PST-S и белок HBHA, 10 кДа фильтрующийся антиген EsxB, сериновая протеаза PepA, фибронектин-связывающий белок D FbpD, секретируемый белок MPT51, периплазматический фосфат-связывающий липопротеин PSTS1 (PBP-1), периплазматический фосфат-связывающий липопротеин PSTS3 (PBP-3, Phos-1), белок PPE-семейства PPE14, белок PPE-семейства PPE68, белок MTB72F, молекулярный шаперон DnaK, липопротеин клеточной поверхности MPT83, липопротеин P23, белок пермеазы системы транспорта фосфата PstA, 14 кДа антиген, фибронектин-связывающий белок C FbpC1, аланиндегидрогеназа TB43 и глутаминсинтетаза 1, в каждом случае Mycobacterium tuberculosis.
b) Антигены, ассоциированные с аллергией или аллергическим заболеванием (аллергенные антигены или аллергены):
Согласно другому альтернативному варианту один следующий класс антигенов включает аллергенные антигены. Такие аллергенные антигены могут быть выбраны из антигенов, полученных из разных источников, например, животных, растений, грибов, бактерий и т.д. Источники аллергенов в данном контексте включают, например, травы, пыльцу, плесени, лекарственные средства или многочисленные возбудители из окружающей среды, и т.д. Аллергенные антигены обычно относятся к разным классам соединений, таким как нуклеиновые кислоты и их фрагменты, белки или пептиды и их фрагменты, углеводы, полисахариды, сахара, липиды, фосфолипиды и т.д. Особый интерес в контексте настоящего изобретения представляют белковые или пептидные антигены и их фрагменты или эпитопы, или нуклеиновые кислоты и их фрагменты, в частности, нуклеиновые кислоты и их фрагменты, кодирующие такие белковые или пептидные антигены и их фрагменты или эпитопы.
В альтернативных вариантах указанный антиген представляет собой пептидный или белковый антиген или фрагмент, вариант и/или производное указанного пептидного или белкового антигена, такой как пептидный или белковый антиген, входящий в состав препарата, выделенного из указанного источника. В альтернативных вариантах пептидный или белковый антиген, используемый в настоящем изобретении, не является антигеном, входящим в состав препарата, выделенного из указанного источника, и/или является антигеном, которые не получен из препарата, выделенного из указанного источника.
Антигены, ассоциированные с аллергией или аллергическим заболеванием (аллергены), предпочтительно получены из источника, выбранного из списка, включающего:
Acarus spp (Aca s 1, Aca s 10, Aca s 10.0101, Aca s 13, Aca s 13.0101, Aca s 2, Aca s 3, Aca s 7, Aca s 8), Acanthocybium spp (Aca so 1), Acanthocheilonema spp (Aca v 3, Aca v 3.0101), Acetes spp (Ace ja 1), Actinidia spp (Act a 1, Act c 1, Act c 10, Act c 10.0101, Act c 2, Act c 4, Act c 5, Act c 5.0101, Act c 8, Act c 8.0101, Act c Хитиназа, Act d 1, Act d 1.0101, Act d 10, Act d 10.0101, Act d 10.0201, Act d 11, Act d 11.0101, Act d 2, Act d 2.0101, Act d 3, Act d 3.0101, Act d 3.02, Act d 4, Act d 4.0101, Act d 5, Act d 5.0101, Act d 6, Act d 6.0101, Act d 7, Act d 7.0101, Act d 8, Act d 8.0101, Act d 9, Act d 9.0101, Act d Хитиназа, Act e 1, Act e 5), Acyrthosiphon spp (Acy pi 7, Acy pi 7.0101, Acy pi 7.0102), Adenia spp (Ade v RIP), Aedes spp (Aed a 1, Aed a 1.0101, Aed a 2, Aed a 2.0101, Aed a 3, Aed a 3.0101, Aed a 4, Aed a 7, Aed a 7.0101, Aed a 7.0102, Aed a 7.0103, Aed a 7.0104, Aed a 7.0105, Aed a 7.0106, Aed a 7.0107, Aed a 7.0108, Aed a 7.0109, Aed a 7.0110, Aed a 7.0111, Aed al 1, Aed al 3, Aed al 37 кДа, Aed v 37 кДа, Aed v 63 кДа), Aegilops spp (Aeg ta 28, Aeg ta альфа_глиадин, Aeg um 28, Aeg un 28), Aethaloperca spp (Aet ro 1), Agropyron spp (Agr c 7), Agrostis spp (Agr ca 1, Agr ca 5, Agr g 1, Agr g 4, Agr s 5), Agrobacterium spp (Agr sp CP4 EPSPS), Ailuropoda spp (Ail me Фосвитин, Ail me TCTP), Aix spp (Aix ga 1, Aix sp 1), Aleuroglyphus spp (Ale o 1, Ale o 10, Ale o 10.0101, Ale o 10.0102, Ale o 13, Ale o 14, Ale o 2, Ale o 20, Ale o 3, Ale o 5, Ale o 7, Ale o 8, Ale o 9), Allium spp (All a 3, All a Аллиинлиаза, All c 3, All c 30 кДа, All c 4, All c Аллиинлиаза, All p Аллиинлиаза, All s Аллиинлиаза), Alnus spp (Aln g 1, Aln g 1.0101, Aln g 1/Bet v 1/Cor a 1 TPC7, Aln g 1/Bet v 1/Cor a 1 TPC9, Aln g 2, Aln g 4, Aln g 4.0101), Alopochen spp (Alo ae 1), Alopecurus spp (Alo p 1, Alo p 5), Alternaria spp (Alt a 1, Alt a 1.0101, Alt a 1.0102, Alt a 10, Alt a 10.0101, Alt a 12, Alt a 12.0101, Alt a 13, Alt a 13.0101, Alt a 2, Alt a 3, Alt a 3.0101, Alt a 4, Alt a 4.0101, Alt a 5, Alt a 5.0101, Alt a 6, Alt a 6.0101, Alt a 7, Alt a 7.0101, Alt a 70 кДа, Alt a 8, Alt a 8.0101, Alt a 9, Alt a MnSOD, Alt a NTF2, Alt a TCTP, Alt ar 1, Alt arg 1, Alt b 1, Alt bl 1, Alt br 1, Alt c 1, Alt ca 1, Alt ce 1, Alt ch 1, Alt ci 1, Alt co 1, Alt cr 1, Alt ct 1, Alt cu 1, Alt cy 1, Alt d 1, Alt du 1, Alt e 1, Alt et 1, Alt eu 1, Alt ga 1, Alt gr 1, Alt j 1, Alt l 1, Alt lo 1, Alt m 1, Alt me 1, Alt mi 1, Alt mo 1, Alt o 1, Alt p 1, Alt ph 1, Alt po 1, Alt ps 1, Alt r 1, Alt s 1, Alt se 1, Alt sm 1, Alt so 1, Alt su 1, Alt t 1, Alt te 1, Alt to 1), Amaranthus spp (Ama r 2, Ama r 2.0101, Ama v 2, Ama v 2.0101, Ama v 2.0201), Ambrosia spp (Amb a 1, Amb a 1.0101, Amb a 1.0201, Amb a 1.0202, Amb a 1.0301, Amb a 1.0302, Amb a 1.0303, Amb a 1.0304, Amb a 1.0305, Amb a 1.0401, Amb a 1.0402, Amb a 1.0501, Amb a 1.0502, Amb a 10, Amb a 10.0101, Amb a 3, Amb a 3.0101, Amb a 4, Amb a 4.0101, Amb a 5, Amb a 5.0101, Amb a 6, Amb a 6.0101, Amb a 7, Amb a 7.0101, Amb a 8, Amb a 8.0101, Amb a 8.0102, Amb a 9, Amb a 9.0101, Amb a 9.0102, Amb a CPI, Amb p 1, Amb p 5, Amb p 5.0101, Amb p 5.0201, Amb t 5, Amb t 5.0101, Amb t 8), Ammothea spp (Amm h 7, Amm h 7.0101), Anadara spp (Ana br 1), Ananas spp (Ana c 1, Ana c 1.0101, Ana c 2, Ana c 2.0101, Ana c 2.0101 (MUXF3)), Anas spp (Ana ca 1), Anarhichas spp (Ana l 1), Anacardium spp (Ana o 1, Ana o 1.0101, Ana o 1.0102, Ana o 2, Ana o 2.0101, Ana o 3, Ana o 3.0101), Anas spp (Ana p 1, Ana p 2, Ana p 3), Anguilla spp (Ang a 1, Ang j 1), Anisakis spp (Ani s 1, Ani s 1.0101, Ani s 10, Ani s 10.0101, Ani s 11, Ani s 11.0101, Ani s 12, Ani s 12.0101, Ani s 2, Ani s 2.0101, Ani s 24 кДа, Ani s 3, Ani s 3.0101, Ani s 4, Ani s 4.0101, Ani s 5, Ani s 5.0101, Ani s 6, Ani s 6.0101, Ani s 7, Ani s 7.0101, Ani s 8, Ani s 8.0101, Ani s 9, Ani s 9.0101, Ani s CCOS3, Ani s Цитохром B, Ani s FBPP, Ani s NADHDS4L, Ani s NARaS, Ani s PEPB, Ani s Тропонин), Annona spp (Ann c Хитиназа), Anopheles spp (Ano da 17, Ano da 17.0101, Ano da 27, Ano da 27.0101, Ano da 7, Ano da 7.0101, Ano g 7, Ano g 7.0101), Anser spp (Ans a 1, Ans a 2, Ans a 3, Ans in 1), Anthoxanthum spp (Ant o 1, Ant o 1.0101, Ant o 12, Ant o 13, Ant o 2, Ant o 4, Ant o 5, Ant o 6, Ant o 7), Apis spp (Api c 1, Api c 1.0101, Api c 10, Api c 2, Api c 4, Api d 1, Api d 1.0101, Api d 4, Api fl 4), Apium spp (Api g 1, Api g 1.0101, Api g 1.0201, Api g 2, Api g 2.0101, Api g 3, Api g 3.0101, Api g 4, Api g 4.0101, Api g 5, Api g 5.0101, Api g 6, Api g 6.0101), Apis spp (Api m 1, Api m 1.0101, Api m 10, Api m 10.0101, Api m 11, Api m 11.0101, Api m 11.0201, Api m 13 кДа, Api m 2, Api m 2.0101, Api m 3, Api m 3.0101, Api m 4, Api m 4.0101, Api m 5, Api m 5.0101, Api m 6, Api m 6.0101, Api m 7, Api m 7.0101, Api m 8, Api m 8.0101, Api m 9, Api m 9.0101, Api m A1-A2, Api m A1-A2-A3, Api m Апальбумин 1, Api m Апальбумин 2, Api me 1, Api me 4), Arachis spp (Ara d 2, Ara d 6, Ara f 3, Ara f 4, Ara h 1, Ara h 1.0101, Ara h 10, Ara h 10.0101, Ara h 10.0102, Ara h 11, Ara h 11.0101, Ara h 2, Ara h 2.0101, Ara h 2.0102, Ara h 2.0201, Ara h 2.0202, Ara h 3, Ara h 3.0101, Ara h 4, Ara h 4.0101, Ara h 5, Ara h 5.0101, Ara h 6, Ara h 6.0101, Ara h 7, Ara h 7.0101, Ara h 7.0201, Ara h 7.0202, Ara h 8, Ara h 8.0101, Ara h 8.0201, Ara h 9, Ara h 9.0101, Ara h 9.0201, Ara h Агглютинин, Ara h Олеозин 18 кДа, Ara i 2, Ara i 6), Arabidopsis spp (Ara t 3, Ara t 8, Ara t GLP), Archosargus spp (Arc pr 1), Archaeopotamobius spp (Arc s 8, Arc s 8.0101), Aequipecten spp (Arg i 1), Argas spp (Arg r 1, Arg r 1.0101), Ariopsis spp (Ari fe 1), Armoracia spp (Arm r HRP), Arrhenatherum spp (Arr e 1, Arr e 5), Artemisia spp (Art a 1, Art ap 1), Artemia spp (Art fr 1, Art fr 1.0101, Art fr 5, Art fr 5.0101), Arthrobacter spp (Art gl CO), Achorion spp (Art gy 7), Artocarpus spp (Art h 17 кДа, Art h 4), Arthrospira spp (Art pl бета_Фикоцианин), Artemisia spp (Art v 1, Art v 1.0101, Art v 1.0102, Art v 1.0103, Art v 1.0104, Art v 1.0105, Art v 1.0106, Art v 1.0107, Art v 2, Art v 2.0101, Art v 3, Art v 3.0101, Art v 3.0201, Art v 3.0202, Art v 3.0301, Art v 4, Art v 4.0101, Art v 4.0201, Art v 47 кДа, Art v 5, Art v 5.0101, Art v 6, Art v 6.0101, Art v 60 кДа), Arthroderma spp (Art va 4), Ascaris spp (Asc l 3, Asc l 3.0101, Asc l 3.0102, Asc l 34 кДа, Asc s 1, Asc s 1.0101, Asc s 3, Asc s 3.0101, Asc s GST), Aspergillus spp (Asp aw Глюкоамилаза, Asp c 22, Asp f 1, Asp f 1.0101, Asp f 10, Asp f 10.0101, Asp f 11, Asp f 11.0101, Asp f 12, Asp f 12.0101, Asp f 13, Asp f 13.0101, Asp f 15, Asp f 15.0101, Asp f 16, Asp f 16.0101, Asp f 17, Asp f 17.0101, Asp f 18, Asp f 18.0101, Asp f 2, Asp f 2.0101, Asp f 22, Asp f 22.0101, Asp f 23, Asp f 23.0101, Asp f 27, Asp f 27.0101, Asp f 28, Asp f 28.0101, Asp f 29, Asp f 29.0101, Asp f 3, Asp f 3.0101, Asp f 34, Asp f 34.0101, Asp f 4, Asp f 4.0101, Asp f 5, Asp f 5.0101, Asp f 56 кДа, Asp f 6, Asp f 6.0101, Asp f 7, Asp f 7.0101, Asp f 8, Asp f 8.0101, Asp f 9, Asp f 9.0101, Asp f AfCalAp, Asp f AT_V, Asp f Каталаза, Asp f Хитозаназа, Asp f CP, Asp f DPPV, Asp f FDH, Asp f гамма_актин, Asp f Глюкозидаза, Asp f GPI, Asp f GST, Asp f GT, Asp f IAO, Asp f IPMI, Asp f LPL1, Asp f LPL3, Asp f Маннозидаза, Asp f MDH, Asp f PL, Asp f PUP, Asp f RPS3, Asp f SXR, Asp fl 13, Asp fl 13.0101, Asp fl 18, Asp fl 2, Asp fl 21, Asp fl 3, Asp fl 4, Asp fl 7, Asp fl 8, Asp fl 9, Asp me Seaprose, Asp n 14, Asp n 14.0101, Asp n 18, Asp n 18.0101, Asp n 25, Asp n 25.0101, Asp n 30, Asp n Глюкоамилаза, Asp n Гемицеллюлаза, Asp n Пектиназа, Asp o 13, Asp o 13.0101, Asp o 21, Asp o 21.0101, Asp o 3, Asp o 4, Asp o 7, Asp o 8, Asp o Лактаза, Asp o Липаза, Asp oc 13, Asp r 1, Asp sa AP, Asp sp Глюкоамилаза, Asp sp Глюкозаоксидаза, Asp sp PL, Asp sp PME, Asp sy 13, Asp v 13, Asp v 13.0101, Asp v Каталаза A, Asp v Енолаза, Asp v GAPDH, Asp v MDH, Asp v SXR), Asparagus spp (Aspa o 1, Aspa o 1.01, Aspa o 1.02, Aspa o 17 кДа, Aspa o 4), Aspergillus spp (Aspe ni 2, Aspe ni 3, Aspe ni 4, Aspe ni 7, Aspe ni 8, Aspe ni 9), Avena spp (Ave s 1, Ave s 12, Ave s 13, Ave s 2, Ave s 4, Ave s 5, Ave s 7), Babylonia spp (Bab ja 1), Bacillus spp (Bac al Субтилизин, Bac cl Субтилизин, Bac l Субтилизин, Bac li aA, Bac li Субтилизин), Bactrocera spp (Bac ol 27, Bac ol 27.0101), Bacillus spp (Bac sp aA1, Bac sp aA3, Bac sp Декарбоксилаза, Bac st amyM, Bac su Субтилизин, Bac t Cry1Ab, Bac t Cry1Fa, Bac t Cry3Bb1, Bac t Cry9c), Bagre spp (Bag ma 1), Balistes spp (Bal ca 1), Balanus spp (Bal r 1, Bal r 1.0101), Beauveria spp (Bea b Ald, Bea b Enol, Bea b f2, Bea b Hex), Bertholletia spp (Ber e 1, Ber e 1.0101, Ber e 2, Ber e 2.0101), Beryx spp (Ber sp 1), Betula spp (Bet ab 1, Bet al 1, Bet ch 1, Bet co 1, Bet da 1, Bet gr 1, Bet hu 1, Bet le 1, Bet me 1, Bet n 1, Bet p 1, Bet pa 1, Bet po 1, Bet pu 1, Bet pu 2, Bet pu 4, Bet pu 6, Bet pu 7, Bet sc 1, Bet ut 1, Bet v 1, Bet v 1 B1-B1-B1, Bet v 1 fv Mal 4x, Bet v 1.0101, Bet v 1.0102, Bet v 1.0103, Bet v 1.0201, Bet v 1.0301, Bet v 1.0401, Bet v 1.0402, Bet v 1.0501, Bet v 1.0601, Bet v 1.0602, Bet v 1.0701, Bet v 1.0801, Bet v 1.0901, Bet v 1.1001, Bet v 1.1101, Bet v 1.1201, Bet v 1.1301, Bet v 1.1401, Bet v 1.1402, Bet v 1.1501, Bet v 1.1502, Bet v 1.1601, Bet v 1.1701, Bet v 1.1801, Bet v 1.1901, Bet v 1.2001, Bet v 1.2101, Bet v 1.2201, Bet v 1.2301, Bet v 1.2401, Bet v 1.2501, Bet v 1.2601, Bet v 1.2701, Bet v 1.2801, Bet v 1.2901, Bet v 1.3001, Bet v 1.3101, Bet v 2, Bet v 2.0101, Bet v 3, Bet v 3.0101, Bet v 4, Bet v 4.0101, Bet v 6, Bet v 6.0101, Bet v 6.0102, Bet v 7, Bet v 7.0101, Bet v 8, Bet v Глюканаза), Бета spp (Бета v 1, Бета v 1.0101, Бета v 2, Бета v 2.0101), Blattella spp (Bla g 1, Bla g 1.0101, Bla g 1.0102, Bla g 1.0103, Bla g 1.0201, Bla g 1.0202, Bla g 2, Bla g 2.0101, Bla g 2.0201, Bla g 36 кДа, Bla g 4, Bla g 4.0101, Bla g 4.0201, Bla g 5, Bla g 5.0101, Bla g 5.0201, Bla g 6, Bla g 6.0101, Bla g 6.0201, Bla g 6.0301, Bla g 7, Bla g 7.0101, Bla g 8, Bla g 8.0101, Bla g 9, Bla g Енолаза, Bla g GSTD1, Bla g RACK1, Bla g TPI, Bla g Трипсин, Bla g Вителлогенин), Blatta spp (Bla o 1, Bla o 7), Blomia spp (Blo t 1, Blo t 1.0101, Blo t 1.0201, Blo t 10, Blo t 10.0101, Blo t 10.0102, Blo t 11, Blo t 11.0101, Blo t 12, Blo t 12.0101, Blo t 12.0102, Blo t 13, Blo t 13.0101, Blo t 14, Blo t 15, Blo t 18, Blo t 19, Blo t 19.0101, Blo t 2, Blo t 2.0101, Blo t 2.0102, Blo t 2.0103, Blo t 20, Blo t 21, Blo t 21.0101, Blo t 3, Blo t 3.0101, Blo t 4, Blo t 4.0101, Blo t 5, Blo t 5.0101, Blo t 6, Blo t 6.0101, Blo t 7, Blo t 8, Blo t 9, Blo t HSP70), Bombus spp (Bom ar 4, Bom hy 4, Bom p 1, Bom p 1.0101, Bom p 2, Bom p 3, Bom p 4, Bom p 4.0101, Bom t 1, Bom t 1.0101, Bom t 4, Bom t 4.0101), Bombyx spp (Bomb m 1, Bomb m 1.0101, Bomb m 7, Bomb m 7.0101, Bomb m 7.0102, Bomb m 7.0103, Bomb m 7.0104, Bomb m 7.0105, Bomb m 7.0106), Boophilus spp (Boo m 1, Boo m 7, Boo m 7.0101), Bos spp (Bos d 2, Bos d 2.0101, Bos d 2.0102, Bos d 2.0103, Bos d 3, Bos d 3.0101, Bos d 4, Bos d 4.0101, Bos d 5, Bos d 5.0101, Bos d 5.0102, Bos d 6, Bos d 6 (MDA), Bos d 6.0101, Bos d 7, Bos d 7.0101, Bos d 8, Bos d 8 альфаS1, Bos d 8 альфаS2, Bos d 8 бета, Bos d 8 каппа, Bos d альфа2I, Bos d альфа2I.0101, Bos d Химозин, Bos d Фибрин, Bos d Желатин, Bos d HG, Bos d Инсулин, Bos d Лактоферрин, Bos d Лактопероксидаза, Bos d Миоглобин, Bos d OBP, Bos d OSCP, Bos d Фосвитин, Bos d PLA2, Bos d PRVB, Bos d Тромбин, Bos d TI, Bos gr ALA, Bos gr Миоглобин), Bothrops spp (Bot as 1, Bot at 1), Bouteloua spp (Bou g 1), Biting spp (Bov ov 1), Brama spp (Bra du 1), Brassica spp (Bra j 1, Bra j 1.0101, Bra n 1, Bra n 1.0101, Bra n 4, Bra n 7, Bra n 8, Bra n PG, Bra ni 8, Bra o 3, Bra o 3.0101, Bra r 1, Bra r 1.0101, Bra r 2, Bra r 2.0101, Bra r 3, Bra r 4, Bra r 7), Bromus spp (Bro a 1, Bro a 4), Brosme spp (Bro br 1), Bromus spp (Bro i 1, Bro i 5, Bro i 7), Brugia spp (Bru m 3, Bru m 3.0101, Bru m Bm33), Bubalus spp (Bub b ALA, Bub b BLG, Bub b Казеин, Bub b Казеин альфаS1, Bub b Казеин альфаS2, Bub b Казеин бета, Bub b Казеин каппа), Caenorhabditis spp (Cae b 3, Cae b 3.0101, Cae br 3, Cae br 3.0101, Cae e 3, Cae e 3.0101, Cae e 3.0102, Cae re 13, Cae re 13.0101), Cajanus spp (Caj c 1), Caligus spp (Cal cl 1, Cal cl 1.0101, Cal cl 1.0102), Calamus spp (Cal le 1), Callinectes spp (Cal s 2), Camelus spp (Cam d ALA, Cam d Казеин, Cam d Казеин альфаS1, Cam d Казеин альфаS2, Cam d Казеин бета, Cam d Казеин каппа), Camponotus spp (Cam fl 7, Cam fl 7.0101), Canis spp (Can f 1, Can f 1.0101, Can f 2, Can f 2.0101, Can f 3, Can f 3.0101, Can f 4, Can f 4.0101, Can f 5, Can f 5.0101, Can f 6, Can f 6.0101, Can f Feld1-подобный, Can f Homs2-подобный, Can f Фосвитин, Can f TCTP), Canthidermis spp (Can ma 1), Cancer spp (Can mg 2, Can p 1), Cannabis spp (Can s 3), Candida spp (Cand a 1, Cand a 1.0101, Cand a 3, Cand a 3.0101, Cand a CAAP, Cand a CyP, Cand a Енолаза, Cand a FPA, Cand a MnSOD, Cand a PGK, Cand b 2, Cand b 2.0101, Cand b FDH, Cand r Липаза), Capsicum spp (Cap a 1, Cap a 1.0101, Cap a 17 кДа, Cap a 2, Cap a 2.0101, Cap a 30 кДа, Cap a Глюканаза, Cap ch 17 кДа), Caprella spp (Cap e 1), Capra spp (Cap h ALA, Cap h BLG, Cap h Казеин, Cap h Казеин альфаS1, Cap h Казеин альфаS2, Cap h Казеин бета, Cap h Казеин каппа, Cap h GSA), Capitulum spp (Cap m 1), Carassius spp (Car au 1), Carpinus spp (Car b 1, Car b 1.0101, Car b 1.0102, Car b 1.0103, Car b 1.0104, Car b 1.0105, Car b 1.0106, Car b 1.0107, Car b 1.0108, Car b 1.0109, Car b 1.0110, Car b 1.0111, Car b 1.0112, Car b 1.0113, Car b 1.0201, Car b 1.0301, Car b 1.0302, Car b 2, Car b 4), Caranx spp (Car cr 1), Carya spp (Car i 1, Car i 1.0101, Car i 2, Car i 4, Car i 4.0101), Carcinus spp (Car ma 2), Caryota spp (Car mi 2), Carica spp (Car p 1, Car p Хитиназа, Car p Химопапаин, Car p Эндопептидаза), Castanea spp (Cas c 24 кДа, Cas s 1, Cas s 1.0101, Cas s 1.0102, Cas s 1.0103, Cas s 2, Cas s 5, Cas s 5.0101, Cas s 8, Cas s 8.0101, Cas s 9, Cas s 9.0101), Catharanthus spp (Cat r 1, Cat r 1.0101, Cat r 17 кДа, Cat r 2), Caulolatilus spp (Cau ch 1), Cavia spp (Cav p 1, Cav p 1.0101, Cav p 2, Cav p 2.0101, Cav p 3, Cav p 3.0101, Cav p Желатин, Cav p GSA), Centropristis spp (Cen s 1), Cephalopholis spp (Cep so 1), Charybdis spp (Cha f 1, Cha f 1.0101), Chaetodipterus spp (Cha fa 1), Chamaecyparis spp (Cha o 1, Cha o 1.0101, Cha o 2, Cha o 2.0101), Chenopodium spp (Che a 1, Che a 1.0101, Che a 2, Che a 2.0101, Che a 3, Che a 3.0101), Chironomus spp (Chi k 1, Chi k 10, Chi k 10.0101), Chinchilla spp (Chi l 21 кДа_a, Chi l 21 кДа_b), Chionoecetes spp (Chi o 1, Chi o 1.0101, Chi o 2, Chi o 4, Chi o 6, Chi o альфа_актин, Chi o SERCA), Chironomus spp (Chi t 1, Chi t 1.0101, Chi t 1.0201, Chi t 2, Chi t 2.0101, Chi t 2.0102, Chi t 3, Chi t 3.0101, Chi t 4, Chi t 4.0101, Chi t 5, Chi t 5.0101, Chi t 6, Chi t 6.0101, Chi t 6.0201, Chi t 7, Chi t 7.0101, Chi t 8, Chi t 8.0101, Chi t 9, Chi t 9.0101), Chlamys spp (Chl n 1), Chloephaga spp (Chl pi 1), Chortoglyphus spp (Cho a 10), Chrysomela spp (Chr tr 7, Chr tr 7.0101), Cicer spp (Cic a 2S Альбумин, Cic a Альбумин), Cichorium spp (Cic i 1), Cimex spp (Cim l Нитрофорин), Citrus spp (Cit l 1, Cit l 3, Cit l 3.0101), Citrullus spp (Cit la 2, Cit la MDH, Cit la TPI), Citrus spp (Cit r 3, Cit r 3.0101, Cit s 1, Cit s 1.0101, Cit s 2, Cit s 2.0101, Cit s 3, Cit s 3.0101, Cit s 3.0102, Cit s IFR), Cladosporium spp (Cla c 14, Cla c 14.0101, Cla c 9, Cla c 9.0101, Cla h 1, Cla h 10, Cla h 10.0101, Cla h 12, Cla h 12.0101, Cla h 2, Cla h 2.0101, Cla h 42 кДа, Cla h 5, Cla h 5.0101, Cla h 6, Cla h 6.0101, Cla h 7, Cla h 7.0101, Cla h 8, Cla h 8 CSP, Cla h 8.0101, Cla h 9, Cla h 9.0101, Cla h abH, Cla h GST, Cla h HCh1, Cla h HSP70, Cla h NTF2, Cla h TCTP), Clostridium spp (Clo hi Коллагеназа, Clo t Токсоид), Clupea spp (Clu h 1, Clu h 1.0101, Clu h 1.0201, Clu h 1.0301), Cocos spp (Coc n 2, Coc n 4, Coc n 5), Coccidioides spp (Coc po 8), Coffea spp (Cof a 1, Cof a 1.0101), Columba spp (Col l PSA), Coprinus spp (Cop c 1, Cop c 1.0101, Cop c 2, Cop c 2.0101, Cop c 3, Cop c 3.0101, Cop c 4, Cop c 5, Cop c 5.0101, Cop c 6, Cop c 7, Cop c 7.0101), Corylus spp (Cor a 1, Cor a 1.0101, Cor a 1.0102, Cor a 1.0103, Cor a 1.0104, Cor a 1.0201, Cor a 1.0301, Cor a 1.0401, Cor a 1.0402, Cor a 1.0403, Cor a 1.0404, Cor a 10, Cor a 10.0101, Cor a 11, Cor a 11.0101, Cor a 12, Cor a 12.0101, Cor a 13, Cor a 13.0101, Cor a 14, Cor a 14.0101, Cor a 2, Cor a 2.0101, Cor a 2.0102, Cor a 8, Cor a 8.0101, Cor a 9, Cor a 9.0101), Corynebacterium spp (Cor d Токсоид), Corylus spp (Cor he 1), Coryphaena spp (Cor hi 1), Coriandrum spp (Cor s 1, Cor s 11 кДа, Cor s 2), Cotoneaster spp (Cot l 3), Crangon spp (Cra c 1, Cra c 1.0101, Cra c 2, Cra c 2.0101, Cra c 4, Cra c 4.0101, Cra c 5, Cra c 5.0101, Cra c 6, Cra c 6.0101, Cra c 8, Cra c 8.0101), Crassostrea spp (Cra g 1), Cricetus spp (Cri c HSA), Crivellia spp (Cri pa 1), Crocus spp (Cro s 1, Cro s 1.0101, Cro s 2, Cro s 2.0101, Cro s 3, Cro s 3.01, Cro s 3.02), Cryptomeria spp (Cry j 1, Cry j 1.0101, Cry j 1.0102, Cry j 1.0103, Cry j 2, Cry j 2.0101, Cry j 2.0102, Cry j 3, Cry j 3.1, Cry j 3.2, Cry j 3.3, Cry j 3.4, Cry j 3.5, Cry j 3.6, Cry j 3.7, Cry j 3.8, Cry j 4, Cry j AP, Cry j Хитиназа, Cry j CPA9, Cry j IFR, Cry j LTP, Cry j P1-P2), Cryphonectria spp (Cry p AP), Ctenocephalides spp (Cte f 1, Cte f 1.0101, Cte f 2, Cte f 2.0101, Cte f 3, Cte f 3.0101), Ctenopharyngodon spp (Cte id 1), Cucumis spp (Cuc m 1, Cuc m 1.0101, Cuc m 2, Cuc m 2.0101, Cuc m 3, Cuc m 3.0101, Cuc m Lec17, Cuc m MDH), Cucurbita spp (Cuc ma 18 кДа, Cuc ma 2, Cuc p 2, Cuc p AscO), Cucumis spp (Cuc s 2), Culicoides spp (Cul n 1, Cul n 10, Cul n 11, Cul n 2, Cul n 3, Cul n 4, Cul n 5, Cul n 6, Cul n 7, Cul n 8, Cul n 9, Cul n HSP70), Culex spp (Cul q 28 кДа, Cul q 35 кДа, Cul q 7, Cul q 7.0101, Cul q 7.0102), Culicoides spp (Cul so 1), Cuminum spp (Cum c 1, Cum c 2), Cupressus spp (Cup a 1, Cup a 1.0101, Cup a 1.02, Cup a 2, Cup a 3, Cup a 4, Cup a 4.0101, Cup s 1, Cup s 1.0101, Cup s 1.0102, Cup s 1.0103, Cup s 1.0104, Cup s 1.0105, Cup s 3, Cup s 3.0101, Cup s 3.0102, Cup s 3.0103, Cup s 8), Cochliobolus spp (Cur l 1, Cur l 1.0101, Cur l 2, Cur l 2.0101, Cur l 3, Cur l 3.0101, Cur l 4, Cur l 4.0101, Cur l ADH, Cur l GST, Cur l MnSOD, Cur l Оризин, Cur l Trx, Cur l ZPS1), Cyanochen spp (Cya cy 1), Cynoscion spp (Cyn ar 1), Cynosurus spp (Cyn cr 1, Cyn cr 5), Cynodon spp (Cyn d 1, Cyn d 1.0101, Cyn d 1.0102, Cyn d 1.0103, Cyn d 1.0104, Cyn d 1.0105, Cyn d 1.0106, Cyn d 1.0107, Cyn d 1.0201, Cyn d 1.0202, Cyn d 1.0203, Cyn d 1.0204, Cyn d 10, Cyn d 11, Cyn d 12, Cyn d 12.0101, Cyn d 13, Cyn d 15, Cyn d 15.0101, Cyn d 2, Cyn d 22, Cyn d 22.0101, Cyn d 23, Cyn d 23.0101, Cyn d 24, Cyn d 24.0101, Cyn d 4, Cyn d 5, Cyn d 6, Cyn d 7, Cyn d 7.0101), Cynoscion spp (Cyn ne 1), Cynomys spp (Cyn sp Липокалин), Cyprinus spp (Cyp c 1, Cyp c 1.01, Cyp c 1.02), Daboia spp (Dab ru 1), Dactylis spp (Dac g 1, Dac g 1.01, Dac g 1.0101, Dac g 1.02, Dac g 12, Dac g 13, Dac g 2, Dac g 2.0101, Dac g 3, Dac g 3.0101, Dac g 4, Dac g 4.0101, Dac g 5, Dac g 5.0101, Dac g 7), Dama spp (Dam d CSA), Danio spp (Dan re 1, Dan re 2, Dan re альфа2I, Dan re CK), Dasyatis spp (Das ak 1, Das am 1, Das sa 1), Daucus spp (Dau c 1, Dau c 1.0101, Dau c 1.0102, Dau c 1.0103, Dau c 1.0104, Dau c 1.0105, Dau c 1.0201, Dau c 1.0301, Dau c 3, Dau c 4, Dau c 4.0101, Dau c CyP), Decapterus spp (Dec ru 1), Dendronephthya spp (Den n 1, Den n 1.0101), Dermatophagoides spp (Der f 1, Der f 1.0101, Der f 1.0102, Der f 1.0103, Der f 1.0104, Der f 1.0105, Der f 1.0106, Der f 1.0107, Der f 1.0108, Der f 1.0109, Der f 1.0110, Der f 10, Der f 10.0101, Der f 10.0102, Der f 11, Der f 11.0101, Der f 13, Der f 13.0101, Der f 14, Der f 14.0101, Der f 15, Der f 15.0101, Der f 16, Der f 16.0101, Der f 17, Der f 17.0101, Der f 18, Der f 18.0101, Der f 2, Der f 2.0101, Der f 2.0102, Der f 2.0103, Der f 2.0104, Der f 2.0105, Der f 2.0106, Der f 2.0107, Der f 2.0108, Der f 2.0109, Der f 2.0110, Der f 2.0111, Der f 2.0112, Der f 2.0113, Der f 2.0114, Der f 2.0115, Der f 2.0116, Der f 2.0117, Der f 20, Der f 21, Der f 22, Der f 22.0101, Der f 3, Der f 3.0101, Der f 4, Der f 5, Der f 6, Der f 6.0101, Der f 7, Der f 7.0101, Der f 8, Der f 9, Der f HSP70), Dermanyssus spp (Der g 10, Der g 10.0101), Dermatophagoides spp (Der m 1, Der m 1.0101, Der p 1, Der p 1.0101, Der p 1.0102, Der p 1.0103, Der p 1.0104, Der p 1.0105, Der p 1.0106, Der p 1.0107, Der p 1.0108, Der p 1.0109, Der p 1.0110, Der p 1.0111, Der p 1.0112, Der p 1.0113, Der p 1.0114, Der p 1.0115, Der p 1.0116, Der p 1.0117, Der p 1.0118, Der p 1.0119, Der p 1.0120, Der p 1.0121, Der p 1.0122, Der p 1.0123, Der p 1.0124, Der p 10, Der p 10.0101, Der p 10.0102, Der p 10.0103, Der p 11, Der p 11.0101, Der p 13, Der p 14, Der p 14.0101, Der p 15, Der p 18, Der p 2, Der p 2.0101, Der p 2.0102, Der p 2.0103, Der p 2.0104, Der p 2.0105, Der p 2.0106, Der p 2.0107, Der p 2.0108, Der p 2.0109, Der p 2.0110, Der p 2.0111, Der p 2.0112, Der p 2.0113, Der p 2.0114, Der p 2.0115, Der p 20, Der p 20.0101, Der p 21, Der p 21.0101, Der p 23, Der p 23.0101, Der p 3, Der p 3.0101, Der p 4, Der p 4.0101, Der p 5, Der p 5.0101, Der p 5.0102, Der p 6, Der p 6.0101, Der p 7, Der p 7.0101, Der p 8, Der p 8.0101, Der p 9, Der p 9.0101, Der p 9.0102, Der p P1-P2, Der p P2-P1, Der s 1, Der s 2, Der s 3), Dianthus spp (Dia c RIP), Dicranopteris spp (Dic l 2S Альбумин), Diospyros spp (Dio k 17 кДа, Dio k 4, Dio k IFR), Dioscorea spp (Dio p TSP), Diplodus spp (Dip ho 1), Distichlis spp (Dis s 1, Dis s 7), Ditrema spp (Dit te 1), Dolichovespula spp (Dol a 1, Dol a 2, Dol a 5, Dol a 5.0101), Dolichos spp (Dol b Агглютинин), Dolichovespula spp (Dol m 1, Dol m 1.0101, Dol m 1.02, Dol m 2, Dol m 2.0101, Dol m 5, Dol m 5.0101, Dol m 5.02), Drosophila spp (Dro an 7, Dro an 7.0101, Dro er 7, Dro er 7.0101, Dro er 7.0102, Dro gr 7, Dro gr 7.0101, Dro gr 7.0102, Dro m 7, Dro m 7.0101, Dro m 7.0102, Dro m 7.0103, Dro m 7.0104, Dro m 7.0105, Dro m 7.0106, Dro m 7.0107, Dro m 7.0108, Dro m 7.0109, Dro m 7.0110, Dro m 7.0111, Dro m 7.0112, Dro m 7.0113, Dro m 9, Dro m MnSOD, Dro mo 7, Dro mo 7.0101, Dro pp 7, Dro pp 7.0101, Dro se 7, Dro se 7.0101, Dro si 7, Dro si 7.0101, Dro si 7.0102, Dro vi 7, Dro vi 7.0101, Dro wi 7, Dro wi 7.0101, Dro y 7, Dro y 7.0101, Dro y 7.0102, Dro y 7.0103), Echium spp (Ech p Цитохром C), Elaeis spp (Ela g 2, Ela g Bd31 кДа), Elops spp (Elo sa 1), Embellisia spp (Emb a 1, Emb i 1, Emb nz 1, Emb t 1), Engraulis spp (Eng e 1), Enteroctopus spp (Ent d 1), Epinephelus spp (Epi bl 1, Epi co 1, Epi fl 1, Epi mc 1, Epi mo 1), Epicoccum spp (Epi p 1, Epi p 1.0101, Epi p 12 кДа, Epi p GST), Epinephelus spp (Epi po 1, Epi un 1), Equisetum spp (Equ a 17 кДа), Equus spp (Equ as 4, Equ as DSA, Equ bu 4, Equ c 1, Equ c 1.0101, Equ c 2, Equ c 2.0101, Equ c 2.0102, Equ c 3, Equ c 3.0101, Equ c 4, Equ c 4.0101, Equ c 5, Equ c 5.0101, Equ c ALA, Equ c BLG, Equ c Казеин, Equ c Казеин бета, Equ c Казеин каппа, Equ c PRVB, Equ he 4, Equ z ZSA), Erimacrus spp (Eri i 1, Eri i 1.0101, Eri i 1.0102), Eriocheir spp (Eri s 1, Eri s 1.0101, Eri s 2), Erwinia spp (Erw ch Аспарагиназа), Escherichia spp (Esc c Аспарагиназа, Esc c бета GAL), Esox spp (Eso l 1), Euphausia spp (Eup p 1, Eup p 1.0101), Euphasia spp (Eup s 1, Eup s 1.0101), Euroglyphus spp (Eur m 1, Eur m 1.0101, Eur m 1.0102, Eur m 1.0103, Eur m 10, Eur m 14, Eur m 14.0101, Eur m 2, Eur m 2.0101, Eur m 2.0102, Eur m 3, Eur m 3.0101, Eur m 4, Eur m 4.0101), Evynnis spp (Evy j 1), Fagopyrum spp (Fag e 1, Fag e 1.0101, Fag e 10 кДа, Fag e 19 кДа, Fag e 2, Fag e 2.0101, Fag e TI), Fagus spp (Fag s 1, Fag s 1.0101, Fag s 2, Fag s 4), Fagopyrum spp (Fag t 1, Fag t 10 кДа, Fag t 2, Fag t 2.0101), Felis spp (Fel d 1, Fel d 1.0101, Fel d 2, Fel d 2.0101, Fel d 3, Fel d 3.0101, Fel d 4, Fel d 4.0101, Fel d 5, Fel d 5.0101, Fel d 6, Fel d 6.0101, Fel d 7, Fel d 7.0101, Fel d 8, Fel d 8.0101, Fel d IgG), Fenneropenaeus spp (Fen c 1, Fen c 2, Fen me 1, Fen me 1.0101), Festuca spp (Fes e 1, Fes e 13, Fes e 4, Fes e 5, Fes e 7, Fes p 1, Fes p 13, Fes p 4, Fes p 4.0101, Fes p 5, Fes r 1, Fes r 5), Ficus spp (Fic c 17 кДа, Fic c 4, Fic c Фицин), Foeniculum spp (Foe v 1, Foe v 2), Forsythia spp (For s 1), Forcipomyia spp (For t 1, For t 1.0101, For t 2, For t 2.0101, For t 7, For t FPA, For t Миозин, For t TPI), Fragaria spp (Fra a 1, Fra a 1.0101, Fra a 3, Fra a 3.0101, Fra a 3.0102, Fra a 3.0201, Fra a 3.0202, Fra a 3.0203, Fra a 3.0204, Fra a 3.0301, Fra a 4, Fra a 4.0101, Fra c 1), Fraxinus spp (Fra e 1, Fra e 1.0101, Fra e 1.0102, Fra e 1.0201, Fra e 12, Fra e 2, Fra e 3, Fra e 9), Fragaria spp (Fra v 1), Fusarium spp (Fus c 1, Fus c 1.0101, Fus c 2, Fus c 2.0101, Fus c 3, Fus s 1, Fus s 45 кДа, Fus sp Липаза), Gadus spp (Gad c 1, Gad c 1.0101, Gad c APDH, Gad m 1, Gad m 1.0101, Gad m 1.0102, Gad m 1.0201, Gad m 1.0202, Gad m 45 кДа, Gad m Желатин, Gad ma 1), Gallus spp (Gal d 1, Gal d 1.0101, Gal d 2, Gal d 2.0101, Gal d 3, Gal d 3.0101, Gal d 4, Gal d 4.0101, Gal d 5, Gal d 5.0101, Gal d 6, Gal d 6.0101, Gal d Apo I, Gal d Apo VI, Gal d GPI, Gal d HG, Gal d IgY, Gal d L-PGDS, Gal d Овомуцин, Gal d Фосвитин, Gal d PRVB, Gal la 4), Galleria spp (Gal m 18 кДа, Gal m 24 кДа), Gallus spp (Gal so 4), Gammarus spp (Gam s TM), Gelonium spp (Gel m RIP), Geothelphusa spp (Geo de 1), Glossina spp (Glo m 5, Glo m 5.0101, Glo m 7, Glo m 7.0101, Glo m 7.0102, Glo m 7.0103), Glycine spp (Gly a Bd30K, Gly ar Bd30K, Gly ca Bd30K, Gly cl Bd30K, Gly cu Bd30K, Gly cy Bd30K), Glycyphagus spp (Gly d 10, Gly d 10.0101, Gly d 13, Gly d 2, Gly d 2.0101, Gly d 2.0201, Gly d 2.03, Gly d 2/Lep d 2 L1, Gly d 2/Lep d 2 L2, Gly d 2/Lep d 2 L3, Gly d 2/Lep d 2 L4, Gly d 2/Lep d 2 R1, Gly d 2/Lep d 2 R2, Gly d 2/Lep d 2 R3, Gly d 2/Lep d 2 R4, Gly d 2/Lep d 2 R5, Gly d 20, Gly d 3, Gly d 5, Gly d 5.01, Gly d 5.02, Gly d 7, Gly d 8), Glycine spp (Gly f Bd30K, Gly l Bd30K, Gly m 1, Gly m 1.0101, Gly m 1.0102, Gly m 2, Gly m 2.0101, Gly m 2S Альбумин, Gly m 3, Gly m 3.0101, Gly m 3.0102, Gly m 39 кДа, Gly m 4, Gly m 4.0101, Gly m 5, Gly m 5.0101, Gly m 5.0201, Gly m 5.0301, Gly m 5.0302, Gly m 50 кДа, Gly m 6, Gly m 6.0101, Gly m 6.0201, Gly m 6.0301, Gly m 6.0401, Gly m 6.0501, Gly m 68 кДа, Gly m Агглютинин, Gly m Bd28K, Gly m Bd30K, Gly m Bd60K, Gly m CPI, Gly m EAP, Gly m TI, Gly mi Bd30K, Gly s Bd30K, Gly t Bd30K, Gly to Bd30K), Gossypium spp (Gos h Вицилин), Haemophilus spp (Hae in P6), Haemaphysalis spp (Hae l 7, Hae l 7.0101, Hae q 7, Hae q 7.0101), Haliotis spp (Hal a 1, Hal d 1, Hal di 1, Hal di PM, Hal m 1, Hal m 1.0101, Hal r 1, Hal r 49 кДа, Hal ru 1), Harmonia spp (Har a 1, Har a 1.0101, Har a 2, Har a 2.0101), Harpegnathos spp (Har sa 7, Har sa 7.0101, Har sa 7.0102), Helianthus spp (Hel a 1, Hel a 1.0101, Hel a 2, Hel a 2.0101, Hel a 2S Альбумин, Hel a 3, Hel a 3.0101, Hel a 4), Helix spp (Hel ap 1, Hel as 1, Hel as 1.0101), Heligmosomoides spp (Hel p 3, Hel p 3.0101), Helianthus spp (Hel tu 1), Hemanthias spp (Hem le 1), Hemifusus spp (Hem t 1), Heterodera spp (Het g 3, Het g 3.0101), Hevea spp (Hev b 1, Hev b 1.0101, Hev b 10, Hev b 10.0101, Hev b 10.0102, Hev b 10.0103, Hev b 11, Hev b 11.0101, Hev b 11.0102, Hev b 12, Hev b 12.0101, Hev b 13, Hev b 13.0101, Hev b 14, Hev b 14.0101, Hev b 2, Hev b 2.0101, Hev b 3, Hev b 3.0101, Hev b 4, Hev b 4.0101, Hev b 5, Hev b 5.0101, Hev b 6, Hev b 6.01, Hev b 6.02, Hev b 6.0202, Hev b 6.03, Hev b 7, Hev b 7.01, Hev b 7.02, Hev b 7.D2, Hev b 7.S2, Hev b 8, Hev b 8.0101, Hev b 8.0102, Hev b 8.0201, Hev b 8.0202, Hev b 8.0203, Hev b 8.0204, Hev b 9, Hev b 9.0101, Hev b Цитрат-связывающий белок, Hev b GAPDH, Hev b HSP80, Hev b IFR, Hev b Субъединица протеосомы, Hev b Ротамаза, Hev b SPI, Hev b Trx, Hev b UDPGP), Hexagrammos spp (Hex ot 1), Hippoglossus spp (Hip h 1), Hippoglossoides spp (Hip pl 1), Hippoglossus spp (Hip st 1), Hirudo spp (Hir me Гирудин), Holcus spp (Hol l 1, Hol l 1.0101, Hol l 1.0102, Hol l 2, Hol l 4, Hol l 5, Hol l 5.0101, Hol l 5.0201), Holocnemus spp (Hol pl 9, Hol pl Гемоцианин), Homarus spp (Hom a 1, Hom a 1.0101, Hom a 1.0102, Hom a 1.0103, Hom a 3, Hom a 3.0101, Hom a 4, Hom a 6, Hom a 6.0101, Hom g 1, Hom g 2), Homo spp (Hom s 1, Hom s 1.0101, Hom s 2, Hom s 2.0101, Hom s 3, Hom s 3.0101, Hom s 4, Hom s 4.0101, Hom s 5, Hom s 5.0101, Hom s AAT, Hom s ACTH, Hom s Адалимумаб;, Hom s ALA, Hom s альфа_актин, Hom s альфа-Галактозидаза, Hom s APDH, Hom s Арилсульфатаза B, Hom s Казеин, Hom s CyP A, Hom s CyP B, Hom s CyP C, Hom s DSF70, Hom s DSG3, Hom s eIF6, Hom s Этанерцепт, Hom s Фактор IX, Hom s Фактор VII, Hom s Фактор VIII, Hom s G-CSF, Hom s Глюкоцереброзидаза, Hom s Глюкозидаза, Hom s HLA-DR-альфа, Hom s HSA, Hom s Идуронидаза, Hom s Идурсульфаза, Hom s IgA, Hom s Инсулин, Hom s Лактоферрин, Hom s Ламинин гамма_2, Hom s MnSOD, Hom s Окситоцин, Hom s P2, Hom s Фосвитин, Hom s Профилин, Hom s PSA, Hom s RP1, Hom s TCTP, Hom s TL, Hom s TPA, Hom s TPO, Hom s Трансальдолаза, Hom s Trx, Hom s Тубулин-альфа, Hom s/Mus m Базиликсимаб, Hom s/Mus m Цетуксимаб, Hom s/Mus m Цетуксимаб (Gal-Gal), Hom s/Mus m Инфликсимаб, Hom s/Mus m Натализумаб, Hom s/Mus m Омализумаб, Hom s/Mus m Паливизумаб, Hom s/Mus m Ритуксимаб, Hom s/Mus m Тоцилизумаб, Hom s/Mus m Трастузумаб), Hoplostethus spp (Hop a 1), Hordeum spp (Hor v 1, Hor v 12, Hor v 12.0101, Hor v 13, Hor v 14, Hor v 15, Hor v 15.0101, Hor v 16, Hor v 16.0101, Hor v 17, Hor v 17.0101, Hor v 18 кДа, Hor v 2, Hor v 21, Hor v 21.0101, Hor v 28, Hor v 33, Hor v 4, Hor v 5, Hor v 5.0101, Hor v BDAI, Hor v BTI), Humicola spp (Hum in Целлюлаза), Humulus spp (Hum j 1, Hum j 1.0101, Hum j 10 кДа, Hum j 2), Huso spp (Hus h 1), Hylocereus spp (Hyl un LTP), Hymenocephalus spp (Hym st 1), Hyperoglyphe spp (Hyp by 1), Hypophthalmichthys spp (Hyp mo 1), Hypophthalmichthy spp (Hyp no 1), Ictalurus spp (Ict fu 1, Ict p 1), Imperata spp (Imp c 4, Imp c 5, Imp c VIIIe1), Ixodes spp (Ixo r 2, Ixo sc 7, Ixo sc 7.0101), Jasus spp (Jas la 1, Jas la 1.0101, Jas la 1.0102), Juglans spp (Jug ca 1, Jug ca 2, Jug ci 1, Jug ci 2, Jug n 1, Jug n 1.0101, Jug n 2, Jug n 2.0101, Jug r 1, Jug r 1.0101, Jug r 2, Jug r 2.0101, Jug r 3, Jug r 3.0101, Jug r 4, Jug r 4.0101, Jug r 5), Juniperus spp (Jun a 1, Jun a 1.0101, Jun a 1.0102, Jun a 2, Jun a 2.0101, Jun a 3, Jun a 3.0101, Jun c 1, Jun o 1, Jun o 4, Jun o 4.0101, Jun r 3, Jun r 3.1, Jun r 3.2, Jun v 1, Jun v 1.0101, Jun v 1.0102, Jun v 3, Jun v 3.0101, Jun v 3.0102, Jun v 4), Katsuwonus spp (Kat p 1), Kyphosus spp (Kyp se 1), Lachnolaimus spp (Lac ma 1), Lachesis spp (Lac mu 1), Lactuca spp (Lac s 1, Lac s 1.0101), Lagocephalus spp (Lag la 1), Larus spp (Lar a 1, Lar a 2, Lar a 3), Larimichthys spp (Lar po 1), Lates spp (Lat c 1), Lateolabrax spp (Lat ja 1), Lathyrus spp (Lat oc Агглютинин), Leiostomus spp (Lei xa 1), Lens spp (Len c 1, Len c 1.0101, Len c 1.0102, Len c 1.0103, Len c 2, Len c 2.0101, Len c 3, Len c 3.0101, Len c Агглютинин), Leopardus spp (Leo p 1), Lepidoglyphus spp (Lep d 10, Lep d 10.0101, Lep d 12, Lep d 13, Lep d 13.0101, Lep d 2, Lep d 2.0101, Lep d 2.0102, Lep d 2.0201, Lep d 2.0202, Lep d 3, Lep d 39 кДа, Lep d 5, Lep d 5.0101, Lep d 5.0102, Lep d 5.0103, Lep d 7, Lep d 7.0101, Lep d 8, Lep d альфа Тубулин), Lepomis spp (Lep gi 1), Leptomelanosoma spp (Lep i 1), Lepomis spp (Lep ma 1), Lepisma spp (Lep s 1, Lep s 1.0101, Lep s 1.0102), Lepeophtheirus spp (Lep sa 1, Lep sa 1.0101, Lep sa 1.0102, Lep sa 1.0103), Leptailurus spp (Lep se 1), Lepidorhombus spp (Lep w 1, Lep w 1.0101), Lethocerus spp (Let in 7, Let in 7.0101, Let in 7.0102), Leuciscus spp (Leu ce 1), Lewia spp (Lew in 1), Ligustrum spp (Lig v 1, Lig v 1.0101, Lig v 1.0102, Lig v 2), Lilium spp (Lil l 2, Lil l PG), Limanda spp (Lim fe 1), Limnonectes spp (Lim m 1), Limulus spp (Lim p 1, Lim p 1.0101, Lim p 2, Lim p LPA), Liposcelis spp (Lip b 1, Lip b 1.0101), Litchi spp (Lit c 1, Lit c 1.0101, Lit c IFR, Lit c TPI), Lithobates spp (Lit ca 1), Litopenaeus spp (Lit se 1, Lit v 1, Lit v 1.0101, Lit v 2, Lit v 2.0101, Lit v 3, Lit v 3.0101, Lit v 4, Lit v 4.0101), Filiaria spp (Loa lo 3, Loa lo 3.0101), Lobotes spp (Lob su 1), Locusta spp (Loc m 7, Loc m 7.0101), Loligo spp (Lol b 1, Lol e 1), Lolium spp (Lol m 2, Lol m 5, Lol p 1, Lol p 1.0101, Lol p 1.0102, Lol p 1.0103, Lol p 10, Lol p 11, Lol p 11.0101, Lol p 12, Lol p 13, Lol p 2, Lol p 2.0101, Lol p 3, Lol p 3.0101, Lol p 4, Lol p 4.0101, Lol p 5, Lol p 5.0101, Lol p 5.0102, Lol p 7, Lol p CyP, Lol p FT, Lol p Легумин), Lonomia spp (Lon o 7, Lon o 7.0101), Lophodytes spp (Lop cu 1), Lophonetta spp (Lop sp 1), Lupinus spp (Lup a 1, Lup a альфа_Конглютин, Lup a дельта_Конглютин, Lup a гамма_Конглютин, Lup an 1, Lup an 1.0101, Lup an альфа_Конглютин, Lup an дельта_Конглютин, Lup an гамма_Конглютин, Lup l 17 кДа), Lutjanus spp (Lut a 1, Lut c 1, Lut cy 1, Lut gr 1, Lut gu 1, Lut jo 1), Lutraria spp (Lut p 1), Lutjanus spp (Lut pu 1, Lut sy 1), Lycopersicon spp (Lyc e 1, Lyc e 1.0101, Lyc e 11S Глобулин, Lyc e 2, Lyc e 2.0101, Lyc e 2.0102, Lyc e 3, Lyc e 3.0101, Lyc e 4, Lyc e 4.0101, Lyc e ARP60S, Lyc e Хитиназа, Lyc e Глюканаза, Lyc e Пероксидаза, Lyc e PG, Lyc e PME, Lyc e PR23, Lyc e Вицилин), Maconellicoccus spp (Mac h 7, Mac h 7.0101), Macruronus spp (Mac ma 1, Mac n 1), Maclura spp (Mac po 17 кДа), Macrobrachium spp (Mac ro 1, Mac ro 1.0101, Mac ro Гемоцианин), Macropus spp (Macr s Желатин), Malus spp (Mal d 1, Mal d 1.0101, Mal d 1.0102, Mal d 1.0103, Mal d 1.0104, Mal d 1.0105, Mal d 1.0106, Mal d 1.0107, Mal d 1.0108, Mal d 1.0109, Mal d 1.0201, Mal d 1.0202, Mal d 1.0203, Mal d 1.0204, Mal d 1.0205, Mal d 1.0206, Mal d 1.0207, Mal d 1.0208, Mal d 1.0301, Mal d 1.0302, Mal d 1.0303, Mal d 1.0304, Mal d 1.0401, Mal d 1.0402, Mal d 1.0403, Mal d 2, Mal d 2.0101, Mal d 3, Mal d 3.0101, Mal d 3.0102, Mal d 3.0201, Mal d 3.0202, Mal d 3.0203, Mal d 4, Mal d 4.0101, Mal d 4.0102, Mal d 4.0201, Mal d 4.0202, Mal d 4.0301, Mal d 4.0302), Malpighia spp (Mal g 4, Mal g Гевеин), Malus spp (Mal p 1), Malassezia spp (Mala f 2, Mala f 2.0101, Mala f 3, Mala f 3.0101, Mala f 4, Mala f 4.0101, Mala g 10, Mala s 1, Mala s 1.0101, Mala s 10, Mala s 10.0101, Mala s 11, Mala s 11.0101, Mala s 12, Mala s 12.0101, Mala s 13, Mala s 13.0101, Mala s 5, Mala s 5.0101, Mala s 6, Mala s 6.0101, Mala s 7, Mala s 7.0101, Mala s 8, Mala s 8.0101, Mala s 9, Mala s 9.0101), Manihot spp (Man e 5, Man e 5.0101, Man e FPA, Man e GAPDH), Mangifera spp (Man i 1, Man i 14 кДа, Man i 2, Man i 3, Man i 3.01, Man i 3.02, Man i Хитиназа), Marsupenaeus spp (Mar j 1, Mar j 1.0101, Mar j 2, Mar j 4), Matricaria spp (Mat c 17 кД), Mecopoda spp (Mec e 7), Megalobrama spp (Meg am 2, Meg am CK), Megathura spp (Meg c Гемоцианин), Megalops spp (Meg sp 1), Melanogrammus spp (Mel a 1), Meleagris spp (Mel g 1, Mel g 2, Mel g 3, Mel g PRVB, Mel g TSA), Melicertus spp (Mel l 1), Menticirrhus spp (Men am 1), Mercurialis spp (Mer a 1, Mer a 1.0101), Merluccius spp (Mer ap 1, Mer au 1, Mer bi 1, Mer ca 1, Mer ga 1, Mer hu 1), Merlangius spp (Mer me 1), Merluccius spp (Mer mr 1, Mer pa 1, Mer po 1, Mer pr 1, Mer se 1), Meriones spp (Mer un 23 кДа), Metarhizium spp (Met a 30), Metapenaeopsis spp (Met ba 1), Metapenaeus spp (Met e 1, Met e 1.0101, Met e 2), Metasequoia spp (Met gl 2), Metapenaeus spp (Met j 1, Met j 2), Metanephrops spp (Met ja 1), Metapenaeopsis spp (Met la 1), Metanephrops spp (Met t 2), Micromesistius spp (Mic po 1), Micropogonias spp (Mic un 1), Mimachlamys spp (Mim n 1), Momordica spp (Mom c RIP), Morus spp (Mor a 17 кДа, Mor a 4), Morone spp (Mor am 1), Morus spp (Mor n 3, Mor n 3.0101), Morone spp (Mor sa 1, Mor sc 1), Mugil spp (Mug c 1), Muraenolepis spp (Mur mi 1), Musa spp (Mus a 1, Mus a 1.0101, Mus a 2, Mus a 2.0101, Mus a 3, Mus a 3.0101, Mus a 4, Mus a 4.0101, Mus a 5, Mus a 5.0101, Mus a 5.0102), Mus spp (Mus m 1, Mus m 1.0101, Mus m 1.0102, Mus m 2, Mus m Желатин, Mus m IgG, Mus m MSA, Mus m Муромонаб, Mus m Фосвитин), Mustela spp (Mus p 17 кДа), Musa spp (Mus xp 1, Mus xp 2, Mus xp 5), Mycteroperca spp (Myc bo 1, Myc mi 1, Myc ph 1), Myceliophthora spp (Myc sp Лакказа), Myrmecia spp (Myr p 1, Myr p 1.0101, Myr p 2, Myr p 2.0101, Myr p 2.0102, Myr p 3, Myr p 3.0101), Mytilus spp (Myt e 1, Myt g 1, Myt g PM), Myzus spp (Myz p 7, Myz p 7.0101), Nemorhedus spp (Nae go Hya), Necator spp (Nec a Кальретикулин), Nemipterus spp (Nem vi 1), Neosartorya spp (Neo fi 1, Neo fi 22), Neochen spp (Neo ju 1), Neoscona spp (Neo n 7, Neo n 7.0101), Nephelium spp (Nep l GAPDH), Nephrops spp (Nep n 1, Nep n DF9), Neptunea spp (Nep po 1, Nep po 1.0101), Nicotiana spp (Nic t 8, Nic t Осмотин, Nic t Виллин), Nimbya spp (Nim c 1, Nim s 1), Nippostrongylus spp (Nip b Ag1), Nycticebus spp (Nyc c 1), Octopus spp (Oct f 1, Oct l 1, Oct v 1, Oct v 1.0101, Oct v PM), Ocyurus spp (Ocy ch 1), Olea spp (Ole e 1, Ole e 1.0101, Ole e 1.0102, Ole e 1.0103, Ole e 1.0104, Ole e 1.0105, Ole e 1.0106, Ole e 1.0107, Ole e 10, Ole e 10.0101, Ole e 11, Ole e 11.0101, Ole e 11.0102, Ole e 12, Ole e 13, Ole e 2, Ole e 2.0101, Ole e 3, Ole e 3.0101, Ole e 36 кДа, Ole e 4, Ole e 4.0101, Ole e 5, Ole e 5.0101, Ole e 6, Ole e 6.0101, Ole e 7, Ole e 7.0101, Ole e 8, Ole e 8.0101, Ole e 9, Ole e 9.0101), Ommastrephes spp (Omm b 1, Omm b 1.0101), Oncorhynchus spp (Onc ke 1, Onc ke 18 кДа, Onc ke альфа2I, Onc ke Вителлогенин, Onc m 1, Onc m 1.0101, Onc m 1.0201, Onc m альфа2I, Onc m Протамин, Onc m Вителлогенин, Onc ma 1, Onc ma FPA, Onc ma FSA, Onc ma TPI, Onc n 1), Onchocerca spp (Onc o 3, Onc o 3.0101), Oncorhynchus spp (Onc ts 1), Onchocerca spp (Onc v 3, Onc v 3.0101), Oratosquilla spp (Ora o 1, Ora o 1.0101), Oreochromis spp (Ore a 1, Ore mo 1, Ore mo 2, Ore mo FPA, Ore mo SCAF7145, Ore ni 1, Ore ni 18 кДа, Ore ni 45 кДа), Ornithonyssus spp (Orn sy 10, Orn sy 10.0101, Orn sy 10.0102), Oryctolagus spp (Ory c 1, Ory c 1.0101, Ory c 2, Ory c Казеин, Ory c Фосвитин, Ory c RSA), Oryza spp (Ory s 1, Ory s 1.0101, Ory s 11, Ory s 12, Ory s 12.0101, Ory s 13, Ory s 14, Ory s 17 кДа, Ory s 19 кДа, Ory s 2, Ory s 23, Ory s 3, Ory s 7, Ory s aA_TI, Ory s GLP52, Ory s GLP63, Ory s Глиоксалаза I, Ory s NRA), Ostrya spp (Ost c 1, Ost c 1.0101), Ovis spp (Ovi a ALA, Ovi a BLG, Ovi a Казеин, Ovi a Казеин альфаS1, Ovi a Казеин альфаS2, Ovi a Казеин бета, Ovi a Казеин каппа, Ovi a Фосвитин, Ovi a SSA), Pachycondyla spp (Pac c 3), Pagrus spp (Pag m 1, Pag pa 1), Pampus spp (Pam ar 1, Pam c 1), Pandalus spp (Pan b 1, Pan b 1.0101), Pangasius spp (Pan bo 1), Pandalus spp (Pan e 1, Pan e 1.0101, Pan e 4), Panulirus spp (Pan h 1, Pan hy 1), Pangasius spp (Pan hy 18 кДа, Pan hy 45 кДа), Panulirus spp (Pan j 1), Panthera spp (Pan l 1, Pan o 1, Pan p 1), Panulirus spp (Pan s 1, Pan s 1.0101), Panthera spp (Pan t 1), Pan spp (Pan tr TCTP), Papaver spp (Pap s 17 кДа, Pap s 2, Pap s 34 кД), Papilio spp (Pap xu 7, Pap xu 7.0101, Pap xu 7.0102), Paralicаhthys spp (Par a 1), Parasilurus spp (Par as 1, Par c 1), Paralithodes spp (Par c 1.0101, Par c 1.0102, Par f 1), Parthenium spp (Par h 1), Parietaria spp (Par j 1, Par j 1.0101, Par j 1.0102, Par j 1.0103, Par j 1.0201, Par j 2, Par j 2.0101, Par j 2.0102, Par j 3, Par j 3.0101, Par j 3.0102, Par j 4, Par j 4.0101, Par j J1-J2), Paralichthys spp (Par le 1), Parietaria spp (Par m 1, Par o 1, Par o 1.0101), Paralichthys spp (Par ol 1, Par ol альфа2I), Parahucho spp (Par pe Вителлогенин), Passiflora spp (Pas e Хитиназа, Pas e Гевеин), Paspalum spp (Pas n 1, Pas n 1.0101, Pas n 13), Patinopecten spp (Pat y 1), Pediculus spp (Ped h 7, Ped h 7.0101), Penaeus spp (Pen a 1, Pen a 1.0101, Pen a 1.0102, Pen a 1.0102 (103-117), Pen a 1.0102 (109-123), Pen a 1.0102 (1-15), Pen a 1.0102 (115-129), Pen a 1.0102 (121-135), Pen a 1.0102 (127-141), Pen a 1.0102 (13-27), Pen a 1.0102 (133-147), Pen a 1.0102 (139-153), Pen a 1.0102 (145-159)), Farfantepenaeus spp (Pen a 1.0102 (151-165)), Penaeus spp (Pen a 1.0102 (157-171), Pen a 1.0102 (163-177), Pen a 1.0102 (169-183), Pen a 1.0102 (175-189), Pen a 1.0102 (181-195), Pen a 1.0102 (187-201), Pen a 1.0102 (193-207), Pen a 1.0102 (19-33), Pen a 1.0102 (199-213), Pen a 1.0102 (205-219), Pen a 1.0102 (211-225), Pen a 1.0102 (217-231), Pen a 1.0102 (223-237), Pen a 1.0102 (229-243)), Farfantepenaeus spp (Pen a 1.0102 (235-249)), Penaeus spp (Pen a 1.0102 (241-255), Pen a 1.0102 (247-261), Pen a 1.0102 (253-267), Pen a 1.0102 (25-39), Pen a 1.0102 (259-273), Pen a 1.0102 (265-279), Pen a 1.0102 (270-284), Pen a 1.0102 (31-45), Pen a 1.0102 (37-51), Pen a 1.0102 (43-57), Pen a 1.0102 (49-63)), Farfantepenaeus spp (Pen a 1.0102 (55-69)), Penaeus spp (Pen a 1.0102 (61-75), Pen a 1.0102 (67-81), Pen a 1.0102 (7-21), Pen a 1.0102 (73-87), Pen a 1.0102 (79-93), Pen a 1.0102 (85-99), Pen a 1.0102 (91-105), Pen a 1.0102 (97-111), Pen a 1.0103), Penicillium spp (Pen b 13, Pen b 13.0101, Pen b 26, Pen b 26.0101, Pen c 1, Pen c 13, Pen c 13.0101, Pen c 18, Pen c 19, Pen c 19.0101, Pen c 2, Pen c 22, Pen c 22.0101, Pen c 24, Pen c 24.0101, Pen c 3, Pen c 3.0101, Pen c 30, Pen c 30.0101, Pen c 32, Pen c 32.0101, Pen c MnSOD, Pen ch 13, Pen ch 13.0101, Pen ch 18, Pen ch 18.0101, Pen ch 20, Pen ch 20.0101, Pen ch 31, Pen ch 31.0101, Pen ch 33, Pen ch 33.0101, Pen ch 35, Pen ch 35.0101, Pen ch MnSOD), Penaeus spp (Pen i 1, Pen i 1.0101, Pen m 1, Pen m 1.0101, Pen m 1.0102, Pen m 2, Pen m 2.0101, Pen m 3, Pen m 3.0101, Pen m 4, Pen m 4.0101, Pen m 6, Pen m 6.0101), Penicillium spp (Pen o 18, Pen o 18.0101), Penaeus spp (Pena o 1, Pena o 1.0101), Periplaneta spp (Per a 1, Per a 1.0101, Per a 1.0102, Per a 1.0103, Per a 1.0104, Per a 1.0105, Per a 1.0201, Per a 10, Per a 10.0101, Per a 2, Per a 3, Per a 3.0101, Per a 3.0201, Per a 3.0202, Per a 3.0203, Per a 4, Per a 5, Per a 6, Per a 6.0101, Per a 7, Per a 7.0101, Per a 7.0102, Per a 7.0103, Per a 9, Per a 9.0101, Per a Катепсин, Per a FABP, Per a Трипсин, Per f 1, Per f 7, Per f 7.0101), Perna spp (Per v 1), Persea spp (Pers a 1, Pers a 1.0101, Pers a 4), Petroselinum spp (Pet c 1, Pet c 2, Pet c 3), Phalaris spp (Pha a 1, Pha a 1.0101, Pha a 5, Pha a 5.0101, Pha a 5.02, Pha a 5.03, Pha a 5.04), Phaseolus spp (Pha v 3, Pha v 3.0101, Pha v 3.0201, Pha v aAI, Pha v aAI.0101, Pha v Хитиназа, Pha v PHA, Pha v Фазеолин), Phleum spp (Phl p 1, Phl p 1.0101, Phl p 1.0102, Phl p 11, Phl p 11.0101, Phl p 12, Phl p 12.0101, Phl p 12.0102, Phl p 12.0103, Phl p 13, Phl p 13.0101, Phl p 2, Phl p 2.0101, Phl p 3, Phl p 3.0101, Phl p 3.0102, Phl p 4, Phl p 4.0101, Phl p 4.0102, Phl p 4.0201, Phl p 4.0202, Phl p 4.0203, Phl p 4.0204, Phl p 5, Phl p 5.0101, Phl p 5.0102, Phl p 5.0103, Phl p 5.0104, Phl p 5.0105, Phl p 5.0106, Phl p 5.0107, Phl p 5.0108, Phl p 5.0109, Phl p 5.0201, Phl p 5.0202, Phl p 5.0203, Phl p 5.0204, Phl p 5.0205, Phl p 5.0206, Phl p 5.0207, Phl p 6, Phl p 6.0101, Phl p 6.0102, Phl p 7, Phl p 7.0101, Phl p P1-P2-P5-P6, Phl p P2-P6, Phl p P5-P1, Phl p P6-P2), Phoenix spp (Pho d 2, Pho d 2.0101, Pho d 40 кДа, Pho d 90 кДа), Phodopus spp (Pho s 21 кД), Phoma spp (Pho t 1), Phragmites spp (Phr a 1, Phr a 12, Phr a 13, Phr a 4, Phr a 5), Phytolacca spp (Phy a RIP), Pimpinella spp (Pim a 1, Pim a 2), Pinna spp (Pin a 1), Piper spp (Pip n 14 кДа, Pip n 28 кДа), Pisum spp (Pis s 1, Pis s 1.0101, Pis s 1.0102, Pis s 2, Pis s 2.0101, Pis s 5, Pis s Агглютинин, Pis s Альбумин), Pistacia spp (Pis v 1, Pis v 1.0101, Pis v 2, Pis v 2.0101, Pis v 2.0201, Pis v 3, Pis v 3.0101, Pis v 4, Pis v 4.0101, Pis v 5, Pis v 5.0101), Platanus spp (Pla a 1, Pla a 1.0101, Pla a 2, Pla a 2.0101, Pla a 3, Pla a 3.0101, Pla a 8), Platichthys spp (Pla f 1), Plantago spp (Pla l 1, Pla l 1.0101, Pla l 1.0102, Pla l 1.0103, Pla l Цитохром C), Platanus spp (Pla oc 1, Pla or 1, Pla or 1.0101, Pla or 2, Pla or 2.0101, Pla or 3, Pla or 3.0101, Pla or 4, Pla or CyP, Pla r 1), Plectropomus spp (Ple ar 1), Pleospora spp (Ple h 1), Plectropomus spp (Ple le 1), Plodia spp (Plo i 1, Plo i 1.0101, Plo i 2, Plo i 2.0101), Poa spp (Poa p 1, Poa p 1.0101, Poa p 10, Poa p 12, Poa p 13, Poa p 2, Poa p 4, Poa p 5, Poa p 5.0101, Poa p 6, Poa p 7), Polistes spp (Pol a 1, Pol a 1.0101, Pol a 2, Pol a 2.0101, Pol a 5, Pol a 5.0101, Pol d 1, Pol d 1.0101, Pol d 1.0102, Pol d 1.0103, Pol d 1.0104, Pol d 4, Pol d 4.0101, Pol d 5, Pol d 5.0101, Pol e 1, Pol e 1.0101, Pol e 2, Pol e 4, Pol e 4.0101, Pol e 5, Pol e 5.0101, Pol f 5, Pol f 5.0101, Pol g 1, Pol g 1.0101, Pol g 2, Pol g 4, Pol g 5, Pol g 5.0101, Pol he MLT, Pol m 5, Pol m 5.0101), Polypedilum spp (Pol n 1), Pollicipes spp (Pol po 1), Pollachius spp (Pol vi 1), Polybia spp (Poly p 1, Poly p 1.0101, Poly p 2, Poly p 5, Poly s 5, Poly s 5.0101), Pomatomus spp (Pom sa 1), Pongo spp (Pon ab HSA), Pontastacus spp (Pon l 4, Pon l 4.0101, Pon l 7, Pon l 7.0101), Portunus spp (Por s 1, Por s 1.0101, Por s 1.0102, Por tr 1, Por tr 1.0101), Protortonia spp (Pro ca 38 кДа), Procumbarus spp (Pro cl 1, Pro cl 1.0101, Pro cl 21 кДа), Prosopis spp (Pro j 20 кДа), Prunus spp (Pru ar 1, Pru ar 1.0101, Pru ar 3, Pru ar 3.0101, Pru av 1, Pru av 1.0101, Pru av 1.0201, Pru av 1.0202, Pru av 1.0203, Pru av 2, Pru av 2.0101, Pru av 3, Pru av 3.0101, Pru av 4, Pru av 4.0101, Pru c 1, Pru d 1, Pru d 2, Pru d 3, Pru d 3.0101, Pru d 4, Pru du 1, Pru du 2, Pru du 2S Альбумин, Pru du 3, Pru du 3.0101, Pru du 4, Pru du 4.0101, Pru du 4.0102, Pru du 5, Pru du 5.0101, Pru du 6, Pru du 6.0101, Pru du 6.0201, Pru du Конглютин, Pru p 1, Pru p 1.0101, Pru p 2, Pru p 2.0101, Pru p 2.0201, Pru p 2.0301, Pru p 3, Pru p 3.0101, Pru p 3.0102, Pru p 4, Pru p 4.0101, Pru p 4.0201, Pru sa 3), Psilocybe spp (Psi c 1, Psi c 1.0101, Psi c 2, Psi c 2.0101), Psoroptes spp (Pso o 1, Pso o 10, Pso o 10.0101, Pso o 11, Pso o 13, Pso o 14, Pso o 2, Pso o 21, Pso o 3, Pso o 5, Pso o 7), Puma spp (Pum c 1), Punica spp (Pun g 3), Pyrus spp (Pyr c 1, Pyr c 1.0101, Pyr c 3, Pyr c 3.0101, Pyr c 4, Pyr c 4.0101, Pyr c 5, Pyr c 5.0101, Pyr py 2), Quercus spp (Que a 1, Que a 1.0101, Que a 1.0201, Que a 1.0301, Que a 1.0401, Que a 2, Que a 4), Rachycentron spp (Rac ca 1), Rana spp (Ran e 1, Ran e 1.0101, Ran e 2, Ran e 2.0101), Ranina spp (Ran ra 1), Rangifer spp (Ran t BLG), Rattus spp (Rat n 1, Rat n 1.0101, Rat n Казеин, Rat n Желатин, Rat n IgG, Rat n Фосвитин, Rat n RSA, Rat n Трансферрин), Rhizomucor spp (Rhi m AP), Rhizopus spp (Rhi nv Липаза, Rhi o Липаза), Rhomboplites spp (Rho au 1), Rhodotorula spp (Rho m 1, Rho m 1.0101, Rho m 2, Rho m 2.0101), Ricinus spp (Ric c 1, Ric c 1.0101, Ric c 2, Ric c 3, Ric c 8, Ric c RIP), Rivulus spp (Riv ma 1), Robinia spp (Rob p 2, Rob p 4, Rob p Глюканаза), Rosa spp (Ros r 3), Roystonea spp (Roy e 2), Rubus spp (Rub i 1, Rub i 1.0101, Rub i 3, Rub i 3.0101, Rub i Хитиназа, Rub i CyP), Saccharomyces spp (Sac c Карбоксипептидаза Y, Sac c CyP, Sac c Енолаза, Sac c Глюкозидаза, Sac c Инвертаза, Sac c MnSOD, Sac c P2, Sac c Профилин), Salvelinus spp (Sal f 1), Salsola spp (Sal k 1, Sal k 1.0101, Sal k 1.0201, Sal k 1.0301, Sal k 1.0302, Sal k 2, Sal k 2.0101, Sal k 3, Sal k 3.0101, Sal k 4, Sal k 4.0101, Sal k 4.0201, Sal k 5, Sal k 5.0101), Salvelinus spp (Sal le Вителлогенин), Salmo spp (Sal s 1, Sal s 1.0101, Sal s 1.0201, Sal s 2, Sal s 2.0101, Sal s Желатин), Sambucus spp (Sam n 1), Sander spp (San lu 1), Saponaria spp (Sap o RIP), Sardinops spp (Sar m 1), Sarkidiornis spp (Sar ml 1), Sardina spp (Sar p 1), Sarcoptes spp (Sar s 1, Sar s 14, Sar s 3, Sar s GST, Sar s PM), Sardinops spp (Sar sa 1, Sar sa 1.0101), Schistosoma spp (Sch j GST, Sch j PM, Sch j Sj22, Sch j Sj67, Sch ma Sm20, Sch ma Sm21, Sch ma Sm22, Sch ma Sm31), Sciaenops spp (Sci oc 1), Scomber spp (Sco a 1), Scombermorus spp (Sco ca 1), Scomberomorus spp (Sco g 1), Scomber spp (Sco j 1, Sco ma 1, Sco s 1), Scolopendra spp (Sco y 7, Sco y 7.0101), Scylla spp (Scy o 1, Scy o 1.0101, Scy o 2, Scy pa 1, Scy pa 2, Scy s 1, Scy s 1.0101, Scy s 2), Sebastes spp (Seb fa 1, Seb in 1, Seb m 1, Seb m 1.0101, Seb m 1.0201), Secale spp (Sec c 1, Sec c 12, Sec c 13, Sec c 2, Sec c 20, Sec c 20.0101, Sec c 20.0201, Sec c 28, Sec c 3, Sec c 4, Sec c 4.0101, Sec c 4.0201, Sec c 5, Sec c 5.0101, Sec c aA_TI, Sec c aA_TI.0101), Senecio spp (Sen j MDH, Sen j PL), Sepia spp (Sep e 1, Sep e 1.0101), Sepioteuthis spp (Sep l 1, Sep l 1.0101), Sepia spp (Sep m 1), Seriola spp (Ser d 1, Ser la 1), Sergestes spp (Ser lu 1), Seriola spp (Ser q 1, Ser ri 1), Sesamum spp (Ses i 1, Ses i 1.0101, Ses i 2, Ses i 2.0101, Ses i 3, Ses i 3.0101, Ses i 4, Ses i 4.0101, Ses i 5, Ses i 5.0101, Ses i 6, Ses i 6.0101, Ses i 7, Ses i 7.0101, Ses i 8), Shigella spp (Shi bo GST, Shi dy GST), Simulia spp (Sim vi 1, Sim vi 2, Sim vi 3, Sim vi 4, Sim vi 70 кДа), Sinapis spp (Sin a 1, Sin a 1.0101, Sin a 1.0104, Sin a 1.0105, Sin a 1.0106, Sin a 1.0107, Sin a 1.0108, Sin a 2, Sin a 2.0101, Sin a 3, Sin a 3.0101, Sin a 4, Sin a 4.0101), Sinonovacula spp (Sin c 1, Sin c 1.0101), Solenopsis spp (Sol g 2, Sol g 2.0101, Sol g 3, Sol g 3.0101, Sol g 4, Sol g 4.0101, Sol g 4.0201, Sol i 1, Sol i 1.0101, Sol i 2, Sol i 2.0101, Sol i 3, Sol i 3.0101, Sol i 4, Sol i 4.0101), Solenocera spp (Sol me 1), Solenopsis spp (Sol r 1, Sol r 2, Sol r 2.0101, Sol r 3, Sol r 3.0101, Sol s 2, Sol s 2.0101, Sol s 3, Sol s 3.0101, Sol s 4), Solea spp (Sol so 1, Sol so TPI), Solanum spp (Sola t 1, Sola t 1.0101, Sola t 2, Sola t 2.0101, Sola t 3, Sola t 3.0101, Sola t 3.0102, Sola t 4, Sola t 4.0101, Sola t 8, Sola t Глюканаза), Sorghum spp (Sor b 1, Sor h 1, Sor h 1.0101, Sor h 12, Sor h 7), Sparus spp (Spa a 1), Sphyrna spp (Sph ti 1), Spirulina spp (Spi mx бета_Фикоцианин), Spinacia spp (Spi o 2, Spi o RuBisCO), Squilla spp (Squ ac 1, Squ ac 1.0101, Squ o 1, Squ o 1.0101), Staphylococcus spp (Sta a FBP, Sta a SEA, Sta a SEB, Sta a SEC, Sta a SED, Sta a SEE, Sta a TSST), Stachybotrys spp (Sta c 3, Sta c 3.0101, Sta c Целлюлаза, Sta c Гемолизин, Sta c SchS34, Sta c Стахираза A), Stemphylium spp (Ste b 1, Ste c 1, Ste v 1), Stolephorus spp (Sto i 1), Struthio spp (Str c 1, Str c 2, Str c 3), Streptococcus spp (Str dy Стрептокиназа), Streptomyces spp (Str g Проназа), Streptococcus spp (Str pn PspC), Strongylocentrotus spp (Str pu 18 кДа, Str pu Вителлогенин), Streptococcus spp (Str py SPEA, Str py SPEC, Str py Стрептокиназа), Strongyloides spp (Str st 45 кДа), Streptomyces spp (Str v PAT), Styela spp (Sty p 1), Suidasia spp (Sui m 1, Sui m 13, Sui m 2, Sui m 3, Sui m 5, Sui m 5.01, Sui m 5.02, Sui m 5.03, Sui m 6, Sui m 7, Sui m 8, Sui m 9), Sus spp (Sus s ACTH, Sus s ALA, Sus s Амилаза, Sus s BLG, Sus s Казеин, Sus s Казеин альфаS1, Sus s Казеин альфаS2, Sus s Казеин бета, Sus s Казеин каппа, Sus s Желатин, Sus s HG, Sus s Инсулин, Sus s Липаза, Sus s Пепсин, Sus s Фосвитин, Sus s PRVB, Sus s PSA, Sus s TCTP), Syntelopodeuma spp (Syn y 7, Syn y 7.0101), Syringa spp (Syr v 1, Syr v 1.0101, Syr v 1.0102, Syr v 1.0103, Syr v 2, Syr v 3, Syr v 3.0101), Tabanus spp (Tab y 1, Tab y 1.0101, Tab y 2, Tab y 2.0101, Tab y 5, Tab y 5.0101), Tadorna spp (Tad ra 1), Talaromyces spp (Tal st 22, Tal st 3, Tal st 8), Taraxacum spp (Tar o 18 кДа), Taxodium spp (Tax d 2), Tegenaria spp (Teg d Гемоцианин), Teladorsagia spp (Tel ci 3), Thaumetopoea spp (Tha p 1, Tha p 1.0101, Tha p 2, Tha p 2.0101), Theragra spp (The c 1), Thermomyces spp (The l Липаза, The sp Липаза, The sp Ксиланаза), Thunnus spp (Thu a 1, Thu a 1.0101, Thu a Коллаген, Thu al 1, Thu at 1, Thu o 1, Thu o Коллаген), Thuja spp (Thu oc 3, Thu p 1), Thunnus spp (Thu t 1, Thu to 1), Thyrsites spp (Thy at 1), Thyrophygus spp (Thy y 7, Thy y 7.0101), Todarodes spp (Tod p 1, Tod p 1.0101, Tod p 1.0102), Toxoptera spp (Tox c 7, Tox c 7.0101), Toxocara spp (Tox ca TES120, Tox ca TES26, Tox ca TES30), Toxoplasma spp (Tox g HSP70), Trachypenaeus spp (Tra c 1), Trachinotus spp (Tra ca 1), Trachurus spp (Tra j 1, Tra j Желатин, Tra tr Желатин), Triticum spp (Tri a 1, Tri a 10 кДа, Tri a 12, Tri a 12.0101, Tri a 12.0102, Tri a 12.0103, Tri a 12.0104, Tri a 13, Tri a 14, Tri a 14.0101, Tri a 14.0201, Tri a 15, Tri a 15.0101, Tri a 18, Tri a 18.0101, Tri a 19, Tri a 19.0101, Tri a 2, Tri a 21, Tri a 21.0101, Tri a 23 кДа, Tri a 25, Tri a 25.0101, Tri a 26, Tri a 26.0101, Tri a 27, Tri a 27.0101, Tri a 28, Tri a 28.0101, Tri a 29, Tri a 29.0101, Tri a 29.0201, Tri a 3, Tri a 30, Tri a 30.0101, Tri a 31, Tri a 31.0101, Tri a 32, Tri a 32.0101, Tri a 33, Tri a 33.0101, Tri a 34, Tri a 34.0101, Tri a 35, Tri a 35.0101, Tri a 36, Tri a 36.0101, Tri a 37, Tri a 37.0101, Tri a 4, Tri a 4.0101, Tri a 4.0201, Tri a 5, Tri a 7, Tri a aA_SI, Tri a альфа_глиадин, Tri a bA, Tri a Bd36K, Tri a бета_Глиадин, Tri a Хитиназа, Tri a CM16, Tri a DH, Tri a Эндохитиназа, Tri a гамма_Глиадин, Tri a Гермин, Tri a Глиадин, Tri a GST, Tri a LMW Glu, Tri a LMW-GS B16, Tri a LMW-GS P42, Tri a LMW-GS P73, Tri a LTP2, Tri a омега2_Глиадин, Tri a Пероксидаза, Tri a Пероксидаза 1, Tri a SPI, Tri a TLP, Tri a Tritin, Tri a XI), Tritirachium spp (Tri al Протеинкиназа K), Tribolium spp (Tri ca 17, Tri ca 17.0101, Tri ca 7, Tri ca 7.0101), Trichostrongylus spp (Tri co 3, Tri co 3.0101), Trichophyton spp (Tri eq 4), Trigonella spp (Tri fg 1, Tri fg 2, Tri fg 3, Tri fg 4), Trichosanthes spp (Tri k RIP), Trichiurus spp (Tri le 1), Triticum spp (Tri m Пероксидаза), Trichophyton spp (Tri me 2, Tri me 4), Trisetum spp (Tri p 1, Tri p 5), Trichinella spp (Tri ps 3, Tri ps 3.0101), Trichophyton spp (Tri r 2, Tri r 2.0101, Tri r 4, Tri r 4.0101), Trichoderma spp (Tri rs Целлюлаза), Triticum spp (Tri s 14), Trichophyton spp (Tri sc 2, Tri sc 4, Tri so 2), Trichinella spp (Tri sp 3, Tri sp 3.0101, Tri sp 3.0102, Tri sp 3.0103, Tri sp 3.0104, Tri sp 3.0105, Tri sp 3.0106), Trichophyton spp (Tri t 1, Tri t 1.0101, Tri t 4, Tri t 4.0101), Triticum spp (Tri td 14, Tri td aA_TI), Trichoderma spp (Tri v Целлюлаза), Trichophyton spp (Tri ve 4), Triatoma spp (Tria p 1, Tria p 1.0101), Triplochiton spp (Trip s 1), Turbo spp (Tur c 1, Tur c PM), Tyrophagus spp (Tyr p 1, Tyr p 10, Tyr p 10.0101, Tyr p 10.0102, Tyr p 13, Tyr p 13.0101, Tyr p 2, Tyr p 2.0101, Tyr p 24, Tyr p 24.0101, Tyr p 3, Tyr p 3.0101, Tyr p 4, Tyr p 5, Tyr p 5.01, Tyr p 5.02, Tyr p 5.03, Tyr p 7, Tyr p альфа Тубулин), Ulocladium spp (Ulo a 1, Ulo at 1, Ulo b 1, Ulo c 1, Ulo co 1, Ulo cu 1, Ulo mu 1, Ulo ob 1, Ulo se 1, Ulo su 1, Ulo tu 1), Uncia spp (Unc u 1), Urophycis spp (Uro te 1), Vaccinium spp (Vac m 3), Varroa spp (Var j 13 кДа), Venerupis spp (Ven ph 1, Ven ph 1.0101), Vespula spp (Ves f 1, Ves f 2, Ves f 5, Ves f 5.0101, Ves g 1, Ves g 2, Ves g 5, Ves g 5.0101, Ves m 1, Ves m 1.0101, Ves m 2, Ves m 2.0101, Ves m 5, Ves m 5.0101, Ves m MLT, Ves p 1, Ves p 2, Ves p 5, Ves p 5.0101, Ves s 1, Ves s 1.0101, Ves s 2, Ves s 5, Ves s 5.0101, Ves v 1, Ves v 1.0101, Ves v 2, Ves v 2.0101, Ves v 2.0201, Ves v 3, Ves v 3.0101, Ves v 5, Ves v 5.0101, Ves v 5-Pol a 5, Ves vi 5, Ves vi 5.0101), Vespa spp (Vesp c 1, Vesp c 1.0101, Vesp c 2, Vesp c 5, Vesp c 5.0101, Vesp c 5.0102, Vesp m 1, Vesp m 1.0101, Vesp m 5, Vesp m 5.0101, Vesp ma 1, Vesp ma 2, Vesp ma 5, Vesp ma MLT, Vesp v MLT), Vigna spp (Vig r 1, Vig r 1.0101, Vig r 17 кДа, Vig r 5, Vig r 8S Глобулин, Vig r Альбумин, Vig r бета-Конглицин), Vitis spp (Vit v 1, Vit v 1.0101, Vit v 4, Vit v 5, Vit v Глюканаза, Vit v TLP), Xiphias spp (Xip g 1, Xip g 1.0101, Xip g 25 кДа), Zea spp (Zea m 1, Zea m 1.0101, Zea m 11, Zea m 12, Zea m 12.0101, Zea m 12.0102, Zea m 12.0103, Zea m 12.0104, Zea m 12.0105, Zea m 13, Zea m 14, Zea m 14.0101, Zea m 14.0102, Zea m 2, Zea m 20S, Zea m 22, Zea m 25, Zea m 25.0101, Zea m 27 кДа Zein, Zea m 3, Zea m 4, Zea m 5, Zea m 50 кДа Zein, Zea m 7, Zea m Хитиназа, Zea m G1, Zea m G2, Zea m PAO, Zea m Zm13), Zeus spp (Zeu fa 1), Ziziphus spp (Ziz m 1, Ziz m 1.0101), Zoarces spp (Zoa a ISP III), Zygophyllum spp (Zyg f 2).
В данном контексте терминами в скобках указаны конкретные предпочтительные аллергены из конкретного источника.
Наиболее предпочтительно антиген, ассоциированный с аллергией или аллергическим заболеванием, предпочтительно получен из источника, выбранного из списка, состоящего из пыльцы травянистых растений (например, пыльцы ржи), пыльцы деревьев (например, пыльцы ореха, березы, ольхи, ясеня), цветочной пальцы, пыльцы трав (например, пыльцы полыни обыкновенной), пылевого клеща (например, Der f 1, Der p 1, Eur m 1, Der m 1, Der f 2, Der p 2, Eur m 2, Tyr p 2, Lep d 2), плесени (например, аллергены Acremonium, Aspergillus, Cladosporium, Fusarium, Mucor, Penicillium, Rhizopus, Stachybotrys, Trichoderma или Alternaria), животных (например, Fel d1, Fel d 2, Fel d3 или Fel d4 кошек), пищевых продуктов (например, аллергены рыб (например, окуня, трески, камбалы), морепродуктов (например, краба, лобстера, креветок), яиц, пшеницы, орехов (например, арахиса, миндаля, кешью, грецкого ореха), сои, молока и т.д.) или яда насекомых (например, аллергены из яда ос, пчел, шершней, муравьев, комаров или клещей).
c) Антигены, ассоциированные с аутоиммунным заболеванием:
Антигены, ассоциированные с аутоиммунным заболеванием, предпочтительно выбраны из аутоантигенов, ассоциированных с аутоиммунными заболеваниями, выбранными из болезни Аддисона (аутоиммунного адреналита, аддисоновой болезни), очаговой алопеции, анемии Аддисона (болезни Бирмера), аутоиммунной гемолитической анемии (AIHA), аутоиммунной гемолитической анемии (AIHA) холодового типа (холодовой гемагглютининовой болезни, холодовой аутоиммунной гемолитической анемии (AIHA) (холодовой агглютининовой болезни), (CHAD)), аутоиммунной гемолитической анемии (AIHA) теплового типа (тепловой AIHA, тепловой аутоиммунной гемолитической анемии (AIHA)), аутоиммунной гемолитической анемии Доната-Ландштейнера (пароксизмальной холодовой гемоглобинурии), антифосфолипидного синдрома (APS), атеросклероза, аутоиммунного артрита, височного артериита, артериита Такаясу (болезни Такаясу, заболевания дуги аорты), височного артериита/узелкового периартериита, аутоиммунного хронического гастрита, аутоиммунного бесплодия, аутоиммунного заболевания внутреннего уха (AIED), базедовой болезни (Morbus Basedow), болезни Бехтерова (Morbus Bechterew, анкилозирующего спондилита, spondylitis ankylosans), синдрома Бехчета (Morbus Behcet), заболевания кишечника, включая аутоиммунное воспалительное заболевание кишечника (включая язвенный колит (Morbus Crohn, болезнь Крона), кардиомиопатии, в частности аутоиммунной кардиомиопатии, идиопатической дилятационной кардиомиопатии (DCM), целиакии-спру-дерматита (глутеновой энтеропатии), синдрома хронической усталости и иммунной дисфункции (CFIDS), хронической воспалительной демиелинизирующей полиневропатии (CIDP), хронического полиартрита, синдрома Черджа-Стросса, рубцующегося пемфигоида, синдрома Когана, CREST-синдрома (синдрома с кальцинозом кожи, феноменом Рейно, расстройствами моторики пищевода, склеродактилией и телеангиэктозией), болезни Крона (Morbus Crohn, язвенного колита), герпетиформного дерматита Дюринга, дерматологических аутоиммунных заболеваний, дерматомиозита, диабета, сахарного диабета типа 1 (диабета типа I, инсулинозависимого сахарного диабета), сахарного диабета типа 2 (диабета типа II), эссенциальной криоглобулинемии смешанного типа, эссенциальной криоглобулинемии смешанного типа, фибромиалгии, фибромиозита, синдрома Гудпасчера (анти-GBM-опосредованного гломерулонефрита), болезни «трансплантат против хозяина», синдрома Гийена-Барре (GBM, полирадикулонейрита), гематологических аутоиммунных заболеваний, тиреоидита Хашимото, гемофилии, приобретенной гемофилии, гепатита, аутоиммунного гепатита, особых аутоиммунных форм хронического гепатита, идиопатического легочного фиброза (IPF), идиопатической тромбоцитопенической пурпуры, иммуно-тромбоцитопенической пурпуры (болезни Верхофа; ITP), IgA-нефропатии, бесплодия, аутоиммунного бесплодия, ювенильного ревматоидного артрита (болезни Стилла, синдрома Стилла), синдрома Ламберта-Итона, красного плоского лишая, склерозирующего лишая, красной волчанки, системной красной волчанки (SLE), красной волчанки (дискоидной формы), артрита Лайма (болезни Лайма, артрита при боррелиозе), болезни Меньера (Morbus Meniere); заболевания смешанного соединительной ткани (MCTD), рассеянного склероза (MS, диссеминированного энцефаломиелита, болезни Шарко), тяжелой псевдопаралитической миастении (миастении, MG), миозита, полимиозита, нервных аутоиммунных болезней, нейродермита, вульгарного пемфигуса, буллезного пемфигоида, рубцующегося пемфигоида; нодозного полиартериита (нодозного периартериита), полихондрита (панхондрита), полигландулярного (аутоиммунного) синдрома (PGA-синдрома, синдрома Шмидта), ревматической полимиалгии, первичной агаммаглобулинемии, первичного билиарного цирроза PBC, первичного аутоиммунного холангита, прогрессирующего системного склероза (PSS), псориаза, вульгарного псориаза, феномена Рейно, синдрома Рейтера (Morbus Reiter, уретро-конъюктиво-синовиального синдрома)), ревматоидного артрита (RA, хронического полиартрита, ревматоидного заболевания суставов, острой ревматической лихорадки), саркоидоза (болезни Бека, болезни Бенье-Бека-Шауманна), синдрома мышечной скованности, склеродермии, склеродермы, синдрома Шегрена, симпатической офтальмии; временной непереносимости глютена, отторжения трансплантированного органа, увеита, аутоиммунного увеита, васкулита, витилиго (лейкодермы, пестрой кожи) и болезни Вегнера (Morbus Wegner, гранулематоза Вегнера).
Особенно предпочтительными в данном контексте являются аутоантигены, выбранные из:
- основного миелиного белка (MBP), протеолипидного белка (PLP) и гликопротеина миелина олигодендроцитов (MOG), в каждом случае ассоциированных с рассеянным склерозом (MS);
- CD44, препроинсулина, проинсулина, инсулина, декарбоксилазы глутаминовой кислоты (GAD65), подобного тирозиновой фосфатазе антигена инсулиномы 2 (IA2), переносчика цинка (ZnT8) и белка теплового шока 60 (HSP60), в каждом случае ассоциированного с диабетом типа I;
- межфоторецепторного ретиноид-связывающего белка (IRBP), ассоциированного с аутоиммунным увеитом;
- ацетилхолинового рецептора AchR и рецептора инсулин-подобного фактора роста-1 (IGF-1R), в каждом случае ассоциированного с тяжелой псевдопаралитической миастенией;
- M-белка из бета-гемолитических стрептококков (псевдоаутоантиген), ассоциированного с острой ревматической лихорадкой;
- фактора, ингибирующего миграцию макрофагов, ассоциированного с артритом;
- RNP-комплекса Ro/La, альфа- и бета-фодрина, аутоантигена островковых клеток, поли(АДФ)рибозаполимеразы (PARP), NuMA, NOR-90, аутоантигена Ro60 и антигена p27, в каждом случае ассоциированного с синдромом Шегрена;
- аутоантигена Ro60, липопротеинов низкой плотности, Sm-антигенов комплекса малых ядерных рибонуклеопротеинов U-1 (B/B', D1, D2, D3, E, F, G) и RNP-рибонуклеопротеинов, в каждом случае ассоциированного с красной волчанкой;
- oxLDL, бета(2)GPI, HSP60/65 и oxLDL/бета(2)GPI, в каждом случае ассоциированного с атеросклерозом;
- бета(1)-адренергического рецептора сердца, ассоциированного с идиопатической дилятационной кардиомиопатией (DCM);
- гистидил-тРНК-синтетазы (HisRS), ассоциированной с миозитом;
- топоизомеразы I, ассоциированной со склеродермией.
Кроме того, в других вариантах указанный антиген ассоциирован с соответствующим аутоиммунным заболеванием, например, IL-17, белки теплового шока и/или любой идиотипический патогенный T-клеточный или хемокинный рецептор, который экспрессируется иммунными клетками, вовлеченными в аутоиммунный ответ в случае указанного аутоиммунного заболевания (такого как любые аутоиммунные заболевания, описанные в настоящей публикации).
d) Антигены, ассоциированные с раком или опухолевым заболеванием («опухолевые антигены»):
«Опухолевые антигены» в данном контексте представляют собой антигены, которые предпочтительно локализованы на поверхности (опухолевой) клетки. Опухолевые антигены также могут быть выбраны из белков, которые сверхэкспрессируются в опухолевых клетках по сравнению с нормальными клетками. Кроме того, опухолевые антигены также включают антигены, экспрессированные в клетках, которые являются (были) не сами по себе (или исходно не сами по себе) дегенерированными, но ассоциированы с предполагаемой опухолью. Также включены антигены, которые связаны со снабжающими опухоли сосудами или их повторным образованием, в частности, антигены, которые ассоциированы с неоваскуляризацией, например, факторами роста, такими как VEGF, bFGF и т.д. Антигены, связанные с опухолью, кроме того, включают антигены из клеток или тканей, в которых обычно заключена опухоль. Кроме того, некоторые вещества (обычно белки или пептиды) экспрессируются у пациентов, страдающих (зная или не зная об этом) от злокачественного заболевания, и они находятся в повышенных концентрациях в жидкостях организма указанных пациентов. Такие вещества также называют «опухолевыми антигенами», однако они не являются антигенами в строгом значении определения вещества, индуцирующего иммунный ответ. Класс опухолевых антигенов может быть подразделен на специфичные для опухоли антигены (TSA) и ассоциированные с опухолью антигены (TAA). TSA могут быть представлены только на опухолевых клетках и никогда на нормальных «здоровых» клетках. Обычно они являются результатом специфичной для опухоли мутации. TAA, которые более распространены, обычно представлены как на опухолевых, так и на здоровых клетках. Такие антигены распознаются, и антигенпрезентирующая клетка может быть разрушена цитотоксическими T-клетками. Дополнительно, опухолевые антигены также могут встречаться на поверхности опухоли, например, в форме мутантного рецептора. В данном случае они могут распознаваться антителами. Особенно предпочтительные опухолевые антигены выбраны из группы, состоящей из 5T4, 707-AP, 9D7, AFP, AlbZIP HPG1, альфа-5-бета-1-интегрина, альфа-5-бета-6-интегрина, альфа-актинин-4/m, альфа-метилацил-кофермент A-рацемазы, ART-4, ARTC1/m, B7H4, BAGE-1, BCL-2, bcr/abl, бета-катенина/m, BING-4, BRCA1/m, BRCA2/m, CA 15-3/CA 27-29, CA 19-9, CA72-4, CA125, кальретикулина, CAMEL, CASP-8/m, катепсина B, катепсина L, CD19, CD20, CD22, CD25, CDE30, CD33, CD4, CD52, CD55, CD56, CD80, CDC27/m, CDK4/m, CDKN2A/m, CEA, CLCA2, CML28, CML66, COA-1/m, коактозин-подобного белка, коллагена XXIII, ЦОГ-2, CT-9/BRD6, Cten, циклина B1, циклина D1, cyp-B, CYPB1, DAM-10, DAM-6, DE-CAN, EFTUD2/m, EGFR, ELF2/m, EMMPRIN, EpCam, EphA2, EphA3, ErbB3, ETV6-AML1, EZH2, FGF-5, FN, Frau-1, G250, GAGE-1, GAGE-2, GAGE-3, GAGE-4, GAGE-5, GAGE-6, GAGE 7b, GAGE-8, GDEP, GnT-V, gp100, GPC3, GPNMB/m, HAGE, HAST-2, гепсина, Her2/neu, HERV-K-MEL, HLA-A*0201-R17I, HLA-A11/m, HLA-A2/m, HNE, гомеобокса NKX3.1, HOM-TES-14/SCP-1, HOM-TES-85, HPV-E6, HPV-E7, HSP70-2M, HST-2, hTERT, iCE, IGF-1R, IL-13Ra2, IL-2R, IL-5, незрелого рецептора ламинина, калликреина-2, калликреина-4, Ki67, KIAA0205, KIAA0205/m, KK-LC-1, K-Ras/m, LAGE-A1, LDLR-FUT, MAGE-A1, MAGE-A2, MAGE-A3, MAGE-A4, MAGE-A6, MAGE-A9, MAGE-A10, MAGE-A12, MAGE-B1, MAGE-B2, MAGE-B3, MAGE-B4, MAGE-B5, MAGE-B6, MAGE-B10, MAGE-B16, MAGE-B17, MAGE-C1, MAGE-C2, MAGE-C3, MAGE-D1, MAGE-D2, MAGE-D4, MAGE-E1, MAGE-E2, MAGE-F1, MAGE-H1, MAGEL2, маммаглобина A, MART-1/мелан-A, MART-2, MART-2/m, белка матрикса 22, MC1R, M-CSF, ME1/m, мезотелина, MG50/PXDN, MMP11, MN/CA IX-антигена, MRP-3, MUC-1, MUC-2, MUM-1/m, MUM-2/m, MUM-3/m, миозина класса I/m, NA88-A, N-ацетилглюкозаминилтрансферазы-V, Neo-PAP, Neo-PAP/m, NFYC/m, NGEP, NMP22, NPM/ALK, N-Ras/m, NSE, NY-ESO-1, NY-ESO-B, OA1, OFA-iLRP, OGT, OGT/m, OS-9, OS-9/m, остеокальцина, остеопонтина, p15, p190 минорного bcr-abl, p53, p53/m, PAGE-4, PAI-1, PAI-2, PAP, PART-1, PATE, PDEF, Pim-1-киназы, Pin-1, PmI/PARальфа, POTE, PRAME, PRDX5/m, простеина, протеиназы-3, PSA, PSCA, PSGR, PSM, PSMA, PTPRK/m, RAGE-1, RBAF600/m, RHAMM/CD168, RU1, RU2, S-100, SAGE, SART-1, SART-2, SART-3, SCC, SIRT2/m, Sp17, SSX-1, SSX-2/HOM-MEL-40, SSX-4, STAMP-1, STEAP, сурвивина, сурвивина- 2B, SYT-SSX-1, SYT-SSX-2, TA-90, TAG-72, TARP, TEL-AML1, TGFбета, TGFбетаRII, TGM-4, TPI/m, TRAG-3, TRG, TRP-1, TRP-2/6b, TRP/INT2, TRP-p8, тирозиназы, UPA, VEGF, VEGFR1, VEGFR-2/FLK-1 и WT1. Такие опухолевые антигены предпочтительно могут быть выбраны из группы, состоящей из p53, CA125, EGFR, Her2/neu, hTERT, PAP, MAGE-A1, MAGE-A3, мезотелина, MUC-1, NY-ESO-1, GP100, MART-1, тирозиназы, PSA, PSCA, PSMA VEGF, VEGFR1, VEGFR2, Ras, CEA или WTI, и более предпочтительно из PAP, NY-ESO-1, MAGE-A3, WT1 и MUC-1.
В данном контексте и в случае некоторых вариантов всех аспектов настоящего изобретения антиген, ассоциированный с раком или опухолевым заболеванием, не включает (x) идиотипический иммуноглобулин (идиотипическое антитело или идиотипический B-клеточный рецептор); или (y) идиотипический T-клеточный рецептор, и необязательно не является фрагментом, вариантом и/или производным такого антигена.
Кроме того, по меньшей мере один антиген, если он представлен в виде белкового или пептидного антигена, в некоторых вариантах не является модельным антигеном овальбумина или фрагмента овальбумина, такого как полученный из овальбумина пептид SIINFEKL (SEQ ID NO: 116).
По меньшей мере один антиген в фармацевтической композиции согласно изобретению может быть представлен в виде белка или пептида или может кодироваться нуклеиновой кислотой, например, ДНК (например, плазмидной ДНК или вирусной ДНК) или РНК (например, мРНК или вирусной РНК). Предпочтительно, по меньшей мере один антиген представлен в виде белка или пептида или фрагмента, варианта и/или производного указанного белкового или пептидного антигена. В некоторых вариантах указанный белковый или пептидный антиген (или фрагмент, вариант и/или производное указанного белкового или пептидного антигена) входит в состав, предлагается в виде или получен из определенного образца, например, образца с известным количеством и/или составом компонентов. Например, указанный белковый или пептидный антиген в каждом случае не входит в состав или не предлагается в виде, или не получен из смеси (например, неопределенной) других компонентов, такой как смесь, являющаяся препаратом инактивированного или ослабленного вируса или патогена (такой как в каждом случае любой из описанных в настоящей публикации). Например, антиген, используемый в любом аспекте настоящего изобретения, может представлять собой или может быть получен в виде изолированного и/или очищенного белкового или пептидного антигена. Как будет понятно специалисту, изолированный (и/или очищенный) антиген включает такие антигены, которые присутствуют (или представлены) в (исходной) композиции, которая содержит менее чем примерно 40%, 30%, 20%, 10%, 5%, 2% или 1% нежелательных или других специфичных компонентов, таких как другие белки/пептиды или примеси.
Белковые или пептидные антигены могут, например, быть получены следующим образом.
Белковые или пептидные антигены, которые описаны выше, могут быть получены с использованием способов основанного на рекомбинации получения, таких как способы, описанные в настоящей публикации, или, например, с помощью молекулярно-биологических способов, известных специалисту. Такой антиген может быть описан в соответствующем случае как «рекомбинантный белковый антиген» и/или «рекомбинантный пептидный антиген».
Альтернативно, белок или пептид, которые описаны выше (например, фрагменты, домены, эпитопы или белковые антигены и/или пептидные аналоги), могут быть получены с использованием способов пептидного синтеза, таких как способы, описанные в настоящей публикации, или, например, другими способами, известными специалисту. Такой антиген может быть описан в соответствующем случае как «синтетический белковый антиген» и/или «синтетический пептидный антиген».
В том случае, когда по меньшей мере один антиген представлен в виде белкового или пептидного антигена (или его фрагмента, варианта и/или производного), пептидный или белковый антиген может быть представлен в первом альтернативном варианте в отдельном компоненте фармацевтической композиции согласно изобретению. В таком случае по меньшей мере один белковый или пептидный антиген не является частью комплекса полимерного носителя и переносимого вещества, или другими словами: в данном случае комплекс полимерного носителя и переносимого вещества не включает по меньшей мере один антиген. Во втором альтернативном варианте по меньшей мере один белковый или пептидный антиген может быть представлен в виде компонента комплекса полимерного носителя и переносимого вещества. В данном случае пептидный или белковый антиген может быть добавлен к комплексу полимерного носителя и переносимого вещества во время стадии полимеризации c) способа получения комплекса полимерного носителя и переносимого вещества, который описан в настоящей публикации. Таким образом, пептидный или белковый антиген интегрирован в комплекс полимерного носителя и переносимого вещества. Особенно предпочтительной в данном контексте является ситуация, когда пептидный или белковый антиген несет по меньшей мере один SH-остаток для полимеризации с другими компонентами полимерного носителя в комплексе полимерного носителя и переносимого вещества. Кроме того, в следующем альтернативном варианте предлагается белковый или пептидный антиген в виде компонента полимерного носителя комплекса полимерного носителя и переносимого вещества и предлагается по меньшей мере один дополнительный белковый или пептидный антиген (такой же или другой) в виде отдельного компонента фармацевтической композиции согласно изобретению, который не является частью комплекса полимерного носителя и переносимого вещества.
Кроме того, по меньшей мере один антиген (или его фрагмент, вариант и/или производное) может быть представлен в фармацевтической композиции согласно изобретению в форме нуклеиновых кислот, кодирующих по меньшей мере один антиген (или его фрагменты, варианты и/или производные).
В данном контексте нуклеиновые кислоты, кодирующие по меньшей мере один антиген (или его фрагменты, варианты и/или производные), определяют, как указано выше для переносимой нуклеиновой кислоты, входящей в состав комплекса полимерного носителя и переносимого вещества, используемого в качестве адъюванта в фармацевтической композиции согласно изобретению. Таким образом, специально включены также фрагменты, варианты, производные и модификации нуклеиновой кислоты, которая определена в настоящем описании.
По меньшей мере один антиген (или его фрагмент, вариант и/или производное), если он представлен в фармацевтической композиции согласно изобретению в форме нуклеиновых кислот, кодирующих по меньшей мере один антиген (или их фрагменты, варианты и/или производные), может быть получен с использованием всех способов синтеза нуклеиновых кислот, известных специалисту. Особенно предпочтительными являются способы синтеза нуклеиновых кислот, которые определены в настоящем описании.
Также в данном случае существуют два альтернативных варианта. В первом альтернативном варианте предлагается нуклеиновая кислота, кодирующая по меньшей мере один антиген, в виде части комплекса полимерного носителя и переносимого вещества (например, в виде переносимой молекулы нуклеиновой кислоты), а во втором альтернативном варианте предлагается нуклеиновая кислота, кодирующая по меньшей мере один антиген, в виде отдельного компонента фармацевтической композиции согласно изобретению. Таким образом, в данном случае нуклеиновая кислота, кодирующая по меньшей мере один антиген, не является частью комплекса полимерного носителя и переносимого вещества.
В следующем варианте осуществления настоящего изобретения, по меньшей мере один антиген (или его фрагмент, вариант и/или производное), кодируемый нуклеиновой кислотой, может быть представлен в виде части (адъюванта) комплекса полимерного носителя и переносимого вещества (например, в виде переносимой нуклеиновой кислоты, кодирующей по меньшей мере один антиген), и дополнительно антиген, кодируемый нуклеиновой кислотой, может быть представлен с виде отдельного компонента, который не является частью комплекса полимерного носителя и переносимого вещества.
В изобретении, кроме того, предлагается альтернативный вариант, в котором по меньшей мере один антиген представлен в виде нуклеиновой кислоты (в виде части комплекса полимерного носителя и переносимого вещества или не в виде части такого комплекса) и в котором по меньшей мере один дополнительный антиген представлен в виде белкового или пептидного антигена (в виде части комплекса полимерного носителя и переносимого вещества или не в виде части такого комплекса).
В качестве следующего варианта, по меньшей мере один антиген, если он представлен в виде белка или пептида или в виде нуклеиновой кислоты, кодирующей по меньшей мере один антиген, может дополнительно содержать или кодировать сигнальный пептид, который определен в настоящем описании.
В качестве дополнительного ингредиента фармацевтическая композиция может содержать по меньшей мере один дополнительный фармацевтически активный компонент. Фармацевтически активный компонент в таком контексте представляет собой соединение, которое оказывает терапевтический эффект, способствуя излечению, ослаблению или предотвращению конкретного показания, предпочтительно опухолевых или раковых заболеваний, аутоиммунного заболевания, аллергий или инфекционных болезней. Такие соединения включают без ограничения пептиды или белки, предпочтительно, которые определены в настоящем описании, нуклеиновые кислоты, предпочтительно, которые определены в настоящем описании, (терапевтически активные) низкомолекулярные органические или неорганические соединения (молекулярная масса менее 5000, предпочтительно менее 1000), сахара, антигены или антитела, предпочтительно, которые определены в настоящем описании, терапевтические средства, уже известные в данной области, антигенные клетки, антигенные клеточные фрагменты, клеточные фракции; компоненты клеточной стенки (например, полисахариды), модифицированные, ослабленные или дезактивированные (например, химически или под действием излучения) патогены (вирусы, бактерии, т.д.), адъюванты, предпочтительно, которые определены в настоящем описании, и т.д.
Кроме того, фармацевтическая композиция согласно изобретению может содержать фармацевтически приемлемый носитель и/или наполнитель. В контексте настоящего изобретения фармацевтически приемлемый носитель обычно включает жидкую или нежидкую основу фармацевтической композиции. Если фармацевтическая композиция предлагается в жидкой форме, носителем обычно является апирогенная вода; изотонический раствор соли или забуференные (водные) растворы, например, фосфатный, цитратный и т.д. забуференные растворы. Инъекционный буфер может быть гипертоническим, изотоническим или гипотоническим по отношению к конкретной эталонной среде, т.е. буфер может иметь более высокое, идентичное или более низкое содержание соли по сравнению с конкретной эталонной средой, при этом предпочтительно можно использовать такие концентрации указанных выше солей, которые не приводят к повреждению клеток вследствие осмоса или других концентрационных эффектов. Эталонными средами являются, например, жидкости, встречающиеся в способах «in vivo», такие как кровь, лимфа, цитозольные жидкости или другие жидкости организма, или, например, жидкости, которые можно использовать в качестве эталонных сред в способах «in vitro», такие как общепринятые буферы или жидкости. Такие общепринятые буферы или жидкости известны специалисту.
Однако в случае фармацевтической композиции также можно использовать один или несколько совместимых твердых или жидких наполнителей или разбавителей, или инкапсулирующих соединений, которые подходят для введения пациенту, подвергаемому лечению. Термин «совместимый» в используемом в настоящем описании смысле означает, что такие составляющие фармацевтической композиции могут быть смешаны с комплексом полимерного носителя и переносимого вещества, который определен в настоящем описании, таким образом, чтобы не происходило взаимодействие, которое может значимо снижать фармацевтическую эффективность фармацевтической композиции в типичных условиях применения. Фармацевтически приемлемые носители, наполнители и разбавители конечно должны иметь достаточно высокую чистоту и достаточно низкую токсичность, чтобы они были подходящими для введения человеку, подвергаемому лечению. Некоторыми примерами соединений, которые можно использовать в качестве фармацевтически приемлемых носителей, наполнителей или составляющих их компонентов, являются сахара, такие как, например, лактоза, глюкоза и сахароза; крахмалы, такие как, например, кукурузный крахмал или картофельный крахмал; целлюлоза и ее производные, такие как, например, карбоксиметилцеллюлоза натрия, этилцеллюлоза, ацетат целлюлозы; порошкообразная трагакантовая камедь; солод; желатин; говяжий жир; твердые скользящие вещества, такие как, например, стеариновая кислота, стеарат магния; сульфат кальция; растительные масла, такие как, например, арахисовое масло, хлопковое масло, кунжутное масло, оливковое масло, кукурузное масло и какао-масло; полиолы, такие как, например, полипропиленгликоль, глицерин, сорбит, маннит и полиэтиленгликоль; альгиновая кислота.
Согласно конкретному варианту фармацевтическая композиция согласно изобретению может содержать (дополнительный) адъювант. В данном контексте адъювант можно понимать как любое соединение, которое подходит для инициации или повышения иммунного ответа врожденной иммунной системы, т.е. неспецифичного иммунного ответа. Другими словами, при введении фармацевтическая композиция обычно вызывает врожденный иммунный ответ благодаря адъюванту, необязательно входящему в ее состав. Такой адъювант может быть выбран из любого адъюванта, известного специалисту и подходящего для данного случая, т.е. поддерживающего индукцию врожденного иммунного ответа у млекопитающего.
Фармацевтическую композицию согласно изобретению можно вводить перорально, парентерально, с помощью ингаляционного спрея, местно, ректально, назально, буккально, вагинально или с использованием имплантируемой емкости. Термин «парентеральный» в используемом в настоящем описании смысле включает подкожный, внутривенный, внутримышечный, внутрисуставной, внутриузловой, внутрисиновиальный, интрастернальный, интратекальный, внутрипеченочный, внутриочаговый, интракраниальный, трансдермальный, интрадермальный, внутрилегочный, внутрибрюшинный, внутрисердечный, внутриартериальный и подъязычный способы инъекции или инфузии.
Предпочтительно, фармацевтическая композиция согласно изобретению может быть введена путем парентеральной инъекции, более предпочтительно подкожным, внутривенным, внутримышечным, внутрисуставным, внутриузелковым, внутрисиновиальным, интрастернальным, интратекальным, внутрипочечным, внутриочаговым, интракраниальным, трансдермальным, внутридермальным, внутрилегочным, внутрибрюшинным, внутрисердечным, внутриартериальным и подъязычным способами инъекции или инфузии. Особенно предпочтительно является интрадермальная, подкожная и внутримышечная инъекция. Стерильные инъекционные формы фармацевтических композиций могут представлять собой водные или масляные суспензии. Такие суспензии могут быть приготовлены способом, известным в данной области, с использованием подходящих диспергирующих средств или увлажнителей и суспендирующих средств. Стерильный инъекционный препарат также может представлять собой стерильный инъекционный раствор или суспензию в нетоксичном парантерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. К приемлемым наполнителям и растворителям, которые можно применять, относятся вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, обычно в качестве растворителя или суспензионной среды используют стерильные нелетучие масла. С указанной целью можно использовать любое безвкусное нелетучее масло, включая синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные, применимы для получения инъекционных средств, так как они являются природными фармацевтически приемлемыми маслами, такими как оливковое масло или касторовое масло, особенно в их полиоксиэтилированных формах. Такие масляные растворы или суспензии также могут содержать длинноцепочечный спиртовой разбавитель или диспергирующее средство, такое как карбоксиметилцеллюлоза или сходные диспергирующие средства, которые обычно используют при приготовлении фармацевтически приемлемых дозированных форм, включая эмульсии и суспензии. Другие широко используемые поверхностно-активные вещества, такие как твины, спаны и другие эмульгаторы, или усилители биодоступности, которые обычно используют в производстве фармацевтически приемлемых твердых, жидких или других дозированных форм, также можно применять в целях приготовления фармацевтической композиции.
Фармацевтическую композицию согласно изобретению, которая определена в настоящем описании, также можно вводить перорально в любой перорально приемлемой дозированной форме, включая без ограничения капсулы, таблетки, водные суспензии или растворы. В случае таблеток для перорального применения обычно используемые носители включают лактозу и кукурузный крахмал. Также обычно добавляют скользящие вещества, такие как стеарат магния. В случае перорального введения в форме капсул применимые разбавители включают лактозу и сухой кукурузный крахмал. Когда для перорального применения требуются водные суспензии, активный ингредиент, т.е. комплекс полимерного носителя и переносимого вещества, объединяют с эмульгаторами и суспендирующими средствами. При необходимости также могут быть добавлены подсластители, корригенты или красители.
Фармацевтическую композицию согласно изобретению также можно вводить местно, особенно когда мишени лечения включают области или органы, легко доступные при местном применении, например, включая заболевания кожи или другой доступной эпителиальной ткани. Подходящие препараты местного действия легко получают для каждой из области или органа. В случае местных применений фармацевтическая композиция может быть приготовлена в виде подходящей мази, содержащей комплекс полимерного носителя и переносимого вещества, суспендированный или растворенный в одном или нескольких носителях. Носители для местного введения включают без ограничения минеральное масло, вазелиновое масло, белый вазелин, пропиленгликоль, полиоксиэтилен, соединение полиоксипропилена, эмульгирующий воск и воду. Альтернативно, фармацевтическая композиция может быть приготовлена в виде подходящего лосьона или крема. В контексте настоящего изобретения подходящие носители включают без ограничения минеральное масло, моностеарат сорбитана, полисорбат 60, воск, содержащий цетиловые эфиры, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду.
Фармацевтическая композиция согласно изобретению обычно содержит «безопасное и эффективное количество» компонентов фармацевтической композиции, в частности, комплекса полимерного носителя и переносимого вещества, который определен в настоящем описании, или нуклеиновой кислоты как таковой. В используемом в настоящем описании смысле «безопасное и эффективное количество» означает количество комплекса полимерного носителя и переносимого вещества, как такового, которое достаточно для того, чтобы значимо индуцировать положительную модификацию заболевания или расстройства, которое определено в настоящем описании. Однако в то же время «безопасное и эффективное количество» достаточно мало, чтобы избежать серьезных побочных эффектов и осуществить рациональную взаимосвязь между преимуществом и риском. Определение таких пределов обычно осуществляется в рамках рационального медицинского решения. «Безопасное и эффективное количество» компонентов фармацевтической композиции, в частности, комплекса полимерного носителя и переносимого вещества или по меньшей мере одного антигена, который определен в настоящем описании, кроме того, будет варьировать в зависимости от конкретного состояния, подвергаемого лечению, а также возраста и физического состояния пациента, подвергаемого лечению, массы тела, общего состояния здоровья, пола, диеты, времени введения, скорости экскреции, сочетания лекарственных средств, активности комплекса полимерного носителя и переносимого вещества или антигена, тяжести состояния, продолжительности лечения, природы сопутствующей терапии, конкретного используемого фармацевтически приемлемого носителя и сходных факторов, в зависимости от знаний и опыта лечащего врача. Фармацевтическую композицию можно применять в отношении человека, а также в целях ветеринарии, предпочтительно в медицинских целях для человека, обычно в виде фармацевтической композиции или в виде вакцины.
Фармацевтическая композиция согласно изобретению может дополнительно содержать одно или несколько вспомогательных вещества для того, чтобы при необходимости повысить ее иммуногенность или иммуностимулирующую способность. При этом предпочтительно достигается синергетическое действие (адъювантного) комплекса полимерного носителя и переносимого вещества, который определен в настоящем описании, и вспомогательного вещества, которое может необязательно входить в состав фармацевтической композиции согласно изобретению, которая определена в настоящем описании. В зависимости от различных типов вспомогательных вещества могут быть учтены различные механизмы. Например, соединения, которые способствуют созреванию дендритных клеток (DC), например, липополисахариды, TNF-альфа или CD40-лиганд, образуют первый класс подходящих вспомогательных веществ. В общем, можно использовать в качестве вспомогательного вещества любое средство, которое влияет на иммунную систему как «сигнал опасности» (LPS, GP96 и т.д.), или цитокины, такие как GM-CFS, которые позволяют усиливать иммунный ответ и/или влиять на него целенаправленным образом. Особенно предпочтительными вспомогательными веществами являются цитокины, такие как монокины, лимфокины, интерлейкины или хемокины, которые дополнительно стимулируют врожденный иммунный ответ, такие как IL-1, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-12, IL-13, IL-14, IL-15, IL-16, IL-17, IL-18, IL-19, IL-20, IL-21, IL-22, IL-23, IL-24, IL-25, IL-26, IL-27, IL-28, IL-29, IL-30, IL-31, IL-32, IL-33, INF-альфа, IFN-бета, INF-гамма, GM-CSF, G-CSF, M-CSF, LT-бета или TNF-альфа, факторы роста, такие как hGH.
Дополнительными добавками, которые могут быть включены в фармацевтическую композицию согласно изобретению, являются эмульгаторы, такие как, например, твин®; увлажнители, такие как, например, лаурилсульфат натрия; красители; средства, придающие вкус, фармацевтические носители; средства для формирования таблеток; стабилизаторы; антиоксиданты; консерванты.
Фармацевтическая композиция согласно изобретению также дополнительно может содержать любое дополнительное соединение, которое, как известно, является иммуностимулирующим благодаря его аффинности связывания (в качестве лиганда) с человеческими Toll-подобными рецепторами TLR1, TLR2, TLR3, TLR4, TLR5, TLR6, TLR7, TLR8, TLR9, TLR10 или вследствие его аффинности связывания (в качестве лиганда) с мышиными Toll-подобными рецепторами TLR1, TLR2, TLR3, TLR4, TLR5, TLR6, TLR7, TLR8, TLR9, TLR10, TLR11, TLR12 или TLR13.
Фармацевтическая композиция согласно изобретению также может дополнительно или альтернативно содержать иммуностимулирующую РНК, т.е. РНК, полученную из иммуностимулирующей РНК, которая запускает или повышает (врожденный) иммунный ответ. Предпочтительно, такая иммуностимулирующая РНК может быть в общем такой, которая определена в настоящем описании выше.
Другим классом соединений, которые можно добавлять к фармацевтической композиции согласно изобретению в данном контексте, могут быть CpG-нуклеиновые кислоты, в частности, CpG-РНК или CpG-ДНК. CpG-РНК или CpG-ДНК могут представлять собой однонитевую CpG-ДНК (он-CpG-ДНК), двунитевую CpG-ДНК (дн-ДНК), однонитевую CpG-РНК (он-CpG-РНК) или двунитевую CpG-РНК (дн-CpG-РНК). CpG-нуклеиновая кислота предпочтительно имеет форму CpG-РНК, более предпочтительно форму однонитевой CpG-РНК (он-CpG-РНК). CpG-нуклеиновая кислота предпочтительно содержит по меньшей мере одну или несколько (митогенных) цитозин/гуанин-динуклеотидных последовательностей (CpG-мотивов). Согласно первому предпочтительному альтернативному варианту, по меньшей мере один CpG-мотив, входящий в такие последовательности, другими словами C (цитозин) и G (гуанин) CpG-мотива, не метилирован. Все другие цитозины или гуанины, необязательно входящие в состав таких последовательностей, могут быть либо метилированными, либо неметилированными. Однако согласно следующему предпочтительному альтернативному варианту C (цитозин) и G (гуанин) CpG-мотива также могут присутствовать в метилированной форме.
В контексте настоящего изобретения переносимая нуклеиновая кислота в комплексе полимерного носителя и переносимого вещества, входящего в состав фармацевтической композиции согласно изобретению, предпочтительно представляет собой нуклеиновую кислоту, которая определена выше. Более предпочтительно, нуклеиновая кислота комплекса полимерного носителя и переносимого вещества, предпочтительно входящего в состав фармацевтической композиции, обычно представляет собой иммуностимулирующую нуклеиновую кислоту, которая определена в настоящем описании, например, CpG-ДНК или иммуностимулирующую РНК (исРНК), предпочтительно исРНК. Альтернативно или дополнительно, нуклеиновая кислота комплекса полимерного носителя и переносимого вещества, предпочтительно входящего в состав фармацевтической композиции, представляет собой кодирующую последовательность нуклеиновой кислоты, которая определена в настоящем описании, предпочтительно кДНК или мРНК, более предпочтительно кодирующую адъювантный белок, предпочтительно белок, который определен в настоящем описании. В данном контексте комплекс полимерного носителя и переносимого вещества обычно инициирует врожденный иммунный ответ у пациента, подвергаемого лечению.
В конкретном варианте в данном контексте предпочтительно, чтобы адъювантный белок являлся компонентом комплекса полимерного носителя и переносимого вещества, и предпочтительно полимерного носителя.
Согласно следующему аспекту настоящее изобретение также относится к наборам, в частности наборам частей, содержащим в качестве компонентов отдельно или в сочетании с необязательными дополнительными ингредиентами, и включающим (в качестве первого компонента):
(A) комплекс полимерного носителя и переносимого вещества, содержащий:
a) (в качестве носителя) полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами; и
b) (в качестве переносимого вещества) по меньшей мере одну молекулу нуклеиновой кислоты,
и (в качестве второго компонента):
(B) по меньшей мере один антиген, который выбран из:
(i) антигена из патогена, ассоциированного с инфекционной болезнью;
(ii) антигена, ассоциированного с аллергией или аллергическим заболеванием;
(iii) антигена, ассоциированного с аутоиммунным заболеванием; или
(iv) антигена, ассоциированного с раком или опухолевым заболеванием, при этом в некоторых вариантах антиген, ассоциированный с раком или опухолевым заболеванием, представляет собой другой антиген, отличный от антигена, содержащего: (x) идиотипический иммуноглобулин (например, идиотипическое антитело или идиотипический B-клеточный рецептор); и/или (y) по меньшей мере один идиотипический T-клеточный рецептор,
или фрагмент, вариант и/или производное указанного антигена;
в каждом случае, который определен в настоящем описании, и необязательно технические инструкции с информацией о введении и дозе комплекса полимерного носителя и переносимого вещества и по меньшей мере одного антигена. Такие наборы, предпочтительно наборы частей, можно использовать, например, в случае любых применений, которые определены в настоящем описании. Такие наборы, когда они представляют собой наборы, состоящие из частей, могут, кроме того, содержать каждый компонент фармацевтической композиции согласно изобретению в разных частях набора.
В некоторых вариантах наборов согласно настоящему изобретению антиген входит в состав вакцины.
Настоящее изобретение, кроме того, относится к нескольким применениям фармацевтической композиции согласно изобретению (например, содержащей адъювант вакцины) или наборов или наборов частей, содержащих фармацевтическую композицию, которые определены в настоящем описании.
В данном контексте настоящее изобретение также относится к способу трансфекции и/или обработки клетки, ткани или организма с нанесением или введением фармацевтической композиции согласно изобретению, в частности, с терапевтическими целями. В данном контексте обычно после получения фармацевтической композиции согласно изобретению фармацевтическую композицию согласно изобретению предпочтительно вводят в клетку, ткань или организм, предпочтительно используя любой из способов введения, который описан в настоящей публикации. Способ трансфекции и/или обработки клетки может быть осуществлен in vitro, in vivo или ex vivo.
Кроме того, настоящее изобретение относится к применению фармацевтической композиции или наборов или наборов частей в каждом случае, который определен в настоящем описании, для терапии и/или в качестве лекарственного средства, предпочтительно в качестве вакцины, такой как содержащая адъювант вакцина.
Также в некоторых вариантах всех аспектов настоящего изобретения по меньшей мере один антиген не выбран из: (x) идиотипического иммуноглобулина (идиотипического антитела или идиотипического B-клеточного рецептора); или (y) по меньшей мере одного идиотипического T-клеточного рецептора; и необязательно не является фрагментом, вариантом и/или производным такого антигена.
В данном аспекте настоящего изобретения особенно предпочтительным является применение фармацевтической композиции согласно изобретению или наборов или наборов частей, содержащих фармацевтическую композицию, которые определены в настоящем описании, при лечении инфекционных болезней, аллергии или аллергических заболеваний, аутоиммунных заболеваний и рака или опухолевых заболеваний, в каждом случае, как определено в настоящем описании.
В данном контексте инфекционными болезнями предпочтительно являются бактериальные или вызванные простейшими инфекционные болезни. Такие инфекционные болезни, предпочтительно (вирусные, бактериальные или вызванные простейшими) инфекционные болезни обычно выбраны из перечня, состоящего из инфекций Acinetobacter, африканской сонной болезни (африканского трипаносомоза, СПИД (синдрома приобретенного иммунодефицита), амебиаза, анаплазмоза, сибирской язвы, аппендицита, инфекций Arcanobacterium haemolyticum, аргентинской геморрагической лихорадки, аскариоза, аспергиллеза, астровирусных инфекций, эпидермофитии стопы, бабезиоза, инфекций Bacillus cereus, бактериального менингита, бактериальной пневмонии, бактериального вагиноза (BV), бактероидных инфекций, балантидиаза, инфекций Baylis ascaris, бильгарциоза, инфекций BK-вирусами, черной пьедры, инфекций Blastocystis hominis, бластомикоза, боливийской геморрагической лихорадки, инфекций боррелиями (боррелиоза), ботулизма (и ботулизма у новорожденных), бычьего цепня, бразильской геморрагической лихорадки, бруцеллеза, инфекции Burkholderia, язвы Бурули, инфекции калицивирусами (норовирусом и саповирусом), кампилобактериоза, кандидоза, инфекций собачьим цепнем, болезни кошачьих царапин, болезни Шагаса (американского трипаносомоза), шанкроида, ветряной оспы, инфекций хламидиями, инфекций Chlamydia trachomatis, инфекций Chlamydophila pneumoniae, холеры, хромобластомикоза, климатического бубона, клонорхоза, инфекции Clostridium difficile, кокцидиоидомикоза, инфекции верхних дыхательных путей, колорадской клещевой лихорадки (CTF), вирусной инфекции верхних дыхательных путей (острого вирусного ринофарингита; острого ринофарингита), остроконечной кондиломы, конъюнктивита, болезни Крейтцфельдта-Якоба (CJD), геморрагической лихорадки Крым-Конго (CCHF), криптококкоза, криптоспоридиоза, кожной мигрирующей личинки (CLM), кожного лейшманиоза, циклоспориаза, цистицеркоза, цитомегаловирусных инфекций, лихорадки Денге, дерматофитоза, диентаамебиаза, дифтерии, дифиллоботриоза, донаваноза, дракункулеза, весенне-летнего менингоэнцефалита (FSME), геморрагической лихорадки Эбола, эхинококкоза, эрлихиоза, энтеробиоза (инфекции острицами), энтерококковой инфекции, энтеровирусной инфекции, эпидемического сыпного тифа, эпиглоттита, инфекционного мононуклеоза, вызванного вирусом Эпштейн-Барр, инфекционной эритемы (пятой болезни), внезапной экзантемы, фасциолопсиаза, фасциолеза, спорадической фатальной инсомнии (FFI), пятой болезни, филяриоза, отравления рыбой (сигуатеры), заражения широким лентецом, острого респираторного заболевания, пищевого отравления Clostridium perfringens, лисьего цепня, инфекции свободноживущими амебами, инфекций фузобактериями, газовой гангрены, геотрихоза, синдрома Герстманна-Штреусслера-Шейнкера (GSS)), жиардиаза, сапа, гнатостомиаза, гонореи, паховой гранулемы (донованоза, стрептококковых инфекций группы A, стрептококковых инфекций группы B, инфекций Haemophilus influenzae, болезни рук, стоп и полости рта (HFMD), хантавирусного легочного синдрома (HPS), инфекций Helicobacter pylori, гемолитико-уремического синдрома (HUS), геморрагической лихорадки с почечным синдромом (HFRS), хенипавирусных инфекций, гепатита A, гепатита B, гепатита C, гепатита D, гепатита E, простого герпеса, простого герпеса типа I, простого герпеса типа II, опоясывающего герпеса, гистоплазмоза, бородавок, анкилостомоза, инфекций бокавирусом человека, эрлихиоза человека, вызванного ewingii, гранулоцитарного анаплазмоза человека (HGA), инфекций метапневмовирусом человека, моноцитарного эрлихиоза человека, инфекций вирусом папилломы человека (HPV), инфекций вирусом парагриппа человека, гименолепидоза, гриппа, изоспориаза, японского энцефалита, болезни Кавасаки, кератита, инфекций Kingella kingae, куру, лямблиоза (жиардиаза), лихорадки Ласса, легионеллеза (болезни легионеров, лихорадки Понтиак), лейшманиоза, лепры, лептоспироза, педикулеза, листериоза, боррелиоза Лайма, болезни Лайма, лимфатического филяриотоза (элефантиаза), лимфоцитарного хориоменингита, малярии, геморрагической лихорадки Марбург (MHF), вируса Марбург, кори, мелиоидоза (болезни Уитмора), менингита, менингококкового заболевания, метагонимоза, микроспоридиоза, миниатюрного цепня, выкидыша (воспаления простаты), контагиозного моллюска (MC); мононуклеоза, эпидемического паротита, мышиного тифа (эндемического тифа), мицетомы, Mycoplasma hominis, Mycoplasma pneumonia, миаза, дерматита подгузников/пеленочного дерматита, неонатального конъюнктивита (офтальмии новорожденных), неонатального сепсиса (хориоамнионита), нокардиоза, номы, инфекции вирусом Норфолк, онхоцеркоза (речной слепоты), остеомиелита, отита среднего уха, паракокцидиоидомикоза (южно-американского бластомикоза), парагонимоза, паратифа, пастереллеза, головного педикулеза (головных вшей), нательного педикулеза (нательных вшей), лобкового педикулеза (лобковых вшей), воспаления органов таза (PID), коклюша (судорожного кашля), железистой лихорадки Пфейффера, чумы, пневмококковых инфекций, плазмоклеточной пневмонии (PCP), пневмонии, полиомиелита (детской хромоты), полиомиелита, свиного цепня, инфекций превотеллами, первичного амебного менингоэнцефалита (PAM), прогрессирующей мультифокальной лейкоэнцефалопатии, ложного крупа, орнитоза, Q-риккетсиоза, кроличьей лихорадки, бешенства, болезни укуса крыс, синдрома Рейтера, инфекций респираторно-синцитиальным вирусом (RSV), риноспоридиоза, риновирусных инфекций, риккетсиоза, везикулярного риккетсиоза, лихорадки долины Рифт (RVF), пятнистой лихорадки Скалистых гор (RMSF), ротавирусных инфекций, краснухи, паратифа, вызванного сальмонеллами, тифа, вызванного сальмонеллами, сальмонеллеза, SARS (тяжелого острого респираторного синдрома), чесотки, скарлатины, шистосоматоза (бильгарциоза), клещевого тропического тифа, сепсиса, шигеллеза (бактериальной дизентерии), опоясывающего лишая, натуральной оспы (оспы), мягкого шанкра, споротрихоза, стафилококкового пищевого отравления, стафилококковых инфекций, стронгилоидоза, сифилиса, тениоза, столбняка, трехдневной лихорадки, клещевого энцефалита, дерматомикоза бороды и усов (стафилококкового фолликулита), глубокой трихофитии (дерматомикоза волосистой части головы), дерматофитии туловища (дерматомикоза гладкой кожи), пахового дерматомикоза (паховой эпидермофитии), дерматофитии ладоней и кистей рук (трихофитии рук), черного лишая, дерматофитии стопы (эпидермофитии стопы), дерматофитного онихомикоза (онихомикоза), отрубевидного лишая (разноцветного лишая), токсокароза (глазной формы синдрома мигрирующей личинки (OLM) и висцеральной формы синдрома мигрирующей личинки (VLM)), токсоплазмоза, трихинеллеза, трихомоноза, трихоуроза (инфекции власоглавом), триппера, трипаносомоза (сонной болезни), японской речной лихорадки, туберкулеза, туляремии, тифа, сыпного тифа, инфекций Ureaplasma urealyticum, вагинита (кольпита), вариантов болезни Крейтцфельдта-Якоба (vCJD, nvCJD), венесуэльского энцефалита лошадей, венесуэльской геморрагической лихорадки, вирусной пневмонии, висцерального лейшманиоза, бородавок, лихорадки Западного Нила, западного энцефалита лошадей, белой пьедры (белого микоза), коклюша, дрожжевой пятнистости, желтой лихорадки, инфекций Yersinia pseudotuberculosis, иерсиниоза и зигомикоза.
Аллергия или аллергические заболевания предпочтительно выбраны из аллергии на пыльцу (аллергия на пыльцу травянистых растений, пыльцу деревьев (например, пыльцу ореха, березы, ольхи, ясеня), цветочную пальцу, пыльцу трав (например, пыльцу полыни обыкновенной), аллергию на пылевого клеща, аллергию на плесень (например, аллергию на Acremonium, Aspergillus, Cladosporium, Fusarium, Mucor, Penicillium, Rhizopus, Stachybotrys, Trichoderma или Alternaria), аллергию на домашних питомцев (аллергию на животных, например, кошек, собак, лошадей), пищевую аллергию (например, аллергию на рыб (например, окуня, треску, камбалу), морепродукты (например, краба, лобстера, креветок), яйца, пшеницу, орехи (например, арахис, миндаль, кешью, грецкий орех), сою, молоко и т.д.) или аллергию на укус насекомых (например, аллергию на яд насекомых, например, яд ос, пчел, шершней, муравьев, комаров или клещей).
Согласно другому конкретному варианту, заболевания, которые определены в настоящем описании, включают аутоиммунные заболевания, которые указаны далее. Аутоиммунные заболевания предпочтительно выбраны из болезни Аддисона (аутоиммунного адреналита, аддисоновой болезни), очаговой алопеции, анемии Аддисона (болезни Бирмера), аутоиммунной гемолитической анемии (AIHA), аутоиммунной гемолитической анемии (AIHA) холодового типа (холодовой гемагглютининовой болезни, холодовой аутоиммунной гемолитической анемии (AIHA) (холодовой агглютининовой болезни), (CHAD)), аутоиммунной гемолитической анемии (AIHA) теплового типа (тепловой AIHA, тепловой аутоиммунной гемолитической анемии (AIHA)), аутоиммунной гемолитической анемии Доната-Ландштейнера (пароксизмальной холодовой гемоглобинурии), антифосфолипидного синдрома (APS), атеросклероза, аутоиммунного артрита, височного артериита, артериита Такаясу (болезни Такаясу, заболевания дуги аорты), височного артериита/узелкового периартериита, аутоиммунного хронического гастрита, аутоиммунного бесплодия, аутоиммунного заболевания внутреннего уха (AIED), базедовой болезни (Morbus Basedow), болезни Бехтерова (Morbus Bechterew, анкилозирующего спондилита, spondylitis ankylosans), синдрома Бехчета (болезни Бехчета), заболевания кишечника, включая аутоиммунное воспалительное заболевание кишечника (включая язвенный колит (Morbus Crohn, болезнь Крона)), кардиомиопатии, в частности аутоиммунной кардиомиопатии, идиопатической дилятационной кардиомиопатии (DCM), целиакии-спру-дерматита (глутеновой энтеропатии), синдрома хронической усталости и иммунной дисфункции (CFIDS), хронической воспалительной демиелинизирующей полиневропатии (CIDP), хронического полиартрита, синдрома Черджа-Стросса, рубцующегося пемфигоида, синдрома Когана, CREST-синдрома (синдрома с кальцинозом кожи, феноменом Рейно, расстройствами моторики пищевода, склеродактилией и телеангиэктозией), болезни Крона (Morbus Crohn, язвенного колита), герпетиформного дерматита Дюринга, дерматологических аутоиммунных заболеваний, дерматомиозита, диабета, сахарного диабета типа 1 (диабета типа I, инсулинозависимого сахарного диабета), сахарного диабета типа 2 (диабета типа II), эссенциальной криоглобулинемии смешанного типа, эссенциальной криоглобулинемии смешанного типа, фибромиалгии, фибромиозита, синдрома Гудпасчера (анти-GBM-опосредованного гломерулонефрита), болезни «трансплантат против хозяина», синдрома Гийена-Барре (GBM, полирадикулонейрита), гематологических аутоиммунных заболеваний, тиреоидита Хашимото, гемофилии, приобретенной гемофилии, гепатита, аутоиммунного гепатита, особых аутоиммунных форм хронического гепатита, идиопатического легочного фиброза (IPF), идиопатической тромбоцитопенической пурпуры, иммуно-тромбоцитопенической пурпуры (болезни Верхофа; ITP), IgA-нефропатии, бесплодия, аутоиммунного бесплодия, ювенильного ревматоидного артрита (болезни Стилла, синдрома Стилла), синдрома Ламберта-Итона, красного плоского лишая, склерозирующего лишая, красной волчанки, системной красной волчанки (SLE), красной волчанки (дискоидной формы), артрита Лайма (болезни Лайма, артрита при боррелиозе), болезни Меньера (Morbus Meniere); смешанного соединительно-тканного заболевания (MCTD), рассеянного склероза (MS, диссеминированного энцефаломиелита, болезни Шарко), тяжелой псевдопаралитической миастении (миастении, MG), миозита, полимиозита, нервных аутоиммунных болезней, нейродермита, вульгарного пемфигуса, буллезного пемфигоида, рубцующегося пемфигоида; нодозного полиартериита (нодозного периартериита), полихондрита (панхондрита), полигландулярного (аутоиммунного) синдрома (PGA-синдрома, синдрома Шмидта), ревматической полимиалгии, первичной агаммаглобулинемии, первичного билиарного цирроза PBC, первичного аутоиммунного холангита, прогрессирующего системного склероза (PSS), псориаза, вульгарного псориаза, феномена Рейно, синдрома Рейтера (Morbus Reiter, уретро-конъюнктиво-синовиального синдрома)), ревматоидного артрита (RA, хронического полиартрита, ревматоидного заболевания суставов, острой ревматической лихорадки), саркоидоза (болезни Бека, болезни Бенье-Бека-Шауманна), синдрома мышечной скованности, склеродермии, склеродермы, синдрома Шегрена, симпатической офтальмии; временной непереносимости глютена, отторжения трансплантированного органа, увеита, аутоиммунного увеита, васкулита, витилиго (лейкодермы, пестрой кожи) и болезни Вегнера (Morbus Wegner, гранулематоза Вегнера).
Кроме того, рак или опухолевые заболевания предпочтительно выбраны из меланом, злокачественных меланом, карцином ободочной кишки, лимфом, сарком, бластом, почечных карцином, опухолей желудочно-кишечного тракта, глиом, опухолей простаты, рака мочевого пузыря, опухолей почек, рака желудка, рака пищевода, рака поджелудочной железы, рака печени, карцином молочной железы (= рака молочной железы), рака матки, рака шейки матки, острого миелоидного лейкоза (AML), острого лимфоидного лейкоза (ALL), хронического миелоидного лейкоза (CML), хронического лимфоцитарного лейкоза (CLL), гепатом, индуцированных разными вирусами опухолей, таких как, например, индуцированные вирусом папилломы карциномы (например, карциномы шейки матки = рака шейки матки), аденокарцином, индуцированных вирусом герпеса опухолей (например, лимфомы Беркитта, EBV-индуцированной B-клеточной лимфомы), индуцированных вирусом гепатита B опухолей (гепатоклеточных карцином), HTLV-1- и HTLV-2-индуцированных лимфом, нейромы слухового нерва, карцином легкого (= рака легкого = карциномы бронхов), мелкоклеточных карцином легкого, рака глотки, карциномы ануса, глиобластомы, карциномы прямой кишки, астроцитомы, опухолей головного мозга, ретинобластомы, базалиомы, метастазов головного мозга, медуллобластом, рака влагалища, рака поджелудочной железы, рака семенников, синдрома Ходжкина, менингиом, болезни Шнибергера, опухоли гипофиза, фунгоидной гранулемы, карциноидов, невриномы, спиналиомы, лимфомы Беркитта, рака гортани, рака почек, тимомы, карциномы тела матки, рака костей, неходжкинских лимфом, рака уретры, CUP-синдрома, опухолей головы/шеи, олигодендроглиомы, рака вульвы, рака кишечника, карциномы ободочной кишки, карциномы пищевода (= рака пищевода), поражения бородавками, опухолей тонкого кишечника, краниофарингиомы, карциномы яичника, опухолей половых органов, рака яичника (= карциномы яичника), карциномы поджелудочной железы (= рака поджелудочной железы), карциномы эндометрия, метастазов печени, рака пениса, рака языка, рака желчного пузыря, лейкоза, плазмоцитомы, опухоли века, рака простаты (= опухолей простаты) и т.д.
В следующем аспекте настоящее изобретение относится к комплексу полимерного носителя и переносимого вещества, который определен в настоящее описании, такому как комплекс, содержащий:
a) (в качестве носителя) полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами; и
b) (в качестве переносимого вещества) по меньшей мере одну молекулу нуклеиновой кислоты
для применения в терапии в сочетании по меньшей мере с одним антигеном, предпочтительно белковым или пептидным антигеном или его фрагментом, вариантом и/или производным, в каждом случае таким, который определен в настоящем описании, в частности, в лечении инфекционных болезней, аллергии или аллергических заболеваний, аутоиммунных заболеваний и рака или опухолевых заболеваний, которые определены выше.
Кроме того, настоящее изобретение относится по меньшей мере к одному антигену, предпочтительно белковому или пептидному антигену или его фрагменту, варианту и/или производному, который в каждом случае определен в настоящем описании, для применения в терапии в сочетании с комплексом полимерного носителя и переносимого вещества, который определен в настоящем описании, таким как комплекс, содержащий:
a) (в качестве носителя) полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами; и
b) (в качестве переносимого вещества) по меньшей мере одну молекулу нуклеиновой кислоты;
в частности, в лечении инфекционных болезней, аллергии или аллергических заболеваний, аутоиммунных заболеваний и рака или опухолевых заболеваний, которые определены выше.
В некоторых вариантах таких аспектов настоящего изобретения антиген входит в состав вакцины, такой как коммерчески доступная вакцина.
В данном контексте «в сочетании» означает, что разные компоненты (комплекс полимерного носителя и переносимого вещества и по меньшей мере один антиген или его фрагмент, вариант и/или производное) могут быть представлены вместе в одной и той же композиции или могут быть приготовлены отдельно в разных композициях, т.е. одной композиции, содержащей или предоставляющей комплекс полимерного носителя и переносимого вещества, который определен в настоящем описании, и одной дополнительной композиции, содержащей по меньшей мере один антиген или его фрагмент, вариант и или производное, которые определены в настоящем описании. В случае предоставления в разных композициях комплекс полимерного носителя и переносимого вещества и по меньшей мере один антиген или его фрагмент, вариант и/или производное можно вводить по отдельности в течение определенного периода времени (со сдвигом по времени) и/или можно вводить в разные места введения и/или разными путями введения. Это означает, что комплекс полимерного носителя и переносимого вещества можно вводить, например, перед, одновременно или после по меньшей мере одного антигена или его фрагмента, варианта и/или производного, или наоборот. Последовательное введение означает, что каждый компонент, используемый в терапии, вводят в пределах периода времени примерно 48 часов, 24 часов, 12 часов, 8 часов, 6 часов, 4 часа, 2 часа, 1 час, 30 минут, 15 минут или 5 минут друг от друга.
В следующем аспекте настоящее изобретение относится к фармацевтической упаковке, содержащей:
(A) комплекс полимерного носителя и переносимого вещества, содержащий:
a) (в качестве носителя) полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами, и
b) (в качестве переносимого вещества) по меньшей мере одну молекулу нуклеиновой кислоты,
которые определены в настоящем описании; и
(B) инструкции, описывающие применение указанного комплекса полимерного носителя и переносимого вещества в терапии в сочетании по меньшей мере с одним антигеном или его фрагментом, вариантом и/или производным, которые определены в настоящем описании.
Фармацевтическая упаковка может дополнительно содержать по меньшей мере один антиген или его фрагмент, вариант и/или производное, которые определены в настоящем описании.
Кроме того, настоящее изобретение относится в дополнительном варианте осуществления к фармацевтической упаковке, содержащей:
(A) по меньшей мере один антиген или его фрагмент, вариант и/или производное, в каждом случае такие, которые определены в настоящем описании;
и
(B) инструкции, описывающие применение указанного антигена или его фрагмента, варианта и/или производного в терапии в сочетании с комплексом полимерного носителя и переносимого вещества, который определен в настоящем описании.
Фармацевтическая упаковка может дополнительно содержать комплекс полимерного носителя и переносимого вещества, содержащий:
a) (в качестве носителя) полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами, и
b) (в качестве переносимого вещества) по меньшей мере одну молекулу нуклеиновой кислоты,
которые определены в настоящем описании.
В данном контексте изобретение, кроме того, относится к применению компонентов, включенных в определенные выше фармацевтические упаковки, в лечении конкретного заболевания (показания), выбранного из инфекционной болезни, аллергии или аллергического заболевания, аутоиммунного заболевания или рака или опухолевого заболевания, которые определены выше. Соответствующее заболевание может представлять собой заболевание, которое описано в настоящей публикации.
В настоящем изобретении, если не указано иное, разные признаки альтернативных вариантов и вариантов осуществления изобретения можно в соответствующих случаях сочетать друг с другом.
Итак, в предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов, соответствующих формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmCn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты согласно любой из SEQ ID NO: 15-108 и 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов, соответствующих формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmСn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген,
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбраны из:
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов, соответствующих формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmСn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген;
при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из:
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием;
и предпочтительно при этом белковый или пептидный антиген и/или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmСn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген;
при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно антигена из патогена, ассоциированного с инфекционной болезнью,
более предпочтительно антигена из патогена, выбранного из вируса бешенства, вируса гепатита B, вируса папилломы человека (hPV), Bacillus anthracis, респираторно-синцитиального вируса (RSV), вируса простого герпеса (HSV), вируса гриппа и Mycobacterium tuberculosis,
более предпочтительно антигена из патогена, выбранного из вируса бешенства, вируса гепатита B, вируса папилломы человека (hPV);
и предпочтительно при этом белковый или пептидный антиген и/или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmСn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген;
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно антигена из патогена, ассоциированного с инфекционной болезнью,
более предпочтительно антигена из патогена, выбранного из вируса бешенства, вируса гепатита B, вируса папилломы человека (hPV), Bacillus anthracis, респираторно-синцитиального вируса (RSV), вируса простого герпеса (HSV), вируса гриппа и Mycobacterium tuberculosis,
еще более предпочтительно антигена из вируса бешенства, наиболее предпочтительно антигена из вируса бешенства, который выбран из нуклеопротеина (N), фосфопротеина (P), белка матрикса (M), гликопротеина (G) и вирусной РНК-полимеразы (L);
и предпочтительно при этом белковый или пептидный антиген и или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше, такой как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmСn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и, по меньшей мере, один белковый или пептидный антиген;
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно антигена из патогена, ассоциированного с инфекционной болезнью, более предпочтительно антигена из патогена, выбранного из вируса бешенства, вируса гепатита B, вируса папилломы человека (hPV), Bacillus anthracis, респираторно-синцитиального вируса (RSV), вируса простого герпеса (HSV), вируса гриппа и Mycobacterium tuberculosis,
еще более предпочтительно антигена из вируса гепатита B, наиболее предпочтительно антигена из вируса гепатита B, который выбран из поверхностного антигена гепатита B (HBsAg), корового антигена гепатита B (HbcAg), ДНК-полимеразы вируса гепатита B, белка HBx, среднего поверхностного белка preS2, большого S-белка, вирусного белка VP1, вирусного белка VP2, вирусного белка VP3 и вирусного белка VP4;
и предпочтительно при этом белковый или пептидный антиген и/или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmCn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген;
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно антигена из патогена, ассоциированного с инфекционной болезнью, более предпочтительно антигена из патогена, выбранного из вируса бешенства, вируса гепатита B, вируса папилломы человека (hPV), Bacillus anthracis, респираторно-синцитиального вируса (RSV), вируса простого герпеса (HSV), вируса гриппа и Mycobacterium tuberculosis,
еще более предпочтительно антигена из вируса гриппа, наиболее предпочтительно антигена из вируса гриппа, который выбран из гемагглютинина (HA), нейраминидазы (NA), нуклеопротеина (NP), белка M1, белка M2, белка NS1, белка NS2 (белок NEP: белок ядерного экспорта), белка PA, белка PB1 (основной белок полимеразы 1), белка PB1-F2 и белка PB2 вируса гриппа;
и предпочтительно при этом белковый или пептидный антиген и/или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmCn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген;
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно антигена из патогена, ассоциированного с инфекционной болезнью, предпочтительно антигена из патогена, выбранного из вируса бешенства, вируса гепатита B, вируса папилломы человека (hPV), Bacillus anthracis, респираторно-синцитиального вируса (RSV), вируса простого герпеса (HSV), вируса гриппа и Mycobacterium tuberculosis,
более предпочтительно антигена из вируса папилломы человека (hPV), еще более предпочтительно антигена из вируса папилломы человека (hPV), который выбран из белка E1, белка E2, белка E3, белка E4, белка E5, белка E6, белка E7, белка E8, белка L1 и белка L2;
и предпочтительно при этом белковый или пептидный антиген и или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmCn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген;
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно антигена из патогена, ассоциированного с инфекционной болезнью,
предпочтительно антигена из патогена, выбранного из вируса бешенства, вируса гепатита B, вируса папилломы человека (hPV), Bacillus anthracis, респираторно-синцитиального вируса (RSV), вируса простого герпеса (HSV), вируса гриппа и Mycobacterium tuberculosis,
более предпочтительно антигена из Bacillus anthracis, еще более предпочтительно антигена из Bacillus anthracis, который выбран из защитного антигена (PA), вызывающего отек фактора (EF), летального фактора (LF) и гомологичных белков S-слоя (SLH);
и предпочтительно при этом белковый или пептидный антиген и/или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmCn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген;
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно антигена из патогена, ассоциированного с инфекционной болезнью,
более предпочтительно антигена из патогена, выбранного из вируса бешенства, вируса гепатита B, вируса папилломы человека (hPV), Bacillus anthracis, респираторно-синцитиального вируса (RSV), вируса простого герпеса (HSV), вируса гриппа и Mycobacterium tuberculosis,
еще более предпочтительно антигена из респираторно-синцитиального вируса (RSV),
наиболее предпочтительно антигена из респираторно-синцитиального вируса (RSV), который выбран из белка слияния (F), нуклеокапсидного белка (N), фосфопротеина (P), белка матрикса (M), гликопротеина (G), большого белка (L; РНК-полимераза), неструктурного белка 1 (NS1), неструктурного белка 2 (NS2), малого гидрофобного белка (SH), фактора элонгации M2-1 и белка регуляции транскрипции M2-2;
и предпочтительно при этом белковый или пептидный антиген и/или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmCn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген;
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно антигена из патогена, ассоциированного с инфекционной болезнью,
более предпочтительно антигена из патогена, выбранного из вируса бешенства, вируса гепатита B, вируса папилломы человека (hPV), Bacillus anthracis, респираторно-синцитиального вируса (RSV), вируса простого герпеса (HSV), вируса гриппа и Mycobacterium tuberculosis,
еще более предпочтительно антигена из вируса простого герпеса (HSV), наиболее предпочтительно антигена из вируса простого герпеса (HSV), который выбран из гликопротеина L (UL1), урацил-ДНК-гликозилазы UL2, белка UL3, белка UL4, белка UL5 репликации ДНК, портального белка UL6, белка созревания вириона UL7, ДНК-геликазы UL8, белка, связывающего начало репликации, UL9, гликопротеина M (UL10), белка UL11, щелочной экзонуклеазы UL12, сериновой-треониновой протеинкиназы UL13, белка тегумента UL14, терминазы (UL15), белка тегумента UL16, белка UL17, капсидного белка VP23 (UL18), основного капсидного белка VP5 (UL19), мембранного белка UL20, белка тегумента UL21, гликопротеина H (UL22), тимидинкиназы UL23, белка UL24, белка UL25, капсидного белка P40 (UL26, VP24, VP22A), гликопротеина B (UL27), белка ICP18.5 (UL28), основного ДНК-связывающего белка ICP8 (UL29), ДНК-полимеразы UL30, белка ядерного матрикса UL31, гликопротеина оболочки UL32, белка UL33, белка внутренней ядерной мембраны UL34, капсидного белка VP26 (UL35), большого белка тегумента UL36, белка сборки капсида UL37, белка VP19C (UL38), рибонуклеотидредуктазы (большой субъединицы) UL39, рибонуклеотидредуктазы (малой субъединицы) UL40, белка тегумента/белка выключения генов хозяина вирионом VHS (UL41), фактора процессивности ДНК-полимеразы UL42, мембранного белка UL43, гликопротеина C (UL44), мембранного белка UL45, белков тегумента VP11/12 (UL46), белка тегумента VP13/14 (UL47), белка созревания вириона VP16 (UL48, альфа-TIF), белка оболочки UL49, dUTP-дифосфатазы UL50, белка тегумента UL51, белка комплекса ДНК-геликаза/праймаза UL52, гликопротеина K (UL53), белка регуляции транскрипции IE63 (ICP27, UL54), белка UL55, белка UL56, белка вирусной репликации ICP22 (IE68, US1), белка US2, сериновой/треониновой протеинкиназы US3, гликопротеина G (US4), гликопротеина J (US5), гликопротеина D (US6), гликопротеина I (US7), гликопротеина E (US8), белка тегумента US9, белка капсида/тегумента US10, белка Vmw21 (US11), белка ICP47 (IE12, US12), основного активатора транскрипции ICP4 (IE175, RS1), убиквитинлигазы E3 ICP0 (IE110), связанного с латентностью белка 1 (LRP1), связанного с латентностью белка 2 (LRP2), фактора нейровирулентности RL1 (ICP34.5) и ассоциированного с латентностью транскрипта (LAT);
и предпочтительно при этом белковый или пептидный антиген и/или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmCn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген;
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно антигена из патогена, ассоциированного с инфекционной болезнью,
более предпочтительно антигена из патогена, выбранного из вируса бешенства, вируса гепатита B, вируса папилломы человека (hPV), Bacillus anthracis, респираторно-синцитиального вируса (RSV), вируса простого герпеса (HSV) и Mycobacterium tuberculosis,
еще более предпочтительно антигена из Mycobacterium tuberculosis,
наиболее предпочтительно антигена из Mycobacterium tuberculosis, который выбран из белка ESAT-6, белка ESX-1, белка CFP10, белка TB10.4, белка MPT63, белка MPT64, белка MPT83, белка MTB12, белка MTB8, белка AG85A, белка AG85B, Rpf-подобных белков, белка KATG, белка PPE18, белка MTB32, белка MTB39, кристаллина, белка HSP65, белка PST-S и белка HBHA, 10-кДа фильтрующегося антигена EsxB, сериновой протеазы PepA, фибронектин-связывающего белка D FbpD, секретируемого белка MPT51, периплазматического фосфат-связывающего липопротеина PSTS1 (PBP-1), периплазматического фосфат-связывающего липопротеина PSTS3 (PBP-3, Phos-1), белка PPE-семейства PPE14, белка PPE-семейства PPE68, белка MTB72F, молекулярного шаперона DnaK, липопротеина клеточной поверхности MPT83, липопротеина P23, пермеазного белка системы транспорта фосфата PstA, антигена 14 кДа, фибронектин-связывающего белка C FbpC1, аланиндегидрогеназы TB43 и глутаминсинтетазы 1;
и предпочтительно при этом белковый или пептидный антиген и/или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиция, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmCn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген;
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно белкового или пептидного антигена, который ассоциирован с аллергией или аллергическим заболеванием и получен из источника, выбранного из перечня, состоящего из: пыльцы трав, пыльцы деревьев, цветочной пыльцы, пыльцы травянистых растений, пылевых клещей, плесени, животных, пищевых продуктов и яда насекомых, предпочтительно пыльцы деревьев, цветочной пыльцы, пыльцы травянистых растений, пылевых клещей, пищевых продуктов и яда насекомых, наиболее предпочтительно аллергена из указанного выше перечня,
и предпочтительно при этом белковый или пептидный антиген и/или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmCn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген,
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно антигена, ассоциированного с аутоиммунным заболеванием,
более предпочтительно антигена, ассоциированного с рассеянным склерозом (MS); диабетом типа I; аутоиммунным увеитом; тяжелой псевдопаралитической миастенией; острой ревматической лихорадкой; артритом; синдромом Шегрена; красной волчанкой; атеросклерозом; идиопатической дилятационной кардиомиопатией (DCM); миозитом или склеродермией,
еще более предпочтительно антиген выбран из группы, состоящей из основного белка миелина (MBP), белка протеолипида (PLP) и гликопротеина миелина олигодендроцитов (MOG), CD44, препроинсулина, проинсулина, инсулина, декарбоксилазы глутаминовой кислоты (GAD65), антигена 2 инсулиномы, подобного тирозинфосфатазе (IA2), переносчика цинка (ZnT8) и белка теплового шока 60 (HSP60), межфоторецепторного ретиноид-связывающего белка (IRBP), рецептора ацетилхолина AchR и инсулиноподобного фактора роста 1 (IGF-1R), M-белка из бета-гемолитических стрептококков (псевдоаутоантиген), фактора, ингибирующего миграции макрофагов, RNP-комплекса Ro/La, альфа- и бета-фодрина, аутоантигена островковых клеток, поли(ADP)рибоза-полимеразы (PARP), NuMA, NOR-90, аутоантигена Ro60 и антигена p27, аутоантигена Ro60, липопротеинов низкой плотности, Sm-антигенов малого ядерного рибонуклеопротеинового комплекса U-1 (B/B', D1, D2, D3, E, F, G) и рибонуклеопротеинов RNP, oxLDL, бета(2)GPI, HSP60/65 и oxLDL/бета(2)GPI, бета(1)-адренергического рецептора сердца, гистидил-тРНК-синтетазы (HisRS), топоизомеразы I, IL-17 или белков теплового шока;
и предпочтительно при этом белковый или пептидный антиген и/или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
При условии, что антиген ассоциирован с аутоиммунным заболеванием, кроме того, может быть предпочтительной ситуация, когда антиген является идиотипом иммуноглобулина или идиотипом T-клеточного рецептора лимфоидной клетки, предпочтительно B-клетки или T-клетки. Такие лимфоидные клетки, например, B-клетки или T-клетки, могут быть ответственны за разрушение клеток организма, таких как, например, бета-клетки поджелудочной железы, если они ошибочно запрограммированы узнавать и бороться против собственных эпитопов организма. В данном контексте идиотип иммуноглобулина можно понимать, как пептид или белок, имеющий конкретную молекулярную форму вариабельной области иммуноглобулина, экспрессируемого конкретным типом B-клеток. Такой идиотип можно использовать в качестве антигена, чтобы вызвать иммунный ответ, направленный против такого конкретного типа B-клеток, например, против злокачественных B-клеток. Идиотип T-клеточного рецептора можно понимать как пептид или белок, имеющий конкретную молекулярную форму вариабельной области T-клеточного рецептора, экспрессируемого конкретным типом T-клеток. Такой идиотип можно использовать в качестве антигена, чтобы вызвать иммунный ответ, направленный против такого конкретного типа T-клеток, например, против злокачественных T-клеток. Фармацевтическую композицию согласно изобретению можно применять, например, для вакцинации против таких ошибочно запрограммированных лимфоидных клеток. Например, лечение пациента, страдающего от аутоиммунного заболевания, такого как, например, диабет, болезнь Крона, рассеянный склероз или тому подобное, может быть осуществлено за счет разрушения лимфоидных клеток с нарушенной функцией, которые атакуют собственный организм, и последующей вакцинации фармацевтической композицией согласно изобретению.
В следующем предпочтительном варианте изобретение относится к
фармацевтической композиции, содержащей
комплекс полимерного носителя и переносимого вещества и
по меньшей мере один белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена;
при этом комплекс полимерного носителя и переносимого вещества содержит
полимерный носитель,
предпочтительно полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты, предпочтительно образованный поперечно сшитыми дисульфидными связями катионными компонентами,
более предпочтительно один или несколько пептидов согласно формуле (I) (Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa)x, которая определена выше, наиболее предпочтительно соответствующих подформуле (IA) или (IB), которые определены выше,
и по меньшей мере одну молекулу нуклеиновой кислоты,
предпочтительно молекулу нуклеиновой кислоты, содержащую, предпочтительно состоящую из последовательности нуклеиновой кислоты согласно формуле (II) GlXmGn, формуле (III) ClXmCn, формуле (IV) (NuGlXmGnNv)a или формуле (V) (NuClXmCnNv)a, которые определены выше, такую как молекула нуклеиновой кислоты, содержащая или состоящая из последовательности нуклеиновой кислоты, соответствующей любой из последовательностей SEQ ID NO: 15-108 и 122, или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична любой из последовательностей SEQ ID NO: 15-108 и 122, например, молекулу нуклеиновой кислоты, содержащую или состоящую из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122,
или молекулу нуклеиновой кислоты, которая кодирует антиген, более предпочтительно молекулу нуклеиновой кислоты, которая кодирует антиген, который представляет собой такой же антиген, что и по меньшей мере один белковый или пептидный антиген;
и при этом белковый или пептидный антиген
или фрагмент, вариант и/или производное указанного белкового или пептидного антигена выбран из
антигена из патогена, ассоциированного с инфекционной болезнью,
антигена, ассоциированного с аллергией или аллергическим заболеванием,
антигена, ассоциированного с аутоиммунным заболеванием,
антигена, ассоциированного с раком или опухолевым заболеванием,
предпочтительно антигена, ассоциированного с раком или опухолевым заболеванием, более предпочтительно антигена, выбранного из p53, CA125, EGFR, Her2/neu, hTERT, PAP, MAGE-A1, MAGE-A3, мезотелина, MUC-1, NY-ESO-1, GP100, MART-1, тирозиназы, PSA, PSCA, PSMA VEGF, VEGFR1, VEGFR2, Ras, CEA и WT1;
и предпочтительно при этом белковый или пептидный антиген и/или фрагмент, вариант и/или производное указанного белкового или пептидного антигена не включен в комплекс полимерного носителя и переносимого вещества.
В каждом из указанных вариантов комплекс полимерного носителя и переносимого вещества предпочтительно предназначен для применения в качестве адъюванта, при этом более предпочтительно по меньшей мере одна молекула нуклеиновой кислоты представляет собой иммуностимулирующую нуклеиновую кислоту, которая определена в настоящем описании, еще более предпочтительно по меньшей мере одна молекула нуклеиновой кислоты представляет собой РНК, наиболее предпочтительно иммуностимулирующую РНК (исРНК). Особенно предпочтительными переносимыми нуклеиновыми кислотами в контексте настоящего изобретения являются молекулы нуклеиновых кислот, содержащие или состоящие из последовательности нуклеиновой кислоты согласно SEQ ID NO: 105 или 122 или последовательности нуклеиновой кислоты, которая по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% и наиболее предпочтительно по меньшей мере на 95% идентична последовательности SEQ ID NO: 105 или 122.
Кроме того, в каждом из указанных вариантов комплекс полимерного носителя и переносимого вещества может представлять собой комплекс полимерного носителя и переносимого вещества, в котором катионные компоненты полимерного носителя и переносимая молекула нуклеиновой кислоты, входящие в состав указанного комплекса полимерного носителя и переносимого вещества, представлены в N/P-соотношении в диапазоне 0,1-20, или в диапазоне 0,1-5, или в диапазоне 0,1-1, или в диапазоне 0,5-0,9.
В некоторых вариантах может быть предпочтительным, при условии, что комплекс полимерного носителя и переносимого вещества содержит полимерный носитель, предпочтительно полимерный носитель, образованный поперечно сшитыми дисульфидными связями катионными компонентами, и по меньшей мере одну молекулу нуклеиновой кислоты, чтобы фармацевтическая композиция не являлась композицией, содержащей комплекс полимерного носителя и переносимого вещества, образованный поперечно сшитыми дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК 722A (SEQ ID NO: 105) или исРНК 722B (SEQ ID NO: 122) в качестве переносимой нуклеиновой кислоты, с овальбумином белковой вакцины (белком OVA).
В некоторых вариантах может быть предпочтительным, при условии, что комплекс полимерного носителя и переносимого вещества содержит полимерный носитель, предпочтительно полимерный носитель, образованный поперечным сшитыми дисульфидными связями катионными компонентами, и по меньшей мере одну молекулу нуклеиновой кислоты, чтобы фармацевтическая композиция не представляла собой композицию, содержащую комплекс полимерного носителя и переносимого вещества, образованный поперечно сшитыми дисульфидными связями катионным пептид CR12C в качестве носителя и исРНК 722A (SEQ ID NO: 105) или исРНК 722B (SEQ ID NO: 122) в качестве переносимой нуклеиновой кислоты со специфичной для овальбумина пептидной вакциной SIINFEKL
Соответственно, в некоторых вариантах может быть предпочтительным, чтобы фармацевтическая композиция не являлась композицией, содержащей комплекс полимерного носителя и переносимого вещества, образованный поперечно сшитыми дисульфидными связями катионным пептидом CR12C (SEQ ID NO: 6) в качестве носителя и исРНК 722A (SEQ ID NO: 105) или исРНК 722B (SEQ ID NO: 122) в качестве переносимой нуклеиновой кислоты, и антиген, который представляет собой овальбумин (белок OVA) (SEQ ID NO: 117).
В некоторых вариантах может быть предпочтительным, при условии, что фармацевтическая композиция содержит комплекс полимерного носителя и переносимого вещества, содержащий полимерный носитель, образованный поперечно сшитыми дисульфидными связями катионными компонентами, и по меньшей мере, одну молекулу нуклеиновой кислоты, чтобы по меньшей мере один антиген не являлся антигеном, ассоциированным с раком или опухолевым заболеванием, в частности лимфомой или ассоциированным с лимфомой заболеванием, при этом указанный антиген является идиотипом иммуноглобулина лимфоидной клетки крови или идиотипом T-клеточного рецептора лимфоидной клетки крови, или фрагментом, вариантом и/или производным такого идиотипа иммуноглобулина или идиотипа T-клеточного рецептора.
В данном контексте следует подразумевать, что идиотип иммуноглобулина является пептидом или белком, имеющим конкретную молекулярную форму вариабельной области иммуноглобулина, экспрессируемого конкретным типом B-клеток. Такой идиотип можно применять в качестве антигена для того, чтобы вызвать иммунный ответ, направленный против такого конкретного типа B-клеток, например, против злокачественных B-клеток. Следует подразумевать, что идиотип T-клеточного рецептора является пептидом или белком, имеющим конкретную молекулярную форму вариабельной области T-клеточного рецептора, экспрессируемого конкретным типом T-клеток. Такой идиотип можно применять в качестве антигена для того, чтобы вызвать иммунный ответ, направленный против такого конкретного типа T-клеток, например, против злокачественных T-клеток.
В некоторых вариантах может быть предпочтительным, при условии, что фармацевтическая композиция содержит комплекс полимерного носителя и переносимого вещества, содержащий полимерный носитель, образованный поперечно сшитыми дисульфидными связями катионными компонентами, и по меньшей мере одну молекулу нуклеиновой кислоты, чтобы по меньшей мере один антиген, ассоциированный с раком или опухолевым заболеванием, не являлся антигеном, ассоциированным с лимфомой, предпочтительно не ассоциирован с B-клеточной лимфомой, T-клеточной лимфомой или неходжкинской лимфомой.
В некоторых вариантах может быть предпочтительным, при условии, что фармацевтическая композиция содержит комплекс полимерного носителя и переносимого вещества, содержащий полимерный носитель, образованный поперечно сшитыми дисульфидными связями катионными компонентами, и по меньшей мере одну молекулу нуклеиновой кислоты, чтобы по меньшей мере один антиген, ассоциированный с раком или опухолевым заболеванием, не являлся антигеном, полученным из злокачественной клетки, предпочтительно не получен из злокачественной B-клетки или злокачественной T-клетки.
В некоторых дополнительных вариантах может быть предпочтительной ситуация, когда фармацевтическая композиция может не содержать другого компонента, кроме компонентов A) и B), предпочтительно не содержать другого мРНК-компонента (отличного от мРНК-компонента, входящего в компонент A), предпочтительно фармацевтическая композиция может совсем не содержать никакой мРНК.
В некоторых дополнительных вариантах может быть предпочтительным, при условии, что фармацевтическая композиция содержит мРНК (отличную от нуклеиновой кислоты компонента A), чтобы мРНК не представляла собой мРНК, кодирующую пептид или антиген, соответствующий B), кроме того, предпочтительно, чтобы мРНК не могла представлять собой мРНК, кодирующую овальбумин, PSMA, люциферазу или STEAP.
В некоторых дополнительных вариантах может быть предпочтительным, при условии, что фармацевтическая композиция содержит мРНК (отличную от нуклеиновой кислоты компонента A), в частности мРНК, кодирующую пептид или антиген, соответствующий B), и/или мРНК, кодирующую овальбумин, PSMA, люциферазу или STEAP, чтобы мРНК не могла быть в комплексе с протамином, предпочтительно не в соотношении 2:1 или 4:1 или от 2:1 до 4:1.
В некоторых дополнительных вариантах может быть предпочтительным, чтобы заявленная фармацевтическая композиция не могла быть применена для лечения карциномы поджелудочной железы или немелкоклеточной карциномы легкого.
В некоторых дополнительных вариантах может быть предпочтительным, при условии, что фармацевтическая композиция содержит мРНК (отличную от нуклеиновой кислоты компонента A), чтобы мРНК не могла представлять собой свободную мРНК.
В некоторых дополнительных вариантах может быть предпочтительным, при условии, что фармацевтическая композиция содержит мРНК (отличную от нуклеиновой кислоты компонента A), чтобы мРНК не могла быть в комплексе с протамином.
В некоторых дополнительных вариантах может быть предпочтительным, при условии, что фармацевтическая композиция содержит свободную мРНК, чтобы мРНК не могла кодировать терапевтически активный белок и не могла кодировать антитело, и не могла кодировать антиген.
В некоторых дополнительных вариантах в отношении компонента A) фармацевтической композиции согласно изобретению может быть предпочтительным, чтобы a) не могла быть протамином.
В некоторых дополнительных вариантах в отношении компонента A) фармацевтической композиции согласно изобретению может быть предпочтительным, чтобы белок-носитель не мог быть протамином.
В некоторых дополнительных вариантах может быть предпочтительным, при условии, что a) компонента A) является протамином, чтобы a) не присутствовал в соотношении 1:2 или 1:4 или от 1:2 до 1:4 по отношению к b) компонента A).
В некоторых дополнительных вариантах может быть предпочтительным, при условии, что белок-носитель компонента A) является протамином, чтобы белок-носитель не присутствовал в соотношении 1:2 или 1:4 по отношению к нуклеиновой кислоте компонента A).
В некоторых дополнительных вариантах в отношении компонента A) может быть предпочтительным, чтобы нуклеиновая кислота не являлась мРНК.
В некоторых дополнительных вариантах может быть предпочтительным, при условии, что нуклеиновая кислота компонента A) представляет собой мРНК, чтобы мРНК не кодировала овальбумин, PSMA, люциферазу или STEAP.
В некоторых дополнительных вариантах может быть предпочтительным, при условии, что нуклеиновая кислота, т.е. b), компонента A) представляет собой мРНК, чтобы мРНК не являлась свободной мРНК, а присутствовала исключительно в комплексе с белком-носителем a).
В некоторых дополнительных вариантах компонент (B) не является овальбумином или фрагментом овальбумина. Предпочтительно, фармацевтическая композиция, набор или фармацевтическая упаковка согласно настоящему изобретению не содержит овальбумин или фрагмент овальбумина или последовательность нуклеиновой кислоты, кодирующую овальбумин или кодирующую фрагмент овальбумина.
Фигуры
Следующие фигуры предназначены для дополнительной иллюстрации изобретения. При этом они не предназначены для ограничения объекта изобретения.
Фигура 1: демонстрирует корреляционную кривую исходных данных, полученных для комплексов полимерного носителя и переносимого вещества, образованных поперечно сшитыми дисульфидными связями катионными пептидами CR12C и CR7C в качестве носителя, после лиофилизации по сравнению с комплексами с неполимеризующимися катионными пептидами в качестве носителя (R12 и R7) на основании динамического светорассеяния с использованием Zetasizer Nano (Malvern Instruments, Malvern, UK). Гидродинамические диаметры измеряли, используя свежеприготовленные комплексы и восстановленные комплексы после лиофилизации. Соотношение масс пептид:РНК составляло 1:2. В результате можно было наблюдать, что размер комплексов полимерного носителя и переносимого вещества, включающих в себя пептиды, содержащие цистеин, в качестве катионных компонентов, что приводило к полимеризации полимерного носителя дисульфидными связями, не изменялся, в отличие от комплексов, образованных неполимеризующимися пептидами, размер которых увеличивался и которые, следовательно, были нестабильными во время стадии лиофилизации. Таким образом, комплексы с полимеризуемыми пептидами в качестве полимерных носителей проявляли предпочтительные свойства в случае лиофилизации.
Фигура 2: демонстрирует дзета-потенциал комплексов полимерного носителя и переносимого вещества, образованных поперечно сшитым дисульфидными связями катионным пептидом CR12C и R722 в качестве переносимой нуклеиновой кислоты при разных соотношениях масс./масс. Как можно видеть, дзета-потенциал изменяется от положительных к отрицательным значениям, когда масс./масс.-соотношение изменяется от избытка пептида до соотношения 1:1 (пептид/РНК).
Фигура 3A: демонстрирует секрецию цитокина hIFNa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR12C и CpG 2216 в качестве переносимой нуклеиновой кислоты в массовом соотношении 1:2,5 (масс./масс.) (CR12C/CpG 2216). Как можно видеть, комплексы полимерного носителя и переносимого вещества приводят к увеличению высвобождения цитокина hIFNa в hPBMC по сравнению с переносимой нуклеиновой кислотой отдельно или катионным пептидом отдельно.
Фигура 3B: демонстрирует секрецию цитокина hTNFa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR12C и CpG 2216 в качестве переносимой нуклеиновой кислоты в массовом соотношении 1:2,5 (масс./масс.) (CR12C/CpG 2216). Как можно видеть, комплексы полимерного носителя и переносимого вещества не приводят к увеличению высвобождения цитокина hTNFa в hPBMC по сравнению с переносимой нуклеиновой кислотой отдельно или катионным пептидом отдельно.
Фигура 4A: демонстрирует секрецию цитокина hIFNa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR12C и мРНК R491, кодирующей люциферазу, в качестве переносимой нуклеиновой кислоты в массовом соотношении 1:2 (масс./масс.) (CR12C/R491). Как можно видеть, комплексы полимерного носителя и переносимого вещества приводят к увеличению высвобождения цитокина hIFNa в hPBMC по сравнению с переносимой нуклеиновой кислотой отдельно или катионным пептидом отдельно.
Фигура 4B: демонстрирует секрецию цитокина hTNFa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR12C и мРНК R491, кодирующей люциферазу, в качестве переносимой нуклеиновой кислоты в массовом соотношении 1:2 (масс./масс.) (CR12C/R491). Как можно видеть, комплексы полимерного носителя и переносимого вещества приводят к увеличению высвобождения цитокина hTNFa в hPBMC по сравнению с переносимой нуклеиновой кислотой отдельно или катионным пептидом отдельно.
Фигура 5A: демонстрирует секрецию цитокина hIFNa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR12C и коротким GU-богатым РНК-олигонуклеотидом (короткий GU-богатый) в качестве переносимой нуклеиновой кислоты в массовом соотношении 1:2,5 (масс./масс.) (CR12C/короткий GU-богатый). Как можно видеть, комплексы полимерного носителя и переносимого вещества приводят к увеличению высвобождения цитокина hIFNa в hPBMC по сравнению с переносимой нуклеиновой кислотой отдельно или катионным пептидом отдельно.
Фигура 5B: демонстрирует секрецию цитокина hTNFa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR12C и коротким GU-богатым РНК-олигонуклеотидом (короткий GU-богатый) в качестве переносимой нуклеиновой кислоты в массовом соотношении 1:2,5 (масс./масс.) (CR12C/короткий GU-богатый). Как можно видеть, комплексы полимерного носителя и переносимого вещества приводят к увеличению высвобождения цитокина hTNFa в hPBMC по сравнению с переносимой нуклеиновой кислотой отдельно или катионным пептидом отдельно.
Фигура 6A: демонстрирует секрецию цитокина hIFNa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR7C и длинной некодирующей GU-богатой исРНК R722 в качестве переносимой нуклеиновой кислоты. Как можно видеть, комплексы полимерного носителя и переносимого вещества (CR7C/R722) приводят к увеличению высвобождения цитокина hIFNa в hPBMC по сравнению с комплексами переносимого вещества (R7/R722), образованными с неполимеризуемым пептидом R7.
Фигура 6B: демонстрирует секрецию цитокина hTNFa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR7C и длинной некодирующей GU-богатой исРНК R722 в качестве переносимой нуклеиновой кислоты. Как можно видеть, комплексы полимерного носителя и переносимого вещества (CR7C/R722) приводят только к слабому увеличению высвобождения цитокина hTNFa в hPBMC по сравнению с комплексами носителя и переносимого вещества (R7/R722), образованными неполимеризуемым пептидом R7.
Фигура 7A: демонстрирует секрецию цитокина hIFNa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR9C и длинной некодирующей GU-богатой исРНК R722 в качестве переносимой нуклеиновой кислоты. Как можно видеть, комплексы полимерного носителя и переносимого вещества согласно изобретению (CR9C/R722) приводят к увеличению высвобождения цитокина hIFNa в hPBMC по сравнению с комплексами носителя и переносимого вещества (R9/R722), образованными неполимеризуемым пептидом R9.
Фигура 7B: демонстрирует секрецию цитокина hTNFa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR9C и длинной некодирующей GU-богатой исРНК R722 в качестве переносимой нуклеиновой кислоты. Как можно видеть, комплексы полимерного носителя и переносимого вещества (CR9C/R722) не приводят к увеличению высвобождения цитокина hTNFa в hPBMC по сравнению с комплексами носителя и переносимого вещества (R9/R722), образованными неполимеризуемым пептидом R9.
Фигура 8A: демонстрирует секрецию цитокина hIFNa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR12C и исРНК R722 в качестве переносимой нуклеиновой кислоты при разных масс./масс.-соотношениях. Как можно видеть, комплексы полимерного носителя и переносимого вещества приводят к увеличению высвобождения цитокина hIFNa в hPBMC по сравнению с переносимой нуклеиновой кислотой отдельно или катионным пептидом отдельно.
Фигура 8B: демонстрирует секрецию цитокина hTNFa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя и переносимого вещества, образованными поперечно сшитым дисульфидными связями катионным пептидом CR12C и исРНК R722 в качестве переносимой нуклеиновой кислоты при разных масс./масс.-соотношениях. Как можно видеть, комплексы полимерного носителя и переносимого вещества приводят к увеличению высвобождения цитокина hTNFa в hPBMC по сравнению с переносимой нуклеиновой кислотой отдельно или катионным пептидом отдельно.
Фигура 9A: демонстрирует секрецию цитокина hIFNa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя, образованными катионными пептидами CH6R4H6C, CH3R4H3C и CHK7HC и исРНК R722 в качестве переносимой нуклеиновой кислоты при разных N/P-соотношениях. Как можно видеть, комплексы полимерного носителя и переносимого вещества приводят к увеличению высвобождения цитокина hIFNa в hPBMC по сравнению с переносимой нуклеиновой кислотой отдельно или катионным пептидом отдельно.
Фигура 9B: демонстрирует секрецию цитокина hTNFa (in vitro) в hPBMC после стимуляции комплексами полимерного носителя, образованными поперечно сшитыми дисульфидными связями катионными пептидами CH6R4H6C, CH3R4H3C и CHK7HC и исРНК R722 в качестве переносимой нуклеиновой кислоты при разных N/P-соотношениях. Как можно видеть, комплексы полимерного носителя и переносимого вещества приводят к увеличению высвобождения цитокина hTNFa в hPBMC по сравнению с переносимой нуклеиновой кислотой отдельно или катионным пептид отдельно. В частности, комплексы полимерного носителя и переносимого вещества с N/P-соотношением, больше или равным 1, приводят к секреции TNFальфа.
Фигура 10: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к белковому антигену овальбумину (белок OVA) для применения в качестве адъюванта в экспериментах с провокационным введением опухолей.
С указанной целью 7 самок мышей C57BL/6 вакцинировали три раза в течение двух недель, используя 5 мкг белка овальбумина в сочетании с 45 мкг CR12C/R722 (1:2; масс./масс.). Для сравнения мышам проводили инъекции без комплексов полимерного носителя и переносимого вещества.
Как можно видеть, комплекс полимерного носителя и переносимого вещества в высокой степени замедлял рост опухолей по сравнению с белковым антигеном отдельно, который не оказывал влияния на рост опухолей в сравнении с контрольным буфером.
Фигура 11: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к белковому антигену овальбумину (белок OVA) для применения в качестве адъюванта на индукцию овальбумин-специфичных IgG2a-антител.
С указанной целью по 5 самок мышей C57BL/6 на группу вакцинировали три раза в течение двух недель 5 мкг белка овальбумина в сочетании с 45 мкг CR12C/R722 (1:2; масс./масс.). Для сравнения мышам проводили инъекции без комплексов полимерного носителя и переносимого вещества.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивал B-клеточный ответ, что доказывает полезные адъювантные свойства комплексов полимерного носителя и переносимого вещества, в частности, в отношении индукции сдвинутого в сторону Th1 иммунного ответа.
Фигура 12: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к белковому антигену овальбумину (белок OVA) или овальбумин-специфичному пептидному антигену SIINFEKL для применения в качестве адъюванта на индукцию овальбумин-специфичных цитотоксических T-клеток.
С указанной целью по 5 самок мышей C57BL/6 на группу вакцинировали три раза в течение двух недель, используя 5 мкг белка овальбумина или 50 мкг пептида SIINFEKEL в сочетании с 45 мкг CR12C/R722 (1:2; масс./масс.). Для сравнения мышам проводили инъекции без комплексов полимерного носителя и переносимого вещества.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивал индукцию овальбумин-специфичных цитотоксических T-клеток по сравнению с вакцинацией белком или пептидом отдельно, что дополнительно подтверждает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества, в частности, в отношении индукции сдвинутого в сторону Th1 иммунного ответа.
Фигура 13: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к вакцине рабипур® (содержащей инактивированный вирус бешенства) для применения в качестве адъюванта на индукцию специфичных для бешенства IgG-антител (как показано по OD 405 нм).
С указанной целью 8 самкам мышей BALB/c внутримышечно инъецировали 0,1, 0,01 и 0,001-кратную человеческую дозу рабипур® и 30 мкг R722 и 8,1 мкг CR12C (3,7:1 масс./масс.). Через 21 день после иммунизации отбирали образцы крови и анализировали в отношении общих IgG-антител, направленных против вируса бешенства.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию специфичных для бешенства IgG-антител по сравнению с вакцинацией рабипур® отдельно, что дополнительно доказывает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества.
Фигура 14: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к вакцине рабипур® или HDC (содержащей инактивированный вирус бешенства) для применения в качестве адъюванта на индукцию специфичных для бешенства цитотоксических T-клеток (которое показано в виде количества пятен в анализе ELISPOT).
С указанной целью 5 самкам мышей BALB/c внутримышечно инъецировали 0,01-кратную человеческую дозу рабипур® или HDC и 30 мкг R722 и 8,1 мкг CR12C (3,7:1 масс./масс.). Через 5 дней после иммунизации мышей умерщвляли, извлекали селезенки и выделяли спленоциты.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию специфичных для бешенства цитотоксических T-клеток по сравнению с вакцинацией рабипур® или HDC отдельно, что дополнительно подтверждает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества, в частности, в отношении индукции сдвинутого в сторону Th1 иммунного ответа.
Фигура 15: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к вакцине рабипур® (содержащей инактивированный вирус бешенства) для применения в качестве адъюванта на индукцию специфичных для бешенства IgG-антител. Кроме того, показано влияние комплекса полимерного носителя и переносимого вещества на индукцию антител с высокой аффинностью по отношению к антигену (что показано в виде %-содержания связанного IgG).
С указанной целью 8 самкам мышей BALB/c внутримышечно инъецировали 0,01-кратную человеческую дозу рабипур® и 30 мкг R722 и 8,1 мкг CR12C (3,7:1 масс./масс.). Через 7 и 21 день после иммунизации собирали образцы крови и анализировали в отношении общих IgG-антител, направленных против вируса бешенства. Чтобы исследовать аффинность образованных антител, направленных против вируса бешенства, во время осуществления ELISA связанные антитела промывали возрастающими концентрациями мочевины.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию специфичных для бешенства IgG-антител с высокой аффинностью к антигену по сравнению с вакцинацией рабипур® отдельно, что дополнительно подтверждает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества, в частности, в отношении индукции антител с высокой аффинностью.
Фигура 16: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к вакцине HDC (содержащей инактивированный вирус бешенства) для применения в качестве адъюванта на индукцию антител, нейтрализующих вирус бешенства (что показано в виде межд. ед./мл).
С указанной целью 8 самкам мышей BALB/c внутримышечно инъецировали 0,01-кратную человеческую дозу HDC и 30 мкг R722 и 15 мкг CR12C (2:1 масс./масс.). Через 21 день после иммунизации собирали образцы крови и анализировали нейтрализацию вируса.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно повышает титр нейтрализующих антител по сравнению с вакцинацией HDC отдельно, что дополнительно подтверждает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества.
Фигура 17: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к вакцине против свиного гриппа пандемрикс® (содержащей инактивированный вирус гриппа H1N1) для применения в качестве адъюванта на индукцию специфичных для вируса H1N1 IgG2a-антител.
С указанной целью 5 самкам мышей BALB/c внутримышечно инъецировали 0,1 мкг пандемрикс® и 30 мкг R722 и 15 мкг CR12C (2:1 масс./масс.). Через 14 дней после иммунизации собирали образцы крови и анализировали в отношении индукции IgG2a-антител, направленных против вируса гриппа H1N1 (что показано в виде OD 405 нм).
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию специфичных для вируса гриппа IgG2a-антител по сравнению с вакцинацией пандемрикс® отдельно, что дополнительно подтверждает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества, в частности, в отношении индукции сдвинутого в сторону Th1 иммунного ответа.
Фигура 18: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к вакцине против вируса гриппа A(H1N1)pdm09 цельвапан® (содержащей инактивированный вирус гриппа A(H1N1)pdm09) для применения в качестве адъюванта на индукцию A(H1N1)pdm09-специфичных цитотоксических T-клеток (что показано в виде количества пятен в анализе ELISPOT).
С указанной целью 5 самкам мышей BALB/c внутримышечно инъецировали 0,1 мкг цельвапан® и 15 мкг R722 и 7,5 мкг CR12C (2:1 масс./масс.). Через 6 дней после иммунизации мышей умерщвляли, извлекали селезенки и выделяли спленоциты.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию A(H1N1)pdm09-специфичных цитотоксических T-клеток по сравнению с вакцинацией цельвапан® отдельно, что дополнительно подтверждает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества, в частности, в отношении индукции сдвинутого в сторону Th1 иммунного ответа.
Фигура 19: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к вакцине против сезонного гриппа бегривак® (содержащей инактивированные штаммы вируса сезонного гриппа, которые рекомендованы ВОЗ) для применения в качестве адъюванта на индукцию специфичных для вируса гриппа IgG2a-антител (что показано в виде OD 405 нм).
С указанной целью 8 самкам мышей BALB/c внутримышечно инъецировали 0,1 мкг бегривак® и 30 мкг R722 и 15 мкг CR12C (2:1 масс./масс.). Через 28 дней после иммунизации собирали образцы крови и анализировали в отношении IgG2a-антител, направленных против вируса гриппа.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию специфичных для вируса гриппа IgG2a-антител по сравнению с вакцинацией бегривак® отдельно, что дополнительно подтверждает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества, в частности, в отношении индукции сдвинутого в сторону Th1 иммунного ответа.
Фигура 20: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к вакцине против гепатита B энджерикс®-B (содержащей рекомбинантный поверхностный антиген гепатита B (HBsAg)) для применения в качестве адъюванта на индукцию HBsAG-специфичных антител (что представлено по флуоресценции).
С указанной целью 8 самкам мышей BALB/c внутримышечно инъецировали 0,5 мкг энджерикс®-B и 6,25 мкг R722 и 1,7 мкг CR12C (3,7:1 масс./масс.). Через 28 дней после иммунизации собирали образцы крови и анализировали в отношении IgG2a-антител, направленных против HBsAGg.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию HBsAg-специфичных IgG2a-антител по сравнению с вакцинацией энджерикс®-B отдельно, что дополнительно подтверждает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества, в частности, в отношении индукции сдвинутого в сторону Th1 иммунного ответа.
Фигура 21: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к полученному из вируса папилломы человека 16 (HPV16) пептиду для применения в качестве адъюванта на индукцию HPV16 E7-специфичных цитотоксических T-клеток (что представлено в виде количества пятен в анализе ELISPOT).
С указанной целью 5 самкам мышей C57BL/6 интрадермально инъецировали 100 мкг полученного из HPV16 E7 пептида E7aa43-77 и 50 мкг R722 и 25 мкг CR12C (2:1 масс./масс.). Через 8 дней после иммунизации мышей умерщвляли, извлекали селезенки и выделяли спленоциты.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию HPV16 E7-специфичных цитотоксических T-клеток по сравнению с вакцинацией пептидом отдельно, что дополнительно подтверждает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества, в частности, в отношении индукции сдвинутого в сторону Th1 иммунного ответа.
Фигура 22: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к полученному из вируса папилломы человека 16 (HPV16) пептиду для применения в качестве адъюванта на индукцию HPV16 E7-специфичных цитотоксических T-клеток (что представлено количеством пятен в анализе ELISPOT).
С указанной целью 5 самкам мышей C57BL/6 интрадермально инъецировали 100 мкг полученного из HPV16 E7 пептида E7aa43-77 и 50 мкг R722 и 25 мкг CR12C (2:1 масс./масс.). Кроме того, мышам инъецировали комплекс полимерного носителя и переносимого вещества, дополнительно содержащий антигенный пептид E7aa43-77. Через семь дней после иммунизации мышей умерщвляли, извлекали селезенки и выделяли спленоциты.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию HPV16 E7-специфичных цитотоксических T-клеток по сравнению с вакцинацией пептидом отдельно. Кроме того, результаты показывают, что включение антигенного пептида в комплекс полимерного носителя и переносимого вещества дополнительно улучшает индукцию HPV16 E7-специфичных цитотоксических T-клеток. Таким образом, данный эксперимент также доказывает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества, в частности, в отношении индукции сдвинутого в сторону Th1 иммунного ответа.
Фигура 23: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к белку NY-ESO-1 человека для применения в качестве адъюванта на индукцию NY-ESO-1-специфичных цитотоксических T-клеток (что представлено в виде количества пятен в анализе ELISPOT).
С указанной целью 5 самкам мышей C57BL/6 внутримышечно инъецировали 5 мкг белка NY-ESO-1 и 30 мкг R722 и 15 мкг CR12C (2:1 масс./масс.) 2 раза в течение 15 дней. Через 7 дней после последней иммунизации мышей умерщвляли, извлекали селезенки и выделяли спленоциты.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию NY-ESO-1-специфичных цитотоксических T-клеток по сравнению с вакцинацией белком отдельно, что дополнительно подтверждает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества, в частности, в отношении индукции сдвинутого в сторону Th1 иммунного ответа.
Фигура 24: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к вакцине рабипур® (содержащей инактивированный вирус бешенства) для применения в качестве адъюванта для усиления защиты от летальной экспериментальной вирусной инфекции.
С указанной целью 8 самкам мышей BALB/c внутримышечно инъецировали 0,001-кратную человеческую дозу рабипур® и 3 мкг R722 и 0,81 мкг CR12C (3,7:1 масс./масс.). Через 37 дней после вакцинации мышам инъецировали летальную дозу вируса бешенства, используемого для экспериментального заражения вирусного штамма (CVS), используя 25-кратную LD50 (дозы, летальные на 50%).
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно повышает выживаемость мышей в случае инфекции вирусом бешенства по сравнению с вакцинацией рабипур® отдельно, что дополнительно подтверждает полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества.
Фигура 25: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к полученному из вируса папилломы человека 16 (HPV16) длинноцепочечному пептиду E7aa43-77 для применения в качестве адъюванта в экспериментах с провокационным введением опухолей.
С указанной целью 8 мышам C57BL/6 на группу вводили в 1 день 1x105 клеток TC-1, которые экспрессируют белок HPV E6 и E7. Вакцинацию начинали на 7 день после провокационного введения опухоли (медианный объем опухолей 31-48 мм3). Мышей интрадермально вакцинировали 5 раз (на 8, 12, 15, 19 и 22 день) 5 мкг или 50 мкг пептида E7 в сочетании с 50 мкг CR12C/R722 (1:2; масс./масс.). Для сравнения мышам инъецировали комплексы полимерного носителя и переносимого вещества отдельно.
Как можно видеть, комплекс полимерного носителя и переносимого вещества в сочетании с полученным из HPV-16 пептидом E7 E7aa43-77 еще ослабляет рост опухолей по сравнению с комплексом полимерного носителя и переносимого вещества отдельно.
Фигура 26: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к полученному из вируса папилломы человека 16 (HPV16) E7-пептиду E7aa43-77 для применения в качестве адъюванта в экспериментах с провокационным введением опухолей.
С указанной целью 8 мышам C57BL/6 на группу вводили в 1 день 1x105 клеток TC-1. Вакцинацию начинали на 7 день после провокационного введения опухоли (медианный объем опухолей 31-48 мм3). Мышей вакцинировали интрадермально 5 (на 8, 12, 15, 19 и 22 день), используя 5 мкг или 50 мкг E7-пептида E7aa43-77 в сочетании с 50 мкг CR12C/R722 (1:2; масс./масс.). Для сравнения мышам инъецировали пептид E7 или комплексы полимерного носителя и переносимого вещества отдельно. Инъекция буфера PBS служила в качестве отрицательного контроля.
Как можно видеть, комплекс полимерного носителя и переносимого вещества в сочетании с полученным из HPV-16 пептидом E7 сильно повышал выживаемость несущих опухоли мышей (среднее время выживаемости 44,5 дня в случае 50 мкг пептида E7+50 мкг комплекса полимерного носителя и переносимого вещества; среднее время выживаемости 22 дня в случае 5 мкг пептида E7+50 мкг комплекса полимерного носителя и переносимого вещества) по сравнению с пептидом E7 или 50 мкг комплекса полимерного носителя и переносимого вещества отдельно.
Фигура 27: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к полученному из вируса папилломы человека 16 (HPV16) E7-пептиду E7aa43-77 для применения в качестве адъюванта в экспериментах по провокационному введению опухолей.
С указанной целью 13 мышей C57BL/6 на группу внутридермально вакцинировали один раз в неделю в течение четырех недель комплексом полимерного носителя и переносимого вещества, образованным поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, и пептидом E7, как показано на фигуре. Через восемь недель после четвертой вакцинации 5 мышей/группу умерщвляли, выделяли спленоциты и определяли частоту встречаемости антигенспецифичных T-клеток CD8+, используя окрашивание HPV-пентамером и проточную цитометрию согласно примеру 13.
Как можно видеть, комплекс полимерного носителя и переносимого вещества в сочетании с полученным из HPV-16 E7-пептидом E7aa43-77 приводит к статистически значимому увеличению количества антигенспецифичных T-клеток CD8+ по сравнению с мышами, которых вакцинировали с использованием 50 мкг пептида E7 отдельно (p=0,0007 в случае 5 мкг пептида E7 и p=0,0002 в случае 50 мкг пептида E7; статистические различия между группами оценивали, используя двухвыборочный t-критерий для независимых выборок). Таким образом, сочетание комплекса полимерного носителя и переносимого вещества с полученным из HPV-16 пептидом E7 индуцирует мощный ответ T-клеток-памяти CD8+.
Фигура 28: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к полученному из вируса папилломы человека 16 (HPV16) E7-пептиду E7aa43-77 для применения в качестве адъюванта в экспериментах по провокационному введению опухолей.
С указанной целью 13 мышей C57BL/6 на группу внутридермально вакцинировали один раз в неделю в течение четырех недель комплексом полимерного носителя и переносимого вещества, образованным поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, и пептидом E7, как указано на фигуре. Через восемь недель после четвертой вакцинации 8 мышам/группу вводили 1×105 опухолевых клеток TC-1 и наблюдали за ростом опухолей.
Как можно видеть, комплекс полимерного носителя и переносимого вещества в сочетании с полученным из HPV-16 E7-пептидом E7aa43-77 приводит к сильному замедлению роста опухолей (4 полных ответа в случае 5 мкг пептида E7+50 мкг комплекса полимерного носителя и переносимого вещества; 7 полных ответов в случае 50 мкг пептида E7+50 мкг комплекса полимерного носителя и переносимого вещества). Таким образом, сочетание комплекса полимерного носителя и переносимого вещества с полученным из HPV-16 пептидом E7 индуцирует мощный ответ T-клеток-памяти CD8+.
Фигура 29: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к вакцине против сезонного гриппа мутагрип® (содержащей инактивированные штаммы вируса сезонного гриппа, которые рекомендованы ВОЗ) для применения в качестве адъюванта на индукцию титров ингибирования специфичной для вируса гриппа гемагглютинации (HI) (которая представлена в виде титров HI).
С указанной целью 8 самкам мышей BALB/c внутримышечно инъецировали 0,45 мкг или 0,045 мкг мутагрип® и 5 мкг R722+1,35 мкг CR12C (3,7:1, масс./масс.). Через 21 день после иммунизации собирали образцы крови и определяли титры HI в сыворотке. Титр HI широко используют в качестве суррогатного параметра эффективности вакцины против гриппа, при этом титр HI≥1:40 обычно определяют как предел защиты для человека.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию титров HI, специфичных для вируса гриппа A H1N1 (A), и титров HI, специфичных для H3N2 (B), по сравнению с вакцинацией мутагрип® отдельно, что дополнительно демонстрирует полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества.
Фигура 30: демонстрирует влияние (in vivo) добавления комплекса полимерного носителя и переносимого вещества, образованного поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, к вакцине против сезонного гриппа мутагрип® (содержащей инактивированные штаммы вируса сезонного гриппа, которые рекомендованы ВОЗ) для применения в качестве адъюванта на индукцию специфичных для вируса гриппа IgG2a-антител (которая представлена в виде титра IgG2a).
С указанной целью 8 самкам мышей BALB/c внутримышечно инъецировали 4,5 мкг или 0,045 мкг мутагрип® и 5 мкг R722+1,35 мкг CR12C (3,7:1 масс./масс.). Через 21 день после иммунизации собирали образцы крови и анализировали в отношении IgG2a-антител, направленных против вируса гриппа A H1N1.
Как можно видеть, комплекс полимерного носителя и переносимого вещества сильно увеличивает индукцию специфичных для вируса гриппа A H1N1 IgG2a-антител по сравнению с вакцинацией мутагрип® отдельно, что дополнительно демонстрирует полезные адъювантные свойства комплекса полимерного носителя и переносимого вещества, в частности, в отношении использования щадящих доз вакцины против сезонного гриппа.
Примеры
Следующие примеры предназначены для дополнительной иллюстрации изобретения. При этом они не предназначены для ограничения объекта изобретения.
1. Реагенты:
Катионные пептиды в качестве катионного компонента полимерного носителя:

Нуклеиновые кислоты в качестве переносимого вещества комплекса полимерного носителя и переносимого вещества:
R1180: мРНК, кодирующая люциферазу (SEQ ID NO: 112)


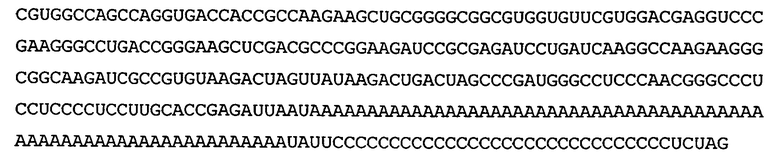
(R1180)
R722A: длинная некодирующая GU-богатая исРНК (SEQ ID NO: 105)
R722B: длинная некодирующая GU-богатая исРНК (SEQ ID NO: 122)
R491: мРНК, кодирующая люциферазу (SEQ ID NO: 113)

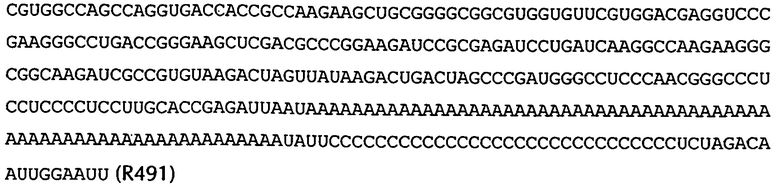
CpG 2216: CpG-олигонуклеотид GGGGGACGATCGTCGGGGGG (SEQ ID NO: 114)
Короткий GU-богатый: GU-богатый РНК-олигонуклеотид GGUUUUUUUUUUUUUUUGGG (SEQ ID NO: 115)
Эксперименты, показывающие применение переносимой нуклеиновой кислоты R722, осуществляли, используя последовательности R722A и/или R722B.
Антигены и эпитопы:
Полученный из овальбумина пептид SIINFEKL (SEQ ID NO: 116)
Овальбумин:

2. Получение последовательностей нуклеиновых кислот:
Для указанных примеров получали последовательности нуклеиновых кислот, которые указаны в примере 1, и использовали для образования полимеризованных комплексов полимерного носителя и переносимого вещества или неполимеризованных комплексов носителя и переносимого вещества для сравнения. Такие комплексы полимерного носителя и переносимого вещества использовали для трансактивации in vitro и in vivo, для иммуностимуляции in vitro и для характеристики частиц.
Согласно первому этапу получения получали последовательности ДНК, кодирующие соответствующие последовательности РНК R1180, R722 и R491. Последовательности соответствующих РНК показаны в списке последовательностей (SEQ ID NO: 112, 105 и 113).
Короткие GU-богатые последовательности и олигонуклеотиды CpG 2216 получали, используя автоматизированный твердофазный синтез с помощью химии фосфорамидитов. Последовательности показаны в списке последовательностей (SEQ ID NO: 115 и 114).
Транскрипция in vitro:
Соответствующие ДНК-плазмиды, полученные согласно примеру 2 для R1180, R722 и R491, транскрибировали in vitro, используя полимеразу T7 (набор для мРНК T7-Opti, CureVac, Tübingen, Germany), следуя инструкциям производителя. Затем мРНК очищали, используя PureMessenger® (CureVac, Tübingen, Germany).
3. Синтез комплексов полимерного носителя и переносимого вещества:
Последовательности нуклеиновых кислот, определенные выше в примере 1, смешивали с катионными компонентами, которые определены в примере 1. Таким образом, указанное количество последовательности нуклеиновой кислоты смешивали с соответствующим катионным компонентом в указанных массовых соотношениях с образованием при этом комплекса. Если использовали полимеризующиеся катионные компоненты согласно настоящему изобретению, то полимеризация катионных компонентов происходила одновременно с образованием комплекса с переносимой нуклеиновой кислотой. Затем полученный раствор доводили водой до конечного объема 50 мкл и инкубировали в течение 30 минут при комнатной температуре. Разные соотношения катионный компонент/нуклеиновая кислота, используемые в экспериментах, показаны в таблице 1.
N/P-соотношение: является мерой ионного заряда катионного компонента полимерного носителя или полимерного носителя как такового. В том случае, когда катионные свойства катионного компонента формируются за счет атомов азота, N/P-соотношение представляет собой отношение основных атомов азота к фосфатным остаткам, если считать, что атомы азота придают положительные заряды, а фосфаты фосфатного остова нуклеиновой кислоты придают отрицательный заряд.
N/P предпочтительно вычисляют по следующей формуле:
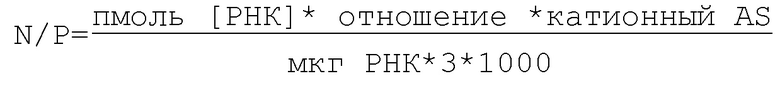
В качестве примера использовали РНК R722 согласно SEQ ID NO: 122, которая имеет молекулярную массу 186 кДа. Таким образом, 1 мкг РНК R722 дает 5,38 пмоль РНК.
4. Стимуляция цитокинов в hPBMC:
Клетки HPBMC из периферической крови здоровых доноров выделяли, используя градиент фикола, и затем промывали 1×PBS (фосфатно-солевым буфером). Затем клетки высевали в 96-луночные планшеты для микротитрования (200×103/лунку). Клетки hPBMC инкубировали в течение 24 часов с 10 мкл комплекса полимерного носителя и переносимого вещества из примера 3, содержащего указанное количество нуклеиновой кислоты, в среде X-VIVO 15 (BioWhittaker). Иммуностимулирующий эффект измеряли, выявляя продукцию цитокинов в hPBMC (фактора некроза опухолей альфа и интерферона альфа). Соответственно, планшеты для микротитрования, используемые в ELISA (Nunc Maxisorb), инкубировали в течение ночи с буфером для связывания (0,02% NaN3, 15 мМ Na2CO3, 15 мМ NaHCO3(pH 9,7), дополнительно содержащим специфичное для цитокина антитело. Затем клетки блокировали, используя 1×PBS, содержащий 1% БСА (бычий сывороточный альбумин). Добавляли надосадок клеток и инкубировали в течение 4 часов при 37°C. Затем планшет для микротитрования промывали 1×PBS, содержащим 0,05% твин-20, и затем инкубировали в меченном биотином вторым антителом (BD Pharmingen, Heidelberg, Germany). В планшет добавляли связанную со стрептавидином пероксидазу хрена. Затем планшет снова промывали 1×PBS, содержащим 0,05% твин-20, и добавляли ABTS (2,2'-азино-бис(3-этилбензтиазолин-6-сульфоновая кислота) в качестве субстрата. Количество цитокина определяли, измеряя оптическую плотность при 405 нм (OD 405), используя стандартную кривую, полученную с использованием рекомбинантных цитокинов (BD Pharmingen, Heidelberg, Germany), с помощью считывающего устройства для ELISA Sunrise из Tecan (Crailsheim, Germany). Соответствующие результаты показаны на фиг. 3-9.
5. Измерения дзета-потенциала:
Дзета-потенциал комплексов полимерного носителя и переносимого вещества оценивали способом электрофореза с лазерным допплеровским анализом, используя Zetasizer Nano (Malvern Instruments, Malvern, UK). Измерение осуществляли при 25°C и использовали угол светорассеяния 173°. Результаты показаны на фиг. 2.
6. Стабильность комплексов после лиофилизации
Гидродинамические диаметры комплексов полимерного носителя и переносимого вещества, полученных, как описано выше, измеряли на основании динамического светорассеяния, используя Zetasizer Nano (Malvern Instruments, Malvern, UK) согласно инструкция производителя. Измерения осуществляли при 25°C в буфере, анализировали способом кумулянтов, чтобы получить гидродинамические диаметры и показатели полидисперсности комплексов полимерного носителя и переносимого вещества. Комплексы полимерного носителя и переносимого вещества образовывали, как указано в примере 3, и гидродинамические диаметры измеряли с использованием свежеприготовленных комплексов и с использованием восстановленных комплексов после лиофилизации. Соответствующие результаты эксперимента показаны на фиг. 1.
7. Эксперименты по иммунизации:
a) Иммунизация овальбумином или SIINFEKL:
Для иммунизации вакцины на основе овальбуминового белка (OVA) (5 мкг) или овальбумин-специфичного пептида SIINFEKL (50 мкг) объединяли с комплексами полимерного носителя и переносимого вещества R722/CR12C (в соотношении 2:1 масс./масс.) (30 мкг R722/15 мкг CR12C) в качестве адъюванта и инъецировали интрадермально самкам мышей C57BL/6 (7 мышей на группу в случае провокационного введения опухолей и 5 мышей на группу в случае выявления иммунного ответа). Вакцинацию повторяли 2 раза в течение 2 недель. Для сравнения мышам инъецировали антигены отдельно.
b) Иммунизация вакциной против бешенства:
Для иммунизации вакцину рабипур® или HDC (обе содержат инактивированный вирус бешенства) (0,1-, 0,01- и 0,001-кратную человеческую дозу) объединяли с комплексами полимерного носителя и переносимого вещества R722/CR12C (в соотношении 3,7:1 масс./масс.) (30 мкг R722/8,1 мкг CR12C) в качестве адъюванта и инъецировали внутримышечно самкам мышей Balb/c (5 или 8 мышей на группу; как указано). Для сравнения мышам инъецировали рабипур® или HDC отдельно.
c) Иммунизация вакциной против гриппа A(H1N1)pdm09 (свиного гриппа):
Для иммунизации вакцину пандемрикс® или цельвапан® (обе содержат инактивированный вирус гриппа A(H1N1)pdm09) (0,1 мкг/дозу) объединяли с комплексами полимерного носителя и переносимого вещества R722/CR12C (в соотношении 2:1 масс./масс.) (15 мкг R722/7,5 мкг CR12C в случае цельвапан® и 30 мкг R722/15 мкг CR12C в случае пандемрикс®) в качестве адъюванта и инъецировали внутримышечно самкам мышей Balb/c (5 мышей на группу). Для сравнения мышам инъецировали пандемрикс® или цельвапан® отдельно.
d) Иммунизация вакциной против сезонного гриппа:
Для иммунизации вакцину против сезонного гриппа бегривак® (содержит инактивированные штаммы вируса гриппа, которые рекомендованы ВОЗ; сезон 2009/2010) (0,1 мкг/дозу) объединяли с комплексами полимерного носителя и переносимого вещества R722/CR12C (в соотношении 2:1 масс./масс.) (30 мкг R722/15 мкг CR12C) в качестве адъюванта и инъецировали внутримышечно самкам мышей Balb/c (8 мышей на группу). Для сравнения мышам инъецировали бегривак® отдельно.
e) Иммунизация вакциной против гепатита B:
Для иммунизации вакцину против гепатита B энджерикс®-B (содержит рекомбинантный поверхностный антиген вируса гепатита B) (0,5 мкг/дозу) объединяли с комплексами полимерного носителя и переносимого вещества R722/CR12C (в соотношении 3,7:1 масс./масс.) (6,25 мкг R722/1,7 мкг CR12C) в качестве адъюванта и инъецировали внутримышечно самкам мышей Balb/c (8 мышей на группу). Для сравнения мышам инъецировали энджерикс®-B отдельно.
f) Иммунизация полученным из вируса папилломы человека 16 (HPV16) пептидом E7:
Для иммунизации полученный из HPV16 пептид E7 aa43-77 (100 мкг/дозу) объединяли с комплексами полимерного носителя и переносимого вещества R722/CR12C (в соотношении 2:1 масс./масс.) (50 мкг R722/25 мкг CR12C) в качестве адъюванта и инъецировали интрадермально самкам мышей C57BL/6 (5 мышей на группу). Для сравнения мышам инъецировали пептид отдельно.
В следующем эксперименте (фиг. 22) полученный из HPV пептид E7 aa43-77 (100 мкг/дозу) объединяли с комплексами полимерного носителя и переносимого вещества R722/CR12C (в соотношении 2:1 масс./масс.) (50 мкг R722/25 мкг CR12C) во время стадии полимеризации c) способа получения комплекса полимерного носителя и переносимого вещества, который описан выше. При этом полученный из HPV пептид является частью комплекса полимерного носителя и переносимого вещества и указан в виде E7 aa43-77/R722/CR12C. Для сравнения в данном эксперименте мышам инъецировали пептид отдельно (E7 aa43-77) и фармацевтическую композицию согласно изобретению, содержащую пептид E7 aa43-77 в качестве антигена и комплекс полимерного носителя и переносимого вещества в качестве адъюванта, при этом комплекс полимерного носителя и переносимого вещества не содержал антигена (E7 aa43-77+R722/CR12C).
g) Иммунизация белком NY-ESO-1:
Для иммунизации опухолевый белковый антиген NY-ESO-1 (5 мкг/дозу) объединяли с комплексами полимерного носителя и переносимого вещества R722/CR12C (в соотношении 2:1 масс./масс.) (30 мкг R722, 15 мкг CR12C) в качестве адъюванта и инъецировали 2 раза в течение 15 дней внутримышечно самкам мышей C57BL/6 (5 мышей на группу). Для сравнения мышам инъецировали белок отдельно.
8. Определение антигенспецифичного иммунного ответа (B-клеточного иммунного ответа):
a) Определение антител, направленных против овальбумина:
Определение антигенспецифичного иммунного ответа (B-клеточного иммунного ответа) осуществляли, выявляя антигенспецифичные антитела. При этом собирали образцы крови от вакцинированных мышей через 5 дней после последней вакцинации и готовили сыворотку. Планшеты MaxiSorb (Nalgene Nunc International) покрывали белком овальбумином Callus gallus. После блокирования с использованием 1×PBS, содержащего 0,05% твин-20 и 1% БСА, планшеты инкубировали с разбавленной сывороткой мышей. Затем добавляли связанное с биотином второе антитело (антитело против IgG2a мыши, Pharmingen). После промывки планшет инкубировали с пероксидазой хрена-стрептавидином и затем измеряли превращение субстрата ABTS (2,2'-азино-бис(3-этил-бензтиазолин-6-сульфоновая кислота). Результаты такой индукции антител при вакцинации фармацевтической композицией согласно изобретению показаны на фиг. 11.
b) Выявление антител, направленных против вируса бешенства:
Выявление антигенспецифичного иммунного ответа (B-клеточного иммунного ответа) осуществляли путем выявления специфичных для вируса бешенства суммарных IgG-антител. При этом собирали образцы крови от вакцинированных мышей через 7 и 21 день после вакцинации и готовили сыворотку. Планшеты MaxiSorb (Nalgene Nunc International) покрывали коммерчески доступной вакциной против бешенства, содержащей инактивированный вирус (HDC; 1:10000). После блокирования 1×PBS, содержащим 0,05% твин-20 и 1% БСА, планшеты инкубировали с разбавленной сывороткой мышей. Затем добавляли связанное с пероксидазой хрена второе антитело (антитело против IgG мыши, Pharmingen). После промывки планшет проявляли, используя ABTS, и затем измеряли превращение субстрата ABTS (2,2'-азино-бис(3-этилбензтиазолин-6-сульфоновая кислота). Результаты такой индукции антител при вакцинации фармацевтической композицией согласно изобретению показаны на фиг. 13.
c) Определение аффинности антител, направленных против вируса бешенства:
Выявление суммарных IgG-антител, направленных против вируса бешенства, осуществляли, как описано в пункте b) с той разницей, что сыворотку мышей тестировали только в разведении 1:40. Кроме того, после инкубации с сывороткой мышей планшеты промывали возрастающими концентрациями мочевины (6, 7 и 8 М мочевиной). При промывке мочевиной можно выявлять только антитела с высокой аффинностью к антигену. Результаты такой индукции антител при вакцинации фармацевтической композицией согласно изобретению показаны на фиг. 15.
d) Выявление антител, направленных против вируса гриппа A(H1N1)pdm09 (свиного гриппа):
Выявление антигенспецифичного иммунного ответа (B-клеточного иммунного ответа) осуществляли путем выявления специфичных для вируса гриппа A(H1N1)pdm09 IgG2a-антител. При этом собирали образцы крови от вакцинированных мышей через 14 дней после вакцинации и готовили сыворотку. Планшеты MaxiSorb (Nalgene Nunc International) покрывали инактивированным вирусом гриппа A Калифорния/7/09 A(H1N1)pdm09 (NIBSC, UK) (1 мкг/мл). После блокирования 1×PBS, содержащим 0,05% твин-20 и 1% БСА, планшеты инкубировали с разбавленной сывороткой мышей. Затем добавляли связанное с биотином второе антитело (антитело против IgG2a мыши, Pharmingen). После промывки планшет инкубировали с пероксидазой хрена-стрептавидином и затем измеряли превращение субстрата ABTS (2,2'-азино-бис(3-этилбензтиазолин-6-сульфоновая кислота), чтобы определить индукцию IgG2a-антител. Результаты такой индукции антител при вакцинации фармацевтической композицией согласно изобретению показаны на фиг. 17.
e) Выявление антител, направленных против штаммов вирусов сезонного гриппа:
Выявление антигенспецифичного иммунного ответа (B-клеточного иммунного ответа) осуществляли, выявляя специфичные для вируса гриппа IgG2a-антител. При этом собирали образцы крови от вакцинированных мышей через 28 дней после вакцинации и готовили сыворотку. Планшеты MaxiSorb (Nalgene Nunc International) покрывали инфлувак 2009/10® (5 мкг/мл), содержащей несколько антигенов вируса гриппа, в качестве противовирусной вакцины, используемой для вакцинации. После блокирования 1×PBS, содержащим 0,05% твин-20 и 1% БСА, планшеты инкубировали с разбавленной сывороткой мышей. Затем добавляли связанное с биотином второе антитело (антитело против IgG2a мыши, Pharmingen). После промывки планшет инкубировали с пероксидазой хрена-стрептавидином и затем измеряли превращение субстрата ABTS (2,2'-азино-бис(3-этилбензтиазолин-6-сульфоновой кислоты), чтобы определить индукцию IgG2a-антител. Результаты такой индукции антител при вакцинации фармацевтической композицией согласно изобретению показаны на фиг. 19.
f) Выявление антител, направленных против поверхностного антигена вируса гепатита B (HBsAg):
Выявление антигенспецифичного иммунного ответа (B-клеточного иммунного ответа) осуществляли, выявляя HBsAG-специфичные IgG2a-антитела. При этом собирали образцы крови от вакцинированных мышей через 28 дней после вакцинации и готовили сыворотку. Планшеты MaxiSorb (Nalgene Nunc International) покрывали рекомбинантным поверхностным антигеном вируса гепатита B (HBsAG) (Aldevron, USA) (1 мкг/мл). После блокирования 1×PBS, содержащим 0,05% твин-20 и 1% БСА, планшеты инкубировали с разбавленной сывороткой мышей. Затем добавляли связанное с биотином второе антитело (антитело против IgG2a мыши, Pharmingen). После промывки планшет инкубировали с пероксидазой хрена- стрептавидином и затем измеряли превращение субстрата ABTS (2,2'-азино-бис(3-этилбензтиазолин-6-сульфоновой кислоты), чтобы определить индукцию IgG2a-антител. Результаты такой индукции антител при вакцинации фармацевтической композицией согласно изобретению показаны на фиг. 20.
9. Выявление антигенспецифичного клеточного иммунного ответа в ELISPOT:
a) Выявление цитотоксического T-клеточного ответа, направленного против овальбумина:
Через 5 дней после последней вакцинации мышей умерщвляли, извлекали селезенки и выделяли спленоциты. Для выявления INF-гамма планшет для множественного скрининга (Millipore) инкубировали в течение ночи с буфером для покрывания (0,1 М карбонатный-бикарбонатный буфер, pH 9,6, 10,59 г/л Na2CO3, 8,4 г/л NaHCO3), содержащим антитело против INFγ (BD Pharmingen, Heidelberg, Germany). На следующий день добавляли 1×106 клеток/лунку и повторно стимулировали, используя 1 мкг/лунку соответствующего пептида (SIINFEKL овальбумина), нерелевантного пептида (коннексин = контрольный пептид) или буфер без пептида. Затем клетки инкубировали в течение 24 часов при 37°C. На следующий день планшеты 3 раза промывали PBS, один раз водой и один раз PBS/0,05% твин-20 и затем инкубировали со связанным с конъюгированным с биотином вторым антителом в течение 11-24 часов при 4°C. Затем планшеты промывали PBS/0,05% твин-20 и инкубировали в течение 2 часов при комнатной температуре со щелочной фосфатазой, связанной со стрептавидином, в блокирующем буфере. После промывки PBS/0,05% твин-20 в планшет добавляли субстрат (жидкую субстратную систему 5-бром-4-хлор-3-индолилфосфат/нитросиний тетразолий из Sigma Aldrich, Taufkirchen, Germany) и визуально выявляли превращение субстрата. Затем реакцию останавливали, промывая планшеты водой. Затем высушенные планшеты регистрировали, используя устройство для считывания планшетов ELISPOT. В случае визуализации уровней пятен числовые значения корректировали, вычитая фон. Результаты такой индукции специфичных цитотоксических T-клеток при вакцинации фармацевтической композицией согласно изобретению показаны на фиг. 12.
b) Выявление цитотоксического T-клеточного ответа, направленного против вируса бешенства:
Через 5 дней после вакцинации мышей умерщвляли, извлекали селезенки и выделяли спленоциты. Для выявления INF-гамма планшет для множественного скрининга (Millipore) инкубировали в течение ночи с буфером для покрывания (0,1 М карбонатный-бикарбонатный буфер, pH 9,6, 10,59 г/л Na2CO3, 8,4 г/л NaHCO3), содержащим антитело против INFγ (BD Pharmingen, Heidelberg, Germany). На следующий день добавляли 5×105 клеток/лунку и повторно стимулировали инактивированным вирусом бешенства (рабипур® 1:100 или HDC 1:100)) или буфером без пептида (БСА). Затем клетки инкубировали в течение 24 часов при 37°C. На следующий день планшеты 3 раза промывали PBS, в течение 5 минут водой и один раз PBS/0,05% твин-20, и затем инкубировали со связанным с биотином вторым антителом в течение 11-24 часов при 4°C. Затем планшеты промывали PBS/0,05% твин-20 и инкубировали в течение 2 часов при комнатной температуре со щелочной фосфатазой, связанной со стрептавидином, в блокирующем буфере. После промывки PBS/0,05% твин-20 в планшет добавляли субстрат (жидкая субстратная система 5-бром-4-хлор-3-индолилфосфат/нитросиний тетразолий из Sigma Aldrich, Taufkirchen, Germany) и визуально можно было наблюдать превращение субстрата. Затем реакцию останавливали, промывая планшеты водой. Затем высушенные планшеты регистрировали, используя устройство для считывания планшетов ELISPOT. В случае визуализации уровней пятен числовые значения корректировали вычитанием фона. Результаты такой индукции специфичных цитотоксических T-клеток при вакцинации фармацевтической композицией согласно изобретению показаны на фиг. 14.
c) Выявление цитотоксического T-клеточного ответа, направленного против вируса свиного гриппа (A(H1N1)pdm09):
Через 6 дней после вакцинации мышей умерщвляли, извлекали селезенки и выделяли спленоциты. Для выявления INF-гамма планшет для множественного скрининга (Millipore) инкубировали в течение ночи с буфером для покрывания (0,1 М карбонатный-бикарбонатный буфер, pH 9,6, 10,59 г/л Na2CO3, 8,4 г/л NaHCO3), содержащим антитело против INFγ (BD Pharmingen, Heidelberg, Germany). На следующий день добавляли 5×105 клеток/лунку и повторно стимулировали инактивированным вирусом гриппа A/Калифорния 7/09 A(H1N1)pdm09 (NIBSC, UK) (10 мкг/мл) или буфером без пептида (БСА). Затем клетки инкубировали в течение 24 часов при 37°C. На следующий день планшеты 3 раза промывали PBS, в течение 5 минут водой и один раз PBS/0,05% твин-20 и затем инкубировали со связанным с биотином вторым антителом в течение 11-24 часов при 4°C. Затем планшеты промывали PBS/0,05% твин-20 и инкубировали в течение 2 часов при комнатной температуре со щелочной фосфатазой, связанной со стрептавидином, в блокирующем буфере. После промывки PBS/0,05% твин-20 в планшет добавляли субстрат (жидкая субстратная система 5-бром-4-хлор-3-индолилфосфат/нитросиний тетразолий от Sigma Aldrich, Taufkirchen, Germany) и можно было визуально выявить превращение субстрата. Затем реакцию останавливали промывкой планшетов водой. Затем высушенные планшеты регистрировали, используя устройство для считывания планшетов ELISPOT. В случае визуализации уровней пятен числовые значения корректировали, вычитая фон. Результаты такой индукции специфичных цитотоксических T-клеток при вакцинации фармацевтической композицией согласно изобретению показаны на фиг. 18.
d) Выявление цитотоксического T-клеточного ответа, направленного против белка E7 вируса папилломы человека 16 (HPV16):
Через 8 дней после вакцинации мышей умерщвляли, извлекали селезенки и выделяли спленоциты. Для выявления INF-гамма планшет для множественного скрининга (Millipore) инкубировали в течение ночи с буфером для покрывания (0,1 М карбонатный-бикарбонатный буфер, pH 9,6, 10,59 г/л Na2CO3, 8,4 г/л NaHCO3), содержащим антитело против INFγ (BD Pharmingen, Heidelberg, Germany). На следующий день добавляли 5×105 клеток/лунку и повторно стимулировали разбавленными полученными из E7 пептидами (E7aa43-77, E748-57, E7aa49-57) (1 мкг/мл), нерелевантным пептидом (LacZ-пептид H-2 Ld) или буфером без пептида (ДМСО). Затем клетки инкубировали в течение 24 часов при 37°C. На следующий день планшеты 3 раза промывали PBS, в течение 5 минут водой и один раз PBS/0,05% твин-20 и затем инкубировали со связанным с биотином вторым антителом в течение 11-24 часов при 4°C. Затем планшеты промывали PBS/0,05% твин-20 и инкубировали в течение 2 часов при комнатной температуре со щелочной фосфатазой, связанной со стрептавидином, в блокирующем буфере. После промывки PBS/0,05% твин-20 в планшет добавляли субстрат (жидкую систему субстратов 5-бром-4-хлор-3-индолилфосфат/нитросиний тетразолий из Sigma Aldrich, Taufkirchen, Germany) и можно было визуально выявлять превращение субстрата. Затем реакцию останавливали, промывая планшеты водой. Затем высушенные планшеты регистрировали, используя устройство для считывания планшетов ELISPOT. В случае визуализации уровней пятен числовые значения корректировали вычитанием фона. Результаты такой индукции специфичных цитотоксических T-клеток при вакцинации фармацевтической композицией согласно изобретению, содержащей пептидный антиген из патогена, ассоциированного с инфекционной болезнью, показаны на фиг. 21 для пептидного антигена E7aa43-77, не включенного в комплекс полимерного носителя и переносимого вещества, и дополнительно для пептидного антигена E7aa43-77 в случае включения в комплекс полимерного носителя и переносимого вещества на фиг. 22.
e) Выявление цитотоксического T-клеточного ответа, направленного против опухолевого антигена NY-ESO-1:
Через 7 дней после вакцинации мышей умерщвляли, извлекали селезенки и выделяли спленоциты. Для выявления INF-гамма планшет для множественного скрининга (Millipore) инкубировали в течение ночи с буфером для покрывания (0,1 м карбонатный-бикарбонатный буфер, pH 9,6, 10,59 г/л Na2CO3, 8,4 г/л NaHCO3), содержащим антитело против INFγ (BD Pharmingen, Heidelberg, Germany). На следующий день добавляли 1×106 клеток/лунку и повторно стимулировали, используя библиотеку эпитопов NY-ESO-1, содержащую предполагаемые эпитопы MHC I и MHC II. Затем клетки инкубировали в течение 24 часов при 37°C. На следующий день планшеты 3 раза промывали PBS, один раз водой и один раз PBS/0,05% твин-20, и затем инкубировали со связанным с биотином вторым антителом в течение 11-24 часов при 4°C. Затем планшеты промывали PBS/0,05% твин-20 и инкубировали в течение 2 часов при комнатной температуре с щелочной фосфатазой, связанной со стрептавидином в блокирующем буфере. После промывки PBS/0,05% твин-20 в планшет добавляли субстрат (жидкую субстратную систему 5-бром-4-хлор-3-индолилфосфат/нитросиний тетразолий из Sigma Aldrich, Taufkirchen, Germany) и можно было визуально выявлять превращение субстрата. Затем реакцию останавливали, промывая планшеты водой. Затем высушенные планшеты регистрировали, используя устройство для считывания планшетов ELISPOT. В случае визуализации уровней пятен числовые значения корректировали, вычитая фон. Результаты такой индукции специфичных цитотоксических T-клеток при вакцинации фармацевтической композицией согласно изобретению, включающей в себя по меньшей мере один опухолевый антиген, показаны на фиг. 23.
10. Введение опухолей:
Через неделю после последней вакцинации вакцинированным мышам подкожно имплантировали 1×106 клеток E.G7-OVA (опухолевые клетки, которые стабильно экспрессируют овальбумин). Рост опухолей контролировали, измеряя размер опухолей в 3 направлениях, используя штангенциркуль. Результаты индукции противоопухолевого ответа после вакцинации фармацевтической композицией согласно изобретению показаны на фиг. 10.
11. Тест нейтрализации вируса:
Выявление ответа в виде нейтрализующих вирус антител (специфичного B-клеточного иммунного ответа) осуществляли в анализе нейтрализации вируса. При этом собирали образцы крови от вакцинированных мышей через 21 день после вакцинации и готовили сыворотку. Полученные сыворотки использовали во флуоресцентном тесте нейтрализации вирусов антителами (FAVN), используя адаптированный для культуры клеток предназначенный для иммунизации вирусный штамм (CVS) вируса бешенства, который рекомендован OIE (Всемирной организацией здравоохранения животных) и впервые описан в публикации Cliquet F., Aubert M. and Sagne L. (1998); J. Immunol. Methods, 212, 79-87. Кратко, инактивированную нагреванием сыворотку тестировали в четырех повторах, используя двукратные серийные разведения, в отношении их потенциала нейтрализовать 100 TCID50 (дозы, инфицирующие культуру ткани на 50%) CVS в объеме 50 мкл. Для этого разведения сыворотки инкубировали с вирусом в течение 1 часа при 37°C (в инкубаторе с увлажнение и 5% CO2) и затем добавляли обработанные трипсином клетки BHK-21 (4×105 клеток/мл; 50 мкл на лунку). Инфицированные культуры клеток инкубировали в течение 48 часов в инкубаторе с увлажнением при 37°C и 5% CO2. Инфекцию клеток анализировали после фиксации клеток с использованием 80% ацетона при комнатной температуре, используя конъюгат ФИТЦ-антитела против вируса бешенства. Планшеты два раза промывали, используя PBS, и избыток PBS удаляли. Культуры клеток оценивали положительно или отрицательно в отношении присутствия вируса бешенства. Отрицательно оцениваемые клетки в обработанных сывороткой лунках представляли нейтрализацию вируса бешенства. Каждый тест FAVN включал в себя стандартную сыворотку, рекомендованную ВОЗ или OIE (положительная эталонная сыворотка), которая служит в качестве эталона для стандартизации анализа. Нейтрализующую активность тестируемых сывороток вычисляли по отношению к стандартной сыворотке и выражали в виде международных единиц/мл (межд. ед./мл). Результаты такого эксперимента показаны на фиг. 16.
12. Провокационная инфекция мышей вирусом бешенства:
Через 37 дней после однократной внутримышечной иммунизации мышей с использованием 0,001-кратной человеческой дозы рабипур® и 3 мкг R722 и 0,81 мкг CR12C (3,7:1 масс./масс.) всех мышей в эксперименте интракраниально (и/к) инфицировали, используя 25-кратную LD50 штамма CVS вируса бешенства. За мышами наблюдали в отношении специфичных симптомов заболевания бешенством и изменения массы тела. Результаты данного эксперимента показаны на фиг. 24.
13. Введение опухолей с использованием клеток TC-1 (измерение роста опухолей и выживаемости животных в условиях терапии):
Восьми мышам C57BL/6 на группу в 1 день вводили 1×105 клеток TC-1, которые экспрессируют белок E6 и E7 HPV. Вакцинацию начинали на 7 день после провокационного введения опухолей (медианный объем опухолей 31-48 мм3). Мышей интрадермально вакцинировали 5 раз (в 8, 12, 15, 19 и 22 день), используя 5 мкг или 50 мкг пептида E7 в сочетании с 50 мкг CR12C/R722 (1:2; масс./масс.). Для сравнения мышам инъецировали комплексы полимерного носителя и переносимого вещества отдельно.
Комплекс полимерного носителя и переносимого вещества в сочетании с полученным из HPV-16 E7-пептидом E7aa43-77 еще ослаблял рост опухолей по сравнению с комплексом полимерного носителя и переносимого вещества отдельно (фигура 25).
Комплекс полимерного носителя и переносимого вещества в сочетании с полученным из HPV-16 пептидом E7 значительно повышал выживаемость мышей, несущих опухоли (среднее время выживаемости 44,5 дня в случае 50 мкг пептида E7+50 мкг комплекса полимерного носителя и переносимого вещества; среднее время выживаемости 22 дня в случае 5 мкг пептида E7+50 мкг комплекса полимерного носителя и переносимого вещества) по сравнению с пептидом E7 или 50 мкг комплекса полимерного носителя и переносимого вещества отдельно (фигура 26).
14. Введение опухолей с использованием клеток TC-1 (индукция ответа T-клеток-памяти):
Тринадцать мышей C57BL/6 на группу подвергали интрадермальной вакцинации один раз в неделю в течение четырех недель (в 0, 7, 14 и 21 день), используя комплекс полимерного носителя и переносимого вещества, образованный поперечно сшитым дисульфидными связями катионным пептидом CR12C в качестве носителя и исРНК R722 в качестве переносимой нуклеиновой кислоты, и пептид E7.
Через восемь недель после четвертой вакцинации 5 мышей/группу умерщвляли, выделяли спленоциты и определяли частоту встречаемости антигенспецифичных T-клеток CD8+, используя окрашивание HPV-пентамером и проточную цитометрию согласно примеру 15.
Комплекс полимерного носителя и переносимого вещества в сочетании с полученным из HPV-16 E7-пептидом E7aa43-77 приводит к статистически значимому увеличению количества антигенспецифичных T-клеток CD8+ по сравнению с мышами, вакцинированными с использованием 50 мкг пептида E7 отдельно (p=0,0007 в случае 5 мкг пептида E7 и p=0,0002 в случае 50 мкг пептида E7; статистические различия между группами оценивали, используя двухвыборочный t-критерий для независимых выборок). Таким образом, сочетание комплекса полимерного носителя и переносимого вещества с полученным из HPV-16 пептидом E7 индуцирует мощный ответ T-клеток памяти CD8+ (фигура 27).
Через восемь недель после четвертой вакцинации 8 мышам/группу вводили 1×105 опухолевых клеток TC-1 и наблюдали рост опухолей.
Комплекс полимерного носителя и переносимого вещества в сочетании с полученным из HPV-16 E7-пептидом E7aa43-77 приводит к сильному замедлению роста опухолей (4 полных ответа в случае 5 мкг пептида E7+50 мкг комплекса полимерного носителя и переносимого вещества; 7 полных ответов в случае 50 мкг пептида E7+50 мкг комплекса полимерного носителя и переносимого вещества). Таким образом, сочетание комплекса полимерного носителя и переносимого вещества с полученным из HPV-16 пептидом E7 индуцирует мощный ответ T-клеток-памяти CD8+ (фигура 28).
15. Выявление антигенспецифичных клеточных иммунных ответов с использованием окрашивания пентамером:
Свежевыделенные спленоциты высевали в 96-луночные планшеты (2×106 клеток/лунку) и красили, используя Fc-Block (1:100, анти-CD16/CD32; BD Biosciences). После 20-минутной инкубации добавляли H-2Db-RAHYNIVTF-пентамер (HPV 16 E7 49-57)-пентамер-PE (10 мкл/лунку) и клетки инкубировали еще в течение 30 минут при 4°C. После промывки клетки красили следующими антителами: CD19-ФИТЦ (1:200), CD8-PerCP-Cy5.5 (1:200), KLRG1-PECy7 (1:200), CD44-APC (1:100), CD127-eFluor450 (1:100) (eBioscience) и CD3-APC-Cy7 (1:200) (BD Biosciences). Aqua Dye использовали для того, чтобы отличить живые/мертвые клетки (Invitrogen). Клетки собирали, используя проточный цитометр Canto II (Beckton Dickinson). Данные проточной цитометрии анализировали, используя компьютерную программу Flowjo (Tree Star, Inc.). Статистический анализ осуществляли, используя компьютерную программу GraphPad Prism, версию 5.01. Статистические различия между группами оценивали, используя двухвыборочный t-критерий для независимых выборок с поправкой Уэлча.
16. Иммунизация вирусами сезонного гриппа и выявление антител:
Для иммунизации вакцину против сезонного гриппа мутагрип® (содержит инактивированные штаммы вируса гриппа, которые рекомендованы ВОЗ; сезон 2011/2012) (4,5, 0,45 и 0,045 мкг) объединяли с комплексами полимерного носителя и переносимого вещества R722/CR12C (в соотношении 3,7:1 масс./масс.) (5 мкг R722/1,35 мкг CR12C) в качестве адъюванта и инъецировали внутримышечно самкам мышей Balb/c (8 мышей на группу). Для сравнения мышам инъецировали мутагрип® отдельно.
Выявление антигенспецифичного иммунного ответа (B-клеточного иммунного ответа) осуществляли, выявляя титры ингибирования гемагглютинации вируса гриппа (HI). При этом собирали образцы крови от вакцинированных мышей через 21 день после вакцинации, и сыворотки инактивировали нагреванием, инкубировали с каолином и предварительно адсорбировали на эритроцитах цыплят. Для анализа HI 50 мкл 2-кратных разведений предварительно обработанных сывороток инкубировали с инактивированным вирусом гриппа A California/7/2009 H1N1 или вирусом гриппа A Victoria/210/2009 H3N2 (оба NIBSC) и добавляли 50 мкл 0,5% эритроцитов цыпленка. Результаты такой индукции титров HI при вакцинации фармацевтической композицией согласно изобретению показаны на фигуре 29.
Выявление антигенспецифичного иммунного ответа (B-клеточного иммунного ответа) осуществляли, выявляя специфичные для вируса гриппа IgG2a-антитела. При этом собирали образцы крови от вакцинированных мышей через 21 день после вакцинации и готовили сыворотку. Планшеты MaxiSorb (Nalgene Nunc International) покрывали инактивированным вирусом гриппа A/California/7/2009 H1N1 (NIBSC, Potters Bar, UK) в концентрации 1 мкг/мл. После блокирования 1×PBS, содержащим 0,05% твин-20 и 1% БСА, планшеты инкубировали с разбавленной сывороткой мышей. Затем добавляли связанное с биотином второе антитело (антитело против IgG2a мыши, Pharmingen). После промывки планшет инкубировали с пероксидазой хрена-стрептавидином и затем измеряли превращение субстрата ABTS (2,2'-азино-бис(3-этил-бензтиазолин-6-сульфоновой кислоты), чтобы определить индукцию IgG2a-антител. Результаты такой индукции антител при вакцинации фармацевтической композицией согласно изобретению показаны на фигуре 30.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛУЧЕНИЕ КОМПЛЕКСОВ НУКЛЕИНОВЫХ КИСЛОТ И ПОПЕРЕЧНО СШИТЫХ ДИСУЛЬФИДНЫМИ СВЯЗЯМИ КАТИОННЫХ КОМПОНЕНТОВ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ТРАНСФЕКЦИИ И ИММУНОСТИМУЛЯЦИИ | 2011 |
|
RU2575603C2 |
| РЕЖИМЫ ПРАЙМ-БУСТ, ВКЛЮЧАЮЩИЕ ВВЕДЕНИЕ ПО МЕНЬШЕЙ МЕРЕ ОДНОЙ КОНСТРУКЦИИ мРНК | 2016 |
|
RU2742993C2 |
| КОМБИНАЦИЯ ПРОТИВОРАКОВОЙ РНК-ВАКЦИНЫ И ИНГИБИТОРА ПУТИ PD-1 И ЕЕ ПРИМЕНЕНИЕ | 2014 |
|
RU2718988C2 |
| ГИБРИДНЫЕ НОСИТЕЛИ ДЛЯ ДОСТАВКИ НУКЛЕИНОВЫХ КИСЛОТ | 2017 |
|
RU2751001C2 |
| СВЯЗАННЫЕ ДИСУЛЬФИДНОЙ СВЯЗЬЮ КОНЪЮГАТЫ ПОЛИЭТИЛЕНГЛИКОЛЯ/ПЕПТИДА ДЛЯ ТРАНСФЕКЦИИ НУКЛЕИНОВЫХ КИСЛОТ | 2010 |
|
RU2552352C2 |
| ИММУНОСТИМУЛИРУЮЩИЕ И ВАКЦИННЫЕ КОМПОЗИЦИИ | 2011 |
|
RU2578420C2 |
| РЕЦЕПТУРА ДЛЯ ВВЕДЕНИЯ РНК | 2019 |
|
RU2797147C2 |
| СЛИТЫЕ ПОЛИПЕПТИДЫ И ВАКЦИНЫ | 2014 |
|
RU2699006C2 |
| КОНЪЮГАТЫ И КОМПОЗИЦИИ ДЛЯ ИММУНОТЕРАПИИ И ПРОТИВООПУХОЛЕВОГО ЛЕЧЕНИЯ | 2010 |
|
RU2597989C2 |
| СОСТАВ ДЛЯ ВВЕДЕНИЯ РНК | 2017 |
|
RU2746118C2 |
































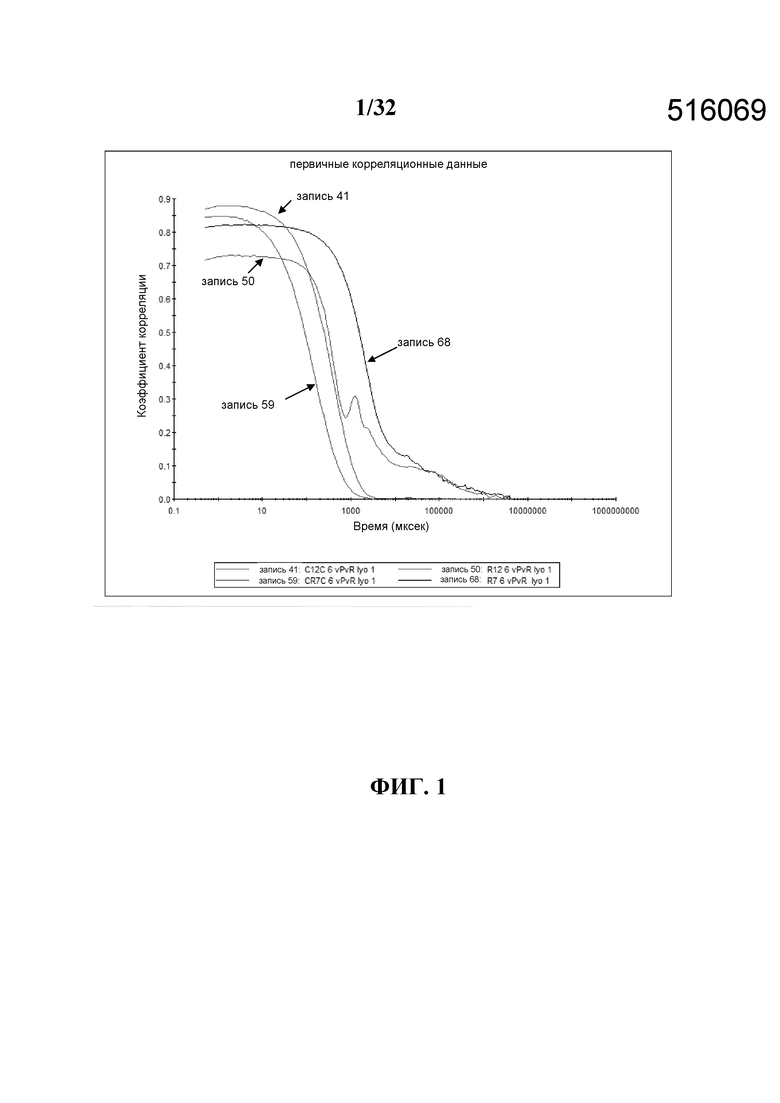
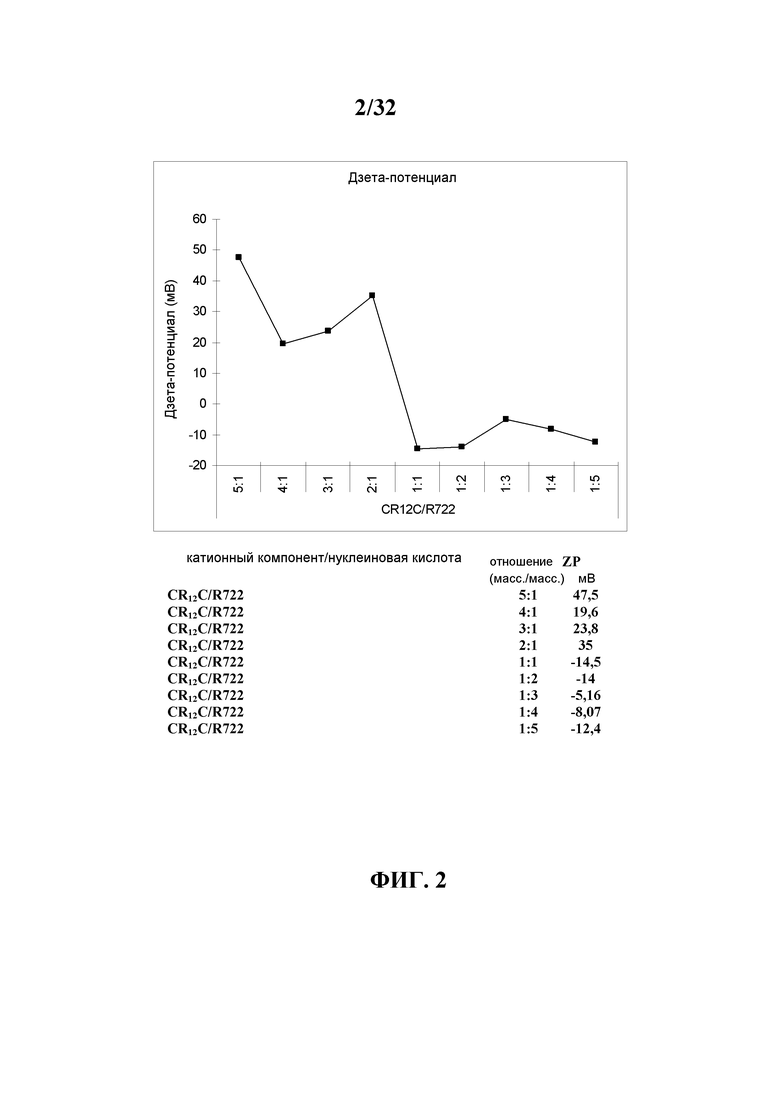
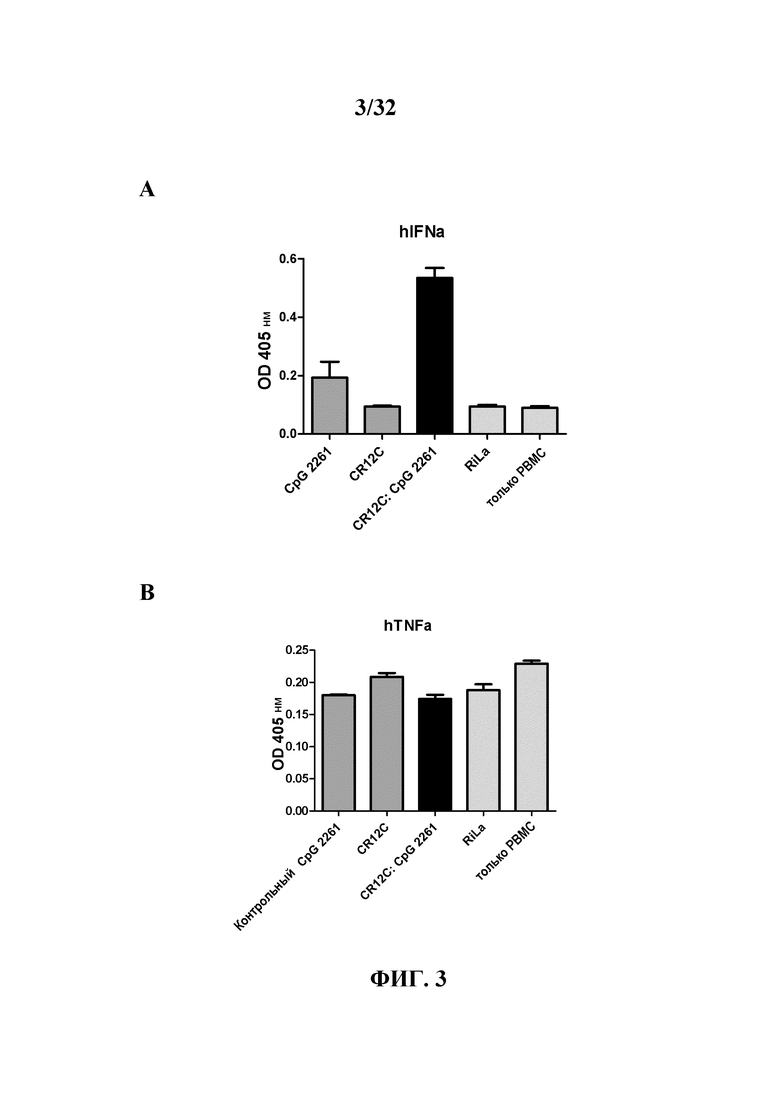
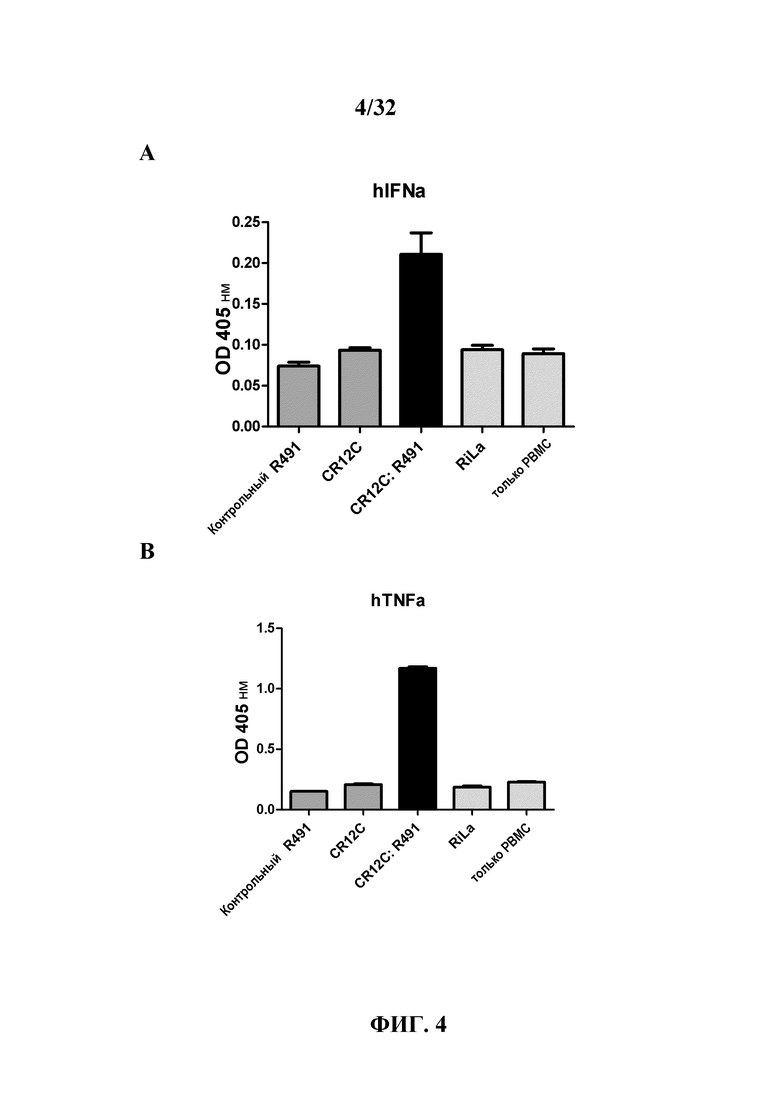
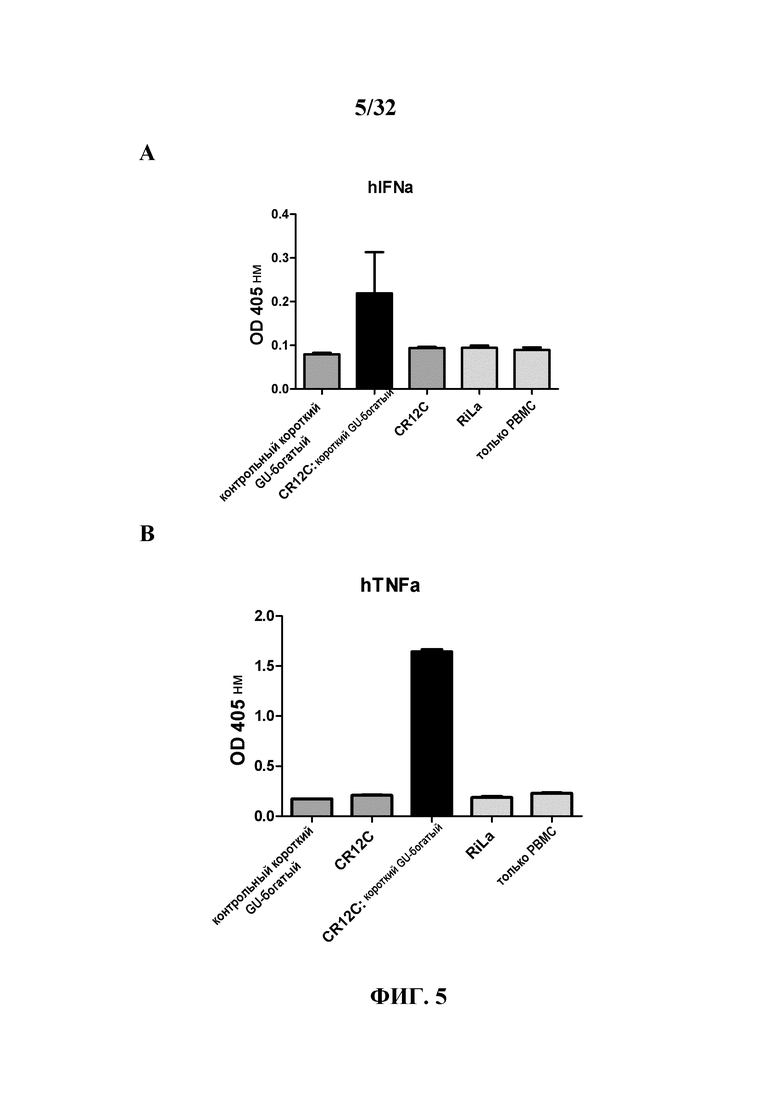
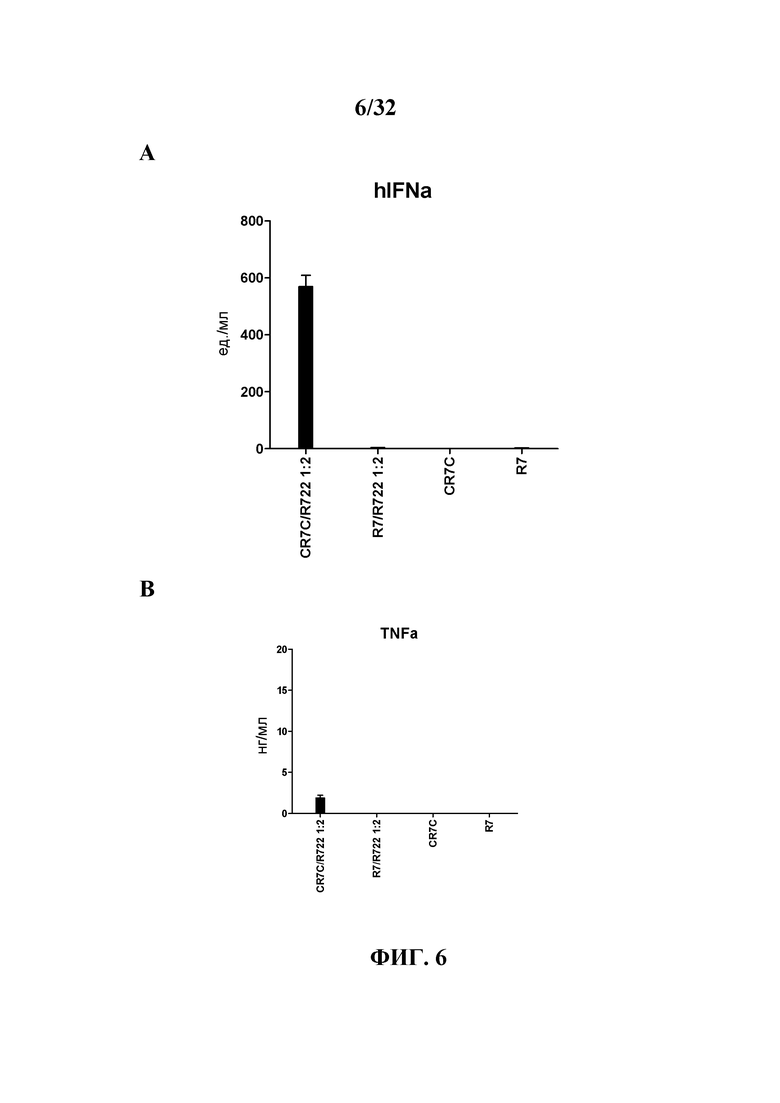
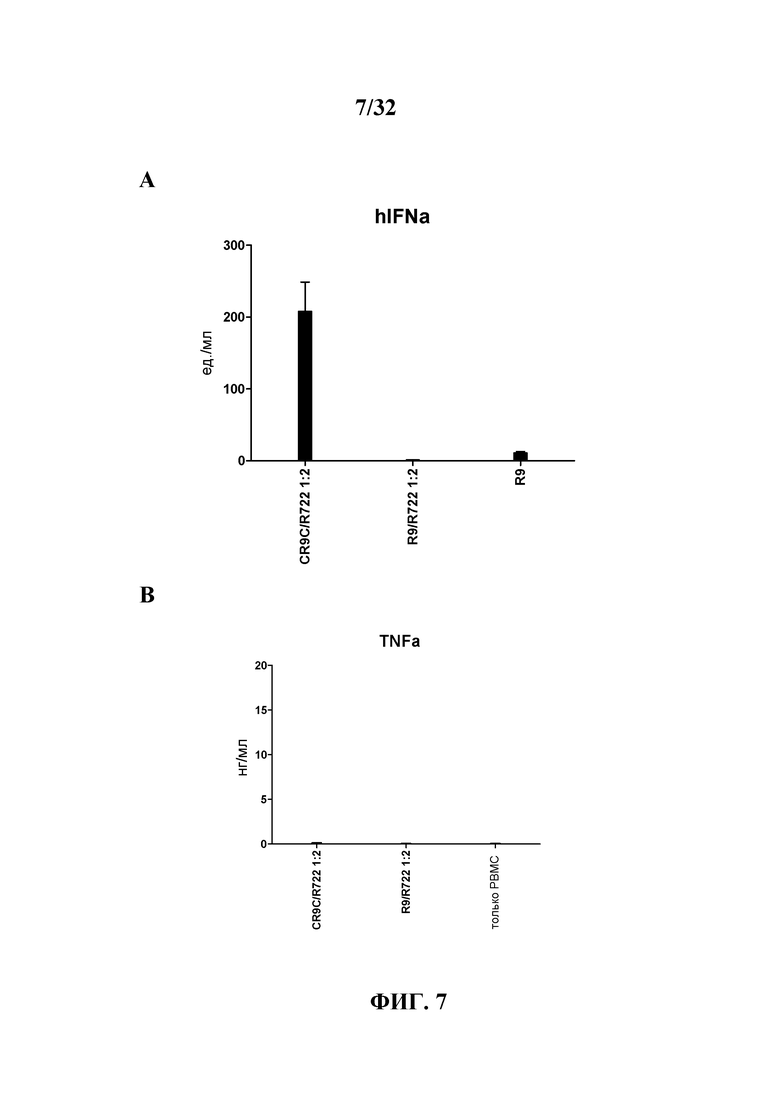
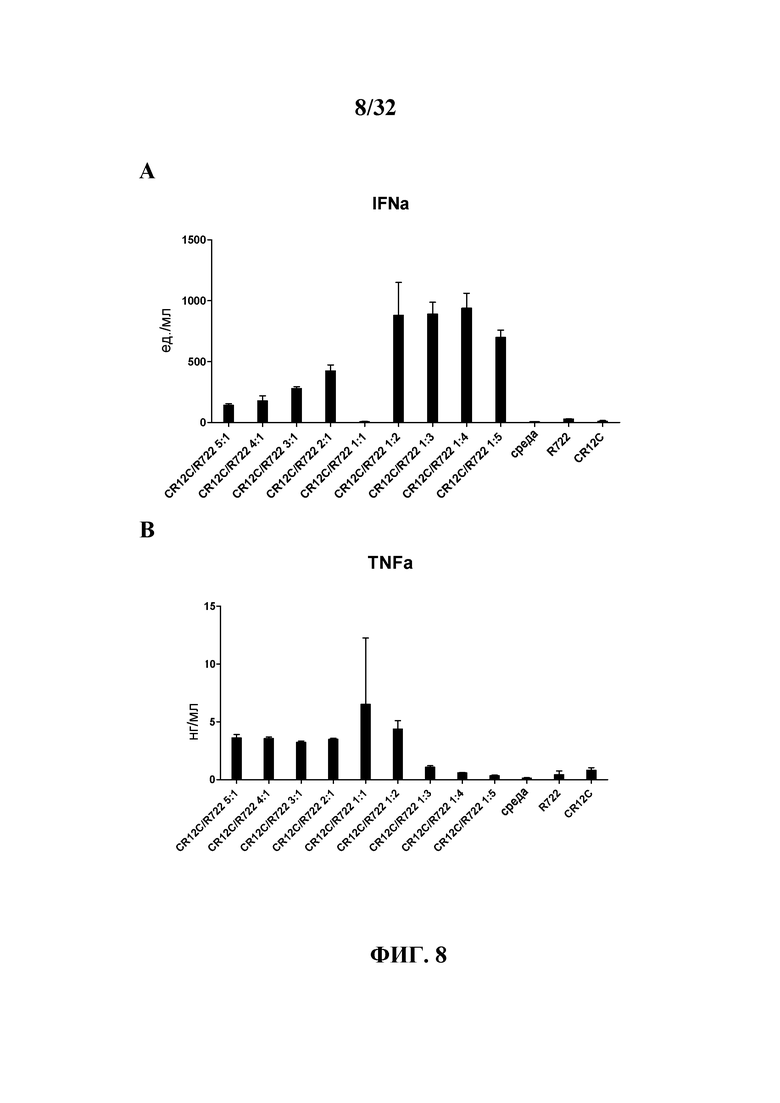
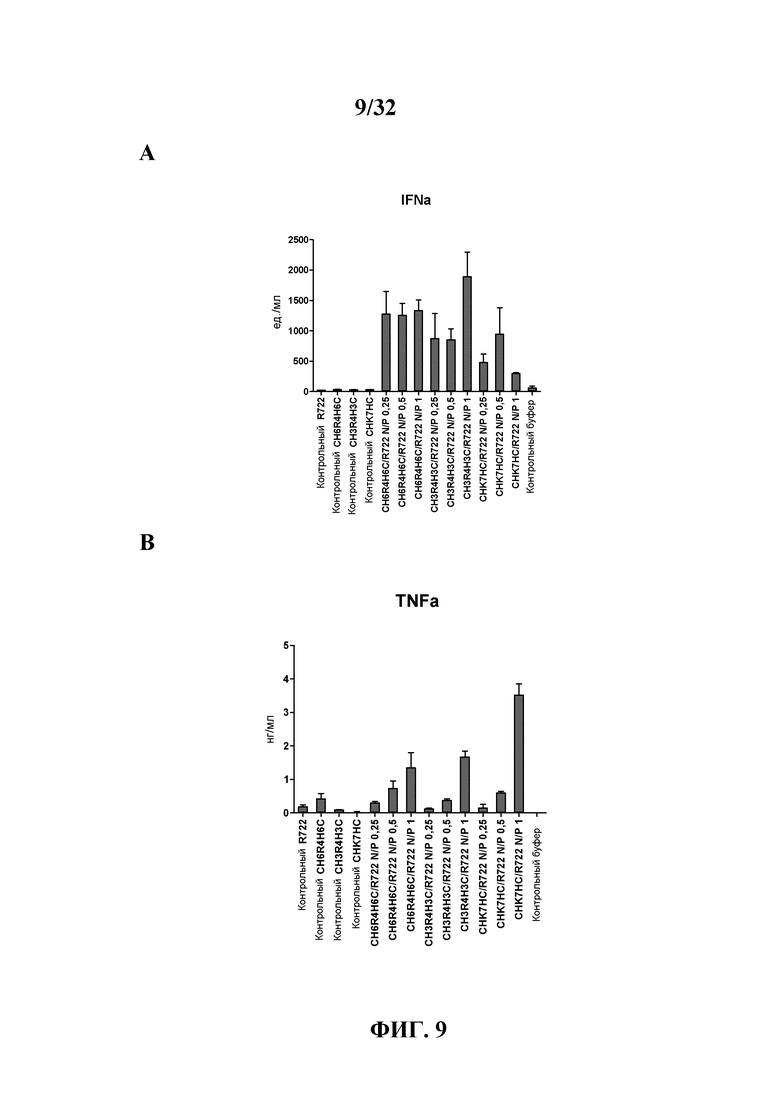
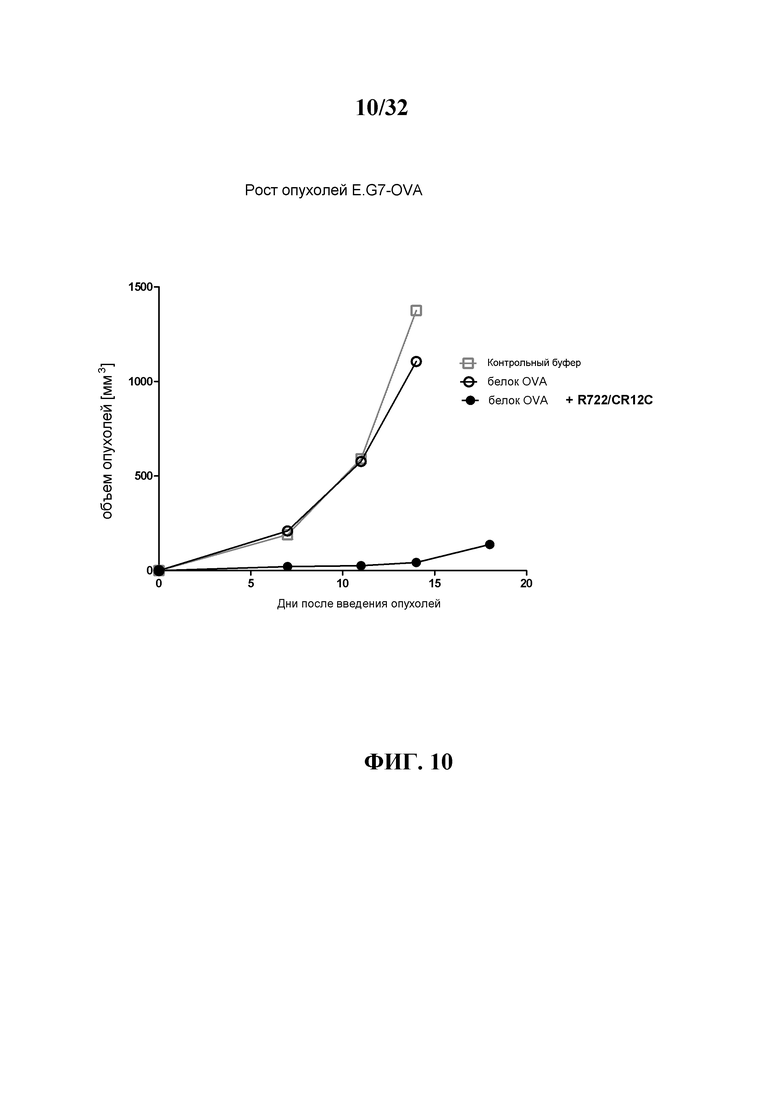
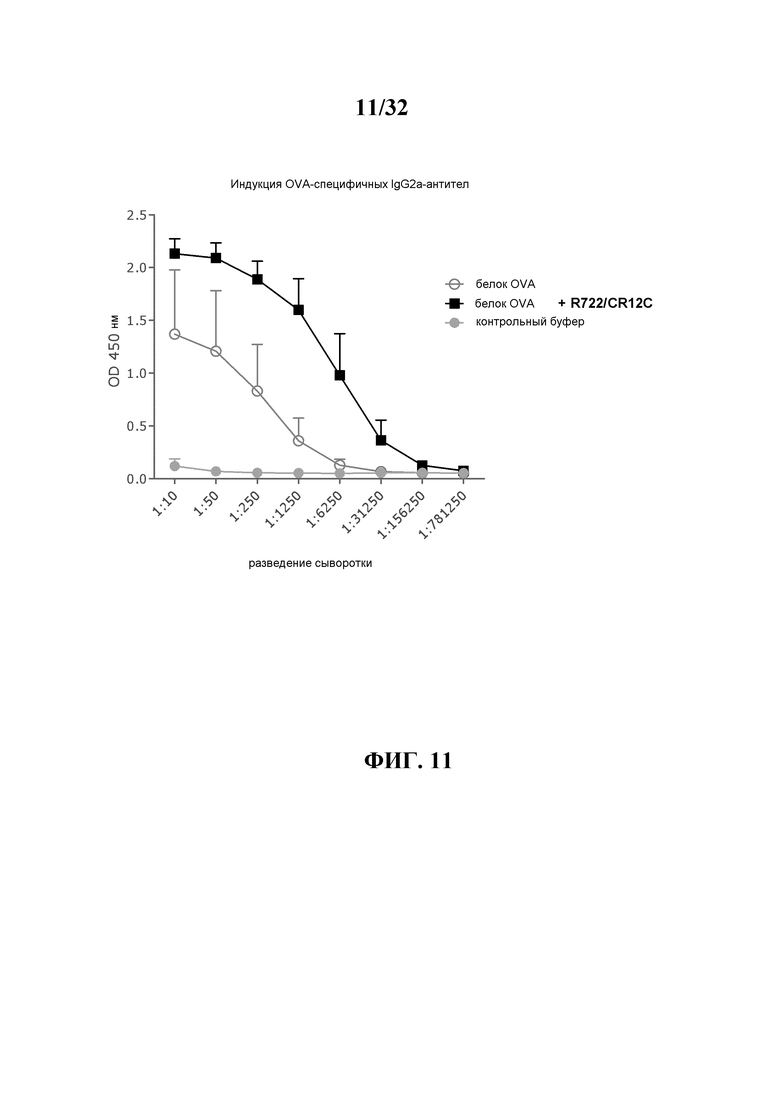
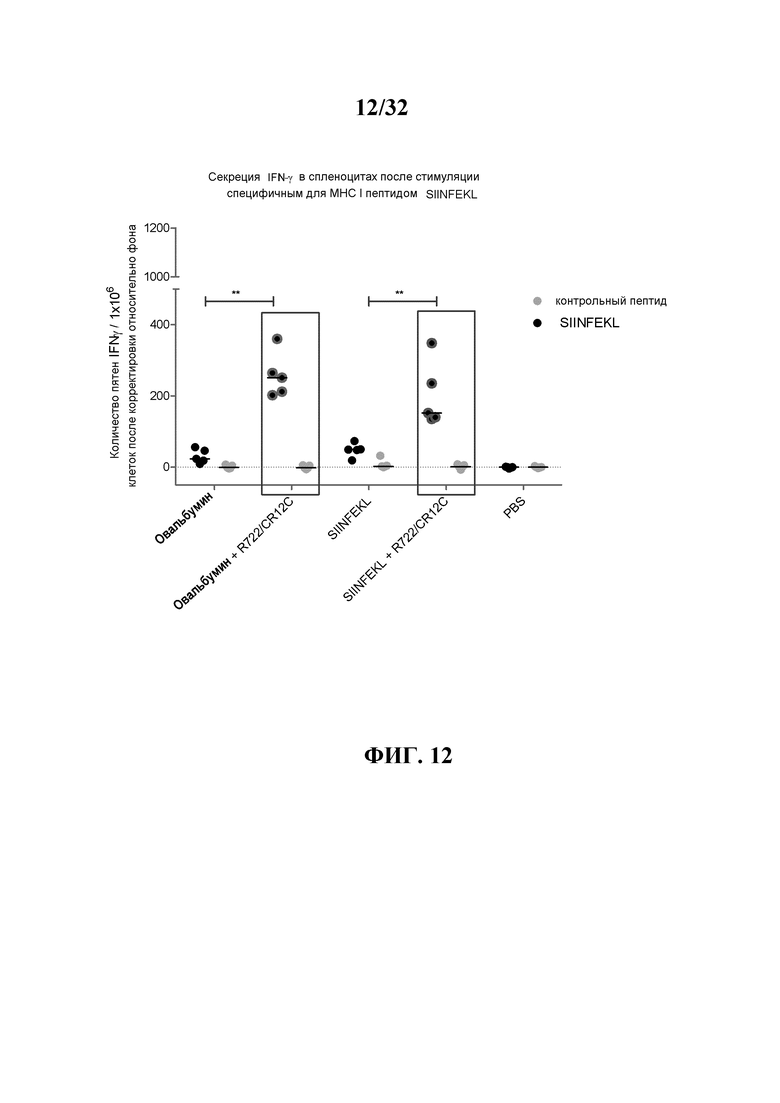
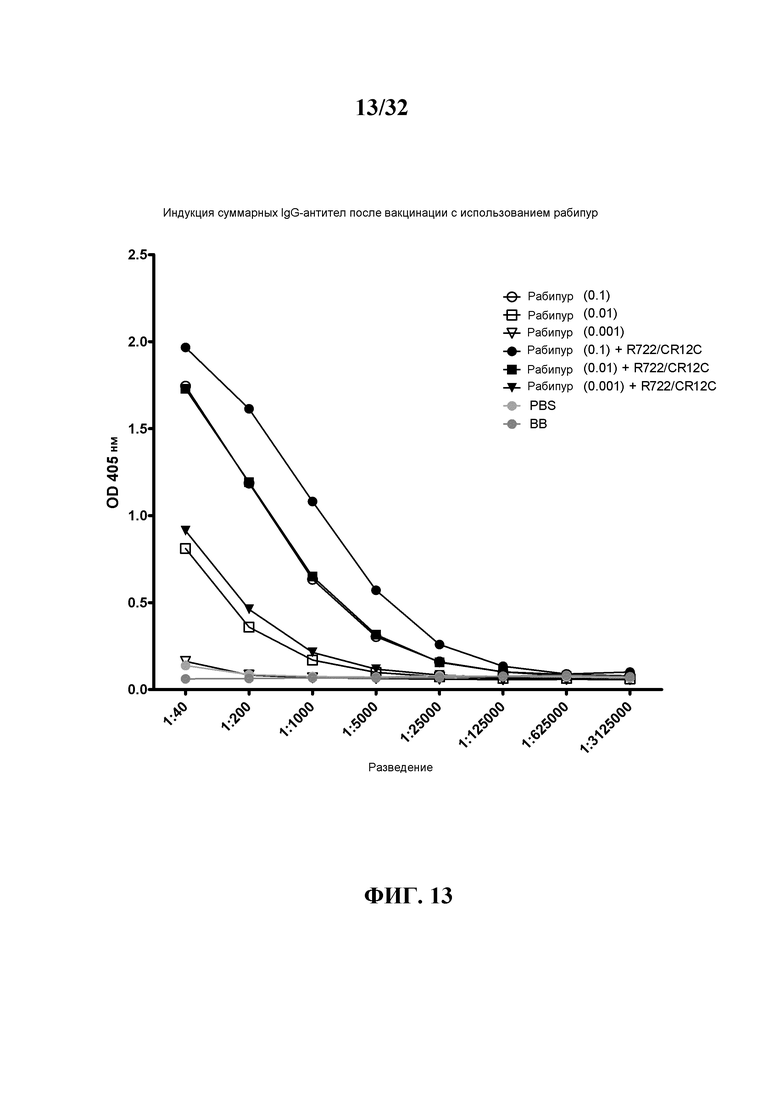
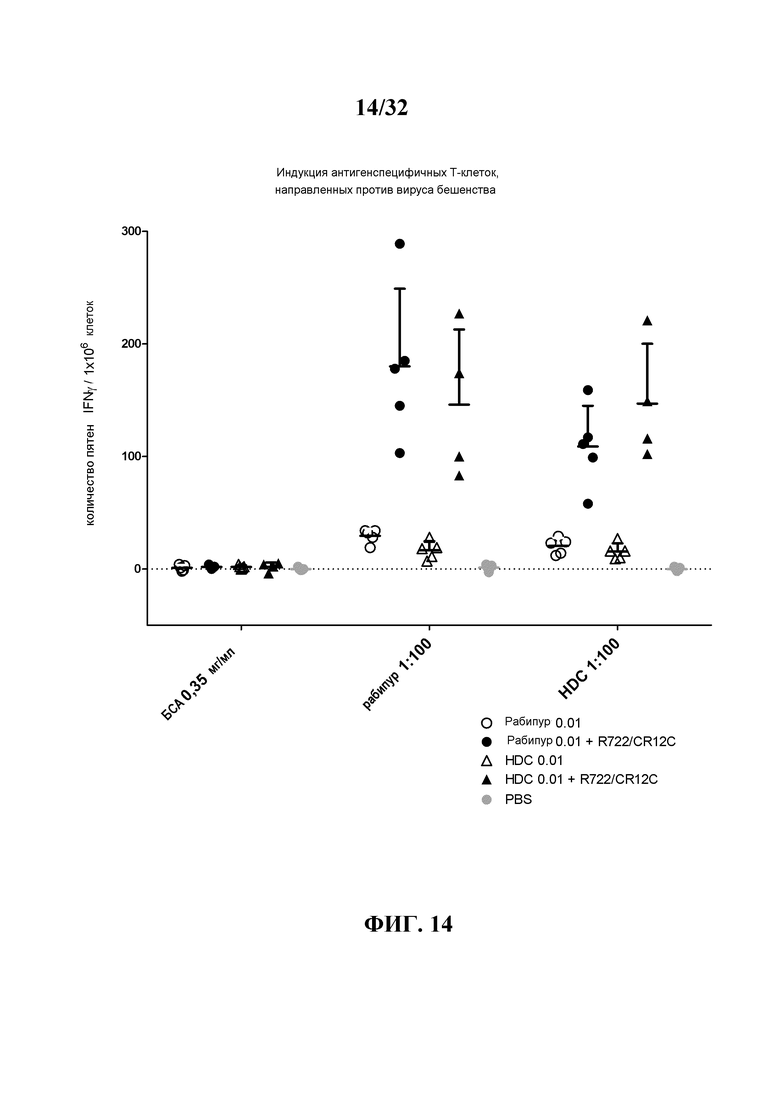
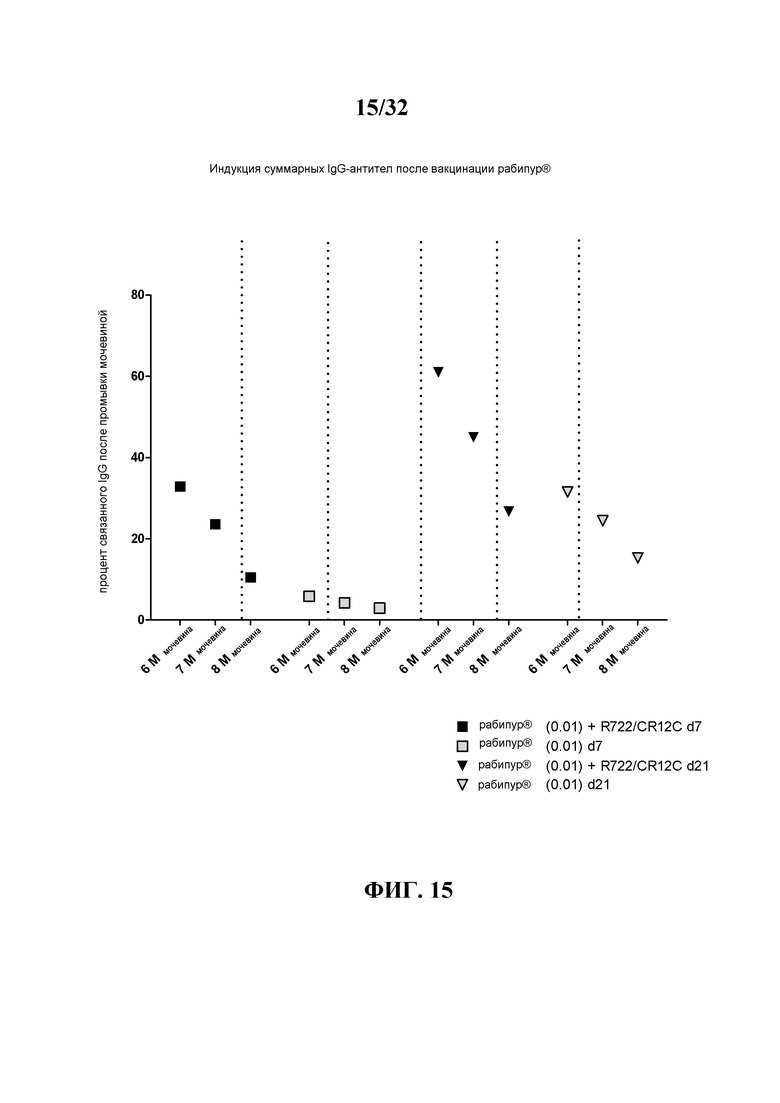
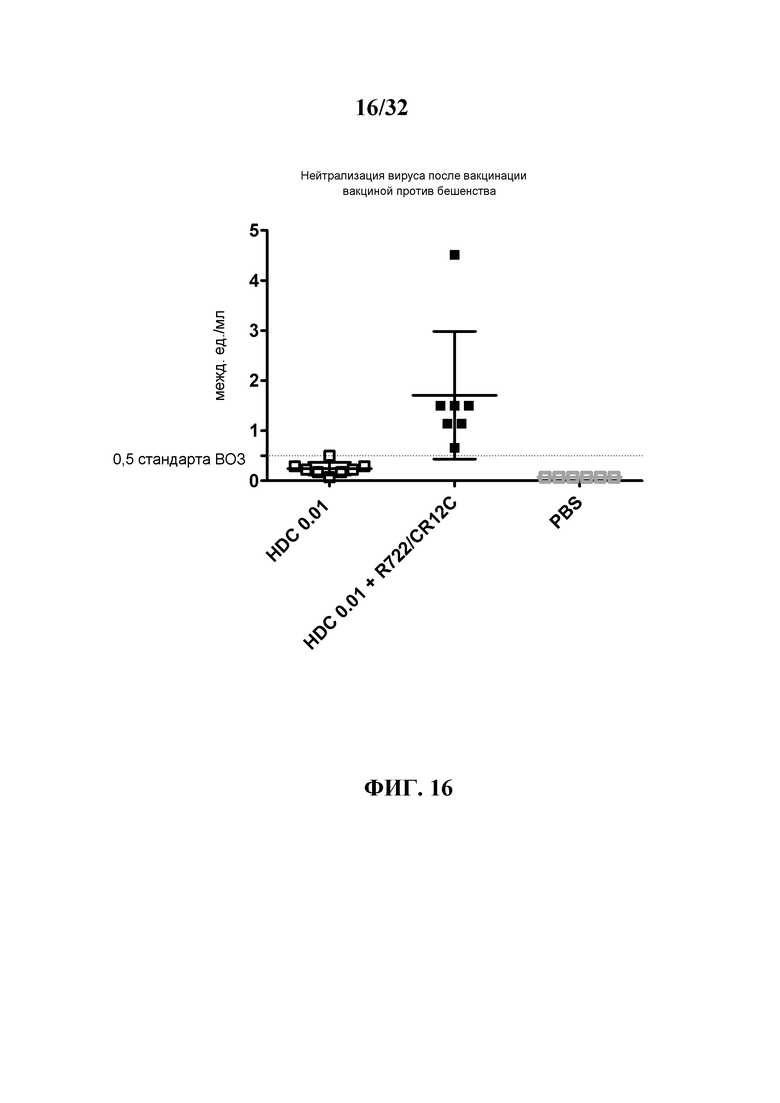
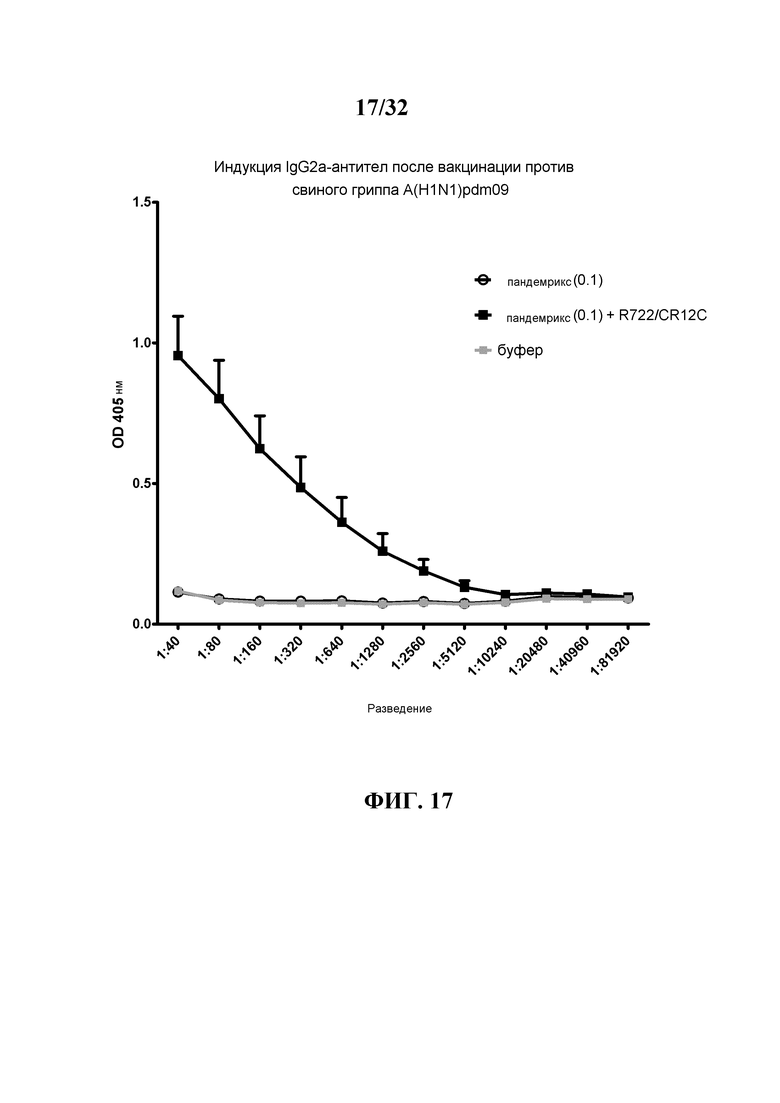
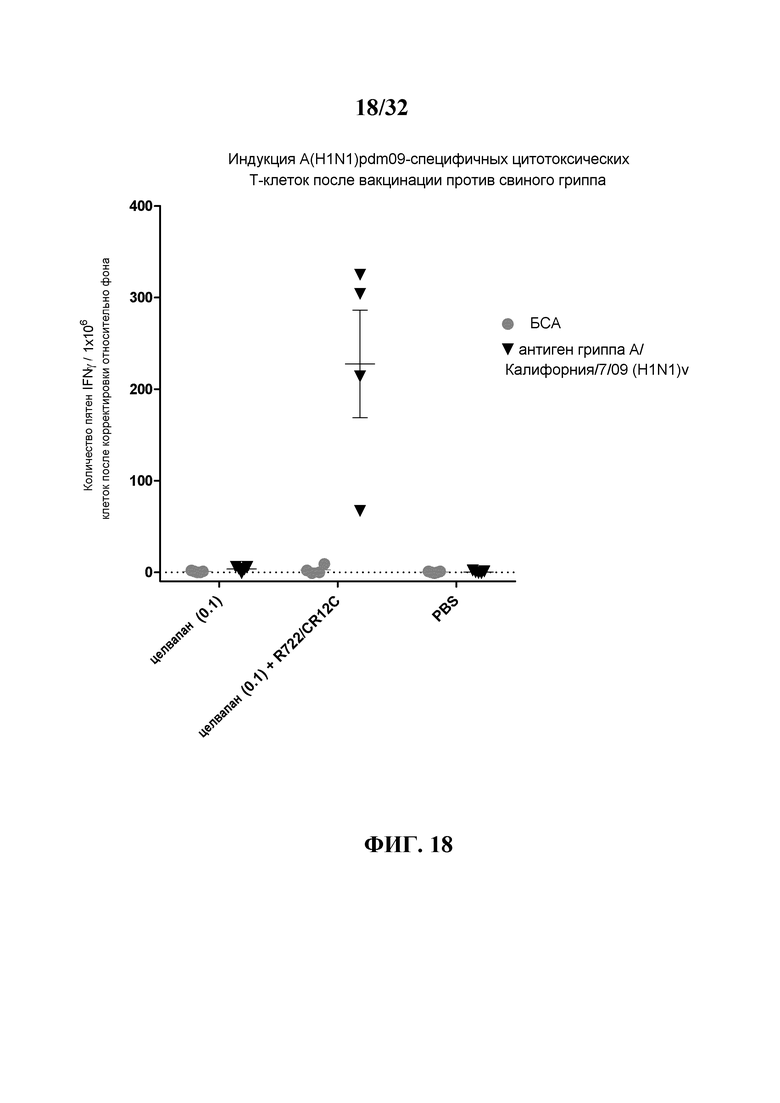
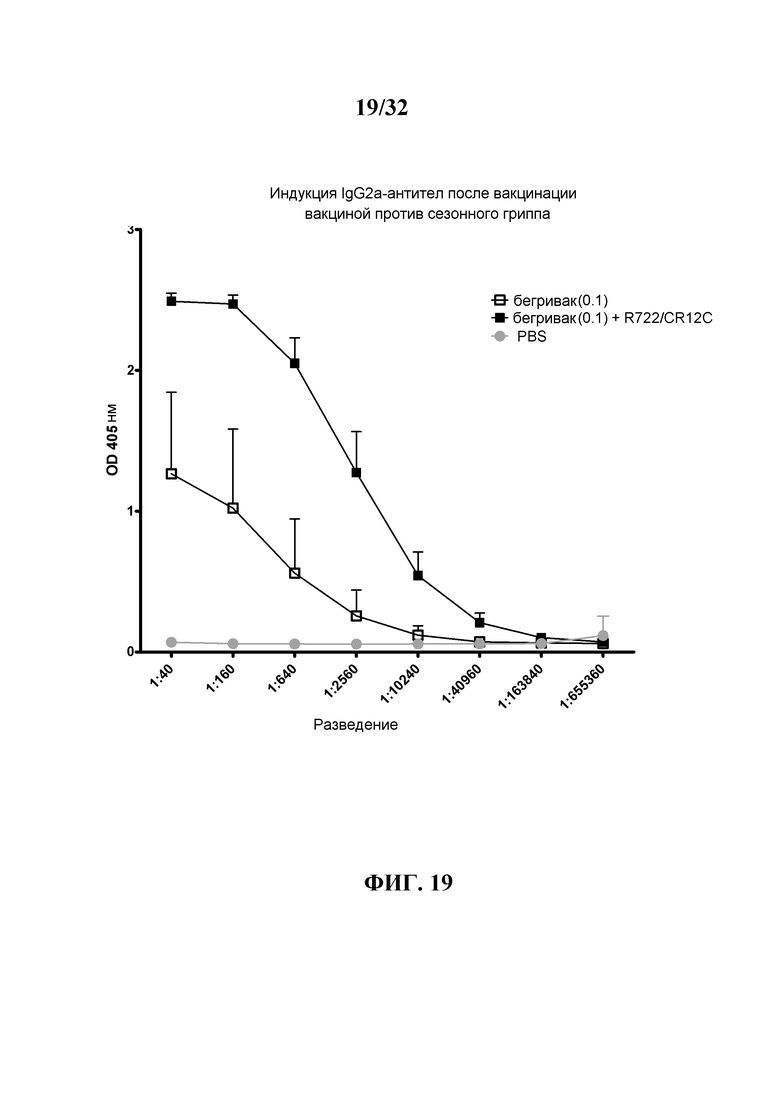
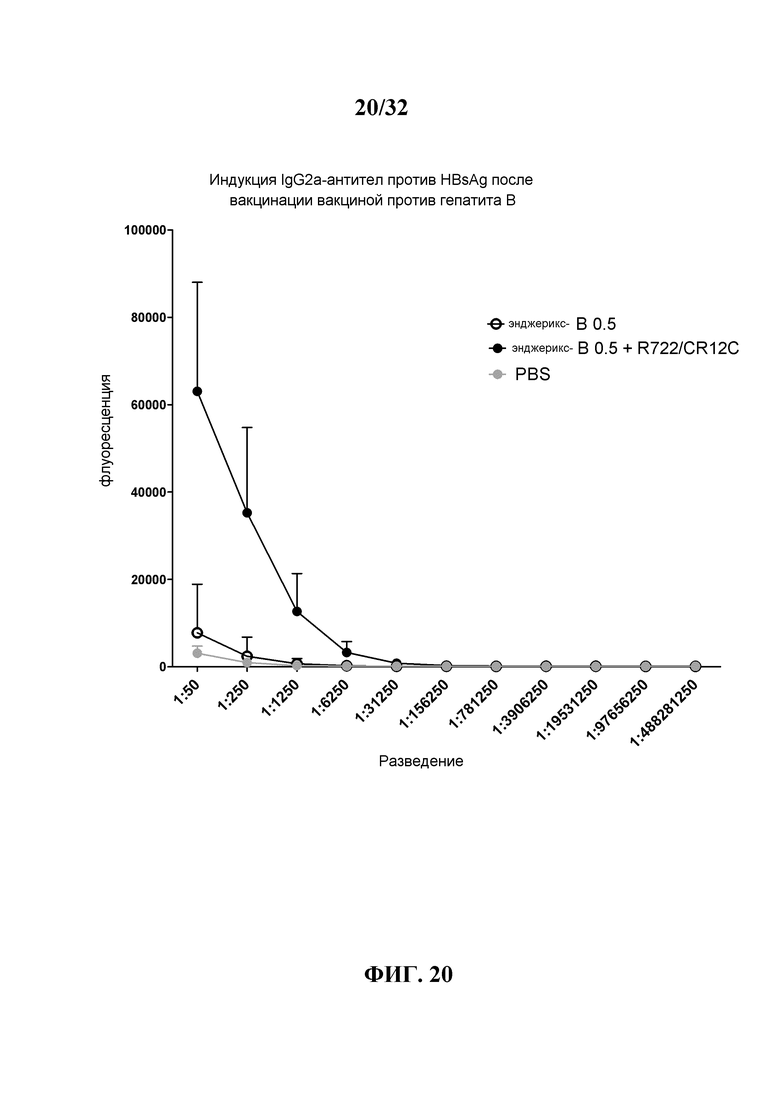
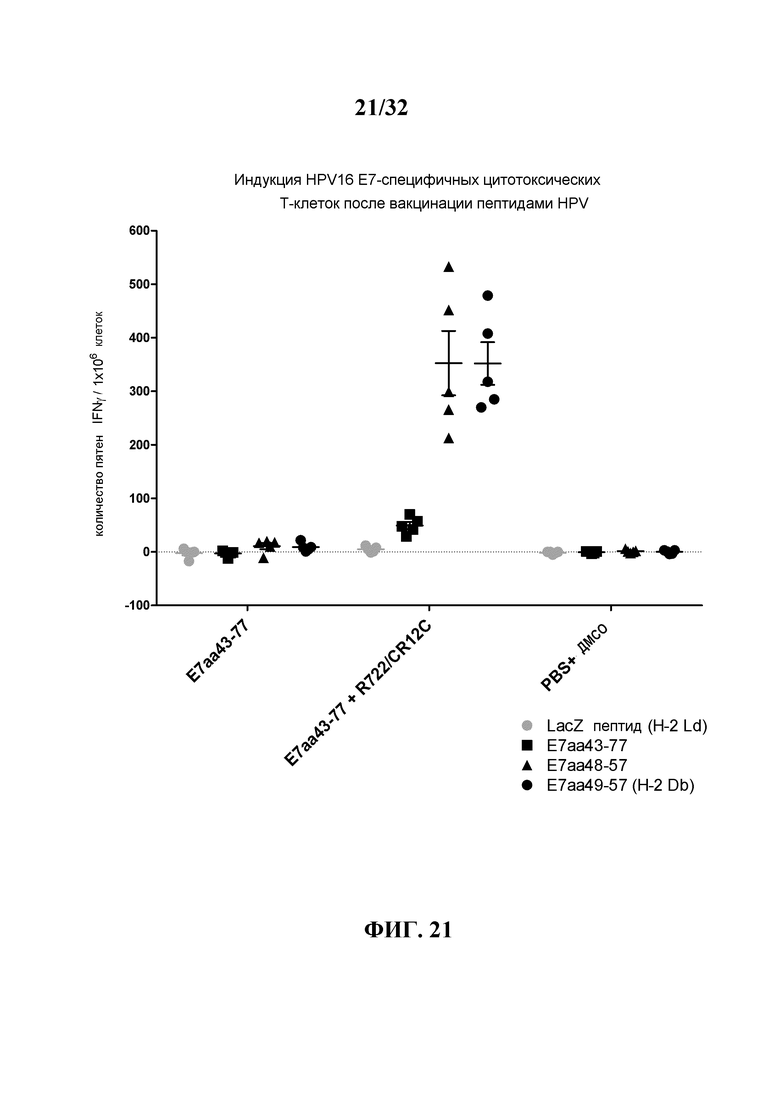
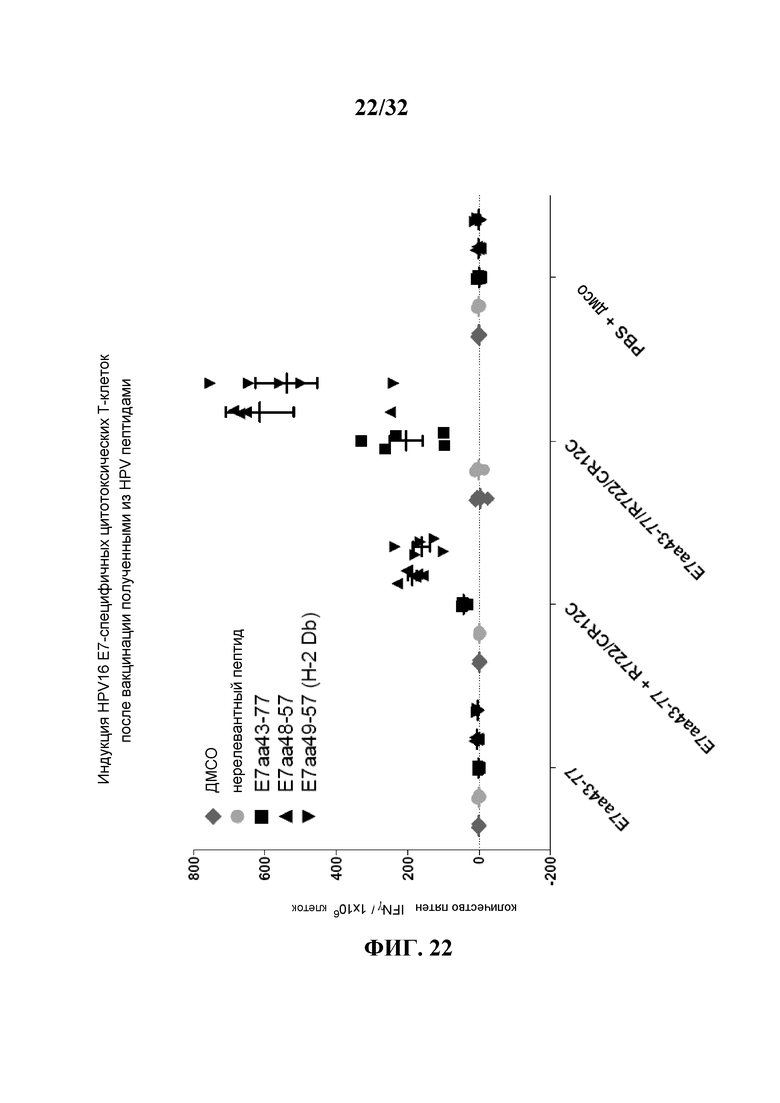
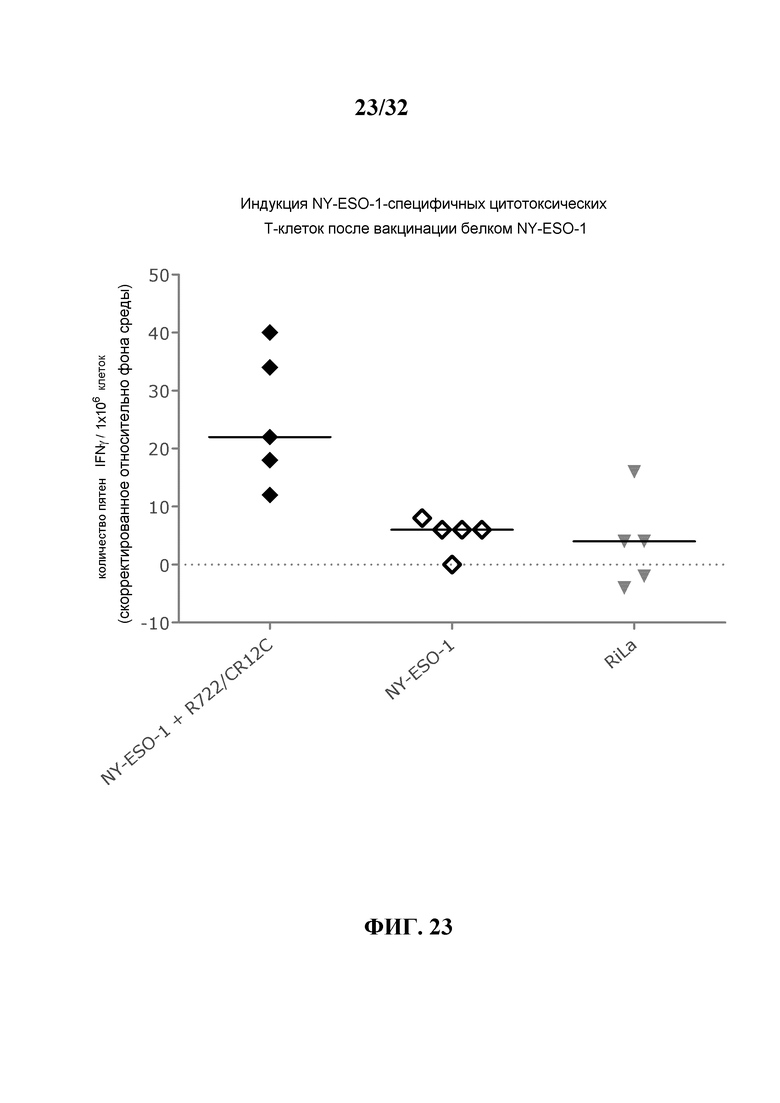

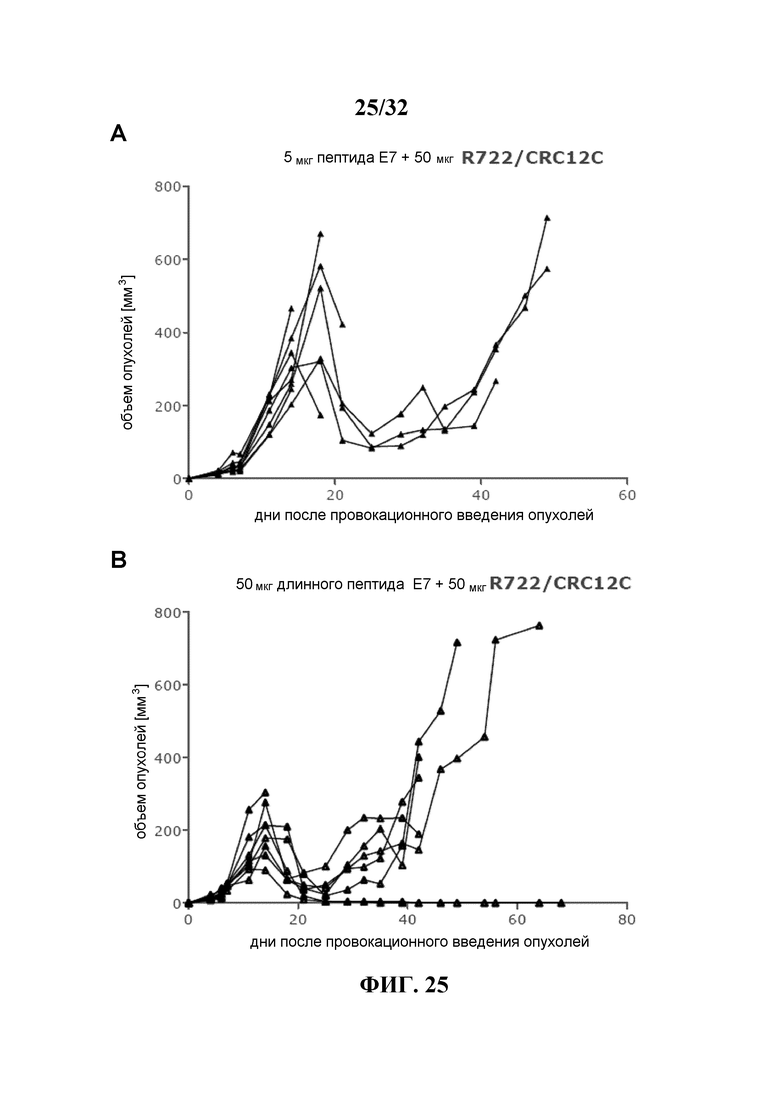
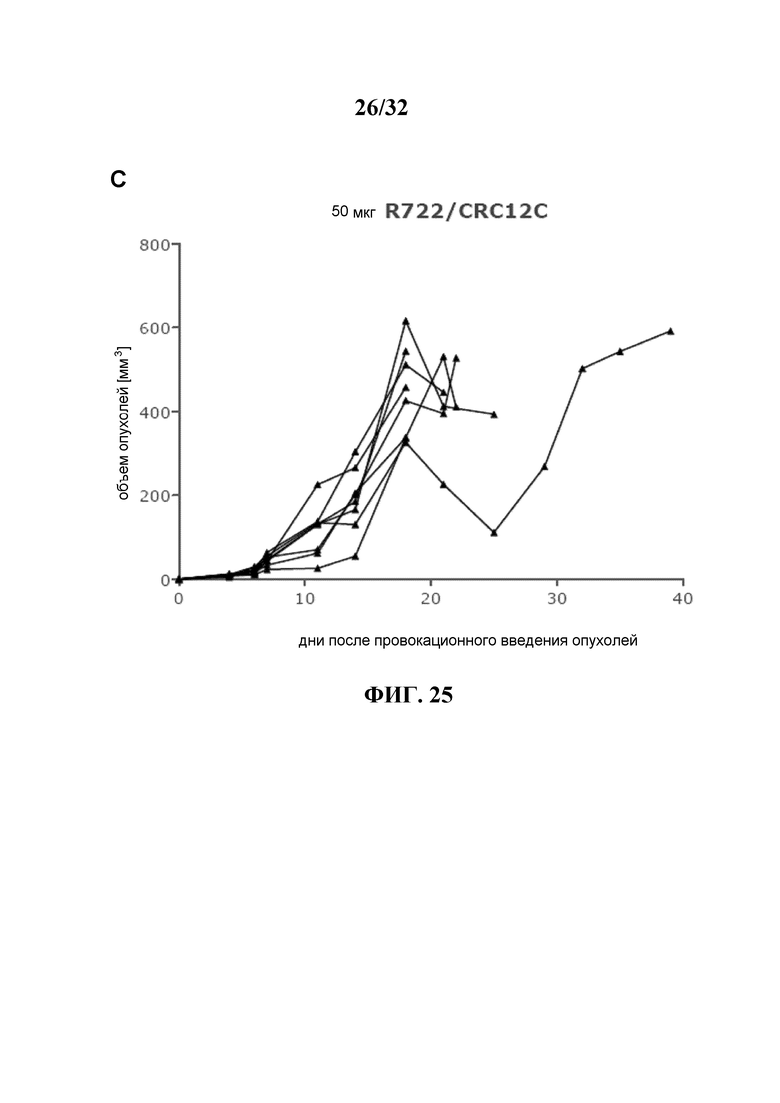
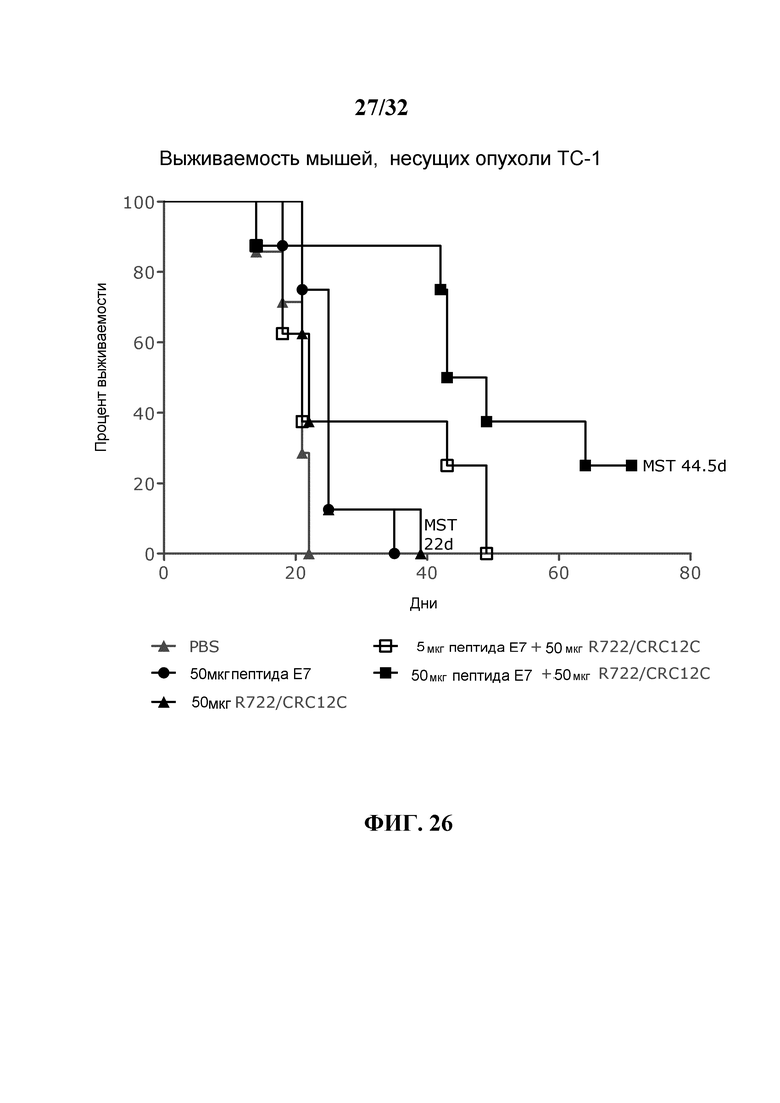
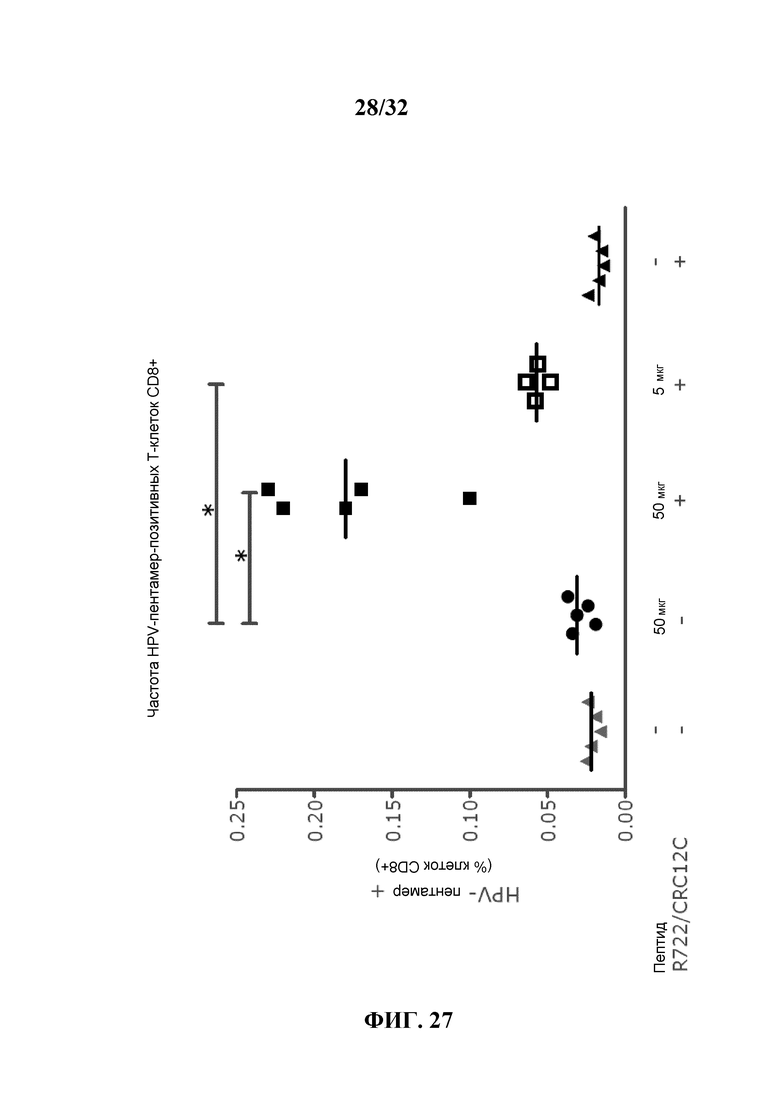
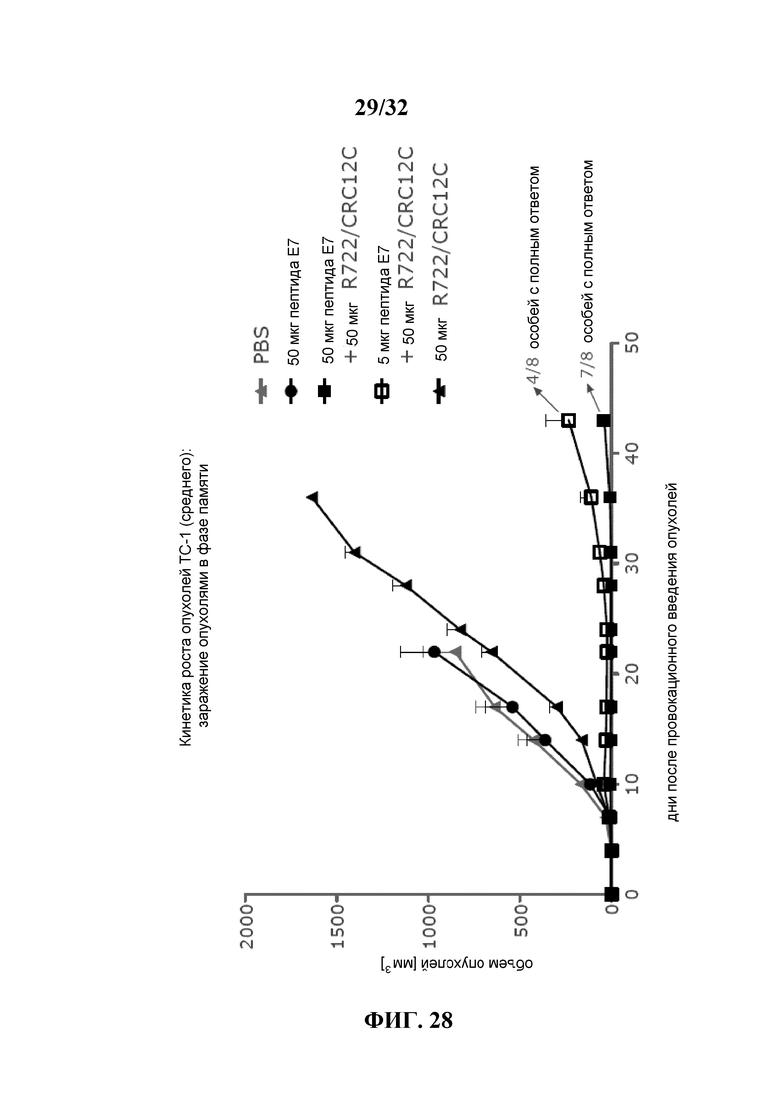
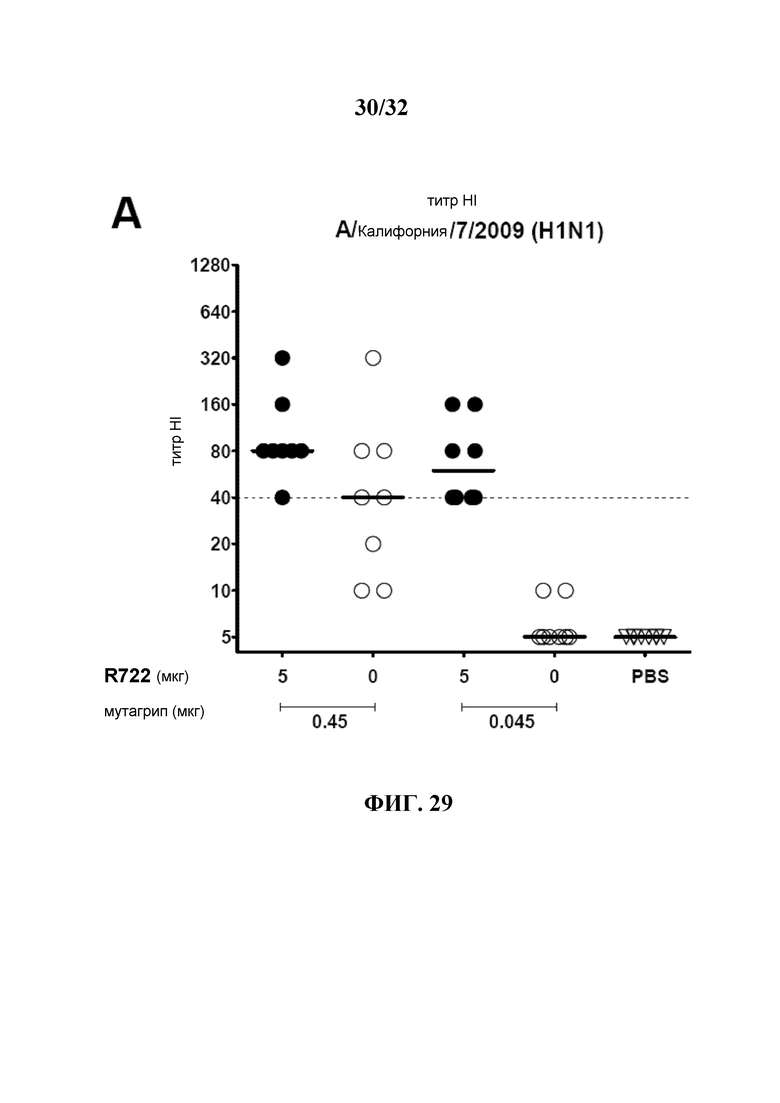
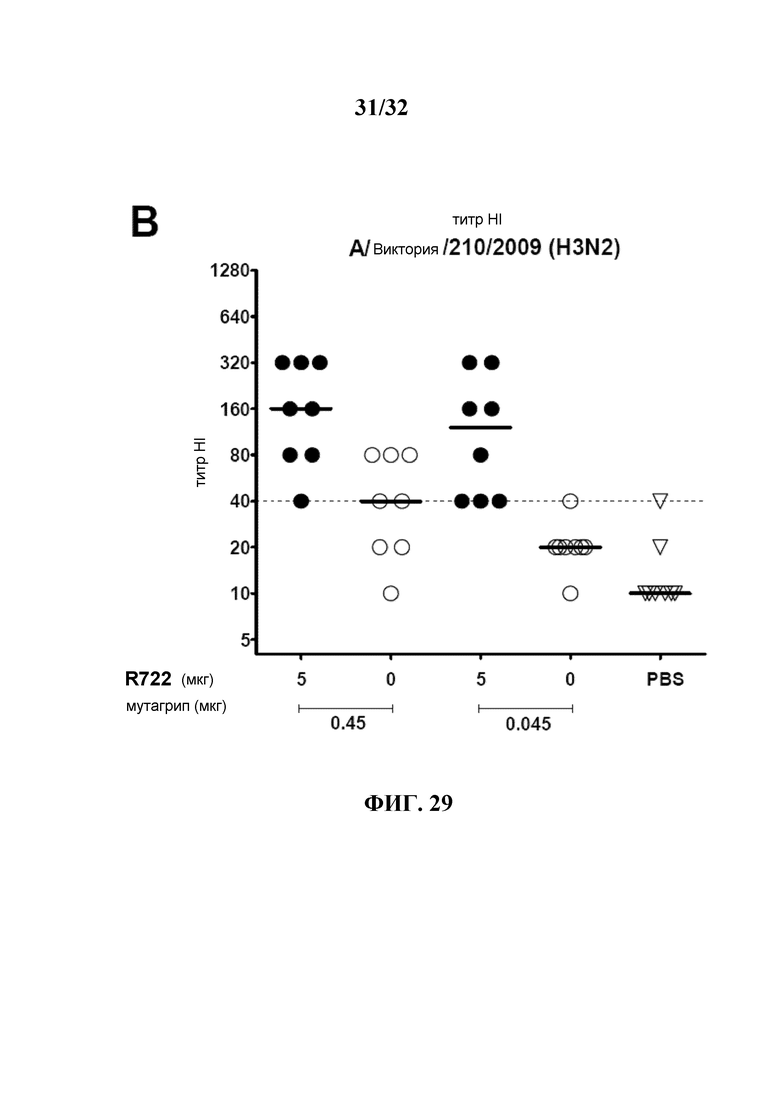
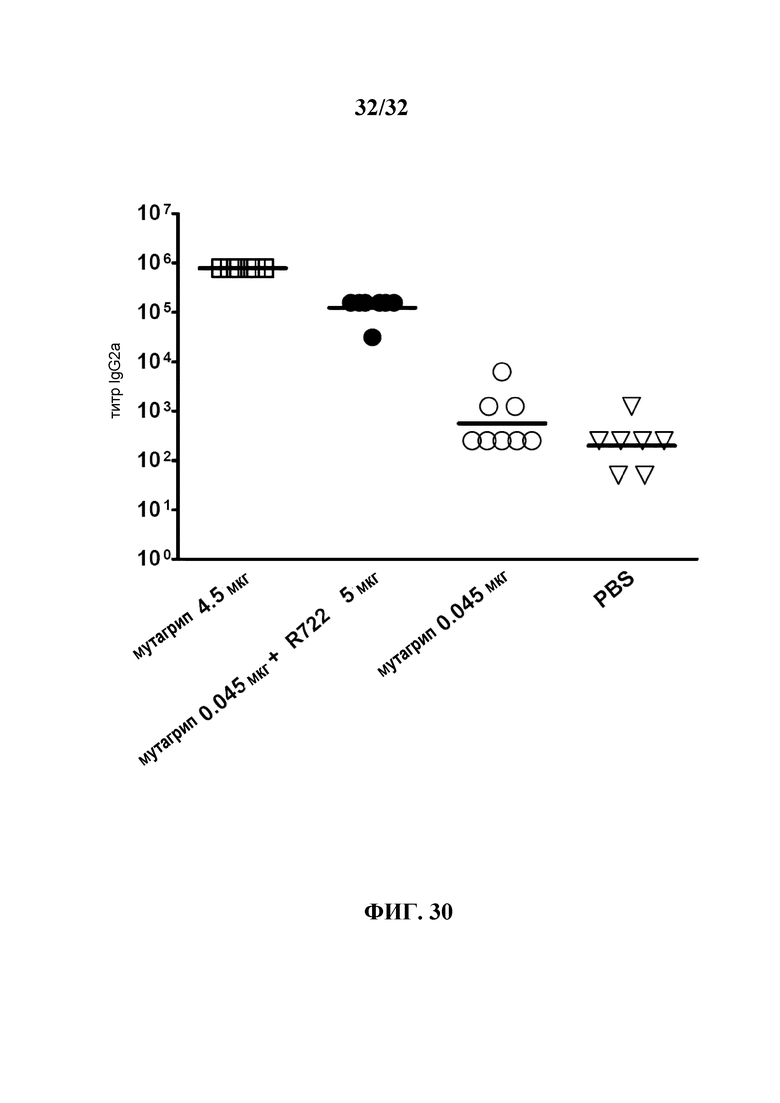
Группа изобретений относится к медицине и касается фармацевтической композиции для вакцинации против инфекционной болезни, аллергии или аллергического заболевания, аутоиммунного заболевания, или рака или опухолевого заболевания, содержащей комплекс полимерного носителя и переносимого вещества, по меньшей мере один белковый или пептидный антиген. Группа изобретений также касается набора для вакцинации против инфекционной болезни, аллергии или аллергического заболевания, аутоиммунного заболевания, или рака, или опухолевого заболевания; применения указанной фармацевтической композиции в качестве вакцины. Группа изобретений обеспечивает увеличение иммунного ответа против пептида или белка. 4 н. и 9 з.п. ф-лы, 16 пр., 30 ил., 1 табл.
1. Фармацевтическая композиция для вакцинации против инфекционной болезни, аллергии или аллергического заболевания, аутоиммунного заболевания, или рака, или опухолевого заболевания, содержащая:
(A) комплекс полимерного носителя и переносимого вещества, содержащий:
a) полимерный носитель, содержащий поперечно сшитые дисульфидными связями катионные компоненты в качестве носителя; и
b) по меньшей мере одну молекулу нуклеиновой кислоты в качестве переносимого вещества, и
(B) по меньшей мере один белковый или пептидный антиген, который выбран из группы, состоящей из:
(i) антигена из патогена, ассоциированного с инфекционной болезнью;
(ii) антигена, ассоциированного с аллергией или аллергическим заболеванием;
(iii) антигена, ассоциированного с аутоиммунным заболеванием; и
(iv) антигена, ассоциированного с раком или опухолевым заболеванием,
или фрагмента, варианта и/или производного указанного белкового или пептидного антигена;
где катионные компоненты представляют собой катионные пептиды, выбранные из пептидов, соответствующих подформуле (Ia):
{(Arg)l;(Lys)m;(His)n;(Orn)o;(Xaa')x(Cys)y},
или из пептидов, соответствующих подформуле (Ib)
Cysl{(Arg)1;(Lys)m;(His)n;(Orn)o;(Xaa)x}Cys2,
где
сумма l, m, n, о и x представляет собой значение от 3 до 100, и l, m, n или о независимо друг от друга являются любым числом, выбранным из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21-30, 31-40, 41-50, 51-60, 61-70, 71-80, 81-90 и 91-100, при условии, что общее содержание Arg, Lys, His и Orn составляет по меньшей мере 10% от всех аминокислот катионного пептида; и Хаа означает любую аминокислоту, выбранную из нативных (= встречающихся в природе) или ненативных аминокислот, за исключением Arg, Lys, His или Orn; и
х означает любое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21-30, 31-40, 41-50, 51-60, 61-70, 71-80, 81-90, при условии, что общее содержание Хаа не превышает 90% всех аминокислот катионного пептида;
Хаа' означает любую аминокислоту, выбранную из нативных (= встречающихся в природе) или ненативных аминокислот, за исключением Arg, Lys, His, Orn; или Cys, и
y означает любое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21-30, 31-40, 41-50, 51-60, 61-70, 71-80 и 81-90, при условии, что общее содержание Arg (аргинина), Lys (лизина), His (гистидина) и Orn (орнитина) составляет по меньшей мере 10% от всех аминокислот олигопептида,
и при этом Cys1 и Cys2 означают цистеины, расположенные проксимально или терминально по отношению к (Arg)l; (Lys)m; (His)n; (Orn)o; (Xaa)x;
где переносимая молекула нуклеиновой кислоты представляет собой иммуностимулирующую РНК (исРНК).
2. Фармацевтическая композиция по п. 1, в которой компонент (В) не связан ковалентно с компонентом (А).
3. Фармацевтическая композиция по п. 1 или 2, в которой указанный белковый или пептидный антиген получен из патогена, выбранного из перечня, состоящего из: вируса бешенства, вируса гепатита В, вируса папилломы человека (hPV), Bacillus anthracis, респираторно-синцитиального вируса (RSV), вируса простого герпеса (HSV), вируса гриппа и Mycobacterium tuberculosis.
4. Фармацевтическая композиция по п. 1 или 2, в которой указанный белковый или пептидный антиген выбран из перечня, состоящего из:
- гемагглютинина (НА), нейраминидазы (NA), нуклеопротеина (NP), белка M1, белка М2, белка NS1, белка NS2 (белка NEP: белка ядерного экспорта), белка РА, белка РВ1 (основного белка 1 полимеразы), белка PB1-F2 и белка РВ2 вируса гриппа;
- нуклеопротеина (N), фосфопротеина (Р), белка матрикса (М), гликопротеина (G) и вирусной РНК-полимеразы (L), в каждом случае вируса бешенства;
- поверхностного антигена гепатита В (HBsAg), корового антигена гепатита В (HbcAg), ДНК-полимеразы вируса гепатита В, белка НВх, среднего поверхностного белка preS2, большого белка S, вирусного белка VP1, вирусного белка VP2, вирусного белка VP3 и вирусного белка VP4, в каждом случае вируса гепатита В;
- белка Е1, белка Е2, белка Е3, белка Е4, белка Е5, белка Е6, белка Е7, белка Е8, белка L1 и белка L2, в каждом случае вируса папилломы человека (hPV);
- защитного антигена (РА), фактора отека (EF), летального фактора (LF) и белков гомологии S-слоя (SLH), в каждом случае Bacillus anthracis;
- белка слияния (F), нуклеокапсидного (N) белка, фосфопротеина (Р), белка матрикса (М), гликопротеина (G), большого белка (L; РНК-полимеразы), неструктурного белка 1 (NS1), неструктурного белка 2 (NS2), малого гидрофобного (SH) белка, фактора элонгации М2-1 и белка регуляции транскрипции М2-2, в каждом случае респираторно-синцитиального вируса (RSV);
- гликопротеина L (UL1), урацил-ДНК-гликозилазы UL2, белка UL3, белка UL4, белка ДНК-репликации UL5, портального белка UL6, белка созревания вириона UL7, ДНК-геликазы UL8, белка, связывающего начало репликации, UL9, гликопротеина М (UL10), белка UL11, щелочной экзонуклеазы UL12, сериновой-треониновой протеинкиназы UL13, белка тегумента UL14, терминазы (UL15), белка тегумента UL16, белка UL17, капсидного белка VP23 (UL18), основного капсидного белка VP5 (UL19), мембранного белка UL20, белка тегумента UL21, гликопротеина Н (UL22), тимидинкиназы UL23, белка UL24, белка UL25, капсидного белка Р40 (UL26, VP24, VP22A), гликопротеина В (UL27), белка ICP18.5 (UL28), основного ДНК-связывающего белка ICP8 (UL29), ДНК-полимеразы UL30, белка ядерного матрикса UL31, гликопротеина оболочки UL32, белка UL33, белка внутренней ядерной мембраны UL34, капсидного белка VP26 (UL35), большого белка тегумента UL36, белка сборки капсида UL37, белка VP19C (UL38), рибонуклеотидредуктазы (большой субъединицы) UL39, рибонуклеотидредуктазы (малой субъединицы) UL40, белка тегумента/белка выключения генов хозяина вирионом VHS (UL41), фактора процессивности ДНК-полимеразы UL42, мембранного белка UL43, гликопротеина С (UL44), мембранного белка UL45, белков тегумента VP11/12 (UL46), белка тегумента VP13/14 (UL47), белка созревания вириона VP16 (UL48, альфа-TIF), белка оболочки UL49, dUTP-дифосфатазы UL50, белка тегумента UL51, белка комплекса ДНК-геликаза/праймаза UL52, гликопротеина K (UL53), белка регуляции транскрипции IE63 (ICP27, UL54), белка UL55, белка UL56, белка репликации вируса ICP22 (IE68, US1), белка US2, сериновой/треониновой протеинкиназы US3, гликопротеина G (US4), гликопротеина J (US5), гликопротеина D (US6), гликопротеина I (US7), гликопротеина Е (US8), белка тегумента US9, белка капсида/тегумента US10, белка Vmw21 (US11), белка ICP47 (IE12, US12), основного активатора транскрипции ICP4 (IE175, RS1), Е3-убиквитинлигазы ICP0 (IE110), связанного с латентностью белка 1 (LRP1), связанного с латентностью белка 2 (LRP2), фактора нейровирулентности RL1 (ICP34.5) и ассоциированного с латентностью транскрипта (LAT), в каждом случае вируса простого герпеса (HSV); или
- белка ESAT-6, белка ESX-1, белка CFP10, белка ТВ10.4, белка МРТ63, белка МРТ64, белка МРТ83, белка МТВ12, белка МТВ8, белка AG85A, белка AG85B, Rpf-подобных белков, белка KATG, белка РРЕ18, белка МТВ32, белка МТВ39, кристаллина, белка HSP65, белка PST-S и белка НВНА, фильтрующегося антигена 10 кДа EsxB, сериновой протеазы РерА, фибронектин-связывающего белка D FbpD, секретируемого белка МРТ51, периплазматического фосфат-связывающего липопротеина PSTS1 (РВР-1), периплазматического фосфат-связывающего липопротеина PSTS3 (РВР-3, Phos-1), белка РРЕ-семейства РРЕ14, белка РРЕ-семейства РРЕ68, белка MTB72F, молекулярного шаперона DnaK, липопротеина клеточной поверхности МРТ83, липопротеина Р23, белка пермеазы системы транспорта фосфата PstA, антигена 14 кДа, фибронектин-связывающего белка С FbpC1, аланиндегидрогеназы ТВ43 и глутаминсинтетазы 1, в каждом случае Mycobacterium tuberculosis.
5. Фармацевтическая композиция по п. 1 или 2, в которой указанный белковый или пептидный антиген ассоциирован с аллергией или аллергическим заболеванием и получен из источника, выбранного из перечня, состоящего из: пыльцы травянистых растений, пыльцы деревьев, цветочной пыльцы, пыльцы трав, пылевых клещей, плесени, животных, пищевых продуктов и яда насекомых.
6. Фармацевтическая композиция по п. 1 или 2, в которой указанный белковый или пептидный антиген ассоциирован с аутоиммунным заболеванием и выбран из перечня, состоящего из:
- основного белка миелина (МБР), белка протеолипида (PLP) и гликопротеина миелина олигодендроцитов (MOG), в каждом случае ассоциированного с рассеянным склерозом (MS);
- CD44, препроинсулина, проинсулина, инсулина, декарбоксилазы глутаминовой кислоты (GAD65), тирозинфосфатаза-подобного антигена 2 инсулиномы (IA2), переносчика цинка (ZnT8) и белка теплового шока 60 (HSP60), в каждом случае ассоциированного с диабетом типа I;
- межфоторецепторного ретиноид-связывающего белка (IRBP), ассоциированного с аутоиммунным увеитом;
- ацетилхолинового рецептора AchR и рецептора инсулин-подобного фактора роста-1 (IGF-1R), в каждом случае ассоциированного с тяжелой псевдопаралитической миастенией;
- М-белка из бета-гемолитических стрептококков (псевдоаутоантигена), ассоциированного с острой ревматической лихорадкой;
- фактора, ингибирующего миграцию макрофагов, ассоциированного с артритом;
- RNP-комплекса Ro/La, альфа- и бета-фодрина, аутоантигена островковых клеток, поли(АДФ)рибозаполимеразы (PARP), NuMA, NOR-90, аутоантигена Ro60 и антигена р27, в каждом случае ассоциированного с синдромом Шегрена;
- аутоантигена Ro60, липопротеинов низкой плотности, Sm-антигенов комплекса малых ядерных рибонуклеопротеинов U-1 (В/В', D1, D2, D3, Е, F, G), и RNP-рибонуклеопротеинов, в каждом случае ассоциированного с красной волчанкой;
- oxLDL, бета(2)GPI, HSP60/65 и oxLDL/бета(2)GPI, в каждом случае ассоциированного с атеросклерозом;
- бета(1)-адренергического рецептора сердца, ассоциированного с идиопатической дилятационной кардиомиопатией (DCM);
- гистидил-тРНК-синтетазы (HisRS), ассоциированной с миозитом;
- топоизомеразы I, ассоциированной со склеродермией, IL-17; или
белков теплового шока.
7. Фармацевтическая композиция по п. 1 или 2, в которой указанный белковый или пептидный антиген ассоциирован с раком или опухолевым заболеванием и выбран из перечня, состоящего из: р53, СА125, EGFR, Her2/neu, hTERT, PAP, MAGE-A1, MAGE-A3, мезотелина, MUC-1, NY-ESO-1, GP100, MART-1, тирозиназы, PSA, PSCA, PSMA VEGF, VEGFR1, VEGFR2, Ras, CEA и WT1.
8. Фармацевтическая композиция по п. 1 или 2, в которой указанный комплекс полимерного носителя и переносимого вещества предназначен для применения в качестве адъюванта.
9. Фармацевтическая композиция по п. 1 или 2, в которой катионные компоненты полимерного носителя и переносимая молекула нуклеиновой кислоты, входящие в состав указанного комплекса полимерного носителя и переносимого вещества, представлены в N/P-соотношении в диапазоне 0,1-20, или в диапазоне 0,1-5, или в диапазоне 0,1-1, или в диапазоне 0,5-0,9.
10. Фармацевтическая композиция по п. 1 или 2, в которой указанный комплекс полимерного носителя и переносимого вещества не включает в себя указанный белковый или пептидный антиген.
11. Набор для вакцинации против инфекционной болезни, аллергии или аллергического заболевания, аутоиммунного заболевания, или рака, или опухолевого заболевания, содержащий:
а) комплекс полимерного носителя и переносимого вещества, как определено в отношении фармацевтической композиции по пп. 1, 2 или любому из пп. 8-10; и
b) по меньшей мере один белковый или пептидный антиген или его фрагмент, вариант и/или производное, как определено в отношении фармацевтической композиции по любому из пп. 1-7.
12. Применение фармацевтической композиции по любому из пп. 1-10 или набора по п. 11 в качестве вакцины.
13. Применение комплекса полимерного носителя и переносимого вещества, как определено в отношении фармацевтической композиции по пп. 1, 2 или любому из пп. 8-10, для терапии инфекционной болезни, аллергии или аллергического заболевания, аутоиммунного заболевания, или рака, или опухолевого заболевания в сочетании по меньшей мере с одним белковым или пептидным антигеном или его фрагментом, вариантом и/или производным, как определено в отношении фармацевтической композиции по любому из пп. 1-7.
| HEFFERNAN M.J | |||
| et al., Disulfide-crosslinked polyion micelles for delivery of protein therapeutics.Ann Biomed Eng | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
Авторы
Даты
2017-04-19—Публикация
2013-01-31—Подача