Изобретение относится к (2-гидроксинафталин-1-ил)азинам - лигандам для получения эффективных и селективных катализаторов, в том числе и для реакций асимметрического синтеза (получение соединений в оптически чистых формах), к способу их синтеза.
Разработка способов получения новых лигандов для проведения катализируемых металлами превращений является одной из важнейших задач современной органической химии. Особое место среди лигандов занимают биарилы (вещества, структура которых содержит два непосредственно соединенных С-С-связью бензольных (арильных) кольца), которые можно получить в виде соединений с аксиальной хиральностью (атропоизомеры).
Одним из наиболее известных Р,Р лигандов является 2,2'-бис(дифенилфосфино)-1,1'-бинафтил (BINAP), который впервые был применен в реакциях асимметрического гидрирования α-(ациламино)акриловых кислот (A. Miyashita, A. Yasuda, Н. Takaya, K. Toriumi, Т. Ito, Т. Souchi, R. Noyori, J. Am. Chem. Soc., 1980, 102, 7932-7934).
(2-Гидроксинафталин-1-ил)азины - это гетероциклические аналоги известного лиганда QUINAPa (1-(2-дифенилфосфинонафталин-1-ил)изохинолина), широко применяющегося в реакциях энантиоселективного гидроборирования олефинов (J.М. Brown, D.I. Hulmes, Т.P. Layzell, J. Chem. Soc., Chem. Commun., 1993, 1673-1674), энантиоселективного присоединения терминальных алкинов к иминам (А.М. Taylor, S.L. Schreiber, Org. Lett., 2006, 8, 143-146), синтезе хиральных пропаргиламинов (N. Gommermann, A. Gehrig, P. Knochel, Synlett, 2005, 18, 2796-2798), реакциях 1,3-диполярного циклоприсоединения (С. Chen, X. Li, S.L. Schreiber, J. Am. Chem. Soc., 2003, 125, 10174-10175).
Наиболее распространенными способами получения гетероциклических аналогов QUINAPa являются С-С сочетание азинов, содержащих атомы галогена, с 2-нафтолом в присутствии кислот Льюиса (AlCl3, FeCl3), а также реакция кросс-сочетания 2-метокси-1-нафтилборной кислоты с галогенпроизводными гетероциклов, катализируемая переходными металлами (главным образом, палладием). Приведенные методы не соответствуют принципам «зеленой химии» (трудоемкость очистки от побочных металлосодержащих соединений) и «атомной экономии» (использование дополнительных каталитических реагентов, введение атомов галогена в структуру исходных соединений).
В опубликованной работе (L. Milhau, P.J. Guiry. Synlett, 2011, 3, 383-385) синтез (2-гидроксинафталин-1-ил)хиназолина осуществляют с использованием 1-хлорхиназолина, 2-нафтола и 3-кратного избытка AlCl3 с выходом до 70% при температуре 80°С. Также известен способ (D.J. Connolly, P.М. Lacey, М. McCarthy, С.P. Saunders, А.-М. Carroll, R. Goddard, P.J. Guiry. J. Org. Chem., 2004, 69, 6572-6589), согласно которому (2-гидроксинафталин-1-ил)хиназолин образуется в результате реакции кросс-сочетания 1-хлорхиназолина с 2-метокси-1-нафтилборной кислотой при 80°С в присутствии Pd(PPh3)4 в качестве катализатора. Далее метиловый эфир гидролизуют действием бортрибромида, общий выход целевого продукта составляет 69%. Основными недостатками данных способов синтеза являются: использование в качестве исходного соединения хлорпроизводного хиназолина, применение каталитических (Pd(PPh3)4) или дополнительных (AlCl3) реагентов, нагревание реакционной массы до 80°С, использование атмосферы инертного газа.
Наиболее близким по технической сущности к заявляемому способу является способ получения (2-гидроксинафталин-1-ил)хиназолина с использованием 1-хлорхиназолина, 2-нафтола и AlCl3 как дополнительного реагента - прототип (схема 1) (L. Milhau, P.J. Guiry. Synlett, 2011, 3, 383-385). К раствору 1-хлорхиназолина (1 ммоль, 0,198 г) в 10 мл дихлорэтана при перемешивании добавляют AlCl3 (3,0 ммоль, 0,400 г) и оставляют перемешиваться в течение 2-5 мин. Затем добавляют 2-нафтол (1 ммоль, 0,144 г) и оставляют перемешиваться в течение 3,5 часов при 80°С в токе азота. Затем реакционную смесь охлаждают до комнатной температуры и выливают в колотый лед при непрерывном перемешивании в течение 15-20 мин. Полученный продукт фильтруют и очищают колоночной хроматографией на силикагеле с использованием смеси гексан/этилацетат как элюента (подвижной фазы для разделения смеси веществ).
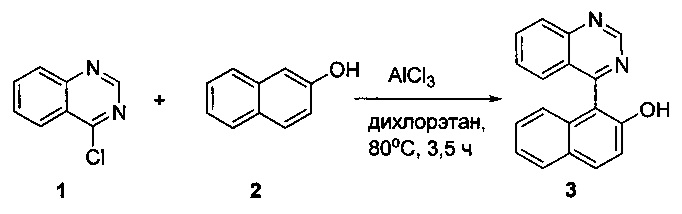
Схема 1. Получение (2-гидроксинафталин-1-ил)хиназолина (прототип)
Выход составляет 70%. К недостаткам данного способа относится использование дополнительного реагента (AlCl3), проведение реакции в инертной атмосфере и нагревание реакционной массы.
Задачей данного изобретения является расширение арсенала би(гетеро)арильных лигандов, упрощение способа синтеза гетероциклических аналогов QUINAPa за счет исключения использования дополнительного реагента, применение хиназолина как исходного соединения, проведение реакции при комнатной температуре.
Поставленная задача решается тем, что в заявленном способе получения (2-гидроксинафталин-1-ил)азина (хиназолина, пиримидина, 3,6-дифенил-1,2,4-триазина) реакцию 2-нафтола проводят с незамещенным хиназолином в среде трифторуксусной кислоты, которую затем упаривают, а остаток обрабатывают гексацианоферратом калия в щелочной среде.
Предлагаемый способ синтеза (2-гидроксинафталин-1-ил)азина (схема 2) позволяет получать целевые продукты с выходом 36-85%, без использования переходных металлов и AlCl3. Преимуществом данного способа является также то, что нет необходимости в использовании галогенпроизводных азинов, а реакции протекают при комнатной температуре.
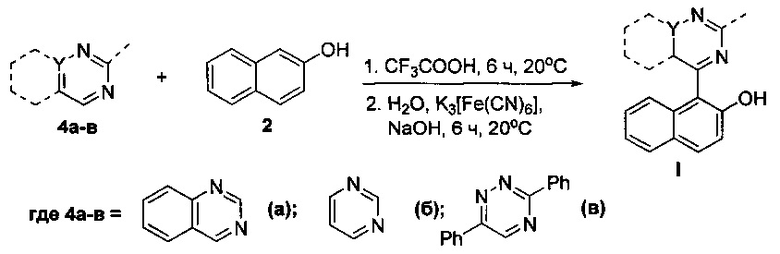
Схема 2. Получение (2-гидроксинафталин-1-ил)азина I (предлагаемый способ)
Способ получения (2-гидроксинафталин-1-ил)азина общей формулы I
Процесс осуществляют в две стадии без выделения промежуточного продукта. На первой стадии смесь азина и 2-нафтола, взятых в мольном соотношении 1:1, перемешивают при комнатной температуре в трифторуксусной кислоте в течение 6 ч. Затем кислоту упаривают при пониженном давлении, а остаток используют далее без очистки.
Затем сухой остаток (1 ммоль) растворяют в воде (или в метаноле) и добавляют гексацианоферрат калия (2 ммоль) и гидроксид натрия (4 ммоль) (в воде). Реакционную массу перемешивают при комнатной температуре в течение 10 часов, затем экстрагируют этилацетатом. Полученный экстракт концентрируют при пониженном давлении, а затем подвергают колоночной хроматографии на SiO2 с использованием смеси гексан/этилацетат в качестве элюента (или полученную суспензию концентрируют при пониженном давлении, осадок растворяют в смеси вода/этилацетат (1:1), органический слой отделяют, концентрируют и подвергают колоночной хроматографии на SiO2 с использованием смеси гексан/этилацетат в качестве элюента).
Полученные продукты проанализированы методами ЯМР 1Н и 13С спектроскопии, масс-спектрометрии, элементного анализа. Спектры ЯМР 1Н (400 МГц), 13С ЯМР (100 МГц) записаны на спектрометре «Bruker-400 AVANCE II» в ДМСО-d6, химические сдвиги приведены в шкале δ относительно Me4Si. Масс-спектры получены на приборе «Shimadzu GCMS-QP2010 Ultra ЕI», ионизация электронным ударом (EI). Элементный анализ выполнен на приборе «Perkin Elmer 2400-II CHNS/О». Для определения температуры плавления использован прибор «Boetius». Значение Rf измерено на пластинах с закрепленным слоем Poligram Alox N/UV254 (Macheray-Nagel). Для колоночной хроматографии используют силикагель 60 фирмы «Merck» (0.063-0.200 мм).
Ниже приведены примеры осуществления способа.
Пример 1. Синтез 4-(2-гидроксинафталин-1-ил)хиназолина
В колбу помещают 2,0 мл (≈30,0 ммоль) трифторуксусной кислоты, 0,130 г (1,0 ммоль) хиназолина и 0,144 г (1,0 ммоль) 2-нафтола. Смесь перемешивают при комнатной температуре в течение 8 ч, затем кислоту упаривают досуха. К сухому остатку добавляют 5 мл воды, 2,0 ммоль гексацианоферрата калия и 4,0 ммоль гидроксида натрия. Реакционную массу перемешивают при комнатной температуре в течение 10 часов. Затем экстрагируют при помощи этилацетата. Экстракт концентрируют и подвергают колоночной хроматографии на SiO2 с использованием смеси гексан/этилацетат (1:1) в качестве элюента. Выход 0,23 г (85%), Тпл=198°С, 1Н-ЯМР (400 МГц): 6.97 (дд, 1H, J=8.23 Гц), 7.27-7.39 (м, 3Н), 7.52 (дд, 1Н, J=8.93 Гц), 7.60 (дд, 1Н, J=8.93 Гц), 7.92 (дд, 1H, J=7.33 Гц), 7.99-8.03 (м, 2Н), 8.12-8.15 (дд, 1H, J=8.42 Гц), 9.47 (с, 1H), 9.94 (с, 1Н, ОН); 13С-ЯМР (100 МГц): 116.36, 118.67, 123.44, 123.96, 125.30, 127.36, 127.39, 128.14, 128.51, 128.56, 128.74, 131.25, 133.34, 134.74, 150.31, 153.20, 155.39, 167.60. Данные элементного анализа: С 79,48%, Н 4,46%, N 10,22% (расчет: С 79,39%, Н 4,44%, N 10,29%), ESI-MS, m/z (%): [М]=272 (63,12%), [М-Н]=271 (100,00%).
Пример 2. Синтез 4-(2-гидроксинафталин-1-ил)пиримидина
В колбу помещают 2,0 мл (≈30,0 ммоль) трифторуксусной кислоты, 0,080 г (1,0 ммоль) пиримидина и 0,144 г (1,0 ммоль) 2-нафтола. Смесь перемешивают при комнатной температуре в течение 6 ч, затем кислоту упаривают досуха. К сухому остатку добавляют 5 мл воды, 2,0 ммоль гексацианоферрата калия и 4,0 ммоль гидроксида натрия. Реакционную массу перемешивают при комнатной температуре в течение 10 часов. Затем экстрагируют при помощи этилацетата. Экстракт концентрируют и подвергают колоночной хроматографии на SiO2 с использованием смеси гексан/этилацетат (1:1) в качестве элюента. Выход 0,08 г (36%), Tпл=174°C, 1Н-ЯМР (400 МГц): 7.30-7.40 (м, 3Н), 7.50 (дд, 1Н, J=8.34 Гц), 7.69 (д, 1H, J=4.07 Гц), 7.86-7.93 (дд, 2Н, J=8.92 Гц), 7.90 (д, 1H, J=5.16 Гц), 9.35 (с, 1H), 10.11 (с, 1H, ОН); 13C-ЯМР (100 МГц): 117.43, 118.29, 122.94, 123.51, 124.44, 126.83, 127.76, 128.07, 130.87, 132.13, 152.75, 156.85, 158.42, 163.67. Данные элементного анализа: С 75,60%, Н 4,51%, N 12,58% (расчет: С 75,66%, Н 4,54%, N 12,60%), ESI-MS, m/z (%): [М]=222 (60,70%), [М-Н]=221 (100,00%).
Пример 3. Синтез 5-(2-гидроксинафталин-1-ил)-3,6-дифенил-1,2,4-триазина
В колбу помещают 2,0 мл (≈30,0 ммоль) трифторуксусной кислоты, 0,233 г (1,0 ммоль) 3,6-дифенил-1,2,4-триазина и 0,144 г (1,0 ммоль) 2-нафтола. Смесь перемешивают при комнатной температуре в течение 10 ч, затем кислоту упаривают досуха. К сухому остатку добавляют 5 мл воды и 5 мл метанола, 2,0 ммоль гексацианоферрата калия и 4,0 ммоль гидроксида натрия. Реакционную массу перемешивают при комнатной температуре в течение 10 часов. Затем полученную суспензию концентрируют при пониженном давлении, осадок растворяют в смеси вода/этилацетат (1:1), органический слой отделяют, концентрируют и подвергают колоночной хроматографии на SiO2 с использованием смеси гексан/этилацетат (8:2) в качестве элюента. Выход 0,30 г (80%), Тпл=210°С, 1Н-ЯМР (400 МГц): 7.11-7.14 (д, 1Н, J=8.93 Гц), 7.24-7.28 (м, 2Н), 7.31-7.37 (дт, 2Н, J=7.37 Гц), 7.41 (дт, 1Н, J=7.00 Гц), 7.49-7.50 (дд, 2Н, J=7.16 Гц), 7.56-7.58 (м, 1Н), 7.61-7.63 (м, 3Н), 7.90 (дд, 2Н, J=8.85 Гц), 8.48-8.50 (дд, 2Н, J=7.15 Гц), 10.06 (с, 1Н, ОН); 13С-ЯМР (100 МГц): 115.67, 117.94, 123.18, 123.27, 127.41, 127.61, 127.78, 128.01, 128.03, 128.25, 129.08, 129.35, 131.38, 131.61, 132.47, 134.64, 135.37, 152.46, 155.61, 158.36, 161.07. Данные элементного анализа: С 79,88%, Н 4,49%, N 11,15% (расчет: С 79,98%, Н 4,56%, N 11,19%), ESI-MS, m/z (%): [М]=375 (15,68%).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 3-ГЕТАРИЛ-7-АМИНОКУМАРИНОВ | 2022 |
|
RU2802966C1 |
| НОВЫЕ 2',5'-ДИАРИЛСПИРО[ИНДОЛ-3,3'-ПИРРОЛИДИН]-2(1Н)-ОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2019 |
|
RU2730287C1 |
| РЕАГЕНТ ДЛЯ ОБНАРУЖЕНИЯ КАТИОНОВ МЕТАЛЛОВ НА ОСНОВЕ ИЗОХИНОЛИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2668134C2 |
| Производные 4-((арил)(метил)амино)хиназолин-7-карбоновой кислоты с противоопухолевым действием и способ их получения | 2024 |
|
RU2834688C1 |
| Замещенные 4-арил-гексагидро-7Н-имидазоло[1,5-b][1,2]оксазин-7-оны и способ их получения | 2018 |
|
RU2670097C1 |
| Ингибитор основной протеазы коронавируса SARS-CoV-2 | 2023 |
|
RU2840908C2 |
| Гидроксамовые кислоты, производные 4-аминохиназолина, обладающие противоопухолевой активностью | 2022 |
|
RU2802463C1 |
| РЕАГЕНТ ДЛЯ ОБНАРУЖЕНИЯ КАТИОНОВ МЕТАЛЛОВ НА ОСНОВЕ 2,2’-БИПИРИДИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2668133C2 |
| СПОСОБЫ СЕЛЕКТИВНОГО ВВЕДЕНИЯ ЗАЩИТНЫХ ГРУПП В ПРОИЗВОДНЫЕ РЕЗОРЦИНА | 2019 |
|
RU2738408C1 |
| 1-(4-(4-МЕТОКСИФЕНИЛ)-[2,2'-БИПИРИДИН]-6-ИЛ)-N,N-БИС(ПИРИДИН-2-ИЛМЕТИЛ)МЕТАНАМИН - МОНОМОЛЕКУЛЯРНЫЙ ХИМИЧЕСКИЙ СЕНСОР ДЛЯ ФЛУОРЕСЦЕНТНОГО ОПРЕДЕЛЕНИЯ КАТИОНОВ Zn IN VITRO | 2023 |
|
RU2822106C1 |
Изобретение относится к способу получения (2-гидроксинафталин-1-ил)азина общей формулы I
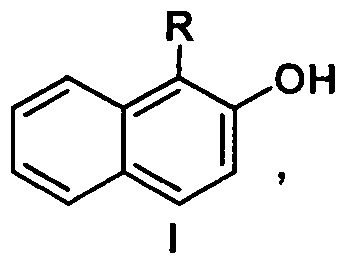
где
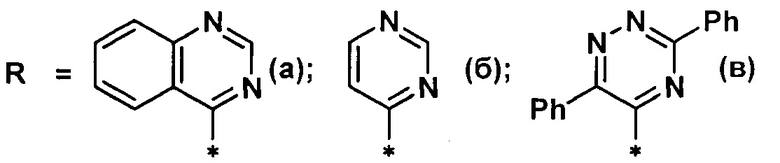
взаимодействием 2-нафтола с производным азина в среде органического растворителя, причем реакцию 2-нафтола проводят с незамещенным хиназолином (а), или незамещенным пиримидином (б), или 3,6-дифенил-1,2,4-триазином (в) в среде трифторуксусной кислоты, которую затем упаривают, а остаток обрабатывают гексацианоферратом калия в щелочной среде. Технический результат: предложен новый способ получения (2-гидроксинафталин-1-ил)азинов с высокими выходами, без использования дополнительных реагентов, позволяющий снизить температуру проведения процесса до комнатной. 3 пр.
Способ получения (2-гидроксинафталин-1-ил)азина общей формулы I
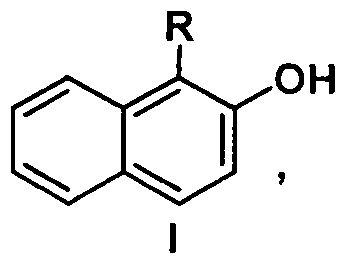
где 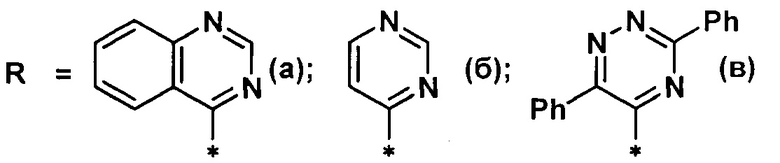
взаимодействием 2-нафтола с производным азина в среде органического растворителя, отличающийся тем, что реакцию 2-нафтола проводят с незамещенным хиназолином (а), или незамещенным пиримидином (б), или 3,6-дифенил-1,2,4-триазином (в) в среде трифторуксусной кислоты, которую затем упаривают, а остаток обрабатывают гексацианоферратом калия в щелочной среде.
| L | |||
| Milhau et al | |||
| "Novel Palladium-Free Synthesis of a Key Quinazolinap Precursor" SYNLETT, N3, 2011, 383-385 | |||
| D | |||
| J | |||
| Connoly et al | |||
| "Preparation and Resolution of a Modular Class of Axially Chiral Quinazoline-Containing Ligands and Their Application in Asymmetric Rhodium-Catalyzed Olefin Hydroboration" JOURNAL OF ORGANIC CHEMYCTRY, Vol | |||
| Способ приготовления пищевого продукта сливкообразной консистенции | 1917 |
|
SU69A1 |
| Способ изготовления эластичного алюминиевого экрана | 1924 |
|
SU840A1 |
Авторы
Даты
2017-07-27—Публикация
2016-07-18—Подача