Изобретение относится к биотехнологии и фармацевтике и касается нового лентивирусного вектора для экспрессии белка CD47 в клетках млекопитающих.
Современное производство рекомбинантных белков главным образом базируется на прокариотических системах экспрессии, таких как, например, различные модификации бактериального штамма E. coli. Однако, в современных научных исследованиях все чаще используются белки, экспрессированные в клетках эукариот, в частности, в клетках млекопитающих. Выбор такой системы объясняется наличием в клетках эукариот молекулярных механизмов посттрансляционной модификации белковых молекул, а также более точными процессами фолдинга сложных полипептидов. Необходимость использования эукариотической системы возникает и в случае с экспрессией человеческого рецептора CD47, в составе которого присутствует достаточно большой гликозилированный домен. Рецептор CD47 экспрессируется на многих типах клеток и участвует во множестве клеточных процессов, включая такие механизмы, как пролиферация, дифференцировка, клеточная миграция, адгезия клеток и проведение сигналов, обеспечивающих апоптоз [Brown E.J., Frazier W.A. Integrin-associated protein (CD47) and its ligands // Trends. Cell Biol. - 2001. - Vol. 11, N. 3. - P. 130-135]. С другой стороны, последние исследования показали, что CD47 гиперэкспрессирован в различных типах опухолевых клеток таких, например как, клетки рака мочевого пузыря или клетки острого миелобластного лейкоза [B. Edris et al., Antibody therapy targeting the CD47 protein is effective in a model of aggressive metastatic leiomyosarcoma, 2012]. Таким образом, CD47 может выступать в качестве потенциальной мишени в противораковой терапии.
В качестве эффективной противоопухолевой терапии могут быть использованы одноцепочечные антитела. Однако для создания подходящих моноклональных антител методом фагового или рибосомного дисплеев требуется значительное количество соответствующего белка. Данная задача может быть решена созданием экспрессионного плазмидного лентивирусного вектора, с последующим получением высокопроизводительной клеточной линии экспрессора CD47.
Среди клеточных линий млекопитающих, используемых в биофармацевтическом производстве и научных исследованиях, наиболее распространены такие клеточные линии, как HEK293 (human embrionic kidney 293 cells), CHO (Chinese hamster ovary cells), PER.C6 (protein manufacturing adopted human cells) [http://www.science-education.ru/pdf72012/5/237.pdf]. Выбор линии продуцента определяется специфичностью синтезируемого белка и общей целью его производства. Получение стабильной клеточной линии, экспрессирующей заданную генетическую последовательность, не составляет труда благодаря стандартным методикам и широкому спектру имеющихся на рынке химических трансфекционных препаратов. Но, стоит отметить, что создание эффективной линии продуцента определяется не только успешным введением последовательности ДНК в геном клетки хозяина, а, главным образом, уровнем целевой мРНК и, в конечном счете, количеством стабильных молекул целевого белка.
Эффективность экспрессии во многом зависит от выбора промоторной области, контролирующей транскрипцию введенной последовательности ДНК. Различные промоторные регионы различаются не только своей способностью к привлечению транскрипционного аппарата клетки, но и различными уровнями метилирования. Так, вирусные промоторы чаще инактивируются метилированием по сравнению с промоторами клеток. Значительную роль играют мутации, проявляющиеся в процессе пролиферации клеток. Возникновение спонтанных делеций и транслокаций может значительно снизить уровень экспрессии целевой кассеты. Последние исследования показали, что процессы метилирования и хромосомных перестановок можно снизить путем создания горячих точек рекомбинации в целевой последовательности, которые были бы гомологичны определенным последовательностям в транскрипционно активной части генома клетки. Также вероятность делеций или метилирования может быть снижена за счет сближения последовательности целевого белка и последовательности маркера селекции. Таким образом, создание эффективного продуцента достигается использованием следующих подходов:
- использование наиболее подходящего промоторного региона
- снижение вероятности метилирования и мутаций целевой последовательности путем направленной ее интеграции в транскрипционно активные участки генома.
- максимальное сближение целевой последовательности и маркера селекции
Также, большую роль играет выбор самого маркера, обуславливающего отбор клеток, получивших генетическую конструкцию. Все чаще, для получения суперпродуцентов, используют рекомбинантные плазмиды, несущие в своем составе маркеры, приводящие к амплификации целевого гена. К таким системам относятся конструкции, содержащие последовательность DHFR (дегидрофолатредуктазы) и GS (глутатион синтетазы) (например, RU 2488633, EA 018099). Однако, для использования таких систем необходимы специальные клеточные линии, дефицитные по этим генам. Кроме того, получение клеток, обладающих высоким уровнем экспрессии, требует значительного количества времени и материалов, что связано с длительным, постепенным увеличением МТХ (метотрексата) в культуральной среде. Использование антибиотиков в качестве маркера селекции, также требует значительного количества времени, затраченного на селекцию. При этом возникают серьезные трудности с отбором наиболее эффективных продуцентов из большого количества клонов, получивших устойчивость к определенному антибиотику.
Техническое решение таких проблем может быть связано с использованием рекомбинантной плазмидной ДНК, обладающей следующими свойствами:
- сильный промоторный регион, обеспечивающий высокий и стабильный уровень транскрипции ДНК последовательности целевой кассеты
- использование лентивирусной системы доставки целевой последовательности в геном клетки хозяина. Использование лентивирусной системы позволяет получить практически неограниченное количество событий интеграции заданной последовательности в хромосому клетки. Иногда такое свойство несет негативные последствия, отражающиеся в снижении общего метаболизма клетки, что, в конечном счете, приводит к ее гибели. Однако количество интеграций легко контролируется снижением (или увеличением) титра вирусных частиц. Таким образом, очень высока вероятность попадания нужного гена в области с высокой транскрипционной активностью.
- выбор наиболее оптимального маркера селекции, максимально приближенного к целевой последовательности. Для снижения расстояния между последовательностью гена целевого белка и селекционного маркера, главным образом, принято использовать последовательность IRES (внутренний сайт посадки рибосом). Данная последовательность позволяет рибосоме практически беспрерывно перейти с одной транслируемой области на другую, не затрачивая времени на полную разборку комплекса и процесс сканирования мРНК. Альтернативным методом максимального сближения последовательностей может служить создание слитого ДНК конструкта, продуктом экспрессии которого является более сложная молекула полипептида.
В описании к патенту US 8562997 описан способ получения CD47-растворимого белка с помощью экспрессионных векторов с последовательностью CD47, используя клетку-хозяин e. coli с последующей очисткой выделенного белка. Отмечается, что кассеты транскрипции могут быть введены во множество векторов, например, в плазмиды, ретровирус, лентивирус; аденовирус. Но конкретные конструкции не раскрыты.
Патент US 8329462 касается лентивирусных векторов, которые являются безопасными, эффективными и очень мощными для экспрессии трансгенов, например, эритропоэтина, интегрина для генотерапии человека в клетках крови. Лентивирусные векторы включают промотор, такой как EF1.alpha, PGK, gp91hox, clotting Factor IX, a clotting Factor V111, инсулин, a PDX1, CD11, CD4, CD2mra gp47. He раскрывается возможность экспрессии CD47.
Техническая задача состояла в создании вектора для получения высокопродуктивных и стабильных систем экспрессии рекомбинантных белков в клетках млекопитающих, в частности в клетках HEK293.
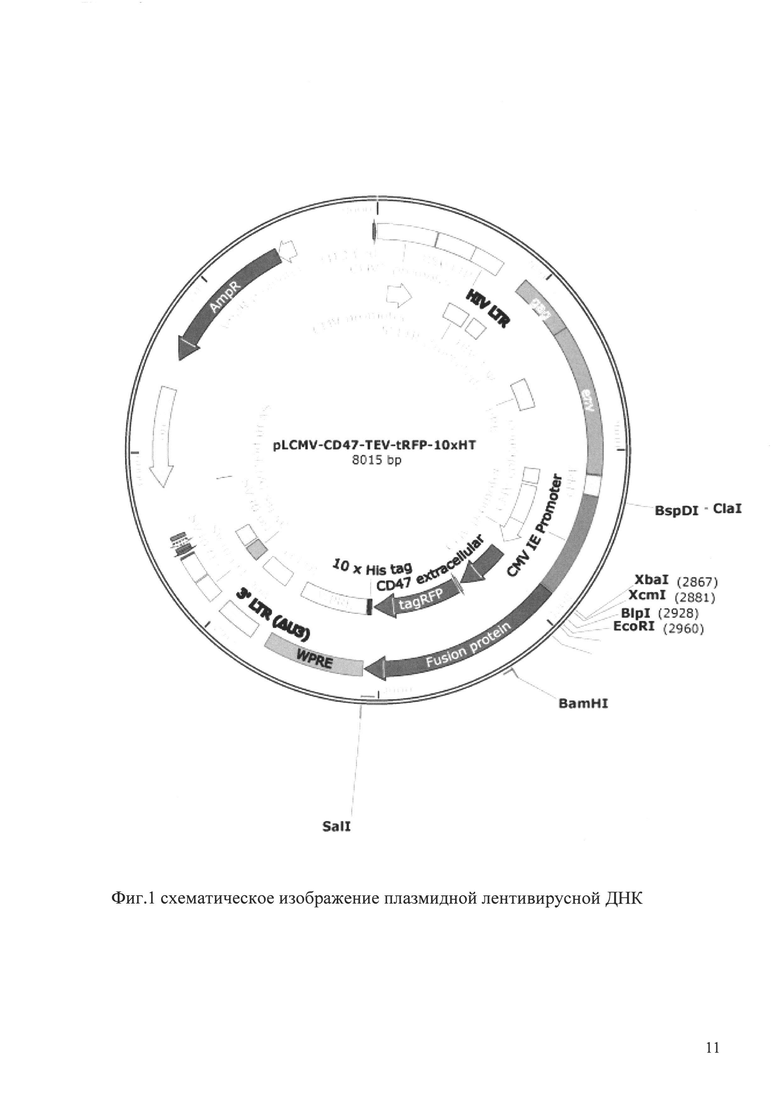
В основе изобретения лежит разработанный авторами плазмидный лентивирусный ДНК вектор (фиг. 1), включающий цитомегаловирусный промотор, обеспечивающий высокий уровень продукции мРНК, последовательность внеклеточного домена рецептора CD47, участок распознавания и расщепления протеазой TEV (tobacco etch virus), последовательность гена tagRFP - красного флуоресцентного белка, позволяющего отсортировать только клетки содержащие вставки целевой последовательности. Все три последовательности находятся в одной рамке считывания под контролем данного промотора.
Последовательность CD47 (SEQ ID NO 1):
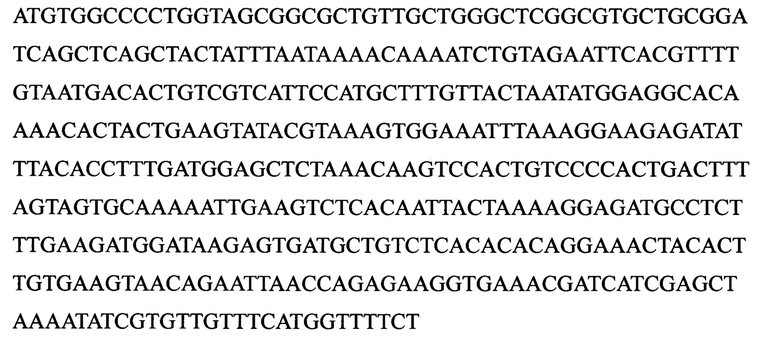
Последовательность цитомегаловирусного промотора (SEQ ID NO 2):

Последовательность сайта узнавания протеазы TEV (SEQ ID NO 3):
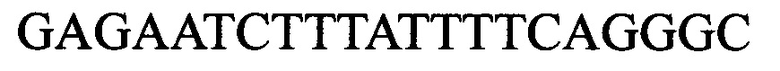
Нуклеотидная последовательность, кодирующая красный флуоресцентный белок tagRFP (SEQ ID NO 4):

Нуклеотидная последовательность, кодирующая 10 остатков гистидина (SEQ ID NO 5):
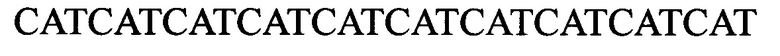
Нуклеотидная последовательность, кодирующая слитой белок, включающий участки SEQ ID NO 1, SEQ ID NO 3, SEQ ID NO 4 и SEQ ID NO 5 (SEQ ID NO 6):

Термин «экспрессионный вектор» означает плазмидную ДНК, содержащую все необходимые генетические элементы для экспрессии внедренного в нее целевого гена, например, промотор и терминатор, и элементы для амплификации экспрессионной кассеты и отбора клонов с множественными копиями экспрессионной кассеты в геноме. Размер вектора - 8015 bp (пар оснований).
Полная последовательность встраиваемого в хромосому клетки фрагмента включает в себя следующие элементы:
- 5' и 3' LTR - длинные концевые повторы - последовательности, используемые вирусом для встраивания собственного генома в геном хозяина путем гомологичной рекомбинации.
- Центральный полипуриновый тракт (сРРТ) - обеспечивает проникновение целевой последовательности в ядра митотически неактивных клеток.
- Посттранскрипционный регуляторый элемент (WPRE) - регуляторная область, усиливающая экспрессию целевой последовательности.
- Козак - консенсусная последовательность, необходимая для посадки рибосом и инициации трансляции мРНК.
- CD47 - последовательность внеклеточного домена CD47
- TEV - сайт расщепления протеазой TEV (tobacco etch virus)
- tagRFP - красный флуоресцентный белок, выступает в качестве селективного маркера
- НТ – последовательность, включающая 10 остатков гистидина, необходимая для хроматографической очистки полученного белка
Вектор был получен с использованием стандартных методов генной инженерии, коммерчески доступных плазмид и химически синтезированных олигонуклеотидов (Sambrook J, Fritsch EF, Maniatis Т. Molecular Cloning. 2nd ed. New York, NY: Cold Spring Harbor Laboratory Press; 1989) путем конструирования новой экспрессионной лентивирусной плазмидной ДНК (фиг. 1),
Настоящее изобретение предназначено для получения высокопродуктивных и стабильных систем экспрессии рекомбинантного человеческого рецептора CD47 в клетках млекопитающих с целью дальнейшего производства очищенного белка CD47. Технический результат достигается путем введения в клетки полученной лентивирусной конструкции, содержащей регуляторные элементы для гетерологичной экспрессии рекомбинантного белка, высокочастотной интеграции заданной последовательности и селективного маркера, позволяющего отследить качество и количество таких интеграций. Данная векторная система позволяет практически моментально отобрать нужные клоны - клетки содержащие вставку. Количество вставок и, следовательно, общее количество синтезируемого белка может быть определено по интенсивности свечения красного флуоресцентного белка tagRFP. Сортировка клеток производится методом клеточного сортинга на любом подходящем для этого оборудовании. В дальнейшем, в процессе очистки белковых молекул, слитые последовательности CD47 и флуоресцентного белка могут быть разделены путем обработки очищенного препарата протеазой TEV. После чего целевой белок может быть очищен от примесей методом хроматографического разделения.
Выращивание клеток, выделение и очистка целевого белка из культуральной или подобной ей жидкости может быть осуществлена стандартным способом культивирования. Питательная среда, используемая для культивирования, может быть как синтетической, так и натуральной, при условии, что указанная среда содержит источники углерода, азота, минеральные добавки и, если необходимо, соответствующее количество питательных добавок, необходимых для роста клеток. В качестве источника углерода могут использоваться различные углеводы, такие как глюкоза или сахароза и другие органические кислоты. В качестве источника азота могут использоваться различные неорганические соли аммония, такие как аммиак и сульфат аммония, другие соединения азота, такие как амины, природные источники азота. В качестве минеральных добавок могут использоваться фосфат калия, сульфат магния, хлорид натрия, сульфат железа, сульфат марганца, хлорид кальция и подобные им соединения. В качестве витаминов могут использоваться тиамин, дрожжевой экстракт и т.п.
Выращивание может осуществляться на стандартной среде DMEM, содержащей 10% эмбриональной сыворотки крупного рогатого скота, 4 мМ L-глутамина, 1 мМ пирувата натрия, стрептомицин/ пенициллин в концентрации 100 мкг/мл и 100 ед/мл соответственно, pH 8,1±0,1 в аэробных условиях, предпочтительно с повышенным содержанием CO2 (5%), таких как перемешивание культуральной жидкости в колбах, при температуре 37°C. Для продукции достаточного количества белка требуется в среднем от 3 до 5 суток культивации.
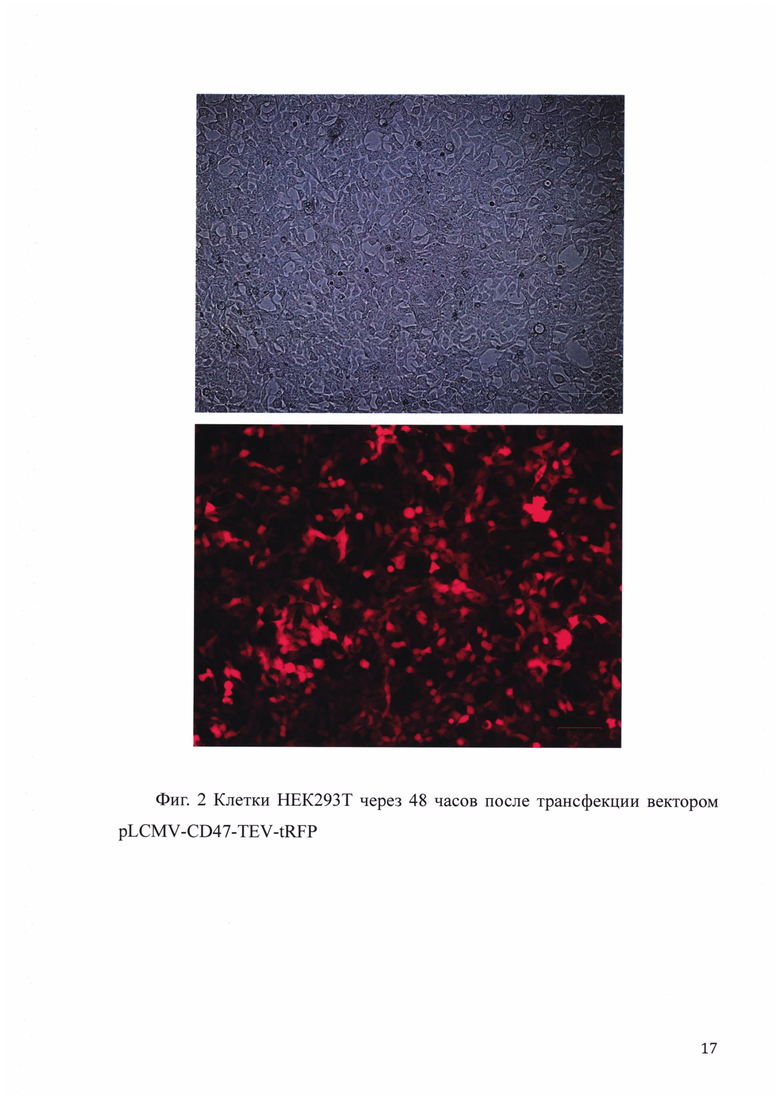
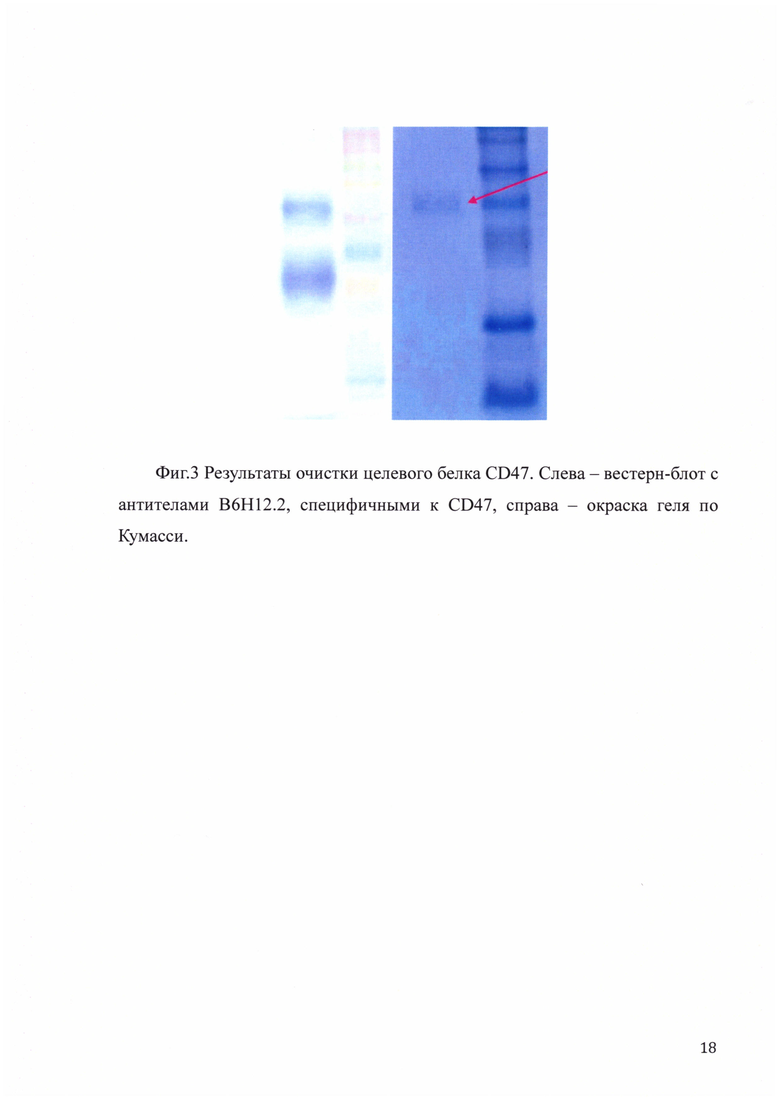
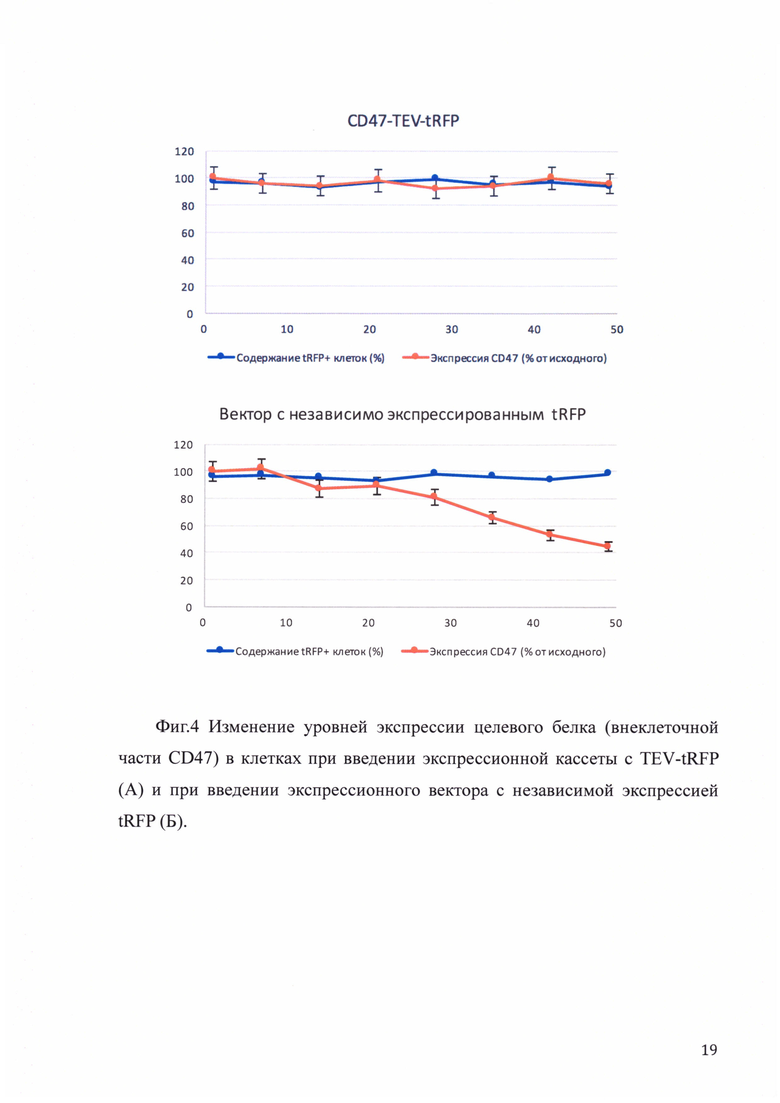
Для испытания изобретения, представленного в п. 1 Формулы изобретения, введение вектора в клетки трансформированного эпителия почки человека (клетки HEK293T) проводили с помощью наборов для липофекции фирмы Invitrogene (LipofectAMINE Plus). Одновременно с лентивирусными конструкциями вводили три упаковывающие плазмиды: pREV, pGAG и pVSV-G, которые кодируют, соответственно, обратную транскриптазу, белок GAG вируса иммунодефицита человека (ВИЧ1) и G-белок вируса везикулярного стоматита. Оптимальное соотношение плазмид при трансфекции, дающее максимальные титры рекомбинантных вирионов, определяли экспериментально (вектор : pREV : pGAG : pVSV - G = 2:4:2:1), после чего эффективность трансфекции была оценена визуально с помощью флуоресцентного микроскопа (фиг.2). Рекомбинантные вирионы собирали в течение 72 часов с интервалами в 8 часов. Супернатанты объединяли и вирионы осаждали 12% полиэтиленгликолем при 4°C 12 часов с последующим центрифугированием в течение 10 минут при 5000 об/мин. Вирионы затем суспендировали в свежей среде (1/10 от исходного объема) и фильтровали через стерилизующую насадку для шприца. Стерильные вирионы расфасовывали на порции и хранили в заморозке при -70°C. Для введения вектора в клетки с целью экспрессии белка CD47 были использованы перевиваемые клетки почки эмбриона человека HEK293T. Через 72 часа инфицированные клетки подвергались сортировке на клеточном сортере, в результате которой отбиралась фракция наиболее яркосветящихся клеток, в которые встроилось наибольшее количество копий конструкции. Отобранные клетки наращивались в необходимом количестве, после чего из них был выделен и очищен на хроматографической колонке белок CD47 (фиг. 3). Полученная клеточная линия с введенной генетической конструкцией может быть заморожена и использована в дальнейшем для получения следующих партий белка, поскольку в отличие от обычных экспрессионных конструкций, после введения которых экспрессия целевого белка постепенно "затухает", клетки экспрессирующие лентивирусный вектор, описанный в п. 1 Формулы изобретения сохраняют изначальный, стабильно высокий уровень экспрессии целевого белка. Уровень экспрессии CD47 в клетках с введенным вектором pLCMV-CD47-TEV-tRFP оценивался методом ELISA каждые 10 дней на протяжении 50 дней в сравнении с клетками, где экспрессировался конструкт pLCMV-CD47-tRFP (фиг. 4).
Изобретение относится к области биотехнологии, конкретно к плазмидному лентивирусному вектору для гетерологичной экспрессии рекомбинантного человеческого белка CD47 в клетках млекопитающих. Вектор содержит высокофункциональный цитомегаловирусный промотор (CMV), последовательность внеклеточного домена рецептора CD47, последовательность распознавания цистеиновой протеазой TEV, последовательность флуоресцентного белка tagRFP, выступающего в качестве селективного маркера. Все три последовательности находятся в одной рамке считывания под контролем данного промотора. Изобретение позволяет получить высокопродуктивную и стабильную систему экспрессии белка для дальнейшего производства его очищенной формы. 1 з.п. ф-лы, 1 пр., 4 ил.
1. Экспрессионный плазмидный лентивирусный вектор для гетерологичной экспрессии рекомбинантного человеческого белка CD47 в клетках млекопитающих, характеризующийся тем, что он включает цитомегаловирусный промотор, обеспечивающий высокий уровень продукции мРНК, следующую за ним нуклеотидную последовательность, кодирующую внеклеточный домен рецептора CD47 (SEQ ID NO: 1), соединенную с последовательностью, кодирующей пептидный участок распознавания и расщепления протеазой TEV (tobacco etch virus), соединенный с нуклеотидной последовательностью гена tagRFP, кодирующего красный флуоресцентный белок, позволяющий отсортировать только клетки, содержащие вставки целевой последовательности.
2. Плазмидный лентивирусный ДНК вектор по п. 1, характеризующийся тем, что полная последовательность встраиваемого в хромосому клетки фрагмента включает в себя следующие элементы:
5' и 3' LTR - длинные концевые повторы - последовательности, используемые вирусом для встраивания собственного генома в геном хозяина при помощи вирусной интегразы;
центральный полипуриновый тракт (сРРТ), обеспечивающий проникновение целевой последовательности в ядра митотически неактивных клеток;
посттранскрипционный регуляторый элемент (WPRE) - регуляторная область, усиливающая экспрессию целевой последовательности;
Козак - консенсусная последовательность, необходимая для посадки рибосом и инициации трансляции мРНК;
CD47 - последовательность внеклеточного домена CD47;
TEV - сайт расщепления протеазой TEV (tobacco etch virus);
tagRFP - красный флуоресцентный белок, выступающий в качестве селективного маркера;
НТ - последовательность, включающая 10 остатков гистидина, необходимая для хроматографической очистки полученного белка.
| BROWN E.J | |||
| et al., Integrin-associated protein (CD47) and its ligands, Trends in cell biology, 2001, v | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Реверсивный дисковый культиватор для тросовой тяги | 1923 |
|
SU130A1 |
| US 8329462 B2, 11.12.2012 | |||
| СПОСОБЫ ВНУТРИКЛЕТОЧНОГО ПРЕВРАЩЕНИЯ ОДНОЦЕПОЧЕЧНЫХ БЕЛКОВ В ИХ ДВУХЦЕПОЧЕЧНУЮ ФОРМУ | 2011 |
|
RU2569185C2 |
| RU 2012123633 A1, 20.12.2013 | |||
| US 8562997 B2, 22.10.2013. | |||
Авторы
Даты
2017-08-03—Публикация
2015-12-29—Подача