ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее раскрытие направлено на визуализирующие вещества, фармацевтические композиции и способы для визуализации перфузии миокарда, включающие введение пациенту соединения, связанного с фрагментом, обеспечивающим визуализацию, где указанное соединение связывается с МС-1, и сканирование пациента при помощи диагностической визуализации. Настоящее изобретение также относится к наборам, содержащим указанное визуализирующее вещество или соединения-предшественники, связанные или не связанные с фрагментом, обеспечивающим визуализацию.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Ишемическая болезнь сердца (CAD) является основной причиной смерти в западном мире. Методики визуализации для диагностики и прогнозирования являются очень важными для лечения CAD с тем, чтобы снизить смертность. Визуализация для оценки коронарного кровотока для определения необходимого лечения (часто хирургическая операция) играет важную роль для медицинской помощи при CAD. В настоящее время однофотонная эмиссионная компьютерная томография (SPECT) является основной методикой для визуализации при CAD, но требуются улучшенные способы диагностики.
Клетки сердца, миокарда, имеют очень высокую внутриклеточную плотность, весовое процентное содержание, митохондрий. Таким образом, было обосновано, что соединения, которые избирательно связываются с митохондриями, будут присутствовать в миокарде в большом количестве. Некоторые инсектициды действуют посредством связывания с митохондриальным комплексом I (MCI). К этой группе инсектицидов принадлежат ротенон, пиридабен, тебуфенпирад и феназаквин. Предполагалось, что такие соединения, избирательные по отношению к MCI, можно применять для визуализации ткани, богатой митохондриями. Патентный документ, относящийся к применению меченого ротенона для визуализации коронарного кровотока, был раскрыт в 2001 году.
В 2005 году BMS подали патентную заявку (WO 2005/079391), в которой описываются 18F-меченые соединения на основе инсектицидов пиридабена, тебуфенпирада и феназаквина для применения в качестве РЕТ-лигандов для диагностики и визуализации коронарного кровотока при CAD. Патенты, принадлежащие BMS, в дальнейшем были приобретены Lantheus Medical Imaging. Применительно к одному из соединений на основе пиридабена, флурпирадаза (BMS747158), проводили интенсивные исследования, и в настоящее время оно находится в фазе III исследований по отношению к визуализации миокарда. Флурпиридаз, как было обнаружено, обеспечивает лучшую оценку функции миокарда, чем вещество для SPECT 99mTc sestamibi.
Respiratorius, фармацевтическая компания, расположенная в Лунде, Швеция, работает над созданием новых бронходилатирующих лекарственных средств. Главной частью исследовательской работы Respiratorius является скрининг малых молекул, которые могут приводить к расслаблению ткани дыхательных путей человека ex vivo. В ходе этого процесса ряд новых 1,8-нафтиридинов был обнаружен в качестве соединений, оказывающих сильный бронхорасслабляющий эффект (описаны в патентной заявке WO/2010/097410). В результате дополнительных фармакологических исследований было обнаружено, что представители этого класса соединений связывались с митохондриальным комплексом I и ингибировали его.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Было обнаружено, что бронходилатирующее соединение, принадлежащее к классу 1,8-нафтиридинов, также может ингибировать функцию митохондрий при расслаблении гладкой мускулатуры дыхательных путей, изменять функцию митохондрий или связываться с митохондриальным комплексом I. Если эти соединения будут мечеными фрагментом, обеспечивающим визуализацию, станет доступным важный диагностический маркер для визуализации перфузии миокарда.
Настоящее изобретение относится к визуализирующему веществу, имеющему структуру
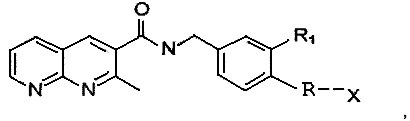
где R1 представляет собой H, F, CF3, Cl, R представляет собой линкер, и X представляет собой фрагмент, обеспечивающий визуализацию, или аналог или фармацевтическую соль указанного визуализирующего вещества.
Во втором аспекте настоящее изобретение относится к фармацевтической композиции, содержащей визуализирующее вещество, показанное выше, и фармацевтически приемлемый носитель, разбавитель буфер. Визуализирующее вещество и композиция приводят к высокому отношению накопления в сердце по сравнению с нецелевым участком, причем с минимальным перераспределением. Это также будет приводить в результате к лучшему качеству изображения и выявлению и диагностике заболевания. Будет получено практически подчиняющееся линейному закону накопление в зависимости от потока: до 5 мл/мин./г (высокое значение экстракции при первом прохождении). Это обеспечивает количественную оценку абсолютного значения потока в миокарде и будет эффективным как при физической, так и фармакологической нагрузке. Это также будет характеризоваться соответствующим профилем безопасности и будет доступным в виде стандартной дозы (например, 18F-меченое соединение).
В третьем аспекте настоящее изобретение относится к способу визуализации сердца у пациента, включающему введение пациенту диагностически эффективного количества визуализирующего вещества или фармацевтической композиции, определенной выше, и получение изображения сердца пациента. В последнем аспекте настоящее изобретение относится к набору для диагностики, содержащему соединение, имеющее следующую формулу

где R1 представляет собой Н, F, CF3, Cl, R представляет собой линкер, и X представляет собой уходящую группу, выбранную из группы, состоящей из тозилата, мезилата, трифлата, нонафлата и галогена, или аналог указанного соединения, и при этом указанный набор можно применять для получения визуализирующего вещества, определенного выше.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 показан путь синтеза для получения визуализирующего соединения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
В контексте настоящей заявки и настоящего изобретения применяются следующие определения.
Выражение "фармацевтически приемлемая соль" относится к таким солям, которые сохраняют биологическую эффективность и свойства свободных оснований и которые получены путем реакции с неорганическими или органическими кислотами, такими как соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота, яблочная кислота, малеиновая кислота, янтарная кислота, винная кислота, лимонная кислота и т.п.
Аналог представляет собой молекулу, которая отличается по химической структуре от исходного соединения, например, гомолог (отличающийся дополнительным элементом в химической структуре, например, различие по длине алкильной цепи), фрагмент молекулы, структура, которая отличается одной или несколькими функциональными группами, изменение образования ионов. Структурные аналоги часто находят с использованием количественных соотношений структура-активность (QSAR) при помощи методик, таких как те, которые раскрыты в Remington (The Science and Practice of Pharmacology, 19th Edition (1995), chapter 28).
Выражение "связывающая группа", используемое в данном документе, относится к части молекулы, которая служит в качестве спейсера между двумя другими частями молекулы. Связывающие группы также могут выполнять другие функции, как описано в данном документе. Примеры связывающих групп включают линейный, разветвленный или циклический алкил, арил, эфир, полигидрокси, полиэфир, полиамин, гетероциклил, ароматическую группу, гидразид, пептид, пептоид или другие физиологически совместимые ковалентные связи или их комбинации.
В первом варианте осуществления настоящее изобретение относится к визуализирующему веществу, имеющему структуру

где R1 представляет собой H, F, CF3, Cl, R представляет собой линкер, и X представляет собой фрагмент, обеспечивающий визуализацию, или аналог или фармацевтически приемлемая соль указанного визуализирующего вещества.
R может представлять собой неразветвленный алкил, этиленгликоль (эфир) или полиэтиленгликоль.
Один пример представляет собой

где R представляет собой линкер, и X представляет собой фрагмент, обеспечивающий визуализацию.
Другой пример представляет собой визуализирующее вещество с формулой, показанной ниже:

где X представляет собой фрагмент, обеспечивающий визуализацию.
X может представлять собой изотоп галогена, например, изотоп фтора, брома, хлора или йода. Примеры включают 18F, 19F, 120I, 121I, 122I, 123I, 124I, 125I, 127I, 131I, 35Cl, 37Cl, 75Br, 76Br, 77Br, 79Br, 80Br, 80mBr, 81Br или 64Cu. В конкретном примере применяют 18F или 19F.
В другом варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей визуализирующее вещество, определенное выше, и фармацевтически приемлемый носитель, разбавитель или буфер.
"Фармацевтически приемлемый" означает нетоксичный материал, который не снижает эффективность биологической активности активных ингредиентов, т.е. пептида (пептидов), полипептида (полипептидов) или их вариантов. Такие фармацевтически приемлемые буферы, носители или наполнители хорошо известны в данной области техники (см. Remington's Pharmaceutical Sciences, 18th edition, A.R Gennaro, Ed., Mack Publishing Company (1990) и Handbook of Pharmaceutical Excipients, 3rd edition, A. Kibbe, Ed., Pharmaceutical Press (2000).
Выражение "буфер", как предполагается, означает водный раствор, содержащий кислотно-основную смесь, предназначенную для стабилизации pH.
Выражение "разбавитель", как предполагается, означает водный или неводный раствор, предназначенный для разбавления пептида в фармацевтическом препарате. Разбавитель может представлять собой одно или несколько из солевого раствора, воды, человеческого сывороточного альбумина, например, трис(гидроксиметил)аминометана (и его солей), фосфата, цитрата, бикарбоната, спиртов, в том числе этанола, стерильной воды, физиологического раствора или сбалансированных ионных растворов, содержащих хлоридные и/или бикарбонатные соли или катионы нормальной плазмы крови, такие как кальций, калий, натрий и магний. Меченое соединение может присутствовать в количестве 1,0-50 милликюри, например, 1,0-10, 10-20, 20-30, 30-40, 40-50 милликюри.
Фармацевтический состав в соответствии с настоящим изобретением можно вводить системно. Пути введения включают парентеральный (внутривенный, подкожный и внутримышечный), пероральный, парентеральный, вагинальный и ректальный. Подходящие формы препарата представляют собой, например, дисперсии, суспензии, аэрозоли, капли или раствор для инъекций в ампульной форме, а также препараты с длительным высвобождением активных соединений, причем в этом препарате обычно применяют наполнители, разбавители или носители, описанные выше.
Визуализирующие вещества по настоящему изобретению можно применять в способах визуализации, в том числе способах визуализации по отношению к пациенту. Например, способ может включать введение визуализирующего вещества пациенту путем инъекции (например, внутривенной инъекции), инфузии или любого другого известного способа и визуализацию сердца субъекта, где локализовано явление, представляющее интерес.
Подходящие дозы, подлежащие введению, и конкретный способ введения будут различаться в зависимости от таких факторов, как возраст, вес, предполагаемое диагностическое применение и форма состава, например, суспензия, эмульсия, микросфера, липосома или т.п., что будет полностью очевидно для специалистов в данной области техники.
Как правило, дозу вводят при низких уровнях и увеличивают до достижения требуемого диагностического эффекта (например, получение изображения). В одном варианте осуществления описанные выше визуализирующие вещества можно вводить путем внутривенной инъекции, обычно в солевом растворе, при дозе от приблизительно 0,1 до приблизительно 100 мКи на 70 кг веса тела (и все комбинации и подкомбинации диапазонов доз и конкретные дозы в их пределах) или в некоторых вариантах осуществления при дозе от приблизительно 0,5 до приблизительно 50 мКи. Визуализацию осуществляют при помощи методик, хорошо известных специалисту в данной области техники.
Другой аспект настоящего изобретения предусматривает наборы для диагностики для получения визуализирующих веществ/диагностических средств для определения (например, выявления), визуализации и/или мониторинга по отношению к по меньшей мере части сердца. Наборы для диагностики по настоящему изобретению могут включать один или несколько флаконов, содержащих стерильный апирогенный состав, содержащий предварительно определенное количество реактива (например, предшественника контрастного вещества) по настоящему изобретению и необязательно другие компоненты, такие как хелатирующие вещества, растворители, буферы, добавки для нейтрализации, добавки для лиофилизации, добавки для стабилизации, добавки для придания растворимости и бактериостатические средства, как более полно описано ниже.
Некоторые неограничивающие примеры буферов, пригодных для получения контрастных веществ и наборов, включают, например, фосфатный, цитратный, сульфосалицилатный и ацетатный буферы. Более полный список можно найти в Фармакопее США.
Некоторые неограничивающие примеры добавок для лиофилизации, пригодных для получения контрастных веществ и наборов, включают, например, маннит, лактозу, сорбит, декстран, полимер FICOLL.RTM. и поливинилпирролидон (PVP).
Некоторые неограничивающие примеры добавок для стабилизации, пригодных для получения контрастных веществ и наборов, включают, например, этанол, аскорбиновую кислоту, этанол, цистеин, тиоглицерин, бисульфит натрия, метабисульфит натрия, гентизиновую кислоту и инозит.
Некоторые неограничивающие примеры добавок для придания растворимости, пригодных для получения контрастных веществ и наборов, включают, например, этанол, глицерин, полиэтиленгликоль, пропиленгликоль, полиоксиэтиленсорбитан моноолеат, сорбитан моноолеат, полисорбаты, сополимеры из блоков поли(оксиэтилен)-поли(оксипропилен)-поли(оксиэтилен) ("Pluronics.RTM.") и лецитин.
Некоторые неограничивающие примеры бактериостатических средств, пригодных для получения контрастных веществ и наборов, включают, например, бензиловый спирт, хлорид бензалкония, хлорбутанол и метил-, пропил- или бутилпарабен.
Соединения и композиции в соответствии с настоящим изобретением можно применять при помощи методик визуализации, таких как позитронно-эмисионная томография (PET) и однофотонная эмиссионная компьютерная томография (SPECT). Визуализация при помощи PET представляет собой диагностическое обследование, которое предусматривает получение изображений, отражающих физиологическое состояние, на основе детектирования излучения в результате испускания позитронов радиоактивным соединением, введенным пациенту. Радиоактивное соединение, как правило, вводят посредством внутривенной инъекции. Различные цвета или степени яркости на PET-изображении отражают различные уровни функции ткани или органа. Визуализация при помощи SPECT является трехмерной методикой в сочетании с компьютерной реконструкцией изображений органов для выявления как структуры, так и функции. Как и при визуализации при помощи PET, пациентам, подвергающимся визуализации при помощи SPECT, вводят радиоактивную метку. PET- и SPECT-изображения можно применять для оценки при ряде заболеваний и их обычно применяют в областях, связанных с онкологией, кардиологией и неврологией.
Способы синтеза контрастных веществ
Как правило, визуализирующие вещества, описанные в данном документе, можно синтезировать путем осуществления реакции по меньшей мере первого компонента и второго компонента, так что между ними образуется связь. Например, 18F-меченые соединения можно синтезировать путем осуществления реакции двух компонентов посредством вытеснения соответствующей уходящей группы, связанной по меньшей мере с одним компонентом. Примеры таких уходящих групп включают сложные эфиры сульфоновой кислоты, например, толуолсульфонат (тозилат, TsO-), метансульфонат (мезилат, MsO-) или трифторметансульфонат (трифлат, TfO-), нонафлат или галоген. Уходящая группа также может представлять собой галогенид, фосфиноксид (при помощи реакции Мицунобу) или внутреннюю уходящую группу (например, эпоксид или циклический сульфат). Очистку обычно осуществляют посредством удаления соли при помощи обращенно-фазовой хроматографии.
Типичные способы получения соединений описаны в следующих примерах. Вышеизложенные химические превращения можно осуществлять при помощи методик, которые будут полностью очевидными для специалиста в данной области техники, в сочетании со сведениями, описанными в данном документе. В некоторых случаях способы синтеза контрастных веществ могут предусматривать применение одного или нескольких реакционных растворителей. Типичные реакционные растворители включают, например, DMF, NMP, DMSO, THF, этилацетат, дихлорметан и хлороформ. Реакционный раствор может оставаться нейтральным или основным после добавления амина, например, триэтиламина или DIEA. В некоторых случаях химические превращения (например, реакции) можно осуществлять при температуре окружающей среды и с защитой от воздействия кислорода и воды при помощи атмосферы азота, аргона или гелия.
В некоторых вариантах осуществления временные защитные группы можно применять для предотвращения того, чтобы другие реакционноспособные функциональные группы, например, амины, тиолы, спирты, фенолы и карбоновые кислоты, участвовали или в реакции или препятствовали ей. Типичные защитные группы для аминов включают, например, трет-бутоксикарбонил и тритил (удаление осуществляется в слабокислотных условиях), Fmoc (удаление осуществляется при помощи вторичных аминов, таких как пиперидин) и бензилоксикарбонил (удаление осуществляется при помощи сильной кислоты или при помощи каталитического гидрогенолиза). Тритильную группу также можно применять для защиты тиолов, фенолов и спиртов. В определенных вариантах осуществления защитные группы для карбоновых кислот включают, например, трет-бутиловый сложный эфир (удаление осуществляется при помощи слабой кислоты), бензиловый сложный эфир (обычно удаление осуществляется при помощи каталитического гидрогенолиза) и алкиловые сложные эфиры, например, метиловый или этиловый (обычно удаление осуществляется при помощи слабого основания). Удаление всех защитных групп можно осуществлять по завершению синтеза с применением условий, описанных выше для отдельных защитных групп, и конечный продукт можно очищать при помощи методик, которые будут полностью очевидными для специалиста в данной области техники, в сочетании со сведениями, описанными в данном документе.
Следующие примеры предназначены для иллюстрирования, а не для ограничения настоящего изобретения любым образом, видом или формой, либо явным образом, либо косвенно.
ПРИМЕРЫ
ПРИМЕР 1
Синтез визуализирующего соединения
Пример 1
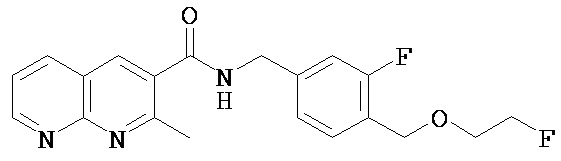
N-[[3-фтор-4-(2-фторэтоксиметил)фенил]метил]-2-метил-1,8-нафтиридин-3-карбоксамид
Колбу с раствором 19 мг 2-[[2-фтор-4-[[(2-метил-1,8-нафтиридин-3-карбонил)амино]метил]фенил]метокси]этил-4-метилбензолсульфоната (0,036 ммоля), 26 мг Kryptofix 222 (4,7,13,16,21,24-гексаокса-1,10-диазабицикло[8.8.8]гексакозан) (0,069 ммоля) и 4 мг KF (0,069 ммоля) в 1,0 мл безводного MeCN добавляли на предварительно нагретую масляную баню и нагревали при 90°C в течение 30 мин. Реакционную смесь охлаждали до комнатной температуры и разбавляли водой. Смесь дважды экстрагировали EtOAc. Объединенные органические фазы промывали солевым раствором, высушивали (MgSO4) и концентрировали. При помощи флэш-хроматографии получали 9,6 мг (72%).
1Н ЯМР (CDCl3) δ 8,97 (dd, 1Н), 8,03 (s,1H), 8,01 (m, 1Н), 7,42 (m, 2Н), 7,19 (dd, 1Н), 7,13 (m, 1Н), 7,08 (t, 1Н), 4,67 (m, 2Н), 4,65 (s, 3Н), 4,53 (m, 1Н), 3,80 (m, 1Н), 3,73 (m, 1Н).
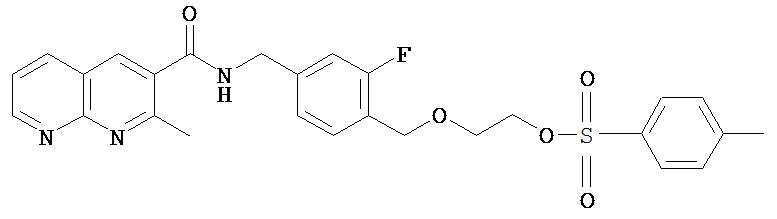
2-[[2-фтор-4-[[(2-метил-1,8-нафтиридин-3-карбонил)амино]метил]фенил]метокси]этил-4-метилбензолсульфонат
25 мг тозилхлорида (0,13 ммоля) добавляли к раствору 40 мг N-[[3-фтор-4-(2-гидроксиэтоксиметил)фенил]метил]-2-метил-1,8-нафтиридин-3-карбоксамида (0,11 ммоля), 23 мкл диизопропилэтиламина (6,13 ммоля) и 13 мг DMAP (0,11 ммоля) в 1,0 мл CH2Cl2 при комнатной температуре. Раствор перемешивали в течение 2 ч. Реакционную смесь непосредственно помещали на колонку с SiO2 и очищали при помощи флэш-хроматографии (CH2Cl2/MeOH 50:1). Получали 52 мг (90%).
1Н ЯМР (CDCl3) δ 8,89 (m, 1Н), 7,99 (s, 1Н), 7,82 (m, 1Н), 7,73 (m, 3Н), 7,31 (m, 4Н), 7,13 (m, 2Н), 4,65 (d, 2Н), 4,51 (s, 2Н), 4,15 (d, 2Н), 3,68 (m, 2Н), 2,77 (s, 3Н), 2,41 (s, 3Н).
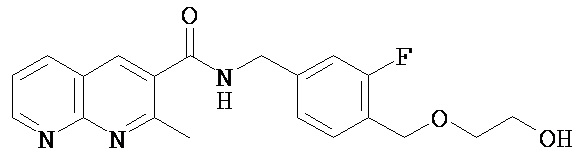
N-[[3-фтор-4-(2-гидроксиэтоксиметил)фенил]метил]-2-метил-1,8-нафтиридин-3-карбоксамид
45 мкл оксалилхлорида (0,53 ммоля) добавляли к смеси 50 мг 2-метил-1,8-нафтиридин-3-карбоновой кислоты (0,27 ммоля) в 3 мл CH2Cl2 с одной каплей DMF. Реакционную смесь перемешивали в течение 1,5 ч и затем выпаривали досуха при пониженном давлении. Остаток растворяли в 3 мл CH2Cl2. 4 мг DMAP (0,03 ммоля) и 188 мкл триэтиламина (1,35 ммоля) добавляли к раствору с последующим добавлением 54 мг 2-[[4-(аминометил)-2-фторфенил]метокси]этанола (0,27 ммоля). Реакционную смесь перемешивали в течение 4 ч и затем разбавляли водой. Фазы разделяли и водную фазу экстрагировали CH2Cl2. Объединенные органические фазы высушивали (MgSO4) и концентрировали. При помощи флэш-хроматографии (SiO2, CH2Cl2/MeOH 20:1) получали 36 мг (36%) титульного соединения.
1Н ЯМР (CDCl3) δ 8,82 (m, 1Н), 7,96 (s, 1Н), 7,95 (m, 1Н), 7,88 (m, 1Н), 7,31 (m, 2Н), 7,10 (m, 2Н), 4,60 (d, 2Н), 4,56 (s, 2Н), 3,75 (m, 2Н), 3,61 (m, 2Н), 2,68 (s, 3Н).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И УСТРОЙСТВО ДЛЯ СИНТЕЗИРОВАНИЯ РАДИОФАРМАЦЕВТИЧЕСКИХ ПРЕПАРАТОВ И ИХ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ | 2011 |
|
RU2631500C2 |
| ДЕЙТРИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВ ВИЗУАЛИЗАЦИИ | 2015 |
|
RU2696492C2 |
| ДЕЙТРИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВ ВИЗУАЛИЗАЦИИ | 2015 |
|
RU2791900C1 |
| КОМПОЗИЦИИ, СПОСОБЫ И СИСТЕМЫ ДЛЯ СИНТЕЗА И ПРИМЕНЕНИЕ ВИЗУАЛИЗИРУЮЩИХ СРЕДСТВ | 2011 |
|
RU2710736C2 |
| ТРИЦИКЛИЧЕСКИЕ ИНДОЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ЛИГАНДОВ PBR | 2010 |
|
RU2525196C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗОБРАЖЕНИЯ КРОВОСНАБЖЕНИЯ МИОКАРДА | 2012 |
|
RU2648358C2 |
| ПРОИЗВОДНЫЕ ИЗАТИНА ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ АГЕНТОВ ВИЗУАЛИЗАЦИИ IN VIVO | 2009 |
|
RU2535975C2 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ СВОЙСТВОМ СВЯЗЫВАТЬ АМИЛОИД, И СПОСОБ ДЕТЕКЦИИ ОТЛОЖЕНИЙ АМИЛОИДА У МЛЕКОПИТАЮЩЕГО | 2004 |
|
RU2440995C2 |
| ПРОИЗВОДНЫЕ ИНДОЛА, ПОДХОДЯЩИЕ ДЛЯ ВИЗУАЛИЗАЦИИ НЕЙРОВОСПАЛЕНИЯ | 2009 |
|
RU2512288C2 |
| Химические соединения для покрытия наноструктур | 2018 |
|
RU2757904C2 |
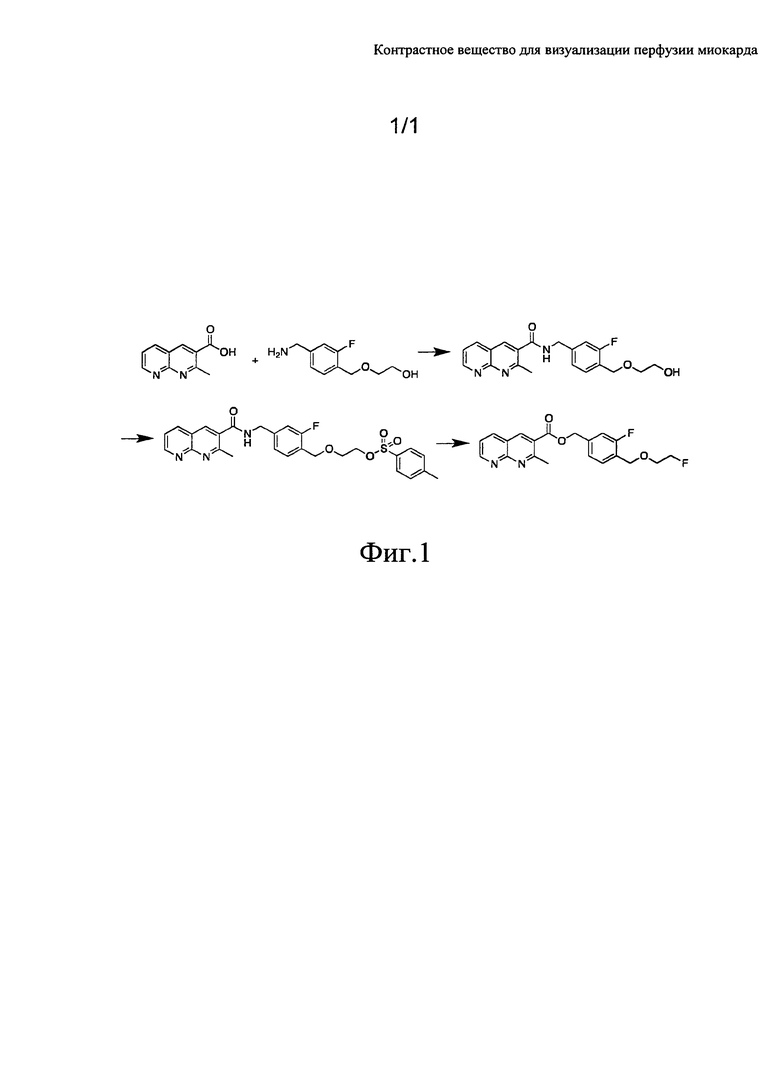
Группа изобретений относится к медицине. Описаны соединения и способы для визуализации перфузии миокарда, включающие введение пациенту соединения, связанного с фрагментом, обеспечивающим визуализацию, где указанное соединение связывается с митохондриальным комплексом I (МС-I), и сканирование пациента при помощи диагностической визуализации. Изобретение также относится к наборам, содержащим указанное соединение или соединения-предшественники, связанные или не связанные с фрагментом, обеспечивающим визуализацию. Соединения для визуализацию делают доступным важный диагностический маркер для визуализации перфузии миокарда. 5 н. и 2 з.п. ф-лы, 1 ил., 1 пр.
1. Визуализирующее вещество, имеющее структуру
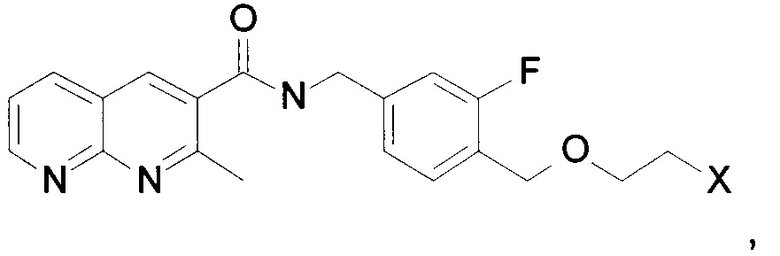
где X представляет собой изотоп галогена.
2. Визуализирующее вещество по п. 1, где X представляет собой 18F, 19F, 120I,121I,122I,123I, 124I, 125I, 127I, 131I, 35Cl, 37Cl, 75Br, 76Br, 77Br, 79Br, 80Br, 80mBr или 81Br.
3. Визуализирующее вещество по п. 2, где X представляет собой 18F или 19F.
4. Фармацевтическая композиция для визуализации сердца у пациента, содержащая визуализирующее вещество по любому из пп. 1-3 и фармацевтически приемлемый носитель, разбавитель или буфер.
5. Набор для визуализации сердца у пациента, содержащий визуализирующее вещество по любому из пп. 1-3 или фармацевтическую композицию по п. 4 и инструкцию по применению указанного набора.
6. Способ визуализации сердца у пациента, включающий:
1) введение пациенту диагностически эффективного количества визуализирующего вещества по любому из пп. 1-3 или фармацевтической композиции по п. 4 и
2) получение изображения сердца пациента.
7. Набор для визуализации сердца у пациента, содержащий:
1) соединение, имеющее следующую формулу
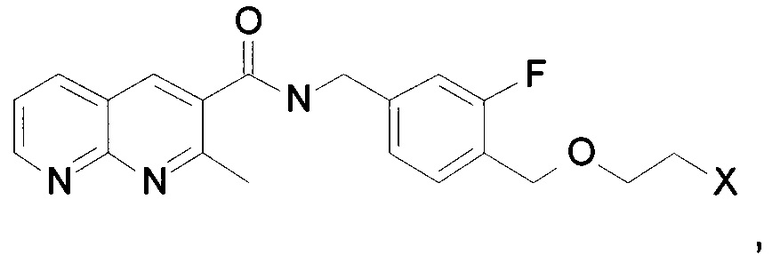
где X представляет собой уходящую группу, выбранную из группы, состоящей из мезилата, трифлата и нонафлата, и
2) изотоп галогена.
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
Авторы
Даты
2017-09-04—Публикация
2012-12-18—Подача