Изобретение относится к области медицины, биологии, биотехнологии, молекулярной биологии, нанобиотехнологии и фармакологии и представляет собой конъюгаты и способы их получения, состоящие из цитостатиков, биодеградируемого полимера, поверхностно-активного вещества, криопротектора и векторных молекул для направленной доставки цитостатиков в опухолевые клетки.
В качестве цитостатических препаратов используются противоопухолевые препараты антрациклинового ряда, выбранные из группы: (доксорубицин, даунорубицин, эпирубицин, идарубицин, митоксантрон, акларубицин, зорубицин, пирарубицин, валрубицин), в качестве биодеградируемого полимера - сополимеры молочной и гликолевой кислот, в качестве поверхностно-активного вещества - поливиниловый спирт различной концентрации, в качестве криопротектора - моно- и дисахариды, в качестве векторных молекул - рекомбинантные белковые молекулы альфа-фетопротеина (АФП) с и без His- и Tag-последовательностей и/или фрагмент рекомбинантной белковой молекулы альфа-фетопротеина (АФП). Конъюгаты выполнены в виде лиофилизатов, предназначенных для внутривенного введения, и обеспечивают направленное и пролонгированное действие.
Изобретение способствует повышению таргетности в отношении опухолевых клеток, что повышает эффективность лечения и снижает общую токсичность.
Способом решения вышеперечисленных проблем является разработка системы направленной (векторной) доставки химиотерапевтических препаратов в виде полимерных или липосомальных форм, связанных (конъюгированных) с векторными молекулами, обладающими специфическим сродством к поверхности опухолевых клеток.
Известна работа Farokhzad О.С. с соавторами, в которой представлена система направленной доставки противоопухолевых препаратов на основе полимерных частиц PLGA-PEG-COOH к клеткам рака предстательной железы. В качестве векторной молекулы служил аптамер А10 PSMA, селективно связывающий внеклеточный участок простатспецифического антигена [1].
Известны технические решения, защищенные патентами US 20130052134, WO 2013127949, CN 103745793, СА 2648099, в которых описаны способы конъюгации с использованием различных производных карбодиимида и где использованы сополимеры, такие как PEG-PLGA-PLL, DSPE-PEG-COOH, PLGA-b-PEG и т.п.
Недостатком этих способов является относительно узкая область применения.
Известны также технические решения, защищенные патентами CN 101744789, PT 1539976, WO 2010028217, US 7105158, US 6555110, в которых описаны способы конъюгации с применением карбодиимидов.
Недостатком этих изобретений является относительно большое время протекания основной реакции.
Известен также способ, защищенный патентом US 7163698 B2, представляющий собой синтез полимера PLGA с использованием пептидных векторных молекул и активирующего агента EDC, при котором используют органические фазы во время реакции конъюгации для получения модифицированного полимера, после чего получают полимерные частицы.
Известны также способы получения конъюгатов противоопухолевых препаратов с антителами, выступающими в качестве векторных систем [патенты WO 2016036794, WO 2014119624], в которых в качестве векторных молекул используются антитела.
Недостатком указанных изобретений является тот факт, что применяемые векторные молекулы не обеспечивают эффективную таргетность в отношении опухолевых клеток-мишеней, а также характеризуются относительно низкой концентрацией препарата в конечном конъюгате. Помимо этого, способы отличаются относительно высокой сложностью, вызванной необходимостью введения дополнительного линкера для получения векторной системы.
Известны также работы, в которых представлены результаты по применению в качестве вектора бомбезина (BBN) (Hitesh et al., 2014), система направленной доставки на основе полимерных частиц с использованием моноклональных антител (Li et al., 2011) [2, 3]. В ряде других работ в качестве векторной молекулы для доставки противоопухолевых препаратов используют белок альфа-фетопротеин (АФП) человека, т.к. он имеет рецепторы на поверхности опухолевых клеток [4]. В патентах РФ представлены данные по разработке ряда препаратов на основе АФП и способах их получения из природных источников [RU 2121350 С1, 10.11.1998; RU 2123009 С1, 10.12.1998; RU 2154468 С1, 09.11.1999; RU 2105567 С1, 27.02.1998].
В патенте US 20090068115 описан способ активации карбоксильных групп полимерных частиц с использованием EDC, для чего проводят реакцию в 0.1 М буфере TEMED, pH 4.8, а также дальнейшую очистку с помощью диализа.
Недостатком способа является относительно большие временные затраты.
В патенте US 2010015051 описан способ конъюгации в водных средах в боратном буфере при слабокислых значениях pH, причем избыток белка трансферрина удаляют ультрацентрифугированием.
Недостатком способа является относительно большая сложность и относительно большие временные затраты.
В патенте РФ [RU 2317102 C1, А61К 38/08, 20.02.2008] описано использование в качестве векторной молекулы пептида QMTOVNOG - аналога фрагмента альфа-фетопротеина. В частности, предложено применение пептида формулы QMTOVNOG, являющегося аналогом фрагмента α-фетопротеина с 472-й по 479-ю аминокислоту, способного избирательно захватываться опухолевыми клетками, в качестве векторной молекулы для направленной доставки противоопухолевых препаратов в опухолевые клетки. Кроме того, предложен конъюгат пептида формулы QMTOVNOG с доксорубицином, в котором доксорубицин ковалентно присоединен к указанному пептиду через тиоэфирную связь, в котором ковалентная тиоэфирная связь между ними создана путем взаимодействия SH-группы производного пептида, полученного реакцией пептида с N-гидроксисукцинимидным эфиром S-ацетилтиогликолевой кислоты, и двойной связи малеимидной группы гидразона доксорубицина, полученного реакцией доксорубицина с 4-(N-малеимидометил)циклогексан-1-карбонилгидразидом. Предложена также фармацевтическая композиция для лечения онкологических заболеваний, содержащая конъюгат доксорубицина с векторной молекулой в эффективном количестве и подходящий для внутривенного введения фармацевтический носитель, отличающаяся тем, что в качестве конъюгата доксорубицина она содержит предложенный конъюгат.
Недостатком этого конъюгата является относительно низкая таргетность в отношении опухолевых клеток-мишеней.
Одним из близких к предложенной системе направленной доставки является противоопухолевой пептидный препарат, созданный на основе рекомбинантного фргамента альфа-фетопротеина (АФП) человека. Препарат способен связываться с рецептором альфа-фетопротеина и ингибировать эстрадиол-индуцированный рост клеток гормонзависимых опухолей, а также выполнять функцию векторной молекулы для направленной доставки химитерапевтического препарата в опухолевые клетки [RU 2285537 C1, А61К 38/12, 20.10.2006].
Недостатком данного препарата является относительно низкая эффективность применения.
Наиболее близким к предложенному препарату является противоопухолевый препарат [RU 2451509 C1, А61К 31/337, 27.05.2012], представляющий собой стабильные наночастицы и включающий цитостатик, биодеградирующий полимер, поверхностно-активное вещество, криопротектор и векторную молекулу для адресной доставки частиц в пораженные органы и ткани, при этом в качестве цитотостатика содержит паклитаксел - 0,4÷1,0 мас.%, в качестве биодеградирующего полимера - сополимер молочной и гликолевой кислот (PLGA 50:50) - 14,0÷15,0 мас.%, в качестве поверхностно-активного вещества - сукцинилированный поливиниловый спирт - 3,5÷4,0 мас.%, в качестве векторной молекулы для адресной доставки частиц в пораженные органы и ткани - C-концевой домен альфа-фетопротеина (р3дАФП) - 0,1÷0,3 мас.%, а в качестве криопротектора - D-маннит - 75,0÷80,0 мас.%.
Недостатком наиболее близкого технического решения относительно предложенного противоопухолевого препарата является относительно низкая эффективность, обусловленная относительно низкой таргетностью в отношении опухолевых клеток, что снижает эффективность лечения и повышает общую токсичность при его применении.
Наиболее близким к предложенному способу является способ получения конъюгата полимеркапсулированного противоопухолевого агента из группы таксанов с активным фрагментом АФП, описанный в том же техническом решении [RU 2451509 C1, А61К 31/337, 27.05.2012], в частности способ получение конъюгата сополимера молочной и гликолевой кислот с доксорубицином, согласно которому 150.0 мг сополимера молочной и гликолевой кислот (PLGA-COOH 50/50), содержащего свободную концевую карбоксильную группу, растворяют в 1,5 мл хлороформа, к раствору добавляют 18.0 мг дициклогексилкарбодиимида и 10.0 мг N-гидроксисукцинимида (10-кратные молярные избытки по отношению к полимеру), реакционную смесь перемешивают в течение 2 ч при комнатной температуре и отделяют от выпавшего осадка дициклогексилмочевины с помощью фильтрации, к смеси прибавляют 5.0 мкл триэтиламина и 7,5 мг доксорубицина гидрохлорида, реакционную смесь перемешивают в течение 15 ч, очистку реакционной смеси от избытка доксорубицина производят с помощью трехкратной экстракции 0.1 М водным раствором соляной кислоты, продукт реакции очищают преципитацией в ледяном метаноле, осадок собирают центрифугированием при 18 тыс.g в течение 30 мин, предварительно выпарив из раствора хлороформ под вакуумом.
Недостатком наиболее близкого к предложенному способа является относительно узкая область применения, обусловленная тем, что он не может быть использован для получения противоопухолевого препарата, обладающего более высокой эффективностью, определяемой повышенной таргетностью в отношении опухолевых клеток и более низкой токсичностью при его применении.
Кроме того, известный способ отличается и относительно большим временем проведения реакции. Дополнительно можно отметить, что поскольку операция очистки в известном способе заключается в центрифугировании и ультрафильтрации, то полученный конъюгат возможно отделить лишь от низкомолекулярных примесей и невозможно отделить несвязавшиеся молекулы белка, что может привести к снижению эффективности препарата за счет блокировки рецепторов на поверхности опухолевых клеток, что, в свою очередь, приводит к снижению уровня связывания целевого препарата.
Задачей, которая решается в предложенном изобретении, является разработка противоопухолевого препарата, обладающего более высокой эффективностью применения за счет повышения таргетности в отношении опухолевых клеток и снижения токсичность при его применении, а также способа его получения, обладающего более широкой областью применения, меньшим временем получения более чистого препарата.
Техническим результатом заявленного изобретения является расширение арсенала средств с доказанной противоопухолевой активностью и способов их получения путем получения противоопухолевого препарата, обладающего более высокой эффективностью применения за счет повышения таргетности в отношении опухолевых клеток и снижения токсичность при его применении, а также способа его получения, обладающего более широкой областью применения, меньшим временем получения более чистого препарата.
Поставленная задача решается, а требуемый технический результат достигается тем, что предложен конъюгат, обладающий противоопухолевой активностью, при получении которого обеспечивают взаимодействие частиц из сополимеров молочной и гликолевой кислот с включенными в них противоопухолевыми препаратами антрациклинового ряда, с -COOH группами, активированными 1-этил-3-(3-диметиламинопропила) карбодиимидом и N-гидроксисукцинимидом при их не менее 5-кратном избытке по отношению к карбоксильным группам, с аминогруппами рекомбинатнтного белка альфа-фетопротеина, имеющего последовательности, выбранные из группы: SEQ1, SEQ2, SEQ3, SEQ4, в эквимолярных количествах в отношении карбоксильных групп, при pH от 7.4 до 9, а также проводят последующую очистку на колонке с носителем Superose 12 и осуществляют разделение продуктов реакции и выделяют целевой конъюгат в чистом виде.
Кроме того, требуемый технический результат достигается тем, что, в качестве включенных в сополимеры молочной и гликолевой кислот противоопухолевых препаратов антрациклинового ряда используют или доксорубицин, или даунорубицин, или иэпирубицин, или идарубицин, или митоксантрон, или акларубицин, или зорубицин, или пирарубицин, или валрубицин.
Кроме того, требуемый технический результат достигается тем, что для получения конъюгата используют способ, характеризующийся тем, что COOH группы полимерных частиц активируют 1-этил-3-(3-диметиламинопропила) карбодиимидом и N-гидроксисукцинимидом при их не менее 5-кратном избытке по отношению к карбоксильным группам, добавляют не больше 2 мкл 2-меркаптоэтанола и инкубируют 10 минут, затем добавляют рекомбинантный белок не меньше, чем в эквимолярных количествах в отношении активированных карбоксильных групп, доводят pH реакционной смеси до щелочных значений (от 7.4 до 9), оставляют для перемешивания 30 минут, далее останавливают реакцию и вводят не более 2 мкл этаноламина, после чего реакционную смесь очищают на колонке с носителем Superose 12 с полным разделением продуктов реакции и выделяют целевой конъюгата в чистом виде.
На чертеже графических материалах представлены:
на фиг. 1 - уровень связывания (+4°C) и эндоцитоза (+37°C) опухолевыми клетками аденокарциномы молочной железы человека линии MCF7 после 1 ч инкубации с белками: АФП абортный и рекомбинантный АФП;
на фиг. 2 - хроматограмма разделения продуктов реакции конъюгации полимерных частиц, содержащих противоопухолевый препарат антрациклинового ряда, и белковой векторной молекулы с использованием эксклюзионной хроматографии на смоле Superose 12;
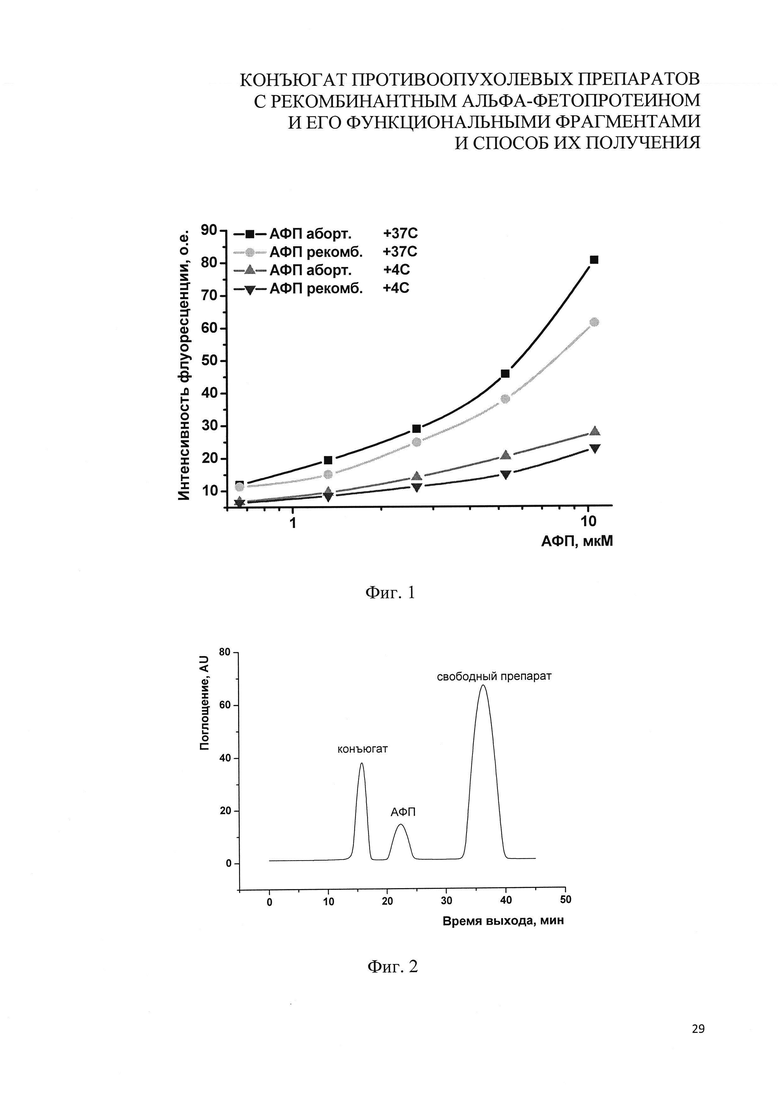
на фиг. 3 - уровень связывания (+4°C) и эндоцитоза (+37°C) опухолевыми клетками лимфолейкоза мыши линии Р388 после 1 ч инкубации с конъюгатом наночастиц, содержащих доксорубицин, с векторным белком (АФП-Fitc) и несвязанного векторного белка (АФП-Fitc);
на фиг. 4 - уровень связывания (+4°C) и эндоцитоза (+37°C) опухолевыми клетками карциномы шейки матки человека линии HeLa после 1 ч инкубации с наночастицами и конъюгатом наночастиц, содержащих доксорубицин, с векторным белком (АФП3Д);
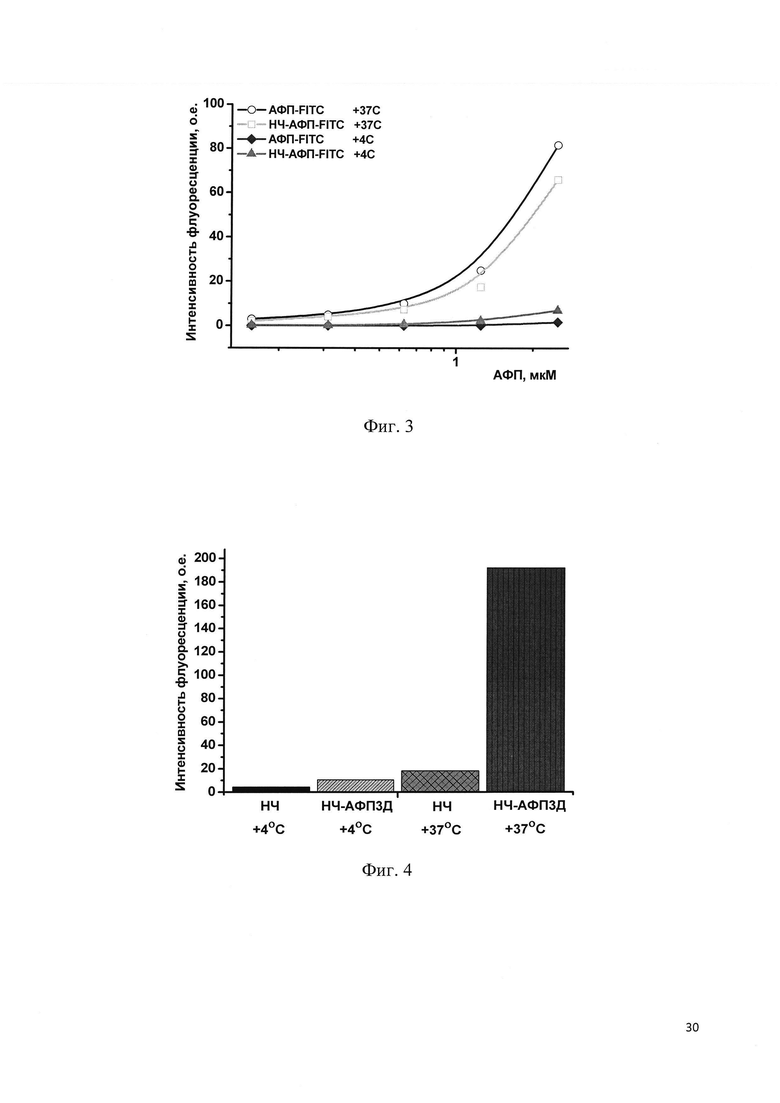
на фиг. 5 - выживаемость клеток (IC50, концентрация доксорубицина мкМ) аденокарциномы молочной железы человека линии MCF-7 после инкубации с лекарственной субстанцией доксорубицина (ДР) и конъюгата полимерных частиц доксорубицина с рАФП (рАФП-нано-ДР);
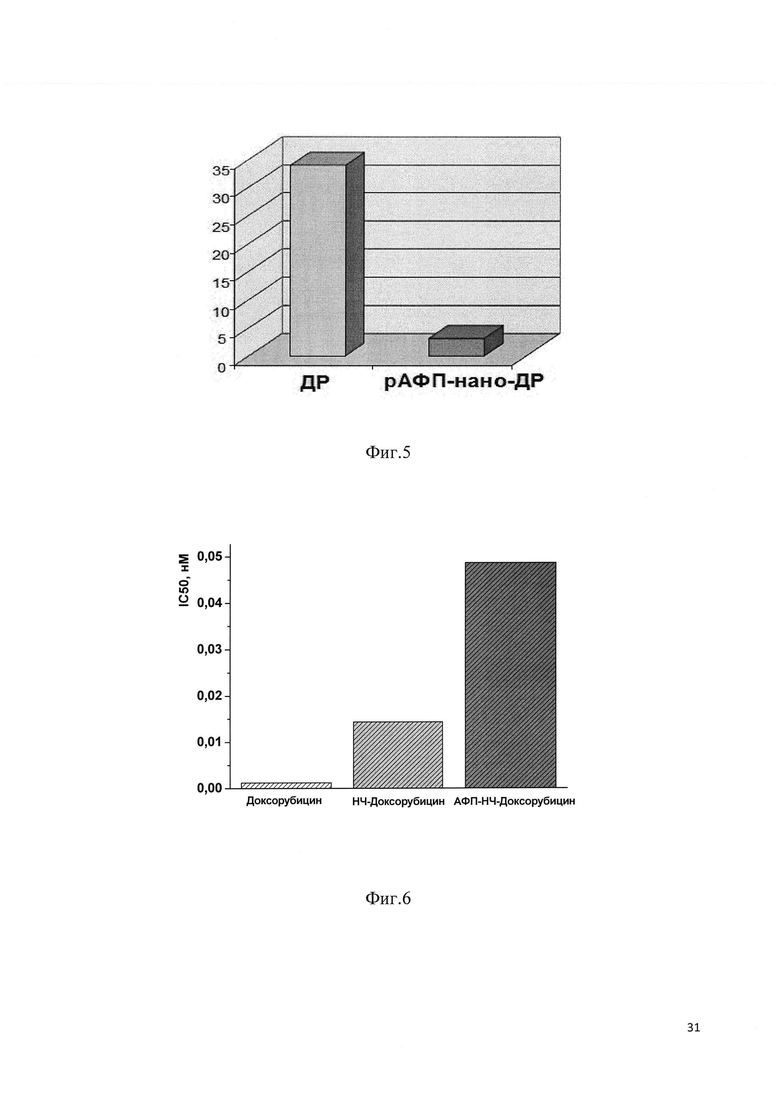
на фиг. 6 - сравнение значений IC50 (концентрация доксорубицина, нМ) для клеток лимфоцитов периферической крови человека после 72 ч инкубации с доксорубицином, наночастицами и конъюгатом наночастиц, содержащих доксорубицин, с векторным белком (рАФП);
на фиг. 7 - аминокислотная последовательность рекомбинантного АФП (SEQ1);
на фиг. 8 - аминокислотная последовательность рекомбинантного фрагмента АФП (АФП3Д) (SEQ2);
на фиг. 9 - аминокислотная последовательность рекомбинантного АФП с аффинной меткой his-tag (АФП-His) (SEQ3);
на фиг. 10 - аминокислотная последовательность рекомбинантного АФП с аффинной меткой FLAG-tag (подчеркнут) (АФП-Flag) (SEQ4).
Способ получения конъюгата противоопухолевых препаратов с рекомбинантным альфа-фетопротеином и его функциональными фрагментами осуществляется следующим образом.
Получаемый предложенным способом противоопухолевый препарат обеспечивает направленную доставку противоопухолевых препаратов непосредственно в опухолевые клетки, защищая их от воздействия резистентных механизмов и обеспечивая пролонгированный эффект.
Заявленный способ предназначен для получения конъюгатов полимерных частиц, содержащих цитостатические препараты, с рекомбинантным АФП и его функциональными фрагментами.
Для получения конъюгатов использовали карбодиимидный способ. Этот способ отличается простотой, относительно небольшим временем проведения реакции, а также относительно приемлемыми условиями, в которых она протекает.
Отметим, что, одним из способов лечения онкологических заболеваний является применение химиотерапевтических препаратов. На протяжении многих лет в качестве противоопухолевых веществ используются антибиотики антрациклинового ряда [5]. Первые антрациклины были выделены из пигментопродуцирующих бактерий Streptomyces peucetius в 1960-х годах. Данные препараты активно используются при терапии злокачественных опухолей различного происхождения, таких как различных гематологических видов онкологии, саркомы мягких тканей, карциномы и других опухолей. Спектр показаний к применению конкретного антибиотика определяется его химическим строением, индивидуальными фармакокинетическими и фармакодинамическими свойствами и степенью его изученности.
Механизм действия препаратов данной группы обусловлен ингибированием синтезануклеиновых кислот путем интеркаляции между парами азотистых оснований, что приводит к нарушению вторичной спирализации ДНК за счет взаимодействия с топоизомеразой II. Кроме того, происходит взаимодействие с липидами клеточных мембран, нарушая, тем самым, транспорт ионов и целый ряд других функций клетки.
Настоящее изобретение относится к терапевтическим комбинациям, содержащим препараты антрациклинового ряда. К таковым относятся следующие препараты, не ограничивающие объема изобретения:
1. «Доксорубицин» - антрациклиновый антибиотик. Его применяют для лечения лимфобластного лейкоза, саркомы мягких тканей, остеогенной саркомы, саркомы Юинга, рака молочной железы, рака щитовидной железы, опухоли Вильмса, нейробластомы, рака мочевого пузыря, рака желудка, рака яичников, лимфогранулематоза, неходжкинских лимфом, трофобластических опухолей, рефрактерного рака яичника, саркомы Капоши [6-10].
Механизм действия доксорубицина заключается во взаимодействии с ДНК, образовании свободных радикалов и прямом воздействии на мембраны клеток с подавлением синтеза нуклеиновых кислот. Клетки чувствительны к препарату в S- и G2-фазах. Однако, ввиду высокой токсичности доксорубицина, его применение сопряжено с рядом побочных эффектов: тромбоцитопенией, лейкопенией, анемией, кардиомиопатией, сердечная недостаточностью, аритмией, стоматитом, эзофагитом, тошнотой, рвотой, диареей, азооспермиеей, аменореей, аллергическими реакциями, алопецией, гиперурикемией, нефропатией и др.
2. «Даунорубицин» применяют для лечения острого лимфобластного и нелимфобластного (миелобластного, монобластного, эритробластного) лейкоза, неходжкинских лимфом, опухоли Юинга, опухоли Вильмса, бластного криза хронического миелолейкоза, лимфосаркомы, хорионэпителиомы матки, злокачественного гистоцитоза (у взрослых и детей), саркомы мягких тканей, нейробластомы (у детей). Применяют в комбинации с другими противоопухолевыми средствами в составе программ индукции ремиссии [11, 12].
Механизм действия даунорубицина заключается в воздействии на S-фазу митоза. Кроме того, даунорубицин блокирует матричную функцию ДНК, нарушая синтез нуклеиновых кислот и белка. Противоопухолевая активность реализуется также через взаимодействие с мембранами и образование свободных радикалов семихинонного типа.
Даунорубицин обладает рядом побочных эффектов, к которым можно отнести следующие: угнетение костномозгового кроветворения (анемия, лейкопения, нейтропения, тромбоцитопения), развитие или усугубление сердечной недостаточности (аритмия, одышка, отечность в области голеностопных суставов), тошноту, снижение аппетита, рвоту, диарею, изъязвление слизистой оболочки ЖКТ (язвенный стоматит, эзофагит), гиперурикемию (болезненное или затрудненное мочеиспускание, цистит), аменорею, азооспермию, аллергические реакции, головную боль, алопецию и др.
Таким образом, существенным недостатком используемых в настоящее время противоопухолевых препаратов является их высокая токсичность, которая вызывает интоксикацию организма пациента, а также множественные побочные эффекты.
Другим недостатком является возникновение у опухолевых клеток множественной лекарственной устойчивости (МЛУ). Механизм МЛУ связан с гиперэкспрессией трансмембранных белков семейства АВС-транспортеров, которые способны удалять химиотерапевтические агенты из опухолевой клетки [13].
Изобретение может быть применено для лечения опухолевых злокачественных новообразований при наличии на поверхности опухолевых клеток рецепторов к альфа-фетопротеину (АФП), а именно: для лечения аденокарциномы молочной железы человека линий MCF 7 и сублинии MCF 7 Adr, резистентной к антрациклиновым антибиотикам; карциномы шейки матки человека линии HeLa; остеосаркомы человека линии MG 63; аденокарциномы яичника человека линии SKOV3, резистентной линии SKVLB и линии OVCAR 8; B-клеточных лимфом человека линий Raji и Namalva; Т-клеточных лимфом человека линий СЕМ, Molt-4, Jukart, QOS; эритролейкоза человека линии K562; миелолейкоза человека линий TF-1 и KG-1; аденокарциномы предстательной железы человека линий LnCaP и Du145; эпидермоидной карциномы человека А-431; нейробластомы человека линии IMR-32; гепатомы человека линии Alexander и HepG2; карциномы сигмовидной кишки человека линии Colo320; аденокарциномы ободочной кишки человека линии Caco-2; аденокарциномы 12-перстной кишки человека линии HuTu80; аденокарциномы прямой кишки человека линии SW837; немелкоклеточной карциномы легкого человека линии А549; глиомы человека линии U373MG; миеломы человека линий U266 и IM9; лейкосаркомы человека линии SK-UT-1B; карциномы глотки человека линии KB; мелкоклеточной карциномы легкого человека линии Н69; меланомы человека линий SK-MEL-1, MS и Bro В19.
Термины «рак» и «злокачественная опухоль» относятся или описывают физиологическое состояние у млекопитающих, которое обычно характеризуется нерегулируемым клеточным ростом/пролиферацией.
Примеры злокачественной опухоли включают без ограничения карциному, лимфому, бластому, саркому и лейкоз. Более конкретные примеры таких злокачественных опухолей включают плоскоклеточный рак, мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарциному легкого, плоскоклеточную карциному легкого, рак брюшины, гепатоклеточный рак, рак желудочно-кишечного тракта, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичника, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак ободочной кишки, рак прямой и ободочной кишки, карциному эндометрия или матки, карциному слюнных желез, рак почек, рак печени, рак простаты, рак вульвы, рак щитовидной железы, карциному печени и различные типы рака головы и шеи.
Термин «противоопухолевая активность» означает активность конъюгата в отношении как гормоно-зависимых, так и гормоно-независимых опухолей.
Термины «химиотерапевтические препараты», «противоопухолевые препараты», «цитотоксическое средство» обозначают химические соединения, пригодные для лечения онкологических заболеваний, обладающие схожим механизмом действия, структурной формулой и физико-химическими свойствами. Данные термины включают противоопухолевые антибиотики антрациклинового ряда или другие интеркалирующие агенты, отвечающие вышеуказанным требованиям (такие как: доксорубицин, даунорубицин и др., не включая дактиномицин).
«Химиотерапевтическим средством» является химическое соединение, которое можно использовать для лечения злокачественной опухоли. Примеры химиотерапевтических средств включают алкилирующие агенты, такие как тиотепа и CYTOXAN® циклофосфамид; алкилсульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбоквон, метуредопа и уредопа; этиленимины и метилмеламины, включая алтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид и триметилмеламин; ацетогенины (в частности, буллатацин и буллатацинон); дельта-9-тетрагидроканнабинол (дронабинол, MARINOL®); бета-лапахон; лапахол; колхицины; бетулиновую кислоту; камптотецин (включая синтетический аналог топотекан (HYCAMTIN®), СРТ-11 (иринотекан, CAMPTOSAR®), ацетилкамптотецин, скополектин и 9-аминокамптотецин); бриостатин; каллистатин; СС-1065 (включая его синтетические аналоги адозелезин, карзелезин и бизелезин); подофиллотоксин; подофиллиновую кислоту; тенипозид; криптофицины (в частности, криптофицин 1 и криптофицин 8); доластатин; дуокармицин (включая синтетические аналоги KW-2189 и СВ1-ТМ1); элеутеробин; панкратистатин; саркодиктиин; спонгистатин; азотистые иприты, такие как хлорамбуцил, хлорнафазин, холофосфамид, эстрамустин, ифосфамид, мехлорэтамин, гидрохлорид оксида мехлорэтамина, мелфалан, новембихин, фенестерин, преднимустин, трофосфамид, урамустин; нитрозомочевины, такие как кармустин, хлорозотоцин, фотемустин, ломустин, нимустин и ранимустин; антибиотики, такие как энедииновые антибиотики (например, калихеамицин, в частности калихеамицин гамма II и калихеамицин омега II (смотри, например, Agnew, Chem Intl. Ed. Engl., 33: 183-186 (1994)); динемицин, включая динемицин А; эсперамицин; а также хромофор неокарциностатина и родственные хромофоры хромопротеинов - энедииновые антибиотики), аклациномизины, актиномицин, аутрамицин, азасерин, блеомицины, кактиномицин, карабицин, карминомицин, карзинофилин, хромомицин, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, доксорубицин ADRIAMICIN® (включая морфолинодоксорубицин, цианоморфолинодоксорубицин, 2-пирролинодоксорубицин и дезоксидоксорубицин), эпирубицин, эзорубицин, идарубицин, марцелломицин, митомицины, такие как митомицин С, микофеноловую кислоту, ногаламицин, оливомицины, пепломицин, потфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин; антиметаболиты, такие как метотрексат и 5-фторурацил (5-FU); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; аналоги пурина, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; аналоги пиримидина, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин, флоксуридин; андрогены, такие как калустерон, пропионат дромостанолона, эпитиостанол, мепитиостан, тестолактон; средства, подавляющие функции надпочечников, такие как аминоглютетимид, митотан, трилостан; компенсатор фолиевой кислоты, такой как фолиновая кислота; ацеглатон; гликозид альдофосфамид; аминолевулиновую кислоту; энилурацил; амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демеколцин; диазихон; элфорнитин; ацетат эллиптиния; эпотилон; этоглуцид; нитрат галлия; гидроксимочевину; лентинан; лонидаинин; мейтанзиноиды, такие как мейтанзин и ансамитоцины; митогуазон; митоксантрон; мопиданмол; нитраэрин; пентостатин; фенамет; пирарубицин; лозоксантрон; 2-этилгидразид; прокарбазин; полисахаридный комплекс PSK® (JHS Natural Products, Eugene, OR); разоксан; ризоксин; сизофиран; спирогерманий; тенуазоновая кислота; триазиквон; 2,2',2-трихлортриэтиламин; трихотецены (в частности, токсин Т-2, верракурин А, роридин А и ангуидин); уретан; виндезин (ELDISINE®, FILDESIN®); дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид («ara-C»); тиотепа; таксоиды, например, паклитаксел TAXOL® (Bristol-Myers Squibb Oncology, Princeton, N.J.), не содержащий кремофора препарат паклитаксела на основе сконструированных связанных с альбумином наночастиц ABRAXANE ТМ (American Pharmaceutical Partners, Schaumberg, Illinois) и доксетаксел TAXOTERE® (Rhone-Poulenc Rorer, Antony, France); хлорамбуцил; гемцитабин (GEMZAR®); 6-тиогуанин; меркаптопурин; метотрексат; аналоги платины, такие как цисплатин и карбоплатин; винбластин (VELBAN®); платину; этопозид (VP-16); ифосфамид; митоксантрон; винкристин (ONCOVIN®); оксалиплатин; лейковорин; винорелбин (NAVELBINE®); новантрон; эдатрексат; дауномицин; аминоптерин; ибандронат; ингибитор топоизомеразы RFS 2000; дифторметилорнитин (DMFO); ретиноиды, такие как ретиноевая кислота; капецитабин (XELODA®); фармацевтически приемлемые соли, кислоты и производные любого агента, указанного выше; а также комбинации двух или более указанных выше средств, такие как CHOP, сокращенное название комбинированной терапии циклофосфамидом, доксорубицином, винкристином и преднизолоном, и FOLFOX, сокращенное название схемы лечения оксалиплатином (ELOXATIN ТМ) в сочетании с 5-FU и лейковорином.
Также в указанное определение включены противогормональные средства, которые действуют, регулируя, уменьшая, блокируя или ингибируя эффекты гормонов, которые могут стимулировать рост злокачественной опухоли, и часто их используют в форме системного лечения или лечения на уровне целого организма. Они сами могут являться гормонами. Примеры включают антиэстрогены и избирательные модуляторы рецепторов эстрогена (SERM), включая, например, тамоксифен (включая тамоксифен NOLVADEX®), ралоксифен EVISTA®, дролоксифен, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY117018, онапристон и торемифен FARESTON®; антипрогестероны; понижающие регуляторы рецептора эстрогена (ERD); средства, которые функционируют, подавляя или прекращая работу яичников, например агонисты рилизинг-гормона лютеинизирующего гормона (LHRH), такие как ацетат лейпролида LUPRON® и ELIGARD®, ацетат гозерелина, ацетат бузерелина и триптерелин; другие антиандрогены, такие как флутамид, нилутамид и бикалутамид; и ингибиторы ароматазы, которые ингибируют фермент ароматазу, которая регулирует продукцию эстрогена в надпочечниках, такие как, например, 4(5)-имидазолы, аминоглутетимид, ацетат мегестрола MEGASE®, эксеместан AROMASIN®, форместан, фадрозол, ворозол RIVISOR®, летрозол FEMARA® и анастрозол ARIMIDEX®. Кроме того, такое определение химиотерапевтических средств включает бисфосфонаты, такие как клодронат (например, BONEFOS® или OSTAC®), этидронат DIDROCAL®, NE-58095, золедроновую кислоту/золедронат ZOMETA®, алендронат FOSAMAX®, памидронат AREDIA®, тилудронат SKELID® или ризедронат ACTONEL®; а также троксацитабин (1,3-диоксолановый нуклеозидный аналог цитозина); антисмысловые олигонуклеотиды, в частности олигонуклеотиды, которые ингибируют экспрессию генов в путях передачи сигналов, вовлеченных в аномальную пролиферацию клеток, таких как, например, PKC-альфа, Raf, H-Ras и рецептор эпидермального фактора роста (EGF-R); вакцины, такие как вакцина THERATOPE® и вакцины для генной терапии, например вакцина ALLOVECTIN®, вакцина LEUVECTLN® и вакцина VAXID®; ингибитор топоизомеразы 1 LURTOTECAN®; rmRH ABARELIX®; дитозилат лапатиниба (низкомолекулярный двойной ингибитор тирозинкиназ ErbB-2 и EGFR, также известный как GW572016); и фармацевтически приемлемые соли, кислоты или производные любого из указанных выше средств.
Примеры реализации предложенного изобретения.
Пример 1. Получение биомассы рекомбинантного фрагмента АФП (r3D AFP).
Работы с бактериальными штаммами проводили под ламинаром в стерильных условиях. Для трансформации использовали компетентные клетки Bl21 (DE3) фирмы Stratogen. Пробирку с клетками (0.1 мл) размораживали на льду, добавляли 5 мкл раствора плазмиды в концентрации 20 нг/мл и инкубировали 10-15 минут на льду, после чего подвергали тепловому шоку при 42°C в течение 2 минут. Затем пробирку помещали в лед на 30 с, далее добавляли 1 мл среды LB и инкубировали 30-45 минут при 37°C при перемешивании. Затем клетки осаждали центрифугированием (2000 g, 5 минут), удаляли 1 мл супернатанта, осадок ресуспендировали в оставшейся среде и высевали на чашки Петри с агаризованной средой LB, содержащей ампициллин (100 мкг/мл). 2-3 колонии трансформантов помещали в 10 мл среды LB, содержащей ампициллин (100 мкг/мл) и инкубировали при 37°C при активном перемешивании в течение ночи. Из полученной жидкой культуры производили посев на чашку Петри с агаризованной средой LB, содержащей ампициллин (100 мкг/мл). Чашку инкубировали при 37°C в течение ночи. Из выросших колоний отбирали 6 наиболее крупных, каждую из которых помещали в 10 мл среды LB с добавлением ампициллина и инкубировали при 37°C. По достижении оптической плотности OD600 от 0.5 до 1.2 единиц добавляют ИПТГ (изопропил-β-D-1-тиогалактопиранозида) до конечной концентрации от 0.1 до 2 мМ и инкубацию продолжают в течение 3 ч, после чего определяли уровень экспрессии целевого белка с помощью электрофореза в ПААГ. Полученную биомассу центрифугируют в течение 15 мин при 10000 RPM.
Пример 2. Очистка и выделение рекомбинантного фрагмента АФП (r3D AFP).
Влажную биомассу (6 г) ресуспензировали в 100 мл буфера pH=8,0, содержащего 50 мМ фосфата натрия и 2 таблетки ингибиторов протеаз без ЭДТА (Roche). Далее добавляли лизоцим до концентрации 50 мг/л и инкубировали 10 мин при комнатной температуре, перемешивая стеклянной палочкой. Далее проводили ультразвуковую обработку 7 раз по 40 ударов при 0°C. Затем добавляли дезоксихолат натрия до 0,2 мас.%, и перемешивали 10 мин при комнатной температуре. Далее центрифугировали 10 мин в режиме 10000 об/мин. Собирали растворимую фракцию. Осадок несколько раз промывали фосфатным буфером и центрифугировали при 10000 об/мин. Осадок телец включения и растворимую фракцию хранили при -20°C. Осадок телец включения ресуспендировали в 10 мл солюбилизирующего буфера (150 мМ NaCl, 10 мМ KH2PO4, 8 М мочевина, 12 мМ меркаптоэтанол, pH 7.4) и оставляли при перемешивании при комнатной температуре на 1 час. Полученный раствор центрифугировали (10000 об/мин, 10 мин) и использовали в дальнейшем для рефолдинга супернатант. Через колонку с носителем Superose 12 предварительно пропускали 5 объемов ренатурирующего буфера (150 мМ NaCl, 10 мМ KH2PO4, 1 мМ GSSG, 5 мМ GSH, pH 8.5, +4°C). Затем готовили разведения солюбилизирующего буфера ренатурирующим, по 0,5 мл, до конечной концетрации мочевины в растворе 8, 6, 4, 2 и 0 М и меркаптоэтанола 12, 9, 6, 3, 0 мМ соответственно, и наносили на колонку, начиная с раствора с самой низкой концентрацией денатурирующих агентов. На подготовленную колонку наносили 2 мл солюбилизированного r3D AFP (k) (не более 20 мг), затем 0,5 мл солюбилизирующего буфера и элюировали целевой белок 3 объемами ренатурирующего буфера. Полученную фракцию диализовали против 1000-кратного объема фосфатно-солевого буфера при pH=8.5 и хранили при -70°C. Рекомбинантный белок дополнительно очищали с помощью металло-хелатной хроматографии на носителе содержащем ионы Ni2+ и, при необходимости, концентрировали с помощью концентрирующих ячеек.
Пример 3. Получение биомассы рекомбинантного АФП (АФП-His, АФП-Flag, АФП).
Работы с дрожжевыми штаммами проводили под ламинаром в стерильных условиях. Для работы использовали дрожжевые штаммы Pichia Pastoris GS115 и KM 71 трансформированных генетическими конструктами на основе коммерческих плазмид pPIC9K и pPICZ А несущими нуклеотидную последовательность, кодирующую полноразмерный АФП человека, а также АФП человека с добавочными аминокислотными вставками (his-tag и flag-tag). Трансформантов высевали на чашки с агаризованной средой YPD, содержащей генитицин (в случае АФП), либо зеоцин (в случае АФП-His, АФП-Flag) в концентрации 50 мкг/мл. После трех дней инкубации при 28°C, рекомбинантные клоны перекалывали на свежие чашки с антибиотиком, подращивали и высевали в пробирки с 5 мл среды BMGY. Пробирки инкубировали на роторной качалке 16 ч при 28°C, после чего биомассу осаждали центрифугированием. Клетки промывали физиологическим раствором, затем ресуспендировали в 5 мл среды BMMY. Индуцированные клетки инкубировали на роторной качалке в течение 6 суток, при этом ежедневно добавляли метанол до концентрации 1%. Полученную биомассу центрифугировали на 3000 RPM в течение 15 мин, после чего декантируют супернатант от осадка. К полученной культуральной жидкости добавляют 0,1% азида и хранят при -70C.
Пример 4. Очистка и выделение рекомбинантного АФП (АФП-His).
Культуральную жидкость АФП-His после наращивания в шейкере объемом 1 л цетрифугируют 10 мин при 3000 об/мин +4C. Супернатант декантируют, доводят pH до 7.4 10 М NaOH, после чего наблюдается выпадение солей, от которых избавляются центрифугированием в течение 10 мин при 7000 об/мин, затем супернатант аккуратно декантируют. В полученный супернатант добавляют имидазол до конечной концентрации 25 мМ. Колонка с Ni-сефарозой уравновешивается 1*PBS, после чего смола переносится в колбу с КЖ и в течение 1 ч при комнатной температуре стоит на качалке при небольшом перемешивании. Через 1 ч перемешивания КЖ со смолой переносят в пластиковые фальконы на 50 мл, после чего смолу осаждают центрифугированием в течение 2 мин при 500 об/мин при комнатной температуре. После центрифугирования всю смолу переносят в колонку. После внесения смолы в колонку ее промывают раствором (1*PBS, содержащий 25 мМ имидазол и 0,5М NaCl), затем проводят элюирование раствором (1*PBS, содержащий 0,5М имидазол и 0,5М NaCl). Очищенный белок необходимо диализовать в течение суток, после чего белок лиофилизируют с 1% Д-маннита по общему объему белка в течение суток. Полученный лиофилизат концентрируют в 10 раз, добавляют 0,1% азида и хранят при -70°C.
Пример 5. Очистка и выделение рекомбинантных АФП (АФП -Flag, АФП).
Культуральную жидкость в объеме 1 л пропускают через колонку с носителем Br-CN-sepharose, конъюгированный с антителами к AFP, в течение суток при +4°C. Далее при комнатной температуре промывают 10 объемами 1×PBS, после чего элюируют 3M NaSCN. Очищенный белок необходимо диализовать в течение суток, после чего белок лиофилизируют с 1% Д-маннита по общему объему белка. Полученный лиофилизат концентрируют в 10 раз, добавляют 0,1% азида и хранят при -70°C.
Пример 6. Получение конъюгата полимерных частиц, содержащих цитостатический препарат, с рекомбинантными белками (АФП-His, АФП-Flag, АФП, r3D AFP).
К 25 мг полимерных частиц, полученных известным способом с использованием PLGA-COOH (14, 15, 16), заранее отмытых от избытка поверхностно-активного вещества, растворенных в 1*PBS, добавляют не менее 5-кратного избытка EDC и NHS по отношению к количеству карбоксильных групп (концентрация растворов 10 мг/мл в 1*PBS) и перемешивают 15 мин. После чего к реакционной смеси добавляют не больше, чем 2 мкл 2-меркаптоэтанола и инкубируют 10 мин, затем к активированным полимерным частицам добавляют рекомбинантный белок не меньше, чем в эквимолярных количествах в отношении активированных карбоксильных групп и доводят pH реакционной смеси до щелочных значений (от 7.4 до 9), затем оставляют перемешиваться еще 30 мин. Для остановки реакции вводят не больше, чем 2 мкл этаноламина (или любого аминопроизводного с аналогичными свойствами), после чего реакционную смесь очищают на колонке с носителем Superose 12 с полным разделением продуктов реакции, и тем самым, выделением целевого конъюгата в чистом виде. Очищенный конъюгат лиофилизируют с добавлением криопротектора в течение суток, после чего хранят в виде лиофилизата при -70°C.
Пример 7. Определение уровней цитотоксической активности.
Опухолевые клетки культивировали в среде DMEM, в пластиковых культуральных флаконах, содержащей 10% эмбриональной бычьей сыворотки и 50 мкг/мл гентамицина, в CO2-инкубаторе при 37°C в увлажненной атмосфере, содержащей 5% CO2. Клетки рассевали 2 раза в неделю с помощью раствора Версена. Мононуклеарные лейкоциты периферической крови здоровых добровольцев выделяли с помощью центрифугирования крови через градиент раствора фиколл-пак по методу 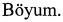
Для оценки цитотоксической активности опухолевые клетки высевали в 96-луночные планшеты по 5 тысяч клеток в лунку за сутки до эксперимента. Мононуклеарные лейкоциты периферической крови здоровых добровольцев выделяли с помощью центрифугирования крови через градиент раствора фиколл-пак по методу Boyum и рассевали в 96-луночные планшеты по 270 тысяч клеток в лунку в день эксперимента. Препараты добавляли к клеткам в триплетах и инкубировали в стандартных условиях. В случае лимфоцитов культивировали в течение 1 ч, затем 2 раза отмывали PBS с pH 7.4, помещали в 200 мкл DMEM с 10% FBS (лимфоциты помещали в RPMI1640 с 10% FBS) и инкубировали в течение 72 ч. Выживаемость клеток определяли с помощью MTT-теста. За 4 ч до окончания инкубации в каждую лунку добавляли по 50 мкл раствора МТТ в концентрации 1 мг/мл в среде для культивирования клеток. После развития окраски среду удаляли, выпавшие кристаллы формазана растворяли в 100 мкл ДМСО и измеряли интенсивность окраски по поглощению при 540 нм с помощью планшетного фотометра. Выживаемость клеток оценивали в процентах от необработанного контроля. Для построения графиков выживаемости, расчета значений IC50 и статистической обработки результатов использовали программу OriginPro (OriginLab Corporation).
Таким образом, в предложенном техническом решении достигается требуемый технический результат, заключающийся в расширении арсенала средств с доказанной противоопухолевой активностью и способов их получения, поскольку предложенный способ обеспечивает получение противоопухолевого препарата, обладающего более высокой эффективностью применения за счет повышения таргетности в отношении опухолевых клеток и снижения токсичность при его применении. Предложенный препарат обеспечивает направленную доставку противоопухолевых препаратов непосредственно в опухолевые клетки, защищая их от воздействия резистентных механизмов и обеспечивая пролонгированный эффект.
СПИСОК ЛИТЕРАТУРЫ
1. Farokhzad О.С. Targeted nanoparticle-aptamer bioconjugates for cancer chemotherapy in vivo / Farokhzad O.C., Cheng J., Teply B.A., Sherifi I., Jon S., Kantoff P.W. // Proceedings of the National Academy of Sciences - 103 (16) - 2006 - P. 6315-6320.
2. Hitesh Kulhari. Peptide conjugated polymeric nanoparticles as a carrier for targeted delivery of docetaxel / Hitesh Kulhari, Deep Pooja, Shweta Shrivastava et al. // Colloids and Surfaces B: Biointerfaces 117 - 2014 - P. 166-173.
3. Li Wang. Monoclonal antibody targeting MUC1 and increasing sensitivity to docetaxel as a novel strategy in treating human epithelial ovarian cancer / Li Wang, Hongmin Chen, Feng Hua Liu et al. // Cancer Letters - 2011 - Volume 300 - Issue 2, 28 - P. 122-133.
4. Moro R., Tcherkassova J., Song E. et al. // IVD Technology Magazine - 2005. - Vol. 11 - №5.
5. Weiss R. The anthracyclines: will we ever find a better doxorubicin / R. Weiss // Semin. Oncol. - 1992. - Vol. 19. - P. 670-686.
6. Gruber B. The effect of new anthracycline derivatives on the induction of apoptotic processes in human neoplastic cells. / B. Gruber, E. Anuszewska, W. Priebe // Folia Histochem. Cytobiol. - 2004. - Vol. 42. - P. 127-130.
7. O'Shaughnessy J. Liposomal anthracyclines for breast cancer: overview / J. O'Shaughnessy // Oncologist. - 2003. - Vol. 8. - P. 1-2.
8. Petrioli R. The role of doxorubicin and epirubicin in the treatment of patients with metastatic hormonerefractory prostate cancer / R. Petrioli, A. Fiaschi, E. Francini, A. Pascucci, G. Francini // Cancer Treat. Rev. - 2008. - Vol. 34. - P. 710-718.
9. Gewirtz D. A critical evaluation of the mechanism of action proposed for the antitumor effects of the anthracycline antibiotics adriamycin and daunorubicin / D. Gewirtz // Biochem. Pharmacol. - 1999. - Vol. 57. - P. 727-741.
10. Breslow N. Doxorubicin for Favorable Histology, Stage II-III Wilms Tumor Results from the National Wilms Tumor Studies / N. Breslow, S. Ou, M. Beckwith, G. Haase, J. Kalapurakal, M. Ritchey, R. Shamberger, P. Thomas, G.D'Angio, D. Green // Cancer. - 2004. - Vol. 101. - P. 1072-1080.
11. Arcamone F. Doxorubicin. - London: Academic Press – 1981.
12. Даунорубицина гидрохлорид Daunorubicin hydrochloride // European Pharmacopoeia. Fifth Edition: монография. - 2005. - С. 1389-1390.
13. Северин E.C. Проблемы и перспективы современной противоопухолевой терапии / Северин Е.С., Родина А.В. // Успехи биологической химии. - 200. - Т. 46. - С. 43-64.
14. Betancourt Т., Brown В., Brannon-Peppas L. Doxorubicin-loaded PLGA nanoparticles by nanoprecipitation: preparation, characterization and in vitro evaluation. Nanomedicine (Lond). 2007. 2(2):219-32. (http//www.ncbi.nlm.nih.gov/pubmed/17716122).
15. Chittasupho C., Lirdprapamongkol K., Kewsuwan P., Sarisuta N. Targeted delivery of doxorubicin to A549 lung cancer cells by CXCR4 antagonist conjugated PLGA nanoparticles. Eur J Pharm Biopharm. 2014. 88(2):529-38 (http://www.ncbi.nlm.nih.gov/pubmed/25119723).
16. Park J, Fong PM, Lu J et al. PEGylated PLGA nanoparticles for the improved delivery of doxorubicin. Nanomedicine: nanotechnology, biology, and medicine. 2009.5(4):410-418. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2789916/).
MGYQELLEKCFQTENPLECQDKGEEELQKYIQESQALAKRSCGLFQKLGEYYLQNAFLVAYTKKAPQLTSSELMAITRKMAATAATCCQLSEDKLLACGEGAADIIIGHLCIRHEMTPVNPGVGQCCTSSYANRRPCFSSLVVDETYVPPAFSDDKFIFHKDLCQAQGVALQTMKQEFLINLVKQKPQITEEQLEAVIADFSGLLEKCCQGQEQEVCFAEEGQKLISKTRAALGVLEHHHHHH
EAEARTLHRNEYGIASILDSYQCTAEISLADLATIFFAQFVQEATYKEVSKMVKDALTAIEKPTGDEQSSGCLENQLPAFLEELCHEKEILEKYGHSDCCSQSEEGRHNCFLAHKKPTPASIPLFQVPEPVTSCEAYEEDRETFMNKFIYEIARRHPFLYAPTILLWAARYDKIIPSCCKAENAVECFQTKAATVTKELRESSLLNQHACAVMKNFGTRTFQAITVTKLSQKFTKVNFTEIQKLVLDVAHVHEHCCRGDVLDCLQDGEKIMSYICSQQDTLSNKITECCKLTTLERGQCIIHAENDEKPEGLSPNLNRFLGDRDFNQFSSGEKNIFLASFVHEYSRRHPQLAVSVILRVAKGYQELLEKCFQTENPLECQDKGEEELQKYIQESQALAKRSCGLFQKLGEYYLQNAFLVAYTKKAPQLTSSELMAITRKMAATAATCCQLSEDKLLACGEGAADIIIGHLCIRHEMTPVNPGVGQCCTSSYANRRPCFSSLVVDETYVPPAFSDDKFIFHKDLCQAQGVALQTMKQEFLINLVKQKPQITEEQLEAVIADFSGLLEKCCQGQEQEVCFAEEGQKLISKTRAALGVHHHHHH
EAEADYKDDDDKRTLHRNEYGIASILDSYQCTAEISLADLATIFFAQFVQEATYKEVSKMVKDALTAIEKPTGDEQSSGCLENQLPAFLEELCHEKEILEKYGHSDCCSQSEEGRHNCFLAHKKPTPASIPLFQVPEPVTSCEAYEEDRETFMNKFIYEIARRHPFLYAPTILLWAARYDKIIPSCCKAENAVECFQTKAATVTKELRESSLLNQHACAVMKNFGTRTFQAITVTKLSQKFTKVNFTEIQKLVLDVAHVHEHCCRGDVLDCLQDGEKIMSYICSQQDTLSNKITECCKLTTLERGQCIIHAENDEKPEGLSPNLNRFLGDRDFNQFSSGEKNIFLASFVHEYSRRHPQLAVSVILRVAKGYQELLEKCFQTENPLECQDKGEEELQKYIQESQALAKRSCGLFQKLGEYYLQNAFLVAYTKKAPQLTSSELMAITRKMAATAATCCQLSEDKLLACGEGAADIIIGHLCIRHEMTPVNPGVGQCCTSSYANRRPCFSSLVVDETYVPPAFSDDKFIFHKDLCQAQGVALQTMKQEFLINLVKQKPQITEEQLEAVIADFSGLLEKCCQGQEQEVCFAEEGQKLISKTRAALGV
| название | год | авторы | номер документа |
|---|---|---|---|
| ВЫСОКОЭФФЕКТИВНЫЙ СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОЙ ФОРМЫ АДРЕСНОГО ДЕЙСТВИЯ ДЛЯ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2019 |
|
RU2727924C1 |
| ПРОТИВООПУХОЛЕВЫЙ ПРЕПАРАТ | 2011 |
|
RU2451509C1 |
| Штамм Pichia pastoris Y-4349 - продуцент альфа-фетопротеина человека, способ получения альфа-фетопротеина и композиции его содержащей | 2024 |
|
RU2838856C1 |
| ПРОТИВООПУХОЛЕВЫЙ ПЕПТИДНЫЙ ПРЕПАРАТ НА ОСНОВЕ ФРАГМЕНТА АЛЬФА-ФЕТОПРОТЕИНА, ЕГО КОНЪЮГАТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ГОРМОНЗАВИСИМЫХ ОПУХОЛЕЙ | 2005 |
|
RU2285537C1 |
| СПОСОБ ПОЛУЧЕНИЯ АКТИВНОГО ФРАГМЕНТА АЛЬФА-ФЕТОПРОТЕИНА ЧЕЛОВЕКА | 2010 |
|
RU2448116C2 |
| КОНЪЮГАТЫ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ С α -ФЕТОПРОТЕИНОМ, ОБЛАДАЮЩИЕ ИЗБИРАТЕЛЬНЫМ ДЕЙСТВИЕМ ПО ОТНОШЕНИЮ К РАКОВЫМ ОПУХОЛЯМ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1996 |
|
RU2071351C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТА ФРАГМЕНТА АЛЬФА-ФЕТОПРОТЕИНА ЧЕЛОВЕКА С ЦИПРОФЛОКСАЦИНОМ | 2010 |
|
RU2431639C1 |
| ПОЛИПЕПТИД, ЯВЛЯЮЩИЙСЯ АНАЛОГОМ РЕЦЕПТОРСВЯЗЫВАЮЩЕГО ФРАГМЕНТА ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА С 21-Й ПО 31-Ю АМИНОКИСЛОТУ, ЕГО КОНЪЮГАТ С ДОКСОРУБИЦИНОМ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2001 |
|
RU2196604C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ДЛЯ НАПРАВЛЕННОЙ ДОСТАВКИ ПРОТИВООПУХОЛЕВОГО ЛЕКАРСТВА В РАКОВУЮ КЛЕТКУ | 1996 |
|
RU2097060C1 |
| ПЕПТИД, ЯВЛЯЮЩИЙСЯ АНАЛОГОМ ФРАГМЕНТА АЛЬФА-ФЕТОПРОТЕИНА, КОНЪЮГАТ ПЕПТИДА С ДОКСОРУБИЦИНОМ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ ДЛЯ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2006 |
|
RU2317102C1 |



Группа изобретений относится к области медицины и биотехнологии и может быть использовано для получения противоопухолевых препаратов, содержащих конъюгат на основе альфа-фетопротеина и противоопухолевого средства. Конъюгат характеризуется тем, что получен в виде частиц из сополимеров молочной и гликолевой кислот с включенным в них противоопухолевым средством антрациклинового ряда путем взаимодействия -СООН групп частиц, активированных 1-этил-3-(3-диметиламинопропила)карбодиимидом и N-гидроксисукцинимидом при их не менее 5-кратном избытке по отношению к карбоксильным группам, с аминогруппами рекомбинантного белка альфа-фетопротеина, имеющего последовательности, выбранные из группы: SEQ1, SEQ2, SEQ3, SEQ4, не меньше, чем в эквимолярных количествах в отношении активированных карбоксильных групп, при рН от 7.4 до 9, с последующей очисткой на колонке с носителем Superose 12 с полным разделением продуктов реакции и выделением целевого конъюгата в чистом виде. Раскрыт также способ получения конъюгата. Группа изобретений обеспечивает повышение эффективности противоопухолевого препарата. 2 н. и 1 з.п. ф-лы, 7 пр., 10 ил.
1. Конъюгат с противоопухолевой активностью на основе рекомбинантного альфа-фетопротеина или его функционального фрагмента и противоопухолевого средства, характеризующийся тем, что получен в виде частиц из сополимеров молочной и гликолевой кислот с включенным в них противоопухолевым средством антрациклинового ряда путем взаимодействия -СООН групп частиц, активированных 1-этил-3-(3-диметиламинопропила)карбодиимидом и N-гидроксисукцинимидом при их не менее 5-кратном избытке по отношению к карбоксильным группам, с аминогруппами рекомбинантного белка альфа-фетопротеина, имеющего последовательности, выбранные из группы: SEQ1, SEQ2, SEQ3, SEQ4, не меньше, чем в эквимолярных количествах в отношении активированных карбоксильных групп, при рН от 7.4 до 9, с последующей очисткой на колонке с носителем Superose 12 с полным разделением продуктов реакции и выделением целевого конъюгата в чистом виде.
2. Конъюгат по п. 1, характеризующийся тем, что в качестве противоопухолевого средства антрациклинового ряда, включенного в сополимеры молочной и гликолевой кислот, содержит доксорубицин, даунорубицин, эпирубицин, идарубицин, митоксантрон, акларубицин, зорубицин, пирарубицин, валрубицин.
3. Способ получения конъюгата с противоопухолевой активностью по п. 1, характеризующийся тем, что -СООН группы полимерных частиц из сополимеров молочной и гликолевой кислот с включенным в них противоопухолевым средством антрациклинового ряда активируют 1-этил-3-(3-диметиламинопропила)карбодиимидом и N-гидроксисукцинимидом при их не менее 5-кратном избытке по отношению к карбоксильным группам, добавляют не больше 2 мкл 2-меркаптоэтанола и инкубируют 10 мин, затем добавляют рекомбинантный белок альфа-фетопротеина, имеющий последовательности, выбранные из группы: SEQ1, SEQ2, SEQ3, SEQ4, не меньше, чем в эквимолярных количествах в отношении активированных карбоксильных групп, доводят рН реакционной смеси до щелочных значений от 7,4 до 9, оставляют для перемешивания 30 мин, далее останавливают реакцию введением не более 2 мкл этаноламина, после чего реакционную смесь очищают на колонке с носителем Superose 12 с полным разделением продуктов реакции и выделяют целевой конъюгат в чистом виде.
| ПРОТИВООПУХОЛЕВЫЙ ПЕПТИДНЫЙ ПРЕПАРАТ НА ОСНОВЕ ФРАГМЕНТА АЛЬФА-ФЕТОПРОТЕИНА, ЕГО КОНЪЮГАТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ГОРМОНЗАВИСИМЫХ ОПУХОЛЕЙ | 2005 |
|
RU2285537C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ДЛЯ НАПРАВЛЕННОЙ ДОСТАВКИ ПРОТИВООПУХОЛЕВЫХ ЛЕКАРСТВ В РАКОВУЮ КЛЕТКУ | 1993 |
|
RU2026688C1 |
| US8574856, 05.11.2013 | |||
| ГОДОВАННЫЙ А.В | |||
| Использование С-концевого домена альфа-протеина для адресной доставки противоопухолевых препаратов.Автореф | |||
| дисс.к.б.н., Москва, 2012. | |||
Авторы
Даты
2017-09-15—Публикация
2016-08-05—Подача