ПЕРЕКРЕСТНЫЕ ССЫЛКИ
Данная заявка притязает на приоритет по предварительной заявке США No 61/317223, поданной 24 марта 2010 года, полностью включенной в данный документ посредством отсылки.
УРОВЕНЬ ТЕХНИКИ
Киназы регулируют основные процессы развития рака и других гиперпролиферативных нарушений, включая такие аспекты, как пролиферация, миграция и метастазирование, неоваскуляризация и химиорезистентность. Таким образом, ингибиторы киназы являются основной целью разработки лекарственных средств, и некоторые ингибиторы киназы в настоящее время одобрены для различных показаний к применению против рака. Как правило, ингибиторы киназы выбирают методом высококопроизводительного скрининга с использованием каталитических доменов киназы при низкой концентрации АТР, и этот процесс часто приводит к получению миметиков АТР, лишенных специфичности и/или со слабой функцией в клетках, в которых уровни АТР являются высокими.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Согласно настоящему изобретению предложено соединение, имеющее структуру (I), или его N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль:

в которой:
Q представляет собой О или S;
W представляет собой C6-C12арил или C3-C12гетероарил, содержащий 1-3 гетероатома;
каждый из Х и Y независимо отсутствует или представляет собой NH;
каждый из Z1 и z2 независимо выбран из группы, состоящей из CH, N и NR5, где R5 представляет собой водород или низший алкил;
Z3 представляет собой О, S, N или NR5, где R5 представляет собой водород или низший алкил;
r1 представляет собой незамещенный или замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, или алкил, замещенный незамещенным или замещенным C3-C12гетероарилом, содержащим 1-3 гетероатома;
каждый R2 и R3 независимо выбран из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, необязательно замещенного C3-C12циклоалкила, необязательно замещенного C3-C10гетероцикла, содержащего 1-3 гетероатома, необязательно замещенного C6-C12арила, необязательно замещенного C3-C12гетероарила, содержащего 1-3 гетероатома, CF3, галогена, CN, CONHR6 и CO2R’, где R’ представляет собой водород или C1-C6алкил; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла;
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, NO2, -CN, C1-C6алкокси, -NHSO2R6, -SO2NHR6, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, CO2R6, -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила; p=0-4; и n равен 1 или 2.
В некоторых вариантах предложено соединение, имеющее структуру (II), или его N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль:

в которой:
каждый из Z1 и Z2 независимо выбран из группы, состоящей из CH, N и NR5, где R5 представляет собой водород или низший алкил;
Z3 представляет собой О, S, N или NR5, где R5 представляет собой водород или низший алкил;
каждый R2 и R3 независимо выбран из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, необязательно замещенного C3-C12циклоалкила, необязательно замещенного C3-C10гетероцикла, содержащего 1-3 гетероатома, необязательно замещенного C6-C12арила, необязательно замещенного C3-C12гетероарила, содержащего 1-3 гетероатома, CF3, галогена, CN, CONHR6 и CO2R’, где R’ представляет собой водород или C1-C6алкил; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла;
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, NO2, -CN, C1-C6алкокси, -NHSO2R6, -SO2NHR6, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, CO2R6, -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила; n равен 1 или 2; и
R8 и R9 независимо выбраны из группы, состоящей из водорода, галогена, необязательно замещенного C1-C6алкила, -CF3, -OH, необязательно замещенного C1-C6алкокси, -NR10R11 и -SOmR12, где R10 и R11 независимо выбраны из группы, состоящей из водорода, необязательно замещенного C1-C6алкила, -SO2R12, -S(O)R12 и -COR12, и R12 представляет собой необязательно замещенный алкил или необязательно замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, и m равен 0-2.
В других вариантах предложено соединение, имеющее структуру (III), или его N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль:
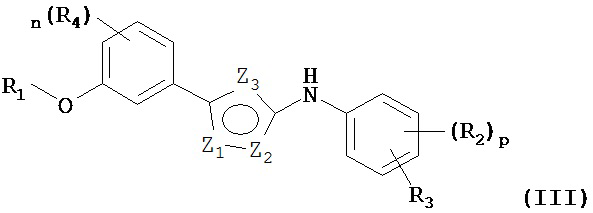
в которой:
каждый из Z1 и Z2 независимо выбран из группы, состоящей из CH, N и NR5, где R5 представляет собой водород или низший алкил; и
Z3 представляет собой О, S, N или NR5, где R5 представляет собой водород или низший алкил;
R1 представляет собой незамещенный или замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, или алкил, замещенный незамещенным или замещенным C3-C12гетероарилом, содержащим 1-3 гетероатома;
каждый R2 и R3 независимо выбран из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, необязательно замещенного C3-C12циклоалкила, необязательно замещенного C3-C10гетероцикла, содержащего 1-3 гетероатома, необязательно замещенного C6-C12арила, необязательно замещенного C3-C12гетероарила, содержащего 1-3 гетероатома, CF3, галогена, CN, CONHR6 и CO2R’, где R’ представляет собой водород или C1-C6алкил; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла;
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, NO2, -CN, C1-C6алкокси, -NHSO2R6, -SO2NHR6, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, CO2R6, -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила; p=0-4; и n равен 1 или 2.
В некоторых вариантах предложено соединение, имеющее структуру (IV), или его N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль:

в которой:
каждый из Z1 и Z2 независимо выбран из группы, состоящей из CH, N и NR5, где R5 представляет собой водород или низший алкил;
Z3 представляет собой О, S или NR5, где R5 представляет собой водород или низший алкил;
R1 представляет собой незамещенный или замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, или алкил, замещенный незамещенным или замещенным C3-C12гетероарилом, содержащим 1-3 гетероатома;
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, NO2, -CN, C1-C6алкокси, -NHSO2R6, -SO2NHR6, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, CO2R6, -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила, и n равен 1 или 2; и
R13 представляет собой необязательно замещенный N-(C1-C6алкил)пиразолил или выбран из группы, состоящей из следующих структур:
 ,
,  ,
, 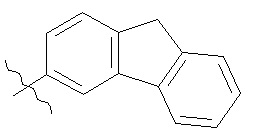 ,
,
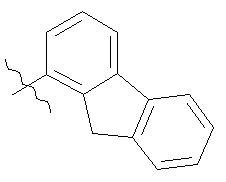 ,
,  ,
,  ,
,
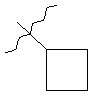 ,
, 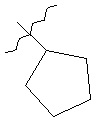 ,
,  ,
,
 ,
,  ,
, 
 ,
,  ,
, 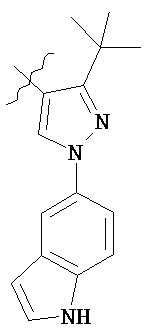 .
.
В других вариантах предложено соединение, имеющее структуру (V), или его N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль:

в которой:
Z3 представляет собой О или S;
R1 представляет собой незамещенный или замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, или алкил, замещенный незамещенным или замещенным C3-C12гетероарилом, содержащим 1-3 гетероатома;
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, NO2, -CN, C1-C6алкокси, -NHSO2R6, -SO2NHR6, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, CO2R6 и -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила; n равен 1 или 2; и
R14 выбран из группы, состоящей из необязательно замещенного C1-C12алкила, необязательно замещенного C3-C12циклоалкила, необязательно замещенного C3-C10гетероцикла, содержащего 1-3 гетероатома, необязательно замещенного C6-C12арила и необязательно замещенного C3-C12гетероарила, содержащего 1-3 гетероатома.
В некоторых вариантах предложены способы супрессии, предупреждения или ингибирования лимфоангиогенеза, неоваскуляризации, рекрутинга периэндотелиальных клеток, ангиогенеза, гиперпролиферативных нарушений, фибротического поражения, заболеваний глаз и/или роста опухоли. Способ включает контактирование опухоли с соединением структур I-V или Ia-Va, или фармацевтической композицией, содержащей соединение структур I-V или Ia-Va.
В некоторых вариантах предложены способы лечения рака, рестеноза, гиперплазии интимы, фиброзирующих заболеваний или расстройств, связанных с ангиогенезом, у пациента-человека. Способы включают введение пациенту, нуждающемуся в этом, соединения структур I-V или Ia-Va, или фармацевтической композиции, содержащей соединение структур I-V или Ia-Va.
В определенных вариантах предложены способы предупреждения ингибирования ASK1-опосредованного апоптоза в клетке, сенсибилизации клетки экзогенному стрессу или ингибирования MEK1/2- и/или ERK-1/2-опосредованной клеточной пролиферации или миграции. Способы включают контактирование опухоли с соединением структур I-V или Ia-Va, или фармацевтической композицией, содержащей соединение структур I-V или Ia-Va.
В некоторых вариантах предложены способы ингибирования протеинкиназы, включающие контактирование протеинкиназы с ингибирующей концентрацией соединения структур I-V или Ia-Va, или фармацевтической композицией, содержащей соединение структур I-V или Ia-Va.
ВКЛЮЧЕНИЕ В ОПИСАНИЕ ИЗОБРЕТЕНИЯ СВЕДЕНИЙ ПУТЕМ ОТСЫЛКИ
Все публикации, патенты и патентные заявки, упомянутые в настоящем описании, включены в него посредством отсылки в той мере, как если бы каждая отдельная публикация, патент или патентная заявка была специально и отдельно включена в описание посредством отсылки.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Новые признаки изобретения изложены подробно в прилагаемой формуле изобретения. Лучшее понимание признаков и преимуществ настоящего изобретения будет получено при обращении к следующему подробному описанию, в котором изложены иллюстративные варианты, использующие принципы изобретения, и сопровождающим чертежам, в которых:
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
В случае 1,2,4-триазолов существует три таутомерные структуры, как показано ниже:

Какая таутомерная структура является доминирующей, зависит от заместителей на триазольном фрагменте и от условий реакции. Как известно средним специалистам в данной области, как правило, 1H-1,2,4-триазол является наиболее общей таутомерией формой, особенно, если аминозаместитель присоединен к кольцу. Даже если все три таутомерные структуры присутствуют и взаимно превращаются друг в друга, все общие структуры и все примеры, имеющие 1,2,4-триазольный фрагмент, показаны здесь в одной таутомерной форме, такой как 4H-1,2,4-триазол, для простоты изложения и для сопоставления с ее прямыми аналогами, такими как примеры, содержащие 1,3,4-оксадиазольный фрагмент. Использование только 4H-таутомерной формы для графического представления структур для простоты изложения не означает, что предложенные здесь соединения существуют в этой конкретной таутомерной форме.
Согласно настоящему изобретению предложено соединение, имеющее структуру (I), или его N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль:

в которой:
Q представляет собой О или S;
W представляет собой C6-C12арил или C3-C12гетероарил, содержащий 1-3 гетероатома;
каждый из Х и Y независимо отсутствует или представляет собой NH;
каждый из Z1 и Z2 независимо выбран из группы, состоящей из CH, N и NR5, где R5 представляет собой водород или низший алкил;
Z3 представляет собой О, S, N или NR5, где R5 представляет собой водород или низший алкил;
R1 представляет собой незамещенный или замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, или алкил, замещенный незамещенным или замещенным C3-C12гетероарилом, содержащим 1-3 гетероатома;
каждый R2 и R3 независимо выбран из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, необязательно замещенного C3-C12циклоалкила, необязательно замещенного C3-C10гетероцикла, содержащего 1-3 гетероатома, необязательно замещенного C6-C12арила, необязательно замещенного C3-C12гетероарила, содержащего 1-3 гетероатома, CF3, галогена, CN, CONHR6 и CO2R’, где R’ представляет собой водород или C1-C6алкил; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла;
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, NO2, -CN, C1-C6алкокси, -NHSO2R6, -SO2NHR6, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, CO2R6, -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила; p=0-4; и n равен 1 или 2.
Согласно настоящему изобретению предложены обогащенные дейтерием соединения, имеющие структуру (I), или их N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль. Атомы водорода, присутствующие на соединениях структуры (I), обладают разными способностями к обмену с дейтерием. Некоторые являются легко обмениваемыми под воздействием физиологических условий (например, любых кислотных атомов водорода), которые могут быть обменены во время или после синтеза конечных соединений. Некоторые не являются легко обмениваемыми и могут быть введены при помощи дейтерированных исходных материалов или промежуточных соединений во время получения конечных соединений.
В некоторых вариантах, кроме того, предложено соединение, имеющее структуру (I), или его N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль, в которой Z3, представляет собой О или S. В некоторых вариантах Q представляет собой S. В других вариантах Q представляет собой О. В определенных вариантах n равен 2. В некоторых вариантах W представляет собой C3-C10гетероцикл, содержащий 1-3 гетероатома. В определенных вариантах W выбран из группы, состоящей из тиофена, пиридина, пиридазина, пиримидина и пиразина. Например, соединение выбрано из группы, состоящей из:
 ,
, ,
, ,
,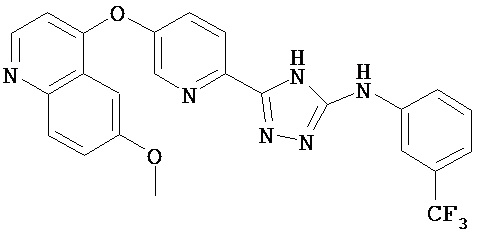 ,
, и
и  .
.
В других вариантах W представляет собой С6-С12арил. В определенных вариантах W представляет собой фенил. В определенных вариантах Z3 представляет собой О или S, и каждый R2 и R3 независимо выбран из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, -CF3, галогена, -CN и -CO2R’, где R’ представляет собой водород или C1-C6алкил; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла. В некоторых вариантах R1 представляет собой незамещенный или замещенный C3-C12гетероарил, содержащий 1-3 гетероатома. В определенных вариантах R1 представляет собой незамещенный или замещенный пиридин. В определенных вариантах R1 представляет собой незамещенный пиридин или C1-C6алкил-замещенный пиридин. В определенных вариантах R1 представляет собой незамещенный или замещенный пиримидин. В некоторых вариантах соединение имеет структуру (I), в которой R4 представляет собой водород. В некоторых вариантах соединение имеет структуру (I), в которой каждый R2 и R3 независимо выбран из группы, состоящей из C1-C6алкила, -CF3 и галогена, где p равен 0 или 1; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла.
В определенных вариантах соединение, имеющее структуру (I), выбрано из группы, состоящей из:
 ,
,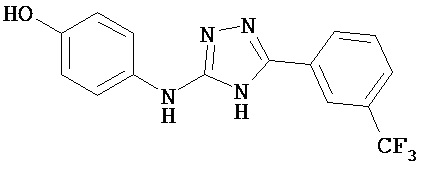 ,
,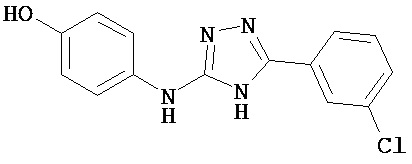 ,
, ,
,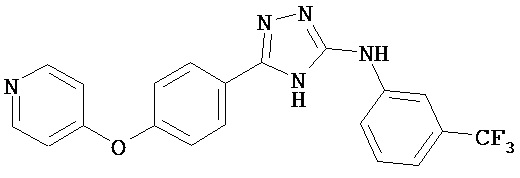 ,
, ,
, ,
, ,
, ,
, ,
,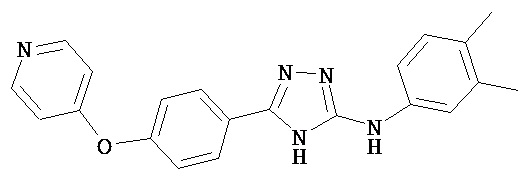 ,
,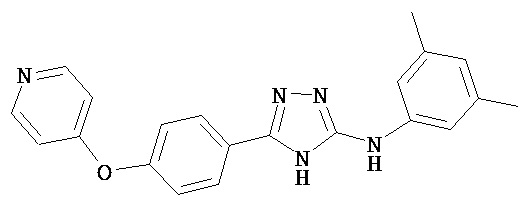 ,
, ,
,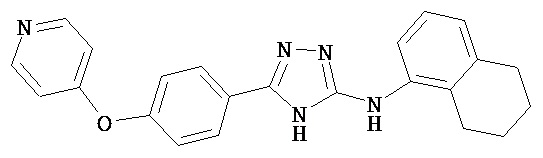 ,
, ,
, ,
, ,
, ,
,
 ,
, ,
, ,
, ,
,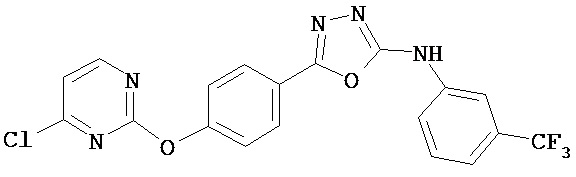 ,
, ,
, ,
, ,
, ,
, ,
, ,
,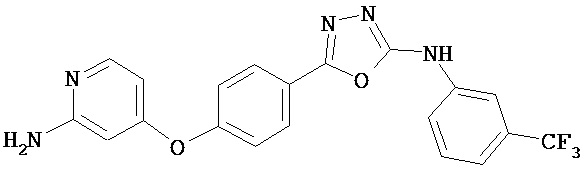 ,
, ,
, ,
, ,
,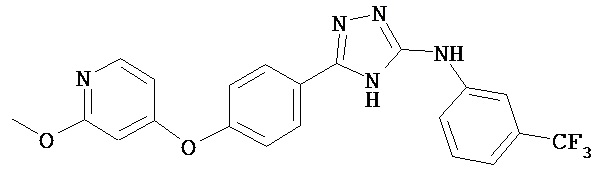 ,
,
 ,
, ,
,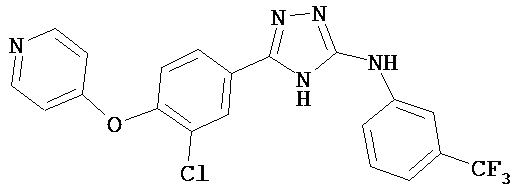 ,
, ,
, ,
, ,
, ,
,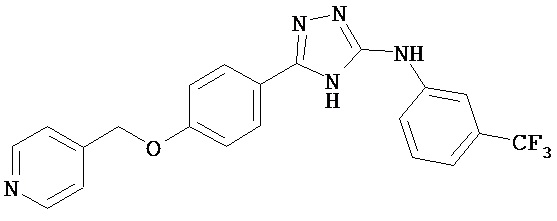 ,
, ,
, ,
, ,
,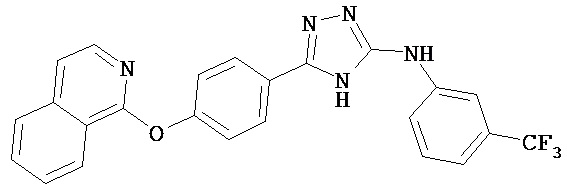 ,
, ,
,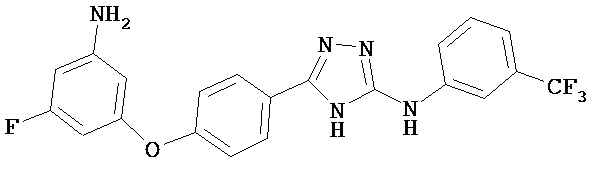 ,
,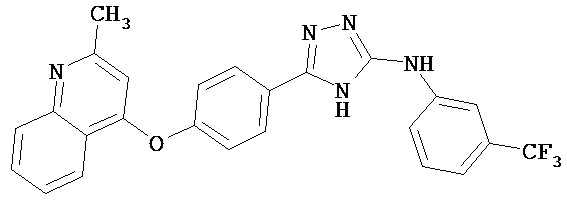 ,
, ,
, ,
,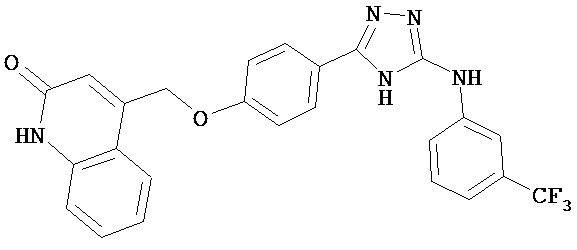 ,
,
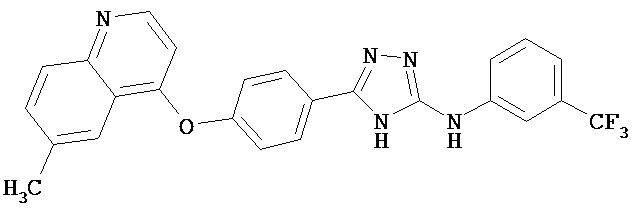 ,
, ,
, ,
, ,
, ,
,  ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
,
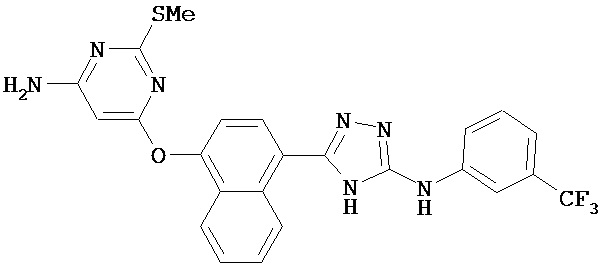 ,
, ,
,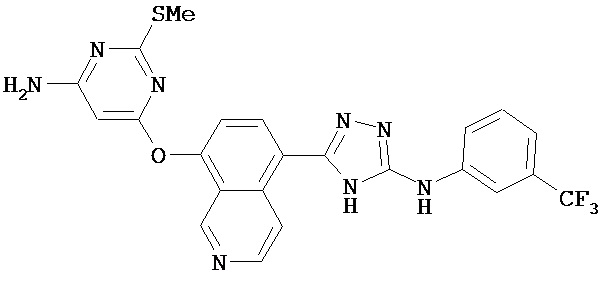 ,.
,. ,
, ,
,
 ,
, , и им подобных.
, и им подобных.
В некоторых вариантах предложены соединения, имеющие структуру (I), выбранные из группы, состоящей из:
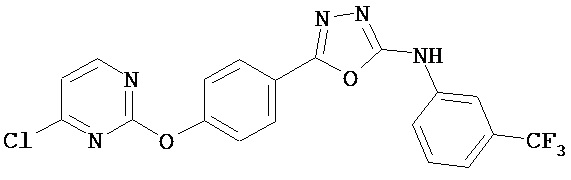 ,
, ,
, ,
, ,
,
 ,
, ,
, ,
, ,
, ,
, , и
, и
В некоторых вариантах предложены соединения, имеющие структуру (I), выбранные из группы, состоящей из:
 ,
, ,
, ,
, ,
, ,
, ,
, ,
,
 ,
, ,
, , и им подобных.
, и им подобных.
В некоторых вариантах предложено соединение, имеющее структуру (II), или его N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль:

в которой:
каждый из Z1 и Z2 независимо выбран из группы, состоящей из CH, N и NR5, где R5 представляет собой водород или низший алкил;
Z3 представляет собой O, S, N или NR5, где R5 представляет собой водород или низший алкил;
каждый R2 и R3 независимо выбран из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, необязательно замещенного C3-C12циклоалкила, необязательно замещенного C3-C10гетероцикла, содержащего 1-3 гетероатома, необязательно замещенного C6-C12арила, необязательно замещенного C3-C12гетероарила, содержащего 1-3 гетероатома, CF3, галогена, CN, CONHR6 и CO2R’, где R’ представляет собой водород или C1-C6алкил; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла;
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, NO2, -CN, C1-C6алкокси, -NHSO2R6, -SO2NHR6, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, CO2R6, -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила; n равен 1 или 2; и
R8 и R9 независимо выбраны из группы, состоящей из водорода, галогена, необязательно замещенного C1-C6алкила, -CF3, -OH, необязательно замещенного C1-C6 алкокси, -NR10R11 и -SOmR12, где R10 и R11 независимо выбраны из группы, состоящей из водорода, необязательно замещенного C1-C6алкила, -SO2R12, -S(O)R12 и -COR12, и R12 представляет собой необязательно замещенный алкил или необязательно замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, и m равен 0-2.
В некоторых вариантах предложены соединения, имеющие структуру (II), в которой каждый R2 и R3 независимо выбран из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, -CF3, галогена, -CN и -CO2R’, где R’ представляет собой водород или C1-C6алкил; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла. В некоторых вариантах R4 представляет собой водород. В некоторых вариантах R8 и R9 независимо выбраны из группы, состоящей из необязательно замещенного C1-C6алкокси, -NR10R11 и -SOmR12, и m равен 0-2. В определенных вариантах R8 представляет собой C1-C6алкокси или -SR12. В некоторых вариантах каждый R2 и R3 независимо выбран из группы, состоящей из C1-C6алкила, -CF3 и галогена, где p равен 0 или 1, или 2; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла.
В другом варианте предложено соединение структуры (II), в которой R2 и R3 независимо выбраны из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, -CF3, галогена и -CO2R’, где R’ представляет собой водород или C1-C6алкил.
В определенных вариантах соединение, имеющее структуру (II), выбрано из группы, состоящей из:
 ,
, ,
, ,
, ,
, ,
,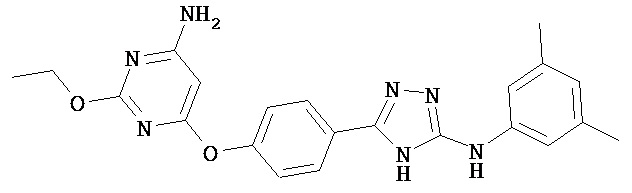 ,
,
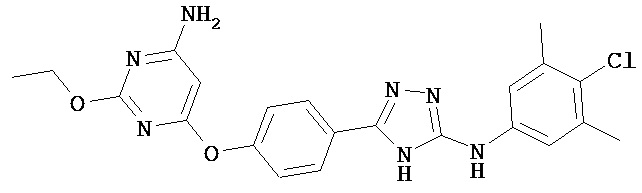 ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
,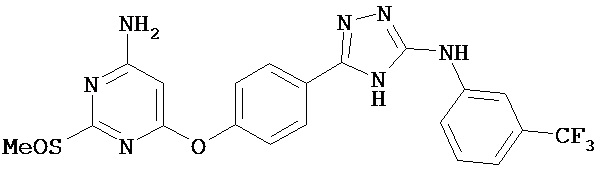 ,
, ,
, ,
, ,
, ,
,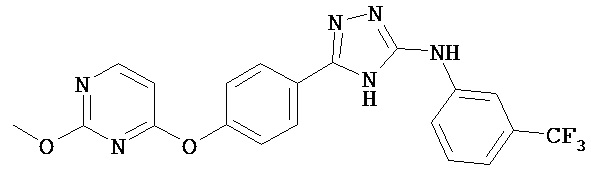 ,
, ,
,
 ,
,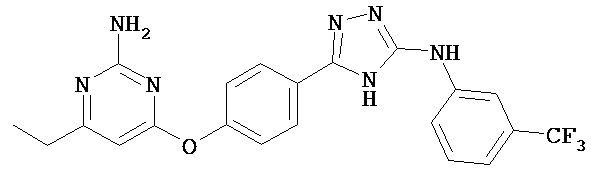 ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
,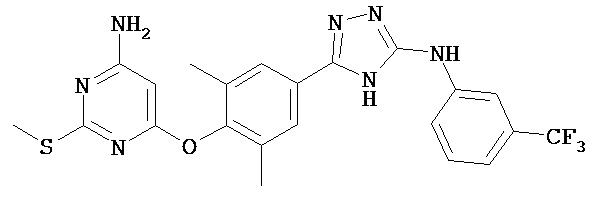 ,
, ,
, ,
, ,
, ,
, ,
, ,
,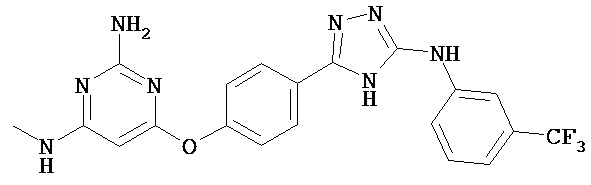 ,
,
 ,
, ,
, ,
, ,
,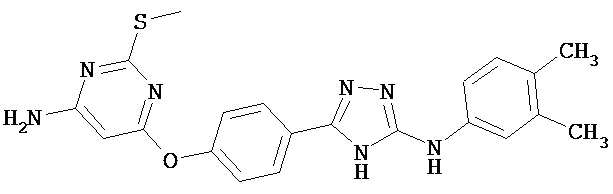 ,
, ,
, ,
, ,
, ,
,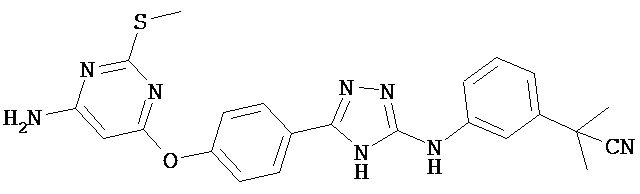 ,
,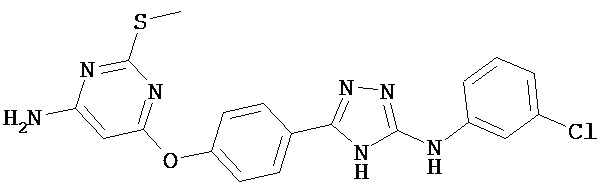 ,
, ,
, ,
, ,
, ,
, ,
,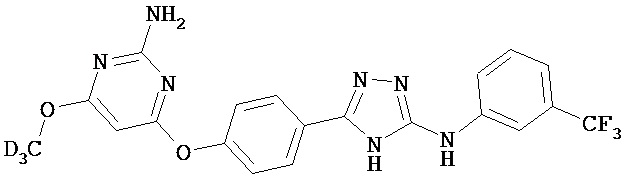 ,
, ,
,
 ,
, ,
, ,
,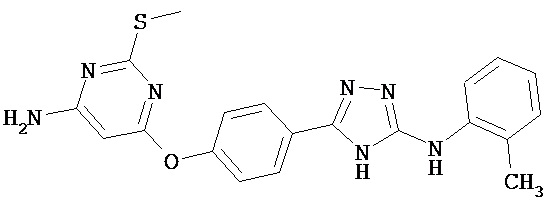 ,
, ,
, ,
, ,
, ,
, , и им подобных.
, и им подобных.
В некоторых вариантах предложены соединения, имеющие структуру (II), выбранные из группы, состоящей из:
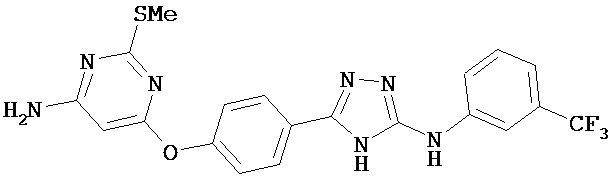 ,
, ,
,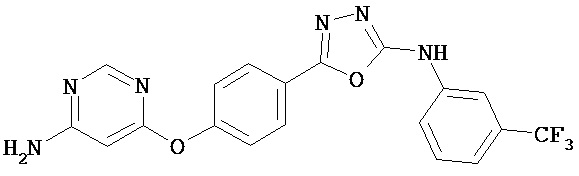 , и им подобных.
, и им подобных.
В некоторых вариантах предложены соединения, имеющие структуру (II), выбранные из группы, состоящей из:
 ,
, ,
, , и им подобных.
, и им подобных.
В других вариантах предложено соединение, имеющее структуру (III), или его N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль:
 ,
,
в которой:
каждый из Z1 и Z2 независимо выбран из группы, состоящей из CH, N и NR5, где R5 представляет собой водород или низший алкил; и
Z3 представляет собой O, S, N или NR5, где R5 представляет собой водород или низший алкил;
R1 представляет собой незамещенный или замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, или алкил, замещенный незамещенным или замещенным C3-C12гетероарилом, содержащим 1-3 гетероатома;
каждый R2 и R3 независимо выбран из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, необязательно замещенного C3-C12циклоалкила, необязательно замещенного C3-C10гетероцикла, содержащего 1-3 гетероатома, необязательно замещенного C6-C12арила, необязательно замещенного C3-C12гетероарила, содержащего 1-3 гетероатома, CF3, галогена, CN, CONHR6 и CO2R’, где R’ представляет собой водород или C1-C6алкил; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла;
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, NO2, -CN, C1-C6алкокси, -NHSO2R6, -SO2NHR6, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, CO2R6, -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила; p=0-4; и n равен 1 или 2.
В некоторых вариантах соединения имеют структуру (III), в которой Z3 представляет собой О или S. В некоторых вариантах каждый R2 и R3 независимо выбран из группы, состоящей из C1-C6алкила, -CF3 и галогена, где p равен 0 или 1, или 2; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла. В некоторых вариантах R1 представляет собой незамещенный или замещенный C3-C12гетероарил, содержащий 1-3 гетероатома. Например, R1 представляет собой замещенный или незамещенный пиридин. В определенных вариантах R1 представляет собой незамещенный пиридин или C1-C6алкил-замещенный пиридин. В других вариантах R1 представляет собой незамещенный или замещенный пиримидин. В некоторых вариантах предложено соединение, имеющее структуру (III), где R4 представляет собой водород.
В другом варианте предложено соединение, имеющее структуру формулы (III), в которой:
R2 и R3 независимо выбраны из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, -CF3, галогена, -CN и -CO2R’, где R’ представляет собой водород или C1-C6алкил; и
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, -NO2, -CN, C1-C6алкокси, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, -CO2R6 и -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила, и n равен 1 или 2. В некоторых вариантах R2 и R3 независимо выбраны из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, -CF3, галогена, -CN и -CO2R’, где R’ представляет собой водород или C1-C6алкил; и R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, -NO2, -CN, C1-C6алкокси, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, S(O)R6, -CO2R6 и -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила.
В определенных вариантах соединение, имеющее структуру (III), выбрано из группы, состоящей из:
 ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
,
 ,
, ,
, ,
, ,
,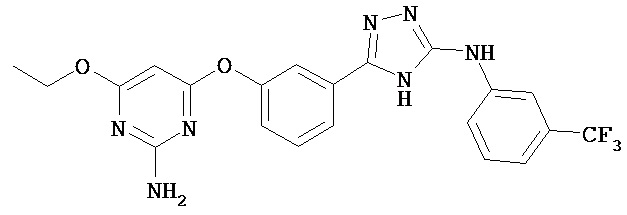 ,
,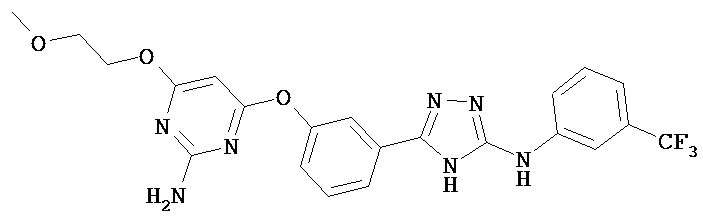 ,
,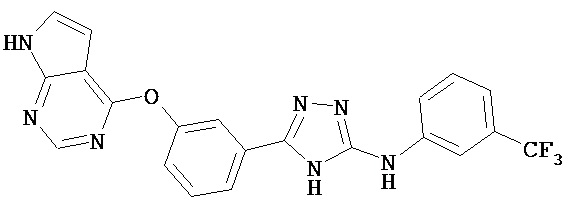 ,
, ,
,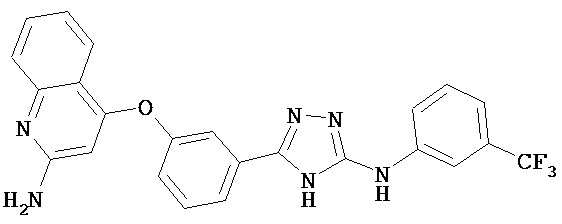 ,
, ,
, ,
,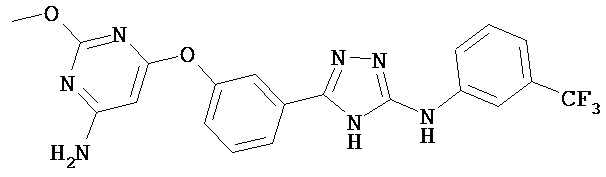 ,
, ,
, ,
, ,
,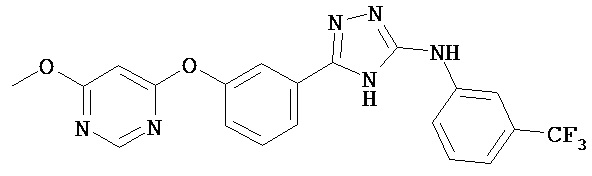 ,
, ,
, ,
,
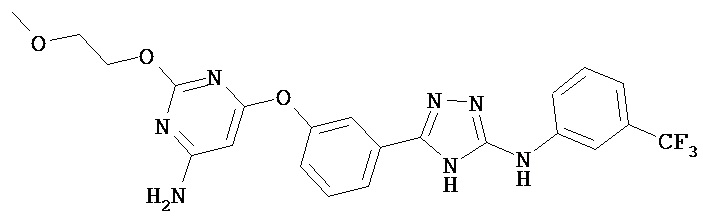 ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
,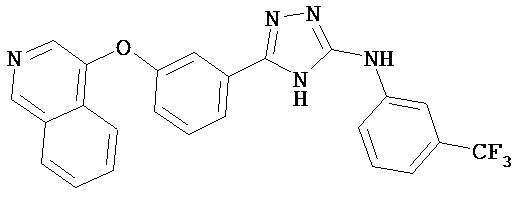 ,
, ,
, ,
, ,
, ,
,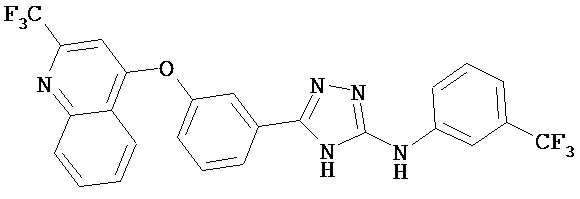 ,
, ,
, ,
,
 ,
,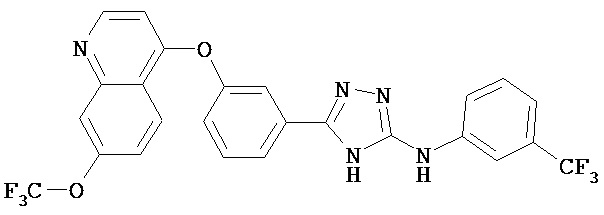 ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
,
 ,
,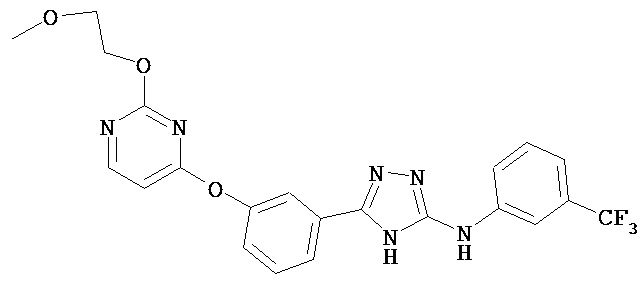 ,
,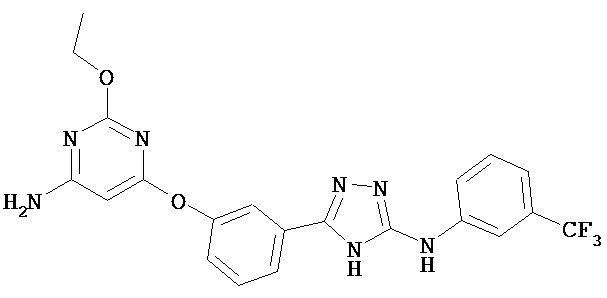 ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
,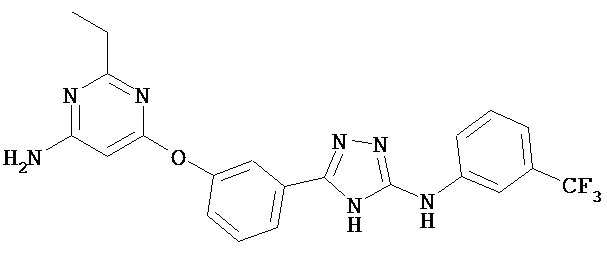 ,
,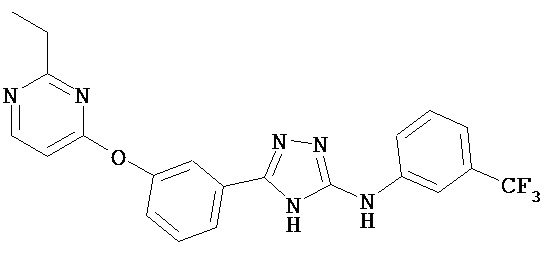 .
.
В некоторых вариантах соединение, имеющее структуру (III):
 ,
, ,
,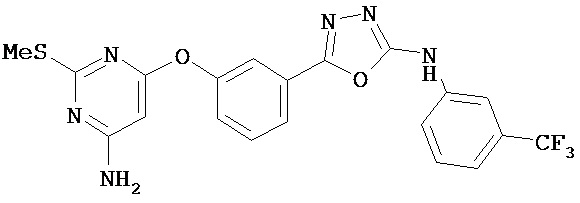 ,
, ,
, ,
, ,
, ,
,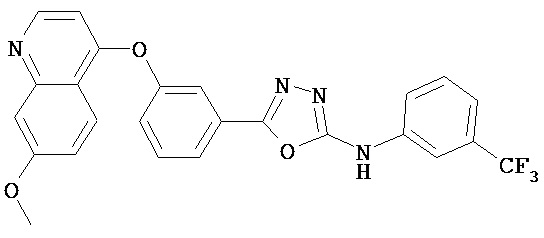 ,
,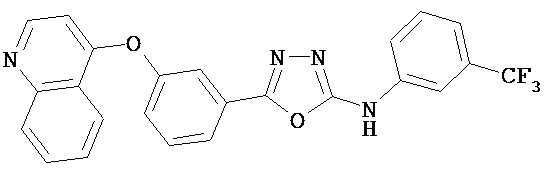 и
и  .
.
В некоторых вариантах предложено соединение, имеющее структуру (IV), или его N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль:

в которой:
каждый из Z1 и Z2 независимо выбран из группы, состоящей из CH, N и NR5, где R5 представляет собой водород или низший алкил;
Z3 представляет собой O, S или NR5, где R5 представляет собой водород или низший алкил;
R1 представляет собой незамещенный или замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, или алкил, замещенный незамещенным или замещенным C3-C12гетероарилом, содержащим 1-3 гетероатома;
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, NO2, -CN, C1-C6алкокси, -NHSO2R6, -SO2NHR6, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, CO2R6, -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила, и n равен 1 или 2; и
R13 представляет собой необязательно замещенный N-(C1-C6алкил)пиразолил или выбран из группы, состоящей из следующих структур:
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
, 
 ,
,  ,
,  .
.
В некоторых вариантах соединение имеет структуру (IV), в которой n равен 2. В некоторых вариантах Z3 представляет собой O или S. В определенных вариантах соединение, имеющее структуру (IV), выбрано из группы, состоящей из:
 ,
,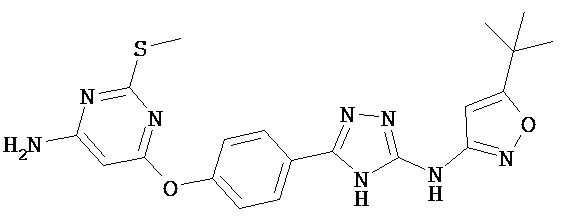 ,
, ,
, ,
, ,
, ,
, ,
,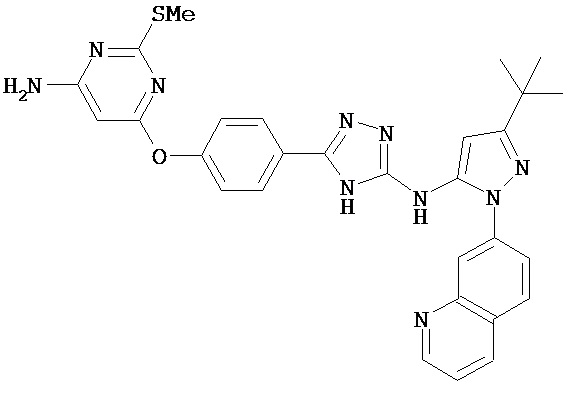 ,
, , и
, и 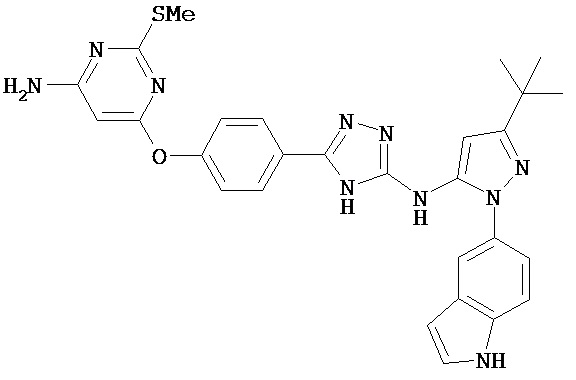 .
.
В других вариантах предложено соединение, имеющее структуру (V), или его N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемая соль:

в которой:
R1 представляет собой незамещенный или замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, или алкил, замещенный незамещенным или замещенным C3-C12гетероарилом, содержащим 1-3 гетероатома;
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, NO2, -CN, C1-C6алкокси, -NHSO2R6, -SO2NHR6, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, CO2R6 и -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила; n равен 1 или 2; и
R14 выбран из группы, состоящей из необязательно замещенного C1-C12алкила, необязательно замещенного C3-C12циклоалкила, необязательно замещенного C3-C10гетероцикла, содержащего 1-3 гетероатома, необязательно замещенного C6-C12арила и необязательно замещенного C3-C12гетероарила, содержащего 1-3 гетероатома.
В определенных вариантах соединение, имеющее структуру (V), выбрано из группы, состоящей из:
 ,
, ,
, ,
, ,
, ,
, ,
, и
и  .
.
Углеродно-водородная связь по природе является ковалентной химической связью. Такая связь образуется, когда два атома аналогичной электроотрицательности обобществляют некоторые из своих валентных электронов, создавая тем самым силу, которая удерживает атомы вместе. Эта сила или прочность связи может быть оценена количественно и выражена в единицах энергии, и соответственно, ковалентные связи между различными атомами могут быть классифицированы согласно тому, какое количество энергии должно применяться к связи для того, чтобы разорвать связь или разделить два атома.
Прочность связи прямо пропорциональна абсолютной величине колебательной энергии основного состояния связи. Эта колебательная энергия, которая также известна как колебательная энергия нулевой точки, зависит от массы атомов, которые образуют связь. Абсолютная величина колебательной энергии нулевой точки увеличивается по мере увеличения массы одного или обоих атомов, образующих связь. Так как масса дейтерия (D) в два раза больше массы водорода (H), следует, что связь C-D сильнее, чем соответствующая связь C-H. Соединения со связями C-D часто являются бесконечно стабильными в H2O, и их широко использовали в изотопных исследованиях. Если связь C-H нарушается на стадии определения скорости химической реакции (то есть на стадии с самой высокой энергией переходного состояния), то замена водорода на дейтерий будет вызывать снижение скорости реакции, и процесс будет замедляться. Это явление известно как кинетический изотопный эффект дейтерия (DKIE) и может изменяться примерно от 1 (никакого изотопного эффекта) до очень больших показателей, таких как 50 или выше, что означает, что реакция может протекать в пятьдесят или более раз медленнее, когда водород заменен на дейтерий. Большая величина DKIE может отчасти являться результатом явления, известного как туннелирование, которое является следствием принципа неопределенности. Туннелирование приписывается маленькому размеру атома водорода и происходит из-за того, что иногда переходные состояния, включающие протон, могут формироваться в отсутствие необходимой энергии активации. Молекула дейтерия крупнее и по статистике имеет намного меньшую вероятность подвергаться воздействию данного явления. Замена водорода на тритий приводит к образованию еще более сильной связи, чем при использовании дейтерия, и дает численно большие изотопные эффекты.
Дейтерий (D или 2H) является стабильным нерадиоактивным изотопом водорода и имеет молекулярную массу 2.0144. Природная распространенность дейтерия составляет 0.015%. Таким образом, во всех химических соединениях с атомом H, атом H фактически представляет смесь H и D, в которой примерно 0.015% составляет D. Обогащенные дейтерием соединения имеют молекулярную массу и/или размеры, отличные от их водородных аналогов. Дейтерирование фармацевтических продуктов для улучшения фармакокинетики (PK), фармакодинамики (PD) и профилей токсичности было продемонстрировано ранее применительно к нескольким классами лекарственных средств. Например, DKIE использовали для понижения гепатотоксичности галотана путем возможного ограничения выработки активных частиц, таких как хлорангидрид трифторуксусной кислоты.
В некоторых вариантах соединения изобретения, имеющие структуру с (I) по (V), являются обогащенными дейтерием путем замены, по меньшей мере, одного атома водорода на атом дейтерия. В другом варианте обогащение дейтерием составляет, по меньшей мере, примерно 1%.
В определенных вариантах соединения изобретения имеют структуры Ia-Va или представляют собой их N-оксид, N,N’-диоксид, N,N’,N’’-триоксид, или фармацевтически приемлемую соль:
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
в которой:
R’’ представляет собой H или D,
Q представляет собой O или S;
W представляет собой C6-C12арил или C3-C12гетероарил, содержащий 1-3 гетероатома;
каждый из X и Y независимо отсутствует или представляет собой NH;
каждый из Z1 и Z2 независимо выбран из группы, состоящей из CH, N и NR5, где R5 представляет собой водород или низший алкил;
Z3 представляет собой O, S или NR5, где R5 представляет собой водород или низший алкил;
R1 представляет собой незамещенный или замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, или алкил, замещенный незамещенным или замещенным C3-C12гетероарилом, содержащим 1-3 гетероатома;
каждый R2 и R3 независимо выбран из группы, состоящей из водорода, C1-C6алкокси, необязательно замещенного C1-C6алкила, необязательно замещенного C3-C12циклоалкила, необязательно замещенного C3-C10гетероцикла, содержащего 1-3 гетероатома, необязательно замещенного C6-C12арила, необязательно замещенного C3-C12гетероарила, содержащего 1-3 гетероатома, CF3, гелогена, CN, CONHR6 и CO2R’, где R’ представляет собой водород или C1-C6алкил; или, необязательно, R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла;
R4 независимо выбран из группы, состоящей из водорода, галогена, C1-C6алкила, -OH, NO2, -CN, C1-C6алкокси, -NHSO2R6, -SO2NHR6, -NHCOR6, -NH2, -NR6R7, -SR6, -S(O)R6, -S(O)2R6, CO2R6, -CONR6R7, где R6 и R7 независимо выбраны из группы, состоящей из водорода и необязательно замещенного C1-C6алкила; и n равен 1 или 2;
R8 и R9 независимо выбраны из группы, состоящей из водорода, галогена, необязательно замещенного C1-C6алкила, -CF3, -OH, необязательно замещенного C1-C6алкокси, -NR10R11 и -SOmR12, где R10 и R11 независимо выбраны из группы, состоящей из водорода, необязательно замещенного C1-C6алкила, -SO2R12, -S(O)R12 и -COR12, и R12 представляет собой необязательно замещенный алкил или необязательно замещенный C3-C12гетероарил, содержащий 1-3 гетероатома, и m равен 0-2;
R13 представляет собой необязательно замещенный N-(C1-C6алкил)пиразолил или выбран из группы, состоящей из следующих структур:
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
, 
 ,
,  ,
,  ;
;
R14 выбран из группы, состоящей из необязательно замещенного C1-C12алкила, необязательно замещенного C3-C12циклоалкила, необязательно замещенного C3-C10гетероцикла, содержащего 1-3 гетероатома, необязательно замещенного C6-C12арила и необязательно замещенного C3-C12гетероарила, содержащего 1-3 гетероатома; и, по меньшей мере, один атом водорода соединения заменен на атом дейтерия.
В определенных вариантах соединение выбрано из группы, состоящей из:
 ,
, ,
, ,
, ,
, ,
, ,
, , и
, и 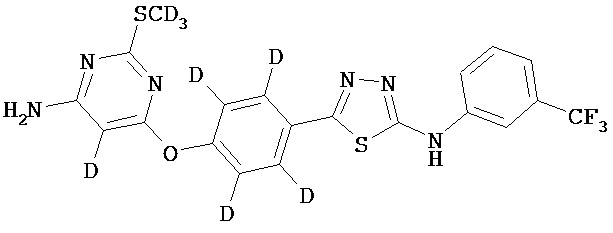 .
.
В некоторых вариантах предложены фармацевтические композиции, содержащие соединение, имеющее структуру (I)-(V) или (Ia)-(Va), в фармацевтически приемлемом носителе.
В других вариантах предложены фармацевтические композиции, содержащие соединение, имеющее структуру (I)-(V) или (Ia)-(Va), и фармацевтически приемлемое вспомогательное вещество.
В некоторых вариантах предложены способы супрессии, предупреждения или ингибирования лимфоангиогенеза, ангиогенеза и/или роста опухоли. Способы включают контактирование опухоли с соединением структур I-V, Ia-Va или фармацевтической композицией, содержащей соединение структур I-V или Ia-Va.
Благодаря гидрофобным взаимодействиям и специфическому водородному связыванию, необходимому для ингибирования II типа, аллостерический центр, примыкающий к активному центру киназы, может быть использован для улучшения специфичности по сравнению с ингибиторами I типа, которые взаимодействуют только с активной конформацией киназы в высококонсервативном шарнирном участке. В определенных вариантах соединение, предложенное здесь, представляет собой селективный ингибитор II типа рецептора PDGF или RAF-киназы. В определенных вариантах соединение, предложенное здесь, представляет собой аллостерический ингибитор PDGFRα, PDGFRβ, Flt3, A-RAF, B-RAF, C-RAF и/или c-Kit.
Примеры режимов введения доз и схем лечения
В одном аспекте композиции, содержащие соединения структур I-V или Ia-Va, вводят для профилактического и/или терапевтического лечения. В терапевтических применениях композиции вводят субъекту-человеку (пациенту), уже страдающему заболеванием, нарушением или состоянием, в количестве, достаточном для излечения или, по меньшей мере, частичного купирования симптомов заболевания, нарушения или состояния. Количества, эффективные для этого применения, будут зависеть от тяжести и течения заболевания, нарушения или состояния, предшествующей терапии, состояния здоровья пациента, массы тела и ответа на лекарственные средства, и заключения лечащего врача.
В профилактических применениях композиции, содержащие соединения структур I-V или Ia-Va, вводят пациенту, восприимчивому или иным образом имеющему риск развития конкретного заболевания, нарушения или состояния. Такое количество определено как «профилактически эффективное количество или доза». В этом применении точные количества также зависят от состояния здоровья пациента, массы тела, и тому подобного. В некоторых вариантах при применении у пациента эффективные количества для такого применения зависят от тяжести и течения заболевания, нарушения или состояния, предшествующей терапии, состояния здоровья пациента, массы тела и ответа на лекарственные средства, и заключения лечащего врача.
В некоторых вариантах, в случае отсутствия улучшения состояния пациента по усмотрению врача введение соединений структур I-V или Ia-Va осуществляют длительно, то есть в течение длительного периода времени, включая продолжительность жизни пациента, для улучшения или иного контроля, или ограничения симптомов заболевания, нарушения или состояния у пациента.
В некоторых вариантах, когда состояние пациента улучшается, по усмотрению врача введение соединений структур I-V или Ia-Va осуществляют непрерывно; альтернативно, дозу вводимого лекарственного средства временно снижают или временно прекращают на некоторый промежуток времени (то есть «лекарственные каникулы»). В других вариантах продолжительность лекарственных каникул варьирует от 2 суток до 1 года, включая, в качестве примера только, около 2 суток, около 4 суток, около 5 суток, около 6 суток, около 7 суток, около 10 суток, около 12 суток, около 15 суток, около 20 суток, около 28 суток, около 35 суток, около 50 суток, около 70 суток, около 100 суток, около 120 суток, около 150 суток, около 180 суток, около 200 суток, около 250 суток, около 280 суток, около 300 суток, около 320 суток, около 350 суток, или около 365 суток. В дополнительных вариантах снижение дозы во время лекарственных каникул составляет примерно от 10% до 100%, включая, в качестве примера только, примерно 10%, примерно 15%, примерно 20%, примерно 25%, примерно 30%, примерно 35%, примерно 40%, примерно 45%, примерно 50%, примерно 55%, примерно 60%, примерно 65%, примерно 70%, примерно 75%, примерно 80%, примерно 85%, примерно 90%, примерно 95%, или примерно 100%.
При улучшении состояния пациента вводят поддерживающую дозу при необходимости. Впоследствии, в других вариантах, дозу или частоту введения, или и то и другое, снижают как функцию симптомов до уровня, при котором сохраняется улучшение заболевания, нарушения или состояния. Тем не менее, в дополнительных вариантах пациентам потребуется длительная интермиттирующая терапия при повторном возникновении симптомов.
В других вариантах количество вводимого агента, которое соответствует такому количеству, изменяется в зависимости от факторов, таких как конкретное соединение, заболевание, нарушение или состояние и его тяжесть, индивидуальные параметры (например, масса тела) субъекта или хозяина, нуждающегося в лечении, но, тем не менее, легко определяется в соответствии с конкретными обстоятельствами случая, включая, например, конкретный вводимый агент, способ введения, состояние, по поводу которого проводят лечение, и субъекта или хозяина, проходящего лечение. В некоторых вариантах, тем не менее, дозы, применяемые для лечения взрослого человека, как правило, находятся в диапазоне примерно от 0.02 до примерно 5000 мг в сутки или примерно от 1 до примерно 1500 мг в сутки. В дополнительных вариантах желаемая доза подходящим образом представлена в виде однократной дозы или в виде разделенных доз, вводимых одновременно (или в течение короткого периода времени), или с соответствующими интервалами, например, в виде двух, трех, четырех или более суб-доз в сутки.
В некоторых вариантах фармацевтические композиции, описанные здесь, представлены в виде стандартных лекарственных форм, подходящих для однократного введения точно рассчитанных доз. В стандартной лекарственной форме препарат разделен на стандартные дозы, содержащие подходящие количества одного или нескольких соединений. В других вариантах стандартная доза представлена в форме упаковки, содержащей дискретные количества препарата. Неограничивающими примерами являются упакованные таблетки или капсулы, и порошки во флаконах или ампулах. В другом варианте композиции на основе водных суспензий упакованы в не поддающиеся повторной герметизации контейнеры на одну дозу. В дополнительных вариантах используются поддающиеся повторной герметизации контейнеры на множество доз, и в этом случае в композицию обычно включают консервант. Исключительно в качестве примера, препараты для парентеральной инъекции представлены в стандартной лекарственной форме, которая включает, но без ограничения, ампулы или контейнеры на множество доз с добавленным консервантом.
Суточные дозы, подходящие для соединений структур I-V или Ia-Va, описанных здесь, составляют примерно от 0.01 до примерно 200 мг/кг массы тела. Указанная суточная доза у крупного млекопитающего, включая, но без ограничения, людей, находится в диапазоне от примерно 0.5 мг до примерно 2000 мг, и ее подходящим образом вводят в виде разделенных доз, включая, но без ограничения, до четырех раз в сутки или в форме с пролонгированным высвобождением. Подходящие стандартные лекарственные формы для перорального введения содержат примерно от 1 до 200 мг активного ингредиента. Вышеуказанные диапазоны являются всего лишь иллюстративными, поскольку число переменных в отношении индивидуальной схемы лечения велико, и значительные отклонения от этих рекомендуемых величин не являются редкими. В дополнительных вариантах такие дозы изменяются в зависимости от числа переменных, не ограничивающихся активностью используемого соединения, заболеванием, нарушением или состоянием, подлежащим лечению, и заключения лечащего врача.
В еще других вариантах токсичность и терапевтическая эффективность таких схем лечения определяется стандартными фармацевтическими способами на клеточных культурах или экспериментальных животных, включая, но без ограничения, определение средней летальной дозы LD50 (дозы, летальной для 50% популяции) и средней эффективной дозы ED50 (дозы, терапевтически эффективной у 50% популяции). Соотношение доз между токсическими и терапевтическими эффектами представляет собой терапевтический индекс и в некоторых вариантах выражено как соотношение между LD50 и ED50. В других вариантах данные, полученные в анализах на клеточных культурах и исследованиях на животных, используются в определении диапазона доз для применения у человека. В некоторых вариантах доза таких соединений обычно лежит в диапазоне концентраций в циркулирующей крови, включающей ED50 с минимальной токсичностью. В еще других вариантах доза изменяется в пределах этого диапазона в зависимости от используемой лекарственной формы и используемого способа введения.
В некоторых вариантах предложены способы лечения рака, рестеноза, гиперплазии интимы, фиброзирующих заболеваний или расстройств, связанных с ангиогенезом, у пациента-человека. Способы включают введение пациенту, нуждающемуся в этом, соединения структур I-V или Ia-Va, или фармацевтической композиции, содержащей соединение структур I-V или Ia-Va. В определенных вариантах соединение представляет собой аллостерический ингибитор PDGFRα, PDGFRβ, Flt3, A-RAF, B-RAF, C-RAF и/или c-Kit. В другом варианте соединение ингибирует гетеродимеризацию B-RAF с C-RAF или C-RAF с C-RAF. В определенных вариантах соединение представляет собой селективный ингибитор II типа рецептора PDGF или RAF-киназы.
В определенных вариантах рак является резистентным, рефракторным или невосприимчивым к ингибитору I типа протеинкиназы. В определенных вариантах рак является резистентным, рефракторным или невосприимчивым к лекарственному средству с активностью в отношении пан-RAF-киназы или ATP-конкурентного ингибитора. В определенных вариантах рак является резистентным, рефракторным или невосприимчивым к лекарственному средству, выбранному из сорафениба, PLX4032, XL281, RAF265, 885-A, ZM336372, L-779450, AZ628, AAL881, LBT613, MCP110, 17-DMAG, CI1040, AZD6244/ARRY142886, PD0325901, SB590885, DP3346 и DP2514. В определенных вариантах рак является резистентным, рефракторным или невосприимчивым к VEGF-направленной терапии. В определенных вариантах рак ассоциирован с мутантной формой RAF-киназы; мутантная форма RAF-киназы может представлять собой B-RAF-киназу, выбранную из мутантнов T529I, T529N, G464A, G464E, G464V, G466A, G466E, G466V, G469A, G469E, N581S, E586K, F595L, G596R, L597V, L597R, T599I, V600E и K601E; альтернативно, мутантная форма RAF-киназы представляет собой мутант гена-привратние C-RAF, выбранный из T421N и T421I. В определенных вариантах рак выбран из меланомы, рака молочной железы, колоректального рака, рака поджелудочной железы, рака легкого, рака почки и колоректального рака. Рак может характеризоваться опухолями, богатыми стромой. В определенных вариантах рак имеет мутацию или аберрацию, выбранную из N-RAS, H-RAS, K-RAS, B-RAF(V600E), B-RAF/Ras, HER1, р53, PTEN и PI3K. В определенных вариантах рак проявляет активацию сигнального пути RAF-MEK-ERK. В другом варианте соединение структур I-V или Ia-Va вводят перорально пациенту, нуждающемуся в этом. В другом варианте субъект-человек получает терапию, выбранную из антиангиогенной терапии, молекулярно-направленной терапии (такой как терапии, направленные на другие киназы (например, EGFR, HER2, HER4, MEK, VEGFR, с-MET, PI3K, AKT и др.)). химиотерапии или лучевой терапии. В другом варианте, ответ субъекта-человека на соединение контролируют по ингибированию фосфорилирования S338 C-RAF.
В некоторых вариантах виды рака, которые можно лечить способами, предложенными здесь, включают, но без ограничения: Кардиальный: саркома (ангиосаркома, фибросаркома, рабдомиосаркома, липосаркома), миксома, рабдомиома, фиброма, липома и тератома; Легочный: бронхогенный рак (плоскоклеточный, недифференцированный мелкоклеточный, немелкоклеточный, недифференцированный крупноклеточный, аденокарцинома), альвеолярная (бронхиолярная) карцинома, аденома бронха, саркома, лимфома, хондроматозная гамартома, мезотелиома; Желудочно-кишечный: пищевода (плоскоклеточная карцинома, аденокарцинома, лейомиосаркома, лимфома), желудока (карцинома, лимфома, лейомиосаркома, стромальная), поджелудочной железы (аденокарцинома протока, инсулинома, глюкагонома, гастринома, карциноидные опухоли, ВИПома), тонкой кишки или тонкого кишечника (аденокарцинома, лимфома, карциноидные опухоли, саркома Капоши, лейомиома, гемангиома, липома, нейрофиброма, фиброма), толстой кишки или толстого кишечника (аденокарцинома, тубулярная аденома, ворсинчатая аденома, гамартома, лейомиома); Мочеполовой системы: почек (аденокарцинома, опухоль Вильмса [аденосаркома почки], лимфома, лейкоз), мочевого пузыря и мочеиспускательного канала (плоскоклеточная карцинома, переходно-клеточная карцинома, аденокарцинома), предстательной железы (аденокарцинома, саркома), яичка (семинома, тератома, эмбриональная карцинома, тератокарцинома, хориокарцинома, саркома, интерстициально-клеточная карцинома, фиброма, фиброаденома, аденоматоидные опухоли, липома); Печени: гепатома (гепатоцеллюлярная карцинома), холангиокарцинома, гепатобластома, ангиосаркома, гепатоцеллюлярная аденома, гемангиома; Кости: остеобластическая саркома (остеосаркома), фибросаркома, злокачественная фиброзная гистиоцитома, хондросаркома, саркома Юинга, злокачественная лимфома (ретикулоклеточная саркома), множественная миелома, злокачественная гигантоклеточная саркома, хордома, остеохронфрома (костно-хрящевые экзостозы), доброкачественная хондрома, хондробластома, хондромиксофиброма, остеоид-остеома и гигантоклеточные опухоли; Нервной системы: черепа (остеома, гемангиома, гранулема, ксантома, деформирующий остит), мягких оболочек мозга (менингиома, менингиосаркома, глиоматоз), мозга (астроцитома, медуллобластома, глиома, эпендимома, герминома [пинеалома], мультиформная глиома, олигодендроглиома, шваннома, ретинобластома, врожденные опухоли), спинного мозга (нейрофиброма, менингиома, глиома, саркома); Гинекологический: матки (карцинома эндометрия), шейки матки (карцинома шейки матки, доопухолевая цервикальная дисплазия); яичников (карцинома яичника [серозная цистаденокарцинома, мукоидная цистаденокарцинома, эндометриоидные опухоли, целиобластома, светло клеточная карцинома, неклассифицированная карцинома], гранулезотекаклеточные опухоли, опухоли из клеток Сертоли, дисгерминома, злокачественная тератома), женских наружных половых органов (плоскоклеточная карцинома, внутриэпителиальная карцинома, аденокарцинома, фибросаркома, меланома), влагалища (светлоклеточная кацинома, плоскоклеточная карцинома, ботриоидная саркома [эмбриональная рабдомиосаркома], фаллопиевых труб (карцинома); Гематологический: крови (миелоидный лейкоз [острый и хронический], острый лифобластный лейкоз, хронический лимфоцитарный лейкоз, миелопролиферативные заболевания, множественная миелома, миелодиспластический синдром), болезнь Ходжкина, неходжкинская лимфома [злокачественная лимфома]; Кожи: злокачественная меланома, базально-клеточная карцинома, плоскоклеточная карцинома, саркома Капоши, кератоакантома, диспластическая невоидная опухоль, липома, ангиома, дерматофиброма, келоиды, псориаз; и Надпочечников: нейробластома.
В некоторых вариантах острый миелоцитарный лейкоз (AML) и/или острый лимфоцитарный лейкоз (ALL) лечат с использованием соединений структур I-V или Ia-Va в монотерапии или комбинированной терапии.
Рестеноз в буквальном смысле означает повторное возникновение стеноза, сужения кровеносных сосудов, приводящее к ограниченному потоку крови. Рестеноз обычно относится к артерии или другому крупному кровеносному сосуду, который стал суженным, подвергался лечению для очистки закупорки и в дальнейшем снова стал суженным. Это, как правило, представляет собой рестеноз артерии или другого кровеносного сосуда, или возможно сосуда внутри органа. Рестеноз обычно происходит в результате баллонной агниопластики и/или замены стента, что приводит к случайной закупорке артерий в результате процесса, описанного как новообразованная гиперплазия (NIH). После повреждения артерии возникает чрезмерная пролиферация васкулярных гладкомышечных клеток, которая, как было показано ранее, зависит от обоих, PDGFRα/β (Englesbe et al. (2004) J Vase Surg 39, 440-6) и пути активации MAPK (Li, et al. (2005) Circulation 111, 1672-8; Pintucci, et al. (2006) Faseb J 20, 398-400). Таким образом, комбинация ингибирования PDGFRβ/B-RAF будет являться оптимальным лечением для NIH. Представленные здесь соединения структур I-V или Ia-Va могут быть выбранными ингибиторами PDGFRβ/B-RAF. В определенных вариантах рестеноз согласно способам изобретения представляет собой стимулированный гиперплазией интимы рестеноз после васкулярного повреждения.
Термины «фиброз» или «фиброзирующее нарушение», используемые здесь, относятся к состояниям, которые ассоциированы с ненормальным накоплением клеток и/или фибронектина, и/или коллагена, и/или увеличенным рекрутингом фибробластов, и включают, но без ограничения, фиброз отдельных органов или тканей, таких как сердце, почки, печень, суставы, легкое, ткань плевры, перитонеальную ткань, кожу, роговую оболочку глаза, сетчатку, костно-мышечную систему и желудочно-кишечный тракт.
Примеры заболеваний, нарушений или состояний, в которые вовлечен фиброз, включают, но без ограничения: Заболевания легких, ассоциированные с фиброзом, например, идиопатический легочный фиброз, вторичный легочный фиброз вследствие системного воспалительного заболевания, такой как ревматоидный артрит, склеродерма, волчанка, криптогенный фиброзирующий альвеолит, фиброз, вызванный облучением, хронические обструктивные болезни легких (COPD), склеродерма, хроническая астма, силикоз, индуцированный асбестом легочный или плевральный фиброз, острое повреждение легких и острый респираторный дистресс-синдром (включая вызванный бактериальной пневмонией, вызванный травмой, вызванный вирусной пневмонией, вызванный респиратором, вызванный внелегочным сепсисом, и вызванный аспирацией); Хроническую нефропатию, ассоциированную с повреждением/фиброзом (фиброзом почек), например, вторичный гломерулонефрит вследствие системных воспалительных заболеваний, таких как волчанка и склеродерма, диабет, гломерулярный нефрит, фокальный сегментарный гломерулярный склероз, IgA-нефропатия, гипертензия, аллографт и синдром Альпорта; Фиброз кишки, например, склеродерма и вызванный облучением фиброз кишки; Фиброз печени, например, цирроз, вызванный алкоголем фиброз печени, неалкогольный стеатогепатит (NASH), повреждение желчного протока, билиарный первичный цирроз печени, фиброз печени, вызванный инфекцией или вирусом (например, хроническая HCV инфекция), и аутоиммунный гепатит; Фиброз головы и шеи, например, вызванный радиацией; Корнеальное рубцевание, например, LASIK (лазерная кератопластика in situ), корнеальный трансплантат и трабекулэктомия; Гипертрофическое рубцевание и келоиды, например, индуцированное ожогом или хирургическое; и Другие фиброзирующие болезни, например, саркоидоз, склеродерма, повреждение спинного мозга/фиброз, миелофиброз, сосудистый рестеноз, атеросклероз, артериосклероз, грануломатоз Вегенера, смешанное заболевание соединительной ткани и болезнь Пейрони. В определенных вариантах фиброз в соответствии со способами изобретения представляет собой фиброз легких или фиброз печени.
В одном варианте соединения структур I-V или Ia-Va вводят субъекту-человеку, имеющему фиброз органа или ткани, или предрасположенному к развитию фиброза органа или ткани, с одним или несколькими другими агентами, которые применяют для лечения фиброза. В одном аспекте один или несколько агентов включают кортикостероиды. В другом аспекте один или несколько агентов включают иммунодепрессанты. В одном аспекте один или несколько агентов включают B-клеточные антагонисты. В другом аспекте один или несколько агентов включают утероглобин.
В определенных вариантах предложены способы предупреждения ингибирования ASK1-опосредованного апоптоза в клетке, сенсибилизации клетки экзогенному стрессу или ингибирования MEK1/2- и/или ERK1/2-опосредованной клеточной пролиферации или миграции. Способы включают контактирование опухоли с соединением структур I-V или Ia-Va, или фармацевтической композицией, содержащей соединение структур I-V или Ia-Va.
Киназа RAF является важной конвергентной точкой на пути передачи сигнала FGFR и VEGFR2 в эндотелиальных клетках и играет ключевую роль в выживании эндотелиальных клеток во время ангиогенеза. Стромальный компартмент вносит важный вклад в ангиогенез и рост опухоли. Это включает перициты, ассоциированные с вновь образованным эндотелием, которые стабилизируют васкулатуру и способствуют васкуляризации. PDGFRβ представляет собой тирозинкиназный рецептор (RTK), который является важным для развития надлежащей функции перицитов, связанной со стабилизацией кровеносных сосудов и созреванием сосудов. Передача сигнала PDGFRβ усиливает рекрутинг перицитов во вновь образующиеся сосуды и секрецию проангиогенных молекул, таких как VEGFA, FGF2 и Ang1 в локальном микроокружении. Это способствует стабилизации сосудов и ремоделированию незрелой сосудистой сети в высокоорганизованную сеть. Поддержание сосудистого компартмента зависит от паракринных петель, таких как секреция PDGF-BB и FGF2, что приводит к повышенной экспрессии FGFR1 на VSMCs, и PDGFRα/β на ECs, соответственно. Таким образом, гомеостаз муральных и сосудистых компартментов является ключевым для эффективного ангиогенеза. Такое ингибирование этих двух компартментов одновременно будет инициировать возможное ингибирование ангиогенеза.
В определенных вариантах соединение представляет собой аллостерический ингибитор PDGFRα, PDGFRβ, Flt3, A-RAF, B-RAF, C-RAF и/или c-Kit. В другом варианте соединение ингибирует гетеродимеризацию B-RAF с C-RAF или C-RAF с С-RAF. В определенных вариантах соединение представляет собой селективный ингибитор II типа рецептора PDGF или киназы B-RAF. В определенных вариантах экзогенный стресс выбран из гипоксии, химиотерапии, радиационной терапии или глюкозного/питательного голодания. В определенных вариантах соединение структур I-V или Ia-Va согласно способам изобретения блокирует VEGF- и/или FGF-стимулированные реакции эндотелия в ангиогенезе опухоли.
В некоторых вариантах предложены способы ингибирования протеинкиназы, включающие контактирование протеинкиназы с ингибирующей концентрацией соединения структур I-V или Ia-Va, или фармацевтической композицией, содержащей соединение структур I-V или Ia-Va.
Некоторая фармацевтическая и медицинская терминология
Термин «приемлемый» в отношении препарата, композиции или ингредиента, используемый здесь, означает не имеющий стойкого неблагоприятного воздействия на общее состояние здоровья субъекта, проходящего лечение.
Термин «антагонист», используемый здесь, относится к молекуле, такой как соединение, которая ослабляет, ингибирует или предупреждает действие другой молекулы или активность рецепторного сайта. Антагонисты включают, но без ограничения, конкурентные антагонисты, неконкурентные антагонисты, внеконкурентные антагонисты, частичные агонисты и обратные агонисты.
Конкурентные антагонисты обратимо связываются с рецепторами в том же сайте связывания (активный центр), что и эндогенный лиганд или агонист, но без активации рецептора.
Аллостерические ингибиторы (также известные как неконкурентные антагонисты) связываются с отдельными от агониста сайтами связывания, проявляя свое действие в отношении этого рецептора через другой сайт связывания. Неконкурентные антагонисты не конкурируют с агонистами за связывание. Связанные антагонисты могут привести к пониженной аффинности агониста в отношении этого рецептора, или, альтернативно, могут предупреждать конформационные изменения в рецепторе, требуемые для активации рецептора после связывания агониста.
Термин «рак», используемый здесь, относится к ненормальному росту клеток, что приводит к пролиферации неконтролируемым способом и в некоторых случаях к метастазу (распространению). Виды рака включают, но без ограничения, солидные опухоли (такие как опухоли мочевого пузыря, кишечника, мозга, молочной железы, эндометрия, сердца, почки, легкого, лимфатической ткани (лимфома), яичника, поджелудочной железы или другого эндокринного органа (щитовидная железа), предстательной железы, кожи (меланома)) или гематологические злокачественные опухоли (такие как лейкемия).
Термин «носитель», используемый здесь, относится к относительно нетоксичным химическим соединениям или агентам, которые облегчают введение соединения в клетки или ткани.
Термины «совместное введение» или подобные, используемые здесь, охватывают введение выбранных терапевтических агентов одному пациенту, и подразумевают включение схем лечения, в которых агенты вводят одинаковыми или различными способами, или в одно и то же или разное время.
Термин «разбавитель» относится к химическим соединениям, которые используются для разведения интересующего соединения перед доставкой. Разбавители также могут быть использованы для стабилизации соединений, поскольку они могут обеспечить более стабильную среду. В данной области техники в качестве разбавителей используют соли, растворенные в забуференных растворах (которые также могут обеспечить контроль или поддержание pH), включая, но без ограничения, забуференный фосфатном физиологический раствор.
Термины «эффективное количество» или «терапевтически эффективное количество», используемые здесь, относятся к количеству вводимого агента или соединения, достаточному для облегчения до некоторой степени одного или нескольких симптомов заболевания или состояния, по поводу которого проводят лечение. Результатом может являться уменьшение и/или ослабление признаков, симптомов или причин заболевания, или любое другое желаемое изменение биологической системы. Например, «эффективное количество» для терапевтических применений представляет собой количество композиции, содержащей соединение, описанное здесь, необходимое для обеспечения клинически значимого уменьшения симптомов заболевания. Соответствующее «эффективное количество» в каждом отдельном случае может быть определено с применением таких методик, как исследование с увеличением дозы.
Термины «усиливать» или «усиление», используемые здесь, означают увеличение или продление желаемого эффекта, либо по силе, либо по продолжительности. Таким образом, в отношении усиления эффекта терапевтических агентов термин «усиление» относится к способности увеличивать или продлевать эффект других терапевтических агентов на систему, либо по силе, либо по продолжительности. «Усиливающее эффективное количество», используемое здесь, относится к количеству, адекватному усилению действия другого терапевтического агента в желаемой системе.
«Метаболит» соединения, раскрытого здесь, представляет собой производное этого соединения, образуемое при метаболизме соединения. Термин «активный метаболит» относится к биологически активному производному соединения, образуемому при метаболизме соединения. Термин «метаболизированный», используемый здесь, относится к совокупности процессов (включая, но без ограничения, реакции гидролиза и реакции, катализируемые ферментами), посредством которых организм изменяет определенное вещество. Таким образом, ферменты могут вызывать определенные структурные изменения соединения. Например, цитохром Р450 катализирует множество окислительных и восстановительных реакций, в то время как уридиндифосфатглюкуронилтрансферазы катализируют перенос активированной молекулы глюкуроновой кислоты на ароматические спирты, алифатические спирты, карбоновые кислоты, амины и свободные сульфидрильные группы. Метаболиты соединений, раскрытых здесь, могут быть необязательно идентифицированы либо введением соединений хозяину и анализом образов ткани от хозяина, либо инкубацией соединений с клетками печени in vitro и анализом полученных соединений.
Термин «фармацевтическая комбинация», используемый здесь, означает продукт, полученный в результате смешивания или объединения более одного активного ингредиента, и включает как фиксированные, так и нефиксированные комбинации активных ингредиентов. Термин «фиксированная комбинация» означает, что активные ингредиенты, например, соединение структур I-V или Ia-Va и сопутствующий агент вводят пациенту одновременно в форме одного целого или дозы. Термин «нефиксированная комбинация» означает, что активные ингредиенты, например, соединение структур I-V или Ia-Va и сопутствующий агент вводят пациенту в виде отдельных объектов одновременно, параллельно или последовательно без определенных ограничений по промежуткам времени, при этом такое введение обеспечивает эффективные уровни двух соединений в организме человека. Последнее также применимо к смешанной терапии, например, введению трех или более активных ингредиентов.
Термин «фармацевтическая композиция» относится к смеси соединения (то есть соединения структур I-V или Ia-Va, описанных здесь), с другими химическими компонентами, такими как носители, стабилизаторы, разбавители, диспергирующие агенты, суспендирующие агенты, загустители и/или вспомогательные вещества. Фармацевтическая композиция облегчает введение соединения в организм. В данной области техники существует множество методик введения соединения, включая, но без ограничения: внутривенное, пероральное, аэрозольное, парентеральное, глазное, ингаляционное и местное введение.
Термин «субъект» или «пациент» охватывает млекопитающих. Примеры млекопитающих включают, но без ограничения, любой член класса млекопитающих: человека, всех приматов, кроме человека, таких как шимпанзе, и другие разновидности человекообразных обезьян и мартышек; фермерских животных, таких как крупный рогатый скот, лошади, овцы, козы, свиньи; домашних животных, таких как кролики, собаки и кошки; лабораторных животных, включая грызунов, таких как крысы, мыши и морские свинки, и им подобные. В одном варианте млекопитающим является человек.
Термины «лечить», «лечение» или «терапия», используемые здесь, включают частичное снятие, смягчение или уменьшение интенсивности, по меньшей мере, одного симптома заболевания или состояния, предупреждение дополнительных симптомов, ингибирование заболевания или состояния, например, купирование развития заболевания или состояния, облегчение заболевания или состояния, индукцию регрессии заболевания или состояния, облегчение состояния, вызванного заболеванием или состоянием, или прекращение симптомов заболевания или состояния, профилактически и/или терапевтически.
Способы введения
Подходящие способы введения включают, но без ограничения, пероральное, внутривенное, ректальное, аэрозольное, парентеральное, глазное, ингаляционное, трансмукозальное, трансдермальное, вагинальное, ушное, назальное и местное введение. Дополнительно, в качестве примера только, парентеральная доставка включает внутримышечные, подкожные, внутривенные, интрамедуллярные инъекции, а также интратекальные, прямые интравентрикулярные, интраперитонеальные, внутрилимфатические и интраназальные инъекции.
В определенных вариантах соединение, как описано здесь, вводят скорее местным, а не системным способом, например, инъекцией соединения непосредственно в орган, часто в виде депо-препарата или состава с замедленным высвобождением. В конкретных вариантах составы пролонгированного действия вводят путем имплантации (например, подкожно или внутримышечно) или путем внутримышечной инъекции. Кроме того, в других вариантах лекарственное средство доставляется в системе направленной доставки лекарственного средства, например, в липосоме, покрытой орган-специфическим антителом. В таких вариантах липосомы воздействуют направлено и селективно поглощаются органом. В еще других вариантах соединение, как описано здесь, представлено в форме состава с быстрым высвобождением, в форме состава с пролонгированным высвобождением или в форме состава с промежуточным высвобождением. В еще других вариантах соединение, описанное здесь, вводят местно.
Фармацевтическая композиция/состав
В некоторых вариантах соединения, описанные здесь, представлены в виде фармацевтических композиций. В конкретных вариантах фармацевтические композиции изготовлены обычным способом с использованием одного или нескольких физиологически приемлемых носителей, содержащих вспомогательные вещества и добавки, которые облегчают обработку активных соединений в препараты, которые могут быть использованы фармацевтически. Подходящий состав зависит от выбранного способа введения. Любые фармацевтически приемлемые методики, носители и вспомогательные вещества могут быть использованы как подходящие для изготовления фармацевтических композиций, описанных здесь: Remington: The Science and Practice of Pharmacy, Nineteenth Ed (Easton, Pa.: Mack Publishing Company, 1995); Hoover, John E., Remington’s Pharmaceutical Sciences, Mack Publishing Co., Easton, Pennsylvania 1975; Liberman, H.A. and Lachman, L., Eds., Pharmaceutical Dosage Forms,
Marcel Decker, New York, N.Y., 1980; and Pharmaceutical Dosage Forms and Drug Delivery Systems, Seventh Ed. (Lippincott Williams & Wilkins 1999).
В данном документе предложены фармацевтические композиции, содержащие соединение (то есть соединение структур I-V или Ia-Va, описанных здесь) и фармацевтически приемлемый разбавитель(и), вспомогательное вещество(а) или носитель(и). В определенных вариантах описанные соединения вводят в виде фармацевтических композиций, в которых соединение (то есть соединение структур I-V или Ia-Va, описанных здесь) смешано с другими активными ингредиентами, как в комбинированной терапии. В данном документе охвачены все комбинации активных веществ, представленные в разделе комбинированных терапий далее и по всему данному описанию. В конкретных вариантах фармацевтические композиции содержат одно или несколько соединений (то есть соединение структур I-V или Ia-Va, описанных здесь).
Фармацевтическая композиция, используемая здесь, относится к смеси соединения (то есть соединения структур I-V или Ia-Va, описанных здесь) с другими химическими компонентами, такими как носители, стабилизаторы, разбавители, диспергирующие агенты, суспендирующие агенты, загустители и/или вспомогательные вещества. В определенных вариантах фармацевтическая композиция облегчает введение соединения в организм. В некоторых вариантах, при практическом осуществлении способов лечения или применения, предложенного здесь, терапевтически эффективные количества соединений (то есть соединений структур I-V или Ia-Va, описанных здесь) вводят в виде фармацевтической композиции млекопитающему, имеющему заболевание или состояние, подлежащее лечению. В конкретных вариантах млекопитающим является человек. В определенных вариантах терапевтически эффективные количества изменяются в зависимости от тяжести заболевания, возраста и относительного состояния здоровья субъекта, активности применяемого соединения и других факторов. Соединения, описанные здесь, могут применяться отдельно или в комбинации с одним или несколькими терапевтическими агентами как компонентами смесей.
В одном варианте соединение (то есть соединение структур I-V или Ia-Va, описанных здесь) изготовлено в водном растворе. В конкретных вариантах водный раствор выбран, в качестве примера только, из физиологически совместимого буфера, такого как раствор Хэнка, раствор Рингера или буфера физиологического раствора. В других вариантах соединение (то есть соединение структур I-V или Ia-Va, описанных здесь) изготовлено для введения через слизистую оболочку. В конкретных вариантах составы для трансмукозального введения содержат смачивающие вещества, подходящие для проникновения через барьер. В еще других вариантах, в которых описанные здесь соединения изготовлены для других парентеральных инъекций, подходящие составы включают водные или неводные растворы. В конкретных вариантах такие растворы включают физиологически совместимые буферы и/или вспомогательные вещества.
В другом варианте соединения, описанные здесь, изготовлены для перорального введения. Соединения, описанные здесь, включающие соединение (то есть соединение структур I-V или Ia-Va, описанных здесь), изготовлены путем объединения активных соединений, например, с фармацевтически приемлемыми носителями или вспомогательными веществами. В различных вариантах соединения, описанные здесь, изготовлены в виде пероральных лекарственных форм, которые включают, в качестве примера только, таблетки, порошки, пилюли, драже, капсулы, жидкости, гели, сиропы, элексиры, взвеси, суспензии, и им подобные.
В определенных вариантах фармацевтические препараты для перорального применения получены путем смешивания одного или нескольких твердых вспомогательных веществ с одним или несколькими из соединений, описанных здесь, необязательного измельчения полученной смеси, и обработки смеси гранул после добавления подходящих вспомогательных веществ, при желании, для получения таблеток или ядер драже. Подходящие вспомогательные вещества представляют собой, в частности, наполнители, такие как сахара, включая лактозу, сахарозу, маннит или сорбит; целлюлозные препараты, такие как: например, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагантовая камедь, метилцеллюлоза, микрокристаллическая целлюлоза, гидроксипропилметилцеллюлоза, натрийкарбоксиметилцеллюлоза; или другие, такие как: поливинилпирролидон (PVP или повидон) или фосфат кальция. В конкретных вариантах необязательно добавлены дезинтегрирующие агенты. Дезинтегрирующие агенты включают, в качестве примера только, сшитую кроскармеллозу натрия, поливинилпирролидон, агар или альгиновую кислоту, или ее соль, такую как альгинат натрия.
В одном варианте лекарственные формы, такие как ядра драже и таблетки, имеют одно или несколько подходящих покрытий. В конкретных вариантах для покрытия лекарственной формы используют концентрированные растворы сахаров.
Растворы сахаров необязательно содержат дополнительные компоненты, такие как, в качестве примера только, аравийскую камедь, тальк, поливинилпирролидон, карбополовый гель, полиэтиленгликоль и/или диоксид титана, лаковые растворы и подходящие органические растворители или смеси растворителей. В покрытия также необязательно добавлены красители или пигменты для идентификации. К тому же, красители и/или пигменты необязательно используют для отличия различных комбинаций доз активного соединения.
В определенных вариантах терапевтически эффективные количества, по меньшей мере, одного из соединений, описанных здесь, изготовлены в виде других лекарственных форм для перорального введения. Лекарственные формы для перорального введения включают твердые (push-fit) капсулы, изготовленные из желатина, а также мягкие закрытые капсулы, изготовленные из желатина и пластификатора, такого как глицерин или сорбит. В конкретных вариантах твердые (push-fit) капсулы содержат активные ингредиенты с добавками одного или нескольких наполнителей. Наполнители включают, в качестве примера только, лактозу, связующие, такие как крахмалы, и/или смазывающие вещества, такие как тальк или стеарат магния, и необязательно стабилизаторы. В других вариантах мягкие капсулы содержат одно или несколько активных соединений, которые растворены или суспендированы в подходящей жидкости. Подходящие жидкости включают, в качестве примера только, одно или несколько нелетучих масел, вазелиновое масло или жидкий полиэтиленгликоль. Кроме того, необязательно добавлены стабилизаторы.
В других вариантах терапевтически эффективные количества, по меньшей мере, одного из соединений, описанных здесь, изготовлены для буккального или сублингвального введения. Препараты, подходящие для буккального или сублингвального введения, включают, в качестве примера только, таблетки, пастилки или гели. В еще других вариантах соединения, описанные здесь, изготовлены для парентеральной инъекции, включая препараты, подходящие для болюсной инъекции или непрерывной инфузии. В конкретных вариантах препараты для инъекции представлены в виде стандартной лекарственной формы (например, в ампулах) или многодозных контейнеров. В инъекционные составы необязательно добавлены консерванты. В еще других вариантах фармацевтические композиции соединения (то есть соединения структур I-V или Ia-Va, описанных здесь) изготовлены в форме, подходящей для парентеральной инъекции, в виде стерильных суспензий, растворов или эмульсий в масляных или водных носителях. Инъекционные составы для парентерального введения необязательно содержат протокольные агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. В конкретных вариантах фармацевтические препараты для парентерального введения включают водные растворы активных соединений в водорастворимой форме. В дополнительных вариантах суспензии активных соединений приготовлены в виде подходящих масляных суспензий для инъекции. Подходящие липофильные растворители или носители для использования в фармацевтических композициях, описанных здесь, включают, в качестве примера только, нелетучие масла, такие как кунжутное масло, или синтетические эфиры жирных кислот, такие как этилолеат или триглицериды, или липосомы. В определенных конкретных вариантах водные суспензии для инъекций содержат вещества, которые повышают вязкость суспензии, такие как натрийкарбокисметилцеллюлоза, сорбит или декстран. Необязательно суспензия содержит подходящие стабилизаторы или агенты, повышающие растворимость соединений для получения высококонцентрированных растворов. Альтернативно, в других вариантах активный ингредиент находится в форме порошка для восстановления подходящим носителем перед применением, например, стерильной апирогенной водой.
В одном аспекте соединения (то есть соединения структур I-V или Ia-Va, описанных здесь) приготовлены в виде растворов для парентеральной инъекции, как описано здесь или известно в данной области, и вводятся при помощи автоматического инъектора. Автоматические инъекторы, такие как описанные в патенте США под номерами 4,031,893, 5,358,489; 5,540,664; 5,665,071, 5,695,472 и WO /2005/087297 (каждый из которых включен здесь посредством отсылки), являются известными. В целом, все автоматические инъекторы содержат объем раствора, который включает соединение (то есть соединение структур I-V или Ia-Va, описанных здесь), подлежащее инъецированию. В целом, автоматические инъекторы содержат резервуар для раствора, который находится в жидком взаимодействии с иглой, предназначенной для доставки лекарственного средства, а также механизм для автоматической установки иглы, введения иглы пациенту и доставки дозы пациенту. Иллюстративные инъекторы содержат примерно 0.3 мл раствора при концентрации от 0.5 мг до 10 мг соединения (то есть соединения структур I-V или Ia-Va, описанных здесь) на 1 мл раствора. Каждый инъектор способен доставлять только одну дозу соединения.
В еще других вариантах соединения (то есть соединение структур I-V или Ia-Va, описанных здесь) вводят местно. Соединения, описанные здесь, изготовлены в виде различных вводимых местно композиций, таких как растворы, суспензии, лосьоны, гели, пасты, лекарственные шпатели, бальзамы, кремы или мази. Такие фармацевтические композиции необязательно содержат солюбилизаторы, стабилизаторы, агенты, усиливающие тоничность, буферы и консерванты.
В еще других вариантах соединения (то есть соединения структур I-V или Ia-Va, описанных здесь) изготовлены для трансдермального введения. В конкретных вариантах препараты для трансдермального введения используют устройства для трандермальной доставки и пластыри для трансдермальной доставки, и могут представлять собой липофильные эмульсии или забуференные водные растворы, растворенные и/или диспергированные в полимере или связывающем веществе. В различных вариантах такие пластыри разработаны для непрерывной, прерывистой доставки или доставки фармацевтических агентов по требованию. В дополнительных вариантах трансдермальная доставка соединения (то есть соединений структур I-V или Ia-Va, описанных здесь) осуществляется посредством ионтофоретических пластырей и им подобных. В определенных вариантах трансдермальные пластыри обеспечивают контролируемую доставку соединения (то есть соединения структур I-V или Ia-Va, описанных здесь). В конкретных вариантах скорость абсорбции замедлена путем использования контролирующих скорость мембран или захвата соединения в полимерную матрицу или гель. В альтернативных вариантах усилители абсорбции используются для увеличения абсорбции. Усилители абсорбции или носители включают абсорбируемые фармацевтически приемлемые растворители, которые способствуют прохождению через кожу. Например, в одном варианте трансдермальные устройства представлены в форме повязки, состоящей из основы, резервуара, содержащего соединение, необязательно с носителями, необязательно контролирующим скорость барьером для доставки соединения в кожу хозяина с контролируемой и заранее установленной скоростью в течение продолжительного периода времени, и средства закрепления устройства на коже.
Препараты для трансдермальной доставки, описанные здесь, могут быть введены с использованием различных устройств, которые описаны в данной области. Например, такие устройства включают, но без ограничения, патент США под номером 3,598,122, 3,598,123, 3,710,795, 3,731,683, 3,742,951, 3,814,097, 3,921,636, 3,972,995, 3,993,072, 3,993,073, 3,996,934, 4,031,894, 4,060,084, 4,069,307, 4,077,407, 4,201,211, 4,230,105, 4,292,299, 4,292,303, 5,336,168, 5,665,378, 5,837,280, 5,869,090, 6,923,983, 6,929,801 и 6,946,144.
Лекарственные формы для трансдермальной доставки, описанные здесь, могут содержать определенные фармацевтически приемлемые вспомогательные вещества, обычно используемые в данной области. В одном варианте трансдермальные препараты, описанные здесь, содержат, по меньшей мере, три компонента: (1) препарат соединения (то есть соединения структур I-V или Ia-Va, описанных здесь); (2) усилитель проникновения; и (3) водное вспомогательное лекарственное средство. Дополнительно, трансдермальные препараты могут содержать дополнительные компоненты, такие как, но без ограничения, гелирующие агенты, кремы и мазевые основы, и им подобные. В некоторых вариантах трансдермальный препарат, кроме того, содержит тканый или нетканый материал основы для усиления абсорбции и предотвращения удаления трансдермального состава из кожи. В других вариантах трансдермальные препараты, описанные здесь, сохраняют насыщенное или супернасыщенное состояние для способствования диффузии в кожу.
В других вариантах соединения структур I-V или Ia-Va изготовлены для введения путем ингаляции. Различные формы, подходящие для введения путем ингаляции, включают, но без ограничения, аэрозоли, туманы или порошки. Фармацевтические композиции соединения (то есть аллостерические ингибиторы киназы, описанные здесь) подходящим образом доставляются в форме распыленного аэрозоля из упаковок под давлением или небулайзера с использованием подходящего пропеллента (например, дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа). В конкретных вариантах единица дозы определяется клапаном для доставки отмеренного количества. В определенных вариантах капсулы и картриджи, изготовленные, в качестве примера только, из желатина для применения в ингаляторе или инсуффляторе, содержат порошковую смесь соединения и подходящую порошковую основу, такую как лактоза или крахмал.
Препараты для интраназального применения хорошо известны в данной области техники, и они описаны, например, в патентах США №4,476,116, 5,116,817 и 6,391,452, каждый из которых особо включен посредством отсылки. Препараты, которые включают в себя соединение (то есть соединение структур I-V или Ia-Va, описанных здесь), которые изготовлены согласно этим и другим методикам, хорошо известным в данной области, приготовлены в виде растворов в физиологическом растворе с использованием бензилового спирта или других подходящих консервантов, фторуглеродов, и/или других солюбилизирующих, или диспергирующих агентов, известных в данной области. Смотри, например, Ansel, Н.С. et al., Pharmaceutical Dosage Forms and Drug Delivery Systems, Sixth Ed. (1995). Предпочтительно, чтобы эти композиции и препараты были приготовлены с подходящими нетоксичными фармацевтически приемлемыми ингредиентами. Эти ингредиенты обнаружены в источниках, таких как REMINGTON: THE SCIENCE AND PRACTICE OF PHARMACY, 21st edition, 2005, что является стандартной ссылкой в данной области техники. Выбор подходящих носителей в значительной степени зависит от конкретной природы желаемой назальной лекарственной формы, например, растворов, суспензий, мазей или гелей. Назальные лекарственные формы в большинстве случаев содержат значительное количество воды в дополнение к активному ингредиенту. Могут также присутствовать небольшие количества других ингредиентов, таких как регуляторы рН, эмульгаторы или диспергирующие агенты, консерванты, поверхностно-активные вещества, желирующие агенты или буферные или другие стабилизирующие и солюбилизирующие агенты. Предпочтительно, чтобы назальная лекарственная форма была изотонична назальным секретам.
Для введения ингаляцией соединения, описанные здесь, могут быть представлены в форме аэрозоля, тумана или порошка. Доставку фармацевтических композиций, описанных здесь, подходящим образом осуществляют в форме получения распыленного аэрозоля из упаковок под давлением или небулайзера с использованием подходящего пропеллента, например, дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа. В случае аэрозоля под давлением, единица дозы будет определена клапаном для доставки отмеренного количества. Могут быть изготовлены капсулы и картриджи, такие как, только в качестве примера, из желатина, для применения в ингаляторе или инсуффляторе, содержащие порошковую смесь соединения, описанного здесь, и подходящую основу порошка, такого как лактоза или крахмал.
В еще других вариантах соединения структур I-V или Ia-Va изготовлены в форме композиций для ректального введения, таких как клизмы, гели для ректального введения, пены для ректального введения, аэрозоли для ректального введения, суппозитории, гелевые суппозитории или удерживающие клизмы, содержащие обычные суппозиторные основы, такие как масло какао или другие глицериды, а также синтетические полимеры, такие как поливинилпирролидон, PEG, и им подобные. В формах в виде суппозиториев сначала происходит расплавление легкоплавкого воска, такого как, без ограничения, смесь глицеридов жирных кислот, необязательно в комбинации с маслом какао.
В определенных вариантах фармацевтические композиции изготовлены любым подходящим способом с использованием одного или нескольких физиологически приемлемых носителей, содержащих вспомогательные вещества и добавки, которые облегчают обработку активных соединений в препараты, которые могут быть использованы фармацевтически. Подходящий состав зависит от выбранного способа введения. Любые фармацевтически приемлемые методики, носители и вспомогательные вещества необязательно используются как подходящие и как понимаются в данной области. Фармацевтические композиции, содержащие соединение (то есть аллостерические ингибиторы киназы, описанные здесь) могут быть изготовлены обычным способом, таким как, в качестве примера только, обычное смешивание, растворение, гранулирование, изготовление драже, растирание в порошок, эмульгирование, инкапсулирование, захват или прессование.
Фармацевтические композиции содержат, по меньшей мере, один фармацевтически приемлемый носитель, разбавитель или вспомогательное вещество и, по меньшей мере, одно соединение (то есть соединение структур I-V или Ia-Va, описанных здесь), описанное здесь, в качестве активного ингредиента. Активный ингредиент находится в форме свободной кислоты или свободного основания, или в форме фармацевтически приемлемой соли. К тому же, способы и фармацевтические композиции, описанные здесь, включают применение JV-оксидов, кристаллических форм (также известных как полиморфы), а также активных метаболитов этих соединений, имеющих такой же тип активности. Все таутомеры соединений, описанных здесь, включены в объем соединений, представленных здесь. Дополнительно, соединения, описанные здесь, охватывают несольватированные, а также сольватированные формы с фармацевтически приемлемыми растворителями, такими как вода, этанол и им подобные. Сольватированные формы представленных здесь соединений также рассматриваются как раскрытые здесь. К тому же, фармацевтические композиции необязательно содержат другие лекарственные или фармацевтические агенты, носители, вспомогательные вещества, такие как консерванты, стабилизаторы, смачивающие агенты или эмульгаторы, промоторы растворения, соли для регулирования осмотического давления, буферы и/или другие терапевтически доступные вещества.
Способы приготовления композиций, содержащих соединения, описанные здесь, включают изготовление соединений с одним или несколькими инертными, фармацевтически приемлемыми вспомогательными веществами или носителями с образованием твердого вещества, полутвердого вещества или жидкости. Твердые композиции включают, но без ограничения, порошки, таблетки, диспергируемые гранулы, капсулы, крахмальные капсулы и суппозитории. Жидкие композиции включают растворы, в которых соединение является растворенным, эмульсии, содержащие соединение, или раствор, содержащий липосомы, мицеллы, или наночастицы, содержащие соединение, как описано здесь. Полутвердые композиции включают, но без ограничения, гели, суспензии и кремы. Форма фармацевтических композиций, описанных здесь, включает жидкие растворы или суспензии, твердые формы, подходящие для раствора или суспензии в жидкости перед использованием, или в качестве эмульсий. Эти композиции также необязательно содержат минимальные количества нетоксичных вспомогательных веществ, таких как смачивающие или эмульгирующие агенты, регулирующие pH буферные агенты и так далее.
В некоторых вариантах фармацевтическая композиция, содержащая, по меньшей мере, одно соединение (то есть соединение структур I-V или Ia-Va, описанных здесь), для иллюстрации принимает форму жидкости, когда агенты присутствуют в растворе, в суспензии или обоих. Как правило, когда композиция вводится в виде раствора или суспензии, первая часть агента присутствует в растворе и вторая часть агента присутствует в форме частиц в суспензии в жидкой матрице. В некоторых вариантах жидкая композиция включает гелевую композицию. В других вариантах жидкая композиция является водной.
В определенных вариантах фармацевтические водные суспензии содержат один или несколько полимеров в качестве суспендирующих агентов. Полимеры включают водорастворимые полимеры, такие как целлюлозные полимеры, например, гидроксипропилметилцеллюлоза и водорастворимые полимеры, такие как сшитые карбоксилсодержащие полимеры. Определенные фармацевтические композиции, описанные здесь, содержат мукоадгезивный полимер, выбранный, например, из карбоксиметилцеллюлозы, карбомера (полиакриловой кислоты), полиметилметакрилата, полиакриламида, поликарбофила, сополимеров акриловой кислоты и бутилакрилата, альгината натрия и декстрана.
Фармацевтические композиции также необязательно включают солюбилизирующие агенты для способствования растворимости соединения (то есть соединения структур I-V или Ia-Va, описанных здесь). Термин «солюбилизирующий агент» в целом включает агенты, которые приводят к образованию мицеллярного раствора или чистого раствора агента. Определенные приемлемые неионные поверхностно-активные вещества, например полисорбат 80, являются эффективными в качества солюбилизирующих агентов, также как офтальмологически приемлемые гликоли, полигликоли, например, полиэтиленгликоль 400 и простые эфиры гликолей.
Кроме того, фармацевтические композиции необязательно содержат один или несколько регулирующих pH агентов или буферных агентов, включая кислоты, такие как уксусная, борная, лимонная, молочная, фосфорная и соляная кислоты; основания, такие как гидроксид натрия, фосфат натрия, борат натрия, цитрат натрия, ацетат натрия, лактат натрия и трис-гидроксиметиламинометан; и буферы, такие как цитрат/декстроза, бикарбонат натрия и хлорид аммония. Такие кислоты, основания и буферы содержатся в количестве, требуемом для поддержания рН композиции в приемлемом диапазоне.
Дополнительно, фармацевтические композиции необязательно содержат одну или несколько солей в количестве, требуемом для доведения осмотического давления композиции до приемлемого диапазона. К таким солям относятся соли, имеющие катионы натрия, калия или аммония и анионы хлорида, цитрата, аскорбата, бората, фосфата, бикарбоната, сульфата, тиосульфата или бисульфата; подходящими солями являются хлорид натрия, хлорид калия, тиосульфат натрия, бисульфит натрия и сульфат аммония.
Другие фармацевтические композиции необязательно содержат один или несколько консервантов для подавления микробной активности. Подходящие консерванты включают ртутьсодержащие вещества, такие как мерфен и тиомерсаль; стабилизированный диоксид хлора; и четвертичные аммониевые соединения, такие как бензалкония хлорид, цетилтриметиламмония бромид и цетилпиридиния хлорид.
Еще другие фармацевтические композиции содержат одно или несколько поверхностно-активных веществ для повышения физической стабильности или для других целей. Подходящие неионные поверхностно-активные вещества включают полиоксиэтилен глицериды жирных кислот и растительные масла, например полиоксиэтилен (60) гидрированное касторовое масло; и полиоксиэтилен простые алкиловые и алкилфениловые эфиры, например октоксинол 10, октоксинол 40.
Еще другие фармацевтические композиции могут содержать один или несколько антиоксидантов для усиления химической стабильности при необходимости. Подходящие антиоксиданты включают, в качестве примера только, аскорбиновую кислоту и метабисульфит натрия.
В определенных вариантах фармацевтические композиции в виде водных суспензий упакованы в не герметизируемые повторно контейнеры на стандартную дозу. Альтернативно, используют герметизируемые повторно контейнеры на множество доз, в этом случае в состав композиции обычно вводят консервант.
В альтернативных вариантах используют другие системы доставки гидрофобных фармацевтических соединений. Липосомы и эмульсии являются примерами доставляющих носителей или наполнителей.
В альтернативных вариантах используются другие системы доставки гидрофобных фармацевтических композиций. Липосомы и эмульсии являются примерами доставляющих носителей или наполнителей. В определенных вариантах также используют органические растворители, такие как N-метилпирролидон. В дополнительных вариантах соединения, описанные здесь, доставляются с использованием систем с замедленным высвобождением, таких как полупроницаемые матрицы твердых гидрофобных полимеров, содержащих терапевтический агент. Различные материалы с замедленным высвобождением являются здесь эффективными. В некоторых вариантах капсулы с замедленным высвобождением высвобождают соединения в течение нескольких часов вплоть до более 24 часов. В зависимости от химической природа и биологической стабильности терапевтического реагента могут быть использованы дополнительные стратегии стабилизации белка.
В определенных вариантах препараты, описанные здесь, содержат один или несколько антиоксидантов, металл-хелатирующих агентов, тиолсодержащих соединений и/или другие стабилизирующие агенты. В качестве примера такие стабилизирующие агенты содержат, но без ограничения: (a) примерно от 0.5% до примерно 2% масса/объем глицерина, (b) примерно от 0.1% до примерно 1% масса/объем метионина, (c) примерно от 0.1% до примерно 2% масса/объем монотиоглицерина, (d) примерно от 1 мМ до примерно 10 мМ ЭДТА, (e) примерно от 0.01% до примерно 2% масса/объем аскорбиновой кислоты, (f) от 0.003% до примерно 0.02% масса/объем полисорбата 80, (g) от 0.001% до примерно 0.05% масса/объем полисорбата 20, (h) аргинин, (i) гепарин, (j) декстран сульфат, (k) циклодекстрины, (l) пентозан полисульфат и другие гепариноиды, (m) двухвалентные катионы, такие как катионы магния и цинка; или (n) их комбинации.
Если не определено иначе, все технические и научные термины, используемые здесь, имеют такое же значение, как их обычно понимает специалист в области техники, к которой относится заявленный объект изобретения. В случае, если используемые здесь термины имеют множество определений, основными являются определения этого раздела. Там, где сделана ссылка на URL или другой такой идентификатор или адрес, подразумевают, что такие идентификаторы могут изменяться, и конкретная информация в Интернете может появляться и исчезать, но эквивалентная информация может быть найдена при поиске в Интернете. Ссылка на них является свидетельством доступности и публичного распространения такой информации.
Следует понимать, что последующее общее описание и последующее подробное описание являются лишь примером и объяснением, и не ограничивают ни один из заявленных объектов изобретения. При использовании в настоящем описании артикли единственного числа «a», «an», «the» содержат в себе множественное число, если в тексте четко не указано иное. Необходимо отметить, что при использовании в данном описании и прилагаемой формуле изобретения формы единственного числа, указывающие на неопределенное количество, включают множественные референты, если контекстом четко не продиктовано иное. Более того, применение термина «включая», а также других форм, таких как «включать», «включает» и «включенный», не является ограничивающим.
Если не указано иное, используют обычные методы масс-спектроскопии, ЯМР, ВЭЖХ, химии белка, биохимии, методов рекомбинатной ДНК и фармакологии. Если не приведены специальные определения, используется стандартная номенклатура и стандартные лабораторные способы и методики аналитической химии, синтетической органической химии и медицинской и фармацевтической химии. В определенных случаях для химического синтеза, химических анализов, получения, изготовления и доставки фармацевтических средств и лечения пациентов используются стандартные методики. В определенных вариантах для рекомбинантных ДНК, синтеза олигонуклеотидов и культивирования и трансформации тканей используются стандартные методики (например, электропорация, липофекция). В некоторых вариантах реакции и методики очистки проводятся, например, с применением наборов описаний изготовителя, или как обычно проводят в данной области техники, или как описано здесь.
Как использовано в настоящем описании и прилагаемой формуле изобретения, следующие термины имеют следующие значения:
Термин «алкенил», используемый здесь, означает прямую, разветвленную цепь или циклический (в этом случае также известный как «циклоалкенил») углеводород, содержащий 2-10 атомов углерода и содержащий, по меньшей мере, одну углерод-углеродную двойную связь, образованную путем удаления двух атомов водорода. В некоторых вариантах в зависимости от структуры алкенильная группа представляет собой монорадикал или дирадикал (то есть алкениленовую группу). В некоторых вариантах алкенильные группы являются необязательно замещенными. Типичные примеры алкенила включают, но без ограничения, этенил, 2-пропенил, 2-метил-2-пропенил, 3-бутенил, 4-пентенил, 5-гексенил, 2-гептенил, 2-метил-1-гептенил и 3-деценил.
Термин «алкокси», используемый здесь, означает алкильную группу, как определено здесь, присоединенную к основному молекулярному фрагменту через атом кислорода. Типичные примеры алкокси включают, но без ограничения, метокси, этокси, пропокси, 2-пропокси, бутокси, трет-бутокси, пентилокси и гексилокси.
Термин «алкил», используемый здесь, означает прямую, разветвленную цепь или циклический (в этом случае также известный как «циклоалкил») углеводород, содержащий 1-10 атомов углерода. Типичные примеры алкила включают, но без ограничения, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил, 3-метилгексил, 2,2-диметилпентил, 2,3-диметилгексил, н-гептил, н-октил, н-нонил и н-децил.
Термин «C1-C6-алкил», используемый здесь, означает прямую, разветвленную цепь или циклический (в этом случае также известный как «циклоалкил») углеводород, содержащий 1-6 атомов углерода. Типичные примеры алкила включают, но без ограничения, метил, этил, н-пропил, изопропил, циклопропил, н-бутил, втор-бутил, трет-бутил, циклобутил, н-пентил, изопентил, неопентил, циклопентил и н-гексил.
Термин «циклоалкил», используемый здесь, означает моноциклический или полициклический радикал, который содержит только углерод и водород, и включает те радикалы, которые являются насыщенными, частично ненасыщенными или полностью ненасыщенными. Циклоалкильные группы включают группы, содержащие от 3 до 10 атомов в кольце. Типичные примеры циклоалкильных групп включают, но без ограничения, следующие группы:
 ,
,  ,
,  ,
,  ,
, 
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
, 
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
, 
 ,
,  ,
,  . В некоторых вариантах в зависимости от структуры циклоалкильная группа представляет собой монорадикал или дирадикал (например, циклоалкиленовая группа).
. В некоторых вариантах в зависимости от структуры циклоалкильная группа представляет собой монорадикал или дирадикал (например, циклоалкиленовая группа).
Термин «циклоалкильные группы», используемый здесь, относится к группам, которые являются необязательно замещенными 1, 2, 3 или 4 заместителями, выбранными из алкенила, алкокси, алкоксиалкила, алкоксикарбонила, алкила, алкилкарбонила, алкилкарбонилокси, алкилтио, алкилтиоалкила, алкинила, карбокси, циано, формила, галоалкокси, галоалкила, галогена, гидроксила, гидроксиалкилена, маркапто, оксо, -NRARA, и NRARB)карбонила.
Термин «циклоалкилалкил», используемый здесь, означает циклоалкильную группу, как определено здесь, присоединенную к основному молекулярному фрагменту через алкильную группу, как определено здесь. Типичные примеры циклоалкилалкила включают, но без ограничения, циклопропилметил, 2-циклобутилэтил, циклопентилметил, циклогексилметил и 4-циклогептилбутил.
Термин «карбоциклический», используемый здесь, относится к соединению, которое содержит одну или несколько ковалентно закрытых кольцевых структур и атомы, образующие основное кольцо, все являются атомами углерода.
Термин «карбоцикл», используемый здесь, относится к кольцу, в котором каждый из атомов, образующих кольцо, представляет собой атом углерода. Карбоциклические кольца включают кольца, образованные тремя, четырьмя, пятью, шестью, семью, восьмью, девятью или больше, чем девятью атомами углерода. Карбоциклы являются необязательно замещенными.
Термин «алкоксиалкил», используемый здесь, означает, по меньшей мере, одну алкоксигруппу, как определено здесь, присоединенную к основному молекулярному фрагменту через алкильную группу, как определено здесь. Типичные примеры алкоксиалкила включают, но без ограничения, 2-метоксиэтил, 2-этоксиэтил, трет-бутоксиэтил и метоксиметил.
Термин «алкоксикарбонил», используемый здесь, означает алкоксигруппу, как определено здесь, присоединенную к основному молекулярному фрагменту через карбонильную группу, как определено здесь. Типичные примеры алкоксикарбонила включают, но без ограничения, метоксикарбонил, этоксикарбонил и трет-бутоксикарбонил.
Термин «алкоксикарбонилалкил», используемый здесь, означает алкоксикарбонильную группу, как определено здесь, присоединенную к основному молекулярному фрагменту через алкильную группу, как определено здесь.
Термин «алкилкарбонил», используемый здесь, означает алкильную группу, как определено здесь, присоединенную к основному молекулярному фрагменту через карбонильную группу, как определено здесь. Типичные примеры алкилкарбонила включают, но без ограничения, ацетил, 1-оксопропил, 2,2-диметил-1-оксопропил, 1-оксобутил и 1-оксопентил.
Термин «алкилкарбонилокси», используемый здесь, означает алкилкарбонильную группу, как определено здесь, присоединенную к основному молекулярному фрагменту через атом кислорода. Типичные примеры алкилкарбонилокси включают, но без ограничения, ацетилокси, этилкарбонилокси и трет-бутилкарбонилокси.
Термин «алкилтио» или «тиоалкокси», используемый здесь, означает алкильную группу, как определено здесь, присоединенную к основному молекулярному фрагменту через атом серы. Типичные примеры алкилтио включают, но без ограничения, метилтио, этилтио, бутилтио, трет-бутилтио и гексилтио.
Термин «алкилтиоалкил», используемый здесь, означает алкилтиогруппу, как определено здесь, присоединенную к основному молекулярному фрагменту через алкильную группу, как определено здесь. Типичные примеры алкилтиоалкила включают, но без ограничения, метилтиометил, 2-(этилтио)этил, бутилтиометил и гексилтиоэтил.
Термин «алкинил», используемый здесь, означает углеводород с прямой, разветвленной цепью, содержащий 2-10 атомов углерода и содержащий, по меньшей мере, одну углерод-углеродную тройную связь. В некоторых вариантах алкинильные группы являются необязательно замещенными. Типичные примеры алкинила включают, но без ограничения, ацетиленил, 1-пропинил, 2-пропинил, 3-бутинил, 2-пентинили 1-бутинил.
Термин «ароматическое», используемый здесь, относится к плоскому кольцу, имеющему делокализованную π-электронную систему, содержащую 4n+2π - электронов, где n представляет собой целое число. В некоторых вариантах ароматические кольца образованы пятью, шестью, семью, восьмью, девятью или более чем девятью атомами. В других вариантах ароматические структуры являются необязательно замещенными. Термин включает моноциклические или полициклические группы с конденсированным кольцом (то есть циклы, которые имеют общие пары атомов углерода).
Термин «арил», используемый здесь, относится к ароматическому кольцу, в котором каждый из атомов, образующих кольцо, представляет собой атом углерода. В некоторых вариантах арильные кольца образованы пятью, шестью, семью, восьмью, девятью или более чем девятью атомами углерода. Примеры арильных групп включают, но без ограничения, фенил, нафталенил, фенантренил, антраценил, флуоренил и инденил.
В некоторых вариантах термин «арил», используемый здесь, означает арильную группу, которая необязательно является замещенной одним, двумя, тремя, четырьмя или пятью заместителями, независимо выбранными из группы, состоящей из алкенила, алкокси, алкоксиалкила, алкоксикарбонила, алкила, алкилкарбонила, алкилкарбонилокси, алкилтио, алкилтиоалкила, алкинила, карбонила, циано, формила, галоалкокси, галоалкила, галогена, гидроксила, гидроксиалкилена, меркапто, нитро, -NRARA и (NRARB)карбонила.
Термин «арилалкил», используемый здесь, означает арильную группу, как определено здесь, присоединенную к основному молекулярному фрагменту через алкильную группу, как определено здесь. Типичные примеры арилалкила включают, но без ограничения, бензил, 2-фенилэтил, 3-фенилпропил, 1-метил-3-фенилпропил и 2-нафт-2-илэтил.
Термин «карбонил», используемый здесь, означает -C(O)-группу.
Термин «карбокси», используемый здесь, означает -COOH-группу.
Термин «циано», используемый здесь, означает -CN-группу.
Термин «формил», используемый здесь, означает -C(O)H группу.
Термин «гало» или «галоген», используемый здесь, означает -Cl, -Br, -I или -F.
Термин «меркапто», используемый здесь, означает -SH группу.
Термин «нитро», используемый здесь, означает -NO2 группу.
Термин «гидрокси», используемый здесь, означает -OH группу.
Термин «оксо», используемый здесь, означает =O группу.
Термин «связь» или «одинарная связь», используемый здесь, относится к химической связи между двумя атомами или двумя группами, когда атомы, соединенные связью, считаются частью более крупной подструктуры.
Термины «галогеналкил», «галогеналкенил», «галогеналкинил» и «галогеналкокси», используемые здесь, включают структуры алкила, алкенила, алкинила и алкокси, в которых, по меньшей мере, один атом водорода заменен на атом галогена. В определенных вариантах, в которых два или более атомов водорода заменены на атомы галогена, атомы галогена все являются одинаковыми. В других вариантах, в которых два или более атомов водорода заменены на атомы галогена, атомы галогена не являются одинаковыми. Термины «фторалкил» и «фторалкокси» включают галогеналкил и галогеналкоксигруппы, соответственно, в которых галоген представляет собой фтор. В определенных вариантах галоалкилы являются необязательно замещенными.
Термин «алкиламин» относится к -N(алкил)xHy-группе, где x и y выбраны из x=1, y=1 и x=2, y=0. В некоторых вариантах, когда x=2, алкильные группы, взятые вместе с атомом N, к которому они присоединены, необязательно образуют циклическую кольцевую систему.
Термин «амид», используемый здесь, представляет собой химическую группу формулы -C(O)NHR или -NHC(O)R, в которой R выбран из водорода, алкила, циклоалкила, арила, гетероарила (связанного через циклический атом углерода) и гетероциклоалкила (связанного через циклический атом углерода). В некоторых вариантах амидная группа образует связь между аминокислотой или молекулой пептида и соединением, описанным здесь, образуя, таким образом, пролекарство. В некоторых вариантах любой амин или карбоксильная боковая цепь на соединениях, описанных здесь, является амидированной.
Термин «сложный эфир» относится к химической группе формулы -COOR, где R выбран из алкила, циклоалкила, арила, гетероарила (связанного через циклический атом углерода) и гетероциклоалкила (связанного через циклический атом углерода). В некоторых вариантах любая гидрокси или карбоксильная группа боковой цепи на соединениях, описанных здесь, является этерифицированной.
Термины «гетероалкил», «гетероалкенил» и «гетероалкинил», используемые здесь, включают необязательно замещенный алкильный, алкенильный и алкинильный радикалы, в которых один или несколько атомов основной цепи выбраны из атома, отличного от углерода, например, кислорода, азота, серы, кремния, фосфора или их комбинаций.
Термин «гетероатом», используемый здесь, относится к атому, отличному от углерода или водорода. Гетероатомы, как правило, независимо выбраны из кислорода, серы, азота, кремния и фосфора, но не ограничиваются этими атомами. В вариантах, в которых присутствуют два или более гетероатомов, два или более гетероатомов являются одинаковыми, или некоторые или все из двух или более гетероатомов являются отличными друг от друга.
Термин «кольцо», используемый здесь, относится к любой ковалентно закрытой структуре. Кольца включают, например, карбоциклы (например, арилы и циклоалкилы), гетероциклы (например, гетероарилы и гетероциклоалкилы), ароматические соединения (например, арилы и гетероарилы) и неароматические соединения (например, циклоалкилы и гетероциклоалкилы). В некоторых вариантах кольца являются необязательно замещенными. В некоторых вариантах кольца образуют часть кольцевой системы.
Используемый здесь термин «кольцевая система» относится к двум или более кольцам, при этом два или более из колец являются конденсированными. Термин «конденсированные» относится к структурам, в которых два или более колец имеют одну или несколько общих связей.
Термин «гетероарил» или, альтернативно, «гетероароматическая» относится к арильной группе, которая содержит одно или несколько гетероатомов кольца, выбранных из азота, кислорода и серы. N-содержащая «гетероароматическая» или «гетероарильная» группа относится к ароматической группе, в которой, по меньшей мере, один из атомов основного кольца представляет собой атом азота. В некоторых вариантах полициклическая гетероарильная группа является конденсированной или неконденсированной. Типичные гетероарильные группы включают, но без ограничения, следующие группы:
 ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  ,
, 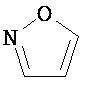 ,
,  ,
,  ,
, 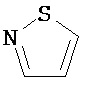
 ,
,  ,
, 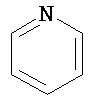 ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  . В некоторых вариантах в зависимости от структуры гетероарильная группа представляет собой монорадикал или дирадикал (то есть гетероариленовую группу).
. В некоторых вариантах в зависимости от структуры гетероарильная группа представляет собой монорадикал или дирадикал (то есть гетероариленовую группу).
Термин «гетероарил» означает гетероарильные группы, которые являются замещенными 0, 1, 2, 3 или 4 заместителями, независимо выбранными из алкенила, алкокси, алкоксиалкила, алкоксикарбонила, алкила, алкилкарбонила, алкилкарбонилокси, алкилтио, алкилтиоалкила, алинила, карбокси, циано, формила, галоалкокси, галоалкила, галогена, гидроксила, гидроксиалкилена, меркапто, нитро, -NRARB и -(NRARB)карбонила.
Термин «гетероарилалкил», используемый здесь, означает гетероарил, как определено здесь, присоединенный к основному молекулярному фрагменту через алкильную группу, как определено здесь. Типичные примеры гетероарилалкила включают, но без ограничения, пиридинилметил.
Термин «гетероциклоалкил» или «неароматический гетероцикл», используемый здесь, относится к неароматическому кольцу, в котором один или несколько атомов, образующих кольцо, представляют собой гетероатом. «Гетероциклоалкильная» или «неароматическая гетероциклическая» группа относится к циклоалкильной группе, которая содержит, по меньшей мере, один гетероатом, выбранный из азота, кислорода и серы. В некоторых вариантах радикалы конденсированы с арилом или гетероарилом. В некоторых вариантах гетероциклоалкильные кольца образованы тремя, пятью, шестью, семью, восьмью, девятью или больше чем девятью атомами. В некоторых вариантах гетероциклоалкильные кольца необязательно являются замещенными. В определенных вариантах гетероциклоалкилы содержат один или несколько карбонильных или тиокарбонильных групп, таких как, например, оксо- и тио-содержащие группы. Примеры гетероциклоалкилов включают, но без ограничения, лактамы, лактоны, циклические имиды, циклические тиоимиды, циклические карбаматы, тетрагидротиопиран, 4Н-пиран, тетрагидропиран, пиперидин, 1,3-диоксин, 1,3-диоксан, 1,4-диоксин, 1,4-диоксан, пиперазин, 1,3-оксатиан, 1,4-оксатиин, 1,4-оксатиан, тетрагидро-1,4-тиазин, 2H-1,2-оксазин, малеимид, сукцинимид, барбитуровая кислота, тиобарбитуровая кислота, диоксопиперазин, гидантоин, дигидроурацил, морфолин, триоксан, гексагидро-1,3,5-триазин, тетрагидротиофен, тетрагидрофуран, пирролин, пирролидин, пирролидон, пирролидион, пиразолин, пиразолидин, имидазолин, имидазолидин, 1,3-диоксол, 1,3-диоксолан, 1,3-дитиол, 1,3-дитиолан, изоксазолин, изоксазолидин, оксазолин, оксазолидин, оксазолидинон, тиазолин, тиазолидин и 1,3-оксатиолан. Типичные примеры гетероциклоалкильных групп, также называемых как неароматические гетероциклы, включают, но без ограничения
 ,
,  ,
,  ,
, 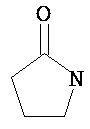 ,
,  ,
,  ,
,  ,
,
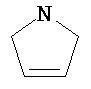 ,
,  ,
, 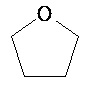 ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
, 
 ,
,  ,
,  ,
,  . Термин гетероциклоалкил также включает все кольцевые формы карбогидратов, включая, но без ограничения, моносахариды, дисахариды и олигосахариды.
. Термин гетероциклоалкил также включает все кольцевые формы карбогидратов, включая, но без ограничения, моносахариды, дисахариды и олигосахариды.
Термин «гетероцикл» относится к гетероарилу и гетероциклоалкилу, используемым здесь, относится к группам, содержащим от одного до четырех гетероатомов, каждый из которых выбран из O, S и N, при этом каждая гетероциклическая группа содержит от 4 до 10 атомов в своей циклической системе, и при условии, что кольцо указанной группы не содержит двух примыкающих атомов O или S. Здесь, независимо от указанного количества атомов углерода в гетероцикле (например, C1-C6гетероцикл), по меньшей мере, один другой атом (гетероатом) должен присутствовать в кольце. Обозначения, такие как «C1-C6гетероцикл», относятся только к количеству атомов углерода в кольце и не относятся в общему количеству атомов в кольце. В некоторых вариантах следует понимать, что гетероциклическое кольцо содержит дополнительные гетероатомы в кольце. Обозначения, такие как "4-6-членный гетероцикл», относятся к общему количеству атомов, которые содержатся в кольце (то есть четырех-, пяти- или шести-членное кольцо, в котором, по меньшей мере, один атом представляет собой атом углерода, по меньшей мере, один атом представляет собой гетероатом и оставшиеся от двух до четырех атомов представляют собой атомы углерода или гетероатомы). В некоторых вариантах в гетероциклах, которые содержат два или более гетероатомов, эти два или более гетероатомов являются одинаковыми или отличными друг от друга. В некоторых вариантах гетероциклы являются необязательно замещенными. В некоторых вариантах присоединение к гетероциклу происходит по гетероатому или через атом углерода. Гетероциклоалкильные группы включают группы, содержащие только 4 атома в их кольцевой системе, но гетероарильные группы должны содержать, по меньшей мере, 5 атомов в их кольцевой системе. Гетероциклические группы включают бензо-конденсированные кольцевые системы. Примером 4-членной гетероциклической группы является азетидинил (производное азетидина). Примером 5-членной гетероциклической группы является тиазолил. Примером 6-членной гетероциклической группы является пиридил, и примером 10-членной гетероциклической группы является хинолинил. Примерами гетероциклоалкильных групп являются пирролидинил, тетрагидрофуранил, дигидрофуранил, тетрагидротиенил, тетрагидропиранил, дигидропиранил, тетрагидротиопиранил, пиперидино, морфолино, тиоморфолино, тиоксанил, пиперазинил, азетидинил, оксетанил, тиетанил, гомопиперидинил, оксепанил, тиепанил, оксазепинил, диазепинил, тиазепинил, 1,2,3,6-тетрагидропиридинил, 2-пирролинил, 3-пирролинил, индолинил, 2Н-пиранил, 4Н-пиранил, диоксанил, 1,3-диоксоланил, пиразолинил, дитианил, дитиоланил, дигидропиранил, дигидротиенил, дигидрофуранил, пиразолидинил, имидазолинил, имидазолидинил, 3-азабицикло[3.1.0]гексанил, 3-азабицикло[4.1.0]гептанил, 3H-индолил и хинолизинил. Примерами гетероарильных групп являются пиридинил, имидазолил, пиримидинил, пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, пиридазинил, изоиндолил, птеридинил, пиринил, оксадиазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензоксазолил, хиназолинил, хиноксалинил, нафтиридинил и фуропиридинил. В некоторых вариантах вышеуказанные группы, такие как группы, полученные из групп, перечисленных выше, являются C-присоединенными или N-присоединенными, где такое является возможным. Например, в некоторых вариантах группа, полученная из пиррола, представляет собой пиррол-1-ил-(N-присоединенный) или пиррол-3-ил (C-присоединенный). Кроме того, в некоторых вариантах группа, полученная из имидазола, представляет собой имидазол-1-ил или имидазол-3-ил (обе N-присоединенные) или имидазол-2-ил, имидазол-4-ил или имидазол-5-ил (все C-присоединенные). Гетероциклические группы включают бензо-конденсированные кольцевые системы и кольцевые системы, замещенные одной или двумя оксо(=O) группами, такими как пирролидин-2-он. В некоторых вариантах в зависимости от структуры гетероциклическая группа представляет собой монорадикал или дирадикал (то есть гетероцикленовую группу).
Гетероциклы, описанные здесь, являются замещенными 0, 1, 2, 3 или 4 заместителями, независимо выбранными из алкенила, алкокси, алкоксиалкила, алкоксикарбонила, алкила, алкилкарбонила, алкилкарбонилокси, алкилтио, алкилтиоалкила, алинила, карбокси, циано, формила, галоалкокси, галоалкила, галогена, гидроксила, гидроксиалкилена, меркапто, нитро, -NRARB и -(NRARB)карбонила.
Термин «гетероциклоалкокси» относится к гетероциклоалкильной группе, как определено здесь, присоединенной к основному молекулярному фрагменту через алкоксигруппу.
Термин «гетероциклоалкилтио» относится к гетероциклоалкильной группе, как определено здесь, присоединенной к основному молекулярному фрагменту через алкилтио-группу.
Термин «гетероциклоокси» относится к гетероциклоалкильной группе, как определено здесь, присоединенной к основному молекулярному фрагменту через атом кислорода.
Термин «гетероциклотио» относится к гетероциклоалкильной группе, как определено здесь, присоединенной к основному молекулярному фрагменту через атом серы.
Термин «гетероарилалкокси» относится к гетероарильной группе, как определено здесь, присоединенной к основному молекулярному фрагменту через алкокси группу.
Термин «гетероарилалкилтио» относится к гетероарильной группе, как определено здесь, присоединенной к основному молекулярному фрагменту через алкилтио-группу.
Термин «гетероарилокси» относится к гетероарильной группе, как определено здесь, присоединенной к основному молекулярному фрагменту через атом кислорода.
Термин «гетероарилтио» относится к гетероарильной группе, как определено здесь, присоединенной к основному молекулярному фрагменту через атом серы.
В некоторых вариантах термин «членное кольцо» охватывает любую циклическую структуру. Термин «членный» обозначает количество атомов каркаса, составляющих кольцо. Таким образом, например, циклогексил, пиридин, пиран и тиопиран представляют собой 6-членные кольца, и циклопентил, пиррол, фуран и тиофен представляют собой 5-членные кольца.
Термин «неароматический 5, 6, 7, 8, 9, 10, 11 или 12-членный бициклический гетероцикл», используемый здесь, означает гетероциклоалкил, как определено здесь, состоящий из двух карбоциклических колец, конденсированных вместе по одному и тому же атому углерода (образуя спиро структуру) или по различным атомам углерода (кольца которых имеют одну или несколько общих связей), содержащий от 5 до 12 атомов во всей кольцевой системе, при этом один или несколько атомов, образующих кольцо, являются гетероатомами. Типичные примеры неароматического 5, 6, 7, 8, 9, 10, 11 или 12-членного бициклического гетероциклического кольца включают, но без ограничения, 2-азабицикло[2.2.1]гептанил, 7-азабицикло[2.2.1]гептанил, 2-азабицикло[3.2.0]гептанил, 3-азабицикло[3.2.0]гептанил, 4-азаспиро[2.4]гептанил, 5-азаспиро[2.4]гептанил, 2-окса-5-азабицикло[2.2.1]гептанил, 4-азаспиро[2.5]октанил, 5-азаспиро[2.5]октанил, 5-азаспиро[3.4]октанил, 6-азаспиро[3.4]октанил, 4-окса-7-азаспиро[2.5]октанил, 2-азабицикло[2.2.2]октанил, 1,3-диазабицикло[2.2.2]октанил, 5-азаспиро[3.5]нонанил, 6-азаспиро [3.5]нонанил, 5-оксо-8-азаспиро[3.5]нонанил, октагидроциклопента[c]пирролил, октагидро-1H-хинолизинил, 2,3,4,6,7,9а-гексагидро-1H-хинолизинил, декагидропиридо[1,2-а]азепинил, декагидро-1H-пиридо[1,2-а]азоцинил, 1-азабицикло [2.2.1]гептанил, 1-азабицикло[3.3.1]нонанил, хинуклидинил и 1-азабицикло[4.4.0]деканил.
Термин «гидроксиалкилен», используемый здесь, означает, по меньшей мере, одну гидроксильную группу, как определено здесь, присоединенную к основному молекулярному фрагменту через алкиленовую группу, как определено здесь. Типичные примеры гидроксиалкилена включают, но без ограничения, гидроксиметилен, 2-гидроксиэтилен, 3-гидроксипропилен и 4-гидроксигептилен.
Термин «NRANRB», используемый здесь, означает две группы, RA и RB, которые присоединены к основному молекулярному фрагменту через атом азота. RA и RB, каждый, независимо представляет собой водород, алкил и алкилкарбонил. Типичные примеры NRARB включают, но без ограничения, амино, метиламино, ацетиламино и ацетилметиламино.
Термин «(NRANRB)карбонил», используемый здесь, означает RARB, группу, как определено здесь, присоединенную к основному молекулярному фрагменту через карбонильную группу, как определено здесь. Типичные примеры (NRARB)карбонила включают, но без ограничения, аминокарбонил, (метиламино)карбонил, (диметиламино)карбонил и (этилметиламино)карбонил.
Термин «NRCNRD», используемый здесь, означает две группы, RC и RD, которые присоединены к основному молекулярному фрагменту через атом азота. RC и RD, каждая, независимо выбрана из водорода, алкила и алкилкарбонила. Типичные примеры NRCRD включают, но без ограничения, амино, метиламино, ацетиламино и ацетилметиламино.
Термин «(NRCNRD)карбонил», используемый здесь, означает RCRD группу, как определено здесь, присоединенную к основному молекулярному фрагменту через карбонильную группу, как определено здесь. Типичные примеры (NRCRD)карбонила включают, но без ограничения, аминокарбонил, (метиламино)карбонил, (диметиламино)карбонил и (этилметиламино)карбонил.
Используемый здесь термин «меркаптил» относится к (алкил) S-группе.
Используемый здесь термин «фрагмент» относится к конкретному сегменту или функциональной группе молекулы. Химические фрагменты часто представляют собой распознаваемые химические соединения, включенные или присоединенные к молекуле.
Используемый здесь термин «сульфинил» относится к -S(=O)-R, где R выбран из группы, состоящей из алкила, циклоалкила, арила, гетероарила (присоединенного через кольцевой атом углерода) и гетероциклоалкила (присоединенного через кольцевой атом углерода).
Используемый здесь термин «сульфонил» относится к -S(=O)2-R, где R выбран из группы, состоящей из алкила, циклоалкила, арила, гетероарила (присоединенного через кольцевой атом углерода) и гетероциклоалкила (присоединенного через кольцевой атом углерода).
Используемый здесь термин «O карбокси» относится к группе формулы RC(=O)O-.
Используемый здесь термин «C карбокси» относится к группе формулы -C(=O)OR.
Используемый здесь термин «ацетил» относится к группе формулы -С(=O)CH3.
Используемый здесь термин «тригалометансульфонил» относится к группе формулы X3CS(=O)2-, где X представляет собой галоген.
Используемый здесь термин «изоцианато» относится к группе формулы -NCO.
Используемый здесь термин «тиоцианато» относится к группе формулы -CNS.
Используемый здесь термин «изотиоцианато» относится к группе формулы -NCS.
Используемый здесь термин «S сульфонамидо» относится к группе формулы -S(=O)2NR2.
Используемый здесь термин «N сульфонамидо» относится к группе формулы -RS(=O)2NH-.
Используемый здесь термин «тригалометансульфонамидо» относится к группе формулы X3CS(=O)2NR-.
Используемый здесь термин «O карбамил» относится к группе формулы -OC(=O)NR2.
Используемый здесь термин «N карбамил» относится к группе формулы ROC(=O)NH-.
Используемый здесь термин «O тиокарбамил» относится к группе формулы -OC(=S)NR2.
Используемый здесь термин «N тиокарбамил» относится к группе формулы ROC(=S)NH-.
Используемый здесь термин «C амидо» относится к группе формулы -C(=O)NR2.
Используемый здесь термин «N амидо» относится к группе формулы RC(=O)NH-.
Используемый здесь заместитель «R», появляющийся как таковой и без числового обозначения, относится к заместителю, выбранному из алкила, циклоалкила, арила, гетероарила (связанного через атом углерода кольца) и неароматического гетероцикла (связанного через атом углерода кольца).
Термин «замещенный» означает, что названная группа является необязательно замещенной (замещенной или незамещенной) одной или несколькими дополнительными группами, отдельно и независимо выбранными из алкила, циклоалкила, арила, гетероарила, гетероалициклической группы, гидрокси, алкокси, арилокси, меркапто, алкилтио, арилтио, алкилсульфоксида, арилсульфоксида, алкилсульфона, арилсульфона, циано, галогена, карбонила, тиокарбонила, изоцианато, тиоцианато, изотиоцианато, нитро, пергалогеналкила, перфторалкила, силила и амино, включая моно- и дизамещенные аминогруппы, и их производных, содержащих защитные группы. В качестве примера, необязательные заместители представляют собой LsRs, где каждый Ls независимо выбран из связи, -O-, -C(=O)-, -S-, -S(=O)-, S(=O)2-, -NH-, -NHC(O)-, -C(O)NH-, -S(=O)2NH-, -NHS(=O)2, -OC(O)NH-, -NHC(O)O-, -(замещенного или незамещенного C1-C6алкила) или -(замещенного или незамещенного C2-C6 алкенила); и каждый Rs независимо выбран из H, (замещенного или незамещенного низшего алкила), (замещенного или незамещенного низшего циклоалкила), гетероарила или гетероалкила.
Термин «защитная группа» относится к удаляемой группе, которая модифицирует реакционную способность функциональной группы, например, гидроксильной, кетона или амина, защищает от нежелательной реакции по ходу синтеза и позже подлежит удалению. Примеры гидрокси-защитных групп включают, но без ограничения, метилтиометил, трет-диметилсилил, трет-бутилдифенилсилил, простые эфиры, такие как метоксиметиловый, и сложные эфиры, включающие ацетил, бензоил и им подобные. Примеры защитных групп кетона включают, но без ограничения, кетали, оксимы, O-замещенные оксимы, например O-бензилоксим, O-фенилтиометилоксим, 1-изопропоксициклогексилоксим, и им подобные. Примеры аминозащитных групп включают, но без ограничения, трет-бутоксикарбонил (Boc) и карбобензоилокси (Cbz).
Термин «необязательно замещенный», как определено здесь, означает, что указанная группа является незамещенной или замещенной одним или несколькими заместителями, как определено здесь.
Термин «защищенный гидрокси» относится к гидроксильной группе, замещенной гидрокси-защитной группой, как определено выше.
В некоторых вариантах соединения, описанные здесь, существуют в виде стереоизомеров, в которых присутствуют асимметрические или хиральные центры. Стереоизомеры обозначаются как (R) или (S) в зависимости от конфигурации заместителей вокруг хирального атома углерода. Термин (R) и (S), используемый здесь, представляет собой конфигурации, как определено в IUPAC 1974 Recommendations for Section E, Fundamental Stereochemistry, Pure Appl. Chem., (1976), 45:13-30, включенной здесь посредством отсылки. Варианты, описанные здесь, в частности включают различные стереоизомеры и их смеси. Стереоизомеры включают энантиомеры, диастереомеры и смеси энантиомеров или диастереомеров. В некоторых вариантах индивидуальные стереоизомеры соединений приготовлены синтетически из коммерчески доступных исходных материалов, которые содержат ассиметрические или хиральные центры, или путем приготовления рацемических смесей с последующим повторным растворением. Данные способы повторного растворения характеризуются (1) присоединением смеси энантиомеров к хиральному вспомогательному веществу, разделением полученной смеси диастереомеров путем рекристаллизации или хроматографии и высвобождением оптически чистого продукта из вспомогательного вещества или (2) прямым разделением смеси оптических энантиомеров на хиральной хроматографической колонке.
Способы и составы, описанные здесь, включают использование N-оксидов, кристаллических форм (также известных как полиморфы) или фармацевтически приемлемых солей соединений, описанных здесь, а также активных метаболитов этих соединений, имеющих такой же тип активности. В некоторых случаях соединения существуют в виде таутомеров. Все таутомеры включены в объем соединений, представленных здесь. В некоторых вариантах соединения, описанные здесь, существуют в несольватированной, а также сольватированной формах с фармацевтически приемлемыми растворителями, такими как вода, этанол и им подобные. Сольватированные формы соединений, представленные здесь, также предполагаются быть здесь раскрытыми.
Во всем описании изобретения группы и их заместители выбраны в определенных вариантах для обеспечения стабильных фрагментов и соединений.
Примеры
Даже если все три таутомерные структуры могут существовать, все общие структуры и все примеры, имеющие 1,2,4-триазольный фрагмент, показаны только в одной таутомерией форме, такой как 4H-1,2,4-триазол, для простоты изложения и для сопоставления с его прямыми аналогами, такими как примеры, содержащие 1,3,4-оксадиазольный фрагмент. Доменирующая таутомерная структура зависит от заместителей на триазольном фрагменте и от условий реакции. Как представлено в уровне технике, 1H-1,2,4-триазол, как правило, является наиболее общей таутомерией формой, особенно, если аминозаместитель присоединен к кольцу. Использование только 4H-таутомерной формы для графического представления структур для простоты изложения не предполагает, что соединения по примерам, показанным ниже, обязательно существуют в этой конкретной таутомерной форме. Используя такой подход, IUPAC наименования для примеров, представленных ниже, обеспечены только для 4H-таутомерной формы, тем не менее понятно, что для правильной идентификации конкретной таутомерной структуры нумерация заместителей может отличаться от представленной.
Пример 1. Синтез 1,2,4-триазольных ядер:
Синтез 1,2,4-триазольных ядер проводили, как показано на схеме ниже. Подробная методика эксперимента и аналитические данные следуют далее.

Методика эксперимента:
Стадия-2: Приготовление гидрокси-бензогидразида

В перемешанный раствор метил 3-гидроксибензоата (7 г, 46.05 ммоль) в этаноле (150 мл) добавляли гидразин-гидрат (23 г, 460.5 ммоль) при комнатной температуре, и реакционную смесь нагревали с обратным холодильником в течение 10-12 ч. Ход реакции контролировали с помощью ТСХ; после исчезновения исходного материала реакционную массу охлаждали до комнатной температуры, и отгоняли этанол для получения сырого продукта. В этот неочищенный продукт добавляли ацетон (20 мл) при 10-15°C и перемешивали в н-гексане (100 мл) в течение 30 мин. Белый твердый осадок фильтровали и сушили в вакууме при 55°C для получения чистого продукта (Выход: 6.9 г, 85.71% теоретически).
Выход: 95.71%
ВЭЖХ чистота: 98.7%
1H ЯМР: Соответствует структуре.
ЖХ-МС: m/z=153 (МН+)
Стадия-3: Приготовление 3-(трифторметил)фенилизотиоцианата

В перемешанный раствор 3-(трифторметил)анилина (20 г, 124.2 ммоль) в DCM (100 мл) добавляли тиофосген (21.24 г, 186.4 ммоль) при 5-10°C, и реакционную смесь перемешивали при комнатной температуре в течение 1-2 ч. Ход реакции контролировали с помощью ТСХ (подвижная фаза - 40% этилацетат в н-Гексане, Rf. S.M. - 0.25, продукт - 0.5). После исчезновения исходного материала реакционную массу разбавляли DCM, органический слой промывали 10% NaHCO3, водой и солевым раствором. Органический слой сушили и концентрировали в вакууме при температуре ниже, чем 45°C для получения продукта в виде желтого масла (Выход: 19.2 г, 76.19% теоретически).
Выход: 76.19%
1Н ЯМР: Соответствует структуре
Стадия-4: Приготовление (3-трифторметил)фенилтиомочевины

В перемешанный раствор 1-изотиоцианато-3-(трифторметил)бензола (10 г, 49.26 ммоль) в метаноле (100 мл) добавляли водный раствор аммония (6.69 г, 394 ммоль) по каплям при 5°C-10°C. После завершения добавления аммония реакционную смесь перемешивали при комнатной температуре в течение 2-3 ч. Когда ТСХ (подвижная фаза - 40% этилацетат в н-Гексане, Rf. S.M. - 0.80, продукт - 0.2) показала отсутствие исходного материала и образование продукта, метанол концентрировали, добавляли воду и экстрагировали этилацетатом. Органический слой промывали солевым раствором, сушили над Na2SO4 и концентрировали для получения чистого продукта в виде грязно-белого твердого вещества (Выход: 9.2 г, 84.94% теоретически).
Выход: 84.94%
ВЭЖХ чистота: 99.75%
1Н ЯМР: Соответствует структуре
ЖХ-МС: MH+: 221 (Мол. масса 220)
Стадия-5: Приготовление гидроиодида S-метилизотиомочевины

В раствор 1-(3-(трифторметил)фенил)тиомочевины (15 г, 68 ммоль) в метаноле (150 мл) добавляли метилиодид (15.13 г, 102 ммоль) по каплям при комнатной температуре. Реакционную смесь перемешивали при 50°C в течение 7-8 ч. Когда ТСХ (подвижная фаза - 5% метанол в хлороформе, Rf. S.M. - 0.30, продукт - 0.2) показала отсутствие исходного материала и образование продукта, метанол концентрировали для получения чистого продукта в виде грязно-белого твердого вещества (Выход: 22 г, 89.39% теоретически).
Выход: 89.39%
ВЭЖХ чистота: 95.84%
1H ЯМР: Соответствует структуре
ЖХ-МС: MH+: 235 (Мол. масса 234)
Стадия-6: Приготовление каркаса - Способ 1
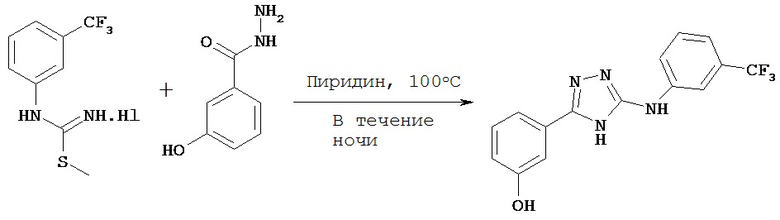
В суспензию метил S-Метил-3-(трифторметил)фенилизотиомочевины гидроиодида (5 г, 13.81 ммоль) в безводном пиридине (30 мл) добавляли 3-гидрокси бензогидразид (2.32 г, 15.26 ммоль) в атмосфере N2. После завершения добавления гидразида реакционную смесь перемешивали при 100°C в течение 10-12 ч. Когда ТСХ (подвижная фаза - 10% метанол в хлороформе, Rf. S.M. - 0.20, продукт - 0.4) показала отсутствие исходного материала, реакционную смесь охлаждали до комнатной температуры и пиридин концентрировали в вакууме для получения сырого продукта (желтого масла). Продукт очищали колоночной хроматографией для получения требуемого каркаса в чистой форме.
Выход: 42.35%
ВЭЖХ чистота: 98.08%
1Н ЯМР: Соответствует структуре
ЖХ-МС: MH+: 321 (Мол. масса 320)
Стадия-6: Приготовление каркаса - Способ 2

В суспензию метил S-Метил-3-(трифторметил)фенилизотиомочевины иодгидрида (6 г, 16.57 ммоль) в ацетонитриле (60 мл) добавляли 2,6-лутидин (3.53 г, 33 ммоль) в атмосфере N2 при комнатной температуре с последующим 4-гидроксибензогидразидом (3.02 г, 19.8 ммоль) и перемешивали при комнатной температуре в течение 15 мин. После завершения добавления гидразида реакционную смесь перемешивали при 80°C в течение 18-20 ч. Когда ТСХ (подвижная фаза - 10% метанол в хлороформе, Rf. S.M. - 0.20, продукт - 0.5) показала отсутствие исходного материала и образование продукта, реакционную смесь охлаждали до комнатной температуры, и ацетонитрил удаляли в вакууме. Остаток поглощали в этилацетате, и органический слой промывали водой (2Х) с последующим 10% раствором лимонной кислоты (2Х) и под конец солевым раствором. Органический слой отделяли и сушили над Na2SO4 (твердый), и концентрировали для получения сырого продукта. Неочищенный продукт очищали колоночной хроматографией для получения требуемого продукта (3.1 г).
Выход: 58.84%
ВЭЖХ чистота: 96%
ЖХ-МС: MH+: 321 (Мол. масса 320)
Пример 2: Синтез 1,3.4-оксадиазольных ядер:
Синтез 1,3,4-оксадиазольных ядер проводили, как показано на схеме ниже:

Методика эксперимента
Стадия-4: Приготовление каркаса

В суспензию метил 3-гидроксибензогидразида (1 г, 6.5 ммоль) в THF: Толуол: DMF (5 мл) каждого добавляли 1-изотиоцианато-3-(трифторметил)бензол (1.33 г, 6.5 ммоль) в атмосфере N2↑ при комнатной температуре. После завершения добавления изотиоцианата реакционную смесь перемешивали при 80°C в течение 30 мин. Затем добавляли DCC (1.49 г, 7.23 ммоль), и реакционную смесь перемешивали при 80°C в течение 5-6 ч. Когда ТСХ (подвижная фаза - 5% метанол в хлороформе, Rf. S.M. - 0.30, продукт - 0.5) показала отсутствие исходного материала и образование продукта, реакционную смесь охлаждали до комнатной температуры; добавляли воду и реакционную смесь экстрагировали этилацетатом (3×50 мл). Объединенный органический слой сушили над Na2SO4 и концентрировали в вакууме для получения сырого продукта. Неочищенный продукт очищали колоночной хроматографией для получения требуемого продукта (750 мг).
Выход: 35.5%
ВЭЖХ чистота: 90.6%
1H ЯМР: Соответствует структуре
ЖХ-МС: MH+: 322 (Мол. масса 321)
Пример 3: Синтез 1.3,4-тиадиазольных ядер:
Синтез 1,3,4-тиадиазольных ядер проводили, как показано на схеме ниже.

Методика эксперимента для синтеза 1,3,4-тиадиазольных ядер:
Стадия-2: Приготовление N-(3-(трифторметил)фенил)гидразинкарботиоамида

В перемешанный раствор 1-изотиоцианато-3-(трифторметил)бензола (250 мг, 1.23 ммоль) в метаноле (5 мл) добавляли гидразин-гидрат (307 мг, 6.16 ммоль) по каплям при 5°C-10°C. После завершения добавления гидразин-гидрата реакционную смесь перемешивали при комнатной температуре в течение 2-3 ч. Когда ТСХ (подвижная фаза - 30% этилацетат в н-Гексане, Rf. S.M. - 0.80, продукт - 0.2) показала отсутствие исходного материала, метанол концентрировали, добавляли воду и экстрагировали этилацетатом. Объединенный органический слой промывали солевым раствором, сушили над Na2SO4 и концентрировали для получения чистого продукта в виде грязно-белого твердого вещества (Выход: 200 мг, 69.4% теоретически).
Выход: 69.4%
ЖХ-МС: MH+: 236 (Мол. масса 235)
Стадия-3: Приготовление каркаса

Раствор N-(3-(трифторметил)фенил)гидразинкарботиоамида (350 мг, 1.5 ммоль), 4-гидроксибензойной кислоты (246 мг, 1.78 ммоль) в POCl3 (2 мл) перемешивали в течение 5-6 ч при 80°C. Когда ТСХ (подвижная фаза - 10% метанола в хлороформе, Rf. S.M. - 0.20, продукт - 0.5) показала отсутствие исходного материала и образование продукта, реакционную смесь охлаждали до 10-15°C, и осаждали ледяной водой; твердый осадок фильтровали и сушили в печи при 50°C. Продукт очищали колоночной хроматографией для получения грязно-белого твердого вещества (Выход: 130 мг, 25.9% теоретически).
Выход: 25.9%
1Н ЯМР: Соответствует структуре
ЖХ-МС: MH+: 338 (Мол. масса 337)
Пример 3. Синтез инвертированных аминотриазольных ядер:
Синтез 1,2,4-триазольных ядер проводили, как показано на схеме ниже.

Методика эксперимента:
Нижеприведенная методика эксперимента аналогична методике, описанной для синтеза 1,2,4-триазольных ядер. Аналитические данные для промежуточных соединений и каркасов представлены ниже.
(1) Приготовление каркаса Е43:
Стадия-1: Приготовление гидразида 9а

Стадии-2 и 3: Приготовление тиомочевины 12a

Стадия-4: Приготовление гидроиодида S-метил-изотиомочевины 6a

Стадия-5: Приготовление каркаса 15a

(II) Приготовление каркаса К36:
Стадия-4: Приготовление гидроиодида S-метил-изотиомочевины 6b

Стадия-5: Приготовление каркаса 15b

Пример 4: Синтез 2-амино-имидазольных ядер
Синтез 2-амино-имидазольных ядер проводили, как показано на нижеприведенной схеме. Подробная методика эксперимента и аналитические данные следуют далее.

Методики экспериментов для синтеза 2-амино-имидазольного ядра К38:
Стадия-1: Приготовление ди-Boc-гуанидина
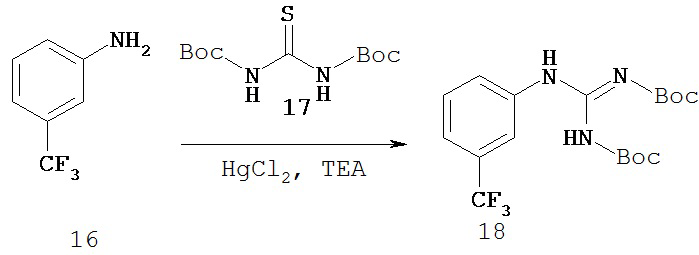
В суспензию 3-трифторметиланилина (81 мг, 0.5 ммоль), бис-Boc-тиомочевины (138 мг, 0.5 ммоль) и Et3N (152 мг, 1.5 ммоль) в DCM добавляли хлорид ртути(II) (150 мг, 0.55 ммоль) при 0°C. Реакционную смесь перемешивали при 0°C в течение 1 ч и затем оставляли нагреваться до комнатной температуры, и перемешивали в течение ночи. Когда ТСХ (подвижная фаза - 40% этилацетат в н-Гексане, Rf. S.M. - 0.30, продукт - 0.5) показала образование продукта с некоторым количеством непрореагировавшего исходного материала, реакционную смесь разбавляли этилацетатом, и неорганический побочный продукт отфильтровывали. Органический слой промывали водой (2×25 мл) с последующим солевым раствором (1×25 мл).
Органический слой сушили над Na2SO4 и концентрировали в вакууме для получения продукта (200 мг).
Выход: 89.39%
ВЭЖХ чистота: 95.38%
1H ЯМР: Соответствует структуре
Стадия-2: Приготовление 1-(3-(трифторметил)фенил)гуанидина

В суспензию соединения 18 (806 мг, 2 ммоль) в DCM (10 мл) добавляли TFA (2.28 г, 20 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. ТСХ (подвижная фаза - 40% этилацетат в н-Гексане, Rf. S.M. - 0.6, продукт - 0.2) показала отсутствие исходного материала и образование продукта. Добавляли воду в реакционную смесь и перемешивали в течение 15-20 мин. Водный слой отделяли и подщелачивали 10% раствором NaHCO3 до pH ~10. Свободное основание экстрагировали этилацетатом; объединенный органический слой сушили над Na2SO4 и концентрировали в вакууме для получения продукта (350 мг).
Выход: 72.4%
ВЭЖХ чистота: 84.04%
1H ЯМР: Соответствует структуре
ЖХ-МС: MH+: 338 (Мол. масса 337)
Стадия-3: Приготовление 2-амино-имидазольного каркаса К38
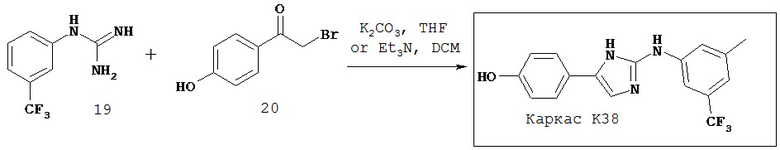
В раствор 1-(3-(трифторметил)фенил)гуанидина (456 мг, 2.25 ммоль) в THF (10 мл) добавляли K2CO3 (249 мг, 1.18 ммоль) с последующим 2-бром-1-(4-гидроксифенил)этаноном (323 мг, 1.5 ммоль) при 0°C. Реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи. ЖХ-МС и ТСХ (подвижная фаза - 10% метанол в хлороформе, Rf. S.M. - 0.2, продукт - 0.35) показали образование продукта и отсутствие исходного материала. Неочищенный продукт после обработки водой очищали препаративной ВЭЖХ для получения 120 мг каркаса К38.
Выход: 25%
ВЭЖХ чистота: 90.6%
1H ЯМР: Соответствует структуре
ЖХ-МС: MH+: 338 (Мол. масса 337)
Пример 5. Синтез иллюстративного соединения библиотеки меркапто Н2-29
Синтез меркапто ядра проводили, как показано на схеме ниже. Подробные методики эксперимента и аналитические данные следуют далее.
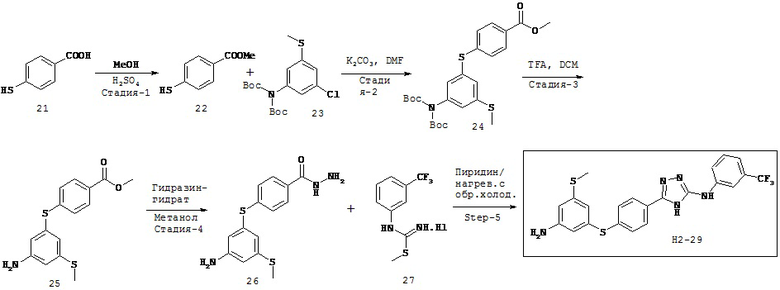
Методики эксперимента для синтеза Н2-29
Стадия-1: Приготовление метил 4-меркаптобензоата

В раствор 4-меркаптобензойной кислоты (5 г, 32.4 ммоль) в метаноле (25 мл) добавляли каталитическое количество N3804 (1-2 капли) и нагревали с обратным холодильником в течение 5-6 ч. ТСХ (подвижная фаза - 10% метанол в хлороформе, Rf. S.M. - 0.2, продукт - 0.6) показала отсутствие исходного материала и образование продукта; метанол отгоняли в вакууме, и остаток разбавляли этилацетатом. Органический слой промывали водой (2×25 мл) с последующим 10% водным раствором бикарбоната натрия. Органический слой сушили над Na2SO4 и концентрировали в вакууме для получения продукта в виде грязно-белого твердого вещества (Выход - 5 г).
Выход: 97.7%
ВЭЖХ чистота: 97.08%
1Н ЯМР: Соответствует структуре
ЖХ-МС: MH+: 169 (Mol. Wt 168)
Стадия - 2: Реакция конденсации меркаптобензоата и ди-Boc-хлор-варианта

В перемешанный раствор ди-Boc-хлорпроизводного 3 (1.35 г, 3.57 ммоль) в DMF (10 мл) добавляли K2CO3 (500 мг, 3.57 ммоль) и метил 4-меркаптобензоат (500 мг, 2.97 ммоль) при комнатной температуре. Реакционную массу перемешивали при комнатной температуре в течение 2-3 ч. ТСХ (подвижная фаза - 40% этилацетат в н-гексане, Rf. S.M. - 0.5, продукт - 0.4) и ЖХ-МС показали образование продукта и отсутствие исходного материала. Реакционную смесь разбавляли этилацетатом (25 мл) и промывали водой (3×30 мл) с последующим солевым раствором. Органический слой сушили над Na2SO4 и концентрировали в вакууме для получения требуемого продукта (900 мг).
Выход: 60%
ВЭЖХ чистота: 92%
ЖХ-МС: MH+: 308 (Mol. Wt 507). Снятая Boc-защита
Стадия-3: Приготовление метил 4-(3-амино-5-(метилтио)фенилтио)бензоата

В перемешанный раствор соединения 24 (287 мг, 0.53 ммоль) в DMF (10 мл) добавляли трифторуксусную кислоту (364 мг, 3.2 ммоль) при 5-10°C.Реакционную массу перемешивали при комнатной температуре в течение ночи. ТСХ (подвижная фаза - 10% метанол в хлороформе, Rf. S.M. - 0.5, продукт - 0.2) и ЖХ-МС показали образование продукта и отсутствие исходного материала. В реакционную смесь добавляли воду и перемешивали в течение 15-20 мин. Водный слой отделяли и подщелачивали 10% раствором NaHCO3 до pH ~10. Свободное основание экстрагировали этилацетатом; объединенный органический слой сушили над Na2SO4 и концентрировали в вакууме для получения продукта (350 мг).
Выход: 73.6%
ВЭЖХ чистота: 97.89%
ЖХ-МС: MH+: 308 (Mol. Wt 307).
Стадия-4: Приготовление 4-(3-амино-5-(метилтио)фенилтио)бензогидразида
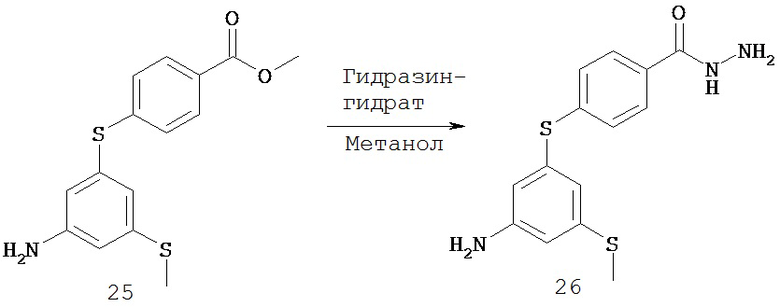
В перемешанный раствор соединения 25 (250 мг, 0.81 ммоль) в метаноле (10 мл) добавляли гидразин-гидрат (325 мг, 6.5 ммоль) при комнатной температуре. Реакционную смесь нагревали с обратным холодильником в течение 5-6 ч. ТСХ (подвижная фаза - 10% метанол в хлороформе, Rf. S.M. - 0.5, продукт - 0.2) и ЖХ-МС показали образование продукта и отсутствие исходного материала. Реакционную смесь охлаждали до комнатной температуры, и метанол отгоняли в вакууме для получения сырого продукта. Продукт перемешивали в н-гексан:ацетон (95:05) и осажденное твердое вещество фильтровали для получения продукта (210 мг).
Выход: 84%
ВЭЖХ чистота: 91.3%
ЖХ-МС: MH+: 308 (Mol. Wt 307).
Стадия-5: Приготовление целевой молекулы Н2-29

Раствор соединения 26 (100 мг, 0.32 ммоль), соединения 27 (129 мг, 0.36 ммоль) в пиридине (5 мл) перемешивали при 80°C в течение 6-7 ч. ТСХ (подвижная фаза - 10% метанол в хлороформе, Rf. S.M. - 0.2, продукт - 0.3) и ЖХ-МС показали образование продукта и отсутствие исходного материала. Реакционную смесь охлаждали до комнатной температуры. Пиридин отгоняли в вакууме, и полученный неочищенный продукт очищали препаративной ВЭЖХ для получения чистого соединения библиотеки меркапто Н2-29 (60 мг).
Выход: 38.96%
ВЭЖХ чистота: 98.71%
1Н ЯМР: Соответствует структуре
ЖХ-МС: MH+: 308 (Mol. Wt 307).
Пример 6. Приготовление библиотеки
Способы создания
(A) Соединения, полученные с помощью реакции конденсации ядра и галоген-варианта: Большинство целевых соединений были получены путем связывания каркасов с различными хлор-вариантами. Способы, используемые для связывания, описаны вкратце ниже.
Связывание проводили с более 50 галоген-вариантами, включая производные пиридина/пиримидина/хинолина/изохинолина. Схема реакции и общая методика эксперимента описана ниже.
Общая методика реакции конденсации галоген-вариантов с K1/K2

Обозначения: (i) Cs2CO3, DMF, 110°C, в течение ночи; (i) Cs2CO3, THF, 65°C, в течение ночи; (i) Cs2CO3, DMF, MW, 200/240°C, 20-30 мин.
Способ A1 (условия (i)):
В смесь каркаса (K1/K2, 160 мг, 0.5 ммоль), галоген-варианта (1.2 экв., 0.6 ммоль) и Cs2CO3 (196 мг, 0.6 ммоль) добавляли DMF (0.3 мл), и реакционную смесь нагревали при 110°C в течение ночи. Затем в реакционную смесь добавляли H2O (10 мл) и экстрагировали EtOAc (4×20 мл). Объединенный органический слой промывали водой и солевым раствором, и сушили над NO2SO4. Удаление растворителя при пониженном давлении позволило получить остаток, который очищали препаративной ВЭЖХ для получения чистого продукта.
Выход и чистота: Как указано в Таблице ниже.
Способ А2 (условия (ii)):
В смесь каркаса (K1/K2, 160 мг, 0.5 ммоль), галоген-варианта (1.2 экв., 0.6 ммоль) и Cs2CO3 (196 мг, 0.6 ммоль) добавляли THF (0.3 мл) и реакционную смесь нагревали при 65°C в течение ночи. Затем в реакционную смесь добавляли H2O (10 мл) и экстрагировали EtOAc (4×20 мл). Объединенный органический слой промывали водой и солевым раствором, и сушили над Na2SO4. Удаление растворителя при пониженном давлении позволило получить остаток, который очищали препаративной ВЭЖХ для получения чистого продукта.
Выход и чистота: Как указано в Таблице.
Способ A3 (условия (iii)):
В смесь каркаса (K1/K2, 160 мг, 0.5 ммоль), галоген-варианта (1.2 экв., 0.6 ммоль) и Cs2CO3 (196 мг, 0.6 ммоль) добавляли DMF (0.3 мл), и реакционную смесь нагревали при 200/240°C в микроволновой печи в течение 20-30 мин. Затем в реакционную смесь добавляли H2O (10 мл) и экстрагировали EtOAc (4×20 мл). Объединенный органический слой промывали водой и солевым раствором, и сушили над Na2SO4. Удаление растворителя при пониженном давлении позволило получить остаток, который очищали препаративной ВЭЖХ для получения чистого продукта.
Выход и чистота: Как указано в Таблице.
(B) Соединения, полученные из интермедиата гидразида H3: Некоторые из соединений были приготовлены из обычного интермедиата гидразида (H3, структура показана ниже). Это было указано как «гидразидный способ» под колонкой «способ синтеза» в таблице. Общая схема синтеза этих соединений также показана.
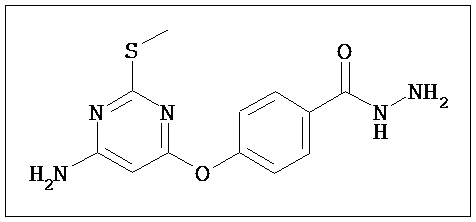

Методики эксперимента для синтеза гидроиодида S-метил-изотиомочевины 29 (3-стадии из 28 посредством соответствующего изотиоцианата и тиомочевины) и для приготовления соединения библиотеки (реакция циклизации, в которую вовлечено соединение 29 и интермедиат гидразид H3) являются такими же, которые описаны ранее в синтезе ядер.
(C) Соединения, полученные путем реакции замещения на 2-пиримидинил (замещение сульфоксида или сильфона)

В перемешанный раствор соединения KG-5-SO2 (150 мг, 0.31 ммоль) в DMF (2.5 мл) добавляли K2CO3 (51.3 мг, 0.37 ммоль) и N-(2-меркаптоэтил)ацетамид (54.5 мг, 0.46 ммоль) при комнатной температуре, и реакционную смесь нагревали при 80°C в течение 3-4 ч. ТСХ (подвижная фаза - 10% MeOH в CHCl3 Rf. S.M. - 0.4), продукт - 0.3) показала отсутствие исходного материала и образование нового пятна. Реакционную смесь охлаждали до комнатной температуры и добавляли воду, и экстрагировали этилацетатом; органический слой промывали солевым раствором, сушили над Na2SO4 и концентрировали в вакууме для получения сырого продукта, который очищали препаративной ВЭЖХ (кол-во: 40 мг).
Выход: 25%
ВЭЖХ чистота: 99.6%
1Н ЯМР: Соответствует структуре
ЖХ-МС: MH+: 532 (Mol. Wt 531)
Пример 7: Жизнеспособность линии клеток рака легкого человека A549
Пример 29: Анализы жизнеспособности клеток
Опухолевые клетки легких (A549) высевали с плотностью 2500 клеток/лунка 96-луночного планшета в готовую питательную среду (DMEM + 10% FBS, антибиотик/антимикотин, фунгизон, L-глутамат, пируват натрия и неосновные аминокислоты). Клетки оставляли для роста в течение ночи и затем тестируемые соединения при концентрации 5 мкМ, 1 мкМ и 0.2 мкМ в DMSO добавляли в свежую готовую питательную среду и добавляли в клетки на 72 ч. Клеточную жизнеспособность измеряли путем добавления в клетки MTT (Sigma) при 5 мг/мл в течение 4 ч и затем удаления среды, и повторного ресуспендирования каждой лунки в 50 мкл DMSO для солюбилизации кристаллов. 96-луночные планшеты считывали на сканирующем спектрофотометре для чтения планшетов (BioTek) при поглощении 560 нм. Результаты обобщены в Таблице ниже.
Иллюстративные соединения и их свойства перечислены в следующей Таблице. Хотя в настоящем изобретении были показаны и описаны предпочтительные варианты, опытному специалисту в данной области будет понятно, что такие варианты приведены исключительно в качестве примера. Множество вариантов, изменений и заместителей будут очевидными опытным специалистам в данной области без отступления от изобретения. Должно быть понятно, что различные альтернативы вариантам изобретения, описанным здесь, могут быть использованы при практическом применении изобретения. Предполагается, что следующая формула изобретения определяет объем изобретения, и что способы и структуры, входящие в объем данной формулы изобретения и их эквиваленты, являются охваченными.



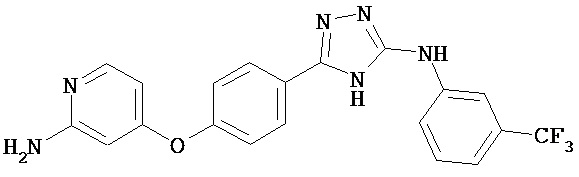



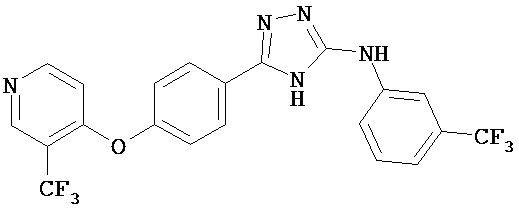

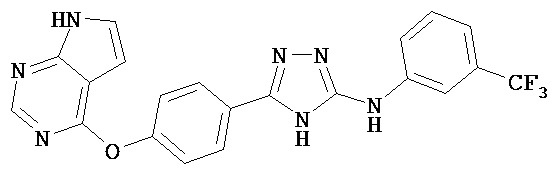






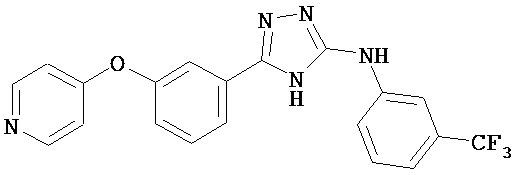

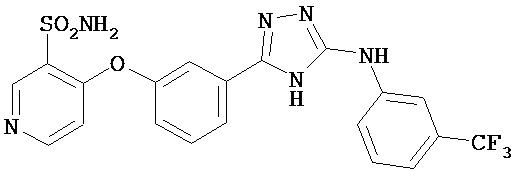

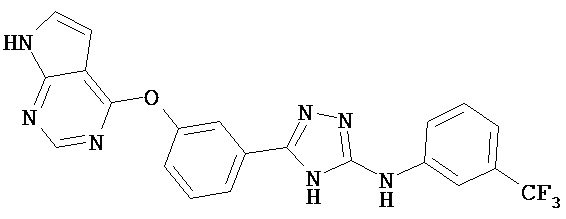







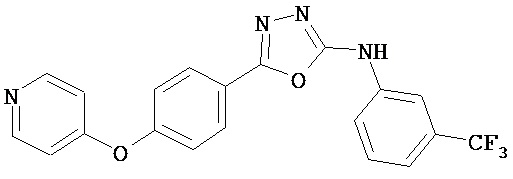






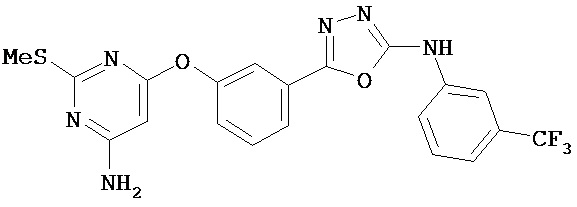

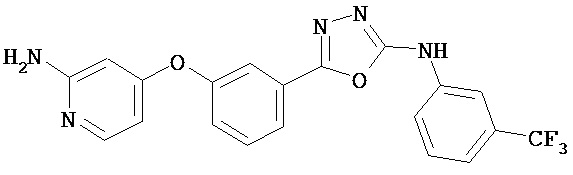





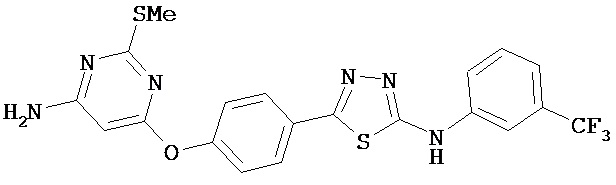


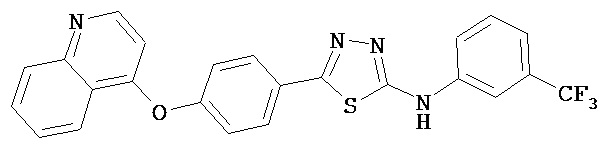
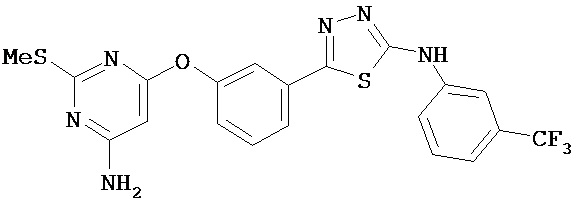
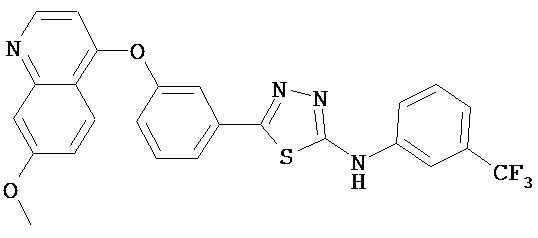










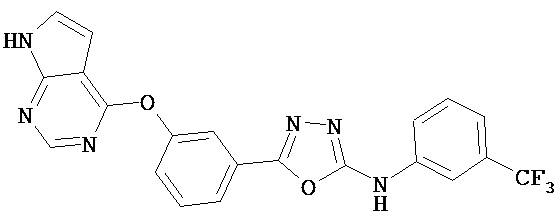








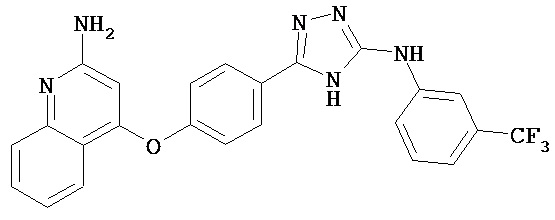









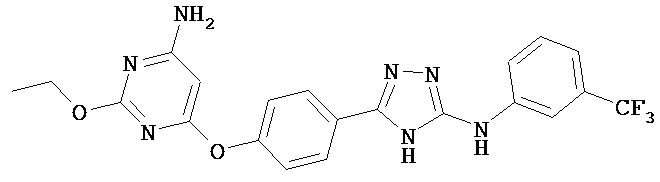









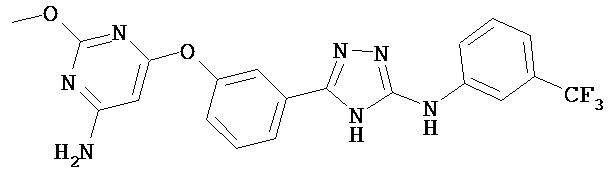


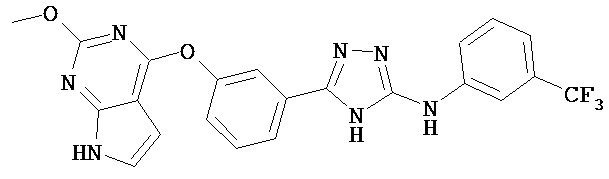

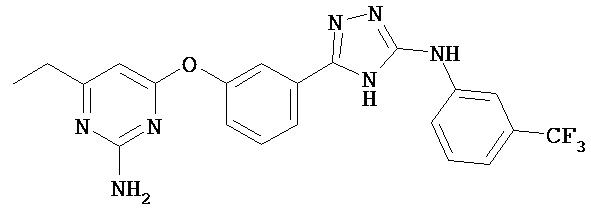

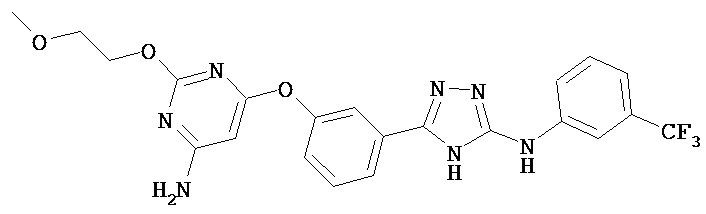










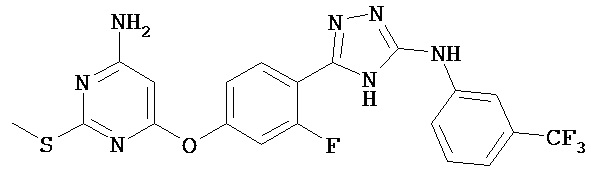



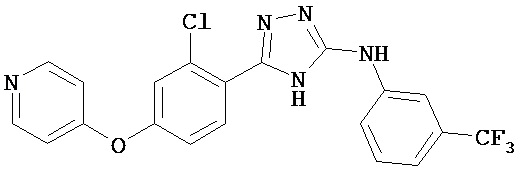







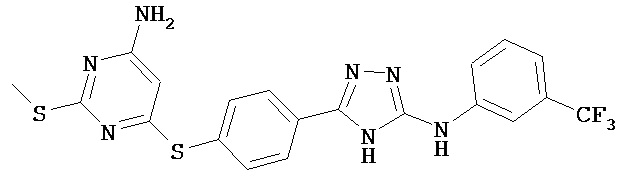
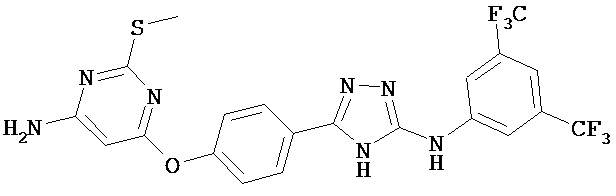
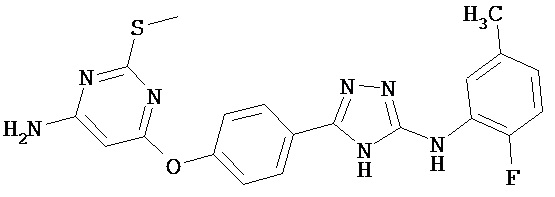



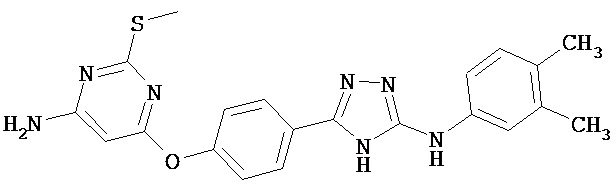
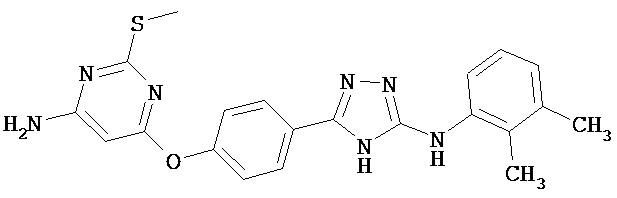







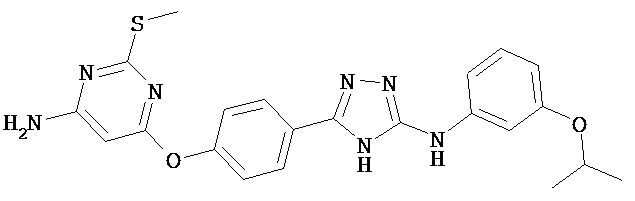



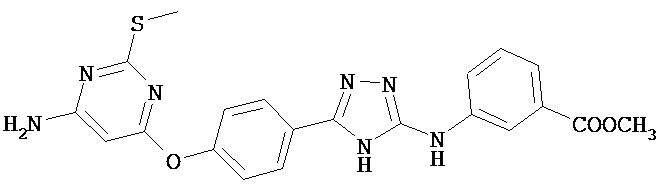













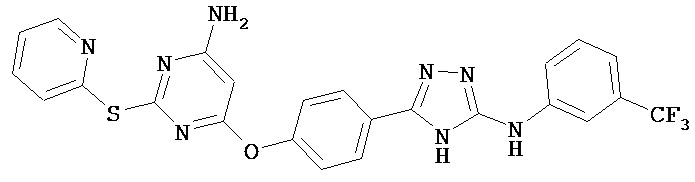

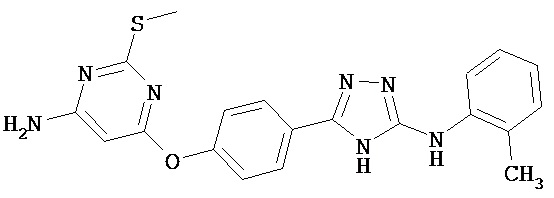





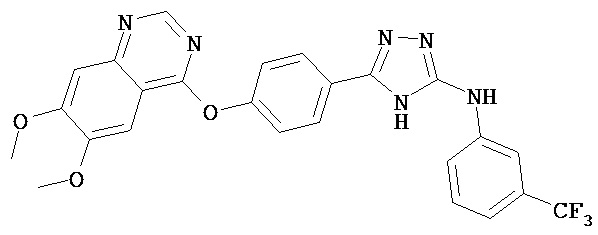

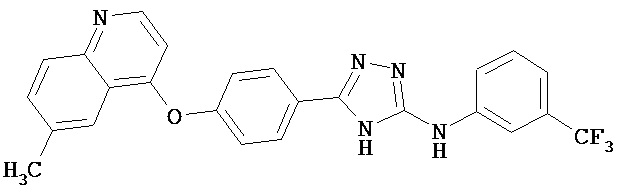




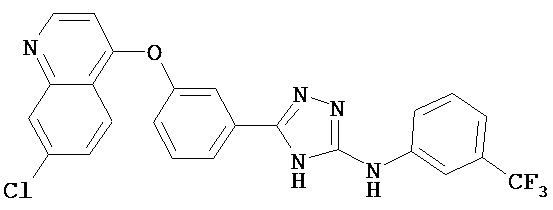


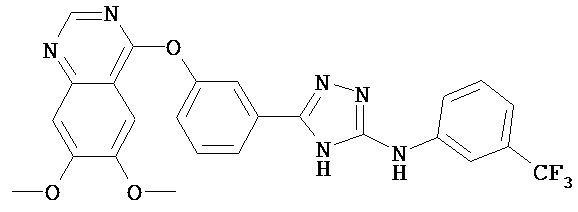

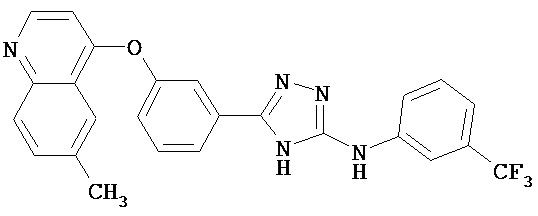


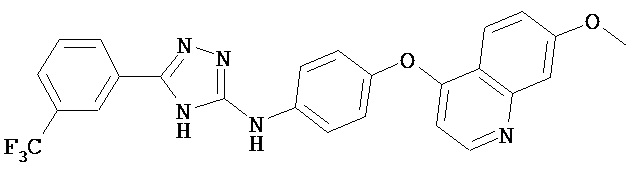





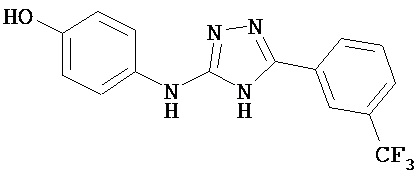





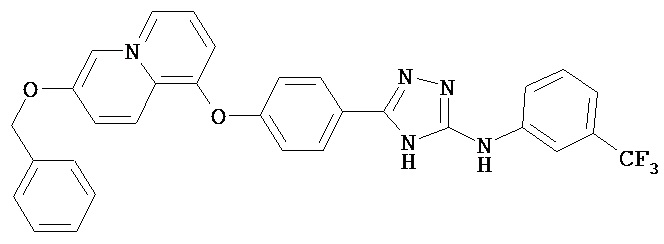



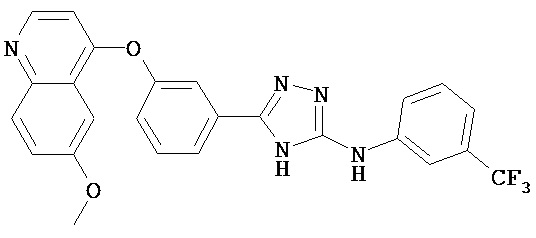






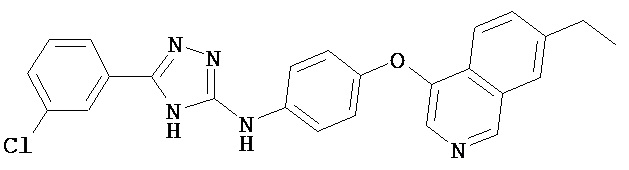

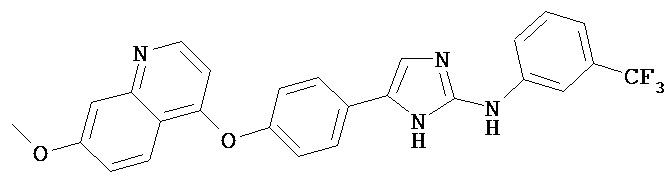

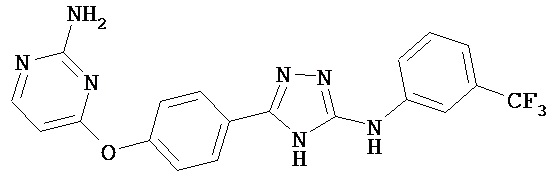



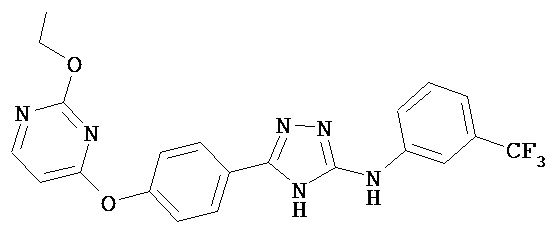






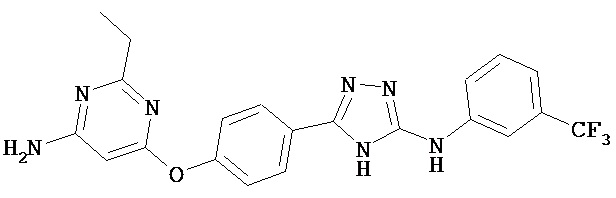



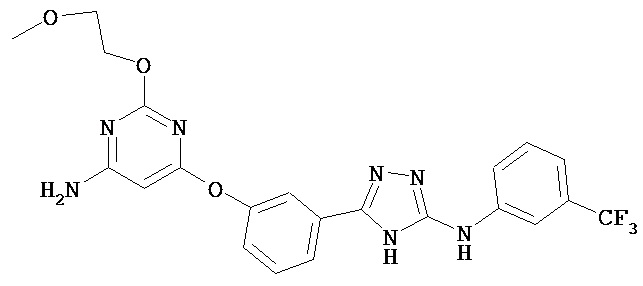


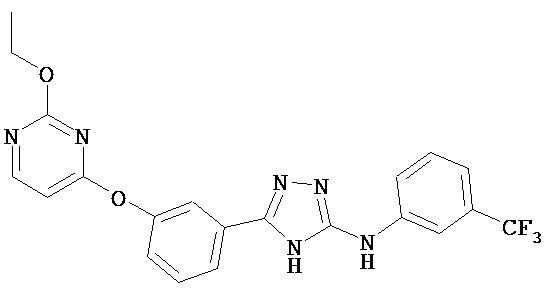











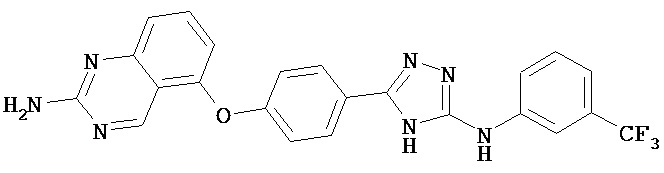


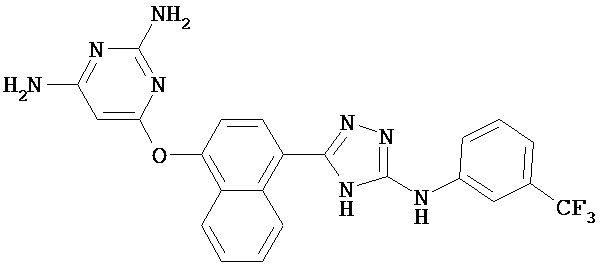

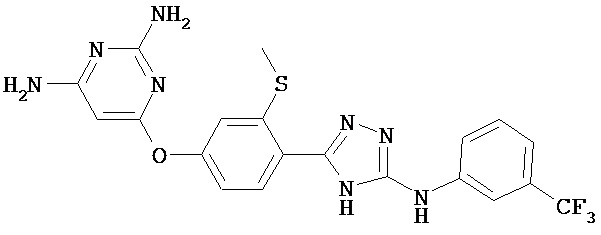




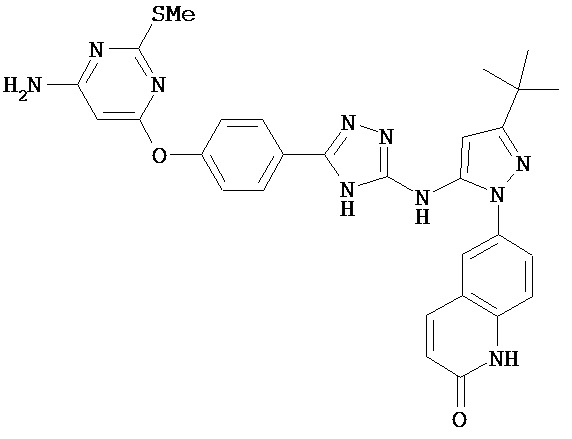
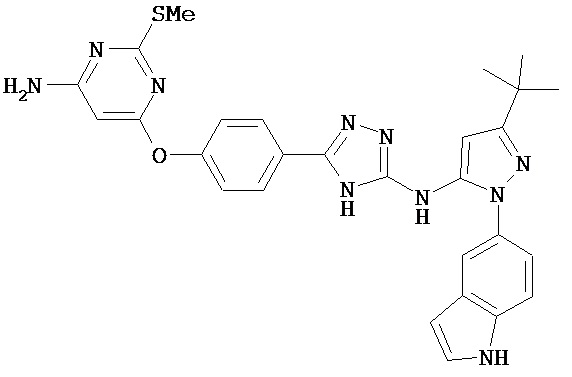





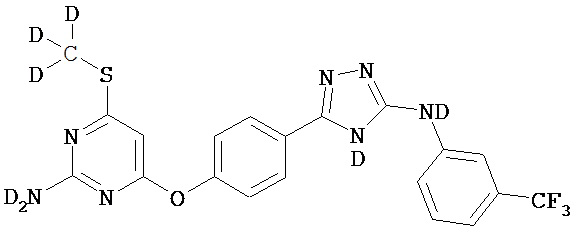

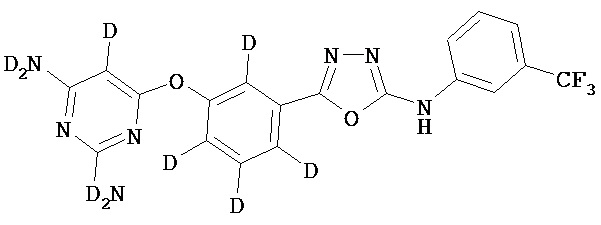





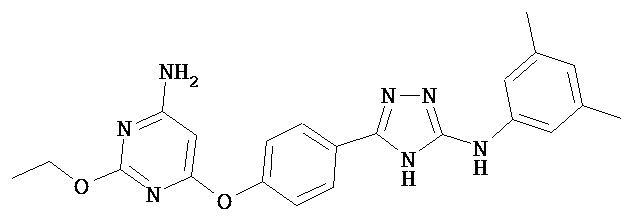

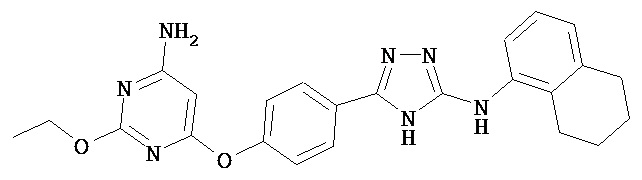

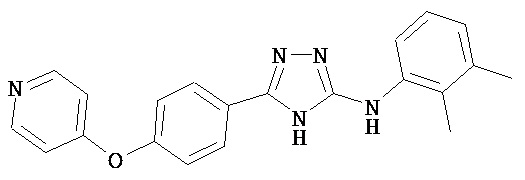




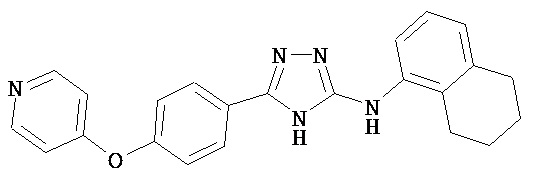


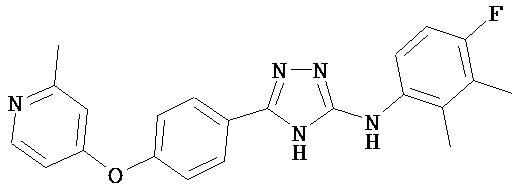
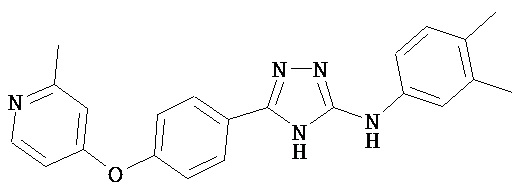
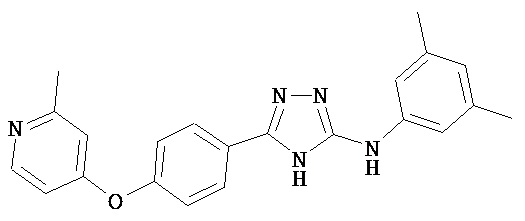

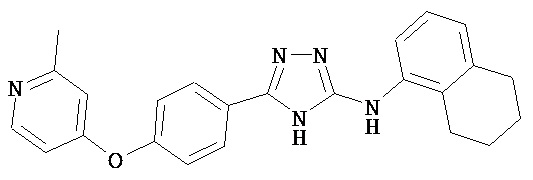

| название | год | авторы | номер документа |
|---|---|---|---|
| КОНДЕНСИРОВАННЫЕ БИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ | 2015 |
|
RU2706007C2 |
| АРИЛЬНЫЕ, ГЕТЕРОАРИЛЬНЫЕ И ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ОПОСРЕДОВАННЫХ КОМПЛЕМЕНТОМ РАССТРОЙСТВ | 2015 |
|
RU2707749C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ СОСТОЯНИЙ, АССОЦИИРОВАННЫХ С АКТИВНОСТЬЮ NLRP | 2019 |
|
RU2795108C2 |
| СОЕДИНЕННЫЕ МОСТИКОВОЙ СВЯЗЬЮ N-ЦИКЛИЧЕСКИЕ СУЛЬФОНАМИДО-ИНГИБИТОРЫ ГАММА-СЕКРЕТАЗЫ | 2006 |
|
RU2422443C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ СОСТОЯНИЙ, АССОЦИИРОВАННЫХ С АКТИВНОСТЬЮ NLRP | 2018 |
|
RU2786719C2 |
| МОНОМЕРНЫЕ ПРОИЗВОДНЫЕ ГЛИКОПЕПТИДНОГО АНТИБИОТИКА | 2005 |
|
RU2424248C2 |
| ИНГИБИТОРЫ ГИСТОНДЕАЦЕТИЛАЗЫ | 2014 |
|
RU2673819C2 |
| ПРИМЕНЕНИЕ 2-(2-НИТРО-4-ТРИФТОРМЕТИЛБЕНЗОИЛ)-1,3-ЦИКЛОГЕКСАНДИОНА ПРИ ЛЕЧЕНИИ БОЛЕЗНИ ПАРКИНСОНА | 2006 |
|
RU2420272C2 |
| КУРС ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АГОНИСТА РЕЦЕПТОРА S1P | 2005 |
|
RU2478384C2 |
| СОЕДИНЕНИЯ | 2016 |
|
RU2734877C2 |
Изобретение относится к соединению формулы (I) или его фармацевтически приемлемой соли, в которой Q представляет собой О; W представляет собой фенил; X отсутствует; Y представляет собой NH; Z1 и Z2 представляют собой N; Z3 представляет собой NR5, где R5 представляет собой водород; R1 представляет собой пиридин или пиримидин; необязательно замещенные C1-С6алкилом, C1-C6алкокси, -NR10R11 или -SOmR12, где R10 и R11 представляют собой водород, R12 представляет собой C1-C6алкил; и m равно 0; R3 представляет собой C1-С6алкил; R2 представляет собой C1-С6алкил, когда р равно 1; или один R2 представляет собой C1-С6алкил и один R2 представляет собой галоген, когда р равно 2; или один R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла; R4 представляет собой водород; р=1 или 2; и n равен 1. Технический результат – гетероциклические соединения, предназначенные для лечения рака. 11 з.п. ф-лы, 1 табл., 8 пр.

1. Соединение формулы (I)

или его фармацевтически приемлемая соль,
в которой:
Q представляет собой О;
W представляет собой фенил;
X отсутствует;
Y представляет собой NH;
Z1 и Z2 представляют собой N;
Z3 представляет собой NR5, где R5 представляет собой водород;
R1 представляет собой пиридин или пиримидин; необязательно замещенные C1-С6алкилом, C1-C6алкокси, -NR10R11 или -SOmR12, где R10 и R11 представляют собой водород, R12 представляет собой C1-C6алкил; и m равно 0;
R3 представляет собой C1-С6алкил;
R2 представляет собой C1-С6алкил, когда р равно 1; или
один R2 представляет собой C1-С6алкил и один R2 представляет собой галоген, когда р равно 2; или
один R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла;
R4 представляет собой водород;
р=1 или 2; и
n равен 1.
2. Соединение по п. 1, в котором R3 представляет собой C1-С6алкил, R2 представляет собой C1-C6алкил и р=1.
3. Соединение по п. 1, в котором R3 представляет собой C1-С6алкил, один R2 представляет собой C1-С6алкил, один R2 представляет собой галоген и р=2.
4. Соединение по п. 1, в котором один R2 и R3 объединены вместе с образованием от пяти- до семичленного карбоцикла.
5. Соединение по п. 1, где соединение формулы (I) выбрано из группы, состоящей из:
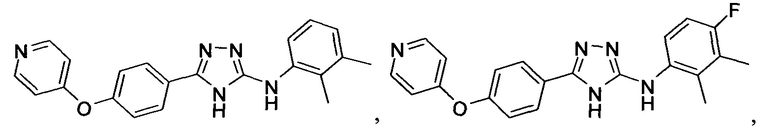



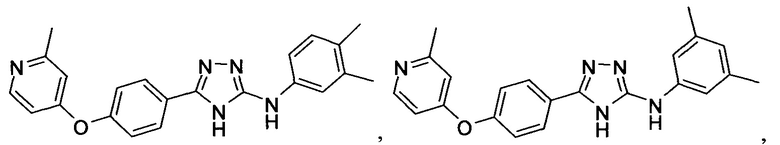
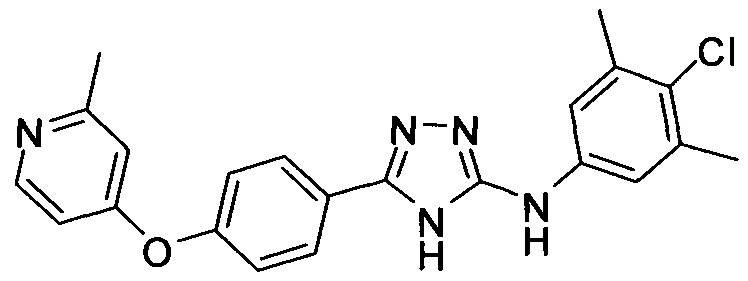 и
и 
или его фармацевтически приемлемая соль.
6. Соединение по п. 1 формулы (II):

или его фармацевтически приемлемая соль,
где:
R8 и R9 независимо выбраны из группы, состоящей из C1-С6алкокси, -NR10R11, и -SOmR12, где R10 и R11 представляют собой водород, R12 представляет собой C1-С6алкил, и m равен 0.
7. Соединение по п. 6, в котором R8 и R9 независимо выбраны из группы, состоящей из C1-C6алкокси и -NR10R11.
8. Соединение по п. 6, в котором R8 и R9 независимо выбраны из группы, состоящей из -SOmR12 и -NR10R11.
9. Соединение по п. 6, в котором R3 представляет собой C1-C6алкил, R2 представляет собой C1-C6алкил, и р=1.
10. Соединение по п. 6, в котором R3 представляет собой C1-С6алкил, один R2 представляет собой C1-С6алкил, один R2 представляет собой галоген, и р=2.
11. Соединение по п. 6, в котором один R2 и R3 объединены вместе с образование от пяти- до семичленного карбоцикла.
12. Соединение по п. 6, где соединение формулы (II) выбрано из группы, состоящей из:

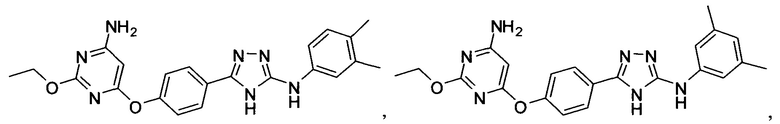

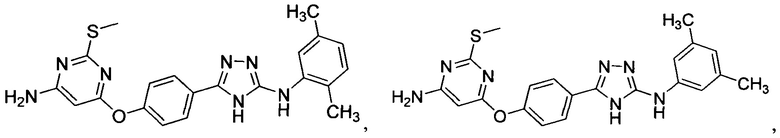
 и
и 
или его фармацевтически приемлемая соль.
| ERIC A.MURPHY et al.: "Disruption of angiogenesis and tumor growth with an orally active drug that stabilizes the inactive state of PDGFR beta/B-RAF", PROCEEDINGS OF THE NATIONAL ACADEMY OF SCIENCES, NATIONAL ACADEMY OF SCIENCES, 2010, vol.107, no.9, p.4299-4304 | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| СОСТАВ ВЗРЫВЧАТОГО ВЕЩЕСТВА | 1997 |
|
RU2128156C1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| GAONKAR S.L | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ДИАМИНОТРИАЗОЛЫ, ПРИГОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2003 |
|
RU2350606C2 |
Авторы
Даты
2018-01-18—Публикация
2011-03-24—Подача