Изобретение относится к области медицины, в частности к онкологии, и может быть использовано как эффективный метод лечения и профилактики больных с запущенными формами онкологических заболеваний органов брюшной полости, осложненных карциноматозом брюшины и малигнизированным асцитом.
Известен способ лечения этих заболеваний путем внутрибрюшинной химиотерапии [Spiliotis J., Halkia Е., and de Bree E. Treatment of peritoneal surface malignancies with hyperthermic intraperitoneal chemotherapy-current perspectives // Curr Oncol. - 2016. - Vol. 23. - P. 266-275].
Недостатками указанного способа являются ограничение результативности лечения особенностями гистологической структуры опухоли, ее размерами, степенью резистентности опухолевой ткани к химиопрепаратам и глубиной проникновения лекарственного средства.
Известен способ лечения с применением комбинации внутрибрюшинной химиотерапии и регионарной гипертермии - внутрибрюшинная химиогипермическая перфузия (HIPEC) [Balaphas А., Belfontali V., Ris F., Lanitis A., Meier R.P., Amram M.L., Roth A., Huber O., Berney Т., Morel P. Management of peritoneal carcinomatosis with cytoreductive surgery and hyperthermic intraperitoneal chemotherapy // Rev Med Suisse. - 2016. - Vol. 12. - P.1190-1194]. Большинство исследователей поддерживают температуру перфузата в брюшной полости в пределах 40,7-44°C в течение 1-2-х часов. Из химиопрепаратов рекомендуют применять митомицин-С в концентрации 10 мг/л раствора (суммарная доза 40-60 мг) и цисплатин в дозировках от 3 до 150 мг/м2 или 20-30 мг/л раствора [Ahmed S., Stewart J.H., Shen P., Votanopoulos K.I., Levine E.A. Outcomes with cytoreductive surgery and HIPEC for peritoneal metastasis // J Surg Oncol. - 2014. - Vol. 110. - P. 575-584].
Недостатками способа HIPEC является высокая травматичность способа, большие сложности повторного применения, высокий процент осложнений, высокая стоимость оборудования и расходного материала.
Известен способ лапароскопической аэрозольной химиотерапии (PIPAC), при котором в брюшной полости в условиях карбоксиперитонеума с помощью специальных устройств создается аэрозоль из химиопрепарата с последующей экспозицией. Способ обладает рядом преимуществ: большая глубина проникновения лекарств, низкая травматичность и его можно использовать многократно. В качестве цитостатиков используют доксорубицин в дозировке 1.5 мг/м2 и цисплатин - 7.5 мг/м2, растворенные в 150 мл физиологического раствора. Экспозиция составляет 30 минут, внутрибрюшное давление 12 мм рт. ст., температура подаваемой смеси - 37°C. Дозы цитостатиков составляют 10% от системных [Reymond М.А. Intraperitoneal Chemotherapy of Peritoneal Carcinomatosis Using Pressurized Aerosol as an Alternative to Liquid Solution: First Evidence for Efficacy // Ann Surg Oncol (2014) 21:553-559].
Недостатками указанного способа являются: применение только в паллиативных целях у инкурабельных больных, крайне низкая дозировка химиопрепаратов, отсутствие показаний в сочетании способа и хирургических вмешательств (межкишечные анастомозы), отсутствие данных о профилактическом применении метода и оптимальных режимов проведения способа.
Цель изобретения - повысить эффективность лечения больных с карциноматозом брюшины и малигнизированным асцитом.
Цель достигается путем создания в брюшной полости микродисперсного аэрозоля химиопрепарата в условиях избыточного давления карбоксиперитонеума с помощью оригинального распылителя с десятикратным увеличением концентрации химиопрепарата (цисплатин 75 мг/м2) и снижением в 2 раза времени экспозиции (15 минут).
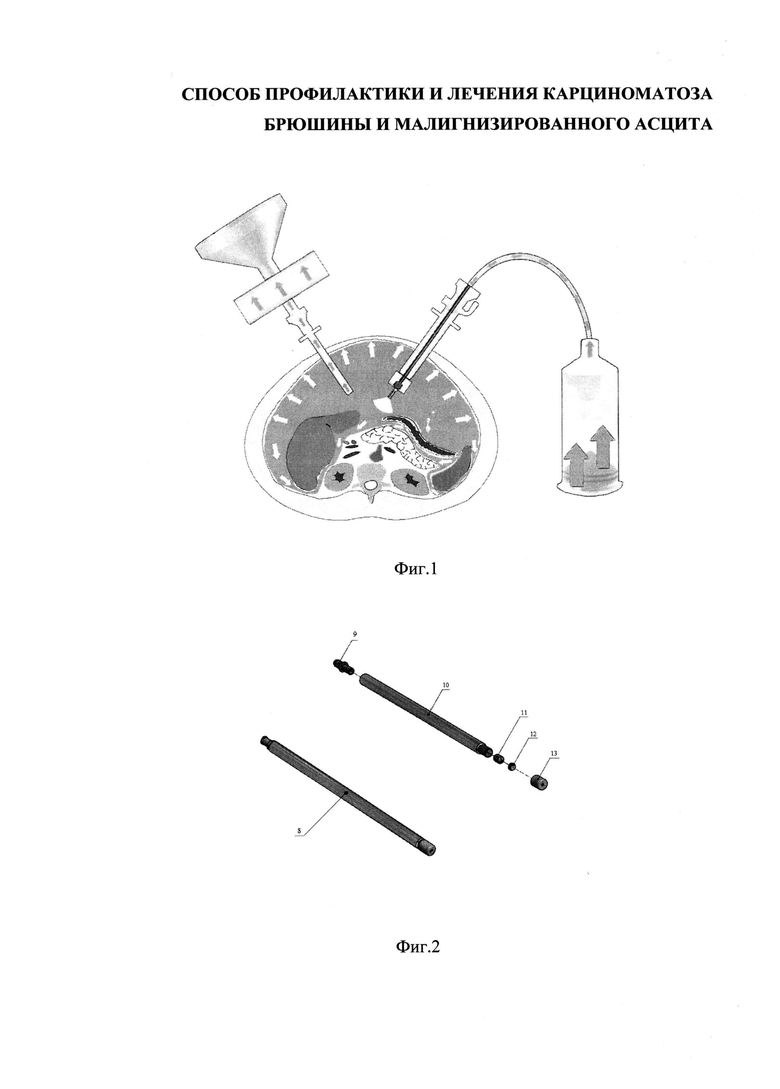
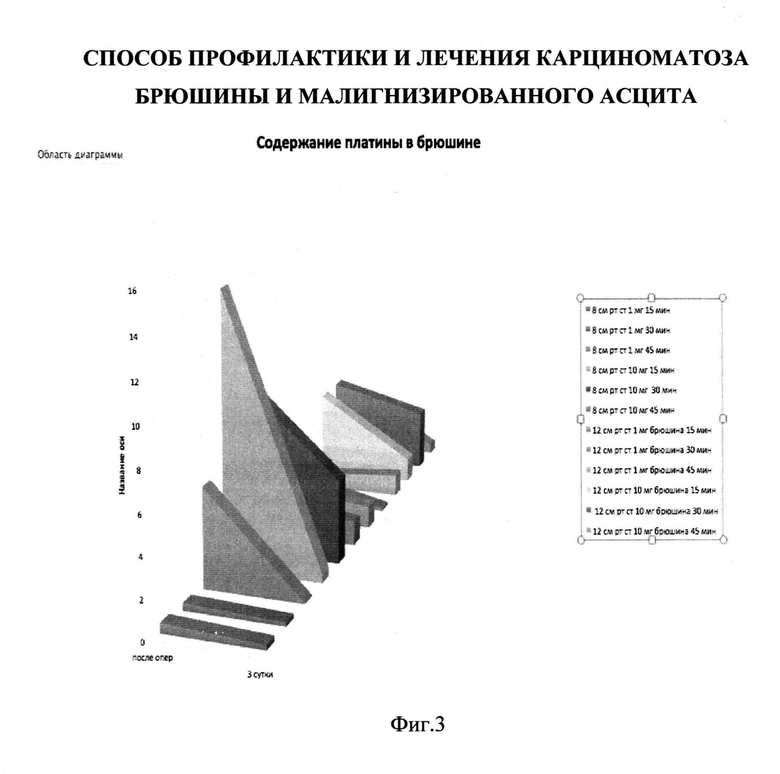
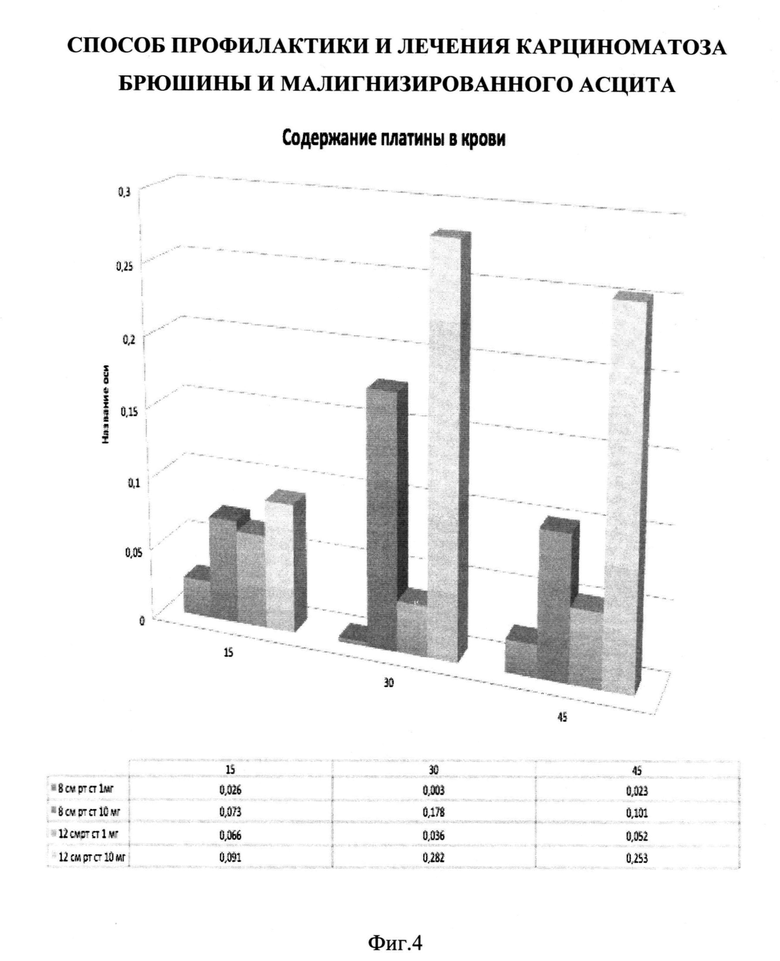
Изобретение поясняется с помощью фиг. 1, на которой приведена схема устройства для проведения аэрозольной лапароскопической внутрибрюшинной химиотерапии, фиг. 2, на которой показано строение распылителя, фиг. 3, на которой приведена концентрация вводимого препарата в тканях, и фиг. 4, на которой приведена концентрация вводимого препарата в крови.
Способ реализуется следующим образом.
Под общим наркозом в брюшную полость устанавливается 2 10-мм троакара (4 и 3). Один - в околопупочную область (3), второй - в правую подвздошную (4). После проведения диагностической лапароскопии в брюшной полости поддерживается карбоксиперитонеум 12 мм рт. ст. В троакар в правой подвздошной области (4) устанавливается и фиксируется лапароскоп для визуального контроля во время сеанса аэрозольной химиотерапии. Во второй троакар (3) помещается оригинальный распылитель (8), соединенный с помощью соединительной системы (7) с инжектором высокого давления (1) (20 бар), в который помещена помпа с химиопрепаратом (2) (75 мг/м2 цисплатина в разведении физиологическим раствором до 200 мл). В течение 5 минут работы инжектора происходит создание аэрозоля. После 15-минутной экспозиции остатки газовой смеси цитостатиков эвакуируются через систему фильтров (5) в емкости для утилизации (6).
Авторами экспериментально установлено, что увеличение времени экспозиции и величины внутрибрюшного давления незначительно способствуют росту концентрации препарата в тканях (Фиг. 3), однако значительно повышают его концентрацию в крови (Фиг. 4), тем самым вызывая токсические эффекты и осложнения. Доказано, что безопасно использовать десятикратно увеличенную концентрацию химиопрепарата - до системно применяемых доз (цисплатин 75 мг/м2) при снижении в 2 раза времени экспозиции (15 минут).
Клинико-лабораторный анализ показал незначительное нарастание значений лейкоцитов, трансаминаз и мочевины через сутки после проведения метода, которые нормализовались к 7 послеоперационному дню.
При гистологическом исследовании органов выявлены признаки дистрофических изменений и расстройства кровообращения в виде умеренного отека стромы и неравномерного кровенаполнения. Изменения в брюшине укладываются в картину слабовыраженного серозного перитонита в реактивную фазу. Изменения в функциональных элементах органов сводились к зернистой и вакуольной (белковой) дистрофии. Нарушение проницаемости клубочков почек сопровождается формированием гиалиновых цилиндров. Гистологических признаков острой почечной недостаточности не выявлено.
Предлагаемый режим проведения лапароскопической аэрозольной химиотерапии не сопровождался угрожающими жизни в послеоперационном периоде патологическими изменениями внутренних органов животных.
Клиническая апробация метода подтвердила его безопасность и эффективность.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения перитонеального канцероматоза при раке яичников | 2021 |
|
RU2745478C1 |
| Способ внутрибрюшного аэрозольного лаважа растворами антисептиков при перитонитах под давлением | 2024 |
|
RU2837717C1 |
| СПОСОБ ПРОВЕДЕНИЯ ВНУТРИБРЮШИННОЙ ХИМИОГИПЕРТЕРМИЧЕСКОЙ ПЕРФУЗИИ БРЮШНОЙ ПОЛОСТИ У ПАЦИЕНТОВ С КАНЦЕРОМАТОЗОМ БРЮШИНЫ | 2015 |
|
RU2582567C1 |
| СПОСОБ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ РАКА ЖЕЛУДКА С ОГРАНИЧЕННОЙ ПЕРИТОНЕАЛЬНОЙ ДИССЕМИНАЦИЕЙ | 2021 |
|
RU2763665C2 |
| СПОСОБ ОДНОМОМЕНТНОЙ УСТАНОВКИ ВНУТРИБРЮШИННОЙ ПОРТ-СИСТЕМЫ В СОЧЕТАНИИ С ИНТРАОПЕРАЦИОННОЙ ГИПЕРТЕРМИЧЕСКОЙ ХИМИОПЕРФУЗИЕЙ (HIPEC), ВКЛЮЧАЮЩИЙ ИНТРАОПЕРАЦИОННУЮ УСТАНОВКУ ВНУТРИБРЮШИННОЙ ПОРТ-СИСТЕМЫ С ВОЗМОЖНОСТЬЮ ДАЛЬНЕЙШЕГО ПРОВЕДЕНИЯ НОРМОТЕРМИЧЕСКОЙ ХИМИОПЕРФУЗИИ ЧЕРЕЗ ПОРТ-СИСТЕМУ | 2020 |
|
RU2740628C1 |
| Способ комбинированного лечения резектабельного местнораспространенного рака желудка с канцероматозом брюшины с применением персонализированной системной и интраперитонеальной химиотерапии | 2021 |
|
RU2773100C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ РАКОМ ЖЕЛУДКА С ОГРАНИЧЕННЫМ ПЕРИТОНЕАЛЬНЫМ КАРЦИНОМАТОЗОМ | 2021 |
|
RU2769493C2 |
| СПОСОБ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ ДИССЕМИНИРОВАННОГО РАКА ЖЕЛУДКА | 2003 |
|
RU2270677C2 |
| СПОСОБ РЕГИОНАЛЬНОЙ ГИПЕРТЕРМИИ БРЮШНОЙ ПОЛОСТИ | 1998 |
|
RU2143292C1 |
| Комбинация дегидроксиметилэпоксихиномицина (DHMEQ) и цитостатиков для лечения рака яичника | 2018 |
|
RU2704020C1 |
Изобретение относится к области медицины, а именно к онкологии. Создают в брюшной полости микродисперсный аэрозоль химиопрепарата в условиях избыточного давления карбоксиперитонеума с помощью распылителя. При этом используют цисплатин в концентрации 75 мг/м2 с временем экспозиции 15 мин. Способ позволяет повысить эффективность лечения и профилактики больных с запущенными формами онкологических заболеваний органов брюшной полости, осложненных карциноматозом брюшины и малигнизированным асцитом, без возникновения патологических изменений внутренних органов, угрожающих жизни в послеоперационном периоде. 4 ил.
Способ профилактики и лечения карциноматоза брюшины и малигнизированного асцита путем создания в брюшной полости микродисперсного аэрозоля химиопрепарата в условиях избыточного давления карбоксиперитонеума с помощью распылителя, отличающийся тем, что используют цисплатин в концентрации 75 мг/м2 с временем экспозиции 15 мин.
| REYMOND М.А | |||
| Intraperitoneal Chemotherapy of Peritoneal Carcinomatosis Using Pressurized Aerosol as an Alternative to Liquid Solution: First Evidence for Efficacy // Ann Surg Oncol., 2014, N 21, p | |||
| Ветряный двигатель | 1922 |
|
SU553A1 |
| КОЛОННЫЙ ЭКСТРАКТОР | 0 |
|
SU258267A1 |
| Устройство для вытягивания стеклянной ленты со свободной поверхности расплавленной стекломассы | 1937 |
|
SU53676A1 |
| ЗАХАРЕНКО А.А | |||
| и др | |||
| Аэрозольная внутрибрюшинная химиотерапия - новый эффективный способ лечения канцероматоза брюшины // Онкология, 2015, т | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Катодная лампа | 1924 |
|
SU834A1 |
| FEDERICO COCCOLINI | |||
| Peritoneal carcinomatosis // World J Gastroenterol., 2013, 19 (41), p | |||
| Вставная фурма для вагранок | 1923 |
|
SU6979A1 |
Авторы
Даты
2018-02-08—Публикация
2016-11-07—Подача