Техническая область
Изобретение относится к новым макролидным антибиотикам в генной инженерии, и особенно левовращающему изовалерилспирамицину III, его кристаллам, фармацевтическим препаратам, способам приготовления и применению в противоинфекционных средствах.
Техническая среда
Макролидные антибиотики занимают важное место в клинике, обладают хорошей активностью в отношении грамположительных бактерий и микоплазмы, также действуют на грамотрицательные бактерии, обладают благоприятной антибактериальной активностью и проницаемостью тканей в отношении распространяющихся токсоплазмов, легионелл и других трудно контролируемых возбудителей, при пероральном употреблении быстро поглощаются с редкими неблагоприятными действиями, в принципе не оказывают отрицательное воздействие на функцию печени и почки, обладают также потенциальной иммунологической регуляцией, в девяностых годах прошлого года считались соперником β-лактамных препаратов при лечении инфекционных заболеваний дыхательных путей взрослых.
Хиральность (Chirality) - основное свойство трехмерных предметов, является одним из основных свойств природы. В качестве важной основы жизненной деятельности, почти все биологические макромолекулы, как протеин, полисахарид, нуклеиновая кислота, ферменты и т.д., хиральные, и эти макромолекулы, как правило, исполняют важную физиологическую функцию внутри тела. Под хиральными лекарствами (chiral drug) понимаются пары оптических антиподов, являющихся зеркальными отражениями друг друга и полученных после ввода хирального центра в молекулярную структуру лекарства. Эти оптические антиподы обладают принципиально аналогичными физико-химическими свойствами, отличаются только оптической активностью, откуда и выделились R (правовращающие) или S (левовращающие), рацемические. За последние 20 лет углубленные изучения в фармацепии доказали различную стереоспецифичность (stereoselectivity) антиподов лекарственных веществ, они имеют различный аффинитет с рецепторами, в результате чего сильно отличаются фармакологические свойства. Антиподы хиральных лекарств, имеющие повышенную активность, называют оптимальными антиподами (Eutomer); а антиподы, имеющие низкую активность или не имеющие активности, называют неактивными антиподами (Distomer). В большинстве случаев, неактивные антиподы не дают эффективности, но они еще частично нейтрализуют эффективность оптимальных антиподов, иногда даже вызывают серьезные токсичные и побочные реакции, что доказало сложность в разнице эффективности лекарственных средств и значительное отличие терапевтического индексантипод одного антипода от его рацемата, как всем известно, что терапевтическая эффективность синтомицина DL-(+-) составляет только половину хлорамфеникола D(-); а активность L-изомера пропранолола (propranolol) в 100 раз больше чем D-изомер; (-) метадон представляет собой сильное болеутоляющее средство, а (+) не действующее. Сильно отличается и токсичность, например, оба антипода талидомида (thalidomide) обладают аналогичным успокаивающим действием в отношении мышей, но только S(-) изомер и его метаболит обладают зародышевой токсичностью и тератогенезом; кетамин - широкораспространенные наркотические и болеутоляющие средства, но они дают галлюцинацию и другие побочные действия. Изучения показали, что S(+) дает эффект в 3-4 раза больше R(-), а токсичные и побочные действия явно связаны с последним. Значительное различие в терапевтической эффективности хиральных лекарств стимулировало развитию работ по разработке, разделению и анализу хиральных лекарств. Применение техники «Хиральность» позволило удалять из лекарственных средств составы, не дающие эффекта или имеющие токсичные и побочные действия, производить чистые хиральные лекарственные вещества, имеющие структуру с одним направлением, что позволило повышать чистоту состава препарата, быстро проявлять терапевтическую эффективность и сокращать курс лечения. В связи с этим, разработка хиральных лекарств стала одним из новых направлений в разработке новых лекарственных средств мира. Правительства и крупные фармацевтические фирмы начали вносить большие средства в разработку хиральных лекарственных препаратов, хирального сырья и хиральных интермедиатов, чтобы завоевать фармацевтический рынок мира хиральных лекарственных веществ. Более того, с непрерывным улучшением хиральной технологии и быстрым распространением жидкостной хроматографии была продвинута работа по разделению, анализу и определению антиподов хиральных лекарств. Хиральные моноэнантиомерные средства получили широкое применение. Карримицин (Carrimycin) - дериват спирамицина нового поколения, разработанный с помощью генной инженерии, носил первоначальное название «Biotechspiramycin», также биотехмицин, Biotechmycin [пат. ZL 97104440.6]. Согласно «Принципу выбора названий лекарственных препаратов Китая» в результате технической проверки и изучения Государственной фармакопейной комиссией Китая было принято решение переименовать Biotechspiramycin в Карримицин (Carrimycin), название на английском языке «Carrimycin». С точки зрения химической структуры основным составом Карримицин (Carrimycin) является 4ʺ-изовалерилспирамицин, включающий 4ʺ-изовалерилспирамицины I, II, III, кроме этого, Карримицин (Carrimycin) содержит и примерно 6 видов спирамицином с ацилированной 4-оксигруппой, поэтому он носит общее химическое название «4ʺ-ацилированный спирамицин».
Химическая структура основного состава Карримицин (Carrimycin) показана на (1):

где Р в изовалерилспирамицине I выбирают из Ч;
Р в изовалерилспирамицине II выбирают из СОСН3;
R в изовалерилспирамицине III выбирают из СОСН2СН3.
Карримицин (Carrimycin) представляет собой шестнадцатичленные макролидные антибиотики, механизм действия заключается в сочетании с тельцем Паладе бактерий для ингибирования синтеза белков.
Результаты фармакокинетических исследований показали, что в Карримицине (Carrimycin) самыми активными составами являются изовалерилспирамицины I, II, III. После поступления в организм карримицин (Carrimycin) быстро метаболирует с образованием спирамицина, расчет суммы AUC0-t материнских средств изовалерилспирамицинов I, II, III и активных метаболитов - спирамицинов I, II, III показал, что при пероральном применении абсолютная биодоступность составляет в среднем 91,6%. По источникам абсолютная биодоступность спирамицина при пероральном применении для человека составляет в пределах 30-40% (Frydman AM et al JAntimicrob Chemother. 1988, 22 (suppl B):93-103). Чем доказано, что структура изовалерилспирамицина в значительной степени улучшила биологическую доступность активного вещества - спирамицина. Разовый прием Карримицина (Carrimycin) медленно дает эффект, Т1/2 в пределах 23-27 ч.
Результаты теста in vitro показали, что Карримицин (Carrimycin) хорошо воздействует на грамположительные бактерии, особенно некоторые лекарственно-устойчивые микробы (к примеру, золотистый стафилококк, стойкий к β-лактаму, золотистый стафилококк, стойкий к эритромицину и т.д.), не имеет заметной перекрестной устойчивости к подобным лекарственным средствам. Тем временем, обладает хорошей антибактериальной активностью в отношении микоплазмы и хламидии, части грамотрицательных бактерий, обладает благоприятной антибактериальной активностью и проницаемостью тканей в отношении токсоплазм, легионеллы, а также потенциальной иммунологической регуляцией. Антибактериальная активность внутри организма превосходит активность вне организма (ZL 200310122420.9). Клинические исследования показали, что прием таблеток Карримицин (Carrimycin) в течение 5-7 дней по 200 - 400 мг в день, дает положительные эффекты в лечении острого бактериального фарингита и острого гнойного тонзиллита, вызванного streptococcus pyogenes; бактериального хронического синусита и острого бронхита, вызванного сенситивными бактериями; не сильной пневмонии, вызванной пневмококком, гемофильной палочкой и микоплазмой пневмония; негонококкового уретрита, вызванного микоплазмой, хламидией; инфекции кожи и мягких тканей, периодонтита, тимпанита и других инфекционных болезней, вызванных сенситивными бактериями. Общий коэффициент полезного действия составляет 92,68%.
Клинические исследования показали, что Карримицин (Carrimycin) является безопасным и эффективным для перорального применения антибиотиком. Тем не менее, Карримицин (Carrimycin) является многокомпонентным лекарственным средством, полученным в результате ферментации, его дальнейшее отделение и очистка оказывается очень трудно. В настоящее время создание высокоэффективной жидкостной хроматографии позволяет отделить образцы Карримицин (Carrimycin) от ацилированных спирамицинов, например, степень отделения изовалерилспирамицин II от изобутирил-спирамицина III, степень отделения изобутирил-спирамицин II от пропионил-спирамицина III, степень отделения пропионил-спирамицина III от его предыдущих малых компонентов, степень отделения пропионил-спирамицина II от ацетилспирамицина III более 1,5, установленной Китайской фармакопеей; а степень отделения ацетилспирамицин III от его предыдущих малых компонентов составляет 1,2.
В результате многочисленных исследований, регулирования и оптимизации условий культивирования и ферментации изобретателем был получен левовращающий Карримицин (Carrimycin), который обладает более благоприятной противоинфекционной активностью.
В настоящее время применяется высокоэффективная жидкостная хроматография для определения 9 видов ацилированных спирамицинов Карримицина (Carrimycin), в т.ч. общее содержание изовалерилспирамицинов (I+II+III) не менее 60%, общее содержание ацилированных спирамицинов не менее 80%. В отношении многокомпонентного антибиотика, полученного в результате ферментации, трудно достигать критерия контроля качества средств для инъекций среди химикатов, но в отношении тяжелых больных или больных, которым не подходит пероральное применение лекарства, инъекция дает результаты быстро, ввиду этого, разработка однокомпонентного препарата изовалерилспирамицина имеет очень глубокий смысл. В результате дальнейших исследований левовращающего Карримицина (Carrimycin) был получен однокомпонентный левовращающий изовалерилспирамицин I чистотой до 98 мас.%.
Общее описание изобретения
Первый объект изобретения относится к левовращающему изовалерилспирамицину III.
Второй объект изобретения относится к препаратам, содержащим левовращающий изовалерилспирамицин III.
Третьим объектом изобретения является способ приготовления левовращающего изовалерилспирамицина III.
Четвертым объектом изобретения также является употребление левовращающего изовалерилспирамицина III.
Пятым объектом изобретения также являются кристаллы левовращающего изовалерилспирамицина III, а также препараты, содержащие указанные виды кристалла.
Изобретение относится к левовращающему изовалерилспирамицину III, химическая структура указанного левовращающего изовалерилспирамицина III приведена в (I),
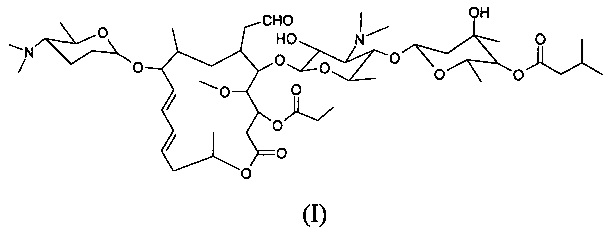
Удельная постоянная вращения составляет [α]D=(-)-(49)–(-51)° (С=0,02 г/мл, CHCl3, 25°С, λ=589, 3 нм); точка плавления составляет 116-118°С.
Изобретение относится к препаратам левовращающего изовалерилспирамицина III, отличающимся тем, что указанные препараты содержат изовалерилспирамицин III, фармацевтическую соль изовалерилспирамицина III, фармацевтически приемлемые для изовалерилспирамицина III и вспомогательные материалы, или фармацевтически приемлемые для фармацевтической соли изовалерилспирамицина III вспомогательные материалы. Чистота указанного изовалерилспирамицина III более 90 мас.%, предпочтительная чистота более 95 мас.%, более предпочтительная чистота более 98 мас.%.
Первый предпочтительный вариант изобретения: препараты изобретения могут быть жидкими, твердыми, полутвердыми или газообразными; указанный жидкий препарат выбирают среди раствора для инъекции, трансфузионной среды, раствора, микстуры, сахарного сиропа, настойки, золи, ароматизированной воды, глицеринового раствора, коллоидального раствора, слизи, взвеси или эмульсии; указанный твердый препарат выбирают среди порошка для инъекций, лиофилизированного порошка, таблеток, желатиновых капсул, порошка, пилюль или пленок; указанный полутвердый препарат выбирают среди мази, пластыри, свечи; суппозитория, экстракта, желатинирующего вещества; указанный газообразный препарат выбирают среди аэрозоли или распыляемого раствора, предпочтительны раствор для инъекций, порошок для инъекций и лиофилизированный порошок для инъекций.
Второй предпочтительный вариант изобретения: единичные дозы изовалерилспирамицина III, содержимого в препаратах изобретения, составляют 10-1500 мг, предпочтительно 50-1000 мг, более предпочтительно 100-500 мг.
Третий предпочтительный вариант изобретения: в препаратах массовый процент левовращающего изовалерилспирамицина III составляет 10-95%, предпочтительно 50-95%, более предпочтительно 75-95%.
Изобретение также относится к препаратам, содержащим левовращающий изовалерилспирамицин III.
Указанные препараты включают раствор для инъекций, порошок для инъекций или лиофилизированный порошок для инъекций, приготовленный из изовалерилспирамицина III и, по крайней мере, одного среди лимоннокислоты, адипиновой кислоты, малеиновой кислоты.
В т.ч. мольное отношение левовращающего изовалерилспирамицина III к лимоннокислое составляет 1:0,8-1,2, мольное отношение левовращающего изовалерилспирамицина III к адипиновой кислоте составляет 1:0,8-1,2, мольное отношение левовращающего изовалерилспирамицина III к малеиновой кислоте составляет 1:0,8-1,2.
Изобретение также относится к способу приготовления левовращающего изовалерилспирамицина III, включающему приготовление левовращающего Карримицина (Carrimycin), очистку левовращающего изовалерилспирамицина III.
В т.ч. процесс приготовления левовращающего Карримицина (Carrimycin) включает культивирование клонированного штамма WSP-195 бактерий, продуцирующих спирамицин, с содержанием гена 4ʺ-изовалерил-трансферазы, биологическое сбраживание и экстрагирование сбраживаемой жидкости; сбраживание при уровне рН 6,0-9,0, предпочтительно 6,0-8,0, более предпочтительно 6,0-7,5, зависимость уровня рН от времени показывала три непрерывных этапа, первый этап удовлетворяет уравнению y1=k1x1+6,0, где 0,0227≤k1≤0,1364, 0<x1≤22; второй этап удовлетворяет уравнению y2=k2x2+b2, где - 0,0735≤k2<0, 6,5<b2≤10,62, 22≤х2≤56, третий этап удовлетворяет уравнению y3=k3x3+b3, где 0<k3≤0,0078, 6,06≤b3<6,5, 56≤х3≤120. Регулировали и оптимизировали условия культивирования и сбраживания, особенно регулировали уровень рН в процессе сбраживания с помощью средства для регулирования уровня рН, чтобы зависимость уровня рН от времени в процессе сбраживания показывала три непрерывных этапа, каждый из этапов удовлетворяет определенному уравнению, таким образом, получали левовращающий Карримицин (Carrimycin) с оптической активностью. Получали левовращающий изовалерилспирамицин III.
Предпочтительно, что условия биологического сбраживания: клонированный штамм WSJ-195 бактерий, продуцирующих спирамицин, с содержанием гена 4ʺ-изовалерил-трансферазы, культивировали в течение 8-15 сут при рН 6,5-7,5 и 28~38°С на наклонной питательной среде, содержащей муку из бобового жмыха 2%, глюкозу 1%, крахмал 3%, СаСО3 0,5%, NaCl 0,4% и агара 2%, засевали на питательную среду семени, содержащую муку из бобового жмыха 1,5%, крахмал 3,0%, NaCl 0,4%, СаСО3 0,5%, рыбный пептон 0,3% и KH2PO4 0,05%, культивировали в течение 40-80 ч при рН 6,5-7,5 и 25~30°С, далее засевали прививочную дозу 0,1-20% на питательную ферментационную среду, содержащую глюкозу 0,5%, крахмал 6,0%, сухие дрожжи 0,5%, рыбную муку 2,0%, NH4NO3 0,6%, NaCl 1,0%, СаСО3 0,5%, KH2PO4 0,05%, MgSO4 0,1%, бобовое масло 0,5% и противовспениватель 0,02%, культивировали в течение 72-120 ч при рН6,5-7,5 и 26~30°С, таким образом, получали сбраживаемую жидкость.
В качестве указанного средства для регулирования уровня рН выбирают, по крайней мере, один среди соляной кислоты, уксусной кислоты, нашатырного спирта, каустической соды, гидроокиси калия.
Предпочтительно, что экстрагирование биологически сбраживаемой жидкости по следующим шагам: обрабатывали полученную сбраживаемую жидкость сернокислым алюминием для получения фильтрата, регулировали уровень рН фильтрата до 8,5-9,0, экстрагировали бутилацетатом, промывали бутилацетатный экстракт обессоленной водой и 1% NaH2PO4 соответственно, экстрагировали водой рН 2,0-2,5 для получения водофазного экстракта, регулировали уровень рН до 4,5-5,5, удаляли остаточный бутилацетат возгонкой для получения водного экстракта, фильтровали, регулировали уровень рН фильтрата до 8,5-9,0, осаждали, орошали очищенной водой для получения влажного вещества, далее осушали и получали левовращающий Карримицин (Carrimycin).
В т.ч. для регулирования уровня рН применяли, по крайней мере, одну среди соляной кислоты, уксусной кислоты, лимоннокислоты, каустической соды, гидроокиси калия, натрия гидрокарбоната, углекислого натрия.
В т.ч. подробный процесс очистки изовалерилспирамицина III включает: очистку образцов левовращающего Карримицина (Carrimycin) хроматографическим разделением, градиентную элюцию хроматографической колонной ODS с помощью ацетонитрила и буферного раствора уксуснокислого аммония, выделение целевого пика состава левовращающего изовалерилспирамицина III.
Предпочтительно, что в процессе очистки левовращающего изовалерилспирамицина I III, принимали припрепаративную высокоэффективную жидкостную хроматографию, ультрафиолетовый контроль, регистрировали ультрафиолетовую спектрограмму. Собирали образцы согласно времени выдержки левовращающего изовалерилспирамицина III - 48,009 мин.
Более предпочтительно, что в процессе очистки левовращающего изовалерилспирамицина III, очищали собранный левовращающий изовалерилспирамицин III от ацетонитрила вращающим испарением, потом экстрагировали этилацетатом, удаляли этилацетат из экстракта испарением, получали пастообразные образцы; перерастворяли полученные образцы петролейным эфиром, удаляли петролейный эфир испарением, получали белые порошковые частицы левовращающего изовалерилспирамицина III.
В т.ч. указанной подвижной фазой является смешанный растворитель ацетонитрила А и водного раствора уксуснокислого аммония рН=8,5, 150 мМ.
Конкретные условия очистки левовращающего изовалерилспирамицина III: применяли линейный градиент: 0-60 мин, А: 25%-65%; 61-90 мин, А: 65%-90%;
Скорость потока: 260 мл/мин;
Объем вводимого образца: 10 мл;
Концентрация вводимого образца: 0.5 г/мл;
Контрольная длина волны: 231 нм;
Способ сбора: ультрафиолетовый пуск.
Изобретение также относится к кристаллам левовращающего изовалерилспирамицина III, порошковая рентгеновская дифракция, измеренная Cu-Ka-лучами, показывала характеристический пик при 2θ, равном, 8,0°, 10,0°, 11,2°, 11,7°, 16,4°, 19,1°, 19,6°, 20,0°, 21,4°, 22,9°, 23,6° и 29,4°. Диаграмма порошковой рентгеновской дифракции показана на Рис. 5.
Способ приготовления указанных кристаллов левовращающего изовалерилспирамицина III заключается в том, что сначала растворяют твердые частицы левовращающего изовалерилспирамицина III в смеси растворителей безводного метанола, абсолютного этилового спирта и безводного ацетона, потом наливают очищенную воду с одновременным перемешиванием, после налива очищенной воды температура снижается до 5-15°С, при этом продолжают перемешивание до получения кристаллов левовращающего изовалерилспирамицина III.
В т.ч. первое предпочтительное техническое решение по приготовлению кристаллов левовращающего изовалерилспирамицина III заключается в том, что объем вводимой очищенной воды в 2-9 раз больше суммы объема безводного метанола, абсолютного этилового спирта и безводного ацетона, предпочтительно 2,5-7,5 раза; скорость ввода очищенной воды 4-10 мл/мин, предпочтительно 6-8 мл/ мин.
Второе предпочтительное техническое решение по приготовлению кристаллов левовращающего изовалерилспирамицина III заключается в том, что в примененной смеси растворителей отношение объема безводного метанола к объему абсолютного этилового спирта и к объему безводного ацетона составляет 1:0,1-10:0,5-1, предпочтительно 1:2-8:0,8-1.
Третье предпочтительное техническое решение по приготовлению указанных кристаллов левовращающего изовалерилспирамицина III заключается в том, что скорость перемешивания вводимой очищенной воды 30-60 об/мин, предпочтительно 45-60 об/мин; после ввода очищенной воды скорость перемешивания 10-30 об/мин, предпочтительно 10-20 об/мин.
Четвертое предпочтительное техническое решение по приготовлению указанных кристаллов левовращающего изовалерилспирамицина III заключается в том, что скорость охлаждения после ввода очищенной воды 1-3°С/ч, предпочтительно 1-1.5°С/ч.
В элементарных ячейках различных форм молекулы имеют различную пространственную конфигурацию, конфирмацию и расположение, их растворимость тоже сильно отличается, препараты имеют различную скорость растворения внутри тела, что оказывало непосредственное воздействие на поглощение, распределение, экскрецию и метаболизм препаратов в теле, в результате чего различная биологическая доступность приведет к получению различных клинических эффектов. В изобретении проводили соответственное сравнение терапевтической эффективности приготовленных кристаллов левовращающего изовалерилспирамицина III с эффективностью левовращающего изовалерилспирамицина III, и было обнаружено, что терапевтическая эффективность приготовленных по изобретению кристаллов левовращающего изовалерилспирамицина IIII, превосходит эффективность левовращающего изовалерилспирамицина III.
Изобретение относится также к препаратам кристаллов левовращающего изовалерилспирамицина III, указанные препараты включают кристаллы изовалерилспирамицина III, фармацевтическую соль кристаллов левовращающего изовалерилспирамицина III, фармацевтически приемлемые для кристаллов изовалерилспирамицина III вспомогательные материалы, или фармацевтически приемлемые для фармацевтической соли кристаллов изовалерилспирамицина III вспомогательные материалы, чистота указанных кристаллов изовалерилспирамицина III более 99 мас.%.
Изобретение относится также к употреблению изоамил-спирамицина III или его кристаллов, и его препаратов в приготовлении лечебных и/или профилактических средств против инфекционных заболеваний. Указанные инфекционные заболевания вызваны заражением грамположительными бактериями, золотистым Стафилококком, пневмококком, микоплазмой пневмония, хламидией пневмониз, уреаплазмой уреалитикум, трахоматозными хламидиями, streptococcus pyogenes, микрококком катаральным, нейссерией гонорея, гемофильной палочкой, легионеллой или анаэробными бактериями.
Изобретение относится также к употреблению изоамил-спирамицина III или его кристаллов, и его препаратов в приготовлении антибактериальных средств, указанные бактерии: пневмококк, стрептококк группы A, streptococcus pyogenes, энтерококк, золотистый стафилококк, эпидермальный стафилококк, микрококк катаральный, нейссерия гонорея, гемофильная палочка, колибацилла или кишечная палочка, энтеротоксигенные кишечные палочки, патогенная кишечная палочка, enteroinvasive escherichia coli, синегнойная палочка, клебсиелла пневмонии, протеус вульгарис, тифозная палочка, акинетобактерии, лимоннокислота, цитробактер, serratia marcescens, шигелла зонне, шигелла Флекснера, бацилла, tritirachium album; легионеллы, как легионеллезная пневмония, legionella gormanii, legionella bozemanii, legionella dumoffii, legionella jordanis, legionella micdadei; анаэробные бактерии, как бактероиды фрагилис, bacteroides thetaiotaomicron, бактероиды вульгатус, Bacteroides distasonis, bacteroides ruminicola, prevotella asaccharolyticus, prevotella oralis, палочка Плаута, fusobacterium russii, бифидобактерии, лактобацилла, пептострептококки, пропионибактерии акне, клостридии перфрингенс, дрожжеподобный гриб.
Ниже приведено подробное описание изобретения.
Изобретение относится к левовращающему изовалерилспирамицину III, который получали путем регулирования и оптимизирования условий культивирования и сбраживания, а также строгого контролирования уровня рН раствора.
Левовращающий изовалерилспирамицин III обладает повышенной антибактериальной активностью, стали новыми ассортиментами антибиотических средств для инъекций, что предоставило новую возможность для решения технической задачи по антибиотикоустойчивости в настоящее время.
В т.ч. метод определения удельной постоянной вращения левовращающего изовалерилспирамицина III: точно взвешивают указанный препарат, добавляют трихлорметан, растворяют и разбавляют до концентрации 20 мг/1 мл, определяют постоянную вращения калиброванным поляриметром с разрешением до 0,0001° с помощью D-линии спектра натрия (589,3 нм), длина 1 дм, температура 25°С.
Метод определения точки плавления левовращающего изовалерилспирамицина III: взвешивают сухой левовращающий изовалерилспирамицин III в умеренном количестве, кладут в капилляр для определения точки плавления, повторяют определение три раза и принимают среднюю величину.
Изобретение также относится к препаратам, содержащим левовращающий изовалерилспирамицин III. Составом препаратов являются левовращающий изовалерилспирамицин III и фармацевтически приемлемые носили и/или вспомогательные материалы, в т.ч. частота изовалерилспирамицина III более 90 мас.%, предпочтительно более 95 мас.%, более предпочтительно более 98 мас.%.
Препараты, содержащие левовращающий изовалерилспирамицин III или их кристаллы: предпочтительны раствор для инъекций, порошок для инъекций и лиофилизированный порошок для инъекций. Приготавливают раствор для инъекций или порошок для инъекций из препаратов, содержащих однокомпонентный левовращающий изовалерилспирамицин III, чтобы левовращающий изовалерилспирамицин III был быстро поглощен в организме человека и достигалась антиинфекционная функция.
Препараты изобретения, содержащие левовращающий изовалерилспирамицин III, включают следующую единичную дозу: левовращающий изовалерилспирамицин III 10-1500 мг, предпочтительно 50-1000 мг, более предпочтительно 100-500 мг.
Препараты изобретения, содержащие кристаллы левовращающего изовалерилспирамицина III, включают следующую единичную дозу: кристаллы левовращающего изовалерилспирамицина III 10-1500 мг, предпочтительно 50-1000 мг, более предпочтительно 100-500 мг.
В препаратах изобретения, содержащих левовращающий изовалерилспирамицин III, массовый процент левовращающего изовалерилспирамицина III составляет 10-90%, предпочтительно 50-90%, более предпочтительно 75-90%.
В препаратах изобретения, содержащих кристаллы левовращающего изовалерилспирамицина III, массовый процент кристаллов левовращающего изовалерилспирамицина III составляет 10-90%, предпочтительно 50-90%, более предпочтительно 75-90%.
Препараты изобретения для приема внутрь могут содержать частоприменяемые воспринимающие средства, как святитель, заполняющие вещества, разбавитель, таблетки, мягчительные средства, дезинтегрант, краситель, приправы и смачиватель, при необходимости покрывают таблетки покровным слоем. В т.ч. применимые заполняющие вещества включают фибрин, маннитол, лактозу и другие подобные заполняющие вещества. Применимый дезинтегрант включает крахмал, поливиниловый пирролидин и дериваты крахмала, например гликолят натрий крахмал. Применимые мягчительные средства включают, например стеарат магния. Применимый смачиватель, приемлемый для лекарственных средств, включает додецил сульфата кантрия.
Твердые препараты для введения внутрь через рот приготавливают смешиванием, наполнением, таблетированием и другими распространенными методами.
Формы жидких препаратов для перорального приема, например водянистая или жирная взвесь, раствор, эмульсия, сахарный сироп или эликсир, или сухой продукт, который можно приготовить вместе с водой или другими подходящими носителями до его применения. Такие жидкие препараты могут содержать обычные добавки, например суспендирующие вещества, как сорбит, сахарный сироп, метилцеллюлоза, желатина, оксиэтилцеллюлоза, карбоксиметилцеллюлоза, гель стеаринового алюминия или пищевой гидрированный жир, эмульсоры, например лецитин, дегидратационный сорбит-олеин или гуммиарабик, неводные носители (могут содержать пищевое масло), например миндальное масло, фракционированное кокосовое масло, как масляный эфир глицерида, пропиленгликоль или этиловый алкоголь; антисептики, например липид-n-гидроксибензойной кислоты или n-гидроксифенилмравьинопропиловый эфир или сорбиновая кислота, при необходимости могут содержать обычные ароматизирующее вещества или краситель.
Препараты для инъекций могут содержать любые обычные фармацевтические носители и/или воспринимающие средства, стабилизирующие вещества, антиоксиданты, комплексообразователь, а также фармацевтические антисептики, буферы или местно-анестезирующие средства и т.д. Применяют обычные методы приготовления.
Фармацевтически приемлемые носители, применяемые в препаратах изобретения, выбирают среди: маннитола, сорбита, пиросернистокислого натрия, бисульфита натрия, тиосульфата натрия, цистеина гидрохлорида, тиогликовой кислоты, метионина, витамина С, этилендиаминтетраацетата натрия, этилендиаминтетраацетата кальция-натрия, карбоната, ацетатаф, фосфата или его водного раствора, соляной кислоты, уксусной кислоты, серной кислоты, фосфорной кислоты, аминокислоты, хлористого натрия, хлористого калия одновалентных щелочных металлов, лактата натрия, ксилитола, мальтозы, глюкозы, фруктозы, декстрана, глицина, крахмала, сахарозы, лактозы, лактобиозы, маннитола, деривата кремния, фибрина и его деривата, соли альгиновой кислоты, желатина, поливинилового пирролидона, глицерина, полисорбата 80, агара, углекислого кальция, гидрокарбоната кальция, поверхностно-активного агента, полиэтиленгликоля, циклодекстрина, β-циклодекстрина, фосфатидных материалов, каолина, талькового порошка, стеаринового кальция, стеаринового магния, стеарата магния и т.д..
Способ применения и дозы препаратов определяют в зависимости от реального состояния пациента, можно внутреннее употребление или введение инъекцией 1-3 раза в день по 1-20 доз.
Эффективность изобретения:
(1) Левовращающий изовалерилспирамицин I, левовращающий изовалерилспирамицин II, левовращающий изовалерилспирамицин III обладают благоприятными антибактериальными свойствами. Согласно современной мармакологии в связи с различной стереоспецифичностью антипода лекарственных веществ, они имеют различный аффинитет с рецепторами, в результате чего сильно отличаются фармакологические свойства, ввиду этого, левовращающий изовалерилспирамицин I, левовращающий изовалерилспирамицин II, левовращающий изовалерилспирамицин III обладают очень большой фармакологической активностью.
(2) В элементарных ячейках различных форм молекулы имеют различную пространственную конфигурацию, конформацию и расположение, их растворимость тоже сильно отличаются, препараты имеют различную скорость растворения внутри тела, что оказывало непосредственное воздействие на поглощение, распределение, экскрецию и метаболизм препаратов в теле, в результате чего различная биологическая доступность приведет к получению различных клинических эффектов. Проводили сравнение терапевтической эффективности приготовленных по изобретению кристаллов левовращающих изовалерилспирамицинов I, II или III с эффективностью левовращающих изовалерилспирамицинов I, II или III, и было обнаружено, что терапевтическая эффективность приготовленных по изобретению кристаллов левовращающих изовалерилспирамицинов I, II или III превосходит эффективность левовращающих изовалерилспирамицинов I, II или III.
(3) Однокомпонентные реагенты для инъекций, содержащие левовращающий изовалерилспирамицин I, II или III, однокомпонентные реагенты для инъекций, содержащие кристаллы левовращающего изовалерилспирамицина I, II или III, предоставляли тяжелым больным и больным, которым не подходит введение лекарств через рот, возможность применения быстродействующих и приемлемых лекарственных форм.
(4) Однокомпонентные препараты, содержащие левовращающий изовалерилспирамицин I, II или III, однокомпонентные препараты, содержащие кристаллы левовращающего изовалерилспирамицина I, II или III, отличаются стабильной технологией производством и возможностью контроля качества, рассчитаны на масштабное промышленное производство.
Список рисунков
Рис. 1: Хроматограмма собранных ультрафиолетовым пуском левовращающих изовалерилспирамицинов I, II и III по Примеру 1;
Рис. 2: Зависимость уровня рН от времени в процессе браживания по примеру 1 изобретения;
Рис. 3: Зависимость уровня рН от времени в процессе браживания по примеру 2 изобретения;
Рис. 4: Зависимость уровня рН от времени в процессе браживания по примеру 3 изобретения;
Рис. 5: Диаграмма порошковой рентгеновской дифракции левовращающего изовалерилспирамицина III изобретения;
Настоящее изобретение поясняется с помощью нижеследующих примеров, которые нужно рассматривать как пояснительные, а не ограничивающие объем охраны изобретения.
Подробные примеры
Пример 1. Разделение и приготовление левовращающих изовалерилспирамицинов I, II и III.
(1) Биологическое сбраживание: клонированный штамм WSJ-195 бактерий, продуцирующих спирамицин, с содержанием гена 4"-изовалерил-трансферазы, культивировали в течение 8-15 сут, при рН 6,5-7,5 и 28~38°С на наклонной питательной среде, содержащей муку из бобового жмыха 2%, глюкозу 1%, крахмал 3%, СаСО3 0,5%, NaCl 0,4% и агара 2%, засевали на питательную среду семени, содержащую муку из бобового жмыха 1,5%, крахмал 3,0%, NaCl 0,4%, СаСО3 0,5%, рыбный пептон 0,3% и KH2PO4 0,05%, культивировали в течение 40-80 ч при рН 6,5-7,5 и 25~30°С, далее засевали прививочную дозу 0,1-20% на питательную ферментационную среду, содержащую глюкозу 0,5%, крахмал 6,0%, сухие дрожжи 0,5%, рыбную муку 2,0%, NH4NO3 0,6%, NaCl 1,0%, СаСО3 0,5%, KH2PO4 0,05%, MgSO4 0,1%, бобовое масло 0,5% и противовспениватель 0,02%, культивировали в течение 72-120 ч при рН 6,5-7,5 и 26~30°С, таким образом, получали сбраживаемую жидкость;
В т.ч. строго контролировали уровень рН раствора путем регулирования и оптимизирования условий культирования и сбраживания, проводили сбраживание при уровне рН 6,0-9,0, время сбраживания составляет 120 ч, и зависимость уровня рН от времени показывала три непрерывных этапа, первый этап удовлетворяет уравнению y1=0,1364x1+6,0, где 0<x1≤22; второй этап удовлетворяет уравнению y2=-0,0735х2+10,64, где 22≤х2≤56; третий этап удовлетворяет уравнению y3=0,0078х3+6,06, где 56≤х3≤120, зависимость уровня рН от времени приведена на Рис. 2, таким образом, получали сбраживаемую жидкость.
(2) Экстрагирование биологически сбраживаемой жидкости: обрабатывали сбраживаемую жидкость, полученную по п. (1), сернокислым алюминием для получения фильтрата, регулировали уровень рН фильтрата до 8,5, экстрагировали бутилацетатом, промывали бутилацетатный экстракт обессоленной водой и 1% NaH2PO4 соответственно, экстрагировали водой рН 2,0 для получения водофазного экстракта, регулировали уровень рН до 4,5, удаляли остаточный бутилацетат возгонкой для получения водного экстракта, фильтровали, регулировали уровень рН фильтрата до 8,5, осаждали, орошали очищенной воды для получения влажного вещества, далее осушали и получали левовращающий Карримицин (Carrimycin).
(3) Очистка левовращающих изовалерилспирамицинов I, II, III: очищали образцы, полученные после предварительного выделения, препаративной высокоэффективной жидкостной хроматографией, приготавливали хроматографическую колонну из ODS, проводили градиентную элюцию с помощью ацетонитрила и буферного раствора уксуснокислого аммония, ультрафиолетовый контроль, регистрировали ультрафиолетовую спектрограмму выделения, собирали целевой пик состава левовращающего изовалерилспирамицина I, целевой пик состава левовращающего изовалерилспирамицина II, целевой пик состава левовращающего изовалерилспирамицина III.
Хроматографическая колонна: приготовление хроматографической колонны из ODS;
Подвижная фаза: ацетонитрил (А), 100 мМ водный раствор уксуснокислого аммония (В);
Градиент: применяли линейный градиент 0-60 мин, А: 25-65%; 61-90 мин, А: 65-90%;
Скорость потока: 260 мл/мин;
Объем вводимого образца: 10 мл;
Концентрация вводимого образца: 0,5 г/мл;
Контрольная длина волны: 231 нм;
Способ сбора: ультрафиолетовый пуск.
Собирали образцы изовалерилспирамицина I согласно времени выдержки изовалерилспирамицина I - 44,759 мин, собирали образцы согласно времени выдержки левовращающего изовалерилспирамицина II - 43,34 мин, собирали образцы согласно времени выдержки левовращающего изовалерилспирамицина III - 48,009 мин.
Очищали собранные образцы от ацетонитрила вращающим испарением, потом экстрагировали однократным этилацетатом, удаляли этилацетат из экстракта вращающим испарением, получали пастообразные образцы; перерастворяли полученные образцы петролейным эфиром, удаляли петролейный эфир вращающим испарением, получали белые порошковые частицы изовалерилспирамицинов I, II или III соответственно.
Пример 2. Разделение и приготовление левовращающих изовалерилспирамицинов I, II и III
(1) Биологическое сбраживание: клонированный штамм WSJ-195 бактерий, продуцирующих спирамицин, с содержанием гена 4ʺ-изовалерил-трансферазы, культивировали в течение 12 сут при рН 7,2 и 32°С на наклонной питательной среде, содержащей муку из бобового жмыха 2%, глюкозу 1%, крахмал 3%, СаСО3 0,5%, NaCl 0,4% и агара 2%, засевали на питательную среду семени, содержащую муку из бобового жмыха 1,5%, крахмал 3,0%, NaCl 0,4%, СаСО3 0,5%, рыбный пептон 0,3% и KH2PO4 0,05%, культивировали в течение 70 ч при рН 7,2 и 27°С, далее засевали прививочную дозу 12% на питательную ферментационную среду, содержащую глюкозу 0,5%, крахмал 6,0%, сухие дрожжи 0,5%, рыбную муку 2,0%, NH4NO3 0,6%, NaCl 1,0%, СаСО3 0,5%, KH2PO4 0,05%, MgSO4 0,1%, бобовое масло 0,5% и противовспениватель 0,02%, культивировали в течение 100 ч при рН 6,0-9,0 и 26~30°С, таким образом, получали сбраживаемую жидкость; проводили сбраживание при уровне рН 6,0-8,0, время сбраживания составляет 110 ч, и зависимость уровня рН от времени показывала три непрерывных этапа, первый этап удовлетворяет уравнению y1=0,0909x1+6,4, где 0<x1<22; второй этап удовлетворяет уравнению y2=-0,0441x2+7,8, где 22<х2<56; третий этап удовлетворяет уравнению y3=0,0078х3+6,06, где 56≤х3≤110, зависимость уровня рН от времени приведена на Рис. 3, таким образом, получали сбраживаемую жидкость. Подробная зависимость показана на Рис. 3.
(2) Экстрагирование биологически сбраживаемой жидкости: обрабатывали сбраживаемую жидкость, полученную по п. (1), сернокислым алюминием для получения фильтрата, регулировали уровень рН фильтрата до 8,6, экстрагировали бутилацетатом, промывали бутилацетатный экстракт обессоленной водой и 1% NaH2PO4 соответственно, экстрагировали водой рН 2,3 для получения водофазного экстракта, регулировали уровень рН до 5,0, удаляли остаточный бутилацетат возгонкой для получения водного экстракта, фильтровали, регулировали уровень рН фильтрата до 8,6, осаждали, орошали очищенной воды для получения влажного вещества, далее осушали и получали левовращающий Карримицин (Carrimycin).
(3) Очистка левовращающих изовалерилспирамицинов I, II, III: очищали образцы, полученные после предварительного выделения, препаративной высокоэффективной жидкостной хроматографией, приготавливали хроматографическую колонну из ODS, проводили градиентную элюцию с помощью ацетонитрила и буферного раствора уксуснокислого аммония, ультрафиолетовый контроль, регистрировали ультрафиолетовую спектрограмму выделения, собирали целевой пик состава левовращающего изовалерилспирамицина I, целевой пик состава левовращающего изовалерилспирамицина II, целевой пик состава левовращающего изовалерилспирамицина III.
Хроматографическая колонна: приготовление хроматографической колонны из ODS;
Подвижная фаза: ацетонитрил (А), 100 мМ водный раствор уксуснокислого аммония (В);
Градиент: применяли линейный градиент 0-60 мин, А: 25-65%; 61-90 мин, А: 65-90%;
Скорость потока: 260 мл/мин;
Объем вводимого образца: 10 мл;
Концентрация вводимого образца: 0,5 г/мл;
Контрольная длина волны: 231 нм;
Способ сбора: ультрафиолетовый пуск.
Собирали образцы левовращающего изовалерилспирамицина I согласно времени выдержки левовращающего изовалерилспирамицина I - 44,759 мин, собирали образцы согласно времени выдержки левовращающего изовалерилспирамицина II - 43,34 мин, собирали образцы согласно времени выдержки левовращающего изовалерилспирамицина III - 48,009 мин.
Очищали собранные образцы от ацетонитрила вращающим испарением, потом экстрагировали однократным этилацетатом, удаляли этилацетат из экстракта вращающим испарением, получали пастообразные образцы; перерастворяли полученные образцы петролейным эфиром, удаляли петролейный эфир вращающим испарением, получали белые порошковые частицы изовалерилспирамицинов I, II или III соответственно.
Пример 3. Разделение и приготовление левовращающих изовалерилспирамицинов I II, III.
(1) Культивирование и сбраживание: культивировали клонированный штамм WSJ-195 бактерий, продуцирующих спирамицин, с содержанием гена 4ʺ-изовалерил-трансферазы, на наклонной питательной среде, потом засевали на питательную среду семени, культивировали, далее засевали на питательную ферментационную среду, контролировали процесс сбраживания с помощью глюкозы и лимоннокислоты. проводили сбраживание при уровне рН 6,0-7,5, время сбраживания 115 ч, зависимость уровня рН от времени показывала три непрерывных этапа, первый этап удовлетворяет уравнению yi=0,0682x1+6,0, где 0<x1<22; второй этап удовлетворяет уравнению y2=-0,0294х2+8,147, где 22<х2<56; третий этап удовлетворяет уравнению y3=0,0078х3+6,06, где 56<х3<115, зависимость уровня рН от времени приведена на Рис. 4, таким образом, получается сбраживаемая жидкость.
(2) Экстрагирование биологически сбраживаемой жидкости: обрабатывали сбраживаемую жидкость, полученную по п. (1), сернокислым алюминием для получения фильтрата, регулировали уровень рН фильтрата до 8,6, экстрагировали бутилацетатом, промывали бутилацетатный экстракт обессоленной водой и 1% NaH2PO4 соответственно, экстрагировали водой рН 2,3 для получения водофазного экстракта, регулировали уровень рН до 5,0, удаляли остаточный бутилацетат возгонкой для получения водного экстракта, фильтровали, регулировали уровень рН фильтрата до 8,6, осаждали, орошали очищенной воды для получения влажного вещества, далее осушали и получали левовращающий Карримицин (Carrimycin).
(3) Очистка левовращающих изовалерилспирамицинов I, II, III: очищали образцы, полученные после предварительного выделения, препаративной высокоэффективной жидкостной хроматографией, приготавливали хроматографическую колонну из ODS, проводили градиентную элюцию с помощью ацетонитрила и буферного раствора уксуснокислого аммония, ультрафиолетовый контроль, регистрировали ультрафиолетовую спектрограмму выделения, собирали целевой пик состава левовращающего изовалерилспирамицина I, целевой пик состава левовращающего изовалерилспирамицина II, целевой пик состава левовращающего изовалерилспирамицина III.
Хроматографическая колонна: приготовление хроматографической колонны из ODS.
Подвижная фаза: ацетонитрил (А), 100 мМ водный раствор уксуснокислого аммония (В).
Градиент: применяли линейный градиент 0-60 мин, А: 25-65%; 61-90 мин, А: 65-90%;
Скорость потока: 260 мл/мин;
Объем вводимого образца: 10 мл;
Концентрация вводимого образца: 0,5 /мл;
Контрольная длина волны: 231 нм;
Способ сбора: ультрафиолетовый пуск.
Собирали образцы согласно времени выдержки левовращающего изовалерилспирамицина I - 44,759 мин, собирали образцы согласно времени выдержки левовращающего изовалерилспирамицина II - 43,34 мин, собирали образцы согласно времени выдержки левовращающего изовалерилспирамицина III - 48,009 мин.
Очищали собранные образцы от ацетонитрила вращающим испарением, потом экстрагировали однократным этилацетатом, удаляли этилацетат из экстракта вращающим испарением, получали пастообразные образцы; перерастворяли полученные образцы петролейным эфиром, удаляли петролейный эфир вращающим испарением, получали белые порошковые частицы изовалерилспирамицинов I, II или III соответственно.
Пример 4. Приготовление раствора для инъекций левовращающего изовалерилспирамицина I
(1) Равномерно перемешивали изовалерилспирамицин I 100 мг с адипиновой кислотой эквимолекулярных количеств, растворяли в дистилированной воде 1-5 мл, и получали желтоватый прозрачный раствор уровнем рН 4,6-5,6.
(2) Наливали активный уголь 0,1% (объем.) в приготовленный по п. (1) раствор и фильтровали.
(3) Проводили заправку, герметизацию, стерилизацию, проверку и упаковку в стерильных условиях.
Пример 5. Приготовление раствора для инъекций изовалерилспирамицина I
(1) Равномерно перемешивали изовалерилспирамицин I 100 мг с лимоннокислотой эквимолекулярных количеств, растворяли в дистиллированной воде 1-5 мл, получали желтоватый прозрачный раствор, уровнем рН 4,6-5,6.
(2) Наливали активный уголь 0,1% (объем.) в приготовленный по п. (1) раствор и фильтровали.
(3) Проводили заправку, герметизацию, стерилизацию, проверку и упаковку в стерильных условиях.
Пример 6. Приготовление раствора для инъекций изовалерилспирамицина I
(1) Равномерно перемешивали изовалерилспирамицин I 100 мг с малеиновой кислотой эквимолекулярных количеств, растворяли в дистилированной воде 1-5 мл, получали желтоватый прозрачный раствор уровнем рН 4,6-5,6.
(2) Наливали активный уголь 0,1% (объем) в приготовленный по п. (1) раствор и фильтровали.
(3) Проводили заправку, герметизацию, стерилизацию, проверку и упаковку в стерильных условиях.
Пример 7. Приготовление порошка для инъекций левовращающего изовалерилспирамицина I
(1) Равномерно перемешивали изовалерилспирамицин I 100 мг с лимоннокислотой эквимолекулярных количеств, растворяли в дистилированной воде 1-5 мл, получали желтоватый прозрачный раствор, уровнем рН 4,6-5,6.
(2) Наливали активный уголь 0,1% (объем) в приготовленный по п. (1) раствор и фильтровали.
(3) Добавляли маннитол 30-150 мг в качестве расклинивающего агента лиофилизированного порошка, быстро замораживали в течение 9 ч. в криогенном режиме, замораживали и осушали, получали желтоватый рыхлый массив, устанавливали крышку, проверяли и упаковывали в стерильных условиях.
Пример 8. Приготовление порошка для инъекций левовращающего изовалерилспирамицина I.
(1) Равномерно перемешивали изовалерилспирамицин I 100 мг с малеиновой кислотой эквимолекулярных количеств, растворяли в дистилированной воде 1-5 мл, получали желтоватый прозрачный раствор уровнем рН 4,6-5,6.
(2) Наливали активный уголь 0,1% (объем) в приготовленный по п. (1) раствор и фильтровали.
(3) Добавляли маннитол 30-150 мг в качестве расклинивающего агента лиофилизированного порошка, быстро замораживали в течение 9 ч. в криогенном режиме, замораживали и осушали, получали желтоватый рыхлый массив, устанавливали крышку, проверяли и упаковывали в стерильных условиях.
Пример 9. Приготовление порошка для инъекций левовращающего изовалерилспирамицина I
(1) Равномерно перемешивали изовалерилспирамицин I 100 мг с лимоннокислотой эквимолекулярных количеств, растворяли в дистилированной воде 1-5 мл, получали желтоватый прозрачный раствор, уровнем рН 4,6-5,6.
(2) Наливали активный уголь 0,1% (объем) в приготовленный по п. (1) раствор и фильтровали.
(3) Добавляли маннитол 30-150 мг в качестве расклинивающего агента лиофилизированного порошка, быстро замораживали в течение 9 ч. в криогенном режиме, замораживали и осушали, получали желтоватый рыхлый массив, устанавливали крышку, проверяли и упаковывали в стерильных условиях.
Пример 10. Таблетки Левовращающий изовалерилспирамицин I (1000 таблеток)
Рецептура:
Технология приготовления: взвешивали крахмал в подходящем количестве, растворяли до концентрации 15%, нагревали до пастообразного состояния, чтобы получить связитель; просеивали на сите в 100 меш основное сырье Карримицин (Carrimycin), вспомогательные материалы - крахмал, оксипропилцеллюлозу с низкой степенью замещения, карбоксиметил-крахмал натрия, и стеарат магния, взвешивали основное сырье и вспомогательные материалы в необходимом количестве согласно рецептуре; равномерно перемешивали левовращающий изовалерилспирамицин I, крахмал и оксипропилцеллюлозу с низкой степенью замещения, приготавливали мягкий агент с помощью крахмальной пасты концентрацией крахмала 15%, гранулировали на сите в 14 меш, осушали при 50-60°С, обеспечивали влажность в пределах 3-5%, формировали гранулы на сите в 14 меш, добавляли карбоксиметил-крахмал натрия и стеариновый магний, и перемешивали, определяли содержание частиц; согласно содержанию частиц рассчитывали вес таблетки, таблетировали (шампон диаметром 9 мм с неглубокой впадиной), проверяли разницу веса таблетки; после получения положительных результатов проводили упаковку.
Пример 11. Желатиновые капсулы Левовращающий изовалерилспирамицин I (1000 капсул)
Рецептура:
Технология приготовления: взвешивали основное сырье - левовращающий изовалерилспирамицин I и вспомогательные материалы - фармацевтический крахмал согласно рецептуре, положили в миксер и равномерно перемешивали в течение 1,5-2 ч; отобрали пробы и проверяли содержание, результаты должны принципиально соответствовать теоретическим данным (содержимое в каждой капсуле примерно 0,105 г), положили проверенные с положительными результатами фармацевтические капсулы #3 и перемешанную смесь в загрузочный аппарат для наполнения капсул согласно требованиям к эксплуатации автоматизированной капсулонаполнительной машины, проверяли разницу наполненных капсул (в пределах ±10%, менее 0,3 г), скорость растворения отвечала требованиям, потом положили проверенные с положительными результатами капсулы в фармацевтическую полировочную машину, куда наливали жидкий парафин для проведения полирования в течение 15-20 мин, далее вынимали, проводили упаковку конечных продуктов и проверку.
Пример 12. Дражированные таблетки Левовращающий изовалерилспирамицин I (1000 таблеток)
Рецептура: то же, как Пример 10.
Технология приготовления: согласно Примеру 11 положили годные таблетки-ядра в сосуд для нанесения сахарного слоя, медленно положили приготовленный сахарный сироп (концентрация 65-70%) в сосуд, постепенно повышали температуру до 40°С, добавляли умеренное количество талькового порошка, осушали несколько раз подачей воздуха по 25-30 мин, после выравнивания талькового слоя, покрывали сахарным слоем в течение 15-20 мин, после выравнивания сахарного слоя наносили покровный слой нужного цвета, положили приготовленную густотертую краску в сахарный сироп, равномерно перемешивали и положили в сосуд, повторяли процесс перемешивания по 15-20 мин.
Пример 13. Сахарный сироп Левовращающий изовалерилспирамицин I (1000 пакетов)
Рецептура:
Технология приготовления: измельчали сырой порошок левовращающего изовалерилспирамицина I, лимонную кислоту и сахарозу высокоскоростным измельчителем до частицы, рассеивали 85% частиц на сите в 300 меш, 15% - на сите в 180 меш, далее взвешивали измельченный мелкозернистый порошок по рецептуре и равномерно перемешивали в течение 1-1,5 ч, определяли содержание и рассчитывали вместимость (теоретическая вместимость 500 мг/пакет), далее вмещали смесь в упаковочную машину, устанавливали алюминиевую фольгу, сортировали согласно требованиям к эксплуатации сортировочной машины, разница вместимости в пределах ±5%, после этого проверяли и проводили наружную упаковку.
Пример 14. Кишечно-растворимая таблетка Левовращающий изовалерилспирамицин I (1000 таблеток)
Рецептура: то же, как Пример 10.
Технология приготовления: таблетки-ядра приготавливали по Примеру 5, положили годные таблетки-ядра в сосуд для нанесения сахарного слоя, покрывали трем нижним слоем с помощью сахарного сиропа концентрацией 60~70% и талькового порошка, потом покрывали изоляционным слоем, добавляли 10%-спиртовый раствор зеина, продували вращением в течение 10-15 мин, далее закапывали в сосуд диэтилфталат, ацетон, ацетатфталат целлюлозы, спиртовой раствор, т.е. кишечно-растворимый раствор, 2-3 раза продували вращением в течение 10-15 мин. После проверки с получением положительных результатов покрывали слоем сахара по Примеру 13.
Пример 15. Желудочно-растворимая таблетка Левовращающий изовалерилспирамицин I (1000 таблеток)
Рецептура: то же, как Пример 10.
Технология приготовления: таблетки-ядра приготавливали по Примеру 11, положили годные таблетки-ядра в высокоэффективную машину для нанесения покровного слоя, потом приготавливали из годного порошка (включая липорастворимый и водорастворимый порошок) раствор для нанесения покровного слоя, далее положили раствор для нанесения покровного слоя в коллоид, измельчали и фильтровали. Подогревали высокоэффективный сосуд для нанесения покровного слоя с загруженными таблетками-ядрами при скорости вращения в пределах 5-10 р/мин и температуре в пределах 45-60°С, опрыскивали аэрозольным соплом (более 300 меш) в сосуд раствор для нанесения покровного слоя, потом осушали 8-12 раз по 25-35 мин до равномерного нанесения, осушали естественным способом, проверяли и упаковывали.
Пример 16. Гранулы Левовращающий изовалерилспирамицин I (1000 пакетов)
Рецептура:
Технология приготовления: рассеивали сырой порошок левовращающего изовалерилспирамицина I, сахарную пудру и декстрин на сите в 120, взвешивали левовращающий изовалерилспирамицин I, сахарную пудру и декстрин согласно рецепту и равномерно перемешивали, приготавливали мягкий агент из равномерно перемешенных вышеуказанных материалов с помощью плазмагеля 5% PVP-K30, осушали и формировали колеблющие гранулы при 70°С, проверяли с положительными результатами и проводили сортировку.
Пример 17. Приготовление раствора для инъекций Левовращающий изовалерилспирамицин II.
(1) Равномерно перемешивали изовалерилспирамицин II 100 мг с адипиновой кислотой эквимолекулярных количеств, растворяли в дистилированной воде 1-5 мл, и получали желтоватый прозрачный раствор уровнем рН 4,6-5,6.
(2) Наливали активный уголь 0,1% (объем) в приготовленный по п. (1) раствор и фильтровали.
(3) Проводили заправку, герметизацию, стерилизацию, проверку и упаковку в стерильных условиях.
Пример 18. Приготовление раствора для инъекций Левовращающий изовалерилспирамицин II.
(1) Равномерно перемешивали изовалерилспирамицин II 100 мг с лимонной кислотой эквимолекулярных количеств, растворяли в дистиллированной воде 1-5 мл, получали желтоватый прозрачный раствор, уровнем рН 4,6-5,6.
(2) Наливали активный уголь 0,1% (объем) в приготовленный по п. (1) раствор и фильтровали.
(3) Проводили заправку, герметизацию, стерилизацию, проверку и упаковку в стерильных условиях.
Пример 19. Приготовление порошка для инъекций Левовращающий изовалерилспирамицин II.
(1) Равномерно перемешивали изовалерилспирамицин II 100 мг с лимонной кислотой эквимолекулярных количеств, растворяли в дистиллированной воде 1-5 мл, получали желтоватый прозрачный раствор, уровнем рН 4,6-5,6.
(2) Наливали активный уголь 0,1% (объем) в приготовленный по п. (1) раствор и фильтровали.
(3) Добавляли маннитол 30-150 мг в качестве расклинивающего агента лиофилизированного порошка, быстро замораживали в течение 9 ч в криогенном режиме, замораживали и осушали, получали желтоватый рыхлый массив, устанавливали крышку, проверяли и упаковывали в стерильных условиях.
Пример 20. Таблетки Левовращающий изовалерилспирамицин II (1000 таблеток)
Рецептура:
Технология приготовления: взвешивали крахмал в подходящем количестве, растворяли до концентрации 15%, нагревали до пастообразного состояния, чтобы получить связитель; просеивали на сите в 100 меш основное сырье Карримицин (Carrimycin), вспомогательные материалы - крахмал, оксипропилцеллюлозу с низкой степенью замещения, карбоксиметил-крахмал натрия, и стеарат магния, взвешивали основное сырье и вспомогательные материалы в необходимом количестве согласно рецепту; равномерно перемешивали левовращающий изовалерилспирамицин II, крахмал и оксипропилцеллюлозу с низкой степенью замещения, приготавливали мягкий агент с помощью крахмальной пасты концентрацией крахмала 15%, гранулировали на сите в 14 меш, осушали при 50-60°С, обеспечивали влажность в пределах 3-5%, формировали гранулы на сите в 14 меш, добавляли карбоксиметил-крахмал натрия и стеариновый магний, и перемешивали, определяли содержание частиц; согласно содержанию частиц рассчитывали вес таблетки, таблетировали (шампон диаметром 9 мм с неглубокой впадиной), проверяли разницу веса таблетки; после получения положительных результатов проводили упаковку.
Пример 21. Желатиновые капсулы Левовращающий изовалерилспирамицин II (1000 капсул)
Рецептура:
Технология приготовления: взвешивали основное сырье - левовращающий изовалерилспирамицин II и вспомогательные материалы - фармацевтический крахмал согласно рецепту, положили в миксер и равномерно перемешивали в течение 1,5-2 ч; отобрали пробы и проверяли содержание, результаты должны принципиально соответствовать теоретическим данным (содержимое в каждой капсуле примерно 0,105 г), положили проверенные с положительными результатами фармацевтические капсулы #3 и перемешанную смесь в загрузочный аппарат для наполнения капсул согласно требованиям к эксплуатации автоматизированной капсулонаполнительной машины, проверяли разницу наполненных капсул (в пределах ±10%, менее 0,3 г), скорость растворения отвечала требованиям, потом положили проверенные с положительными результатами капсулы в фармацевтическую полировочную машину, куда наливали жидкий парафин для проведения полирования в течение 15-20 мин, далее вынимали, проводили упаковку конечных продуктов и проверку.
Пример 22. Приготовление раствора для инъекций Изовалерилспирамицин III
(1) Равномерно перемешивали изовалерилспирамицин III 100 мг с малеиновой кислотой эквимолекулярных количеств, растворяли в дистилированной воде 1-5 мл, получали желтоватый прозрачный раствор уровнем рН 4,6-5,6.
(2) Наливали активный уголь 0,1% (объем) в приготовленный по п. (1) раствор и фильтровали.
(3) Проводили заправку, герметизацию, стерилизацию, проверку и упаковку в стерильных условиях.
Пример 23. Приготовление порошка для инъекций Левовращающий изовалерилспирамицин III
(1) Равномерно перемешивали изовалерилспирамицин III 100 мг с малеиновой кислотой эквимолекулярных количеств, растворяли в дистилированной воде 1-5 мл, получали желтоватый прозрачный раствор уровнем рН 4,6-5,6.
(2) Наливали активный уголь 0,1% (объем) в приготовленный по п. (1) раствор и фильтровали.
(3) Добавляли маннитол 30-150 мг в качестве расклинивающего агента лиофилизированного порошка, быстро замораживали в течение 9 ч в криогенном режиме, замораживали и осушали, получали желтоватый рыхлый массив, устанавливали крышку, проверяли и упаковывали в стерильных условиях.
Пример 24. Желатиновые капсулы Левовращающий изовалерилспирамицин III (1000 капсул)
Рецептура:
Технология приготовления: взвешивали основное сырье - левовращающий изовалерилспирамицин III и вспомогательные материалы - фармацевтический крахмал согласно рецепту, положили в миксер и равномерно перемешивали в течение 1,5-2 ч; отобрали пробы и проверяли содержание, результаты должны принципиально соответствовать теоретическим данным (содержимое в каждой капсуле примерно 0,105 г), положили проверенные с положительными результатами фармацевтические капсулы #3 и перемешанную смесь в загрузочный аппарат для наполнения капсул согласно требованиям к эксплуатации автоматизированной капсулонаполнительной машины, проверяли разницу наполненных капсул (в пределах ±10%, менее 0,3 г), скорость растворения отвечала требованиям, потом положили проверенные с положительными результатами капсулы в фармацевтическую полировочную машину, куда наливали жидкий парафин для проведения полирования в течение 15-20 мин, далее вынимали, проводили упаковку конечных продуктов и проверку.
Пример 25. Сахарный сироп Левовращающий изовалерилспирамицин III (1000 пакетов)
Рецептура:
Технология приготовления: измельчали сырой порошок левовращающего изовалерилспирамицина III, лимонную кислоту и сахарозу высокоскоростным измельчителем до частицы, рассеивали 85% частиц на сите в 300 меш, 15% - на сите в 180, далее взвешивали измельченный мелкозернистый порошок по рецепту и равномерно перемешивали в течение 1-1,5 ч, определяли содержание и рассчитывали вместимость (теоретическая вместимость 500 мг /пакет), далее вмещали смесь в упаковочную машину, устанавливали алюминиевую фольгу, сортировали согласно требованиям к эксплуатации сортировочной машины, разница вместимости в пределах ±5%, после этого проверяли и проводили наружную упаковку.
Пример 26. Гранулы Левовращающий изовалерилспирамицин III (1000 пакетов)
Рецептура:
Технология приготовления: рассеивали сырой порошок левовращающего изовалерилспирамицина III, сахарную пудру и декстрин на сите в 120, взвешивали левовращающий изовалерилспирамицин III, сахарную пудру и декстрин согласно рецепту и равномерно перемешивали, приготавливали мягкий агент из равномерно перемешенных вышеуказанных материалов с помощью плазмагеля 5% PVP-K30, осушали и формировали колеблющие гранулы при 70°С, проверяли с положительными результатами и проводили сортировку.
Пример 27.
Приготовление кристаллов из белых порошковых частиц левовращающего изовалерилспирамицина I, полученных по Примеру 1.
Способ приготовления кристаллов левовращающего изовалерилспирамицина I:
1. Растворяли твердые частицы левовращающего изовалерилспирамицина I, полученные по Примеру 1, в смеси растворителей этилацетата, абсолютного этилового спирта и безводного ацетона, в примененной смеси растворителей отношение объема этилацетата к объему абсолютного этилового спирта и к объему безводного ацетона составляло 1:10:1;
2. Потом наливали очищенную воду с одновременным перемешиванием, объем налитой воды в 2,5 раза больше суммы объема этилацетата, абсолютного этилового спирта и безводного ацетона, скорость ввода очищенной воды 4 мл/мин; скорость перемешивания при наливе очищенной воды 30 р/мин;
3. После налива очищенной воды температура снижалась до 5°С, скорость понижения температуры 1°С в час, при этом продолжали перемешивание скоростью 10 р/мин; таким образом, получали кристаллы левовращающего изовалерилспирамицина I.
Порошковая рентгеновская дифракция полученных кристаллов левовращающего изовалерилспирамицина I, измеренная Cu-Kα-лучами, показывала характеристический пик при 2θ, равном 7,6°, 8,0°, 10,0°, 11,4°, 16,4°, 17,0°, 17,5°, 17,9°, 19,5°, 22,7°, 23,7° и 24,4°, диаграмма порошковой рентгеновской дифракции показана на Рис. 5.
Пример 28.
Приготовление кристаллов из белых порошковых частиц левовращающего изовалерилспирамицина I, полученных по Примеру 1.
Способ приготовления кристаллов левовращающего изовалерилспирамицина I:
1. Растворяли твердые частицы левовращающего изовалерилспирамицина I в смеси растворителей этилацетата, абсолютного этилового спирта и безводного ацетона, в примененной смеси растворителей отношение объема этилацетата к объему абсолютного этилового спирта и к объему безводного ацетона составляло 1:10:1;
2. Потом наливали очищенную воду с одновременным перемешиванием, объем налитой воды в 9 раз больше суммы объема этилацетата, абсолютного этилового спирта и безводного ацетона, скорость ввода очищенной воды 10 мл/мин; скорость перемешивания при наливе очищенной воды 60 р/мин;
3. После налива очищенной воды температура снижалась до 15°С, скорость понижения температуры 3°С в час, при этом продолжали перемешивание скоростью 10 р/мин; таким образом, получали кристаллы левовращающего изовалерилспирамицина I.
Диаграмма порошковой рентгеновской дифракции кристаллов левовращающего изовалерилспирамицина I, измеренная Cu-Kα-лучами аналогична Рис. 5.
Пример 29. Приготовление раствора для инъекций кристаллов левовращающего изовалерилспирамицина I
Применяли кристаллы левовращающего изовалерилспирамицина I, полученные по Примеру 27, для приготовления раствора для инъекций по вышеуказанному способу.
Пример 30. Приготовление порошка для инъекций кристаллов левовращающего изовалерилспирамицина I
Применяли кристаллы левовращающего изовалерилспирамицина I, полученные по Примеру 28, для приготовления порошка для инъекций по вышеуказанному способу.
Пример 31. Приготовление таблеток кристаллов левовращающего изовалерилспирамицина I
Применяли кристаллы левовращающего изовалерилспирамицина I, полученные по Примеру 27, для приготовления таблеток по вышеуказанному способу.
Пример 32. Приготовление кристаллов из белых порошковых частиц левовращающего изовалерилспирамицина II, полученных по Примеру 1.
Способ приготовления кристаллов левовращающего изовалерилспирамицина II:
1. Растворяли твердые частицы левовращающего изовалерилспирамицина II, полученные по Примеру 1, в смеси растворителей безводного метанола, абсолютного этилового спирта и безводного ацетона, в примененной смеси растворителей отношение объема безводного метанола к объему безводного ацетона и к объему абсолютного этилового спирта составляло 1:10:1.
2. Потом наливали очищенную воду с одновременным перемешиванием, объем налитой воды в 2.5 раза больше суммы объема безводного метанола, абсолютного этилового спирта и безводного ацетона, скорость ввода очищенной воды 4 мл/мин; скорость перемешивания при наливе очищенной воды 30 р/мин.
3. После налива очищенной воды температура снижалась до 5°С, скорость понижения температуры 1°С в час, при этом продолжали перемешивание скоростью 10 р/мин; таким образом, получали кристаллы левовращающего изовалерилспирамицина II.
Порошковая рентгеновская дифракция полученных кристаллов левовращающего изовалерилспирамицина II, измеренная Cu-Kα-лучами, показывала характеристический пик при 2θ, равном 10,0°, 11,6°, 16,4°, 17,3°, 19,1°, 21,2°, 22,1°, 22,7°, 26,4°, 26,9°, 27,5° и 31,5°, диаграмма порошковой рентгеновской дифракции показана на Рис. 6.
Пример 33. Приготовление кристаллов из белых порошковых частиц левовращающего изовалерилспирамицина II, полученных по Примеру 1.
Способ приготовления кристаллов левовращающего изовалерилспирамицина II:
1. Растворяли твердые частицы левовращающего изовалерилспирамицина II в смеси растворителей безводного метанола, абсолютного этилового спирта и безводного ацетона, в примененной смеси растворителей отношение объема безводного метанола к объему безводного ацетона и к объему абсолютного этилового спирта составляло 1:10:0,8.
2. Потом наливали очищенную воду с одновременным перемешиванием, объем налитой воды в 9 раз больше суммы объема безводного метанола, абсолютного этилового спирта и безводного ацетона, скорость ввода очищенной воды 10 мл/мин; скорость перемешивания при наливе очищенной воды 60 об/мин.
3. После налива очищенной воды температура снижалась до 15°С, скорость понижения температуры 3°С в час, при этом продолжали перемешивание скоростью 10 об/мин; таким образом, получали кристаллы левовращающего изовалерилспирамицина II.
Диаграмма порошковой рентгеновской дифракции кристаллов левовращающего изовалерилспирамицина II, измеренная Cu-Kα-лучами аналогична Рис. 6.
Пример 34
Приготовление кристаллов из белых порошковых частиц левовращающего изовалерилспирамицина II, полученных по Примеру 2.
Способ приготовления кристаллов левовращающего изовалерилспирамицина II:
1. Растворяли твердые частицы левовращающего изовалерилспирамицина II в смеси растворителей безводного метанола, абсолютного этилового спирта и безводного ацетона, в примененной смеси растворителей отношение объема безводного метанола к объему безводного ацетона и к объему абсолютного этилового спирта составляло 1:5:1.
2. Наливали очищенную воду с одновременным перемешиванием, объем налитой воды в 7.5 раза больше суммы объема безводного метанола, абсолютного этилового спирта и безводного ацетона, скорость ввода очищенной воды 6 мл/мин; скорость перемешивания при наливе очищенной воды 40 р/мин.
3 После налива очищенной воды температура снижалась до 10°С, скорость понижения температуры 2°С в час, при этом продолжали перемешивание скоростью 15 об/мин; таким образом, получали кристаллы левовращающего изовалерилспирамицина II.
Диаграмма порошковой рентгеновской дифракции кристаллов левовращающего изовалерилспирамицина II, измеренная Cu-Kα-лучами аналогична Рис. 6.
Пример 35. Приготовление кристаллов из белых порошковых частиц левовращающего изовалерилспирамицина II, полученных по Примеру 3.
Способ приготовления кристаллов левовращающего изовалерилспирамицина II:
1. Растворяли твердые частицы левовращающего изовалерилспирамицина II в смеси растворителей безводного метанола, абсолютного этилового спирта и безводного ацетона, в примененной смеси растворителей отношение объема безводного метанола к объему безводного ацетона и к объему абсолютного этилового спирта составляло 1:3:1.
2. Потом наливали очищенную воду с одновременным перемешиванием, объем налитой воды в 7,5 раза больше суммы объема безводного метанола, абсолютного этилового спирта и безводного ацетона, скорость ввода очищенной воды 8 мл/мин; скорость перемешивания при наливе очищенной воды 45 об/мин.
3. После налива очищенной воды температура снижалась до 12°С, скорость понижения температуры 2,5°С в час, при этом продолжали перемешивание скоростью 20 р/мин; таким образом, получали кристаллы левовращающего изовалерилспирамицина II.
Диаграмма порошковой рентгеновской дифракции кристаллов левовращающего изовалерилспирамицина II, измеренная Cu-Kα-лучами аналогична Рис. 6.
Пример 36. Приготовление кристаллов из белых порошковых частиц левовращающего изовалерилспирамицина II, полученных по Примеру 3.
Способ приготовления кристаллов левовращающего изовалерилспирамицина II:
1. Растворяли твердые частицы левовращающего изовалерилспирамицина II в смеси растворителей безводного метанола, абсолютного этилового спирта и безводного ацетона, в примененной смеси растворителей отношение объема безводного метанола к объему безводного ацетона и к объему абсолютного этилового спирта составляло 1:6:0,8.
2. Потом наливали очищенную воду с одновременным перемешиванием, объем налитой воды в 5 раз больше суммы объема безводного метанола, абсолютного этилового спирта и безводного ацетона, скорость ввода очищенной воды 7 мл/мин; скорость перемешивания при наливе очищенной воды 60 об/мин.
3. После налива очищенной воды температура снижалась до 12°С, скорость понижения температуры 1,2°С в час, при этом продолжали перемешивание скоростью 15 р/мин; таким образом, получали кристаллы левовращающего изовалерилспирамицина II.
Диаграмма порошковой рентгеновской дифракции кристаллов левовращающего изовалерилспирамицина II, измеренная Cu-Kα-лучами аналогична Рис. 5.
Пример 37. Приготовление раствора для инъекций кристаллов левовращающего изовалерилспирамицина II
Применяли кристаллы левовращающего изовалерилспирамицина II, полученные по Примеру 34, для приготовления раствора для инъекций по вышеуказанному способу.
Пример 38. Приготовление раствора для инъекций кристаллов левовращающего изовалерилспирамицина II
Применяли кристаллы левовращающего изовалерилспирамицина II, полученные по Примеру 33, для приготовления раствора для инъекций по вышеуказанному способу.
Пример 39. Приготовление порошка для инъекций кристаллов левовращающего изовалерилспирамицина II
Применяли кристаллы левовращающего изовалерилспирамицина II, полученные по Примеру 36, для приготовления порошка для инъекций по вышеуказанному способу.
Пример 40. Приготовление порошка для инъекций кристаллов левовращающего изовалерилспирамицина II
Применяли кристаллы левовращающего изовалерилспирамицина II, полученные по Примеру 35, для приготовления порошка для инъекций по вышеуказанному способу.
Пример 41. Приготовление таблеток кристаллов левовращающего изовалерилспирамицина II
Применяли кристаллы левовращающего изовалерилспирамицина II, полученные по Примеру 36, для приготовления таблеток по вышеуказанному способу.
Пример 42. Приготовление желатиновых капсул кристаллов левовращающего изовалерилспирамицина II
Применяли кристаллы левовращающего изовалерилспирамицина II, полученные по Примеру 32, для приготовления желатиновых капсул по вышеуказанному способу.
Пример 43. Приготовление гранул кристаллов левовращающего изовалерилспирамицина II
Применяли кристаллы левовращающего изовалерилспирамицина II, полученные по Примеру 33, для приготовления гранул по вышеуказанному способу.
Пример 44. Приготовление кристаллов из белых порошковых частиц левовращающего изовалерилспирамицина III, полученных по Примеру 1.
Способ приготовления кристаллов левовращающего изовалерилспирамицина III:
1. Растворяли твердые частицы левовращающего изовалерилспирамицина III, полученные по Примеру 1, в смеси растворителей безводного метанола, абсолютного этилового спирта и безводного ацетона, в примененной смеси растворителей отношение объема безводного метанола к объему абсолютного этилового спирта и к объему безводного ацетона составляет 1:10:1.
2. Потом наливали очищенную воду с одновременным перемешиванием, объем налитой воды в 2.5 раза больше суммы объема безводного метанола, абсолютного этилового спирта и безводного ацетона, скорость ввода очищенной воды 4 мл/мин; скорость перемешивания при наливе очищенной воды 30 об/мин.
3. После налива очищенной воды температура снижалась до 5°С, скорость понижения температуры 1°С в час, при этом продолжали перемешивание скоростью 10 об/мин; таким образом, получали кристаллы левовращающего изовалерилспирамицина III.
Порошковая рентгеновская дифракция полученных кристаллов левовращающего изовалерилспирамицина III, измеренная Cu-Kα-лучами, показывала характеристический пик при 2θ, равном 8,0°, 10,0°, 11,2°, 11,7°, 16,4°, 19,1°, 19,6°, 20,0°, 21,4°, 22,9°, 23,6° и 29,4°, диаграмма порошковой рентгеновской дифракции показана на Рис. 7.
Пример 45. Приготовление кристаллов из белых порошковых частиц левовращающего изовалерилспирамицина III, полученных по Примеру 2.
Способ приготовления кристаллов левовращающего изовалерилспирамицина III:
1. Растворяли твердые частицы левовращающего изовалерилспирамицина III в смеси растворителей безводного метанола, абсолютного этилового спирта и безводного ацетона, в примененной смеси растворителей отношение объема безводного метанола к объему абсолютного этилового спирта и к объему безводного ацетона составляет 1:10:1.
2. Потом наливали очищенную воду с одновременным перемешиванием, объем налитой воды в 9 раз больше суммы объема безводного метанола, абсолютного этилового спирта и безводного ацетона, скорость ввода очищенной воды 10 мл/мин; скорость перемешивания при наливе очищенной воды 60 об/мин.
3. После налива очищенной воды температура снижалась до 15°С, скорость понижения температуры 3°С в час, при этом продолжали перемешивание скоростью 10 р/мин; таким образом, получали кристаллы левовращающего изовалерилспирамицина III.
Диаграмма порошковой рентгеновской дифракции кристаллов левовращающего изовалерилспирамицина III, измеренная Cu-Kα-лучами аналогична Рис. 7.
Пример 46. Приготовление кристаллов из белых порошковых частиц левовращающего изовалерилспирамицина III, полученных по Примеру 2.
Способ приготовления кристаллов левовращающего изовалерилспирамицина III:
1. Растворяли твердые частицы левовращающего изовалерилспирамицина III в смеси растворителей безводного метанола, абсолютного этилового спирта и безводного ацетона, в примененной смеси растворителей отношение объема безводного метанола к объему абсолютного этилового спирта и к объему безводного ацетона составляет 1:5:0,8.
2. Потом наливали очищенную воду с одновременным перемешиванием, объем налитой воды в 7,5 раза больше суммы объема безводного метанола, абсолютного этилового спирта и безводного ацетона, скорость ввода очищенной воды 6 мл/мин; скорость перемешивания при наливе очищенной воды 40 об/мин.
3. После налива очищенной воды температура снижалась до 10°С, скорость понижения температуры 2°С в час, при этом продолжали перемешивание скоростью 15 об/мин; таким образом, получали кристаллы левовращающего изовалерилспирамицина III.
Диаграмма порошковой рентгеновской дифракции кристаллов левовращающего изовалерилспирамицина III, измеренная Cu-Kα-лучами аналогична Рис. 7.
Пример 47. Приготовление кристаллов из белых порошковых частиц левовращающего изовалерилспирамицина III, полученных по Примеру 3.
Способ приготовления кристаллов левовращающего изовалерилспирамицина III:
1. Растворяли твердые частицы левовращающего изовалерилспирамицина III в смеси растворителей безводного метанола, абсолютного этилового спирта и безводного ацетона, в примененной смеси растворителей отношение объема безводного метанола к объему абсолютного этилового спирта и к объему безводного ацетона составляет 1:2:1.
2. Потом наливали очищенную воду с одновременным перемешиванием, объем налитой воды в 7.5 раза больше суммы объема безводного метанола, абсолютного этилового спирта и безводного ацетона, скорость ввода очищенной воды 8 мл/мин; скорость перемешивания при наливе очищенной воды 45 об/мин.
3. После налива очищенной воды температура снижалась до 12°С, скорость понижения температуры 2,5°С в час, при этом продолжали перемешивание скоростью 20 об/мин; таким образом, получали кристаллы левовращающего изовалерилспирамицина III.
Диаграмма порошковой рентгеновской дифракции кристаллов левовращающего изовалерилспирамицина III, измеренная Cu-Kα-лучами аналогична Рис. 7.
Пример 48. Приготовление раствора для инъекций кристаллов левовращающего изовалерилспирамицина III
Применяли кристаллы левовращающего изовалерилспирамицина III, полученные по Примеру 44, для приготовления раствора для инъекций по вышеуказанному способу.
Пример 49. Приготовление порошка для инъекций кристаллов левовращающего изовалерилспирамицина III
Применяли кристаллы левовращающего изовалерилспирамицина III, полученные по Примеру 45, для приготовления порошка для инъекций по вышеуказанному способу.
Пример 50. Приготовление таблеток кристаллов левовращающего изовалерилспирамицина III
Применяли кристаллы левовращающего изовалерилспирамицина III, полученные по Примеру 46, для приготовления таблеток по вышеуказанному способу.
Пример 51. Приготовление желатиновых капсул кристаллов левовращающего изовалерилспирамицина III
Применяли кристаллы левовращающего изовалерилспирамицина III, полученные по Примеру 47, для приготовления желатиновых капсул по вышеуказанному способу.
Опытный пример 1 Испытание на острую токсичность левовращающих изовалерилспирамицинов I, II, III
I. Метод испытания
Введение через рот лекарств (левовращающие изовалерилспирамицины I, II, III, полученные по Примеру 1) мышам и крысам
До испытания мыши и крысы находились под наблюдением 2 дня и те, у которых не была обнаружена аномалия, стали подопытными. До испытания мыши и крысы прошли голодание на ночь. Результаты предварительных испытаний показали, что введение лекарства в дозе 4000 мг/кг прямо в желудок мышей и крыс не вызывало гибель подопытных животных. Ввели лекарство в дозе 4000 мг/кг прямо в желудок мышей и крыс, мышам по 100 мг/мл, объем раствора, вводимого в желудок 0,6-0,8 мл/особь; крысам по 173 мг/мл, объем раствора, вводимого в желудок 0,8-1,0 мл/50 г. Наблюдали токсическую реакцию и число гибели животных в течение одной недели после введения лекарства в желудок.
II. Результаты испытания приведены на табл. 1 и 2


Левовращающие изовалерилспирамицины I, II, III или препараты левовращающих изовалерилспирамицинов I, II, III, приготовленные для остальных примеров изобретения, прошли одинаковые испытания и дали аналогичные результаты.
Опытный пример 2 Эффективность препарата левовращающих изовалерилспирамицинов III, III и их кристаллов in vivo
Метод испытания: приготовление раствора с заразными бактериями: взяли раствор с тестовыми бактериями, хранившийся в холодильнике при -80°С, оставили при комнатной температуре в течение 1 ч, взяли по 0,1 мл раствор с бактериями пневмококк, stpeptococcus pyogenes, энтерококк и засеяли в 2 мл раствор МН соответственно (с добавкой 10% инактивированной лошадиной сыворотки), засеяли раствор с золотистым стафилококком 0,1 мл в раствор МН 2 мл по вышеуказанному способу, положили в инкубатор 37°С и культивировали в течение 18 ч, получили основной раствор с бактериями, его растворяли 5% желудочной слизью и получили раствор с заразными бактериями, который стал летальной дозой (ЛД100).
Предполагается пероральное применение Карримицина (Carrimycin) в клинике, поэтому для испытания Карримицина (Carrimycin) выбирают введение прямо в желудок. Левовращающий изовалерилспирамицин I (полученный по Примеру 1), кристаллы левовращающего изовалерилспирамицина I (полученные по Примеру 27) ввели внутримышечно.
После введения в брюшную полость мышей 0,5 мл в летальной дозе животные проявляли заметное понижение двигательной активности, покой, взъерошенную шерсть и другие симптомы. После заражения ввели лекарства в дозе 0,2 мл прямо в желудок каждой мыши через 0,5-6 ч, не было никаких неблагоприятных воздействий. Наблюдали смертность особей в течение 7 дней, рассчитали среднюю эффективную дозу (ED50) лекарственных форм для зараженных мышей, используя программу Bliss, провели сравнение защитной эффективности с другими формами. Результаты теста in vivo:


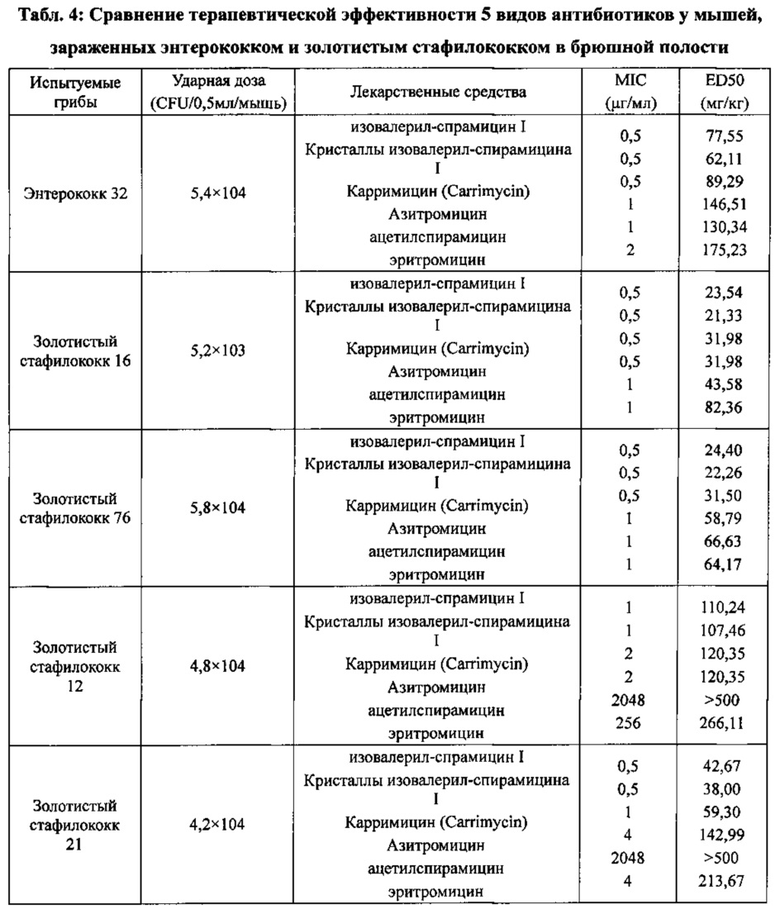
Результаты теста in vivo:
Терапевтическая эффективность изовалерилспирамицина I при лечении мышей, зараженных 12 штаммами бактерий, приведена на табл. 3 и 4, что показало благоприятную защитную эффективность; а кристаллы изовалерилспирамицина I проявляли более благоприятную защитную эффективность у мышей, зараженных 12 штаммами бактерий.
Левовращающий изовалерилспирамицин I, кристаллы левовращающего изовалерилспирамицина I или препараты, содержащие левовращающий изовалерилспирамицин I или кристаллы левовращающего изовалерилспирамицина I, приготовленные для остальных примеров изобретения, прошли одинаковые испытания и дали аналогичные результаты.
Опытный пример 3: Эффективность препарата левовращающего изовалерилспирамицина II и его кристаллов in vivo
Применяли левовращающий изовалерилспирамицин II, приготовленный по Примеру 1, и кристаллы левовращающего изовалерилспирамицина II, приготовленные по Примеру 36, и способ испытания, приведенный в Опытном примере 2.
Результаты теста in vivo приведены на табл. 5 и 6:
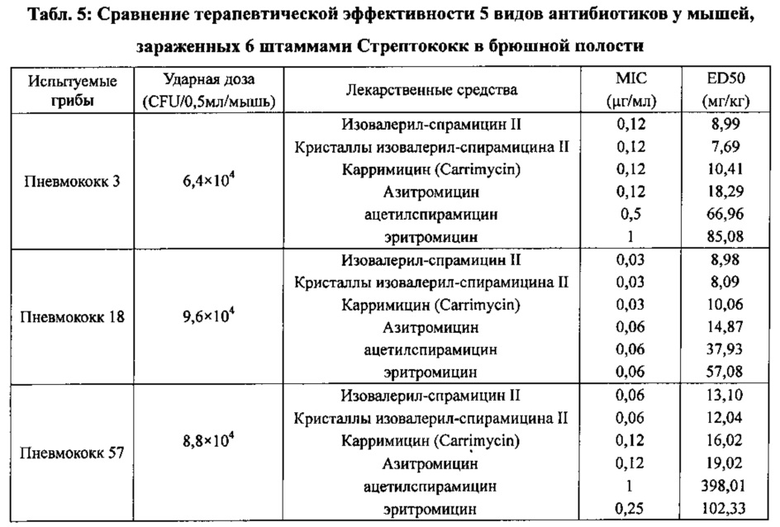



Результаты теста in vivo:
Терапевтическая эффективность кристаллов изовалерилспирамицина II при лечении мышей, зараженных 12 штаммами бактерий, приведена на табл. 13 и 14, что проявляло благоприятную защитную эффективность и превосходство перед изовалерилспирамицином II.
Кристаллы левовращающего изовалерилспирамицина II или препараты, содержащие кристаллы левовращающего изовалерилспирамицина II, приготовленные для остальных примеров изобретения, прошли одинаковые испытания и дали аналогичные результаты. Опытный пример 4. Эффективность препарата левовращающего изовалерилспирамицина III и его кристаллов in vivo.
Применяли левовращающий изовалерилспирамицин III, приготовленный по Примеру 1, и кристаллы левовращающего изовалерилспирамицина III, приготовленные по Примеру 45, и способ испытания, приведенный в Опытном примере 2.
Результаты теста in vivo приведены на табл.7 и 8:
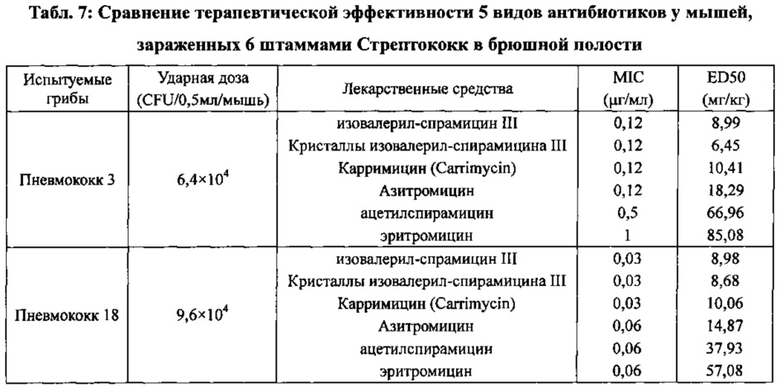



Результаты теста in vivo:
Терапевтическая эффективность кристаллов изовалерилспирамицина III при лечении мышей, зараженных 12 штаммами бактерий, приведена на табл.7 и 8, что проявляло благоприятную защитную эффективность и превосходство перед изовалерилспирамицином III.
Кристаллы левовращающего изовалерилспирамицина III или препараты, содержащие кристаллы левовращающего изовалерилспирамицина III, приготовленные для остальных примеров изобретения, прошли одинаковые испытания и дали аналогичные результаты.
Опытный пример 5 Тест in vitpo
I. Определение клинически дислоцированных бактерий:
Метод испытания: применение метода двойного разбавления в плоскодонном сосуде: налили плавленый агар в определенном количестве в плоскодонный сосуд с различной концентрацией лекарственных средств, равномерно перемешали с лекарственным раствором (добавили стрептококк и энтерококк в 5% дефибринированную кровь овцы для получения кровяной питательной среды, гемофильную палочку в 7% дефибринированную кровь овцы для получения кровяной питательной среды, питательную среду с нейссерией гонорея в 7% дефибринированную кровь овцы для получения шоколадной питательной среды), после затвердения, растворили свежий культивированный раствор с бактериями до 106 CFU/мл, засеяли многоточечным шприцем в агар плоскодонного сосуда, содержащий антибактериальные лекарственные средства, культивировали в течение 18 ч при 37°С; культивировали нейссерию гонорея в 5% CO2 инкубаторе в течение 24 ч; культивировали легионеллу в 5% CO2 инкубаторе в течение 48 ч; культивировали анаэробную бактерию в анаэробной банке в течение 48 ч при 37°С. Наблюдали минимальную ингибирующую концентрацию, при которой антибактериальные средства смогут ингибировать выращивание бактерий, т.е. минимальную бактериостатическую концентрацию (MIC), рассчитали MIC50 и MIC90 средства и провели сравнение с контрольными лекарственными средствами.
Примечание: MIC50 - 50% минимальная ингибирующая концентрация.
MIC90 - 90% минимальная ингибирующая концентрация.
Результаты испытания приведены на табл.9:
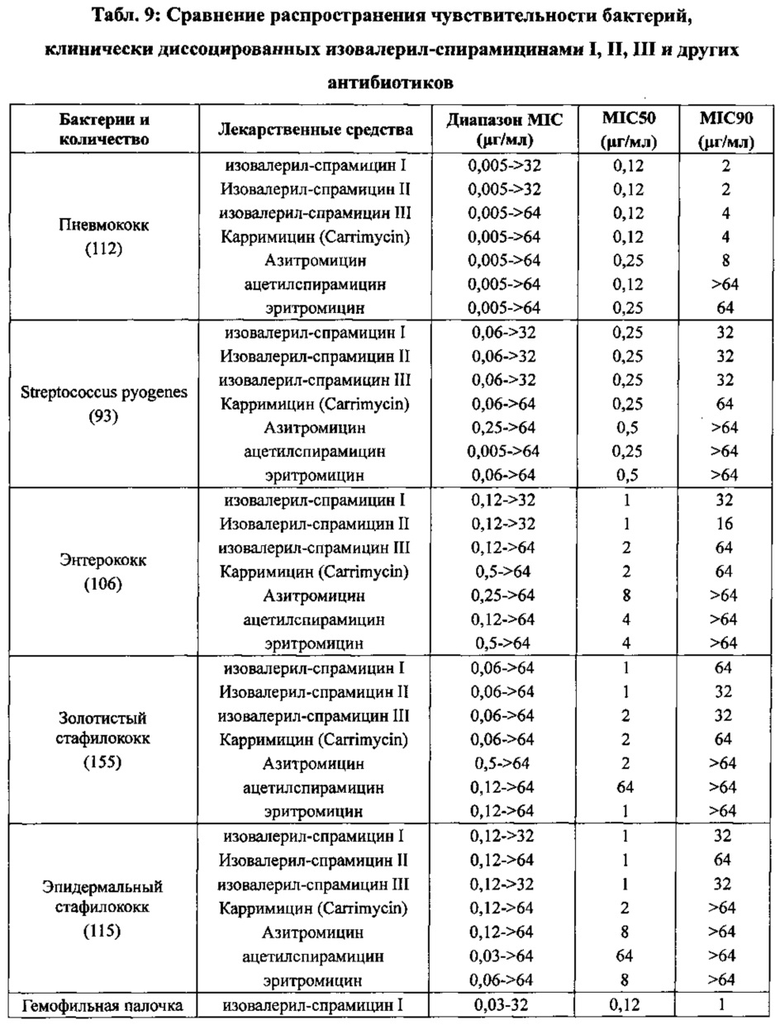

II. Определение устойчивости к трахоматозным хламидиям и хламидии пневмониз во внешней среде
Метод испытания
1. Засевали клетки НЕр-2 и McCoy на пластине для культирования клеток с 96 дырочками (Фирмы Costap), 37°С, 5% CO2 культивировали в течение 48 ч, получали однослойные клетки.
2. Растворили вакцинируемые бактерии до 10000~20000 ifu (единица, формирующая хламидийное включение)/мл, засеяли по 0,1 мл/дырочка. Засеяли серотипные B/TW-5/OT, D/UW-3/Cx трахоматозных хламидий на пластину для культирования клеток McCoy, засеяли хламидию пневмониз CWL-029 на пластину для культирования клеток НЕр-2. Сначала всосали раствор для культивирования клеток из пластины с 96 дырочками, потом засеяли по ОДмл/дырочка. В т.ч. не засевали в 4 дырочки (A11-D11) и 2 дырочки (С12 и D12).
3. После засева центрифугировали пластину для культивирования клеток с 96 дырочками на центрифуге J-6MC производства Компании Beckman-Coulter при центробежной силе ×1500g и 35°С в течение 60 мин.
4. По завершении центробежной обработки, всосали засеянные трахоматозные хламидии или хламидия пневмониз, налили 4 вида разбавленные антибиотиковых средств по 0,1 мл/дырочка соответственно.
5. Культивировали при 37°С в 5% CO2, далее культивировали на пластине для испытания на чувствительность к трахоматозным хламидиям в течение 48 ч, культивировали на пластине для испытания на чувствительность к хламидиям пневмониз в течение 72 ч. После культивирования взяли раствор с антибиотиковыми средствами и промыли два раза PBS (0.01 M, рН 7,4), обработали 100% метанолом при комнатной температуре в течение 15 мин.
6. Идентификация непрямым иммунофлюоресцентным окрашиванием: на пластину для испытания на чувствительность к трахоматозным хламидиям и к хламидиям пневмониз налили очищенные моноклональное антитело (N54 клонирование), устойчивое к трахоматозным хламидиям, и моноклональное антитело (Р33 клонирование), устойчивое к хламидиям пневмониз по 50 мкл/дырочка, культивировали во влажной камере при 37°С в течение 30 мин, потом четыре раза промыли пластину с помощью специального аппарата, далее наливали Pabbit anti pat fluopescent antibody (Фирма Sigma) по 50 мкл/дырочка, культивировали и промыли пластину по тому же методу и при тех же условиях. Налили глицерин с уплотнителем по 100 мкл/дырочка, наблюдали результаты под инвертированным флуоресцентным микроскопом Nikon (Diaphot-200).
7 Определение MIC: минимальная концентрация разбавленных антибиотиков на испытательной пластине с 96 дырочками, при которой полностью ингибировано выращивание тельца трахоматозных хламидий или хламидий пневмониз (во всех дырочках не было обнаружено включение с флуоресцентным окрашиванием).

1. В отношении серотипных B/TW-5/OT трахоматозных хламидий, изовалерилспирамицины I, II, III превосходят Карримицин (Carrimycin), эритромицин, азитромицин, ацетилспирамицин (MIC - 4 μг/мл) чуть хуже.
2. В отношении серотипных D/UW-3/Cx трахоматозных хламидий, изовалерилспирамицины I, II, III и Карримицин (Carrimycin), азитромицин обладают аналогичным внетелесным эффектом, MIC - 0.25 μг/мл, относятся к чувствительным; далее идет эритромицин (0.5 μг/мл), ацетилспирамицин (MIC - 2 μг/мл) чуть хуже.
3. В отношении хламидии пневмониз CWL-029, изовалерилспирамицин II и эритромицин являются самыми чувствительными, MIC≤0.016 μг/мл, азитромицин и Карримицин (Carrimycin), изовалерилспирамицин I, изовалерилспирамицин III более чувствительны, ацетилспирамицин (MIC - 0.5 μг/мл) чуть хуже.
4. В общем говоря, изовалерилспирамицин обладает лучшим эффектом в отношении хламидии против других испытуемых лекарственных средств.
III. Устойчивость к уреаплазмам уреалитикум и трахоматозным хламидиям во внешней среде
1. Метод испытания: наливали в дырочку стерильной пластины для культивирования клеток с 12 дырочками U-PPLO 0,8 мл (в контрольную дырочнку для раствора с бактериями налили 0,9 мд, в контрольную дырочку для питательной среды налили 1,0 мл).
2. В тестовую дырочку налили 0,1 мл раствор с бактериями Uu 104 CCU/мл, окончательное количество бактерий в дырочке 103 CCU/мл (в контрольную дырочку для питательной среды не наливали раствор с бактериями).
3. Разбили на три группы (основной антибиотиковый раствор 100 μг/мл, 10 μг/мл, 1 μг/мл), в экспериментальные дырочки), налили антибиотики для испытания с помощью стерильного Tip по двукратно убывающей концентрации: 100 мкл, 50 мкл, 25 мкл, 12.5 мкл (не наливали антибиотики в контрольные дырочки для раствора с бактериями, контрольные дырочки для питательной среды, тем временем, установили контрольные дырочки для антибиотика).
4. Равномерно перемешали вышеуказанные дырочки, уплотнили пластину клейкой лентой, положили в ингибитор для культивирования при 37°С.
5. Наблюдали и регистрировали результаты выращивания Uu в 17-24 ч после испытания. Когда в контрольных дырочках для раствора с бактериями Uu показывает положительный рост, в этом случае под минимальной MIC данной формы понимается минимальная концентрация антибиотика, при которой можно ингибировать рост Uu, под окончательной MIC (24 ч) понимается MIC, измеренная по окончании испытания.
Четыре раза определяли MIC штаммов, устойчивых к уреаплазме уреалитикум и трахоматозным хламидиям, ниже приведены результаты определения:
Величина MIC изовалерилспирамицина I: 0,025-0,125 μг/мл.
Величина MIC изовалерилспирамицина II: 0,025-0,125 μг/мл.
Величина MIC изовалерилспирамицина III: 0,025-0,125 μг/мл.
Карримицин (Carrimycin): 0,025-0,125 μг/мл.
Ацетилспирамицин: 0,5 μг/мл.
Эритромицин: 5 μг/мл.
Азитромицин: 0,025-0,125 μг/мл.
Вышеприведенные результаты показали, что изовалерилспирамицины I, II, III, Карримицин (Carrimycin) обладают благоприятной устойчивостью к Uu, как азитромицин, превосходят ацетилспирамицин, среди образцов форм данной группы эритромицин обладает наихудшей устойчивостью к Uu.
Левовращающие изовалерилспирамицины I, II, III или препараты левовращающих изовалерилспирамицинов I, II, III, приготовленные для остальных примеров изобретения, прошли одинаковые испытания и дали аналогичные результаты.
Опытный пример 4 Клинические испытание левовращающих изовалерилспирамицинов I II, III
Терапевтическая эффективность и безопасность левовращающими изовалерилспирамицинами I, II, III (полученными по Примеру 1), азитромицином при лечении острой инфекции дыхательных путей у взрослых, в т.ч. острый бактериальный фарингит, гнойный тонзиллит, острый трахеобронхит, не сильная пневмония и т.д., вызванные сенситивными бактериями.
Применяли мультицентрические, случайные, двойные слепые испытания и контролируемые испытания двойной имитацией. Испытания проводились одновременно в 5 клиниках по одинаковому варианту клинических испытаний.
I. Критерий включения испытуемых
1. Взрослые больные (мужчины и женщины) возрастом от 18 до 65 лет.
2. Острая инфекция дыхательных путей, вызванная сенситивными бактериями, в т.ч. острый бактериальный фарингит, острый гнойный тонзиллит, острый трахеобронхит, не сильная пневмония и острый назосинусит и т.д.
3. Необходимо подписание формы информированного согласия до включения.
4. Все испытуемые должны принимать противозачаточные средства в процессе исследования и не менее трех месяцев после введения лекарства.
II. Критерий исключения испытуемых
1. Больные, у которых печеночно-почечная недостаточность (Cr в крови >1,5 мг/дл ALT> нормальный верхний предел).
2. Беременная женщина или кормилица.
3. Больные, заболевшие желудочно-кишечными заболеваниями, которым не подходит пероральный прием лекарства.
4. Больные, принимавшие антибактериальные средства в течение недели до включения.
5. Человек, длительно злоупотребляющий алкоголем.
Результаты статистики показали, что клиническая эффективность (FAS):
Терапевтическая эффективность изовалерилспирамицина I, изовалерилспирамицина II, изовалерилспирамицина III и азитромицин составляет 92,30%, 92,30%, 92,30%, 89,61%) соответственно.
Клиренс бактерий:
Клиренс бактерий изовалерилспирамицина I, изовалерилспирамицина II, изовалерилспирамицина III и азитромицин составляет 97,56%, 97,56%, 97,56%, 92,86% соответственно. Неблагоприятные действия:
Неблагоприятные действия изовалерилспирамицина I, изовалерилспирамицина II, изовалерилспирамицина III и азитромицин составляет 2,5%, 2,5%, 2,5%, 7,6% соответственно.
Клинические испытания показали, что изовалерилспирамицины I, II, III являются безопасными и эффективными новыми противоинфекционными средствами.
Левовращающие изовалерилспирамицины I, II, III или препараты левовращающих изовалерилспирамицинов I, II, III, приготовленные для остальных примеров изобретения, прошли одинаковые испытания и дали аналогичные результаты.

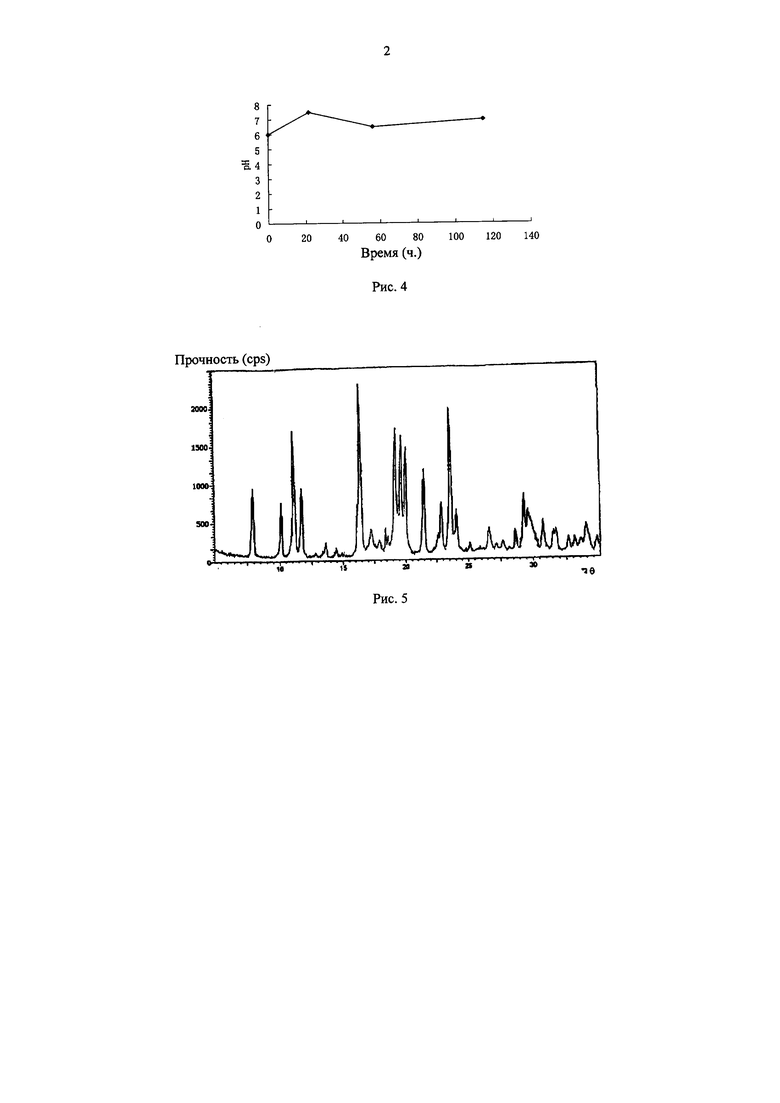
Изобретение относится к кристаллическому левоизовалерилспирамицину III формулы (I), его применению в медицине и способу его получения
 . (1),
. (1),
характеризующемуся температурой плавления 116-118°С и дифракцией рентгеновских лучей, измеренной излучением Cu-Kα с пиками при 2θ=8,0°, 10,0°, 1 1,2°, 11,7°, 16,4°, 19,1°, 19,6°, 20,0°, 21,4°, 22,9°, 23,6° и 29,4°; причем при растворении указанного соединения в хлороформе при 25°С и концентрации 0,02 г/мл угол оптического вращения [α]D составляет (-49)-(-51)°. Предложенный способ включает растворение левоизовалерилспирамицина III в смеси абсолютного метилового спирта, абсолютного этилового спирта и безводного ацетона в соотношении 1:0.1-10:0.5-1, добавление дистиллированной воды при перемешивании, охлаждение до 5-15°С до получения кристаллического соединения III. Предложен новый эффективный способ получения новой кристаллической формы, которая может быть эффективно использована для приготовления средства для лечения и/или профилактики инфекционных заболеваний. 7 н. и 12 з.п. ф-лы, 56 пр., 10 табл., 5 ил.
1. Кристаллическое соединение левоизовалерилспирамицина III, характеризующееся химической структурной формулой (I)
 (1),
(1),
с температурой плавления 116-118°С и дифракцией рентгеновских лучей на порошке кристаллического соединения левоизовалерилспирамицина III, измеренной излучением Cu-Kα с характерными пиками при 2θ=8,0°, 10,0°, 1 1,2°, 11,7°, 16,4°, 19,1°, 19,6°, 20,0°, 21,4°, 22,9°, 23,6° и 29,4°; при этом при растворении указанного кристаллического соединения хлороформом при температуре 25°С и концентрации 0,02 г/мл, измеренный угол оптического вращения [α]D составляет –(49)-(-51)°.
2. Кристаллическое соединение левоизовалерилспирамицина III по п. 1, отличающееся тем, что чистота левоизовалерилспирамицина III превышает 90 мас.%.
3. Кристаллическое соединение левоизовалерилспирамицина III по п. 1, отличающееся тем, что чистота левоизовалерилспирамицина III превышает 95 мас.%.
4. Кристаллическое соединение левоизовалерилспирамицина III по п. 1, отличающееся тем, что чистота левоизовалерилспирамицина III превышает 98 мас.%.
5. Препарат, содержащий кристаллическое соединение левоизовалерилспирамицина III по одному из пп. 1-4 и фармацевтически приемлемый носитель, отличающийся тем, что препарат выполнен в форме пилюли, капсулы, гранулы или таблетки, а содержание левоизовалерилспирамицин III составляет 10-1500 мг в одной дозе.
6. Препарат по п. 5, отличающийся тем, что содержание левоизовалерилспирамицина III составляет 50-1000 мг.
7. Препарат по п. 5, отличающийся тем, что содержание левоизовалерилспирамицина III составляет 100-500 мг.
8. Препарат по любому из пп. 2-4, отличающийся тем, что массовая доля левоизовалерилспирамицина III составляет 10-95%.
9. Препарат по п. 8, отличающийся тем, что массовая доля левоизовалерилспирамицина III составляет 50-95%.
10. Препарат по п. 8, отличающийся тем, что массовая доля левоизовалерилспирамицина III составляет 75-95%.
11. Способ приготовления кристаллического соединения левоизовалерилспирамицина III по п. 1, включающий растворение твердого соединения левоизовалерилспирамицина III в смеси растворителей абсолютного метилового спирта, абсолютного этилового спирта и безводного ацетона, добавление дистиллированной воды с одновременным перемешиванием, охлаждение до 5-15°С после добавления дистиллированной воды с продолжением перемешивания до получения кристаллического соединения левоизовалерилспирамицина III, причем отношение объема абсолютного метилового спирта, абсолютного этилового спирта и безводного ацетона в смеси растворителей составляет 1:0.1-10:0.5-1.
12. Способ приготовления кристаллического соединения левоизовалерилспирамицина III по п. 11, включающий
приготовление левовкарримицина и очистку левоизовалерилспирамицина III, причем процесс приготовления левокарримицина включает: культивирование и биологическое сбраживание клонированного штамма грибов WSJ-195, продуцируемого спирамицином с содержанием гена 4''-изовалерилтрансферазы и экстрагирование сбраживаемой жидкости;
причем упомянутый процесс культивирования представляет собой: культивирование клонированного штамма грибов WSJ-195, продуцируемого спирамицином с содержанием гена 4''-изовалерил-трансферазы на питательной среде скошенного агара, содержащей 2% муки из бобового жмыха, 1% глюкозы, 3% крахмала, 0,5% СаСО3, 0,4% NaCl и 2% агара в течение 8-15 сут при рН 6,5-7,5 и температуре 28-38°С, засев в среду для посева, содержащую 1,5% муки из бобового жмыха, 3,0% крахмала, 0,4% NaCl, 0,5% CaCO3, 0,3% рыбного пептона и 0,05%) KH2PO4 и культивирование в течение 40-80 ч при рН 6,5-7,5 и температуре 25-30°С, введение в сбраживаемую среду, содержащую 0,5% глюкозы, 6,0% крахмала, 0,5% сухих дрожжей, 2,0% рыбной муки, 0,6% NH4NO3, 1,0% NaCl, 0,5% CaCO3, 0,05% KH2PO4, 0,1% MgSO4, 0,5% бобового масла и 0,02% противовспенивателя и культивирование в течение 72-120 ч при 26-30°С, 0,1-20% количества засева для получения сбраживаемой жидкости,
причем брожение происходит при рН 6,0-9,0, когда кривые изменения рН со временем составляют три непрерывные фазы, причем первая фаза удовлетворяет условиям y1=0.1364x1+6.0, или y1=0.0909x1+6.4, или y1=0.0682x1+6.0 где 0<х1≤22; вторая фаза удовлетворяет условиям у2=-0.0735х2+10.64 или у2=-0.0441х2+7.8 или у2=-0.0294х2+8.147, где 22≤х2≤56; а третья фаза удовлетворяет условиям у3=0.0078х3+6.06, где 56≤х3≤120, где x1 х2 и х3 означают, соответственно, часы, a y1, у2 и у3 указывают значение рН, соответственно, в течение каждого ферментационного процесса;
стадия экстрагирования биологически сбраживаемой жидкости включает: обработку сбраживаемой жидкости сернокислым алюминием для получения фильтрата, регулировку уровня рН фильтрата до 8,5 - 9,0, экстрагирование бутилацетатом, промывку бутилацетатного экстракта обессоленной водой и l% NaH2PO4, последующее экстрагирование водой рН 2,0-2,5 для получения водного экстракта, регулирование уровня рН до 4,5-5,5, испарение и удаление остаточного бутилацетата для получения водного экстракта, фильтрование и регулировку уровня рН фильтрата до 8,5-9,0, осаждение и орошение фильтрата очищенной водой для получения влажного вещества, последующее осушение для получения левокарримицина,
стадия очистки левоизовалерилспирамицина III включает: очистку образца левовращающего карримицина хроматографическим разделением, градиентную элюцию и выделение целевого пика состава левоизовалерилспирамицина III хроматографической колонной ODS с помощью ацетонитрила и буферного раствора уксуснокислого аммония,
при очистке левоизовалерилспирамицина III регистрировали ультрафиолетовую спектрограмму выделения левоизовалерилспирамицина III с помощью препаративной высокоэффективной жидкостной хроматографии и ультрафиолетового контроля и собирали образцы левоизовалерилспирамицина III согласно времени выдержки 48,009 мин,
подвижной фазой является смешанный растворитель ацетонитрила А и водного раствора уксуснокислого аммония рН=8,5, 150 мМ,
условия, необходимые для очистки левоизовалерилспирамицина III: линейный градиент: 0-60 мин, А: 25-65%; и 61-90 мин, А: 65-90%;
скорость потока: 260 мЛ/мин;
объем вводимого образца: 10 мЛ;
концентрация вводимого образца: 0,5 г/ мЛ;
контрольная длина волны: 231 нм;
способ сбора: ультрафиолетовый пуск
в процессе очистки левоизовалерилспирамицина III очищали собранный левоизовалерилспирамицин III от ацетонитрила вращающим испарением, экстрагировали этилацетатом и удаляли этилацетат из экстракта испарением для получения пастообразных образцов; проводили повторное растворение полученных образцов петролейным эфиром и удаление петролейного эфира испарением для получения белого порошка левоизовалерилспирамицина III.
13. Способ по п. 12, отличающийся тем, что брожение происходит при рН 6,0-8,0.
14. Способ по п. 12, отличающийся тем, что брожение происходит при рН 6,0-7,5.
15. Способ по п. 11, отличающийся тем, что отношение объема абсолютного метилового спирта, абсолютного этилового спирта и безводного ацетона в смеси растворителей составляет 1:2-8:0,8-1.
16. Применение кристаллического соединения левоизовалерилспирамицина III по п. 1 для приготовления средства для лечения и/или профилактики инфекционных заболеваний
17. Применение препарата по любому из пп. 5-10 для приготовления средства для лечения и/или профилактики инфекционных заболеваний.
18. Применение кристаллического соединения левоизовалерилспирамицина III по п. 1 для приготовления антибактериальных средств, включая следующие бактерии: пневмококк, стрептококк группы А, стрептококк пиогенный, энтерококк, золотистый стафилококк, эпидермальный стафилококк, микрококк катаральный, гонококк, гемофильная палочка, кишечная палочка, энтеротоксигенная кишечная палочка, патогенная кишечная палочка, энтероинвазивная кишечная палочка, синегнойная палочка, клебсиелла пневмонии, вульгарный протей, брюшнотифозная палочка, акинетобактерии, цитробактер, серрация марцесценс, шигелла Зонне, шигелла Флекснера, Tritirachium album; легионеллы, такие как легионелла пневмофила, legionella gormanii, legionella bozemanii, legionella dumoffii, legionella jordanis и legionella micdadei; анаэробные бактерии, такие как бактероиды фрагилис, B.thetaiotaomicron, бактероиды вульгатус, B.distasonis, В. prevotella, Prevotella asaccharolyticus, Prevotella oralis, палочка Плаута, Fusobacterium russii, бифидобактерии, лактобацилла, пептострептококки, пропионибактерии акне, клостридия перфрингенс или дрожжеподобный грибок.
19. Применение препарата по любому из пп. 5-10 для приготовления антибактериальных средств, включая следующие бактерии: пневмококк, стрептококк группы А, стрептококк пиогенный, энтерококк, золотистый стафилококк, эпидермальный стафилококк, микрококк катаральный, гонококк, гемофильная палочка, кишечная палочка, энтеротоксигенная кишечная палочка, патогенная кишечная палочка, энтероинвазивная кишечная палочка, синегнойная палочка, клебсиелла пневмонии, вульгарный протей, брюшнотифозная палочка, акинетобактерии, цитробактер, серрация марцесценс, шигелла Зонне, шигелла Флекснера, Tritirachium album; легионеллы, такие как легионелла пневмофила, legionella gormanii, legionella bozemanii, legionella dumoffii, legionella jordanis и legionella micdadei; анаэробные бактерии, такие как бактероиды фрагилис, B.thetaiotaomicron, бактероиды вульгатус, B.distasonis, В. prevotella, Prevotella asaccharolyticus, Prevotella oralis, палочка Плаута, Fusobacterium russii, бифидобактерии, лактобацилла, пептострептококки, пропионибактерии акне, клостридия перфрингенс или дрожжеподобный грибок.
| Yang Ya-li et al, HPLC, 2009, 44(10) 1183-1186 | |||
| CN 1554355 A, 15.12.2004 | |||
| CN 1405299 A, 31.03.1978 | |||
| JP 53034788 A, 31.03.1978 | |||
| RU 2007108544 A, 20.09.2008. |
Авторы
Даты
2018-03-14—Публикация
2011-05-25—Подача