Область техники
Настоящее изобретение относится к соединению для ингибирования активностей тирозинкиназы Брутона (ВТК) и/или Янус-киназы 3 (JAK3), его фармацевтической композиции, их применению в изготовлении лекарственного средства, способу использования этого соединения в ингибировании активностей ВТК и/или JAK3 и способу использования этого соединения в лечении и/или предупреждении ВТК- и/или JAK3-опосредованных заболеваний или расстройств у млекопитающих, в частности у людей.
Предшествующий уровень техники
Протеинкиназа представляет одно из самых больших семейств человеческих ферментов, и к настоящему времени было идентифицировано более 500 видов протеинкиназ в организме человека. Такие протеинкиназы модулируют активности конкретных белков путем переноса фосфатных групп на эти белки и затем контролируют сложные пути передачи сигналов. Нарушение активности протеинкиназ связано со многими заболеваниями, включая злокачественные новообразования, аутоиммунные расстройства и другие. Благодаря значительной роли протеинкиназ в путях передачи сигналов и связи между киназной активностью и многими заболеваниями, ингибиторы киназ стали актуальным предметом для поиска и разработки новых химических веществ.
BTK (тирозинкиназа Брутона) представляет собой нерецепторную тирозинкиназу семейства TEC. BTK является основным посредником в пути передачи сигналов B-клеточного рецептора (BCR) и является ключевым модулятором раннего созревания B-клетки, а также активации, передачи сигналов и выживания зрелых B-клеток. Таким образом, ингибиторы ВТК могут быть использованы для лечения заболеваний, ассоциированных с аберрантной активацией B-клеток, например, аутоиммунных заболеваний, включая ревматоидный артрит и системную красную волчанку, и так далее. Эффективность ингибитора ВТК для лечения аутоиммунных заболеваний была предварительно продемонстрирована в доклинических животных моделях (Honigberg, L.A. et al, Proceedings of the National Academy of Sciences of the United States of America, 2010, 107, 13075-13080). Помимо В-клеток, экспериментальные подтверждения показывают, что ВТК также участвует в путях передачи сигналов моноцитов, макрофагов, нейтрофилов и тучных клеток. Ингибитор ВТК может подавлять FcγR-индуцированное высвобождение цитокинов, включая фактор некроза опухоли альфа (TNFa), интерлейкины IL-1β и IL-6, из моноцитов и макрофагов, а также может снижать FcγR-индуцированную дегрануляцию тучных клеток (Chang В.Y. et al, Arthritis Research & Therapy, 2011, 13, R115).
Путь передачи сигнала, опосредованный B-клеточным рецептором (BCR), крайне необходим для выживания многих лимфом. В качестве ключевой киназы в BCR пути, BTK представляет таким образом потенциальную терапевтическую мишень для лимфом. В клинических испытаниях ингибиторы BTK демонстрируют значительные эффекты в лечении хронического лимфоцитарного лейкоза (CLL). Ингибиторы ВТК также проявляют значительные эффекты в отношении других лимфом, таких как диффузная крупноклеточная B-клеточная лимфома и лимфома из клеток зоны мантии, и так далее (Buggy, J.J. et al, International Reviews of Immunology, 2012, 31, 119-132).
Янус-киназы представляют собой принципиально важные тирозинкиназы для модулирования клеточной функции лимфатических и гемопоэтических клеток. Янус-киназы включают четыре известных представителя семейства, представляющие собой JAK1, JAK2, JAK3 и TYK2, соответственно, и где JAK3 (Янус тирозинкиназа 3) экспрессируется главным образом в лимфоцитах и природных клетках-киллерах. JAK3 конститутивно связана с общей γc-цепью, которая является общей рецепторной субъединицей для IL-2, IL-4, IL-7, IL-9, IL-15 и IL-21 (Ghoreschi К. et al, Immunological Reviews, 2009, 228, 273-87). Эти цитокины, опосредуемые через JAK3, являются существенными для пролиферации, дифференцировки и функционирования лимфоцитов. Потеря функции JAKS-киназы приведет к иммунодефициту как у людей, так и у мышей. В виду существенной роли JAKS-киназы в иммунной системе JAK3-киназа представляет очень привлекательную мишень для лечения связанных с иммунитетом заболеваний, например аутоиммунных заболеваний типа ревматоидного артрита или отторжения аллотрансплантата у пациентов с трансплантацией органов. Селективный ингибитор JAK3 показывает значительную эффективность в клинических испытаниях ревматоидного артрита.
Помимо индивидуальной эффективности ингибиторов ВТК и ингибиторов JAK3, одновременное ингибирование как BTK пути, так и JAK3 пути будет потенциально давать синергетические эффекты при клиническом применении. Например, в экспериментах Cetkovic-Cvrlje М et al подтверждают, что комбинированное использование ингибиторов BTK и JAK3 может улучшать индексы выживания у животных в моделях реакции «трансплантат против хозяина» (GVHD) (Cetkovic-Cvrlje М. et al, British Journal of Haematology, 2004, 126, 821-827).
Таким образом, необходима разработка новых соединений, нацеленных на BTK и/или JAK3 пути, проявляющих хорошую эффективность и доступных для перорального приема, которые также демонстрируют фармакокинетические свойства, благоприятные для терапевтических применений, а также проявляющих достаточно низкие токсические и побочные эффекты in vivo.
Краткое изложение сущности изобретения
Согласно одному аспекту настоящего изобретения предложено соединение, представленное формулой I (далее иногда называемое соединением формулы I):
 ,
,
где:
R представляет собой С3-8циклоалкил, замещенный группой -NR2W; 4-10-членную насыщенную N-гетероциклическую группу, которая содержит только один атом азота в своем кольце, и этот атом азота замещен W; или C1-4алкил, замещенный 4-10-членной насыщенной N-гетероциклической группой, которая содержит только один атом азота в своем кольце, и этот атом азота замещен W;
W представляет собой 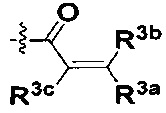 или
или  ;
;
V представляет собой C или N;
X представляет собой O, S или NR4;
Y представляет собой CH, O или S;
Z представляет собой CH, O, S или NR5;
R1 представляет собой C6-12арил или 5-12-членный гетероарил, возможно замещенный одним или более R6;
R2 представляет собой водород или C1-8алифатик;
R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(C1-8алифатик)аминометила;
R4 представляет собой водород или C1-8алифатик;
R5 представляет собой водород или C1-8алифатик;
каждый R6 независимо выбран из группы, состоящей из галогена, нитро, циано, гетероциклила, C6-12арила, 5-12-членного гетероарила, C1-8алифатика, С1-8галогеналифатика, гетероциклил-C1-8алифатика, гидрокси-C1-8алифатика, С1-8алифатикокси-С1-8алифатика, С1-8алифатиккарбонилокси-С1-8алифатика, амино-С1-8алифатика, карбокси-C1-8алифатика, C1-8алифатикамино-С1-8алифатика, ди(С1-8алифатик)амино-С1-8алифатика, С1-8алифатикациламино-С1-8алифатика, С1-8алифатиккарбонил-С1-8алифатика, C1-8алифатикоксикарбонил-C1-8алифатика, аминоацил-С1-8алифатика, С1-8алифатикаминоацил-С1-8алифатика, ди(С1-8алифатик)аминоацил-С1-8алифатика, C1-8алифатиксульфонил-С1-8алифатика, С1-8алифатиксульфинил-С1-8алифатика, С1-8алифатиксульфониламино, С1-8алифатиксульфониламино-С1-8алифатика, сульфамоил-С1-8алифатика, С1-8алифатикаминосульфонил-С1-8алифатика, ди(С1-8алифатик)аминосульфонил-С1-8алифатика, ди(С1-8алифатик)фосфонил-С1-8алифатика, гидрокси, С1-8алифатикокси, гетероциклилокси, гетероциклил-C1-8алифатикокси, гидрокси-С1-8алифатикокси, С1-8алифатикокси-С1-8алифатикокси, амино-C1-8алифатикокси, С1-8алифатикамино-С1-8алифатикокси, ди(С1-8алифатик)амино-С1-8алифатикокси, С1-8алифатикациламино-С1-8алифатикокси, С1-8алифатиккарбонил-С1-8алифатикокси, аминоацил-C1-8алифатикокси, C1-8алифатикаминоацил-С1-8алифатикокси, ди(С1-8алифатик)аминоацил-С1-8алифатикокси, амино, C1-8алифатикамино, ди(C1-8алифатик)амино, гетероциклиламино, гетероциклил-C1-8алифатикамино, гидрокси-C1-8алифатикамино, C1-8алифатикокси-C1-8-алифатикамино, амино-C1-8алифатикамино, C1-8алифатикамино-С1-8алифатикамино, ди(C1-8алифатик)амино-C1-8алифатикамино, С1-8алифатикациламино-C1-8алифатикамино, C1-8алифатиккарбонил-C1-8алифатикамино, аминоацил-C1-8алифатикамино, C1-8алифатикаминоацил-C1-8алифатикамино, ди(C1-8алифатик)аминоацил-С1-8алифатикамино, C1-8алифатикациламино, гетероциклил-C1-8алифатикациламино, гетероциклилациламино, гидрокси-C1-8алифатикациламино, С1-8алифатикокси-С1-8алифатикациламино, амино-C1-8алифатикациламино, C1-8алифатикамино-C1-8алифатикациламино, ди(C1-8алифатик)амино-С1-8алифатикациламино, C1-8алифатиккарбонила, гетероциклилкарбонила, гетероциклил-C1-8алифатиккарбонила, C1-8алифатикоксикарбонила, гетероциклил-C1-8алифатикоксикарбонила, ди(C1-8алифатик)амино-С1-8алифатикоксикарбонила, аминоацила, C1-8алифатикаминоацила, ди(C1-8алифатик)аминоацила, гетероциклил-C1-8алифатикаминоацила, гетероциклиламиноацила, гидрокси-C1-8алифатикаминоацила, С1-8алифатикокси-С1-8алифатикаминоацила, амино-C1-8алифатикаминоацила, С1-8алифатикамино-C1-8алифатикаминоацила, ди(C1-8алифатик)амино-C1-8алифатикаминоацила, С1-8алифатиксульфгидрила, гетероциклилсульфгидрила, гетероциклил-C1-8алифатиксульфгидрила, C1-8алифатиксульфонила, C1-8алифатиксульфинила, гетероциклилсульфонила, гетероциклилсульфинила, гетероциклил-C1-8алифатиксульфонила, гетероциклил-C1-8алифатиксульфинила, сульфамоила, C1-8алифатикаминосульфонила, ди(С1-8алифатик)аминосульфонила, гетероциклил-С1-8алифатикаминосульфонила, гетероциклиламиносульфонила, ди(С1-8алифатик)амино-С1-8алифатикаминосульфонила, аминосульфинила, C1-8алифатикаминосульфинила, ди(С1-8алифатик)аминосульфинила, гетероциклиламиносульфинила и ди(C1-8алифатик)фосфонила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-12-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, О и S; возможно, каждый гетероциклил независимо замещен одним или более заместителями, выбранными из группы, состоящей из галогена, C1-8алифатика, гидрокси-C1-8алифатика, C1-8алифатикокси-C1-8алифатика, амино-C1-8алифатика, C1-8алифатикамино-C1-8алифатика, ди(С1-8алифатик)амино-С1-8алифатика, гетероциклил-C1-8алифатика, гетероциклила, 5-12-членного гетероарила, гидрокси, C1-8алифатикокси, амино, C1-8алифатикамино, ди(С1-8алифатик)амино, C1-8алифатиккарбонила, гетероциклилкарбонила, гетероциклил-C1-8алифатиккарбонила, гидрокси-C1-8алифатиккарбонила, C1-8алифатикокси-C1-8алифатиккарбонила, ди(С1-8алифатик)амино-С1-8алифатиккарбонила, C1-8алифатикоксикарбонила, аминоацила, С1-8алифатикаминоацила, ди(C1-8алифатик)аминоацила, С1-8алифатиксульфонила, C1-8алифатиксульфинила, гетероциклилсульфонила, гетероциклилсульфинила, гетероциклил-C1-8алифатиксульфонила, гетероциклил-С1-8алифатиксульфинила, сульфамоила, C1-8алифатикаминосульфонила, ди(C1-8алифатик)аминосульфонила; и
возможно, С6-12арил и 5-12-членный гетероарил независимо замещены одним или более заместителями, выбранными из группы, состоящей из галогена, C1-8алифатика, гидрокси, С1-8алифатикокси, амино, C1-8алифатикамино и ди(С1-8алифатик)амино,
где С1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, С2-8алкенила, C2-8алкинила, С3-8циклоалкила и С4-8циклоалкенила,
или его стереоизомер, таутомер, сольват или фармацевтически приемлемая соль.
В некоторых воплощениях в настоящем изобретении предложено соединение, представленное формулой Ia (далее иногда называемое соединением формулы Ia):
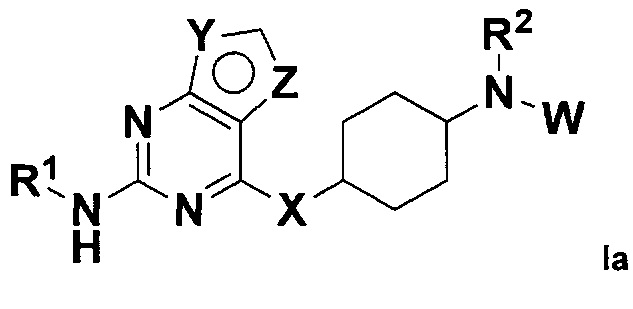 ,
,
где X, Y, Z, W, R1 и R2 все являются такими, как определено в формуле I, или его стереоизомер, таутомер, сольват или фармацевтически приемлемая соль.
В некоторых воплощениях в настоящем изобретении предложено соединение, представленное формулой Ib (далее иногда называемое соединением формулы Ib):
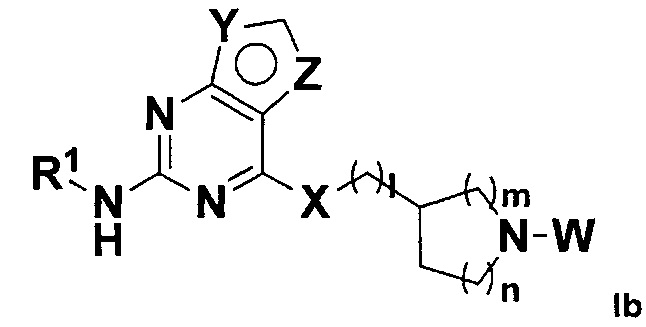 ,
,
где:
X, Y, Z, W и R1 все являются такими, как определено в формуле I;
I равно 0, 1, 2, 3 или 4, причем когда I равно 0,  представляет собой
представляет собой 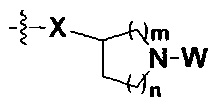 ;
;
m равно 0, 1, 2, 3 или 4; причем когда m равно 0, 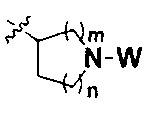 представляет собой
представляет собой 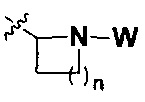 ; и
; и
n равно 0, 1, 2 или 3; причем когда n равно 0, 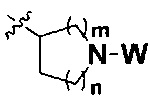 представляет собой
представляет собой 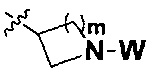 ,
,
или его стереоизомер, таутомер, сольват или фармацевтически приемлемая соль.
В некоторых воплощениях в настоящем изобретении предложено соединение, представленное формулой Ic (далее иногда называемое соединением формулы Ic):
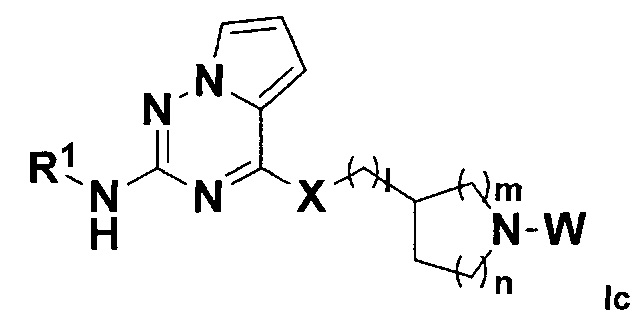 ,
,
где:
X, W и R1 все являются такими, как определено в формуле I;
I равно 0, 1, 2, 3 или 4; причем когда I равно 0, 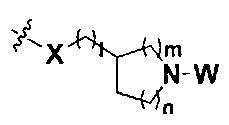 представляет собой
представляет собой 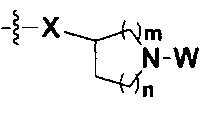 ;
;
m равно 0, 1, 2, 3 или 4; причем когда m равно 0, 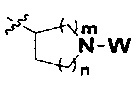 представляет собой
представляет собой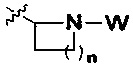 ; и
; и
n равно 0, 1, 2 или 3; причем когда n равно 0,  представляет собой
представляет собой  ,
,
или его стереоизомер, таутомер, сольват или фармацевтически приемлемая соль.
Еще один аспект настоящего изобретения относится к фармацевтической композиции, содержащей одно или более соединений формулы I (в частности соединений формул Ia, Ib и Ic) по настоящему изобретению или их стереоизомер, таутомер, сольват или фармацевтически приемлемую соль и фармацевтически приемлемые эксципиенты.
Фармацевтическая композиция по настоящему изобретению дополнительно содержит один или более чем один агент, выбранный из группы, состоящей из: иммунодепрессантов, кортикостероидов, нестероидных противовоспалительных лекарственных средств, специфических ингибиторов циклооксигеназы-2 (Cox-2), белков, связывающих фактор некроза опухоли альфа (TNF-α), интерферонов и интерлейкинов.
Еще один аспект настоящего изобретения относится к применению соединения формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомера, таутомера, сольвата или фармацевтически приемлемой соли в изготовлении лекарственного средства для ингибирования активностей тирозинкиназы Брутона (ВТК) и/или Янус-киназы 3 (JAK3).
Еще один аспект настоящего изобретения относится к применению соединения формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомера, таутомера, сольвата или фармацевтически приемлемой соли в изготовлении лекарственного средства для предупреждения или лечения ВТК- и/или JAK3-опосредованных заболеваний.
Еще один аспект настоящего изобретения относится к применению фармацевтической композиции по настоящему изобретению, содержащей одно или более соединений формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомер, таутомер, сольват или фармацевтически приемлемую соль и фармацевтически приемлемые эксципиенты, в изготовлении лекарственного средства для ингибирования активностей ВТК и/или JAK3. В некоторых воплощениях фармацевтическая композиция дополнительно содержит, в дополнение к вышеупомянутым соединениям, один или более агентов, выбранных из группы, состоящей из иммунодепрессантов, кортикостероидов, нестероидных
противовоспалительных лекарственных средств, специфических ингибиторов Cox-2, белков, связывающих TNF-α, интерферонов и интерлейкинов.
Еще один аспект настоящего изобретения относится к применению фармацевтической композиции по настоящему изобретению, содержащей одно или более соединений формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению, или их стереоизомеры, таутомеры, сольваты или фармацевтически приемлемые соли и фармацевтически приемлемые эксципиенты, в изготовлении лекарственного средства для предупреждения или лечения ВТК- и/или JAK3-опосредованных заболеваний. В некоторых воплощениях фармацевтическая композиция дополнительно содержит, в дополнение к вышеупомянутым соединениям, один или более агентов, выбранных из группы, состоящей из иммунодепрессантов, кортикостероидов, нестероидных противовоспалительных лекарственных средств, специфических ингибиторов Cox-2, белков, связывающих TNF-α, интерферонов и интерлейкинов.
Еще один аспект настоящего изобретения относится к соединению формулы I, в частности соединениям формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомеру, таутомеру, сольвату или фармацевтически приемлемой соли для ингибирования активностей ВТК и/или JAK3.
Еще один аспект настоящего изобретения относится к соединению формулы I, в частности соединениям формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомеру, таутомеру, сольвату или фармацевтически приемлемой соли для предупреждения или лечения ВТК- и/или JAK3-опосредованного заболевания.
Еще один аспект настоящего изобретения относится к фармацевтической композиции, содержащей соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению или его стереоизомер, таутомер, сольват или фармацевтически приемлемую соль, для ингибирования активностей ВТК и/или JAK3.
Еще один аспект настоящего изобретения относится к фармацевтической композиции, содержащей соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению или его стереоизомер, таутомер, сольват или фармацевтически приемлемую соль, для предупреждения или лечения ВТК- и/или JAK3-опосредованного заболевания.
Еще один аспект настоящего изобретения относится к способу ингибирования активностей ВТК и/или JAK3 в биологической системе, включающему приведение указанной биологической системы в контакт с соединением формулы I, в частности соединениями формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомером, таутомером, сольватом или фармацевтически приемлемой солью или с фармацевтической композицией, содержащей соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению или его стереоизомер, таутомер, сольват или фармацевтически приемлемую соль.
Еще один аспект настоящего изобретения относится к способу предупреждения или лечения ВТК- и/или JAK3-опосредованных заболеваний, включающему введение млекопитающему (в частности человеку), нуждающемуся в этом, терапевтически эффективного количества соединения формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомера, таутомера, сольвата или фармацевтически приемлемой соли или фармацевтической композиции, содержащей соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению или его стереоизомер, таутомер, сольват или фармацевтически приемлемую соль.
Еще один аспект настоящего изобретения относится к применению соединения формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомера, таутомера, сольвата или фармацевтически приемлемой соли в комбинации с одним или более чем одним агентом, выбранным из группы, состоящей из иммунодепрессантов, кортикостероидов, нестероидных противовоспалительных лекарственных средств, специфических ингибиторов Cox-2, белков, связывающих TNF-α, интерферонов и интерлейкинов, в изготовлении лекарственного средства для лечения ВТК- и/или JAKS-опосредованного заболевания.
В настоящей заявке ВТК- и/или JAK3-опосредованные заболевания выбраны из группы, состоящей из аутоиммунных заболеваний, воспалительных заболеваний, гетероиммунных состояний или заболеваний, тромбоэмболических заболеваний и злокачественных новообразований.
Краткое описание графических материалов
На Фиг. 1 показан ингибирующий эффект соединения 132 в отношении ВТК пути в клетках Ramos.
На Фиг. 2 показаны баллы для соединения 132 в модели mCIA.
На Фиг. 2 показаны баллы для соединения 132 в модели rAIA.
Подробное описание воплощений
Если не указано иное, используемые здесь научные и технические термины имеют такие же значения, как они обычно понимаются специалистом в данной области техники.
Следует понимать, что представленное выше краткое изложение и следующее ниже подробное описание даны только для иллюстративных целей без ограничения каким-либо образом объема объекта по настоящему изобретению.
Все литературные источники или разделы из литературных источников включающие, без ограничения, патенты, заявки на патенты, статьи, книги, руководства и тезисы докладов, как цитировано в настоящей заявке, включены в данное описание ссылкой во всей полноте.
Общее количество атомов углерода в химической группе, как определено здесь, представлено в виде сокращенной формы записи перед группой. Например, C1-8алифатик относится к алифатической группе, как определено ниже, имеющей суммарно от 1 до 8 атомов углерода; C1-8алкил относится к алкильной группе, как определено ниже, имеющей суммарно от 1 до 8 атомов углерода; C3-8циклоалкил относится к циклоалкильной группе, как определено ниже, имеющей суммарно от 3 до 8 атомов углерода; С6-12арил относится к арильной группе, как определено ниже, имеющей суммарно от 6 до 12 атомов углерода. Атомы углерода, которые могут существовать в заместителях данной химической группы, не включены в суммарное количество атомов углерода, указанное в сокращенной форме записи.
Если иное не указано в описании, все объединенные группы согласно настоящему изобретению (то есть, группы, содержащие две или более групп) присоединены к остальной части молекулы таким образом, чтобы последняя описанная группа служила в качестве точки присоединения. Например, "гетероциклилалифатик" означает, что гетероциклическая группа присоединена к остальной части молекулы через алифатическую группу; "алифатикокси" означает, что алифатическая группа присоединена к остальной части молекулы через оксигруппу; и так далее.
В дополнение к указанному выше, как используют в описании и формуле изобретения, если не указано иное, следующие термины имеют значения, как изложено ниже:
"Амино" относится к группе -NH2.
"Циано" относится к группе -CN.
"Гидрокси" относится к группе -OH.
"Нитро" относится к группе -NO2.
"Оксо" относится к заместителю =O.
"Карбонил" или "ацил" относится к группе -C(=O)-.
"Сульфгидрил" относится к группе -S.
"Сульфонил" относится к группе -S(=O)2-.
"Сульфинил" относится к группе -S(=O)-.
"Фосфонил" относится к группе -P(=O)(ОН)2.
"Аминоацил" относится к группе -C(=O)-NH2.
"Сульфамоил" относится к группе -S(=O)2-NH2.
"Аминосульфинил" относится к группе -S(=O)-NH2.
В настоящей заявке термин "галоген" относится к фтору, хлору, брому или йоду, предпочтительно фтору или хлору.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "алифатик" или "алифатическая группа" относится к насыщенной или ненасыщенной группе, имеющей фундаментальные свойства алифатического соединения, состоящей исключительно из атомов углерода и атомов водорода, и которая присоединена к остальной части молекулы простой связью. Алифатическая группа включает прямые или разветвленные алкильные, алкенильные, алкинильные, циклоалкильные и циклоалкенильные группы, где алкил, алкенил, алкинил, циклоалкил и циклоалкенил являются такими, как определено здесь ниже. В настоящей заявке алифатик относится к алкилу, алкенилу, алкинилу, циклоалкилу и/или циклоалкенилу, предпочтительно относится к алкилу и/или циклоалкилу. Все атомы водорода в алифатической группе возможно заменены любыми подходящими группами, например галогеном, гидрокси, амино, монозамещенным амино, дизамещенным амино, алкокси, гетероциклилом, и тому подобным.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "алкил" или "алкильная группа" относится к прямой или разветвленной группе, состоящей исключительно из атомов углерода и водорода, не содержащей ненасыщенные связи, и которая присоединена к остальной части молекулы простой связью. Алкильная группа может содержать, например, от 1 до 18, предпочтительно от 1 до 12, более предпочтительно от 1 до 8 атомов углерода. Примеры алкила включают, без ограничения, метил, этил, пропил, изопропил, н-бутил, изобутил, трет-бутил, н-пентил, 2-пентил, гексил, гептил, 2-метилгексил, 3-метилгексил, октил, нонил, децил, и тому подобное, предпочтительно метил, этил, пропил, изопропил и н-бутил, более предпочтительно метил, этил, пропил и изопропил. Все атомы водорода в алкильной группе могут быть заменены любыми подходящими группами, например галогеном, гидрокси, амино, монозамещенным амино, дизамещенным амино, алкокси, гетероциклилом и тому подобным.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "алкенил" или "алкенильная группа" относится к углеводородной группе с прямой или разветвленной цепью, состоящей исключительно из атомов углерода и водорода, содержащей по меньшей мере одну двойную связь, имеющей, например, от 2 до 18, предпочтительно от 2 до 10, более предпочтительно от 2 до 8 атомов углерода, и которая присоединена к остальной части молекулы простой связью, включающей, без ограничения, этенил, пропенил, аллил, бут-1-енил, бут-2-енил, пент-1-енил, пент-2-енил, пент-1,4-диенил и тому подобное, предпочтительно этенил и пропенил. Все атомы водорода в алкенильной группе могут быть заменены любыми подходящими группами, например галогеном, гидрокси, амино, монозамещенным амино, дизамещенным амино, алкокси, гетероциклилом и тому подобным.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "алкинил" или "алкинильная группа" относится к углеводородной группе с прямой или разветвленной цепью, состоящей исключительно из атомов углерода и водорода, содержащей по меньшей мере одну тройную связь и возможно содержащей одну или более двойных связей, имеющей, например, от 2 до 18, предпочтительно от 2 до 10, более предпочтительно от 2 до 8 атомов углерода, и которая присоединена к остальной части молекулы простой связью. Примеры алкинила включают, без ограничения, этинил, проп-1-инил, пент-1-ен-4-инил, и тому подобное. Все атомы водорода в алкинильной группе возможно заменены любыми подходящими группами, например галогеном, гидрокси, амино, алкокси, гетероциклилом и тому подобным.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "циклоалкил" или "циклоалкильная группа" относится к подходящей насыщенной неароматической моноциклической или полициклической углеводородной группе, состоящей исключительно из атомов углерода и водорода, которая может включать конденсированные или связанные мостиковой связью циклические системы, имеющей, например, от 3 до 15, предпочтительно от 3 до 10, более предпочтительно от 3 до 8 атомов углерода, и которая присоединена к остальной части молекулы простой связью через подходящий атом углерода в кольце. Циклоалкильная группа включает, без ограничения, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, бицикло[2.2.1]гептил, 7,7-диметил-бицикло[2.2.1]гептил, бицикло[2.2.2]октил, бицикло[3.1.1]гептил, бицикло[3.2.1]октил, адамантил, и тому подобное, предпочтительно группы циклобутил, циклопентил и циклогексил. Все атомы водорода в циклоалкильной группе могут быть возможно заменены любыми подходящими группами, например галогеном, гидрокси, амино, монозамещенным амино, дизамещенным амино, алкилом, алкокси, гетероциклилом и тому подобным.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "циклоалкенил" относится к подходящей неароматической моноциклической или полициклической углеводородной группе, состоящей исключительно из атомов углерода и водорода, и содержащей по меньшей мере одну двойную связь, которая может включать конденсированные или связанные мостиковой связью циклические системы, имеющей, например, от 3 до 15, предпочтительно от 3 до 10, более предпочтительно от 3 до 8 атомов углерода, и которая присоединена к остальной части молекулы простой связью через подходящий атом углерода в кольце. Примеры циклоалкенила включают, без ограничения, циклобутенил, циклопентенил, циклогексенил, 1,3-циклогексадиен, 1,4-циклогексадиен, 1H-инденил, 2,3-дигидро-инденил, 1,2,3,4-тетрагидро-нафтил, 5,6,7,8-тетрагидро-нафтил, 8,9-дигидро-7H-бензоциклогептен-6-ил, 6,7,8,9-терагидро-5H-бензоциклогептенил, 5,6,7,8,9,10-гексагидро-бензоциклооктенил, флуоренил, бицикло[2.2.1]гептенил, бицикло[2.2.2]октил, бицикло[2.2.2]октенил, бицикло[3.2.1]октенил, октагидро-4,7-метилен-1H-инденил, октагидро-2,5-метилен-пентадиенил, и тому подобное. Все атомы водорода в циклоалкенильной группе возможно заменены любыми подходящими группами, например галогеном, гидрокси, амино, монозамещенным амино, дизамещенным амино, алкилом, алкокси, гетероциклилом и тому подобным.
В настоящей заявке, термин "галогеналифатик" относится к алифатической группе, как она определена выше, которая замещена одним или более атомами галогена. Примеры галогеналифатика включают, без ограничения, фторметил, дифторметил, трифторметил, фторэтил, 1,1-дифторэтил, хлорметил, хлорэтил, дихлорметил, 1,2-дихлорэтил, фторэтенил, фторциклопентил, фторциклогексил, хлорциклогексенил, и тому подобное, предпочтительно фторэтил.
В настоящей заявке, термин "гидроксиалифатик" относится к алифатической группе, как она определена выше, замещенной одной или более гидроксигруппами. Примеры гидроксиалифатика включают, без ограничения, 1-гидроксиэтил, 1,2-дигидроксиэтил, 3-гидрокси-циклопентил, 4-гидрокси-циклогексил, 3,4-дигидрокси-циклогексил, и тому подобное, предпочтительно 1-гидроксиэтил.
В настоящей заявке, термин "аминоалифатик" относится к алифатической группе, как она определена выше, замещенной одной или более аминогруппами.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "алифатикокси" относится к группе, представленной формулой -ORa, где Ra представляет собой алифатическую группу, как она определена выше. Алифатическая группировка алифатикоксигруппы может быть возможно замещена как описано выше для алифатической группы. Примеры алифатикокси включают, без ограничения, метокси, этокси, изобутокси, н-бутокси, изобутокси, трет-бутокси, этенилокси, 1-пропенилокси, 1-пропинилокси, циклопентилокси, циклогексилокси, и тому подобное, предпочтительно метокси и этокси.
В настоящей заявке, термин "гидроксиалифатикокси" относится к алифатической группе, как она определена выше, где алифатическая группировка замещена одной или более гидроксигруппами. Примеры гидроксиалифатикокси включают, без ограничения, 1-гидроксиэтокси, 1-гидроксипропокси, 3-гидрокси-циклопентилокси, 3,4-дигидроксициклогексилокси, и тому подобное, предпочтительно 1-гидроксиэтокси.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "алифатиккарбонил" относится к группе формулы -C(=O)-Ra, где Ra представляет собой алифатическую группу, как она определена выше. Алифатическая группировка в группе алифатиккарбонил может быть возможно замещена как описано выше для алифатической группы. Алифатиккарбонил включает алкилкарбонил, алкенилкарбонил, алкинилкарбонил, циклоалкилкарбонил и циклоалкенилкарбонил, где алкил, алкенил, алкинил, циклоалкил и циклоалкенил являются такими, как определено выше. В настоящей заявке алифатиккарбонил предпочтительно относится к алкилкарбонилу и/или циклоалкилкарбонилу. Примеры алифатиккарбонила включают, без ограничения, метилкарбонил (также называемый ацетил), этилкарбонил (также называемый пропионил), изопропилкарбонил, бутилкарбонил, этенилкарбонил, пропенилкарбонил, циклопентилкарбонил, циклогексилкарбонил, и тому подобное, предпочтительно метилкарбонил.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "алифатикамино" относится к группе формулы -NHRa, где Ra представляет собой алифатическую группу, как она определена выше. Апалифатикаминогруппа включает алкиламино, алкениламино, алкиниламино, циклоалкиламино и циклоалкениламино, где указанные группировки алкил, алкенил, алкинил, циклоалкил и циклоалкенил все являются такими, как определено выше. В настоящей заявке группа алифатикамино предпочтительно относится к группам алкиламино и/или циклоалкиламино. Примеры включают, без ограничения, метиламино, этиламино, изопропиламино, этениламино, пропениламино, пропиниламино, циклобутиламино, циклопентиламино, циклогексиламино, циклогексениламино, и тому подобное, предпочтительно метиламино, этиламино, циклогексиламино.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "диалифатикамино" относится к аминогруппе, в которой два атома водорода соответственно заменены алифатической группой, и которая может быть представлена формулой -NRaRb, где Ra и Rb независимо представляют собой алифатическую группу, как она определена выше. В настоящей заявке группа диалифатикамино предпочтительно относится к группе диалкиламино. Примеры диалкиламино включают, без ограничения, диметиламино, диэтиламино, дипропиламино, метилэтиламино, и тому подобное, предпочтительно диметиламино.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "алифатикоксиалифатикокси" относится к группе алифатикокси, как она определена выше, где алифатическая группировка замещена группой алифатикокси, как она определена выше. Группа алифатикоксиалифатикокси предпочтительно относится к группам алкоксиалкокси, алкоксициклоалкокси и/или циклоалкоксиалкокси. Примеры алифатикоксиалифатикокси включают, без ограничения, метоксизтокси, этоксиэтокси, метоксициклопентилокси, метоксициклогексилокси, циклопентилоксиметокси, и тому подобное.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "алифатикаминоалифатик" относится к алифатической группе, как она определена выше, которая замещена группой алифатикамино, как она определена выше.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "диалифатикаминоалифатик" относится к алифатической группе, как она определена выше, которая замещена группой диалифатикамино, как она определена выше. Примеры диалифатикаминоалифатика включают, без ограничения, диметиламиноэтил, диэтиламиноэтил, (метил)(этил)аминоэтил, и тому подобное, предпочтительно диметиламиноэтил.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "диалифатикаминоалифатикамино" относится к группе алифатикамино, как она определена выше, где алифатическая группировка замещена группой диалифатикамино, как определено выше. Примеры включают, без ограничения, диметиламиноэтиламино, диэтиламиноэтиламино, (метил)(этил)аминоэтиламино, и тому подобное, предпочтительно диметиламиноэтиламино.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "алифатикаминоацил" относится к аминоацильной группе, где один атом водорода в аминогруппировке замещен алифатической группой, как она определена выше, и которая может быть представлена формулой -С(=O)-NH-Ra, где Ra представляет собой алифатическую группу, как определено выше. Примеры алифатикаминоацила включают, без ограничения, -C(=O)-NH-CH3, -C(=O)-NH-C2H5, циклогексиламиноацил, и тому подобное, предпочтительно -C(=O)-NH-CH3.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "гетероциклил" относится к стабильной 3-18-членной неароматической кольцевой группе, содержащей от 1 до 6 гетероатомов, выбранных из азота, кислорода и серы. Если в описании конкретно не указано иное, гетероциклическая группа может представлять собой моноциклическую, бициклическую, трициклическую или полициклическую кольцевую систему, которая может включать конденсированные или связанные мостиковой связью системы. Для целей настоящего изобретения, гетероциклил предпочтительно представляет собой стабильную 3-12-членную неароматическую моноциклическую или бициклическую кольцевую группу, содержащую от 1 до 3 гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы, более предпочтительно стабильную 3-8-членную неароматическую моноциклическую кольцевую группу, содержащую от 1 до 3 гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы. Атом азота, углерода и серы в указанной гетероциклической группе может быть возможно окисленным; атом азота может быть возможно кватернизированным; и гетероциклическая группа может быть частично или полностью насыщенной. Гетероциклическая группа может быть присоединена к остальной части молекулы простой связью через атом углерода или гетероатом. В гетероциклической группе, содержащей конденсированные кольца, одно или более колец могут представлять собой арильные или гетероарильные кольца, при условии что точка присоединения гетероциклической группы к остальной части молекулы находится по атому в неароматическом кольце. Примеры таких гетероциклических групп включают, без ограничения, азетидинил, пиранил, тетрагидропиранил, тиопиранил, тетрагидрофуранил, морфолинил, тиоморфолинил, пиперазинил, пиперидинил, оксазинил, диоксоланил, тетрагидроизохинолин, декагидроизохинолинил, имидазолинил, имидазолидинил, хинолизинил, тиазолидинил, изотиазолидинил, изоксазолидинил, индолинил, октагидроиндолил, октагидроизоиндолил, пирролидинил, пиразолидинил, фталимидо, и тому подобное, предпочтительно пиперазинил, пиперидил, тетрагидропиранил и морфолинил. Гетероциклическая группа может быть возможно замещена любыми подходящими заместителями, включая, без ограничения, галоген, гидрокси, амино, алкил, алкокси, алкилкарбонил, и тому подобное.
В настоящей заявке, "N-гетероциклил" относится к гетероциклической группе, как она определена выше, содержащей по меньшей мере один атом азота в ее кольце.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "гетероциклилокси" относится к группе формулы -ORh, где Rh представляет собой гетероциклическую группу, как она определена выше. Гетероциклическая группировка в группе гетероциклилокси может быть возможно замещена как описано выше для гетероциклической группы.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "гетероциклилкарбонил" относится к группе формулы -С(=O)-Rh, где Rh представляет собой гетероциклическую группу, как она определена выше. Гетероциклическая группировка в группе гетероциклилкарбонил может быть возможно замещена как описано выше для гетероциклической группы.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "гетероциклиламино" относится к группе формулы Rh-NH-, где Rh представляет собой гетероциклическую группу, как она определена выше. Гетероциклическая группировка в группе гетероциклиламино может быть возможно замещена как описано выше для гетероциклической группы.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "гетероциклиламиноацил" относится к группе аминоацил, как она определена выше, где один водород в аминогруппировке заменен гетероциклической группой, как она определена выше, и который может быть представлен формулой -C(=O)-NH-Rh, где Rh представляет собой гетероциклическую группу, как она определена выше. Гетероциклическая группировка в группе гетероциклиламиноацил может быть возможно замещена как описано выше для гетероциклической группы.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "гетероциклилалифатик" относится к алифатической группе, как она определена выше, которая замещена гетероциклической группой, как она определена выше. Гетероциклическая группировка в группе гетероциклилалифатик может быть возможно замещена как описано выше для гетероциклической группы, и алифатическая группировка в группе гетероциклилалифатик может быть возможно замещена как описано выше для алифатической группы.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "гетероциклилалифатикокси" относится к группе алифатикокси, как она определена выше, в которой алифатическая группировка замещена гетероциклической группой, как она определена выше. Гетероциклическая группировка в группе гетероциклилалифатикокси может быть возможно замещена как описано выше для гетероциклической группы, и алифатическая группировка в группе гетероциклилалифатикокси может быть возможно замещена как описано выше для алифатической группы.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "арил" относится к системной группе, имеющей от 6 до 18, предпочтительно от 6 до 12, атомов углерода и по меньшей мере одно ароматическое кольцо. Для целей настоящего изобретения арильная группа может представлять собой моноциклическую, бициклическую, трициклическую или полициклическую кольцевую систему, которая может включать конденсированные или связанные мостиковой связью системы. Арильная группа присоединена к остальной части молекулы простой связью через атом в ароматическом кольце. Примеры таких арильных групп включают, без ограничения, фенил, нафтил, антрил, фенантрил, флуоренил, 2-бензоксазолинон, 2Н-1,4-бензоксазин-3(4H)-он-7-ил, и тому подобное, предпочтительно фенил.
В настоящей заявке, в независимой группе или как часть другой(их) групп(ы), термин "гетероарил" относится к 5-16-членной кольцевой системной группе, содержащей от 1 до 4 гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы, и по меньшей мере одно ароматическое кольцо. Если в настоящем описании не указано иное, гетероарильная группа может представлять собой моноциклическую, бициклическую, трициклическую или полициклическую кольцевую систему, которая может включать конденсированные или связанные мостиковой связью кольцевые системы, при условии что точка присоединения находится по атому ароматического кольца. Атомы азота, углерода или серы в гетероарильной группе могут быть возможно окисленными; и атом азота может быть возможно кватернизированным. Для целей настоящего изобретения гетероарильная группа предпочтительно представляет собой стабильную 5-12-членную ароматическую моноциклическую или бициклическую кольцевую группу, содержащую от 1 до 3 гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы, более предпочтительно стабильную 5-8-членную ароматическую моноциклическую или бициклическую кольцевую группу, содержащую от 1 до 3 гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы, и наиболее предпочтительно стабильную 5-6-членную ароматическую моноциклическую кольцевую группу, содержащую 1-2 гетероатома, выбранные из группы, состоящей из азота, кислорода и серы. Примеры таких гетероарильных групп включают, без ограничения, тиенил, фурил, пирролил, имидазолил, бензимидазолил, пиразолил, бензопиразолил, триазолил, тетразолил, пиридинил, пиразинил, триазинил, пиримидинил, пиридазинил, индолизинил, индолил, изоиндолил, индазолил, изоиндазолил, пуринил, хинолил, изохинолил, нафтиридинил, нафтиридинил, хиноксалинил, птеридинил, карбазолил, карболинил, фенантридинил, фенантролинил, акридинил, феназинил, тиазолил, изотиазолил, бензотиазолил, бензотиенил, оксазолил, изоксазолил, оксадиазолил, оксатриазолил, циннолинил, хиназолинил, фенилтио, индолизинил, фенантролинил, феноксазинил, фенотиазинил, 4,5,6,7-тетрагидро-бензо[b]тиенил, нафтопиридинил, имидазо[1,2-a]пиридинил, и тому подобное, предпочтительно пирролил, пиразолил, имидазолил, тиенил, изоксазолил, тиазолил, изотиазолил, пиридинил и имидазо[1,2-a]пиридинил, и более предпочтительно пиразолил, тиенил, изоксазолил, тиазолил и изотиазолил.
В настоящей заявке, "возможный" или "возможно" означает, что последующие описанные случай или обстоятельство могут иметь место или могут не существовать и что описание включает примеры, где указанные случай или обстоятельство имеют место, и примеры, в которых их нет. Например, "алкил, возможно замещенный одним или более галогеном" означает алкильную группу, незамещенную или замещенную одним или более галогенами, и что описание включает как замещенные алкильные группы, так и незамещенные алкильные группы.
"Стереоизомер" относится к соединению, состоящему из тех же атомов, связанных теми же связями, но имеющих другие трехмерные структуры. Настоящее изобретение предусматривает разные стереоизомеры и их смеси.
Так как соединения формулы I по настоящему изобретению содержат олефиновые двойные связи, и если не указано иное, подразумевается, что соединения включают как E-, так и Z-геометрические изомеры.
"Таутомер" относится к изомеру, полученному в результате протонового сдвига от одного атома молекулы к другому атому той же молекулы. Все таутомерные формы соединения формулы I по настоящему изобретению включены в объем настоящего изобретения.
В настоящей заявке термин "фармацевтически приемлемая соль" включает фармацевтически приемлемые соли присоединения кислоты и основания.
"Фармацевтически приемлемая соль присоединения кислоты" относится к таким солям, которые способны сохранять биологическую эффективность свободных оснований без каких-либо нежелательных эффектов и которые получают с неорганическими или органическими кислотами. Неорганические кислоты включают, без ограничения, соляную кислоту, бромоводородную кислоту, серную кислоту, азотную кислоту, фосфорную кислоту и тому подобное; и органические кислоты включают, без ограничения, муравьиную кислоту, уксусную кислоту, трифторуксусную кислоту, пропионовую кислоту, каприловую кислоту, капроновую кислоту, каприновую кислоту, ундециленовую кислоту, гликолевую кислоту, глюконовую кислоту, молочную кислоту, щавелевую кислоту, себациновую кислоту, адипиновую кислоту, глутаровую кислоту, малоновую кислоту, малеиновую кислоту, янтарную кислоту, фумаровую кислоту, винную кислоту, лимонную кислоту, пальмитиновую кислоту, стеариновую кислоту, олеиновую кислоту, коричную кислоту, лауриновую кислоту, яблочную кислоту, глутаминовую кислоту, пироглутаминовую кислоту, аспарагиновую кислоту, бензойную кислоту, метансульфоновую кислоту, лзра-толуолсульфоновую кислоту, альгиновую кислоту, аскорбиновую кислоту, салициловую кислоту, 4-аминосалициловую кислоту, нафталин-дисульфоновую кислоту, и тому подобное. Эти соли могут быть получены способами, известными в данной области техники.
"Фармацевтически приемлемая соль присоединения основания" относится к тем солям, которые способны сохранять биологические эффективности свободных кислот без каких-либо нежелательных эффектов. Эти соли получают в результате добавления неорганического основания или органического основания к свободной кислоте. Соли, получаемые с неорганическими основаниями, включают, без ограничения, соли натрия, калия, лития, аммония, кальция, магния, железа, цинка, меди, марганца, алюминия и тому подобные. Предпочтительные неорганические соли представляют собой соли аммония, натрия, калия, кальция и магния. Соли, получаемые с органическими основаниями, включают, без ограничения, соли первичных, вторичных и третичных аминов, замещенных аминов, включая природные замещенные амины, циклические амины и основные ионообменные смолы, например аммоний, изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, диэтаноламин, триэтаноламин,
диметилэтаноламин, 2-диметиламиноэтанол, 2-диэтиламиноэтанол, дициклогексиламин, лизин, аргинин, гистидин, кофеин, холин, бетаин, этилендиамин, глюкозамин, метилглюкамин, теобромин, трометамин, пурины, пиперазин, пиперидин, N-этилпиперидин, полиаминные смолы, и тому подобное.
В зависимости от количества заряженных функциональных групп и валентности катионов и анионов, соединение по настоящему изобретению может содержать множество катионов или анионов.
Часто при кристаллизациях образуется сольват соединения по настоящему изобретению. В настоящей заявке "сольват" относится к агрегату, содержащему одну или более молекул соединения по настоящему изобретению с одной или более молекулами растворителя. Они либо реагируют друг с другом в растворителе, либо осаждаются или кристаллизуются из растворителя. Растворитель может представлять собой воду, в таком случае сольват является гидратом. Альтернативно, растворитель может представлять собой органический растворитель. Сольваты соединений по настоящему изобретению также входят в объем настоящего изобретения.
В настоящей заявке "фармацевтическая композиция" относится к композиции, приготовленной из соединения по настоящему изобретению и среды, общепринятой в данной области техники для доставки биологически активного соединения млекопитающим, например людям. Указанная среда включает фармацевтически приемлемые эксципиенты. Фармацевтическая композиция по настоящему изобретению может представлять собой единый препарат, либо она может представлять собой комбинацию из нескольких препаратов.
В настоящей заявке "фармацевтически приемлемый эксципиент" включает, без ограничения, любой адъювант, носитель, эксципиент, смазывающее вещество, подсластитель, разбавитель, консервант, краситель/окрашивающий агент, корригент, поверхностно-активное вещество, увлажняющий агент, диспергирующий агент, суспендирующий агент, стабилизатор, изотонический агент, растворитель или эмульгатор, который был одобрен соответствующими государственными органами как пригодный для использования у людей и домашних животных.
В настоящей заявке "терапевтически эффективное количество" относится к такому количеству соединения по настоящему изобретению, которое при введении млекопитающему, например человеку, является достаточным для эффективного лечения заболевания или расстройства у животного, например человека. Количество соединения по изобретению, которое составляет "терапевтически эффективное количество", будет варьировать в зависимости от конкретно используемого соединения, конкретного расстройства, подлежащего лечению, причины расстройства, мишеней лекарственного средства, тяжести заболевания, пути введения, а также возраста, веса, физического состояния и др., млекопитающего, подлежащего лечению, но может быть рутинным образом определено специалистом в данной области в соответствии с его собственными знаниями и согласно описанию настоящей заявки.
Согласно одному аспекту настоящего изобретения в настоящем изобретении предложено соединение, представленное формулой I:

где:
R представляет собой C3-8циклоалкил, замещенный группой -NR2W; 4-10-членную насыщенную N-гетероциклическую группу, которая содержит только один атом азота в своем кольце, и этот атом азота замещен W; или C1-4алкил, замещенный 4-10-членной насыщенной N-гетероциклической группой, которая содержит только один атом азота в своем кольце, и этот атом азота замещен W;
W представляет собой  или
или 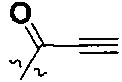 ;
;
V представляет собой C или N;
X представляет собой O, S или NR4;
Y представляет собой CH, O или S;
Z представляет собой CH, O, S или NR5;
R1 представляет собой С6-12арил или 5-12-членный гетероарил, возможно замещенный одним или более R6;
R2 представляет собой водород или C1-8алифатик;
R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(С1-8алифатик)аминометила;
R4 представляет собой водород или C1-8алифатик;
R5 представляет собой водород или C1-8алифатик;
каждый R6 независимо выбран из группы, состоящей из галогена, нитро, циано, гетероциклила, C6-12арила, 5-12-членного гетероарила, C1-8алифатика, C1-8галогеналифатика, гетероциклил-C1-8алифатика, гидрокси-С1-8алифатика, C1-8алифатикокси-C1-8алифатика, C1-8алифатиккарбонилокси-C1-8алифатика, амино-C1-8алифатика, C1-8валифатикамино-C1-8алифатика, ди(C1-8алифатик)амино-С1-8алифатика, С1-8алифатикациламино-С1-8алифатика, C1-8алифатиккарбонил-С1-8алифатика, С1-8алифатикоксикарбонил-С1-8алифатика, аминоацил-С1-8алифатика, С1-8алифатикаминоацил-С1-8алифатика, ди(C1-8алифатик)аминоацил-С1-8алифатика, С1-8алифатиксульфонил-С1-8алифатика, С1-8алифатиксульфинил-С1-8алифатика, С1-8алифатиксульфониламино, C1-8алифатиксульфониламино-С1-8алифатика, сульфамоил-С1-8алифатика, C1-8алифатикаминосульфонил-С1-8алифатика, ди(C1-8алифатик)аминосульфонил-С1-8алифатика, ди(С1-8алифатик)фосфонил-С1-8алифатика, гидрокси, C1-8алифатикокси, гетероциклилокси, гетероциклил-C1-8алифатикокси, гидрокси-C1-8алифатикокси, C1-8алифатикокси-C1-8алифатикокси, амино-C1-8алифатикокси, С1-8алифатикамино-С1-8алифатикокси, ди(С1-8алифатик)амино-C1-8алифатикокси, C1-8алифатикациламино-С-изалифатикокси, C1-8алифатиккарбонил-С1-8алифатикокси, аминоацил-C1-8алифатикокси, C1-8алифатикаминоацил-С1-8алифатикокси, ди(С1-8алифатик)аминоацил-C1-8алифатикокси, амино, С1-8алифатикамино, ди(С1-8алифатик)амино, гетероциклиламино, гетероциклил-C1-8алифатикамино, гидрокси-C1-8алифатикамино, С1-8алифатикокси-С1-8алифатикамино, амино-C1-8алифатикамино, С1-8алифатикамино-С1-8алифатикамино, ди(C1-8алифатик)амино-С1-8алифатикамино, С1-8алифатикациламино-C1-8алифатикамино, С1-8алифатиккарбонил-С1-8алифатикамино, аминоацил-C1-8алифатикамино, С1-8алифатикаминоацил-C1-8алифатикамино, ди(C1-8алифатик)аминоацил-C1-8алифатикамино, C1-8алифатикациламино, гетероциклил-C1-8алифатикациламино, гетероциклилациламино, гидрокси-C1-8алифатикациламино, С1-8алифатикокси-С1-8алифатикациламино, амино-C1-8алифатикациламино, С1-8алифатикамино-С1-8алифатикациламино, ди(C1-8алифатик)амино-С1-8алифатикациламино, С1-8алифатиккарбонила, гетероциклилкарбонила, гетероциклил-С1-8алифатиккарбонила, C1-8алифатикоксикарбонила, гетероциклил-С1-8алифатикоксикарбонила, ди(C1-8алифатик)амино-С1-8алифатикоксикарбонила, аминоацила, C1-8алифатикаминоацила, ди(С1-8алифатик)аминоацила, гетероциклил-C1-8алифатикаминоацила, гетероциклиламиноацила, гидрокси-C1-8алифатикаминоацила, C1-8алифатикокси-C1-8алифатикаминоацила, амино-C1-8алифатикаминоацила, С1-8алифатикамино-С1-8алифатикаминоацила, ди(C1-8алифатик)амино-С1-8алифатикаминоацила, С1-8алифатиксульфгидрила, гетероциклилсульфгидрила, гетероциклил-С1-8алифатиксульфгидрила, C1-8алифатиксульфонила, С1-8алифатиксульфинила, гетероциклилсульфонила, гетероциклилсульфинила, гетероциклил-С1-8алифатиксульфонила, гетероциклил-С1-8алифатиксульфинила, сульфамоила, C1-8алифатикаминосульфонила, ди(С1-8алифатик)аминосульфонила, гетероциклил-С1-8алифатикаминосульфонила, гетероциклиламиносульфонила, ди(С1-8алифатик)амино-С1-8алифатикаминосульфонила, аминосульфинила, C1-8алифатикаминосульфинила, ди(С1-8алифатик)аминосульфинила, гетероциклил-С1-8алифатикаминосульфинила, гетероциклиламиносульфинила, ди(С1-8алифатик)фосфонила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-12-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, О и S; возможно, каждый гетероциклил независимо замещен одним или более заместителями, выбранными из группы, состоящей из галогена, C1-8алифатика, гидрокси-C1-8алифатика, C1-8алифатикокси-С1-8алифатика, амино-С1-8алифатика, С1-8алифатикамино-С1-8алифатика, ди(С1-8алифатик)амино-C1-8алифатика, гетероциклил-C1-8алифатика, гетероциклила, 5-12-членного гетероарила, гидрокси, C1-8алифатикокси, амино, C1-8алифатикамино, ди(С1-8алифатик)амино, C1-8алифатиккарбонила, гетероциклилкарбонила, гетероциклил-C1-8алифатиккарбонила, гидрокси-C1-8алифатиккарбонила, C1-8алифатикокси-C1-8алифатиккарбонила, ди(С1-8алифатик)амино-С1-8алифатиккарбонила, C1-8алифатикоксикарбонила, аминоацила, С1-8алифатикаминоацила, ди(C1-8алифатик)аминоацила, C1-8алифатиксульфонила, С1-8алифатиксульфинила, гетероциклилсульфонила, гетероциклилсульфинила, гетероциклил-C1-8алифатиксульфонила, гетероциклил-C1-8алифатиксульфинила, сульфамоила, C1-8алифатикаминосульфонила и ди(С1-8алифатик)аминосульфонила; и
возможно, C6-12арил и 5-12-членный гетероарил независимо замещены одним или более заместителями, выбранными из группы, состоящей из галогена, C1-8алифатика, гидрокси, С1-8алифатикокси, амино, C1-8алифатикамино и ди(С1-8алифатик)амино,
где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила,
или его стереоизомер, таутомер, сольват или фармацевтически приемлемая соль.
В некоторых воплощениях соединения формулы I, R представляет собой C3-8циклоалкил, замещенный группой -NR2W, где R2 представляет собой водород или C1-8алифатик; и W представляет собой  или
или 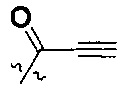 , где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена, и ди(C1-8алифатик)аминометила, где С1-8алифатик в каждом случае независимо выбран из группы, состоящей из С1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила.
, где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена, и ди(C1-8алифатик)аминометила, где С1-8алифатик в каждом случае независимо выбран из группы, состоящей из С1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила.
В некоторых воплощениях соединения формулы I, R представляет собой циклогексил, замещенный группой -NR2W, где R2 представляет собой водород или C1-8алифатик; и W представляет собой 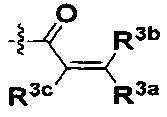 или
или 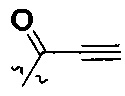 , где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(C1-8алифатик)аминометила, где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила.
, где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(C1-8алифатик)аминометила, где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила.
В некоторых воплощениях соединения формулы I, R представляет собой циклогексил, замещенный группой -NR2W, где R2 представляет собой водород или C1-8алкил; и W представляет собой  или
или  , где R3a, R3b и R3c все представляют собой водород.
, где R3a, R3b и R3c все представляют собой водород.
В некоторых воплощениях соединения формулы I, R представляет собой 4-10-членную насыщенную N-гетероциклическую группу, которая содержит только один атом азота в своем кольце, и этот атом азота замещен W, где W представляет собой 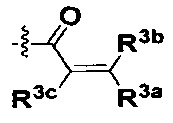 , где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(С1-8алифатик)аминометила, где C1-8алифатик выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила.
, где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(С1-8алифатик)аминометила, где C1-8алифатик выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях R представляет собой 4-10-членную насыщенную N-гетероциклическую группу, которая содержит только один атом азота в своем кольце, и этот атом азота замещен W, где W представляет собой  , где R3a, R3b и R3c все представляют собой водород.
, где R3a, R3b и R3c все представляют собой водород.
В некоторых воплощениях соединения формулы I, R представляет собой 4-10-членную насыщенную N-гетероциклическую группу, которая содержит только один атом азота в своем кольце, и этот атом азота замещен W, где W представляет собой 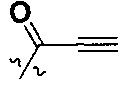 .
.
В некоторых воплощениях соединения формулы I, R представляет собой C1-4алкил, замещенный 4-10-членной насыщенной N-гетероциклической группой, которая содержит только один атом азота в своем кольце, и этот атом азота замещен W, где W представляет собой  , где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(C1-8алифатик)аминометила, где C1-8алифатик выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила.
, где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(C1-8алифатик)аминометила, где C1-8алифатик выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы I, R представляет собой C1-4алкил, замещенный 4-10-членной насыщенной N-гетероциклической группой, которая содержит только один атом азота в своем кольце, и этот атом азота замещен W, где W представляет собой 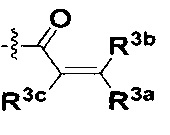 , где R3a, R3b и R3c все представляют собой водород.
, где R3a, R3b и R3c все представляют собой водород.
В некоторых воплощениях соединения формулы I, R представляет собой C1-4алкил, замещенный 4-10-членной насыщенной N-гетероциклической группой, которая содержит только один атом азота в своем кольце, и этот атом азота замещен W, где W представляет собой 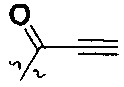 .
.
В некоторых воплощениях соединения формулы I, X представляет собой О. В некоторых других воплощениях соединения формулы I, X представляет собой S. В некоторых дополнительных воплощениях соединения формулы I, X представляет собой NR4, R4 представляет собой водород или C1-8алифатик, где C1-8алифатик независимо выбран из группы, состоящей из С1-8алкила, C2-8алкенила, C2-8алкинила, С3-8циклоалкила и C4-8циклоалкенила. В некоторых воплощениях, X представляет собой NR4, R4 представляет собой водород или C1-8алкил, и более предпочтительно, водород или метил.
В некоторых воплощениях соединения формулы I, V представляет собой С. В некоторых других воплощениях соединения формулы I, V представляет собой N.
В некоторых воплощениях соединения формулы I, Y представляет собой CH. В некоторых других воплощениях соединения формулы I, Y представляет собой O. В некоторых дополнительных воплощениях соединения формулы I, Y представляет собой S.
В некоторых воплощениях соединения формулы I, Z представляет собой CH. В некоторых других воплощениях соединения формулы I, Z представляет собой O. В некоторых дополнительных воплощениях соединения формулы I, Z представляет собой S. В некоторых дополнительных воплощениях соединения формулы I, Z представляет собой NR5, R5 представляет собой водород или C1-8алифатик, где C1-8алифатик независимо выбран из группы, состоящей из C1-8алкила, С2-8алкенила, С2-8алкинила, С3-8циклоалкила и C4-8циклоалкенила. В некоторых воплощениях, R5 представляет собой водород или C1-8алкил, и более предпочтительно, водород или метил.
В некоторых воплощениях соединения формулы I по меньшей мере один из V, Y и Z представляет собой гетероатом.
В некоторых воплощениях соединения формулы I, R1 представляет собой C6-12арил или 5-12-членный гетероарил, возможно замещенный одним или более R6, где каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, C1-8алифатика, C1-8галогеналифатика, гетероциклил-C1-8алифатика, гидрокси-C1-8алифатика, C1-8алифатикокси-C1-8алифатика, амино-C1-8алифатика, С1-8алифатикамино-С1-8алифатика, ди(С1-8алифатик)амино-C1-8алифатика, C1-8алифатикокси, гетероциклилокси, гетероциклил-C1-8алифатикокси, гидрокси-C1-8алифатикокси, C1-8алифатикокси-C1-8алифатикокси, С1-8алифатикамино, ди(C1-8алифатик)амино, гетероциклиламино, амино-C1-алифатикамино, С1-8алифатикамино-С1-8алифатикамино, ди(C1-8алифатик)амино-C1-8алифатикамино, C1-8алифатиккарбонила, гетероциклилкарбонила, аминоацила, C1-8алифатикаминоацила, ди(С1-8алифатик)аминоацила, гетероциклиламиноацила, сульфамоила, C1-8алифатикаминосульфонила, ди(С1-8алифатик)аминосульфонила, гетероциклиламиносульфонила, аминосульфинила, C1-8алифатикаминосульфинила, ди(С1-8алифатик)аминосульфинила и гетероциклиламиносульфинила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, O и S; возможно, каждый гетероциклил замещен одним или более заместителями, выбранными из группы, состоящей из гидрокси, C1-8алифатика, C1-8алифатикокси, амино и C1-8алифатиккарбонила;
где С1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, С3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы I, R1 представляет собой C6-12арил или 5-12-членный гетероарил, возможно замещенный одним или более R6; каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, C1-8алифатика, C1-8галогеналифатика, гетероциклил-C1-8алифатика, гидрокси-C1-8алифатика, C1-8алифатикокси-C1-8алифатика, C1-8алифатикамино-C1-8алифатика, ди(С1-8алифатик)амино-С1-8алифатика, гетероциклилокси, гетероциклил-C1-8алифатикокси, гетероциклиламино, C1-8алифатиккарбонила, гетероциклилкарбонила, гетероциклиламиноацила, где: гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, O и S; возможно, каждый гетероциклил независимо замещен одним или более C1-8алифатическими заместителями.
В некоторых воплощениях соединения формулы I, R1 представляет собой C6-12арил, возможно замещенный одним или более R6; каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, C1-8алифатика, C1-8галогеналифатика, C1-8алифатикокси, гетероциклилокси, гетероциклил-C1-8алифатикокси, гидрокси-C1-8алифатикокси, C1-8алифатикокси-C1-8алифатикокси, C1-8алифатикамино, ди(C1-8алифатик)амино, гетероциклиламино, амино-C1-8алифатикамино, C1-8алифатикамино-C1-8алифатикамино, ди(C1-8алифатик)амино-C1-8алифатикамино, C1-8алифатиккарбонила, гетероциклилкарбонила, аминоацила, C1-8алифатикаминоацила, ди(C1-8алифатик)аминоацила, гетероциклиламиноацила, сульфамоила, C1-8алифатикаминосульфонила, ди(С1-8алифатик)аминосульфонила, гетероциклиламиносульфонила, аминосульфинила, C1-8алифатикаминосульфинила, ди(С1-8алифатик)аминосульфинила и гетероциклиламиносульфинила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, O и S; возможно, каждый гетероциклил независимо замещен одним или более заместителями, выбранными из группы, состоящей из гидрокси, C1-8алифатика, C1-8алифатикокси, амино и C1-8алифатиккарбонила;
где С1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы I, R1 представляет собой фенил, возможно замещенный одним или более R6; каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, С1-8алифатика, C1-8алифатикокси, гетероциклилокси, гетероциклил-C1-8алифатикокси, гидрокси-C1-8алифатикокси, С1-8алифатикокси-C1-8алифатикокси, C1-8алифатикамино, ди(C1-8алифатик)амино, гетероциклиламино, С1-8алифатикамино-С1-8алифатикамино, ди(С1-8алифатик)амино-С1-8алифатикамино, С1-8алифатиккарбонила, гетероциклилкарбонила, С1-8алифатикаминоацила, ди(C1-8алифатик)аминоацила и гетероциклиламиноацила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, предпочтительно один или два гетероатома, выбранные из группы, состоящей из N, O и S, и предпочтительно выбранную из группы, состоящей из пиперидинила, пиперазинила, морфолинила и тетрагидропиранила; возможно, каждый гетероциклил независимо замещен одним или более, предпочтительно одним или двумя, заместителями, выбранными из группы, состоящей из гидрокси, С1-8алифатика, C1-8алифатикокси и С1-8алифатиккарбонила;
где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, С2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы I, R1 представляет собой фенил, возможно замещенный одним или более R6; каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, С1-8алифатика, гетероциклил-С1-8алифатикокси, гетероциклиламино, гетероциклилкарбонила, гетероциклиламиноацила, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 5-6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из N, O и S, и предпочтительно выбранную из группы, состоящей из пиперидинила, пиперазинила и морфолинила; возможно, каждый гетероциклил независимо замещен одним или двумя C1-8алифатическими заместителями, где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила и C3-8циклоалкила.
В некоторых воплощениях соединения формулы I, R1 представляет собой 5-12-членную гетероарильную группу, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, C1-8алифатика, C1-8галогеналифатика, гетероциклил-C1-8алифатика, гидрокси-C1-8алифатика, C1-8алифатикокси-C1-8алифатика, амино-C1-8алифатика, С1-8алифатикамино-С1-8алифатика, ди(С1-8алифатик)амино-C1-8алифатика, C1-8алифатикокси, С1-8алифатиккарбонила, гетероциклилкарбонила и гетероциклилокси, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, O и S; возможно, каждый гетероциклил независимо замещен одним или более заместителями, выбранными из группы, состоящей из гидрокси, C1-8алифатика, С1-8алифатикокси, амино и C1-8алифатиккарбонила;
где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы I, R1 представляет собой 5-10-членную гетероарильную группу, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из гетероциклила, C1-8алифатика, С1-8галогеналифатика, гетероциклил-С1-8алифатика, гидрокси-C1-8алифатика, С1-8алифатикокси-С1-8алифатика, амино-C1-8алифатика, C1-8алифатикамино-C1-8алифатика, ди(С1-8алифатик)амино-С1-8алифатика, C1-8алифатикокси и C1-8алифатиккарбонила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, предпочтительно один или два гетероатома, выбранные из группы, состоящей из N, O и S; возможно, каждый гетероциклил независимо замещен одним или более, предпочтительно одним или двумя, C1-8алифатическими заместителями;
где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, С3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы I, соединение формулы I представлено формулой Ia:
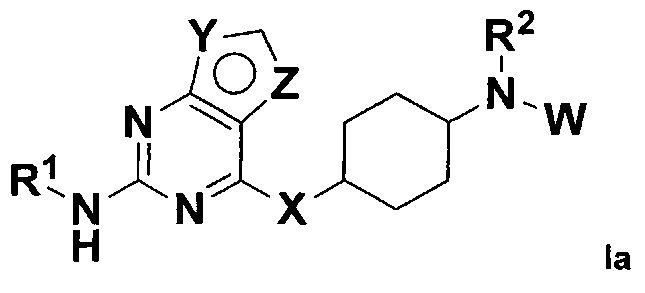
где X, Y, Z, W, R1 и R2 все являются такими, как определено в формуле I. В некоторых воплощениях соединения формулы Ia каждая группа в формуле Ia определена следующим образом:
W представляет собой  или
или  ;
;
X представляет собой S, O или NR4;
Y представляет собой СН, O или S;
Z представляет собой CH, O, S или NR5;
R1 представляет собой C6-12арил или 5-12-членный гетероарил, возможно замещенный одним или более R6;
R2 представляет собой водород или C1-8алифатик;
R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(С1-8алифатик)аминометила;
R4 представляет собой водород или C1-8алифатик;
R5 представляет собой водород или C1-8алифатик;
каждый R6 независимо выбран из группы, состоящей из галогена, нитро, циано, гетероциклила, C6-12арила, 5-12-членного гетероарила, C1-8алифатика, C1-8галогеналифатика, гетероциклил-C1-8алифатика, гидрокси-С1-8алифатика, C1-8алифатикокси-C1-8алифатика, C1-8алифатиккарбонилокси-C1-8алифатика, амино-С1-8алифатика, C1-8алифатикамино-C1-8алифатика, ди(C1-8алифатик)амино-С1-8алифатика, C1-8алифатикациламино-C1-8алифатика, C1-8алифатиккарбонил-С1-8алифатика, C1-8алифатикоксикарбонил-C1-8алифатика, аминоацил-С1-8алифатика, C1-8алифатикаминоацил-C1-8алифатика, ди(С1-8алифатик)аминоацил-С1-8алифатика, C1-8алифатиксульфонил-C1-8алифатика, С1-8алифатиксульфинил-С1-8алифатика, C1-8алифатиксульфониламино-C1-8алифатика, сульфамоил-С1-8алифатика, С1-8алифатикаминосульфонил-C1-8алифатика, ди(С1-8алифатик)аминосульфонил-С1-8алифатика, ди(C1-8алифатик)фосфонил-С1-8алифатика, гидрокси, C1-8алифатикокси, гетероциклилокси, гетероциклил-C1-8алифатикокси, гидрокси-С1-8алифатикокси, С1-8алифатикокси-С1-8алифатикокси, амино-C1-8алифатикокси, C1-8алифатикамино-С1-8алифатикокси, ди(C1-8алифатик)амино-С1-8алифатикокси, С1-8алифатикациламино-С1-8алифатикокси, C1-8алифатиккарбонил-C1-8алифатикокси, аминоацил-С1-8алифатикокси, С1-8алифатикаминоацил-C1-8алифатикокси, ди(С1-8алифатик)аминоацил-С1-8алифатикокси, амино, C1-8алифатикамино, ди(С1-8алифатик)амино, гетероциклиламино, гетероциклил-C1-8алифатикамино, гидрокси-С1-8алифатикамино, С1-8алифатикокси-C1-8алифатикамино, амино-С1-8алифатикамино, С1-8алифатикамино-C1-8алифатикамино, ди(C1-8алифатик)амино-С1-8алифатикамино, C1-8алифатикациламино-C1-8алифатикамино, С1-8алифатиккарбонил-C1-8алифатикамино, аминоацил-С1-8алифатикамино, C1-8алифатикаминоацил-C1-8алифатикамино, ди(С1-8алифатик)аминоацил-С1-8алифатикамино, C1-8алифатикациламино, гетероциклил-С1-8алифатикациламино, гетероциклилациламино, гидрокси-С1-8алифатикациламино, С1-8алифатикокси-С1-8алифатикациламино, амино-С1-8алифатикациламино, С1-8алифатикамино-С1-8алифатикациламино, ди(С1-8алифатик)амино-С1-8алифатикациламино, C1-8алифатиккарбонила, гетероциклилкарбонила, гетероциклил-C1-8алифатиккарбонила, C1-8алифатикоксикарбонила, гетероциклил-C1-8алифатикоксикарбонила, ди(С1-8алифатик)амино-С1-8алифатикоксикарбонила, аминоацила, C1-8алифатикаминоацила, ди(C1-8алифатик)аминоацила, гетероциклил-C1-8алифатикаминоацила, гетероциклиламиноацила, гидрокси-C1-8алифатикаминоацила, С1-8алифатикокси-С1-8алифатикаминоацила, амино-С1-8алифатикаминоацила, С1-8алифатикамино-С1-8алифатикаминоацила, ди(C1-8алифатик)амино-С1-8алифатикаминоацила, C1-8алифатиксульфгидрила, гетероциклилсульфгидрила, гетероциклил-С1-8алифатиксульфгидрила, C1-8алифатиксульфонила, С1-8алифатиксульфинила, гетероциклилсульфонила, гетероциклилсульфинила, гетероциклил-C1-8алифатиксульфонила, гетероциклил-С1-8алифатиксульфинила, сульфамоила, C1-8алифатикаминосульфонила, ди(С1-8алифатик)аминосульфонила, гетероциклил-С1-8алифатикаминосульфонила, гетероциклиламиносульфонила, ди(С1-8алифатик)амино-С1-8алифатикаминосульфонила, аминосульфинила, C1-8алифатикаминосульфинила, ди(C1-8алифатик)аминосульфинила, гетероциклиламиносульфинила и ди(С1-8алифатик)фосфонила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-12-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, O и S; возможно, каждый гетероциклил независимо замещен одним или более заместителями, выбранными из группы, состоящей из галогена, C1-8алифатика, гидрокси-С1-8алифатика, C1-8алифатикокси-C1-8алифатика, амино-C1-8алифатика, С1-8алифатикамино-C1-8алифатика, ди(C1-8алифатик)амино-С1-8алифатика, гетероциклил-C1-8алифатика, гетероциклила, 5-12-членного гетероарила, гидрокси, C1-8алифатикокси, амино, C1-8алифатикамино, ди(C1-8алифатик)амино, C1-8алифатиккарбонила, гетероциклилкарбонила, гетероциклил-C1-8алифатиккарбонила, гидрокси-С1-8алифатиккарбонила, C1-8алифатикокси-C1-8алифатиккарбонила, ди(C1-8алифатик)амино-C1-8алифатиккарбонила, C1-8алифатикоксикарбонила, аминоацила, С1-8алифатикаминоацила, ди(C1-8алифатик)аминоацила, С1-8алифатиксульфонила, С1-8алифатиксульфинила, гетероциклилсульфонила, гетероциклилсульфинила, гетероциклил-C1-8алифатиксульфонила, гетероциклил-C1-8алифатиксульфинила, сульфамоила, С1-8алифатикаминосульфонила, ди(С1-8алифатик)аминосульфонила; и
возможно, C6-12арил и 5-12-членный гетероарил независимо замещены одним или более заместителями, выбранными из группы, состоящей из галогена, С1-8алифатика, гидрокси, С1-8алифатикокси, амино, С1-8алифатикамино и ди(С1-8алифатик)амино,
где С1-8алифатик в каждом случае независимо выбран из группы, состоящей из С1-8алкила, С2-8алкенила, С2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ia, W представляет собой 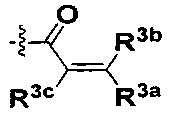 , где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(С1-8алифатик)аминометила, где С1-8алифатик независимо выбран из группы, состоящей из С1-8алкила, С2-8алкенила, С2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила. В некоторых воплощениях, W представляет собой
, где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(С1-8алифатик)аминометила, где С1-8алифатик независимо выбран из группы, состоящей из С1-8алкила, С2-8алкенила, С2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила. В некоторых воплощениях, W представляет собой  , где R3a, R3b и R3c все представляют собой водород.
, где R3a, R3b и R3c все представляют собой водород.
В некоторых воплощениях соединения формулы Ia, W представляет собой 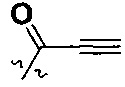 .
.
В некоторых воплощениях соединения формулы Ia, X представляет собой S. В некоторых других воплощениях соединения формулы Ia, X представляет собой О. В дополнительных воплощениях соединения формулы Ia, X представляет собой NR4, где R4 представляет собой водород или С1-8алифатик, где С1-8алифатик независимо выбран из группы, состоящей из С1-8алкила, С2-8алкенила, C2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила. В некоторых воплощениях X представляет собой NR4, где R4 представляет собой водород или С1-8алкил, более предпочтительно представляет собой водород или метил, и наиболее предпочтительно представляет собой водород.
В некоторых воплощениях соединения формулы Ia, Y представляет собой СН. В некоторых других воплощениях соединения формулы Ia, Y представляет собой O. В дополнительных воплощениях соединения формулы Ia, Y представляет собой S.
В одном воплощении соединения формулы Ia, Z представляет собой СН. В некоторых других воплощениях соединения формулы Ia, Z представляет собой О. В дополнительных воплощениях соединения формулы Ia, Z представляет собой S. В других дополнительных воплощениях соединения формулы Ia, Z представляет собой NR5, где R5 представляет собой водород или С1-8алифатик, где С1-8алифатик независимо выбран из группы, состоящей из С1-8алкила, С2-8алкенила, С2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила. В других дополнительных воплощениях, Z представляет собой NR5, где R5 предпочтительно представляет собой водород или С1-8алкил, более предпочтительно представляет собой водород или метил, и наиболее предпочтительно представляет собой водород.
В некоторых воплощениях соединения формулы Ia по меньшей мере один из Y и Z представляет собой гетероатом.
В некоторых воплощениях соединения формулы Ia, Y представляет собой S, и Z представляет собой СН.
В некоторых воплощениях соединения формулы Ia, Y представляет собой O, и Z представляет собой СН.
В некоторых воплощениях соединения формулы Ia, Y представляет собой СН, и Z представляет собой S. В некоторых других воплощениях соединения формулы Ia, Y представляет собой CH, и Z представляет собой O.
В некоторых воплощениях соединения формулы Ia, Y представляет собой СН, Z представляет собой NR5, где R5 представляет собой водород или C1-8алифатик, где C1-8алифатик выбран из группы, состоящей из С1-8алкила, C2-8алкенила, С2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила. В некоторых воплощениях Y представляет собой CH, и Z представляет собой NR5, где R5 представляет собой водород.
В некоторых воплощениях соединения формулы Ia, R1 представляет собой C6-12арильную или 5-12-членную гетероарильную группу, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, C1-8алифатика, C1-8галогеналифатика, гетероциклил-C1-8валифатика, гидрокси-C1-8алифатика, С1-8алифатикокси-C1-8алифатика, амино-С1-8алифатика, C1-8алифатикамино-C1-8алифатика, ди(C1-8алифатик)амино-C1-8алифатика, С1-8алифатикокси, гетероциклилокси, гетероциклил-С1-8алифатикокси, гидрокси-С1-8алифатикокси, С1-8алифатикокси-С1-8алифатикокси, амино, С1-8алифатикамино, ди(C1-8алифатик)амино, гетероциклиламино, амино-C1-8алифатикамино, C1-8валифатикамино-C1-8алифатикамино, ди(С1-8алифатик)амино-С1-8алифатикамино, гетероциклилкарбонила, аминоацила, C1-8алифатикаминоацила, ди(C1-8алифатик)аминоацила, гетероциклиламиноацила, сульфамоила, С1-8алифатикаминосульфонила, ди(С1-8алифатик)аминосульфонила, гетероциклиламиносульфонила, аминосульфинила, C1-8алифатикаминосульфинила, ди(С1-8алифатик)аминосульфинила и гетероциклиламиносульфинила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, предпочтительно один или два гетероатома, выбранные из группы, состоящей из N, O и S; который возможно независимо замещен одним или более, возможно одним или двумя, заместителями, выбранными из группы, состоящей из C1-8алифатика, гидрокси, C1-8алифатикокси и C1-8алифатиккарбонила,
где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ia, R1 представляет собой C6-12арил, возможно замещенный одним или более R6, где каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, C1-8алифатика, C1-8алифатикокси, гетероциклилокси, гетероциклил-C1-8алифатикокси, гидрокси-С1-8алифатикокси, С1-8алифатикокси-С1-8алифатикокси, амино, С1-8алифатикамино, ди(С1-8алифатик)амино, гетероциклиламино, амино-С1-8алифатикамино, С1-8алифатикамино-С1-8алифатикамино, ди(C1-8алифатик)амино-C1-8алифатикамино, С1-8алифатиккарбонила, гетероциклилкарбонила, аминоацила, С1-8алифатикаминоацил-ди(C1-8алифатик)аминоацила, гетероциклиламиноацила, сульфамоила, C1-8алифатикаминосульфонила, ди(C1-8алифатик)аминосульфонила, гетероциклиламиносульфонила, аминосульфинила, C1-8алифатикаминосульфинила, ди(С1-8алифатик)аминосульфинила и гетероциклиламиносульфинила, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из N, O и S; возможно, гетероциклил независимо замещен одним или двумя заместителями, выбранными из группы, состоящей из С1-8алифатика, гидрокси, C1-8алифатикокси и С1-8алифатиккарбонила, и где С1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, С2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ia, R1 представляет собой фенил, возможно замещенный одним или более R6, где каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, C1-8алифатика, C1-8алифатикокси, гетероциклилокси, гетероциклил-C1-8алифатикокси, гидрокси-C1-8алифатикокси, C1-8алифатикокси-C1-8алифатикокси, ди(С1-8алифатик)амино, С1-8алифатикамино, гетероциклиламино, ди(C1-8алифатик)амино-C1-8алифатикамино, C1-8алифатиккарбонила, гетероциклилкарбонила, С1-8алифатикаминоацила и гетероциклиламиноацила, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 5-6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из N, O и S, и предпочтительно выбранную из группы, состоящей из пиперидинила, пиперазинила, морфолинила и тетрагидропиранила; возможно, каждый гетероциклил независимо замещен одним или более заместителями, выбранными из группы, состоящей из C1-8алифатика, гидрокси, C1-8алифатикокси и C1-8алифатиккарбонила, и где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила и С3-8циклоалкила.
В некоторых воплощениях соединения формулы Ia, R1 представляет собой фенил, возможно замещенный одним или более R6, где каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, 8алифатика, гетероциклилокси, гетероциклил-C1-8алифатикокси, гетероциклиламино, гетероциклилкарбонила и гетероциклиламиноацила, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 5-6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из N, O и S, и предпочтительно выбранную из группы, состоящей из пиперидинила, пиперазинила и морфолинила; возможно, каждый гетероциклил независимо замещен одним или двумя C1-8алифатическими заместителями, и где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из С1-8алкила и C3-8циклоалкила.
В некоторых воплощениях соединения формулы Ia, R1 представляет собой фенил, возможно замещенный одним или более R6, где каждый R6 независимо выбран из группы, состоящей из фтора, хлора, метила, метокси, диметиламино, метиламиноацила, гидроксиэтилокси, метоксиэтилокси, диметиламиноэтиламино, гетероциклилэтилокси, гетероциклила, циклогексиламино, гетероциклиламино, гетероциклилокси, гетероциклилкарбонила и гетероциклиламиноацила, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 5-6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из O, N и S, и предпочтительно выбранную из группы, состоящей из пиперидинила, пиперазинила, морфолинила и тетрагидропиранила; возможно, каждый гетероциклил независимо замещен одним или более заместителями, выбранными из группы, состоящей из метила, метилкарбонила, гидрокси, метокси и изопропила.
В некоторых воплощениях соединения формулы Ia, R1 представляет собой фенил, возможно замещенный одним или более R6, где каждый R6 независимо выбран из группы, состоящей из фтора, хлора, метила, гетероциклила, гетероциклилэтилокси, гетероциклиламино, гетероциклилокси, гетероциклилкарбонила и гетероциклиламиноацила, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 5-6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из O, N и S, и предпочтительно выбранную из группы, состоящей из пиперидинила, пиперазинила и морфолинила; возможно, каждый гетероциклил независимо замещен метилом или изопропилом.
В некоторых воплощениях соединения формулы Ia, R1 представляет собой 5-12-членную гетероарильную группу, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из гетероциклила, C1-8алифатика, C1-8галогеналифатика, гетероциклил-C1-8алифатика, гидрокси-С1-8алифатика, амино-С1-8алифатика, С1-8алифатикамино-C1-8алифатика, ди(C1-8алифатик)амино-C1-8-аалифатика, С1-8алифатикокси и С1-8алифатикокси-С1-8алифатика, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из O, N и S; возможно, гетероциклил независимо замещен одной или более С1-8алифатическими группами, и где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, С2-8алкинила, С3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ia, R1 представляет собой 5-10-членную гетероарильную группу, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из гетероциклила, C1-8алифатика, C1-8галогеналифатика, гетероциклил-С1-8алифатика, гидрокси-C1-8алифатика, амино-C1-8алифатика, C1-8алифатикамино-C1-8алифатика, ди(С1-8алифатик)амино-С1-8алифатика, C1-8алифатикокси и C1-8алифатикокси-C1-8алифатика, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 5-6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из O, N и S, и предпочтительно выбранную из группы, состоящей из морфолинила, пиперидинила, пиперазинила и тетрагидропиранила; возможно, каждый гетероциклил независимо замещен одним или более С1-8алифатическими заместителями, и где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила и C3-8циклоалкила.
В некоторых воплощениях соединения формулы Ia, R1 представляет собой 5-10-членную гетероарильную группу, предпочтительно выбранную из группы, состоящей из пирролила, пиразолила, имидазолила, тиенила, тиазолила, изотиазолила, изоксазолила, пиридинила и имидазо[1,2-a]пиридинила, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из метила, циклобутила, циклопентила, гидроксиэтила, метокси, метоксиэтила, фторэтила, диметиламиноэтила, 1-метил-пиперазин-4-ила и морфолин-4-ил-этила.
В некоторых воплощениях соединения формулы Ia, R1 представляет собой 5-членный гетероарил, предпочтительно выбранный из группы, состоящей из пиразолила, тиенила, тиазолила, изотиазолила и изоксазолила, возможно замещенный одним или более R6, где каждый R6 независимо выбран из группы, состоящей из C1-8алифатика, C1-8галогеналифатика, гетероциклил-C1-8алифатика, гидрокси-C1-8алифатика, С1-8алифатикамино-C1-8алифатика, ди(C1-8алифатик)амино-С1-8алифатика и С1-8алифатикокси-C1-8алифатика, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 5-6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из O, N и S; возможно, каждый гетероциклил независимо замещен одним или более C1-8алифатическими заместителями, и где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила и C3-8циклоалкила.
В некоторых воплощениях соединения формулы Ia, R1 представляет собой 5-членную гетероарильную группу, предпочтительно выбранную из группы, состоящей из пиразолила, тиенила, тиазолила, изотиазолила и изоксазолила, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из метила, циклобутила, циклопентила, гидроксиэтила, метоксиэтила, фторэтила, диметиламиноэтила и морфолин-4-ил-этила.
В некоторых воплощениях соединения формулы Ia, R1 выбран из группы, состоящей из:
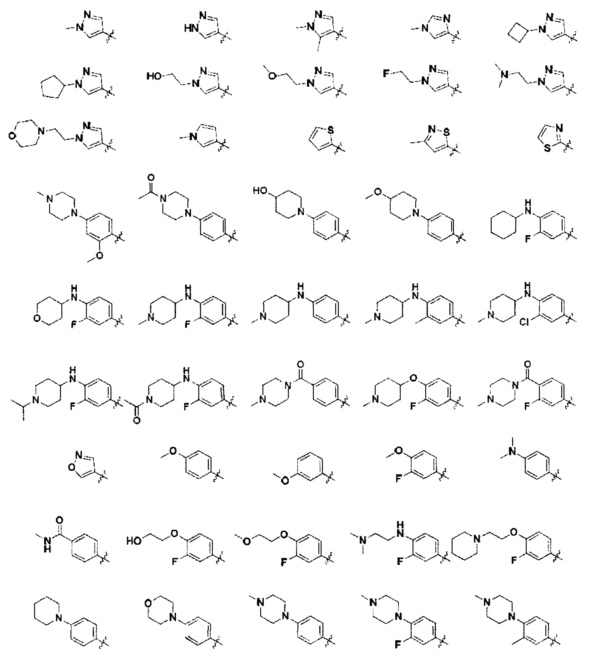
 .
.
В некоторых воплощениях соединения формулы Ia, R2 представляет собой водород или С1-8алифатик, где C1-8алифатик независимо выбран из группы, состоящей из С1-8алкила, C2-8алкенила, С2-8алкинила, С3-8циклоалкила и C4-8циклоалкенила. В некоторых воплощениях R2 представляет собой водород или C1-8алкил. В некоторых воплощениях R2 представляет собой водород или метил. В некоторых воплощениях, R2 представляет собой водород.
В некоторых воплощениях соединения формулы Ia каждая группа в формуле Ia определена следующим образом:
W представляет собой 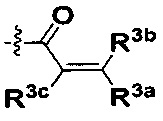 или
или 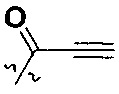 ;
;
X представляет собой O, S или NR4;
Y представляет собой CH, O или S;
Z представляет собой СН, О, S или NR5;
R1 представляет собой C6-12арил или 5-12-членный гетероарил, возможно замещенный одним или более R6;
R2 представляет собой водород;
R3a, R3b и R3c все представляют собой водород;
R4 представляет собой водород или С1-8алифатик;
R5 представляет собой водород;
каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, С1-8алифатика, С1-8 галогеналифатика, гетероциклил-С1-8алифатика, гидрокси-C1-8алифатика, C1-8алифатикокси-С1-8алифатика, амино-С1-8алифатика, С1-8алифатикамино-С1-8алифатика, ди(С1-8алифатик)амино-C1-8алифатика, С1-8алифатикокси, гетероциклилокси, гетероциклил-С1-8алифатикокси, гидрокси-С1-8алифатикокси, С1-8алифатикокси-С1-8алифатикокси, С1-8алифатикамино, ди(С1-8алифатик)амино, гетероциклиламино, амино-С1-8алифатикамино, С1-8алифатикамино-С1-8алифатикамино, ди(C1-8алифатик)амино-С1-8алифатикамино, С1-8алифатиккарбонила, гетероциклилкарбонила, аминоацила, С1-8алифатикаминоацила, ди(C1-8алифатик)аминоацила, гетероциклиламиноацила, сульфамоила, C1-8алифатикаминосульфонила, ди(C1-8алифатик)аминосульфонила, гетероциклиламиносульфонила, аминосульфинила, C1-8алифатикаминосульфинила, ди(С1-8алифатик)аминосульфинила и гетероциклиламиносульфинила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-12-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, О и S; возможно, каждый гетероциклил независимо замещен одним или более заместителями, выбранными из группы, состоящей из гидрокси, С1-8алифатика, C1-8алифатикокси и C1-8алифатиккарбонила;
где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, С2-8алкенила, С2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ia каждая группа в формуле Ia определена следующим образом:
W представляет собой 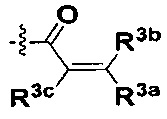 или
или 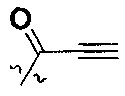 ;
;
X представляет собой NR4;
Y представляет собой CH;
Z представляет собой O или S;
R1 представляет собой С6-12арильную или 5-12-членную гетероарильную группу, возможно замещенную одним или более R6;
R2 представляет собой водород;
R3a, R3b и R3c все представляют собой водород;
R4 представляет собой водород;
каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, С1-8алифатика, С1-8галогеналифатика, гетероциклил- С1-8алифатика, гидрокси-С1-8алифатика, С1-8алифатикокси-С1-8алифатика, амино-С1-8алифатика, С1-8алифатикамино-С1-8алифатика, ди(С1-8алифатик)амино-С1-8алифатика, гетероциклилокси, гетероциклил- С1-8алифатикокси, гетероциклиламино, гетероциклилкарбонила и гетероциклиламиноацила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, O и S; возможно, каждый гетероциклил независимо замещен одним или более С1-8алифатическими заместителями,
где С1-8алифатик в каждом случае независимо выбран из группы, состоящей из С1-8алкила, С2-8алкенила, С2-8алкинила, С3-8циклоалкила и С4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ia, соединение формулы Ia выбрано из группы, состоящей из:

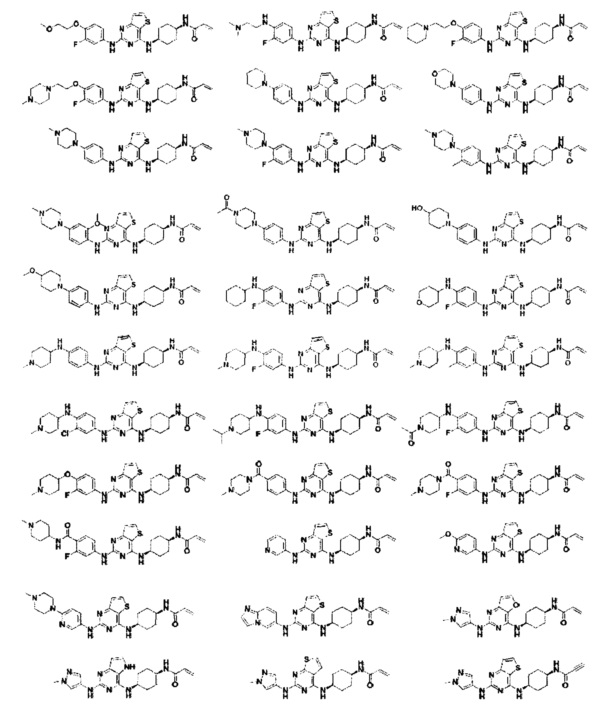 .
.
В некоторых воплощениях соединения формулы I, соединение формулы I представлено формулой Ib:
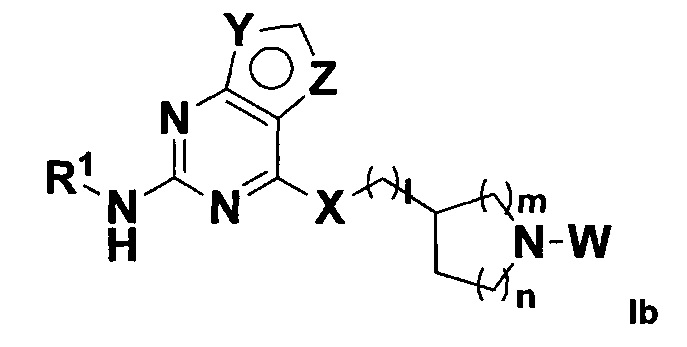
где:
X, Y, Z, W и R1 все являются такими, как определено в формуле I;
I равно 0, 1, 2, 3 или 4, причем когда I равно 0, 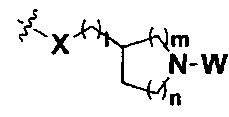 представляет собой
представляет собой  ;
;
m равно 0, 1, 2, 3 или 4; причем когда m равно 0, 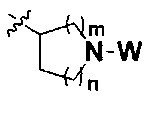 представляет собой
представляет собой 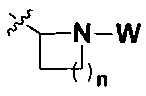 ; и
; и
n равно 0, 1, 2 или 3; причем когда n равно 0, 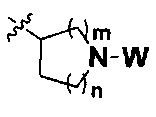 представляет собой
представляет собой 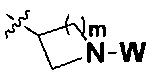 .
.
В некоторых воплощениях соединения формулы Ib каждый заместитель в формуле Ib определен следующим образом:
W представляет собой 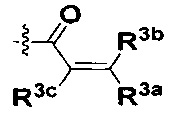 или
или 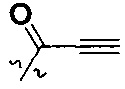 ;
;
X представляет собой O, S или NR4;
Y представляет собой CH, O или S;
Z представляет собой СН, О, S или NR5;
I равно 0, 1, 2, 3 или 4, причем когда I равно 0, 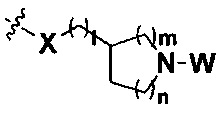 представляет собой
представляет собой 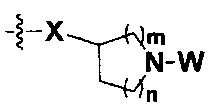 ;
;
m равно 0, 1, 2, 3 или 4; причем когда m равно 0,  представляет собой
представляет собой  ;
;
n равно 0, 1, 2 или 3; причем когда n равно 0, 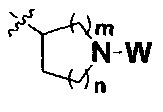 представляет собой
представляет собой 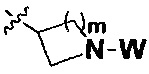 ;
;
R1 представляет собой 5-6-членную гетероарильную группу, возможно замещенную одним или более R6;
R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(C1-8алифатик)аминометила;
R4 представляет собой водород или C1-8алифатик;
R5 представляет собой водород или C1-8алифатик;
каждый R6 независимо выбран из группы, состоящей из галогена, нитро, циано, C1-8алифатика, C1-8галогеналифатика, гидрокси-С1-8алифатика, С1-8алифатикокси-C1-8алифатика, амино-С1-8алифатика, С1-8алифатикамино-C1-8алифатика, ди(С1-8алифатик)амино-С1-8алифатика, гетероциклил-С1-8алифатика, С1-8алифатиккарбонил-С1-8алифатика, C1-8алифатикоксикарбонил-С1-8алифатика, С1-8алифатиккарбонилокси-С1-8алифатика, аминоацил-C1-8алифатика, C1-8алифатикаминоацил-C1-8алифатика, ди(C1-8алифатик)аминоацил-С1-8алифатика, C1-8алифатикациламино-C1-8алифатика, C1-8алифатиксульфонил-С1-8алифатика, С1-8алифатиксульфинил-С1-8алифатика, C1-8алифатиксульфониламино-C1-8алифатика, сульфамоил-C1-8алифатика, C1-8алифатикаминосульфонил-С1-8алифатика, ди(C1-8алифатик)аминосульфонил-С1-8алифатика, C1-8алифатиккарбонила, С1-8алифатикоксикарбонила, аминоацила, C1-8алифатикаминоацила, ди(С1-8алифатик)аминоацила, C1-8алифатикокси, C1-8алифатиксульфонила, C1-8алкилсульфинила, C1-8алифатиксульфониламино, сульфамоила, C1-8алифатикаминосульфонила, ди(C1-8алифатик)аминосульфонила, гетероциклила, С6-12арила и 5-12-членного гетероарила, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, O и S; каждый гетероциклил возможно замещен одним или более заместителями, выбранными из группы, состоящей из галогена, гидрокси, C1-8алифатика, C1-8алифатикокси и C1-8алифатиккарбонила; и возможно С6-12арил и 5-12-членный гетероарил независимо замещены одним или более заместителями, выбранными из группы, состоящей из галогена и C1-8алифатика,
где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ib, W представляет собой 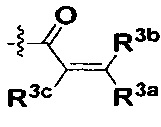 , где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(С1-8алифатик)аминометила, где C1-8алифатик независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила. В некоторых воплощениях W представляет собой
, где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(С1-8алифатик)аминометила, где C1-8алифатик независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила. В некоторых воплощениях W представляет собой 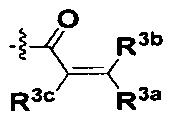 , где R3a, R3b и R3c все представляют собой водород.
, где R3a, R3b и R3c все представляют собой водород.
В некоторых воплощениях соединения формулы Ib, W представляет собой  .
.
В некоторых воплощениях соединения формулы Ib, X представляет собой O.
В некоторых воплощениях соединения формулы Ib, X представляет собой NR4, где R4 представляет собой водород или C1-8алифатик, где C1-8алифатик независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила. В некоторых воплощениях X представляет собой NR4, где R4 представляет собой водород или C1-8алкил. В некоторых воплощениях X представляет собой NR4, где R4 представляет собой водород или метил.
В некоторых воплощениях соединения формулы Ib, Y представляет собой CH. В некоторых других воплощениях соединения формулы Ib, Y представляет собой S. В некоторых дополнительных воплощениях соединения формулы Ib, Y представляет собой О.
В некоторых воплощениях соединения формулы Ib, Z представляет собой СН. В некоторых других воплощениях соединения формулы Ib, Z представляет собой S. В некоторых дополнительных воплощениях соединения формулы Ib, Z представляет собой О. В некоторых дополнительных воплощениях соединения формулы Ib, Z представляет собой NR5, где R5 представляет собой водород или C1-8алифатик, где C1-8алифатик независимо выбран из группы, состоящей из C1-8алкила, С2-8алкенила, С2-8алкинила, С3-8циклоалкила и C4-8циклоалкенила. В некоторых воплощениях, Z представляет собой NR5, где R5 представляет собой водород или C1-8алкил. В некоторых воплощениях, Z представляет собой NR5, где R5 представляет собой водород или метил.
В некоторых воплощениях соединения формулы Ib по меньшей мере один из Y и Z представляет собой гетероатом.
В некоторых воплощениях соединения формулы Ib, Y представляет собой S, и Z представляет собой СН. I В некоторых других воплощениях, Y представляет собой О, и Z представляет собой СН.
В некоторых воплощениях соединения формулы Ib, Y представляет собой СН, и Z представляет собой S. В некоторых других воплощениях, Y представляет собой СН, и Z представляет собой О. В некоторых дополнительных воплощениях, Y представляет собой СН, и Z представляет собой NR5, где R5 представляет собой водород или C1-8алифатик, где C1-8алифатик независимо выбран из группы, состоящей из C1-8алкила, С2-8алкенила, С2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила. В некоторых дополнительных воплощениях Y представляет собой СН, и Z представляет собой NR5, где R5 представляет собой водород или C1-8алкил, и предпочтительно представляет собой водород или метил.
В некоторых воплощениях соединения формулы Ib, R1 представляет собой 5-6-членную гетероциклическую группу, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, C1-8алифатика, C1-8галогеналифатика, гетероциклил-С1-8алифатика, гидрокси-С1-8алифатика, С1-8алифатикокси-С1-8алифатика, амино-C1-8алифатика, С1-8алифатикамино-С1-8алифатика, ди(C1-8алифатик)амино-C1-8алифатика, C1-8алифатикокси, C1-8алифатиккарбонила, гетероциклилкарбонила и гетероциклилокси, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, О и S; возможно, каждый гетероциклил независимо замещен одним или более заместителями, выбранными из группы, состоящей из гидрокси, С1-8алифатика, C1-8алифатикокси, амино и С1-8алифатиккарбонила;
где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из С1-8алкила, С2-8алкенила, C2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ib, R1 представляет собой 5-членную гетероциклическую группу и предпочтительно выбран из группы, состоящей из пирролила, пиразолила, имидазолила, тиенила, изоксазолила, тиазолила и изотиазолила, и R1 возможно замещен одним или двумя R6; где каждый R6 независимо выбран из группы, состоящей из галогена, C1-8алифатика, гидрокси-C1-8алифатика, C1-8алифатикокси, C1-8алифатикокси-C1-8алифатика, амино-C1-8алифатика, C1-8алифатикамино-C1-8алифатика, ди(C1-8алифатик)амино-С1-8алифатика, гетероциклил-С1-8алифатика, C1-8алифатиккарбонила и гетероциклила, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из N, О и S, и предпочтительно выбран из группы, состоящей из морфолинила, пиперидинила, пиперазинила и тетрагидропиранила; каждый гетероциклил возможно замещен одним или более C1-8алифатическими заместителями, и где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила и C3-8циклоалкила.
В некоторых воплощениях соединения формулы Ib, R1 представляет собой 5-членную гетероциклическую группу и предпочтительно выбран из группы, состоящей из пиразолила, тиенила, изоксазолила, тиазолила и изотиазолила, и R1 возможно замещен одним или двумя R6; где каждый R6 независимо выбран из группы, состоящей из C1-8алифатика, C1-8алифатикокси-C1-8алифатика, C1-8алифатикамино-C1-8алифатика, ди(C1-8алифатик)амино-C1-8алифатика, C1-8алифатиккарбонила, гетероциклила и гетероциклил-C1-8алифатика, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 5-6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из N, О и S, и предпочтительно выбран из группы, состоящей из морфолинила и тетрагидропиранила; где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила и C3-8циклоалкила.
В некоторых воплощениях соединения формулы Ib, R1 представляет собой 5-членную гетероциклическую группу и предпочтительно выбранную из группы, состоящей из пирролила, пиразолила, имидазолила, тиенила, изоксазолила, тиазолила и изотиазолила, и R1 возможно замещен одним или двумя R6, где каждый R6 независимо выбран из группы, состоящей из метила, этила, изопропила, н-бутила, гидроксиэтила, метоксиметила, метоксиэтила, метоксипропила, циклобутила, циклопентила, диметиламиноэтила, морфолин-4-ил-этила, тетрагидропиран-4-ила и метилкарбонила.
В некоторых воплощениях соединения формулы Ib, R1 представляет собой 5-членную гетероциклическую группу и предпочтительно выбранную из группы, состоящей из пиразолила, тиенила, изоксазолила, тиазолила и изотиазолила, и R1 возможно замещен одним или двумя R6, где каждый R6 независимо выбран из группы, состоящей из метила, этила, изопропила, циклобутила, циклопентила, метоксиметила, метоксиэтила, метоксипропила, диметиламиноэтила, морфолин-4-ил-этила, тетрагидропиран-4-ила и метилкарбонила.
В некоторых воплощениях соединения формулы Ib, R1 выбран из группы, состоящей из:
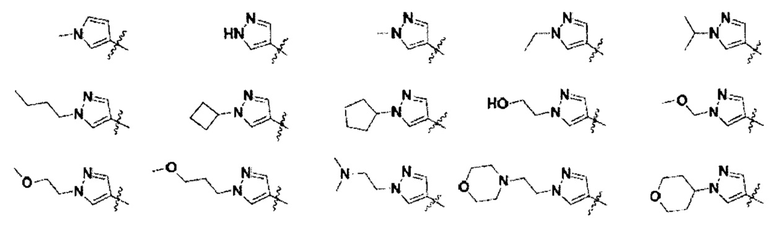

В некоторых воплощениях соединения формулы Ib, I равно 0, 1 или 2.
В некоторых воплощениях соединения формулы Ib, m равно 0, 1, 2 или 3.
В некоторых воплощениях соединения формулы Ib, n равно 0, 1 или 2.
В некоторых воплощениях соединения формулы Ib, m и n не равны одновременно 0.
В некоторых воплощениях соединения формулы Ib, каждая группа в формуле Ib определена следующим образом:
W представляет собой  или
или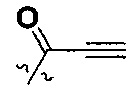 ;
;
X представляет собой O, S или NR4;
Y представляет собой CH, O или S;
Z представляет собой СН, О, S или NR5;
I равно 0, 1 или 2;
m равно 0, 1, 2 или 3;
n равно 0, 1 или 2;
R1 представляет собой 5-6-членную гетероарильную группу, возможно замещенную одним или более R6;
R3a, R3b и R3c все представляют собой водород;
R4 представляет собой водород или C1-8алифатик;
R5 представляет собой водород или С1-8алифатик;
каждый R6 независимо выбран из группы, состоящей из галогена, С1-8алифатика, гидрокси-C1-8алифатика, C1-8алифатикокси-C1-8алифатика, амино-С1-8алифатика, C1-8алифатикамино-С1-8алифатика, ди(С1-8алифатик)амино-C1-8алифатика, гетероциклил-С1-8алифатика, С1-8алифатиккарбонила и гетероциклила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, О и S; каждый гетероциклил возможно замещен одним или более С1-8алифатическими заместителями;
где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, С3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ib, каждая группа в формуле Ib определена следующим образом:
W представляет собой 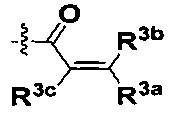 или
или 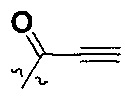 ;
;
X представляет собой O или NR4;
Y представляет собой СН или S;
Z представляет собой СН, O или S;
I равно 0, 1 или 2;
m равно 0, 1, 2 или 3;
n равно 0, 1 или 2;
R1 представляет собой 5-членную гетероарильную группу, возможно замещенную одним или более R6;
R3a, R3b и R3c все представляют собой водород;
R4 представляет собой водород или C1-8алифатик;
каждый R6 независимо выбран из группы, состоящей из галогена, С1-8алифатика, C1-8алифатикокси-C1-8алифатика, амино-C1-8алифатика, С1-8алифатикамино-С1-8алифатика, ди(C1-8алифатик)амино-C1-8алифатика, гетероциклил-C1-8алифатика, C1-8алифатиккарбонила и гетероциклила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 5-6-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, О и S; каждый гетероциклил возможно замещен одним или более C1-8алифатическими заместителями;
где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила и C3-8циклоалкила.
В некоторых воплощениях соединения формулы Ib соединение формулы Ib выбрано из группы, состоящей из:
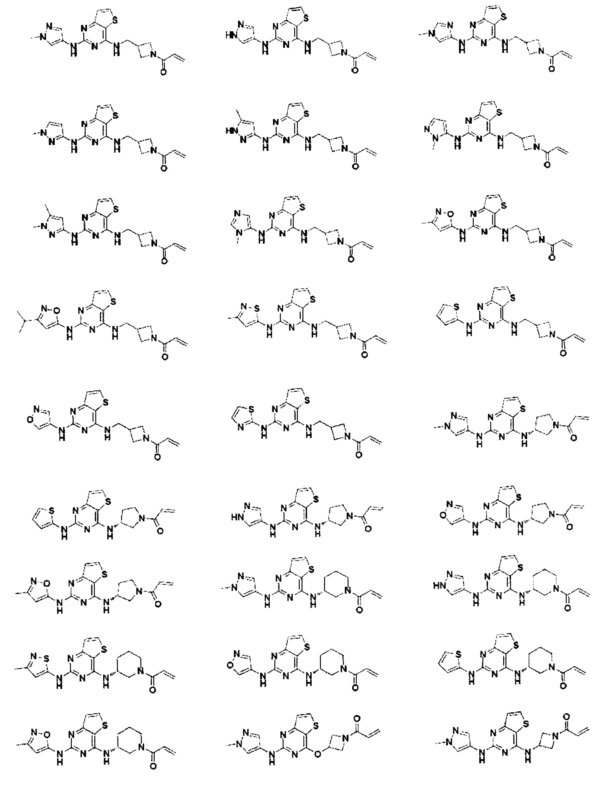
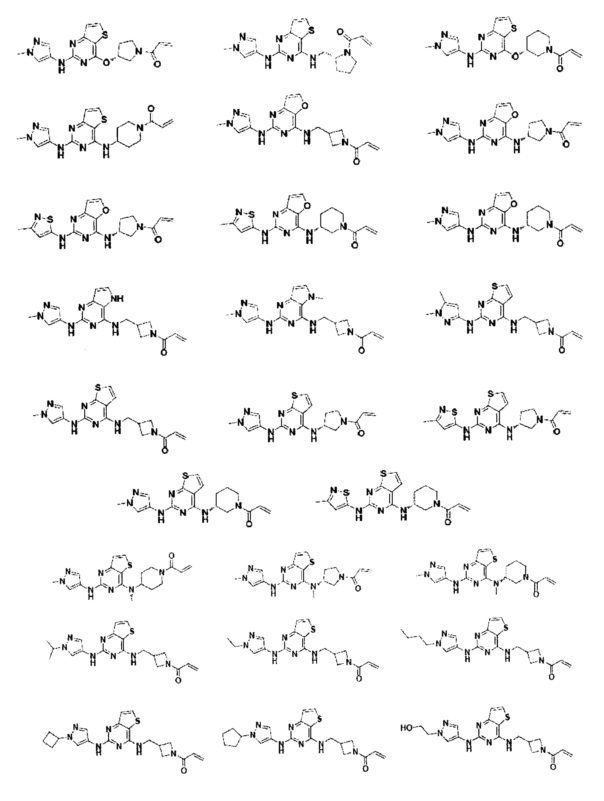
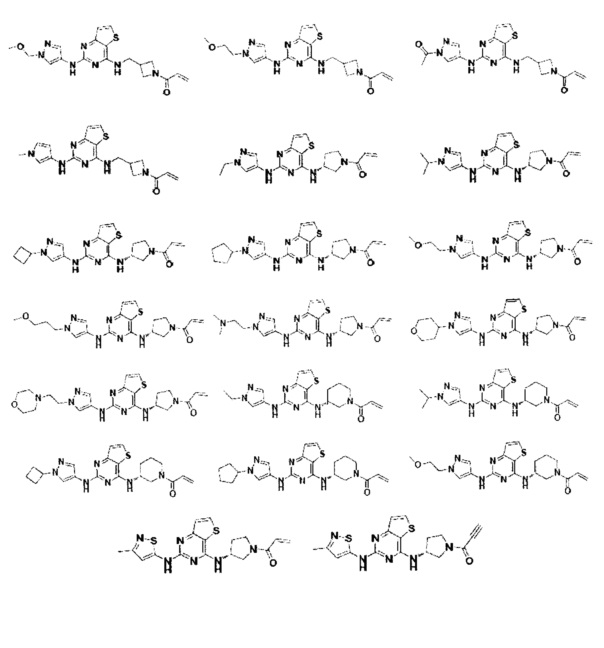 .
.
В некоторых дополнительных воплощениях соединения формулы I соединение формулы I представлено формулой Ic:

где:
X, W и R1 все являются такими, как определено в формуле I;
I равно 0, 1, 2, 3 или 4; причем когда I равно 0, 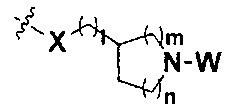 представляет собой
представляет собой  ;
;
m равно 0, 1, 2, 3 или 4; причем когда m равно 0, 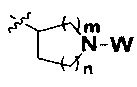 представляет собой
представляет собой  ; и
; и
n равно 0, 1, 2 или 3; причем когда n равно 0, 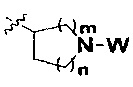 представляет собой
представляет собой  .
.
В некоторых воплощениях соединения формулы Ic каждая группа в формуле Ic определена следующим образом:
W представляет собой 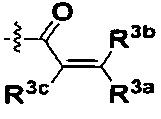 или
или  ;
;
X представляет собой O, S или NR4;
I равно 0, 1, 2, 3 или 4; причем когда I равно 0,  представляет собой
представляет собой 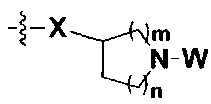 ;
;
m равно 0, 1, 2, 3 или 4; причем когда m равно 0, 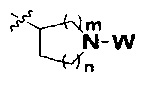 представляет собой
представляет собой 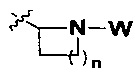 ;
;
n равно 0, 1, 2 или 3; причем когда n равно 0, 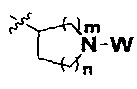 представляет собой
представляет собой 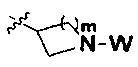 ;
;
R1 представляет собой 5-6-членную гетероарильную группу, возможно замещенную одним или более R6;
R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(C1-8алифатик)аминометила;
R4 представляет собой водород или C1-8алифатик;
каждый R6 независимо выбран из группы, состоящей из галогена, нитро, циано, C1-8алифатика, C1-8галогеналифатика, гидрокси-C1-8алифатика, C1-8алифатикокси-С1-8алифатика, амино-С1-8алифатика, C1-8алифатикамино-C1-8алифатика, ди(С1-8алифатик)амино-C1-8алифатика, гетероциклил-C1-8алифатика, C1-8алифатиккарбонил-С1-8алифатика, С1-8алифатикоксикарбонил-С1-8алифатика, С1-8алифатиккарбонилокси-C1-8алифатика, аминоацил-C1-8алифатика, С1-8алифатикаминоацил-С1-8алифатика, ди(C1-8алифатик)аминоацил-C1-8алифатика, С1-8алифатикациламино-С1-8алифатика, C1-8алифатиксульфонил-C1-8алифатика, C1-8алифатиксульфинил-C1-8алифатика, С1-8алифатиксульфониламино-C1-8алифатика, сульфамоил-C1-8алифатика, C1-8алифатикаминосульфонил-C1-8алифатика, ди(C1-8алифатик)аминосульфонил-C1-8алифатика, C1-8алифатиккарбонила, С1-8алифатикоксикарбонила, аминоацила, С1-8алифатикаминоацила, ди(C1-8алифатик)аминоацила, C1-8алифатикокси, C1-8алифатиксульфонила, С1-8алифатиксульфинила, С1-8алифатиксульфониламино, сульфамоила, C1-8алифатикаминосульфонила, ди(С1-8алифатик)аминосульфонила, гетероциклила, C6-12арила и 5-12-членного гетероарила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, О и S; каждый гетероциклил возможно замещен одним или более заместителями, выбранными из группы, состоящей из галогена, гидрокси, C1-8алифатика, C1-8алифатикокси и C1-8алифатиккарбонила; и
возможно, C6-12арил и 5-12-членный гетероарил независимо замещены одним или более заместителями, выбранными из группы, состоящей из галогена и C1-8алифатика,
где C1-8алифатик в каждом случае независимо выбран из группы, состоящей из C1-8алкила, С2-8алкенила, C2-8алкинила, C3-8циклоалкила и C4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ic, W представляет собой  , где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(C1-8алифатик)аминометила, где C1-8алифатик выбран из группы, состоящей из C1-8алкила, С2-8алкенила, C2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила. В некоторых воплощениях соединения формулы Ic, W представляет собой
, где R3a, R3b и R3c независимо выбраны из группы, состоящей из водорода, галогена и ди(C1-8алифатик)аминометила, где C1-8алифатик выбран из группы, состоящей из C1-8алкила, С2-8алкенила, C2-8алкинила, C3-8циклоалкила и С4-8циклоалкенила. В некоторых воплощениях соединения формулы Ic, W представляет собой 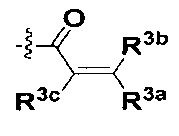 , где R3a, R3b и R3c все представляют собой водород.
, где R3a, R3b и R3c все представляют собой водород.
В некоторых воплощениях соединения формулы Ic, W представляет собой  .
.
В некоторых воплощениях соединения формулы Ic, X представляет собой O. В некоторых других воплощениях соединения формулы Ic, X представляет собой S. В некоторых дополнительных воплощениях соединения формулы Ic, X представляет собой NR4, где R4 представляет собой водород или C1-8алифатик, где C1-8алифатик независимо выбран из группы, состоящей из C1-8алкила, C2-8алкенила, C2-8алкинила, С3-8циклоалкила и C4-8циклоалкенила. В некоторых других воплощениях, X представляет собой NR4, где R4 представляет собой водород или C1-8алкил. В некоторых дополнительных воплощениях, X представляет собой NR4, где R4 представляет собой водород или метил. В некоторых дополнительных воплощениях X представляет собой NR4, где R4 представляет собой водород.
В некоторых воплощениях соединения формулы Ic, R1 представляет собой 5-6-членную гетероарильную группу, предпочтительно выбранную из группы, состоящей из пиридинила, пирролила, пиразолила, имидазолила, тиенила, изоксазолила, тиазолила и изотиазолила, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из галогена, нитро, циано, C1-8алифатика, C1-8галогеналифатика, гидрокси-C1-8алифатика, C1-8алифатикокси-C1-8алифатика, амино-С1-8алифатика, С1-8алифатикамино-C1-8алифатика, ди(С1-8алифатик)амино-C1-8алифатика, гетероциклил-С1-8алифатика, C1-8алифатиккарбонил-C1-8алифатика, C1-8алифатикоксикарбонил-C1-8алифатика, C1-8алифатиккарбонилокси-C1-8алифатика, аминоацил-C1-8алифатика, C1-8алифатикаминоацил-C1-8алифатика, ди(С1-8алифатик)аминоацил-C1-8алифатика, C1-8алифатикациламино-C1-8алифатика, С1-8алифатиксульфонил-С1-8алифатика, C1-8алифатиксульфинил-C1-8алифатика, С1-8алифатиксульфониламино-С1-8алифатика, сульфамоил-С1-8алифатика, C1-8алифатикаминосульфонил-C1-8алифатика, ди(C1-8алифатик)аминосульфонил-С1-8алифатика, C1-8алифатиккарбонила, C1-8алифатикоксикарбонила, аминоацила, C1-8алифатикаминс-ацила, ди(С1-8алифатик)аминоацила, С1-8алифатикокси, С1-8алифатиксульфонила, С1-8алифатиксульфинила, C1-8алифатиксульфониламино, сульфамоила, C1-8алифатикаминосульфонила, ди(С1-8алифатик)аминосульфонила, гетероциклила, C6-12арила и 5-12-членного гетероарила, где:
гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или более гетероатомов, выбранных из группы, состоящей из N, O и S; каждый гетероциклил возможно замещен одним или более заместителями, выбранными из группы, состоящей из галогена, гидрокси, С1-8алифатика, С1-8алифатикокси и C1-8алифатиккарбонила; и
возможно, C6-12арил и 5-12-членный гетероарил независимо замещены одним или более заместителями, выбранными из группы, состоящей из галогена и С1-8алифатика,
где С1-8алифатик в каждом случае независимо выбран из группы, состоящей из С1-8алкила, С2-8алкенила, C2-8алкинила, С3-8циклоалкила и С4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ic, R1 представляет собой 5-членную гетероарильную группу, предпочтительно выбранную из группы, состоящей из пирролила, пиразолила, имидазолила, тиенила, изоксазолила, тиазолила и изотиазолила, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из галогена, С1-8алифатика, гидрокси-С1-8алифатика, С1-8алифатикокси-С1-8алифатика, ди(С1-8алифатик)амино-С1-8алифатика, гетероциклил-С1-8алифатика, С1-8алифатиккарбонила и гетероциклила, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 5-6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из N, О и S, и предпочтительно выбранную из группы, состоящей из пиперидинила, пиперазинила, морфолинила и тетрагидропиранила; каждый гетероциклил возможно замещен одним или более С1-8алифатическими заместителями; и где С1-8алифатик в каждом случае независимо выбран из группы, состоящей из С1-8алкила и С3-8циклоалкила.
В некоторых воплощениях соединения формулы Ic, R1 представляет собой 5-членную гетероарильную группу, предпочтительно выбранную из группы, состоящей из пиразолила и изотиазолила, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из галогена и С1-8алифатика.
В некоторых воплощениях соединения формулы Ic, R1 представляет собой 5-членную гетероарильную группу, и предпочтительно выбранную из группы, состоящей из пирролила, пиразолила, имидазолила, тиенила, изоксазолила, тиазолила и изотиазолила, возможно замещенную одним или более R6, где каждый R6 независимо выбран из группы, состоящей из метила, этила, изопропила, н-бутила, гидроксиэтила, метоксиметила, метоксиэтила, метоксипропила, циклобутила, циклопентила, диметиламиноэтила, морфолин-4-ил-этила, тетрагидропиран-4-ила, циклобутила, циклопентила и метилкарбонила, и более предпочтительно, метила.
В некоторых воплощениях соединения формулы Ic, R1 выбран из группы, состоящей из:
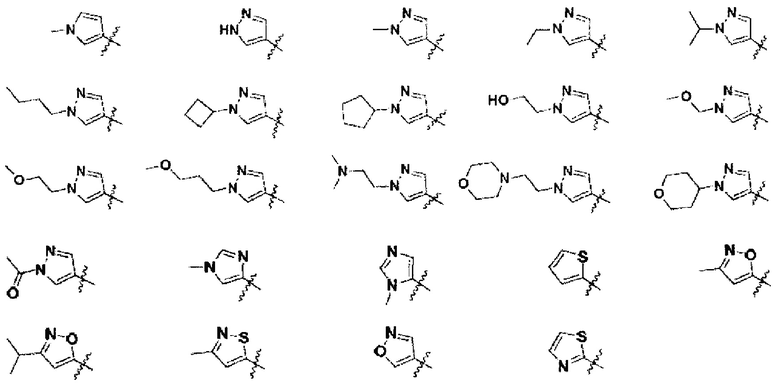 .
.
В некоторых воплощениях соединения формулы Ic, I равно 0, 1 или 2, более предпочтительно равно 0 или 1.
В некоторых воплощениях соединения формулы Ic, m равно 0, 1, 2 или 3, предпочтительно равно 1, 2 или 3.
В некоторых воплощениях соединения формулы Ic, n равно 0, 1 или 2, более предпочтительно равно 0.
В некоторых воплощениях соединения формулы Ic, m и n не равны 0 одновременно.
В некоторых воплощениях соединения формулы Ic каждая группа в формуле Ic определена следующим образом:
W представляет собой  или
или 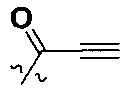 ;
;
X представляет собой NR4;
I равно 0, 1 или 2;
m равно 0, 1, 2 или 3;
n равно 0, 1 или 2;
R1 представляет собой 5-6-членную гетероарильную группу, возможно замещенную одним или более R6;
R3a, R3b и R3c все представляют собой водород;
R4 представляет собой водород;
каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, С1-8алифатика, С1-8галогеналифатика, гидрокси-С1-8алифатика, С1-8алифатикокси-С1-8алифатика, амино-С1-8алифатика, С1-8алифатикамино-С1-8алифатика, ди(С1-8алифатик)амино-С1-8алифатика, гетероциклил-С1-8алифатика и С1-8алифатиккарбонила, где гетероциклил, как независимая группа или как часть другой(их) групп(ы), представляет собой насыщенную или частично ненасыщенную 3-8-членную гетероциклическую группу, содержащую один или два гетероатома, выбранные из группы, состоящей из N, O и S; каждый гетероциклил возможно замещен одним или более заместителями, выбранными из группы, состоящей из галогена и С1-8алифатика,
где С1-8алифатик в каждом случае независимо выбран из группы, состоящей из С1-8алкила, С2-8алкенила, С2-8алкинила, С3-8циклоалкила и С4-8циклоалкенила.
В некоторых воплощениях соединения формулы Ic каждая группа в формуле Ic определена следующим образом:
W представляет собой 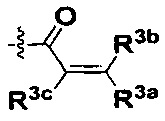 ;
;
X представляет собой NR4;
I равно 0, 1 или 2;
m равно 0, 1, 2 или 3;
n равно 0, 1 или 2;
R1 представляет собой 5-членную гетероарильную группу, возможно замещенную одним или более R6;
R3a, R3b и R3c все представляют собой водород;
R4 представляет собой водород;
каждый R6 независимо представляет собой С1-8алифатик, где С1-8алифатик выбран из группы, состоящей из С1-8алкила, С2-8алкенила, С2-8алкинила, С3-8циклоалкила и С4-8циклоалкенила.
В некоторых воплощениях соединения формулы 1 с соединение формулы Ic выбрано из группы, состоящей из:
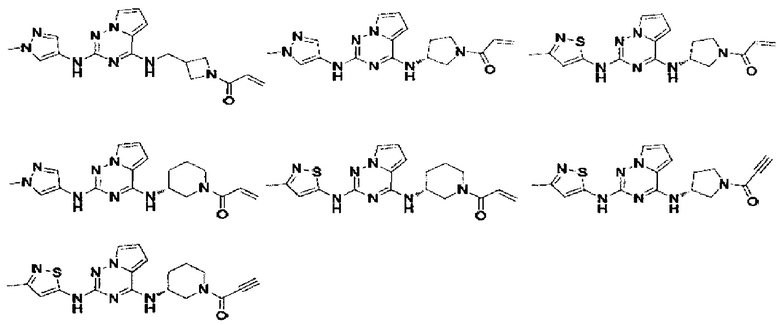 .
.
Соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению или его фармацевтически приемлемая соль могут содержать один или более хиральных атомов углерода, и каждый из асимметрических атомов углерода может быть в форме R- или S-конфигурации, обе из которых входят в объем по настоящему изобретению. Соответственно, соединения могут существовать в форме энантиомеров, диастереомеров или их смесей. Вышеуказанные соединения могут быть получены из рацематов, диастереомеров или энантиомеров в качестве исходных материалов или промежуточных веществ. Оптически активные изомеры могут быть получены с использованием хиральных синтонов или хиральных реагентов, либо разделены с использованием традиционных методик, например, хиральной хроматографией или фракционной кристаллизацией.
Традиционные методики получения/выделения индивидуальных изомеров включают хиральный синтез из подходящего оптически чистого предшественника или разделение рацемата (или рацемата соли или производного) с использованием, например, хиральной жидкостной хроматографии высокого давления, см., например, Gerald Giibitz и Martin G. Schmid (Eds.), Chiral Separations, Methods и Protocols, Methods in Molecular Biology, Vol. 243, 2004; A.M. Stalcup, Chiral Separations, Annu. Rev. Anal. Chem. 3: 341-63, 2010; Fumiss et al. (eds.), VOGEL'S ENCYCLOPEDIA OF PRACTICAL ORGANIC CHEMISTRY 5. sup. TH Ed., Longman Scientific и Technical Ltd., Essex, 1991, 809-816; и Heller, Acc. Chem. Res. 1990, 23, 128.
Еще один аспект настоящего изобретения относится к фармацевтической композиции, содержащей одно или более соединений формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению, или их стереоизомеров, таутомеров, сольватов или их фармацевтически приемлемых солей и фармацевтически приемлемые эксципиенты.
Фармацевтическая композиция по настоящему изобретению может быть изготовлена в виде препаратов в твердой, полутвердой, жидкой или газообразной форме, такой как таблетки, капсулы, порошки, гранулы, мази, растворы, суппозитории, инъекции, ингаляционные формы, гели, микросферы и аэрозоли.
Фармацевтическая композиция по настоящему изобретению может быть изготовлена способом, хорошо известным в фармацевтической области Например, фармацевтическая композиция, предназначенная для введения инъекцией, может быть изготовлена путем объединения соединения формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению, или его фармацевтически приемлемой соли или его пролекарства со стерильной дистиллированной водой с образованием раствора. Поверхностно-активное вещество может быть добавлено для облегчения образования гомогенного раствора или суспензии. Актуальные способы изготовления фармацевтической композиции известны специалистам в данной области техники; например, см. The Science and Practice of Pharmacy, 20th Edition (Philadelphia College of Pharmacy and Science, 2000).
Пути введения фармацевтической композиции по настоящему изобретению включают, без ограничения, пероральный, местный, трансдермальный, внутримышечный, внутривенный, ингаляционный, парентеральный, сублингвальный, ректальный, вагинальный и интраназальный. Например, лекарственные формы, подходящие для перорального введения, включают капсулы, таблетки, гранулы, сиропы и тому подобное. Соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению, включенные в эти лекарственные формы, могут представлять собой твердые порошки или гранулы; растворы или суспензии в водных или неводных жидкостях; эмульсии типа вода-в-масле или масло-в-воде; и тому подобное. Вышеперечисленные лекарственные формы могут быть приготовлены из активных соединений вместе с одним или более носителями или эксципиентами с использованием традиционных фармацевтических методик. Вышеперечисленные носители должны быть совместимыми с активными соединениями или другими эксципиентами. Для твердых препаратов общепринятые используемые нетоксичные носители включают, без ограничения, маннит, лактозу, крахмал, стеарат магния, целлюлозу, глюкозу, сахарозу и тому подобное. Носители для жидких препаратов включают, без ограничения, воду, физиологический солевой раствор, водный раствор глюкозы, этилен гликоль, полиэтиленгликоль и тому подобное. Активное соединение может образовывать раствор или суспензию с вышеуказанными носителями. Конкретный путь введения и лекарственная форма зависят от физических и химических свойств соединений как таковых и от тяжести заболеваний, подлежащих лечению, и так далее. Конкретный путь введения может быть определен специалистом в данной области на основании вышеперечисленных факторов в сочетании с собственными знаниями. См., например, Li jun, "Clinical pharmacology", People's Medical Publishing House, 2008.06; Ding Yufeng, Discussion on Clinical Dosage Form factors and Drug Rational use in Hospital, Herald of Medicine, 26(5), 2007; Howard C. Ansel, Loyd V. Allen, Jr., Nicholas G. Popovich ed., Jiang Zhiqiang translated, "Pharmaceutical Dosage Forms and Drug Delivery System", China Medical Science Press, 2003.05.
Соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению, или фармацевтическая композиция, содержащая соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению могут быть использованы в ассоциации или комбинации с одним или более чем одним другим лекарственным средством. Лекарственные средства, предназначенные для использования в комбинации с соединением формулы I, в частности соединениями формул Ia, Ib и Ic, по настоящему изобретению, или фармацевтической композицией, содержащей соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению, включают, без ограничения:
1) иммунодепрессанты, такие как метотрексат, циклофосфамид и тому подобное;
2) кортикостероиды, такие как дексаметазон, бетаметазон и тому подобное;
3) нестероидные противовоспалительные лекарственные средства, такие как салицилаты, арилалкановая кислота и тому подобное;
4) специфические ингибиторы циклооксигеназы-2 (Cox-2), такие как рофекоксиб, целекоксиб и тому подобное;
5) белки, связывающие фактор некроза опухоли альфа (TNF-α), такие как инфликсимаб, адалимумаб и тому подобное;
6) интерфероны, такие как интерферон-β и интерферон-γ; интерлейкины, такие как интерлейкин-2; и тому подобное.
Еще один аспект настоящего изобретения относится к соединению формулы I, в частности соединениям формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомеру, таутомеру, сольвату или фармацевтически приемлемой соли для ингибирования активностей ВТК и/или JAK3.
Еще один аспект настоящего изобретения относится к соединению формулы I, в частности соединениям формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомеру, таутомеру, сольвату или фармацевтически приемлемой соли для предупреждения и/или лечения ВТК- и/или JAK3-опосредованных заболеваний.
Еще один аспект настоящего изобретения относится к фармацевтической композиции, содержащей соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомер, таутомер, сольват или фармацевтически приемлемую соль, для ингибирования активностей ВТК и/или JAK3.
Еще один аспект настоящего изобретения относится к фармацевтической композиции, содержащей соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению, или его стереоизомер, таутомер, сольват или фармацевтически приемлемую соль, для предупреждения и/или лечения ВТК- и/или JAKS-опосредованных заболеваний.
Еще один аспект настоящего изобретения относится к применению соединения формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению или его стереоизомера, таутомера, сольвата или фармацевтически приемлемой соли или фармацевтической композиции, содержащей соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению или его стереоизомер, таутомер, сольват или фармацевтически приемлемую соль, в изготовлении лекарственного средства для ингибирования активностей ВТК и/или JAK3.
Еще один аспект настоящего изобретения относится к применению соединения формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению или его стереоизомера, таутомера, сольвата или фармацевтически приемлемой соли или фармацевтической композиции, содержащей соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению или его стереоизомер, таутомер, сольват или фармацевтически приемлемую соль, в изготовлении лекарственного средства для лечения и/или предупреждения ВТК- и/или JAK3-опосредованных заболеваний.
Еще один аспект настоящего изобретения относится к применению соединения формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению или его стереоизомера, таутомера, сольвата или фармацевтически приемлемой соли или фармацевтической композиции, содержащей соединение формулы I, в частности соединения формул Ia, Ib и Ic, по настоящему изобретению или его стереоизомер, таутомер, сольват или фармацевтически приемлемую соль, в изготовлении лекарственного средства для лечения и/или предупреждения ВТК- и/или JAK3-опосредованных заболеваний.
Еще один аспект настоящего изобретения относится к способу ингибирования активностей ВТК и/или JAK3 в биологической системе, включающему приведение биологической системы в контакт с соединением формулы I, в частности соединениями формул Ia, Ib и Ic, по настоящему изобретению или его стереоизомером, таутомером, сольватом или фармацевтически приемлемой солью или с фармацевтической композицией, содержащей указанное соединение. В некоторых воплощениях биологическая система представляет собой фермент, клетку или млекопитающего. Примеры млекопитающих включают, без ограничения, людей; не являющихся людьми приматов, таких как шимпанзе и другие виды приматов и обезьян; сельскохозяйственных животных, таких как крупный рогатый скот, лошади, овцы, козы, свиньи; домашних животных, таких как кролики, собаки и кошки; лабораторных животных, включая грызунов, таких как крысы, мыши и морские свинки, и тому подобное.
Еще один аспект настоящего изобретения относится к способу ингибирования ВТК и/или JAK3 у млекопитающего, в частности у человека, включающему введение указанному млекопитающему, в частности человеку, нуждающемуся в этом, терапевтически эффективного количества соединения формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению, его стереоизомера, таутомера, сольвата или фармацевтически приемлемой соли или фармацевтической композиции, содержащей указанное соединение.
Еще один аспект настоящего изобретения относится к способу лечения и/или предупреждения ВТК- и/или JAK3-опосредованных заболеваний, включающему введение млекопитающему, в частности человеку, нуждающемуся в этом, терапевтически эффективного количества соединения формулы I, в частности соединений формул Ia, Ib и Ic, по настоящему изобретению, его стереоизомера, таутомера, сольвата или фармацевтически приемлемой соли или фармацевтической композиции, содержащей указанное соединение.
В настоящей заявке ВТК- и/или JAK3-опосредованные заболевания выбраны из группы, состоящей из аутоиммунных заболеваний, воспалительных заболеваний, гетероиммунных состояний или заболеваний, тромбоэмболических заболеваний и злокачественных новообразований. Аутоиммунные заболевания и воспалительные заболевания выбраны из группы, состоящей из ревматоидного артрита, остеоартрита, юношеского артрита, хронических обструктивных легочных заболеваний, рассеянного склероза, системной красной волчанки, псориаза, псориатического артрита, болезни Крона, неспецифического язвенного колита и синдрома раздраженного кишечника, и тому подобного. Злокачественные новообразования выбраны из группы, состоящей из B-клеточного хронического лимфоцитарного лейкоза, острого лимфоцитарного лейкоза, неходжкинской лимфомы, лимфомы Ходжкина, острого миелоидного лейкоза, диффузной крупноклеточной B-клеточной лимфомы, множественной миеломы, лимфомы клеток мантии и мелкоклеточной лимфоцитарной лимфомы, и тому подобного.
Композицию по настоящему изобретению готовят, определяют количество и вводят способом, удовлетворяющим требованиям медицинской практики. "Терапевтически эффективное количество" соединения по настоящему изобретению определяют в зависимости от конкретных расстройств, подлежащих лечению, индивидуумов, которых лечат, причин расстройств, мишеней лекарственных средств и способов введения. Как правило, доза для парентерального введения может составлять от 1 до 200 мг/кг, и доза для перорального введения может составлять от 1 до 1000 мг/кг.
Диапазоны эффективных доз, предложенные здесь, не предназначены для ограничения объема изобретения, а представляют предпочтительные диапазоны доз. Однако, наиболее предпочтительная дозировка будет подбираться для индивидуального субъекта, как определит специалист в данной области техники (см., например, Berkow et. al. eds., The Merck Manual, 16th edition, Merck Company, Rahway, N.J., 1992).
Получение соединения по изобретению
Следующие реакционные схемы с участием соединений формул Ia, Ib и Ic в качестве примеров иллюстрируют способы получения соединений формулы I по настоящему изобретению.
Специалистам в данной области техники понятно, что в следующем описании комбинации заместителей возможны, только если такие комбинации дают стабильные соединения.
Специалистам в данной области техники также следует понимать, что в описанном ниже процессе функциональные группы непосредственных соединений могут нуждаться в защите подходящими защитными группами "PG". Указанные функциональные группы включают гидроксил, амино, меркапто и карбоновую кислоту. Подходящие защитные группы для гидроксила включают триалкилсилил или диарилалкилсилил (например, трет-бутил-диметилсилил, трет-бутил-дифенилсилил или триметилсилил), тетрагидропиранил, бензил и тому подобное. Подходящие защитные группы для амино, амидино и гуанидино включают трет-бутоксикарбонил, бензилоксикарбонил и тому подобное. Подходящие защитные группы для меркапто включают -C(O)-R'' (где R'' представляет собой алкил, арил или арилалкил), пара-метоксибензил, тритил и тому подобное. Подходящие защитные группы для карбоксила включают алкиловые, ариловые или арилалкиловые сложные эфиры.
Защитные группы могут быть введены и удалены в соответствии со стандартными методиками, которые известны специалистам в данной области техники и как описано в данном описании.
Использование защитных групп описано подробно в Greene, Т.W. и P.G.М. Wuts, Protective Groups in Organic Synthesis, (1999), 4th Ed., Wiley. Защитные группы также могут представлять собой полимерную смолу.
Соединения формулы Ia, Ib и Ic по настоящему изобретению могут быть получены согласно методикам, проиллюстрированным на следующей реакционной схеме I.
Реакционная схема I

где X, Y, Z, W, R1 и R2 в их соответствующих формулах все являются такими, как определено в формуле Ia выше;
или

где X, Y, Z, W, R1, I, m и n в их соответствующих формулах все являются такими, как определено в формуле Ib выше;
или

где X, Y, Z, W, R1, I, m и n в их соответствующих формулах все являются такими, как определено в формуле Ic выше.
Реакционная схема I включает следующие стадии:
Стадия 1: подвергание соединения формулы 1a, 1b или 1c, соответственно, реакции замещения с соединением формулы 2а, 2b или 2c с получением соединения формулы 3a, формулы 3b или формулы 3c.
На этой стадии реакцию предпочтительно осуществляют в присутствии основания. Основание, используемое в реакции, может представлять собой органическое основание, выбранное из группы, состоящей из триэтиламина, N,N-диизопропилэтиламина, пиридина и тому подобного. Основание, используемое в реакции, может также представлять собой неорганическое основание, выбранное из группы, состоящей из карбоната натрия, карбоната калия, гидроксида натрия и тому подобного. Реакция также может быть осуществлена в присутствии кислоты или в нейтральных условиях. Кислота, используемая в реакции, может быть выбрана из группы, состоящей из соляной кислоты, трифторуксусной кислоты, раствора хлористого водорода в 1,4-диоксане, уксусной кислоты, серной кислоты и тому подобного. Температура реакции находится в диапазоне от -80°C до 120°C. Растворитель, используемый в реакции, может быть выбран из группы, состоящей из 1,4-диоксана, тетрагидрофурана, дихлорметана, толуола, метанола, этанола, изопропанола, бутанола и тому подобного.
Стадия 2: удаление защитной группы PG с соединения формулы 3a, 3b или 3c с получением соединения формулы 4а, 4b или 4c.
Защитная группа (PG) соединения формулы 3a, 3b или 3c может представлять собой Алрет-бутоксикарбонил, бензилоксикарбонил, бензил или тому подобное. Снятие защиты может быть осуществлено в условиях кислотного катализа. Кислота, используемая в реакции, может быть выбрана из группы, состоящей из соляной кислоты, трифторуксусной кислоты, раствора хлористого водорода в 1,4-диоксане, уксусной кислоты, серной кислоты и тому подобного. Реакция также может быть осуществлена каталитическим гидрированием с использованием палладиевого катализатора в кислых или нейтральных условиях. Палладиевый катализатор, используемый в настоящем изобретении, может быть выбран из группы, состоящей из палладия на углероде и гидроксида палладия. Кислота, используемая в реакции, может быть выбрана из группы, состоящей из соляной кислоты, трифторуксусной кислоты, раствора хлористого водорода в 1,4-диоксане, серной кислоты и тому подобного. Температура реакции находится в диапазоне от -80°C до 120°C. Растворитель, используемый в реакции, может быть выбран из группы, состоящей из 1,4-диоксана, тетрагидрофурана, дихлорметана, толуола, этанола и тому подобного.
Стадия 3: подвергание соединения формулы 4а, 4b или 4c реакции конденсации с получением соединения формулы 5а, 5b или 5c.
На этой стадии реагент конденсации может быть выбран из группы, состоящей из карбонилдиимидазола (CDI), тетрафторбората O-бензотриазол-1-ил-N,N,N',N'-тетраметилурония (TBTU), дициклогексилкарбодиимида (DCC), 1-(3-диметиламинопропил)-3-этил-карбодиимида (EDCI) и тому подобного. Основание, используемое в реакции, может быть выбрано из группы, состоящей из триэтиламина, N,N-диизопропилэтиламина, пиридина, гидрида натрия и тому подобного. Температура реакции находится в диапазоне от 0°C до 80°C. Растворитель, используемый в реакции, может быть выбран из группы, состоящей из 1,4-диоксана, тетрагидрофурана, дихлорметана, толуола и тому подобного.
Стадия 4: подвергание соединения формулы 5а, 5b или 5c реакции замещения с получением соответствующего соединения Ia, Ib или Ic.
На этой стадии реакция может быть осуществлена в присутствии кислоты или в нейтральных условиях. Кислота, используемая в реакции, может быть выбрана из группы, состоящей из соляной кислоты, трифторуксусной кислоты, раствора хлористого водорода в 1,4-диоксане, уксусной кислоты, серной кислоты и тому подобного. Реакция также может быть осуществлена в присутствии основания. Основание, используемое в реакции, может представлять собой сильное основание, выбранное из группы, состоящей из гидроксида натрия, карбоната цезия, трет-бутоксида натрия, гидрида натрия и тому подобного. Реакция также может быть осуществлена в присутствии палладиевого катализатора. Палладиевый катализатор, который может быть использован в настоящем изобретении, выбран из группы, состоящей из дихлорида бис(трифенилфосфин)палладия (Pd(PPh3)2Cl2), трис(дибензилиденпропанон)дипалладия (Pd2(dba)3), тетра(трифенилфосфин)палладия (Pd(PPh3)4), ацетата палладия (Pd(OAc)2), [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (Pd(dppf)Cl2) и хлорида палладия (PdCl2). Основание, которое может быть полезно в этих условиях, предпочтительно представляет собой неорганическое основание, такое как карбонат натрия, карбонат калия, фосфат калия, карбонат цезия и тому подобное. Температура реакции находится в диапазоне от 80°C до 160°C. Растворитель, используемый в реакции, может быть выбран из группы, состоящей из 1,4-диоксана, толуола, этанола, изопропанола, бутанола, 2-бутанола, воды и их смесей.
Соединения формул Ia, Ib и Ic по настоящему изобретению могут быть получены согласно методикам, проиллюстрированным на следующей реакционной схеме II.
Реакционная схема II

где X, Y, Z, W, R1 и R2 в их соответствующих формулах все являются такими, как определено выше в формуле Ia;
или

где X, Y, Z, W, R1, I, m и n в их соответствующих формулах все являются такими, как определено выше в формуле Ib;
или

где X, Y, Z, W, R1, I, m и n в их соответствующих формулах все являются такими, как определено выше в формуле Ic.
Реакционная схема II включает следующие стадии:
Стадия 1: подвергание соединения формулы 1a, 1b или 1c, соответственно, реакции замещения с соединением формулы 2а, 2b или 2c с получением соединения формулы 3a, 3b или .3c
На этой стадии реакцию предпочтительно осуществляют в присутствии основания. Основание, используемое в реакции, может представлять собой органическое основание, выбранное из группы, состоящей из триэтиламина, N,N-диизопропилэтиламина, пиридина и тому подобного. Основание, используемое в реакции, может также представлять собой неорганическое основание, выбранное из группы, состоящей из карбоната натрия, карбоната калия, гидроксида натрия и тому подобного. Реакция также может быть осуществлена в присутствии кислоты или в нейтральных условиях. Кислота, используемая в реакции, может быть выбрана из группы, состоящей из соляной кислоты, трифторуксусной кислоты, раствора хлористого водорода в 1,4-диоксане, уксусной кислоты, серной кислоты и тому подобного. Температура реакции находится в диапазоне от -80°C до 120°C. Растворитель, используемый в реакции, может быть выбран из группы, состоящей из 1,4-диоксана, тетрагидрофурана, дихлорметана, толуола, метанола, этанола, изопропанола, бутанола и тому подобного.
Стадия 5: подвергание соединения формулы 3a, 3b или 3c реакции замещения с получением соединения формулы 6а, 6b или 6c.
На этой стадии реакция может быть осуществлена в присутствии кислоты или в нейтральных условиях. Кислота, используемая в реакции, может быть выбрана из группы, состоящей из соляной кислоты, трифторуксусной кислоты, раствора хлористого водорода в 1,4-диоксане, уксусной кислоты, серной кислоты и тому подобного. Реакция также может быть осуществлена в присутствии основания. Основание, используемое в реакции, может представлять собой сильное основание, выбранное из группы, состоящей из гидроксида натрия, трет-бутоксида натрия, гидрида натрия и тому подобного. Реакция также может быть осуществлена в присутствии палладиевого катализатора. Палладиевый катализатор, который может быть использован в настоящем изобретении, выбран из группы, состоящей из дихлорида бис(трифенилфосфин)палладия (Pd(PPh3)2Cl2), рис(дибензилиденпропанон)дипалладия (Pd2(dba)3), тетра(трифенилфосфин)палладия (Pd(PPh3)4), ацетата палладия (Pd(OAc)2), [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (Pd(dppf)Cl2) и хлорида палладия (PdCl2). Основание, которое может быть полезно в этих условиях, предпочтительно представляет собой неорганическое основание, такое как карбонат натрия, карбонат калия, фосфат калия, карбонат цезия и тому подобное. Температура реакции находится в диапазоне от 80°C до 160°C. Растворитель, используемый в реакции, может быть выбран из группы, состоящей из 1,4-диоксана, толуола, этанола, изопропанола, бутанола, 2-бутанола, воды и их смесей.
Стадия 6: удаление защитной группы PG соединения формулы 6а, 6b или 6c с получением соединения формулы 7а, 7b или 7c.
Защитная группа (PG) соединения формулы 6а, 6b или 6c может представлять собой трет-бутоксикарбонил, бензилоксикарбонил, бензил или тому подобное. Снятие защиты может быть осуществлено в условиях кислотного катализа. Кислота, используемая в реакции, может быть выбрана из группы, состоящей из соляной кислоты, трифторуксусной кислоты, раствора хлористого водорода в 1,4-диоксане, уксусной кислоты, серной кислоты и тому подобного. Реакция также может быть осуществлена каталитическим гидрированием с использованием палладиевого катализатора в кислых или нейтральных условиях. Палладиевый катализатор, используемый в настоящем изобретении, может быть выбран из группы, состоящей из палладия на углероде и гидроксида палладия, и кислота, используемая в реакции, может быть выбрана из группы, состоящей из соляной кислоты, раствора хлористого водорода в 1,4-диоксане, серной кислоты и тому подобного. Температура реакции находится в диапазоне от -80°C до 120°C. Растворитель, используемый в реакции, может быть выбран из группы, состоящей из 1,4-диоксана, тетрагидрофурана, дихлорметана, толуола, метанола, этанола и тому подобного.
Стадия 7: подвергание соединения формулы 7а, 7b или 7c реакции конденсации с получением соответствующего соединения формулы Ia, Ib или Ic.
На этой стадии реагент конденсации может быть выбран из группы, состоящей из карбонилдиимидазола (CDI), тетрафторбората О-бензотриазол-1-ил-N,N,N',N'-тетраметилурония (TBTU), дициклогексилкарбодиимида (DCC), 1-(3-диметиламинопропил)-3-этил-карбодиимида (EDCI) и тому подобного. Основание, используемое в реакции, может быть выбрано из группы, состоящей из триэтиламина, N,N-диизопропилэтиламина, пиридина и тому подобного. Температура реакции находится в диапазоне от 0°C до 80°C. Растворитель, используемый в реакции, может быть выбран из группы, состоящей из 1,4-диоксана, тетрагидрофурана, дихлорметана, толуола и тому подобного.
Соединение формулы Ia по настоящему изобретению может быть получено согласно методикам, проиллюстрированным на следующей реакционной схеме III.
Реакционная схема III
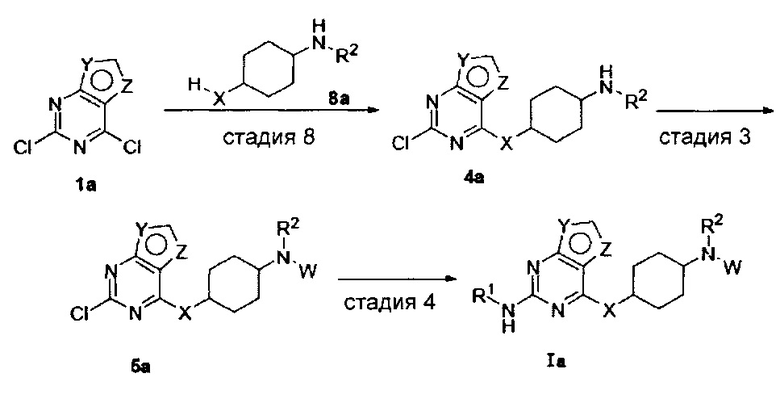
где X, Y, Z, W, R1 и R2 в их соответствующих формулах все являются такими, как определено выше в формуле Ia.
Реакционная схема III включает следующие стадии:
Стадия 8: подвергание соединения формулы 1a реакции замещения с соединением формулы 8а с получением соединения формулы 4а.
На этой стадии реакцию предпочтительно осуществляют в присутствии основания. Основание, используемое в реакции, может представлять собой органическое основание, выбранное из группы, состоящей из триэтиламина, N,N-диизопропилэтиламина, пиридина и тому подобного. Основание, используемое в реакции, может также представлять собой неорганическое основание, выбранное из группы, состоящей из карбоната натрия, карбоната калия, гидроксида натрия и тому подобного. Реакция также может быть осуществлена в присутствии кислоты или в нейтральных условиях. Кислота, используемая в реакции, может быть выбрана из группы, состоящей из соляной кислоты, трифторуксусной кислоты, раствора хлористого водорода в 1,4-диоксане, уксусной кислоты, серной кислоты и тому подобного. Температура реакции находится в диапазоне от -80°C до 120°C. Растворитель, используемый в реакции, может быть выбран из группы, состоящей из 1,4-диоксана, тетрагидрофурана, дихлорметана, толуола, метанола, этанола, изопропанола, бутанола и тому подобного.
Стадия 3: подвергание соединения формулы 4а реакции конденсации с получением соединения формулы 5а.
На этой стадии реагент конденсации может быть выбран из группы, состоящей из карбонилдиимидазола (CDI), тетрафторбората О-бензотриазол-1-ил-N,N,N',N'-тетраметилурония (TBTU), дициклогексилкарбодиимида (DCC), 1-(3-диметиламинопропил)-3-этил-карбодиимида (EDCI) и тому подобного. Основание, используемое в реакции, может быть выбрано из группы, состоящей из триэтиламина, N,N-диизопропилэтиламина, пиридина и тому подобного. Температура реакции находится в диапазоне от 0°C до 80°C. Растворитель, используемый в реакции, может быть выбран из группы, состоящей из 1,4-диоксана, тетрагидрофурана, дихлорметана, толуола и тому подобного.
Стадия 4: подвергание соединения формулы 5а реакции замещения с получением соответствующего соединения формулы Ia.
На этой стадии реакция может быть осуществлена в присутствии кислоты или в нейтральных условиях, и кислота, используемая в реакции, может быть выбрана из группы, состоящей из соляной кислоты, трифторуксусной кислоты, раствора хлористого водорода в 1,4-диоксане, уксусной кислоты, серной кислоты и тому подобного. Реакция также может быть осуществлена в присутствии основания, и основание, используемое в реакции, может представлять собой сильное основание, выбранное из группы, состоящей из гидроксида натрия, трет-бутоксида натрия, гидрида натрия и тому подобного. Реакция также может быть осуществлена в присутствии палладиевого катализатора. Палладиевый катализатор, который может быть использован в настоящем изобретении, выбран из группы, состоящей из дихлорида бис(трифенилфосфин)палладия (Pd(PPh3)2Cl2), трис(дибензилиденпропанон)дипалладия (Pd2(dba)3), тетра(трифенилфосфин)палладия (Pd(PPh3)4), ацетата палладия (Pd(OAc)2), [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (Pd(dppf)Cl2) и хлорида палладия (PdCl2). Основание, которое может быть полезно в этих условиях, предпочтительно представляет собой неорганическое основание, такое как карбонат натрия, карбонат калия, фосфат калия, карбонат цезия и тому подобное. Температура реакции находится в диапазоне от 80°C до 160°C. Растворитель, используемый в реакции, может быть выбран из группы, состоящей из 1,4-диоксана, толуола, этанола, изопропанола, бутанола, 2-бутанола, воды и их смесей.
Специалистам в данной области техники следует понимать, что вышеприведенные реакционные схемы и способы получения приведены только для целей простой и ясной иллюстрации и не предназначены для ограничения и что соединение формулы I по настоящему изобретению также может быть получено способами, аналогичными тому как описано выше, путем выбора соответствующих исходных материалов, которые могут быть коммерчески доступными или могут быть получены с использованием способов, хорошо известных в данной области техники.
Примеры
Следующие эксперименты, способы синтеза и участвующие промежуточные соединения даны в целях иллюстрации настоящего изобретения и не предназначены ограничивать объем настоящего изобретения.
Исходные материалы, используемые в настоящем изобретении, приобретали у поставщиков реагентов или получали из известных материалов, как известно в данной области техники. Если конкретно не указано иное, в примерах применяются следующие условия:
температура выражена в градусах по Цельсию (°C); и комнатная температура определена как 18-25°C;
органический растворитель сушили над безводным сульфатом магния или безводным сульфатом натрия и концентрировали до сухого состояния с использованием роторного испарителя при пониженном давлении при повышенной температуре (например, 15 мм рт.ст., 30°C);
силикагель 200-300 меш использовали в качестве носителя при разделении и очистке посредством колоночной хроматографии, и ТСХ относится к тонкослойной хроматографии;
обычно протекание реакции отслеживали по ТСХ или жидкостной хроматографии/масс-спектрометрии (ЖХ-МС);
идентификацию конечного продукта осуществляли согласно ЯМР (Bruker A VAN СЕ 300, 300 МГц) и ЖХ-МС (Bruker esquine 6000, Agilent 1200 series) спектрометрии.
Пример 1
Получение N-(цис-4-((2-((1-метил-1H-пиразол-4-ил)амино)тиено[3,2-d]пиримидин-4-ил)амино)циклогексил)акриламида
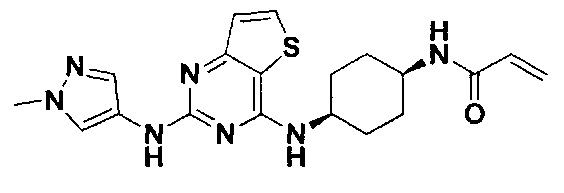
Стадия 1: получение трет-бутил-цис-4-((2-хлор-тиено[3,2-d]пиримидин-4-ил)амино)циклогексилкарбамата
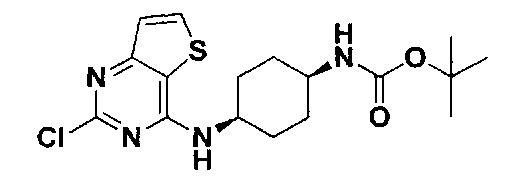
2,4-Дихлор-тиено[3,2-d]пиримидин (678 мг, 3,31 ммоль) и трет-бутил-цис-4-аминоциклогексилкарбамат (849 мг, 3,97 ммоль) растворяли в тетрагидрофуране (10 мл) с последующим добавлением N,N-диизопропилэтиламина (0,9 мл, 4,97 ммоль). Реакционный раствор подвергали взаимодействию при 70°C в течение ночи и затем концентрировали. К остатку добавляли воду (20 мл) и экстрагировали этилацетатом (20 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: н-гексан:этилацетат в соотношении 1:5) с получением белого твердого вещества (1,07 г). Выход: 84,7%. МС (ИЭР (ионизация электрораспылением), m/z): [M+H]+: 383,4; 1Н-ЯМР (300 МГц, CDCl3) δ: 7.74 (d, 1Н, J=5,4 Гц), 7.35 (d, 1Н, J=5,4 Гц), 5.00 (s, 1Н), 4.59 (s, 1Н), 4.31-4.38 (m, 1Н), 3.72-3.74 (m, 1Н), 1.62-2.04 (m, 8Н), 1.45 (s, 9Н).
Стадия 2: получение цис-N1-(2-хлор-тиено[3,2-d]пиримидин-4-ил)циклогексил-1,4-диамина

Продукт, полученный на стадии 1 (840 мг, 2,2 ммоль), растворяли в дихлорметане (10 мл) с последующим медленным добавлением трифторуксусной кислоты (2 мл, 30,8 ммоль). Реакционный раствор подвергали взаимодействию при комнатной температуре в течение 2 часов. Реакционный раствор концентрировали и полученный таким образом неочищенный продукт использовали непосредственно на следующей стадии без дополнительной очистки. МС (ИЭР, m/z): [M+H]+: 282,9.
Стадия 3: получение N-(цис-4-((2-хлор-тиено[3,2-d]пиримидин-4-ил)амино)циклогексил)акриламида

Продукт, полученный на стадии 2 (620 мг, 2,20 ммоль), растворяли в дихлорметане (10 мл) с последующим добавлением триэтиламина (440 мг, 4,4 ммоль). К указанному выше раствору добавляли по каплям при 0°C раствор акрилоилхлорида (0,2 мл, 2,42 ммоль), растворенного в дихлорметане (5 мл). Реакционный раствор выдерживали при комнатной температуре в течение ночи. Реакционный раствор промывали водой (20 мл), органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 70:1) с получением белого твердого вещества (0,56 г). Выход: 75,8%. МС (ИЭР, m/z): [M+H]+: 337,2; 1Н-ЯМР (300 МГц, DMCO-d6) δ: 7.76 (d, 1Н, J=5,4 Гц), 7.36 (d, 1Н, J=5,4 Гц), 6.07-6.35 (m, 2Н), 5.65-5.69 (m, 2Н), 5.23 (bs, 1Н), 4.34-4.38 (m, 1Н), 4.09-4.13 (m, 1Н), 1.68-2.02 (m, 8Н).
Стадия 4: получение N-(цис-4-((2-((1-метил-1Н-пиразол-4-ил)амино)тиено[3,2-d] пиримидин-4-ил)амино)циклогексил)акриламида
Продукт, полученный на стадии 3 (54 мг, 0,162 ммоль), и 1-метил-1Н-пиразол-4-амин (23 мг, 0,244 ммоль) растворяли в 1,4-диоксане (2 мл). Значение pH реакционного раствора доводили до 5 трифторуксусной кислотой и эту реакционную смесь подвергали взаимодействию при 90°C при микроволновом излучении в течение 0,5 часа. Реакционный раствор охлаждали до комнатной температуры и значение pH доводили до 8, используя 1 н. раствор гидроксида натрия. Полученную смесь экстрагировали этилацетатом (10 мл × 3) и органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением бледно-желтого твердого вещества (32 мг). Выход: 49,8%. МС (ИЭР, m/z): [M+H]+: 398,3; 1Н-ЯМР (300 МГц, CDCl3) δ: 7.66-7.69 (m, 3H), 6.99-7.19 (m, 2Н), 6.32 (dd, 1Н, J=1,5 Гц, J=16,8 Гц), 6.15 (dd, 1Н, J=10,2 Гц, J=16,8 Гц), 5.89-5.91 (m, 2Н), 5.66 (dd, 1Н, J=1,5 Гц, J=10,2 Гц), 4.23-4.38 (m, 1Н), 4.08-4.16 (m, 1Н), 3.88 (s, 3H), 1.75-2.05 (m, 8Н).
Следующие соединения (в таблице 1) получали из аналогичных исходных материалов с использованием методов синтеза, аналогичных описанным в Примере 1.
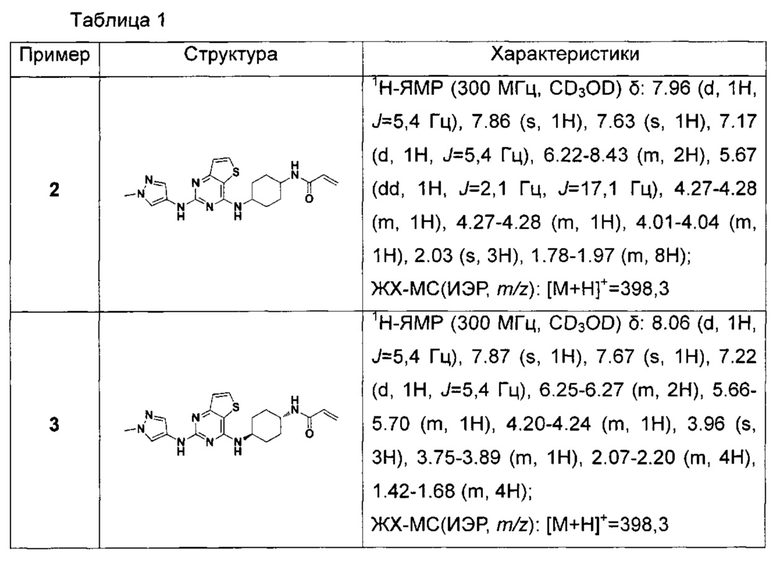
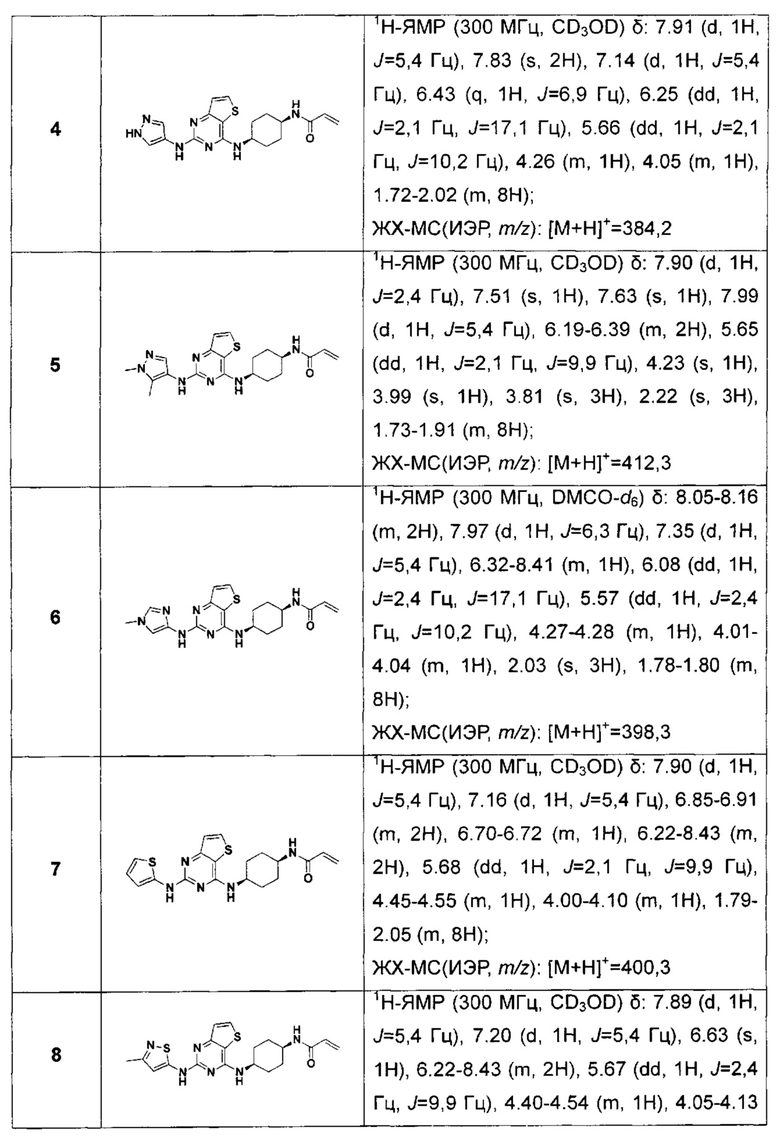


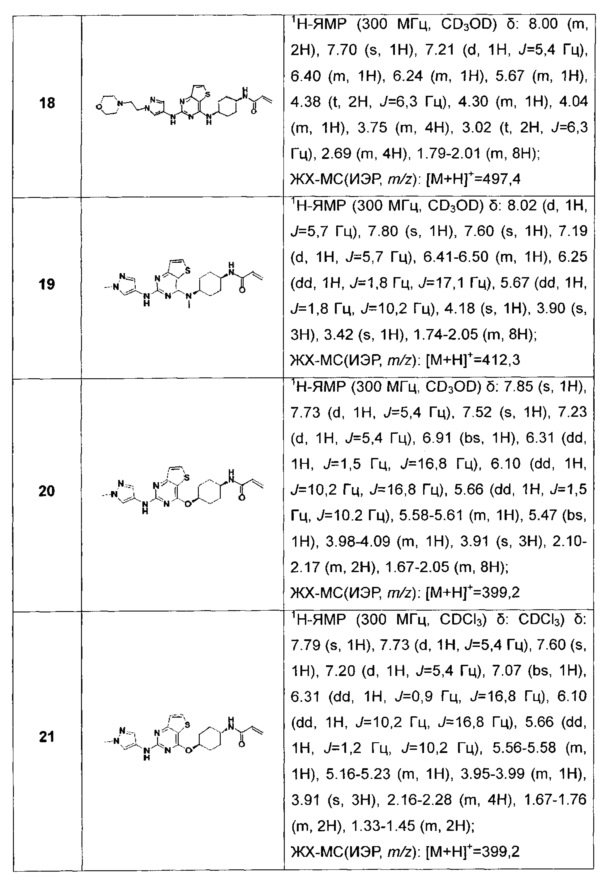
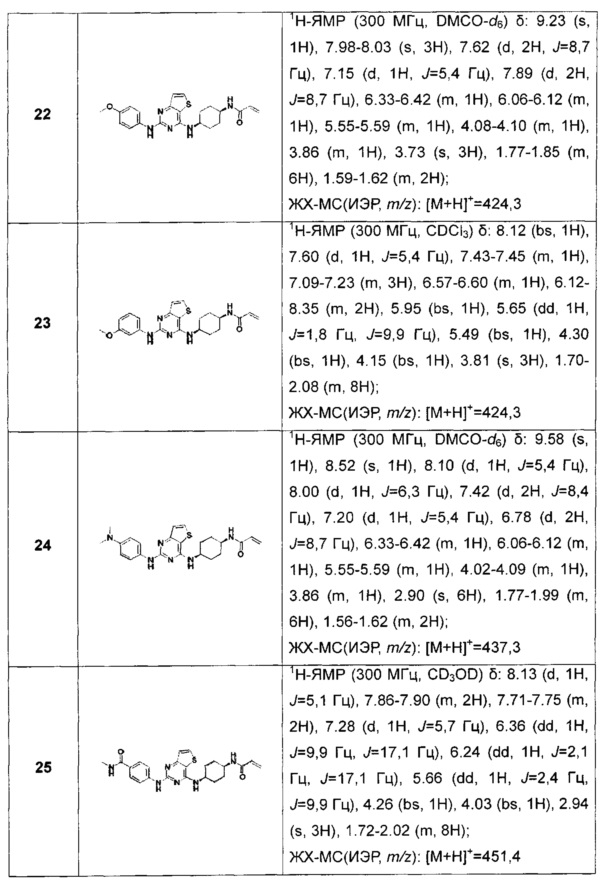
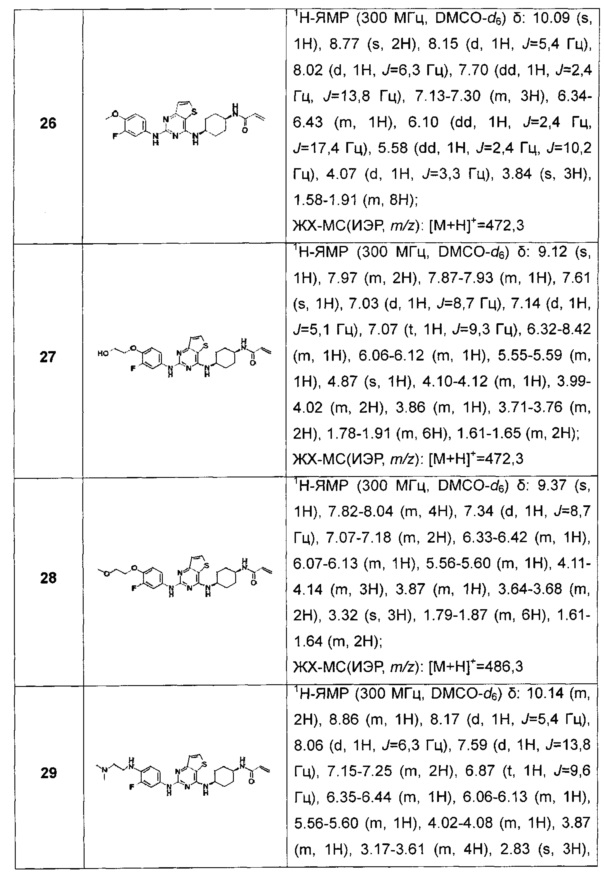
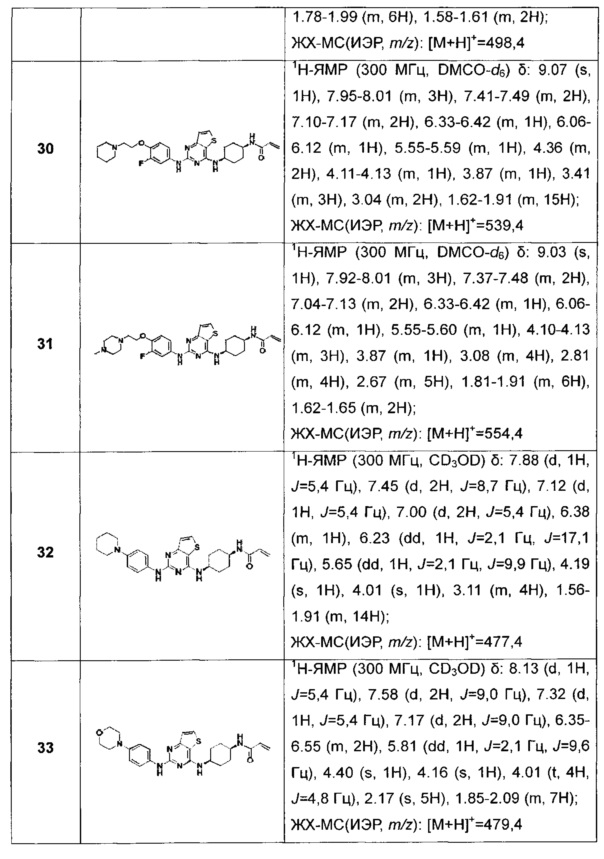
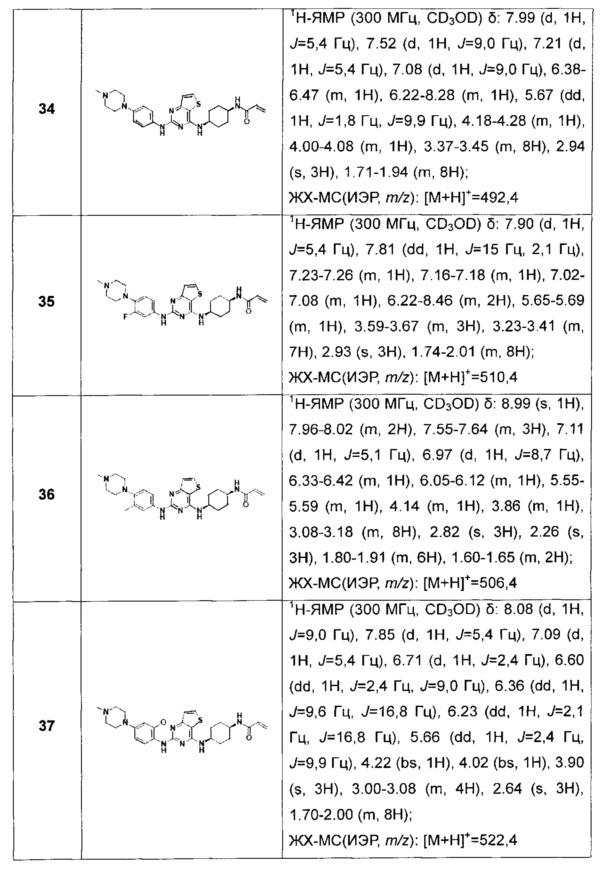
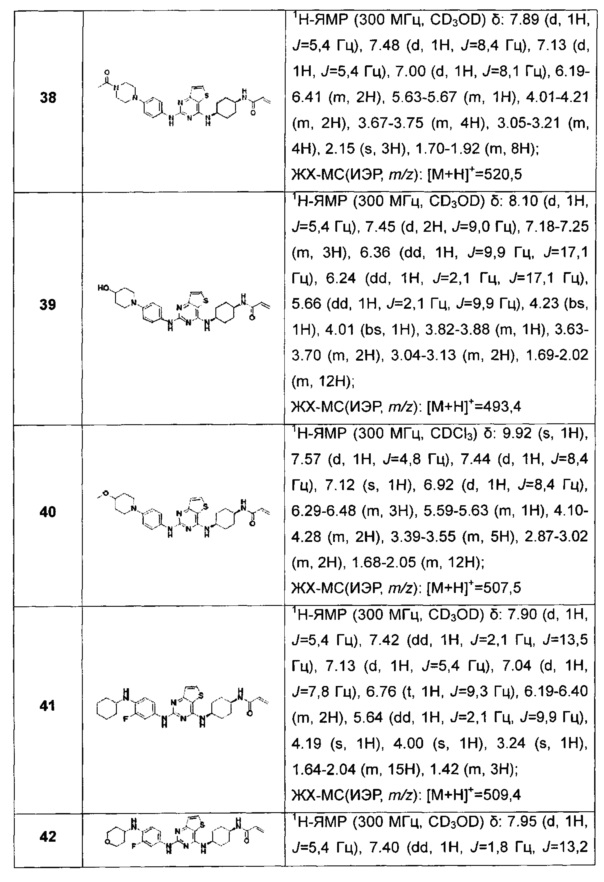


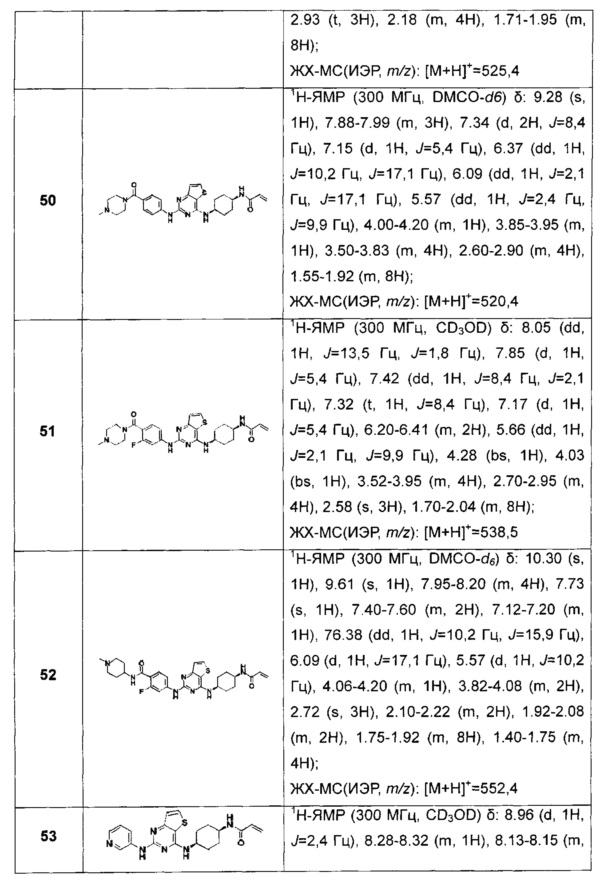

Пример 57
Получение N-(цис-4-((2-((1-метил-1H-пиразол-4-ил)амино)фуро[3,2-d]пиримидин-4-ил)амино)циклогексил)акриламида

Стадия 1: получение цис-N1-(2-хлор-фуро[3,2-d]пиримидин-4-ил)циклогексил-1,4-диамина
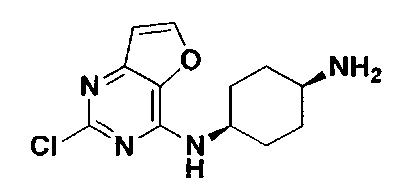
2,4-Дихлор-фуро[3,2-d]пиримидин (188 мг, 1 ммоль) растворяли в дихлорметане (5 мл) и по каплям добавляли к раствору цис-1,4-циклогександиамина (456 мг, 4,0 ммоль) в дихлорметановом (10 мл) растворе. Реакционный раствор перемешивали при комнатной температуре в течение ночи и затем концентрировали. К остатку добавляли воду (20 мл) и экстрагировали этилацетатом (20 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: н-гексан:этилацетат в соотношении 1:1) с получением бледно-желтого твердого вещества (140 мг). Выход: 52,6%. МС (ИЭР, m/z): [M+H]+: 267,1; 1Н-ЯМР (300 МГц, CD3OD): 8.01-8.00 (d, 1Н, J=2,1 Гц), 6.78-6.77 (d, 1Н, J=2,1 Гц), 4.24-2.22 (m, 1Н), 3.07-3.03 (m, 1Н), 1.91-1.66 (m, 8Н).
Стадия 2: получение N-(цис-4-((2-хлор-фуро[3,2-d]пиримидин-4-ил)амино)циклогексил)акриламида
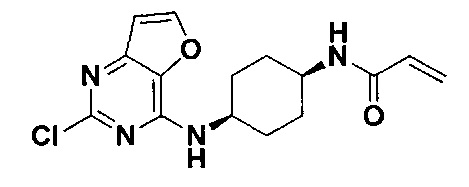
Продукт, полученный на стадии 1 (120 мг, 0,45 ммоль), и триэтиламин (188 мкл, 1,36 ммоль) растворяли в дихлорметане (20 мл) с последующим добавлением акрилоилхлорида (53 мкл, 0,54 ммоль). Реакционный раствор выдерживали при комнатной температуре в течение ночи. После концентрирования остаток очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением оранжевого твердого вещества (0,13 г). Выход: 90,3%. МС (ИЭР, m/z): [M+H]+: 321,1; 1Н-ЯМР (300 МГц, DMCO-d6): 8.24-8.21 (d, 1Н, J=6,3 Гц), 7.99-7.97 (d, 1Н, J=6,3 Гц), 6.41-6.32 (dd, 2Н, J=10,2 Гц, J=17,1 Гц), 5.68-5.64 (dd, 1Н, J=2,4 Гц, J=17,1 Гц), 5.59-5.55 (dd, 1Н, J=2,1 Гц, J=10,2 Гц), 4.11-4.09 (m, 1Н), 3.09-3.05 (m, 1Н), 1.81-1.61 (m, 8Н).
Стадия 3: получение N-(цис-4-((2-((1-метил-1Н-пиразол-4-ил)амино)фуро[3,2-d]пиримидин-4-ил)амино)циклогексил)акриламида
Продукт, полученный на стадии 2 (25 мг, 0,078 ммоль), и 1-метил-1Н-пиразол-4-амин (8,4 мг, 0,086 ммоль) растворяли в изопропаноле (2 мл) с последующим добавлением трифторуксусной кислоты (250 мг, 2,2 ммоль). Реакционный раствор подвергали взаимодействию при 90°C при микроволновом излучении в течение 1 часа. Реакционный раствор охлаждали до комнатной температуры, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением коричневого твердого вещества (10 мг). Выход: 33,7%. МС (ИЭР, m/z): [M+H]+: 382,2; 1Н-ЯМР (300 МГц, CD3OD) δ: 7.94-7.93 (d, 1Н, J=2,1 Гц), 7.86 (s, 1Н), 7.60 (s, 1Н), 6.76-6.75 (d, 1Н, J=2,1 Гц), 6.44-6.35 (t, 1Н, J=10,2 Гц, J=17,1 Гц), 6.26-6.20 (dd, 1Н, J=2,1 Гц, J=17,1 Гц), 5.67-5.63 (dd, 1Н, J=2,1 Гц, J=10,2 Гц), 4.23-4.21 (m, 1Н), 4.02-4.01 (m, 1Н), 3.90 (s, 3H), 1.90-1.74 (m, 8Н).
Пример 58
Получение N-(цис-4-((2-((1-метил-1H-пиразол-4-ил)амино)-5Н-пирроло[3,2-d]пиримидин-4-ил)амино)циклогексил)акриламида
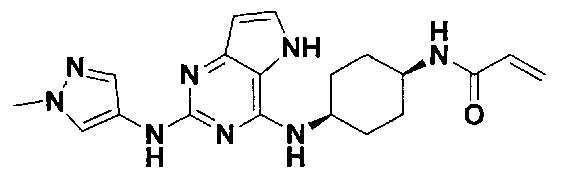
Стадия 1: получение цис-N1-(2-хлор-5Н-пирроло[3,2-d]пиримидин-4-ил)циклогексил-1,4-диамина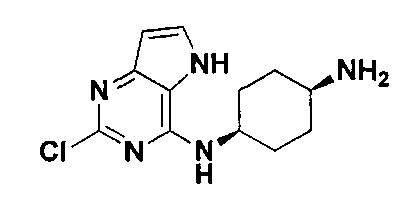
2,4-Дихлор-пирроло[3,2-d]пиримидин (187 мг, 1 ммоль) растворяли в дихлорметане (5 мл) и затем добавляли по каплям к раствору цис-1,4-циклогексилдиамина (456 мг, 4,0 ммоль) в дихлорметане (10 мл). Реакционный раствор перемешивали при комнатной температуре в течение ночи и затем концентрировали. К остатку добавляли воду (20 мл) и экстрагировали этилацетатом (10 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: н-гексан:этилацетат в соотношении 1:1) с получением бледно-желтого твердого вещества (150 мг). Выход: 56,6%. МС (ИЭР, m/z): [M+H]+: 266,1; 1Н-ЯМР (300 МГц, CD3OD): 7.41-7.40 (d, 1Н, J=3,0 Гц), 6.62-8.61 (d, 1Н, J=3,0 Гц), 4.31 (s, 1Н), 3.09 (s, 1Н), 2.01-1.70 (m, 8Н).
Стадия 2: получение N-(цис-4-((2-хлор-5H-пирроло[3,2-d]пиридин-4-ил)амино)циклогексил)акриламида
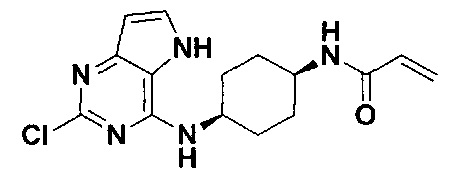
Продукт, полученный на стадии 1 (120 мг, 0,45 ммоль), и триэтиламин (188 мкл, 1,36 ммоль) растворяли в дихлорметане (20 мл) с последующим добавлением акрилоилхлорида (53 мкл, 0,54 ммоль). Реакционный раствор подвергали взаимодействию при комнатной температуре в течение ночи. После концентрирования остаток очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением бледно-желтого твердого вещества (0,1 г). Выход: 69,7%. МС (ИЭР, m/z): [M+H]+: 320,1; 1Н-ЯМР (300 МГц, CDCl3): 7.40-7.38 (d, 1Н, J=7,8 Гц), 7.29-7.21 (m, 1Н), 6.73-6.70 (d, 1Н, J=7,8 Гц), 6.24-6.20 (m, 1Н), 5.57-5.53 (m, 1Н), 4.41 (s, 1Н), 3.97 (s, 1Н), 1.84-1.72 (m, 8Н).
Стадия 3: получение N-(цис-4-((2-((1-метил-1H-пиразол-4-ил)амино)-5Н-пирроло[3,2-d]пиримидин-4-ил)амино)циклогексил)акриламида
Продукт, полученный на стадии 2 (25 мг, 0,078 ммоль), и 1-метил-1Н-пиразол-4-амин (8,4 мг, 0,086 ммоль) растворяли в изопропаноле (2 мл) с последующим добавлением трифторуксусной кислоты (250 мг, 2,2 ммоль). Реакционный раствор подвергали взаимодействию при 90°C при микроволновом излучении в течение 1 часа. Реакционный раствор охлаждали до комнатной температуры, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением коричневого твердого вещества (12 мг). Выход: 40,5%. МС (ИЭР, m/z): [M+H]+: 381,2; 1Н-ЯМР (300 МГц, CD3OD) δ: 7.86 (s, 1Н), 7.64 (s, 1Н), 7.43 (s, 1Н), 6.43-6.34 (m, 1Н), 6.29-6.21 (m, 1Н), 5.69-5.65 (m, 1Н), 4.46-4.35 (m, 1Н), 4.01-4.95 (m, 1Н), 3.94 (s, 3H), 1.99-1.61 (m, 8Н).
Пример 59
Получение N-(цис-4-((2-((1-метил-1H-пиразол-4-ил)амино)-тиено[2,3-d]пиримидин-4-ил)амино)циклогексил)акриламида

Стадия 1: получение трет-бутил-(цис-4-((2-хлор-тиено[2,3-d]пиримидин-4-ил)амино)циклогексил)карбамата

2,4-Дихлор-тиено[2,3-d]пиримидин (204 мг, 1 ммоль) и трет-бутил-цис-4-амино-циклогексилкарбамат (215 мг, 1 ммоль) растворяли в тетрагидрофуране (10 мл) с последующим добавлением N,N-диизопропилэтиламина (0,4 мл, 2 ммоль). Реакционный раствор выдерживали при 70°C в течение ночи и затем концентрировали. К остатку добавляли воду (20 мл) и экстрагировали этилацетатом (20 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: н-гексан:этилацетат в соотношении 1:5) с получением бледно-желтого твердого вещества (150 мг). Выход: 56,6%. МС (ИЭР, m/z): [M+H]+: 383,1; 1Н-ЯМР (300 МГц, DMCO-d6): 7.74-7.72 (d, 1Н, J=6,0 Гц), 7.58-7.56 (d, 1Н, J=6,0 Гц), 4.03 (s, 1Н), 3.46 (m, 1Н), 1.81-1.55 (m, 8Н), 1.40 (s, 9Н).
Стадия 2: получение N-(цис-4-((2-хлор-тиено[2,3-d]пиримидин-4-ил)амино)циклогексил)акриламида

Продукт, полученный на стадии 1 (50 мг, 0,13 ммоль), растворяли в метаноле (2 мл) с последующим добавлением 4 н. раствора хлористого водорода в 1,4-диоксане (4 мл, 1 ммоль). Реакционный раствор выдерживали при комнатной температуре в течение 2 часов. Реакционный раствор концентрировали и оставшуюся вязкую жидкость растворяли в дихлорметане (5 мл) с последующим добавлением триэтиламина (54 мкл, 0,39 ммоль). К вышеуказанному раствору добавляли по каплям при 0°C акрилоилхлорид (14 мкл, 0,14 ммоль). Реакционный раствор подвергали взаимодействию при комнатной температуре в течение ночи. Реакционный раствор промывали водой (10 мл) и органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 8:1) с получением белого твердого вещества (40 мг). Выход: 91,5%. МС (ИЭР, m/z): [M+H]+: 337,1; 1Н-ЯМР (300 МГц, DMCO-d6): 7.75-7.73 (d, 1Н, J=6,0 Гц), 7.57-7.55 (d, 1Н, J=6,0 Гц), 6.38-6.29 (dd, 1Н, J=10,2 Гц, J=17,1 Гц), 6.11-6.04 (dd, 1Н, J=2,4 Гц, J=17,1 Гц), 5.57-5.53 (dd, 1Н, J=2,1 Гц, J=10,2 Гц), 4.05-4.03 (m, 1Н), 3.09-3.05 (m, 1Н), 1.97-1.61 (m, 8Н).
Стадия 3: получение N-(цис-4-((2-((1-метил-1H-пиразол-4-ил)амино)тиено[2,3-d]пиримидин-4-ил)амино)циклогексил)акриламида
Продукт, полученный на стадии 2 (25 мг, 0,078 ммоль), и 1-метил-1Н-пиразол-4-амин (8,4 мг, 0,086 ммоль) растворяли в изопропаноле (2 мл) с последующим добавлением трифторуксусной кислоты (250 мг, 2,2 ммоль). Реакционный раствор подвергали взаимодействию при 90°C при микроволновом излучении в течение 1 часа. Реакционный раствор охлаждали до комнатной температуры, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением коричневого твердого вещества (10 мг). Выход: 33,7%. МС (ИЭР, m/z): [M+H]+: 398,3; 1Н-ЯМР (300 МГц, DMCO-d6) δ: 10.51 (s, 1Н), 9.08 (s, 1Н), 8.20 (d, 1Н, J=5,1 Гц), 8.02 (d, 1Н, J=6,0 Гц), 7.87 (s, 1Н), 7.57 (s, 1Н), 7.21 (d, 1Н, J=5,4 Гц), 6.32-8.41 (m, 1Н), 6.07 (dd, 1Н, J=2,1 Гц, J=17,1 Гц), 5.57 (dd, 1H, J=2,4 Гц, J=9,9 Гц), 4.14 (d, 1H, J=5,4 Гц), 3.84 (s, 3H), 1.25-1.64 (m, 8H).
Пример 60
Получение N-(цис-4-((2-((1-метил-1H-пиразол-4-ил)амино)тиено[3,2-d]пиримидин-4-ил)амино)циклогексил)пропанамида

Стадия 1: получение трет-бутил-(цис-4-((2-((1-метил-1Н-пиразол-4-ил)амино)тиено[3,2-d]пиримидин-4-ил)амино)циклогексил)карбамата
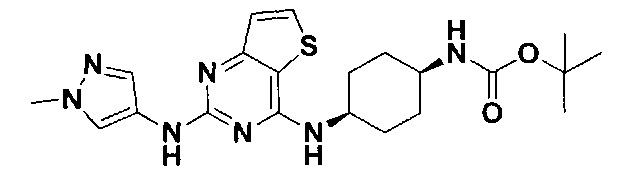
Продукт, полученный на стадии 1 Примера 1 (120 мг, 0,31 ммоль), и 1-метил-1Н-пиразол-4-амин (52 мг, 0,62 ммоль) суспендировали в изопропаноле (2 мл) с последующим добавлением двух капель трифторуксусной кислоты. Эту смесь подвергали взаимодействию в течение 25 минут при микроволновом излучении при температуре 90°C. К этой системе добавляли насыщенный раствор карбоната натрия и значение pH реакционного раствора доводили до примерно 8. Реакционную смесь концентрировали и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан:метанол в соотношении 20:1) с получением желтого твердого вещества (120 мг). Выход: 87,4%. МС (ИЭР, m/z): [M+H]+: 444,3.
Стадия 2: получение N4-(цис-4-аминоциклогексил)-N2-(1-метил-1H-пиразол-4-ил)тиено[3,2-d]пиримидин-2,4-диамина

Продукт, полученный на вышеуказанной стадии 1 (120 мг, 0,27 ммоль), растворяли в дихлорметане (10 мл) с последующим капельным добавлением 4 н. раствора хлористого водорода в 1,4-диоксане (675 мкл, 2,7 ммоль). Реакционный раствор подвергали взаимодействию при комнатной температуре в течение 2 часов. Реакционный раствор концентрировали и полученный неочищенный продукт использовали непосредственно на следующей стадии без дополнительной очистки. МС (ИЭР, m/z): [M+H]+: 344,2.
Стадия 3: получение N-(цис-4-((2-((1-метил-1H-пиразол-4-ил)амино)тиено[3,2-d]пиримидин-4-ил)амино)циклогексил)пропинамида
Продукт, полученный на стадии 2 (38 мг, 0,10 ммоль), и пропионовую кислоту (8,4 мг, 0,12 ммоль) растворяли в тетрагидрофуране (10 мл) с последующим добавлением N,N-диизопропилэтиламина (53 мкл). Эту смесь перемешивали при комнатной температуре в течение 30 минут с последующим добавлением TBTU (4 мг). Смесь перемешивали при комнатной температуре в течение ночи, концентрировали и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением бледно-желтого твердого вещества (2,45 мг). Выход: 6,2%. МС (ИЭР, m/z): [M+H]+: 396,2; 1Н-ЯМР (300 МГц, CD3OD) δ: 7.93 (d, 1Н, J=5,4 Гц), 7.85 (s, 1Н), 7.61 (s, 1Н), 7.16 (d, 1Н, J=5,4 Гц), 3.91 (s, 3H), 3.54-3.61 (m, 2Н), 1.74-2.01 (m, 8Н).
Пример 61
Получение 1-(3-(((2-((1-метил-1Н-пиразол-4-ил)амино)тиено[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
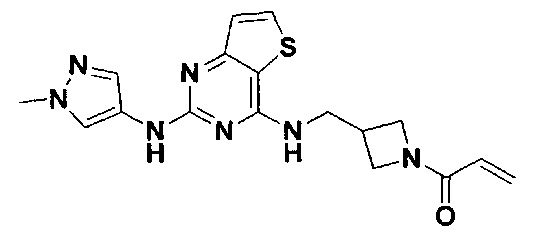
Стадия 1: получение трет-бутил-3-(((2-хлор-тиено[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-карбоксилата

2,4-Дихлор-тиено[3,2-d]пиримидин (205 мг, 1 ммоль) и трет-бутил-3-(аминометил)азетидин-1-карбоксилат (186 мг, 1 ммоль) растворяли в тетрагидрофуране (5 мл) с последующим добавлением N,N-диизопропилэтиламина (258 мг, 2 ммоль). Реакционный раствор подвергали взаимодействию при 70°C в течение ночи и затем концентрировали. К остатку добавляли воду (20 мл) и экстрагировали этилацетатом (10 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: н-гексан:этилацетат в соотношении 5:1) с получением белого твердого вещества (340 мг). Выход: 96,0%. МС (ИЭР, m/z): [M+H]+: 355,1; 1Н-ЯМР (300 МГц, CDCl3): 7.76 (d, 1Н, J=5,4 Гц), 7.37 (d, 1Н, J=5,4 Гц), 5.49 (s, 1Н), 4.05-4.09 (m, 2Н), 3.87-3.91 (m, 2Н), 3.71-3.75 (m, 2Н), 2.94 (m, 1Н), 1.44 (s, 9Н).
Стадия 2: получение N-(азетидин-3-илметил)-2-хлор-тиено[3,2-d]пиримидин-4-амина

Продукт, полученный на стадии 1 (340 мг, 0,96 ммоль), растворяли в дихлорметане (10 мл) с последующим добавлением 4 н. раствора хлористого водорода в 1,4-диоксане (2,5 мл, 10 ммоль). Реакционный раствор подвергали взаимодействию при комнатной температуре в течение 2 часов. Реакционный раствор концентрировали и полученный неочищенный продукт использовали непосредственно на следующей стадии без дополнительной очистки. МС (ИЭР, m/z): [M+H]+: 254,9.
Стадия 3: получение 1-(3-(((2-хлор-тиено[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
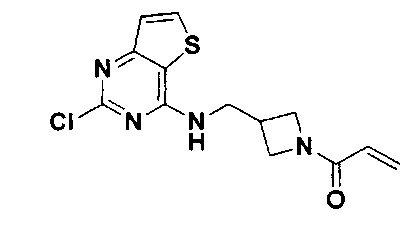
Продукт, полученный на стадии 2 (1,22 г, 4,80 ммоль), растворяли в дихлорметане (10 мл) с последующим добавлением триэтиламина (0,969 г, 9,60 ммоль). К вышеуказанному раствору при 0°C добавляли по каплям раствор акрилоилхлорида (0,434 г, 4,80 ммоль), растворенного в дихлорметане (5 мл). Реакционный раствор достигал комнатной температуры в течение ночи. Реакционный раствор промывали водой (10 мл), органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 70:1), с получением белого твердого вещества (1,00 г). Выход: 67,6%. [M+H]+: 309,0; 1Н-ЯМР (300 МГц, DMCO-d6): 8.50-8.53 (m, 1Н), 8.19 (d, 1Н, J=5,1 Гц), 7.35 (d, 1Н, J=5,4 Гц), 6.25-6.34 (m, 1Н), 6.05-6.12 (m, 1Н), 5.63-5.68 (m, 1Н), 4.27-4.33 (m, 1Н), 3.97-4.03 (m, 2Н), 3.67-3.75 (m, 3H), 2.89-2.98 (m, 1Н).
Стадия 4: получение 1-(3-(((2-((1-метил-1H-пиразол-4-ил)амино)тиено[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
Продукт, полученный на стадии 3 (50 мг, 0,162 ммоль), и 1-метил-1Н-пиразол-4-амин (23 мг, 0,244 ммоль) растворяли в 1,4-диоксане (2 мл). Значение pH реакционного раствора доводили до 5 с использованием трифторуксусной кислоты. Реакционный раствор подвергали взаимодействию при 90°C при микроволновом излучении в течение 0,5 часа. Реакционный раствор охлаждали до комнатной температуры, значение pH доводили 1 н. раствором гидроксида натрия до pH 8 и экстрагировали этилацетатом (10 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением желтого твердого вещества (15 мг). Выход: 25,4%. МС (ИЭР, m/z): [M+H]+: 370,2; 1Н-ЯМР (300 МГц, DMCO-d6) δ: 7.83 (s, 1Н), 7.60 (d, 1Н, J=5,4 Гц), 7.52 (s, 1Н), 7.18 (d, 1Н, J=5,4 Гц), 7.12 (s, 1Н), 6.31-6.37 (m, 1Н), 6.13-6.22 (m, 1Н), 5.65-5.69 (m, 1Н), 5.53 (s, 1Н), 4.01-4.35 (m, 3H), 3.81-3.93 (m, 6Н), 3.07 (m, 1Н).
Следующие соединения (в таблице 2) получали из аналогичных исходных материалов с использованием методов синтеза, аналогичных описанным в Примере 61.
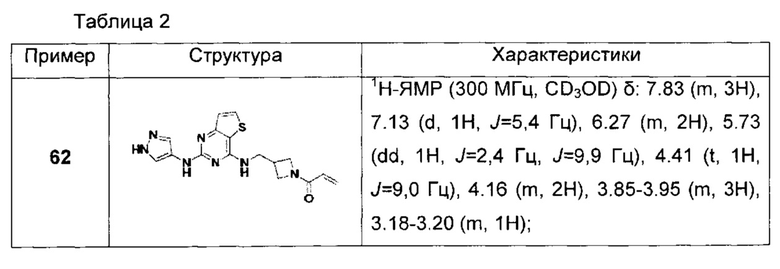
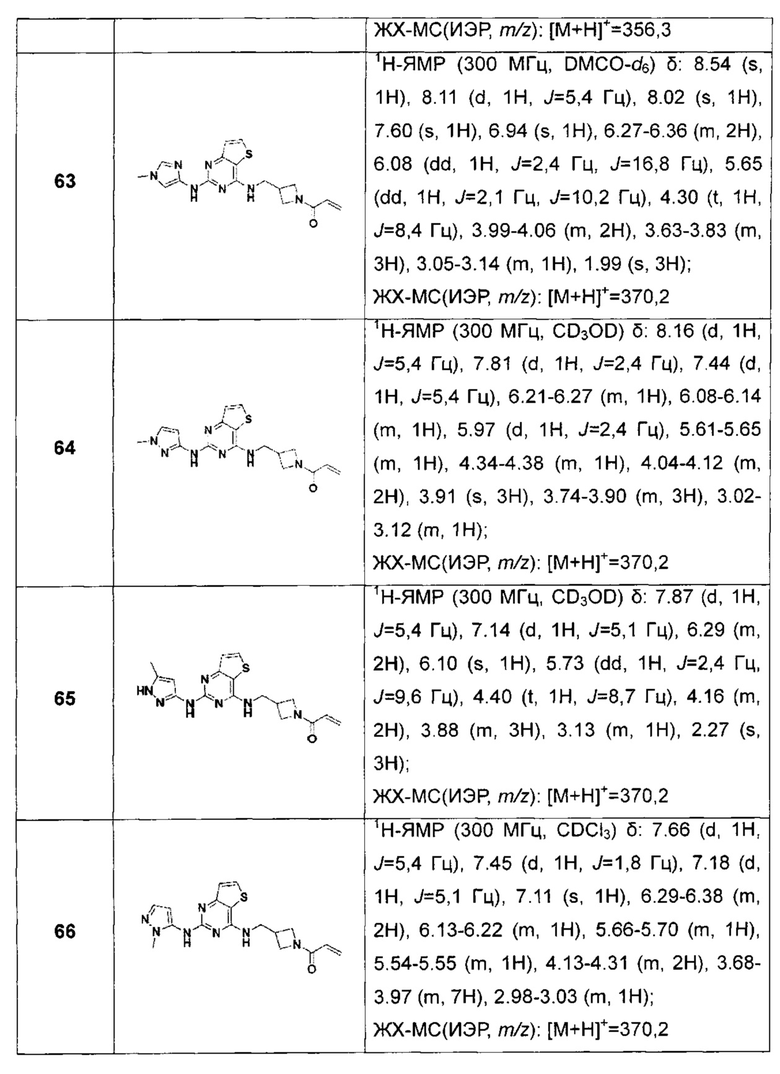

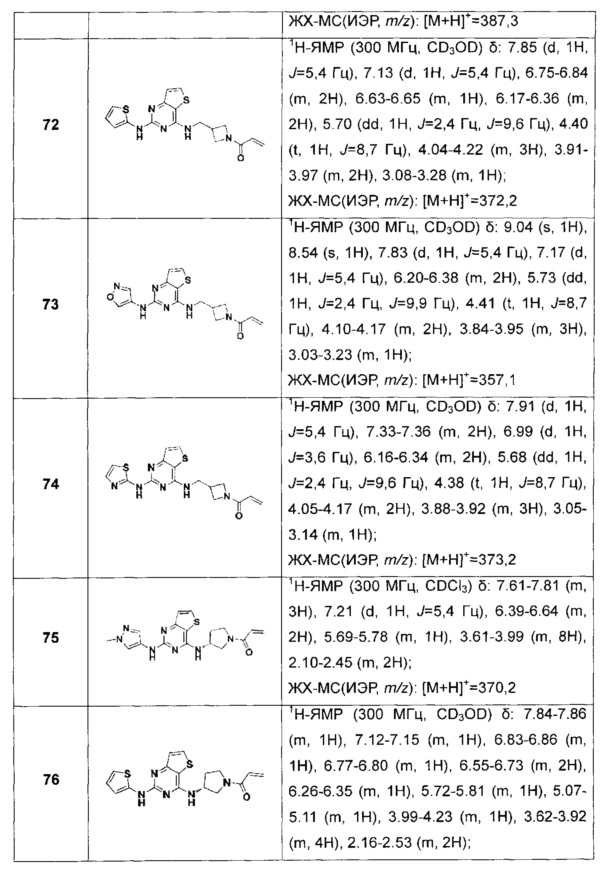
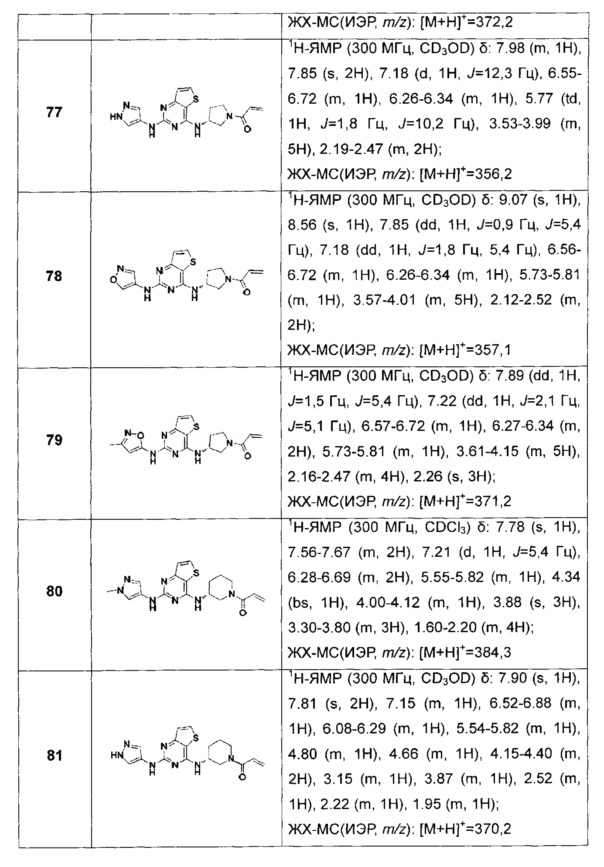
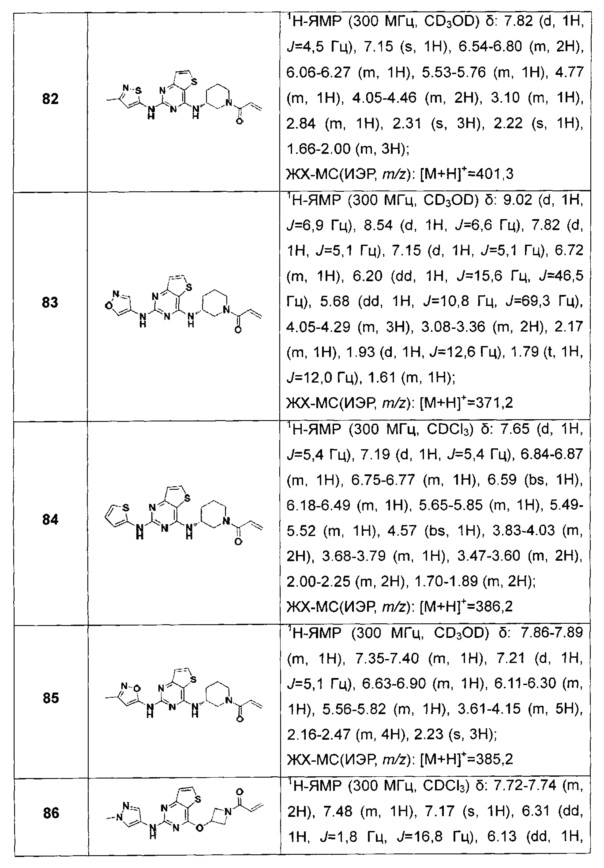
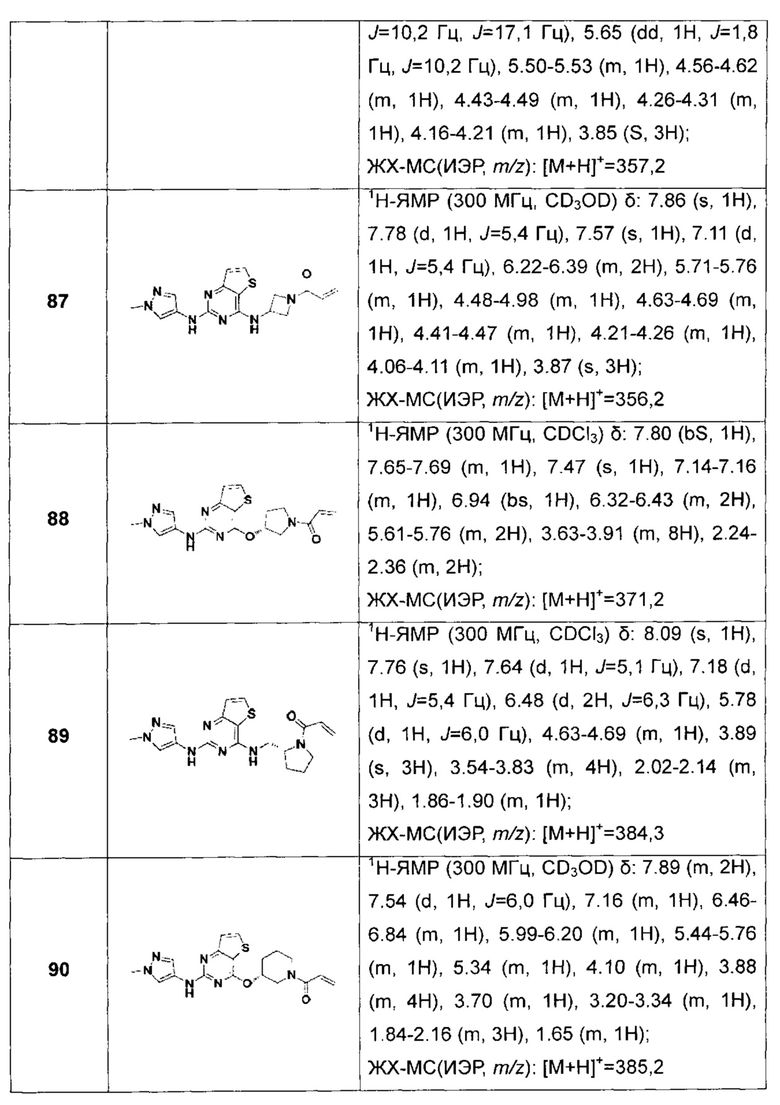
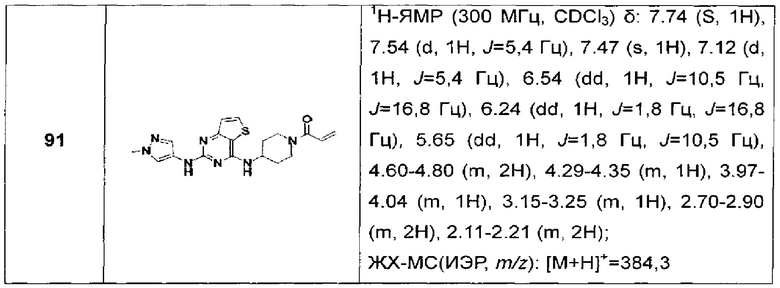
Пример 92
Получение 1-(3-(((2-((1-метил-1H-пиразол-4-ил)амино)фуро[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она

Стадия 1: получение трет-бутил-3-(((2-хлор-фуро[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-карбоксилата

2,4-Дихлор-фуро[3,2-d]пиримидин (189 мг, 1 ммоль) и трет-бутил-3-(аминометил)азетидин-1-карбоксилат (186 мг, 1 ммоль) растворяли в тетрагидрофуране (20 мл) с последующим добавлением N,N-диизопропилэтиламина (258 мг, 2 ммоль). Реакционный раствор подвергали взаимодействию при кипячении с обратным холодильником в течение ночи, затем охлаждали до комнатной температуры и концентрировали. К остатку добавляли воду (20 мл) и экстрагировали этилацетатом (10 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: н-гексан:этилацетат в соотношении 6:1) с получением белого твердого вещества (283 мг). Выход: 83,5%. МС (ИЭР, m/z): [M+H]+: 339,1.
Стадия 2: получение N-(азетидин-3-илметил)-2-хлор-фуро[3,2-d]пиримидин-4-амина
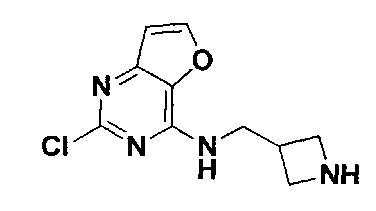
Соединение, полученное на стадии 1 (283 мг, 0,84 ммоль), растворяли в дихлорметане (2 мл) с последующим медленным капельным добавлением раствора трифторуксусной кислоты (1,43 г, 12,5 ммоль) в метиленхлориде (1 мл) в ледяной бане. Реакционный раствор подвергали взаимодействию при комнатной температуре в течение 1 часа и затем концентрировали. Полученный неочищенный продукт использовали непосредственно на следующей стадии без дополнительной очистки. МС (ИЭР, m/z): [M+H]+: 238,9.
Стадия 3: получение 1-(3-(((2-хлор-фуро[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она

Продукт, полученный на стадии 2 (0,84 ммоль), растворяли в дихлорметане (10 мл) с последующим добавлением триэтиламина (254 мг, 2,51 ммоль). К указанному выше раствору в ледяной бане добавляли по каплям раствор акрилоилхлорида (83,1 мг, 0,92 ммоль), растворенного в дихлорметане (5 мл). Реакционный раствор подвергали взаимодействию при комнатной температуре в течение ночи. Реакционный раствор промывали водой (10 мл), органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 70:1) с получением белого твердого вещества (176 мг). Выход: 72,0%. МС (ИЭР, m/z): [M+H]+: 293,0.
Стадия 4: получение 1-(3-(((2-((1-метил-1Н-пиразол-4-ил)амино)фуро[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
Соединение, полученное на стадии 3 (29,3 мг, 0,1 ммоль), и 1-метил-1Н-пиразол-4-амин (14,6 мг, 0,15 ммоль) растворяли в изопропаноле (2 мл). Значение pH реакционного раствора доводили до 5 трифторуксусной кислотой и подвергали взаимодействию при 90°C при микроволновом излучении в течение 0,5 часа. Реакционный раствор охлаждали до комнатной температуры, значение pH доводили с использованием 1 н. раствора гидроксида натрия до pH 8 и экстрагировали этилацетатом (10 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением желтого твердого вещества (15,5 мг). Выход: 43,9%. МС (ИЭР, m/z): [M+H]+: 354,2; 1Н-ЯМР (300 МГц, DMCO-d6) δ: 7.80 (s, 1Н), 7.61 (d, 1Н, J=2,1 Гц), 7.49 (s, 1Н), 7.04 (s, 1Н), 6.66 (d, 1Н, J=1,8 Гц), 6.33 (dd, 1Н, J=1,8 Гц, J=17,1 Гц), 6.12-6.21 (m, 1Н), 5.67 (dd, 1Н, J=2,1 Гц, J=10,2 Гц), 4.00-4.35 (m, 3H), 3.87 (s, 3H), 3.79-3.92 (m, 3H), 3.01-3.06 (m, 1Н).
Следующие соединения (в таблице 3) получали из аналогичных исходных материалов с использованием методов синтеза, аналогичных описанным в Примере 92.


Пример 97
Получение 1-(3-(((2-((1-метил-1H-пиразол-4-ил)амино)-5H-пирроло[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
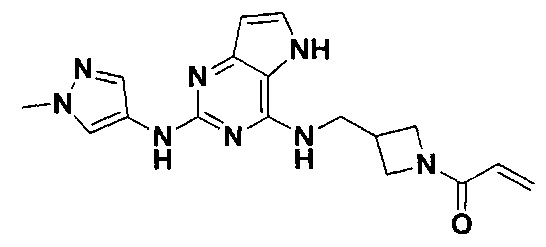
Стадия 1: получение трет-бутил-3-(((2-хлор-5H-пирроло[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-карбоксилата
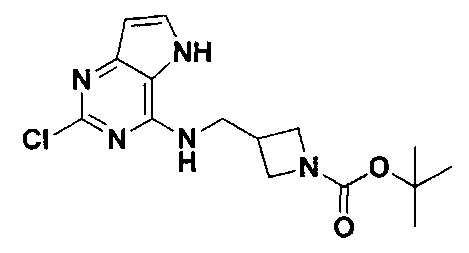
2,4-Дихлор-5Н-пирроло[3,2-d]пиримидин (360 мг, 1,92 ммоль) и трет-бутил-3-(аминометил)азетидин-1-карбоксилат (374 мг, 2,01 ммоль) растворяли в метаноле (20 мл) с последующим добавлением N,N-диизопропилэтиламина (667 мкл, 3,83 ммоль) при перемешивании при комнатной температуре. Реакционный раствор кипятили с обратным холодильником в течение 3 часов и затем концентрировали, снова растворяли в дихлорметане (50 мл), промывали водой (30 мл) и концентрировали с получением белого твердого вещества (350 мг). Выход: 51,2%. МС (ИЭР, m/z): [M+H]+: 338,2.
Стадия 2: получение 1-(3-(((2-хлор-5Н-пирроло[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
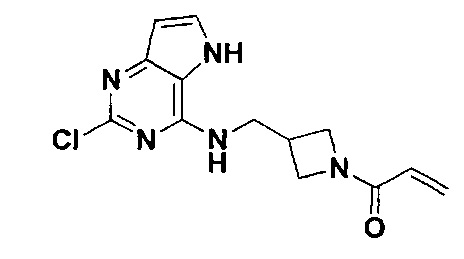
Продукт, полученный на стадии 1 (222 мг, 0,66 ммоль), растворяли в дихлорметане (5 мл) с последующим добавлением трифторуксусной кислоты (2 мл) при перемешивании при комнатной температуре. После перемешивания в течение 3 часов реакционный раствор концентрировали при пониженном давлении для удаления большей части трифторуксусной кислоты и снова растворяли в дихлорметане (30 мл). Добавляли N,N-диизопропилэтиламин (229 мкл, 1,31 ммоль) при перемешивании при комнатной температуре и затем медленно по каплям добавляли в ледяной бане раствор акрилоилхлорида (59 мкл, 0,66 ммоль) в дихлорметане (10 мл). Через 5 часов к этой реакционной системе добавляли воду (50 мл) и органическую фазу отделяли, сушили над безводным сульфатом натрия и концентрировали с получением бледно-желтого твердого вещества, которое затем очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 70:1) с получением белого твердого вещества (150 мг). Выход: 77,7%. МС (ИЭР, m/z): [M+H]+: 292,0.
Стадия 3: получение 1-(3-(((2-((1-метил-1Н-пиразол-4-ил)амино)-5Н-пирроло[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
Соединение, полученное на стадии 2 (40 мг, 0,14 ммоль), и 1-метил-1Н-пиразол-4-амин (15 мг, 0,15 ммоль) растворяли в изопропаноле (2 мл). Значение pH реакционного раствора доводили до 5 трифторуксусной кислотой и затем подвергали взаимодействию при микроволновом излучении при 90°C в течение 0,5 часа. Реакционный раствор охлаждали до комнатной температуры, значение pH доводили с использованием 1 н. раствора гидроксида натрия до pH 8 и экстрагировали этилацетатом (10 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением желтого твердого вещества (2 мг). Выход: 4,1%. МС (ИЭР, m/z): [M+H]+: 353,2; 1Н-ЯМР (300 МГц, DMCO-d6) δ: 7.52 (s, 2Н), 7.41 (s, 1Н), 6.98 (d, 1Н, J=3,0 Гц), 6.13-6.19 (m, 2Н), 5.98 (d, 1Н, J=3,0 Гц), 5.67 (dd, 1Н, J=2,4 Гц, J=9,6 Гц), 4.25-4.35 (m, 1Н), 4.04-4.08 (m, 2Н), 3.80-3.85 (m, 2Н), 3.74 (s, 3H), 3.65-3.73 (m, 1Н), 2.95-3.05 (m, 1Н).
Пример 98
Получение 1-(3-(((5-метил-2-((1-метил-1Н-пиразол-4-ил)амино)-5Н-пирроло[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она

Стадия 1: получение трет-бутил-3-(((2-хлор-5-метил-5H-пирроло[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-карбоксилата

2,4-Дихлор-5-метил-5H-пирроло[3,2-d]пиримидин (300 мг, 1,48 ммоль) и трет-бутил-3-(аминометил)азетидин-1-карбоксилат (290 мг, 1,56 ммоль) растворяли в тетрагидрофуране (10 мл) с последующим добавлением N,N-диизопропилэтиламина (258 мг, 2 ммоль). Реакционный раствор кипятили с обратным холодильником в течение ночи и затем охлаждали до комнатной температуры. Реакционный раствор концентрировали и к остатку добавляли воду (50 мл) и экстрагировали этилацетатом (20 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: н-гексан:этилацетат в соотношении 6:1) с получением бесцветной жидкости (300 мг). Выход: 50,7%. МС (ИЭР, m/z): [M+H]+: 352,2.
Стадия 2: получение 1-(3-(((2-хлор-5-метил-5H-пирроло[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
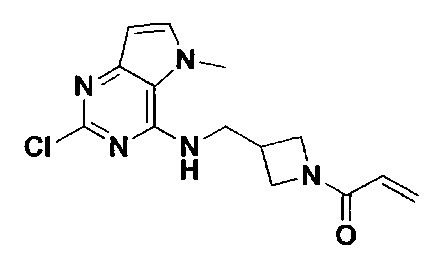
Продукт, полученный на стадии 1 (229 мг), растворяли в дихлорметане (4 мл) с последующим добавлением трифторуксусной кислоты (1,5 мл) при перемешивании при комнатной температуре. После перемешивания в течение 3 часов реакционный раствор концентрировали при пониженном давлении для удаления большей части трифторуксусной кислоты и затем снова растворяли в дихлорметане (20 мл). К этому раствору добавляли при перемешивании при комнатной температуре N,N-диизопропилэтиламин (276 мкл, 1,59 ммоль) и затем медленно по каплям добавляли раствор акрилоилхлорида (64 мкл, 0,66 ммоль) в дихлорметане (10 мл) на ледяной бане. Через 5 часов к этой реакционной системе добавляли воду (50 мл). Органическую фазу отделяли, сушили над безводным сульфатом натрия и концентрировали с получением бледно-желтого твердого вещества, которое затем очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 70:1) с получением белого твердого вещества (180 мг). Выход: 90,5%. МС (ИЭР, m/z): [M+H]+: 306,1.
Стадия 3: получение 1-(3-(((5-метил-2-((1-метил-1Н-пиразол-4-ил)амино)-5Н-пирроло[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
Соединение, полученное на стадии 2 (50 мг, 0,16 ммоль), и 1-метил-1Н-пиразол-4-амин (18 мг, 0,18 ммоль) растворяли в изопропаноле (2 мл). Значение pH реакционного раствора доводили до 5 с использованием трифторуксусной кислоты и подвергали взаимодействию при микроволновом излучении при 90°C в течение 0,5 часа. Реакционный раствор охлаждали до комнатной температуры, значение pH доводили 1 н. раствором гидроксида натрия до pH 8 и экстрагировали этилацетатом (10 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением бледно-желтого твердого вещества (3 мг). Выход: 5%. МС (ИЭР, m/z): [M+H]+: 367,3; 1Н-ЯМР (300 МГц, DMCO-d6) δ: 7.59 (d, 1Н, J=3,0 Гц), 7.54 (s, 1Н), 6.89 (d, 1Н, J=3,0 Гц), 6.77 (bs, 1Н), 6.11-6.30 (m, 3H), 5.68 (dd, 1Н, J=1,8 Гц, J=W,2 Гц), 4.31-4.37 (m, 1Н), 4.11-4.18 (m, 1Н), 3.90-4.06 (m, 5Н), 3.83 (s, 3H), 3.70-3.80 (m, 2Н), 3.05-3.17 (m, 1Н).
Пример 99
Получение 1-(3-(((2-((1-метил-1H-пиразол-4-ил)амино)тиено[2,3-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
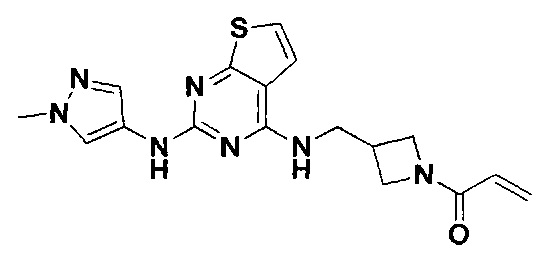
Стадия 1: получение трет-бутил-3-(((2-хлор-тиено[2,3-d]пиримидин-4-ил)амино)метил)азетидин-1-карбоксилата
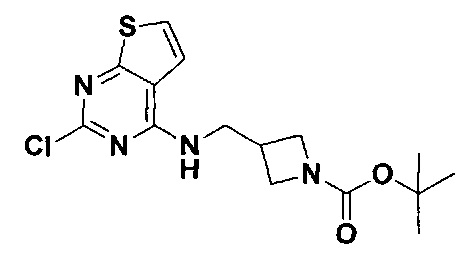
2,4-Дихлор-тиено[2,3-d]пиримидин (300 мг, 1,46 ммоль) и трет-бутил-3-(аминометил)азетидин-1-карбоксилат (272 мг, 1,46 ммоль) растворяли в тетрагидрофуране (25 мл) с последующим добавлением N,N-диизопропилэтиламина (258 мг, 2 ммоль). Реакционный раствор подвергали взаимодействию при 70°C в течение ночи и затем концентрировали. К остатку добавляли воду (50 мл) и экстрагировали этилацетатом (20 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: н-гексан:этилацетат в соотношении 1:5) с получением белого твердого вещества (425 мг). Выход: 81,9%. МС (ИЭР, m/z): [M+H]+: 355,2.
Стадия 2: получение 1-(3-(((2-хлор-тиено[2,3-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она

Продукт, полученный на стадии 1 (425 мг, 1,20 ммоль), растворяли в дихлорметане (10 мл) с последующим добавлением трифторуксусной кислоты (3 мл) при перемешивании при комнатной температуре. После перемешивания в течение 3 часов реакционный раствор концентрировали при пониженном давлении для удаления большей части трифторуксусной кислоты и затем снова растворяли в дихлорметане (30 мл) с последующим добавлением N,N-диизопропилэтиламина (417 мкл, 2,40 ммоль) при перемешивании при комнатной температуре. Затем медленно по каплям добавляли раствор акрилоилхлорида (140 мкл, 1,73 ммоль) в дихлорметане (20 мл) на ледяной бане. Через 5 часов к этой реакционной системе добавляли воду (50 мл) и органическую фазу отделяли, сушили над безводным сульфатом натрия и концентрировали с получением бледно-желтого твердого вещества, которое очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 70:1) с получением белого твердого вещества (300 мг). Выход: 81,1%. МС (ИЭР, m/z): [M+H]+: 309,1.
Стадия 3: получение 1-(3-(((2-((1-метил-1Н-пиразол-4-ил)амино)тиено[2,3-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
Продукт, полученный на стадии 2 (40 мг, 0,13 ммоль), 1-метил-1Н-пиразол-4-амин (19 мг, 0,19 ммоль), три(дибензилиденпропанон)дипалладий (12 мг, 0,013 ммоль), (±)-2,2'-бис(дифенилфосфино)-1,1'-бинафтил (12 мг, 0,019 ммоль) и карбонат цезия (127 мг, 0,39 ммоль) суспендировали в 1,4-диоксане (1,5 мл) с последующим добавлением воды (300 мкл). Поток аргона продували для удаления воздуха и взаимодействие осуществляли при содействии микроволн при 100°C в течение получаса. Реакционную смесь фильтровали через целит и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением желтого твердого вещества (9 мг). Выход: 18,8%. МС (ИЭР, m/z): [M+H]+: 370,2; 1Н-ЯМР (300 МГц, CDCl3) δ: 7.79 (bs, 1Н), 7.07 (s, 1Н), 6.97 (d, 1Н, J=6,0 Гц), 6.91 (s, 1Н), 6.82 (d, 1Н, J=6,0 Гц), 6.75 (bs, 1Н), 6.26 (dd, 1Н, J=1,8 Гц, J=16,8 Гц), 6.10 (dd, 1Н, J=10,2 Гц, J=16,8 Гц), 5.60 (dd, 1Н, J=1,8 Гц, J=10,2 Гц), 4.21-4.27 (m, 1Н), 4.08-4.14 (m, 1Н), 3.92-3.97 (m, 1Н), 3.78-3.86 (m, 5Н), 3.65-3.76 (m, 1Н), 2.95-3.05 (m, 1Н).
Следующие соединения (в таблице 4) получали из аналогичных исходных материалов с использованием методов синтеза, аналогичных описанным в Примере 99.
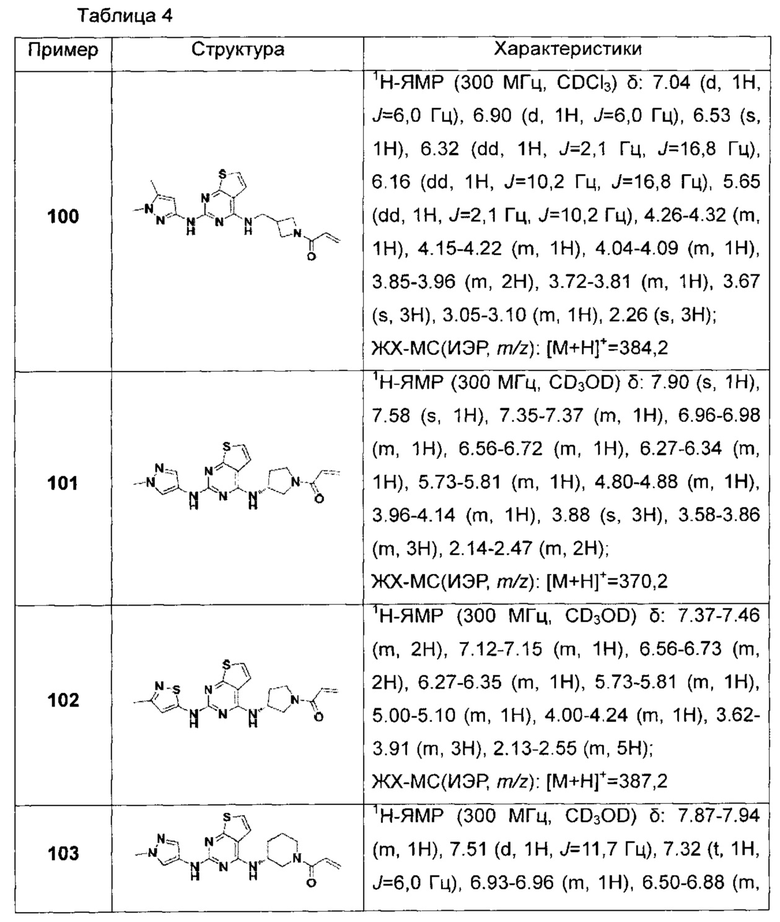
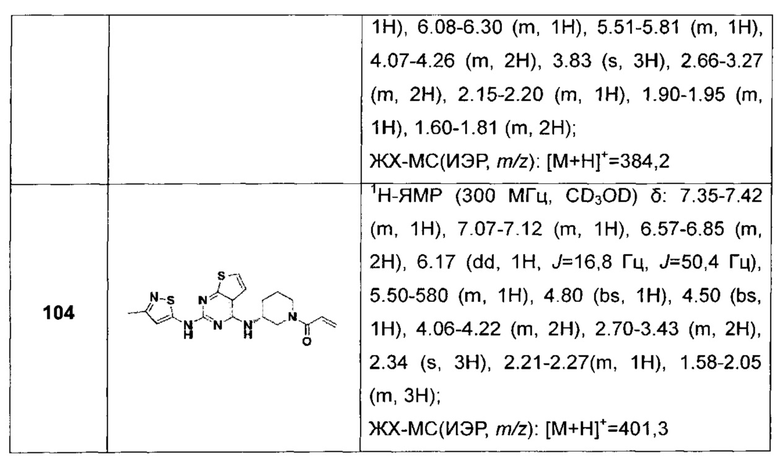
Пример 105
Получение (R)-(3-(метил(2-((1-метил-1H-пиразол-4-ил)амино)тиено[3,2-d]пиримидин-4-ил)амино)пирролидин-1-ил)проп-2-ен-1-она

Стадия 1: получение трет-бутил-(R)-3-((2-хлор-тиено[3,2-d]пиримидин-4-ил)амино)пирролидин-1-карбоксилата
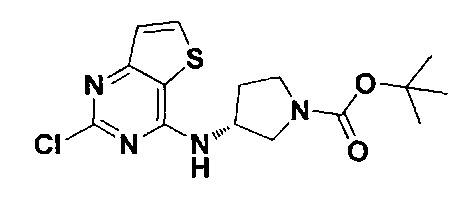
2,4-Дихлор-тиено[3,2-d]пиримидин (2,26 г, 0,011 моль) и трет-бутил-(R)-3-аминопирролидин-1-илкарбоксилат (2,25 г, 0,012 моль) растворяли в тетрагидрофуране (50 мл) с последующим добавлением N,N-диизопропилэтиламина (2,838 г, 0,022 моль). Реакционный раствор подвергали взаимодействию при 70°C в течение ночи и затем концентрировали. К остатку добавляли воду (50 мл) и экстрагировали этилацетатом (50 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: н-гексан:этилацетат в соотношении 5:1) с получением белого твердого вещества (3,8 г). Выход: 97,4%. МС (ИЭР, m/z): [M+H]+: 355,1; 1Н-ЯМР (300 МГц, DMCO-d6): 8.05 (d, 1Н, J=6,3 Гц), 8.02 (d, 1Н, J=5,4 Гц), 7.35 (d, 1Н, J=6,3 Гц), 4.60-4.48 (m, 1Н), 3.60-3.67 (m, 1Н), 3.22-3.48 (m, 3H), 2.15-2.19 (m, 1Н), 1.91-2.01 (m, 1Н), 1.40 (s, 9Н).
Стадия 2: получение (R)-2-хлор-N-(пирролидин-3-ил)тиено[3,2-d]пиримидин-4-амина
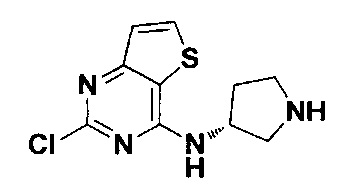
Соединение, полученное на стадии 1 (0,3 г, 0,845 ммоль), растворяли в этаноле (10 мл) с последующим добавлением 4 н. раствора хлористого водорода в 1,4-диоксане (2 мл, 8 ммоль). Реакционный раствор подвергали взаимодействию при 80°C в течение 4 часов и затем концентрировали. Полученный неочищенный продукт использовали непосредственно на следующей стадии без дополнительной очистки. МС (ИЭР, m/z): [M+H]+: 254,9.
Стадия 3: получение (R)-1-(3-((2-хлор-тиено[3,2-d]пиримидин-4-ил)амино)пирролидин-1-ил)проп-2-ен-1-она

Соединение, полученное на стадии 2 (0,497 г, 1,96 ммоль), растворяли в дихлорметане (10 мл) с последующим добавлением триэтиламина (0,396 г, 3,92 ммоль). К вышеуказанному раствору добавляли по каплям при 0°C раствор акрилоилхлорида (0,195 г, 2,15 ммоль), растворенного в дихлорметане (5 мл). Реакционный раствор подвергали взаимодействию при комнатной температуре в течение ночи и затем промывали водой (20 мл). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 70:1) с получением белого твердого вещества (0,44 г). Выход: 72,8%. МС (ИЭР, m/z): [M+H]+: 309,0; 1Н-ЯМР (300 МГц, DMCO-d6): 8.52-8.55 (m, 1Н), 8.20 (m, 1Н), 7.35 (m, 1Н), 6.52-6.67 (m, 1Н), 6.11-6.19 (m, 1H), 5.64-5.71 (m, 1H), 4.63-4.80 (m, 1H), 3.43-3.97 (m, 4H), 2.00-2.23 (m, 2H).
Стадия 4: получение (R)-1-(3-((2-хлор-тиено[3,2-d]пиримидин-4-ил)метил)амино)пиррол идин-1-ил)проп-2-ен-1-она

К раствору соединения, полученного на стадии 3 (100 мг, 0,32 ммоль), и гидрида натрия (60%, в минеральном масле, 39 мг, 0,97 ммоль) в тетрагидрофуране (15 мл) добавляли йодметан (24 мкл, 0,39 ммоль) и перемешивали при комнатной температуре в течение 3 часов. Реакционный раствор концентрировали и затем очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 30:1) с получением белого твердого вещества (80 мг). Выход: 76,5%. МС (ИЭР, m/z): [M+H]+: 323,1; 1Н-ЯМР (300 МГц, CDCl3): 7.79-7.82 (m, 1Н), 7.36-7.38 (m, 1Н), 6.40-6.54 (m, 1Н), 5.58-5.77 (m, 1Н), 3.81-4.03 (m, 2Н), 3.48-3.70 (m, 2Н), 3.40 (s, 3H), 2.12-2.40 (m, 2Н).
Стадия 5: получение (R)-1-(3-(метил(2-((1-метил-1Н-пиразол-4-ил)амино)тиено[3,2-с(1пиримидин-4-ил)амино)пирролидин-1-ил)проп-2-ен-1-она
Соединение, полученное на стадии 4 (40 мг, 0,12 ммоль), 1-метил-1Н-пиразол-4-амин (13 мг, 0,14 ммоль) и трифторуксусную кислоту (20 мг, 0,18 ммоль) растворяли в 2-бутаноле (1,2 мл) и осуществляли взаимодействие при микроволновом излучении при 100°C в течение 40 минут и затем очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 20:1) с получением коричневого твердого вещества (22 мг). Выход: 46,3%. МС (ИЭР, m/z): [M+H]+: 384,3; 1Н-ЯМР (300 МГц, CDCl3): δ: 7.79 (d, 1Н, J=9,9 Гц), 7.68 (d, 1Н, J=5,4 Гц), 7.50 (d, 1Н, J=5,7 Гц), 7.22 (d, 1Н, J=5,7 Гц), 6.42-6.48 (m, 2Н), 5.70-5.77 (m, 1Н), 5.47-5.56 (m, 1Н), 3.79-3.98 (m, 5Н), 3.49-3.67 (m, 2Н), 3.35 (d, 3Н, J=5,4 Гц), 2.12-2.34 (m, 2Н).
Следующие соединения (в таблице 5) получали из аналогичных исходных материалов с использованием методов синтеза, аналогичных описанным в Примере 105.

Пример 108
Получение 1-(3-(((2-((1-изопропил-1Н-пиразол-4-иламино)тиено[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она

Стадия 1: получение 1-изопропил-4-нитро-1Н-пиразола
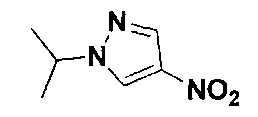
4-Нитро-1H-пиразол (226 мг, 2 ммоль) и 2-йодпропан (340 мг, 2 ммоль) растворяли в N,N-диметилформамиде (5 мл) с последующим добавлением карбоната калия (276 мг, 2 ммоль). Реакционный раствор подвергали взаимодействию при 70°C в течение 2 часов, затем вливали в воду (20 мл) и экстрагировали этилацетатом (20 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: н-гексан/этилацетат в соотношении 5:1) с получением белого твердого вещества (250 мг). Выход: 80,0%. МС (ИЭР, m/z): [M+H]+: 155,8; 1Н-ЯМР (300 МГц, CDCl3) δ: 8.16 (s, 1Н), 8.08 (s, 1Н), 4.48-4.57 (m, 1Н), 1.57 (s, 3H), 1.55 (s, 3H). Стадия 2: получение 1-изопропил-1H-пиразол-4-амина

Продукт, полученный на стадии 1 (250 мг, 1,61 ммоль), растворяли в этаноле (10 мл) с последующим добавлением палладия на углероде (25 мг) и подвергали взаимодействию в атмосфере водорода в течение 2 часов при комнатной температуре. Реакционный раствор фильтровали и концентрировали и полученный неочищенный продукт использовали непосредственно на следующей стадии. МС (ИЭР, m/z): [M+H]+: 125,9.
Стадия 3: получение 1-(3-(((2-((1-изопропил-1Н-пиразол-4-ил-амино)тиено[3,2-d]пиримидин-4-ил)амино)метил)азетидин-1-ил)проп-2-ен-1-она
Продукт, полученный на стадии 3 Примера 61 (30 мг, 0,1 ммоль), 1-изопропил-1Н-пиразол-4-амин (19 мг, 0,15 ммоль) растворяли в 1,4-диоксане (2 мл). Значение pH реакционного раствора доводили до 5 трифторуксусной кислотой и подвергали взаимодействию при микроволновом излучении при 90°C в течение 0,5 часов. Реакционный раствор охлаждали до комнатной температуры, значение pH доводили с использованием 1 н. раствора гидроксида натрия до pH 8 и экстрагировали этилацетатом (10 мл × 3). Органическую фазу сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 20:1) с получением желтого твердого вещества (15 мг). Выход: 37,8%. МС (ИЭР, m/z): [M+H]+: 398,3; 1Н-ЯМР (300 МГц, DMCO-d6) δ: 7.81 (s, 1Н), 7.64 (d, 1Н, J=5,4 Гц), 7.60 (s, 1Н), 7.20 (d, 1Н, J=5,4 Гц), 6.31-6.37 (m, 1Н), 6.13-6.22 (m, 1Н), 5.66-5.70 (m, 1Н), 4.31-4.37 (m, 1Н), 4.18-4.24 (m, 1Н), 4.00-4.05 (m, 1Н), 3.81-3.95 (m, 3H), 3.09 (m, 1Н), 1.53 (s, 3H), 1.51 (s, 3H).
Следующие соединения (в таблице 6) получали из аналогичных исходных материалов с использованием методов синтеза, аналогичных описанным в Примере 108.

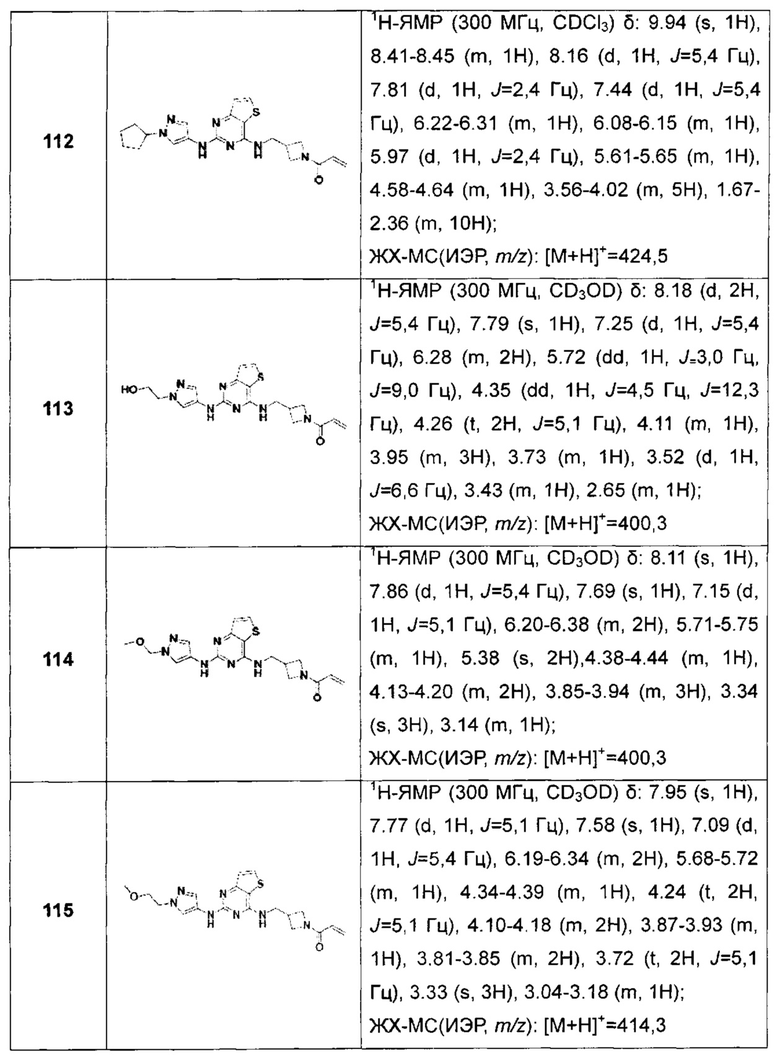
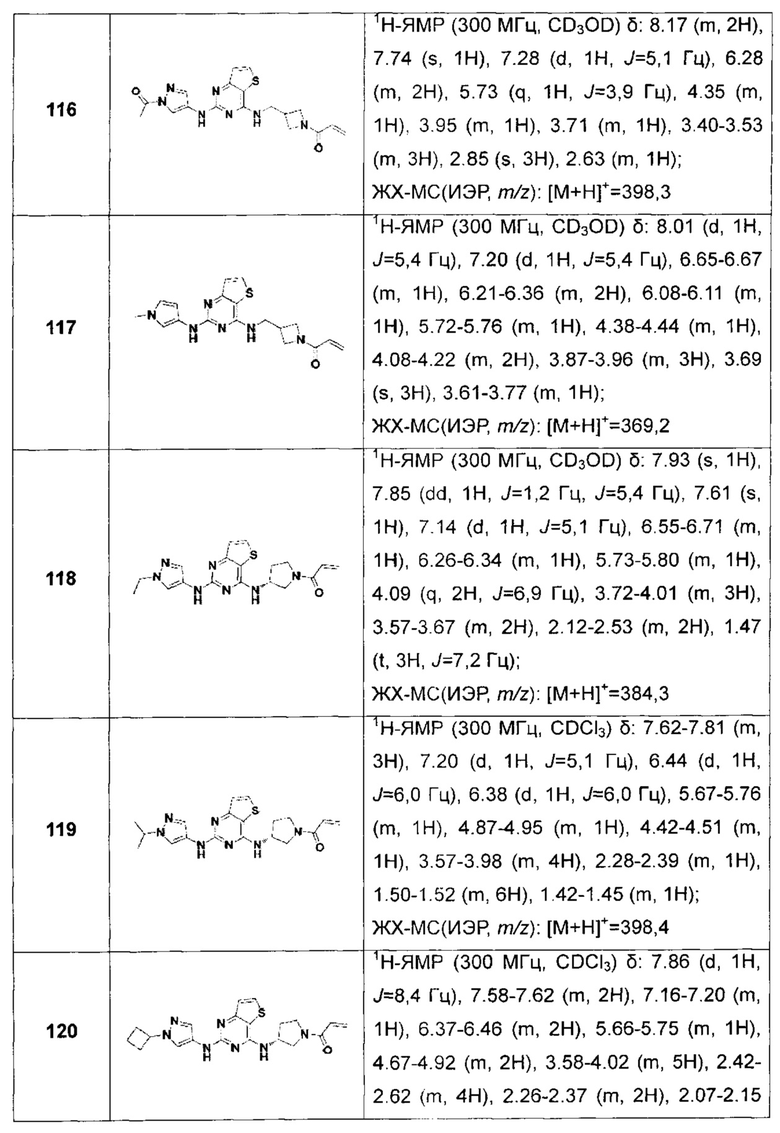

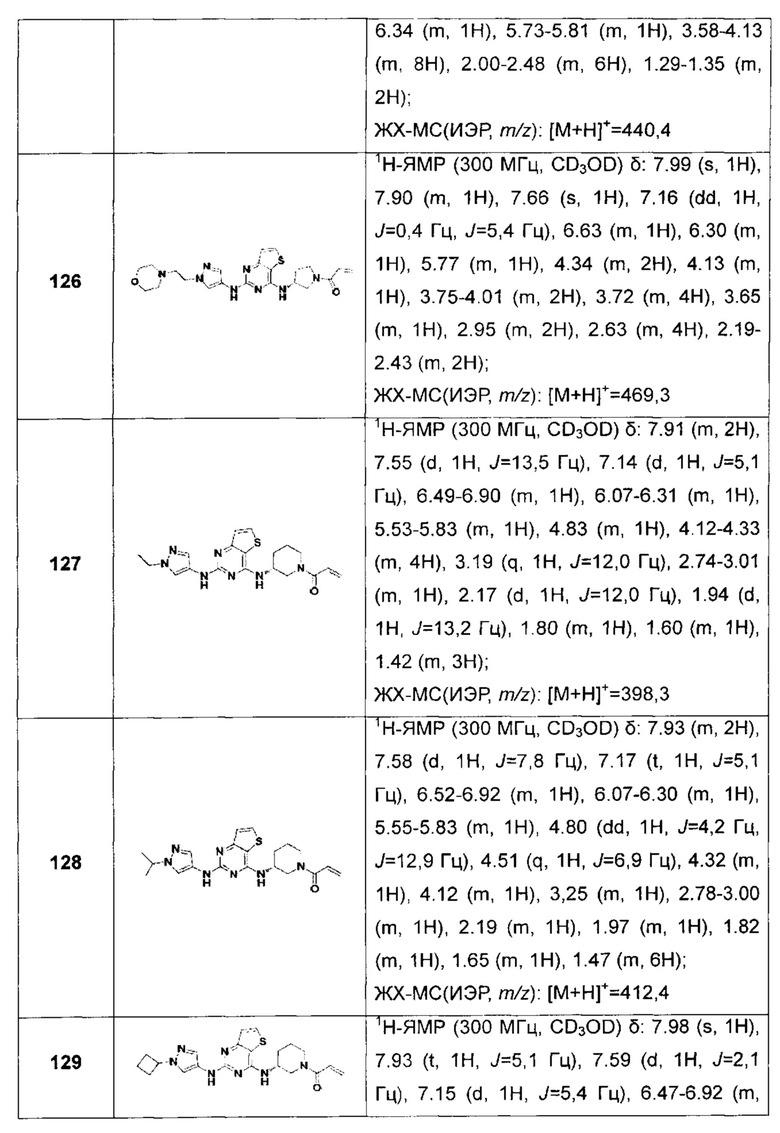

Пример 132
Получение (R)-1-(3-((2-((3-метил-изотиазол-5-ил)амино)тиено[3,2-d]пиримидин-4-ил)амино)пирролидин-1-ил)проп-2-ен-1-она

Стадия 1: получение трет-бутил-(R)-3-((2-((3-метил-изотиазол-5-ил)амино)тиено[3,2-d]пиримидин-4-ил)амино)пирролидин-1-карбоксилата
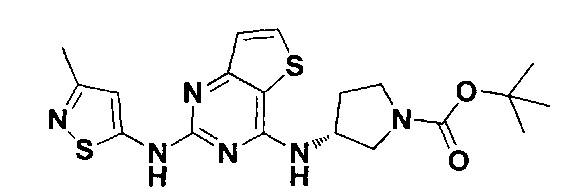
Продукт, полученный на стадии 1 Примера 105 (35,6 г, 0,1 моль), и гидрохлорид 3-метил-изотиазол-5-амина (16,3 г, 0,11 моль) растворяли в смеси 1,4-диоксан/вода (700 мл, 20:1) с последующим добавлением трис(дибензилиденпропанон)дипалладия (7,3 г, 8 ммоль), (±)-2,2'-бис(дифенилфосфино)-1,1'бинафтила (7,5 г, 12 ммоль) и карбоната цезия (130 г, 0,4 моль) в атмосфере азота и кипятили с обратным холодильником при 100°C в течение ночи. Реакционный раствор охлаждали до комнатной температуры и фильтровали через целит. Фильтрат концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан:метанол в соотношении 30:1) с получением неочищенного желтого твердого вещества (44 г). К неочищенному продукту добавляли смесь растворителей (н-гексан:дихлорметан:этилацетат в соотношении 3:1:1) (500 мл). Смесь перемешивали при 70°C в течение 1 часа, охлаждали в ледяной бане и фильтровали с получением бледно-желтого твердого вещества (35 г). Выход: 80,6%. МС (ИЭР, m/z): [M+H]+: 433,3; 1Н-ЯМР (300 МГц, COCl3) δ: 7.69 (d, 1Н, J=3,6 Гц), 7.22 (s, 1Н), 6.46 (s, 1Н), 5.00-5.30 (m, 2Н), 3.46-3.87 (m, 4Н), 2.37-2.40 (m, 4Н), 2.12 (m, 1Н), 1.84-1.86 (m, 1Н), 1.49 (s, 9Н).
Стадия 2: получение (R)-N2-(3-метил-изотиазол-5-ил)-N4-(пирролидин-3-ил)тиено[3,2-d]пиримидин-2,4-диамина

Продукт, полученный на стадии 1 (35 г, 0,081 моль), растворяли в дихлорметане (1,5 л) и добавляли для его солюбилизации метанол (1 л) с последующим добавлением 4 н. раствора хлористого водорода в 1,4-диоксане (200 мл, 0,8 моль) и затем подвергали взаимодействию при комнатной температуре в течение 2 часов. Реакционный раствор концентрировали при пониженном давлении и использовали непосредственно на следующей стадии. МС (ИЭР, m/z): [M+H]+: 333,1.
Стадия 3: получение (R)-1-(3-((2-((3-метилизотиазол-5-ил)амино)тиено[3,2-d]пиримидин-4-ил)амино)пирролидин-1-ил)проп-2-ен-1-она
Продукт, полученный на стадии 2 (26,9 г, 0,081 моль), растворяли в дихлорметане (500 мл) с последующим добавлением триэтиламина (16,36 г, 0,162 моль) в ледяной бане и затем добавляли по каплям раствор акрилоилхлорида (7,33 г, 0,081 моль) в дихлорметане (50 мл) на ледяной бане и подвергали взаимодействию при комнатной температуре в течение ночи. Реакционный раствор концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 30:1) с получением белого твердого вещества (15 г). Выход: 47,9%. МС (ИЭР, m/z): [M+H]+: 387,2; 1Н-ЯМР (300 МГц, DMCO-d6) δ: 8.06-8.14 (m, 2Н), 7.23 (s, 1Н), 6.53-6.70 (m, 2Н), 6.12-6.20 (m, 1Н), 5.64-5.72 (m, 1Н), 4.88 (s, 1Н), 3.51-4.09 (m, 4Н), 2.05-2.66 (m, 6Н).
Пример 133
Получение (R)-1-(3-((2-((3-метил-изотиазол-5-ил)амино)тиено[3,2-d]пиримидин-4-ил)амино)пирролидин-1-ил)проп-2-ин-1-она

Продукт, полученный на стадии 2 (33 мг, 0,10 ммоль), и пропионовую кислоту (8,4 мг, 0,12 ммоль) растворяли в тетрагидрофуране (10 мл) с последующим добавлением N,N-диизопропилэтиламина (53 мкл). Смесь перемешивали при комнатной температуре в течение 30 минут с последующим добавлением TBTU (4 мг), эту смесь перемешивали при комнатной температуре в течение ночи, концентрировали и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением бледно-желтого твердого вещества (6,4 мг). Выход: 16,7%. МС (ИЭР, m/z): [M+H]+: 385,2; 1Н-ЯМР (300 МГц, CD3OD) δ: 7.89-7.92 (m, 1Н), 7.22 (d, 1Н, J=5,1 Гц), 6.62 (s, 1Н), 5.04 (s, 1Н), 3.53-4.86 (m, 5Н), 2.42-2.50 (m, 1Н), 2.35 (s, 3H), 2.20-2.28 (m, 1Н).
Пример 134
Получение (R)-1-(3-((2-((3-метил-изотиазол-5-ил)амино)пирроло[2,1-f][1,2,4]триазин-4-ил)амино)пипеидин-1-ил)проп-2-ен-1-она

Стадия 1: получение трет-бутил-(R)-3-((2-хлор-пирроло[2,1-f][1,2,4]триазин-4-ил)амино)пиперидин-1-карбоксилата
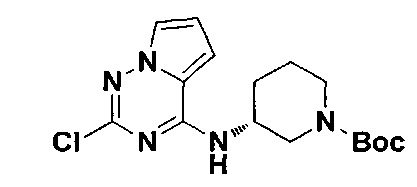
2,4-Дихлор-пирроло[2,1-f][1,2,4]триазин (325 мг, 1,73 ммоль) и (R)-1-трет-бутоксикарбонил-3-аминопиперидин (364 мг, 1,80 ммоль) растворяли в тетрагидрофуране (50 мл) с последующим добавлением N,N-диизопропилэтиламина (603 мкл, 3,46 ммоль) при перемешивании при комнатной температуре и кипятили с обратным холодильником в течение 3 часов. Реакционный раствор концентрировали, снова растворяли в дихлорметане (50 мл), промывали водой (30 мл), концентрировали и сушили над безводным сульфатом натрия с получением неочищенного продукта (640 мг). МС (ИЭР, m/z): [M+H]+: 352,2.
Стадия 2: получение (R)-1-(3-((2-хлор-пирроло[2,1-f][1,2,4]триазин-4-ил)амино)пиперидин-1-ил)проп-2-ен-1-она
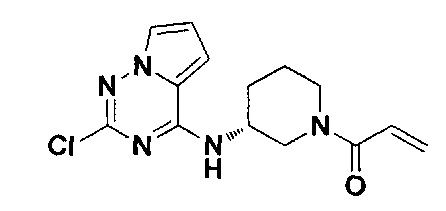
Неочищенный продукт, полученный на стадии 1 (640 мг), растворяли в дихлорметане (3 мл) с последующим добавлением трифторуксусной кислоты (1,5 мл) при перемешивании при комнатной температуре. После перемешивания в течение 3 часов реакционный раствор концентрировали при пониженном давлении для удаления большей части трифторуксусной кислоты. Остаток снова растворяли в дихлорметане (30 мл) с последующим добавлением N,N-диизопропилэтиламина (603 мкл, 3,46 ммоль) при перемешивании при комнатной температуре. Медленно по каплям добавляли раствор акрилоилхлорида (140 мкл, 1,73 ммоль) в дихлорметане (20 мл) на ледяной бане. Через 5 часов к этой реакционной системе добавляли воду (50 мл). Органическую фазу отделяли, сушили над безводным сульфатом натрия и концентрировали с получением бледно-желтого твердого вещества, которое очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 70:1) с получением белого твердого вещества (408 мг). Выход: 77,14%. МС (ИЭР, m/z): [M+H]+: 306,2.
Стадия 3: получение (R)-1-(3-((2-((3-метил-изотиазол-5-ил)амино)пирроло[2,1-f][1,2,4]триазин-4-ил)амино)пиперидин-1-ил)проп-2-ен-1-она
Продукт, полученный на стадии 2 (31 мг, 0,1 ммоль), гидрохлорид 3-метил-изотиазол-5-амина (15 мг, 0,1 ммоль), трис(дибензилиденацетон)дипалладий (9 мг, 0,01 ммоль), 4,5-бис-дифенилфосфин-9,9-диметилксантин (9 мг, 0,015 ммоль) и карбонат цезия (130 мг, 0,4 ммоль) суспендировали в 1,4-диоксане (1,5 мл) и добавляли воду (300 мкл), продували аргоном, подвергали взаимодействию при 100°C при микроволновом излучении в течение получаса. Реакционную смесь фильтровали через целит и фильтрат очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 30:1) с получением желтого твердого вещества (20 мг). Выход: 51,44%. МС (ИЭР, m/z): [M+H]+: 384,3; 1Н-ЯМР (300 МГц, CD3OD) δ: 7.43 (s, 1Н), 6.70-6.89 (m, 2Н), 6.52-6.56 (m, 2Н), 6.20 (dd, 1Н, J=16,8 Гц, J=40,2 Гц), 5.71 (dd, 1Н, J=10,8 Гц, J=55,5 Гц), 4.78-4.82 (m, 1Н), 4.08-4.46 (m, 2Н), 2.82-3.46 (m, 2Н), 2.34 (s, 3H), 2.18-2.30 (m, 1Н), 1.90-2.02 (m, 1Н), 1.60-1.85 (m, 2Н).
Следующие соединения (в таблице 7) получали из аналогичных исходных материалов с использованием методов синтеза, аналогичных описанным в Примере 134.
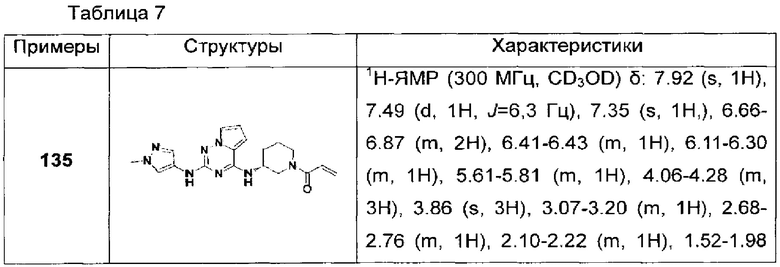
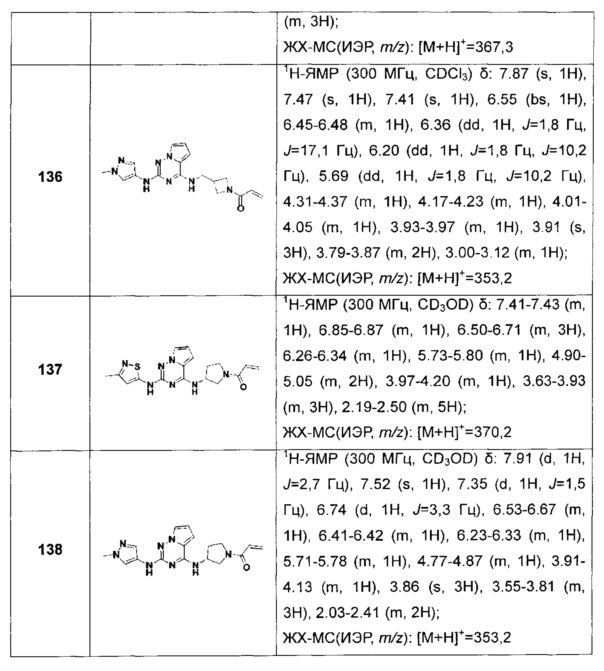
Пример 139
Получение (R)-1-(3-((2-((3-метил-изотиазол-5-ил)амино)пирроло[2,1-f][1,2,4]триазин-4-ил)амино)пиперидин-1-ил)проп-2-ин-1-она
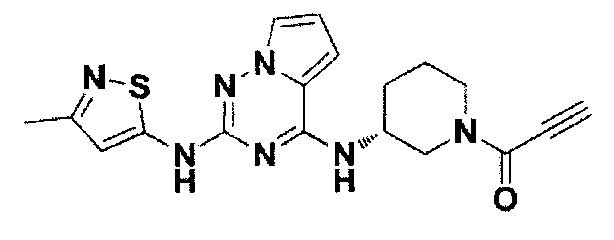
Стадия 1: получение трет-бутил-(R)-3-((2-((3-метил-изотиазол-5-ил)амино)пирроло[2,1-f][1,2,4]триазин-4-ил)амино)пиперидин-1-карбоксилата
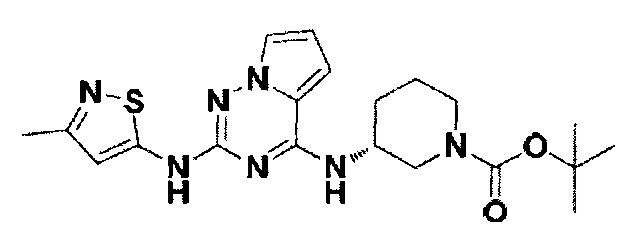
Продукт, полученный на стадии 1 Примера 134 (352 мг, 1 ммоль), и гидрохлорид 3-метил-изотиазол-5-амина (163 мг, 1,1 ммоль) растворяли в смеси 1,4-диоксан/вода (21 мл, 20:1) с последующим добавлением трис(дибензилиденпропанон)дипалладия (46 мг, 0,05 ммоль), (±)-2,2'-бис-(дифенилфосфино)-1,1'-бинафтила (63 мг, 0,1 ммоль) и карбоната цезия (650 мг, 2 ммоль) в атмосфере азота и кипятили с обратным холодильником при 100°C в течение ночи. Реакционный раствор охлаждали до комнатной температуры и фильтровали через целит. Фильтрат концентрировали при пониженном давлении и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан:метанол в соотношении 30:1) с получением бледно-желтого твердого вещества (349 мг). Выход: 81,2%. МС (ИЭР, m/z): [M+H]+: 430,2.
Стадия 2: получение (R)-N2-(3-метил-изотиазол-5-ил)-N4-(пиперидин-3-ил)пирроло[2,1-f][1,2,4]триазин-2,4-диамина
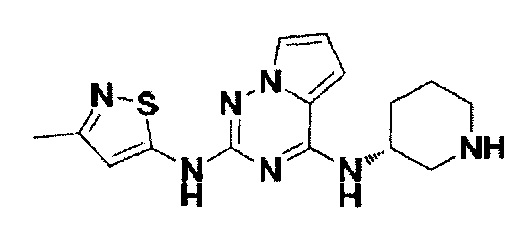
Продукт, полученный на стадии 1 (64 мг, 0,2 ммоль), растворяли в дихлорметане (15 мл) и добавляли для его солюбилизации метанол (10 мл). Затем добавляли 4 н. раствор хлористого водорода в 1,4-диоксане (0,5 мл, 2 ммоль) и смесь подвергали взаимодействию при комнатной температуре в течение 2 часов. Реакционный раствор концентрировали при пониженном давлении и использовали непосредственно на следующей стадии. МС (ИЭР, m/z): [M+H]+: 330,1.
Стадия 3: получение (R)-1-(3-((2-((3-метил-изотиазол-5-ил)амино)пирроло[2,1-f][1,2,4]триазин-4-ил)амино)пиперидин-1-ил)проп-2-ин-1-она
Продукт, полученный на стадии 2 (33 мг, 0,10 ммоль), и пропионовую кислоту (8,4 мг, 0,12 ммоль) растворяли в тетрагидрофуране (10 мл) с последующим добавлением N,N-диизопропилэтиламина (53 мкл). Смесь перемешивали при комнатной температуре в течение 30 минут, добавляли TBTU (4 мг) и затем перемешивали при комнатной температуре в течение ночи. Реакционный раствор концентрировали и очищали посредством колоночной хроматографии на силикагеле (элюент: дихлорметан/метанол в соотношении 10:1) с получением бледно-желтого твердого вещества (6,1 мг). Выход: 16,1%. МС (ИЭР, m/z): [M+H]+: 382,2.
Следующие соединения (в таблице 8) получали из аналогичных исходных материалов с использованием методов синтеза, аналогичных описанным в Примере 139.

Фармакологическая оценка
Пример тестирования 1: анализ ингибирования активности ВТК-киназы
ВТК-киназу (приобретенную в Invitrogen, No.: PV3363) разбавляли реакционным буфером (40 мМ трис-HCl, pH 7,5; 20 мМ MgCl2, 0,1 мг/мл бычьего сывороточного альбумина (BSA); 1 мМ дитиотреитол (DTT); 2 мМ MnCl2) до 2 раз от конечной концентрации (которая составляет 1,1 нг/мкл) и добавляли в количестве 5 мкл/лунку в 96-луночный планшет. Соединения по настоящему изобретению серийно разводили деионизированной водой до четырех раз (то есть, 40 мкМ, 4 мкМ, 0,4 мкМ, 80 нМ, 16 нМ, 3,2 нМ, соответственно) от конечных концентраций (10 мкМ, 1 мкМ, 0,1 мкМ, 20 нМ, 4 нМ, 0,8 нМ, соответственно) и добавляли в количестве 2,5 мкл/лунку к тестируемым лункам данного 96-луночного планшета. После инкубации при 25°C в течение 10 минут добавляли АТР (50 мкМ) (приобретенный в Promega, No.: V9102) и 0,2 мкг/мкл Poly E4Y1 (приобретенного в Sigma, No.: P0275-25MG) в количестве 2,5 мкл/лунку и инкубировали при 25°C в течение 120 минут. По завершении реакции в каждую лунку добавляли по 10 мкл реагента ADP-Glo (набор для анализа киназы ADP-Glo™, приобретенный в Promega, No.: V9102) и осуществляли реакцию при 25°C в течение 40 минут. Затем в каждую лунку добавляли по 20 мкл реагента обнаружения киназы ADP-Glo и проводили реакцию при 25°C в течение 30 минут. Активность киназы определяли посредством люминесценции с использованием набора для анализа киназы ADP-Glo в соответствии с инструкциями производителя и рассчитывали значения IC50 для соединений по настоящему изобретению. Результаты показаны в таблице 9.


В Таблице 9 показана активность выбранных соединений по настоящему изобретению в анализе ингибирования активности ВТК, где "+++" означает, что предусмотренное в нем соединение проявляет значение IC50 ≤50 нМ; "++" означает, что предусмотренное в нем соединение проявляет значение IC50 50<IC50≤100 нМ; и "+" означает, что предусмотренное в нем соединение проявляет значение IC50 100<IC50<1000 нМ.
Пример тестирования 2: анализ ингибирования активности JAK3-киназы
JAKS-киназу (приобретенную в SignalChem, No.: J03-11G) разбавляли реакционным буфером (40 мМ трис-HCl, pH 7,5; 20 мМ MgCl2, 0,1 мг/мл BSA; 1 мМ DTT) до 2 раз от конечной концентрации (которая составляет 0,5 нг/мкл) и добавляли в количестве 5 мкл/лунку в 96-луночный планшет. Соединения по настоящему изобретению серийно разводили деионизированной водой до четырех раз (то есть, 40 мкМ, 4 мкМ, 0,4 мкМ, 80 нМ, 16 нМ, 3,2 нМ, соответственно) от конечных концентраций (10 мкМ, 1 мкМ, 0,1 мкМ, 20 нМ, 4 нМ, 0,8 нМ, соответственно) и добавляли в количестве 2,5 мкл/лунку к тестируемым лункам данного 96-луночного планшета. После инкубации при 25°C в течение 10 минут добавляли 10 мкМ АТР (приобретенного в Promega, No.: V9102) и 0,2 мкг/мкл Poly E4Y1 (приобретенного в Sigma, No.: P0275-25MG) в количестве 2,5 мкл/лунку и инкубировали при 25°C в течение 60 минут. По завершении реакции в каждую лунку добавляли по 10 мкл реагента ADP-Glo (набор для анализа киназы ADP-Glo™, приобретенный в Promega, No.: V9102) и осуществляли реакцию при 25°C в течение 40 минут. Затем в каждую лунку добавляли по 20 мкл реагента обнаружения киназы ADP-Glo и проводили реакцию при 25°C в течение 30 минут. Активность киназы определяли посредством люминесценции с использованием набора для анализа киназы ADP-Glo в соответствии с инструкциями производителя и рассчитывали значения IC50 для соединений по настоящему изобретению. Результаты показаны в таблице 10.

В Таблице 10 показана активность выбранных соединений по настоящему изобретению в анализе ингибирования активности JAK3, где "+++" означает, что предусмотренное в нем соединение проявляет значение IC50≤10 нМ; "++" означает, что предусмотренное в нем соединение проявляет значение IC50 10<IC50≤100 нМ; и "+" означает, что предусмотренное в нем соединение проявляет значение IC50 100<IC50<1000 нМ.
Пример тестирования 3: анализ индуцированной интерлейкином-2 (IL-2) пролиферации клеток CTLL-2
Соединение по настоящему изобретению серийно разводили полной средой RPMI-1640 (приобретенной в Gibco, No.: 22440) до трех раз (то есть, 3 мкМ, 0,6 мкМ, 120 нМ, 24 нМ, 4,8 нМ, 0,96 нМ, соответственно) от конечных концентраций (1 мкМ, 0,2 мкМ, 40 нМ, 8 нМ, 1,6 нМ, 0,32 нМ, соответственно) и добавляли в количестве 50 мкл/лунку в тестируемые лунки 96-луночного планшета. Контрольные лунки с IL-2 (обозначали как IL-2+) (IL-2 приобрели в R & D, No.: 402-ML-020/CF) и без IL-2 (обозначали как IL-2+) (без добавления 50 мкл среды). Клетки CTLL-2 (приобретенные в АТСС, No.: TIB-214) в логарифмической фазе роста промывали буфером PBS (pH 7,2), затем ресуспендировали в полной среде RPMI-1640 без IL-2 и высевали в количестве 50000 клеток/50 мкл/лунку в 96-луночном планшете. Планшет помещали в условия 37°C, 5% CO2 и предварительно инкубировали в течение 1 часа. Затем в тестируемые лунки и контрольные лунки IL-2+добавляли полную среду RPMI-1640, содержащую IL-2 (50 мкл/лунку), в то время как в контрольную лунку IL-2- добавляли полную среду RPMI-1640 без IL-2 (50 мкл/лунку). Клетки стимулировали в течение 24 часов при 37°C и 5% CO2. После этого 96-луночный планшет извлекали из инкубатора. В каждую лунку добавляли 15 мкл реагента ССК-8 (приобретенного в DOJINDO, No.: DOJINDO-CK04) и затем планшет снова помещали в инкубатор и культивировали в течение еще 1-4 часов. Поглощение определяли при длине волны 450 нм и на основании этого рассчитывали значения IC50 соединений по настоящему изобретению. Результаты показаны в таблице 11.

В Таблице 11 показана активность выбранных соединений по настоящему изобретению в анализе пролиферации клеток CTLL-2, где "+++" означает, что предусмотренное в нем соединение проявляет значение IC50≤100 нМ; "++" означает, что предусмотренное в нем соединение проявляет значение IC50 100<IC50<1000 нМ.
Пример тестирования 4: анализ ингибирования р-ВТК и p-PCL-γ2 в клетках Ramos (вестерн-блот анализ)
Клетки Ramos (приобретенные в Beijing Union Medical College) при голодании культуры в течение 1 часа обрабатывали соединениями по настоящему изобретению в течение 1 часа и затем промывали PBS буфером (pH 7,2) для удаления соединений. Затем их ресуспендировали в 100 мкл бессывороточной культуральной среды, содержащей 1 мкМ IgM F(ab')2 против человека (приобретенного в кампании SBA, No.: 2022-01) и стимулировали на льду в течение 10 минут. Клетки промывали буфером PBS (pH 7,2) для удаления IgM и ресуспендировали в 100 мкл буфера для белкового лизиса (приобретенного в Sigma, No.: С2978), а затем готовили и отвешивали образец белка. Брали 100 мкг образца белка и загружали на полиакриламидные гели для проведения электрофореза при напряжении 200 В. По окончании электрофореза белковые блоты переносили на PVDF (поливинилиденфторидную) мембрану. Мембрану блокировали 3%-ным BSA при комнатной температуре в течение 2 часов и инкубировали в течение ночи с соответствующими антителами против р-ВТК (pY223) (приобретено в CST, No.: 5082S); против ВТК (приобретено в Abeam, No.: ab118156); против p-PLCγ2 (pY1217) (приобретено в CST, No.: 3871S); против PLCγ2 (приобретено в CST, No.: 3872S) и против β-актина (приобретено в CWBIO, No.: CW0096A)) при 4°C, а затем инкубировали со вторичным IgG антителом, конъюгированным с пероксидазой хрена (приобретенным в CWBIO. No.: CW0103A), в течение 1 часа. Экспрессию белка обнаруживали по окрашиванию с использованием ECL (электрохемилюминесцентного) субстрата (приобретенного в GE, No.: RPN2109).
Согласно вышеописанному методу было протестировано соединение 132 по настоящему изобретению. Результаты показали, что соединение 132 может значительно ингибировать экспрессии р-ВТК и p-PLCγ2 в клетках Ramos дозозависимым образом.
Результат показан на Фиг. 1.
Пример тестирования 5: модель коллаген-индуцированного артрита типа II (CIA) у мышей DBA/1J
Модель CIA является широко используемой животной моделью в исследовании лекарств для лечения ревматоидного артрита у человека. Экспериментальные животные, используемые в данном эксперименте, представляют собой мышей DBA/1J (самцы возрастом от 6 до 8 недель, приобретены в Shanghai Silaike Laboratroy Animal Co., Ltd., China). Мышей содержали в системе IVC.
Для индуцирования мышиной модели CIA, раствор бычьего коллагена типа II (СII) (приобретенного в кампании Chondrex, No.: 20022) эмульгировали в таком же объеме полного адъюванта Фрейнда (CFA) (приобретенного в Sigma-Aldrich, No.: F5881) с использованием автоматизированного гомогенизатора для получения эмульсии. Затем 70 мкл приготовленной эмульсии внутрикожно инъецировали в основание хвоста мыши в качестве первичной иммунизации. Через три недели после первичной иммунизации осуществляли одну бустерную иммунизацию. Раствор бычьего коллагена типа II эмульгировали в таком же объеме неполного адъюванта Фрейнда (IFA) (приобретенного в Sigma-Aldrich, No.: F5506) для получения эмульсии и затем 70 мкл приготовленной эмульсии внутрикожно инъецировали в основание хвоста мыши в качестве первичной иммунизации в одну точку в заднюю часть спины для завершения иммунизации. Мышей оценивали в соответствии со следующими критериями в отношении тяжести артрита с использованием установленной системы оценки по шкале от 0 до 4 (0 баллов: нет отека или припухлости; 1 балл: слабый отек или покраснение, ограниченные суставами лодыжки и предплюсны; 2 балла: слабые отек и покраснение от сустава лодыжки до предплюсны; 3 балла: умеренные отек и покраснение от сустава лодыжки до плюсневой кости; 4 балла: тяжелые отек и покраснение от лодыжки до всей плюсневой кости и пальцев стоп или анкилоз лодыжки или суставов запястья). Баллы по четырем конечностям каждой мыши складывали вместе, и наивысший балл составлял 16 (4×4).
По своим показателям оценки артрита по 5-7 мышей распределяли в каждую из трех групп: одну модельную контрольную группу и две группы введения. Лечение начинали, когда средний показатель тяжести артрита в каждой группе был равен примерно 1-2. Назначали две дозы 3 мг/кг и 10 мг/кг, которые перорально вводили один раз в сутки в течение 14 суток. Одновременно была сформирована нормальная контрольная группа. Результаты от этих тестируемых групп сравнивали с результатами от нормальной контрольной группы и модельной контрольной группы, для того чтобы определить терапевтический эффект тестируемых соединений в отношении артрита в этой модели.
При сравнении индексов тяжести артрита было подтверждено, что соединение 132 по настоящему изобретению проявляет хороший терапевтический эффект в отношении артрита в назначенных дозах в модели CIA дозозависимым образом.
Результаты показаны на Фиг. 2.
Пример тестирования 6: Модель индуцированного адъювантного артрита (AIA) у крыс
100 мг инактивированной Mycobacterium tuberculosis (приобретенной в BD Difco, No.: 231141), тщательно взвешенной и растворенной в 5 мл неполного адъюванта Фрейнда (IFA) (приобретенного в Sigma, No.: F5506) с добавленными затем 5 мл физиологического солевого раствора, гомогенно эмульгировали в 10 мг/мл полного адъюванта Фрейнда (CFA). Для индуцирования AIA крысиной модели, самцам 50 крыс Lewis в свободном от патогенной флоры (SPF) статусе (приобретенных в BeijingVital River Laboratories (VRL), номер лицензии зоотехнической ассоциации: SCXK (Beijing) 2012-0001) весом 180-200 г и находящимся на адаптивном питании в течение 7 суток инъецировали полный адъювант Фрейнда, содержащий инактивированную Mycobacterium tuberculosis (H37RA, 10 мг/мл), в дозе 0,1 мл/крысу в тыльную часть хвоста для индуцирования артрита у крыс. Одновременно, в качестве нормальной контрольной группы использовали трех неиммунизированных крыс. Крыс оценивали в отношении тяжести артрита с использованием установленной системы оценки по шкале от 0 до 4 следующим образом: 0 - нет эритемы или припухлости; 1 - легкая эритема или припухлость одного из суставов пальцев стопы; 2 - эритема или припухлость более одного из суставов пальцев стопы; 3 - припухлость суставов голеностопа и запястья; 4 - припухлость всех пальцев стопы, включая голеностопный сустав. Все четыре лапы крыс оценивали индивидуально, и наивысший балл был равен 16.
Объемы лап крыс измеряли методом дренирования с использованием плетизмометра (Plethysmometer PV-200, Chengdu Taimeng Science и Technology Co., Ltd.) с определением объемов ниже голеностопных суставов (в мл). Объемы лап крыс измеряли в каждый последующий день начиная с 10-го дня после иммунизации, то есть первый день введения. Объемы четырех конечностей каждой крысы складывали вместе и затем делили на 4 с получением средних значений. Назначали две дозы 30 мг/кг и 100 мг/кг, которые перорально вводили один раз в сутки в течение 7 суток. Одновременно были сформированы контрольная группа и модельная контрольная группа, и результаты от этих тестируемых групп сравнивали с результатами от контрольной группы и модельной контрольной группы, для того чтобы определить терапевтический эффект тестируемых соединений в отношении артрита в этой модели.
При сравнении индексов тяжести артрита было подтверждено, что соединение 132 по настоящему изобретению проявляет хороший терапевтический эффект в отношении артрита в модели AIA в назначенных дозах.
Результаты показаны на Фиг. 3.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ ТИЕНИЛ[3, 2-d]ПИРИМИДИН-4-ОН, СПОСОБ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2624021C2 |
| СОЕДИНЕНИЕ, НАЦЕЛЕННОЕ НА БЕЛОК И ЕГО ДЕГРАДАЦИЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2021 |
|
RU2829459C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА В КАЧЕСТВЕ ИНГИБИТОРОВ АКТИВАЦИИ PD1/PD-L1 | 2018 |
|
RU2783211C2 |
| Новые соединения | 2016 |
|
RU2734256C2 |
| ИНГИБИТОРЫ СЕРИН/ТРЕОНИНОВЫХ КИНАЗ | 2013 |
|
RU2650501C2 |
| ПРОИЗВОДНЫЕ ТЕТРАГИДРОНАФТАЛИНА И ТЕТРАГИДРОИЗОХИНОЛИНА В КАЧЕСТВЕ РАЗРУШИТЕЛЕЙ ЭСТРОГЕНОВОГО РЕЦЕПТОРА | 2017 |
|
RU2797244C2 |
| ПРОИЗВОДНЫЕ ПИРРОЛОПИРИМИДИНА, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ JAK-КИНАЗЫ | 2012 |
|
RU2618673C2 |
| МОДУЛЯТОРЫ ПРОТЕОЛИЗА ЭСТРОГЕНОВЫХ РЕЦЕПТОРОВ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ ПРИМЕНЕНИЯ | 2018 |
|
RU2797808C2 |
| МОДУЛЯТОРЫ ПРОТЕОЛИЗА И СООТВЕТСТВУЮЩИЕ СПОСОБЫ ПРИМЕНЕНИЯ | 2019 |
|
RU2805511C2 |
| ПРОИЗВОДНЫЕ ПИРИДИНКАРБОКСАМИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2015 |
|
RU2694899C2 |

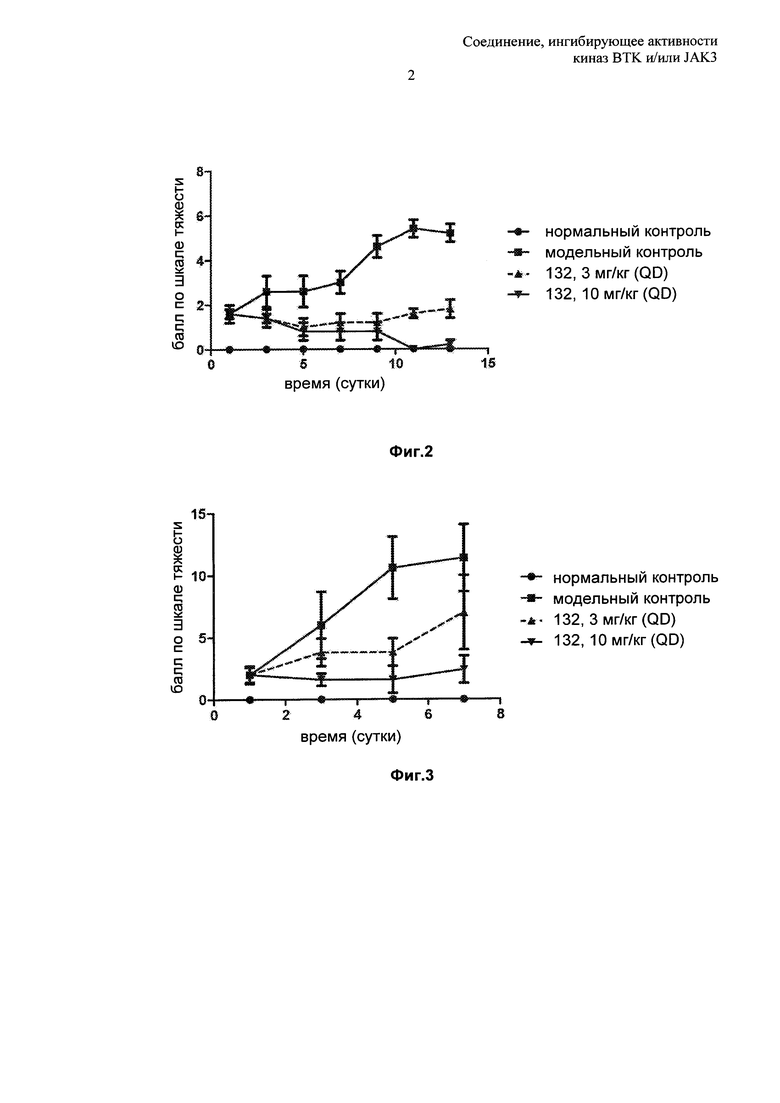
Настоящее изобретение относится к новому соединению формулы I, или его стереоизомеру, или фармацевтически приемлемой соли, обладающим свойствами ингибитора активности тирозинкиназы Брутона (ВТК) и/или Янус-киназы 3 (JAK3). Соединение может найти применение при лечении таких заболеваний, как ревматоидный артрит, остеоартрит, юношеский артрит, системная красная волчанка, псориаз и псориатический артрит, рак, выбранный из группы, состоящей из В-клеточного хронического лимфоцитарного лейкоза, острого лимфоцитарного лейкоза, неходжкинской лимфомы, лимфомы Ходжкина, диффузной крупноклеточной В-клеточной лимфомы, лимфомы клеток мантии и мелкоклеточной лимфоцитарной лимфомы. В формуле I

R представляет собой С3-8циклоалкил, замещенный группой -NR2W; 4-10-членную насыщенную N-гетероциклическую группу, которая содержит только один атом азота в своем кольце и этот атом азота замещен W; или С1-4алкил, замещенный 4-10-членной насыщенной N-гетероциклической группой, которая содержит только один атом азота в своем кольце и этот атом азота замещен W; W представляет собой 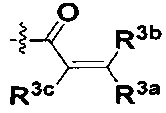 или
или 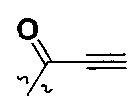 ; V представляет собой С или N; X представляет собой NR4 или О; Y представляет собой СН, S или О; Z представляет собой СН, S, О или NR5; R1 представляет собой фенил или 5-9-членный гетероарил, содержащий 1-2 гетероатома, выбранных из азота, кислорода и серы, возможно замещенный одним или двумя R6; R2 представляет собой водород или С1-8алкил; R3a, R3b и R3c представляют собой водород; R4 представляет собой водород или С1-8алкил; R5 представляет собой водород или С1-8алкил; каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, С1-8алкила, С1-С8циклоалкила, С1-8галогеналкила, гетероциклил-С1-8алкила, гидрокси-С1-8алкила, С1-8алкилокси-С1-8алкила, амино-С1-8алкила, С1-8алкиламино-С1-8алкила, ди(С1-8алкил)амино-С1-8алкила, С1-8алкилокси, гетероциклилокси, гетероциклил-С1-8алкилокси, гидрокси-С1-8алкилокси, С1-8алкилокси-С1-8алкилокси, С1-8алкиламино, ди(С1-8алкил)амино, С3-С8циклоалкиламино, гетероциклиламино, С1-8алкиламино-С1-8алкиламино, ди(С1-8алкил)амино-С1-8алкиламино, С1-8алкилкарбонила, гетероциклилкарбонила, С1-8алкиламиноацила, ди(С1-8алкил)аминоацила и гетероциклиламиноацила, где в указанном С1-8алкиламиноациле, ди(С1-8алкил)аминоациле и гетероциклиламиноациле ацил представляет собой группу -С(=O)-; и гетероциклил как независимая группа или как часть других(ой) групп(ы) представляет собой насыщенную 6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранных из группы, состоящей из N и О; возможно, каждый гетероциклил независимо замещен одним или двумя заместителями, выбранными из группы, состоящей из С1-8алкила, гидрокси, С1-8алкилокси и С1-8алкилкарбонила. 6 н. и 18 з.п. ф-лы, 3 ил., 11 табл., 145 пр.
; V представляет собой С или N; X представляет собой NR4 или О; Y представляет собой СН, S или О; Z представляет собой СН, S, О или NR5; R1 представляет собой фенил или 5-9-членный гетероарил, содержащий 1-2 гетероатома, выбранных из азота, кислорода и серы, возможно замещенный одним или двумя R6; R2 представляет собой водород или С1-8алкил; R3a, R3b и R3c представляют собой водород; R4 представляет собой водород или С1-8алкил; R5 представляет собой водород или С1-8алкил; каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, С1-8алкила, С1-С8циклоалкила, С1-8галогеналкила, гетероциклил-С1-8алкила, гидрокси-С1-8алкила, С1-8алкилокси-С1-8алкила, амино-С1-8алкила, С1-8алкиламино-С1-8алкила, ди(С1-8алкил)амино-С1-8алкила, С1-8алкилокси, гетероциклилокси, гетероциклил-С1-8алкилокси, гидрокси-С1-8алкилокси, С1-8алкилокси-С1-8алкилокси, С1-8алкиламино, ди(С1-8алкил)амино, С3-С8циклоалкиламино, гетероциклиламино, С1-8алкиламино-С1-8алкиламино, ди(С1-8алкил)амино-С1-8алкиламино, С1-8алкилкарбонила, гетероциклилкарбонила, С1-8алкиламиноацила, ди(С1-8алкил)аминоацила и гетероциклиламиноацила, где в указанном С1-8алкиламиноациле, ди(С1-8алкил)аминоациле и гетероциклиламиноациле ацил представляет собой группу -С(=O)-; и гетероциклил как независимая группа или как часть других(ой) групп(ы) представляет собой насыщенную 6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранных из группы, состоящей из N и О; возможно, каждый гетероциклил независимо замещен одним или двумя заместителями, выбранными из группы, состоящей из С1-8алкила, гидрокси, С1-8алкилокси и С1-8алкилкарбонила. 6 н. и 18 з.п. ф-лы, 3 ил., 11 табл., 145 пр.
1. Соединение формулы I
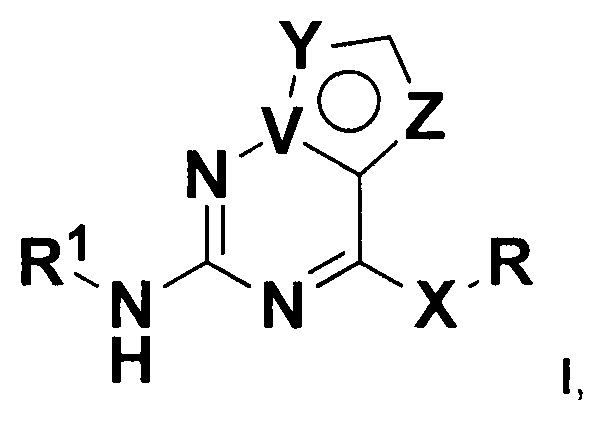
где:
R представляет собой С3-8циклоалкил, замещенный группой -NR2W; 4-10-членную насыщенную N-гетероциклическую группу, которая содержит только один атом азота в своем кольце и этот атом азота замещен W; или С1-4алкил, замещенный 4-10-членной насыщенной N-гетероциклической группой, которая содержит только один атом азота в своем кольце и этот атом азота замещен W;
W представляет собой  или
или 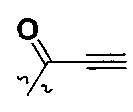 ;
;
V представляет собой С или N;
X представляет собой NR4 или О;
Y представляет собой СН, S или О;
Z представляет собой СН, S, О или NR5;
R1 представляет собой фенил или 5-9-членный гетероарил, содержащий 1-2 гетероатома, выбранных из азота, кислорода и серы, возможно замещенный одним или двумя R6;
R2 представляет собой водород или С1-8алкил;
R3a, R3b и R3c представляют собой водород;
R4 представляет собой водород или С1-8алкил;
R5 представляет собой водород или С1-8алкил;
каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, С1-8алкила, С1-С8циклоалкила, С1-8галогеналкила, гетероциклил-С1-8алкила, гидрокси-С1-8алкила, С1-8алкилокси-С1-8алкила, амино-С1-8алкила, С1-8алкиламино-С1-8алкила, ди(С1-8алкил)амино-С1-8алкила, С1-8алкилокси, гетероциклилокси, гетероциклил-С1-8алкилокси, гидрокси-С1-8алкилокси, С1-8алкилокси-С1-8алкилокси, С1-8алкиламино, ди(С1-8алкил)амино, С3-С8циклоалкиламино, гетероциклиламино, С1-8алкиламино-С1-8алкиламино, ди(С1-8алкил)амино-С1-8алкиламино, С1-8алкилкарбонила, гетероциклилкарбонила, С1-8алкиламиноацила, ди(С1-8алкил)аминоацила и гетероциклиламиноацила, где
в указанном С1-8алкиламиноациле, ди(С1-8алкил)аминоациле и гетероциклиламиноациле ацил представляет собой группу -С(=O)-; и
гетероциклил как независимая группа или как часть других(ой) групп(ы) представляет собой насыщенную 6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранных из группы, состоящей из N и О; возможно, каждый гетероциклил независимо замещен одним или двумя заместителями, выбранными из группы, состоящей из С1-8алкила, гидрокси, С1-8алкилокси и С1-8алкилкарбонила;
или его стереоизомер, или фармацевтически приемлемая соль.
2. Соединение по п. 1, представленное формулой Ia

где X, Y, Z, W, R1 и R2 - все являются такими, как определено в п. 1,
или его стереоизомер, или фармацевтически приемлемая соль.
3. Соединение по п. 2, где
R1 представляет собой фенил или 5-9-членный гетероарил, содержащий 1-2 гетероатома, выбранных из азота, кислорода и серы, возможно замещенный одним или двумя R6;
каждый R6 независимо выбран из группы, состоящей из галогена, гетероциклила, С1-8алкила, С1-С8циклоалкила, С1-8галогеналкила, гетероциклил-С1-8алкила, гидрокси-C1-8алкила, С1-8алкилокси-С1-8алкила, амино-С1-8алкила, С1-8алкиламино-С1-8алкила, ди(С1-8алкил)амино-С1-8алкила, С1-8алкилокси, гетероциклилокси, гетероциклил-С1-8алкилокси, гидрокси-С1-8алкилокси, С1-8алкилокси-С1-8алкилокси, С1-8алкиламино, С3-С8циклоалкиламино, ди(С1-8алкил)амино, гетероциклиламино, ди(С1-8алкил)амино-С1-8алкиламино, гетероциклилкарбонила, С1-8алкиламиноацила и гетероциклиламиноацила, где в указанном С1-8алкиламиноациле и гетероциклиламиноациле ацил представляет собой группу -С(=O)-, и
гетероциклил как независимая группа или как часть других(ой) групп(ы) представляет собой насыщенную 6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранных из группы, состоящей из N и О; возможно, каждый гетероциклил независимо замещен одним или двумя заместителями, выбранными из группы, состоящей из С1-8алкила, гидрокси, С1-8алкилокси и C1-8алкилкарбонила;
или его стереоизомер, или фармацевтически приемлемая соль.
4. Соединение по п. 2 или 3, где R1 выбран из группы, состоящей из

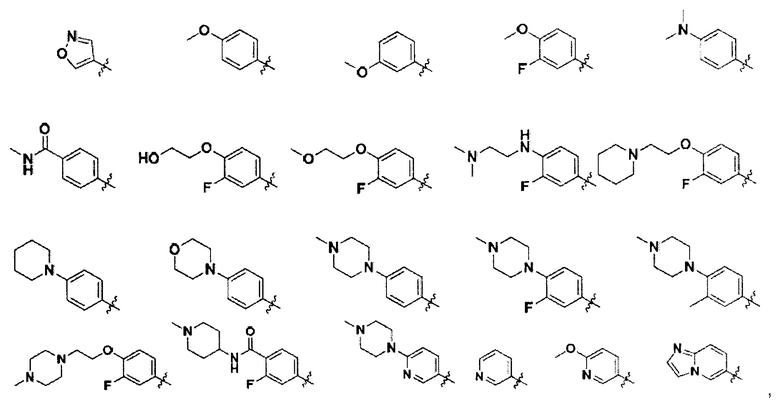
или его стереоизомер, или фармацевтически приемлемая соль.
5. Соединение по любому из пп. 2-4, выбранное из группы, состоящей из
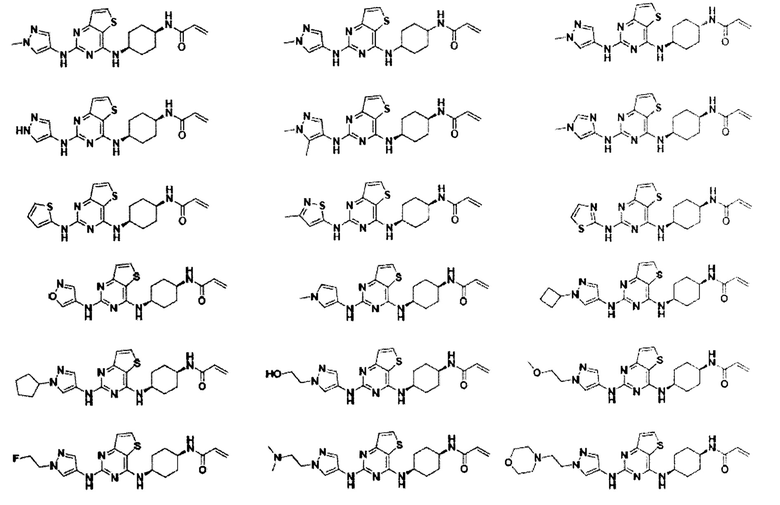
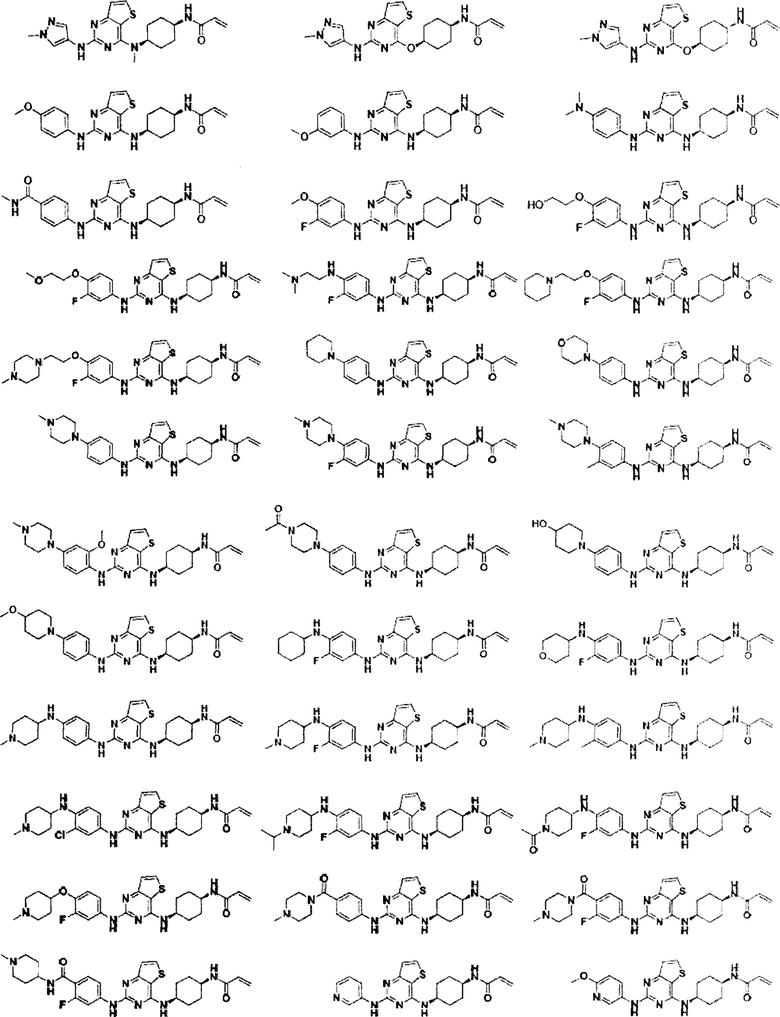
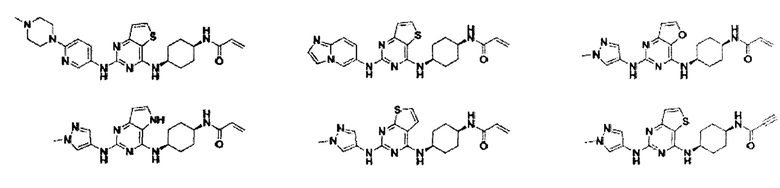
или его стереоизомер, или фармацевтически приемлемая соль.
6. Соединение по п. 1, представленное формулой Ib
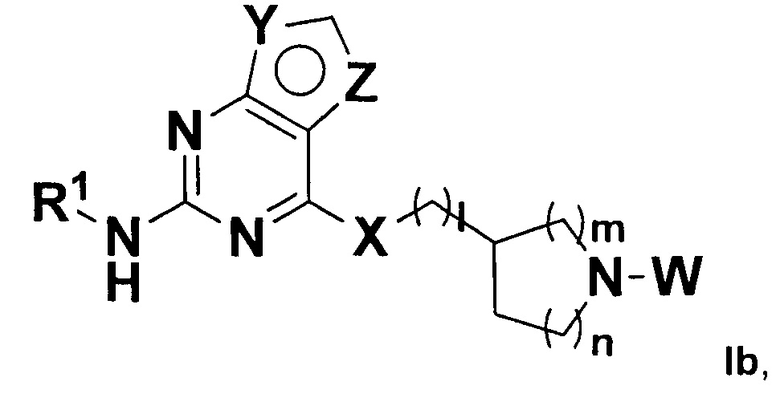
где:
X, Y, Z, W и R1 - все являются такими, как определено в п. 1;
l равно 0, 1 или 2, причем, когда l равно 0,  представляет собой
представляет собой 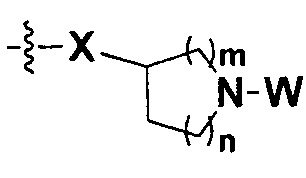 ;
;
m равно 0, 1, 2, 3 или 4; причем, когда m равно 0, 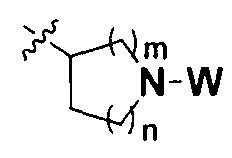 представляет собой
представляет собой  ;
;
n равно 0, 1, 2 или 3; причем, когда n равно 0,  представляет собой
представляет собой 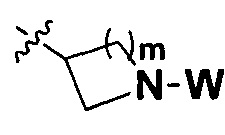 ; и
; и
m и n одновременно не равны 0,
или его стереоизомер, или фармацевтически приемлемая соль.
7. Соединение по п. 6, где
R1 представляет собой 5-членную гетероарильную группу, содержащую 1-2 гетероатома, выбранных из азота, кислорода и серы, возможно замещенную одним или более R6;
каждый R6 независимо выбран из группы, состоящей из С1-8алкила, C1-С8циклоалкила, гидрокси-С1-8алкила, С1-8алкилокси-С1-8алкила, амино-C1-8алкила, С1-8алкиламино-С1-8алкила, ди(С1-8алкил)амино-С1-8алкила, гетероциклил-С1-8алкила и гетероциклила, где гетероциклил как независимая группа или как часть других(ой) групп(ы) представляет собой насыщенную 6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранных из группы, состоящей из N и О; возможно, каждый гетероциклил независимо замещен одним или более заместителями С1-8алкил;
или его стереоизомер, или фармацевтически приемлемая соль.
8. Соединение по п. 6 или 7, где R1 представляет собой 5-членную гетероарильную группу, выбранную из группы, состоящей из пирролила, пиразолила, имидазолила, тиенила, изоксазолила, тиазолила и изотиазолила, и R1 возможно замещен одним или двумя R6; каждый R6 независимо выбран из группы, состоящей из С1-8алкила, С1-С8циклоалкила, гидрокси-С1-8алкила, С1-8алкилокси-С1-8алкила, ди(С1-8алкил)амино-С1-8алкила, гетероциклил-C1-8алкила, С1-8алкилкарбонила и гетероциклила, где гетероциклил как независимая группа или как часть других(ой) групп(ы) представляет собой насыщенную 6-членную гетероциклическую группу, содержащую один или два гетероатома, выбранных из группы, состоящей из N и О;
или его стереоизомер, или фармацевтически приемлемая соль.
9. Соединение по любому из пп. 6-8, где R1 выбран из группы, состоящей из
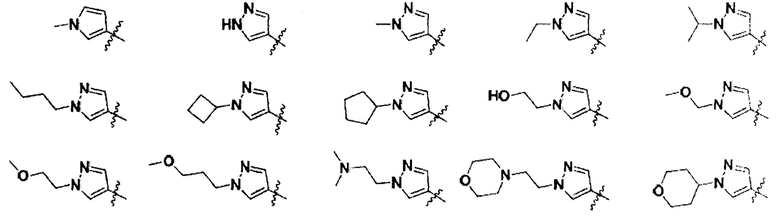
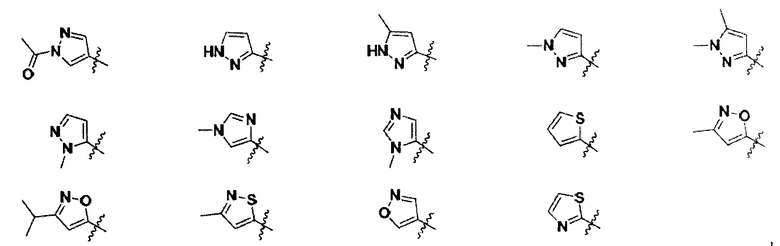
или его стереоизомер, или фармацевтически приемлемая соль.
10. Соединение по любому из пп. 6-9, выбранное из группы, состоящей из
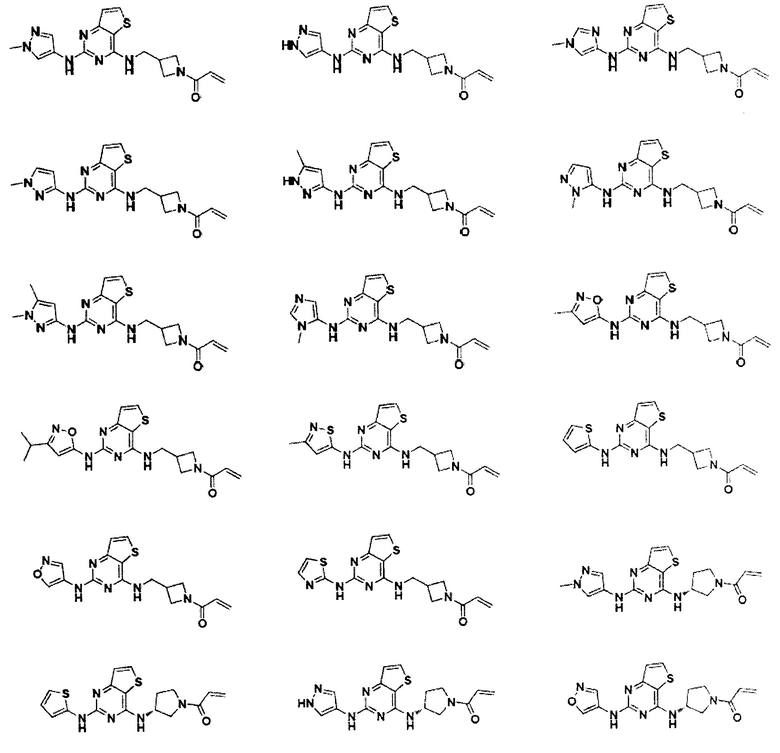
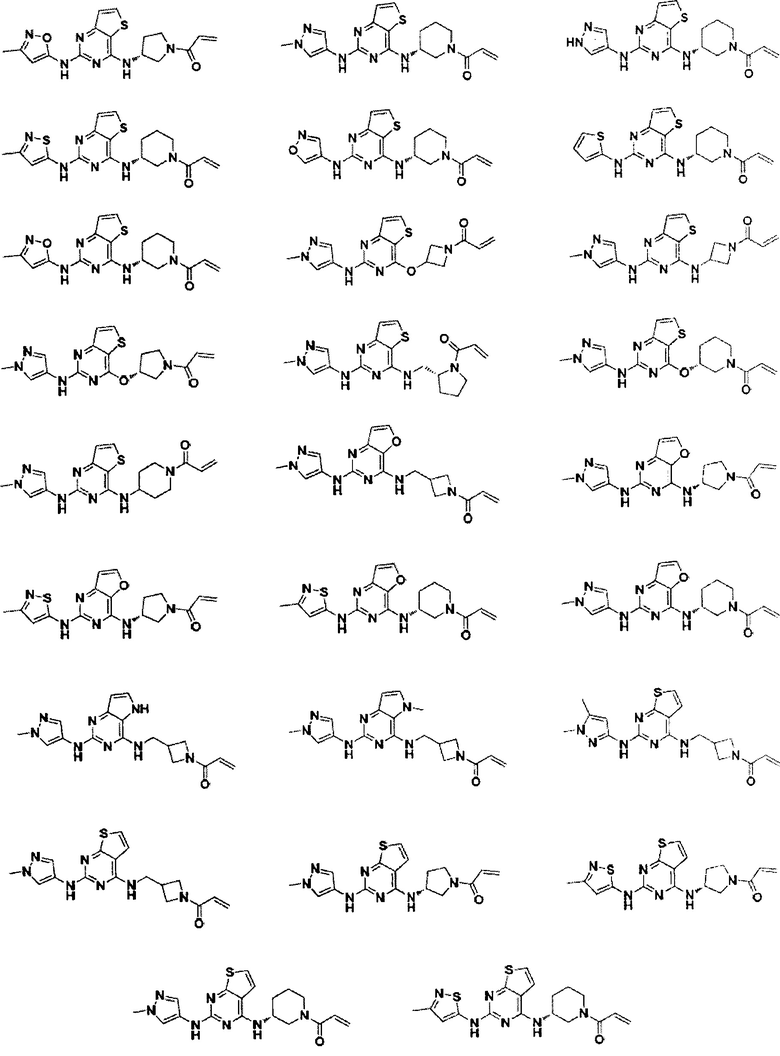
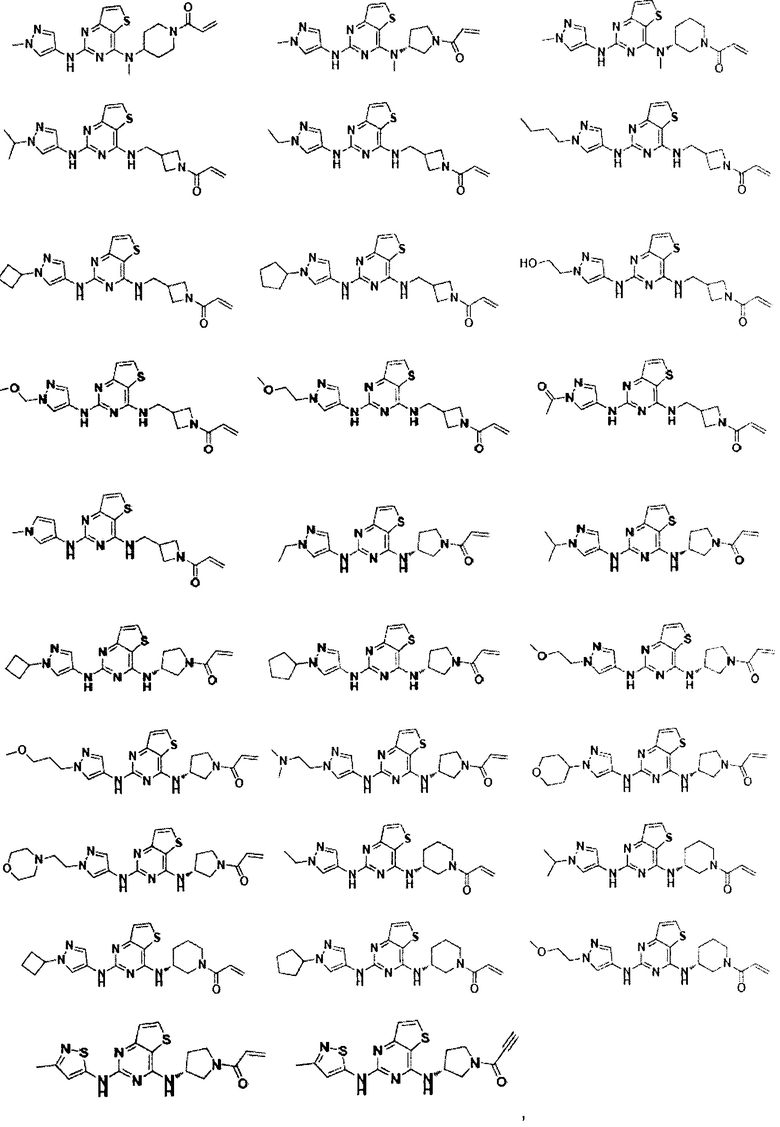
или его стереоизомер, или фармацевтически приемлемая соль.
11. Соединение по п. 1, представленное формулой Ic
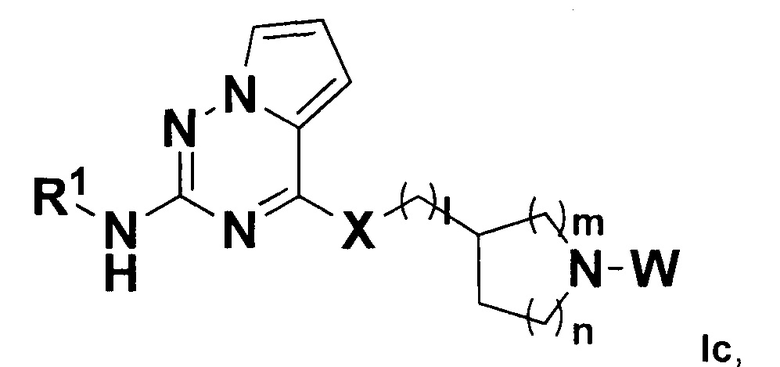
где:
X, W и R1 - все являются такими, как определено в п. 1;
l равно 0, 1 или 2; причем, когда l равно 0, 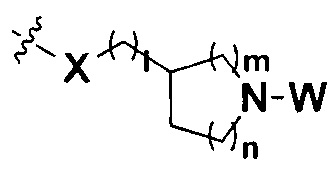 представляет собой
представляет собой 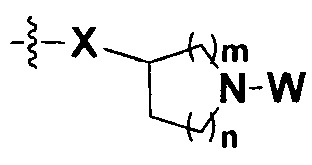 ;
;
m равно 0, 1, 2 или 3; причем, когда m равно 0, 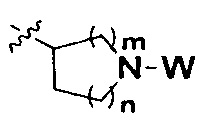 представляет собой
представляет собой  ;
;
n равно 0 или 1; причем, когда n равно 0, 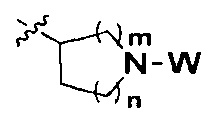 представляет собой
представляет собой 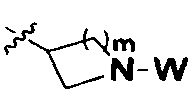 ; и
; и
m и n одновременно не равны 0,
или его стереоизомер, или фармацевтически приемлемая соль.
12. Соединение по п. 11, где
R1 представляет собой 5-членную гетероарильную группу, содержащую 1-2 гетероатома, выбранных из азота, кислорода и серы, возможно замещенную одним или двумя R6;
каждый R6 представляет собой С1-8алкил,
или его стереоизомер, или фармацевтически приемлемая соль.
13. Соединение по п. 11 или 12, где R1 выбран из группы, состоящей из
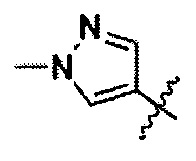 и
и 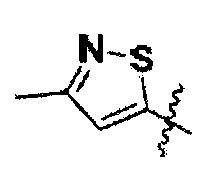 ,
,
или его стереоизомер, или фармацевтически приемлемая соль.
14. Соединение по любому из пп. 11-13, выбранное из группы, состоящей из
 ,
,
или его стереоизомер, или фармацевтически приемлемая соль.
15. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении BTK (тирозинкиназа Брутона) и/или JAK3 (Янус-киназа 3), содержащая в терапевтически эффективном количестве соединение по любому из пп. 1-14, или его стереоизомер, или фармацевтически приемлемую соль и фармацевтически приемлемые эксципиенты.
16. Применение соединения по любому из пп. 1-14, или его стереоизомера, или фармацевтически приемлемой соли в изготовлении лекарственного средства для ингибирования активностей тирозинкиназы Брутона (BTK) и/или Янус-киназы 3 (JAK3).
17. Применение соединения по любому из пп. 1-14, или его стереоизомера, или фармацевтически приемлемой соли в изготовлении лекарственного средства для предупреждения или лечения BTK- и/или JAK3-опосредованного заболевания.
18. Применение по п. 17, где заболевание выбрано из группы, состоящей из аутоиммунного заболевания и рака.
19. Применение по п. 17, где заболевание выбрано из группы, состоящей из ревматоидного артрита, остеоартрита, юношеского артрита, системной красной волчанки, псориаза и псориатического артрита.
20. Применение по п. 18, где рак выбран из группы, состоящей из В-клеточного хронического лимфоцитарного лейкоза, острого лимфоцитарного лейкоза, неходжкинской лимфомы, лимфомы Ходжкина, диффузной крупноклеточной В-клеточной лимфомы, лимфомы клеток мантии и мелкоклеточной лимфоцитарной лимфомы.
21. Способ ингибирования активностей BTK и/или JAK3 в биологической системе, включающий приведение указанной биологической системы в контакт с соединением по любому из пп. 1-14, или с его стереоизомером, или фармацевтически приемлемой солью, или с фармацевтической композицией по п. 15.
22. Способ по п. 21, где биологическая система представляет собой фермент, клетку или млекопитающего.
23. Способ предупреждения или лечения BTK- и/или JAK3-опосредованного заболевания, включающий введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения по любому из пп. 1-14, или его стереоизомера, или фармацевтически приемлемой соли, или фармацевтической композиции по п. 15.
24. Способ по п. 23, где заболевание выбрано из группы, состоящей из аутоиммунного заболевания и рака.
| WO 2013042006 A1, 28.03.2013 & EA 201490673 A1, 30.06.2014 | |||
| WO 2010129053 A2, 11.11.2010 | |||
| WO 2011162515 A2, 29.12.2011 & RU 2585177 C2, 27.05.2016 & RU 2598852 C2, 27.09.2016 | |||
| WO 2011079231 A1, 30.06.2011 | |||
| RU 2010119647 A1, 27.11.2011 & RU 2528340 C2, 10.09.2014. |
Авторы
Даты
2018-04-16—Публикация
2014-09-18—Подача