ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет на основании заявки на патент США №61/671640, поданной 13 июля 2012 г.; и заявки на патент США №61/845948, поданной 13 июля 2013 г., которые полностью включены в настоящий документ посредством ссылок.
ОБЛАСТЬ ТЕХНИКИ
[0002] Настоящее изобретение относится к области рационального дизайна мультиспецифических скаффолдов, содержащих CD3-связывающий домен, для разработки индивидуальной биотерапии.
УРОВЕНЬ ТЕХНИКИ
[0003] В области терапевтических белков антитела, обладающие способностью к мультивалентному связыванию мишеней, представляют собой прекрасные скаффолды/каркасы для дизайна перспективных лекарственных средств. В результате дальнейшего улучшения указанных свойств конструируемые биспецифические антитела и другие гибридные мультиспецифические терапевтические средства проявляют специфичность в отношении двух или нескольких мишеней и дают возможность создавать лекарственные средства с новыми механизмами действия. Разработка таких мультивалентных мультиспецифических терапевтических белков, обладающих благоприятными фармакокинетикой и функциональной активностью, представляла собой сложную задачу.
[0004] Иммунная система как у человека, так и у животных, включает два основных класса лимфоцитов: происходящие из тимуса клетки (Т-клетки), и происходящие из костного мозга клетки (В-клетки). Т-клетки проявляют иммунологическую специфичность и непосредственно вовлечены в клеточно-опосредованный иммунный ответ (такой как отторжение трансплантата). Т-клетки действуют против или в ответ на различные чужеродные структуры (антигены). Во многих случаях указанные чужеродные антигены экспрессируются на клетках-хозяевах в результате инфекции. Однако чужеродные антигены могут также происходить из клеток-хозяев, измененных в результате неоплазии или инфекции.
[0005] Активация Т-клеток представляет собой сложное явление, зависящее от участия различных молекул клеточной поверхности, экспрессируемых на Т-клетках реактивной популяции. Например, антигенспецифический Т-клеточный рецептор (TcR) состоит из связанного дисульфидными связями гетеродимера, содержащего две клонально распределенные интегральные мембранные гликопротеиновые цепи, альфа и бета (α и β), или γ и дельта (γ и δ), нековалентно связанные с комплексом низкомолекулярных инвариантных белков, обычно называемых CD3.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0006] В настоящем изобретении предложены мультиспецифические гетеромультимеры, содержащие CD3-связывающий домен. Согласно одному варианту реализации предложен биспецифический асимметричный гетеродимер, содержащий анти-CD3 конструкции.
[0007] В настоящем изобретении предложены выделенные мультиспецифические гетеромультимерные конструкции, содержащие: первую полипептидную конструкцию, содержащую первый полипептид тяжелой цепи и CD3-связывающую полипептидную конструкцию, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; вторую полипептидную конструкцию, содержащую второй полипептид тяжелой цепи, отличный от указанного первого полипептида тяжелой цепи, и антигенсвязывающую полипептидную конструкцию, которая связывается с целевым антигеном по меньшей мере на одной В-клетке; при этом по меньшей мере одна из указанных CD3-связывающих полипептидных конструкций и указанных антигенсвязывающих полипептидных конструкций содержит одноцепочечную Fv-область; при этом указанная мультиспецифическая гетеромультимерная конструкция одновременно задействует указанную по меньшей мере одну В-клетку и указанную по меньшей мере одну CD3-экспрессирующую клетку таким образом, что CD3-экспрессирующая клетка активируется, тем самым индуцируя киллинг указанной В-клетки; и указанные первый и второй полипептиды тяжелой цепи образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной области Fc со стабильностью, по меньшей мере сравнимой со стабильностью нативной гомодимерной Fc, и с такой чистотой, что при коэкспрессии указанной мультиспецифической гетеромультимерной конструкции стабильной клеткой млекопитающего с получением экспрессионного продукта указанный экспрессионный продукт содержит по меньшей мере приблизительно 70% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций. Согласно определенным вариантам реализации указанную стабильную клетку млекопитающего трансфицируют по меньшей мере первой последовательностью ДНК, кодирующей указанную первую полипептидную конструкцию, и по меньшей мере второй последовательностью ДНК, кодирующей указанную вторую полипептидную конструкцию в заданном заранее соотношении 1:1. Согласно определенным вариантам реализации в состав первой или второй полипептидной конструкции не входит по меньшей мере что-либо одно из легкой цепи иммуноглобулина и первой константной области (СН1) иммуноглобулина.
[0008] Согласно определенным вариантам реализации предложены выделенные гетеромультимерные конструкции согласно описанию в настоящем документе, отличающиеся тем, что указанная гетеродимерная Fc-область содержит вариант СН2-домена или шарнир, содержащий аминокислотные модификации, который предотвращает функционально эффективное связывание со всеми рецепторами Fcγ. Согласно некоторым вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, при этом указанный вариант СН2-домена или шарнир, содержащий аминокислотныаминокислотную модификацию, также предотвращает функционально эффективное связывание с белками комплемента (комплекс C1q). Согласно одному варианту реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанная гетеродимерная Fc-область содержит вариант СН2-домена или шарнир, содержащий аминокислотные модификации, усиливающие связывание с рецептором FcγRIIb.
[0009] Согласно одному варианту реализации предложена выделенная мультиспецифическая гетеромультимерная конструкция, содержащая: первую полипептидную конструкцию, содержащую первый полипептид тяжелой цепи и CD3-связывающую полипептидную конструкцию, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; вторую полипептидную конструкцию, содержащую второй полипептид тяжелой цепи, отличный от указанного первого полипептида тяжелой цепи, и антигенсвязывающую полипептидную конструкцию, которая связывается с целевым антигеном по меньшей мере на одной В-клетке; при этом: по меньшей мере одна из указанных CD3-связывающих полипептидных конструкций и указанных антигенсвязывающих полипептидных конструкций необязательно содержит одноцепочечную Fv-область; указанные первый и второй полипептиды тяжелой цепи образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной области Fc, отличающийся тем, что: указанная гетеродимерная Fc имеет стабильность, по меньшей мере сравнимую со стабильностью нативной гомодимерной Fc, и указанная образующаяся гетеродимерная Fc имеет такую чистоту, что при коэкспрессии указанной мультиспецифической гетеромультимерной конструкции клеткой млекопитающего с получением экспрессионного продукта указанный экспрессионный продукт содержит больше 70% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций; и указанная мультиспецифическая гетеромультимерная конструкция связывает указанную по меньшей мере одну В-клетку с валентностью больше 1, и указанный мультиспецифический гетеромультимер одновременно задействует указанную по меньшей мере одну В-клетку и указанную по меньшей мере одну CD3-экспрессирующую клетку таким образом, что CD3-экспрессирующая клетка активируется, тем самым индуцируя киллинг указанной В-клетки. Согласно определенным вариантам реализации указанная мультиспецифическая гетеромультимерная конструкция связывает указанную по меньшей мере одну В-клетку с валентностью, равной двум.
[0010] В настоящем изобретении предложена выделенная мультиспецифическая гетеромультимерная конструкция, содержащая: первую полипептидную конструкцию, содержащую первый полипептид тяжелой цепи и CD3-связывающую полипептидную конструкцию, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; вторую полипептидную конструкцию, содержащую второй полипептид тяжелой цепи, отличный от указанного первого полипептида тяжелой цепи, и конструкцию, представляющую собой стерический модулятор, демонстрирующую пренебрежимое связывание с рецептором; отличающаяся тем, что: указанная мультиспецифическая гетеромультимерная конструкция одновременно задействует по меньшей мере одну В-клетку и указанную по меньшей мере одну CD3-экспрессирующую клетку таким образом, что CD3-экспрессирующая клетка активируется, тем самым индуцируя киллинг указанной В-клетки; и указанные первый и второй полипептиды тяжелой цепи образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной Fc, отличающийся тем, что: указанная гетеродимерная Fc имеет стабильность, по меньшей мере сравнимую со стабильностью нативной гомодимерной Fc, и указанная образующаяся гетеродимерная Fc имеет такую чистоту, что при коэкспрессии указанной мультиспецифической гетеромультимерной конструкции стабильной клеткой млекопитающего с получением экспрессионного продукта указанный экспрессионный продукт содержит по меньшей мере приблизительно 75% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций.
[0011] Предложена выделенная мультиспецифическая гетеромультимерная конструкция, содержащая: первую полипептидную конструкцию, содержащую первый полипептид тяжелой цепи и CD3-связывающую полипептидную конструкцию, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; вторую полипептидную конструкцию, содержащую второй полипептид тяжелой цепи, отличную от указанного первого полипептида тяжелой цепи, и отличающуюся тем, что указанная вторая полипептидная конструкция не содержит антигенсвязывающую полипептидную конструкцию; при этом указанная мультиспецифическая гетеромультимерная конструкция одновременно задействует по меньшей мере одну В-клетку и указанную по меньшей мере одну CD3-экспрессирующую клетку таким образом, что CD3-экспрессирующая клетка активируется, тем самым индуцируя киллинг указанной В-клетки; и указанные первый и второй полипептиды тяжелой цепи образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной Fc, при этом указанная гетеродимерная Fc имеет стабильность, по меньшей мере сравнимую со стабильностью нативной гомодимерной Fc, и указанная образующаяся гетеродимерная Fc имеет такую чистоту, что при коэкспрессии указанной мультиспецифической гетеромультимерной конструкции стабильной клеткой млекопитающего с получением экспрессионного продукта указанный экспрессионный продукт содержит по меньшей мере приблизительно 75% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций.
[0012] Согласно определенным вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанная гетеродимерная Fc-область содержит вариант СН2-домена, содержащий модификации аминокислот, способствующие селективному связыванию рецептора Fcγ. Согласно некоторым вариантам реализации указанный вариант СН2-домена селективно связывает рецептор FcγIIb лучше, чем СН2-домен дикого типа. Согласно определенным вариантам реализации указанный вариант СН2-домена селективно связывает по меньшей мере один из рецепторов FcγIIIa и FcγIIa лучше, чем СН2-домен дикого типа.
[0013] Согласно определенным вариантам реализации предложена выделенная мультиспецифическая гетеромультимерная конструкция согласно описанию в настоящем документе, отличающаяся тем, что температура плавления (Tm) указанного варианта СН3-домена составляет приблизительно 73°С или более. Согласно некоторым вариантам реализации гетеродимерная Fc-область образуется с чистотой, составляющей больше приблизительно 90%. Согласно определенным вариантам реализации гетеродимерная Fc-область образуется с чистотой, составляющей приблизительно 95% или более, и Tm составляет по меньшей мере приблизительно 75°С. Согласно некоторым дополнительным вариантам реализации гетеродимерная Fc-область образуется с чистотой, составляющей по меньшей мере приблизительно 90%, и Tm составляет приблизительно 75°С. Согласно одному варианту реализации вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации L351Y, F405A и Y407V, а вариант последовательности СН3 второго полипептидного переносчика содержит аминокислотные модификации T366L, К392М и T394W. Согласно другому варианту реализации вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации L351Y, F405A и Y407V, а вариант последовательности СН3 второго полипептида тяжелой цепи содержит аминокислотные модификации T366L, K392L и T394W. Согласно дополнительному варианту реализации вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации T350V, L351Y, F405A и Y407V, а вариант последовательности СН3 второго полипептида тяжелой цепи содержит аминокислотные модификации T350V, T366L, К392М и T394W. Согласно некоторым вариантам реализации вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации T350V, L351Y, F405A и Y407V, а вариант последовательности СН3 второго полипептида тяжелой цепи содержит аминокислотные модификации T350V, T366L, K392L и T394W. Согласно еще одному варианту реализации вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации T366L, N390R, K392R и T394W, а вариант последовательности СН3 второго полипептида тяжелой цепи содержит аминокислотные модификации L351Y, S400E, F405A и Y407V. Согласно некоторым вариантам реализации вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации T350V, T366L, N390R, K392R и T394W, а вариант последовательности СН3 второго полипептида тяжелой цепи содержит аминокислотные модификации T350V, L351Y, S400E, F405A и Y407V.
[0014] Согласно определенным вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанный гетеродимер Fc гликозилирован. Согласно некоторым вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанный гетеродимер Fc афукозилирован. Согласно другому варианту реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанный гетеродимер Fc агликозилирован.
[0015] Согласно некоторым вариантам реализации предложен описанный в настоящем документе выделенный мультиспецифический гетеромультимер, отличающийся тем, что антигенсвязывающая полипептидная конструкция, которая связывается с целевым антигеном по меньшей мере на одной В-клетке, содержит по меньшей мере один связывающий целевой антиген домен, полученный из антитела, фибронектина, аффитела, антикалина, белка типа «цистеиновый узел», искусственного белка с анкириновым повтором (DARPin), авимера, домена Куница или их варианта или производного. Согласно одному варианту реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанное антитело представляет собой антитело, содержащее только тяжелые цепи, не содержащее легких цепей. Согласно дополнительным вариантам реализации выделяют мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанная антигенсвязывающая полипептидная конструкция содержит по меньшей мере один CD19-связывающий домен. Согласно определенным вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанная антигенсвязывающая полипептидная конструкция содержит по меньшей мере один CD20-связывающий домен.
[0016] В настоящем изобретении предложена выделенная мультиспецифическая гетеромультимерная конструкция, содержащая: первую полипептидную конструкцию, содержащую первый полипептидный переносчик, соединенный по меньшей мере с одной CD3-связывающей полипептидной конструкцией, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; вторую полипептидную конструкцию, содержащую второй полипептидный переносчик, отличный от указанного первого полипептидного переносчика, соединенный по меньшей мере с одной антигенсвязывающей полипептидной конструкцией, которая связывается с целевым антигеном по меньшей мере на одной В-клетке; при этом первый и второй полипептидные переносчики получают из белка путем сегментирования указанного белка, каждый полипептид-переносчик содержит аминокислотную последовательность, по меньшей мере на 90% идентичную сегменту указанного белка, и при этом полипептидные переносчики самособираются с образованием квазинативной структуры указанного мономерного белка.
[0017] Согласно определенным вариантам реализации указанные полипептидные переносчики не получены из антитела. Согласно определенному варианту реализации каждый полипептидный переносчик представляет собой производное альбумина. Согласно некоторым вариантам реализации указанный альбумин представляет собой альбумин сыворотки человека. Согласно некоторым вариантам реализации по меньшей мере один полипептидный переносчик представляет собой производное аллоальбумина. Согласно определенным вариантам реализации все полипептидные переносчики получены из разных аллоальбуминов.
[0018] В настоящем изобретении предложены выделенные мультиспецифические гетеромультимерные конструкции, содержащие: первую полипептидную конструкцию, содержащую первый полипептидный переносчик, соединенный по меньшей мере с одной CD3-связывающей полипептидной конструкцией, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; вторую полипептидную конструкцию, содержащую второй полипептидный переносчик, отличный от указанного первого полипептидного переносчика, соединенный по меньшей мере с одной антигенсвязывающей полипептидной конструкцией, которая связывается с целевым антигеном по меньшей мере на одной В-клетке; при этом первый и второй полипептидные переносчики получают путем сегментирования альбумина, и каждый полипептид-переносчик содержит аминокислотную последовательность, по меньшей мере на 90% идентичную сегменту альбумина, таким образом, что указанные полипептидные переносчики самособираются с образованием квазинативного альбумина, и при этом первый транспортный полипептид не содержит какого-либо связывающего домена, присутствующего в указанном втором транспортном полипептиде.
[0019] Согласно определенным вариантам реализации предложен описанный в настоящем документе гетеромультимер, отличающийся тем, что указанная мультиспецифическая гетеромультимерная конструкция одновременно задействует указанную по меньшей мере одну В-клетку и указанную по меньшей мере одну CD3-экспрессирующую клетку таким образом, что активируется CD3-экспрессирующая клетка, индуцируя за счет этого киллинг указанной В-клетки. Согласно некоторым вариантам реализации указанная антигенсвязывающая полипептидная конструкция, которая связывается с целевым антигеном по меньшей мере на одной В-клетке, содержит по меньшей мере один связывающий целевой антиген домен, полученный из антитела, фибронектина, аффитела, антикалина, белка типа «цистеиновый узел», искусственного белка с анкириновым повтором (DARPin), авимера, домена Куница или их варианта или производного. Согласно определенным вариантам реализации указанная антигенсвязывающая полипептидная конструкция содержит по меньшей мере один CD19-связывающий домен.
[0020] Согласно определенным вариантам реализации предложен мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанная антигенсвязывающая полипептидная конструкция содержит по меньшей мере один CD20-связывающий домен.
[0021] Согласно определенным вариантам реализации предложен мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанная по меньшей мере одна CD3-связывающая полипептидная конструкция содержит по меньшей мере один CD3-связывающий домен, полученный из CD3-специфического антитела, нанотела, фибронектина, аффитела, антикалина, белка типа «цистеиновый узел», искусственного белка с анкириновым повтором (DARPin), авимера, домена Куница или их варианта или производного. Согласно некоторым вариантам реализации указанный по меньшей мере один CD3-связывающий домен содержит по меньшей мере одну аминокислотныаминокислотную модификацию, снижающую иммуногенность по сравнению с соответствующим CD3-связывающим доменом, не содержащим указанной модификации. Согласно некоторым вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанный по меньшей мере один CD3-связывающий домен содержит по меньшей мере одну аминокислотныаминокислотную модификацию, увеличивающую его стабильность согласно оценке на основе Tm, по сравнению с соответствующим CD3-связывающим доменом, не содержащим указанной модификации. Согласно некоторым вариантам реализации указанная по меньшей мере одна CD3-связывающая полипептидная конструкция содержит по меньшей мере один CD3-связывающий домен, полученный из CD3-специфического антитела, который представляет собой антитело, содержащее только тяжелые цепи, не содержащее легких цепей. Согласно определенным вариантам реализации указанная по меньшей мере одна CD3-связывающая полипептидная конструкция содержит по меньшей мере один CD3-связывающий домен, полученный из скаффолднового домена белка, не являющегося антителом.
[0022] Согласно одному варианту реализации предложена выделенная гетеромультимерная конструкция согласно описанию в настоящем документе, отличающаяся тем, что по меньшей мере одна из указанных первой и второй полипептидных конструкций дополнительно содержит одноцепочечный Fv-полипептид. Согласно определенным вариантам реализации предложена выделенная гетеромультимерная конструкция согласно описанию в настоящем документе, отличающаяся тем, что по меньшей мере одна из указанных первой и второй полипептидных конструкций дополнительно содержит одноцепочечный Fab-полипептид.
[0023] Согласно некоторым вариантам реализации предложена выделенная гетеромультимерная конструкция согласно описанию в настоящем документе, отличающаяся тем, что CD3-экспрессирующая клетка представляет собой Т-клетку. Согласно определенным вариантам реализации предложен описанный в настоящем документе выделенный гетеромультимер, отличающийся тем, что указанный гетеромультимер связывается с Т-клеткой с достаточной аффинностью и декорирует Т-клетку в достаточной мере для индуцирования киллинговой активности Т-клетки в отношении В-клеток при связывании Т-клетки и В-клетки.
[0024] Предложена выделенная гетеромультимерная конструкция согласно описанию в настоящем документе, отличающаяся тем, что CD3-экспрессирующая клетка представляет собой клетку человека. Согласно определенным вариантам реализации указанная CD3-экспрессирующая клетка представляет собой клетку не являющегося человеком млекопитающего. Согласно некоторым вариантам реализации указанная клетка млекопитающего представляет собой клетку примата. Согласно определенным вариантам реализации указанный примат представляет собой обезьяну. Согласно некоторым вариантам реализации указанная по меньшей мере одна CD3-связывающая полипептидная конструкция связывается с CD3-конструкциями нескольких видов. Согласно определенным вариантам реализации указанный CD3-связывающий полипептид связывается с CD3-конструкциями нескольких видов, которые включают по меньшей мере один или несколько видов из человека, крысы, мыши и обезьяны.
[0025] Предложена выделенная гетеромультимерная конструкция согласно описанию в настоящем документе, отличающаяся тем, что указанная по меньшей мере одна В-клетка связана с заболеванием. Согласно определенным вариантам реализации указанное заболевание представляет собой раковое заболевание, выбранное из карциномы, саркомы, лейкоза, лимфомы и глиомы. Согласно некоторым вариантам реализации указанное раковое заболевание представляет собой по меньшей мере что-либо одно из плоскоклеточной карциномы, аденокарциномы, карциномы переходных клеток, остеосаркомы и саркомы мягких тканей. Согласно одному варианту реализации указанная по меньшей мере одна В-клетка представляет собой аутоиммунную реактивную клетку, которая представляет собой лимфоидную или миелоидную клетку.
[0026] Предложена выделенная гетеромультимерная конструкция согласно описанию в настоящем документе, отличающаяся тем, что указанный гетеромультимер дополнительно содержит по меньшей мере один связывающий домен, который связывает по меньшей мере что-либо одно из: ЕрСАМ, рЭФР (EGFR), IGFR (рИФР), HER-2 neu, HER-3, HER-4, ПСМА, РЭА, MUC-1 (муцина), MUC2, MUC3, MUC4, MUC5, MUC7, CCR4, CCR5, CD19, CD20, CD33, CD30, ганглиозида GD3, 9-О-Ацетил-CD3, GM2, поли (СА), GD2, карбоангидразы IX (MN/CA IX), CD44v6, белка «sonic hedgehog» (Shh), Wue-1, плазмоцитарного антигена (мембраносвязанного), протеогликана хондроитинсульфата меланомы (MCSP), CCR8, предшественника ФНО-альфа, STEAP, мезотелина, антигена А33, АСПК), Ly-6; десмоглеина 4, неоэпитопа Е-кадгерина, ацетилхолинового рецептора фетального типа, CD25, маркера CAI9-9, маркера СА-125 и рецептора ингибирующего вещества Мюллера(М18) II типа, sTn (сиалилированного Tn-антигена; TAG-72), FAP (антиген активации фибробластов), эндосиалина, LG, SAS, ЕРНА4 (эфриновый рецептор человека A4) CD63, содержащих CD3 BsAb (биспецифические антитела) иммуноцитокинов ФНО, ИФНγ, ИЛ-2 и TRAIL.
[0027] Предложена выделенная гетеромультимерная конструкция согласно описанию в настоящем документе, отличающаяся тем, что гетеромультимер необязательно содержит по меньшей мере один линкер. Согласно некоторым вариантам реализации указанный по меньшей мере один линкер представляет собой полипептид, содержащий от приблизительно 1 до приблизительно 100 аминокислот.
[0028] Предложен набор экспрессионных векторов для экспрессии мультиспецифического гетеромультимера согласно описанию в настоящем документе, содержащий по меньшей мере первую последовательность ДНК, кодирующую указанную первую полипептидную конструкцию, и по меньшей мере вторую последовательность ДНК, кодирующую указанную вторую полипептидную конструкцию.
[0029] Предложен способ получения экспрессионного продукта, содержащего мультиспецифический гетеромультимер согласно описанию в настоящем документе, в стабильных клетках млекопитающего, при этом указанный способ включает: трансфицирование по меньшей мере одной клетки млекопитающего: по меньшей мере первой последовательностью ДНК, кодирующей указанную первую полипептидную конструкцию, и по меньшей мере второй последовательностью ДНК, кодирующей указанную вторую полипептидную конструкцию, таким образом, что указанной по меньшей мере одной первой последовательностью ДНК, указанной по меньшей мере одной второй последовательностью ДНК трансфицируют указанную по меньшей мере одну клетку млекопитающего в заранее заданном соотношении с получением стабильных клеток млекопитающих; культивирование указанных стабильных клеток млекопитающих с получением указанного продукта экспрессии, содержащего указанный мультиспецифический гетеромультимер. Согласно некоторым вариантам реализации предложен способ получения экспрессионного продукта, содержащего мультиспецифическую гетеромультимерную конструкцию согласно описанию в настоящем документе, отличающийся тем, что указанное заранее заданное отношение по меньшей мере одной первой последовательности ДНК к по меньшей мере одной второй последовательности ДНК составляет приблизительно 1:1. Согласно некоторым вариантам реализации указанную клетку млекопитающего выбирают из группы, состоящей из клеток VERO, HeLa, НЕК, NS0, клеток яичника китайского хомячка (СНО), W138, ВНК, COS-7, Сасо-2 и MDCK, и их подклассов и вариантов.
[0030] Предложена фармацевтическая композиция, содержащая мультиспецифический гетеромультимер согласно описанию в настоящем документе, и подходящее вспомогательное вещество. Также предложен способ получения указанной фармацевтической композиции, включающий: культивирование клетки-хозяина в условиях, допускающих экспрессию гетеромультимера согласно приведенному в настоящем документе определению; выделение полученного гетеромультимера из культуры; и получение указанной фармацевтической композиции.
[0031] Предложен способ предотвращения, лечения или облегчения по меньшей мере чего-либо одного из: пролиферативного заболевания, минимального остаточного рака, опухолевого заболевания, воспалительного заболевания, иммунологического расстройства, аутоиммунного заболевания, инфекционного заболевания, вирусного заболевания, аллергических реакций, паразитарных реакций, реакций «трансплантат против хозяина» или реакций «хозяин против трансплантата» или злокачественных клеточных новообразований, при этом указанный способ включает введение субъекту, нуждающемуся в таком предотвращении, лечении или облегчении, фармацевтической композиции согласно описанию в настоящем документе. Предложен способ лечения ракового заболевания у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему композиции, содержащей эффективное количество фармацевтической композиции согласно описанию в настоящем документе, необязательно в комбинации с другими фармацевтически активными молекулами. Согласно определенным вариантам реализации указанное раковое заболевание представляет собой солидную опухоль. Согласно некоторым другим вариантам реализации указанная солидная опухоль представляет собой что-либо одно или более из саркомы, карциномы и лимфомы. Согласно некоторым другим вариантам реализации указанное раковое заболевание представляет собой гематологическое раковое заболевание. Согласно дополнительному варианту реализации указанное раковое заболевание представляет собой что-либо одно или более из В-клеточной лимфомы, неходжкинской лимфомы и лейкоза.
[0032] Предложен способ лечения раковых клеток, включающий обеспечение указанной композицией, содержащей гетеромультимер, описанный в настоящем документе. Согласно определенным вариантам реализации указанный гетеромультимер предложен в сочетании с другим терапевтическим агентом.
[0033] Предложен способ лечения ракового заболевания, не поддающегося лечению по меньшей мере чем-либо одним из CD19-литического антитела, CD20-литического антитела и блинатумомаба, у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему композиции, содержащей эффективное количество фармацевтической композиции согласно описанию в настоящем документе.
[0034] Предложен способ лечения раковой клетки, регрессирующей после лечения блинатумомабом, включающий обеспечение указанной раковой клетки композицией, содержащей эффективное количество фармацевтической композиции согласно описанию в настоящем документе.
[0035] Предложен способ лечения индивидуума, страдающего заболеванием, характеризующимся экспрессией В-клеток, отличающийся тем, что указанный способ включает обеспечение указанного индивидуума эффективным количеством композиции, содержащей эффективное количество фармацевтической композиции согласно описанию в настоящем документе. Согласно определенным вариантам реализации указанное заболевание не поддается лечению по меньшей мере чем-либо одним из антитела против CD19 и антитела против CD20.
[0036] Предложен способ лечения аутоиммунного состояния у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему композиции, содержащей эффективное количество фармацевтической композиции согласно настоящему описанию. Согласно определенным вариантам реализации указанное аутоиммунное состояние представляет собой что-либо одно или более из рассеянного склероза, ревматоидного артрита, эритематозной волчанки, псориатического артрита, псориаза, васкулита, увеита, болезни Крона и диабета первого типа.
[0037] Предложен способ лечения воспалительного состояния у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему композиции, содержащей эффективное количество фармацевтической композиции, содержащей гетеромультимер согласно настоящему описанию.
[0038] Предложен набор, содержащий гетеромультимер согласно приведенному в настоящем документе определению, и инструкции по его применению.
[0039] В настоящем изобретении предложена гетеромультимерная конструкция, содержащая: первый мономер, содержащий первый полипептидный переносчик, соединенный с первым транспортным полипептидом, который содержит по меньшей мере один HER2-связывающий домен; второй мономер, содержащий второй полипептидный переносчик, отличный от указанного первого полипептидного переносчика, соединенный с вторым транспортным полипептидом, который содержит по меньшей мере один HER3-связывающий домен; при этом первый транспортный полипептид не содержит какого-либо связывающего домена, присутствующего в указанном втором транспортном полипептиде; при этом первый и второй полипептидный переносчик образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанного гетеродимера со стабильностью, сравнимой с нативным гомодимерным Fe.
[0040] В настоящем изобретении предложена гетеромультимерная конструкция, содержащая: первый мономер, содержащий первый полипептидный переносчик, соединенный с первым транспортным полипептидом, который содержит по меньшей мере один HER2-связывающий домен; второй мономер, содержащий второй полипептидный переносчик, отличный от указанного первого полипептидного переносчика, соединенный со вторым транспортным полипептидом полипептид, который содержит по меньшей мере один НЕК3-связывающий домен; при этом первый и второй полипептидные переносчики получают путем сегментирования альбумина таким образом, что указанные полипептидные переносчики самособираются с образованием квазинативного альбумина.
[0041] В настоящем изобретении предложена фармацевтическая композиция, содержащая выделенный мультиспецифический гетеромультимер согласно приведенному в настоящем документе определению и подходящее вспомогательное вещество. Также предложен способ получения такой фармацевтической композиции, включающий: культивирование клетки-хозяина в условиях, допускающих экспрессию гетеромультимера согласно приведенному в настоящем документе определению; выделение полученного гетеромультимера из культуры; и получение указанной фармацевтической композиции.
[0042]
[0043] В настоящем изобретении предложены клетки-хозяева, содержащие нуклеиновую кислоту, кодирующую гетеромультимер, описанный в настоящем документе. Согласно определенным вариантам реализации нуклеиновая кислота, кодирующая первый мономерный белок, и нуклеиновая кислота, кодирующая второй мономерный белок, входят в состав одного вектора. Согласно определенным вариантам реализации указанная нуклеиновая кислота, кодирующая первый мономерный белок, и нуклеиновая кислота, кодирующая второй мономерный белок, входят в состав отдельных векторов.
[0044] Также предложен набор, содержащий гетеромультимер согласно приведенному в настоящем документе определению и инструкции по его применению.
[0045]
[0046] КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0047]
[0048] Фиг. 1А-В: На фиг. 1А представлен пример схематического изображения гетеромультимерных конструкций согласно настоящему описанию. Так, для анти-CD3×CD19 конструкций на основе иммуноглобулинов показаны разные аспекты гетеромультимеров, например, на рисунке представлены первая и вторая полипептидные конструкции, отличающиеся тем, что первая полипептидная конструкция содержит СН3-связывающую конструкцию (черный), а вторая полипептидная конструкция содержит антигенсвязывающую конструкцию (синий). Согласно некоторым вариантам реализации указанная антигенсвязывающая конструкция отсутствует или заменена на конструкцию, представляющую собой стерический модулятор. Также представлен гетеромультимер Fc, образованный вариантами СН3-областей первой и второй полипептидных конструкций. Фиг. 1В иллюстрирует способность гетеромультимерной конструкции согласно описанию в настоящем документе (v873) и конструкции, которая не содержит гетеромультимер Fc (блинатумомаб CD19-CD3 BiTE (v891, МТ-103)), связывать Т-клетки Jurkat CD3 (Верхний левый сектор) и В-клетки Raji CD19 (нижний правый сектор), согласно FACS-анализу.
[0049] На фиг. 2 видно, что гетеромультимер, описанный в настоящем документе (v873), способен селективно связывать и соединяться с CD3-экспрессирующими Т-клетками Jurkat (нижнее правое поле) и с CD19-экспрессирующими В-клетками Raji (верхнее правое поле). На фиг. 2 также видно, что антитело против CD3 «с одним плечом» специфично связывается с Т-клетками Jurkat (нижние центральные поля) и не вступает в перекрестную реакцию с CD19-экспрессирующими В-клетками (верхние центральные поля), и что указанное антитело против CD 19 «с одним плечом» специфично связывается с В-клетками Raji (верхнее левое поле) и не вступает в перекрестную реакцию с Т-клетками Jurkat (нижнее левое поле).
[0050] Фиг. 3А-3В: Фиг. 3А иллюстрирует способность описанного в настоящем документе гетеромультимера (v873) перенаправлять активированные ИЛ-2 МКПК для киллинга целевых В-клеток Raji от 3 доноров. На фиг. 3В показано, что гетеромультимер, описанный в настоящем документе, способен опосредовать более высокую перенаправленную Т-клеточную цитотоксичность по сравнению с конструкцией, где отсутствует гетеродимерная Fc, у одного из доноров.
[0051] На фиг. 4 показано, что гетеромультимеры согласно описанию в настоящем документе способны связываться с CD3-экспрессирующими Т-клетками Jurkat и с CD19-экспрессирующими В-клетками Raji.
[0052] Фиг. 5А-5В: На фиг. 5А показано, что в протестированной концентрации v1092, который представляет собой гетеромультимер, описанный в настоящем документе, был способен связывать 31% от общего числа клеток, и v873, другая гетеромультимерная конструкция согласно описанию в настоящем документе, была способна связывать 25% от общего числа клеток. На фиг. 5В продемонстрировано, что v1092 способен связывать Т-клетки Jurkat и В-клетки Raji в большей степени, чем v221, и аналогично v891 и v873.
[0053] На фиг. 6 представлено терапевтическое антитело, которое может предлагаться вместе с гетеромультимером согласно описанию в настоящем документе для лечения при некоторых показаниях.
[0054] На фиг. 7 представлен анализ ДСН-ПААГ, показывающий, что примеры гетеромультимерных конструкций согласно описанию в настоящем документе транзиентно экспрессируются в клетках СНО3Е7 при жизнеспособности клеток, составляющей >80%.
[0055] На фиг. 8 показано, что гетеромультимер, описанный в настоящем документе (v873), индуцирует более высокий % цитотоксичности в отношении целевых В-клетки по сравнению с негативным контролем, IgG1 человека (G1), при сравнении индивидуальных доноров.
[0056] Фиг. 9А-9В: На фиг. 9А показано, что IgG человека (hIgG) не связывается с Т-клетками Jurkat и демонстрирует незначительное связывание с В-клетками Raji. На фиг. 9А также показано, что анти-CD19 конструкции с одним плечом селективно связываются с В-клетками Raji и не вступают в перекрестную реакцию с Т-клетками Jurkat. На фиг. 9В представлен FACS-анализ, показывающий, что гетеромультимер v873-a согласно описанию в настоящем документе селективно связывается с Т-клетками Jurkat и с В-клетками Raji.
[0057] На фиг. 10 показано, что гетеромультимер v873-a согласно описанию в настоящем документе не связывается с клетками линии К562, которые не экспрессируют CD19 или CD3.
[0058] На фиг. 11 показано, что гетеромультимер v873-a согласно описанию в настоящем документе не связывается с лимфоидными клетками мыши, которые не экспрессируют CD19 или CD3.
[0059] Фиг. 12.А-В: На фиг. 12А и Фиг. 12В представлены кривые связывания FACS гетеромультимерных конструкций согласно описанию в настоящем документе (v873, v875) и конструкции, в которой отсутствует гетеродимерная Fc (v891), с CD3-экспрессирующими Т-клетками HPB-ALL и CD3-экспрессирующими Т-клетками Jurkat, и с CD19-экспрессирующими В-клетками Raji.
[0060] Фиг. 13А-В: На фиг. 13А приведены кривые связывания FACS
гетеромультимерных конструкций v875, vl379, vl380, vi381, и контроля, v891, с CD19-экспрессирующими клетками Raji при тестировании в диапазоне от 0,1 до 300 нМ. На фиг. 13 В приведена кривая связывания FACS гетеромультимерных конструкций v875, v1379, vi380 с Т-клетками HBP-ALL при тестировании в диапазоне от 0,1 до 300 нМ.
[0061] На фиг. 14 видно, что гетеромультимерные конструкции согласно описанию в настоящем документе (v875 и v891) способствуют сопоставимому связыванию В-клеток Raji с Т-клетками Jurkat. Применение контрольного IgG человека приводило к 2,5% связыванию клеток Raji и Jurkat, тогда как v875 способствовал связыванию 22,9% от общего числа клеток, и v891 способствовал связыванию 14,5% от общего числа клеток.
[0062] Фиг. 15А-15В: На фиг. 15А приведена величина связывания при использовании Т-клеток и В-клеток в пропорции 1:1, при концентрациях гетеромультимеров, варьирующих от 0,3 нМ до 3 нМ. На фиг. 15 В приведена величина связывания при использовании Т-клеток и В-клеток в пропорции 15:1, при концентрациях гетеромультимеров, варьирующих от 0,3 нМ до 3 нМ. Обе пропорции Е:Т (1:1 и 15:1) при тестировании с v875 приводили к аналогичному общему связыванию Т-клеток с В-клетками при выражении в единицах кратности относительно фона.
[0063] Фиг. 16А-16Е: Фиг. 16А иллюстрирует способность v875, v1379 и v1380 опосредовать антителозависимую В-клеточную цитотоксичность за счет перенаправления CD4+ и CD8+ Т-клеток к В-клеткам Raji. На фиг. 16В-16Е представлены данные Фиг. 16А, нормализованные по IgG человека, для v875 (Фиг. 16 В и Фиг. 16С), и для v1379 и v1380 (Фиг. 16D и Фиг. 16Е), включая % цитотоксичности, указанный для каждой из протестированных концентраций антител.
[0064] Фиг. 17А-17В: На фиг. 17А показано, что блокирование Fc ИЛ-2-активированных МКПК приводит к небольшому снижению % цитотоксичности (v875) или не приводит (v873) к снижению % цитотоксичности для целевых В-клеток Raji. На фиг. 17В показано, что блокирование Fc покоящихся МКПК приводит к снижению % цитотоксичности для целевых В-клеток Raji для v875 и v873.
[0065] Фиг. 18А-18В: На фиг. 18А показано, что блокирование Fc ИЛ-2-активированных МКПК приводит к снижению % цитотоксичности для целевых В-клеток Raji при всех протестированных концентрациях антител для v875 и v873. На фиг. 18В показано, что блокирование Fc покоящихся МКПК приводит к снижению % цитотоксичности для целевых В-клеток Raji при всех протестированных концентрациях антител для v875 и v873.
[0066] Фиг. 19А-19В: На фиг. 19А показано, что v875 и v873 вызывают >30% цитотоксичность в отношении целевых В-клеток Raji, с ИЛ-2-активированными CD8+ Т-клетками в качестве эффекторов, и максимальный киллинг целевых клеток наблюдается при концентрации 3 нМ. На фиг. 19В показано, что v875 и v873 вызывают дозозависимую (>20%) цитотоксичность в отношении целевых В-клеток Raji покоящимися CD8+ Т-клетками в качестве эффекторов.
[0067] Фиг. 20А-20В: На фиг. 20А показана опосредованная v875 цитотоксичность в отношении целевых В-клеток Raji ИЛ-2-активированных CD4+ и CD8+ Т-клеток. На фиг. 20В показана опосредованная v875 цитотоксичность в отношении целевых В-клеток Raji покоящихся CD4+ и CD8+ Т-клеток.
[0068] На фиг. 21 показано, что относительно необработанной среды и контрольных IgG человека v875 и v873 (300 нМ) опосредуют киллинг аутологичных В-клеток в совокупности покоящихся МКПК и совокупности ИЛ-2-активированных МКПК.
[0069] На фиг. 22 показано, что относительно необработанной среды и контрольных IgG человека v875 обуславливает более избирательный киллинг В-клеток за счет удержания большего числа аутологичных Т-клеток по сравнению с v873 и v891.
[0070] Фиг. 23A-23D: Фиг. 23А показаны эффекты v875 на жизнеспособность субпопуляций CD20+, CD4+ , CD8+ в культурах ИЛ-2-активированных клеток. На фиг. 23В показаны эффекты v875 на жизнеспособность субпопуляций CD20+, CD4+ , CD8+ покоящихся клеточных культур. На фиг. 23С показаны эффекты v1379 и v1380 на жизнеспособность субпопуляций CD20+, CD4+ , CD8+ в ИЛ-2-активированных клеточных культурах. На фиг. 23D показаны эффекты v1379 и v1380 на жизнеспособность субпопуляций CD20+, CD4+ , CD8+ покоящихся клеточных культур.
[0071] Фиг. 24А-24В: Результаты опосредованного антителами высвобождения ЛДГ в покоящихся эффекторных клетках и В-клетках Raji, представленных на фиг. 24А. Результаты опосредованного антителами высвобождения ЛДГ в активированных эффекторах представлены на фиг. 24 В.
[0072] Фиг. 25A-25D: Фиг 25А иллюстрирует АЗКЦ, опосредуемый ритуксимабом и гетеромультимером, описанным в настоящем документе, с Fc дикого типа (v875) (максимальный лизис клеток ≈40%). На фиг. 25В показано, что v1379, который представляет собой гетеромультимер, описанный в настоящем документе, с Fc дикого типа способен опосредовать АЗКЦ, тогда как способность содержащего нокаутную мутацию Fc L234A L235A v1380 опосредовать направленный на В-клетки Daudi АЗКЦ нарушена. На фиг. 25C-25D представлены результаты анализа КЗЦ, опосредуемого v1380 и v1379 (Фиг. 25С), и v875 (Фиг. 25D), относительно целевых В-клеток Daudi, в сравнении с положительным контролем, ритуксимабом.
[0073] На фиг. 26 показано, что при концентрации 0,3 нМ v875 и v1380 не индуцируют пролиферацию МКПК по сравнению с IgG человека. На нижнем поле фиг. 26 представлены результаты для концентрации антител 100 нМ, и показано, что v875, vi380 и v891 индуцировали более высокие уровни пролиферации клеток относительно IgG человека. На фиг. 26 (нижнее поле) также показано, что при концентрации 100 нМ пролиферативный индекс для v875 был аналогичен индексу для анти-CD3 ОКТ3 во всех 4-х популяциях МКПК.
[0074] На фиг. 27А-27Е показано, что v1380 (нокаутная мутация Fc L234A_L235A) индуцирует меньшее высвобождение цитокинов ФНОα, ИФН-γ, ИЛ-2, ИЛ-4 и ИЛ-10 по сравнению с v875 (Fc дикого типа) и ОКТ3. Результаты анализа на высвобождение цитокинов согласно фиг. 27А-27Е включают сводные графики уровней в супернатанте МКПК ФНОα (Фиг. 27А) ИФН-γ (Фиг. 27В), ИЛ-2 (Фиг. 27С), ИЛ-4 (Фиг. 27D) и ИЛ-10 (Фиг. 27Е) после инкубирования с тестируемыми веществами в 0,3 нМ концентрациях на протяжении 4 дней (на оси у на графике представлены логарифм изированные уровни цитокинов в пг/мл от 4 доноров).
[0075] Фиг. 28А-28 В: представлены результаты оценки среднего индекса стимуляции, индуцируемой v875 в концентрации 0,3 нМ (Фиг. 28А) и 100 нМ (Фиг. 28В) у очищенных CD8+ Т-клеток в отсутствие или в присутствии очищенных CD19+ В-клеток в момент времени через 4 дня инкубирования.
[0076] Фиг. 29А-29В: представлены результаты оценки среднего индекса стимуляции, индуцируемой v1380 в концентрации 0,3 нМ (Фиг. 29А) и 100 нМ (Фиг. 29В) у очищенных CD8+ Т-клеток в отсутствие или в присутствии очищенных CD19+ В-клеток в момент времени через 4 дня инкубирования.
[0077] Фиг. 30А-30С: представлены результаты микроскопического исследования связывания Т-клеток с В-клетками, со сравнением v875 и IgG человека (3 нМ) при увеличении 200х и 400х. На фиг. 30А приведено прямое сравнение IgG человека и v875 при увеличении 200х и демонстрируется большая величина визуально наблюдаемого связывания между В-клетками Raji и Т-клетками Jurkat по сравнению с IgG человека. На фиг. 30В и Фиг. 30С представлены два поля зрения для v875 (Фиг. 30В) и IgG человека (Фиг. 30С) при увеличении 400×.
[0078] Фиг. 31А-31В: на фиг. 31А показан анализ ДСН-ПААГ и относительная чистота v875, v1380, v1379 и v891 после очистки с использованием белка А и ЭХ, и последующего хранения в течение 47 дней при 4°С. На фиг. 31В показан анализ ДСН-ПААГ и относительная чистота дополнительных примеров гетеромультимеров, включая v875, v1653, v1654, v1655, v1656, v1660, v1800, и v1802 после очистки с использованием белка А и ЭХ.
[0079] На фиг. 32 представлены результаты ЖХ-МС для профилей молекулярной массы v875, полученных с помощью Max Ent.
[0080] Фиг. 33А-33С: представлены результаты ДСК для гетеромультимерных конструкций согласно описанию в настоящем документе, показывающие, что v875 имеет расчетную Tm СН3>76°С (Фиг. 33А), v1380 имеет расчетную Tm СН3>82,3°С, и v1379 имеет расчетную Tm СН3>82,5°С (Фиг. 33С).
[0081] Фиг. 34А-С: демонстрируют способность гетеромультимеров согласно описанию в настоящем документе связывать В-клетки Raji с Т-клетками Jurkat (В:Т),. а также В-клетки RajirRaji (В:В) и Т-клетки Jurkat:Jurkat (Т:Т), по оценке с применением FACS. На фиг. 34А представлены величины связывания Т:В, В:В и Т:Т для v875, v1379, v1380, v891, v1381, коммерческих ОКТ3 и IgG человека при проведении экспериментов в трех повторностях. На фиг. 34В представлены величины связывания Т:В, В:В и Т:Т для вариантов, содержащих сконструированные участки с направленным действием против CD3 для повышения стабильности (v1653, v1654, v1655, v1656, v1660, v1800, v1802) и v875, и IgG человека. На фиг. 34C представлены величины связывания Т:В, В:В и Т:Т для нокаутных вариантов Fc, содержащих либо сконструированные участки с направленным действием против CD3 для повышения стабильности (v1666), либо перекрестно-реактивные анти-CD3 и анти-CD19 scFv человека/яванского макака (v4541, v4543, v4545, v4548), контрольного коммерческого анти-CD3OKT3, контрольного v2176 против CD19 и негативного контроля - IgG человека; все варианты опосредуют незначительное связывание Т:Т.
[0082] Фиг. 35 иллюстрирует связывание гетеромультимеров согласно описанию в настоящем документе с CD3 человека (верхнее поле) и связывание с CD3-рецептором яванского макака (нижнее поле), по оценке с помощью ELISA.
[0083] Фиг. 36А-36 В: иллюстрируют аффинность, с использованием линейной и логарифмической шкалы, соответственно, конструкции HER2/HER3 с гетеродимерной Fc, демонстрирующей как биспецифичность, так и авидность.
[0084] Фиг. 37 иллюстрирует связывание варианта 1090 по сравнению с контролем 1087 в клетках MALME-3M и показывает, что связывание v1090 с целевыми клетками MALME-3M аналогично связыванию v1087.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0085] Если не указано иное, все технические и научные термины в настоящем документе имеют значения, общепринятые среди специалистов в областях техники, к которым относится заявленный объект изобретения. В тех случаях, когда существует несколько определений приводимых терминов, преимущественную силу будут иметь определения, приводимые в данном разделе. При указании ссылок на веб-страницы (URL) или использовании другого такого идентификатора или адреса, подразумевается, что такие идентификаторы могут изменяться и конкретная доступная онлайн-информация может появляться и исчезать, однако в сети Интернет может быть найдена эквивалентная информация. Ссылки на них свидетельствуют о доступности и публичном распространении такой информации.
[0086] Следует понимать, что вышеприведенное общее описание и приведенное ниже подробное описание являются иллюстративными и пояснительными, и не ограничивают какие-либо из заявленных объектов изобретения. В данной заявке применение терминов в единственном числе включает и множественное число, если конкретным образом не указано иное.
[0087] Значения каждого из терминов, понятные специалистам в области технологии антител, соответствуют принятым в данной области техники, если иное явным образом не указано в настоящем документе. Известно, что антитела содержат вариабельные области, шарнирную область и константные домены. Обзор структура и функции иммуноглобулинов приведен, например, в источнике: Harlow et al, Eds., Antibodies: A Laboratory Manual, Chapter 14 (Cold Spring Harbor Laboratory, Cold Spring Harbor, 1988).
[0088] В настоящем описании подразумевается, что любой диапазон концентраций, процентный диапазон, диапазон отношений или диапазон целочисленных значений включает значение любого целого числа в указанном диапазоне и, в соответствующих случаях, его долей (например, одну десятую или одну сотую часть целого числа), если не указано иное. В настоящем документе «приблизительно» означает ±10% от указанного диапазона, величины, последовательности или структуры, если не указано иное. Следует понимать, что термины, приводимые в настоящем документе в единственном числе, подразумевают «один или большее количество» перечисленных компонентов, если не указано или не определено контекстом иное. Применение противопоставления (например, с помощью союза «или») подразумевает включение одного, обоих или любой комбинации указанных противопоставленных объектов. В настоящем документе термины «включать» и «содержать» являются синонимами. Кроме того, следует понимать, что индивидуальные одноцепочечные полипептиды или иммуноглобулиновые конструкции, полученные в результате различных комбинаций структур и заместителей согласно описанию в настоящем документе, раскрыты в настоящем описании в той же степени, как если бы каждый одноцепочечный полипептид или гетеродимер был указан индивидуально. Таким образом, конкретные выбранные компоненты для получения индивидуальных одноцепочечных полипептидов или гетеродимеров входят в объем изобретения, раскрытого в настоящем описании.
[0089] Названия разделов в настоящем документе носят исключительно организационный характер и не предназначены для ограничения заявленного предмета изобретения. Все документы или фрагменты документов, цитируемые в настоящей заявке, включая, но не ограничиваясь перечисленными, патенты, патентные заявки, статьи, книги, руководства и научные труды в явной форме включены в настоящий документ включены посредством ссылок полностью для любых целей.
[0090] Следует понимать, что способы и композиции согласно описанию в настоящем документе не ограничиваются конкретными методами, протоколами, клеточными линиями, конструкциями и реагентами согласно описанию в настоящем документе и, соответственно, могут варьировать. Следует также понимать, что терминология, используемая в настоящем документе, используется исключительно для описания конкретных вариантов реализации, и не предназначена для ограничения объема способов и композиций согласно описанию в настоящем документе, ограниченного исключительно прилагаемой формулой изобретения.
[0091] Все упоминаемые в настоящем документе публикации и патенты включены в настоящую заявку полностью посредством ссылок с целью описания и раскрытия, например, конструкций и методов, описанных в публикациях, которые могут быть использованы в сочетании со способами, композициями и соединениями согласно описанию в настоящем документе. Публикации, обсуждаемые в данном документе, приведены исключительно ввиду их раскрытия до даты подачи настоящей заявки. Никакой фрагмент настоящего документа не должен толковаться как допущение того, что авторы настоящего изобретения согласно описанию в настоящем документе не имеют права датировать задним числом такое раскрытие на основании предшествующего изобретения или по любой другой причине.
[0092] В настоящей заявке используются названия аминокислот и наименования атомов (например, N, О, С и т.д.) согласно базе Protein DataBank (PDB) (www.pdb.org), основанной на номенклатуре IUPAC (IUPAC Nomenclature and Symbolism for Amino Acids and Peptides (названия остатков, наименования атомов и т.д.), Eur. J. Biochem., 138, 9-37 (1984), с поправками в Eur. J. Biochem., 152, 1 (1985).
[0093] Термины «полипептид», «пептид» и «белок» используются в настоящем документе взаимозаменяемо, обозначая полимер из аминокислотных остатков, т.е. описание, относящееся к полипептиду, в равной степени применимо к описанию пептида и описанию белка, и наоборот. Указанные термины применимы к встречающимся в природе аминокислотным полимерам, а также аминокислотным полимерам, где один или несколько остатков аминокислот представляют собой не кодируемые в природе аминокислотны. В настоящем документе указанные термины охватывают аминокислотные цепи любой длины, включая полноразмерные белки, где остатки аминокислот соединены ковалентными пептидными связями.
[0094] Термин «нуклеотидная последовательность» предназначен для обозначения непрерывного отрезка из двух или более молекул нуклеотидов. Происхождение нуклеотидной последовательности может быть геномным, кДНК, РНК, полусинтетическим или синтетическим, или представлять собой любую их комбинацию.
[0095] Термин «полимеразная цепная реакция» или «ПЦР», как правило, относится к способу амплификации нужной нуклеотидной последовательности in vitro, согласно описанию, например, в патенте США №4683195. В целом, метод ПЦР включает многократные синтетические циклы удлинения праймеров с применением олигонуклеотидных праймеров, способных преимущественно гибридизоваться с нуклеиновокислотной матрицей.
[0096] Термины «клетка», «клетка-хозяин», «линия клеток» и «клеточная культура» используются в настоящем документе взаимозаменяемо, и все такие термины подразумевают включение потомства, получаемого в результате роста или культивирования клетки. «Трансформация» и «трансфекция» используются взаимозаменяемо и обозначают процесс введения ДНК в клетку.
[0097] Термин «аминокислота» относится к встречающимся в природе и не встречающимся в природе аминокислотам, а также аналогам аминокислот и миметикам аминокислот, функционирующим аналогичным встречающимся в природе аминокислотам образом. Кодируемые в природе аминокислотны представлены 20-ю распространенными аминокислотами (аланин, аргинин, аспарагин, аспарагиновая кислота, цистеин, глутамин, глутаминовая кислота, глицин, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин, серии, треонин, триптофан, тирозин, и валин) и пирролизином и селеноцистеином. Аналоги аминокислот относятся к соединениям, обладающим такой же основной химической структурой, что и встречающиеся в природе аминокислотны, т.е. содержащие атомы углерода, связанные с атомами водорода, карбоксильные группы, аминогруппы и R-группы, например, гомосерин, норлейцин, метионинсульфоксид, метилметионинсульфоний. Такие аналоги содержат модифицированные R-группы (например, норлейцин) или модифицированные пептидные остовы, но сохраняют ту же основную химическую структуру, что и встречающиеся в природе аминокислотны. Ссылка на аминокислоту включает, например, встречающиеся в природе протеогенные L-аминокислотны; D-аминокислотны, химически модифицированные аминокислотны, например, варианты и производные аминокислот; встречающиеся в природе не протеогенные аминокислотны, такие как □-аланин, орнитин и т.д.; и химически синтезированные соединения, имеющие свойства, известные в данной области техники как характерные для аминокислот.Примеры не встречающихся в природе аминокислот включают, не ограничиваясь перечисленными, □-метил-аминокислотны (например, □ □ метил аланин), D-аминокислотны, гистидиноподобные аминокислотны (например, 2-аминогистидин, D-гидроксигистидин, гомогистидин), аминокислотны, содержащие дополнительный метилен на боковой цепи («гомоаминокислотны»), и аминокислотны, в которых карбоновая кислота функциональной группы на боковой цепи заменена на группу сульфоновой кислоты (например, цистеиновой кислоты). Включение отсутствующих в природе аминокислот, включая синтетические отсутствующие в природе аминокислотны, замещенных аминокислот или одной или нескольких D-аминокислот в белки согласно настоящему изобретению может быть благоприятным во многих отношениях. Содержащие D-аминокислотны пептиды и т.п. проявляют повышенную стабильность in vitro или in vivo по сравнению с содержащими L-аминокислотны аналогами. Таким образом, создание пептидов и т.п., включающих D-аминокислотны, может быть полезным, в частности, в тех случаях, когда желательна или требуется большая внутриклеточная стабильность. В частности, D-пептиды и т.п. резистентны к эндогенным пептидазам и протеазам, обеспечивая за счет этого улучшенную биодоступность молекулы и более продолжительные периоды полужизни in vivo в тех случаях, когда желательны такие свойства. Кроме того, D-пептиды и т.п.не могут быть эффективно процессированы для ограниченного главным комплексом гистосовместимости класса II презентирования Т-хелперным клеткам, и, соответственно, с меньшей вероятностью будут индуцировать гуморальный иммунный ответ организма в целом.
[0098] Аминокислотны могут обозначаться в настоящем документе либо общеизвестными трехбуквенными обозначениями, либо однобуквенными символами, рекомендованными комиссией по биохимической номенклатуре ИЮПАК (IUPAC-IUB). Аналогичным образом, нуклеотиды могут обозначаться с помощью общепринятых однобуквенных кодов.
[0099] Термин «консервативно модифицированные варианты» относится как к аминокислотным последовательностям, так и к последовательностям нуклеиновых кислот. В отношении конкретных нуклеиновокислотных последовательностей «консервативно модифицированные варианты» относятся к нуклеиновым кислотам, кодирующим идентичные или по существу идентичные последовательности аминокислот, или, в случае такой нуклеиновой кислоты, которая не кодирует аминокислотную последовательность, к по существу идентичным последовательностям. Ввиду вырожденности генетического кода, любой заданный белок кодируется значительным числом функционально идентичных нуклеиновых кислот. Например, каждый из кодонов GCA, GCC, GCG и GCU кодирует аминокислоту аланин. Таким образом, в каждом положении, где некоторым кодоном задан аланин, указанный кодон может быть заменен на любой из соответствующих описанных кодонов без изменения кодируемого полипептида. Такие варианты нуклеиновых кислот являются «молчащими вариантами», представляющими собой один из видов вариантов с консервативными модификациями. Каждая описанная в настоящем документе последовательность нуклеиновой кислоты, которая кодирует полипептид, также описывает все возможные молчащие варианты указанной нуклеиновой кислоты. Специалисту в данной области техники будет понятно, что каждый кодон в нуклеиновой кислоте (кроме AUG, который в норме кодоном для метионина, и TGG, который в норме является единственным кодоном для триптофана) может быть модифицирован с получением функционально идентичной молекулы. Соответственно, подразумевается, что каждый молчащий вариант нуклеиновой кислоты, кодирующий полипептид, включен в каждую описанную последовательность.
[00100] Что касается последовательностей аминокислот, специалисту в данной области техники будет понятно, что индивидуальные замены, удаления или добавления в нуклеиновой кислоте, пептиде, полипептиде или белковой последовательности, которые изменяют, добавляют или удаляют одну аминокислоту или незначительный процент аминокислот в кодируемой последовательности, представляют собой «консервативно модифицированный вариант» в тех случаях, когда указанное изменение приводит к удалению аминокислотны, добавлению аминокислотны или замене аминокислотны химически аналогичной аминокислотой. Таблицы консервативных замен, где приведены функционально аналогичные аминокислотны, известны среднему специалисту в данной области техники. Такие консервативно модифицированные варианты дополняют и не исключают полиморфные варианты, межвидовые гомологи и аллели согласно настоящему изобретению.
[00101] Таблицы консервативных замен, где приведены функционально аналогичные аминокислотны, известны среднему специалисту в данной области техники. Каждая из следующих восьми групп содержит аминокислотны, являющиеся друг для друга консервативными заменами:
[00102] 1) Аланин (А), Глицин (G);
[00103] 2) Аспарагиновая кислота (D), Глутаминовая кислота (Е);
[00104] 3) Аспарагин (N), Глутамин (Q);
[00105] 4) Аргинин (R), Лизин (К);
[00106] 5) Изолейцин (I), Лейцин (L), Метионин (М), Валин (V);
[00107] 6) Фенилаланин (F), Тирозин (Y), Триптофан (W);
[00108] 7) Серии (S), Треонин (Т); и [0139] 8) Цистеин (С), Метионин (М)
[00109] (см., например, Creighton, Proteins: Structures and Molecular Properties (W H Freeman & Co.; 2nd edition (December 1993)
[00110] Термины «идентичный» или процент «идентичности» в контексте двух или более нуклеиновых кислот или полипептидных последовательностей относятся к двум или более последовательностям или субпоследовательностям, которые являются одинаковыми. Последовательности «по существу идентичны», если они содержат некоторый процент одинаковых аминокислотных остатков или нуклеотидов (т.е. приблизительно на 50% идентичны, приблизительно на 55% идентичны, на 60% идентичны, приблизительно на 65%, приблизительно на 70%, приблизительно на 75%, приблизительно на 80%, приблизительно на 85%, приблизительно на 90% или приблизительно на 95% идентичны на заданном участке) при сравнении и выравнивании с максимальным соответствием в окне сравнения или на протяжении заданного участка, по оценке с применением одного из следующих алгоритмов сравнения последовательностей (или других алгоритмов, доступных для среднего специалиста в данной области техники), или с помощью выравнивания вручную и визуального анализа. Указанное определение также относится к последовательности, комплементарной тестируемой. Идентичность может иметь место для области, длина которой составляет по меньшей мере приблизительно 50 аминокислот или нуклеотидов, или области, длина которой составляет 75-100 аминокислот или нуклеотидов, или, если не указана конкретная длина, для всей последовательности полинуклеотида или полипептида. Полинуклеотид, кодирующий полипептид согласно настоящему изобретению, включая гомологи видов, не являющихся человеком, могут быть получены способом, включающим этапы скрининга библиотеки в строгих условиях гибридизации с меченым зондом, содержащим полинуклеотидную последовательность согласно настоящему изобретению или ее фрагмент, и выделение полноразмерной кДНК и геномных клонов, содержащих указанную полинуклеотидную последовательность. Такие техники гибридизации хорошо известны специалистам в данной области техники.
[00111] О производном или варианте полипептида говорят, что он обладает «гомологией» или «гомологичен» пептиду, если последовательности аминокислот указанного производного или варианта по меньшей мере на 50% идентичны последовательности длиной 100 аминокислот исходного пептида. Согласно определенным вариантам реализации производное или вариант по меньшей мере на 75% идентичен либо пептиду, либо фрагменту пептида, содержащему то же количество аминокислотных остатков, что и указанное производное. Согласно определенным вариантам реализации производное или вариант по меньшей мере на 85% идентичен либо пептиду, либо фрагменту указанного пептида, содержащему то же количество аминокислотных остатков, что и указанное производное. Согласно определенным вариантам реализации аминокислотная последовательность указанного производного по меньшей мере на 90% идентичная последовательности пептида или фрагмента указанного пептида, содержащей то же количество аминокислотных остатков, что и указанное производное. Согласно некоторым вариантам реализации аминокислотная последовательность указанного производного по меньшей мере на 95% идентична пептиду или фрагменту пептида содержащих то же количество аминокислотных остатков, что и указанное производное. Согласно определенным вариантам реализации производное или вариант по меньшей мере на 99% идентичен последовательности либо пептида, либо фрагмента пептида, содержащей то же количество аминокислотных остатков, что и указанное производное.
[00112] Предполагается, что термин «биспецифический» включает любой агент, например, гетеромультимер, мономер, белок, пептид, или белковый или пептидный комплекс, обладающий двумя разными видами связывающей специфичности. Например, согласно некоторым вариантам реализации указанная молекула может связываться или взаимодействовать с (а) поверхностной молекулой целевых клеток и (b) Fc-рецептором на поверхности эффекторной клетки. Согласно определенным вариантам реализации описанного в настоящем документе гетеромультимера по меньшей мере один мономер является биспецифическим и образован путем присоединения к одному и тому же полипептидному переносчику двух транспортных молекул с разной связывающей специфичностью. Согласно определенным вариантам реализации описанного в настоящем документе гетеромультимера указанный гетеромультимер сам по себе является биспецифическим и образован путем присоединения к полипептидным переносчикам по меньшей мере двух транспортных молекул с разной специфичностью.
[00113] Предполагается, что термин «мультиспецифический» или «гетероспецифичный» включает любой агент, например, белок, пептид, или белковый или пептидный комплекс, который обладает более чем двумя разными видами связывающей специфичности. Например, указанная молекула может связываться или взаимодействовать с (а) поверхностной молекулой целевых клеток, например, но не ограничиваясь указанным, антигенами клеточной поверхности, (b) Fc-рецептором на поверхности эффекторной клетки и необязательно (с) по меньшей мере одним другим компонентом. Соответственно, варианты реализации гетеромультимеров согласно описанию в настоящем документе включают, не ограничиваясь перечисленными, биспецифические, триспецифические, тетраспецифические и другие мультиспецифические молекулы. Согласно определенным вариантам реализации указанные молекулы нацелены на антигены клеточной поверхности, такие как CD30, и другие мишени, такие как Fc-рецепторы на эффекторных клетках.
[00114] В настоящем документе «выделенный» гетеромультимер означает гетеромультимер, который был идентифицирован и отделен от и/или выделен из компонента естественной среды клеточной культуры. Загрязняющие компоненты естественной среды представлены материалами, которые мешают диагностическому или терапевтическому применению указанного гетеромультимера, и могут включать ферменты, гормоны и другие белковые или не белковые растворенные компоненты.
[00115] Выражение «селективно (или специфично) гибридизуется» относится к связыванию, спариванию или гибридизации молекул исключительно с конкретной нуклеотидной последовательностью в строгих условиях гибридизации, когда указанная последовательность присутствует в комплексной смеси (включая, но не ограничиваясь указанным, в тотальной ДНК или РНК клетки или библиотеки).
[00116] Выражение «строгие условия гибридизации» относится к гибридизации последовательностей ДНК, РНК или других нуклеиновых кислот, или их комбинаций в условиях низкой ионной силы и высокой температуры, как известно в данной области техники. Как правило, в строгих условиях зонд гибридизуется с целевой субпоследовательностью в комплексной смеси нуклеиновых кислот (включая, но не ограничиваясь перечисленными, тотальную ДНК или РНК клетки или библиотеки), но не гибридизуется с другими последовательностями в комплексной смеси. Строгие условия зависят от последовательности и различаются в разных обстоятельствах. Более длинные последовательности гибридизуются специфично при более высоких температурах. Обширное руководство по гибридизации нуклеиновых кислот содержится в источнике: Tijssen, Laboratory Techniques in Biochemistry and Molecular Biology-Hybridization with Nucleic Probes, «Overview of principles of hybridization and the strategy of nucleic acid assays» (1993).
[00117] В настоящем документе «антитело» или «иммуноглобулин» относится к полипептиду, по существу кодируемому иммуноглобулиновым геном или иммуноглобулиновыми генами, или его фрагментами, которые специфично связываются и распознают аналит (антиген). Известные иммуноглобулиновые гены включают гены константных областей каппа, лямбда, альфа, гамма, дельта, эпсилон и мю, а также большое количество иммуноглобулиновых генов вариабельных областей. Легкие цепи подразделяются на каппа и лямбда. Тяжелые цепи подразделяются на гамма, мю, альфа, дельта или эпсилон, которые в свою очередь определяют классы иммуноглобулинов, IgG, IgM, IgA, IgD и IgE, соответственно.
[00118] Примерная структурная единица иммуноглобулина (антитела) состоит из двух пар полипептидных цепей, каждая пара содержит одну «легкую» (приблизительно 25 кДа) и одну «тяжелую» цепь (приблизительно 50-70 кДа). N-концевой домен каждой цепи определяет вариабельную область длиной приблизительно 100-110 или более аминокислот, в первую очередь отвечающие за распознавание антигена. Термины «вариабельная легкая цепь» (VL) и «вариабельная тяжелая цепь» (VH) относятся к указанным доменам легкой и тяжелой цепей, соответственно. Тяжелая цепь IgG1 содержит домены VH, CH1, СН2 и СН3, соответственно, в направлении от N-конца к С-концу. Легкая цепь содержит домены VL и CL в направлении от N-конца к С-концу. Тяжелая цепь IgG1 содержит шарнир между доменами СН1 и СН2. Согласно определенным вариантам реализации иммуноглобулиновые конструкции содержат по меньшей мере один иммуноглобулиновый домен из IgG, IgM, IgA, IgD, или IgE, соединенный с терапевтическим полипептидом. Согласно некоторым вариантам реализации иммуноглобулиновый домен, входящий в состав иммуноглобулиновой конструкции согласно настоящему описанию, получен из конструкции на основе иммуноглобулина, такой как диатело или нанотело. Согласно определенным вариантам реализации иммуноглобулиновые конструкции согласно описанию в настоящем документе содержат по меньшей мере один иммуноглобулиновый домен антитела, содержащего только тяжелые цепи, такого как антитело камелидов. Согласно определенным вариантам реализации иммуноглобулиновые конструкции согласно настоящему описанию содержат по меньшей мере один иммуноглобулиновый домен антитела млекопитающих, такого как бычье антитело, антитело человека, антитело камелидов, антитело мыши или любое гибридное антитело.
[00119] В настоящем документе термин «антигенная детерминанта» является синонимом «антигена» и «эпитопа» и относится к участку (например, непрерывному отрезку последовательности аминокислот или конформационной конфигурации, обусловленной разными областями не являющегося непрерывным отрезка последовательности аминокислот) полипептидной макромолекулы, с которым связывается антигенсвязывающий фрагмент, образуя комплекс антигенсвязывающий фрагмент/антиген. Подходящие антигенные детерминанты могут быть обнаружены, например, на поверхности опухолевых клеток, на поверхности инфицированных вирусом клеток, на поверхности других пораженных заболеванием клеток, на поверхности иммунных клеток, в свободном состоянии в сыворотке крови и/или во внеклеточном матриксе (ВКМ). Белки, называемые в настоящем описании антигенами (например, MCSP, FAP, CEA, EGFR, CD33, CD3) могут быть представлены любой нативной формой белков любых позвоночных животных, включая млекопитающих, таких как приматы (например, человека) и грызуны (например, мыши и крысы), если не указано иное. Согласно конкретному варианту реализации указанный антиген представляет собой белок человека. В отношении конкретного белка при его упоминании в настоящем описании указанный термин охватывает «полноразмерный» непроцессированный белок, а также любую форму указанного белка, образующуюся в клетке в результате процессинга. Указанный термин также охватывает встречающиеся в природе варианты указанного белка, например, варианты сплайсинга или аллельные варианты. Примеры белков человека, подходящих в качестве антигенов, включают, не ограничиваясь перечисленными: связанный с меланомой протеогликан хондроитинсульфат (MCSP), также известный как протеогликан хондроитинсульфат 4 (UniProt № Q6UVK1 (версия 70), стандартную последовательность NCBI № NP 001888.2); белок активации фибробластов (FAP), также известный как сепраза (UniProt № Q12884, № Q86Z29, № Q99998, № доступа в NCBI NP 004451); раковоэмбриональный антиген (РЭА), также известный как связанная с карциноэмбриональным антигеном молекула клеточной адгезии 5 (UniProt № Р06731 (версия 119), стандартную последовательность NCBI № NP 004354.2); CD33, также известный как gp67, или связывающий сиаловую кислоту иммуноглобулиноподобный лектин-3 (Siglec-3) (UniProt №Р20138, номера доступа NCBI NP 001076087, NP 001171079); рецептор эпидермального фактора роста (EGFR), также известный как ЕгЬВ-1 или Herí (UniProt № Р0053, NCBI №№ доступа NP 958439, NP 958440), и CD3, в частности, эпсилон-субъединицу CD3 (см. UniProt № Р07766 (версия 130), стандартную последовательность NCBI № NP 000724.1, SEQ ID NO: 265 - последовательность человека; или UniProt №Q95LI5 (версия 49), NCBI GenBank № BAB71849.1, SEQ ID NO: 266 - последовательность яванского макака [Macaca fascicularis]). Согласно определенным вариантам реализации активирующая Т-клетки биспецифическая антигенсвязывающая молекула согласно настоящему изобретению связывается с эпитопом активирующего Т-клеточного антигена или антигеном целевой клетки, сохраняющим консервативность среди активирующих Т-клеточных антигенов или целевых антигенов разных видов.
[00120] Под «специфическим связыванием» или «селективным связыванием» подразумевается, что связывание происходит избирательно в отношении указанного антигена, позволяя избежать нежелательного или неспецифического взаимодействия. Способность антигенсвязывающего фрагмента связываться с конкретной антигенной детерминантой может быть измерена либо с помощью иммуносорбентного ферментного анализа (ELISA) или других техник, известных специалистам в данной области техники, например, техники поверхностного плазмонного резонанса (ППР) (анализ с помощью инструмента BIAcore) (Liljeblad et al, Glyco J 17, 323-329 (2000)), и традиционных анализов на связывание (Heeley, Endocr Res 28, 217-229 (2002)). Согласно одному из вариантов реализации степень связывания антигенсвязывающего фрагмента с посторонним белком составляет менее чем приблизительно 10% от связывания указанного антигенсвязывающего фрагмента с антигеном, по оценке, например, с помощью ППР. Согласно определенным вариантам реализации антигенсвязывающий фрагмент, который связывается с антигеном, или антигенсвязывающая молекула, содержащая такой антигенсвязывающий фрагмент, обладает константой диссоциации (KD), составляющей <1 мкМ, <100 нМ, <10 нМ, <1 нМ, <0,1 нМ, <0,01 нМ, или <0,001 нМ (например, 10~8 M или менее, например, от 10~8 M до 10''13 М, например, от 10''9 M до 10''13 М).
[00121] «Аффинность/сродство связывания» относится к силе всей совокупности нековалентных взаимодействий между одним связывающим участком молекулы (например, рецептора) и его партнером для связывания (например, лигандом). Если не указано иное, в настоящем документе «сродство к связыванию» относится к собственному сродству к связыванию, которое отражает взаимодействие 1:1 между участниками связывающейся пары (например, антигенсвязывающего фрагмента и антигена, или рецептора и его лиганда). Аффинность молекулы × в отношении ее партнера Υ, как правило, может быть выражена через константу диссоциации (KD), которая представляет собой отношение констант скорости диссоциации и связывания (k0ff и kon, соответственно). Таким образом, эквивалентные значения аффинности могут включать разные константы скорости, если отношение констант скорости остается одинаковым. Аффинность может быть измерена с применением общепринятых способов, известных в данной области техники, включая описанные в настоящем документе. Конкретный способ измерения аффинности представлен поверхностным плазмонным резонансом (ППР).
[00122] «Пониженное связывание», например, пониженное связывание с Fc-рецептором, относится к уменьшению аффинности в отношении соответствующего взаимодействия, по оценке, например, с применением ППР. Для ясности термин включает также снижение аффинности до нулевой (или ниже предела чувствительности метода анализа), т.е. полное отсутствие взаимодействия. В свою очередь, «повышенное связывание» относится к повышению сродства к связыванию для соответствующего взаимодействия.
[00123] «Активирующий Т-клеточный антиген» в настоящем документе относится к антигенной детерминанте, экспрессируемой на поверхности Т-лимфоцита, в частности, цитотоксического Т-лимфоцита, которая способна индуцировать активацию Т-клеток при взаимодействии с антигенсвязывающей молекулой. В частности, взаимодействие антигенсвязывающей молекулы с активирующим Т-клеточным антигеном может индуцировать активацию Т-клеток, запуская сигнальный каскад Т-клеточного рецепторного комплекса. Согласно конкретному варианту реализации указанный активирующий Т-клеточный антиген представляет собой CD3.
[00124] «Активация Т-клеток» в настоящем документе относится к одному или нескольким клеточным ответам Т-лимфоцита, в частности, цитотоксического Т-лимфоцита, выбранным из: пролиферации, дифференцировки, секреции цитокинов, высвобождения цитотоксических эффекторных молекул, цитотоксической активности и экспрессии маркеров активации. Активирующие Т-клетки биспецифические антигенсвязывающие молекулы согласно настоящему изобретению способны индуцировать активацию Т-клеток. Подходящие анализы для измерения активации Т-клеток известны в описываемых в настоящем документе областях техники.
[00125] «Антиген целевой клетки» в настоящем документе относится к антигенной детерминанте, презентированной на поверхности целевой клетки, например, В-клетки в опухоли, например, раковой клетки или клетки стромы опухоли. В настоящем документе термины «первый» и «второй» в отношении антигенсвязывающих фрагментов и т.п.используются для удобства различения при наличии более чем одного фрагмента каждого типа. Применение указанных терминов не предназначено для обозначения конкретной природы или ориентации активирующей Т-клетки биспецифической антигенсвязывающей молекулы, если явным образом не указано иное.
[00126] «Молекула Fab » относится к белку, состоящему из доменов VH и СН1 тяжелой цепи («Fab тяжелой цепи») и доменов VL и CL легкой цепи («Fab легкой цепи») иммуноглобулина.
[00127] Под «гибридом/соединением» подразумеваются компоненты (например, молекула Fab и субъединица Fc-домена), связанные пептидными связями, либо непосредственно, либо с помощью одного или нескольких пептидных линкеров.
[00128] В настоящем документе термин «одноцепочечный» относится к молекуле, содержащей аминокислотные мономеры, линейно соединенные пептидными связями. Согласно определенным вариантам реализации один из антигенсвязывающих фрагментов представляет собой одноцепочечную молекулу Fab, т.е. молекулу Fab, где легкая цепь Fab и тяжелая цепь Fab соединены пептидным линкером с образованием одной пептидной цепи. Согласно одному такому конкретному варианту реализации С-конец легкой цепи Fab соединен с N-концом тяжелой цепи Fab в одноцепочечной молекуле Fab. Согласно некоторым другим вариантам реализации один из антигенсвязывающих фрагментов представляет собой одноцепочечную молекулу Fv
[00129] Под «кроссоверной» молекулой Fab (также называемой «Crossfab») понимают молекулу Fab, отличающуюся тем, что либо вариабельные области, либо константные области указанных тяжелой и легкой цепей Fab рекомбинированы, т.е. кроссоверная молекула Fab содержит пептидную цепь, состоящую из вариабельной области легкой цепи и константной области тяжелой цепи, и пептидную цепь, состоящую из вариабельной области тяжелой цепи и константной области легкой цепи. Для ясности, в кроссоверной молекуле Fab, где рекомбинированы вариабельные области легкой цепи Fab и тяжелой цепи Fab, пептидная цепь, содержащая константную область тяжелой цепи, в настоящем описании называется «тяжелой цепью» кроссоверной молекулы Fab. В свою очередь, в кроссоверной молекуле Fab, где рекомбинированы константные области легкой цепи Fab и тяжелая цепь Fab, пептидная цепь, содержащая вариабельную область тяжелой цепи, в настоящем описании называется «тяжелой цепью» кроссоверной молекулы Fab.
[00130] «Каркас» или «FR» относится к остаткам вариабельного домена, не являющимся остатками гипервариабельной области (HVR). FR вариабельного домена, как правило, состоит из четырех FR доменов: FR1, FR2, FR3 и FR4. Соответственно, последовательности HVR и FR, как правило, появляются в следующей последовательности в VH (или VL): FR1-H1(L1)-FR2-H2(L2)-FR3-H3(L3)-FR4.
[00131] «Класс» антитела или иммуноглобулина относится к типу константного домена или константной области, обусловленного его тяжелой цепью. Существует пять основных классов антител: IgA, IgD, IgE,
[00132] IgG, и IgM, и некоторые из указанных классов могут дополнительно подразделяться на подклассы (изотипы), например, IgGi, IgG2, IgG3, IgG4, IgAi и IgA2. Константные домены тяжелых цепей, соответствующие разным классам иммуноглобулинов, называются α, δ, ε, γ и μ, соответственно.
[00133] Термин «Fc-домен» или «Fc-область» в настоящем документе используется для определения С-концевой области тяжелой цепи иммуноглобулина, которая содержит по меньшей мере часть константной области. Термин включает нативные последовательности Fc-областей и варианты Fc-областей. Хотя границы Fc-области тяжелой цепи IgG могут незначительно варьировать, Fc-область тяжелой цепи IgG человека, как правило, определяют как простирающуюся от Cys226, или от Pro230, до карбоксильного конца тяжелой цепи. При этом С-концевой лизин (Lys447) Fc-области может присутствовать либо отсутствовать. Если иное не указано в настоящем документе, нумерация аминокислотных остатков Fc-области или константной области соответствует системе нумерации EU, также называемой EU-индексом, согласно описанию в Kabat et al, Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD, 1991. «Субъединица» Fc-домена в настоящем документе относится к одному из двух полипептидов, образующих димерный Fc-домен, т.е. полипептиду, содержащему С-концевые константные области тяжелой цепи иммуноглобулина, способные к стабильному самосвязыванию. Например, субъединица Fc-домена IgG содержит константный домен СН2 IgG и СН3 IgG.
[00134] «Модификация, способствующая связыванию первой и второй субъединиц Fc-домена» представляет собой манипуляции с пептидным остовом или посттрансляционные модификации субъединицы Fc-домена, снижающие или предотвращающие связывание полипептида, содержащего указанную субъединицу Fc-домена, с идентичным полипептидом с образованием гомодимера. Модификация способствующая связыванию, в настоящем документе, в частности, включает отдельные модификации, вносимые в каждую из двух субъединиц Fc-домена, связывание которых требуется (т.е. первую и вторую субъединицы Fc-домена), при этом указанные модификации способствует связыванию указанных двух субъединиц Fc-домена и образованию гетеродимеров. Например, согласно определенным вариантам реализации модификация, способствующая связыванию, может изменять структуру или заряд одной или обеих субъединиц Fc-домена так, что это благоприятствует их связыванию.
[00135] Термин «эффекторные функции» относится к видам биологической активности, обусловленным Fc-областью антитела, варьирующие в зависимости от изотипа антитела. Примеры эффекторных функций антител включают: связывание Clq и комплемент-зависимую цитотоксичность (КЗЦ), связывание Fc-рецептора, антителозависимую клеточноопосредованную цитотоксичность (АЗКЦ), антителозависимый клеточный фагоцитоз (AD CP), секрецию цитокинов, опосредованный иммунным комплексом захват антигена антигенпрезентирующими клетками, понижающую регуляцию рецепторов клеточной поверхности (например, В-клеточного рецептора) и активацию В-клеток.
[00136] В настоящем документе «альбумин» относится в целом к белку или аминокислотной последовательности альбумина, или сегменту или варианту альбумина, обладающему одним или несколькими видами функциональной активности (например, биологической активности) альбумина. В частности, «альбумин» относится к альбумину человека или его сегментам (см., например, ЕР 201239, ЕР 322094 WO 97/24445, WO 95/23857), конкретнее, к зрелой форме альбумина человека, или альбумину других позвоночных животных или его сегментам, или аналогам или вариантам указанных молекул или их фрагментов. Согласно определенным вариантам реализации альбумин относится к усеченной версии альбумина.
[00137] Термин «квазиальбумин» относится к гетеромультимерной молекуле, обладающей структурой и/или функцией, аналогичной(ым) целому альбумину, и при этом гетеромультимерная молекула образуется путем сборки двух или более мономерных полипептидов, сконструированных на основе последовательности целого альбумина. Согласно определенным вариантам реализации указанные мономерный полипептиды представляют «сегменты», которые преимущественно связываются в гетеромультимерные пары с образованием квази-белка. Согласно некоторым вариантам реализации активность указанного квази-альбумина составляет 90% от активности целого альбумина. Согласно некоторым вариантам реализации активность указанного квази-альбумина составляет 75% от активности целого альбумина. Согласно одному варианту реализации активность указанного квази-альбумина составляет 50% от активности целого альбумина. Согласно некоторым вариантам реализации активность указанного квази-альбумина составляет 50-75% от активности целого альбумина. Согласно одному варианту реализации активность квази-альбумина составляет 80% от активности целого альбумина. Согласно некоторым вариантам реализации указанный квази-альбумин содержит 90% структуры целого альбумина согласно определению с помощью молекулярного моделирования. Согласно некоторым вариантам реализации указанный квази-альбумин содержит 80% структуры целого альбумина согласно определению с помощью молекулярного моделирования. Согласно некоторым вариантам реализации указанный квази-альбумин содержит 70% структуры целого альбумина согласно определению с помощью молекулярного моделирования. Согласно некоторым вариантам реализации указанный квази-альбумин содержит 50% структуры целого альбумина согласно определению с помощью молекулярного моделирования. Согласно некоторым вариантам реализации указанный квази-альбумин содержит 50-75% структуры целого альбумина согласно определению с помощью молекулярного моделирования.
[00138] Термины «альбумин сыворотки человека» (ЧСА) и «альбумин человека» (ЧА) используются в настоящем документе взаимозаменяемо. Термины «альбумин и альбумин сыворотки» шире, и охватывают альбумин сыворотки человека (и его фрагменты и варианты) а также альбумин других видов (и его фрагменты и варианты).
[00139] Согласно определенным вариантам реализации каждая конструкция на основе альбумина согласно описанию в настоящем документе основана на варианте нормального ЧА. Термин «варианты» включает вставки, удаления и замены, консервативные или неконсервативные, если такие изменения по существу не изменяют одно или более подходящих онкотических лиганд-связывающих и неиммуногенных свойств альбумина, или активного участка, или активного домена, который обеспечивает терапевтическую активность терапевтических белков.
[00140] Согласно определенным вариантам реализации выделенные гетеромультимерные конструкции согласно описанию в настоящем документе включают встречающиеся в природе полиморфные варианты альбумина человека и фрагменты альбумина человека, например, фрагменты, раскрытые в ЕР 322094 (а именно, ЧА (Pn), где n=369-119).
[00141] Согласно определенным вариантам реализации альбумин получен от любого позвоночного животного, в частности, любого млекопитающего, включая, но не ограничиваясь перечисленными, человека, коров, овец, крысу, мышь, кролика, лошадь, собаку или свинью. Согласно определенным вариантам реализации альбумин получен из альбуминов не являющихся млекопитающими организмов, включая, но не ограничиваясь перечисленными, курицы и лосося.
[00142] Ниже приведена последовательность альбумина человека SEQ ID NO: 1:

[00144] «Аллоальбумин» представляет собой генетический вариант альбумина. Согласно определенным вариантам реализации аллоальбумин представляет собой аллоальбумин человека (ЧАА). Аллоальбумины, отличающиеся электрофоретической подвижностью от альбумина, были идентифицированы при помощи популяционно-генетических исследований в ходе клинического электрофореза, или при исследованиях крови доноров. В качестве маркеров мутаций и миграции аллоальбумины представляют интерес для генетиков, биохимиков и антропологов, но большинство указанных аллоальбуминов не связаны с заболеваниями (Minchioti et al. Human Mutations 29(8), 1007-1016(2008)).
[00148] Термин «сегментирование» относится к точному внутреннему сплайсингу исходной белковой последовательности, которое приводит к получению «сегментов» указанной белковой последовательности, которые преимущественно связываются как гетеромультимеры с образованием квази-белка.
[00149] Квазинативная структура:
[00150] В отношении нативного белка или его структуры квазинативные белки и/или «квазинативные структуры» проявляют подобные нативному белку функциональные и структурные характеристики. Белки являются естественными динамическими молекулами и демонстрируют множество структурных конфигураций, хотя мы приписываем ему некоторую нативную структуру, например, определенную посредством рентгеновской кристаллографии. Альтернативные структурные конфигурации, наблюдаемые в геометрических ансамблях указанного белка, могут рассматриваться как квазинативные структуры друг относительно друга или относительно структуры, наблюдаемой в кристалле. С другой стороны, у гомологичных белковых последовательностей или белков, принадлежащих к общим структурным семействам, наблюдается тенденция к свертыванию в структуры с аналогичной геометрией. Белки, принадлежащие указанному семейству, могут рассматриваться как имеющие квазинативную структуру друг относительно друга. Некоторые из уникальных последовательностей в семействе белков могут также проявлять аналогичные функциональные свойства, и, таким образом, могут рассматриваться как квазинативные друг относительно друга белки. В случае описываемых здесь гетеромультимеров, содержащих две или более белковые конструкции, каждая из которых содержит компонент, представляющий собой полипептидный переносчик, указанные полипептидные переносчики соединяются с образованием квазинативной структуры. Исходный нативный белок в данном случае представлен белком, из которого получен указанный полипептидный переносчик, и исходная нативная структура представлена структурой мономерного белка, из которого получен полипептидный переносчик. Авторы настоящего изобретения описывают случай, когда два или более разных полипептида самособираются с образованием гетеромультимерных структур и проявляют функциональные характеристики, сходные с характеристиками нативного белка, который сам по себе представлен мономером. Согласно определенным вариантам реализации предложены гетеромультимерные конструкции, содержащие полученные из альбумина полипептидные переносчики, которые самособираются с образованием гетеромультимера, проявляющего сходные с характеристиками нативного альбумина функциональные характеристики, такие как связывание FcRn, и структурные характеристики. Указанные гетеромультимеры называют квазинативными.
[00151] «CD3-комплекс» согласно описанию в настоящем документе представляет собой комплекс, составленный по меньшей мере пятью мембраносвязанными полипептидами в зрелых Т-лимфоцитах, нековалентно связанными между собой и с Т-клеточным рецептором. CD3-комплекс включает цепи γ, дельта, эпсилон, зета и эта (также называемые субъединицами). Были разработаны не принадлежащие человеку моноклональные антитела против некоторых из указанных цепей, примеры представлены антителами мыши ОКТ3, SP34, UCHT1 или 64.1. (См., например, June, et al., J. Immunol. 136:3945-3952 (1986); Yang, et al., J. Immunol. 137:1097-1100 (1986); и Hayward, et al., Immunol. 64:87-92 (1988)). Экспрессия некоторых CD-антигенов строго ограничена конкретной линией дифференцировки. Лимфогемопоэтические клетки и, на протяжении последних нескольких лет, антитела против специфические для лимфоидной ткани антигены использовались для разработки способов лечения, эффективных in vitro или в моделях на животных (5-13). В этом смысле CD19, как оказалось, является очень полезной мишенью. CD19 экспрессируется во всех клетках В-клеточной линии, от про-В-клеток до зрелых В-клеток, не подвергается шеддингу, равномерно экспрессируется на всех клетках лимфомы и отсутствует в стволовых клетках.
[00152] Термин «эффективное количество» в настоящем документе относится к количеству вводимой мультиспецифической гетеромультимерной конструкции, которое до определенной степени уменьшает один или несколько симптомов заболевания, состояния или расстройства, лечение которого проводится. Композиции, содержащие мультиспецифическую гетеромультимерную конструкцию согласно описанию в настоящем документе, может вводиться для профилактического, стимулирующего и/или терапевтического лечения.
[00153] В настоящем документе термины «конструировать, сконструированный, конструирование» включают любые манипуляции с пептидным остовом или посттрансляционные модификации встречающегося в природе или рекомбинантного полипептида или его фрагмента. Конструирование включает модификации аминокислотной последовательности последовательности, паттерна гликозилирования или индивидуальных аминокислот групп боковых цепей, а также комбинации указанных подходов. Сконструированные белки экспрессируют и получают путем стандартных техник молекулярной биологии.
[00154] Под «выделенной молекулой нуклеиновой кислоты или полинуклеотидом» понимают молекулу нуклеиновой кислоты, ДНК или РНК, которая была извлечена из естественной среды. Например, рекомбинантный полинуклеотид, кодирующий полипептид, содержащийся в векторе, считают выделенным. Дополнительные примеры выделенных полинуклеотидов включают рекомбинантные полинуклеотиды, поддерживаемые в гетерологичных клетках-хозяева или очищенные (частично или по существу) полинуклеотиды в растворе. Выделенный полинуклеотид включает полинуклеотидную молекулу, содержащуюся в клетках, которые обычно содержат указанную полинуклеотидную молекулу, но при этом указанная полинуклеотидная молекула присутствует экстрахромасомно, либо ее хромосомная локализация отличается от природной хромосомной локализации. Выделенные молекулы РНК включают транскрипты РНК in vivo или in vitro, а также плюс- и минус-нитевые формы, и двуцепочечные формы. Выделенные полинуклеотиды или нуклеиновые кислоты согласно описанию в настоящем документе включают также такие молекулы, полученные синтетическим путем. Кроме того, полинуклеотид или нуклеиновая кислота, согласно определенным вариантам реализации, включают регуляторный элемент, такой как промотор, сайт связывания рибосом или терминатор транскрипции.
[00155] Под нуклеиновой кислотой или полинуклеотидом с нуклеотидной последовательностью, по меньшей мере, например, на 95% «идентичной» исходной нуклеотидной последовательности согласно настоящему изобретению подразумевается, что указанная нуклеотидная последовательность полинуклеотида идентична исходной последовательности, за исключением того, что указанная полинуклеотидная последовательность может включать до пяти точечных мутаций на каждые 100 нуклеотидов исходной нуклеотидной последовательности. Иными словами, для получения полинуклеотида с нуклеотидной последовательностью, по меньшей мере на 95% идентичной исходной нуклеотидной последовательности, до 5% нуклеотидов исходной последовательности может быть удалено или заменено другими нуклеотидам, или количество нуклеотидов, составляющее до 5% совокупности нуклеотидов исходной последовательности, может быть встроено в исходную последовательность. Указанные изменения исходной последовательности могут происходить в 5'- или 3'-концевых положениях исходной нуклеотидной последовательности либо в любом месте между указанными концевыми положениями, индивидуально, чередуясь с остатками исходной последовательности, либо входя в состав одной или нескольких непрерывных групп исходной последовательности. С практической точки зрения, идентичность любой конкретной полинуклеотидной последовательности нуклеотидной последовательности согласно настоящему изобретению, составляющая по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99%, может быть определена стандартным методом с применением известных компьютерных программ, таких как описанные выше для полипептидов (например, ALIGN-2).
[00156] Термин «экспрессионная кассета» относится к полинуклеотиду, полученному рекомбинантным или синтетическим путем, содержащему группу специфичных нуклеиновокислотных элементов, обеспечивающих возможность транскрипции конкретной нуклеиновой кислоты в целевой клетке. Рекомбинантная экспрессионная кассета может быть включена в плазмиду, хромосому, митохондриальную ДНК, ДНК пластиды, вирус или фрагмент нуклеиновой кислоты. Как правило, представленная рекомбинантной экспрессионной кассетой часть экс пресс ионного вектора включает, помимо других последовательностей, транскрибируемую нуклеиновокислотную последовательность и промотор. Согласно определенным вариантам реализации экспрессионная кассета согласно настоящему изобретению содержит полинуклеотидные последовательности, кодирующие биспецифические антигенсвязывающие молекулы согласно настоящему изобретению или их фрагменты.
[00157] Термин «вектор» или «экспрессионный вектор» является синонимом термина «экспрессионная конструкция» и относится к молекуле ДНК, которая используется для введения и направления экспрессии специфического гена, с которым она функционально связана в целевой клетке. Термин включает вектор как самореплицирующуюся нуклеиновокислотную структуру, а также вектор, включенный в геном клетки-хозяина, в которую он был введен. Экспрессионный вектор согласно настоящему изобретению содержит экспрессионную кассету. Экспрессионные векторы обеспечивают транскрипцию значительных количеств стабильных мРНК. После того как экспрессионный вектор попадает в целевую клетку, молекула рибонуклеиновой кислоты или белок, кодируемый геном, синтезируется с помощью механизмов клеточной транскрипции и/или трансляции. Согласно одному из вариантов реализации экспрессионный вектор согласно настоящему изобретению содержит экспрессионную кассету, которая содержит полинуклеотидные последовательности, кодирующие биспецифические антигенсвязывающие молекулы согласно настоящему изобретению или их фрагменты.
[00158] Термины «клетка-хозяин», «линия клеток-хозяев» и «культура клеток-хозяев» используются взаимозаменяемо и относятся к клеткам, в которые введена экзогенная нуклеиновая кислота, включая потомство таких клеток. Клетки-хозяева включают «трансформанты» и «трансформированные клетки», которые включают первичную трансформированную клетку и полученное из нее потомство, безотносительно числа пересевов. Согласно определенным вариантам реализации потомство не полностью идентично родительским клеткам в отношении содержащихся нуклеиновых кислот, и может содержать мутации. Мутантное потомство, обладающее той же функцией или биологической активностью согласно скринингу или отбору, что и исходная трансформированная клетка, включено в настоящее изобретение. Клетка-хозяин представлена любым типом клеточной системы, который может использоваться для получения биспецифических антигенсвязывающих молекул согласно настоящему изобретению. Клетки-хозяева включают культивируемые клетки, например, культивируемые клетки млекопитающих, такими как клетки СНО, ВНК, NS0, SP2/0, клетки миеломы YO, клетки миеломы мышей Р3Х63, клетки PER, PER.C6 или клетки гибридомы, дрожжевые клетки, клетки насекомых и растений, среди прочих, а также клетки, содержащиеся в организме трансгенного животного, трансгенного растения или культивируемой растительной или животной ткани.
[00159] «Активирующий Fc-рецептор» представляет собой Fc-рецептор, при взаимодействии с Fc-доменом антитела запускающий передачу сигналов, стимулирующих осуществление эффекторных функций клеткой, несущей рецептор. Активирующие Fc-рецепторы человека включают FcγRIIIa (CD 16а), Fc□RI (CD64) и FeγRIIa (CD32).
[00160] Антителозависимая клеточноопосредованная цитотоксичность (АЗКЦ) представляет собой иммунный механизм, обеспечивающий лизис покрытых антителами целевых клеток иммунными эффекторными клетками. Целевые клетки представляют собой клетки, с которыми специфично связываются антитела или производные антител, содержащие Fc-область, как правило посредством белковой части, расположенной в направлении N-конца по отношению к Fc-области. В настоящем документе термин «пониженная АЗКЦ» определен или как снижение количества целевых клеток, лизис которых происходит за заданный период времени, при заданной концентрации антитела в среде, окружающей указанные целевые клетки, за счет описанного выше механизма АЗКЦ, и/или как повышение необходимой концентрации антитела в среде, окружающей целевые клетки, для обеспечения лизиса заданного числа целевых клеток за заданный период времени за счет механизма АЗКЦ. Снижение АЗКЦ оценивают относительно АЗКЦ, опосредованной тем же антителом, синтезированным клетками того же типа клеток-хозяев с применением тех же стандартных способов получения, очистки, приготовления составов и хранения (известных специалистам в данной области техники), но не сконструированным. Например, снижение АЗКЦ, опосредованной антителом, содержащим снижающую АЗКЦ замену аминокислотны в Fc-домене, оценивают относительно АЗКЦ, опосредованной тем же антителом, не содержащим указанную аминокислотную замену в Fc-домене.
[00161] «Эффективное количество» агента, такого как мультиспецифический гетеромультимер согласно описанию в настоящем документе, относится к количеству, необходимому для обеспечения физиологического изменения в клетке или ткани, в которую его вводят.
[00162] «Терапевтически эффективное количество» агента, например, фармацевтической композиции, содержащей мультиспецифический гетеромультимер согласно описанию в настоящем документе, относится к количеству, эффективному, в дозировках и на протяжении необходимых периодов времени, для достижения требуемого терапевтического или профилактического результата. Терапевтически эффективное количество агента, например, элиминирует, снижает, задерживает, минимизирует или предотвращает нежелательные эффекты заболевания.
[00163] «Индивидуум» или «субъект» представляет собой млекопитающее. Млекопитающие включают, не ограничиваясь перечисленными, одомашненных животных (например, коров, овец, кошек, собак и лошадей), приматов (например, человека и не являющихся человеком приматов, таких как обезьяны), кроликов и грызунов (например, мышей и крыс). В частности, индивидуум или субъект представляет собой человека.
[00164] Термин «фармацевтическая композиция» относится к составу, представленному в форме, обеспечивающей эффективную реализацию биологической активности содержащейся в нем мультиспецифической гетеромультимернрй конструкции, и не содержащему дополнительных компонентов, неприемлемо токсичных для субъекта, для введения которому предназначен указанный состав.
[00165] «Фармацевтически приемлемый носитель» относится к ингредиенту в составе фармацевтической композиции, не являющемуся активным ингредиентом, и нетоксичному для субъекта. Фармацевтически приемлемый носитель включает, не ограничиваясь перечисленными, буфер, вспомогательное вещество, стабилизатор или консервант.
[00166] В настоящем документе «лечение/обработка» (и грамматические варианты указанного термина, такие как «лечить/обрабатывать») относится к клиническому вмешательству с целью изменения естественного течения заболевания у индивидуума, лечение которого проводят, и может осуществляться либо для профилактики, либо во время в ходе клинической патодиагностики. Желательные эффекты лечения включают, не ограничиваясь перечисленными, предотвращение наступления или рецидива заболевания, облегчение симптомов, уменьшение любых прямых или непрямых патологических последствий указанного заболевания, предотвращение метастазирования, уменьшение скорости прогрессирования заболевания, смягчение или ослабление тяжести указанного заболевания, и ремиссию или улучшение прогноза. Согласно некоторым вариантам реализации мультиспецифические гетеромультимерные конструкции согласно описанию в настоящем документе используются для задержки развития заболевания или замедления прогрессирования заболевания. Термин «инструкции» относится к инструкциям, в обычном порядке помещаемым в коммерческие упаковки терапевтических продуктов, и содержащим информацию относительно показаний, применения, дозировки, введения, комбинированной терапии, противопоказаний и/или предупреждений, касающихся применения таких терапевтических продуктов.
[00167] Термин «межвидовое связывание» в настоящем документе означает связывание связывающего домена согласно описанию в настоящем документе с той же целевой молекулой человека и других организмов, например, не ограничиваясь указанными, не являющихся шимпанзе приматов. Таким образом, «межвидовое связывание» следует понимать как межвидовую реакционноспособность в отношении одной и той же молекулы «X» (т.е. гомолога), экспрессируемой у разных видов, но не в отношении молекулы, не являющейся «X». Межвидовая специфичность моноклонального антитела, распознающего, например, CD3-эпсилон человека, в отношении CD3-эпсилон не являющегося шимпанзе примата, например, CD3-эпсилон макаки, может быть определена, например, с помощью FACS-анализа. FACS-анализ проводят таким образом, что соответствующее моноклональное антитело тестируют на связывание с клетками человека и не являющихся шимпанзе приматов, например, клетками макака, экспрессирующими антигены CD3-эпсилон указанных человека и не являющихся шимпанзе приматов, соответственно. Подходящий анализ представлен в приведенных ниже примерах. Вышесказанное распространяется, с соответствующими поправками, на АПСК, CD 19, С-МЕТ, эндосиалин, ЕрСАМ, IGF-1R (рецептор ИФР-1) и антиген FAPα: Межвидовая специфичность моноклонального антитела, распознающего, например, АСПК, CD19, С-МЕТ, эндосиалина, ЕрСАМ, IGF-1R или FAPα человека, относительно АСПК, CD19, С-МЕТ, эндосиалина, ЕрСАМ, IGF-1R или FAPα не являющихся шимпанзе приматов, например, АСПК, CD 19, С-МЕТ, эндосиалина, ЕрСАМ, IGF-1R или FAPa макака, может быть определен, например, с помощью FACS-анализа. FACS-анализ проводят таким образом, что соответствующее моноклональное антитело тестируют на связывание с клетками человека и не являющихся шимпанзе приматов, например, клетками макака, экспрессирующими указанные антигены АСПК, CD19, С-МЕТ, эндосиалин, ЕрСАМ, IGF-1R или FAPα человека и не являющихся шимпанзе приматов, соответственно.
[00168]
[00169]
[00170] Подробное описание некоторых вариантов реализации
[00171] Мультиспецифические гетеромультимерные конструкции на основе иммуноглобулинов:
[00172] В настоящем изобретении предложены выделенные мультиспецифические гетеромультимерные конструкции, содержащие первую полипептидную конструкцию, содержащую первый полипептид тяжелой цепи и CD3-связывающую полипептидную конструкцию, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; и вторую полипептидную конструкцию, содержащую второй полипептид тяжелой цепи, отличную от указанного первого полипептида тяжелой цепи, и антигенсвязывающую полипептидную конструкцию, которая связывается с целевым антигеном по меньшей мере на одной В-клетке, при этом по меньшей мере одна из указанных CD3-связывающих полипептидных конструкций и указанных антигенсвязывающих полипептидных конструкций содержит одноцепочечную Fv-область; указанная мультиспецифическая гетеромультимерная конструкция одновременно задействует указанную по меньшей мере одну В-клетку и указанную по меньшей мере одну CD3-экспрессирующую клетку таким образом, что CD3-экспрессирующая клетка активируется, тем самым индуцируя киллинг указанной В-клетки; и указанные первый и второй полипептиды тяжелой цепи образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной Fc, которая образуется со стабильностью, по меньшей мере сравнимой со стабильностью нативной гомодимерной Fc, и с такой чистотой, что при экспрессии указанной мультиспецифической гетеромультимерной конструкции клеткой млекопитающего с получением экспрессионного продукта указанный экспрессионный продукт содержит по меньшей мере приблизительно 70% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций. Согласно некоторым вариантам реализации указанный экспрессионный продукт содержит по меньшей мере приблизительно 75% указанного мультиспецифического гетеромультимера и менее чем 15% мономеров или гомодимеров указанных первой или второй полипептидных конструкций. Согласно определенным вариантам реализации указанная экспрессионный продукт содержит по меньшей мере приблизительно 80%) указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций. Согласно дополнительным вариантам реализации экспрессионный продукт содержит по меньшей мере приблизительно 85% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций. Согласно дополнительному варианту реализации экспрессионный продукт содержит по меньшей мере приблизительно 90% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций.
[00173] Согласно определенным вариантам реализации предложена выделенная мультиспецифическая гетеромультимерная конструкция, отличающаяся тем, что в состав первой или второй полипептидной конструкции не входит по меньшей мере что-либо одно из легкой цепи иммуноглобулина и первой константной области (СН1) иммуноглобулина.
[00174] Согласно определенным вариантам реализации предложена выделенная мультиспецифическая гетеромультимерная конструкция, содержащая: первую полипептидную конструкцию, содержащую первый полипептид тяжелой цепи и CD3-связывающую полипептидную конструкцию, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; вторую полипептидную конструкцию, содержащую второй полипептид тяжелой цепи, отличный от указанного первого полипептида тяжелой цепи, и отличающуюся тем, что указанная вторая полипептидная конструкция не содержит антигенсвязывающую полипептидную конструкцию, которая связывается с целевым антигеном на В-клетке; при этом указанная мультиспецифическая гетеромультимерная конструкция одновременно задействует по меньшей мере одну В-клетку и указанную по меньшей мере одну CD3-экспрессирующую клетку таким образом, что CD3-экспрессирующая клетка активируется, тем самым индуцируя киллинг указанной В-клетки; и указанные первый и второй полипептиды тяжелой цепи образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной Fc, при этом указанная гетеродимерная Fc имеет стабильность, по меньшей мере сравнимую со стабильностью нативной гомодимерной Fc, и указанная образующаяся гетеродимерная Fc имеет такую чистоту, что при экспрессии указанной мультиспецифической гетеромультимерной конструкции стабильной клеткой млекопитающего с получением экспрессионного продукта указанный экспрессионный продукт содержит по меньшей мере приблизительно 75% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций. Согласно некоторым вариантам реализации указанная гетеродимерная Fc взаимодействует с рецепторами клеточной поверхности, такими как FcgRIIb, на В-клетке. Согласно определенному варианту реализации указанная гетеродимерная Fc сконструирована таким образом, чтобы преимущественно взаимодействовать с рецептором FcgRIIb относительно обычного антитела.
[00175] В настоящем изобретении предложена выделенная мультиспецифическая гетеромультимерная конструкция, содержащая: первую полипептидную конструкцию, содержащую первый полипептид тяжелой цепи и CD3-связывающую полипептидную конструкцию, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; вторую полипептидную конструкцию, содержащую второй полипептид тяжелой цепи, отличную от указанного первого полипептида тяжелой цепи, и конструкцию, представляющую собой стерический модулятор, демонстрирующую пренебрежимое связывание рецептора; при этом указанная мультиспецифическая гетеромультимерная конструкция одновременно задействует по меньшей мере одну В-клетку и указанную по меньшей мере одну CD3-экспрессирующую клетку таким образом, что CD3-экспрессирующая клетка активируется, тем самым индуцируя киллинг указанной В-клетки; и указанные первый и второй полипептиды тяжелой цепи образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной Fc, при этом указанная гетеродимерная Fc имеет стабильность, по меньшей мере сравнимую со стабильностью нативной гомодимерной Fc, и указанная образующаяся гетеродимерная Fc имеет такую чистоту, что при коэкспрессии указанной мультиспецифической гетеромультимерной конструкции стабильной клеткой млекопитающего с получением экспрессионного продукта указанный экспрессионный продукт содержит по меньшей мере приблизительно 75% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций. Согласно определенному варианту реализации указанная представляющая собой стерический модулятор конструкция фактически неспособна связываться с какой-либо известной целевой тканью или клеточной поверхностью и таким образом функционирует в качестве вспомогательного полипептидного плеча, играя роль исключительно стерического модулятора при взаимодействиях указанной мультиспецифической гетеромультимерной конструкции. Согласно некоторым вариантам реализации указанная представляющая собой стерический модулятор конструкция является полипептидной последовательностью, способствующей модулированию стерических характеристик мультиспецифического гетеромультимера при связывании указанного мультимера с Т- и/или В-клетками. Согласно определенным вариантам реализации указанная представляющая собой стерический модулятор конструкция содержит полипептидный домен, сконструированный de novo. Согласно определенным вариантам реализации указанная представляющая собой стерический модулятор конструкция содержит полипептидные домены, полученные путем конструирования известного полипептидного домена с устранением его связывающих свойств. Например, согласно определенным вариантам реализации указанная представляющая собой стерический модулятор конструкция содержит сконструированную Fab-область или ее фрагмент, сконструированный для устранения связывающих свойств.
[00176] Предложена выделенная мультиспецифическая гетеромультимерная конструкция, содержащая: первую полипептидную конструкцию, содержащую первый полипептид тяжелой цепи и CD3-связывающую полипептидную конструкцию, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; вторую полипептидную конструкцию, содержащую второй полипептид тяжелой цепи, отличную от указанного первого полипептида тяжелой цепи, и отличающуюся тем, что указанная вторая полипептидная конструкция не содержит антигенсвязывающую полипептидную конструкцию; при этом указанная мультиспецифическая гетеромультимерная конструкция одновременно задействует по меньшей мере одну В-клетку и указанную по меньшей мере одну CD3-экспрессирующую клетку таким образом, что CD3-экспрессирующая клетка активируется, тем самым индуцируя киллинг указанной В-клетки; и указанные первый и второй полипептиды тяжелой цепи образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной Fc, при этом указанная гетеродимерная Fc имеет стабильность, по меньшей мере сравнимую со стабильностью нативной гомодимерной Fc, и указанная образующаяся гетеродимерная Fc имеет такую чистоту, что при коэкспрессии указанной мультиспецифической гетеромультимерной конструкции стабильной клеткой млекопитающего с получением экспрессионного продукта указанный экспрессионный продукт содержит по меньшей мере приблизительно 75% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций.
[00177] В некоторых вариантах реализации предложена выделенная мультиспецифическая гетеромультимерная конструкция согласно описанию в настоящем документе, отличающаяся тем, что гетеродимерная Fc-область содержит вариант СН2-домена или шарнир, содержащий аминокислотные модификации, который предотвращают функционально эффективное связывание со всеми рецепторами Fcγ.
[00178] Предложены выделенные мультиспецифические гетеромультимерные конструкции, связывающие по меньшей мере одну В-клетку с валентностью больше 1, и одновременно задействующие указанную по меньшей мере одну В-клетку и по меньшей мере одну CD3-экспрессирующую клетку таким образом, что CD3-экспрессирующая клетка активируется, тем самым индуцируя киллинг указанной В-клетки. Согласно определенным вариантам реализации указанный мультиспецифический гетеромультимер содержит: первую полипептидную конструкцию, содержащую первый полипептид тяжелой цепи и CD3-связывающую полипептидную конструкцию, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; и вторую полипептидную конструкцию, содержащую второй полипептид тяжелой цепи, отличную от указанного первого полипептида тяжелой цепи, и антигенсвязывающую полипептидную конструкцию, которая связывается с целевым антигеном по меньшей мере на одной В-клетке; при этом по меньшей мере одна из указанных CD3-связывающих полипептидных конструкций и указанных антигенсвязывающих полипептидных конструкций необязательно содержит одноцепочечную Fv-область; указанные первый и второй полипептиды тяжелой цепи образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной Fc со стабильностью, по меньшей мере сравнимой со стабильностью нативной гомодимерной Fc, и с такой чистотой, что при экспрессии указанной мультиспецифической гетеромультимерной конструкции клеткой млекопитающего с получением экспрессионного продукта указанный экспрессионный продукт содержит больше 75% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций. Указанная мультиспецифическая гетеромультимерная конструкция способна взаимодействовать с В-клеткой посредством указанной антигенсвязывающей полипептидной конструкции на второй тяжелой цепи, а также взаимодействовать посредством указанной гетеродимерной Fc с рецепторами FcgRIIb на В-клетке, проявляя валентность выше единицы при взаимодействии с В-клеткой.
[00179] Согласно определенным вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что гетеродимерная Fc-область содержит вариант СН2-домена, содержащий аминокислотные модификации, способствующие селективному связыванию рецептора Feγ.
[00180] Согласно некоторым вариантам реализации предложен гетеромультимер, отличающийся тем, что указанный вариант СН2-домена селективно связывает по меньшей мере один из рецепторов FcγIIIa и FcγIIb по сравнению с СН2-доменом дикого типа.
[00181] Согласно определенным вариантам реализации предложена выделенная мультиспецифическая гетеромультимерная конструкция согласно описанию в настоящем документе, отличающаяся тем, что указанный гетеродимер Fc гликозилирован.
[00182] Согласно некоторым вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанный гетеродимер Fc афукозилирован.
[00183] Согласно определенным вариантам реализации предложена выделенная мультиспецифическая гетеромультимерная конструкция согласно описанию в настоящем документе, отличающаяся тем, что указанный гетеродимер Fc агликозилирован. [00184]
[00185] Модификации Fc-области, способствующие гетеродимеризации:
[00186] Предложены мультиспецифические гетеромультимерные конструкции, содержащие разные антигенсвязывающие фрагменты, соединенные либо с первой, либо со второй из двух субъединиц Fc-домена, таким образом, что указанные две субъединицы Fc-домена как правило состоят из двух неидентичных полипептидных цепей. Для повышения выхода и чистоты гетеромультимеров согласно описанию в настоящем документе Fc-область указанных полипептидов модифицируют так, что это способствует связыванию нужных полипептидов.
[00187] Согласно некоторым вариантам реализации первый и второй полипептиды тяжелой цепи гетеромультимерных конструкций согласно описанию в настоящем документе образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной Fc, которая образуется со стабильностью, по меньшей мере сравнимой со стабильностью нативной гомодимерной Fc, и с такой чистотой, что при коэкспрессии указанной мультиспецифической гетеромультимерной конструкции клеткой млекопитающего в виде экспрессионного продукта указанный экспрессионный продукт содержит по меньшей мере приблизительно 75% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций.
[00188] Согласно некоторым вариантам реализации первый и второй полипептиды тяжелой цепи гетеромультимерных конструкций согласно описанию в настоящем документе образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной Fc, которая образуется со стабильностью, по меньшей мере сравнимой со стабильностью нативной гомодимерной Fc, и с такой чистотой, что при коэкспрессии указанной мультиспецифической гетеромультимерной конструкции клеткой млекопитающего в виде экспрессионного продукта указанный экспрессионный продукт содержит по меньшей мере приблизительно 90% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций.
[00189] Согласно некоторым вариантам реализации первый и второй полипептиды тяжелой цепи гетеромультимерных конструкций согласно описанию в настоящем документе образуют гетеродимерную Fc-область, содержащую вариант области СН3 иммуноглобулина, содержащий по меньшей мере одну аминокислотную модификацию, способствующую образованию указанной гетеродимерной Fc, которая образуется со стабильностью, по меньшей мере сравнимой со стабильностью нативной гомодимерной Fc, и с такой чистотой, что при коэкспрессии указанной мультиспецифической гетеромультимерной конструкции клеткой млекопитающего в виде экспрессионного продукта указанный экспрессионный продукт содержит по меньшей мере приблизительно 95% указанного мультиспецифического гетеромультимера и менее 10% мономеров или гомодимеров указанных первой или второй полипептидных конструкций.
[00190] Согласно некоторым вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно настоящему описанию, отличающийся тем, что температура плавления (Tm) указанного варианта СН3-домена составляет приблизительно 73°С или более.
[00191] Согласно определенным вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что чистота образующейся гетеродимерной Fc-области больше приблизительно 78%.
[00192] Согласно одному варианту реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что чистота образующейся гетеродимерной Fc-области, составляющей по меньшей мере приблизительно 78% или более, и Tm составляет по меньшей мере приблизительно 75°С.
[00193] Согласно некоторым вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что чистота образующейся гетеродимерной Fc-области, составляющей по меньшей мере приблизительно 75%, и Tm составляет приблизительно 75°С или более.
[00194] Согласно определенным вариантам реализации предложены выделенные мультиспецифические гетеромультимерные конструкции, отличающиеся тем, что: а) вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации L351Y, F405A и Y407V, а вариант последовательности СН3 второго полипептидного переносчика содержит аминокислотные модификации T366L, К392М и T394W; b) вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации L351Y, F405A и Y407V, а вариант последовательности СН3 второго полипептида тяжелой цепи содержит аминокислотные модификации T366L, K392L и T394W; с) вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации T350V, L351Y, F405A и Y407V, а вариант последовательности СН3 второго полипептида тяжелой цепи содержит аминокислотные модификации T350V, T366L, К392М и T394W; d) вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации T350V, L351Y, F405A и Y407V, а вариант последовательности СН3 второго полипептида тяжелой цепи содержит аминокислотные модификации T350V, T366L, K392L и T394W; е) вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации T366L, N390R, K392R и T394W, а вариант последовательности СН3 второго полипептида тяжелой цепи содержит аминокислотные модификации L351Y, S400E, F405A и Y407V; или f) вариант последовательности СН3 первого полипептида тяжелой цепи содержит аминокислотные модификации T350V, T366L, N390R, K392R и T394W, а вариант последовательности СН3 второго полипептида тяжелой цепи содержит аминокислотные модификации T350V, L351 Y, S400E, F405A и Y407V.
[00195]
[00196] Модификации Fc-области, уменьшающие связывание с Fc-рецептором и/или эффекторную функцию:
[00197] Согласно определенным вариантам реализации Fc-области гетеромультимерных конструкций согласно описанию в настоящем документе содержит вариант СН2-домена, содержащий аминокислотные модификации, способствующие селективному связыванию рецептора Fcγ. Согласно некоторым вариантам реализации выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе содержит вариант СН2-домена, селективно связывающий рецептор FcγIIb со сродством выше, чем у СН2-домена дикого типа. Согласно некоторым вариантам реализации выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе содержит вариант СН2-домена, селективно связывающий рецептор FcγIIA и/или FcγIIIA со сродством выше, чем у СН2-домена дикого типа.
[00198] Согласно определенным вариантам реализации указанная Fc-областей гетеромультимерных конструкций согласно описанию в настоящем документе проявляют пониженное сродство к связыванию с Fc-рецептором и/или пониженную эффекторную функцию по сравнению с нативной Fc-областью IgG1. Согласно одному такому варианту реализации Fc-область проявляет менее чем 50%, как вариант, менее чем 20%, как вариант, менее чем 10%, и, согласно некоторым вариантам реализации, менее чем 5% сродство к связыванию Fc-рецептора, по сравнению с нативной Fc-областью IgG1, и/или эффекторную функцию, составляющую менее чем 50%, как вариант, менее чем 20%, как вариант, менее чем 10%, и, согласно некоторым вариантам реализации, менее чем 5% от эффекторной функции нативной Fc-области IgG1.
[00199] Согласно одному из вариантов реализации Fc-область гетеромультимерной конструкции согласно описанию в настоящем документе по существу не связывается с Fc-рецептором или не индуцирует детектируемую эффекторную функцию. Согласно определенному варианту реализации Fc-рецептор представляет собой рецептор Fc□. Согласно одному варианту реализации указанный Fc-рецептор представляет собой Fc-рецептор млекопитающего. Согласно определенным вариантам реализации указанная Fc-рецептор млекопитающего представляет собой Fc-рецептор человека. Согласно одному варианту реализации Fc-рецептор представляет собой активирующий Fc-рецептор. Согласно конкретному варианту реализации Fc-рецептор представляет собой активирующий Fc□ рецептор человека, в частности Fc□RIIIa, Fc□RI или Fc□RIIa человека, конкретно - Fc□RIIIa человека. Согласно одному варианту реализации указанная эффекторная функция представляет собой одну или несколько функций, выбранных из группы, состоящей из КЗЦ, АЗКЦ, АЗКФ и секреции цитокинов. Согласно конкретному варианту реализации указанная эффекторная функция представляет собой АЗКЦ. Согласно одному варианту реализации указанная Fc-область проявляет сродство к связыванию с неонатальным Fc-рецептором (FcRn). Согласно определенным вариантам реализации указанное сродство к связыванию FcRn по существу аналогично сродству нативной IgG1 Fe. Согласно некоторым вариантам реализации по существу аналогичное связывание с FcRn достигается в том случае, если Fc-область гетеромультимерной конструкции согласно описанию в настоящем документе проявляет больше приблизительно 70%, или согласно некоторым вариантам реализации больше приблизительно 80%, и, согласно некоторым частным вариантам реализации, больше приблизительно 90% сродства к связыванию FcRn относительно нативного IgG1 Fc-домена.
[00200] Согласно определенным вариантам реализации Fc-область гетеромультимерной конструкции согласно описанию в настоящем документе сконструирована таким образом, что имеет пониженное сродство к связыванию с Fc-рецептором и/или пониженную эффекторную функцию по сравнению с не-сконструированным Fc-доменом. Согласно некоторым вариантам реализации указанные сконструированные мутации присутствуют в нижнем шарнире и СН2-домене. Согласно частным вариантам реализации Fc-область описанного в настоящем документе гетеромультимера содержит одну или несколько модификаций аминокислот, снижающих сродство Fc-области к связыванию с Fc-рецептором и/или эффекторную функцию. Согласно некоторым вариантам реализации те же одна или несколько модификаций аминокислот присутствуют в каждой из двух субъединиц Fc-области. Согласно некоторым вариантам реализации в каждую из двух субъединиц Fc-области вводят разные аминокислотные модификации. Согласно одному варианту реализации указанная модификация аминокислотны уменьшает сродство Fc-области к связыванию с Fc-рецептором. Согласно одному варианту реализации указанная модификация аминокислотны уменьшает сродство Fc-области к связыванию с Fc-рецептором по меньшей мере 2-кратно, или, согласно некоторым вариантам реализации, по меньшей мере 5-кратно, или, согласно одному варианту реализации, по меньшей мере 10-кратно. Согласно определенным вариантам реализации, включающим больше одной аминокислотные модификацииы, снижающую сродство к связыванию Fc-области с Fc-рецептором, комбинация указанных модификаций аминокислот уменьшает сродство Fc-области к связыванию с Fc-рецептором по меньшей мере 10-кратно, или, согласно некоторым вариантам реализации, по меньшей мере 20-кратно, или, согласно определенным вариантам реализации, по меньшей мере 50-кратно. Согласно определенному варианту реализации сродство к связыванию Fc-области с Fc-рецептором снижается до уровня, когда уже не удается обнаружить детектируемое связывание мутантного Fc с Fc-рецептором в ходе стандартного связывающего анализа, например, с применением инструмента для ППР. Согласно одному варианту реализации гетеромультимерная конструкция согласно описанию в настоящем документе, содержащая сконструированный Fc-домен, проявляет менее чем 20%, и, согласно определенным вариантам реализации, менее чем 10%, и согласно избранным вариантам реализации менее чем 5% сродство к связыванию с Fc-рецептором по сравнению с соответствующей конструкцией, содержащей Fc-домен, который не был сконструирован с целью снижения связывания с Fc-рецептором. Согласно конкретному варианту реализации Fc-рецептор представляет собой Fc□ рецептор. Согласно некоторым вариантам реализации Fc-рецептор представляет собой Fc-рецептор человека. Согласно некоторым вариантам реализации Fc-рецептор представляет собой активирующий Fc-рецептор. Согласно конкретному варианту реализации Fc-рецептор представляет собой активирующий Fc□ рецептор человека, согласно определенным вариантам реализации представляющий собой один из рецепторов человека FcyRIIIa, FcyRI и FcyRIIa. Согласно некоторым вариантам реализации связывание с каждым из указанных рецепторов снижается. Согласно некоторым вариантам реализации также снижается сродство к связыванию с компонентом комплемента, например, но не ограничиваясь указанным, с C1q. Согласно одному варианту реализации сродство к связыванию с неонатальным Fc-рецептором (FcRn) не снижается. Согласно определенным вариантам реализации Fc-область описанного в настоящем документе гетеромультимера сконструирована таким образом, что имеет пониженную эффекторную функцию по сравнению с несконструированной Fc-областью. Согласно определенным вариантам реализации указанная пониженная эффекторная функция может включать, не ограничиваясь перечисленным, что-либо одно или более из следующего: пониженная комплемент-зависимая цитотоксичность (КЗЦ), пониженная антителозависимая клеточноопосредованная цитотоксичность (АЗКЦ), пониженный антителозависимый клеточный фагоцитоз (АЗКФ), пониженная секреция цитокинов, пониженный опосредованный иммунным комплексом захват антигена антигенпрезентирующими клетками, пониженное связывание с клетками NK, пониженное связывание с макрофагами, пониженное связывание с моноцитами, пониженное связывание с полиморфноядерными клетками, пониженная прямая передача сигнала индукции апоптоза, пониженное перекрестное связывание связанных с мишенью антител, пониженное созревание дендритных клеток или пониженное примирование Т-клеток. Согласно одному варианту реализации указанная пониженная эффекторная функция представляет собой что-либо одно или более, выбранное из группы, состоящей из пониженной КЗЦ, пониженной АЗКЦ, пониженного АЗКФ и пониженной секреции цитокинов. Согласно определенным вариантам реализации указанная пониженная эффекторная функция представляет собой снижение АЗКЦ. Согласно одному варианту реализации указанная пониженная АЗКЦ составляет менее чем 20% АЗКЦ, индуцируемой не-сконструированным Fc-доменом (либо активирующей Т-клетки биспецифической антигенсвязывающей молекулой, содержащие не-сконструированный Fc-домен). Согласно другому варианту реализации указанная пониженная АЗКЦ составляет менее чем 50% от АЗКЦ, индуцируемой не-сконструированным Fc-доменом (или активирующей Т-клетки биспецифической антигенсвязывающей молекулой, содержащей не-сконструированный Fc-домен). Согласно дополнительному варианту реализации указанная пониженная АЗКЦ составляет менее чем 10% от АЗКЦ, индуцируемой не-сконструированным Fc-доменом (или активирующей Т-клетки биспецифической антигенсвязывающей молекулой, содержащей не-сконструированный Fc-домен).
[00201] Согласно определенным вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что гетеродимерная Fc-область содержит вариант СН2-домена, содержащий аминокислотные модификации, способствующие селективному связыванию рецептора Fcγ согласно описанию в настоящем документе.
[00202] Согласно некоторым вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанный вариант СН2-домена селективно связывает по меньшей мере один из рецепторов FcγIIIa и FcγIIb по сравнению с СН2-доменом дикого типа.
[00203] Согласно определенным вариантам реализации мультиспецифическая гетеромультимерная конструкция содержит вариант СН2-области, который связывает по меньшей мере одну В-клетку таким образом, что указанная гетеромультимерная конструкция связывает В-клетки с валентностью большей, чем единица.
[00204]
[00205] Мультиспецифические гетеромультимерные конструкции на основе альбумина:
[00206] Предложены выделенные мультиспецифические гетеромультимерные конструкции, содержащие: первую полипептидную конструкцию, содержащую первый полипептидный переносчик, соединенный по меньшей мере с одной CD3-связывающей полипептидной конструкцией, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; вторую полипептидную конструкцию, содержащую второй полипептидный переносчик, отличный от указанного первого полипептидного переносчика, соединенный по меньшей мере с одной антигенсвязывающей полипептидной конструкцией, которая связывается с целевым антигеном по меньшей мере на одной В-клетке; при этом первый и второй полипептидные переносчики получают из белка путем сегментирования указанного белка, каждый полипептид-переносчик содержит аминокислотную последовательность, по меньшей мере на 90% идентичную сегменту указанного белка, и при этом полипептидные переносчики самособираются с образованием квазинативной структуры указанного мономерного белка. Согласно некоторым вариантам реализации каждый полипептидный переносчик содержит аминокислотную последовательность, по меньшей мере на 85% идентичную сегменту указанного белка. Согласно некоторым вариантам реализации каждый полипептидный переносчик содержит аминокислотную последовательность, по меньшей мере на 80% идентичную сегменту указанного белка. Согласно некоторым вариантам реализации каждый полипептидный переносчик содержит аминокислотную последовательность, по меньшей мере на 95% идентичную сегменту указанного белка. Согласно некоторым другим вариантам реализации каждый полипептидный переносчик содержит аминокислотную последовательность, по меньшей мере на 99% идентичную сегменту указанного белка.
[00207] Согласно определенным вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что указанные полипептидные переносчики не получены из антитела. Согласно дополнительному варианту реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что каждый полипептидный переносчик представляет собой производное альбумина. Согласно некоторым вариантам реализации предложен выделенный мультиспецифический гетеромультимер на основе альбумина, отличающийся тем, что указанный альбумин представляет собой альбумин сыворотки человека. Согласно некоторым вариантам реализации по меньшей мере один полипептидный переносчик представляет собой производное аллоальбумина. Согласно определенным вариантам реализации предложен выделенный мультиспецифический гетеромультимер согласно описанию в настоящем документе, отличающийся тем, что все полипептидные переносчики получены из разных альбуминов. Согласно некоторым вариантам реализации каждый полипептидный переносчик содержит аминокислотную последовательность, по меньшей мере на 75% идентичную сегменту альбумина. Согласно некоторым вариантам реализации каждый полипептидный переносчик содержит аминокислотную последовательность, по меньшей мере на 80% идентичную сегменту альбумина. Согласно некоторым вариантам реализации каждый полипептидный переносчик содержит аминокислотную последовательность, по меньшей мере на 90% идентичную сегменту альбумина. Согласно некоторым другим вариантам реализации каждый полипептидный переносчик содержит аминокислотную последовательность, по меньшей мере на 95% идентичную сегменту альбумина. Согласно некоторым другим вариантам реализации каждый полипептидный переносчик содержит аминокислотную последовательность, по меньшей мере на 99% идентичную сегменту альбумина.
[00208] В настоящем изобретении предложена на основе альбумина выделенная мультиспецифическая гетеромультимерная конструкция, содержащая: первый мономер, содержащий первый полипептидный переносчик, соединенный по меньшей мере с одной CD3-связывающей полипептидной конструкцией, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке; вторую полипептидную конструкцию, содержащую второй полипептидный переносчик, отличный от указанного первого полипептидного переносчика, соединенный по меньшей мере с одной антигенсвязывающей полипептидной конструкцией, которая связывается с целевым антигеном по меньшей мере на одной В-клетке; при этом первый и второй полипептидные переносчики получают путем сегментирования альбумина, и каждый полипептид-переносчик содержит аминокислотную последовательность, по меньшей мере на 90% идентичную сегменту альбумина, так что указанные полипептидные переносчики самособираются с образованием квазинативного альбумина, и при этом первый транспортный полипептид не содержит какого-либо связывающего домена, присутствующего в указанном втором транспортном полипептиде.
[00209] В настоящем изобретении предложены мультиспецифические гетеромультимерные конструкции на основе альбумина согласно описанию выше, отличающиеся тем, что указанная первый полипептидный переносчик, содержащий по меньшей мере одну мутацию, выбранную из А194С, L198C, W214C, А217С, L331C и А335С. Согласно определенным вариантам реализации указанный второй полипептидный переносчик содержит по меньшей мере одну мутацию, выбранную из L331C, А335С, V343C, L346C, А350С, V455C hN458C.
[00210] Предложены выделенные мультиспецифические гетеромультимерные конструкции согласно описанию в настоящем документе, отличающиеся тем, что указанная мультиспецифическая гетеромультимерная конструкция одновременно задействует указанную по меньшей мере одну В-клетку и указанную по меньшей мере одну CD3-экспрессирующую клетку таким образом, что CD3-экспрессирующая клетка активируется, тем самым индуцируя киллинг указанной В-клетки.
[00211] Согласно определенным вариантам реализации предложены гетеромультимерные конструкции, содержащие полученные из альбумина полипептидные переносчики, самособирающиеся с образованием гетеромультимера, который проявляет сходные с характеристиками нативного альбумина функциональные характеристики, такие как связывание FcRn, и структурные характеристики. Согласно определенным вариантам реализации гетеромультимерные конструкции на основе альбумина согласно описанию в настоящем документе при введении нуждающемуся в этом индивидууму направленно мигрируют в опухолевые клетки. Согласно некоторым вариантам реализации указанные опухолевые клетки являются клетками солидной опухоли. Согласно некоторым вариантам реализации гетеромультимерные конструкции согласно описанию в настоящем документе направленно мигрируют в опухолевые клетки и затем связываются с указанными опухолевыми клетками. Согласно определенным вариантам реализации гетеромультимерные конструкции согласно описанию в настоящем документе направленно мигрируют по меньшей мере в одну опухолевую клетку, связываются одновременно с указанной по меньшей мере одной опухолевой клеткой и по меньшей мере с одной Т-клеткой таким образом, что это приводит к лизису указанной опухолевой клетки. Согласно определенным вариантам реализации гетеромультимерные конструкции согласно описанию в настоящем документе направленно мигрируют по меньшей мере к одной опухолевой клетке, связываются одновременно с указанной по меньшей мере одной опухолевой клеткой и по меньшей мере одной Т-клеткой таким образом, что связывание с указанной опухолевой клеткой происходит с большей валентностью по сравнению со связыванием с указанной Т-клеткой и вызывает лизис указанной опухолевой клетки.
[00212] Связывающие CD3-комплекс полипептидные конструкции:
[00213] Согласно определенным вариантам реализации мультиспецифических гетеромультимерных конструкций на основе иммуноглобулинов и альбумина согласно настоящему описанию, указанная гетеромультимерная конструкция содержит по меньшей мере одну CD3-связывающую полипептидную конструкцию, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке. Согласно некоторым вариантам реализации указанная по меньшей мере одна CD3-связывающая полипептидная конструкция содержит по меньшей мере один CD3-связывающий домен CD3-специфического антитела, нанотело, фибронектин, аффитело (Affibody), антикалин, белок типа «цистеиновый узел», дарпин, авимер, домен Куница или их вариант или производное. Согласно некоторым вариантам реализации указанный по меньшей мере один CD3-связывающий домен содержит по меньшей мере одну аминокислотныаминокислотную модификацию, снижающую иммуногенность по сравнению с соответствующим CD3-связывающим доменом, не содержащим указанной модификации. Согласно одному варианту реализации указанный по меньшей мере один CD3-связывающий домен содержит по меньшей мере одну аминокислотныаминокислотную модификацию, увеличивающую его стабильность согласно оценке на основе Tm, по сравнению с соответствующим CD3-связывающим доменом, не содержащим указанной модификации. Согласно некоторым вариантам реализации наблюдается повышение Tm приблизительно на 3 градуса по сравнению с нативным CD3-связывающим доменом, не содержащим указанной по меньшей мере одной модификации. Согласно некоторым вариантам реализации наблюдается повышение Tm, приблизительно на 5 градусов по сравнению с нативным CD3-связывающим доменом, не содержащим указанной по меньшей мере одной модификации. Согласно некоторым вариантам реализации наблюдается повышение Tm приблизительно на 8 градусов по сравнению с нативным CD3-связывающим доменом, не содержащим указанной по меньшей мере одной модификации. Согласно некоторым вариантам реализации наблюдается повышение Tm приблизительно на 10 градусов по сравнению с нативным CD3-связывающим доменом, не содержащим указанной по меньшей мере одной модификации.
[00214] Согласно некоторым вариантам реализации по меньшей мере одна CD3-связывающая полипептидная конструкция согласно описанию в настоящем документе содержит по меньшей мере один CD3-связывающий домен CD3-специфического антитела, при этом указанное CD3-специфическое антитело представляет собой антитело, содержащее только тяжелые цепи, не содержащее легких цепей.
[00215] Согласно некоторым другим вариантам реализации указанная по меньшей мере одна CD3-связывающая полипептидная конструкция согласно описанию в настоящем документе содержит по меньшей мере один CD3-связывающий домен, полученный из скаффолднового домена белка, не являющегося антителом.
[00216] Согласно определенным вариантам реализации указанные CD3-связывающие полипептидные конструкции представляют собой CD3-связывающие Fab- конструкции (т.е. антигенсвязывающие конструкции, содержащие тяжелую и легкую цепь, каждая из которых содержит вариабельную и константную область). Согласно определенному варианту реализации указанная Fab-конструкция принадлежит млекопитающему. Согласно одному варианту реализации указанная Fab-конструкция принадлежит человеку. Согласно другому варианту реализации указанная Fab-конструкция гуманизирована. Согласно еще одному варианту реализации указанная Fab-конструкция содержит по меньшей мере что-либо одно из константных областей тяжелой и легкой цепей человека. Согласно дополнительному варианту реализации указанная Fab-конструкция представляет собой одноцепочечный Fab (scFab).
[00217] Согласно определенным вариантам реализации указанные CD3-связывающие полипептидные конструкции содержат CD3-связывающие scFab конструкции, отличающиеся тем, что С-конец легкой цепи Fab соединен с N-концом тяжелой цепи Fab пептидным линкером. Указанный пептидный линкер обеспечивает расположение указанных тяжелой и легкой цепей Fab с образованием функционального CD3-связывающего фрагмента. Согласно определенным вариантам реализации пептидные линкеры, подходящие для соединения тяжелой и легкой цепей Fab, включают последовательности, содержащие глицин-сериновые линкеры, например, не ограничиваясь перечисленными, (GmS)n-GG, (SGn)m, (SEGn)m, где тип находятся в диапазоне 0-20. Согласно определенным вариантам реализации scFab-конструкция представляет собой кроссоверную конструкцию, отличающуюся тем, что константные области легкой цепи Fab и тяжелой цепи Fab рекомбинированы. Согласно другому варианту реализации кроссоверного Fab рекомбинированы вариабельные области легкой цепи Fab и тяжелой цепи Fab.
[00218] Согласно определенным вариантам реализации указанные CD3-связывающие полипептидные конструкции содержат CD3-связывающие Fv-конструкции (т.е. антигенсвязывающие конструкции, содержащие тяжелую и легкую цепь, каждая из которых содержит вариабельную область). Согласно определенному варианту реализации указанная Fv-конструкция принадлежит млекопитающему. Согласно одному варианту реализации указанная Fv-конструкция принадлежит человеку. Согласно другому варианту реализации указанная Fv-конструкция гуманизирована. Согласно еще одному варианту реализации указанная Fv-конструкция содержит по меньшей мере что-либо одно из вариабельных областей тяжелой и легкой цепей человека. Согласно дополнительному варианту реализации указанная Fv-конструкция представляет собой одноцепочечный Fv (scFv).
[00219] Согласно некоторым вариантам реализации CD3-связывающая полипептидная конструкция мультиспецифической гетеромультимерной конструкции согласно описанию в настоящем документе связывается по меньшей мере с одним компонентом CD3-комплекса. Согласно конкретному варианту реализации CD3-связывающая полипептидная конструкция связывается по меньшей мере с одним из CD3-эпсилон, CD3-y, CD3-дельта или CD3-зета CD3-комплекса. Согласно определенным вариантам реализации указанная CD3-связывающая полипептидная конструкция связывает домен CD3-эпсилон. Согласно определенным вариантам реализации связывающая полипептидная конструкция связывает CD3-комплекс человека. Согласно определенным вариантам реализации указанная CD3-связывающая полипептидная конструкция демонстрирует межвидовое связывание по меньшей мере с одним членом CD3-комплекса.
[00220] В настоящем изобретении предложены мультиспецифические гетеромультимерные конструкции на основе иммуноглобулина и альбумина, содержащие по меньшей мере одну CD3-связывающую полипептидную конструкцию, которая связывается с комплексом CD3 по меньшей мере на одной экспрессирующей CD3 клетке, при этом указанная CD3-экспрессирующая клетка представляет собой Т-клетку. Согласно определенным вариантам реализации указанная CD3-экспрессирующая клетка представляет собой клетку человека. Согласно некоторым вариантам реализации указанная CD3-экспрессирующая клетка представляет собой клетку не являющегося человеком млекопитающего. Согласно некоторым вариантам реализации указанная Т-клетка представляет собой цитотоксическую Т-клетку. Согласно некоторым вариантам реализации указанная Т-клетка представляет собой CD4+ или a CD8+ Т-клетку.
[00221] Согласно определенным вариантам реализации мультиспецифических гетеромультимерных конструкций на основе иммуноглобулина и альбумина согласно настоящему описанию указанная конструкция способна активировать и перенаправлять цитотоксическую активность Т-клетки на целевую клетку, такую как В-клетка. Согласно конкретному варианту реализации указанное перенаправление происходит независимо от опосредованного МНС презентирования пептидных антигенов целевой клеткой и/или специфичности Т-клетки.
[00222] В настоящем изобретении предложены гетеромультимерные конструкции, способные одновременно связываться с В-клеточным антигеном, например, антигеном опухолевой клетки, и активирующим Т-клеточным антигеном. Согласно одному из вариантов реализации указанная гетеромультимерная конструкция способна к перекрестному связыванию Т-клетки и целевой В-клетки за счет одновременного связывания с а В-клеточным антигеном, например, CD19 или CD20, и активирующим Т-клеточным антигеном, например, CD3. Согласно одному из вариантов реализации указанное одновременное связывание приводит к лизису целевой В-клетки, например, опухолевой клетки. Согласно одному из вариантов реализации такое одновременное связывание приводит к активации Т-клетки. Согласно другим вариантам реализации такое одновременное связывание приводит к клеточному ответу Т-лимфоцита, например, цитотоксического Т-лимфоцита, выбранному из группы, состоящей из: пролиферации, дифференцировки, секреции цитокинов, высвобождения цитотоксических эффекторных молекул, цитотоксической активности и экспрессии маркеров активации. Согласно одному из вариантов реализации связывание Т-клеток, активирующих биспецифическую антигенсвязывающую молекулу, с активирующим Т-клеточным антигеном без одновременного связывания с целевым клеточным антигеном не приводит к активации Т-клеток.
[00223]
[00224] Связывающие В-клетки полипептидные конструкции:
[00225] В настоящем изобретении предложены выделенные гетеромультимерные конструкции, содержащий по меньшей мере одну антигенсвязывающую полипептидную конструкцию, которая связывается с целевым антигеном по меньшей мере на одной В-клетке. Согласно определенным вариантам реализации указанная антигенсвязывающая полипептидная конструкция связывает по меньшей мере один член В-клеточного комплекса CD21-CD19-CD81. Согласно некоторым вариантам реализации указанная антигенсвязывающая полипептидная конструкция содержит по меньшей мере один CD 19-связывающий домен или его фрагмент. Согласно одному варианту реализации указанная антигенсвязывающая полипептидная конструкция содержит по меньшей мере один CD20-связывающий домен.
[00226] Согласно некоторым вариантам реализации указанный по меньшей мере один антигенсвязывающий домен представляет собой CD19- или CD20-связывающий домен, полученный из CD19- или CD20-специфического антитела, нанотела, фибронектина, аффитела, антикалина, белка типа «цистеиновый узел», искусственного белка с анкириновым повтором (DARPin), авимера, домена Куница или их варианта или производного. Согласно некоторым вариантам реализации указанная по меньшей мере одна антигенсвязывающая полипептидная конструкция согласно описанию в настоящем документе содержит по меньшей мере один антигенсвязывающий домен, который представляет собой CD19- или CD20-связывающий домен антитела, которое представляет собой антитело, содержащее только тяжелые цепи, не содержащее легких цепей.
[00227] Согласно некоторым вариантам реализации указанный по меньшей мере один антигенсвязывающий домен представляет собой CD19- или CD20-связывающий домен, который содержит по меньшей мере одну аминокислотныаминокислотную модификацию, снижающую иммуногенность по сравнению с соответствующим антигенсвязывающим доменом, не содержащим указанной модификации. Согласно одному варианту реализации указанный по меньшей мере один антигенсвязывающий домен представляет собой CD19- или CD20-связывающий домен, содержащий по меньшей мере одну аминокислотныаминокислотную модификацию, увеличивающую его стабильность по оценке на основе Tm, по сравнению с соответствующим доменом, не содержащим указанной модификации.
[00228] Согласно определенным вариантам реализации указанная по меньшей мере один антигенсвязывающая полипептидная конструкция представляет собой Fab-конструкцию, которая связывает по меньшей мере что-либо одно из CD19 и CD20 на В-клетке. Согласно определенному варианту реализации указанная Fab-конструкция принадлежит млекопитающему. Согласно одному варианту реализации указанная Fab-конструкция принадлежит человеку. Согласно другому варианту реализации указанная Fab-конструкция гуманизирована. Согласно еще одному варианту реализации указанная Fab-конструкция содержит по меньшей мере что-либо одно из константных областей тяжелой и легкой цепей человека. Согласно дополнительному варианту реализации указанная Fab-конструкция представляет собой одноцепочечный Fab (scFab).
[00229] Согласно определенным вариантам реализации CD19- и/или CD20-связывающая полипептидная конструкция содержит scFab-конструкцию, отличающуюся тем, что С-конец легкой цепи Fab соединен с N-концом тяжелой цепи Fab пептидным линкером. Указанный пептидный линкер обеспечивает расположение тяжелой и легкой цепей Fab с образованием функционального CD19- и/или CD20-связывающего фрагмента. Согласно определенным вариантам реализации пептидные линкеры, подходящие для соединения тяжелой и легкой цепей Fab, включают последовательности, содержащие глицин-сериновые линкеры, например, но не ограничиваясь перечисленными, (GmS)n-GG, (SGn)m, (SEGn)m, где тип принимают значения от 0 до 20. Согласно определенным вариантам реализации указанная scFab-конструкция представляет собой кроссоверную конструкцию, отличающуюся тем, что константные области легкой цепи Fab и тяжелая цепь Fab рекомбинированы. Согласно другому варианту реализации кроссоверной Fab рекомбинированы вариабельные области легкой цепи Fab и тяжелая цепь Fab.
[00230] Согласно определенным вариантам реализации указанная по меньшей мере одна антигенсвязывающая полипептидная конструкция представляет собой Fv-конструкцию, которая связывает на В-клетке по меньшей мере что-либо одно из CD19 и CD20. Согласно определенному варианту реализации указанная Fv-конструкция является Fv-конструкцией млекопитающих. Согласно одному варианту реализации указанная Fv-конструкция является Fv-конструкцией человека. Согласно другому варианту реализации указанная Fv-конструкция гуманизирована. Согласно еще одному варианту реализации указанная Fv-конструкция содержит по меньшей мере что-либо одно из вариабельных областей тяжелой и легкой цепей человека. Согласно дополнительному варианту реализации указанная Fv-конструкция представляет собой одноцепочечный Fv (scFv).
[00231] Согласно определенным вариантам реализации наблюдается межвидовое связывание указанной антигенсвязывающей полипептидной конструкции по меньшей мере с одним антигеном, экспрессируемым на поверхности В-клетки. Согласно некоторым вариантам реализации антигенсвязывающая полипептидная конструкция мультиспецифической гетеромультимерной конструкции согласно описанию в настоящем документе связывается по меньшей мере с одним из CD19 и CD20 млекопитающих. Согласно определенным вариантам реализации связывающая полипептидная конструкция связывает CD19 или CD20 человека.
[00232] В настоящем изобретении предложены гетеромультимерные конструкции, способные одновременно связываться с В-клеточным антигеном, например, антигеном опухолевой клетки, и активирующим Т-клеточным антигеном. Согласно одному из вариантов реализации указанная гетеромультимерная конструкция способна к перекрестному связыванию Т-клетки и целевой В-клетки посредством одновременного связывания с В-клеточным антигеном, например, CD19 или CD20, и активирующим Т-клеточным антигеном, например, CD3.
[00233] Согласно определенным вариантам реализации гетеромультимер, описанный в настоящем документе, содержит по меньшей мере одну антигенсвязывающую полипептидную конструкцию, которая связывается с целевым антигеном, таким как CD19 или CD20, по меньшей мере на одной В-клетке, связанной с заболеванием. Согласно некоторым вариантам реализации указанное заболевание представляет собой раковое заболевание, выбранное из карциномы, саркомы, лейкоза, лимфомы и глиомы. Согласно одному варианту реализации указанное раковое заболевание представляет собой по меньшей мере что-либо одно из плоскоклеточной карциномы, аденокарциномы, карциномы переходных клеток, остеосаркомы и саркомы мягких тканей. Согласно определенным вариантам реализации указанная по меньшей мере одна В-клетка представляет собой аутоиммунную реактивную клетку, которая представляет собой лимфоидную или миелоидную клетку.
[00234]
[00235] Дополнительные антигенсвязывающие конструкции:
[00236] Согласно определенным вариантам реализации мультиспецифическая гетеромультимерная конструкция на основе альбумина или иммуноглобулина согласно описанию в настоящем документе дополнительно содержит по меньшей мере один связывающий домен, который связывает по меньшей мере что-либо одно из: ЕрСАМ, EGFR, IGFR, HER-2 neu, HER-3, HER-4, PSMA, РЭА, MUC-1 (муцина), MUC2, MUC3, MUC4, MUC5, MUC7, CCR4, CCR5, CD19, CD20, CD33, CD30, ганглиозида GD3, 9-O-ацетил-GD3, GM2, поли (СА), GD2, карбоангидразы IX (MN/CA IX), CD44v6, белка «sonic hedgehog» (Shh), Wue-1, плазмоцитарного антигена (мембраносвязанного), протеогликана хондроитинсульфата меланомы (MCSP), CCR8, предшественника ФНО-альфа, STEAP, мезотелина, антигена А33, антигена стволовых клеток простаты (АСПК), Ly-6; десмоглеина 4, неоэпитопа Е-кадгерина, ацетилхолинового рецептора фетального типа, CD25, маркера CA19-9, маркера СА-125 и рецептора ингибирующего вещества Мюллера(MIS) II типа, sTn (сиалилированный Tn-антиген; TAG-72), FAP (антигена активации фибробластов), эндосиалина, LG, SAS, ЕРНА4 CD63, содержащих CD3 BsAb иммуноцитокинов ФНО, содержащих CD3-антитело, присоединенное к цитокину, ИФНγ, ИЛ-2 и TRAIL.
[00237]
[00238] Посттрансляционные модификации:
[00239] Согласно определенным вариантам реализации предложены мультиспецифические гетеромультимерные конструкции согласно описанию в настоящем документе, дифференциально модифицируемые во время или после трансляции. Согласно некоторым вариантам реализации указанная модификация представляет собой по меньшей мере что-либо одно из: гликозилирования, ацетилирования, фосфорилирования, амидирования, дериватизации посредством известных защитных/блокирующих групп, протеолитического расщепления и связывания с молекулой антитела или другим клеточным лигандом. Согласно некоторым вариантам реализации указанную гетеромультимерную конструкцию химически модифицируют посредством известных техник, включая, но не ограничиваясь перечисленными, специфическое химическое расщепление бромцианом, трипсином, химотрипсином, папаином, V8-протеазой, NaBH4; ацетилирование, формилирование, окисление, восстановление; и метаболический синтез в присутствии туникамицина.
[00240] Дополнительные посттрансляционные модификации гетеромультимеров согласно описанию в настоящем документе включают, например, N-связанные или О-связанные углеводные цепи, процессинг N-концевых или С-концевых участков), присоединение химических фрагментов к аминокислотному остову, химические модификации N-связанных или О-связанных углеводных цепей, и добавление или удаление N-концевого остатка метионина в результате экспрессии прокариотической клеткой-хозяином. Гетеромультимерные конструкции согласно описанию в настоящем документе модифицируют детектируемой меткой, такой как ферментная, флуоресцентная, изотопная или аффинная метка, что позволяет провести обнаружение и выделение указанного белка. Согласно определенным вариантам реализации примеры подходящих ферментных меток включают пероксидазу хрена, щелочную фосфатазу, бета-галактозидазу или ацетилхолинэстеразу; примеры подходящих комплексов простетической группы включают стрептавидин-биотин и авидин-биотин; примеры подходящих флуоресцентных материалов включают умбеллиферон, флуоресцеин, изотиоцианат флуоресцеина, родамин, дихлортриазиниламин флуоресцеина, дансилхлорид или фикоэритрин; пример люминесцентного материала включает люминол; примеры биолюминесцентных материалов включают люциферазу, люциферин и экворин; примеры подходящих радиоактивных материалов включают йод, углерод, серу, тритий, индий, технеций, таллий, галлий, палладий, молибден, ксенон, фтор.
[00241] Согласно конкретным вариантам реализации гетеромультимерные конструкции согласно описанию в настоящем документе присоединены к макроциклическим хелатообразователям, которые связываются с радиоактивными ионами металлов.
[00242] Согласно некоторым вариантам реализации гетеромультимерные конструкции согласно описанию в настоящем документе модифицируют либо посредством естественных процессов, таким как посттрансляционный процессинг, либо с помощью техник химической модификации, хорошо известных в данной области техники. Согласно определенным вариантам реализации модификации одного и того же типа могут присутствовать в равной или в разной степени на нескольких участках в определенном полипептиде. Согласно определенным вариантам реализации полипептиды гетеромультимеров согласно описанию в настоящем документе являются разветвленными, например, в результате убиквитинирования, и согласно некоторым вариантам реализации предложены циклические полипептиды, разветвленные и неразветвленные. Циклические, разветвленные, и разветвленные циклические полипептиды возникают в результате естественных посттрансляционных процессов или производятся с применением синтетических методов. Модификации включают ацетилирование, ацилирование, АДФ-рибозилирование, амидирование, ковалентное присоединение флавина, ковалентное присоединение фрагмента гема, ковалентное присоединение нуклеотида или производного нуклеотида, ковалентное присоединение липида или производного липида, ковалентное присоединение фосфатидилинозитола, перекрестное сшивание, циклизацию, образование дисульфидных связей, деметилирование, образование ковалентных поперечных связей, образование цистеина, образование пироглутамата, формилирование, γ-карбоксилирование, гликозилирование, образование ГФИ-якоря, гидроксилирование, йодирование, метилирование, миристилирование, окисление, пегилирование, протеолитический процессинг, фосфорилирование, пренилирование, рацемизацию, селеноилирование, сульфатирование, опосредованное тРНК добавление аминокислот к белкам, например, аргинилирование и убиквитинирование. (См., например, PROTEINS-STRUCTURE AND MOLECULAR PROPERTIES, 2nd Ed., T.Ε. Creighton, W.H. Freeman and Company, New York (1993); POST-TRANSLATIONAL COVALENT MODIFICATION OF PROTEINS, В.С. Johnson, Ed., Academic Press, New York, pgs. 1-12 (1983); Seifter et al., Meth. Enzymol. 182:626-646 (1990); Rattan et al., Ann. N.Y. Acad. Sci. 663:48-62 (1992)).
[00243] Согласно определенным вариантам реализации гетеромультимерные конструкций согласно описанию в настоящем документе присоединены к твердым подложкам, которые, в частности, подходят для иммунологических анализов или очистки полипептидов, связываемых, связывающих или ассоциированных с альбуминовыми гибридными белками согласно настоящему изобретению. Такие твердые подложки включают, не ограничиваясь перечисленными, стекло, целлюлозу, полиакриламид, нейлон, полистирол, поливинилхлорид или полипропилен.
[00244]
[00245] Полинуклеотиды:
[00246] В настоящем изобретении предложены полинуклеотидные конструкции, кодирующие мультиспецифические гетеромультимерные конструкции согласно описанию в настоящем документе. Согласно определенным вариантам реализации полинуклеотид или нуклеиновая кислота представляет собой ДНК. Согласно другим вариантам реализации полинуклеотид согласно описанию в настоящем документе представляет собой РНК, например, в форме матричной РНК (мРНК). РНК согласно настоящему изобретению может быть одноцепочечной или двуцепочечной.
[00247] Согласно определенным вариантам реализации предложен набор экспрессионных векторов для экспрессии мультиспецифической гетеромультимерной конструкции согласно описанию в настоящем документе, которая содержит первую, и вторую полипептидную конструкцию, при этом указанный набор содержит по меньшей мере первую последовательность ДНК, кодирующую указанную первую полипептидную конструкцию, и по меньшей мере вторую последовательность ДНК, кодирующую указанную вторую полипептидную конструкцию.
[00248] Согласно определенным вариантам реализации предложены полинуклеотидные последовательности, кодирующие гетеромультимерную конструкцию согласно описанию в настоящем документе или соответствующую ей полипептидную конструкцию с последовательностью согласно настоящему описанию. Согласно определенным вариантам реализации предложен полинуклеотид, содержащий последовательность, по меньшей мере приблизительно на 80%, 85%, 90%, 95%, 96%, 97%, 98%, или 99% идентичную нуклеотидной последовательности, представленной на фиг. _. Согласно определенным вариантам реализации предложены полинуклеотидные последовательности, кодирующие гетеромультимерную конструкцию согласно описанию в настоящем документе или соответствующую ей полипептидную конструкцию, при этом указанный полинуклеотид содержит консервативные мутации указанной последовательности согласно настоящему описанию.
[00249]
[00250] Способы рекомбинантного и синтетического получения мультиспецифических гетеромультимерных конструкций:
[00251] Предложены способы получения экспрессионного продукта, содержащего мультиспецифическую гетеромультимерную конструкцию согласно описанию в настоящем документе в стабильных клетках млекопитающего, при этом указанный способ включает: трансфицирование по меньшей мере одной клетки млекопитающего: по меньшей мере первой последовательностью ДНК, кодирующей указанную первую полипептидную конструкцию, и по меньшей мере второй последовательностью ДНК, кодирующей указанную вторую полипептидную конструкцию, таким образом, что указанной по меньшей мере одной первой последовательностью ДНК, указанной по меньшей мере одной второй последовательностью ДНК трансфицируют указанную по меньшей мере одну клетку млекопитающего в заранее заданном соотношении с получением стабильных клеток млекопитающих; культивирование указанных стабильных клеток млекопитающих с получением указанного продукта экспрессии, содержащего указанный мультиспецифический гетеромультимер. Согласно определенным вариантам реализации указанное заданное отношение по меньшей мере одной первой последовательности ДНК к по меньшей мере одной второй последовательности ДНК составляет приблизительно 1:1. Согласно некоторым другим вариантам реализации указанное заданное отношение по меньшей мере одной первой последовательности ДНК к по меньшей мере одной второй последовательности ДНК сдвигается в сторону большего количества одной первой последовательности ДНК, например, до приблизительно 2:1. Согласно дополнительным вариантам реализации указанное заданное отношение по меньшей мере одной первой последовательности ДНК к по меньшей мере одной второй последовательности ДНК сдвигается в сторону большего количества одной первой последовательности ДНК, например, до приблизительно 1:2. Согласно избранным вариантам реализации клетку млекопитающего выбирают из группы, состоящей из клеток VERO, HeLa, НЕК, NS0, клеток яичника китайского хомячка (СНО), W138, ВНК, COS-7, Сасо-2 и MDCK, и их подклассов и вариантов.
[00252] Согласно определенным вариантам реализации предложены гетеромультимеры. получаемые в виде рекомбинантные молекул путем секретирования дрожжами, микроорганизмом, таким как бактерия, или линией клеток человека или животного. Согласно вариантам реализации указанные полипептиды секретируются клеткам и-хозяевам и.
[00253] Варианты реализации включают клетку, такую как дрожжевая клетка, трансформированную для экспрессии гетеромультимерного белка согласно описанию в настоящем документе. Помимо собственно трансформированных клеток-хозяев, предложена культура указанных клеток, предпочтительно моноклональная (клонально-однородная) культура, или культура, полученная из моноклональной культуры, в питательной среде. Если указанный полипептид секретируется, среда содержит указанный полипептид с клетками или без клеток, если последние были отфильтрованы или отделены центрифугированием. Известны и подходят для применения многие экспрессионные системы, включая бактерии (например, Е. coli и Bacillus subtilis), дрожжи (например, Saccharomyces cerevisiae, Kluyveromyces lactis и Pichia pastoris, мицелиальные грибы (например, Aspergillus), растительные клетки, клетки животных и клетки насекомых.
[00254] Гетеромультимер, описанный в настоящем документе, получают обычными способами, например, из кодирующей последовательности, встроенной в хромосому хозяина, или на свободной плазмиде. Дрожжи трансформируют кодирующей последовательностью нужного белка любым общепринятым способом, например, электропорацией. Способы трансформации дрожжей путем электропорации раскрыты в источнике: Becker & Guarente (1990) Methods Enzymol. 194, 182.
[00255] Успешно трансформированные клетки, т.е., клетки, которые содержат ДНК-конструкцию согласно настоящему изобретению, могут быть идентифицированы путем хорошо известных техник. Например, клетки, полученные в результате встраивания экспрессионной конструкции, могут культивироваться для продуцирования нужного полипептида. Клетки могут быть собраны, лизированы и содержащаяся в них ДНК протестирована на присутствие указанной ДНК с применением такого способа, как описанный у Southern (1975) J. Mol. Biol. 98, 503 или Berent et al. (1985) Biotech. 3, 208. Как вариант, присутствие указанного белка в супернатанте может быть обнаружено с применением антител.
[00256] Подходящие дрожжевые плазмидные векторы включают pRS403-406 и pRS413-416 и, как правило, поставляются Stratagene Cloning Systems, Ла Хойя, Калифорния 92037, США. Плазмиды pRS403, pRS404, pRS405 и pRS406 представляют собой дрожжевые интегративные плазмиды (Yip) и включают дрожжевые селектируемые маркеры HIS3, 7RP1, LEU2 и URA3. Плазмиды pRS413-416 представляют собой дрожжевые центромерные плазмиды (Ycp).
[00257] Разработаны различные способы функционального связывания ДНК с векторами посредством комплементарных липких концов. Например, к сегменту ДНК для встраивания в ДНК-вектор могут быть добавлены комплементарные гомополимерные участки. Указанный вектор и сегмент ДНК затем соединяются за счет водородных связей между комплементарными гомополимерными концевыми участками с образованием рекомбинантных молекул ДНК.
[00258] Синтетические линкеры, содержащие один или несколько участков рестрикции, обеспечивают альтернативный способ соединения ДНК-сегмента с векторами. Сегмент ДНК, полученный путем расщепления рестрикционной эндонуклеазой, обрабатывают ДНК-полимеразой бактериофага Т4 или ДНК-полимеразой 1 Е. coli, ферментами, удаляющими выступающие одноцепочечные концы за счет присущей им 3'-5'-экзонуклеазной активности, и заполняют вырезанные участки на 3'-концах за счет полимеразной активности.
[00259] Комбинация указанных видов активности приводит к образованию сегментов ДНК с тупыми концами. Сегменты с тупыми концами затем инкубируют с линкерными молекулами при значительном молярном избытке последних в присутствии фермента, способного катализировать лигирование молекул ДНК с тупыми концами, такими как ДНК-лигаза бактериофага Т4. Таким образом, продуктами реакции являются ДНК-сегменты, несущие на концах полимерные линкерные последовательности. Указанные ДНК-сегменты затем расщепляют подходящим рестрикционным ферментом и лигируют в экспрессионный вектор, расщепленный ферментом, обеспечивающим получение концов, совместимых с указанным сегментом ДНК.
[00260] Синтетические линкеры, содержащие различные участки эндонуклеазной рестрикции, коммерчески доступны из ряда источников, включая International Biotechnologies Inc, Нью-Хейвен, Коннектикут, США.
[00261] Примерами родов дрожжей, которые рассматриваются как подходящие для реализации настоящего изобретения в качестве хозяев для экспрессии альбуминовых гибридных белков, являются Pichia (ранее классифицировавшиеся как Hansenula), Saccharomyces, Kluyveromyces, Aspergillus, Candida, Torulopsis, Torulaspora, Schizosaccharomyces, Citeromyces, Pachysolen, Zygosaccharomyces, Debaromyces, Trichoderma, Cephalosporium, Humicola, Mucor, Neurospora, Yarrowia, Metschunikowia, Rhodosporidium, Leucosporidium, Botryoascus, Sporidiobolus, Endomycopsis и т.п. Предпочтительный родами являются выбранные из группы, состоящей из Saccharomyces, Schizosaccharomyces, Kluyveromyces, Pichia и Torulaspora. Примеры Saccharomyces spp. представлены S. cerevisiae, S. italicus и S. rouxii.
[00262] Примеры родов Kluyveromyces представлены К. fragilis, К. lactis и К. marxianus. Подходящим видом Torulaspora является T. delbrueckii. Примеры рода Pichia (Hansenula) представлены P. angusta (ранее - H. polymorpha), Р. anomala (ранее - Н. anomala) и P. pastoris. Способы трансформации S. cerevisiae в общем описаны в ЕР 251744, ЕР 258067 и WO 90/01063, каждый из которых включен в настоящий документ посредством ссылок.
[00263] Примеры видов Saccharomyces, подходящих для синтеза гетеромультимерных конструкций согласно описанию в настоящем документе, включают S. cerevisiae, S. italicus, S. diastaticus и Zygosaccharomyces rouxii. Предпочтительные примеры видов Kluyveromyces включают К. fragilis и К. lactis. Предпочтительные примеры видов Hansenula включают Н. polymorpha (в настоящее время Pichia angusta), H. anomala (в настоящее время Pichia anomala) и Pichia capsulata. Дополнительные предпочтительные примеры видов Pichia включают P. pastoris. Предпочтительные примеры видов Aspergillus включают A. niger и А. nidulans. Предпочтительные примеры видов Yarrowia включают Y. lipolytica. Многие предпочтительные виды дрожжей поставляются АТСС. Например, следующие предпочтительные виды дрожжей поставляются АТСС и подходят для экспрессии альбуминовых гибридных белков: Saccharomyces cerevisiae Hansen, телеоморфный мутантный по уарЗ штамм BY4743 (№ доступа АТСС 4022731); Saccharomyces cerevisiae Hansen, телеоморфный мутантный по hsp150 штамм BY4743 (№ доступа АТСС 4021266); Saccharomyces cerevisiae Hansen, телеоморфный мутантный по pmtl штамм BY4743 (№доступа АТСС 4023792); Saccharomyces cerevisiae Hansen, телеоморф (АТСС №№ доступа 20626; 44773; 44774; и 62995); Saccharomyces diastaticus Andrews et Gilliland ex van der Walt, телеоморф (№доступа АТСС 62987); Kluyveromyces lactis (Dombrowski) van der Walt, телеоморф (№ доступа АТСС 76492); Pichia angusta (Teunisson et al.) Kurtzman, телеоморф, помещен на хранение как Hansenula polymorpha de Morais et Maia, телеоморф (№ доступа АТСС 26012); Aspergillus niger van Tieghem, анаморф (№ доступа АТСС 9029); Aspergillus niger van Tieghem, анаморф (№ доступа АТСС 16404); Aspergillus nidulans (Eidam) Winter, анаморф (№ доступа АТСС 48756); и Yarrowia lipolytica (Wickerham et al.) van der Walt et von Arx, телеоморф (№ доступа АТСС 201847).
[00264] Подходящие промоторы для S. cerevisiae включают связанные с геном PGKI, генами GAL1 или GAL10, CYCI, РН05, TRP1, ADH1, ADH2, генами глицеральдегид-3-фосфатдегидрогеназы, гексокиназы, пируватдекарбоксилазы, фосфофруктокиназы, триозофосфатизомеразы, фосфоглюкозоизомеразы, глюкокиназы, альфа-фактора - феромона спаривания, [феромонного фактора спаривания], промотор PRBI, промотор GUT2, промотор GPDI и гибридные промоторы, в том числе гибриды участков 5'-регуляторных областей и участков 5'-регуляторных областей других промоторов или расположенных в 3'-5' направлении участков активации (например, промотор ЕР-А-258067).
[00265] Удобными регулируемыми промоторами для применения у Schizosaccharomyces pombe являются репрессируемый тиамином промотор гена nmt, соответствующий описанию в источнике: Maundrell (1990) J. Biol. Chem. 265, 10857-10864, и репрессируемый глюкозой промотор гена jbpl согласно описанию в Hoffman & Winston (1990) Genetics 124, 807-816.
[00266] Способы трансформации Pichia для экспрессии чужеродных генов описаны, например, у Cregg et al. (1993), и в различных патентах Phillips (например, патенте США №4857467, включенном в настоящий документ посредством ссылки); наборы для экспрессии в Pichia коммерчески доступны от Invitrogen BV, Лек, Нидерланды, и Invitrogen Corp., Сан-Диего, Калифорния. Подходящие промоторы включают АОХ1 и АОХ2. Gleeson et al. (1986) J. Gen. Microbiol. 132, 3459-3465 приводят информацию о векторах и трансформации Hansenula, подходящими промоторами являются МОХ1 и FMD1; в ЕР 361991, Fleer et al. (1991) и других публикациях Rhone-Poulenc Rorer содержится информация о способах экспрессии чужеродных белков в видах Kluyveromyces; подходящим промотором является PGKI.
[00267] Сигнал терминации транскрипции представляет собой предпочтительно 3'-фланкирующую последовательность эукариотического гена, который содержит подходящие сигналы терминации транскрипции и полиаденилирования. Подходящие 3'-фланкирующие последовательности могут, например, представлять собой такие последовательности гена, в естественных условиях связанного с используемой последовательностью контроля экспрессии, т.е. могут соответствовать промотору. Как вариант, они могут быть разными, в этом случае предпочтительным является сигнал терминации гена S. cerevisiae ADHI.
[00268] Согласно определенным вариантам реализации нужный гетеромультимерный белок сначала экспрессируют с лидерной последовательностью, которая может представлять собой любую лидерную последовательность, эффективную для выбранных дрожжей. Лидерные последовательности, подходящие для S. cerevisiae, включают последовательности полипептида альфа-фактора спаривания (MFD-1) и гибридные лидерные последовательности ЕР-А-387319. Такие лидерные (или сигнальные) последовательности расщепляются дрожжами до высвобождения зрелого альбумина в окружающую среду. Также такие лидерные последовательности включают лидерные последовательности инвертазы S. cerevisiae (SUC2), описанные в JP 62-096086 (присвоенный номер 911036516), кислой фосфатазы (РН05), препоследовательность MFα-1,0-глюканазы (BGL2) и киллерного токсина; глюкоамилазы II S. diastaticus; α-галактозидазы S. carlsbergensis (MEL1); киллерного токсина К. lactis; и глюкоамилазы Candida.
[00269] Предложены векторы, содержащие полинуклеотиды, кодирующие гетеромультимерную конструкцию согласно описанию в настоящем документе, клетки-хозяева и получение указанных гетеромультимерных белков с применением синтетических и рекомбинантных техник. Вектор может быть, например, фаговым, плазмидным, вирусным или ретровирусным вектором. Ретровирусные векторы могут быть способными к репликации или дефектными по репликации. В последнем случае, размножение вирусов, как правило, происходит только в соответствующих клетках-хозяевах.
[00270] Согласно определенным вариантам реализации полинуклеотиды, кодирующие гетеромультимерные белки согласно описанию в настоящем документе, соединяют с вектором, содержащим селектируемый маркер, для размножения в хозяине. Как правило, плазмидный вектор вводят в преципитате, таком как кальций-фосфатный преципитат, или в комплексе с заряженным липидом. В том случае, если вектор представляет собой вирус, он может быть «упакован» in vitro с применением подходящей пакующей линии клеток и затем трансдуцирован в хозяйские клетки.
[00271] Согласно определенным вариантам реализации указанная полинуклеотидная вставка функционально связана с подходящим промотором, таким как, помимо прочих, промотор фага лямбда PL, промоторы lac, trp, phoA и гас Ε. coli, ранний и поздний промоторы SV40 и промоторы ретровирусных LTR-последовательностей. Специалистам в данной области техники известны и другие подходящие промоторы. Экспрессионные конструкции также содержат участки инициации транскрипции, терминации транскрипции, и, в транскрибируемой области, сайт связывания рибосом для трансляции. Кодирующая часть транскриптов, экспрессируемых с применением указанных конструкций, предпочтительно включает а кодон инициации трансляции в начале и кодон терминации трансляции (UAA, UGA или UAG), подходящим образом расположенный на конце подлежащего трансляции полипептида.
[00272] Как отмечалось, экспрессионные векторы предпочтительно включают по меньшей мере один селектируемый маркер. Такие маркеры включают дигидрофолатредуктазу, G418, глутаминсинтазу или ген устойчивости к неомицину для культур эукариотических клеток и к тетрациклину, канамицину или ампициллину для культивирования Е. coli и других бактерий. Представительные примеры подходящих хозяев включают, не ограничиваясь перечисленными, бактериальные клетки, такие как Е. coli, клетки Streptomyces и Salmonella typhimurium; клетки грибов, например, клетки дрожжей (например, Saccharomyces cerevisiae или Pichia pastoris (№доступа АТСС 201178)); клетки насекомых, такие как клетки Drosophila S2 и Spodoptera Sf9; клетки животных, например, клетки СНО, COS, NSO, 293 и клетки меланомы Bowes; и растительные клетки. Среды и условия, подходящие для культивирования описанных выше клеток-хозяев, известны в данной области техники.
[00273] Векторы, предпочтительные для применения у бактерий, включают pQE70, pQE60 и pQE-9, поставляемые QIAGEN, Inc.; векторы pBluescript, векторы Phagescript, pNH8A, pNH16a, pNH18A; pNH46A, поставляемые Stratagene Cloning Systems, Inc.; и ptrc99a, pKK223-3, pKK233-3, pDR540, pRIT5, поставляемые Pharmacia Biotech, Inc. Предпочтительные эукариотические векторы включают pWLNEO, pSV2CAT, pOG44, pXT1 и pSG, поставляемые Stratagene; и pSVK3, pBPV, pMSG и pSVL, поставляемые Pharmacia. Предпочтительные экспрессионные векторы для применения в дрожжевых системах включают, не ограничиваясь перечисленными, pYES2, pYD1, pTEF1/Zeo, pYES2/GS, pPICZ, pGAPZ, pGAPZalph, pPIC9, pPIC3.5, pHIL-D2, pHIL-S1, pPIC3.5K, pPIC9K и PA0815 (все они поставляются Invitrogen, Карлбад, Калифорния). Специалист в данной области техники сможет легко определить другие подходящие векторы.
[00274] Согласно одному из вариантов реализации полинуклеотиды, кодирующие мультиспецифическую гетеромультимерную конструкцию согласно описанию в настоящем документе, соединены с сигнальными последовательностями, определяющими локализацию белка согласно настоящему изобретению в определенных компартментах прокариотической или эукариотической клетки и/или направляющими секрецию белка согласно настоящему изобретению из прокариотической или эукариотической клетки. Например, в случае Е. coli, может быть желательно направленную экспрессию указанного белка в периплазматическом пространстве. Примеры сигнальных последовательностей или белков (или их фрагментов), с которыми соединяют указанные гетеромультимерные белки для направленной экспрессии полипептида в периплазматическом пространстве бактерий, включают, не ограничиваясь перечисленными, сигнальную последовательность pelB, сигнальную последовательность связывающего мальтозу белка (МВР), МВР, сигнальную последовательность ompA, сигнальную последовательность В-субъединицы периплазматического термолабильного энтеротоксина Е. coli и сигнальную последовательность щелочной фосфатазы. Коммерчески доступен ряд векторов для конструирования гибридных белков, определяющих локализацию белка, например, серия векторов pMAL (в частности, серия pMAL-.rho.), доступных от New England Biolabs. Согласно конкретному варианту реализации полинуклеотиды альбуминовых гибридных белков согласно настоящему изобретению могут быть соединены с сигнальной последовательностью пектатлиазы pelB для повышения эффективности экспрессии и очистки таких полипептидов у грамотрицательных бактерий. См. патенты США №5576195 и №5846818, содержание которых полностью включено в настоящий документ посредством ссылок.
[00275] Примеры сигнальных пептидов, которые соединены с гетеромультимерными белками для обеспечения направленной секреции в клетках млекопитающих, включают, не ограничиваясь перечисленными, сигнальную последовательность MPIF-1 (например, аминокислотны 1-21 последовательность с № доступа GenBank ААВ51134), сигнальную последовательность станниокальцина (MLQNSAVLLLLVISASA) и консенсусную сигнальную последовательность (MPTWAWWLFLVLLLALWAPARG). Подходящей сигнальной последовательностью для применения в сочетании с бакуловирусными экспрессионными системами является сигнальная последовательность gp67 (например, аминокислотны 1-19 последовательности с №доступа GenBank ААА72759).
[00276] Векторы, где задействована глутаминсинтаза (ГС) или ДГФР в качестве селектируемых маркеров, могут быть амплифицированы в присутствии лекарственных средств метионинсульфоксимина или метотрексата, соответственно. Преимущество основанных на глутаминсинтазе векторов заключается в доступности клеточных линий (например, линии клеток миеломы мыши, NSO), негативных по глутаминсинтазе. Глутаминсинтазные экспрессионные системы могут также функционировать в экспрессирующих глутаминсинтазу клетках (например, клетках яичника китайского хомячка (СНО)) при наличии дополнительного ингибитора, подавляющего функцию эндогенного гена. Глутаминсинтазная экспрессионная система и ее компоненты подробно описаны в РСТ-публикациях: WO 87/04462; WO 86/05807; WO 89/10036; WO 89/10404; и WO 91/06657, которые включены в настоящий документ полностью посредством ссылок. Кроме того, глутаминсинтазные экспрессионные векторы могут быть получены от Lonza Biologies, Inc. (Портсмут, Нью-Гэмпшир). Экспрессия и синтез моноклональных антител с применением ГС экспрессионной системы в клетках миеломы мыши описаны в источниках: Bebbington et al., Bio/technology 10:169(1992) и Biblia and Robinson Biotechnol. Prog. 11:1(1995), которые включены в настоящий документ посредством ссылок.
[00277] Также предложены клетки-хозяева, содержащие векторные конструкции согласно описанию в настоящем документе, и дополнительно клетки-хозяева, содержащие нуклеотидные последовательности, функционально связанные с одной или несколькими гетерологичными контрольными областями (например, промотором и/или энхансером) с применением известных в данной области техник. Клетка-хозяин может представлять собой клетку высших эукариот, такую как клетка млекопитающего (например, клетку, полученную от человека), или низших эукариот, такую как дрожжевая клетка, или указанная клетка-хозяин может представлять собой прокариотическую клетку, такую как бактериальная клетка. Может быть выбран хозяйский штамм, модулирующий экспрессию встроенных генных последовательностей, или модифицирует и процессирует генный продукт конкретным требуемым образом. Экспрессия под определенными промоторами может увеличиваться в присутствии некоторых индукторов; таким образом можно контролировать экспрессию генетически сконструированного полипептида. Кроме того, разным клеткам-хозяевам свойственны характеристики и специфические механизмы трансляционного и посттрансляционного процессинга и модификации (например, фосфорилирование, расщепление) белков. Могут быть подобраны подходящие клеточные линии для обеспечения требуемых модификаций и процессинга экспрессированного чужеродного белка.
[00278] Введение нуклеиновых кислот и нуклеиновокислотных конструкций согласно настоящему изобретению в клетку-хозяина может быть реализовано путем трансфекции с фосфатом кальция, опосредованной диэтиламиноэтилдекстраном трансфекции, опосредованной катионными липидами трансфекции, электропорации, трансдукции, инфекции, или с помощью других способов. Такие способы описаны во многих стандартных лабораторных руководствах, например: Davis et al., Basic Methods In Molecular Biology (1986). Конкретным образом предусмотрена возможность, когда полипептиды согласно настоящему изобретению могут фактически экспрессироваться клеткой-хозяином, в которой отсутствует рекомбинантный вектор.
[00279] Помимо клеток-хозяев, содержащих векторные конструкции, описанные в настоящем документе, настоящее изобретение также охватывает первичные, вторичные, и иммортализованные клетки-хозяева, происходящие из позвоночного животного, в частности, млекопитающего, сконструированные для удаления или замены эндогенного генетического материала (например, кодирующая последовательность, соответствующая транспортному полипептиду, заменена на гетеромультимерный белок/ соответствующий указанному транспортному полипептиду) и/или включения генетического материала. Указанный генетический материал, функционально связанный с эндогенным полинуклеотидом, может активировать, изменять и/или амплифицировать эндогенные полинуклеотиды.
[00280] Кроме того, могут применяться известные в данной области техники методы функционального связывания гетерологичных полинуклеотидов (например, полинуклеотидов, кодирующих белок альбумин, или его фрагмент или вариант) и/или гетерологичных контрольных областей (например, промоторов и/или энхансеров) с эндогенными полинуклеотидными последовательностями, кодирующими терапевтический белок, посредством гомологичной рекомбинации (см., например, патент США №5641670, выданный 24 июня 1997 г; номер международной публикации WO 96/29411; номер международной публикации WO 94/12650; Roller et al., Proc. Natl. Acad. Sci. USA 86:8932-8935 (1989); и Zijlstra et al., Nature 342:435-438 (1989), содержание каждого из которых полностью включено посредством ссылок).
[00281] Гетеромультимерные белки согласно описанию в настоящем документе могут быть выделены и очищены из рекомбинантных клеточных культур путем общеизвестных способов, включая преципитацию сульфатом аммония или этанолом, кислотную экстракцию, анионную ионообменную или катионную ионообменную хроматографию, хроматографию на фосфоцеллюлозе, хроматографию с гидрофобным взаимодействием, аффинную хроматографию, например, с белком А, хроматографию с гидроксиапатитом, хроматографию с гидрофобным взаимодействием/взаимодействием зарядов и лектиновую хроматографию. Наиболее предпочтительно использование для очистки высокоэффективной жидкостной хроматографии («ВЭЖХ»).
[00282] Согласно определенным вариантам реализации гетеромультимерные белки согласно настоящему изобретению очищают с применением анионообменной хроматографии, включая, но не ограничиваясь перечисленным, хроматографию на колонках с Q-сефарозой, сефарозой DEAE, Poros HQ, Poros DEAF, Toyopearl Q, Toyopearl QAE, Toyopearl DEAE, Resource/Source Q и DEAE, Fractogel Q и DEAE.
[00283] Согласно конкретным вариантам реализации белки согласно описанию в настоящем документе очищают с применением катионообменной хроматографии, в том числе, но не ограничиваясь перечисленным, на колонках с SP-сефарозой, СМ-сефарозой, Poros HS, Poros CM, Toyopearl SP, Toyopearl CM, Resource/Source S и CM, Fractogel S и CM, a также эквивалентных и сопоставимых с ними колонках.
[00284] Кроме того, гетеромультимерные белки согласно описанию в настоящем документе могут быть химически синтезированы с применением техник, известных в данной области техники (например, см. Creighton, 1983, Proteins: Structures and Molecular Principles, W.H. Freeman & Co., N.Y and Hunkapiller et al., Nature, 310:105-111 (1984)). Например, полипептид, соответствующий фрагменту полипептида, может быть синтезирован на синтезаторе пептидов. Кроме того, при необходимости в указанную полипептидную последовательность могут вводиться в качестве замены или добавления неклассические аминокислоты или химические аналоги аминокислот. Неклассические аминокислоты включают, не ограничиваясь перечисленными, D-изомеры обычных аминокислот, 2,4-диаминомасляную кислоту, альфа-аминоизомасляную кислоту, 4-аминомасляную кислоту, аминомасляную кислоту (Abu), 2-аминомасляную кислоту, гамма-аминомасляную кислоту (g-Abu), Е-аминокапроновую кислоту (e-Ahx), 6-аминогексановую кислоту, аминоизомасляную кислоту (Aib), 2-аминоизомасляную кислоту, 3-аминопропионовую кислоту, орнитин, норлейцин, норвалин, гидроксипролин, саркозин, цитруллин, гомоцитруллин, цистеиновую кислоту, трет-бутилглицин, трет-бутилаланин, фенилглицин, циклогексилаланин, β-аланин, фторамино кислотны, искусственные аминокислоты, такие как β-метиламинокислоты, Cα-метиламинокислоты, Nα-метиламинокислоты, и аналоги аминокислот в целом. Кроме того, аминокислота может быть D (правовращающей) или L (левовращающей).
[00285]
[00286] Анализы:
[00287] Может проводиться исследование функциональной активности гетеромультимерных конструкций согласно описанию в настоящем документе (например, биологической активности) с применением известных в данной области техники или рутинным образом модифицированных анализов, а также анализов согласно описанию в настоящем документе.
[00288] Например, согласно одному варианту реализации для анализа способности гетеромультимерной конструкции согласно описанию в настоящем документе связывать антиген или конкурировать с другим полипептидом за связывание с антигеном, или связываться с Fc-рецептором и/или антителом против альбумина, могут применяться различные иммунологические анализы, известные в данной области техники, включая, но не ограничиваясь перечисленными, системы конкурентного и неконкурентного анализа, с применением таких техник, как радиоиммуноанализ, ИФА ELISA (ферментный иммуносорбентный анализ), иммунологический «сэндвич-анализ», иммунорадиометрический анализ, реакции диффузной преципитации в геле, анализы с применением иммунодиффузии, иммунологические анализы in situ (например, с применением коллоидного золота, фермента или радиоизотопных меток), вестерн-блоттинг, реакции осаждения, агглютинационный анализ (например, гель-агглютинационный анализ, гемагглютинационный анализ), анализ связывания комплемента, иммунофлуоресцентный анализ, анализы с белком А, и иммуноэлектрофоретический анализ и т.д. Согласно одному из вариантов реализации связывание антитела обнаруживают путем детекции метки на первичном антителе. Согласно другому варианту реализации первичное антитело обнаруживают путем детекции связывания вторичного антитела или реагента с указанным первичным антителом. Согласно дополнительному варианту реализации указанное вторичные антитело является меченым. В данной области техники известно множество способов детекции связывания в ходе иммунологического анализа, и такие способы входят в объем настоящего изобретения.
[00289] Согласно определенным вариантам реализации, при идентифицировании партнера для связывания (например, рецептора или лиганда) антигенсвязывающего домена, содержащегося в гетеромультимере, описанном в настоящем документе, связывание с партнером для связывания гетеромультимером, описанным в настоящем документе, анализируют, например, с помощью общеизвестных в данной области техники способов, таких как, например, редуцирующая и нередуцирующая гель-хроматография, аффинная хроматография белков и аффинный блоттинг.См. в общем Phizicky et al., Microbiol. Rev. 59:94-123 (1995). Согласно другому варианту реализации указанная способность физиологических коррелятов гетеромультимерного белка связываться с субстратом(ами) антигенсвязывающих полипептидных конструкций гетеромультимеров согласно описанию в настоящем документе, может быть рутинно проанализирована с применением методов, известных в данной области техники.
[00290]
[00291] Терапевтическое применение:
[00292] Согласно одному аспекту гетеромультимеры согласно описанию в настоящем документе предназначены для терапии на основе антител, включающей введение описанных гетеромультимеров, содержащих транспортный(ые) полипептид(ы), который(ые) представляет(ют) собой антитело, фрагмент или вариант антитела, пациенту для лечения одного или нескольких описанных заболеваний, расстройств или состояний. Терапевтические соединения согласно описанию в настоящем документе включают, не ограничиваясь перечисленными, гетеромультимеры согласно описанию в настоящем документе, нуклеиновые кислоты, кодирующие гетеромультимеры согласно описанию в настоящем документе.
[00293] Согласно определенным вариантам реализации предложен способ предотвращения, лечения или облегчения по меньшей мере чего-либо одного из: пролиферативного заболевания, минимального остаточного рака, опухолевого заболевания, воспалительного заболевания, иммунологического расстройства, аутоиммунного заболевания, инфекционного заболевания, вирусного заболевания, аллергических реакций, паразитарных реакций, реакций «трансплантат против хозяина» или реакций «хозяин против трансплантата» или злокачественных клеточных новообразований, при этом указанный способ включает введение субъекту, нуждающемуся в таком предотвращении, лечении или облегчении, фармацевтической композиции, содержащей гетеромультимерную конструкцию согласно описанию в настоящем документе.
[00294] Согласно определенным вариантам реализации предложен способ лечения ракового заболевания у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему композиции, содержащей эффективное количество фармацевтической композиции согласно описанию в настоящем документе, необязательно в комбинации с другими фармацевтически активными молекулами. Согласно определенным вариантам реализации указанное раковое заболевание представляет собой солидную опухоль. Согласно некоторым вариантам реализации указанная солидную опухоль представляет собой что-либо одно или более из саркомы, карциномы и лимфомы. Согласно некоторым другим вариантам реализации указанное раковое заболевание представляет собой гематологическое раковое заболевание. Согласно некоторым вариантам реализации указанное раковое заболевание представляет собой что-либо одно или более из В-клеточной лимфомы, неходжкинской лимфомы и лейкоза.
[00295] Предложен способ лечения раковых клеток, включающий обеспечение указанной композицией, содержащей гетеромультимерную конструкцию согласно описанию в настоящем документе. Согласно некоторым вариантам реализации указанный способ включает также обеспечение указанным гетеромультимером в сочетании с другим терапевтическим агентом.
[00296] Предложен способ лечения ракового заболевания, не поддающегося лечению блинатумомабом, у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему композиции, содержащей эффективное количество фармацевтической композиции, содержащей гетеромультимерную конструкцию согласно описанию в настоящем документе.
[00297] Согласно некоторым вариантам реализации предложен способ лечения раковой клетки, регрессирующей после лечения блинатумомабом, включающий обеспечение указанной раковой клетки композицией, содержащей эффективное количество фармацевтической композиции, содержащей гетеромультимерную конструкцию согласно описанию в настоящем документе.
[00298] Согласно некоторым вариантам реализации предложен способ лечения индивидуума, страдающего заболеванием, характеризующимся экспрессией В-клеток, отличающийся тем, что указанный способ включает обеспечение указанного индивидуума эффективным количеством композиции, содержащей эффективное количество фармацевтической композиции, содержащей гетеромультимерную конструкцию согласно описанию в настоящем документе. Согласно некоторым вариантам реализации указанное заболевание не поддается лечению по меньшей мере чем-либо одним из антитела против CD19 и антитела против CD20. Согласно определенным вариантам реализации указанное заболевание представляет собой раковое заболевание или аутоиммунное состояние, резистентное к CD 19- или CD20-литическим антителам.
[00299] Предложен способ лечения аутоиммунного состояния у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему композиции, содержащей эффективное количество фармацевтической композиции согласно описанию в настоящем документе. Согласно определенным вариантам реализации указанное аутоиммунное состояние представляет собой что-либо одно или более из рассеянного склероза, ревматоидного артрита, эритематозной волчанки, псориатического артрита, псориаза, васкулита, увеита, болезни Крона и диабета первого типа.
[00300] Предложен способ лечения воспалительного состояния у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему композиции, содержащей эффективное количество фармацевтической композиции, содержащей гетеромультимер, описанный в настоящем документе.
[00301] На основе принципов, изложенных в настоящем описании, специалисту в данной области техники без проведения чрезмерных экспериментов будет понятно, как применять гетеромультимеры согласно описанию в настоящем документе для диагностики, мониторинга или с терапевтическими целями.
[00302] Гетеромультимеры согласно описанию в настоящем документе, содержащие по меньшей мере фрагмент или вариант антитела, могут вводиться по отдельности или в комбинации с другими видами лечения (например, лучевой терапией, химиотерапией, гормональной терапией, иммунотерапией и противоопухолевыми агентами). Как правило, введение продуктов, происходящих из того же вида или реактивных в отношении того же вида (в случае антител), что и вид, к которому принадлежит пациент, является предпочтительным. Соответственно, согласно одному варианту реализации антитела, фрагменты, производные, аналоги или нуклеиновые кислоты человека, вводят пациенту-человеку для терапии или профилактики.
[00303]
[00304] Генная терапия:
[00305] Согласно конкретному варианту реализации нуклеиновые кислоты, содержащие последовательности, кодирующие гетеромультимерные белки согласно описанию в настоящем документе, вводят для лечения, подавления или предотвращения заболевания или расстройства, связанного с аберрантной экспрессией и/или активностью белка, посредством генной терапии. Генная терапия относится к терапии, осуществляемой путем введения субъекту экспрессированной или подлежащей экспрессии нуклеиновой кислоты. Согласно данному варианту реализации изобретения нуклеиновые кислоты обеспечивают получение кодируемого ими белка, который опосредует терапевтический эффект.Может применяться любой из способов генной терапии, существующих в данной области техники.
[00306] Хотя взаимодействующие с Т-клетками биспецифические одно цепочечные антитела, описанные в данной области техники, обладают значительным терапевтическим потенциалом для лечения злокачественных заболеваний, применение большинства указанных биспецифических молекул ограничено их видоспецифичностью и распознаванием исключительно антигена человека, и - благодаря генетическому сходству предположительно, аналога у шимпанзе. Преимущество настоящего изобретения состоит в обеспечении биспецифического одноцепочечного антитела, содержащего связывающий домен, проявляющий межвидовую специфичность в отношении человека и не являющихся шимпанзе приматов, эпсилон-цепи CD3.
[00307] Демонстрация терапевтической или профилактической активности:
[00308] Гетеромультимеры или фармацевтические композиции согласно описанию в настоящем документе перед применением у человека тестируют in vitro, и затем in vivo на наличие требуемой терапевтической или профилактической активности. Например, in vitro анализы для подтверждения терапевтической или профилактической применимости соединения или фармацевтической композиции включают анализ эффектов соединения на линию клеток или образец ткани пациента. Эффект соединения или композиции на линию клеток и/или образец ткани может быть определен с применением техник, известных специалистам в данной области техники, включая, но не ограничиваясь перечисленными, анализ розеткообразования и анализ клеточного лизиса. В соответствии с настоящим изобретением анализы in vitro, которые подходят для определения того, показано ли введение конкретного соединения, включают анализы клеточных культур in vitro, когда образец ткани пациента культивируют и подвергают действию гетеромультимера, либо вводят гетеромультимер иным образом, и наблюдают эффект такого гетеромультимера на указанный образец ткани.
[00309]
[00310] Терапевтическое/профилактическое введение и состав композиций:
[00311] Предложены способы лечения, подавления и профилактики путем введения субъекту эффективного количества гетеромультимера или фармацевтической композиции согласно описанию в настоящем документе. Согласно одному варианту реализации указанный гетеромультимер является по существу очищенным (например, по существу не содержит веществ, ограничивающих его действие или приводящих к нежелательным побочным эффектам). Согласно определенным вариантам реализации указанный субъект представляет собой животное, в том числе, но не ограничиваясь перечисленными, такое животное, как корова, свинья, лошадь, курица, кошка, собака и т.д., и, согласно определенным вариантам реализации, млекопитающее, наиболее предпочтительно -человек.
[00312] Известны различные системы доставки, подходящие для введения гетеромультимерного состава согласно описанию в настоящем документе, например, инкапсулирование в липосомах, микрочастицах, микрокапсулах, рекомбинантные клетки, способные экспрессировать указанное соединение, опосредованный рецепторами эндоцитоз (см., например, Wu и Wu, J. Biol. Chem. 262:4429-4432 (1987)), конструирование нуклеиновой кислоты для введения в состав ретровирусного или другого вектора, и т.д. Способы введения включают, не ограничиваясь перечисленными, интрадермальный, внутримышечный, интраперитонеальный, внутривенный, подкожный, интраназальный, эпидуральный и пероральный. Указанные соединения или композиции могут вводиться с помощью любого удобного способа, например, путем инфузии или болюсного введения, путем абсорбции через эпителиальные покровы или кожно-слизистые оболочки (например, слизистую оболочку полости рта, прямой кишки и кишечника, и т.д.) и могут вводиться совместно с другими биологически активными агентами. Введение может быть системным или местным. Кроме того, согласно определенным вариантам реализации желательно введение гетеромультимерных композиций согласно описанию в настоящем документе в центральную нервную систему любым подходящим способом, включая интравентрикулярные и интратекальные инъекции; интравентрикулярное введение можно облегчить с помощью применения интравентрикулярного катетера, например, соединенного с резервуаром, таким как резервуар Оммайя. Также может применяться легочное введение, например, с применением ингалятора или небулайзера и состава с аэрозольным агентом.
[00313] Согласно конкретному варианту реализации желательно введение гетеромультимеров или композиций согласно описанию в настоящем документе местно, в область, подлежащую лечению; это может достигаться, например, без ограничения, путем локальной инфузии во время хирургической операции, местного нанесения, например, в сочетании с обработкой раны после хирургического вмешательства, путем инъекции, с помощью катетера, в виде суппозитория или имплантата, при этом указанный имплантат состоит из пористого, непористого или гелеобразного материала, включая мембраны, такие как мембраны из силастика, или волокна. Предпочтительно, при введении белка, в том числе антитела, согласно настоящему изобретению, необходимо применять материалы, которые не абсорбируют указанный белок.
[00314] Согласно другому варианту реализации указанные гетеромультимеры или композиция могут доставляться в везикуле, в частности, в липосоме (см. LaLanger, Science 249:1527-1533 (1990); Treat et al., в Liposomes in the Therapy of Infectious Disease and Cancer, Lopez-Berestein and Fidler (eds.), Liss, New York, pp. 353-365 (1989); Lopez-Berestein, там же, стр. 317-327; см. тот же источник в целом)
[00315] Согласно еще одному варианту реализации указанные гетеромультимеры или композиция могут доставляться в системе контролируемого высвобождения. Согласно одному из вариантов реализации может использоваться помпа (см. Langer, выше; Sefton, CRC Crit. Ref. Biomed. Eng. 14:201 (1987); Buchwald et al., Surgery 88:507 (1980); Saudek et al., N. Engl. J. Med. 321:574 (1989)). Согласно другому варианту реализации могут применяться полимерные материалы (см. Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Pres., Boca Raton, Fla. (1974); Controlled Drug Bioavailability, Drug Product Design and Performance, Smolen and Ball (eds.), Wiley, New York (1984); Ranger and Peppas, J., Macromol. Sci. Rev. Macromol. Chem. 23:61 (1983); см. также Levy et al., Science 228:190 (1985); During et al., Ann. Neurol. 25:351 (1989); Howard et al., J. Neurosurg. 71:105 (1989)). Согласно еще одному варианту реализации система контролируемого высвобождения может быть размещения в непосредственной близости к терапевтической мишени, например, в головном мозге, и, таким образом, требуется только часть системной дозы (см., например, Goodson, в руководстве «Medical Applications of Controlled Release» {«Применение контролируемого высвобождения в медицине»), выше, т. 2, стр. 115-138 (1984)).
[00316] Другие системы контролируемого высвобождения обсуждаются в обзоре Langer (Science 249:1527-1533 (1990)).
[00317] Согласно конкретному варианту реализации, включающему нуклеиновую кислоту, кодирующую гетеромультимер согласно описанию в настоящем документе, указанная нуклеиновая кислота может вводиться in vivo, способствуя экспрессии кодируемого ею белка, путем ее встраивания в подходящий нуклеиновокислотный экспрессионный вектор и введения таким образом, что она становится внутриклеточной, например, с помощью применения ретровирусного вектора (см. патент США №4980286), или с применением прямого инъецирования, или с применением бомбардировки микрочастицами (например, генной пушки; Biolistic, Dupont), или покрытия липидами или рецепторами клеточной поверхности, или агентами для трансфекции, или введения в связанном состоянии с гомеобокс-подобным пептидом, который, по имеющимся данным, проникает в ядро (см., например, Joliot et al., Proc. Natl. Acad. Sri. USA 88:1864-1868 (1991)) и т.д. Как вариант, нуклеиновая кислота может быть введена внутрь клетки и встроена в ДНК клетки-хозяина для экспрессии путем гомологичной рекомбинации.
[00318] Также в настоящем изобретении предложены фармацевтические композиции. Такие композиции содержат терапевтически эффективное количество соединения и фармацевтически приемлемый носитель. Согласно конкретному варианту реализации термин «фармацевтически приемлемый» означает одобренный регулирующим органом федерального правительства или правительства штата, или указанный в Фармакопее США или другой общепризнанной фармакопее как подходящий для применения у животных, и, в частности у человека. Термин «носитель» относится к разбавителю, адъюванту, вспомогательному веществу или основе, с которым вводят терапевтик. Такие фармацевтические носители могут представлять собой стерильные жидкости, например, воду и масла, включая нефтяные масла, масла животного, растительного или синтетического происхождения, например, арахисовое масло, соевое масло, минеральное масло, кунжутное масло и т.п.Вода представляет собой предпочтительный носитель, если фармацевтические композиции вводят внутривенно. Солевые растворы и водные растворы декстрозы и глицерина также могут применяться в качестве жидких носителей, в частности, для инъецируемых растворов. Подходящие фармацевтические вспомогательные вещества включают крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, сухое обезжиренное молоко, глицерин, пропилен, гликоль, воду, этанол и т.п.Композиция, при необходимости, может также содержать небольшие количества смачивающих или эмульгирующих агентов, или рН-буферных агентов. Указанные композиции могут быть представлены в форме растворов, суспензий, эмульсии, таблеток, пилюль, капсул, порошков, составов для пролонгированного высвобождения и т.п.Композиция может входить в состав суппозитория, содержащего традиционные связующие агенты и носители, такие как триглицериды. Состав для перорального применения может содержать стандартные носители, такие как фармацевтически чистые маннит, лактоза, крахмал, стеарат магния, сахарин натрия, целлюлоза, карбонат магния и т.д. Примеры подходящих фармацевтических носителей описаны Е.W. Martin в руководстве «Remington's Pharmaceutical Sciences». Такие композиции содержат терапевтически эффективное количество соединения, предпочтительно в очищенном виде, совместно с подходящим количеством носителя, обеспечивающего получение формы для надлежащего введения пациенту. Состав должен подходить для способа введения.
[00319] Согласно определенным вариантам реализации композицию, содержащую гетеромультимер, в соответствии с рутинными процедурами вводят в состав фармацевтической композиции, предназначенной для внутривенного введения человеку. Как правило, композиции для внутривенного введения представлены растворами в стерильном изотоническом водном буфере. При необходимости композиция может также включать солюбилизирующий агент и местный анестетик, такой как лигнокаин, для снижения болевых ощущений в месте инъекции. Как правило, ингредиенты предоставляются либо отдельно, либо они смешаны в единичной лекарственной форме, например, в виде сухого лиофилизированного порошка или безводного концентрата в герметично закрытом контейнере, таком как ампула или саше, с указанием на нем количества активного агента. Если композиция предназначена для введения путем инфузирования, она может разливаться в инфузионные флаконы, содержащие стерильную воду или солевой раствор фармацевтической чистоты. Если композицию вводят путем инъецирования, может поставляться ампула со стерильной водой для инъекций или солевым раствором, для смешивания ингредиентов перед введением.
[00320] Согласно определенным вариантам реализации композиции согласно описанию в настоящем документе представлены нейтральными или солевыми формами. Фармацевтически приемлемые соли включают образованные анионами, например, полученными из соляной, фосфорной, уксусной, щавелевой, винной кислоты и т.д., и образованные катионами, такими как полученные из натрия, калия, аммония, кальция, гидроксида железа, изопропиламина, триэтиламина, 2-этиламиноэтанола, гистидина, прокаина и т.д.
[00321] Количество композиции согласно описанию в настоящем документе, эффективное для лечения, подавления предотвращения заболевания или расстройства, связанного с аберрантной экспрессией, и/или активности терапевтического белка может быть определено с применением стандартных клинических методов. Кроме того, могут необязательно применяться анализы in vitro для облегчения определения оптимальных диапазонов доз. Точная доза для применения в составе также зависит от способа введения и тяжести указанного заболевания или расстройства, и должна определяться в соответствии с мнением лечащего врача и обстоятельств, связанных с конкретным пациентом. Эффективные дозировки определяют методом экстраполяции на основе кривых «доза-ответ», полученных с помощью тест-систем in vitro или моделей на животных.
[00322] Согласно определенным вариантам реализации гетеромультимерную конструкцию согласно описанию в настоящем документе подходящим образом вводят пациенту одномоментно или на протяжении нескольких этапов лечения. В зависимости от типа и тяжести заболевания возможная начальная дозировка активирующей Т-клетки биспецифической антигенсвязывающей молекулы для введения пациенту может составлять приблизительно от 1 мкг/кг до 15 мг/кг (например, 0,1 мг/кг - 10 мг/кг), либо, например, в виде одного или нескольких отдельных введений, или в виде непрерывной инфузии. Как вариант, примерная ежедневная дозировка может варьировать в диапазоне от приблизительно 1 мкг/кг до 100 мг/кг или более, в зависимости от упомянутых выше факторов. В случае многократного введения на протяжении нескольких дней или более, в зависимости от состояния, лечение, как правило, продолжают до достижения требуемого подавления симптомов. Как вариант, примерная дозировка гетеромультимера согласно описанию в настоящем документе варьирует в диапазоне от приблизительно 0,005 мг/кг до приблизительно 10 мг/кг.Согласно другим неограничивающим примерам доза может также составлять от приблизительно 1 мкг/кг массы тела, от приблизительно 5 мкг/кг массы тела, от приблизительно 10 мкг/кг массы тела, от приблизительно 50 мкг/кг массы тела, от приблизительно 100 мкг/кг массы тела, от приблизительно 200 мкг/кг массы тела, от приблизительно 350 мкг/кг массы тела, от приблизительно 500 мкг/кг массы тела, от приблизительно 1 мг/кг массы тела, от приблизительно 5 мг/кг массы тела, от приблизительно 10 мг/кг массы тела, от приблизительно 50 мг/кг массы тела, от приблизительно 100 мг/кг массы тела, от приблизительно 200 мг/кг массы тела, от приблизительно 350 мг/кг массы тела, от приблизительно 500 мг/кг массы тела, до приблизительно 1000 мг/кг массы тела или более на одно введение, и варьировать в любом диапазоне, входящем в указанные. Согласно неограничивающим примерам диапазонов, определяемых приведенными в настоящем документе значениями, могут вводиться дозы в диапазоне от приблизительно 5 мг/кг массы тела до приблизительно 100 мг/кг массы тела, приблизительно 5 мкг/кг массы тела до приблизительно 500 мг/кг массы тела и т.д., на основе приведенных выше значений. Таким образом, пациенту могут быть введены одна или несколько доз, составляющих приблизительно 0,5 мг/кг, 2,0 мг/кг, 5,0 мг/кг или 10 мг/кг (или любая комбинация перечисленного). Такие дозы могут вводиться с перерывами, например, еженедельно или один раз в три недели (например, таким образом, что пациент получает от приблизительно двух до приблизительно двадцати, или например, приблизительно шесть доз активирующей Т-клетки биспецифической антигенсвязывающей молекулы). Может вводиться более высокая стартовая нагрузочная доза, а затем одна или несколько более низких доз. Однако могут подходить и другие режимы дозирования. Мониторинг хода лечения может быть легко осуществлен с применением общепринятых техник и анализов.
[00323] Гетеромультимеры согласно описанию в настоящем документе, как правило, используют в количестве, эффективном для достижения заданной цели. Для применения в лечении или для предотвращения болезненного состояния гетеромультимер, описанный в настоящем документе, или включающие его фармацевтические композиции, вводят или наносят в терапевтически эффективном количестве. Определение терапевтически эффективного количества вполне соответствует возможностям специалистов в данной области техники, с учетом, в частности, приведенного в настоящем документе подробного описания.
[00324] Терапевтически эффективная доза для системного введения может быть определена сначала на основании анализов in vitro, таких как анализ клеточных культур. Затем доза может быть уточнена в моделях на животных, с получением диапазона циркулирующих концентраций, включающего IC50, определенную для культуры клеток. Такая информация может быть использована для более точного определения подходящих для человека доз.
[00325] Начальные дозировки могут также быть определены на основании данных, полученных in vivo, например, в моделях на животных, с применением техник, хорошо известных в данной области техники. Средний специалист в данной области техники легко сможет оптимизировать введение человеку на основании данных, полученных для животных.
[00326] Величина дозы и интервалы между введениями могут быть подобраны индивидуально для обеспечения в плазме уровней гетеромультимера согласно описанию в настоящем документе, достаточных для поддержания терапевтического эффекта. Обычные дозировки для введения пациенту путем инъецирования варьируют в диапазоне от приблизительно 0,1 до 50 мг/кг/день, как правило, от приблизительно 0,5 до 1 мг/кг/день. Терапевтически эффективные уровни в плазме могут быть достигнуты путем введения нескольких доз ежедневно. Уровни в плазме могут быть измерены, например, с помощью ВЭЖХ.
[00327] При местном введении или избирательном накоплении эффективная местная концентрация гетеромультимера согласно описанию в настоящем документе может быть не связана с концентрацией в плазме. Специалист в данной области техники сможет оптимизировать терапевтически эффективные дозы для местного применения без чрезмерного экспериментирования.
[00328] Терапевтически эффективная доза гетеромультимерных конструкций согласно описанию в настоящем документе, как правило, обеспечивает благоприятный терапевтический эффект без существенной токсичности. Токсичность и терапевтическая эффективность описанного в настоящем документе гетеромультимера могут быть определены с помощью стандартных фармацевтических процедур в культурах клеток или на экспериментальных животных. Для определения LD50 (дозы, летальной для 50% популяции) и ED50 (дозы, терапевтически эффективной для 50% популяции) может применятся анализ клеточных культур и исследования на животных. Соотношение доз, обеспечивающих токсический и терапевтический эффекты, представляет собой терапевтический индекс, который может быть выражен через отношение LD50/ED50. Активирующие Т-клетки биспецифические антигенсвязывающие молекулы, демонстрирующие высокий терапевтический индекс, являются предпочтительными. Согласно одному из вариантов реализации описанная в настоящем документе гетеромультимерная конструкция в соответствии с настоящим изобретением демонстрирует высокий терапевтический индекс.Данные, полученные при анализе клеточных культур и в исследованиях на животных, могут быть использованы для определения диапазона доз, подходящих для применения у человека. Дозировка предпочтительно варьирует в диапазоне циркулирующих концентраций, включающем ED50 с незначительной или отсутствующей токсичностью. Дозировка может варьировать в указанном диапазоне за счет различных факторов, например, используемой лекарственной формы, используемого способа введения, состояния субъекта и т.п.Точный состав, способ введения и дозировка могут выбираться конкретным лечащим врачом с учетом состояния пациента (см., например, Fingl et al, 1975, в источнике: The Pharmacological Basis sof Therapeutics, Ch. 1, p. 1, полностью включенном в настоящий документ посредством ссылки).
[00329] Лечащему врачу пациентов, получающих лечение гетеромультимерными конструкциями согласно описанию в настоящем документе, должно быть понятно, как и когда нужно закончить, прервать или скорректировать введение ввиду токсичности, дисфункции органа и т.п.И, с другой стороны, лечащему врачу также должно быть понятно, как скорректировать лечение с применением более высоких доз, если клинический ответ недостаточен (избегая токсичности). Величина вводимой дозы для управления течением представляющего интерес расстройства варьирует в зависимости от тяжести подлежащего лечению состояния, способа введения и т.п. Оценка тяжести состояния может, например, быть проведена частично с помощью стандартных прогностических методов оценки. Далее, доза и, вероятно, частота введения также будут варьировать в зависимости от возраста, массы тела и реакций индивидуального пациента.
[00330] Также предложен способ получения фармацевтической композиции, содержащей гетеромультимер согласно описанию в настоящем документе, включающий: культивирование клетки-хозяина в условиях, допускающих экспрессию гетеромультимера; выделение полученного гетеромультимера из культуры; и получение указанной фармацевтической композиции.
[00331]
[00332] Другие агенты и варианты лечения:
[00333] Согласно определенным вариантам реализации гетеромультимерные конструкции согласно описанию в настоящем документе при терапии вводят в комбинации с одним или несколькими другими агентами. Например, согласно одному из вариантов реализации гетеромультимер, описанный в настоящем документе, вводят совместно по меньшей мере с одним дополнительным терапевтическим агентом. Термин «терапевтический агент» охватывает любой агент, который вводят для лечения симптому или заболевания индивидууму, нуждающемуся в таком лечении. Такой дополнительный терапевтический агент может включать любые активные ингредиенты, подходящие при конкретных показаниях для лечения, предпочтительно обладающие взаимодополняющей активностью, не оказывающие друг на друга негативных эффектов. Согласно определенным вариантам реализации дополнительный терапевтический агент представляет собой иммуномодулирующий агент, цитостатический агент, ингибитор клеточной адгезии, цитотоксический агент, активатор клеточного апоптоза или агент, повышающий чувствительность клеток к индукторам апоптоза. Согласно конкретному варианту реализации указанный дополнительный терапевтический агент представляет собой противораковый агент, например, агент, разрушающий микротрубочки, антиметаболит, ингибитор топоизомеразы, ДНК-интеркалятор, алкилирующий агент, агент для гормональной терапии, ингибитор киназ, антагонист рецептора, активатор апоптоза опухолевых клеток или антиангиогенный агент.
[00334] Указанные другие агенты при необходимости присутствуют в комбинации, в количествах, эффективных для достижения заданной цели. Эффективное количество таких других агентов зависит от использованного количества активирующей Т-клетки биспецифической антигенсвязывающей молекулы, характера расстройства или лечения, и других факторов, обсуждаемых выше. Гетеромультимеры согласно описанию в настоящем документе вводят, как правило, в дозировках и с помощью способов введения, которые были описаны в настоящем документе, или в дозировках приблизительно от 1 до 99% от дозировок согласно описанию в настоящем документе, или в любых дозах и с помощью любого способа введения, которые были определены как подходящие эмпирически либо клинически.
[00335] Такая упомянутая выше комбинированная терапия включает комбинированное введение (когда два или более терапевтических агента включены в одну композицию или в отдельные композиции), и раздельное введение, когда введение гетеромультимера согласно описанию в настоящем документе может осуществляться до, во время и/или после введения дополнительного терапевтического агента и/или адъюванта. Гетеромультимерные конструкции согласно описанию в настоящем документе могут также применяться в комбинации с лучевой терапией.
[00336]
[00337] Продукты производства:
[00338] Согласно другому аспекту настоящего изобретения предложен продукт производства, содержащий материалы, подходящие для лечения, предотвращения и/или диагностики описанных выше расстройств. Указанный продукт производства содержит контейнер и этикетку или вкладыш, который(ая) размещен (а) на контейнере или связан с контейнером. Подходящие контейнеры включают, например, бутыли, флаконы, шприцы, пакеты для в/в растворов и т.д. Контейнеры могут быть выполнены из различных материалов, например, стекла или пластика. Контейнер содержит композицию, которая сама по себе или в комбинации с другой композицией эффективна для лечения, предотвращения и/или диагностики состояния, и может быть оснащен стерильным портом для доступа (например, указанный контейнер может представлять собой пакет для внутривенного раствора или флакон, имеющий пробку, прокалываемую иглой для подкожных инъекций). По меньшей мере один активный агент в композиции представляет собой активирующую Т-клетки биспецифическую антигенсвязывающую молекулу согласно настоящему изобретению. На этикетке или вкладыше указано, что композиция используется для лечения выбранного состояния. Кроме того, продукт производства может содержать (а) первый контейнер с содержащейся в нем композицией, отличающийся тем, что указанная композиция содержит гетеромультимер, описанный в настоящем документе; и (b) второй контейнер с содержащейся в нем композицией, отличающийся тем, что указанная композиция содержит дополнительный цитотоксический или другой терапевтический агент.Продукт производства согласно указанному варианту настоящего изобретения может также содержать вкладыш, указывающий на возможность применения композиций для лечения конкретного состояния. Как вариант, или дополнительно, продукт производства может также содержать второй (или третий) контейнер, содержащий фармацевтически приемлемый буфер, такой как бактериостатическая вода для инъекций (BWFI), забуференный фосфатом солевой раствор, раствор Рингера и раствор декстрозы. Он может также включать другие материалы, целесообразные с коммерческой и потребительской точки зрения, включая другие буферы, разбавители, фильтры, иглы и шприцы.
[00339]
[00340] ПРИМЕРЫ
[00341] Следующие конкретные неограничивающие примеры должны толковаться исключительно как иллюстративные, и не ограничивающие настоящее описание каким-либо образом. Без дальнейших уточнений, предполагается, что специалист в данной области техники сможет, основываясь на описании в настоящем документе, использовать настоящее раскрытие в максимальной степени. Все публикации, цитируемые в настоящем документе, включены в настоящий документ полностью посредством ссылок. Следует понимать, что, в случае ссылок на веб-страницу (URL-адрес) или другой такой идентификатор или адрес, такие идентификаторы могут изменяться и конкретная информация в сети Интернет может появляться и исчезать, однако с помощью поиска в сети Интернет может быть найдена эквивалентная информация. Ссылки на них свидетельствуют о доступности и публичном распространении такой информация.
[00342]
[00343] Пример 1: Биспецифические CD3-CD19 scFv, соединенные с асимметричным IgG1 Fe.
[00344] Биспецифические CD3-CD19 scFv, соединенные с асимметричным IgG1 Fc-гетеродимером, который проявляет стабильность, сопоставимую с нативным гомодимером Fc, представляет собой новую композицию, идентифицированную как v873. V873 принадлежит новому семейству биспецифических «азиметрических» (Azymetric) IgG1-антител на основе CD3, которые могут быть экспрессированы и очищены со значительно более высоким выходом в клетках СНО млекопитающих по сравнению с биспецифическими антителами Amgen/Micromet bscCD19×CD3 BiTE. V873, неожиданным образом, демонстрирует связывание эффекторов с целевыми клетками, связывание и киллинг целевых клеток.
[00345] V873 и биспецифические «азиметрические» антитела на основе CD3 подходят для направленного опосредованного Т-клетками киллинга пораженных заболеванием клеток и, следовательно, могут подходить для лечения раковых заболеваний и аутоиммунных и воспалительных заболеваний. V873 представляет собой биспецифические CD3-CD19 scFv, соединенные с Fc IgG1 типа «азиметрик». v873 представляет новый класс биспецифических «азиметрических» антител, содержащих один анти-CD3 участок направленного действия и второй участок направленного действия, содержащий антиген клеточной поверхности целевой клетки, и антитело с Fc-гетеродимером, содержащее гетеродимер Fc IgG1. Слияние участка направленного действия на CD3 с цепью А или В указанного Fc имеет важное значение для лекарственных свойств. В качестве дополнительных примеров, V874 и V875 представляют собой два других биспецифических CD3-CD19 scFv, соединенных с асимметричным Fc IgG1, но содержат CD3-участки с другим аминокислотным составом.
[00346] V873, неожиданным образом, демонстрирует высокие уровни экспрессии и очистки в клетках млекопитающих СНО по сравнению с CD3-CD19 BiTE тандемными scFv блинатумомаба от Amgen/Micromet. V873 соединяет Т- и В-клетки и приводит к высокоэффективному киллингу культивируемых клеток лимфомы человека Burkitt (В-клеточная линия лимфомы Raji) с применением покоящихся и ИЛ-2 активированных клеток МКПК человека.
[00347] V873 и родственные ему биспецифические CD3-антитела «азиметрик» отличаются от CD3-CD19 BiTE Amgen/Micromet и содержат гетеродимерную Fc IgG1, который способен связывать FcgR, опосредуя АЗКЦ-, КЗЦ-, АЗКФ-активность эффекторов. V873 способен связывать FcRn; указанный класс гетеродимерной Fc проявляет типичные для антител технологичность (пригодность для производства) и длительный период полужизни, превышающий 8 дней у яванского макака. При этом период полужизни блинатумомаба составляет меньше нескольких часов у не являющихся человеком обезьян и у пациентов-людей.
[00348] Применение V873 и родственных ему биспецифических конструкций на основе CD3 направлено на решение известных проблем со стабильностью тандемных scFv и общеизвестными неблагоприятными для производства свойствами блинатумомаба. Применение V873 направлено на решение проблем, связанных с быстрой фармакокинетикой блинатумомаба и неблагоприятным действием на ЦНС за счет сродства к связыванию его FcRn дикого типа, и молекулярной массой, ограничивающей его распространение в периферическое пространство. Наконец, «азиметрический» гетеродимер Fc обеспечивает дополнительную специализированную опосредованную FcgR эффекторную АЗКЦ-, КЗЦ-, и АЗКФ-активность и, следовательно, эффективность в отношении устойчивых к лекарственной терапии опухолей.
[00349] Способность v873 опосредовать киллинг клетками МКПК (Т-клетками) В-клеток крайне неожиданна. Свойства блинатумомаба bscCD19×CD3 и родственных BiTE в соответствии с имеющимися данными основаны на применении гибко соединенных одноцепочечных вариабельных фрагментов (scFv), которые располагаются тандемом и соединены коротким линкером, что позволяет обеспечить сближение противостоящих клеток значительно большее, чем возможное для более крупных биспецифических форм, таким как квадромные антитела. Гибкая связь, предположительно, должна позволять свободное вращение и сгибание двух плеч scFv, облегчая таким образом одновременное распознавание 2 эпитопов, присутствующих на мембранах 2-х противостоящих клеток, и образование цитолитического иммунного синапса. Следовательно, исходя из имеющихся данных, описывающих свойства BiTE, которые в целом считаются уникальными, то, что биспецифическая CD3-CD19 конструкция согласно описанию в настоящем документе со значительно отличающимся структурным представлением участков scFv с направленным действием против CD3 и CD 19 на гетеродимере Fc способна связывать, соединять Т- и В-клетки и опосредовать киллинг В-клеток клетками МКПК (Т-клетками), является неожиданным. Другие применения включают истощение В-клеток при контролируемых В-клетками аутоиммунных и воспалительных заболеваниях, таких как РА, волчанка, PC, ВЗК. Кроме того, родственные V873 «азиметрические» антитела на основе биспецифических CD3-антител могут подходить для целей диагностики.
[00350] Дополнительная подробная информация относительно вышесказанного изложена в следующих примерах.
[00351]
[00352] Пример 2. Дизайн, экспрессия и очистка гетеромультимерных конструкций с гетеродимерной Fe.
[00353] Примеры биспецифических гетеродимерных антител против CD3 и против CD19
[00354]
[00355] Пример схематического изображения антитела против CD3/CD19 представлен на фиг. 1А.
[00356] v873, v874, v875 являются примерами биспецифических гетеродимерных анти-CD3/анти-CD19 Fc конструкций; их получали и тестировали согласно приведенному ниже описанию. В тех случаях, когда описание включает ссылку на BiTE, оно относится к конструкции антитела, имеющего аминокислотную последовательность, идентичную либо VH, либо VL молекулы анти-CD3/анти-CD19 BiTE, включающей или не включающей модификации ориентации вариабельной тяжелой и вариабельной легкой цепей (например, VH-VL), как отмечено ниже.
[00357] v873 содержит анти-CD 19 BiTE (VL-VH) scFv на цепи А и CD3 BiTE™ (VH-VL) scFv на цепи В гетеродимера Fc, со следующими мутациями: L351Y_F405A_Y407V на цепи А и T366L K392M T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 26 и 28]
[00358] V874 содержит анти-CD 19 BiTE™ (VL-VH) scFv на цепи А и CD3 BiTE™ (VLVH) scFv на цепи В гетеродимера Fc, со следующими мутациями: L351Y_F405A_Y407V на цепи А и T366L_K392M_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 30 и 32]
[00359] V875 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и CD3 ОКТ3 (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями:
L351Y_F405A_Y407V на цепи А и T366L_K392M_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 34 и 36]
[00360] vl379 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 (VH-VL) BiTE на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 87 и 88]
[00361] Бивалентные моноспецифические антитела против CD3 и против CD19 [00362] v865, v866, v867, v868 являются примерами моноспецифических бивалентных анти-CD3 или анти-CD19 scFv-Fc конструкций; их получали и тестировали согласно приведенному ниже описанию:
[00363] v865 содержит анти-CD19 BiTE (VL-VH) scFv на цепи А и анти-CD19 BiTE scFv на цепи В с Fc дикого типа (105кДа). [Полипептидная последовательность соответствует последовательности SEQ ID No: 2]
[00364] v866 содержит анти-CD3 BiTE™ (VH-VL) на цепи А и анти-CD3 BiTE™ (VH-VL) scFv на цепи с Fc дикого типа (105кДа). [Полипептидная последовательность соответствует последовательности SEQ ID No: 4]
[00365] v867 содержит анти-CD3 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 BiTE™ (VL-VH) scFv на цепи В с Fc дикого типа (105кДа). [Полипептидная последовательность соответствует последовательности SEQ ID No: 6]
[00366] v868 содержит анти-CD3 ОКТ3 (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 VL-VH scFv на цепи с Fc дикого типа (105 кДа). [Полипептидная последовательность соответствует последовательности SEQ ID No: 8].
[00367] Моновалентные моноспецифические антитела против CD3
[00368] v869 содержит анти-CD19 BiTE™ scFv (VL-VH) на цепи А и Fc на цепи В гетеродимера Fc, со следующими мутациями: L351Y_F405A_Y407V на цепи А и T366L_K392M_T394W на цепи В(80 кДа). [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 10 и 12].
[00369] v870 содержит анти-CD3 BiTE™ (VH-VL) scFv на цепи В и Fc на цепи А гетеродимера Fc, со следующими мутациями: L351Y_F405A_Y407V на цепи А и T366L K392M T394W на цепи В (80 кДа). [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 14 и 16].
[00370] v871 содержит анти-CD3 BiTE (VL-VH) scFv на цепи В и Fc на цепи А гетеродимера Fc, со следующими мутациями: L351Y_F405A_Y407V на цепи А и T366L_K392M_T394W на цепи В (80 кДа). [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 18 и 20].
[00371] v872 содержит анти-CD3 ОКТ3 (VL-VH) scFv на цепи В и Fc на цепи А гетеродимера Fc, со следующими мутациями: L351Y_F405A_Y407V на цепи А и T366L_K392M_T394W на цепи В (80 кДа). [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 22 и 24].
[00372] Контрольные показатели
[00373] v891 содержит последовательность, идентичную анти-CD3 BiTE scFv и анти-CD19 BiTE scFv блинатумомаба BiTE™ (50 кДа) [Полипептидная последовательность соответствует последовательности SEQ ID No: 90
[00374] Примеры моно- или биспецифических гетеродимерных антител против CD3 и против CD 19 с нокаутным Fc
[00375] V1380 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 VHVL BiTE™ на цепи В гетеродимера Fc, со следующими мутациями: L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и L234A_L235A_T350V_T366L_K392L_T394W на цепи В (соответствуют полипептидным последовательностям SEQ ID NO: 93 и 94).
[00376] vl381 содержит анти-CD19 BiTE™ (Vl-VH) scFv на цепи А и анти-CD3 BiTE™ scFv (VH-VL) на цепи В гетеродимера Fc, со следующими мутациями: N297A_T350V_L351Y_F405A_Y407V на цепи А и N297A_T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 93 и 98) [00377] Варианты со сконструированными участками с направленным действием против CD3 для повышения стабильности
[00378] Следующие варианты содержат мутации анти-CD3 scFv, которые включают либо изменение длины линкера, ориентации VH-VL, либо точечные мутации для повышения стабильности и выхода.
[00379] v1653 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 (VL-VH) (с мутацией C→S в положении 100А VH CDR3) на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 101 и 102)
[00380] v1654 содержит анти-CD19 BiTE™ scFv на цепи А и анти-CD3 ОКТ3 ОКТ3 (VH-VL) с линкером размером 18 аминокислот на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 105 и 106)
[00381] v1655 содержит анти-CD19 BiTE™ scFv на цепи А и анти-CD3 ОКТ3 ОКТ3 (VH-VL) с линкером размером 10 аминокислот на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 109 и 110)
[00382] vl656 содержит анти-CD3 BiTE™ VHVL scFv на цепи А и анти-CD19 BiTE™ (VL-VH) на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 113 и 114)
[00383] v1657 содержит анти-CD3 ОКТ3 (VL-VH) scFv (с мутацией C→S в положении 100А VH CDR3) на цепи А и анти-CD19 BiTE™ (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 117 и 118)
[00384] vi658 содержит анти-CD3 ОКТ3 (VH-VL) scFv с линкером размером 18 аминокислот на цепи А и анти-CD19 BiTE™ (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 121 и 122)
[00385] vi659 содержит анти-CD3 ОКТ3 (VH-VL) scFv с линкером размером 10 аминокислот на цепи А и анти-CD19 BiTE™ (VL VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В, (соответствуют полипептидным последовательностям SEQ ID NO: 125 и 126)
[00386] vi660 содержит анти-CD3 ОКТ3 (VH-VL) scFv с линкером длиной 19 аминокислот на цепи А и анти-CD19 BiTE™ (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 129 и 130)
[00387] Fc-нокаутные варианты, содержащие сконструированные участки с направленным действием против CD3 для повышения стабильности
[00388] Следующие варианты представляют собой Fc-нокаутные варианты, содержащие мутации анти-CD3 scFv, которые включают либо изменение длины линкера, ориентаций VH-VL, либо точечные мутации для повышения стабильности и выхода.
[00389] vi661 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 38 и 40]
[00390] v1662 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 (VL-VH) scFv (с мутацией C→S в положении 100А VH CDR3) на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 42 и 44]
[00391] v1663 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 (VL-VH) scFv с линкером размером 18 аминокислот на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 133 и 134)
[00392] vi664 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 (VH-VL) scFv с линкером размером 10 аминокислот на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 137 и 138)
[00393] v1665 содержит анти-CD3 BiTE™ (VH-VL) scFv на цепи А и анти-CD19 BiTE™ (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 141 и 142)
[00394] v1666 содержит анти-CD3 ОКТ3 (VH-VL) scFv с линкером размером 19 аминокислот на цепи А и анти-CD 19 BiTE™ (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 46 и 48].
[00395] vi667 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: N297A_T350V_L351Y_F405A_Y407V на цепи А и N297A_T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 145 и 146)
[00396] vi668 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 (VL-VH) scFv (с мутацией C→S в положении 100А VH CDR3) на цепи В гетеродимера Fc, со следующими мутациями: N297A_T350V_L351Y_F405A_Y407V на цепи А и N297A_T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 149 и 150)
[00397] v1669 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 (VH-VL) scFv с линкером размером 18 аминокислот на цепи В гетеродимера Fc, со следующими мутациями: N297A_T350V_L351Y_F405A_Y407V на цепи А и N297A_T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 153 и 154)
[00398] v1670 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 (VH-VL) scFv с линкером размером 10 аминокислот на цепи В гетеродимера Fc, со следующими мутациями: N297A_T350V_L351Y_F405A_Y407V на цепи А и N297A_T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 157 и 158)
[00399] vl671 содержит анти-CD3 BiTE™ (VH-VL) scFv на цепи А и анти-CD19 BiTE™ (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: N297A_T350V_L351Y_F405A_Y407V на цепи А и N297A_T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 161 и 162)
[00400] vi672 содержит анти-CD3 ОКТ3 (VH-VL) scFv с линкером размером 19 аминокислот на цепи А и анти-CD 19 BiTE™ (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: N297A_T350V_L351Y_F405A_Y407V на цепи А и N297A_T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 165 и 166)
[00401] Moho валентные анти-CD3 антитела
[00402] Следующие варианты содержат мутации анти-CD3 scFv, которые включают либо изменение длины линкера, ориентации VH-VL, либо точечные мутации для повышения стабильности и производительности.
[00403] vi673 содержит анти-CD3 ОКТ3 (VL-VH) scFv (с мутацией C→S в положении 100А VH CDR3) на цепи В и Fc на цепи А гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 169 и 170)
[00404] vi674 содержит анти-CD3 ОКТ3 (VH-VL) scFv с линкером размером 18 аминокислот на цепи В и Fc на цепи А гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 173 и 174)
[00405] vi798 содержит анти-CD3 ОКТ3 (VH-VL) scFv с линкером размером 10 аминокислот на цепи В и Fc на цепи А гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 177 и 178)
[00406] v1799 содержит анти-CD3 ОКТ3 (VH-VL) scFv с линкером длиной 19 аминокислот на цепи А и Fc на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 181 и 182)
[00407] Биспецифические варианты со стабилизацией дисульфидной связи в положениях 44-100
[00408] Следующие варианты содержат точечные мутации для стабилизации дисульфидной связи в положении 100 вариабельной области легкой и в положении 44 вариабельной области тяжелой цепи (обозначается как 44-100SS).
[00409] v1800 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 (VL-VH) 44-100SS на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 185 и 186)
[00410] v1801 содержит анти-CD19 BiTE™ (VL-VH) scFv на цепи А и анти-CD3 ОКТ3 (VL-VH) (с мутацией C->S в положении 100А VH CDR3) 44-100SS на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 189 и 190)
[00411] v1802 содержит анти-CD3 BiTE™ (VH-VL) 44-100SS scFv на цепи А и против CD19 BiTE™ (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В. (соответствуют полипептидным последовательностям SEQ ID NO: 193 и 194)
[00412] v4541 содержит анти-CD3 BiTE™ (VH-VL) 44-100SS scFv на цепи А и анти-CD19 BiTE™ (VL-VH) scFv на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 50 и 52]
[00413]
[00414] Перекрестно-реактивные анти-CD3/анти-CD19 биспецифические Fc-нокаутные варианты яванского макака/человека со стабилизацией или без стабилизации дисульфидных связей 44-100
[00415] v4542 содержит перекрестно-реактивный анти-CD3 BiTE™ 12С (VH-VL) scFv яванского макака/человека на цепи А и перекрестно-реактивный анти-CD19 MOR208 (VH-VL) scFv яванского макака/человека на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 54 и 56].
[00416] v4543 содержит перекрестно-реактивный анти-CD3 BiTETM 12С (VH-VL) 44-100SS scFv яванского макака/человека на цепи А и перекрестно-реактивный анти-СТ)19 MOR208 (VH-VL) 44-100SS scFv яванского макака/человека на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 58 и 60]
[00417] v4544 содержит перекрестно-реактивный анти-CD3 BiTE™ 12С (VH-VL) scFv яванского макака/человека на цепи А и перекрестно-реактивный анти-CD19 MOR208 (VL-VH) scFv яванского макака/человека на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 62 и 64]
[00418] v4545 содержит перекрестно-реактивный анти-CD3 BiTETM 12С (VH-VL) 44-lOOSS scFv яванского макака/человека на цепи А и перекрестно-реактивный анти-СТ)19 MOR208 (VL-VH) 44-100SS scFv яванского макака/человека на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 66 и 68]
[00419] v4546 содержит перекрестно-реактивный анти-CD3 BiTE™ 12С (VH-VL) scFv яванского макака/человека на цепи А и перекрестно-реактивный анти-CD19 MDX-1342 (VH-VL) scFv яванского макака/человека на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351 Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 70 и 72]
[00420] v4547 содержит перекрестно-реактивный анти-CD3 BiTETM 12С (VH-VL) 44-100SS scFv яванского макака/человека на цепи А и перекрестно-реактивный анти-CD19 MDX-1342 (VH-VL) 44-100SS scFv яванского макака/человека на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 74 и 76].
[00421] v4548 содержит перекрестно-реактивный анти-CD3 BiTE™ 12С (VH-VL) scFv яванского макака/человека на цепи А и перекрестно-реактивный анти-CD19 MDX-1342 (VL-VH) scFv яванского макака/человека на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 78 и 80]
[00422] v4549 содержит перекрестно-реактивный анти-CD3 BiTETM 12С (VH-VL) 44-100SS scFv яванского макака/человека на цепи А и перекрестно-реактивный анти-CD19 MDX-1342 (VL-VH) 44-100SS scFv яванского макака/человека на цепи В гетеродимера Fc, со следующими мутациями: D265S_L234A_L235A_T350V_L351Y_F405A_Y407V на цепи А и D265S_L234A_L235A_T350V_T366L_K392L_T394W на цепи В. [Полипептидные последовательности соответствуют последовательностям SEQ ID No: 82 и 84]
[00423] Указанные антитела и контрольные антитела клонировали и экспрессировали следующим образом. Гены, кодирующие тяжелые и легкие цепи антител, конструировали посредством генного синтеза с применением кодонов, оптимизированных для экспрессии у человека/млекопитающих. Последовательности Fab получали из известного связывающего Her2/neu антитела (Carter P. et al. (1992) Humanization of an anti Ρ185 Her2 antibody for human cancer therapy. Proc Natl Acad Sci 89, 4285.); Fc относится к изотипу IgG1. Последовательности scFv-Fc и OAA получали из известных анти-CD3 и amra-CD19 scFv BiTE (Kipriyanov et. al., 1998, Int. J Cancer: 77,763-772), анти-CD3 BiTE (US 2011/0275787) моноклонального антитела против CD3 ОКТ3 (Drug Bank №: DB00075), антитела против CD 19 MDX-1342 (WO 2009054863; WO 2007002223).
[00424] Полученные генные продукты субклонировали в экспрессионный вектор для млекопитающих рТТ5 (NRC-BRI, Канада) и экспрессировали в клетках СНО (Durocher, Y., Perret, S. & Kamen, A. High-level and high-throughput recombinant protein production by transient transfection of suspension-growing СНО cells. Nucleic acids research 30, E9 (2002)).
[00425] Клетки СНО трансфицировали в экспоненциальной фазе роста (1,5-2 млн кл/мл) водным полиэтиленимином 25кДа в концентрации 1 мг/мл (PEI, Polysciences) с соотношением PEI:ДНК 2,5:1.(Raymond С.et al. A simplified polyethylenimine-mediated transfection process for large-scale and high-throughput applications. Methods. 55(1):44-51 (2011)). Для определения оптимального диапазона концентраций для образования гетеродимеров проводили трансфекцию ДНК в оптимальных пропорциях ДНК тяжелой цепи А (НС-A), легкой цепи (LC) и тяжелой цепи В, обеспечивающих образование гетеродимеров (например, в пропорции НС-А/НС-В/=50,50% (OAA; HC/Fc), 50:50%. Трансфицированные клетки собирали через 5-6 дней с культуральной средой, которую собирали после центрифугирования при 4000 об/мин и очищали с применением фильтра 0,45 мкм.
[00426] Очищенную культуральную среду загружали на колонку MabSelect SuRe (GE Healthcare) с белком А и промывали 10-кратным относительно объема колонки количеством буфера ФСБ при рН 7,2. Антитело элюировали 10-кратным относительно объема колонки количеством цитратного буфера при рН 3,6 с объединенными фракциями, содержащими антитело, нейтрализованное TRIS при рН 11. В конце белок обессоливали с применением колонки Econo-Pac 10DG (Bio-Rad).
[00427] В некоторых случаях белок дополнительно очищали хроматографией с белком L следующим образом. Смолу Capto L уравновешивали ФСБ, очищенным белком А v875, нейтрализовали 1М Tris, добавляли в смолу и инкубировали при КТ на протяжении 30 минут.Смолу промывали ФСБ, собирали вытекающий продукт, связанный белок элюировали 0,5 мл 0,1 M глицина, рН 3.
[00428] В некоторых случаях белок дополнительно очищали путем гель-фильтрации, 3,5 мг смеси антител концентрировали 1,5 мл и загружали на колонку Superdex 200 HiLoad 16/600 200 pg (GE Healthcare) в системе АКТА Express FPLC при скорости потока 1 мл/мин. Буфер ФСБ при рН 7,4 использовали при скорости потока 1 мл/мин. Фракции, соответствующие очищенному антителу, собирали, концентрировали до ~1 мг/мл и хранили при -80°С.
[00429] Транзиентная экспрессия примеров v873, 874, 875 и других «азиметрических» антител по сравнению с эталонным v891 представлено на фиг. 7. ДСН-ПААГ на фиг. 7 показывает, что все примеры гетеромультимеров могут транзиентно экспрессироваться в клетках СНО3Е7 при жизнеспособности клеток, составляющей >80%.
[00430]
[00431] Пример 3: Гетеромультимер v873 способен связывать CD3 Т-клетки Jurkat и CD 19 В-клетки Raji.
[00432] Способность v873 связывать Т-клетки и В-клетки тестировали с помощью FACS-анализа следующим образом.
[00433] Соединение клеток с помощью FACS
[00434] Клетки в концентрации 1×106 кл/мл, суспендированные в RPMI, метили 0,3 мкМ подходящей метки CellTrace, перемешивали и инкубировали при 37°С на водяной бане в течение 25 минут
[00435] Осадок ресуспендировали в 2 мл L10+GS1+NaN3 до конечной концентрации 5х×106 кл/мл.
[00436] Клеточные суспензии анализировали (разведение 1/5) с помощью проточной цитометрии для верификации соответствующих клеточных меток и настроек лазера. Флуоросферы Flow-check Fluorospheres и Flow-set Fluorospheres использовали для верификации калибровки прибора, оптического согласования и струйной системы.
[00437] После верификации проточной цитометрии, и до соединения клеток, все линии клеток смешивают в требуемой пропорции, с получением конечной концентрации 1×106 кл/мл.
[00438] Связывание Т:Т оценивали с применением Jurkat-Violet + Jurkat-FarRed, В:В оценивали с применением RAJI-Violet+RAJI-FarRed; связывание Т:В оценивали с применением Jurkat-violet + RAJI-FarRed.
[00439] Антитела разводили в 2 раза в L10+GSl+NaN3 при комнатной температуре, затем добавляли к клеткам с последующим осторожным перемешиванием и инкубировали в течение 30 минут.
[00440] После инкубирования в течение 30 минут добавляли 2 мкл йодида пропидия и медленно перемешивали и немедленно анализируют с помощью проточной цитометрии.
[00441] % Связывания рассчитывали как процент случаев регистрируемых одновременно меток Violet и Far-red.
[00442]
[00443] Фиг. 1В иллюстрирует способность v873 и блинатумомаба CD19-CD3 BiTE (v891, МТ-103) связывать CD3 Т-клетки Jurkat (Верхний левый сектор) с CD19 В-клетками Raji (нижний правый сектор) с помощью FACS. Связанные Т- и В-клетки находятся в верхнем правом секторе. Этот результат показывает, что в концентрации 300 нМ гетеромультимер v873 способен специфически соединять Т-клетки Jurkat и В-клетки Raji аналогично (23% от общего числа клеток) BiTE (21% от общего числа клеток).
[00444]
[00445] Пример 4: Гетеромультимеры селективно связывают CD3- и CD19-экспрессирующие клетки.
[00446] Способность примера гетеромультимера v873 специфически связываться с CD3 и CD 19 оценивали с помощью FACS. Антитела «с одним плечом» (ОАА, «one-armed antibody») против CD3 и CD19 также получали согласно описанию в примере 2 и тестировали в качестве контроля в FACS-анализе клеточного связывания согласно приведенному ниже описанию.
[00447] Соединение клеток с применением протокола FACS:
[00448] 2×10 кл/мл клеток (жизнеспособность >80%) ресуспендировали в среде L10+GS1, смешивали с разведениями антител и инкубировали на льду в течение 1 часа.
[00449] Клетки промывали добавлением 10 мл холодного буфера R-2, и центрифугировали при 233g в течение 10 минут при 4°С. Клеточную массу ресуспендировали в 100 мкл (разведение 1/100 в среде L10+GS1) флуоресцентно меченых антител против IgG мыши или против IgG человека и инкубировали на протяжении 1 часа при КТ.
[00450] Обработанные клетки промывали добавлением 10 мл холодной R-2 согласно приведенному выше описанию, клеточную массу ресуспендировали 400 мкл холодного L-2 и образец фильтровали через Nitex и добавляли в пробирку, содержащий 4 мкл йодида пропидия.
[00451] Образцы анализировали с помощью проточной цитометрии.
[00452] Результаты представлены на фиг. 2 и показывают, что v873 способен селективно связывать и соединяться с CD3-экспрессирующими Т-клетками Jurkat (нижнее поле) и с CD19-экспрессирующими В-клетками Raji (верхнее поле). На фиг. 2 также показано, что анти-CD3 антитело «с одним плечом» специфично связывается с Т-клетками Jurkat и не вступает в перекрестную реакцию с CD19-экспрессирующими В-клетками, и что анти-CD 19 антитело «с одним плечом» специфично связывается с В-клетками Raji и не вступает в перекрестную реакцию с Т-клетками Jurkat.
[00453] Указанный эксперимент повторяли; результаты представлены на фиг. 9. Как и в предыдущем эксперименте, FACS-анализ показал, что v873 связывает селективно с Т-клетками Jurkat и с В-клетками Raji (фиг. 9В). На фиг. 9А видно, что IgG человека (hlgG) не связывается с Т-клетками Jurkat и проявляет незначительные уровни связывания с В-клеток Raji, предположительно, за счет взаимодействий между hIgG Fc и CD32B на В-клетках Raji. На фиг. 9А также показано, что ОАА против CD 19 связывается селективно с В-клетками Raji и не вступает в перекрестную реакцию с Т-клетками Jurkat.
[00454] Также проводили FACS-анализ для подтверждения того, что v873 не связывается с контрольными клеточными линиями, не экспрессирующими CD3 или CD 19. На фиг. 10 показано, что v873 не связывается с линией клеток К562, которые не экспрессируют CD 19 или CD3. На фиг. 11 показано, что v873 также не связывается с лимфоидными клетками мыши, которые не экспрессируют CD 19 или CD3.
[00455]
[00456] Пример 5: Гетеромультимеры опосредуют киллинг целевых В-клеток Raji клетками МКПК
[00457] В ходе предварительных экспериментов способность примера гетеромультимера, v873, опосредовать Т-клеточную цитотоксичность в отношении целевых Raji В-клеток измеряли с применением стимулированных ИЛ-2 клеток МКПК следующим образом.
[00458] Кровь человека (120-140 мл) от выбранных доноров для индивидуальных исследований собирали в течение двух последовательных дней. У доноров брали свежие МКПК ежедневно в течение указанных 2-х дней, и при необходимости часть МКПК пропускали через колонки EasySep (STEMCELL Technologies Inc.) для обогащения CD4+ и CD8+ . В первый день клетки МКПК и обогащенные фракции активировали инкубированием в течение ночи с 1000-3000 единиц/мл ИЛ-2. Культуру пропускали через колонку для негативной селекции для выделения активированных CD4+ и CD8+ клеток. Затем клетки метили и анализировали с помощью цитометрии для оценки содержания CD69+ клеток в составах. Клетки МКПК и обогащенные фракции второго дня использовали в анализе «как есть» без активации ИЛ-2 или в покоящемся состоянии.
[00459] Покоящиеся и активированные ИЛ-2 клетки МКПК и очищенные CD4+ и CD8+ использовали в качестве эффекторных клеток и В-клетки человека Raj i в качестве целевых клеток в анализе цитотоксичности. Тестировали соотношение эффектор:мишень, составляющее 30:1 для клеток МКПК и 15:1 для очищенных CD4+ и CD8+ клеток. МКПК также тестировали в присутствии гетеродимерного Fc в концентрации 20 мкг/мл и анализировали клеточную цитотоксичность при различных концентрациях тестируемых веществ.
[00460] После инкубирования клеток с тестируемыми веществами в течение 20-26 часов, 50 мкл супернатанта клеточной культуры брали для анализа на ЛДГ с применением ферментного набора для анализа на ЛДГ от Promega. В некоторых исследованиях анализировали относительные пропорции аутологичных Т- и В-клеток и/или аллогенных В-клеток в культуре и содержание клеток 7AAD+
[00461] Применяли сукцинимидиловый эфир карбоксифлуоресцеина (CFSE) и тестировали в качестве дифференциальной метки для отличия Raji и аутологичных В-клеток. Целевые клетки Raji предварительно метили минимальными количествами CFSE до инкубации с эффекторами, с тестируемыми веществами или без них. Клеточную массу ресуспендировали в различных коктейлях антител для анализа с помощью проточной цитометрии. Проточный цитометр Guava 8НТ использовали для анализа клеточных субпопуляций. Все антитела были получены от BD Biosciences, если не указано иное.
[00462] Каждое протестированное состояние включало подходящие контроли; лунки со всеми типами эффекторных и целевых клеток отдельно, для всех доноров, инкубировали со всеми тестируемыми веществами во всех концентрациях, используемых при анализе эффективности.
[00463] Чтобы избежать каких-либо помех для связывания тестируемых веществ с мишенями (CD3 и CD 19), для окрашивания В и Т-клеток использовали анти-CD20 и анти-CD7 маркеры, соответственно, для исследования, представленного на фиг. 23. Указанный анализ проводили с покоящимися и ИЛ-2-активированными клетками МКПК, очищенными CD4+ и CD8+ Т-клетками.
[00464] Анализ данных:
[00465] Для анализа на ЛДГ определяли оптическую плотность (OD) при 490 нМ для каждой лунки с применением ридера Emax от Molecular Devices. Анализ данных проводили с применением программного обеспечения LibreOffïce Cale. Для расчета цитотоксического ответа применяют следующую схему анализа:
[00466] Сначала из всех лунок вычитают средний фоновый сигнал культуральной среды (значения OD) до оценки цитотоксического ответа. Для индуцируемого детергентами максимального высвобождения чистых целевых клеток, используют специфический фоновый сигнал с объемной поправкой с учетом присутствия детергента и вычитают из значений OD максимального высвобождения.
[00467] Самопроизвольное совместное высвобождение эффекторов и мишеней регистрируют в лунках, не содержащих никаких тестируемых веществ, для каждой тестируемой популяции эффекторов: клеток МКПК, негативно селектированных по CD4 и CD8 популяций. Фоновауюактивность ЛДГ тестовой системы лучше оценивать в лунках, содержащих экспериментальную смесь популяций эффекторов-мишеней без каких-либо тестируемых веществ.
[00468] Во всех планшетах, для всех доноров, использовали спонтанное и максимальное высвобождение ЛДГ из клеток Raji, контрольные лунки со средой и лунки для позитивного контроля ЛДГ для отслеживания вариаций между планшетами.
[00469] Фиг. 3А иллюстрирует способность v873 перенаправлять активированные ИЛ-2 МКПК для киллинга целевых В-клеток Raji от 3 доноров. На фиг. 3В видно, что v873 способен опосредовать более высокую перенаправленную Т-клеточную цитотоксичность, чем v891, у одного из доноров. Указанные предварительные результаты указывают на то, что гетеромультимеры, на примере v873, может быть способен опосредовать более высокую Т-клеточную цитотоксичность, чем v891.
[00470] Оценивали способность v873 опосредовать киллинг клетками МКПК В-клеток Raji у 3 доноров по сравнению с контрольным IgGl человека. Способы, используемые в указанном эксперименте, совпадают с описанными в примере 5, со следующими модификациями: стимуляцию ИЛ-2 МКПК тестировали в концентрациях 1000-3000 единиц/мл.
[00471] Результаты, представленные на фиг. 8, показывают, что v873 индуцирует более высокий % цитотоксичности в отношении целевых В-клеток по сравнению с негативным контролем, IgG человека1 (G1), при сравнении индивидуальных доноров. В некоторых случаях, стимуляция более высокими концентрациями ИЛ-2, 3000 единиц/мл, приводила к более высокому % цитотоксичности в отношении целевых В-клеток.
[00472] Пример 6: Гетеромультимеры опосредуют перенаправленный киллинг целевых В-клеток Raji покоящимися и ИЛ-2 активированными CD4+ и CD8+ Т-клетками
[00473] Способность примеров гетеромультимеров v875, v1379, v1380 опосредовать CD4+ и CD8+ Τ-клеточную цитотоксичность в отношении целевых В-клеток Raji измеряли согласно описанию в примере 5.
[00474] Фиг. 16А иллюстрирует способность v875, v1379 и v1380 опосредовать антителозависимую В клеточную цитотоксичность за счет перенаправления CD4+ и CD8+ Т-клеток к В-клеткам Raji. Верхнее поле фиг. 16 иллюстрирует цитотоксичность покоящихся CD4+ и CD8+ Т-клеток в отношении В-клеток Raji. Указанные результаты показывают, что v875, v1380 и v891 вызывают зависимый от концентрации цитотоксический ответ, более выраженный в CD8+ Т-клетках. Нижнее поле фиг. 16 иллюстрирует цитотоксичность стимулированных ИЛ-2 CD4+ и CD8+ Т-клеток в отношении целевых В-клеток Raji. Указанные результаты указывают на то, что v875 и v1379 вызывают аналогичную v891 цитотоксичность в отношении В-клеток Raji активированных ИЛ-2 CD8+ эффекторных Т-клеток. Во всех случаях больший цитотоксический ответ обеспечивали ИЛ-2-активированные CD8+ Т-клетки по сравнению с ИЛ-2-активированными CD4+ Т-клетками. Указанные результаты также указывают на то, что FcGr-нокаутный вариант, v1380, цитотоксичен в отношении целевых В-клеток Raji, однако немного менее эффективен (максимальная цитотоксичность ≈40%) по сравнению с v875 и v1379 (максимум ≈60%), содержащих гетеродимеры Fc дикого типа.
[00475] Фиг. 16В-Е иллюстрируют представленные на фиг. 16А данные, нормализованные по IgG человека, для v875 (Фиг. 16В и С), и v1379 и v1380 (Фиг. 16D и Е), и включают % цитотоксичности, указанный для каждой из протестированных концентраций антител. На фиг. 16 В приведен обусловленный v875% цитотоксичности в отношении целевых В-клеток Raji ИЛ-2 активированных CD4+ и CD8+ эффекторных Т-клеток. На фиг. 16С приведен обусловленный v875% цитотоксичности в отношении целевых В-клеток Raji покоящихся CD4+ и CD8+ эффекторных Т-клеток. На фиг. 16D и Ε представлено прямое сравнение v1379 (Fe дикого типа) и v1380 (Fc-нокаут L234A L235A) в ИЛ-2 активированных (Фиг. 16D) и покоящихся (Фиг. 16Е) CD4+ и GD8+ Т-клетках. Наиболее существенное влияние Fe-нокаута L234A L235A (vi380) на цитотоксичность в отношении целевых В-клеток наблюдается в популяции ИЛ-2-активированных CD8+ Т-клеток (фиг. 16D, левое поле), где v1380 менее цитотоксичен по сравнению с v1379.
[00476] Эксперимент повторяли согласно фиг. 19 с v875, v873 и IgG человека, с использованием покоящихся (Фиг. 19А) и ИЛ-2-активированных CD8+ Т-клеток (Фиг. 19 В) в качестве эффекторных клеток, нацеленных на В-клетки Raji. На фиг. 19А показано, что v875 и v873 вызывают >30% цитотоксичность в отношении целевых В-клеток Raji, обусловленную ИЛ-2-активированными CD8+ Т-клетками в качестве эффекторов, и максимальный киллинг целевых клеток наблюдается при концентрации 3 нМ. На фиг. 19 В видно, что v875 и v873 вызывают дозозависимую (>20%) цитотоксичность покоящихся CD8+ Т-клеток в качестве эффекторов в отношении целевых В-клеток Raji. Более выраженный киллинг целевых В-клеток Raji наблюдается, если в качестве эффекторных клеток использовать ИЛ-2-активированные CD8+ Т-клетки.
[00477] Эксперимент повторяли согласно фиг. 20 для сравнения относительного вклада CD4+ и CD8+ Т-клеток в киллинг целевых В-клеток Raji при концентрациях v875, варьирующих от 0,06 до 10,0 нМ. На фиг. 20А представлена опосредованная v875 цитотоксичность в отношении целевых В-клеток Raji, обусловленная ИЛ-2-активированными CD4+ и CD8+ Т-клетки. Процент киллинга целевых В-клеток, вызванный ИЛ-2-активированными CD4+ и CD8+ Т-клетками, не повышался при концентрациях v875 выше 0,06 нМ. Как и ожидалось, величина киллинга целевых В-клеток ИЛ-2 активированными CD8+ Т-клетками больше, чем ИЛ-2 активированными CD4+ Т-клетками. На фиг. 20 В представлена опосредованная v875 цитотоксичность в отношении целевых В-клеток Raji покоящихся CD4+ и CD8+ Т-клеток. Процент киллинга целевых В-клеток покоящимися CD8+ клетками существенно не возрастает при концентрациях v875 выше 0,1 нМ. Дозозависимый киллинг В-клеток наблюдается для v875 и v873 при использовании CD4+ и CD8+ эффекторных Т-клеток. Как и ожидалось, киллинг целевых В-клеток покоящимися CD8+ Т-клетками выше по сравнению с покоящимися CD4+ Т-клетками.
[00478] Пример 7: Гетеродимерная Fc вносит вклад в цитотоксичность в отношении целевых В-клеток Raji
[00479] Способность примеров гетеромультимеров v875 и v873 опосредовать цитотоксичность в отношении целевых Raji В-клеток в присутствии и в отсутствие Fc измеряли согласно описанию в примере 5.
[00480] Фиг. 17 иллюстрирует опосредованную «азиметрическими» антителами v875 и v873 ИЛ-2-активацию МКПК и цитотоксичность в отношении целевых В-клеток Raji в присутствии или в отсутствие блокирования Fc согласно оценке с помощью ЛДГ-анализа. На фиг. 17А видно, что блокирование Fc ИЛ-2-активированных МКПК приводит к небольшому снижению % цитотоксичности (v875) или не приводит (v873) к снижению % цитотоксичности для целевых В-клеток Raji. На фиг. 17В видно, что блокирование Fc покоящихся МКПК приводит к снижению % цитотоксичности v875 и v873b отношении целевых В-клеток Raji.
[00481] Эксперимент повторяли; результаты представлены на фиг. 18. На фиг. 18А видно, что блокирование Fc ИЛ-2-активированных МКПК приводит к снижению % цитотоксичности v875 и у873для целевых В-клеток Raji при всех протестированных концентрациях антител. На фиг. 18 В видно, что блокирование Fc покоящихся МКПК приводит к снижению % цитотоксичности v875 и у873 для целевых В-клеток Raji при всех протестированных концентрациях антител. На фиг. 17 и 18 видно, что Fc вносит вклад в цитотоксичность в отношении целевых В-клеток Raji в гетеродимерных антителах v875 и v873.
[00482] Пример 8: Гетеромультимеры опосредуют цитотоксичность для аутологичных В-клеток
[00483] Способность примеров гетеромультимеров v875 и v873 к киллингу аутологичных В-клеток измеряли для совокупности МКПК и для покоящихся стимулированных ИЛ-2 клеток МКПК, при этом процент CD19+ 7AAD+ клеток после инкубирования с v875 и v873 (300 нМ, n=3 донора) определяли с помощью проточной цитометрии согласно описанию в примере 5.
[00484] На Фиг. 21 показано, относительно необработанной среды и контрольных IgG человека, что v875 и v873 (300 нМ) опосредуют киллинг аутологичных В-клеток в совокупности покоящихся МКПК (левое поле) и совокупности активированных ИЛ-2 МКПК.
[00485] Пример 9: Гетеромультимер v875 опосредует более избирательную цитотоксичность аутологичных Т-клеток по сравнению с BiTE
[00486] Эффекты обработки примерам гетеромультимеров v875 и v873 популяции аутологичных Т-клеток оценивали для совокупности МКПК и для покоящихся стимулированных ИЛ-2 клеток МКПК, при этом процент CD3+ 7AAD+ клеток после инкубирования с v875 и v873 (300 нМ, n=3 донора) определяли с помощью проточной цитометрии согласно описанию в примере 5.
[00487] На фиг. 22 показано, что v875, относительно необработанной среды и контрольных IgG человека, обуславливает более избирательный киллинг В-клеток за счет удержания большего числа аутологичных Т-клеток по сравнению с v873 и v891.
[00488] Пример 10: Дизайн, экспрессия и очистка гетеромультимеров с альбуминовым скаффолдом.
[00489] Следующие примеры CD3-CD19-связывающих гетеромультимеров на основе альбуминового скаффолда конструировали и получали описанным ниже образом.
[00490] Последовательности областей анти-CD19 и анти-CD3 scFv выбирали из двух молекул, в настоящее время проходящих клинические испытания, стабильность и получение которых подробно описаны и протестированы. Ahth-CD19 и анти-CD3 scFv получали непосредственно из молекулы BiTE блинатумомаба. Выбирали анти-CD3 scFv с ориентацией VH-VL, соответствующей используемой в BiTE. За эталонную молекулу принимали молекулу scFv на основе BiTE (v891). Гибриды AlbuCOREl (АВН2) CD3/CD19 получали путем присоединения участка, направленного против CD3, к природному N-концу фрагмента 1, и анти-CD19 - к С-концу фрагмента 2 (v1092, полипептидные последовательности, соответствующие последовательностям SEQ ID NO:264 и 266). Используемые линкеры были идентичны линкерам, использованным в ходе экспериментов с мультивалентным HER2 AlbuCORE: GGGS на N-конце фрагмента 1 и (GGSG)4GG на С-конце фрагмента 2. Получали вторую молекулу, где участки с направленным действием были расположены в обратном порядке (т.е. участок направленного действия против CD19 на природном N-конце фрагмента 1 и анти-CD3-на С-конце фрагмента 2, v1093. v1094 конструировали таким образом, чтобы расположить два разных гибрида на природных концах полипептида альбумина (полипептидные последовательности, соответствующие последовательности SEQ ID NO: 268). Гибридные scFv соединяли с молекулой альбумина линкером GGS на N-конце и линкером GGSG на С-конце. Длина линкеров соответствует линкерам, используемым в молекуле ММ-111, хотя используется другой тип последовательности.
[00491] V221 представляет собой гетеромультимер на основе альбумина, используемый для конструирования v1092, но без транспортных молекул (полипептидные последовательности, соответствующие последовательностям SEQ ID N0:269 и 270).
[00492] Экспрессию и очистку проводили согласно приведенному выше описанию для мультивалентного HER2.
[00493] Пример 11: Гетеромультимеры с альбуминовым скаффолдом специфически связываются с CD3- или CD19-экспрессирующими клетками
[00494] Способность нагруженного анти-CD3 χ анти-CD19 AlbuCORE-1 (v1092) связываться с CD3+ и CD19+ клетками оценивали с применением FACS и сравнивали с ЧСА дикого типа, нагруженного теми же анти-CD scFv (v1094).
[00495] Результаты представлены на фиг. 4 и показывают, что и v1092, и v1094 способны связываться с CD3-экспрессирующими Т-клетками Jurkat и с CD19-экспрессирующими В-клетками Raji.
[00496] Пример 12: Гетеромультимеры с гетеродимерной Fc или альбуминовыми скаффолдами демонстрируют сопоставимое нацеливание на В-клетки и связывание с Т-клетками
[00497] Способность гетеромультимеров с разными скаффолдами обеспечивать В-клеточный таргетинг и связывание Т-клеток сравнивали с помощью FACS-анализа, в соответствии со способом, описанным в примере 3. Конструкцию v1092 дополнительно тестировали на связывание В-клеток и Т-клеток в сравнении с v873 и контрольным BiTE v891 в соответствии со способом, описанным в примере 4.
[00498] Результаты представлены на фиг. 5А и указывают на то, что в протестированной концентрации v1092 был способен связывать 31% от общего числа клеток, и v873 был способен связывать 25% от общего числа клеток (нижние поля). Верхние поля представляют результаты при использовании среды в качестве контроля. Согласно описанию в примере 3 способность v873 связывать В-клетки с Т-клетками сравнима с контрольным BiTE v891. На фиг. 5А видно также, что способность v1092 связывать В-клетки с Т-клетки сопоставима с v873.
[00499] В дополнительном эксперименте способность v1092 связывать Т-клетки с В- клетками сравнивали непосредственно с контролем v221, и с контролем v873 и v891. Результаты представлены на фиг. 5В; видно, что v1092 способен связывать Т-клетки Jurkat с В-клетками Raji в большей степени, чем v221, и аналогично v891 и v873.
[00500] Пример 13: Примеры гетеромультимеров имеют более высокую анти-CD3 KD и более высокую Вшах при связывании с Т- и В-клетками по оценке с помощью FACS.
[00501] KD примеров гетеромультимеров, v873 и v875, оценивали с помощью FACS согласно описанию в примере 4, анализ данных и аппроксимацию кривых выполняли с помощью GraphPad Prism.
[00502] Результаты данного эксперимента представлены на фиг. 12 и указывают на то, что как v873, так и v875 обладают более высокой анти-CD3 аффинностью по сравнению с v891. KD связывания v873 и v875 с CD19-экспрессирующими клетками Raji сходна для всех антител и сравнима с KD v891. На фиг. 12 А и В приведены кривые связывания FACS для v873, v875 и v891 с CD3-экспрессирующими HPB-ALL и Т-клетками Jurkat, и с CD19-экспрессирующими В-клетками Raji. На фиг. 12 В также видно, что Bmax v875 для связывания с В-клетками Raji и Т-клетками Jurkat выше, чем у v891. В таблице 1 (см. в конце описания) приведены обобщенные данные относительно значений KD связывания HPB-ALL, Jurkat и Raji клеток для v875, v873 и v891.
[00521] KD для связывания с CD19-экспрессирующими Raji клетками примеров гетеромультимеров v875, v1379, v1380, v1381 и v891 оценивали с помощью FACS согласно описанию в примере 4; анализ данных и аппроксимацию кривых выполняли с помощью GraphPad Prism.
[00522] Результаты данного эксперимента представлены на фиг. 13 А и в таблице 2, и указывают на то, что гетеромультимеры v875, v1379, v1380, v1381 и v891 имеют сходные KD связывания с CD19-экспрессирующими клетками Raji. На фиг. 13А приведены кривые связывания FACS, полученные для антител при тестировании в диапазоне концентраций от 0,1 до 300 нМ. В таблице 2 (см. в конце описания) приведены обобщенные данные относительно выведенных KD в нМ, Вшах и наклона кривой (коэффициент Хилла), полученные с помощью FACS-анализа связывания. На фиг. 13А также видно, что Вшах связывания с CD19-экспрессирующими Raji клетками всех протестированных гетеромультимеров больше, чем у BiTE.
[00548]
[00549] Результаты FACS-связывания с HBP-ALL Т-клетками представлены на фиг. 13В и в таблице 3 и указывают на то, что гетеромультимеры v875, v1379, v1380 имеют более низкую KD по сравнению с v891. Фиг. 13В иллюстрирует кривую связывания FACS, полученную для антител при тестировании в диапазоне от 0,1 до 300 нМ. В таблице 3 (см. в конце описания) приведены обобщенные данные относительно выведенных KD в нМ, Вшах и наклона кривой (коэффициент Хилла), полученные с помощью экспериментов с FACS-связыванием. На фиг. 13 В также видно, что Втах для связывания с HBP-ALL всех протестированных гетеромультимеров выше, чем у v891.
[00580]
[00581] Пример 14: Гетеромультимер v875 способен связывать CD3 Т-клетки Jurkat с CD19 В-клетками Raji.
[00582] Способность гетеромультимера v875 связывать Т-клетки и В-клетки тестировали с помощью FACS-анализа согласно описанию в примере 3.
[00583] Результаты данного эксперимента представлены на фиг. 14 и указывают на то, что как v875, так и v891 способствуют сопоставимому связыванию между В-клетками Raji и Т-клетками Jurkat. Применение контрольного IgG человека приводило к 2,5% связыванию между клетками Raji и Jurkat, тогда как v875 способствовал связыванию 22,9% от общего числа клеток, и v891 способствовал связыванию 14,5% от общего числа клеток. Указанные результаты также были выражены в виде единиц кратности относительно фона, где v875 опосредовал 9,2-кратное увеличение связывания относительно фона, тогда как v891 опосредовал 5,8-кратное увеличение связывания относительно фона.
[00584] Пример 15: Устойчивое связывание В-клеток с Т-клетками, вызываемое гетеромультимерами, при варьирующих концентрациях антител или пропорциях клеток.
[00585] Способность v875 связывать В- и Т-клетки при варьирующих концентрациях оценивали с помощью FACS согласно описанию в примере 3, с модификациями, включающими изменения пропорций эффекторных и целевых клеток (Е:Т) (1:1 или 15:1) при трех разных концентрациях v875.
[00586] Результаты представлены на фиг. 15А и 15В. На фиг. 15А представлена величина соединения клеток с применением пропорции Т-клеток и В-клеток 1:1, при концентрациях гетеромультимеров, варьирующих от 0,3 нМ до 3 нМ. На фиг. 15В представлена величина соединения клеток с применением пропорции Т-клеток и В-клеток 15:1, при концентрациях гетеромультимеров, варьирующих от 0,3 нМ до 3 нМ. Оба варианта соотношения Е:Т (1:1 и 15:1) при тестировании с v875 обеспечивали сходное общее связывание Т-клеток с В-клетками при выражении в единицах кратности относительно фона.
[00587] Пример 16: Устойчивое связывание В-клеток с Т-клетками, обусловленное сконструированными различными способами гетеромультимерными конструкциями.
[00588] Способность v875 связывать В-клетки Raji с Т-клетками Jurkat (В:Т), а также В-клетки Raji:Raji (В:В) и Т-клетки Jurkat:Jurkat (Т:Т) оценивали с помощью FACS согласно описанию в примере 3.
[00589] Результаты представлены на фиг. 35А, 34В и 34С. На фиг. 34А представлены величины связывания Т:В, В:В и Т:Т для v875, v1379, v1380, v891, v1381, коммерческих ОКТ3 и IgG человека при проведении экспериментов в трех повторностях. Указанные результаты показывают, что все гетеродимерные антитела опосредуют высокий процент связывания Т:В, и что все варианты обеспечивают % связывания Т:В более высокий, чем v891. Указанные результаты также демонстрируют низкий процент связывания Т:Т и В:В относительно связывания % Т:В для всех вариантов.
[00590] На фиг. 34В представлены величины связывания Т:В, В:В и Т:Т для вариантов, содержащих сконструированные участки с направленным действием против CD3 для повышения стабильности (v1653, v1654, v1655, v1656, v1660, v1800, v1802) и v875, а также IgG человека. Указанные результаты показывают, что все гетеродимерные антитела (v875, v1653, v1654, v1655, v1656, v1660, v1800, v1802) опосредуют более высокий процент связывания Т:В по сравнению с негативным контролем, IgG человека, и все варианты опосредуют низкие уровни Т:Т связывания. Указанные результаты также показывают, что некоторые варианты (v1660, v1654 и v1655) опосредуют более высокий уровень связывания В:В по сравнению со связыванием Т:В.
[00591] Фиг. 34С представлены величины связывания Т:В, В:В и Т:Т Fc-нокаутных вариантов, содержащих либо сконструированные участки с направленным действием против CD3 для повышения стабильности (v1666), либо перекрестно-реактивные анти-CD3 и анти-CD19 scFv человека/яванского макака (v4541, v4543, v4545, v4548) коммерческих контрольных антител ОКТ3 против CD3, контрольного v2176 против CD19 и негативного контроля, IgG человека, и все варианты опосредуют низкий уровень Т:Т связывания. Указанные результаты показывают, что все гетеродимерные антитела (v1666, v4541, v4543, v4545, v4548) опосредуют более высокий процент связывания Т:В по сравнению с негативным контролем, IgG человека. Указанные результаты также показывают, что некоторые варианты (v1666, v4548) опосредуют более высокий уровень связывания В:В относительно связывания Т:В.
[00592] Пример 17: Эффекты v875, vl380, vl379 на ИЛ-2-активированные и покоящиеся CD20+, CD4+ , CD8+ субпопуляции
[00593] Эффекты обработки v875, v1379 и v1380 на жизнеспособность CD20+, CD4+ , CD8+ субпопуляций в ИЛ-2-активированных или покоящихся Т- и В-клеточных культурах, исследовали путем окрашивания 7AAD+ и FACS и нормализовали по контрольному изотипу (n=4 донора), согласно описанию в примере 5.
[00594] Результаты представлены на фиг. 23 и показывают, что примеры гетеромультимеров v875, v1379 и v1380 опосредуют цитотоксичность для CD20+ В-клеток, но не цитотоксичность для CD4+ или CD8+ Т-клеток относительно контрольного IgG человека. На фиг. 23А показаны эффекты v875 на жизнеспособность CD20+, CD4+ , CD8+ субпопуляций в ИЛ-2-активированных клеточных культурах. На фиг. 23В показаны эффекты v875 на жизнеспособность CD20+, CD4+ , CD8+ субпопуляций покоящихся клеточных культур. На фиг. 23С показаны эффекты v1379 и v1380 на жизнеспособность CD20+, CD4+ , CD8+ субпопуляций в ИЛ-2-активированных клеточных культурах. На фиг. 23D показаны эффекты v1379 и v1380 на жизнеспособность CD20+, CD4+ , CD8+ субпопуляций покоящихся клеточных культур. Вклад Fc дикого типа в цитотоксичность для CD20+В-клеток также представлен на фиг. 23С и D, где v1379 опосредует большую цитотоксичность для CD20+ В-клеток как ИЛ-2-активированных, так и покоящихся CD4+ и CD8+ Т-клеток.
[00595] Пример 18: Для опосредования цитотоксических эффектов примеров гетеромультимеров v875 и v873 необходимо присутствие как эффекторных Т-клеток, так и целевых В-клеток
[00596] Влияние инкубирования v875 и v873 по отдельности либо с эффекторными, либо с целевыми клетками оценивали по высвобождению ЛДГ согласно описанию в примерах 5, со следующими модификациями. Клетки, в общем количестве 300000 покоящихся и ИЛ-2-активированных МКПК, 150000 CD8+ эффекторных клеток или 10000 целевых клеток Raji, инкубировали в течение ночи с каждым из антител в концентрации 300 нМ, а также контролем без тестируемых веществ для каждого состояния. Приведенные данные представляют собой усредненные результаты для 3 доноров
[00597] Результаты опосредованного антителами высвобождения ЛДГ в покоящихся эффекторных и В-клетках Raji представлены на фиг. 24А; результаты опосредованного антителами высвобождения ЛДГ в активированных эффекторах представлены на фиг. 24В. На фиг. 24А видно, что v875 и v873 не являются цитотоксичными для популяций CD8+ Т-клеток относительно необработанной среды и контрольного IgG человека. На фиг. 24А также видно, что v875 и 873 увеличивают цитотоксичность в совокупности МКПК популяций, предположительно за счет перенаправленного киллинга эффекторными Т-клетками целевых В-клеток. Кроме того, на фиг. 24А видно, что в отсутствие эффекторных Т-клеток, v875 и v873 не являются цитотоксичными для популяций В-клеток Raji по сравнению со средой и контрольным IgG человека.
[00598] На фиг. 24В представлены результаты опосредованного v875 и v873 высвобождения ЛДГ в активированных эффекторных МКПК и CD8+ Т-клетках. Эти результаты указывают на увеличение уровней клеточной гибели при инкубировании v875 и v873 с активированными МКПК, по-видимому, за счет перенаправленного киллинга В-клеток, опосредованного гетеродимерными антителами в присутствии эффекторных Т-клеток и целевых В-клетках. На фиг. 24 В также видно, что инкубирование v875 с активированными CD8+ Т-клетками, приводит к более высокому проценту клеточной гибели относительно v873, среды и контрольных IgG человека.
[00599] Пример 19: Примеры гетеромультимеров способны опосредовать АЗКЦ или нарушенный АЗКЦ, нацеленный на В-клетки Daudi
[00600] Анализ на антителозависимую клеточноопосредованную цитотоксичность (АЗКЦ) проводили для v875, v1379 и v1380 с применением клеток Daudi в качестве целевых В-клеток и иммобилизированных несущих FcRy3a клеток NK92 в качестве эффекторных клеток (GS193761) с применением следующего способа.
[00601] Исследования зависимости доза-ответ проводили с использованием различных концентраций образцов с эффекторными и целевыми клетками в предварительно оптимизированном соотношении (Е/Т) (5:1). К контрольным клеткам добавляли Triton Х-100 без эффекторных клеток и антитела в конечной концентрации 1% для лизиса целевых клеток; их использовали в качестве контроля максимального лизиса; аналитические буферы добавляли в контрольные клетки без эффекторных клеток и антитела, и использовали в качестве контроля минимального высвобождения ЛДГ. Целевые клетки, инкубированные с эффекторными клетками без антител, использовали в качестве контроля для оценки фонового неспецифического высвобождения ЛДГ при совместном инкубировании обоих типов клеток.
[00602] Тестируемое вещество инкубировали с клетками при 37°С/5%CO2 на протяжении 5-6 часов и жизнеспособности клеток оценивали с помощью ЛДГ-набора. Поглощение регистрировали при OD 492 нм и OD 650 нм. Процентные значения лизиса клеток (OD 492 нМ) рассчитывали по приведенной ниже формуле:
[00603] % лизиса клеток = 100*(1 - (OD для данных образца - OD опухолевых клеток с эффекторными клетками) / (OD максимального высвобождения - OD минимального высвобождения)). Значения полумаксимальной эффективной концентрации (ЕС50) анализировали с помощью нелинейной аппроксимации сигмоидальной функцией кривой «доза-эффект» в GraphPad Prism.
[00604] Результаты представлены на фиг. 25А и В; они показывают, что гетеромультимеры с Fc дикого типа (v875 и v1379) способны опосредовать АЗКЦ (максимальный лизис клеток ≈40%), тогда как индукция направленного на Daudi В-клетки АЗКЦ v1380, содержащим нокаутную мутацию Fc L234A L235A, нарушена. На фиг. 25А и В представлено сравнение с внутренним положительным контролем, Ритуксимабом.
[00605] Пример 20: Примеры гетеромультимеров опосредуют нарушенный КЗЦ-опосредованный лизис В-клеток Daudi
[00606] Клеточные анализы на комплемент-зависимую цитотоксичность (КЗЦ) проводили с v875, v1379 и v1380 с применением клеток Daudi в качестве целевых В-клеток. Сыворотку человека от здоровых доноров (NHS) использовали в качестве источника комплемента. 10 мкл NHS (конечная концентрация 10% в 40 реакционных объемах) добавляли в каждую лунку для инициации каскада КЗЦ и инкубировали на протяжении 2 часов. Жизнеспособность клеток измеряли с помощью набора для анализа жизнеспособности клеток CellTiter-Glo® Luminescent Cell Viability Assay Kit.
[00607] Процент жизнеспособности клеток рассчитывали по формуле:
[00608] % Жизнеспособности клеток = 100 × ((относительных световых единиц RLU образца) / (RLU клетки + NHS)), в которой NHS представляет нормальную сыворотку человека. Полумаксимальная эффективная концентрация (ЕС50) значений анализировали с помощью нелинейной аппроксимации сигмоидальной функцией кривой «доза-эффект» в GraphPad Prism.
[00609] На фиг. 25С и D представлены результаты анализа КЗЦ для целевых В-клеток Daudi, обусловленной v1380 и v1379 (Фиг. 25С) и v875 (Фиг. 25D), и сравнение' с положительным контролем, ритуксимабом. Все гетеромультимеры демонстрируют нарушенный КЗЦ относительно ритуксимаба, и опосредуют максимальный лизис целевых клеток, составляющий 15% или менее.
[00610] Пример 21: Оценка пролиферации клеток и высвобождения цитокинов при использовании примеров гетеромультимеров
[00611] Влияние инкубирования с примерами гетеромультимеров на пролиферацию клеток и высвобождения цитокинов исследовали в МКПК и полученных из МКПК субпопуляциях. Полученные из МКПК субпопуляции включали МКПК, МКПК без В-клеток (МКПК - В), МКПК без клеток NK (МКПК - NK), МКПК без NK- и В-клеток (ΜΚΠΚ-ΝΚ-Β), CD8+ Т-клетки с В-клетками, и CD8+ без В-клеток. Вкратце, четыре (4) донора были протестированы на содержание популяций МКПК и полученных из МКПК субпопуляций CD 19-, CD56- или истощенных по CD19/CD56 МКПК) и два (2) донора были протестированы на содержание CD8 и CD8+ В-клеток в течение периода инкубирования 4 и 6 дней. Анализ пролиферации проводили с тестируемыми веществами при 2-х разных концентрациях (0,3 и 100 нМ), всегда с введением тимидина для индикации пролиферации. Содержание цитокинов измеряли с применением платформы СВА (Cytometric Bead Array) на проточном цитометре с помощью способа, соответствующего приведенному ниже описанию.
[00612] У 6 нормальных доноров брали образцы крови (подсчет CD8 потенциальных доноров для использования на панели CD8 проводили ранее), из которых выбирали двух доноров с высоким содержанием CD8 для экспериментальной панели CD8; один донор был предусмотрен в качестве запасного. На 1 день у каждого из 4 доноров брали приблизительно по 135 мл крови (для панели МКПК), а на 2-й день -165 мл крови брали у каждого из 2 доноров (для панели CD8). Ежедневно в указанные два дня выделяли свежие МКПК и указанные МКПК пропускали через колонки EasySep (STEMCELL Technologies Inc.) для истощения по CD19 и/или CD56 посредством позитивной селекции (день 1) и обогащения CD8 (±CD19) посредством негативной селекции (день 2).
[00613] Для подтверждения состава/чистоты/жизнеспособности отобранных субпопуляций ежедневно в указанные два дня использовали коктейль антител, состоящий из CD8-FITC/CD56-PE/7AAD/CD19-PECY7/CD20-APC.
[00614] Тестируемые вещества готовили в 2-кратной концентрации для получения конечных концентраций (после разведения с клетками) 0,3 и 100 нМ; добавляли в объеме 100 мкл. Клетки МКПК высевали с плотностью 250,000 клеток/лунку в 100 мкл суспензии; фракции CD8 высевали с плотностью 150 ООО клеток/лунку. Смеси инкубировали в течение 3 и 5 дней соответственно, после чего в слабо-связывающие планшеты переносили по 50 мкл клеточного супернатанта на лунку и замораживали для последующего анализа цитокинов. По 50 мкл меченого тритием тимидина добавляли в содержащие клетки лунки для получения конечной концентрации тимидина 0,5 микрокюри/лунку; планшеты инкубировали на протяжении еще 18 часов, после чего планшеты замораживали. Общее время инкубирования составляло 4 и 6 дней.
[00615] Планшеты размораживали через два дня, фильтровали и подсчитывали число импульсов в минуту (имп/мин) с помощью β-счетчика.
[00616] Пролиферацию клеток анализировали при 2-х концентрациях тестируемых веществ (0,3 и 100 нМ). На основе средних значений следующим образом рассчитывали индекс стимуляции (SI), и данные вносили в таблицу: среднее число имп/мин для тестируемого вещества/ среднее число имп/мин для среды без добавок.
[00617] Отражающие состав/жизнеспособность (трипановый синий, 7AAD) относительные пропорции в популяциях клеток МКПК и обогащенных по CD8 клеточных популяциях анализировали после отбора с применением коктейля антител, включающего антитела против: CD8/CD56/7AAD/CD20/CD56.
[00618] После анализа результатов пролиферации супернатанты повторных проб объединяли, с исключением любых идентифицированных выбросов значений по результатам пролиферации. Объединенный супернатант использовали для измерения цитокинов, в двух повторностях, с применением набора СВА Human Thl/Th2 Cytokine Kit II от BD Biosciences. Указанный набор предназначен для измерения ИЛ-2, ИЛ-4, ИЛ-6, ИЛ-10, ФНО и IFg.
[00619] Результаты анализа клеточной пролиферации с 4-дневным инкубированием представлены на фиг. 26 для концентраций 0,3 нМ (верхнее поле) и 100 нМ (нижнее поле) концентраций. На верхнем поле фиг. 26 видно, что при концентрации 0,3 нМ v875 и v1380 не индуцируют пролиферацию МКПК по сравнению с IgG человека. На нижнем поле фиг. 26 представлены результаты для концентрации антител 100 нМ; показано, что v875, v1380 и v891 индуцируют более высокие уровни пролиферации клеток относительно IgG человека. На фиг. 26 (нижнее поле) также видно, что при концентрации 100 нМ, пролиферативный индекс для v875 был аналогичен индексу для анти-CD3 ОКТ3 во всех 4-х популяциях МКПК. Однако v1380 (Fc-нокаутный вариант L234A L235A) и v891, по сравнению с v875, опосредуют пониженную пролиферацию клеток и демонстрируют тенденцию к зависимости клеточной пролиферации от В-клеток, при этом пролиферация клеток снижена в субпопуляциях МКПК-В и ΜΚΠΚ-Β-ΝΚ.
[00620]
[00621] На фиг. 28 представлены результаты оценки среднего индекса стимуляции, индуцируемой применением v875 в концентрациях 0,3
[00622] нМ (Фиг. 28А) и 100 нМ (Фиг. 28 В), очищенных CD8+ Т-клеток в отсутствие или в присутствии очищенных CD19+ В-клеток в момент времени через 4 дня инкубирования. На фиг. 28А видно, что при концентрации 0,3 нМ v875 обеспечивает более высокий индекс стимуляции по сравнению с IgG человека и более низкий по сравнению с ОКТ3. На фиг. 28А также видно, что v875 обеспечивает более высокий индекс стимуляции CD8+ Т-клеток в присутствии целевых В-клеток (CD8+ B). На фиг. 28 В видно, что при концентрации 100 нМ v875 обеспечивает индекс стимуляции, аналогичный ОКТ3, и более высокий по сравнению с IgG человека, при незначительном влиянии или отсутствии влияния популяций целевых В-клеток.
[00623]
[00624] На фиг. 29 приведены результаты оценки среднего индекса стимуляции, индуцируемой с применением vi 380 в концентрациях 0,3 нМ (фиг. 29А) и 100 нМ (фиг. 29 В), очищенных CD8+ Т-клеток в отсутствие или в присутствии очищенных CD19+ В-клеток в момент времени через 4 дня инкубирования. На фиг. 29А видно, что при концентрации 0,3 нМ, v1380 обеспечивает более высокий индекс стимуляции по сравнению с IgG человека и более низкий по сравнению с ОКТ3. На фиг. 28А также показано, что v1380 обеспечивает более высокий индекс стимуляции CD8+ Т-клеток в отсутствие целевых В-клеток (CD8). На фиг. 29 В видно, что при концентрации 100 нМ v1380 обеспечивает индекс стимуляции CD8+ Т-клеток, аналогичный ОКТ3, и более высокий индекс стимуляции по сравнению с IgG человека. Аналогично данным для концентрации 0,3 нМ, vi380 обеспечивает более высокий индекс стимуляции CD8+ Т-клеток в отсутствие целевых В-клеток (CD8). Нокаутная мутация Fc L234A_L235A в v1380, по-видимому, снижает зависимую от В-клеток стимуляцию CD8+ Т-клеток, очевидную при использовании одного из вариантов v875 с Fc дикого типа.
[00625]
[00626] Результаты анализа высвобождения цитокинов представлены на фиг. 27 и включают сводные графики уровней ФНОа (Фиг. 27А) ИФН-γ (Фиг. 27В), ИЛ-2 (Фиг. 27С), ИЛ-4 (Фиг. 27D) и ИЛ-10 (Фиг. 27Е) в супернатанте МКПК после инкубирования с тестируемыми веществами в концентрации 0,3 нМ на протяжении 4 дней (на оси Y графика отмечены логарифмизированные уровни цитокинов в пг/мл от 4 доноров). На фиг. 27 видно, что vi380 (Fc-нокаут L234A_L235A) индуцирует меньшее высвобождение цитокинов ФНОа, ИФН-γ, ИЛ-2, ИЛ-4 и ИЛ-10 по сравнению с v875 (Fc дикого типа) и ОКТ3.
[00627]
[00628] Пример 22: Примеры гетеромультимеров способны связывать две или более целевые В-клетки с эффекторной Т-клеткой
[00629]
[00630] Способность к связыванию и пропорции при связывании Т-клеток с В-клетками исследовали для примера гетеромультимера v875 с помощью микроскопии с применением способа, описанного в примере 3, со следующими модификациями.
[00631]
[00632] Меченые В-клетки Raji (красный) и меченые Т-клетки Jurkat (синий) инкубировали на протяжении 30 минут при КТ с 3 нМ IgG человека или v875. Суспензию клеток концентрировали удалением 180 мкл супернатанта. Клетки ресуспендировали в оставшемся объеме и визуализировали при увеличении 200× и 400×.
[00633]
[00634] На фиг. 30 представлены результаты микроскопического исследования связывания Т-клеток с В-клетками, со сравнением v875 и IgG человека (3 нМ) при увеличении 200× и 400×; представлены изображения, полученные с помощью фазовой (верхнее поле), флуоресцентной (среднее поле) и инвертированной флуоресцентной микроскопии (нижнее поле). На фиг. 30А представлено прямое сравнение IgG человека и v875 при увеличении 200х, и показана большая видимая величина связывания между В-клетками Raji и Т-клетками Jurkat по сравнению с IgG человека. На фиг. 30В и фиг. 30С представлены две зоны визуализации для v875 (фиг. 30В) и IgG человека (фиг. 30С) при увеличении 400х. На фиг. 30В представлены изображения опосредованного v875 формирования иммунного комплекса между Т-клетками Jurkat (темно-серые клетки на изображении, полученном с помощью инвертированной флуоресцентной микроскопии) и В-клетками Raji (светло-серые клетки на изображении, полученном с помощью инвертированной флуоресцентной микроскопии), и что одна Т-клетка Jurkat может соединяются с 1-3 В-клетками Raji. На фиг. 30С представлены снимки после инкубирования IgG человека с Т-клетками Jurkat и В-клетками Raji. Фиг. 30С иллюстрирует отсутствие связывания Jurkat-Raji после инкубирования с IgG человека, по сравнению с опосредованным v875 связыванием Jurkat:Raji, которое можно видеть на фиг. 30В.
[00635] Пример 23: Связывание примеров гетеромультимеров с рецепторами Fey по оценке с применением поверхностного плазмонного резонанса
[00636] Способность примеров гетеромультимерных антител связываться с FcDR CD16a и CD32a/b исследовали с применением поверхностного плазмонного резонанса (ППР).
[00637] Анализ с помощью поверхностного плазмонного резонанса: Аффинность рецепторов FcγR в отношении антитела Fc измеряли с помощью ППР с применением системы ProteOn XPR36 от BIO-RAD. Очищенные антитела на основе анти-CD3/анти-CD19 непрямо захватывали при введении со скоростью 25 мкл/мин в течение 240 секунд (что дает приблизительно 500 RU (единиц ответа)) после введения буфера для получения стабильной исходной фазы.
[00638] FcγR в различных концентрациях (10000, 3333, 1111, 370, 123 нМ) вводили со скоростью 60 мкл/мин в течение 120 секунд с фазой диссоциации 180 секунд для получения набора сенсограмм связывания. Итоговые значения Ко определяли на основе изотерм связывания, аппроксимированных для всего диапазона значений функцией модели связывания Лэнгмюра со стехиометрией 1:1; указанные значения представляют собой среднее для трех независимых анализов.
[00639] Результаты исследований связывания с помощью ППР приведены в таблице 4.
[00640]
[00642]
[00643] В таблице 4 (см. в конце описания) приведены обобщенные данные относительно KD связывания примеров гетеромультимеров с CD16a, CD16aV158, CS32a, CD32aR131, CD32b и CD32bY163. Указанные результаты показывают, что варианты с Fc дикого типа v875, v1379 и герцептин (дикого типа) связываются со всеми рецепторами Fcγ. Указанные результаты также показывают, что Fc-нокаутным вариантам свойственно нарушение связывания с некоторыми (v1380) или всеми (v1381) рецепторами Fcγ.
[00644]
[00645] Пример 24: Примеры гетеромультимеров способны связываться с рецептором CD3 Т-клеток человека и яванского макака
[00646] Связывание примеров гетеромультимеров с рецепторами человека CD3 и рецепторами яванского макака исследовали с помощью ИФА ELISA с помощью следующего способа.
[00647] Антиген CD3 рецептора человека или яванского макака разводили до 20 мкг/мл в ФСБ, в высоко-связывающем микропланшете с половинным объемом лунок Costar 3690, инкубировали в течение ночи при 4°С.Лунки промывали троекратно ФСБ и блокировали БСА 1% в ФСБ на протяжении 30 минут (50 мкл/лунку). Первичные гетеромультимерные антитела разводили в БСА 1% до заданных концентраций и инкубировали на протяжении 2 часов при КТ и лунки 4-кратно промывали ФСБ/0,05% Tween 20. Вторичное антитело (Jackson 115-036-062: специфическое против Fey мыши, или 709-036-098 против Fey человека) разводили 1/5000 в БСА 1% (25 мкл/лунку), инкубировали на протяжении 1 часа при КТ и 4-кратно промывали ФСБ/0,05% Tween 20. Добавляли субстрат ТМБ (25 мкл/лунку) на протяжении 25-30 минут, реакции останавливали 1М H2S04(12,5 мкл/лунку) и регистрировали оптическую плотность (OD) при 450 нм.
[00648] Данные ИФА ELISA представлены на фиг. 35 и иллюстрируют связывание с CD3 человека (верхнее поле) и связывание с CD3-рецептором яванского макака (нижнее поле) по оценке с помощью ELISA. На фиг. 35 показано, что v4543, v4545 и v4548 демонстрируют максимальную степень перекрестной реактивности в отношении CD3-рецептора яванского макака (фиг. 35, нижнее поле).
[00649] Пример 25: Экспрессия и очистка гетеромультимеров
[00650] Способы, применяемые для экспрессии и очистки примера гетеромультимера, описаны в примере 2.
[00651] На фиг. 31А представлен анализ ДСН-ПААГ и относительная чистота v875, v1380, v1379 и v891 после очистки с использованием белка А и ЭХ, и последующего хранения в течение 47 дней при 4°С. Две видимых белковых полосы в образце v891 соответствуют продукту разложения указанного образца в результате хранения.
[00652] На Фиг. 31В показан анализ ДСН-ПААГ и относительная чистота дополнительных примеров гетеромультимеров, включая v875, v1653, v1654, v1655, v1656, v1660, v1800, и v1802 после очистки с использованием белка А и ЭХ.
[00653] Пример 26: Примеры гетеромультимеров могут быть очищены до чистоты >99% гетеродимеров и <1% агрегатов.
[00654] Чистоту примеров гетеромультимеров тестировали путем ЖХ-МС.Сначала гетеромультимеры очищали с применением белка А, белка L и ЭХ согласно описанию в примере 2. ЖХ-МС-анализ гетеродимерной чистоты проводили согласно приведенному ниже описанию.
[00655] Очищенные образцы дегликозилировали ПНГазой F в течение 6 ч при 37°С. Перед МС-анализом образцы впрыскивали на колонку Poros R2 и элюировали в градиенте 20-90% АЦН, 0,1% ФК в течение 3 минут, что приводило к получению единственного пика.
[00656] Пик, полученный на ЖК-колонке, анализировали с помощью масс-спектрометра LTQ-Orbitrap XL с использованием следующих настроек: напряжение на конусе: 50В, напряжение на цилиндрических линзах: 215В; разрешение Фурье-спектрометра: 7500. Масс-спектр интегрировали с помощью программного обеспечения Promass или Max Ent. для получения профилей молекулярной массы.
[00657] Результаты ЖХ-МС для полученных в MaxEnt профилей молекулярной массы v875 представлены на фиг. 32; указанные результаты обобщены в таблице 5.
[00658]
Из таблицы 5 (см. в конце описания) видно, что после очистки с использованием белка А и ЭХ чистота v875 составляет 99,27% гетеродимера (Н1Н2) и менее чем 1% гомодимера анти-CD3 (Н2Н2) и гомодимера анти-CD19 (Н1Н1).
[00662] Чистоту и процент агрегации примеров очищенных с применением белка А и ЭХ гетеромультимеров определяли с помощью СВЭЖХ-ЭХ с помощью описанного способа.
[00663] Анализ СВЭЖХ-ЭХ проводили с применением колонки для ЭХ Waters ВЕН200, установленной на 30°С (2,5 мл, 4,6 х 150 мм, нержавеющая сталь, частицы 1,7 мкм) при скорости 0,4 мл/мин. Продолжительность каждого анализа составляла 7 минут и общий объем на одно введение составлял 2,8 мл с подвижными буферами: 25 мМ фосфатом натрия, 150 мМ ацетатом натрия, рН 7,1; и 150 мМ фосфатом натрия, рН 6,4-7,1. Детекцию по поглощению проводили при 190-400 нм, и по флуоресценции с регистрацией возбуждения на 280 нм и эмиссии на 300-360 нм. Интегрирование пиков анализировали с помощью программного обеспечения Empower 3.
[00664] Результаты ЖХ-МС и СВЭЖХ-ЭХ для примеров гетеромультимеров обобщены в таблице 6. Из таблицы 6 (см. в конце описания) видно, что все гетеромультимеры обладают гетеродимерной чистотой >95% согласно оценке с помощью ЖХ-МС, и все гетеромультимеры содержат <2% агрегатов согласно определению с помощью анализа СВЭЖХ-ЭХ.
[00665]
[00667]
[00668] Пример 27: Tm CH3 примеров гетеромультимеров выше 75°С.
[00669] Стабильность СН3-домена примеров гетеромультимеров исследовали с помощью ДСК с применением следующего способа. Все ДСК-эксперименты проводили с применением инструмента GE VP-Capillary. Белки буферизовали в ФСБ (рН 7,4), разводили 0,137 мл до 0,3-0,7 мг/мл, загружали в ячейку для проб и проводили измерения с частотой сканирования 1°С/мин от 20 до 100°С. Данные анализировали с применением программного обеспечения Origin (GE Healthcare) с вычитанием фона ФСБ-буфера.
[00670] Результаты ДСК, представленные на фиг. 33 А, В и С, показывают, что расчетная Tm СН3 v875 составляет >76°С (Фиг. 33А), расчетная Tm СН3 v1380 составляет >82,3°С (Фиг. 33В), и расчетная Tm СН3 составляет v1379>82,5°С (Фиг. 33С).
[00671] Пример 28: Дизайн, экспрессия и очистка CD3/CD20 и дополнительных CD3/CD19 гетеромультимерных конструкций.
[00672] V5850 (соответствует полипептидным последовательностям SEQ ID NO: 203, 205 и 207), v5851 (соответствует полипептидным последовательностям SEQ ID NO: 209, 211 и 213), v5852 (соответствует полипептидным последовательностям SEQ ID NO: 215, 217 и 219), v6324 (соответствует полипептидным последовательностям SEQ ID NO: 221, 223 и 225), v6325 (соответствует полипептидным последовательностям SEQ ID NO: 225, 227 и 229), v1813 (соответствует полипептидным последовательностям SEQ ID NO: 231, 233 и 235), v1821 (соответствует полипептидным последовательностям SEQ ID NO: 237, 239 и 241), v1823 (соответствует полипептидным последовательностям SEQ ID NO: 243, 245 и 247) являются примерами биспецифических CD3/CD19 или CD3/CD20 гибридных гетеродимерных Fc-конструкций. Биспецифические гибридные варианты состоят из F(ab') на любой из цепей А или В, спаренного с scFv-Fc на другой полипептидной цепи. Цепь А гетеродимера Fc включает следующие мутации: T350V_L351Y_F405A_Y407V, и цепь. В гетеродимера Fc включает следующие мутации: T350V_T366L_K392L_T394W. v6324 является примером биспецифических CD3/CD20 scFv гетеродимерных Fc-конструкций. V1813, v1821 и v1823 являются примерами CD3/CD20 гетеродимерных Fc-конструкций с общей легкой цепью. Варианты с общей легкой цепью состоят из двух разных F(ab'), каждый на дополняющем гетеродимере Fc, у которых имеется одна общая легкая цепь. Конкретный вариант композиции приведен в таблице 7.
[00673] Антитело против CD19 MOR208_scFv-Fc(VHVL), используемое для v5852, получали путем соединения опубликованной вариабельной последовательности тяжелой цепи с вариабельными последовательностями легкой цепи, приведенными в таблице 7, линкером (GGGGS)3 между тяжелой и легкой цепями. Вариабельные домены соединяли с цепью В гетеродимера Fc.
[00674] Ahth-CD20 scFv-Fc(VHVL) офатумумаба, используемое для v6324 и v6325, получали путем соединения опубликованной вариабельной последовательности тяжелой цепи с вариабельными последовательностями легкой цепи, приведенными в таблице 7 (см. в конце описания), линкером (GGGGS)3 между тяжелой и легкой цепями. Вариабельные домены соединяли с цепью В гетеродимера Fc.
[00675] Клонирование, экспрессию и очистку проводили согласно описанию в примере 2.
[00676] Выход и чистота вариантов представлены в таблице 8 (см. в конце описания). Гетеродимерную чистоту определяли при помощи анализа ЖХ/МС в соответствии с примером 26. Все варианты демонстрировали гетеродимерную чистоту свыше 73,8% при средней чистоте 89,6% для всех протестированных вариантов. Образцы содержали небольшие количества неправильно спаренных гомодимеров, варьирующие от 0 до 5,3% от общего количества продукта. Указанные значения представляют собой суммированные значения для всех наблюдавшихся вариантов гомодимеров. Присутствие полуантител наблюдалось чаще, чем гомодимеров и варьировало в диапазоне от 0 до 20,7% общего количества продукта. Указанные значения представляют собой суммированные значения для всех наблюдавшихся вариантов полуантител
[00679]
[00680]
[00684] Пример 29: Варианты гетеромультимеров CD3/CD20 и дополнительные варианты CD3/CD19 связываются с Т-клетками и с В-клетками.
[00685] Способность примеров гетеромультимеров CD3/CD20, v5850, v6324, v6325, v1813, v1821, v1823 связываться с клетками CD3 и CD20 анализировали с помощью FACS-анализа в соответствии с процедурами, описанными в примере 4. Дополнительно аналогичным образом оценивали способность примеров гетеромультимеров CD3/CD19, v5851 и v5852 связываться с клетками CD3 и CD19. Также получали дополнительный вариант v875, конструкцию с антителом CD3/CD19 BiTE Fc, и тестировали в качестве эталонного. Репрезентативные кривые связывания для v875, v5850 и v5851 на клетках Raji и Jurkat представлены на фиг. 36А и 38В. Результаты связывания для каждого варианта, выраженные через кинетические константы Bmax и Kd, приведены ниже в таблицах 9 и 10 (см. в конце описания). В таблице 8 представлено связывание с CD19- и CD20-экспрессирующими В-клетками Raji, а в таблице 10 - связывание с CD3-экспрессирующими Т-клетками Jurkat. В исследованиях связывания Raji (таблица 9) все варианты связывались с более высоким Вшах и более высокой Kd, чем 875. В исследованиях связывания Jurkat (таблица 10) все варианты, кроме v1823, связывались с более высоким Втах, чем 875, и с варьирующими KD.
[00691] Пример 30: Варианты гетеромультимеров CD3/CD20 и дополнительные CD3/CD19 соединяют Т-клетки с В-клетками.
[00692] Способность шести примерных вариантов гетеромультимера CD3/CD20 - а именно, v5850, v6324, v6325, v1813, v1821 и v1823 - и двух примерных вариантов гетеромультимера CD3/CD19 - а именно, v5851 и v5852 - связывать Т-клетки и В-клетки тестировали с помощью FACS-анализа в соответствии с процедурами, описанными в примере 3. Также получали дополнительные конструкции, а именно, v792 и v875, и тестировали в качестве контроля. V792 содержит идентичный анти-Нег2 F(ab') на основе трастузумаба на цепи А и цепи В гетеродимера Fc со следующими мутациями: T350V_L351Y_F405A_Y407V на цепи А и T350V_T366L_K392L_T394W на цепи В (№ доступа Drug Bank - DB00072)
[00693] В таблицах 11 и 12 (см. в конце описания) приведены процентные величины связывания между клетками Jurkat-Jurkat, Raji-Raji и Jurkat-Raji для каждого варианта; в каждой таблице представлен индивидуальный эксперимент.Все варианты эффективно связывали клетки Jurkat с клетками Raji. Далее, ни один из вариантов не соединял две клетки Jurkat; наблюдались, в той или иной степени, определенные уровни связывания клеток Raji-Raji.
[00756] Пример 31: Дизайн, экспрессия и очистка гетеромультимерных HER2/HER3 конструкций.
[00757] Для оценки различных свойств биспецифических HER2/HER3 гетеромультимерных конструкций две формы и различные контроли получали и очищали следующим образом. Первую конструкцию получали путем соединения HER2- и HER3-связывающих scFv с гетеродимерной Fc-областью (v878, HER2/HER3 с гетеродимерной Fc). Вторую конструкцию получали путем соединения Нег2- и Нег3-scFv с платформой на основе альбумина (v1090, AlbuCORE против Her3×Her2). Также получали различные контроли, включая Her2 с гетеродимерной Fc «с одним плечом», Her3 с гетеродимерной Fc «с одним плечом» и контрольный гибридный ЧСА-белок v1087, в качестве контрольных.
[00758] Дизайн
[00759] Биспецифические конструкции HER2/HER3 получали путем соединения Her2 и Her3 scFv на платформах с гетеродимерной Fc или AlbuCORE.
[00760] 1. Вариант 878: моновалентное антитело против Her2 «с одним плечом», где Her2-связывающий домен представляет собой scFv на цепи А, и Fc-область представляет собой гетеродимер, содержащий мутации L351Y_F405A_Y407V на цепи А и T366L K392M T394W на цепи В. Эпитопом антигенсвязывающего домена является домен 1 Her2.
[00761] 2. Вариант 879: моновалентное антитело против Her3 «с одним плечом», где Her3-связывающий домен представляет собой scFv на цепи В, и Fc-область представляет собой гетеродимер, содержащий мутации L351Y_F405A_Y407V на цепи А и T366L_K392M_T394W на цепи В.
[00762] 3. Вариант 880: биспецифическое антитело против Her2/Her3, где Her2-связывающий домен представляет собой scFv на цепи А, Her3-связывающий домен представляет собой scFv на цепи В, и Fc-область представляет собой гетеродимер, содержащий мутации L351Y_F405A_Y407V на цепи А и T366L_K392M_T394W на цепи В.
[00763] 4. Вариант 1087: Молекула ММ-111 представляет собой одиночный полипептид - гибридный белок из двух scFv, анти-Her2 (B1D2) и анти-Her3 (Н3), соединенных с С- и N-концами, соответственно, модифицированного белка альбумина сыворотки человека, и производится Merrimack. Итоговая молекула является биспецифической и бивалентной. В качестве контроля был сконструирован вариант ММ-111 молекулы, в котором участок направленного действия против Her3 (Н3) соединен с N-концом альбумина коротким AAS-линкером, тогда как анти-Her2 (B1D2) соединен с С-концом линкером AAAL, с получением эталонного контрольного варианта 1087. В указанном контрольном варианте отсутствует мутация C34S/N504Q, в оригинале введенная Merrimack в молекулу ММ-111, и имеет полипептидную последовательность, соответствующую последовательности SEQ ID NO: 258.
[00764] 5. Вариант 1090: Гетеромультимер на основе альбумина получали путем комбинирования фрагмента 1, соединенный с анти-HER3 на N-конце линкером GGGS [SEQ ID NO: 260], и фрагмента 2, соединенного с анти-HER2 (B1D2) на С-конце линкером GGGS [SEQ ID NO: 262] (вариант №1090). Указанная молекула содержала участки с направленным действием или транспортные полипептиды в цис-конфигурации и практически идентична v1087. Основные различия между полипептидом 1087 и 1090 состоят к том, что 1) линкеры, используемые в полипептиде 1087, были более гидрофобными, тогда как линкеры, используемые во варианте 1090, представляли собой поли-Gly (S) и 2) Во варианте 1090 отсутствует мутация C34S/N504Q, в оригинале введенная Merrimack.
[00765] Варианты 878, 879 и 880 экспрессировали и очищали согласно описанию в примере 2. Варианты 1087 и 1090 экспрессировали и очищали согласно описанию в примере 10.
[00766] Пример 32: гетеромультимерные HER2/HER3 конструкции на основе Fc биспецифически связываются с рецепторами Нег2 и НегЗ на клетках MALME-3M.
[00767] Способность HER2- и HER3-конструкций v878, v879 и v880 связываться с Her2 и Her3 оценивали с применением FACS-анализа:
[00768] Два моновалентных варианта «с одним плечом» (анти-HER2 «с одним плечом», v878, и анти-HER2 «с одним плечом», v879) и биспецифический анти-HER2/HER3 гетеродимер, v880, инкубировали в диапазоне дозировок с клетками метаномы MALME-3M с последующим FACS-анализом для определения сродства к связыванию каждой молекулы согласно описанию в примере 4.
[00769] Фиг. 37А и 37В иллюстрирует аффинность с использованием линейной и логарифмической шкалы соответственно. Как видно из указанных фигур, конструкция HER2/HER3 с гетеродимерной Fc проявляет как биспецифичность, так и авидность.
[00770] Пример 33: HER2/HER3 конструкции на основе альбумина биспецифически связываются с рецепторами Her2 и Her3 на клетках MALME-3.
[00771] Сродство к связыванию гетеромультимера на основе альбумина, нагруженного анти-Her2 и анти-Her3 scFv в цис-конфигурации, в отношении клеток MALME-3M анализировали и сравнивали с контролем v1087.
[00772] Сродство связывания примера варианта гетеромультимера на основе альбумина 1090 (АВН2против Her2 × против Her3) к клеткам MALME-3M оценивали с применением FACS с мечеными флюоресцеинизотиоцианатом (FITC) антителами против ЧСА, согласно описанию в примере 4.
[00773] Фиг. 38 иллюстрирует связывание варианта 1090 по сравнению с контролем 1087 в клетках MALME-3M и показывает, что ν 1090 связывает целевые клетки MALME-3М аналогично v1087.
[00774] Пример 34: Моновалентные анти-CD3 антитела «с одним плечом» способны связывать Т-клетки Jurkat и В-клетки Raji
[00775] Способность моноспецифических анти-CD3 антител v870, v871, v872 связывать Т-клетки и В-клетки тестировали с помощью FACS-анализа согласно описанию в примере 3.
[00776] Результаты обобщены в таблице 13 (см. в конце описания) и показывают, что v870, v871 и v872 соединяют более высокий процент Т-клеток Jurkat и В-клеток Raji по сравнению с средой и контрольными IgG человека. В таблице 13 также показано, что v870, v871 и v872 соединяют более низкий процент Т-клеток Jurkat и В-клетки Raji по сравнению с биспецифическим антителом против CD3 и CD19, v873.
[00778]
[00779] Следует понимать, что примеры и варианты реализации согласно описанию в настоящем документе предназначены исключительно для иллюстративных целей, и что специалисты в данной области техники смогут предложить различные их модификации или изменения, соответствующие сущности и входящие в объем настоящей заявки и прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| РАЗРАБОТКА СТАБИЛЬНОГО ГЕТЕРОДИМЕРНОГО АНТИТЕЛА С МУТАЦИЯМИ В ДОМЕНЕ Fc | 2012 |
|
RU2675319C2 |
| ПОЛИПЕПТИДЫ, СВЯЗЫВАЮЩИЕСЯ С CD3 | 2013 |
|
RU2673153C2 |
| РАЗРАБОТКА СТАБИЛЬНОГО ГЕТЕРОДИМЕРНОГО АНТИТЕЛА С МУТАЦИЯМИ В ДОМЕНЕ Fc | 2012 |
|
RU2810540C2 |
| ПОЛУЧЕНИЕ ГЕТЕРОМУЛЬТИМЕРНЫХ БЕЛКОВ | 2011 |
|
RU2624027C2 |
| ПОЛУЧЕНИЕ ГЕТЕРОМУЛЬТИМЕРНЫХ БЕЛКОВ С ИСПОЛЬЗОВАНИЕМ КЛЕТОК МЛЕКОПИТАЮЩИХ | 2015 |
|
RU2727012C2 |
| НОВЫЕ БИСПЕЦИФИЧНЫЕ ПОЛИПЕПТИДНЫЕ КОМПЛЕКСЫ ПРОТИВ CD3/CD19 | 2018 |
|
RU2788127C2 |
| БЕЛКИ, СВЯЗЫВАЮЩИЕ СПЕЦИФИЧЕСКИЙ МЕМБРАННЫЙ АНТИГЕН ПРОСТАТЫ, И СООТВЕТСТВУЮЩИЕ КОМПОЗИЦИИ И СПОСОБЫ | 2012 |
|
RU2632647C2 |
| ОДНОЦЕПОЧЕЧНЫЕ АНТИТЕЛА И ДРУГИЕ ГЕТЕРОМУЛЬТИМЕРЫ | 2013 |
|
RU2644341C2 |
| КЛЕТКИ, ЭКСПРЕССИРУЮЩИЕ ХИМЕРНЫЕ АКТИВИРУЮЩИЕ РЕЦЕПТОРЫ И ХИМЕРНЫЕ СТИМУЛИРУЮЩИЕ РЕЦЕПТОРЫ, И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2780020C2 |
| ПОЛИСПЕЦИФИЧЕСКИЕ ПОЛИПЕПТИДНЫЕ КОНСТРУКЦИИ, ОБЛАДАЮЩИЕ ОГРАНИЧЕННЫМ СВЯЗЫВАНИЕМ С СD3, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2813816C2 |
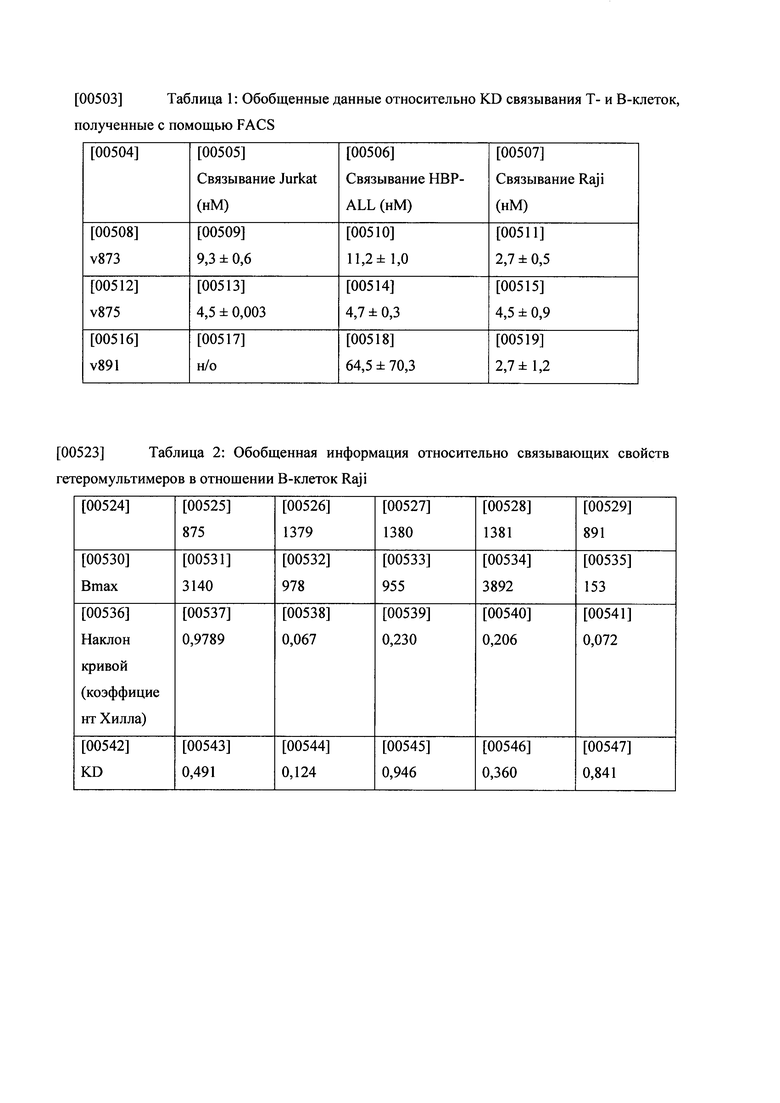
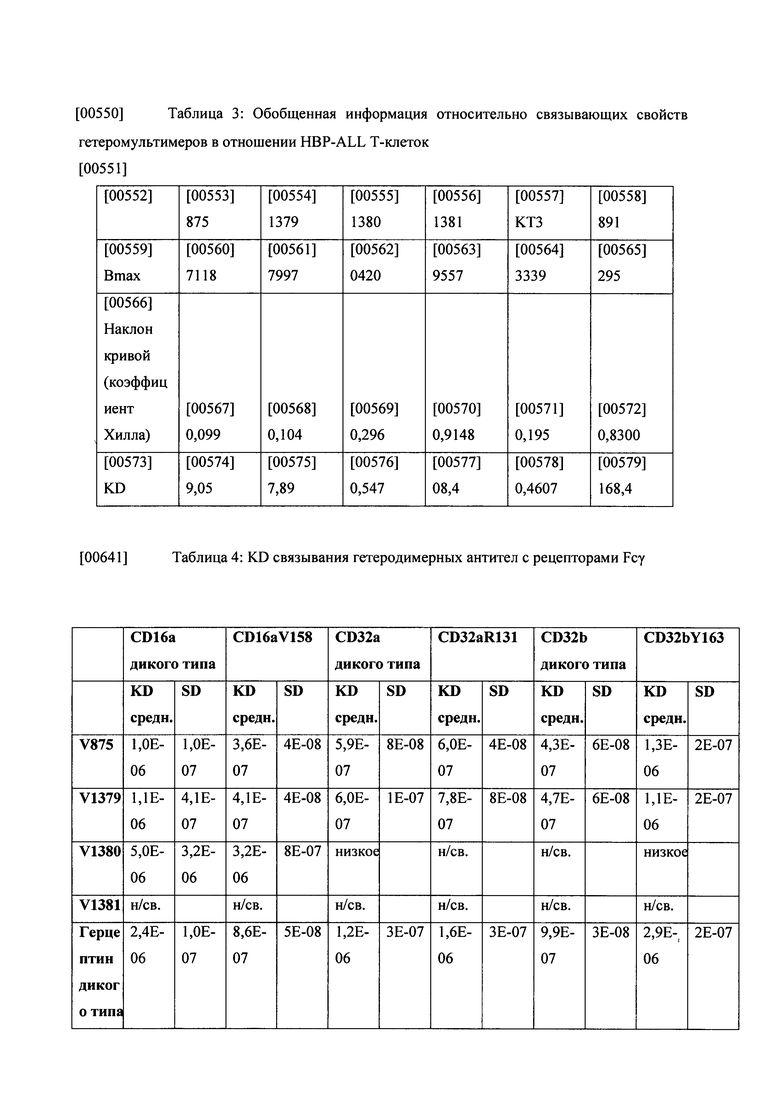

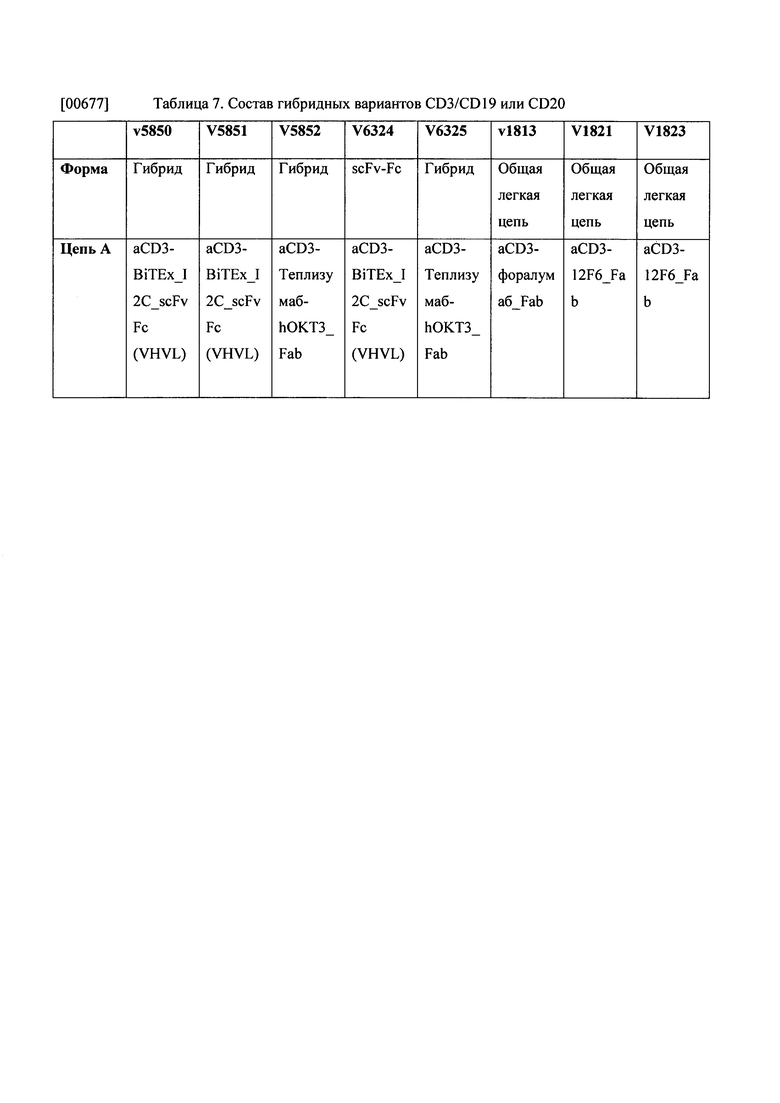
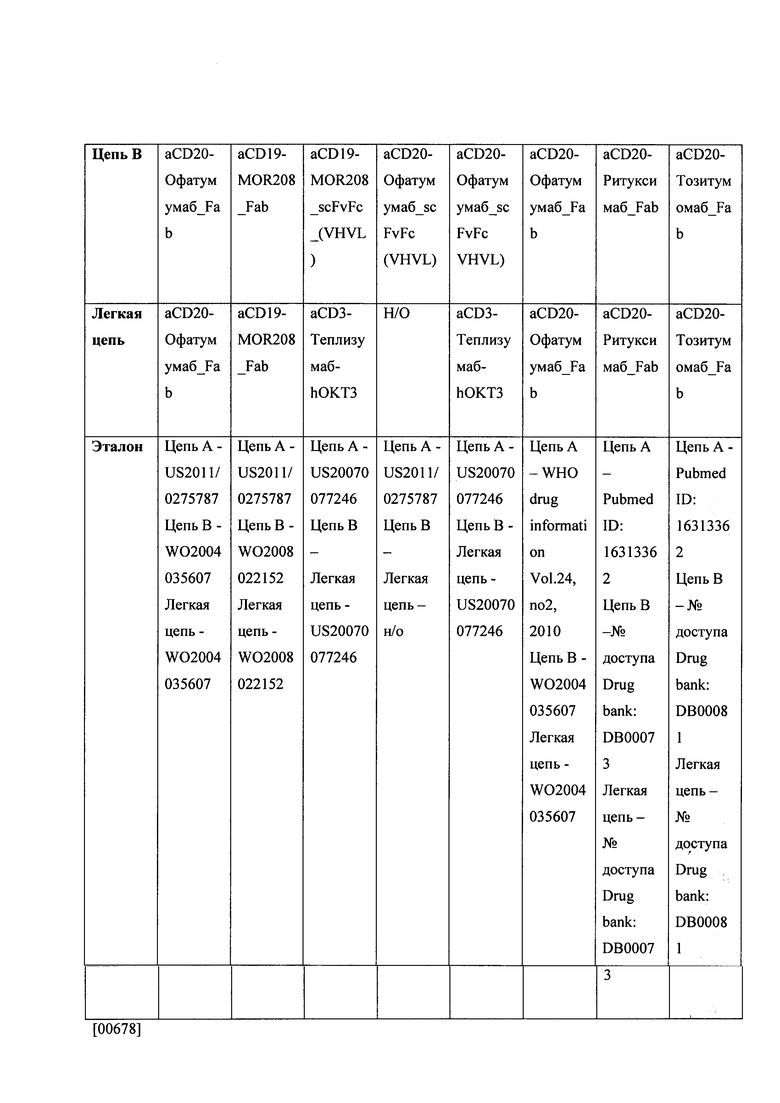
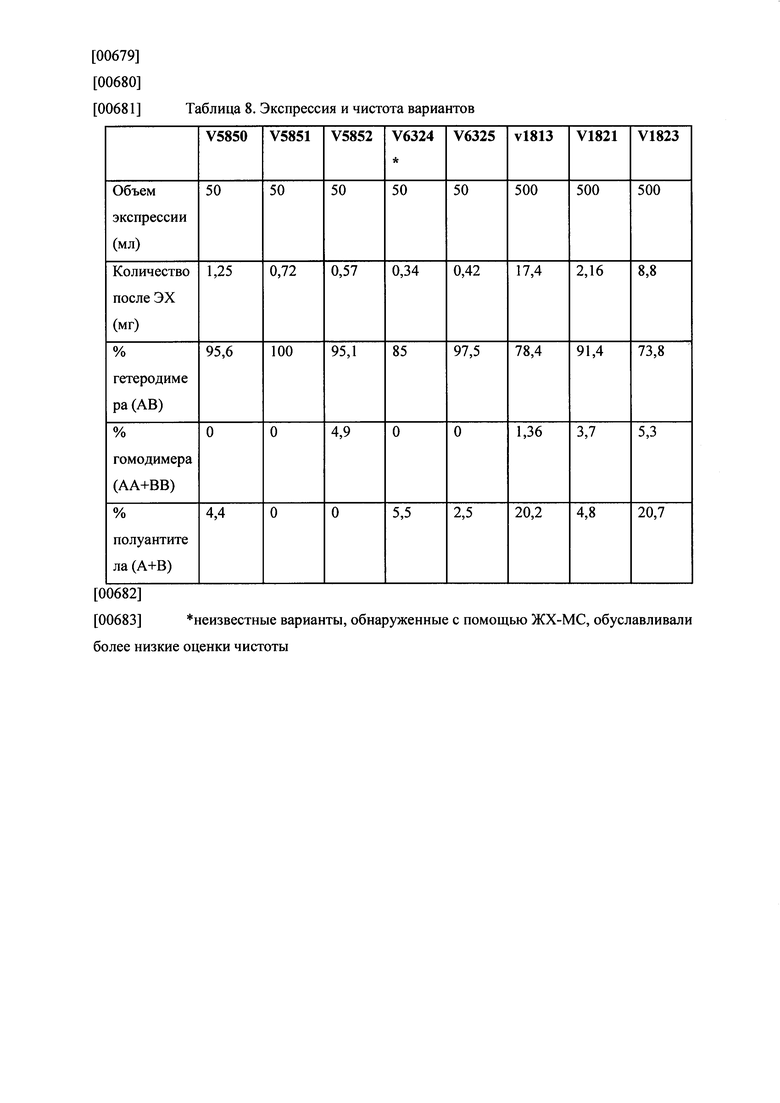
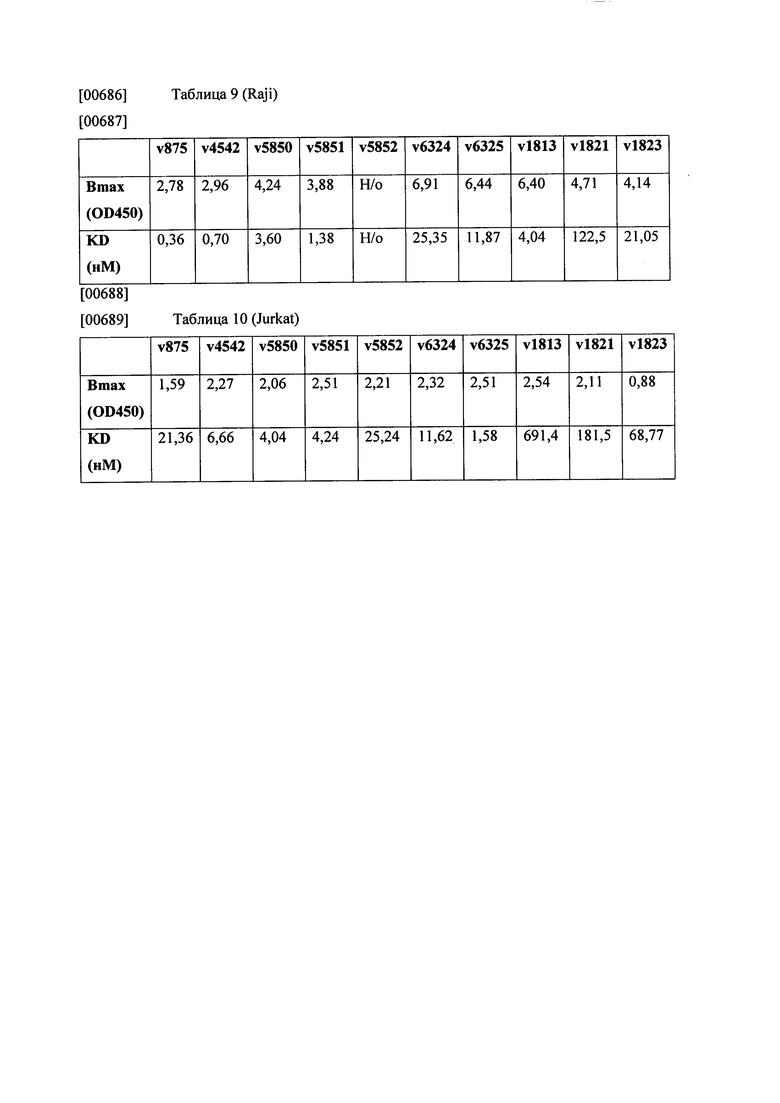

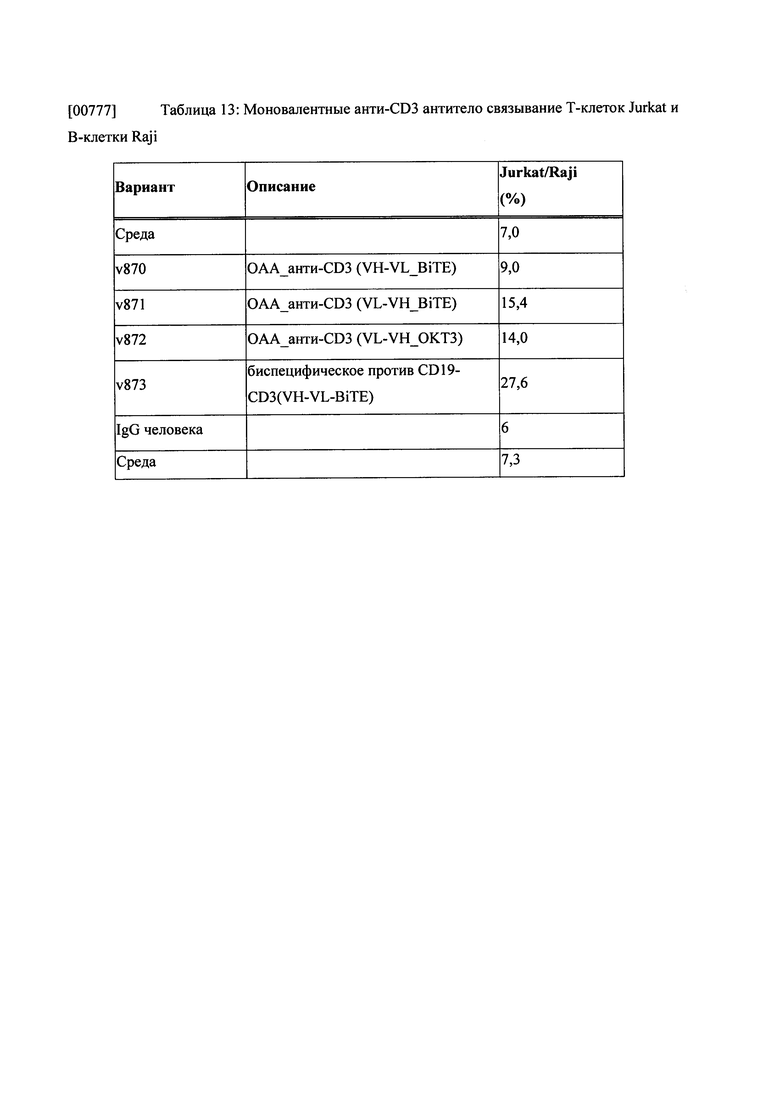






































































































































































































































































































































































































































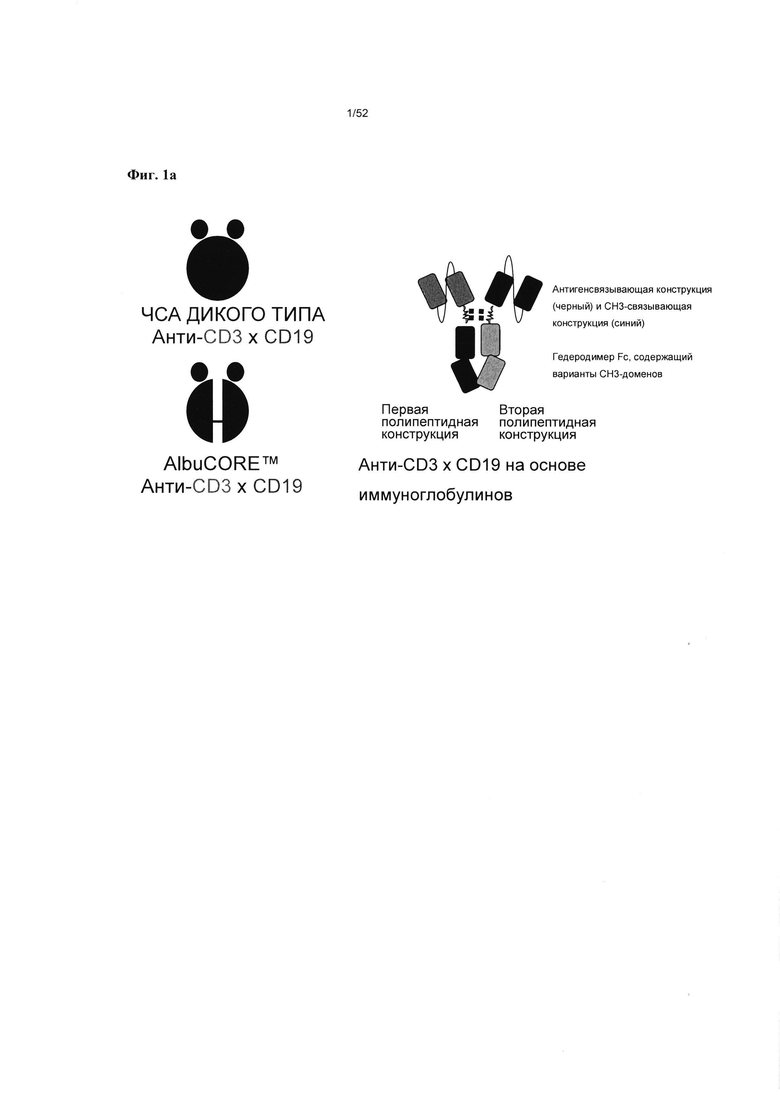
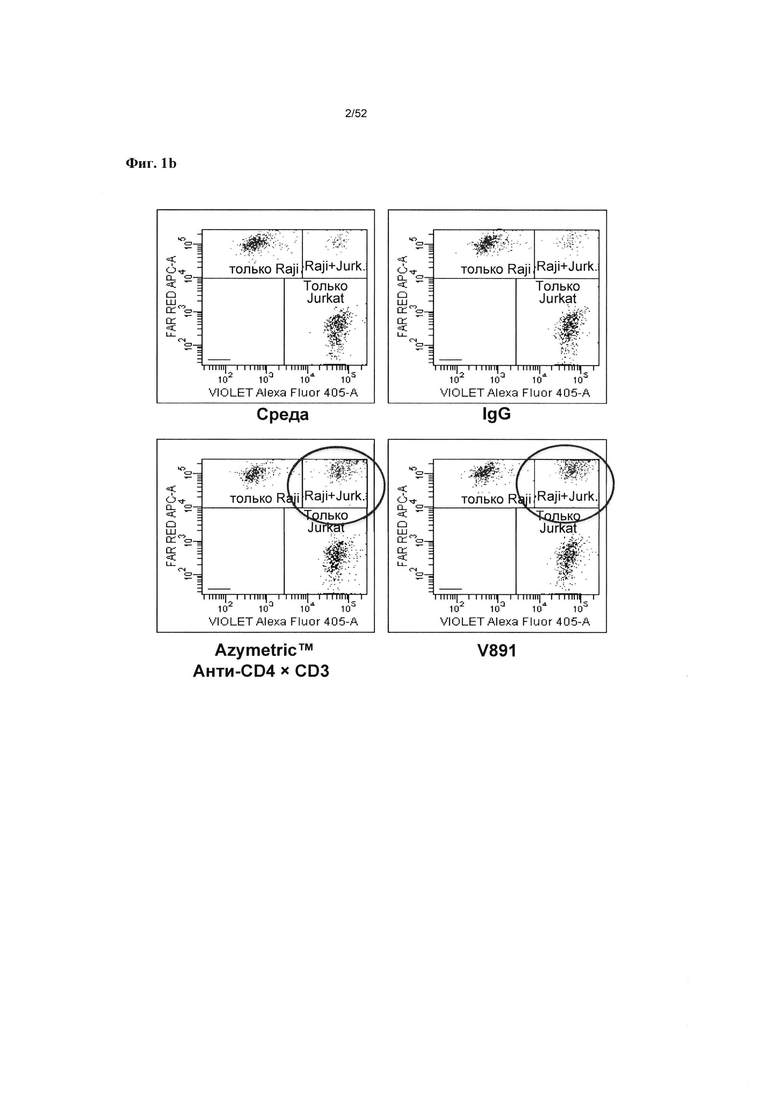
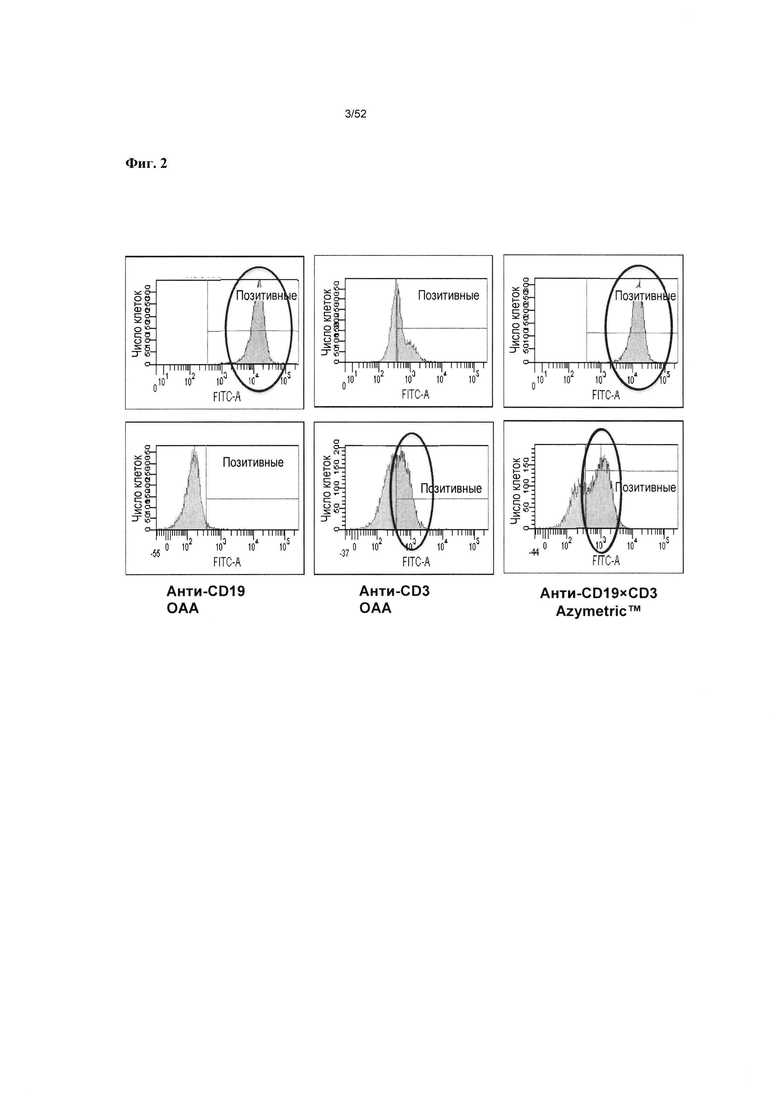
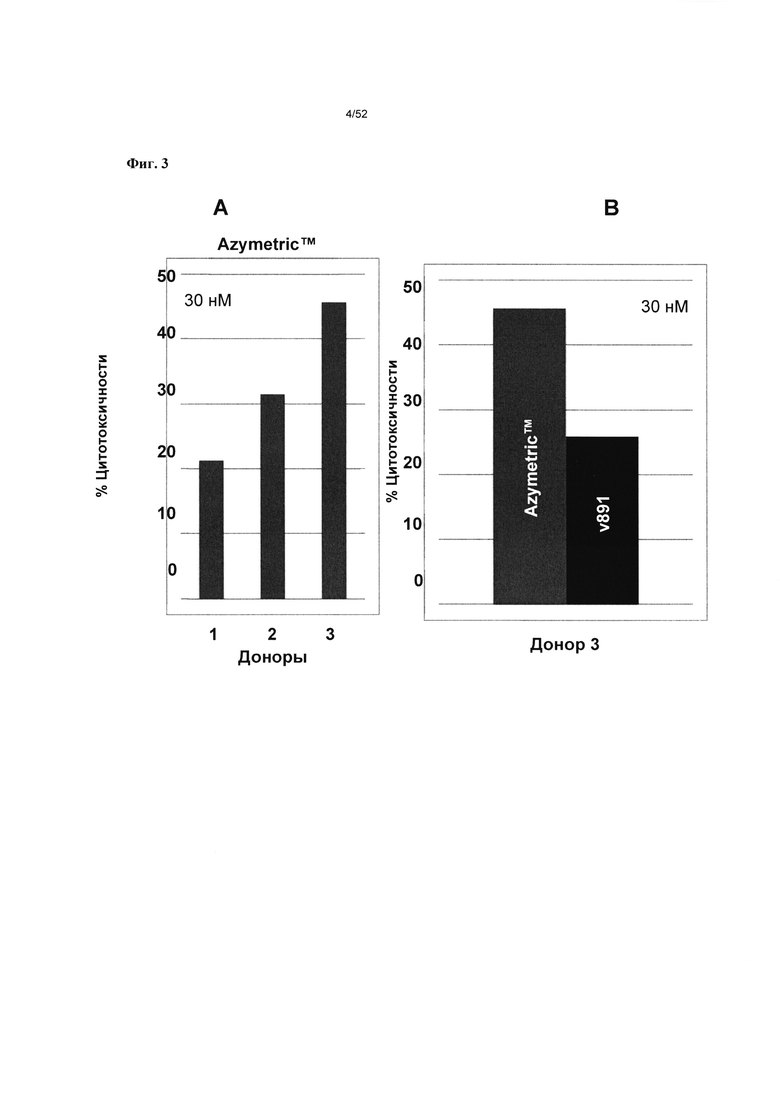
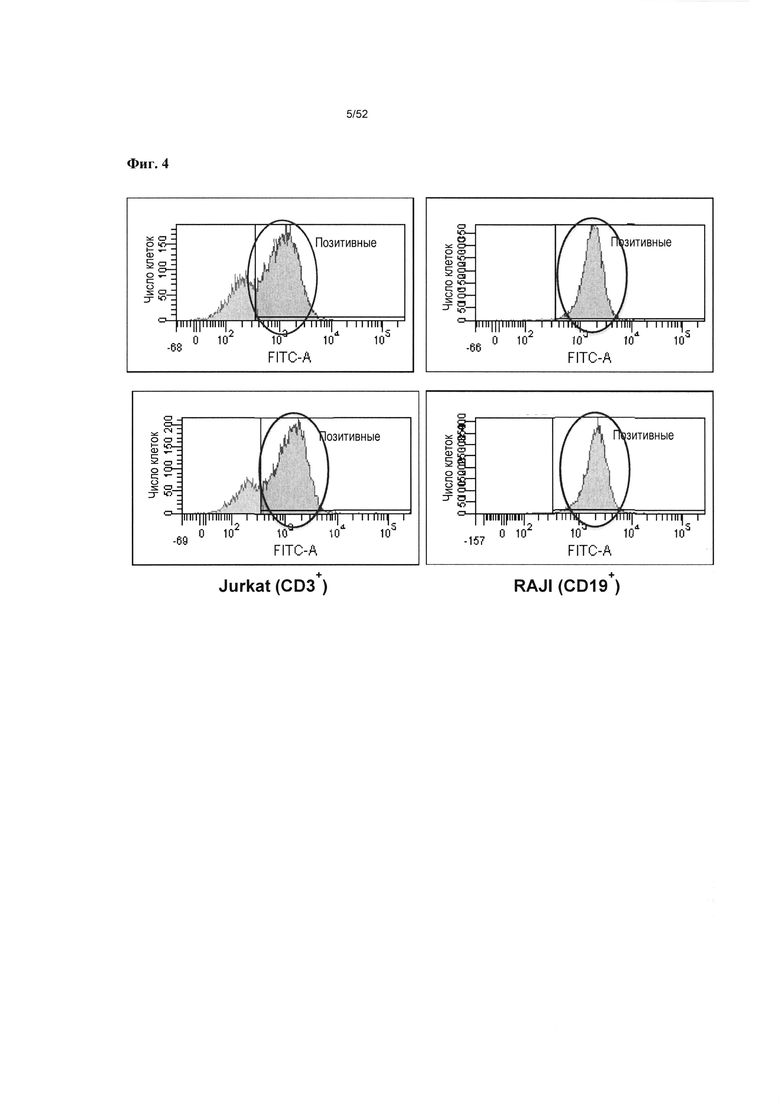
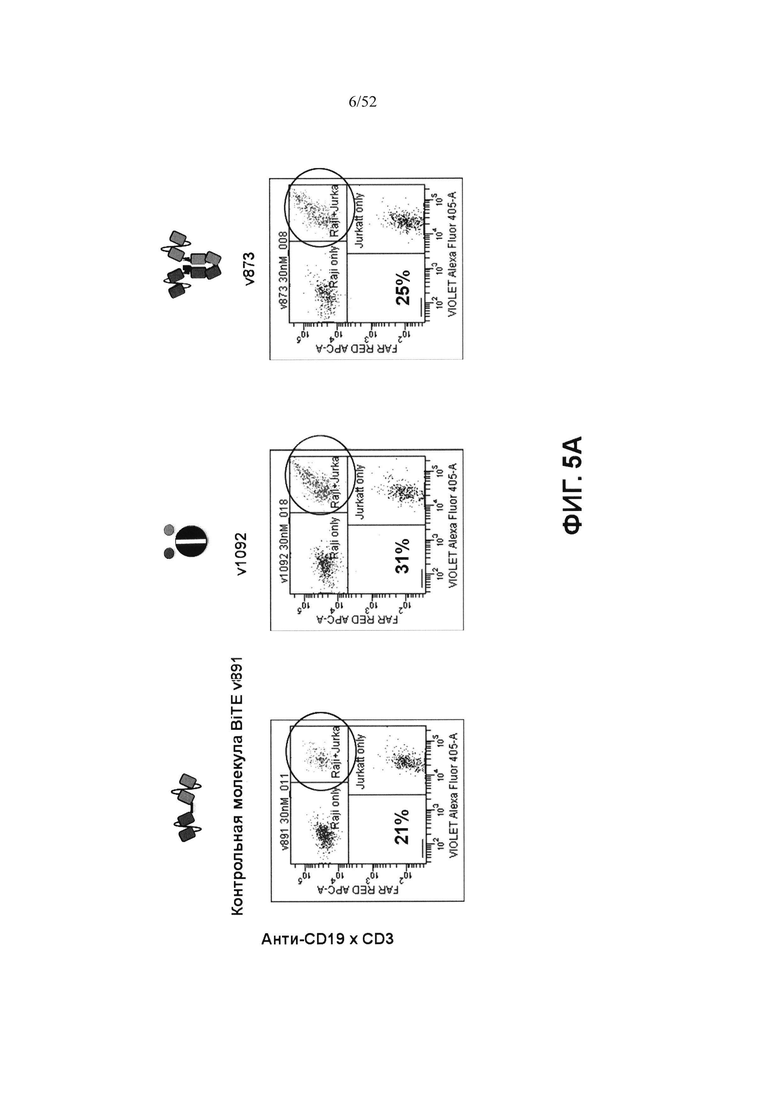

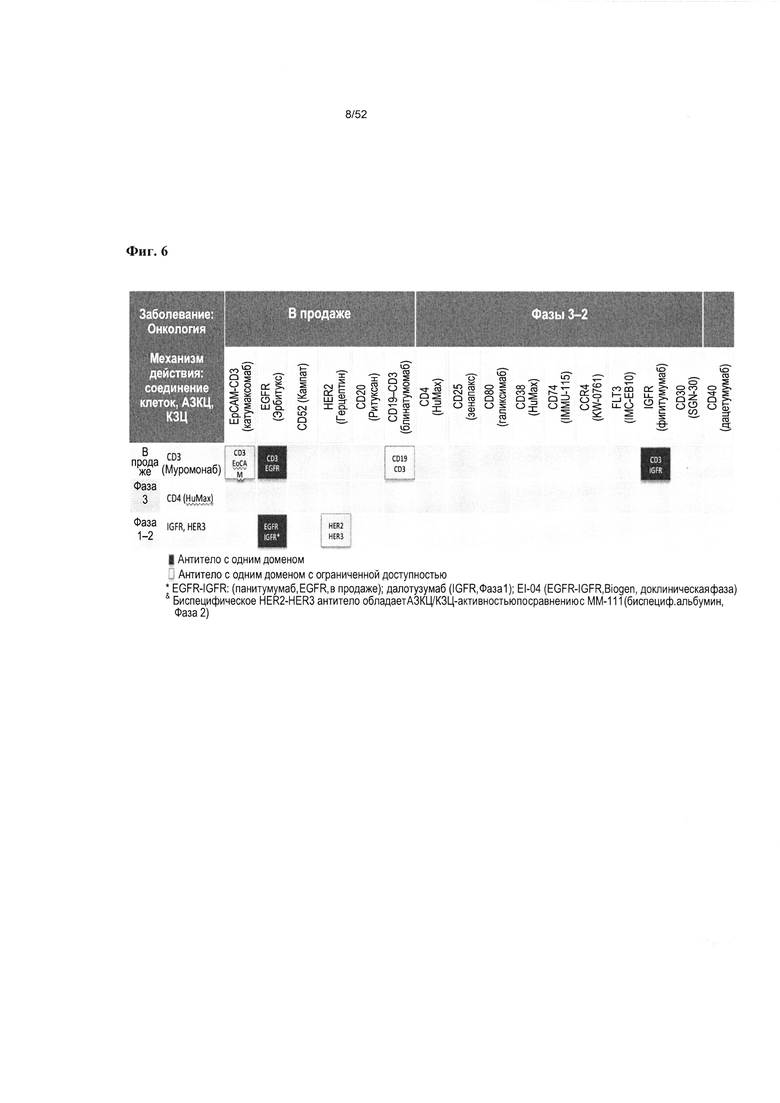

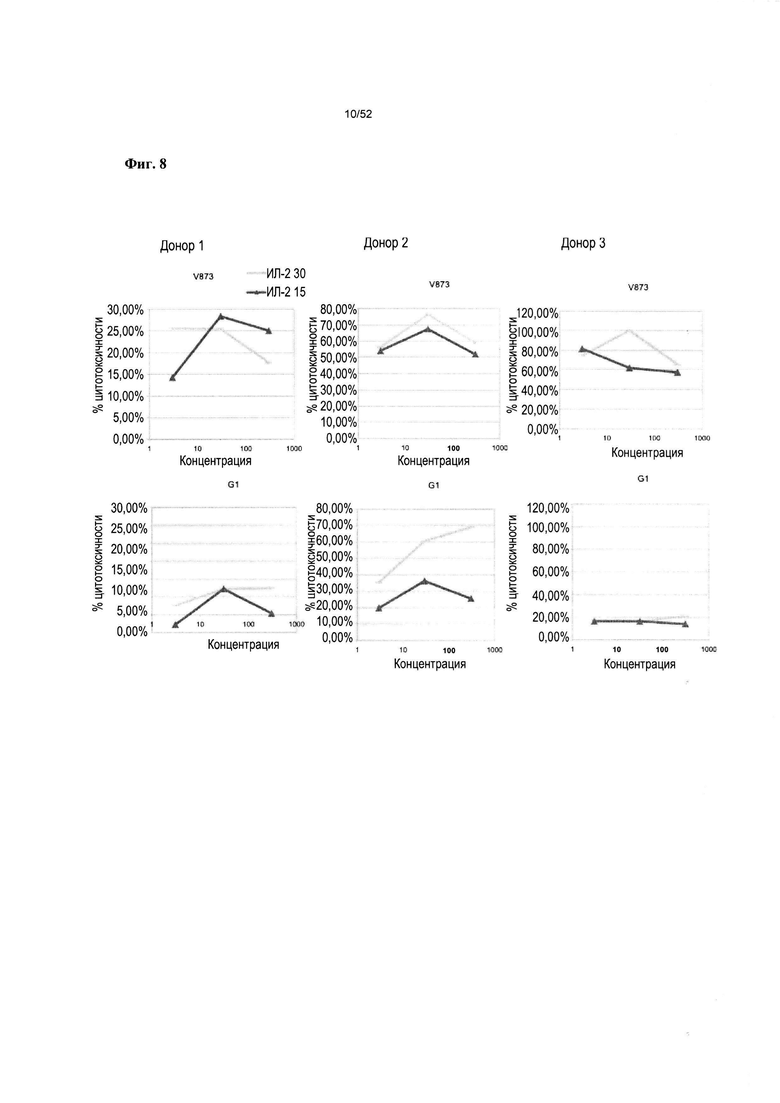
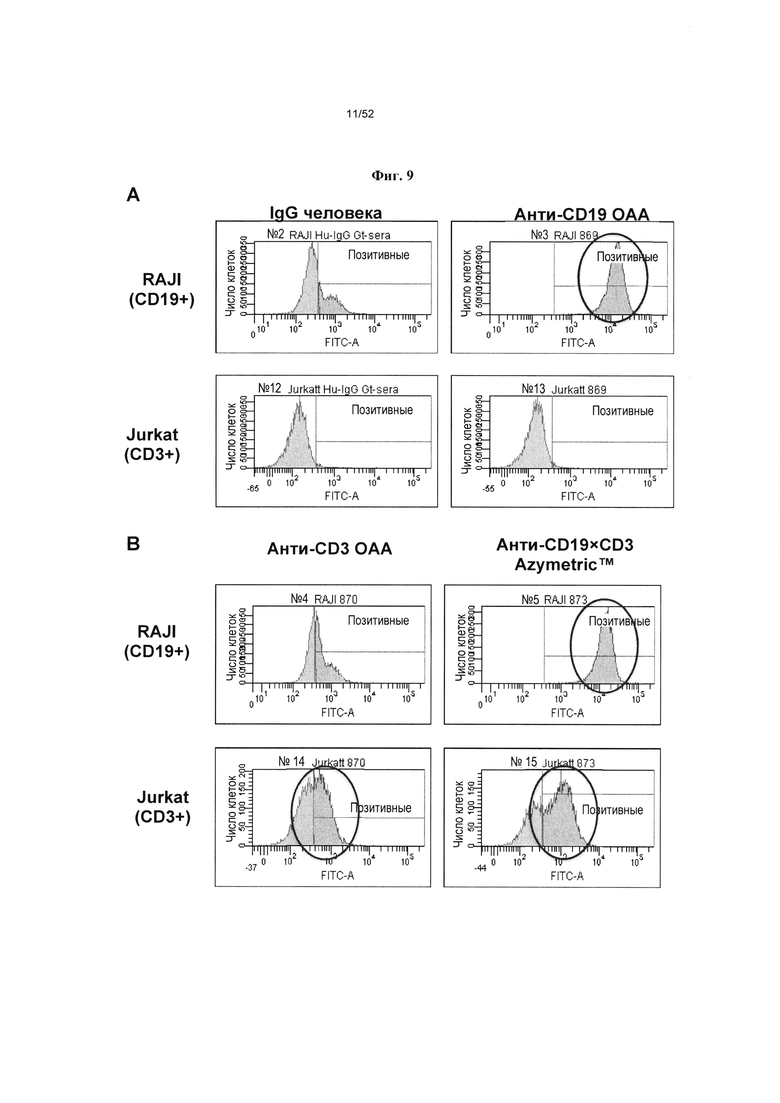
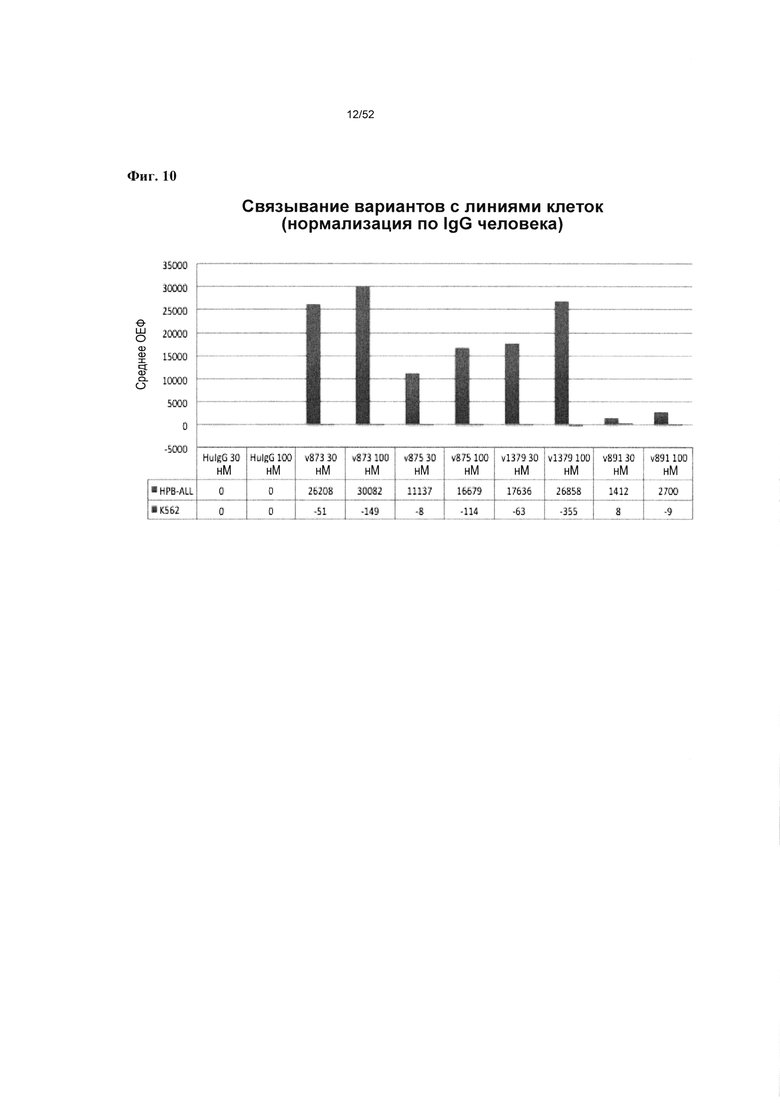
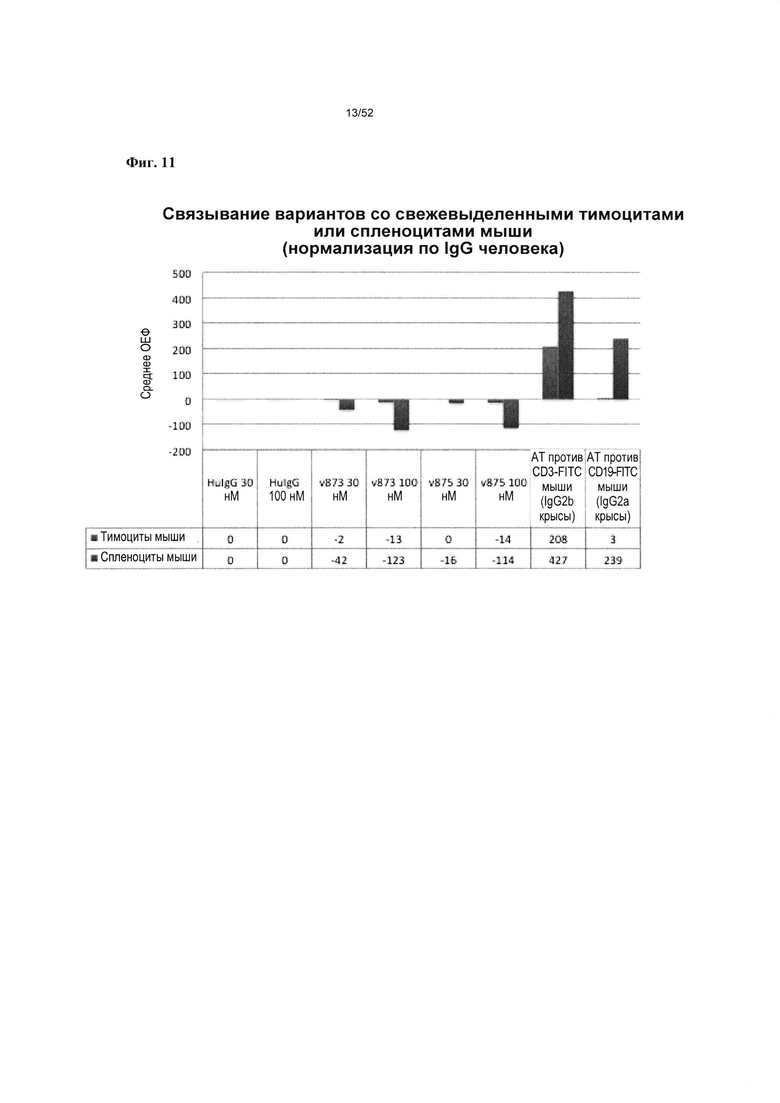
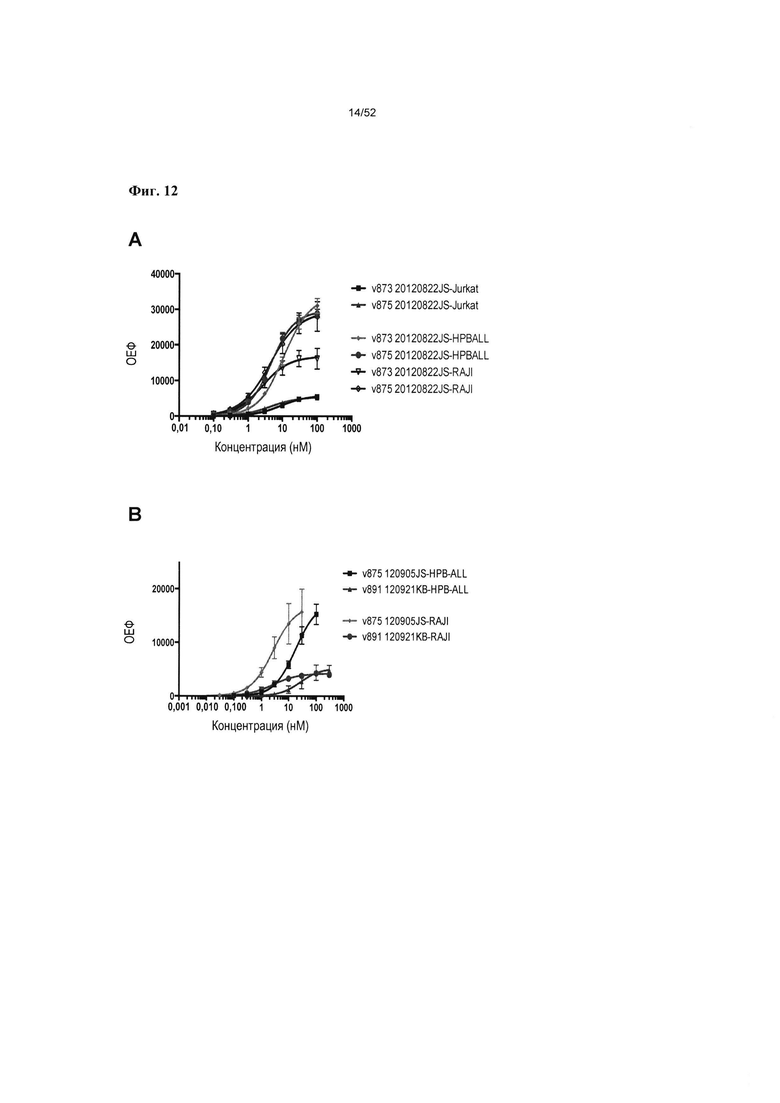
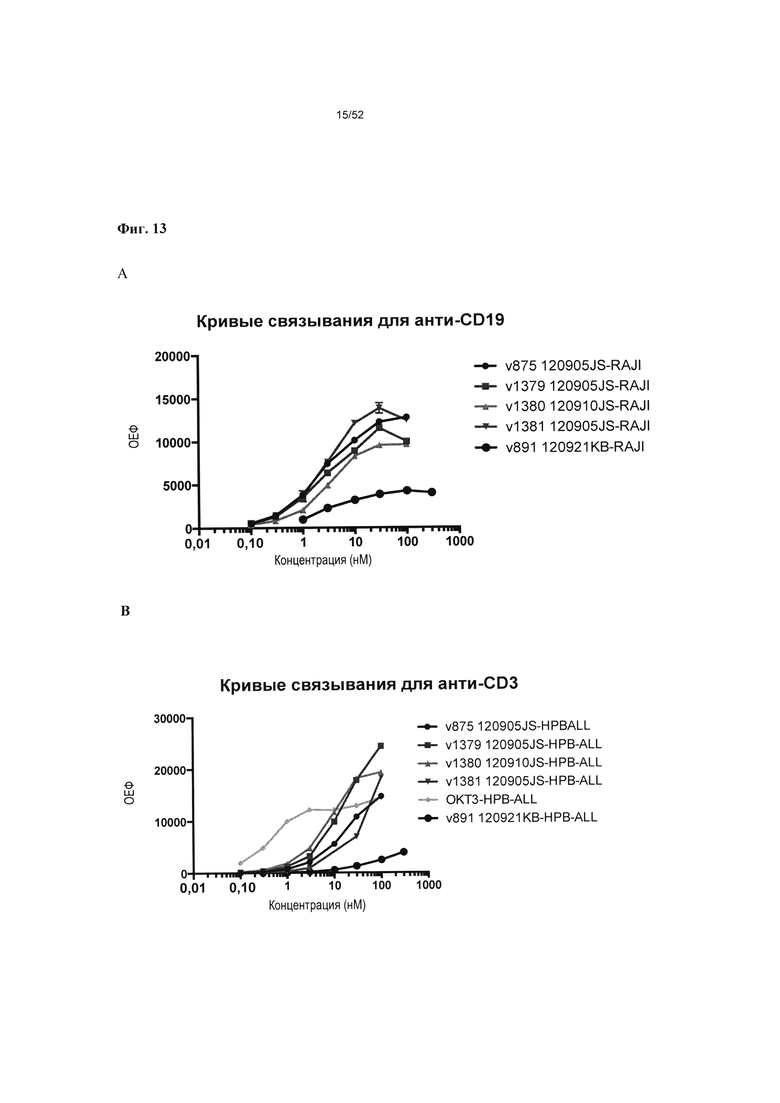
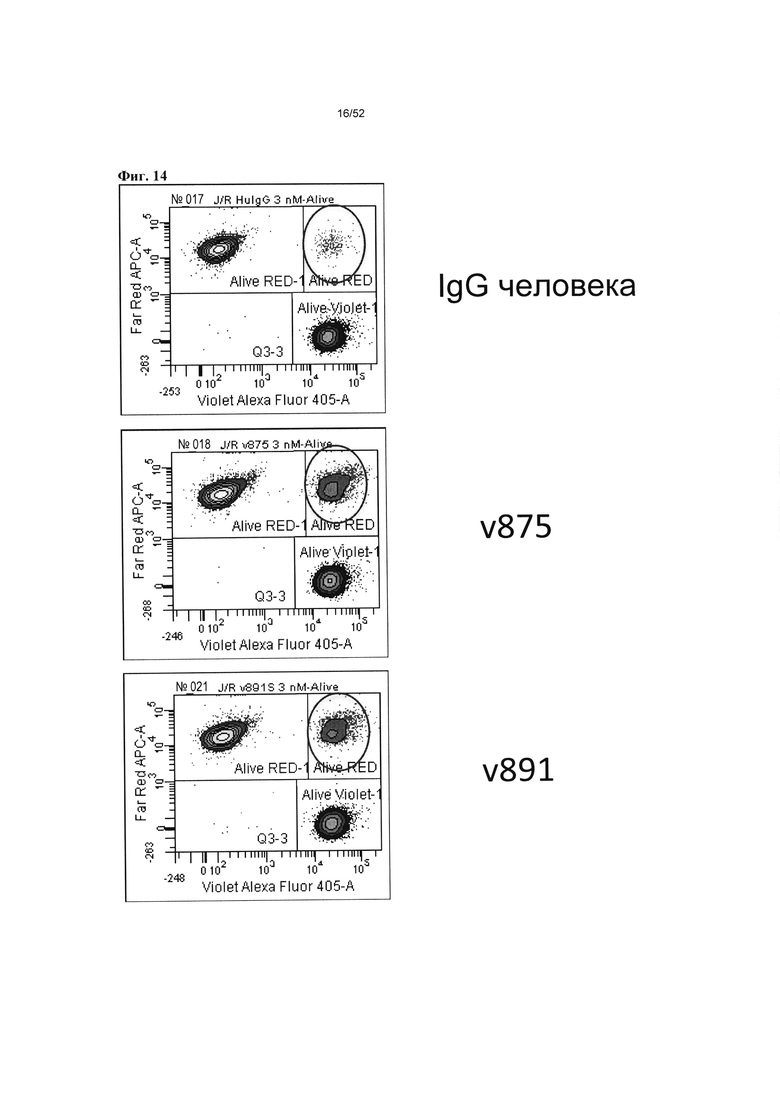
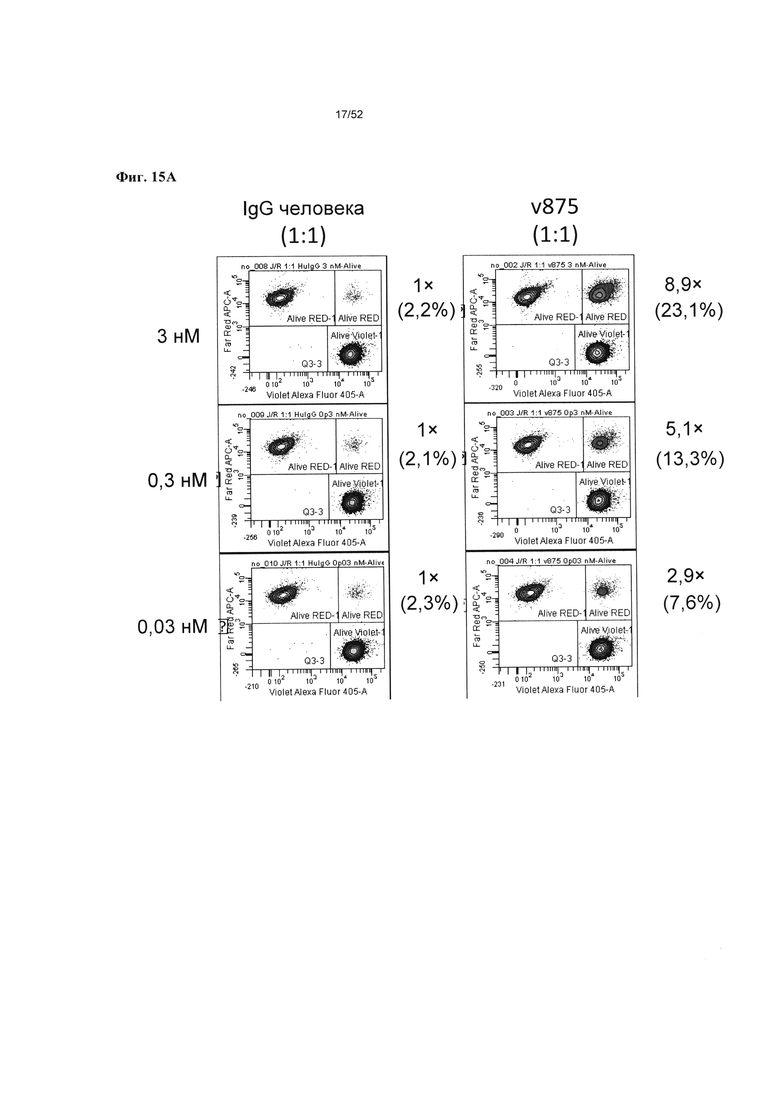
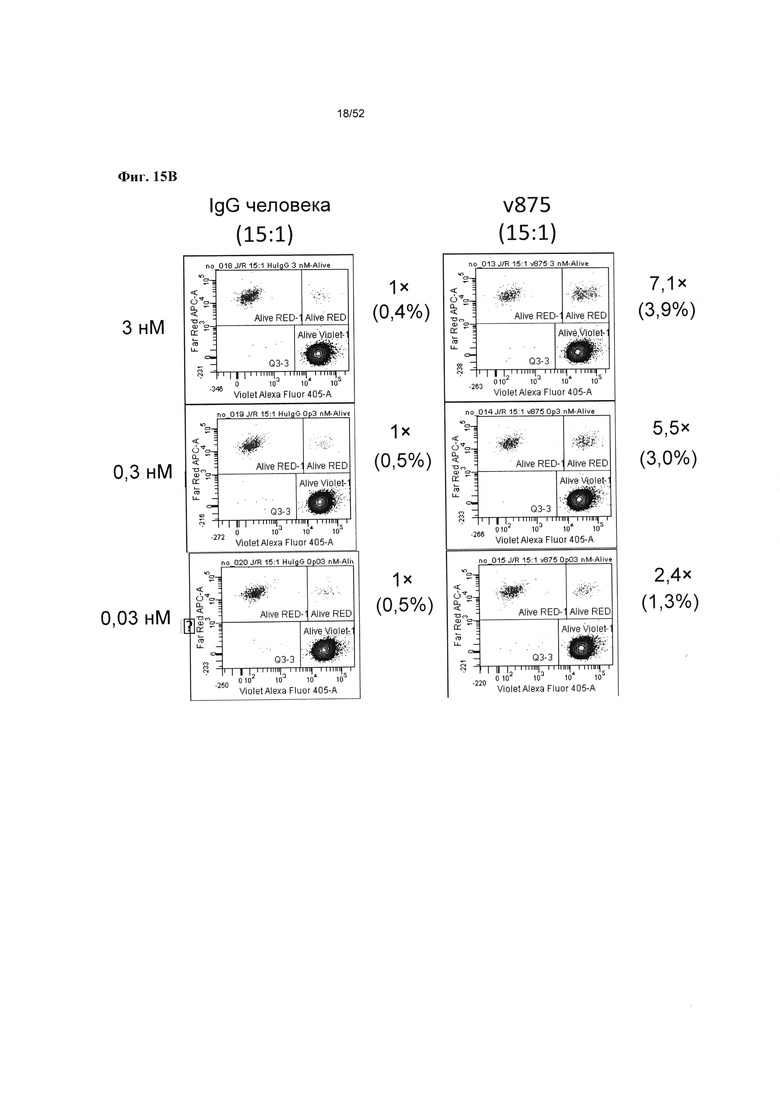
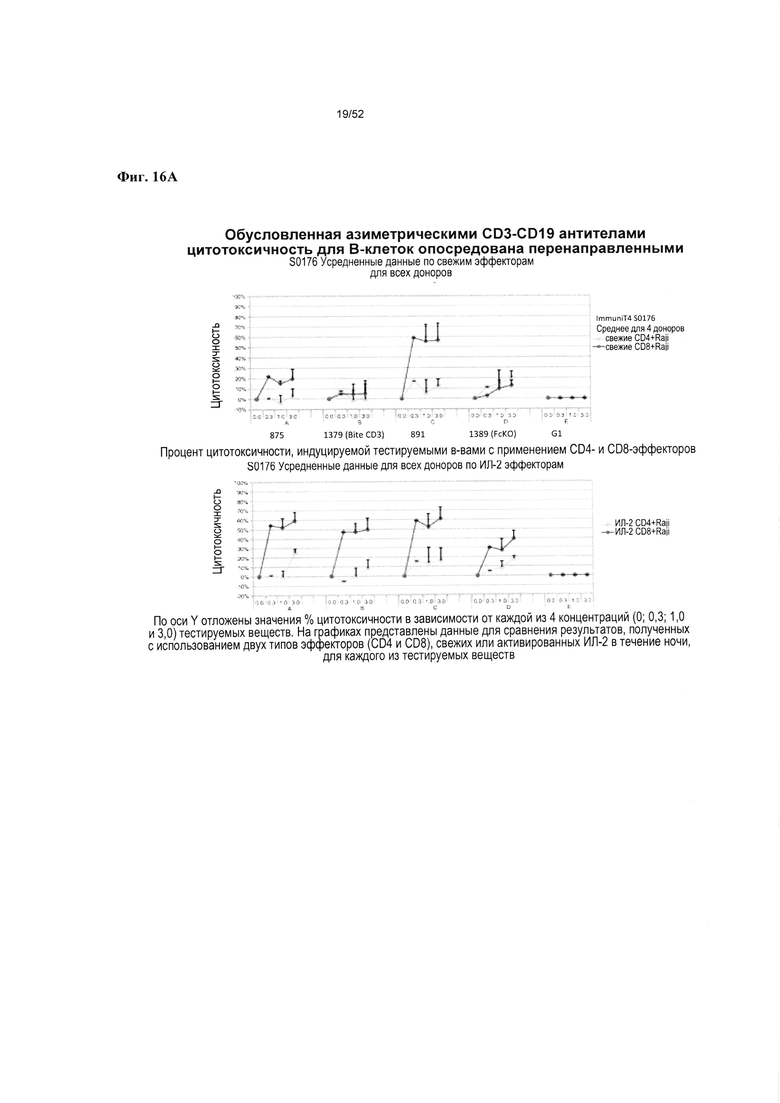
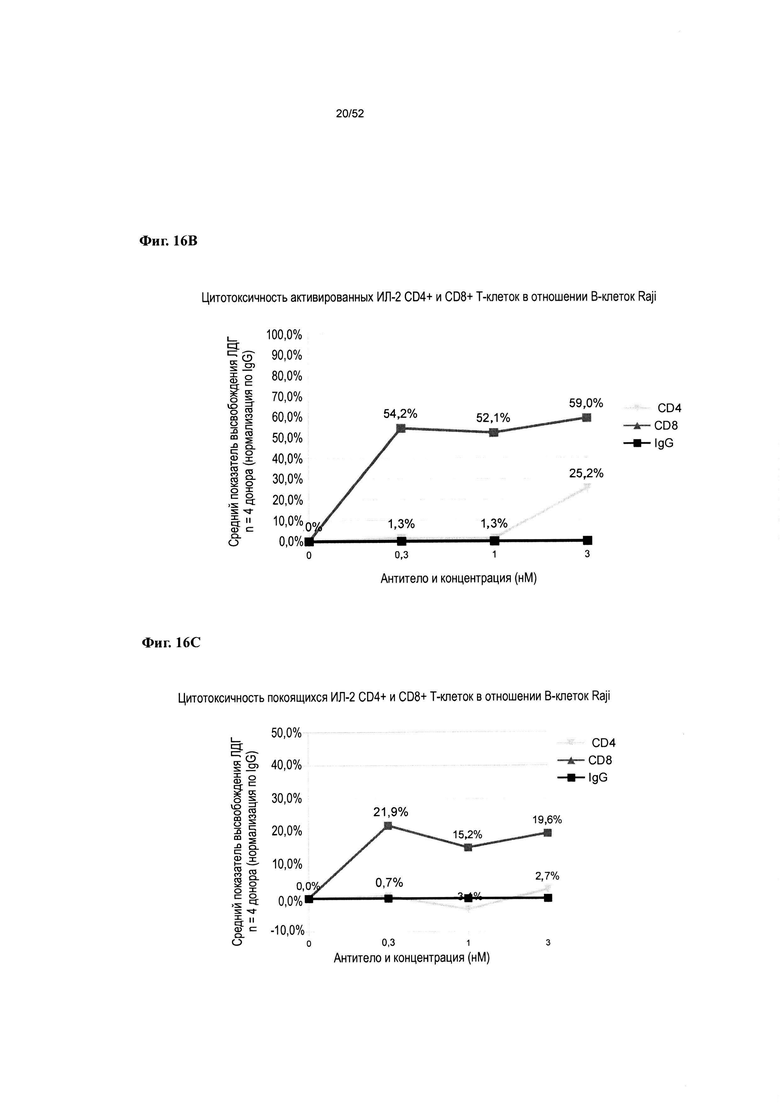
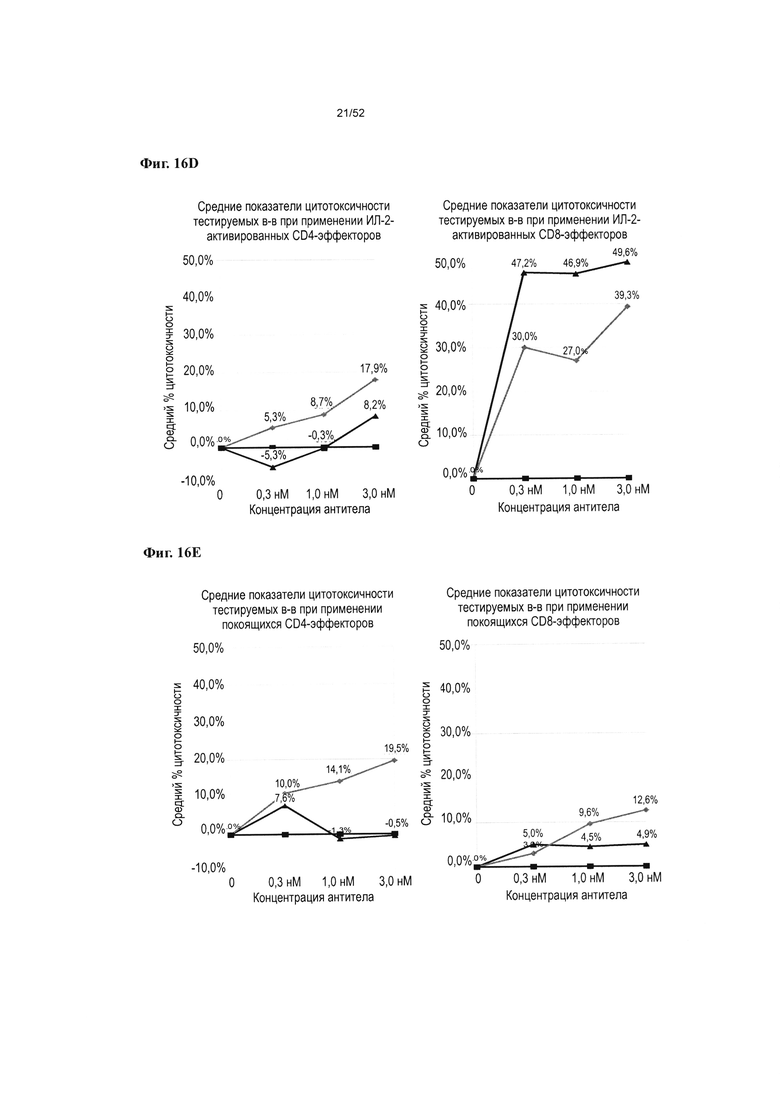
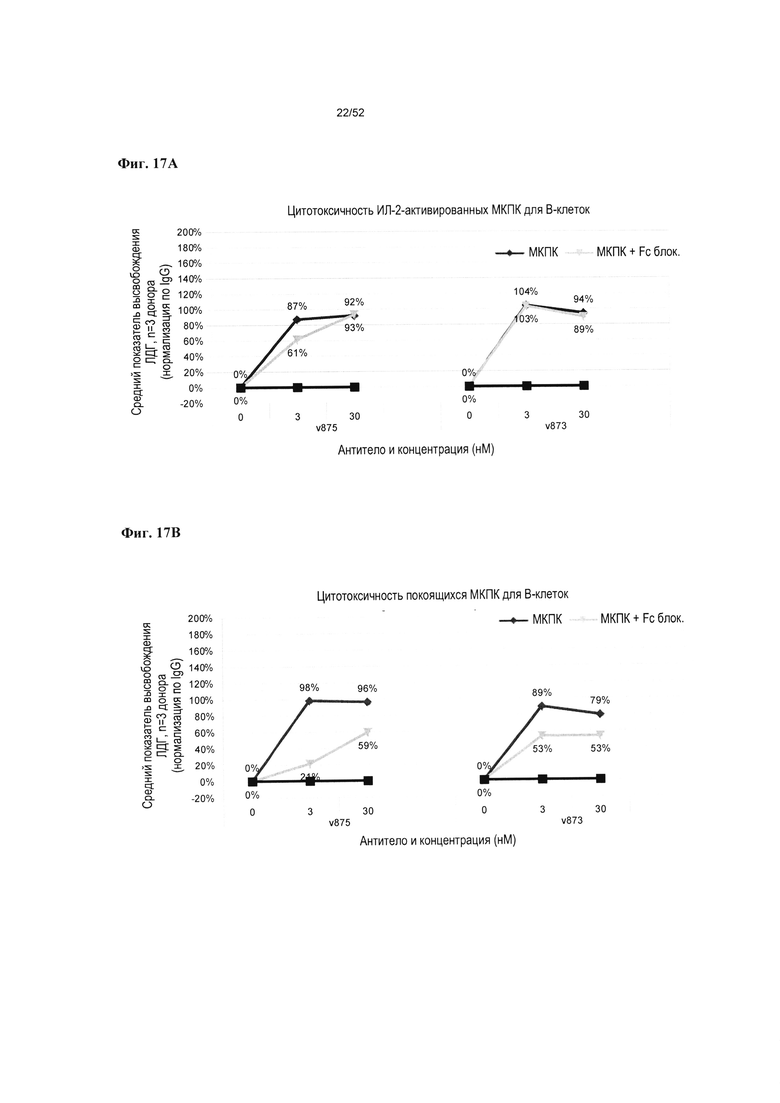
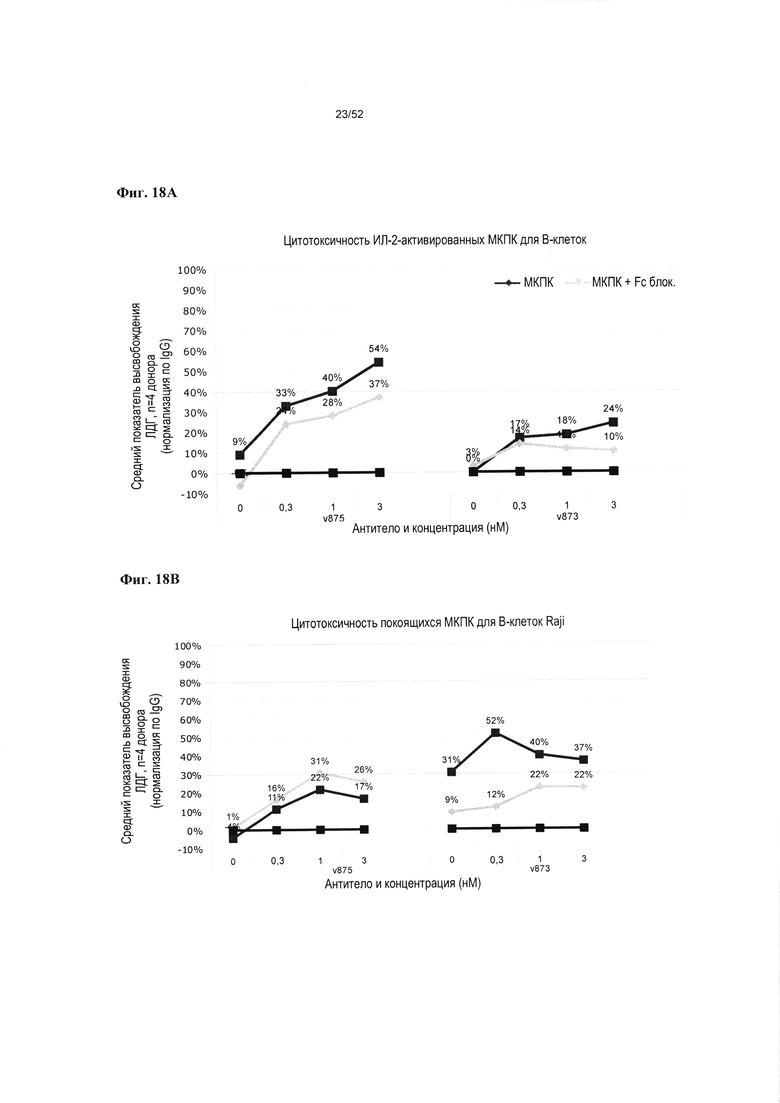
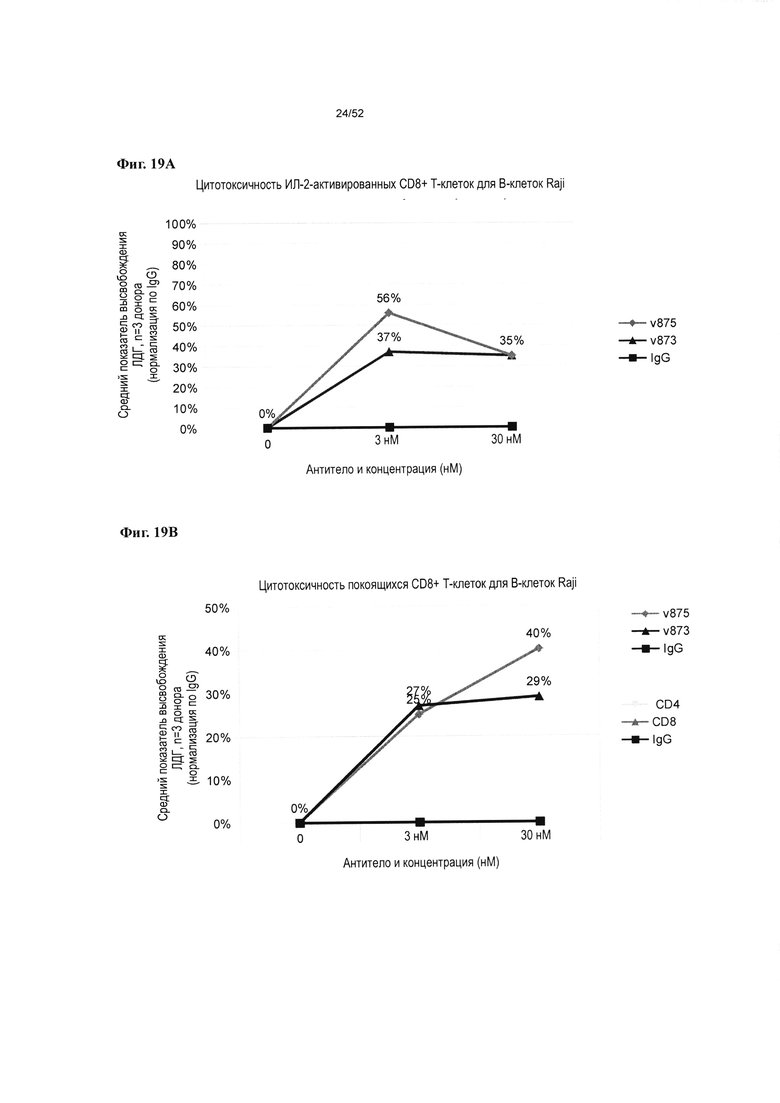
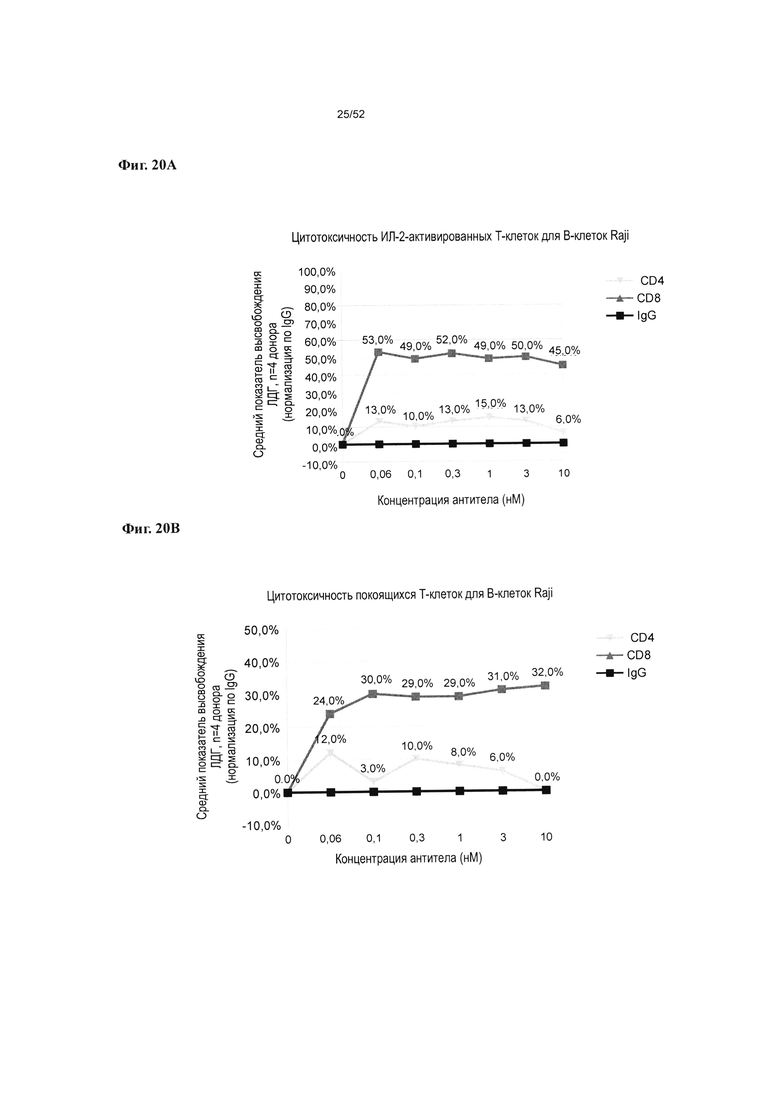
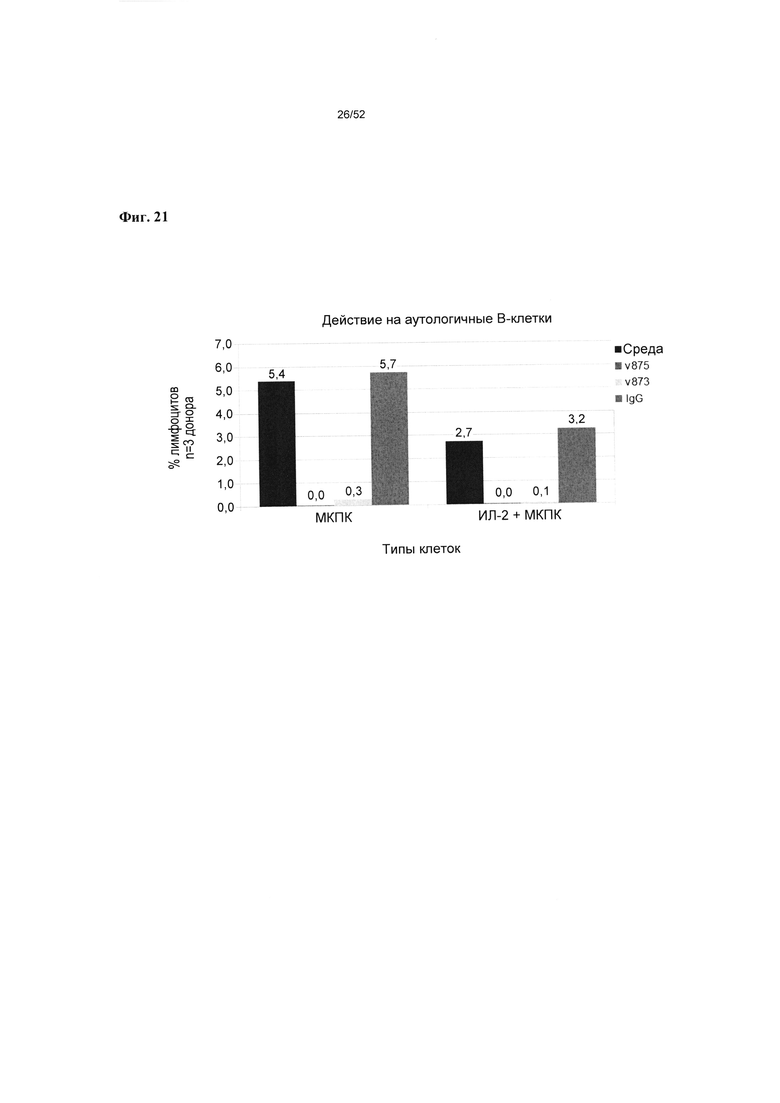

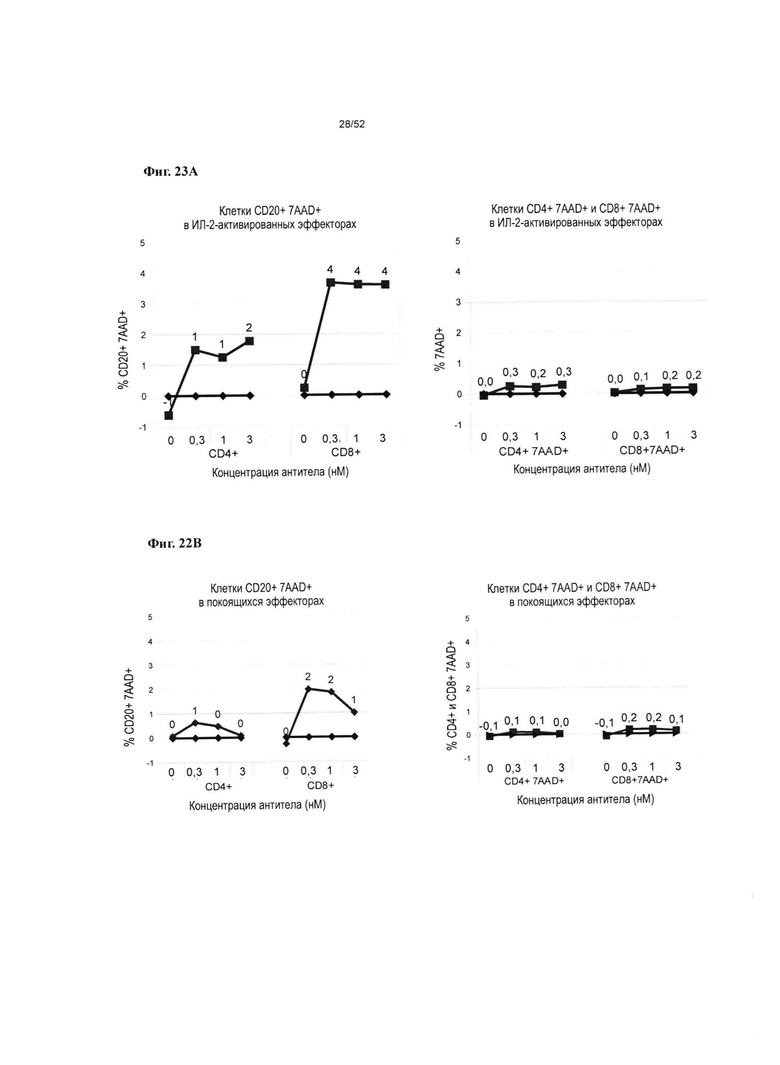
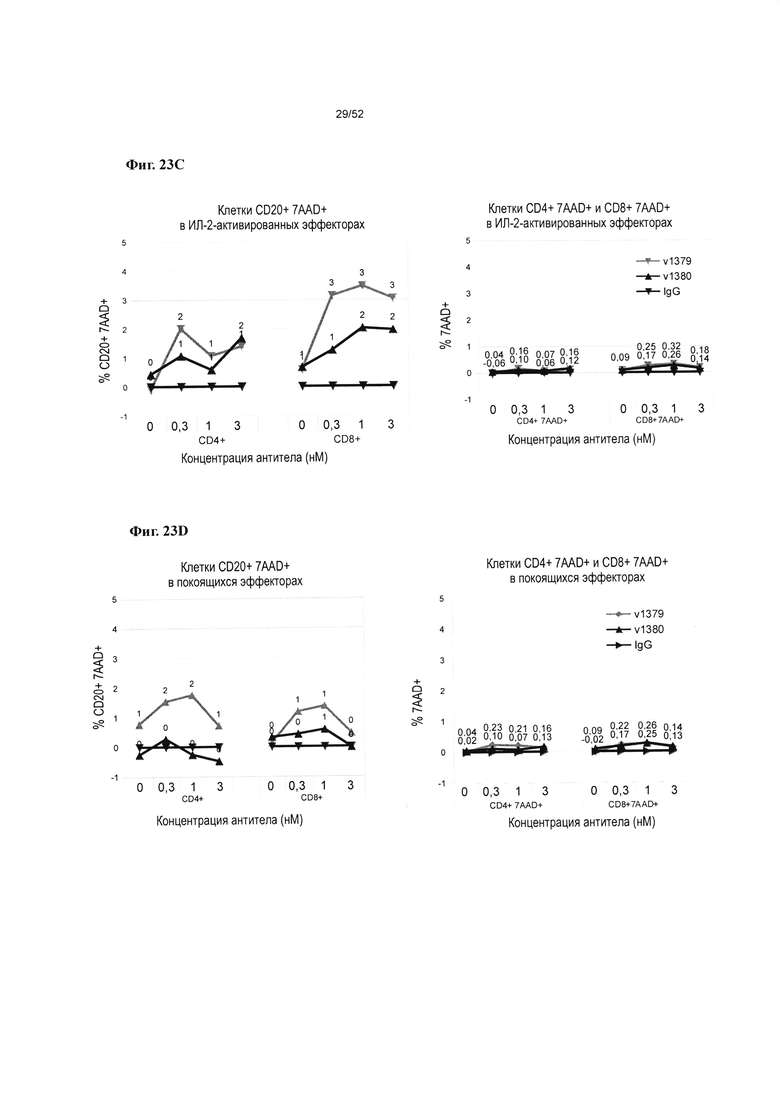
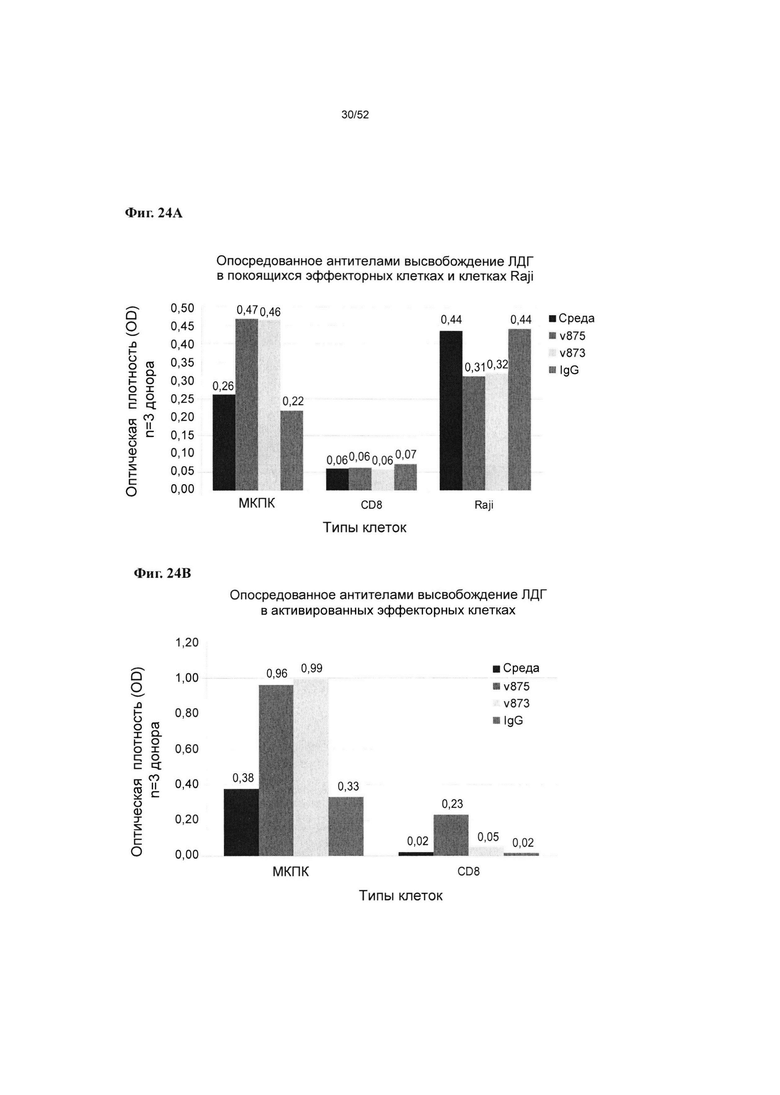
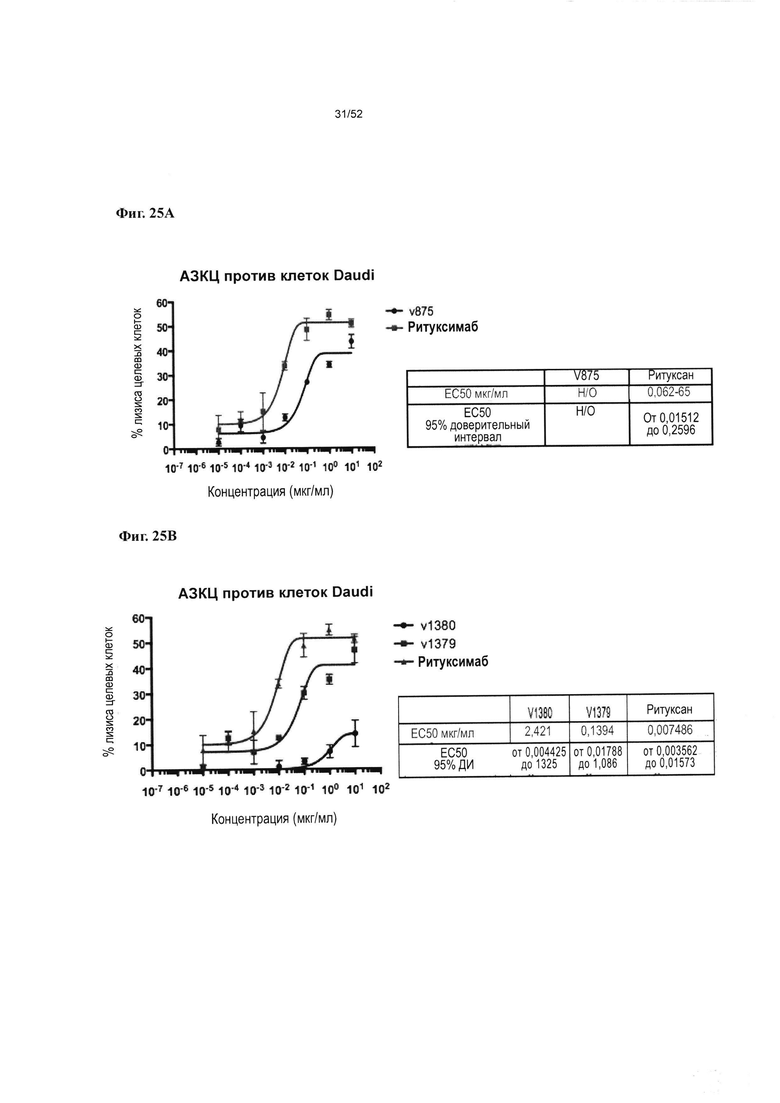
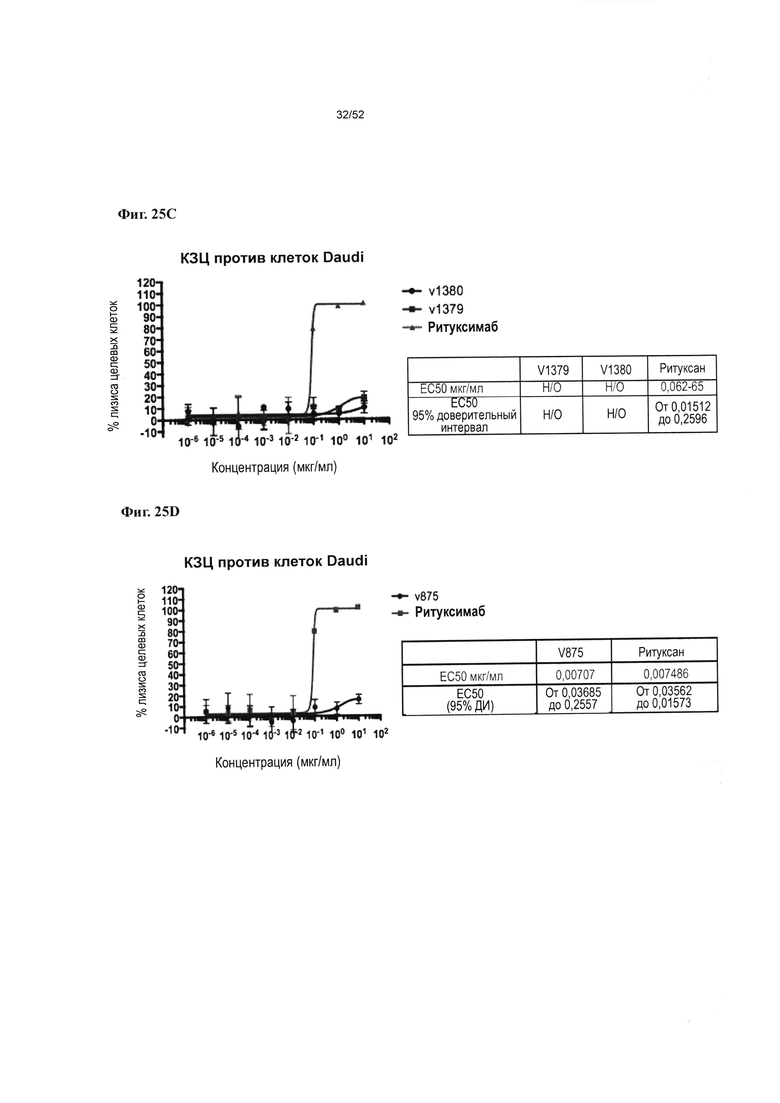
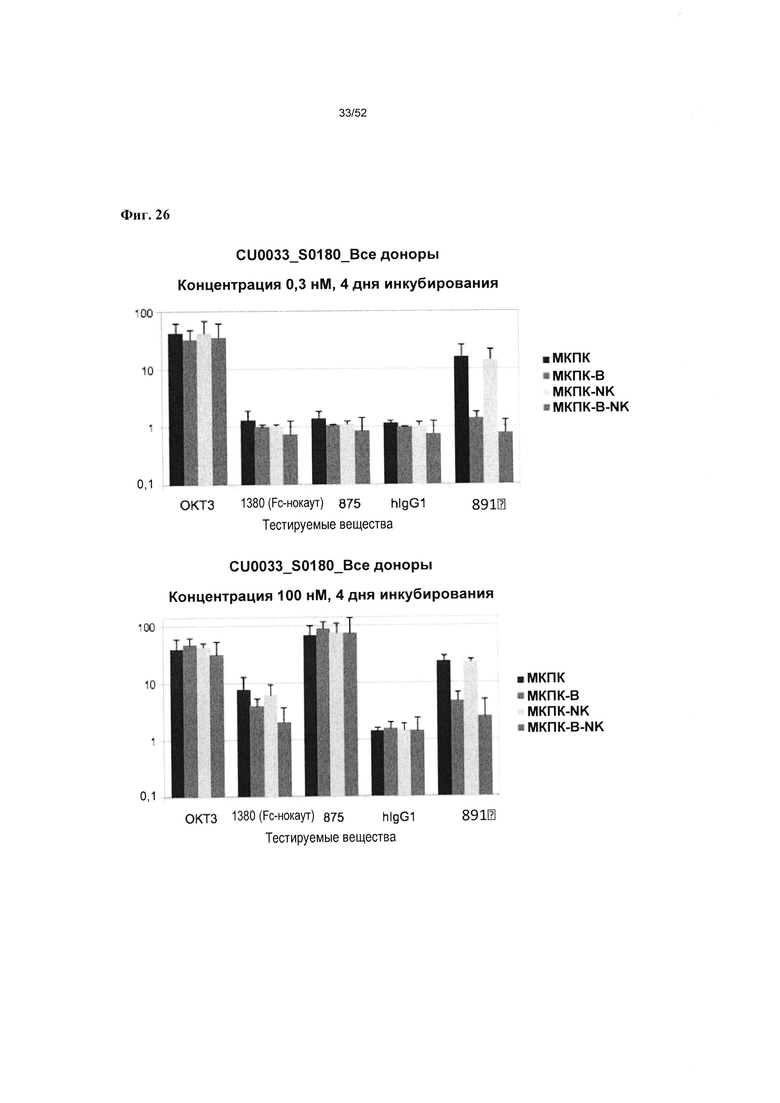

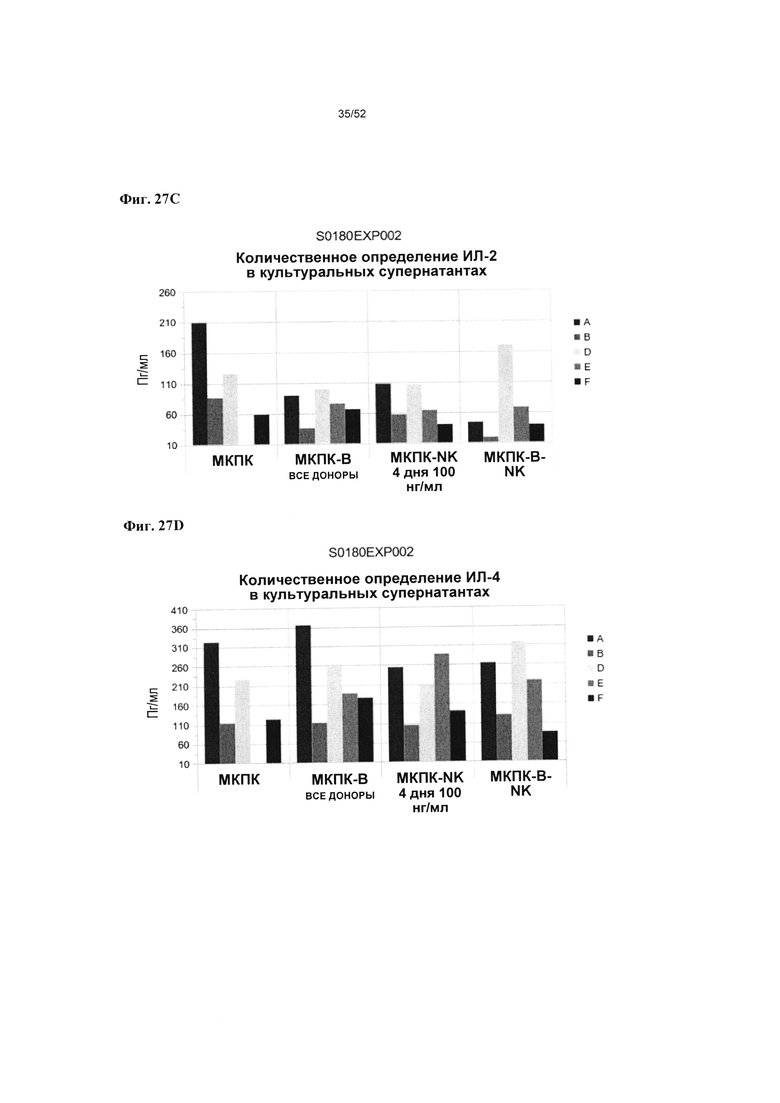
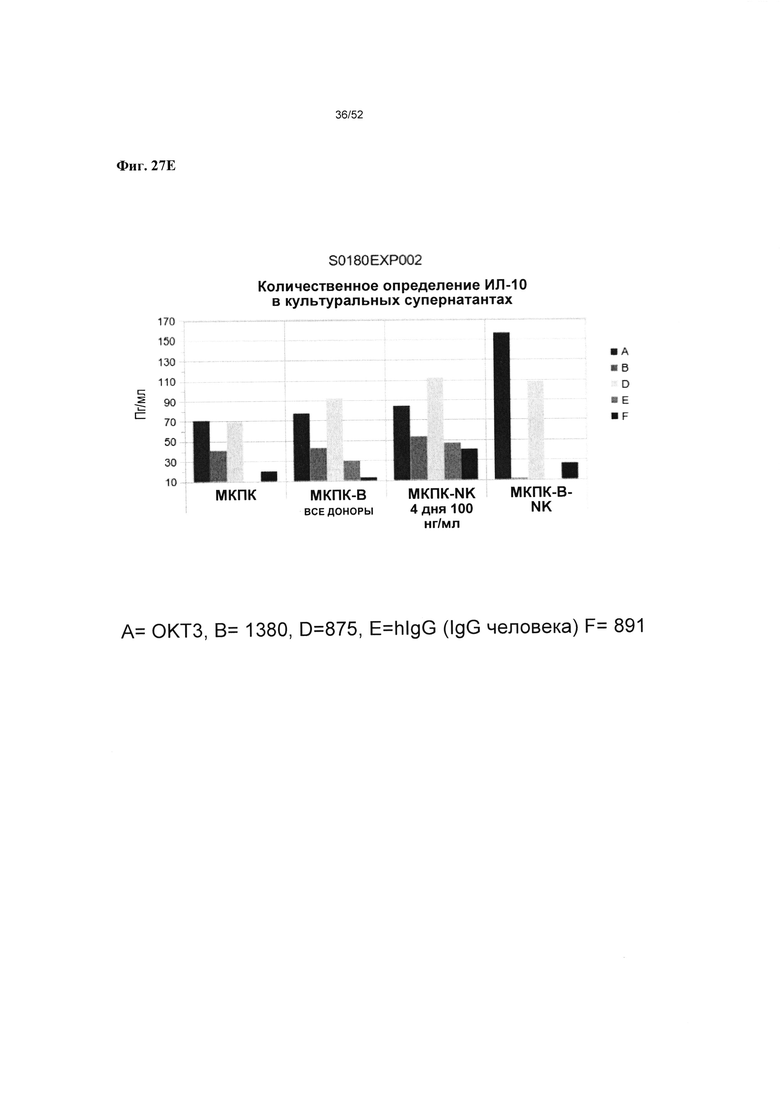
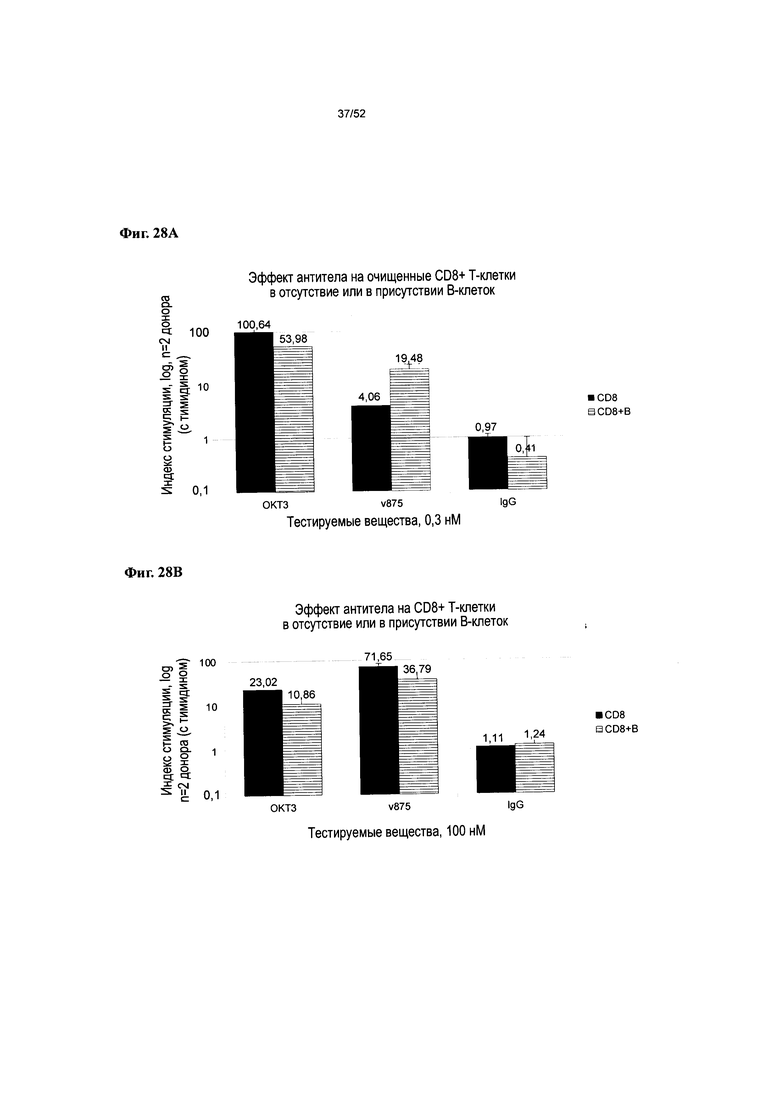
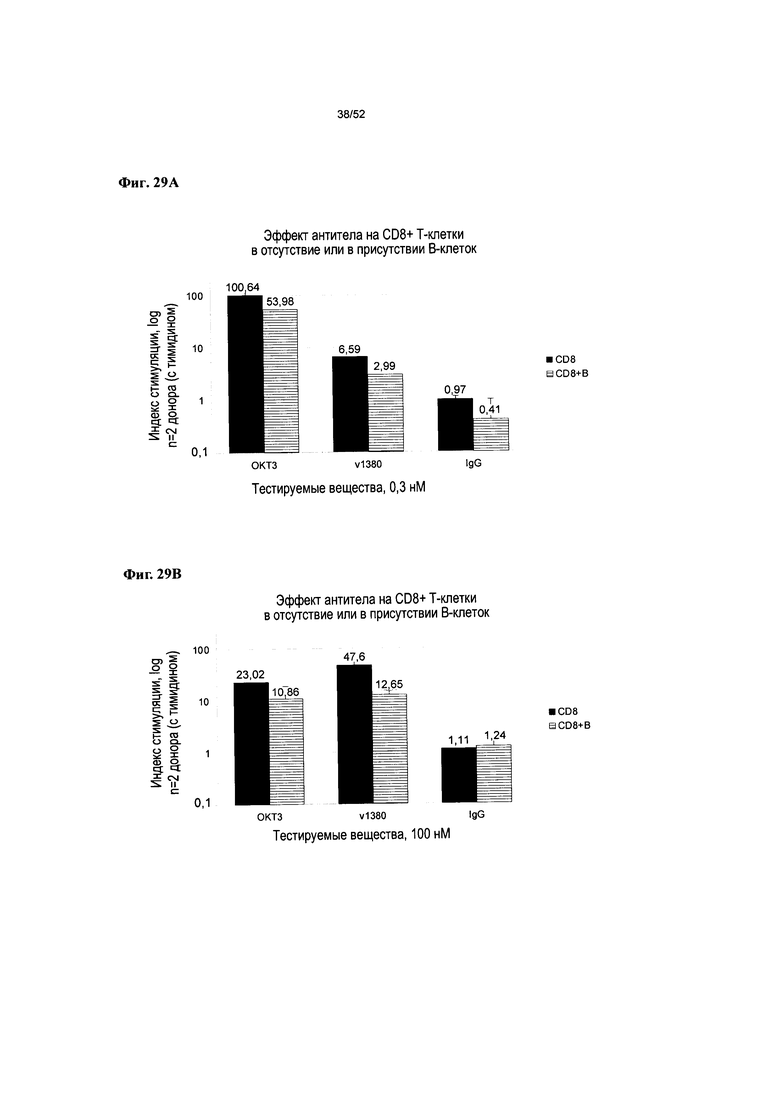
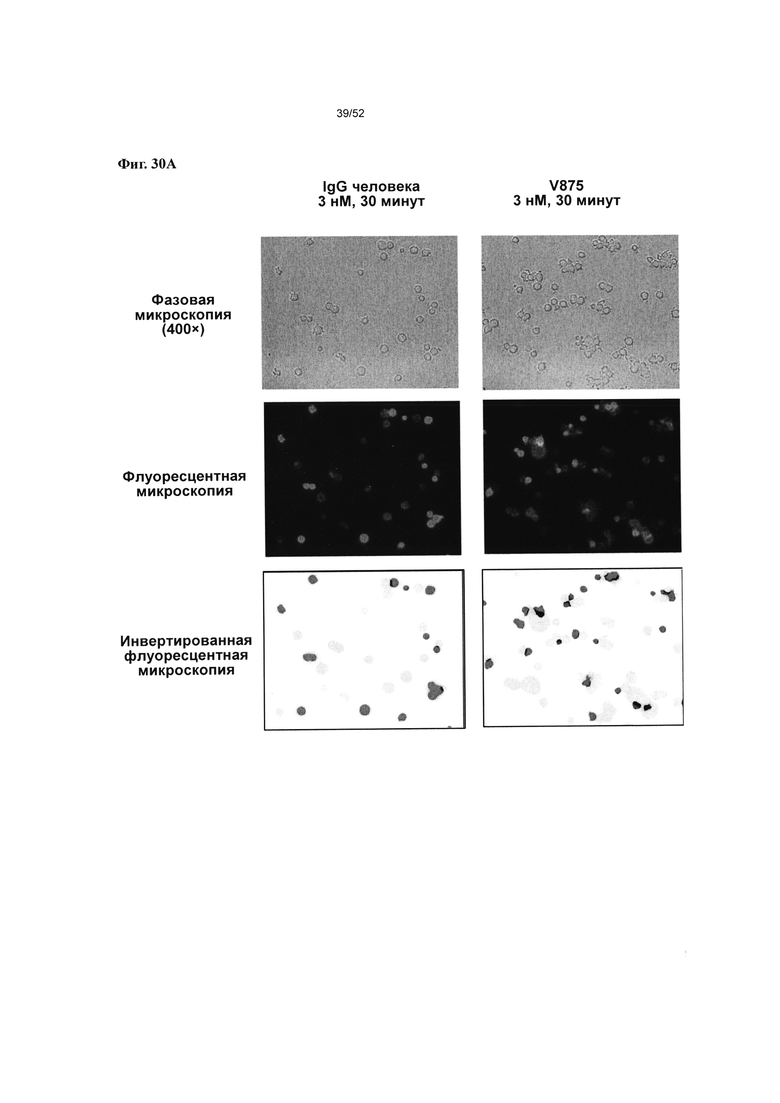
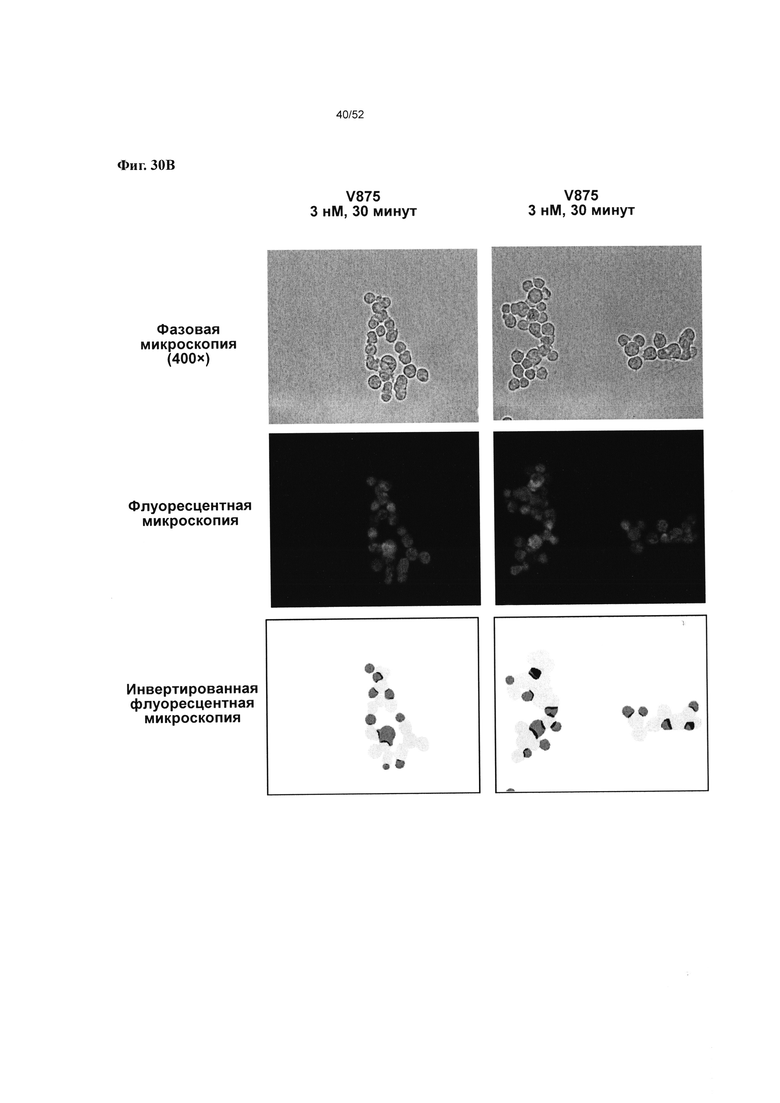
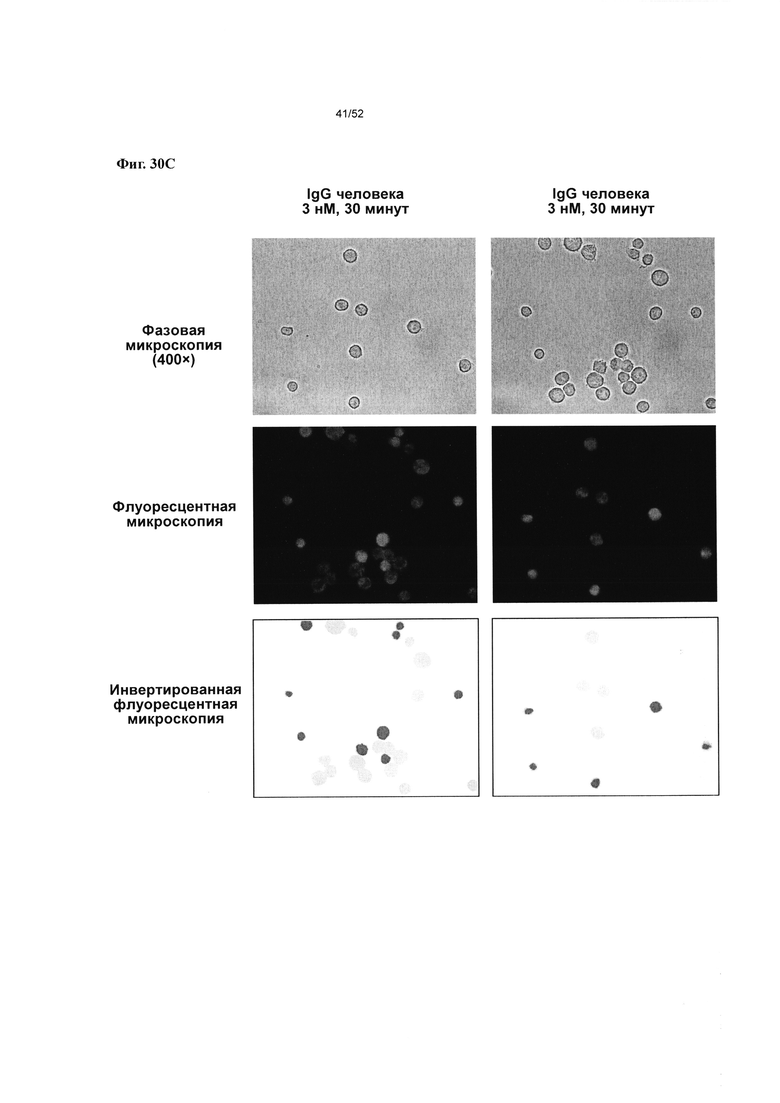
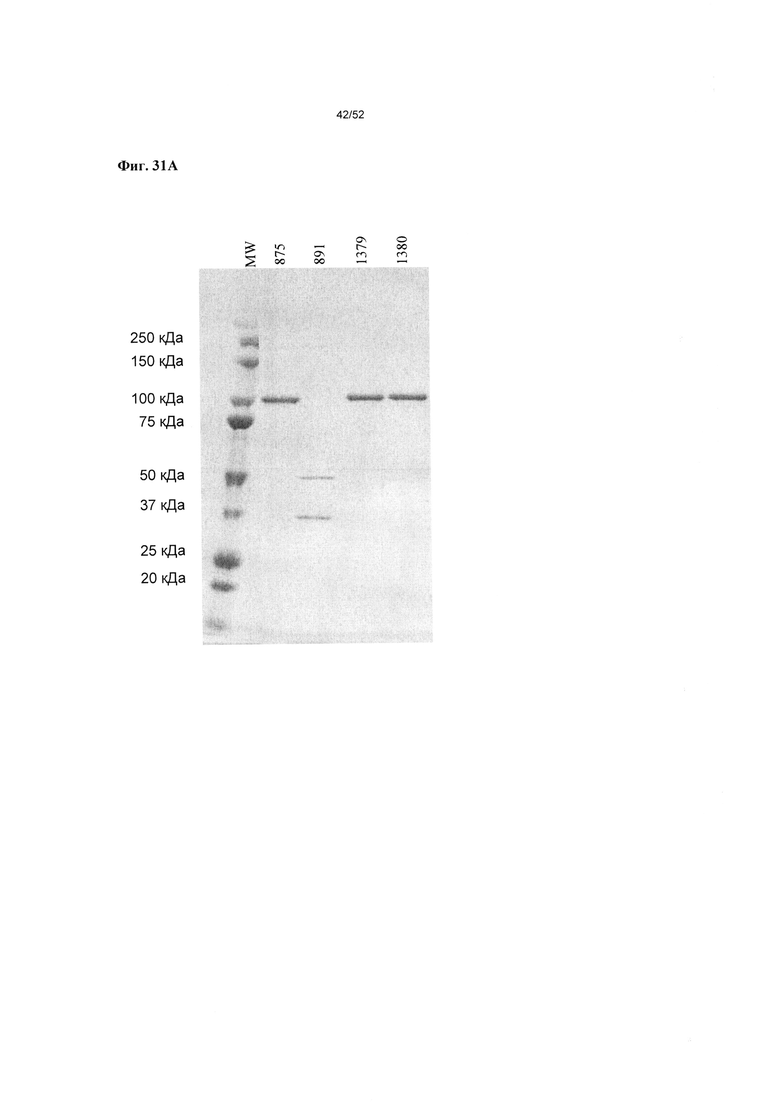
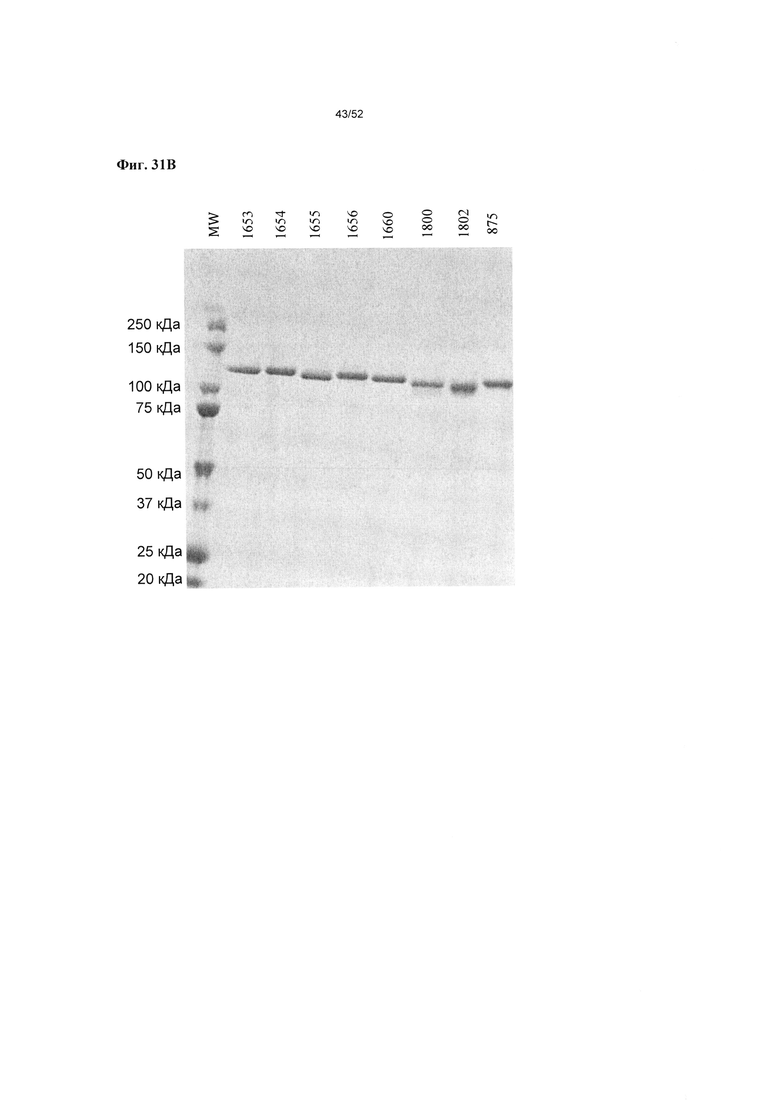
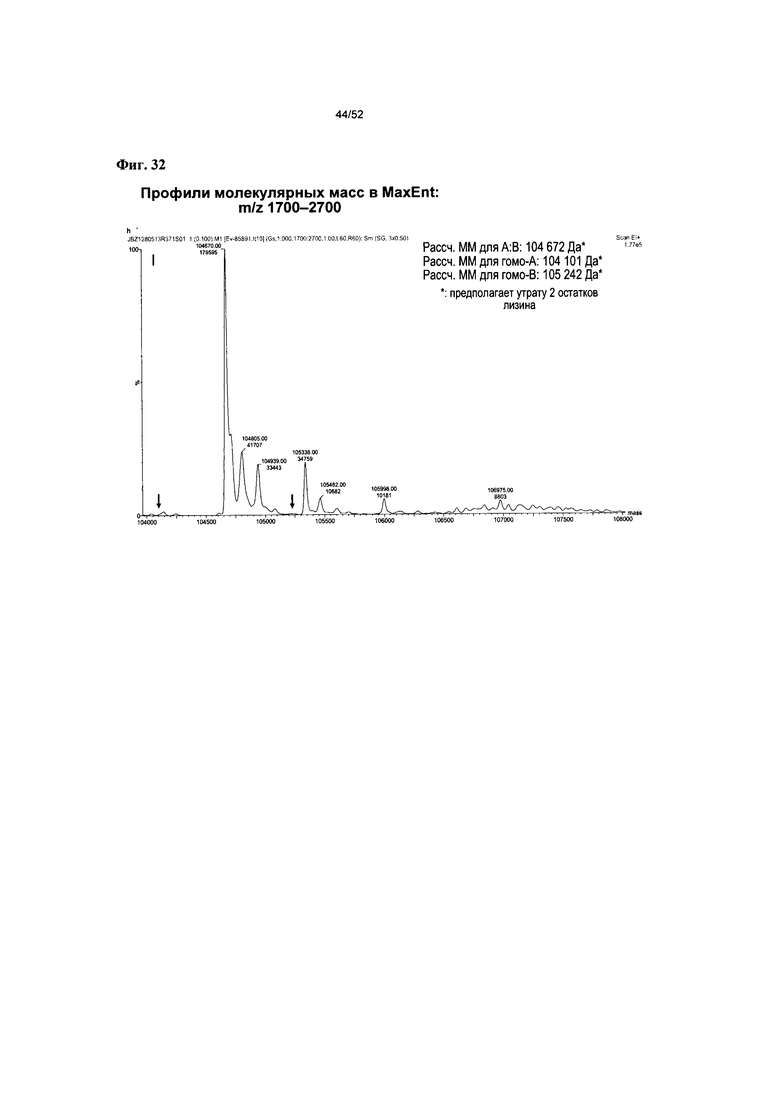
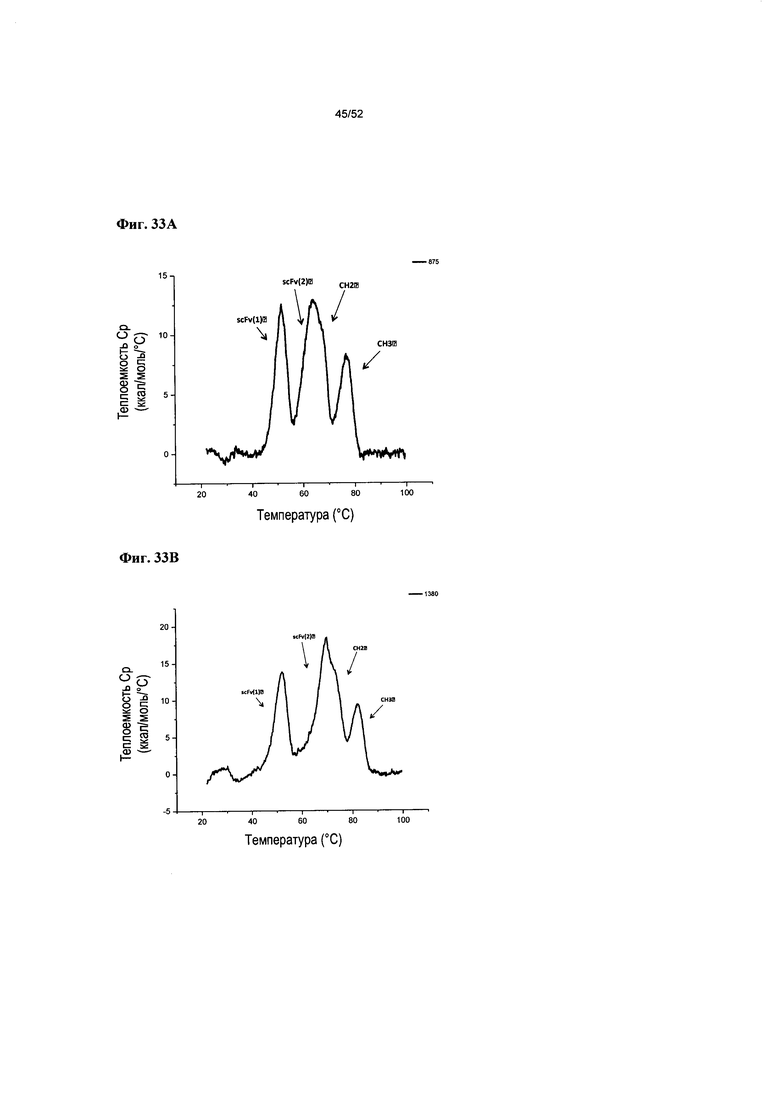
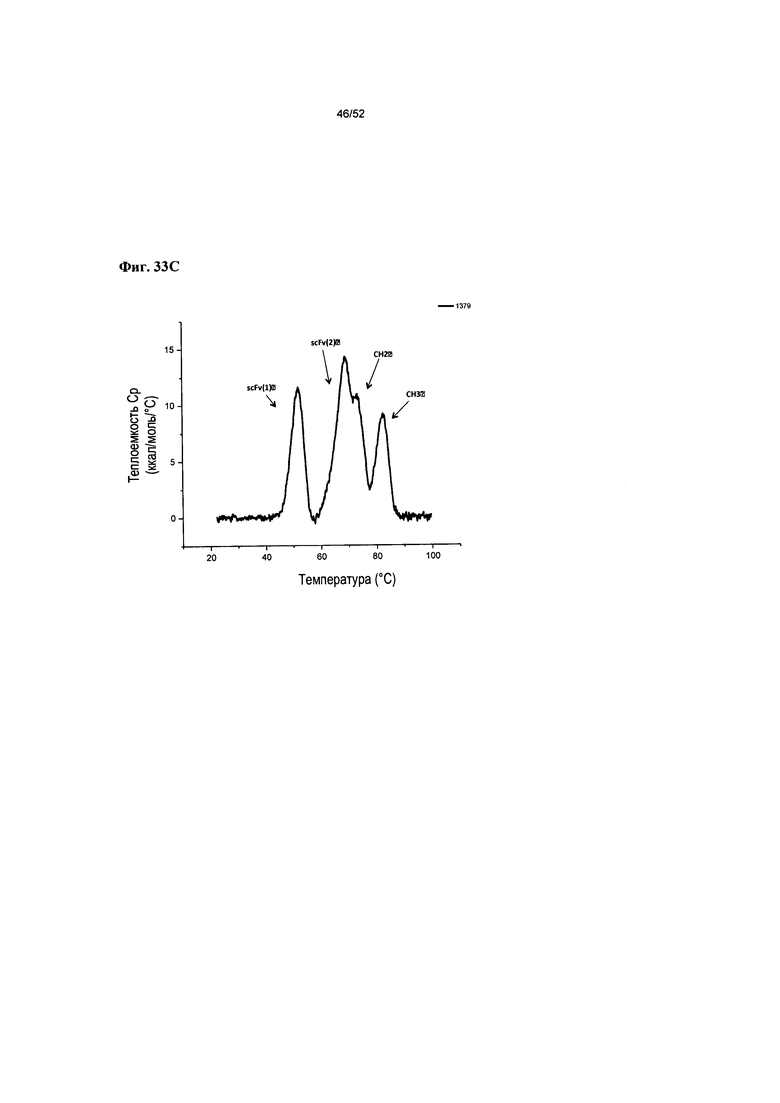
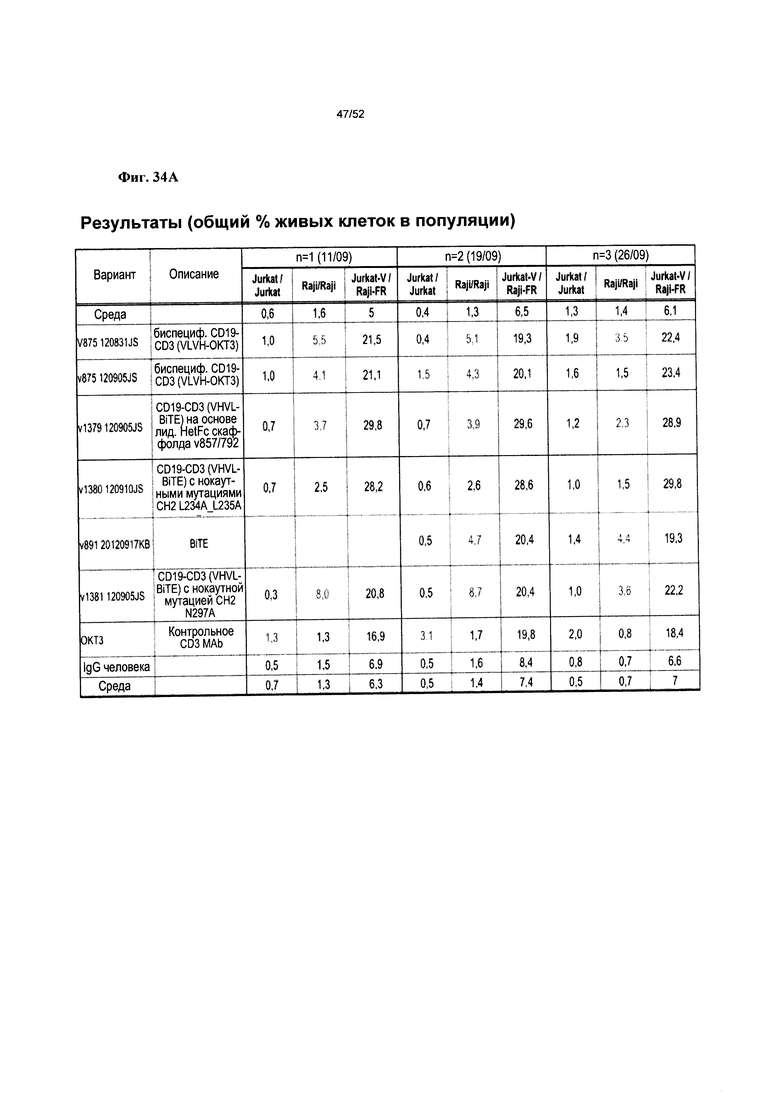
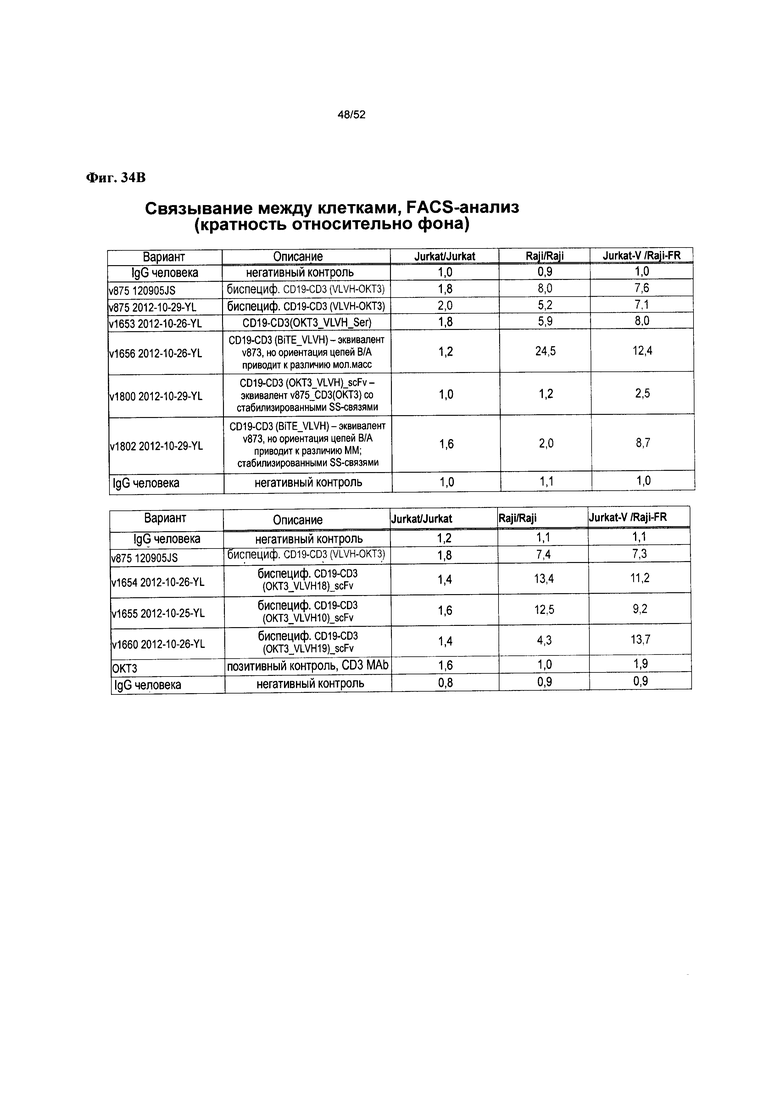
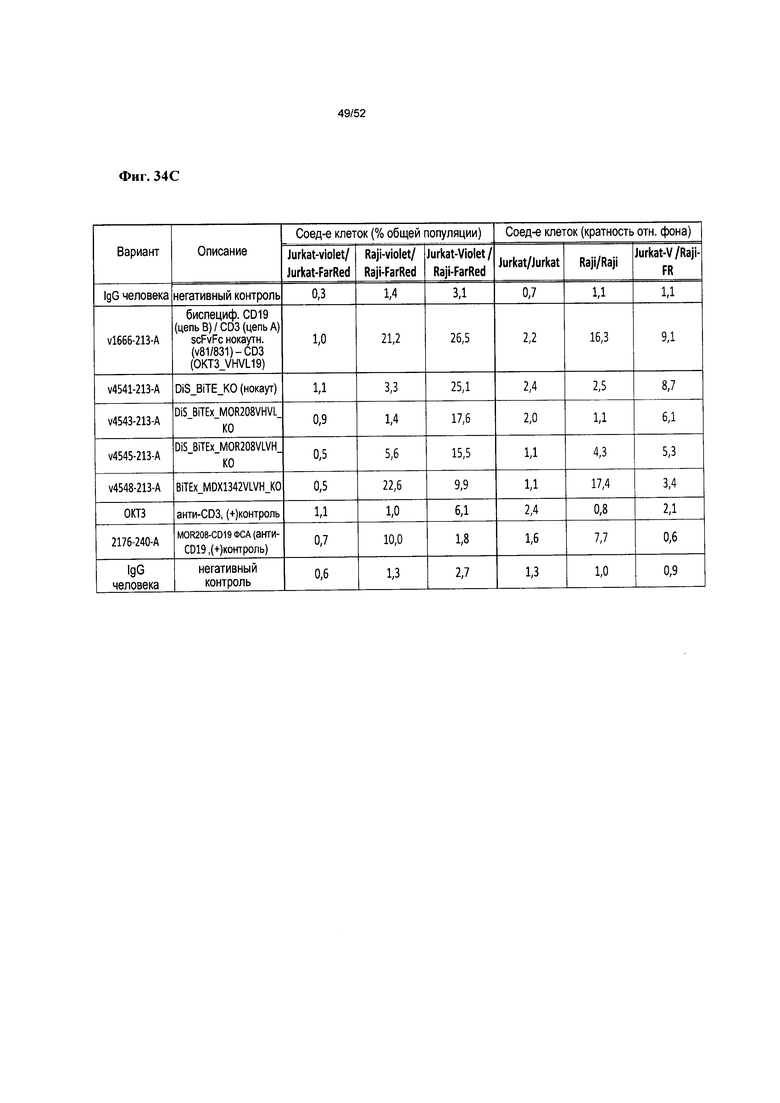
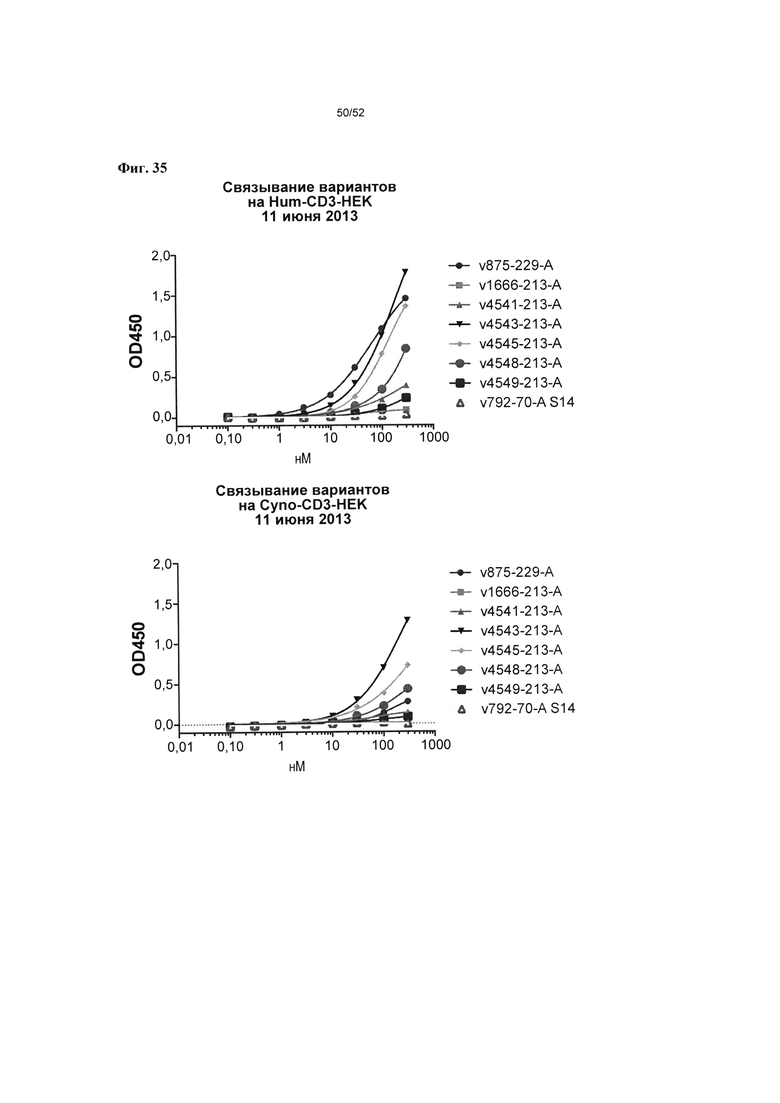

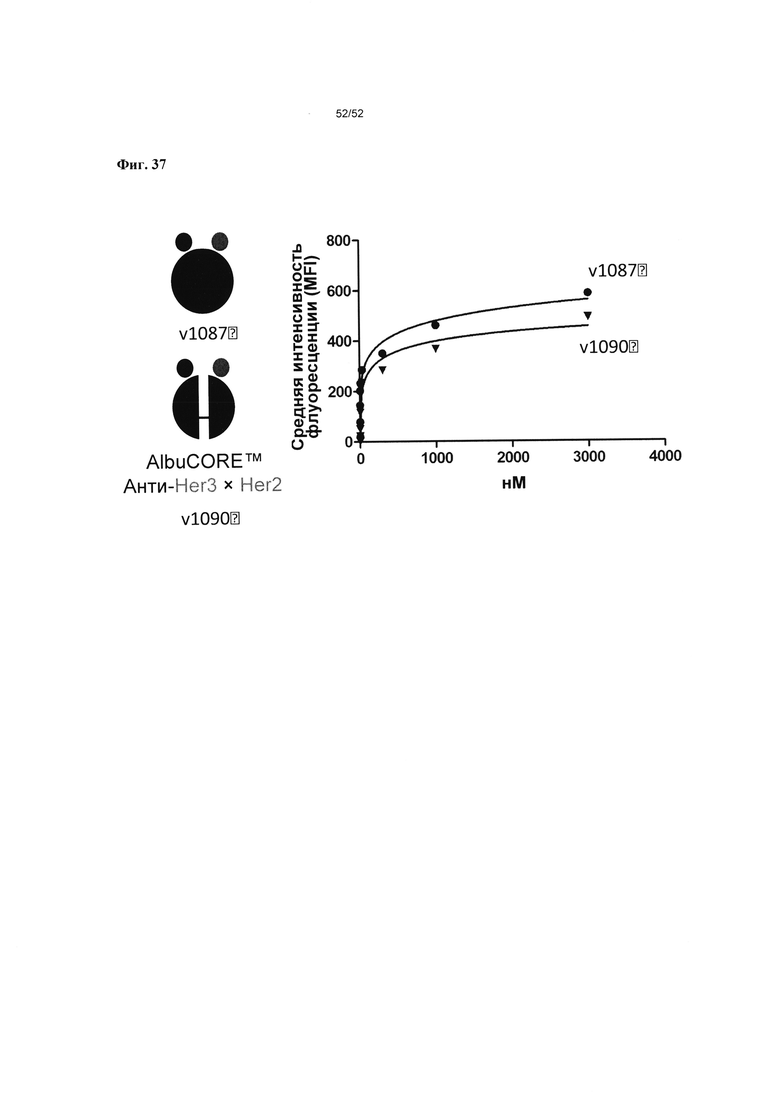
Изобретение относится к биотехнологии. Описана выделенная мультиспецифическая гетеромультимерная конструкция для индуцирования киллинга В-клетки, содержащая: первую полипептидную конструкцию, содержащую CD3-связывающую полипептидную конструкцию, которая связывается с комплексом человека CD3 по меньшей мере на одной экспрессирующей CD3 клетке, при этом первая полипептидная конструкция представляет собой scFv-область; вторую полипептидную конструкцию, содержащую антигенсвязывающую полипептидную конструкцию, которая связывается с целевым антигеном человека CD19 по меньшей мере на одной В-клетке, при этом вторая полипептидная конструкция представляет собой Fab-область или scFv-область; и гетеродимерную Fc-область IgG1 человека, содержащую вариант домена СН3 иммуноглобулина, содержащий первую СН3 последовательность и вторую СН3 последовательность, первая СН3 последовательность содержит аминокислотные замены в L351, F405 и Y407, а вторая СН3 последовательность содержит аминокислотные замены в Т366, K392 и Т394, при этом аминокислотными заменами для L в L351 являются Y, F или W, для F в F405 являются А или G и для Y в Y407 являются V, М, L или I, а аминокислотными заменами для Т в Т366 являются L, I, М или V, для K в K392 являются М, I, L или V и для Т в Т394 являются W, Y или F, при этом и первая полипептидная конструкция, и вторая полипептидная конструкция связаны с N-концом гетеродимерной Fc-области IgG1 человека. Также представлена фармацевтическая композиция для индуцирования киллинга В-клетки, содержащая указанную мультиспецифическую гетеромультимерную конструкцию. Также представлены способ лечения ракового заболевания, в том числе не поддающегося лечению по меньшей мере одним выбранным из CD19-литического антитела, CD20-литического антитела и блинатумомаба, способ лечения аутоиммунного состояния у нуждающегося в этом млекопитающего, способ лечения воспалительного состояния у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему композиции, содержащей эффективное количество указанной фармацевтической композиции, необязательно в комбинации с другими фармацевтически активными молекулами. Также описан набор для индуцирования киллинга В-клетки, содержащий указанную мультиспецифическую гетеромультимерную конструкцию и инструкции по ее применению. 7 н. и 22 з.п. ф-лы, 37 ил., 13 табл., 34 пр.
1. Выделенная мультиспецифическая гетеромультимерная конструкция для индуцирования киллинга В-клетки, содержащая:
первую полипептидную конструкцию, содержащую CD3-связывающую полипептидную конструкцию, которая связывается с комплексом человека CD3 по меньшей мере на одной экспрессирующей CD3 клетке, при этом первая полипептидная конструкция представляет собой scFv-область;
вторую полипептидную конструкцию, содержащую антигенсвязывающую полипептидную конструкцию, которая связывается с целевым антигеном человека CD19 по меньшей мере на одной В-клетке, при этом вторая полипептидная конструкция представляет собой Fab-область или scFv-область; и
гетеродимерную Fc-область IgG1 человека, содержащую вариант домена СН3 иммуноглобулина, содержащий первую СН3 последовательность и вторую СН3 последовательность, первая СН3 последовательность содержит аминокислотные замены в L351, F405 и Y407, а вторая СН3 последовательность содержит аминокислотные замены в Т366, K392 и Т394, при этом аминокислотными заменами для L в L351 являются Y, F или W, для F в F405 являются А или G и для Y в Y407 являются V, М, L или I, а аминокислотными заменами для Т в Т366 являются L, I, М или V, для K в K392 являются М, I, L или V и для Т в Т394 являются W, Y или F, при этом и первая полипептидная конструкция, и вторая полипептидная конструкция связаны с N-концом гетеродимерной Fc-области IgG1 человека.
2. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что чистота образующейся гетеродимерной Fc-области составляет по меньшей мере приблизительно 90% и Tm составляет приблизительно 75°С.
3. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что:
первая последовательность СН3 содержит аминокислотные модификации L351Y, F405A и Y407V, а вторая последовательность СН3 содержит аминокислотные модификации T366L, K392M и T394W;
первая последовательность СН3 содержит аминокислотные модификации L351Y, F405A и Y407V, а вторая последовательность СН3 содержит аминокислотные модификации T366L, K392L и T394W.
4. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что указанная гетеродимерная Fc-область гликозилирована.
5. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что указанная гетеродимерная Fc-область афукозилирована.
6. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что указанная гетеродимерная Fc-область агликозилирована.
7. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что указанная CD3-связывающая полипептидная конструкция представляет собой антитело, содержащее только тяжелые цепи, не содержащее легких цепей.
8. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что обе первая и вторая полипептидные конструкции содержат одноцепочечный Fv-полипептид (scFv-полипептид).
9. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что вторая полипептидная конструкция содержит одноцепочечный Fab-полипептид.
10. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что CD3-экспрессирующая клетка представляет собой Т-клетку.
11. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 10, отличающаяся тем, что указанная выделенная мультиспецифическая гетеромультимерная конструкция связывается с Т-клеткой с достаточной аффинностью и декорирует указанную Т-клетку в достаточной мере для индуцирования киллинговой активности указанной Т-клетки в отношении В-клетки при связывании Т-клетки и В-клетки.
12. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что CD3-экспрессирующая клетка представляет собой клетку человека.
13. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что указанная по меньшей мере одна В-клетка связана с раковым заболеванием.
14. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 13, отличающаяся тем, что указанное заболевание представляет собой раковое заболевание, выбранное из карциномы, саркомы, лейкоза, лимфомы и глиомы.
15. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 14, отличающаяся тем, что указанное раковое заболевание представляет собой по меньшей мере одно из плоскоклеточной карциномы, аденокарциномы, карциномы переходных клеток, остеосаркомы и саркомы мягких тканей.
16. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что указанная по меньшей мере одна В-клетка представляет собой аутоиммунную реактивную клетку, которая представляет собой лимфоидную или миелоидную клетку.
17. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что указанная конструкция содержит линкер между CD3-связанной полипептидной конструкцией и гетеродимерной Fc-областью и/или между второй полипептидной конструкцией и гетеродимерной Fc-областью.
18. Выделенная мультиспецифическая гетеромультимерная конструкция по п. 1, отличающаяся тем, что указанный линкер представляет собой полипептид, содержащий от приблизительно 1 до приблизительно 100 аминокислот.
19. Фармацевтическая композиция для индуцирования киллинга В-клетки, содержащая мультиспецифическую гетеромультимерную конструкцию по пп. 1-18 и подходящее вспомогательное вещество.
20. Способ лечения ракового заболевания у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему композиции, содержащей эффективное количество фармацевтической композиции по п. 19, необязательно в комбинации с другими фармацевтически активными молекулами.
21. Способ по п. 20, отличающийся тем, что указанное раковое заболевание представляет собой солидную опухоль.
22. Способ по п. 21, отличающийся тем, что указанная солидная опухоль представляет собой одно или более из саркомы, карциномы и лимфомы.
23. Способ по п. 20, отличающийся тем, что указанное раковое заболевание представляет собой гематологическое раковое заболевание.
24. Способ по п. 23, отличающийся тем, что указанное раковое заболевание представляет собой одно или более из В-клеточной лимфомы, неходжкинской лимфомы и лейкоза.
25. Способ лечения ракового заболевания, не поддающегося лечению по меньшей мере одним выбранным из CD19-литического антитела, CD20-литического антитела и блинатумомаба, у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему композиции, содержащей эффективное количество фармацевтической композиции по п. 19.
26. Способ лечения аутоиммунного состояния у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему эффективного количества фармацевтической композиции по п. 19.
27. Способ по п. 26, отличающийся тем, что указанное аутоиммунное состояние представляет собой одно или более состояний из рассеянного склероза, ревматоидного артрита, эритематозной волчанки, псориатического артрита, псориаза, васкулита, увеита, болезни Крона и диабета первого типа.
28. Способ лечения воспалительного состояния у нуждающегося в этом млекопитающего, включающий введение указанному млекопитающему фармацевтической композиции, содержащей эффективное количество мультиспецифической гетеромультимерной конструкции по любому из пп. 1-18.
29. Набор для индуцирования киллинга В-клетки, содержащий мультиспецифическую гетеромультимерную конструкцию по любому из пп. 1-18 и инструкции по ее применению.
| US 20110274691 A1, 10.11.2011 | |||
| Запорный клапан для фонтанирующих буровых скважин | 1924 |
|
SU12566A1 |
Авторы
Даты
2018-04-17—Публикация
2013-07-13—Подача