Изобретение относится к области фармацевтики и касается новой фармацевтической композиции в виде мягкой лекарственной формы - геля для лечения грибковых заболеваний кожи, волосистой части головы, ногтей, вызванных дерматофитами и/или дрожжеподобными грибами.
Растущая заболеваемость поверхностными микозами (грибковыми заболеваниями), вызванная различными родами дрожжеподобных грибков и дерматофитов, является важной и до сих пор нерешенной проблемой Здравоохранения во многих странах и в России, в частности (Уварова Ю. Рынок противогрибковых препаратов для лечения заболеваний кожи. Ремедиум 2011, №10, с. 39-41; Antifungals Market to 2017 - Generic Erosion of MajorPolyenes, Azoles, Allylamines and Echinocandins to Slow Value Growth. Reference Code: GBIHC165MR Publication Date: January 2012). У всех лекарственных средств, используемых в настоящее время, существуют проблемы развития резистентности, или недостаточности и узости спектра действия, или нежелательных лекарственных реакций, или ограниченности подходящих лекарственных форм и довольно часто сочетание нескольких или всех перечисленных факторов. С целью преодоления этих проблем неустанно ведется поиск новых молекул, способных преодолевать резистентность, и создаются новые лекарственные формы, позволяющие достигнуть высокого терапевтического эффекта в лечении.
Представители нового класса антимикотиков из ряда производных тиазолидин-2,4-диона выгодно отличаются от большинства широко используемых топических средств (азолов) отличным механизмом действия, направленным не на ингибирование синтеза эргостерола, а на подавление активности белка маннозилтрансферазы, приводящей к разрушению клеточной стенки гриба (WO 2002017915 А1, 2002; WO 2002022612 А1, 2002; WO 2003070238 А1, 2003; WO 2003070239 А1, 2003; US 6740670 В2, 2004). Используемые в качестве действующего вещества 3-алкоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-дионз известны как химические соединения, обладающие противомикробной активностью (SU 1417436 А, 1996).
В РФ запатентованы фармацевтические композиции, содержащие в качестве действующего вещества метиловый (RU 2295958 С1, 2007) или этиловый (RU 2563811 CI, 2015) оксикарбонильный эфир 5-пара-хлорбензилидентиазолидин-2,4-диона с экспериментально доказанной высокой противогрибковой активностью.
Фармацевтический состав препарата Микозидин (RU 2295958 С1, 2007) в качестве липофильной части мазевой основы содержит парафин нефтяной твердый, кислоту стеариновую, масло вазелиновое. В состав фармацевтической композиции была также введена кислота бензойная, обладающая транскутанным и консервирующим действием. Введенный в состав фармацевтической композиции воск эмульсионный делал его близким по строению к лицетину и кефалину, входящим в состав кожного жира, что оказывало смягчающее действие на кожу. Мазь Микозидин на липофильной основе содержит в качестве активного вещества 3-метоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-дион, а также целевые добавки при следующем соотношении компонентов, мас. %:

Состав липофильной основы и предлагаемое соотношение компонентов являлись оптимальными и позволяли обеспечить требуемую скорость и полноту высвобождения действующего вещества и его химиотерапевтическое действие на уровне 70%. При использовании мази с меньшей концентрацией активного вещества (до 2%) эффективность снижалась, а при концентрации выше 5% возникал риск раздражающего действия препарата. Разработанная фармацевтическая композиции на липофильной основе позволяла получить хороший лечебный эффект у препарата «Микозидин», однако вызывала нарекания пациентов по причине неудобства при их использовании, вследствие жирной основы.
Наиболее близкая к предложенной фармацевтическая композиция (RU 2563811 С1, 2015) с действующим веществом - 3-этоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-дион содержит помимо перечисленных добавку мочевины, обеспечивающую повышение процента эффективности при лечении грибковых заболеваний кожи до 84-89%, мас. %:

Способ получения данной фармацевтической композиции заключается в том, что к липофильной основе, приготовленной сплавлением кислоты стеариновой, парафина нефтяного твердого, воска эмульсионного, добавляют кислоту бензойную и масло вазелиновое и после выдержки при 75-85°C в течение 30-40 мин добавляют предварительно приготовленный концентрат 3-этоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-диона в масле вазелиновом, после чего добавляют мочевину в масле вазелиновом до получения однородной массы (RU 2563811 С1, 2015).
Однако, включение в состав фармацевтической композиции мочевины, несмотря на значительное повышение процента эффективности, было признано не удовлетворительным, поскольку состав не выдержал показателя стабильности при хранении. В образцах через год хранения появлялись темные пятна вследствие воздействия мочевины на действующее вещество 3-этоксикарбонил производного тиазолидин-2,4-диона, приводящее к его деструкции и изменению цвета композиции.
Кроме того, в цитируемом патенте ЦХЛС - ВНИХФИ (RU 2295958 С, 2007) было сделано заключение об ограничительных возможностях получения композиции на гидрофильно-липофильной основе из-за специфических физико-химических свойств действующего вещества, что требовало специального подбора компонентов липофильной основы.
Техническая проблема, решаемая настоящим изобретением, заключается в получении устойчивой при хранении фармацевтической композиции с действующим веществом 3-этоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-дион.
Техническая проблема решается фармацевтической композицией для лечения дерматомикозов при местном применении, содержащей в качестве активного вещества 3-этоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-дион, в качестве вспомогательных компонентов масло вазелиновое и воск эмульсионный, которая, согласно изобретению, в качестве вспомогательных компонентов включает также хитозан водорастворимый и воду при следующем соотношении компонентов, мас. %:
Техническая проблема также решается способом получения предложенной фармацевтической композиции, заключающимся в том, что нагретый до 60-65°C воск эмульсионный смешивают с предварительно подготовленным концентратом 3-этоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-диона в масле вазелиновом и добавляют к полученному составу водный раствор хитозана водорастворимого с последующей гомогенизацией.
Технический результат предложенного изобретения заключается в получении устойчивой, не расслаиваемой при хранении лекарственной формы благодаря использованию в составе композиции водорастворимого хитозана, широко применяемого в косметологии и медицине (Сливкин Д.А. и соавт. ХИТОЗАН ДЛЯ ФАРМАЦИИ И МЕДИЦИНЫ. ВЕСТНИК ВГУ, СЕРИЯ: ХИМИЯ. БИОЛОГИЯ. ФАРМАЦИЯ, 2011, №2, 214-232).
В результате экспериментальной работы была получена предложенная фармацевтическая композиция в форме геля, соответствующего требованиям на фармацевтическое средство, получившая рабочее название Миколек.
Оптимальным растворителем для химической субстанции 3-этоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-дион (далее - субстанция) является масло вазелиновое. Введение масляного раствора субстанции в гидрогелевую композицию предполагает создание эмульсионной системы, которая должна отвечать требованиям, предъявляемым к дифильным мазям. В связи с этим выбор структурообразующего компонента осуществлен с учетом термодинамического состояния лекарственной формы, которой присуще расслоение фаз и требуется стабилизация.
Вспомогательные ингредиенты, входящие в состав геля МИКОЛЕК имеют различные гидрофильно-липофильные свойства и выполняют определенное функциональное назначение, которое описано в таблице 1.
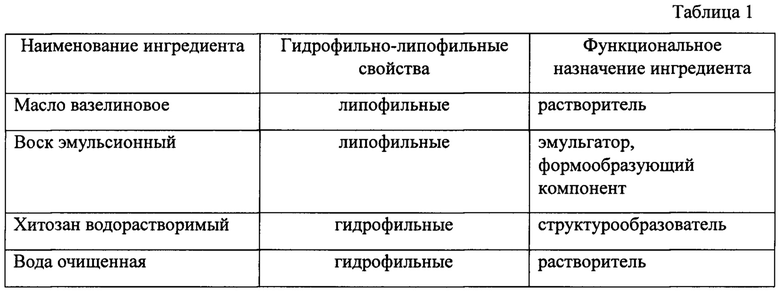
Гель Миколек относится к двухфазным эмульсионным системам.
От качества подготовки компонентов эмульсии, имеющих противоположные гидрофильно-липофильные свойства, зависит однородность, размер капель дисперсной фазы и, как следствие, стабильность готового геля.
В состав геля входят компоненты как растворимые в воде (хитозан), так и нерастворимые в воде (масло вазелиновое, воск эмульсионный). Активное вещество геля - субстанция Миколек так же практически не растворяется в воде, трудно растворяется в масле вазелиновом.
В ходе эксперимента определяли критические параметры и способ подготовки ингредиентов, влияющие на качество эмульгирования геля:
- растворение водорастворимого компонента хитозана в воде;
- подготовку (расплавление) воска эмульсионного;
- определение способа введения субстанции Миколека и вазелинового масла.
В процессе разработки технологии геля Миколека было изучено оптимальное время и способ растворения хитозана.
Хитозан обладает гидрофильными свойствами, поэтому для его введения в композицию геля был выбран способ предварительного смешивания его с частью воды очищенной. В результате чего происходит образование гидрогеля.
Исходя из полученных результатов было установлено, что оптимальное время набухания и растворения 4,0 г хитозана в 800 г воды очищенной составляет 4 часа. При масштабировании процесса время приготовления раствора хитозана увеличивается на 20-30%.
Поэтому помимо контроля времени растворения необходимо при ведении технологического процесса необходимо введение контрольной точки - полноты растворения хитозана, которая определяется методом визуальной оценки полученного гидрогеля.
Воск эмульсионный является эмульгирующим компонентом, поэтому его подготовка имеет первостепенное влияние на качество готового продукта и его стабильность.
Следует учитывать, что эмульгатор будет оказывать должное эмульгирующее действие только в том случае, если эмульгатор, вода и масло будут взяты в строго определенных количествах, мас. %: 3-этоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-дион 2-3; масло вазелиновое 7-9; воск эмульсионный 9-11; хитозан водорастворимый 0,35-0,45; вода - остальное, до 100. Ниже приведены примеры составов препарата, в мас. %.

В связи с этим, критическим параметром технологического процесса является минимизация потерь при подготовке и внесении воска эмульсионного в реактор, т.к. он имеет высокую вязкость.
Для уменьшения вязкости было предложено предварительно расплавлять воск эмульсионный. Выбор оптимальной температуры расплавления проводили экспериментально. Оптимальные результаты получены при расплавлении воска при температуре 60±5°C в течение 15 минут. Этого времени достаточно для полного расплавления воска эмульсионного, полученная консистенция расплава позволяет минимизировать его потери при манипуляциях на технологических стадиях.
Субстанция Миколек имеет неоднородную комковатую структуру, обладает гидрофобными свойствами, практически не растворяется в воде. Поэтому для равномерного введения в гель возникают определенные сложности.
В процессе фармацевтической разработки было установлено, что для равномерного распределения субстанции Миколек оптимальным вариантом является предварительное смешение ее с вазелиновым маслом. Исходя из полученных данных, было установлено, что параметрами, подлежащими контролю, при смешении субстанции Миколек с маслом вазелиновым является температура (40±5)°C и время 10 минут.
Установлена следующая последовательность смешения компонентов геля друг с другом.
В реактор-гомогенизатор загружают 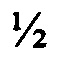 часть от расчетного количества воды очищенной, загружают эмульгатор - расплавленный воск эмульсионный, перемешивают до однородного распределения эмульгатора. Далее небольшими порциями вводят гидрофобные компоненты - смесь субстанции Миколек и масла вазелинового. Тщательно перемешивают и добавляют гидрофильный компонент - подготовленный гидрогель хитозана водорастворимого. После перемешивания добавляют оставшуюся
часть от расчетного количества воды очищенной, загружают эмульгатор - расплавленный воск эмульсионный, перемешивают до однородного распределения эмульгатора. Далее небольшими порциями вводят гидрофобные компоненты - смесь субстанции Миколек и масла вазелинового. Тщательно перемешивают и добавляют гидрофильный компонент - подготовленный гидрогель хитозана водорастворимого. После перемешивания добавляют оставшуюся 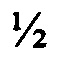 часть воды очищенной.
часть воды очищенной.
Анализ визуальных и микроскопических данных геля, полученного при различных режимах гомогенизации со скоростью вращения 500, 1000, 2000, 4000, 5000 об/мин. наглядно показал, что увеличение скорости вращения ротора гомогенизатора приводит к доказанному уменьшению размера частиц гидрофобной дисперсной фазы, а, следовательно, к улучшению стабильности готовой лекарственной формы.
Пример приготовление геля
Отвешивали на весах 192 г воды очищенной, 8 г хитозана водорастворимого и загружали отвешенные компоненты в стеклянный стакан вместимостью 400 мл.
Перемешивали содержимое стакана стеклянной палочкой и оставляли на 5 часов при комнатной температуре до получения однородного раствора хитозана, периодически перемешивая содержимое стакана стеклянной палочкой.
Отвешивали на весах 62,17 г субстанции, 200 г масла вазелинового и загружали отвешенные компоненты в стеклянный стакан вместимостью 400 мл.
Стакан помещали на водяную баню с температурой (40±5)°C; в стакан опускали мешалку верхнеприводную и перемешивали содержимое стакана в течение 10 минут при температуре (40±5)°C до получения однородной основы.
Отвешивали на весах 160,0 г воска эмульсионного, загружали отвешенное количество в стеклянный стакан вместимостью 400 мл и расплавляли содержимое стакана на водяной бане в течение 15 минут при температуре 63-65°C, периодически перемешивая стеклянной палочкой. Контроль температуры осуществляют по показателям дисплея.
Отвешивали на весах 700,0 г воды очищенной, предварительно нагретой до 40°C, загружали отвешенное количество воды очищенной в реактор-гомогенизатор. Для поддержания в реакторе температуры (40±5)°C периодически включали нагревательный элемент, расположенный в рубашке реактора.
Загружали в реактор-гомогенизатор расплавленный воск эмульсионный из стакана. Перемешивали содержимое реактора в течение 20 минут при температуре (40±5)°C.
Загружали небольшими порциями в реактор-гомогенизатор содержимое стакана - смесь субстанции с вазелиновым маслом; включали гомогенизатор и перемешивали при 5000 об/мин содержимое реактора-гомогенизатора в течение 20 минут при температуре (40±5)°C.
Отвешивали на весах 677,83 г воды очищенной, предварительно нагретой до 40°C, загружали отвешенное количество воды очищенной в реактор-гомогенизатор небольшими порциями и перемешивали при 5000 об/мин содержимое реактора-гомогенизатора в течение 20 минут при температуре (40±5)°C.
Загружали в реактор-гомогенизатор содержимое стакана гидрогель хитозана, включали гомогенизатор и перемешивали при 5000 об/мин содержимое реактора-гомогенизатора в течение 20 минут.
Производили визуальный контроль однородности геля. При необходимости продолжали перемешивание при 5000 об/мин при включенном гомогенизаторе реактора в течение 15 минут.
Отбирают пробу в количестве 2,0 г на анализ. Анализ считается положительным, если гель однородный, белого цвета и количественное содержание субстанции находится в пределах от 2,7 до 3,3%.
Стабильность полученного геля Миколек определяли по показателю внешний вид в процессе хранения геля. В течение 3 месяцев гель сохранял однородность и белый цвет.
Дополнительные преимущества геля Миколек обеспечиваются за счет создания эмульсионной основы типа масла в воде: простота производства эмульсионной основы, хорошее сродство с кожными покровами, нейтральное в отношении тканей значение показателя рН, регенерирующий эффект, органолептические свойства, потребительские качества и др. Кроме того хитозан обеспечивает пластичность водно-эмульсионной системы.
Противогрибковая активность in vivo - результаты исследования противогрибковой активности лекарственной формы Миколек в двух концентрациях 3% и 2%.
Оценка противогрибковой активности субстанции 3-этоксикарбонил-5(4-хлорбензидилен)тиазолидин-2,4-диона и лекарственных форм на его основе (гель 2% и 3%) в отношении возбудителей дерматофитозов проводилась на модели трихофитии и микроспории на морских свинок и накожного кандидоза на лабораторных мышах. Действие препарата оценивали в сравнении с противогрибковыми коммерческими лекарственными препаратами- - Экзодерил® и Низорал®.
Микроорганизмы.
Штамм Trichophyton mentagrophytes 18 ВГНКИ клинический изолят выделен от больной дерматофитозом морской свинки в 1977 году, используется для контроля иммуногенности вакцин против дерматофитозов. Штамм обладает высокой вирулентностью, используется для воспроизведения трихофитоза на моделях лабораторных животных.
Штамм Trichophyton rubrum 2902 ВГНКИ клинический изолят, выделен 2010 году от больного рубромикозом человека. Штамм обладает высокой вирулентностью, используется для воспроизведения трихофитии на моделях лабораторных животных.
Штамм Microsporum canis c.20 ВГНКИ клинический изолят выделен от больной белой мыши. Штамм обладает высокой вирулентностью, используется для воспроизведения микроспории на моделях лабораторных животных.
Штамм Candida albicans АТСС 24443. Штамм получен из Американской коллекции эталонных культур (АТСС), чувствительный к флуконазолу и вориконазолу.
Животные.
Для воспроизведения модели экспериментального дерматофитоза использовались морские свинки массой 200-250 г.
Для воспроизведения модели кожного кандидоза использовали лабораторные белые мыши линии BALB весом 18-26 г.
Для исключения влияния половой принадлежности на результаты эксперимента использовались только самки.
Эксперимент заключался в заражении морских свинок вирулентными штаммами Trichophyton mentagrophytes, Trichophyton rubrum и Microsporum canis. После развития клинической картины дерматофитоза животные подвергались фармакологической терапии согласно приведенной ниже схеме (таблица 2). В ходе эксперимента оценивалась интенсивность заболевания, оценка подтверждалась культуральным исследованием клинического материала.
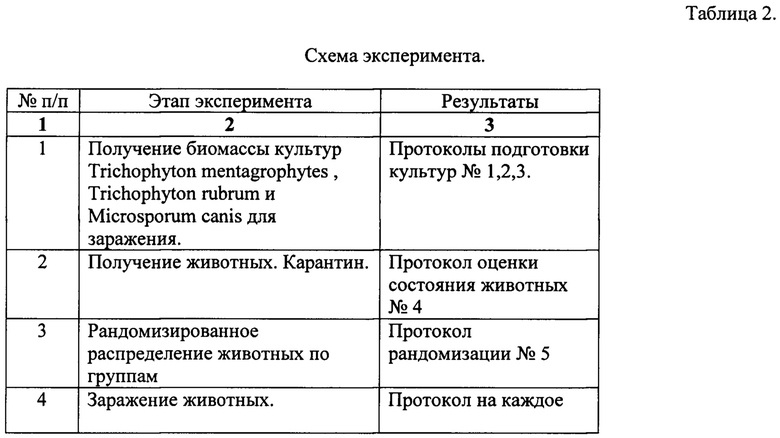

Результаты определения специфической противогрибковой эффективности препаратов «Миколек» (Миколек 2%, Миколек 3%) и гелевой основы* препарата Миколек в отношении возбудителя трихофитии Trichophyton mentagrophytes на модели трихофитии морских свинок представлены в таблицах 3, 4 (2% и 3% - содержание субстанции в препарате, мас. %) (Гелевая основа - состав композиции без действующего вещества).

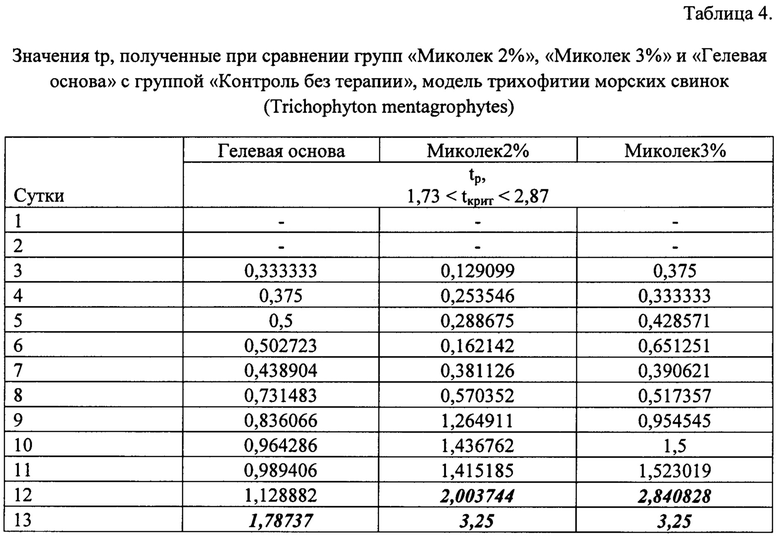
tp - биометрический показатель, применяемый для статистических расчетов (критерий Стьюдента); tкрит - критический биометрический показатель.
Анализируя данные, приведенные в таблице 3, можно сделать вывод о более высокой терапевтической эффективности препарата «Миколек 3%». Так, на 6 сутки терапии показатель ТЭ для препарата «Миколек 3%» достигает 27%, тогда как ТЭ препарата «Миколек 2%» равен 8,1%. Однако эти различия не были статистически достоверными (tp. равен 0,65 и 0,16 соответственно). С 12 суток от начала лечения ТЭ препаратов «Миколек 2%» и «Миколек 3%» становятся равны, что подтверждается статистическим анализом (tp равен 2,00 и 2,84 соответственно).
В целом, эффективность препаратов «Миколек 2%» и «Миколек 3%» можно считать одинаковой, так как достоверные различия между индексом поражения (ИП) в контрольной группе и опытных группах обнаруживаются только на 12-13 сутки, которым соответствует равная терапевтическая эффективность.
Исследование клинического материала, отобранного от животных из этих групп, подтвердило факт полного выздоровления животных в группах «Миколек 2%» и «Миколек 3%». Возбудитель трихофитии в материале, отобранном от этих животных на 13 день лечения, не обнаружен. В материале, отобранном на 10 день терапии, возбудитель также не обнаружен. Из материала, отобранного у животных контрольной группы на 13 сутки терапии, возбудитель выделяется.
Для сравнения, ТЭ препарата Низорал на 13 сутки равна 57,7%, tp 1,75; ТЭ препарата Экзодерил на 13 сутки равна 76,9%, tp 1,76.
ТЭ препарата сравнения Экзодерил также подтверждается культуральным микологическим исследованием (отрицательный результат, отбор на 13 сутки). Из клинического материала, отобранного на 13 сутки от животных из группы «Низорал», удалось выявить возбудителя трихофитии.
Данные, приведенные в таблице 3, говорят о терапевтической эффективности гелевой основы препарата «Миколек», которая равна 73,07% на 13 сутки. Эти данные не являются случайными, так как подтверждены статистически. Возможно, такой эффект связан с размягчающим действием гелевой основы, которое способствует визуальному снижению ИП. Однако выздоровления животных не происходит, что подтверждается культуральным исследованием материала (13 сутки, положительный результат исследования). Результаты определения специфической противогрибковой эффективности препаратов «Миколек» (Миколек 2%, Миколек 3%) и гелевой основы препарата Миколек в отношении возбудителя трихофитии Trichophyton rubrum на модели трихофитии морских свинок представлены в таблицах 5, 6.
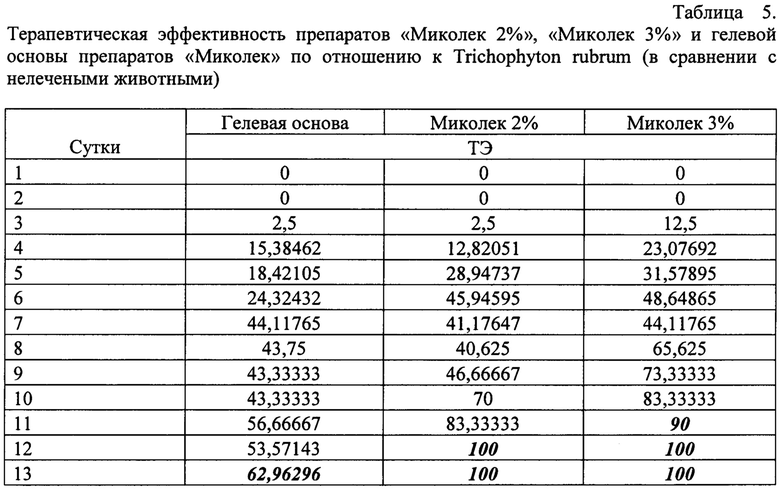
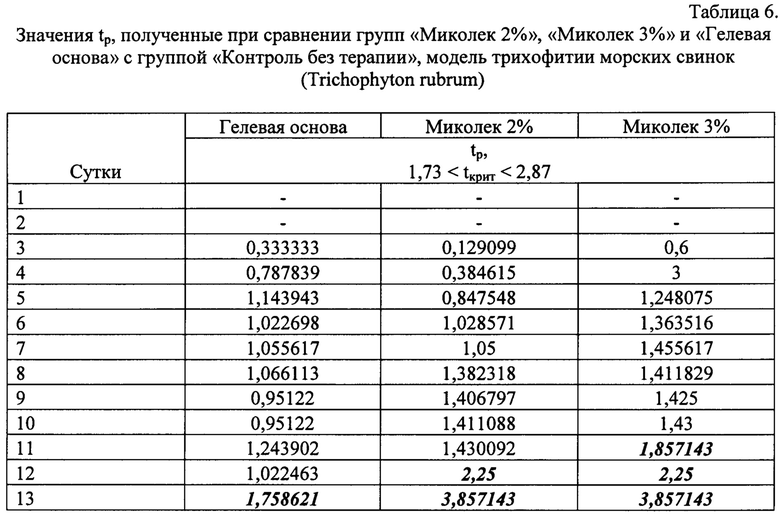
Анализируя данные, приведенные в таблице 5, можно сделать вывод о незначительно более высокой ТЭ препарата «Миколек 3%» по сравнению с препаратом «Миколек 2%». Начиная с 12 суток лечения, оба препарата проявляют 100% терапевтическую эффективность по отношению к инфекции, вызванной Trichophyton rubrum, что подтверждается результатами статистического анализа (значения tp. значительно превышают критические значения, см. табл. 6)
Результаты культурального микологического исследования подтверждают полное микологическое выздоровление животных из групп «Миколек 2%» и «Миколек 3%» (отбор материала на 13 сутки, результат отрицательный). Результат исследования материала от животных из групп «Контроль без терапии» и «Гелевая основа» положительный (отбор на 13 сутки).
Терапевтический эффект, наблюдаемый в группе «Гелевая основа» (62,96% на 13 сутки, tp 1,75), обусловлен размягчающим действием гелевой основы, визуально уменьшающим выраженность клинических признаков. Выздоровления животных при этом не наблюдается (положительное исследование клинического материала)
Для сравнения, ТЭ препарата Низорал на 13 сутки равна 66,6%, tp 1,85; ТЭ препарата Экзодерил на 13 сутки равна 77,7%, tp 1,86.
Исследование клинического материала показало следующее: группа «Низорал», 13 сутки - положительный результат; группа «Экзодерил», 13 сутки - отрицательный результат.
Результаты определения специфической противогрибковой эффективности препаратов «Миколек» (Миколек 2%, Миколек 3%) и гелевой основы препарата Миколек в отношении возбудителя микроспории Microsporum canis на модели микроспории морских свинок представлены в таблицах 7, 8.
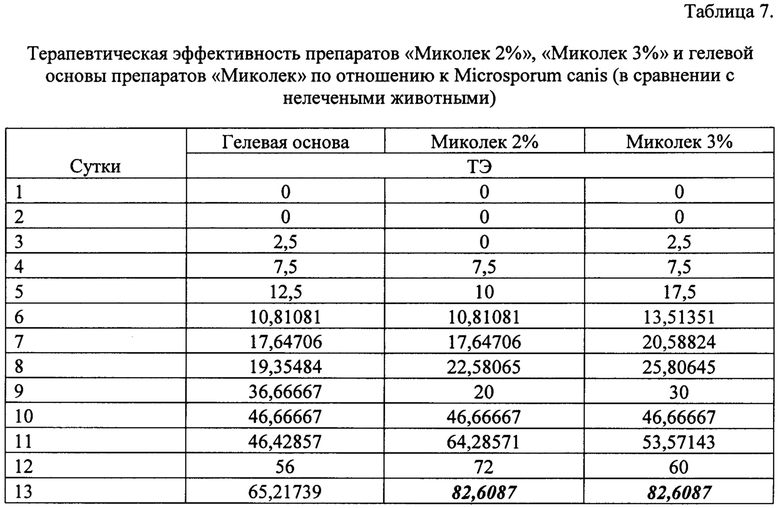
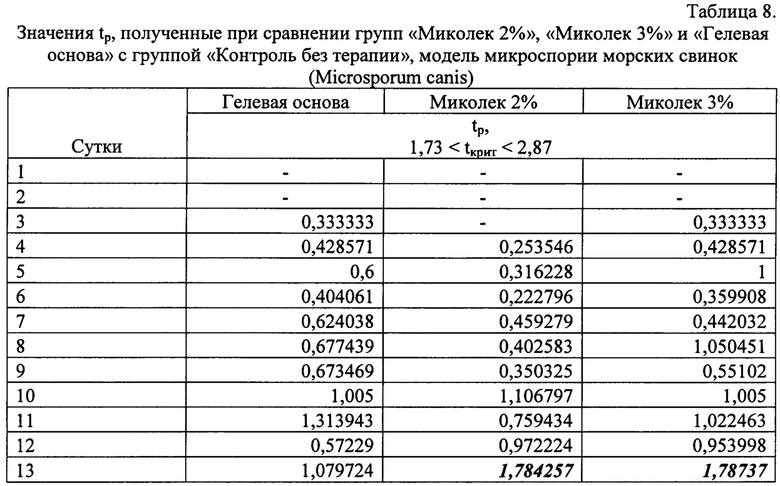
Анализируя данные, приведенные в таблице 7, можно сделать вывод о приблизительно одинаковой эффективности препаратов «Миколек» с концентрацией действующего вещества 2 мас. % и 3 мас. %. Максимальная ТЭ достигается на 13 сутки со дня начала лечения, она составляет 82,6%. Динамика увеличения ТЭ у обоих препаратов приблизительно одинакова, ТЭ так же подтверждается отрицательным результатом культурального исследования (отбор на 10 сутки, отбор на 13 сутки). Результат исследования материала от животных контрольной группы положительный (отбор на 10 и 13 сутки)
Терапевтическая эффективность гелевой основы не подтверждена культуральным исследованием, также не подтверждена статистически.
Значение ТЭ препаратов Миколек 2%» и «Миколек 3%» статистически подтверждается только на 13 сутки со дня начала лечения.
Стоит сказать, что динамика изменения ИП позволяет сделать предположение о возможной стопроцентной эффективности препаратов «Миколек» в отношении Microsporum canis на 15-16 сутки со дня начала лечения. Это касается, главным образом, полного исчезновения клинических признаков, полное выздоровление (отсутствие возбудителя в клиническом материале) наступило в группе «Миколек 3%» на 10 день после начала лечения (ТЭ 46,66%, tp 1,005). В группе «Миколек 2%» полное выздоровление наступило только на 13 сутки (отрицательное значение культурального исследования).
Для сравнения, ТЭ препарата Низорал на 13 сутки равна 56,6%, tp 1,85. Культуральное исследование показало положительный результат (13 сутки). ТЭ препарата Экзодерил на 13 сутки равна 69,6%, tp 1,76. Культуральное исследование показало отрицательный результат (13 сутки). Результаты определения специфической противогрибковой эффективности препаратов «Миколек» (Миколек 2%, Миколек 3%) и гелевой основы препарата Миколек в отношении возбудителя кандидоза Candida albicans на модели кандидоза кожи лабораторных мышей представлены в таблицах 9, 10.
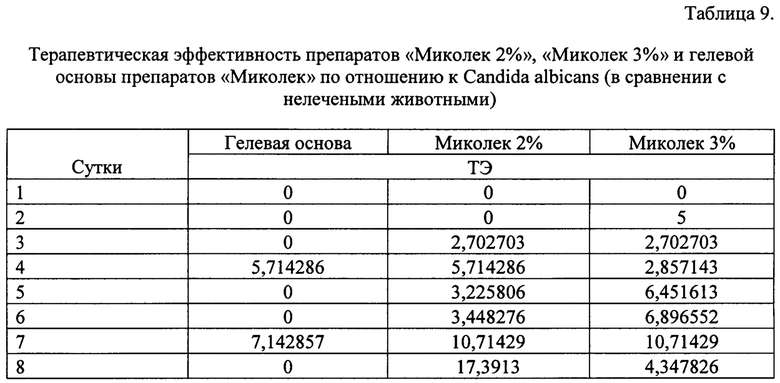
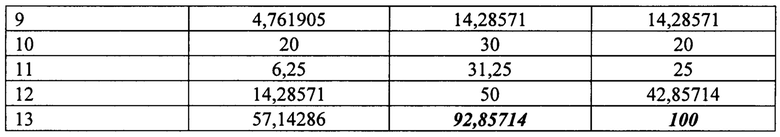
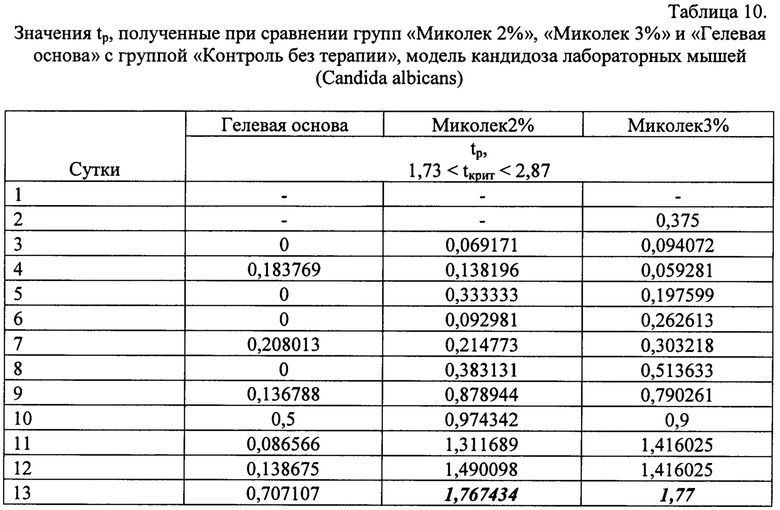
Из данных таблицы 9 можно сделать вывод об эффективности препаратов «Миколек» в отношении Candida albicans. Максимальная подтвержденная статистически эффективность достигается на 13 сутки и равна 92,8% и 100% для препарата с 2% действующего вещества и 3% соответственно.
Динамика увеличения ТЭ препаратов «Миколек» в отношении возбудителя кандидоза выглядит нестабильно: плавное увеличение до 10% (2-7 сутки, затем падение до 4% (8 сутки), увеличение до 14% (9 сутки), плавное повышение до 25% (9-11 сутки). Далее следует резкий скачок ТЭ с 25 до 42% (11-12 сутки), затем еще один, с 42% до 100% (12-13 сутки). Препарат «Миколек 2%» показывает схожие результаты, но изменения ТЭ не такие резкие.
Культуральное исследование (10 сутки, 13 сутки) показывает отрицательные результаты для обеих опытных групп.
Препарат Низорал достигает 100% терапевтической эффективности уже на 10 сутки со дня начала лечения, значение ТЭ подтверждено статистически (сравнение с контрольной группой, не получавшей терапевтических препаратов). ТЭ так же подтверждена культуральным исследованием (10 сутки, 13 сутки)
ТЭ препарата Экзодерил статистически не подтверждена, культуральное исследование положительное на 10 и 13 сутки, что позволяет сделать вывод о неэффективности данного препарата возбудителя кандидоза кожи.
В отношении возбудителя трихофитии Trichophyton mentagrophytes препараты «Миколек 3%» и «Миколек 2%» проявляют стопроцентную терапевтическую эффективность, тогда как Низорал и Экзодерил - 57,7 и 76,9% соответственно. При этом полное выздоровление на 13 сутки наступило в группах «Миколек 2%», «Миколек 3%», Экзодерил, что подтверждено культуральным микологическим исследованием клинического материала. Материал, отобранный у животных из этих групп на 13 сутки после начала лечения, свободен от возбудителя трихофитии. При анализе материала от животных из групп «Контроль без терапии» и «Низорал®», отобранного на 13 сутки после начала лечения, был выделен возбудитель трихофитии (Trichophyton mentagrophytes). Выделенный штамм по морфологическим и биохимическим признакам идентичен штамму Т. mentagrophytes 18.
В отношении другого возбудителя трихофитии - Trichophyton rubrum - препараты «Миколек 2%» и «Миколек 3%» также проявили стопроцентную эффективность. Препараты Низорал® и Экзодерил®, использовавшиеся для сравнения, проявили более низкую терапевтическую эффективность 66,6 и 77,7% соответственно. В остальном картина аналогична той, которая была получена на предыдущей модели трихофитии (возбудитель - Т. mentagrophytes). Эффективность терапии подтверждена культуральным исследованием клинического материала в группах «Миколек 2%», «Миколек 3%» и «Экзодерил» (отрицательный результат на 13 сутки) и не подтверждена для группы «Низорал» (положительный результат на 13 сутки). Штамм, выделенный от животных из группы «Контроль без терапии» идентичен штамму Т. rubrum 2902.
На основании этих данных можно сделать вывод о более высокой эффективности препаратов «Миколек» для лечения трихофитии по сравнению с существующими на рынке Экзодерилом®.
В отношении Microsporum canis, возбудителя микроспории, препараты «Миколек 2%» и «Миколек 3%» проявили одинаковую эффективность, равную всего 82,6% на 13 сутки лечения. Однако культуральное микологическое исследование показало полное выздоровление животных из этих групп (в группе «Миколек 3%» возбудитель не выделялся из материала, отобранного на 10 день лечения). Препарат «Миколек» показал лучшую терапевтическую эффективность, чем существующий на рынке препарат Экзодерил. Эффективность препарата Низорал® не подтверждена культуральным исследованием (положительный результат на 13 сутки)
В отношении возбудителя кандидоза кожи - Candida albicans - препараты «Миколек» проявили неодинаковую терапевтическую эффективность. Так, «Миколек 2%» немного уступает препарату «Миколек 3%»: их эффективность равна соответственно 92,9 и 100% на 13 сутки после начала лечения соответственно. Имеющийся на рынке препарат Низорал® проявил стопроцентную эффективность уже на 10 сутки со дня начала лечения. Эффективность препарата Экзодерил статистически не подтверждена, культуральное исследование показало положительный результат. В случаях с препаратами «Миколек 2%», «Миколек 3%» и Низорал® культуральное исследование показало отрицательный результат.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ГРИБКОВЫХ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2563811C1 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ ДЛЯ ЛЕЧЕНИЯ ГРИБКОВЫХ ЗАБОЛЕВАНИЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2295958C1 |
| ГИБРИДНЫЕ ЭФИРЫ НА ОСНОВЕ ПРОИЗВОДНЫХ ТИАЗОЛИДИН-2,4-ДИОНА И АЗОЛОВ (1Н-1,3-ИМИДАЗОЛА И 1Н-1,3,4-ТРИАЗОЛА) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2662153C1 |
| Новые потенциальные противогрибковые средства на основе тиазолидин-2,4-диона и триазола | 2023 |
|
RU2814730C1 |
| 3,5-Замещенные производные тиазолидин-2,4-диона, обладающие противомикробной активностью | 2018 |
|
RU2690161C1 |
| 3-АЛКОКСИКАРБОНИЛ-5-ЗАМЕЩЕННЫЙ БЕНЗИЛИДЕНТИАЗОЛИДИН-2,4-ДИОНЫ, ОБЛАДАЮЩИЕ ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ | 1986 |
|
SU1417436A1 |
| Композиция на основе противогрибкового средства и модифицированного циклодекстрина | 2023 |
|
RU2831569C1 |
| Гибридные амиды на основе триазола и тиазолидина, обладающие антимикробной активностью | 2018 |
|
RU2703997C1 |
| Средство с противогрибковой активностью на основе золей металлов | 2021 |
|
RU2763885C1 |
| Гибридные производные (1Н-1,2,4) триазола и серосодержащих гетероциклов: производных тиазолидин-2,4-диона, тиоморфолин-3-она и 1,4-тиазепан-3-она, обладающих антимикробной активностью | 2020 |
|
RU2771027C1 |
Изобретение относится к химико-фармацевтической промышленности и представляет собой фармацевтическую композицию для лечения дерматомикозов при местном применении, содержащую в качестве активного вещества 3-этоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-дион, в качестве вспомогательных компонентов масло вазелиновое и воск эмульсионный, отличающееся тем, что в качестве вспомогательных компонентов включает хитозан водорастворимый и воду. Изобретение позволяет получить устойчивую, не расслаиваемую при хранении лекарственную форму. 2 н.п. ф-лы, 10 табл., 6 пр.
1. Фармацевтическая композиция для лечения дерматомикозов при местном применении, содержащая в качестве активного вещества 3-этоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-дион, в качестве вспомогательных компонентов масло вазелиновое и воск эмульсионный, отличающаяся тем, что в качестве вспомогательных компонентов включает хитозан водорастворимый и воду при следующем соотношении компонентов, мас. %:
2. Способ получения фармацевтической композиции по п. 1, заключающийся в том, что нагретый до 60-65°С воск эмульсионный смешивают с предварительно подготовленным концентратом 3-этоксикарбонил-5-(4-хлорбензилиден)тиазолидин-2,4-диона в масле вазелиновом и добавляют к полученному составу водный раствор хитозана водорастворимого с последующей гомогенизацией.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ГРИБКОВЫХ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2563811C1 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ ДЛЯ ЛЕЧЕНИЯ ГРИБКОВЫХ ЗАБОЛЕВАНИЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2295958C1 |
| 3-АЛКОКСИКАРБОНИЛ-5-ЗАМЕЩЕННЫЙ БЕНЗИЛИДЕНТИАЗОЛИДИН-2,4-ДИОНЫ, ОБЛАДАЮЩИЕ ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ | 1986 |
|
SU1417436A1 |
| WO 2012064559 A1, 18.05.2012 | |||
| Уварова Ю | |||
| Рынок противогрибковых препаратов для лечения заболеваний кожи | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Машина для изготовления проволочных гвоздей | 1922 |
|
SU39A1 |
Авторы
Даты
2018-05-22—Публикация
2017-08-16—Подача