Изобретение относится к области биотехнологии, а именно к контролю качества препаратов крови, методам определения функциональной активности молекул иммуноглобулина.
Прототипом является способ определения Fc-функции иммуноглобулиновых препаратов методом, изложенным в статье 2.7.9 Европейской Фармакопеи. Метод основан на измерении гемолиза сенсибилизированных антигеном краснухи эритроцитов человека, обусловленного реакцией антиген-антитело-комплемент. Измерение гемолиза проводят для исследуемого образца иммуноглобулина и для раствора сравнения - биологического референсного препарата иммуноглобулина человека. Строят кривые зависимости изменения оптической плотности от времени, на кривой определяют наибыстрейший участок, рассчитывают угол наклона этого участка путем деления разности оптической плотности на промежуток времени. Для исследуемого препарата вычисляют индекс Fc-функции, который равен отношению углов наклона кривых исследуемого препарата и референсного и выражен в процентах. Значение полученного индекса должно быть не менее величины, указанной в паспорте биологического референсного препарата (European Pharmacopoeia, 8.2, статья 2.7.9., 2015).
Использование в фармакопейном методе в качестве сенсибилизирующего агента труднодоступного антигена краснухи ограничивает его применение в практике контроля качества препаратов крови.
Аналогом патентуемого способа является реакция связывания комплемента (РСК) - серологическая реакция для выявления антител в сыворотке крови человека на определенный антиген при диагностике заболеваний. В реакции участвуют две системы и комплемент. Первая система состоит из антигена и антитела. Вторая система индикаторная, в нее входят эритроциты барана и гемолизин - сыворотка крови кролика, иммунизированного эритроцитами барана. РСК ставят в два приема: вначале соединяют антиген с испытуемой сывороткой крови, в которой отыскивают антитела, а затем добавляют комплемент. Если антиген и антитела соответствуют друг другу, то образуется иммунный комплекс, который связывает комплемент. При отсутствии в сыворотке антител иммунный комплекс не образуется и комплемент остается свободным. Процесс связывания комплемента комплексом визуально невидимый, для его выявления добавляют индикаторную систему. Если в первой системе комплемент связался, то при добавлении индикаторной системы гемолиз эритроцитов не произойдет - реакция положительная. Если же комплемент не связался в первой системе из-за отсутствия антител, то он свяжется с индикаторной системой, в результате чего произойдет гемолиз эритроцитов - реакция отрицательная.
Задачей, на решение которой направлено данное изобретение, является разработка способа определения Fc-функции препаратов иммуноглобулина человека на основе реакции связывания комплемента. Преимуществами предлагаемого способа по сравнению с прототипом являются использование доступных реактивов отечественного производства, не требует серьезного аппаратурного оснащения, простота в интерпретации результатов.
Для осуществления метода готовятся 3 системы и комплемент с определенной гемолитической активностью.
Первая система (основная) включает исследуемый препарат с определенным содержанием белка иммуноглобулина и антиген. Для образования связи антитело-антиген система инкубируется при 37°C в течение часа.
Вторая система (контрольная) состоит из исследуемого препарата с содержанием белка иммуноглобулина, как в основной системе, и физиологического раствора, заменяющего антиген.
Способ предусматривает обязательное использование раствора сравнения - биологического референсного препарата иммуноглобулина для определения Fc-функции. Основная и контрольная системы аналогичным образом готовятся для раствора сравнения.
Третья система (индикаторная) состоит из стандартизованной суспензии эритроцитов барана и гемолизина - сыворотки крови иммунизированных эритроцитами барана кроликов.
В основную и контрольную системы добавляется раствор комплемента с гемолитической активностью 2 CH50/мл. Для образования комплексов антиген-антитело-комплемент обе системы инкубируются при 37°C в течение часа.
При добавлении индикаторной системы в основную и контрольную происходит гемолиз эритроцитов барана. Измеряется оптическая плотность растворов при длине волны 540 нм с длиной оптического пути 10 мм. Рассчитывается степень гемолиза в обеих системах для всех образцов в соответствии с формулой 1

где Y - степень гемолиза в пробе, %;
ОП - оптическая плотность в пробе;
ОПкэр - оптическая плотность в контроле самопроизвольного гемолиза эритроцитов, состоящего из ФР и индикаторной системы;
ОП100% - оптическая плотность в контроле полного гемолиза, состоящего из воды очищенной и индикаторной системы.
Определяется разность степеней гемолиза в основной и контрольной системах для стандарта и испытуемого образца. Индекс Fc-функции испытуемого образца рассчитывается по формуле 2

где IFC - расчетная величина индекса Fc-функции испытуемого образца;
ΔYобр - разность степеней гемолиза в основной и контрольной системах для испытуемого образца;
ΔYBRP - разность степеней гемолиза в основной и контрольной системах для раствора сравнения;
100% - значение индекса Fc-функции раствора сравнения.
Если полученное значение индекса Fc-функции испытуемого образца превышает значение, указанное в паспорте раствора сравнения, считается, что исследуемый препарат обладает достаточной функциональной активностью.
Пример
Перед работой проводится трехкратное отмывание эритроцитов барана в физиологическом растворе натрия хлорида pH 7,0 (ФР), из отмытых эритроцитов готовится 3% суспензия. Полученная суспензия стандартизуется: 0,25 мл готовой суспензии гемолизируются в 1 мл воды очищенной, измеряется величина оптической плотности (ОП) при длине волны 540 нм против воды очищенной. Суспензия считается пригодной при величине ОП 1,2±0,1.
Определяется рабочее разведение гемолитической сыворотки (ГС). Готовится ряд разведений ГС от 1:1000 до 1:9000 с шагом 400. Затем для каждого разведения подготавливается индикаторная система (ИС): смешиваются 0,25 мл 3% суспензии эритроцитов барана и 0,25 мл готового разведения. Смеси инкубируются при 37°С в течение 30 мин. По окончании инкубации во все пробы добавляется по 0,25 мл маточного раствора комплемента морской свинки (разведение 1:10) и по 0,5 мл ФР. Для определения полного гемолиза смешиваются 1,0 мл воды очищенной и 0,25 мл 3% суспензии эритроцитов барана, для контроля самопроизвольного гемолиза - 1,0 мл ФР и 0,25 мл 3% суспензии. Все пробы инкубируются при 37°С 60 минут. По окончании инкубации пробы охлаждаются при 2-8°C в течение 10 минут, центрифугируются при 1500 об/мин в течение 10 минут, измеряется оптическая плотность (ОП) надосадочной жидкости при длине волны 540 нм против ФР. Рассчитывается степень гемолиза Y% согласно формуле 1.
За рабочее разведение (титр) ГС принимается максимальное разведение, при котором наблюдался полный гемолиз 3% суспензии. Для дальнейшего анализа готовится ИС: смешиваются равные объемы 3% суспензии и раствора гемолизина в двойном титре, смесь инкубируется при 37°C в течение 30 минут.
Далее определяется рабочее разведение комплемента морской свинки. Из маточного раствора комплемента (разведение 1:10) готовится 20 разведений в соответствии с таблицей 1.

В два ряда пробирок вносится по 0,25 мл из каждого разведения комплемента, добавляется по 0,5 мл ФР и 0,5 мл ИС. Для контроля самопроизвольного гемолиза - 0,75 мл ФР и 0,5 мл ИС, полного гемолиза - 0,75 мл воды очищенной и 0,5 мл ИС. Пробы инкубируются при 37°C в течение 60 минут. По окончании инкубации пробы охлаждаются при 2-8°C в течение 10 минут, центрифугируются при 1500 об/мин в течение 10 минут, измеряется ОП надосадочной жидкости при длине волны 540 нм против ФР. Рассчитывается степень гемолиза Y% согласно формуле 1. Строится график зависимости степени гемолиза от объема комплемента в пробе (по оси абсцисс - количество добавленного комплемента в мл; по оси ординат - степень гемолиза). За рабочее разведение комплемента принимается наименьшее разведение, при котором наблюдается полный гемолиз 3% суспензии. Данная величина соответствует 2 гемолитическим единицам (2 СН50/мл) комплемента. Готовится рабочее разведение комплемента, содержащее 2 СН50/мл.
Для приготовления основной системы для испытуемого образца и раствора сравнения в пробирки вносится объем препарата, содержащий 2,5 мг белка иммуноглобулина. Общий объем раствора доводится ФР до 0,25 мл. Затем добавляется 0,25 мл раствора антигена - вакцины коревой.
Для приготовления контрольной системы для испытуемого образца и раствора сравнения в пробирки вносится объем препарата, содержащий 2,5 мг белка иммуноглобулина, общий объем доводится до 0,5 мл физиологическим раствором.
Готовятся контрольные пробы: контроль активности комплемента, содержащий 0,5 мл ФР, и контроль спонтанного связывания комплемента антигеном, включающий 0,25 мл ФР и 0,25 мл антигена.
Основная и контрольная системы для испытуемого образца и раствора сравнения, контрольные пробы инкубируются при 37°C в течение часа.
По окончании инкубации в обе системы и контрольные пробы добавляется по 0,25 мл рабочего раствора комплемента с гемолитической активностью 2 СН50/мл. Пробы инкубируются при 2-8°C в течение 18 часов.
Затем во все смеси вносится по 0,5 мл свежеприготовленной ИС. Обе системы и контрольные пробы инкубируются при 37°C в течение часа. Измеряется ОП надосадочной жидкости при 540 нм и длине оптического пути 10 мм. Рассчитывается степень гемолиза Y% по формуле 1. Находится разность степеней гемолиза основной и контрольной систем для испытуемого образца. Аналогично находится разность степеней гемолиза основной и контрольной систем для раствора сравнения.
Рассчитывается индекс Fc-функции (IFc) испытуемого образца иммуноглобулина по формуле 2.
В таблице 2 представлены результаты определения индекса Fc-функции для испытуемого образца.

Величина индекса Fc-функции испытуемого образца составила 98,1%, что превышает значение, указанное в паспорте раствора сравнения - не менее 60%, следовательно, испытуемый препарат обладает достаточной функциональной активностью антител.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ВЛИЯНИЯ ПРЕПАРАТОВ НА ВЗАИМОДЕЙСТВИЕ КОМПЛЕМЕНТА С КОМПЛЕКСОМ АНТИГЕН-АНТИТЕЛО | 2017 |
|
RU2669342C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СТАБИЛИЗАЦИИ С3-КОНВЕРТАЗЫ КЛАССИЧЕСКОГО ПУТИ АКТИВАЦИИ КОМПЛЕМЕНТА ЧЕЛОВЕКА | 2013 |
|
RU2549468C2 |
| Скрининг-тест для определения функциональной активности классического пути системы комплемента | 2018 |
|
RU2704121C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛОЖИТЕЛЬНОГО КОНТРОЛЯ СТАНДАРТНОГО ОБРАЗЦА ИММУНОГЛОБУЛИНА ЧЕЛОВЕКА ДЛЯ ОПРЕДЕЛЕНИЯ АНТИКОМПЛЕМЕНТАРНОЙ АКТИВНОСТИ ПРЕПАРАТОВ ИММУНОГЛОБУЛИНОВ ЧЕЛОВЕКА, И СТАНДАРТНЫЙ ОБРАЗЕЦ ИММУНОГЛОБУЛИНА ЧЕЛОВЕКА ДЛЯ ОПРЕДЕЛЕНИЯ АНТИКОМПЛЕМЕНТАРНОЙ АКТИВНОСТИ ПРЕПАРАТОВ ИММУНОГЛОБУЛИНОВ ЧЕЛОВЕКА | 2015 |
|
RU2577703C1 |
| СПОСОБ ПОСТАНОВКИ РЕАКЦИИ СВЯЗЫВАНИЯ КОМПЛЕМЕНТА | 1992 |
|
RU2057345C1 |
| СПОСОБ ОЦЕНКИ СОСТОЯНИЯ ИММУННОЙ СИСТЕМЫ ОРГАНИЗМА ЧЕЛОВЕКА | 2006 |
|
RU2314529C1 |
| Способ определения активности классического и альтернативного путей системы комплемента мыши | 2022 |
|
RU2800363C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НАРУШЕНИЯ ИММУННОГО СТАТУСА | 2002 |
|
RU2247381C2 |
| Скрининг-тест для определения функциональной активности системы комплемента крысы | 2022 |
|
RU2786208C1 |
| СПОСОБ ЭКСПРЕСС-ДИАГНОСТИКИ АНТИГЕНОВ ЭНТЕРОВИРУСОВ В ЦЕРЕБРОСПИНАЛЬНОЙ ЖИДКОСТИ | 2012 |
|
RU2486520C1 |
Изобретение относится к медицине и касается способа определения FC-функции препаратов иммуноглобулина человека на основе реакции связывания комплемента, в котором оценивается степень гемолиза сенсибилизированных антителами кролика эритроцитов барана в основной системе, включающей растворы иммуноглобулина, антигена, комплемента, и контрольной системе, содержащей растворы иммуноглобулина, ФР (физиологического раствора) и комплемента; определяется разность степеней гемолиза в основной и контрольной системах, рассчитывается индекс FC-функции путем деления разности степеней гемолиза в двух системах для испытуемого препарата на разность степеней гемолиза в двух системах для раствора сравнения с известной величиной индекса FC-функции. Изобретение обеспечивает возможность выполнения способа определения FC-функции препаратов иммуноглобулина человека без использования сложного аппаратурного оснащения, простоту в интерпретации результатов. 1 пр., 2 табл.
Способ определения FC-функции препаратов иммуноглобулина человека на основе реакции связывания комплемента, отличающийся тем, что оценивается степень гемолиза сенсибилизированных антителами кролика эритроцитов барана в основной системе, включающей растворы иммуноглобулина, антигена, комплемента, и контрольной системе, содержащей растворы иммуноглобулина, ФР (физиологического раствора) и комплемента, в соответствии с формулой (1)
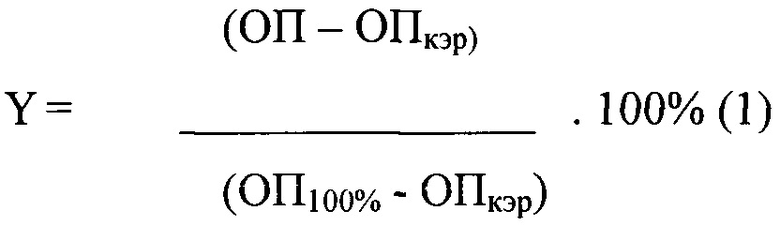
где Y - степень гемолиза в пробе, %;
ОП - оптическая плотность в пробе;
ОПкэр - оптическая плотность в контроле самопроизвольного гемолиза эритроцитов, состоящего из ФР и индикаторной системы;
ОП100% - оптическая плотность в контроле полного гемолиза, состоящего из воды очищенной и индикаторной системы,
где индикаторная система состоит из стандартизованной суспензии эритроцитов барана и гемолизина - сыворотки крови иммунизированных эритроцитами барана кроликов;
определяется разность степеней гемолиза в основной и контрольной системах, рассчитывается индекс FC-функции путем деления разности степеней гемолиза в двух системах для испытуемого препарата на разность степеней гемолиза в двух системах для раствора сравнения с известной величиной индекса FC-функции в соответствии с формулой (2)

где IFC - расчетная величина FC-функции испытуемого образца;
ΔYобр - разность степеней гемолиза в основной и контрольной системах для испытуемого образца;
ΔYBRP - разность степеней гемолиза в основной и контрольной системах для раствора сравнения.
| ПРЕПАРАТЫ АНТИТЕЛ | 2011 |
|
RU2617532C2 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| GEORGAKOPOULOS ET AL., An improved Fc function assay utilizing CMV antigen-coated red blood cells generated with synthetic function-spacer-lipid constructs.Vox Sang | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| GUREVICH V., et al., Determination of Fc function with frozen red blood cells.Biologicals | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2018-07-06—Публикация
2017-06-06—Подача