Область техники изобретения
Настоящее изобретение применяется в медицине, в частности, при диагностировании болезней Альцгеймера и Паркинсона.
Предпосылки создания изобретения
Болезнь Альцгеймера (БА) является наиболее частой причиной деменции. Для полного развития настоящей болезни требуются десятилетия, сопровождающиеся предсимптоматическими эффектами других дегенеративных деменций, первые клинические признаки которых проявляются в виде легких когнитивных нарушений (ЛКН). Зачастую первые симптомы БА ошибочно списывают на старение или стресс.
В настоящее время диагностирование БА осуществляется на основании анамнеза человека, истории болезней родственников и наблюдений за поведением. Посредством подробных нейропсихологических тестов за несколько лет до достижения человеком клинических критериев могут быть обнаружены когнитивные нарушения для диагностирования БА. Малозаметные проблемы со способностью к целенаправленной деятельности, внимательностью, планированием, гибкостью и абстрактным мышлением или нарушения семантической памяти также могут являться клиническими симптомами. Течение заболевания может быть дополнительно определено посредством оценки умственной деятельности, включая тесты на память.
Все попытки практикующих врачей по созданию диагностических критериев, которые могут поспособствовать упрощению и стандартизации процесса диагностирования, ориентируются на эти параметры. В настоящее время для диагностирования БА требуется гистопатологическое подтверждение, включающее гистологическое исследование мозговой ткани.
Текущее определение или диагностирование БА выполняется в клинических условиях. В большинстве случаев в клиническом диагнозе отсутствуют биологические маркеры. Только в моногенетических случаях известные случаи БА имеют генетические маркеры, и они составляют менее 2% случаев заболевания. Открытие Кейном того, что аллель АроЕ4 - фактор риска развития деменции альцгеймеровского типа, повышающий риск и влияющий на возраст манифестации, имел более научное, нежели клиническое значение, и обладает невысокой полезностью при диагностировании (Кейн Р.А., Кейн Р.Л. «Влияние генетических тестов на риск возникновения болезни Альцгеймера». Мед. журнал Новой Англии, 2009, 361(3), 298-299).
Наилучшие способы обнаружения биомаркеров БА включают исследования с визуализацией мозга при магнитно-резонансной или позитронно-резонансной томографии, и такие белки, как бета-амилоид и тау-белок в спинномозговой жидкости (СМЖ). Упор при исследовании БА делался на диагностирование состояния до начала проявления симптомов. Для обеспечения возможности раннего распознавания БА был использован и разработан ряд биомаркеров и биохимических анализов.
Некоторые из наибольших недостатков применения тестов на основе белков включают в себя повышенную себестоимость, необходимость в инвазивных методах и сложности, связанные с интерпретацией результатов, что делает невозможным их длительное использование. Например, нейровизуализация кортикальной амилоидной инфильтрации и объемные изменения в мозгу, а также оценка концентрации белков в СМЖ - диагностические средства, широко не представленные.
Уровень белков автолизосом в крови также может показать отличия между контрольными группами и зараженным населением с периодичностью от 1 до 10 лет перед диагностированием (Гетцль и соавт.«Измененные лизосомальные белки в экзосомах нейронов плазмы при болезни Альцгеймера в преклинической фазе». Neurology 2015, 7 июля; 85(1):40-7). Во время другого недавнего исследования были проверены некоторые ранее описанные биомаркеры, по которым можно прогнозировать деменцию на предшествующих стадиях (Хие и соавт. «Прогнозирование начала деменции на предшествующем болезни этапе с помощью белков плазмы». Alzheimer's & Dementia 2014, 10, 799-807). При этом все эти исследования были сконцентрированы на наборе или выборке биомаркеров, включая белки, липиды или другие метаболиты. В целом, биомаркеры находятся между молекулами из бета-амилоидов и тау-белков. Эти потенциальные биомаркеры служат показателями уже начавшегося заболевания, не оставляя возможности для действительно раннего распознавания или прогнозирования. В данном случае настоящее изобретение хорошо согласуется с научным консенсусом о необходимости диагностирования на стадии преддеменции при БА.
Некоторое время назад были опубликованы несколько работ, в которых описывались молекулярные или биохимические изменения, поддающиеся обнаружению, перед проявлением ранних симптомов деменции, таких как снижение уровня фосфолипидов в плазме (Мэпстоун и соавт.«Определение нарушений памяти, предшествующих болезни, у пожилых пациентов с помощью фосфолипидов в плазме» Nat. Med., 2014, 20 (4) 415-420). В данном исследовании удалось предсказать проявление ЛКН или БА в течение 2-3 лет с помощью выборки из десяти липидов из периферической крови. Ограничение по времени значительно.
В поисках более ярко выраженных клинических фенотипов для интеграции биомаркеров в процесс диагностирования и в целях определения болезнь-модифицирующих и превентивных видов терапии представляет интерес недавняя попытка Дюбуа по постановке диагноза преддеменции при БА, основанная на строгих клинических критериях, тестах с нейровизуализацией и биологических данных, полученных, в основном, из СМЖ (Дюбуа и соавт.«Передовые исследования критериев диагностирования болезни Альцгеймера». Lancet Neurol, июнь 2014; 13(6): 614-29). При этом текущие биомаркеры дали неудовлетворительный результат, так как они или инвазивны, или времязатратны, или дороги, включая их уровень выраженности в СМЖ или при структурной и функциональной магнитно-резонансной томографиях.
В заявке US 20140602046 А1 описывается лечение БА, включающее введение специфических антител против пептидов, взятых из тау-белка. В этом документе указываются медленное развитие болезни и профилактика для бессимптомных субъектов. Профилактическое введение рекомендуется всему населению старше 10 лет. Как было указано выше, весьма вероятно, что тау-изомеры, подлежащие обнаружению, образуются в организме после развития болезни, что исключает прогнозирование.
В заявке US 20110236917 А1 описывается метод диагностирования БА у субъекта, включающий обнаружение выборки из сорока семи (47) белков-биомаркеров в образце сыворотки, взятом у субъекта. В числе маркеров в выборке указываются трансферрин I и II. Первый недостаток этих идей -необходимость наличия образца сыворотки, для извлечения которой необходим профессиональный практический врач. Кроме того, отсутствуют предположения о получении более точной информации с помощью какого-либо конкретного белка из представленных в наборе. На основании идей в этом документе специалист не смог бы самостоятельно найти какой-либо белок, конкретно отвечающий за диагностику БА у субъекта. Безусловно, идеальный одиночный биомаркер, позволяющий осуществлять прогнозирование или раннее распознавание БА, на данный момент обнаружен не был.
В нескольких линиях исследований указывалось на возможную связь воспалительного процесса в мозгу и гигиены полости рта. В последнее время количество публикаций, касающихся протеома слюны, значительно возросло, и в качестве биологической жидкости для диагностики в них предлагается человеческая слюна. В плане низкой инвазивности, минимальной стоимости и легкости сбора и обработки слюна обладает множеством преимуществ. Было описано наличие белков А и тау-белков в человеческой слюне и выдвинуто предположение об их полезности в качестве возможного биомаркера БА (Ши и соавт.«Образцы тау-белков из слюны - возможные биомаркеры болезни Альцгеймера». J Alzheimer's Dis, 2011; 27(2):299-305). Другие белки были описаны в образцах слюны, включая те, которые связывались с воспалительными реакциями и патогенезом БА (Сирегиа и соавт. «Многодисциплинарный подход к исследованиям пары однояйцевых близнецов, дискордантных по синдрому хронической усталости: исследование возможных биомаркеров в слюне». J Transl Med., 2 октября 2013; 11:243).
По этому поводу в документе WO 2013/153461 А2 описывается диагностирование БА после выбора двух биомаркеров из набора молекул, имеющегося в слюне. И снова указанные белки скорее показательны в отношении уже начавшейся болезни и, следовательно, полученные результаты не могут быть использованы для прогнозирования болезни.
Лактоферрин - это железосвязывающий гликобелок из семейства трансферринов, широко применявшийся при диагностировании воспалительных заболеваний. Эта молекула подавляет выработку воспалительных цитокинов и модулирует окислительный стресс. Она также ассоциируется с защитой мозговой ткани от окислительного повреждения при прочих нейродегенеративных болезнях, включая болезнь Паркинсона (БП), и она также была обнаружена в нейрофибриллярных клубках тау-белка и бета-амилоидных (АВ) сенильных бляшках, что является главными гистопатологическими признаками БА наряду со смертью нейронов (Вон и соавт.«Накопление лактоферрина в фибриллярных сенильных бляшках в мозгу моделей линий трансгенных мышей с болезнью Альцгеймера». Neurosci Lett 2010; 481: 164-7). Данный белок - один из компонентов человеческих выделений, синтезируемый экзокринными железами и нейтрофилами на участках заражения/воспаления. Среди слюнных белков это наиважнейший фактор естественного иммунитета, представляющий собой важный защитный фактор от бактериальных заболеваний в слюне.
В работе Уеллинга приводятся некоторые антимикробные пептиды (АМП), которые могут проникать за гематоэнцефалический барьер (ГЭБ) (Уеллинг М. и соавт.«Возможное влияние антимикробных пептидов на раннюю манифестацию болезни Альцгеймера». Alzheimer & Dementia, 11, с. 51-57, 2015). В данной публикации освещается способность лактоферрина пересекать ГЭБ при введении пациенту или выполнять регуляцию с повышением при инфекционных процессах. Кроме того, в ней предлагается возможное использование АМП при обнаружении инфекций головного мозга in vivo. При этом любая связь, которую можно было бы установить между моментом обнаружения регуляции с повышением при инфекционном процессе и эффективным использованием при диагностике БА, спорна.
При этом согласно документу US 2003/0096736 А1 лактоферрин доказал полезность при лечении нескольких заболеваний, включая нейродегенеративные и, в частности, БА. Отсутствуют связь или намек на молекулу, используемую для диагностирования или прогнозирования каких-либо других нейродегенеративных заболеваний, в частности, БА.
На существующем уровне техники не раскрывается использование лактоферрина при диагностировании и/или прогнозировании БА.
Документ WO 2009074331 A3 считается ближайшим аналогом настоящего изобретения. Цель настоящего документа - описание метода раннего распознавания БА, включающего обнаружение продуцируемого белка из нескольких генов в биологическом образце субъекта. В настоящие биомаркеры включены производные гена с трансферрином (ТФ), а также производные других генов, таких как IGF-1R или HISTIH3E. Предлагаемые гены не имеют отношения друг к другу на биологическом основании, и все они демонстрируют прогностическую ценность, которая будет использована в настоящем методе. В частности, среди других производных для использования не предлагается производный продукт гена с ТФ, а также лактоферрин. Получаемая область применения в рамках продуктов гена нецелесообразна, и она влечет неоправданный объем работы для специалиста по проверке диагностики настоящего заболевания. Несмотря на то, что указывается, что биологический образец включает слюну, примеры приведены на основании образцов крови. В этом документе определяется главная проблема методов диагностики, заключающаяся в том, что на существующем уровне техники можно обнаруживать болезнь только у пациентов, уже страдающих от нее. Тем самым, невозможно обеспечить прогнозирование и возможную профилактическую меру. Однако, несмотря на ожидания авторов, необходимо сказать, что проблема остается нерешенной. В действительности, у проверяемых генов HIST3H3E и CNR2 у испытуемых популяций пациентов прослеживается возможность демонстрации наличия болезни, которая, при этом, не представляет какой-либо пользы для прогнозирования. К тому же, ни один из них не имеет отношения к лактоферрину.
Проблема на существующем уровне техники по-прежнему заключается в обнаружении единого биомаркера для диагностирования или прогнозирования болезни Альцгеймера. Решение, предлагаемое по настоящему изобретению, представляет собой метод определения уровня лактоферрина у субъекта.
Что касается БП, из существующего уровня техники известна нейрональная регуляция с повышением лактоферрина в мозгу пациентов (Фоше Б.А. и соавт.«Повышенная экспрессия рецепторов лактоферрина в мезэнцефалоне пациентов с болезнью Паркинсона». Proc Natl Acad Sci USA 92, 9603-9607, 1995; Левегль Б., и соавт.«Клеточное распространение лактотрансферрина железосвязывающего белка в мезэнцефалоне при болезни Паркинсона». Acta Neuropathol 91, 566-5726, 1996). При этом, насколько известно изобретателям, на существующем уровне техники не упоминается или не предполагается регуляция белка в слюне. Забегая вперед, прямую связь с наличием метаболитов в каждой биологической жидкости установить невозможно.
Проблема в отношении БП заключается в нахождении одного биомаркера для диагностирования этой болезни. Решение, предлагаемое по настоящему изобретению, представляет собой метод определения уровня лактоферрина в слюне.
Описание изобретения
Настоящее изобретение представляет собой лактоферрин, или молекулу нуклеиновой кислоты, кодирующую его, для применения при диагностировании или прогнозировании БА. В предпочтительном аспекте диагностирование или прогнозирование выполняются с помощью биологического образца, взятого у субъекта из слизистой ткани (предпочтительно из слизистой ротовой полости) и слюны. Как альтернативный вариант, по настоящему изобретению для диагностирования или прогнозирования БА используется лактоферрин из слюны или образца слюны субъекта.
В рамках объема настоящего изобретения термин «диагностирование» предполагает определенную степень развития болезни, которую можно определить у пациентов, независимо от того, является ли это БА или первыми симптомами ЛКН на одной из его стадий.
В рамках объема настоящего изобретения под термином «прогнозирование» понимается предугадывание БА при отсутствии феноконверсии симптомов, которые можно обнаружить у здорового пациента.
В отношении белка лактоферрина, указанного в пробном диагностическом исследовании, были получены значения точек разделения белков. Прогностическая ценность феноконверсии в ЛКН/БА составила 7,43 мкг/мл. Это значит, что у всех субъектов с диагнозом ЛКН или БА наблюдались значения лактоферрина в слюне менее 7,43 мкг/мл, а у всех здоровых пациентов из контрольной группы значения лактоферрина в слюне составили более 7,43 мкг/мл.
Исходя из этого, другой аспект настоящего изобретения представляет собой метод диагностирования БА у субъекта, включающий оценку уровня лактоферрина в слюне или образце слюны этого субъекта, и определение, выше ли этот уровень или ниже значения 7,43 мкг/мл, причем значение менее 7,43 мкг/мл является показателем БА. Если уровень лактоферрина менее 7,43 мкг/мл, и у субъекта наблюдается феноконверсия в неврологическое заболевание, настоящий метод является показателем БА.
Другой предпочтительный аспект настоящего изобретения представляет собой метод прогнозирования БА у субъекта, включающий оценку уровня лактоферрина в слюне или образце слюны этого субъекта, и определение, выше ли эта концентрация или ниже значения 7,43 мкг/мл, причем значение менее 7,43 мкг/мл является показателем прогнозирования БА. Если уровень лактоферрина менее 7,43 мкг/мл, и у субъекта не наблюдается феноконверсия в неврологическое заболевание, настоящий метод является показателем прогнозирования БА.
При настоящем варианте применения прослеживаются низкие уровни лактоферрина в слюне пациентов с ЛКН и БА в сравнении с контрольной возрастной группой, что дает основания полагать, что этот белок задействуется на ранних стадиях БА. Предполагается, что показания пониженного уровня лактоферрина в слюне свойственны патологии при БА.
В рамках объема настоящего изобретения определение наличия лактоферрина в слюне не предполагает какого-либо инвазивного или хирургического вмешательства, что могло бы повлечь существенный риск для здоровья субъекта, независимо от того, проводилось бы такое определение способом ех-vivo или in-vivo.
В настоящей заявке продемонстрировано, что по разным уровням лактоферрина в слюне, несомненно, можно отделить субъектов с нормальной когнитивной деятельностью, у которых разовьются либо ЛКН, либо БА в течение 5 лет, от субъектов, чья когнитивная деятельность останется нормальной в будущем. Насколько нам известно, это первый описанный единый биомаркер, по которому можно предугадать феноконверсию в течение 5 лет со 100% вероятностью. - С помощью настоящего изобретения даже можно спрогнозировать феноконверсию ЛКН и/или БА из здорового состояния в течение 9 лет.
При логистическом регрессивном анализе с использованием сочетаний уровней содержания лактоферрина в слюне и возраста на момент отбора образца слюны субъекты были точно поделены на группы молодых и пожилых людей (фиг. 5А), а в группе пожилых - на подверженных феноконверсии до ЛКН/БА и не подверженных ей (фиг. 5В).
Время на феноконверсию было определено посредством анализа линейной регрессии с использованием связи между уровнем содержания лактоферрина в слюне и манифестации феноконверсии. Нижний уровень содержания лактоферрина в настоящей модели был связан с повышенным риском феноконверсии до БА (фиг. 6). Было выяснено, что уровень содержания лактоферрина в слюне соотносился со временем манифестации феноконверсии.
В связи с этим при регрессивном анализе было получено уравнение
у=0,6289х+1,6954
в котором приведено соотношение уровня содержания лактоферрина в крови и время манифестации в годовом исчислении. В этой формуле значение «у» - это уровень содержания лактоферрина в слюне, а «х» - время феноконверсии в годах. Применение настоящего уравнения в гипотетическом случае относительно субъекта с уровнем лактоферрина в слюне менее значения точки разделения, например, 7,43 мкг/мл, получившийся промежуток времени составляет более 9 лет на феноконверсию до ЛКН/БА.
Таким образом, по другому предпочтительному аспекту прогнозируемый промежуток времени до проявления феноконверсии до БА у субъекта составляет до девяти лет, а предпочтительнее - до восьми, семи, шести или пяти лет.
В другом предпочтительном аспекте настоящего изобретения субъект представлен млекопитающим, а предпочтительнее - человеком.
Что касается слюны, аналогичные результаты, полученные посредством слез и слизистого осадка из ротовой полости, указывают на то, что уровень содержания лактоферрина, полученный из периферийных неинвазивных образцов из организма, может быть использован в качестве средства диагностирования БА. Возможно, что лактоферрин в слюне представляет собой первую линию защиты даже до обнаружения патологических и/или клинических изменений в мозге, и снижение уровня его содержания у субъектов с ЛКН может рассматриваться как ранний биомаркер БА.
Более того, аналогичное снижение уровня содержания лактоферрина в слюне также прослеживалось на слизистой ротовой полости. Этот результат был получен во время предварительного исследования с двумя группами, здоровыми пациентами из контрольной группы и группами с БА, разделенными на пары по возрасту и полу. Уровень содержания лактоферрина у пациентов с БА был существенно снижен по сравнению со здоровыми субъектами из контрольной группы, составляя 4,35±0,88 мкг/мл у больных БА против 10,78±1,9 мкг/мл. Данные выражены в виде среднего значения ± среднеквадратическое отклонение (СО).
Согласно модели, использованной в настоящем изобретении, были установлено деление на группы с заболеваниями (ЛКН/БА) и здоровые субъекты из контрольной группы со значением AUC 1 и доверительным интервалом (ДИ) 95% с отношением (1-1) для больных ЛКН/БА к контрольной группе (фиг. 4 В). Однако эти данные не воспроизводимы либо в образцах крови, либо СМЖ.
На основании этих результатов было предложено рассматривать любой железосвязывающий белок из семейства трансферринов в качестве потенциального маркера БА.
Другим предпочтительным аспектом является набор для использования метода по настоящему изобретению, включающий как минимум один реактив для количественного выражения содержания лактоферрина в слюне или образце слюны субъекта, и позволяющий проводить сопоставление этого количественного выражения с заданным значением точки разделения, предпочтительно составляющим 7,43 мкг/мл. В более предпочтительном аспекте реактив представлен антителом, специфичным для лактоферрина.
В рамках объема настоящего изобретения предполагается, что антитело, специфичное для лактоферрина, должно выявлять конкретно лактоферрин.
Другим предпочтительным аспектом является набор, включающий как минимум одну емкость, содержащую специфические фармацевтические композиции для количественного выражения лактоферрина в слюне или образце слюны субъекта, инструкции по применению этих композиций и норму для определения повышенного или пониженного содержания лактоферрина в сравнении с заданным значением точки разделения (предпочтительно 7,43 мкг/мл), показательным для БА или риска развития БА у этого субъекта.
В настоящем изобретении предлагается возможность постановки диагноза или осуществления прогноза для большого количества пациентов в других центрах, а не только в тех, где были взяты биологические образцы. В этом смысле дополнительный аспект настоящего изобретения представляет собой систему для предугадывания развития БА у субъекта, включающую средства обработки информации, которые настраиваются для оценки уровня содержания лактоферрина в образце слюны или молекуле нуклеиновой кислоты, кодирующей его, для установления пониженного уровня лактоферрина по сравнению с заданным значением точки разделения (предпочтительно 7,43 мкг/мл) и функционального исхода БА у субъекта по результатам предыдущего определения.
С другой стороны, уровень содержания лактоферрина в слюне пациентов с болезнью Паркинсона (БП) оказался существенно выше, чем у здоровых субъектов из контрольной группы (фиг. 2В). Попарное сопоставление между группами с БП и здоровыми субъектами из контрольной группы продемонстрировало существенные изменения: 12,61±3,31 мкг/мл у больных БП против 10,78±1,0 мкг/мл у здоровых субъектов из контрольной группы. Данные выражены в виде среднего значения ± СО. Как указывалось ранее, эти результаты соответствуют нейрональной регуляции с повышением лактоферрина у пациентов с БП.
Также обнаружена связь количества лактоферрина у пациентов с БП. Так, другой аспект настоящего изобретения относится к лактоферрину или молекуле нуклеиновой кислоты, кодирующей его, и их использованию при диагностировании болезни Паркинсона с помощью слюны или образца слюны субъекта. В предпочтительном аспекте настоящего изобретения субъект представлен млекопитающим, а предпочтительнее - человеком.
Краткое описание чертежей
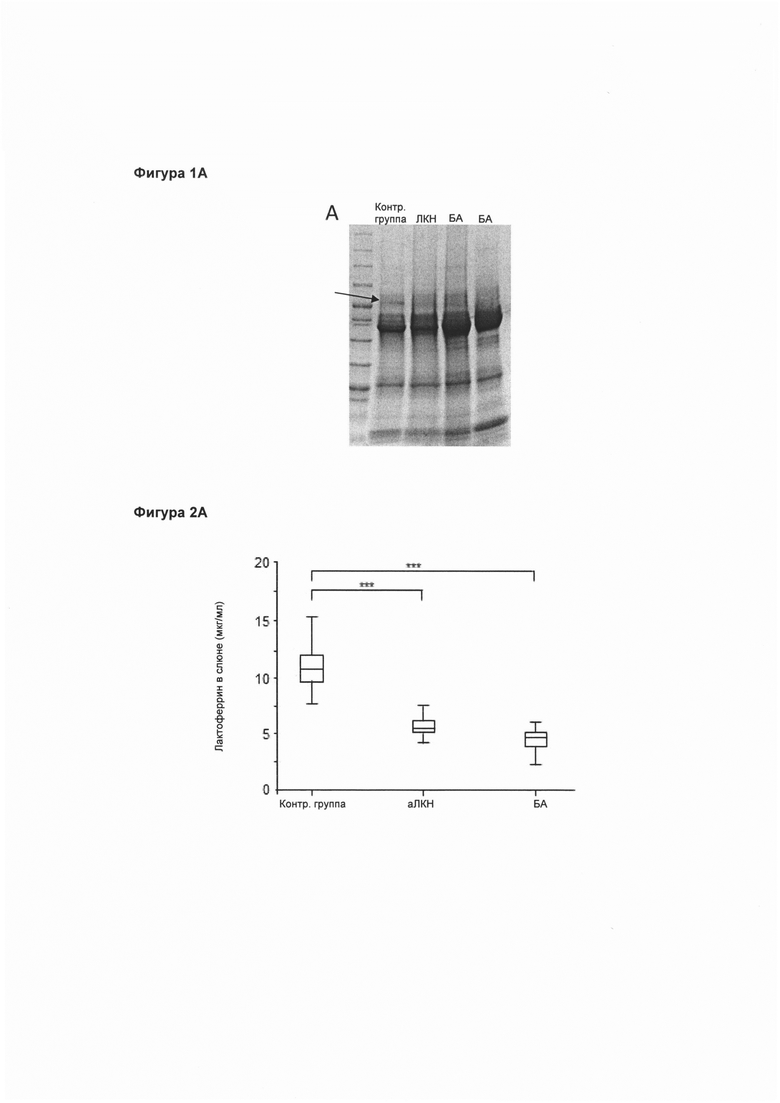
На Фигуре 1А представлена полоса лактоферрина 75 кДа после фракционирования при ДСН-ПААГ-электрофорезе, присутствующая во всех образцах. Определение лактоферрина в человеческой слюне в группах, страдающих ЛКН, БА, и у здоровых представителей контрольных групп. Окрашивание синим красителем кумасси в ДСН-ПААГ, соответствующим выборке слюны. Дорожка 1 - контрольная группа; дорожка 2 - группа с ЛКН; дорожки 3 и 4 - группа с БА. Полоса, соответствующая 75 кДа, обозначена стрелкой.
На фигуре 2А представлены уровни содержания лактоферрина в слюне, измеренные с помощью набора ELISA для людей, которые понизились у пациентов с ЛКН и БА по сравнению с контрольной группой.
На Фигуре 2В представлены уровни содержания лактоферрина в слюне, измеренные с помощью набора ELISA для людей, которые повысились у пациентов с ЛКН и БА по сравнению с контрольной группой.
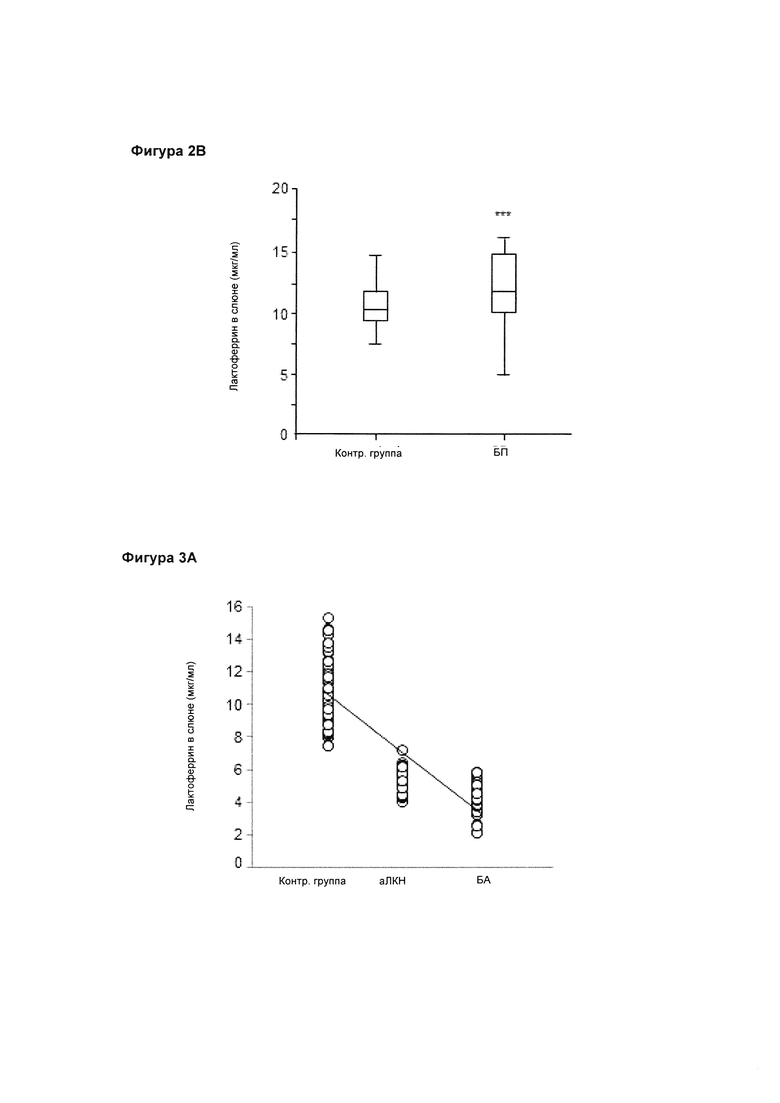
На Фигуре 3А представлена связь уровня содержания лактоферрина в слюне и падения когнитивных способностей в группах с ЛКН и БА. Это отношение было в основном обусловлено существенной отрицательной связью между стадиями заболевания и уровнем лактоферрина (R=-0,74; р<0,001).
На фигуре 3В представлена связь уровней содержания лактоферрина в слюне и баллов по КШОПС (краткой шкале оценки психического статуса), а также эффективность когнитивной функции у пациентов с ЛКН и БА (R=0,73; р<0,001).
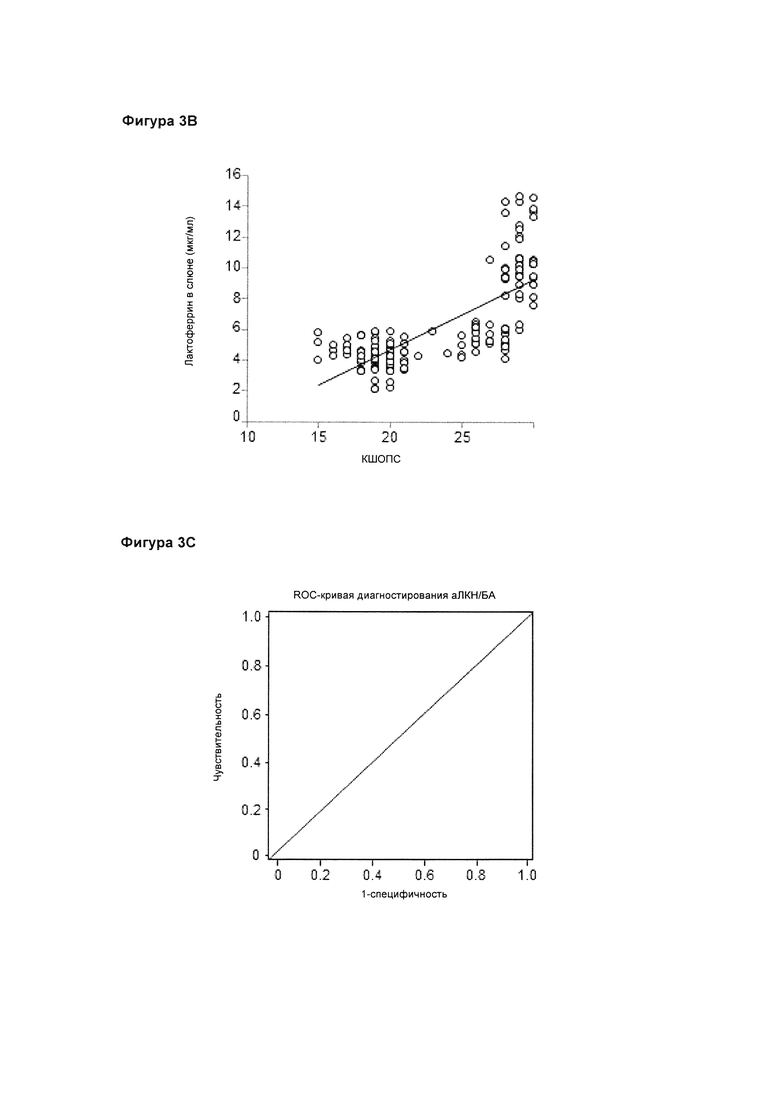
На Фигуре 3С представлена ROC-кривая по тесту на уровень содержания лактоферрина, полученная по всей контрольной группе и группе с ЛКН/БА. На ROC-кривой приведена чувствительность (истинный коэффициент позитивности) по отношению к 1-специфичности (ложный коэффициент позитивности). Площадь под фармакокинетической ROC-кривой AUC=1 (95% ДИ 1-1).
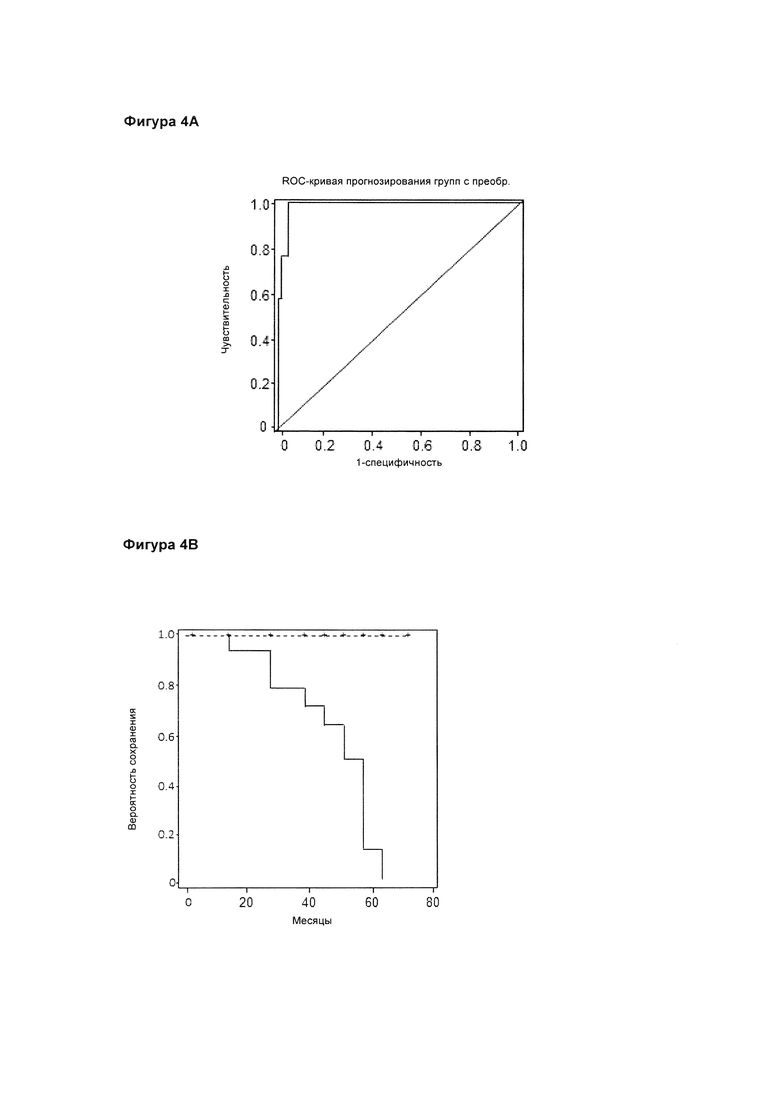
На фигуре 4А представлена кривая соотношений правильного и ложного обнаружения сигналов (ROC) по тесту на уровень содержания лактоферрина, полученная по всей контрольной группе и группе с преобразованиями. На ROC-кривой приведена чувствительность (или истинный коэффициент позитивности) по отношению к 1-специфичности (или ложный коэффициент позитивности). В данной системе с бинарным классификатором (ROC-кривая) была получена устойчивая площадь под фармакокинетической кривой (ROC-кривой) со значением AUC=0,984 (95% ДИ 0,932-1). AUC - мера того, насколько сильно может выделяться параметр в двух диагностических группах, с доверительным интервалом (ДИ) 95% от 0,93 до 1.
На фигуре 4В представлен переход к уровню содержания лактоферрина в слюне, свойственному либо аЛКН, либо БА. На изображении представлено среднее время феноконверсии либо для группы с аЛКН, либо для группы с БА в зависимости от аномально пониженного (положительные показатели) или нормального/высокого (отрицательные показатели) уровней содержания лактоферрина на основании модели пропорциональных рисков Кокса. Пунктирной линией обозначены отрицательные показатели. Сплошной линией обозначены положительные показатели.
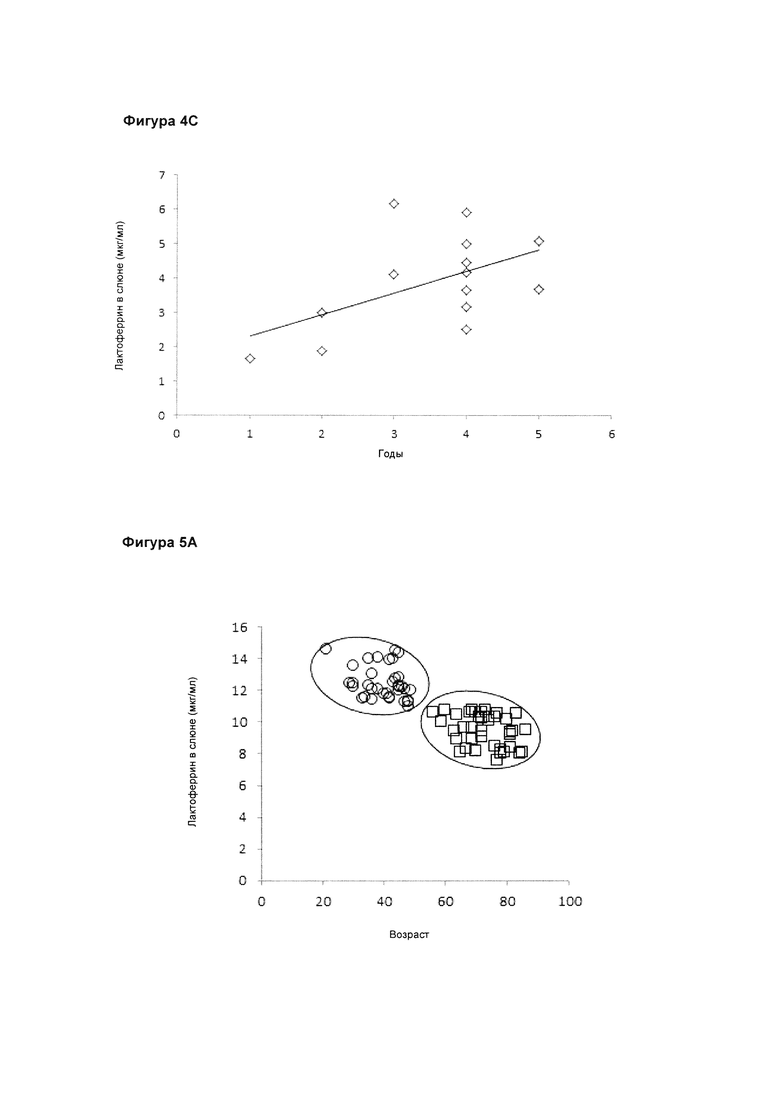
На фигуре 4С приведен логистический регрессивный анализ с использованием значений экспрессии лактоферрина и времени манифестации или феноконверсии в годовом исчислении. Уравнение, полученное с помощью регрессивного анализа, имело вид у=0,6289х+1,6954.
На Фигуре 5А представлен регрессивный анализ с использованием значений содержания лактоферрина в слюне и возраста в качестве точных средств измерения для классификации группы как молодых, так и пожилых людей, ○ Молодые без деменции; □ Пожилые с деменцией.
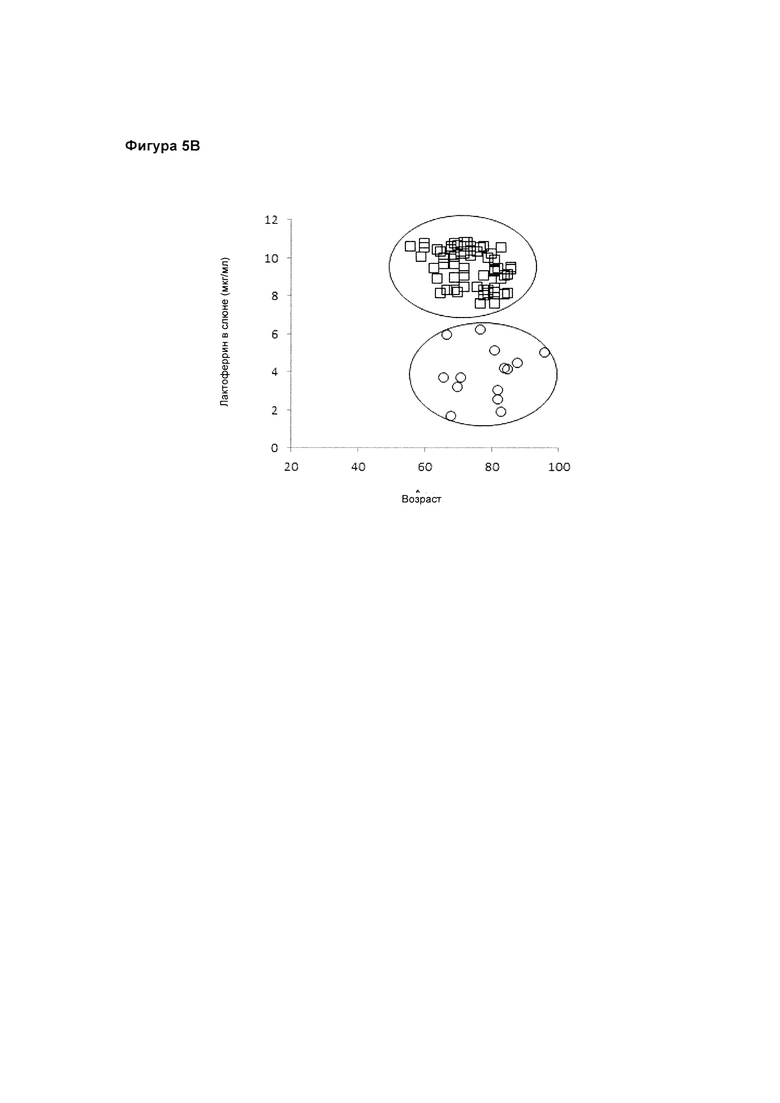
На Фигуре 5В представлен регрессивный анализ с использованием значений экспрессии лактоферрина в слюне и возраста в качестве точных средств измерения для классификации группы как группы пожилых людей (без феноконверсии), так и группы с феноконверсией в ЛКН и БА. ○ С феноконверсией; □ Пожилые без деменции.
Примеры
Следующие примеры приведены с целью наглядной, но не ограничивающей демонстрации настоящего изобретения.
Пример 1. Получение образцов слюны
Пробное диагностическое исследование проводилось на 274 участниках в отделении неврологии Университетского госпиталя 12 октября (Мадрид, Испания). Были определены четыре (4) группы субъектов, подобранные по возрасту, согласно состоянию когнитивной функции: аЛКН, БА, группа с болезнью Паркинсона (БП) и контрольная группа без когнитивных нарушений (таблица 1). Относительно пациентов с БА диагноз устанавливался в Национальном институте неврологических и коммуникативных расстройств и инсульта и по методическим рекомендациям Ассоциации болезни Альцгеймера и сопутствующих заболеваний (NINDS-ADRDA) (МакХанн и соавт. «Диагностирование деменции в результате болезни Альцгеймера: рекомендации от Национального института по проблемам старения-рабочих групп Ассоциации Альцгеймера по методике диагностики болезни Альцгеймера». Alzheimer's Dement. 2011; 7: 263-9). Диагностика пациентов с БП выполнялась по критериям вероятной болезни Паркинсона (Гельб и соавт.«Критерии диагностирования болезни Паркинсона"). Arch Neurol, январь 1999; 56(1):33-9). Также после того, как пациенты с когнитивными нарушениями показали несоответствие критериям деменции, была добавлена группа пациентов с ЛКН (Педерсен. «Легкие когнитивные нарушения как элемент диагностики». J Intern Med 2004; 256: 183-94). Тяжесть заболевания оценивалась по баллам краткой шкалы оценки психического статуса (КШОПС). Согласно Хельсинкской Декларации было получено согласие субъектов, а также одобрение от Комитета исследовательской этики в Госпитале 12 октября. Нестимулированный цельный образец слюны был помещен в стерильные пластмассовые емкости с предварительным покрытием раствором натриевой соли 2%, как было приведено ранее в работе Бермехо-Пареха (Бермехо-Пареха и соавт.«Уровень содержания бета-амилоида 1-42 как потенциальный биомаркер болезни Альцгеймера: предварительное исследование». ВМС Neurol 2010; 10: 108). Отобранные образцы были незамедлительно помещены на лед и предварительно очищены при малой скорости вращения центрифуги 600 g в течение 10 мин при 4°С. Разделенные на ал и квоты образцы по 0,5 мл хранились при -80°С после обработки смесью ингибиторов протеаз (Roche). Результаты оценки белков были проанализированы с помощью набора белковых спектров с бицинхониновой кислотой (Pierce, Рокфорд, шт. Иллинойс) согласно инструкциям производителя.
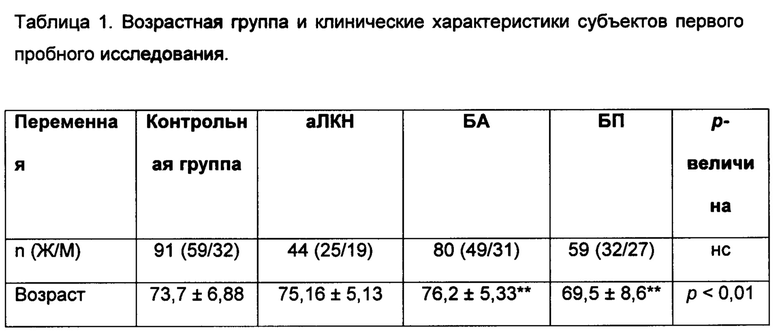

М = мужчина; Ж = женщина; аЛКН = амнестическое легкое когнитивное нарушение; БА = болезнь Альцгеймера; БП = болезнь Паркинсона; КШОПС = баллы по краткой шкале оценки психического статуса; Н/П = не применимо; нз = незначительный. Данные выражены в виде среднего значения ± СО. **р<0,01 в сравнении с контрольной группой; ***р<0,001 в сравнении с контрольной группой.
Пример 2: измерение концентрации лактоферрина в образцах слюны
В объединенных выборках, взятых у пациентов с БА, были замерены уровни экспрессии человеческого лактоферрина (ПОСЛЕДОВАТЕЛЬНОСТЬ №: 1) в сравнении с донорами из группы с ЛКН и контрольной группы. Образцы слюны, взятые у 4 субъектов мужского пола в каждой группе (ЛКН, БА и пожилые люди без деменции из контрольной группы) были объединены в выборку посредством смешивания в равных пропорциях. 50 мкг из каждой выборки были помещены на ДСН-ПААГ. После фракционирования при ДСН-ПААГ-электрофорезе во всех образцах была обнаружена полоса 75 кДа, соответствующая молекулярной массе лактоферрина, что было подтверждено при масс-спектрометрическом анализе (доля 31%). Различия в экспрессии белков были измерены с помощью ПО ImageQuant (от GE Healthcare). При загрузке равного количества белков при интенсивном анализе полосы были обнаружены пониженные концентрации лактоферрина в группах с ЛКН (14%) и БА (51 и 58%) в сравнении со здоровыми субъектами из контрольной группы (фиг. 1А). Для подтверждения наличия лактоферрина в человеческой слюне данный белок был идентифицирован посредством масс-спектрометра типа MALDI-TOF/TOF 4800 Proteomics Analyzer (Applied Biosystems, Фрамингем, шт. Массачусетс) и ПО 4000 Series ExplorerTM (Applied Biosystems) после ферментативного гидролиза в геле с трипсином и эндопептидазой Asp-N (Thermo Fisher Scientific). Доля аминокислот для лактоферрина составила 31%.
Дальнейшее подтверждение этих различий было получено путем усреднения уровней экспрессии лактоферрина с помощью коммерческого набора ELISA для людей (Abeam) в соответствии с инструкциями производителя. Попарное сопоставление трех групп с применением дисперсионного анализа с последующим тестом Тьюки-Крамера продемонстрировало существенное сокращение уровня содержания лактоферрина у пациентов из групп с ЛКН и БА в сравнении со здоровыми субъектами из контрольной группы (р<0,05; фиг. 2А). Уровень содержания лактоферрина в слюне пациентов с БП оказался существенно выше, чем у здоровых субъектов из контрольной группы (фиг. 2В).
Пример 3. Концентрация лактоферрина в слюне как средство диагностики
Уровень содержания лактоферрина в слюне оценивался по мере развития деменции. Связь между концентрацией лактоферрина в слюне и снижением когнитивной функции в группах с ЛКН и БА представляется очевидной. Это отношение было в основном обусловлено существенной отрицательной связью между стадиями заболевания и уровнем лактоферрина (R=-0,742; р<0,001) (фиг. 3А). Для отслеживания развития деменции использовались баллы по КШОПС. Также можно провести корреляцию концентрации лактоферрина в слюне с баллами по КШОПС у пациентов с ЛКН и БА с высокозначимой корреляцией (R=0,731; р<0,001) (фиг. 3В) при показателях 15-10 мкг/мл у здоровых людей, а также менее 7,43 мкг/мл у людей с деменцией, включая страдающих ЛКН и БА. Для анализов корреляции были соответственно использованы коэффициент корреляции рангов Кендалла для тау-белков и коэффициент корреляции рангов Спирмена.
Посредством анализа линейной регрессии было установлено, что концентрация лактоферрина в слюне на миллилитр у пациентов, страдающих БА и аЛКН, была на 6,432 (95% ДИ: 6,850-6,014; р<0,001) и 5,310 мкг (95% ДИ: 5,810-4,810; р<0,001) ниже, чем у здоровых участников соответственно. Эти результаты анализа лактоферрина были использованы нами для построения линейных моделей классификаторов, в которых бы группы с аЛКН/БА отделялись от контрольной группы, и нами был получен анализ рабочих параметров (ROC) для оценки эффективности моделей классификаторов для категоризации групп. В модели классификатора используются результаты анализа концентрации лактоферрина в слюне, дающие площадь под фармакокинетической кривой (AUC), равную 1 (95% ДИ 1-1), при чувствительности 100% (95% ДИ 96,90%-100%) и специфичности 100% (95% ДИ 95,95%-100%) для классификации группы с аЛКН/БА и здоровых субъектов из контрольной группы (фиг. 3С). Значение точки разделения составило 7,43 мкг/мл (индекс Юдена: 1).
Пример 4. Проверка пригодности лактоферрина в слюне в качестве средства диагностики
Далее значение точки разделения для лактоферрина в слюне было проверено в двух новых изолированных и независимых типологических группах, включавших 91 дополнительного участника с аналогичными стандартизированными клиническими показаниями, использованными во время предыдущего исследования. Возрастные группы привлеченных участников были набраны в двух учреждениях: подразделение исследований болезни Альцгеймера, фонд CIEN, Альцгеймеровский центр Фонда королевы Софии (Мадрид, Испания) и университет им. Пабло де Олавиде, Испания. Они приведены в Таблице 2.
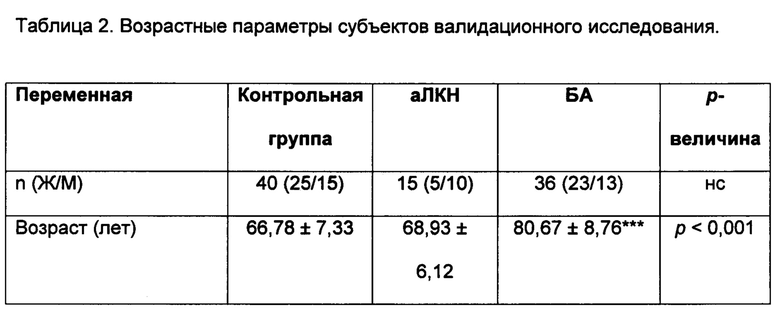
Ж = женщина; М = мужчина; аЛКН = амнестическое легкое когнитивное нарушение; БА = болезнь Альцгеймера; нз = незначительный. Данные выражены в виде среднего значения ± СО. ***р<0,001 в сравнении с контрольной группой.
Результаты показали, что с помощью значения точки разделения по содержанию лактоферрина в слюне (7,43 мкг/мл) все пациенты (ЛКН/БА; n=51) и субъекты без когнитивных нарушений (n=40) были классифицированы верно.
Пример 5. Концентрация лактоферрина в слюне как средство прогнозирования
Для изучения прогностического потенциала концентрации лактоферрина в слюне в данную группу были включены участники контрольной группы без когнитивных нарушений и нарушений памяти (таблица 3).
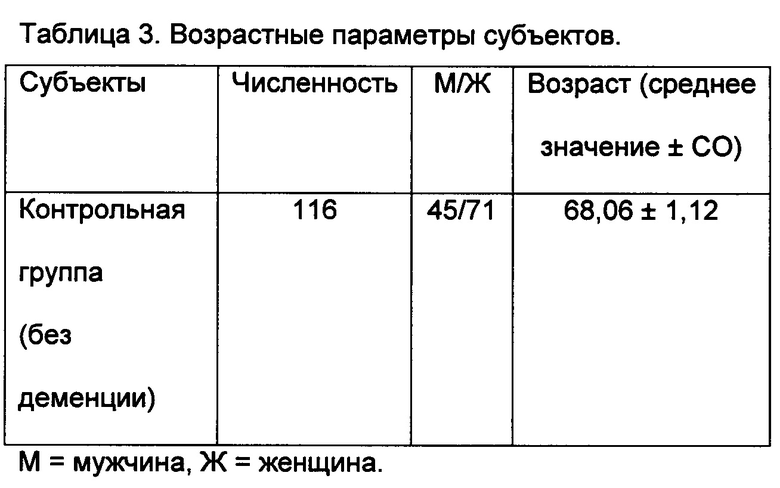
Нестимулированная цельная слюна была помещена в стерильные пластмассовые емкости, а концентрация лактоферрина была определена, как приведено в примере 1. У восьми (8) субъектов проявились значительно сниженные значения концентрации лактоферрина в слюне в сравнении со здоровыми субъектами из контрольной группы (3,47±0,41 мкг/мл в сравнении с 10,54±1,58 мкг/мл; р<0,05). Среднее время феноконверсии либо до ЛКН, либо до БА составило 3,25 лет (на временном промежутке 1-5 лет). В таблице 4 представлена связь между временем феноконверсии (манифестацией) и возрастом, где первое менее продолжительно у более пожилых субъектов.
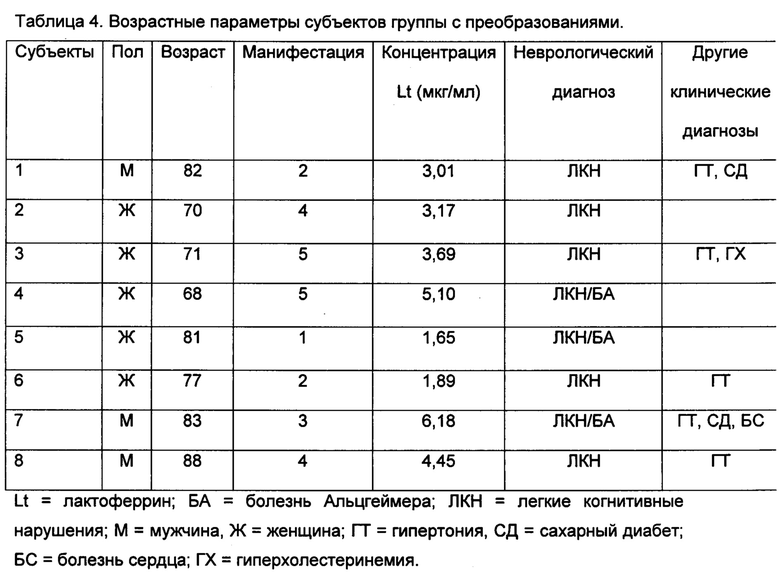
Пример 6. Концентрация лактоферрина на слизистой полости рта
Образцы со слизистой из полости рта были собраны в стерильные пластмассовые емкости согласно методу в работе Аагаарда (Аагаард и соавт. «Стратегия проекта по комплексному отбору образцов микробиома человека и ее значение». FAS ЕВ J. март 2013; 27(3): 1012-22). Вкратце, участники, представленные в таблице 5, сдали образцы слюны в 50-мл пробирках-сборниках после слюнообразования в течение ≥1 минуты. Образцы были центрифугированы при 6000 g в течение 10 мин при 4°С, а осадок хранился при -80°С.

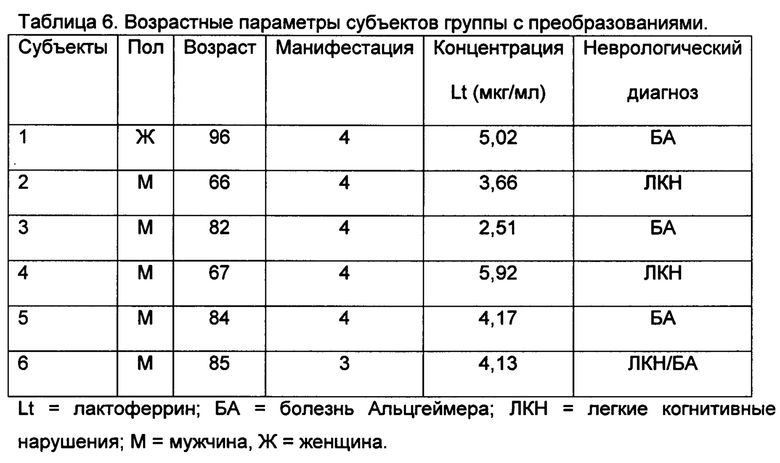
(концентрация лактоферрина была определена, как представлено в примере 1. У шести (6) субъектов проявились значительно сниженные значения концентрации лактоферрина в сравнении со здоровыми субъектами из контрольной группы (4,28±0,50 мкг/мл у группы с БА в сравнении с 9,05±1,47 мкг/мл; р<0,05; таблица 6). Среднее время феноконверсии либо до ЛКН, либо до БА составило 3,83 года (на временном промежутке 4-3 года). В группу, представленную в таблице 5, были включены участники контрольной группы без когнитивных нарушений и нарушений памяти.
Пример 7. Построение прогностической модели феноконверсии в ЛКН/БА
Данные, приведенные в предыдущих примерах анализа Elisa для лактоферрина, были использованы для построения отдельной линейной модели классификатора, благодаря которой можно отличать патологическое и непатологическое состояния БА. Был проведен анализ рабочих параметров (ROC) для оценки эффективности моделей классификаторов для категоризации групп. С помощью модели классификации, в которой использовались полученные уровни концентрации лактоферрина в слюне, при анализе успешно были категоризированы группы с преобразованиями и здоровые субъекты из контрольных групп со значением площади под фармакокинетической кривой (AUC), равным 0,98, с доверительным интервалом (ДИ) 95% (0,93-1) (фиг. 4А). В этой модели была получена чувствительность 100% и специфичность 98,6% при классификации групп с преобразованиями и здоровых субъектов из контрольных групп (фиг. 4А). По настоящей ROC-кривой, являющейся основополагающим средством оценки диагностического теста, была выполнена оценка точности разграничения случаев заболеваний с нормальными случаями по данному тесту. Под ROC-кривой можно понимать график вероятности правильной классификации положительных образцов в сравнении с частотой неверной классификации истинно отрицательных образцов. Таким образом, значение AUC на ROC-кривой - это мера точности прогноза.
Вероятность оценки среднего времени феноконверсии либо для группы с аЛКН, либо для группы с БА в зависимости от аномально пониженного или нормального/высокого уровня содержания лактоферрина была установлена с помощью модели пропорциональных рисков Кокса (фиг. 4 В). Полученные результаты показали, что концентрация лактоферрина в слюне - независимый прогностический фактор, по которому предугадывается вероятность возникновения БА, СВ: 0,428 (95% ДИ 0,324-0,567; р<0,0001).
В настоящем исследовании значение AUC=0,98 при идеальном значении, равном 1, указывает на устойчивую дискриминационную способность. При анализе регрессии было получено уравнение для описания соотношения концентрации лактоферрина в слюне и времени (в годовом исчислении) на феноконверсию (манифестацию) - у=0,6289х+1,6954, где «у» - концентрация лактоферрина в слюне, а «х» - время на феноконверсию в годовом исчислении (фиг. 4С).
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ГЕРОА
<120> Лактоферрин, используемый при диагностике или прогнозировании
болезни Альцгеймера, или диагностике болезни Паркинсона
<130> P2015/11298
<160> 1
<170> BiSSAP 1.3
<210> 1
<211> 711
<212> PRT
<213> Homo sapiens
<400> 1
Met Lys Leu Val Phe Leu Val Leu Leu Phe Leu Gly Ala Leu Gly Leu
1 5 10 15
Cys Leu Ala Gly Arg Arg Arg Arg Ser Val Gln Trp Cys Ala Val Ser
20 25 30
Gln Pro Glu Ala Thr Lys Cys Phe Gln Trp Gln Arg Asn Met Arg Arg
35 40 45
Val Arg Gly Pro Pro Val Ser Cys Ile Lys Arg Asp Ser Pro Ile Gln
50 55 60
Cys Ile Gln Ala Ile Ala Glu Asn Arg Ala Asp Ala Val Thr Leu Asp
65 70 75 80
Gly Gly Phe Ile Tyr Glu Ala Gly Leu Ala Pro Tyr Lys Leu Arg Pro
85 90 95
Val Ala Ala Glu Val Tyr Gly Thr Glu Arg Gln Pro Arg Thr His Tyr
100 105 110
Tyr Ala Val Ala Val Val Lys Lys Gly Gly Ser Phe Gln Leu Asn Glu
115 120 125
Leu Gln Gly Leu Lys Ser Cys His Thr Gly Leu Arg Arg Asn Ala Gly
130 135 140
Trp Asn Val Pro Ile Gly Thr Leu Arg Pro Phe Leu Asn Trp Thr Gly
145 150 155 160
Pro Pro Glu Pro Ile Glu Ala Ala Val Ala Arg Phe Phe Ser Ala Ser
165 170 175
Cys Val Pro Gly Ala Asp Lys Gly Gln Phe Pro Asn Leu Cys Arg Leu
180 185 190
Cys Ala Gly Thr Gly Glu Asn Lys Cys Ala Phe Ser Ser Gln Glu Pro
195 200 205
Tyr Phe Ser Tyr Ser Gly Ala Phe Lys Cys Leu Arg Asp Gly Ala Gly
210 215 220
Asp Val Ala Phe Ile Arg Glu Ser Thr Val Phe Glu Asp Leu Ser Asp
225 230 235 240
Glu Ala Glu Arg Asp Glu Tyr Glu Leu Leu Cys Pro Asp Asn Thr Arg
245 250 255
Lys Pro Val Asp Lys Phe Lys Asp Cys His Leu Ala Arg Val Pro Ser
260 265 270
His Ala Val Val Ala Arg Ser Val Asn Gly Lys Glu Asp Ala Ile Trp
275 280 285
Asn Leu Leu Arg Gln Ala Gln Glu Lys Phe Gly Lys Asp Lys Ser Pro
290 295 300
Lys Phe Gln Leu Phe Gly Ser Pro Ser Gly Gln Lys Asp Leu Leu Phe
305 310 315 320
Lys Asp Ser Ala Ile Gly Phe Ser Arg Val Pro Pro Arg Ile Asp Ser
325 330 335
Gly Leu Tyr Leu Gly Ser Gly Tyr Phe Thr Ala Ile Gln Asn Leu Arg
340 345 350
Lys Ser Glu Glu Glu Val Ala Ala Arg Arg Ala Arg Val Val Trp Cys
355 360 365
Ala Val Gly Glu Gln Glu Leu Arg Lys Cys Asn Gln Trp Ser Gly Leu
370 375 380
Ser Glu Gly Ser Val Thr Cys Ser Ser Ala Ser Thr Thr Glu Asp Cys
385 390 395 400
Ile Ala Leu Val Leu Lys Gly Glu Ala Asp Ala Met Ser Leu Asp Gly
405 410 415
Gly Tyr Val Tyr Thr Ala Gly Lys Cys Gly Leu Val Pro Val Leu Ala
420 425 430
Glu Asn Tyr Lys Ser Gln Gln Ser Ser Asp Pro Asp Pro Asn Cys Val
435 440 445
Asp Arg Pro Val Glu Gly Tyr Leu Ala Val Ala Val Val Arg Arg Ser
450 455 460
Asp Thr Ser Leu Thr Trp Asn Ser Val Lys Gly Lys Lys Ser Cys His
465 470 475 480
Thr Ala Val Asp Arg Thr Ala Gly Trp Asn Ile Pro Met Gly Leu Leu
485 490 495
Phe Asn Gln Thr Gly Ser Cys Lys Phe Asp Glu Tyr Phe Ser Gln Ser
500 505 510
Cys Ala Pro Gly Ser Asp Pro Arg Ser Asn Leu Cys Ala Leu Cys Ile
515 520 525
Gly Asp Glu Gln Gly Glu Asn Lys Cys Val Pro Asn Ser Asn Glu Arg
530 535 540
Tyr Tyr Gly Tyr Thr Gly Ala Phe Arg Cys Leu Ala Glu Asp Ala Gly
545 550 555 560
Asp Val Ala Phe Val Lys Gly Val Thr Val Leu Gln Asn Thr Asp Gly
565 570 575
Asn Asn Asn Glu Ala Trp Ala Lys Asp Leu Lys Leu Ala Asp Phe Ala
580 585 590
Leu Leu Cys Leu Asp Gly Lys Arg Lys Pro Val Thr Glu Ala Arg Ser
595 600 605
Cys His Leu Ala Met Ala Pro Asn His Ala Val Val Ser Arg Met Asp
610 615 620
Lys Val Glu Arg Leu Lys Gln Val Leu Leu His Gln Gln Ala Lys Phe
625 630 635 640
Gly Arg Asn Gly Ser Asp Cys Pro Asp Lys Phe Cys Leu Phe Gln Ser
645 650 655
Glu Thr Lys Asn Leu Leu Phe Asn Asp Asn Thr Glu Cys Leu Ala Arg
660 665 670
Leu His Gly Lys Thr Thr Tyr Glu Lys Tyr Leu Gly Pro Gln Tyr Val
675 680 685
Ala Gly Ile Thr Asn Leu Lys Lys Cys Ser Thr Ser Pro Leu Leu Glu
690 695 700
Ala Cys Glu Phe Leu Arg Lys
705 710
<---
Предложенная группа изобретений относится к области медицины. Предложено применение лактоферрина из слюны субъекта для диагностирования или прогнозирования болезни Альцгеймера, в котором концентрация лактоферрина менее 7,43 мкг/мл является показателем болезни Альцгеймера. Предложен способ диагностирования и способ прогнозирования болезни Альцгеймера у субъекта, у которого наблюдаются симптомы неврологического заболевания, в которых концентрация лактоферрина в слюне менее 7,43 мкг/мл является показателем болезни Альцгеймера. Предложен набор для осуществления способа диагностирования или прогнозирования болезни Альцгеймера, включающий как минимум одну емкость, содержащую реагент, представленный антителом, специфичным для лактоферрина, для определения количественного содержания лактоферрина в слюне или образце слюны субъекта, инструкции по применению и норму для определения повышенного или пониженного содержания лактоферрина в сравнении со значением точки отсечения 7,43 мкг/мл, показательным для болезни Альцгеймера. Предложенная группа изобретений обеспечивает эффективное диагностирование или прогнозирование болезни Альцгеймера. 6 н. и 2 з.п. ф-лы, 5 ил., 6 табл., 7 пр.
1. Применение лактоферрина из слюны или образца слюны субъекта для диагностирования болезни Альцгеймера, причем концентрация лактоферрина менее 7,43 мкг/мл в слюне или образце слюны является показателем болезни Альцгеймера.
2. Способ диагностирования болезни Альцгеймера у субъекта, у которого наблюдаются симптомы неврологического заболевания, включающий:
- оценку концентрации лактоферрина в слюне или образце слюны этого субъекта; и
- определение, выше ли эта концентрация или ниже значения 7,43 мкг/мл, причем значение менее 7,43 мкг/мл является показателем болезни Альцгеймера.
3. Применение лактоферрина из слюны или образца слюны субъекта для прогнозирования развития болезни Альцгеймера, причем концентрация лактоферрина менее 7,43 мкг/мл в слюне или образце слюны является показателем болезни Альцгеймера.
4. Способ прогнозирования случаев развития болезни Альцгеймера у субъекта, у которого наблюдаются симптомы неврологического заболевания, включающий:
- оценку концентрации лактоферрина в слюне или образце слюны этого субъекта; и
- определение, выше ли эта концентрация или ниже значения 7,43 мкг/мл, причем значение менее 7,43 мкг/мл является показателем прогнозирования развития болезни Альцгеймера,
- при этом указанный прогноз привязан к временному промежутку продолжительностью пять или девять лет до проявления у субъекта симптомов болезни Альцгеймера.
5. Способ по любому из пп. 1-4, отличающийся тем, что субъект представлен млекопитающим.
6. Способ по п. 5, отличающийся тем, что млекопитающее представлено человеком.
7. Набор для осуществления способа диагностирования болезни Альцгеймера, включающий как минимум одну емкость, содержащую реагент, представленный антителом, специфичным для лактоферрина, для определения количественного содержания лактоферрина в слюне или образце слюны субъекта, инструкции по применению и норму для определения повышенного или пониженного содержания лактоферрина в сравнении со значением точки отсечения 7,43 мкг/мл, показательным для болезни Альцгеймера.
8. Набор для осуществления способа прогнозирования болезни Альцгеймера, включающий как минимум одну емкость, содержащую реагент, представленный антителом, специфичным для лактоферрина, для определения количественного содержания лактоферрина в слюне или образце слюны субъекта, инструкции по применению и норму для определения повышенного или пониженного содержания лактоферрина в сравнении со значением точки отсечения 7,43 мкг/мл, показательным для болезни Альцгеймера.
| БИОМАРКЕР ДЛЯ БОЛЕЗНИ АЛЬЦГЕЙМЕРА ИЛИ УМЕРЕННОГО КОГНИТИВНОГО РАССТРОЙСТВА | 2011 |
|
RU2563987C2 |
| WO 2010085658 A1, 29.07.2010 | |||
| WO 2013014669 A1, 31.01.2013 | |||
| ЛИТВИН А.А | |||
| и др | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Проблемы здоровья и экологии | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| SHAH R.R | |||
| et al | |||
| Addressing phenoconversion: the Achilles' heel of personalized | |||
Авторы
Даты
2021-03-29—Публикация
2016-11-17—Подача