Изобретение относится к биотехнологии и зоотехнии и может быть использовано при промышленном производстве симбиотического препарата на основе штамма Escherichia coli VL-613.
Способ получения препарата заключается в том, что глубинное культивирование Escherichia coli проводят в питательной среде в соответствии с разработанным алгоритмом управления процессом, полученную культуру концентрируют, бактериальную массу ресуспендируют в защитной среде для сохранения биологических свойств симбиотического препарата и расфасовывают во флаконы.
Разработанный способ позволяет получать комплекс незаменимых аминокислот: аспарагиновую, треонин и лизин, сократить время культивирования, повысить накопление жизнеспособных микробных клеток, улучшить качество биопрепарата, повысить стабильность и стандартность его биологических свойств.
В настоящее время одной из актуальных задач животноводства является обеспечение населения страны экологически чистыми продуктами питания. Доля свинины в общем объеме производства мяса занимает второе место после мяса птицы и составляет 33%.
Увеличение производства свинины достигается за счет увеличения поголовья, использования высокопродуктивных пород и интенсификации технологий содержания и кормления животных. Наиболее эффективным способом откорма для получения высококачественной свинины считается дорогостоящий комбикорм, однако полноценное кормление зачастую не является достаточным для достижения высокой продуктивности. Поэтому немаловажную роль при производстве свинины играет ускорение роста животных за счет использования стимуляторов роста.
Стимуляторы роста - вещества, способствующие увеличению мясной продуктивности животных сверх той, которая обеспечена полноценным сбалансированным кормлением. Широкое использование в качестве стимуляторов получили антибиотики. Однако применение антибиотических стимуляторов роста даже при субтерапевтических дозах продолжительное время может привести к селекции резистентных по отношению к антибиотикам штаммов бактерий у животных, подвергнутых стимуляции, кроме того, антибиотики, которые подавляют патогенную микрофлору, также угнетают и полезные микроорганизмы, участвующие в процессах пищеварения.
Еще одним из распространенных стимуляторов роста в свиноводстве является применение синтетических аминокислот в качестве добавок к кормам, основным недостатком которых служит дороговизна ввиду их производства в основном за границей.
Альтернативой использования антибиотиков и синтетических аминокислот как стимуляторов могут стать симбиотики, которые помогают развитию организма животного и повышают возможности его по перевариванию и наиболее полной усвояемости питательных веществ корма, повышая экономическую рентабельность откорма и полностью удовлетворяя пищевые потребности животных на разных этапа жизни.
Симбиотики - продукты биотехнологического производства, содержащие живые микроорганизмы, продуцирующие в желудочно-кишечном тракте животных аминокислоты (в том числе незаменимые), ферменты и витамины.
В последние годы ученые расширили и детализировали знания об участии представителей микрофлоры желудочно-кишечного тракта в различных функциях и реакциях организма. Они способны оказывать выраженное воздействие на процессы гомеостаза организма хозяина, участвовать в регулировании обменных, эндокринных и иммунных процессов. Даже незначительные изменения в составе микрофлоры кишечника животного отражаются на других органах пищеварения и организме в целом.
Современный подход к разработке пробиотических препаратов подразумевает, во-первых, применение различных видов микроорганизмов в определенных сочетаниях, во-вторых, выпуск их в форме, допускающей длительное хранение при обычной температуре, и, в-третьих, не теряющих своих свойств при внесении их в процессе производства кормов и кормовых добавок.
Большая группа пробиотиков производится с использованием метода лиофильной сушки субстрата живых активных бактерий. Препараты выпускают в форме порошка, таблеток, капсул или свечей. Эти формы имеют длительные сроки годности и не требовательны к непродолжительным изменениям температуры хранения. Существенным их недостатком является то, что процесс лиофилизации приводит бактерии в анабиоз (неактивное состояние). Для возвращения в активное физиологическое состояние им требуется 8-10 ч, а за это время уже большая часть бактерий выводится из организма животных. Поэтому необходимо разработать такие условия лиофилизации, которые позволяют сохранять наибольший процент жизнеспособных клеток после высушивания.
Кроме того, в процессе лиофилизации бактериальные клетки теряют специфические рецепторы, которые помогают им закрепляться на поверхностях клеток, поэтому их пребывание в кишечнике еще более снижается.
При производстве нативных (жидких) пробиотиков микробные клетки остаются в активном состоянии и способны к адгезии и колонизации желудочно-кишечного тракта уже в первые часы после попадания в организм. Жидкие формы препаратов содержат дополнительный лечебный фактор - продукты метаболизма активных форм живых бактерий, часть из которых (например - ферменты) могут разрушаться в процессе сублимационного высушивания. Кроме того, они на 30-40% дешевле сухих форм. Недостатком нативных (жидких) форм препаратов являются трудности с их хранением и транспортировкой.
Известны способы культивирования бактерий рода Escherichia, которые проводятся на жидких [1] и плотных [2] питательных средах.
Однако способ культивирования эшерихий на плотных питательных средах является нетехнологичным и малопродуктивным - культуру эшерихий выращивают в течение 24 ч в чашках Петри на твердой питательной среде. Культивирование в жидких питательных средах проводится без регулирования основных технологических параметров - окислительно-восстановительного потенциала, количества растворенного в культуральной жидкости кислорода и длительностью - в течение 24 - 48 ч.
Известен также способ получения кормовой добавки, содержащей культуру штамма Е. coli - продуцент лизин [3]. Однако в данном случае выращивание эшерихий проводится в неуправляемом режиме - без регулирования окислительно-восстановительного потенциала, количества растворенного в культуральной жидкости кислорода, длительностью 6-12 ч, что не позволяет получить стабильную по биологическим свойствам культуру.
Также известна технология получения симбиотического препарата «Пролизэр» на основе штамма Escherichia coli VL-613, при которой среда высушивания готовится по следующей прописи: концентрация основных компонентов: желатин - 2,0%; сахароза - 10,0%, в качестве растворителя - калий-фосфатный буфер [4].
Известен ближайший аналог (прототип) заявляемого способа [5], включающий засев штамма Escherichia coli VL-613, культивирование в жидкой питательной среде на основе перевара Хоттингера, концентрирование бактериальной суспензии с последующим смешиванием со стабилизатором, расфасовку и лиофилизацию препарата; при этом в процессе культивирования Е. coli VL-613 сразу после засева окислительно-восстановительный потенциал снижают до минус (80-100) мВ, после чего до окончания процесса культивирования рО2 поддерживают на уровне (20±5)% от насыщения кислородом воздуха, рН регулируют на уровне (7,0-7,4), а дробную подачу глюкозы осуществляют дозами до концентрации (0,1-0,2)% при лимитировании роста Escherichia coli VL-613 глюкозой, длительность процесса культивирования составляет 4-6 ч.
Однако в данном случае препарат выпускается только в сухом виде и является продуцентом только одной незаменимой аминокислоты - лизина.
Задачей изобретения является повышение качества целевого продукта за счет получения культуры симбиотических бактерий с высокой выживаемостью и биологической активностью и возможностью длительного хранения.
Технический результат изобретения достигается в способе получения нативного симбиотического препарата путем включения в состав заявляемого препарата в качестве микроорганизмов бактериальной массы штамма Escherichia coli VL - 613, а культивирование проводят течение 4-6 ч в жидкой питательной среде, дополнительно содержащей пептон, натрий фосфорнокислый двузамещенный и дрожжевой экстракт, при следующем соотношении компонентов, мас. %: перевар Хоттингера - 12,0-5,0; пептон - 0,8-1,2; натрий фосфорнокислый двузамещенный - 0,7-0,9; хлористый натрий - 0,7-0,9; глюкоза - 0,15-0,25; дрожжевой экстракт - 0,4-0,6; вода дистиллированная - до 100,0, причем после засева ферментера окислительно-восстановительный потенциал культуральной жидкости поддерживают в течение 75 мин (-160) - (-60) мВ, при перемешивании с оборотами мешалки в пределах (40-80) об/мин, далее в процессе культивирования поддерживается парциональное давление растворенного кислорода в культуральной жидкости на уровне (15±5)% от насыщения кислородом воздуха, дробная подача глюкозы осуществляется дозированно, до концентрации (0,15-0,2)% от объема питательной среды, причем с целью длительного хранения вводят в концентрат бактериальной культуры при соотношении 1:1-2 защитную среду, содержащую: желатин - 0,3 мас. %; сахароза - 10,0 мас. %; глицерин - 0,6 мас. %, хитозан пищевой - 2 мас. % и вода - до 100 мас. %.
В патентной и научно-технической литературе не известны технические решения, содержащие режимы способа получения нативного симбиотичского препарата, аналогичные заявляемому, т.е. предложение соответствует критерию «новизны».
Все режимы способа осуществимы в промышленных условиях, направлены на решение реальной технической задачи, т.е. предложение «промышленно применимо».
Впервые предложен способ изготовления нативного симбиотического препарата, где повышается качество целевого продукта за счет того, что: культивирование проводят в оптимизированной питательной среде в соответствии с разработанным алгоритмом управления процессом, концентрируют полученную культуру и ресуспендируют в защитной среде; осуществлением управляемого периодического процесса культивирования и эффективной защитной среды. Заявляемый препарат обладает высокой профилактической эффективностью при определенных условиях, т.е. предложение соответствует критериям «новизна» и «изобретательский уровень».
Способ осуществляют следующим образом.
За прототип технологии производства жидкого симбиотического препарата были взяты питательная среда и процесс культивирования, приведенные в патенте RU №2450051 (5).
Для этого в стерильный ферментер, который снабжен системой автоматического контроля и регулирования основных технологических параметров (температура, обороты мешалки, рН, рО2, еН), вносят жидкую питательную среду на основе перевара Хоттингера, приготовленную по следующей прописи, мас. %:
- перевар Хоттингера - 18,0-22,0;
- пептон - 0,8-1,2;
- натрий фосфорнокислый двузамещенный - 0,7-0,9;
- хлористый натрий - 0,7-0,9;
- глюкоза - 0,15-0,25;
- дрожжевой экстракт - 0,4-0,6;
- вода дистиллированная - до 100,0.
Глюкозу в виде 40% стерильного раствора добавляют в ферментер после стерилизации питательной среды и охлаждения реактора до 30-40°С. Готовая стерильная питательная среда содержит 160-180 мг % аминного азота и имеет рН 7,4-7,6 ед. рН.
В ферментер с питательной средой, разогретой до (37±1)°С, вносят 18-24-часовую матровую расплодку эшерихий, выращенную в жидкой питательной среде такого же состава, что и среда культивирования, в соотношении 5-10% от объема питательной среды в ферментере, и выращивают при (37±1)°С в течение 4-7 ч.
После засева ферментера окислительно-восстановительный потенциал (еН) культуральной жидкости поддерживают (-100) - (-80) мВ путем выдержки культуры без подачи воздуха на аэрацию и выключенной мешалке, после чего до окончания процесса культивирования с помощью изменения расхода воздуха на аэрацию и скоростью вращения мешалки поддерживают парциональное давление растворенного кислорода (рО2) в культуральной жидкости на уровне (20±5)% от насыщения кислородом воздуха, рН культуральной жидкости регулируют на уровне (7,2-7,4) ед. рН подачей 10%-ного раствора NaOH, а дробную подачу глюкозы осуществляют дозированно, до конечной концентрации в питательной среде 0,1-0,2%. Общая концентрация эшерихий по окончании культивирования составляет (10-16) млрд м.к./см3. После завершения процесса культивирования образцы культуральной жидкости и исходной питательной среды проверяют на содержание свободных аминокислот (табл. 1).
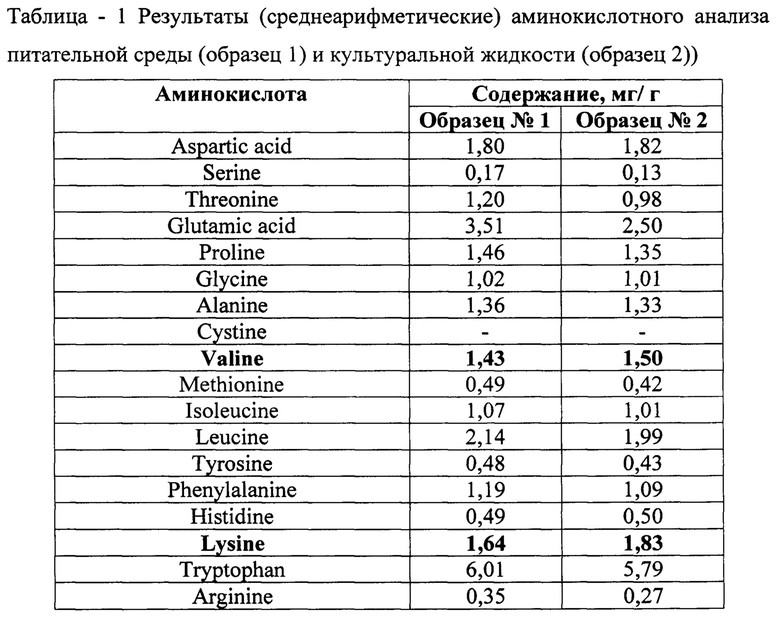
Как видно из представленных данных, в результате культивирования штамма Escherichia coli в питательной среде данного состава существенных изменений в составе аминокислот, кроме лизина, в питательной среде и в культуральной жидкости после выращивания штамма Е. coli не произошло. Отмечено незначительное понижение содержания большинства аминокислот в культуральной жидкости, что свидетельствует об активном процессе их утилизации штаммом Е. coli, с одной стороны, и их избытком в питательной среде, с другой.
Поэтому в разрабатываемой эффективной питательной среде по совершенствованию ростовых качеств среды снижено количество аминного азота на 30% с тем, чтобы нивелировать избыток аминокислот и стимулировать бакмассу к их ферментации. После снижения аминного азота состав усовершенствованной питательной среды принял следующий вид:
- перевар Хоттингера - 12,0-15,0;
- пептон - 0,8-1,2;
- натрий фосфорнокислый двузамещенный - 0,7-0,9;
- хлористый натрий - 0,7-0,9;
- глюкоза - 0,15-0,25;
- дрожжевой экстракт - 0,4-0,6;
- вода дистиллированная - до 100,0.
Проведя культивирование штамма в новой питательной среде по описанной выше методике, отобраны образцы культуральной жидкости, исходной питательной среды и они проверены на содержание аминокислот. Полученные результаты аминокислотного анализа подтвердили предположение о необходимости сокращения азотсодержащих питательных веществ в среде. Изготовленные на новой питательной среде четыре образца жидкого симбиотического препарата также проверены на содержание аминокислот. Среднеарифметические показатели аминокислотного состава данных серий препарата и исходных питательных сред, используемых для их изготовления, представлены в таблице 2.
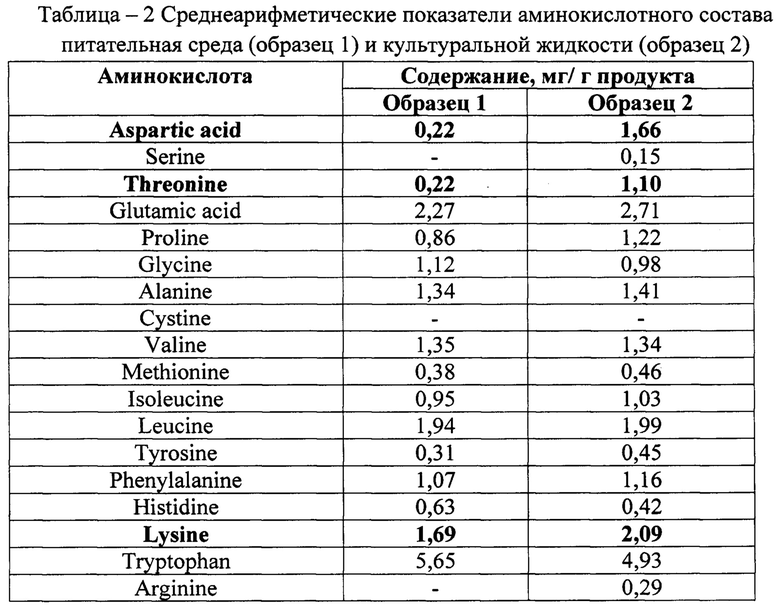
Как следует из представленных данных, в результате культивирования штамма Escherichia coli в питательной среде усовершенствованного состава в культуральной жидкости существенно повысилось содержание аспарагиновой кислоты, треонина и лизина.
В ферментер с питательной средой, разогретой до (37±1)°С, вносят 18-24-часовую матровую расплодку эшерихий из флаконов, выращенную в жидкой питательной среде такого же состава, что и среда культивирования, в соотношении 5-10% от объема питательной среды в ферментере, и выращивают при (37±1)°С в течение 4-6 ч.
После засева ферментера окислительно-восстановительный потенциал (еН) культуральной жидкости поддерживают в течение 75 мин (-160) - (-60) мВ путем выдержки культуры без подачи воздуха на аэрацию и перемешивании с оборотами мешалки в пределах 40-80 об/мин, после чего до окончания процесса культивирования с помощью изменения расхода воздуха на аэрацию и скоростью вращения мешалки поддерживают парциональное давление растворенного кислорода (рО2) в культуральной жидкости на уровне (15±5) % от насыщения кислородом воздуха, рН культуральной жидкости регулируют на уровне (7,2-7,4) ед. рН подачей 10%-ного раствора NaOH, а дробную подачу глюкозы осуществляют дозировано, до концентрации (0,15-0,2)% от объема питательной среды. Общая концентрация эшерихий по окончании культивирования составляет (12-20) млрд м.к./см3.
Полученную бактериальную культуру концентрируют, осадок смешивают с защитной средой сохранения жидкого симбиотического препарата при соотношении 1:1-2. Защитная среда имеет состав: желатин - 0,3%; сахароза - 10,0%; глицерин - 0,6%, хитозан пищевой - 2% и вода - до 100 мас. %. Хитозан пищевой соответсвует ТУ 9289-067-00472124-01 (Изменение №1) «Хитозан пищевой».
После тщательного перемешивания смешанную с защитной средой бактериальную суспензию расфасовывают с соблюдением условий асептики в стерильные флаконы.
Пример 1. В ферментер с питательной средой, разогретой до (37±1)°С, вносили 18-24-часовую матровую расплодку эшерихий из флаконов, выращенную в жидкой питательной среде такого же состава, что и среда культивирования, в соотношении 5-10% от объема питательной среды в ферментере, и выращивали при (37±1)°С в течение 4 ч. еН культуральной жидкости поддерживают - 160 мВ; рО2 поддерживают на уровне 10%; рН в культуральной жидкости регулируют на уровне 7,2 ед. рН; дробная подача глюкозы осуществляется дозами до концентрации 0,15%.
Культивирование - в течение 4 ч. Накопление - 12,0 млрд м.к./см3.
После окончания процесса культивирования биомассу охлаждают до температуры 6°С и центрифугируют при частоте оборотов 3500 об/с, в течение 15 мин. Концентрирование бакмассы E.coli осуществляли с помощью лабораторных центрифуг К-70Д, S-60 и установки «Сартокон-мини» («Владисарт», г. Владимир). Суспензию клеток отделяют от культуральной жидкости и смешивают с защитной средой в соотношении 1:1-2. Защитная среда имеет состав: желатин - 0,3%; сахароза - 10,0%; глицерин - 0,6%, хитозан пищевой - 2% и вода - до 100%. Суспензию разливают дозаторами в стерильные флаконы. Флаконы укупоривают резиновыми пробками и закатывают алюминиевыми колпачками. Срок хранения при этой температуре составляет шесть месяцев. При этом срок хранения жидкого препарата не менее 6 месв, а сохраняемость жизнеспособных клеток выше на 15-17%, чем у прототипа, и выше эффективность применения.
Пример 2. Способ получения препарата с оптимальными значениями параметров
В ферментер с питательной средой, разогретой до (37±1)°С, вносили 18-24-часовую матровую расплодку эшерихий из флаконов, выращенную в жидкой питательной среде такого же состава, что и среда культивирования, в соотношении 5-10% от объема ПС в ферментере, и выращивали при (37±1)°С в течение 5 ч. еН культуральной жидкости поддерживают - 100 мВ; рО2 поддерживают на уровне 15%; рН в культуральной жидкости регулируют на уровне 7,3 ед. рН; дробная подача глюкозы осуществляется дозами до концентрации 0,175%. Культивирование - в течение 5 ч.
Накопление - 22,0 млрд м.к./см3. Затем способ получения препарата ведут по примеру 1. При этом срок хранения жидкого препарата не менее 6 месяцев, а сохраняемость жизнеспособных клеток выше на 15-17%, чем у прототипа, и выше эффективность применения.
Пример 3. Способ получения препарата с максимальными значениями параметров
В ферментер с питательной средой, разогретой до (37±1)°С, вносили 18-24-часовую матровую расплодку эшерихий из флаконов, выращенную в жидкой питательной среде такого же состава, что и среда культивирования, в соотношении 5-10% от объема ПС в ферментере, и выращивали при (37±1)°С. еН культуральной жидкости поддерживают - 60 мВ; рО2 поддерживают на уровне 20%; рН в культуральной жидкости регулируют на уровне 7,4 ед. рН; дробная подача глюкозы осуществляется дозами до концентрации 0,2%.
Культивирование - в течение 6 ч. Накопление - 18,0 млрд м.к./см3. Затем способ получения препарата ведут по примеру 1. При этом срок хранения жидкого препарата - до 6 месяцев, а сохраняемость жизнеспособных клеток выше на 15-17%, чем у прототипа, и выше эффективность применения.
Пример 4. Способ получения препарата со значениями параметров ниже минимальных
В ферментер с питательной средой, разогретой до (37±1)°С, вносили 18-24-часовую матровую расплодку эшерихий из флаконов, выращенную в жидкой питательной среде такого же состава, что и среда культивирования, в соотношении 5-10% от объема питательной среды в ферментере, и выращивали при (37±1)°С. еН культуральной жидкости поддерживают - 170 мВ; рО2 поддерживают на уровне 5%; рН в культуральной жидкости регулируют на уровне 7,1 ед. рН; дробная подача глюкозы осуществляется дозами до концентрации 0,125%.
Культивирование - в течение 3 ч. Накопление - 6,0 млрд м.к./см3. Затем способ получения препарата ведут по примеру 1. При этом срок хранения жидкого препарата - до 3 мес, эффективность применения через 6 мес хранения не соответствует прототипу.
Пример 5. Способ получения препарата со значениями параметров выше максимальных
В ферментер с питательной средой, разогретой до (37±1)°С, вносили 18-24-часовую матровую расплодку эшерихий из флаконов, выращенную в жидкой питательной среде такого же состава, что и среда культивирования, в соотношении 5-10% от объема питательной среды в ферментере, и выращивали при (37±1)°С. еН культуральной жидкости поддерживают - 50 мВ; рО2 поддерживают на уровне 25%; рН в культуральной жидкости регулируют на уровне 7,5 ед. рН; дробная подача глюкозы осуществляется дозами до концентрации 0,225%.
Культивирование - в течение 7 ч. Накопление - 17,0 млрд м.к./см3. Затем способ получения препарата ведут по примеру 1. При этом срок хранения жидкого препарата - до 4 месяцев, а эффективность применения через 6 мес хранения не соответствует прототипу.
Технологические параметры изготовления симбиотического препарата из штамма Escherichia coli VL-613, указанные в примерах, приведены в таблице 3.
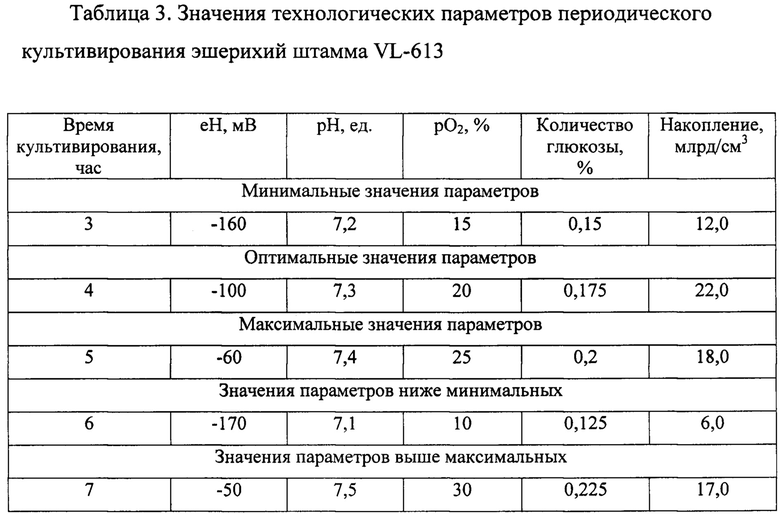
Препарат, приготовленный по примерам 1-3, содержит на конец срока годности 85-95% жизнеспособных клеток и соответствует требованиям технических условий, тогда как препарат, приготовленный по примерам 4 и 5, содержит 65-70% жизнеспособных клеток и является малоэффективным для применения.
Для определения эффективности жидкого симбиотического препарата в таблице 4 представлены данные по влиянию добавок симбиотических препаратов на прирост живой массы поросят. В каждой группе было по 30 поросят-отъемышей и свиней на доращивании, взвешивание производили на 60, 80, 100 и 120-й день доращивания, рацион кормления был одинаковый.
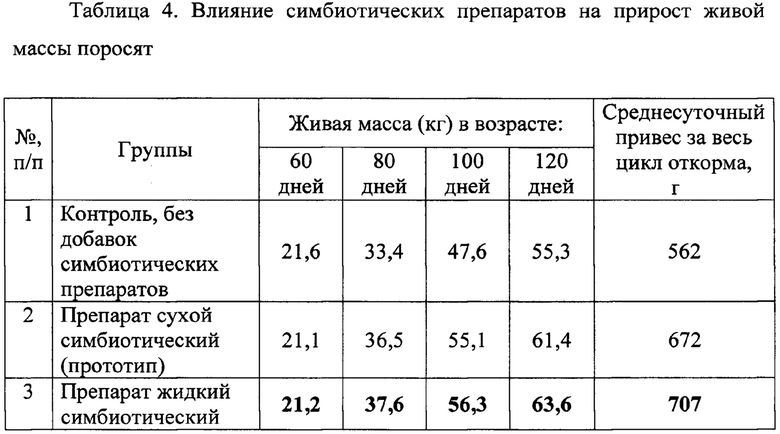
Как следует из таблицы 4, живая масса опытных животных, которым давали жидкий препарат, превышала живой вес контрольных животных и тех, кому давали сухой препарат. При этом она была достоверно выше за весь цикл выращивания поросят по сравнению с прототипом. Заявляемый препарат позволяет обеспечить синтез незаменимых аминокислот в организме поросят в наиболее ответственный период жизни, когда пищеварительная система отличается наибольшей уязвимостью и незрелостью. Использование заявляемого препарата не повлияло отрицательно на сохранность поросят и конверсию корма.
Преимущества способа изготовления нативного препарата на основе штамма Е. coli VL-613 по разработанной технологии:
1. Применение разработанной питательной среды и процесса культивирования симбиотического нативного препарата на основе штамма Е. coli VL-613 позволяет получать комплекс незаменимых аминокислот: аспарагиновую, треонина и лизина, сократить время культивирования до 4-6 ч, повысить накопление бакмассы, жизнеспособность бактерий и эффективность от применения.
2. Использование жидкого препарата снижает расход корма на весь цикл выращивания.
Источники информации
1. Патент РФ №2175351 от 27.01.2001.
2. Патент РФ №2189253 от 09.04.2001.
3. Патент РФ №2347807 от 27.02.2009.
4. Павленко И.В., Самуйленко А.Я., Еремец В.И. и др. Разработка технологии производства симбиотического препарата Пролизэр на основе штамма Escherichia coli VL-613, часть 1, часть 2. // Вестник Казанского технологического университета Т16, - №9, - 2013, - стр. 171-180.
5. Патент РФ №2450051 от 18.08.2010 г. (прототип).
6. ТУ 9289-067-00472124-01 (Изменение №1) «Хитозан пищевой.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СИМБИОТИЧЕСКОГО ПРЕПАРАТА НА ОСНОВЕ Escherichia coli VL-613 | 2010 |
|
RU2450051C1 |
| ЗАЩИТНАЯ СРЕДА ВЫСУШИВАНИЯ ДЛЯ ПОЛУЧЕНИЯ СИМБИОТИЧЕСКОГО ПРЕПАРАТА | 2014 |
|
RU2571157C2 |
| ВАКЦИНА ПОЛИВАЛЕНТНАЯ ПРОТИВ САЛЬМОНЕЛЛЕЗА ПРОДУКТИВНЫХ ЖИВОТНЫХ | 2021 |
|
RU2764118C1 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ИНАКТИВИРОВАННАЯ ГИДРООКИСЬАЛЮМИНИЕВАЯ ПРОТИВ ИНФЕКЦИОННОЙ ПНЕВМОНИИ И САЛЬМОНЕЛЛЕЗА СВИНЕЙ И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2003 |
|
RU2246316C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОМАССЫ ЭНТЕРОБАКТЕРИЙ ESCHERICHIA COLI ИЛИ SALMONELLA В ПРОИЗВОДСТВЕННЫХ БИОРЕАКТОРАХ | 2019 |
|
RU2743396C1 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ГИДРООКИСЬАЛЮМИНИЕВАЯ ПРОТИВ ИНФЕКЦИОННЫХ ПНЕВМОНИЙ СВИНЕЙ БАКТЕРИАЛЬНОЙ ЭТИОЛОГИИ И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2000 |
|
RU2191598C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНАКТИВИРОВАННОЙ ВАКЦИНЫ ПРОТИВ ВИБРИОЗА РЫБ | 2005 |
|
RU2284830C1 |
| ВАКЦИНА ПРОТИВ ИНФЕКЦИОННЫХ МАСТИТОВ И ЭНДОМЕТРИТОВ КОРОВ ИНАКТИВИРОВАННАЯ, СПОСОБ ЕЁ ПОЛУЧЕНИЯ | 2024 |
|
RU2840041C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ ПРОТИВ ЛЕПТОСПИРОЗА ЖИВОТНЫХ | 1995 |
|
RU2088258C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДСОРБИРОВАННОЙ ВАКЦИНЫ ПРОТИВ ВИБРИОЗА ЛОСОСЕВЫХ РЫБ | 2019 |
|
RU2723580C1 |
Изобретение относится к биотехнологии. Способ получения симбиотического препарата предусматривает засев штаммом Escherichia coli VL-613 питательной среды на основе перевара Хоттингера. Осуществляют концентрирование бактериальной суспензии с последующим смешиванием с защитной средой в заданном соотношении с последующей фасовкой во флаконы. При этом окислительно-восстановительный потенциал культуральной жидкости поддерживают в течение 75 мин – (-160) - (-60) мВ, парциональное давление растворенного кислорода в культуральной жидкости - на уровне 15 ±5 % от насыщения кислорода воздуха. Изобретение позволяет сократить продолжительность культивирования и повысить накопление жизнеспособных микробных клеток. 4 табл., 5 пр.
Способ получения нативного симбиотического препарата на основе штамма Escherichia coli VL - 613, включающий засев, культивирование в жидкой питательной среде на основе перевара Хоттингера, концентрирование бактериальной суспензии с последующим смешиванием с защитной средой, сохранение и расфасовку препарата, отличающийся тем, что культивирование проводят течение 4-6 ч в жидкой питательной среде, дополнительно содержащей пептон, натрий фосфорнокислый двузамещенный и дрожжевой экстракт, при следующем соотношении компонентов, мас. %: перевар Хоттингера - 12,0-15,0; пептон - 0,8-1,2; натрий фосфорнокислый двузамещенный - 0,7-0,9; хлористый натрий - 0,7-0,9; глюкоза - 0,15-0,25; дрожжевой экстракт - 0,4-0,6; вода дистиллированная - до 100,0, причем после засева ферментера окислительно-восстановительный потенциал культуральной жидкости поддерживают в течение 75 мин (-160) - (-60) мВ, при перемешивании с оборотами мешалки в пределах 40-80 об/мин, в процессе культивирования поддерживается парциональное давление растворенного кислорода в культуральной жидкости на уровне 15±5 % от насыщения кислородом воздуха, дробная подача глюкозы осуществляется дозированно, до концентрации 0,15-0,2 % от объема питательной среды, причем с целью длительного хранения вводят в концентрат бактериальной культуры при соотношении 1:1-2 защитную среду, содержащую: желатин - 0,3%; сахароза - 10,0%; глицерин - 0,6%, хитозан пищевой - 2% и вода - до 100%.
| СПОСОБ ПОЛУЧЕНИЯ СИМБИОТИЧЕСКОГО ПРЕПАРАТА НА ОСНОВЕ Escherichia coli VL-613 | 2010 |
|
RU2450051C1 |
| ШКОЛЬНИКОВ Е.Э | |||
| и др | |||
| Разработка технологии производства симбиотического препарата на основе E | |||
| УСТРОЙСТВО ДЛЯ ИЗМЕНЕНИЯ ВЕЛИЧИНЫ УСИЛЕНИЯ КАТОДНОГО РЕЛЕ В КАТОДНЫХ МУЗЫКАЛЬНЫХ ПРИБОРАХ | 1922 |
|
SU613A1 |
| Материалы VI Международной конференции, посвященной 55-летию ВНИИФБиП, г | |||
| Боровск, 15-17 сентября 2015, с.219-221 | |||
| САМУЙЛЕНКО А.Я | |||
| и др | |||
| Моделирование и оптимизация технологии производства симбиотического препарата "СИМБИОХИТ", Вестник Казанского Технологического Университета, 2014, т | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Прибор для записи звуковых волн | 1920 |
|
SU219A1 |
Авторы
Даты
2018-07-31—Публикация
2017-04-14—Подача