ОБЛАСТЬ ПРИМЕНЕНИЯ ИЗОБРЕТЕНИЯ
Данное изобретение относится к области иммунологии и биотехнологии, а именно к иммуногенной разработке на основе рекомбинантной ослабленной бактерии для приготовления вакцины для человеческого метапневмовируса (hMPV). Данная разработка включает рекомбинантную бациллу Кальмета-Герена (BCG, БЦЖ), экспрессирующую антигенный пептид Р-протеин из вируса hMPV.
СВЕДЕНИЯ ОБ ИЗОБРЕТЕНИИ
Человеческий метапневмовирус (hMPV, далее) является этиологическим фактором высокого процента госпитализаций и смертности от острых респираторных инфекций верхних и нижних дыхательных путей, особенно у детей, пожилых людей и лиц с ослабленным иммунитетом. Инфекции с этим вирусом связаны с большим кругом заболеваний, таких как бронхиолит и пневмония с повышенными социально-экономическими последствиями. Кроме того, инфекции связаны с гастроэнтеритом, и кератоконъюнктивитом. Данные Calvoet al. (2008) показали, что через 3-летний интервал исследования, кумулятивная заболеваемость острыми респираторными инфекциями, вызванными респираторными вирусами RSV, ADV и hMPV составляла 64,5% госпитализаций детей в возрасте до 2 лет с заболеваемостью для каждого вируса 35.4%, 19.3% и 9,8% соответственно. Одна интересная особенность, которая разделяет hMPV с другой, высокой степенью заболеваемости, респираторными вирусами является возникновение повторных инфекций в детстве, данный феномен, возможно, связан со сбоем в создании защитного иммунного ответа при первичном инфицировании во время первых месяцев жизни. Данный феномен мотивирует систему общественного здравоохранения для создания нового прототипа вакцины с возможностью контроля ежегодных эпидемий респираторных инфекций, тем самым позволяя разгрузить учреждения здравоохранения, и в конечном итоге снизить социально-экономические последствия, связанные с данными инфекциями. На сегодняшний день не проводилось исследований о конкретных экономических последствиях, связанных с hMPV инфекции, однако, число случаев госпитализации для hMPV оценивается в 1/3 случаев госпитализации для человека с респираторно-синцитиальным вирусом (hRSV). Исследования, проведенные в развитых странах, оцениваются индивидуальной стоимостью hRSV-инфекции около 3000 евро ($ 1,86 млн чилийских песо) с верхним пределом до 8400 евро ($ 5,2 млн чилийских песо). Расходы, связанные с индивидуальной госпитализацией, являются приблизительными и основаны на патологическом процессе с аналогичными характеристиками, что требует проведения госпитализации.
Вирус hMPV относится к семейству парамиксовирусов, подсемейству Pneumovirinae, к этому же семейству относится и hRSV, хотя каждый из них сгруппирован в роды Метапневмовирусов и Пневмовирусов, соответственно. Геном HMPV содержит несегментированную, однонитевую, отрицательно-направленную рибонуклеиновую кислоту (ssRNA), так что вирусные белки расположены в 3' в 5' направлении (с точки зрения их последовательности) следующим образом: N, Р, М, F, М2 (ORF1 и 2), SH, G и L. Пять из этих белков отвечают за упаковку генетического материала и определение структуры вирусной частицы, соответствующей нуклеокапсидному белку N и матрице белка М, вместе с трансмембранными гликопротеинами F, G и SH, соответственно. Остальные четыре белка, М2-1, М2-2, Р и L, включены в вирусную репликацию и транскрипцию. Два подтипа hMPV, классифицируются как А и В относительно двух антигенных групп, на основе последовательных различий в первую очередь белков F и G. Хотя эти белки имеют определенную разницу, существует высокая идентичность по сравнению с другими белками, кодируемые вирусным геномом.
Разработки вакцин против респираторных вирусов начались в 1960-х годах, когда первый прототип hRSV вакцины основывался на формалин-инактивированном вирусе (hRSV-FI), что оказывало значительное неблагоприятное воздействие и не позволяло использовать его в программе иммунизации. Внутримышечное введение вместе со вспомогательным гидроксидом алюминия производилось у вакцинированных детей, у которых были более тяжелые симптомы, чем у инфицированных лиц, которые не были привиты. Этот эффект был связан с гиперчувствительностью иммунного ответа на инфекцию, характеризующегося большим количеством инфильтрации паренхимы полиморфно-ядерных клеток, эозинофилов и нейтрофилов и высоким титром комплемент-фиксирующих антител.
Для метапневмовируса человека (hMPV) были разработаны только несколько вакцин и до сих пор нет удовлетворительного результата. Прототип, используя тот же прежний формалин-инактивированный вирус (hMPV-FI), также проявляет симптомы с воспалительной гиперчувствительностью, аналогичными характеристиками, которые проявились на вакцину против hRSV в модели инфекции Sigmodonhispidus (Yim et ah, 2007). В отличие от проявления процессов гиперчувствительности, наблюдаемых для hSRV, была продемонстрирована частичная ликвидации вируса из дыхательных путей. Заболевание, наблюдаемое у мышей вида Sigmodonhispidus, которые подвержены к hSRV-FI, было связаны с иммунопатологическими реакциями, основанными на антителах типа-Th2 и завышенной активации NF-κb. Увеличение NF-кв транскрипционной активности в дальнейшем относится к секреции провоспалительных цитокинов, таких как IL-8. Кроме того, гиперчувствительность легочной ткани после hMPV-инфекции была связана с иммунной реакцией, которая характеризуется наличием IFN-γ и IL-4 в бронхоальвеолярном лаваже и обнаружением нейтрализующих антител IgG1 и IgG2a в сыворотке крови больных мышей, так что наблюдаемое хроническое воспаление объясняется либо патологической реакцией клеток типа-Th1 и -Th2 или недостаточным ответом, основанным на типе клеток -Th1, который сопровождается патологическим ответом на тип-Th2. Что касается последнего предположения, некоторые авторы предположили, что повышенный ответ на тип-Th1 также может усугубить заболевание.
Эти факты подчеркивают важность создания сбалансированной и эффективной иммунной реакции, которая будет в состоянии ограничить протекание воспалительного процесса и, в свою очередь, побудить соответствующее удаление этих вирусов из инфицированных тканей.
Так как респираторное заболевание, вызываемое человеческим метапневмовирусом (hMPV) является подобным наблюдаемому ранее человеческому спума ретровирусу (hSRV), который был связан с неудачей в возбуждении клеточного иммунитета, необходимо создать прототип вакцины, который является хорошим индуктором CD8+ цитотоксических Т-лимфоцитов и CD4+ Т-хелперов, обоих продуцентов гамма-интерферона. В последних экспериментальных подходах все усилия были сосредоточены на разработке вакцин только на один вид вирусов, с использованием различных методов молекулярной генетики и иммунологии. Важно отметить, что в этих исследованиях используется ограниченное количество белков или белковых субъединиц в качестве антигенов для каждого интересующего вируса. Что касается hSRV, некоторые из исследований были основаны на использовании отдельных вирусных белков, как, например, полные субъединицы или фрагменты белков F или G, или их смесь в образцах нечеловеческих вакцин для тестирования на мышах и приматах. Некоторые прототипы вакцин против hSRV были использованы в I и II фазах клинических испытаний, однако, в результате, длительная защитная способность не была доказана. Поэтому такие вакцины далеки от пригодных для широкого использования в профилактике инфекции (Денис и др., 2005; Кэррон и др., 2005).
Аттенуированные штаммы hMPV были разработаны путем исключения генов, которые предположительно были связаны с вирусной патогенностью. Штаммы HMPV с нехваткой генов, кодирующих для белков SH, G, and, М2-1 and М2-2 были предложены в качестве вакцин-кандидатов (Бьякесси и др., 2005). Эти вакцины - кандидаты показали хорошие результаты на образцах для животных, но еще не были изучены в организме человека. Хотя эта альтернатива и имеет право на существование, она очень дорогостоящая, так как требует производства вируса в клеточных культурах, одобренных для использования человеком. Другой источник вакцины - сверхэкспрессия вирусных белков гетерологичными системами, таких как белок F вируса hMPV в сочетании с адъювантами для создания нейтрализующих антител. Но недостатком этого варианта является то, что иммунитет обеспечивается на очень короткий период времени (Херфст и др., 2008а).
Клинические исследования вакцин - кандидатов против вируса hMPV отсутствуют, поскольку разработка прототипов, способных вырабатывать защитный иммунитет, была неудачной. На сегодняшний день прототипы, которые тестировались на образцах для животных, вырабатывают иммунитет на основе антител типа Th2, который является не долгосрочным и неэффективным в профилактике инфекций. У животных, которые были привиты этими прототипами, выработались нейтрализующие антитела, полученные в искусственных условиях, но они не стали защищены от инфекции, а также не уменьшились клинические симптомы болезни, вызванные инфекцией hMPV у мышей (Чсеке и др., 2007) или макак (Херфст и др., 2008б). Иммунитет на основе антител не является эффективной нейтрализацией вируса в организме. Антитела, способные нейтрализовать вирус hMPV в пробирке, не в состоянии предотвратить инфекцию или заболевание, вызванное hMPV, при использовании пассивной иммунизации в качестве терапии (Хамелин и др., 2008). Кроме того, было отмечено, что резолюция вирусных симптомов требует участия клеточной иммунной реакции типа Th1. Было показано, что резолюция вирусного состояния и очистка вирусных частиц зависит от активации лимфоцитов CD4+ и CD8+, хотя активность этих лимфоцитов также отвечает за иммунопатологию болезней (Колли и др., 2008). Совсем недавно было обнаружено, что первичными эффекторами резолюции вирусных симптомов являются цитотоксические клетки типа CD8+, хотя хелперы Т-лимфоцитов CD4+ имеют регулятивное вовлечение в патологический процесс. Таким образом, сбалансированная иммунная реакция клеток типа Th1 необходима для получения резолюции вирусных симптомов, не вызывая воспалительную гиперчувствительность. В результате, в настоящее время отсутствует вакцина против человеческого метапневмовируса (hMPV), способная обеспечить эффективную защиту и отсутствие серьезных побочных эффектов. На самом деле, никаких коммерческих вакцин против этого вируса также не существует.
Изобретатели удивительным образом обнаружили, что использование рекомбинантного штамма микобактерий, экспрессирующих белки Р из человеческого метапневмовируса, позволяет сформировать защитный иммунитет против инфекции, продуцируемой респираторным метапневмовирусом, не вызывая нежелательные побочные эффекты, такие как воспалительная гиперчувствительность дыхательных путей. Данное изобретение решает техническую проблему, которая оставалась нерешенной в предыдущих образцах, состоящих из иммуногенной формулы, обеспечивающей защиту от инфекций hMPV и не вызывающей воспалительную гиперчувствительность.
ОПИСАНИЕ Чертежей
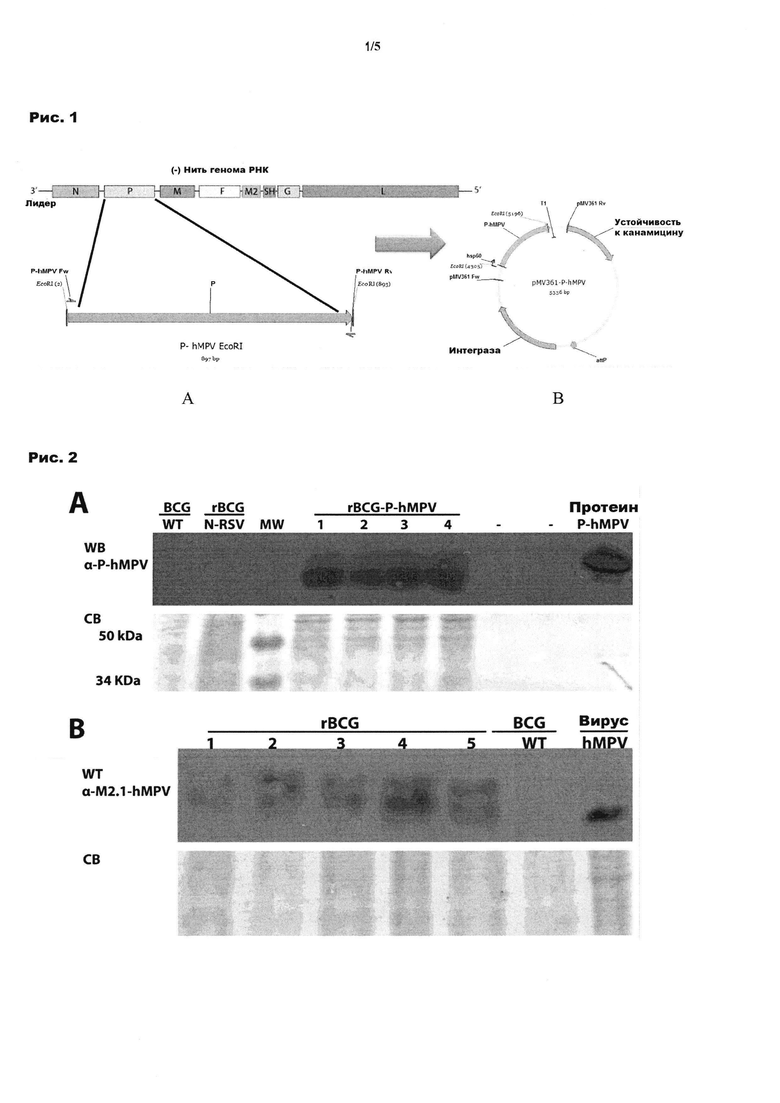
Рис. 1: Создание структуры pMV361-P-hMPV. Обратная транскрипция РНК из метапневмовируса проводилась с универсальными праймерами и затем усиливалась с праймерами P-hMPV-FW и P-hMPV-Pv из открытой рамки считывания гена Р. Сайты EcoRI с двух концов были включены в продукт амплификации, а затем вставлены в сайт EcoRI вектора микобактерий pMV361 для создания структуры вектора pMV361-P-hMPV. На Рис. 1А показан геном вируса hMPV, и ген, кодирующий белок Р, а на Рис. 1В показан вектор pMV361-P-hMPV, включающий вышеупомянутый ген, кодирующий белок Р.
Рис. 2: Экспрессия белка Р или белка М 2.1 из вируса hMPV рекомбинантными штаммами Микобактериальной BCG. Датский штамм Микобактериальной BCG был электротрансформирован с плазмидой pMV361-P-hMPV и был выбран в среду Агар Миддлбрук 7Н10, обогащенную олеиновой кислотой, альбумином, декстрозой и каталазой, с содержанием 20 мг/мл канамицина. Электрофорез белков в полиакриламидном геле в присутствии додецилсульфата натрия по Лэммли (Далее, Электрофорез) и Вестерн блоттинг проводились с использованием моноклональных белковых антител anti-hMPV Р. Рис. 2А: Вестерн блоттинг с использованием моноклональных белковых антител anti-hMPV Р и Рис. 2В: Вестерн блоттинг с использованием моноклональных белковых антител anti-hMPV М2.1. Во время Электрофореза, были нагружены только 25 мг из общего количества белка Р, приготовленного из четырех клонов вакцины BCG - P-hMPV (Рис. 2А) или пяти клонов BCG - M2.1-hMPV (Рис. 2В). В качестве положительного контроля были нагружены 5 мг рекомбинантного белка Р вируса hMPV или 25 мг не активированного вируса hMPV. В качестве отрицательного контроля, был нагружен весь белок из штамма BCG дикого типа и, в случае с pBCG-P-MPV, рекомбинантная BCG с геном N из SRV (штамм N-5) также была нагружена. Можно признать, что все анализируемые клоны экспрессируют клонированные плазмидные белки, а также белок Р, Рис 2А, и белок М2.1, рис. 2В.
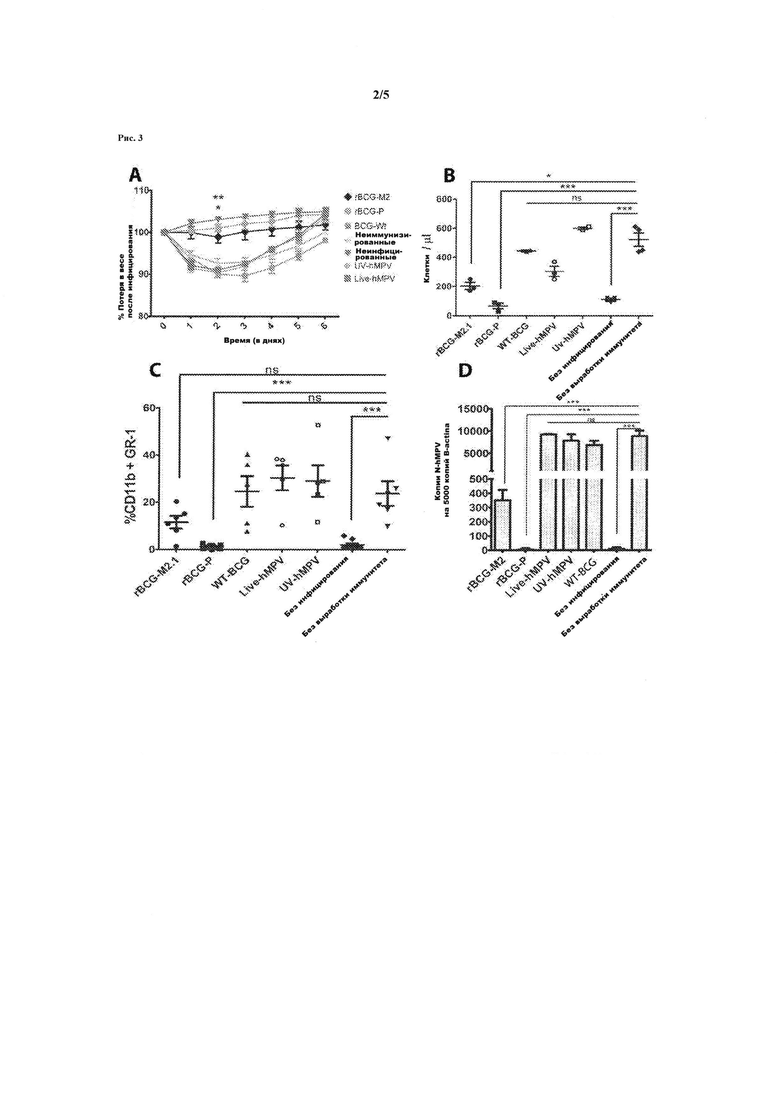
Рис. 3. Иммунизация рекомбинантной pBCG-P-hMPV защищает от инфицирования hMPV. Группы мышей возрастом 4-8 месяцев породы BALB/c получали подкожную дозу 1×108 колониеобразующих единиц (КОЕ) pBCG - M2.1-hMPV, pBCG-P-hMPV или WT-BCG (дикий тип), а также были вакцинированы 1×106 тромбоците - образующими единицами (TOE) живого вируса (Live-hMPV) или UV-инактивированного вируса (UV-hMPV). Затем все группы были интраназально заражены 1×106 TOE вируса hMPV. В контрольную группу были включены непривитые животные и одна группа незараженных животных. В течение последующих шести дней записывались изменения показателей веса животных и в конце каждого эксперимента животные усыплялись, чтобы получить данные бронхоальвеолярного лаважа (БАЛ) и легкие из каждой группы. Символы обозначают отдельных животных, а горизонтальная линия - способ. (Рис. 3А). Графическое отображение потерь в весе для каждой группы животных после инфицирования (Рис. 3В). Общее количество клеток, проникающих в дыхательные пути (Рис. 3С). Процентное соотношение клеток, которые положительно отреагировали на двойное окрашивание с CD11b и Gr1 в БАЛ (Рис. 3D). Выявление РНК вируса hMPV в легких инфицированных мышей путем проведения количественной ПЦР. Общая РНК из легких каждого усыпленного животного была получена и использована для производства комплементарной ДНК (кДНК) путем обратной транскрипции. Впоследствии, полученная кДНК была использована в количественной ПЦР для определения числа копий вирусной РНК, которая присутствует в образце по отношению к количеству экземпляров β-актина РНК. На Рис. 3А можно наблюдать, что рекомбинантная вакцина BCG для белков Р ( ) и М2 (
) и М2 ( ) была защитой от потери веса у инфицированных животных, получая вес такой же, как и у не инфицированных животных. Более того, животные, которые не были иммунизированы или были привиты вакциной BCG дикого типа (WT-BCG) (
) была защитой от потери веса у инфицированных животных, получая вес такой же, как и у не инфицированных животных. Более того, животные, которые не были иммунизированы или были привиты вакциной BCG дикого типа (WT-BCG) ( ), Live-hMPV (
), Live-hMPV ( ) или UV-hMPV (
) или UV-hMPV ( ) страдали от большей потери веса тела после заражения.
) страдали от большей потери веса тела после заражения.
На Рис. 3В и 3С показывается, что рекомбинантная вакцина BCG для белка Р препятствует проникновению иммунных клеток в дыхательные пути животных после заражения, получая такую же инфильтрацию как и у неинфицированных животных. Кроме того, животные, которые не были иммунизированы или были привиты вакциной BCG дикого типа (WT-BCG) ( ), Live-hMPV (
), Live-hMPV ( ) или UV-hMPV (
) или UV-hMPV ( ) страдали от постинфекционной иммунной клеточной инфильтрации в их дыхательные пути. Вакцинация с pBCG-M2 дает неполную защиту. На Рис. 3D видно, что количество вируса hMPV, выраженного в копиях генов N-hMPV в 5000 экземпляров, β-актин присутствует в легких инфицированных животных, которые не были иммунизированы, точно также как и животных, иммунизированных вакцинами WT-BCG, Live-hMPV or UV-hMPV. То есть это значит, что они не будут обеспечивать защиту, а зараженные животные, иммунизированные rBCG P-MPV, практически не имеют вируса, как и неинфицированные животные. Вакцинация rBCG-M2 не гарантирует полную защиту.
) страдали от постинфекционной иммунной клеточной инфильтрации в их дыхательные пути. Вакцинация с pBCG-M2 дает неполную защиту. На Рис. 3D видно, что количество вируса hMPV, выраженного в копиях генов N-hMPV в 5000 экземпляров, β-актин присутствует в легких инфицированных животных, которые не были иммунизированы, точно также как и животных, иммунизированных вакцинами WT-BCG, Live-hMPV or UV-hMPV. То есть это значит, что они не будут обеспечивать защиту, а зараженные животные, иммунизированные rBCG P-MPV, практически не имеют вируса, как и неинфицированные животные. Вакцинация rBCG-M2 не гарантирует полную защиту.
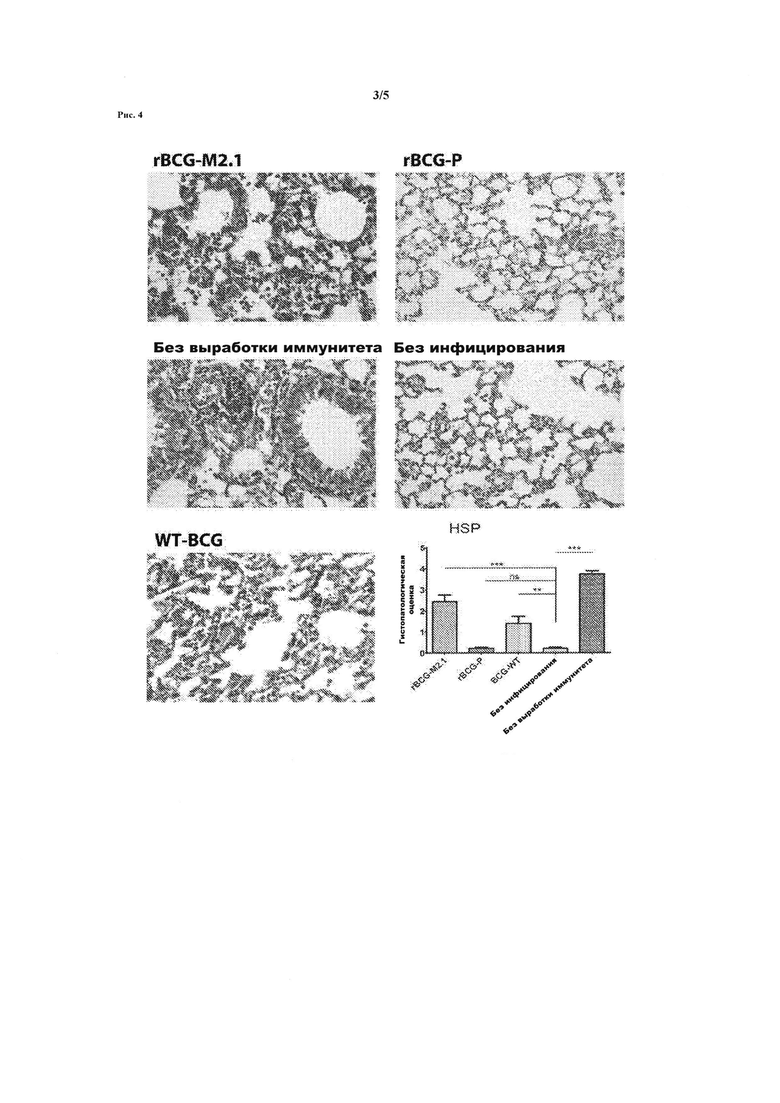
Рисунок 4. Иммунизация rBCG-P-hMPV, (бациллой Кальметта-Герена человеческого метапневмовируса) защищает от воспаления после заражения hMPV. Легкие животных удалили через 6 дней после заражения с 1×106 БОЕ (бляшкообразующая единица) hMPV, зафиксировали в параформальдегиде и залили парафином, 7 мкм срезы были окрашены гематоксилином и эозином. Наблюдалась значительная инфильтрация полиморфных ядерных клеток у иммунизированных животных или животных, иммунизированных rBCG-M2.1-hMPV или WT-BCG. Тем не менее, не наблюдается никаких признаков воспаления в легких, полученных от животных, иммунизированных rBCG-P-hMPV. На изображениях представлено шесть независимых экспериментов. HSP (белок теплового шока) представляет количественное определение показателя воспаления в группе животных (показатель гистопатологии). Позитивным является то, что воспаление у животных, иммунизированных rBCG-P-MPV и инфицированных, было очень слабым или вообще отсутствовало, аналогично неинфицированным животным.
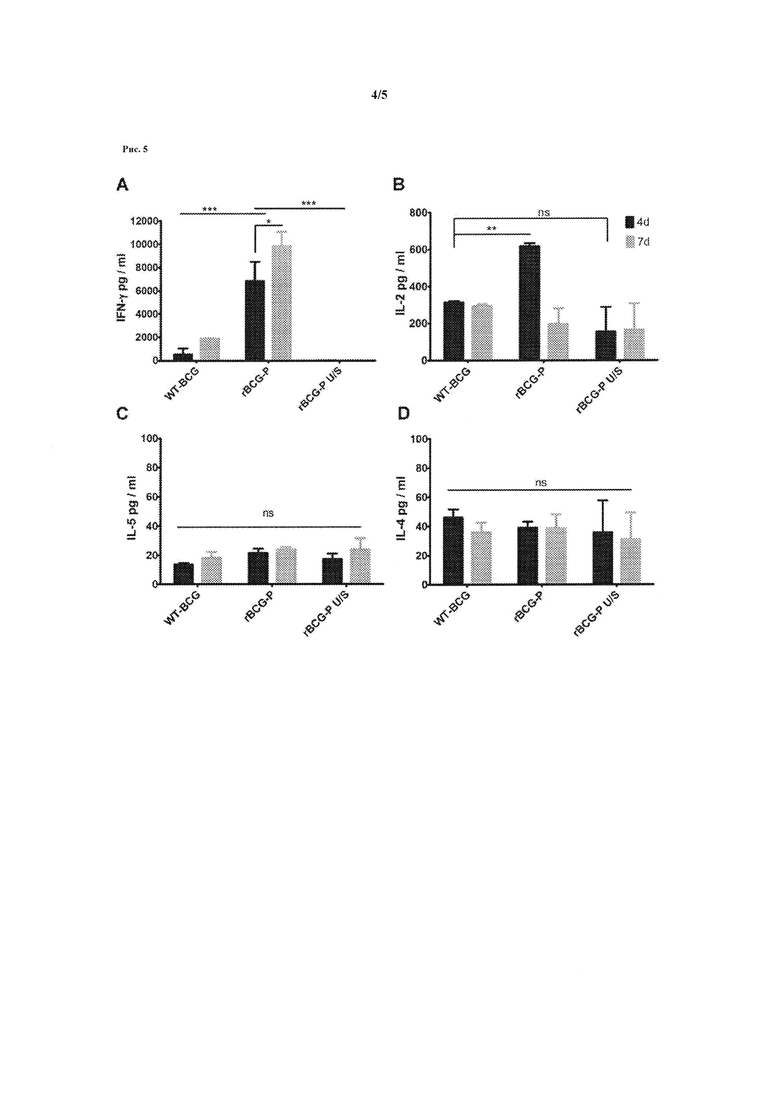
Рисунок 5. Иммунизация rBCG-P-hMPV производит цитокиновый профиль Th1-типа. Для определения типа иммунного ответа, ответственного за rBCG-P-hMPV иммунитета, был проанализирован цитокиновый профиль клеток селезенки лабораторных мышей BALB / cj иммунизированных BCG штаммом рекомбинантного hMPV Р-белка (rBCG-P-hMPV, на графике: rBCG-P). Селезенки четырех мышей BALB / cj иммунизированных с помощью rBCG-P-hMPV были восстановлены и клетки селезенок стимулировали в течение 7 дней инкубации с 10 мкг Р-белок-hMPV или PBS (фосфатно-солевым буфером) (U/S на графике). В качестве контроля клетки селезенки мышей BALB / cJ иммунизированных WT-BCG культивировали при тех же условиях. Кондиционированную среду стимулированных и не стимулированных rBCG-P-hMPV и WT-BCG клеток селезенки анализировали с помощью иммуноферментного анализа для определения уровней (A) IFN-γ, (В) IL-2, (С) IL-5 и (D) IL-4 на 4 и 7 дне культивации. Клетки селезенки, полученные из rBCG-P-hMPV стимулированные Р-протеином-hMPV (rBCG-P) выделяли объемы значительно выше интерферона гамма сравнительно с клетками животных, иммунизированных WT-BCG или не стимулированными клетками (rBCG-P U/S) (*** р<0,001, критерий Стьюдента), Рисунок 5А. Кроме того, объем интерферона гамма увеличился между 4-м и 7-м днем (* р<0,05, критерий Стьюдента), Рисунок 5А. Стимулированные клетки селезенки мышей, иммунизированных rBCG-P-hMPV вырабатывают значительно большее количество IL-2 на 4-й день по сравнению с не стимулированными клетками (rBCG-P U/S) и базальный уровень снизился на 7 день (**, р<0,001; НС = не существенно, критерий Стьюдента), Рисунок 5В. Клетки селезенки выделили небольшое количество IL-5 and IL-4, не показав увеличения по сравнению с клетками селезенки от WT-BCG или без стимуляции (НС = не существенно, критерий Стьюдента), Рисунок 5С.
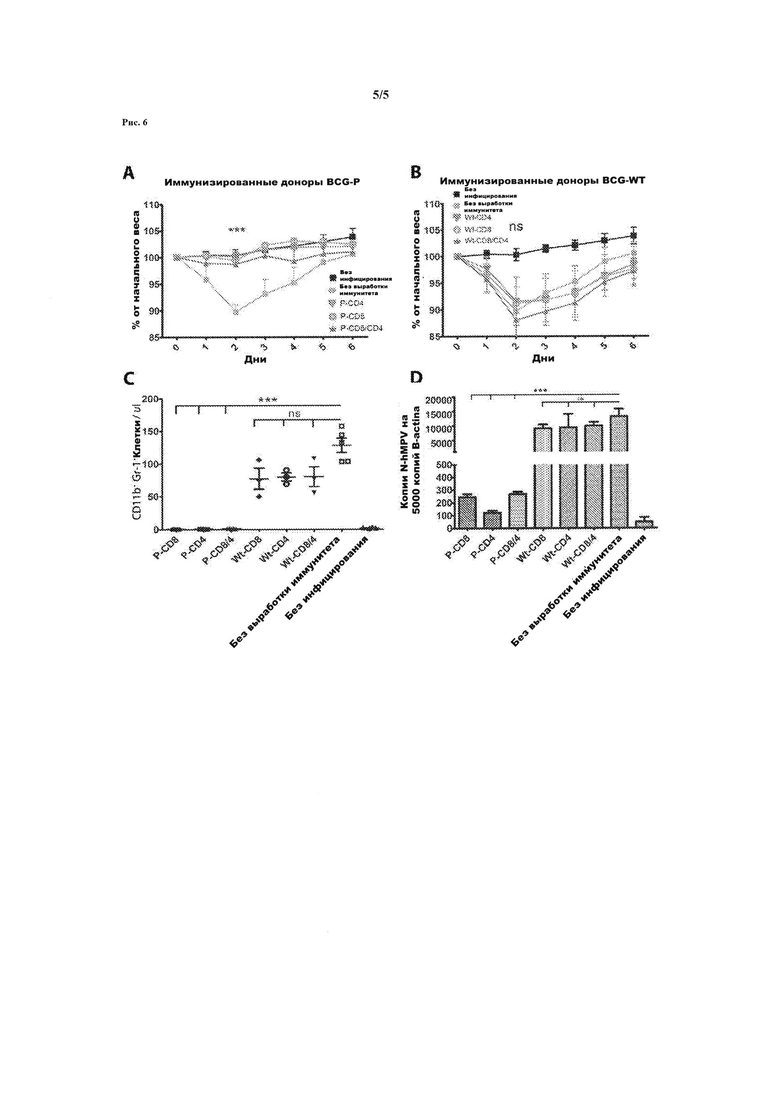
Рисунок 6. Передача Т-лимфоцитов от мышей, иммунизированных rBCG-P-hMPV выработала устойчивость к hMPV-инфекции у неинфицированных мышей. CD4 + Т-лимфоциты и CD8 + Т-клетки очистились от стимулированных и нестимулированных спленоцитов с рекомбинантными вирусными белками. Независимо друг от друга два миллиона стимулированных или нестимулированных CD4 + или CD8 + Т-лимфоцитов от животных, иммунизированных rBCG-P-MPV или WT-BCG были переданы через хвостовую вену неинфицированных мышей. Через двадцать четыре часа после передачи, мыши были интраназально инфицированы 1×106 БОЕ hMPV. На рис. 6А мыши, которым передали CD4+ и/или CD8+ Т-лимфоцитов от животных, иммунизированных rBCG-P-MPV, показали отсутствие различий в массе тела по сравнению с неинфицированными мышами. Напротив, мы наблюдали, что у мышей, которым передали CD4 + и/или CD8 + Т-лимфоцитов от животных, иммунизированных WT-BCG потеряли значительно больше веса после инфицирования по сравнению с инфицированными животными (р<0,0001) (Рисунок 6В). На рисунке 6С, показано, что бронхоальвеолярные выделения, BAL, у неинфицированных мышей, которым ранее передали CD4+ и/или CD8+ Т-лимфоцитов от животных, иммунизированных (P-CD8, Р-CD4, P-CD8/4), показывает инфильтрацию гранулоцитов значительно ниже по сравнению с мышами которым передали Т лимфоциты из WT-BCG (Wt-CD8, Wt-CD4, Wt-CD8/4) (*** p<0,0001, тест Стьюдента). Инфильтрация гранулоцитов в бронхоальвеолярных выделениях, BAL, у мышей которым передали Т лимфоциты из WT-BCG или неиммунизированных мышей не показали существенных различий с инфильтрацией у мышей, которые не получили Т-лимфоциты (NS = не существенно, тест Стьюдента). Рисунок 6D показывает, что уровень вирусной нагрузки в легких мышей которым передали Т лимфоциты (P-CD8, P-CD4, P-CD8/4) от мышей, иммунизированных rBCG-P-hMPV, был низким по сравнению с уровнем вирусной нагрузки у мышей, которым передали Т лимфоциты (Wt-CD8, Wt-CD4, Wt-CD8/4) от животных, иммунизированных штаммом WT-BCG и неиммунизированных животных (***, р<0,0001, тест Стьюдента). Вирусная нагрузка в легких мышей которым передали Т лимфоциты из WT-BCG (Wt-CD8, Wt-CD4, Wt-CD8/4), показывает отсутствие существенных различий с неиммунизированными мышами (NS = не существенно, тест Стьюдента). Уровень вирусной нагрузки количественно определялся как генные копии N-hMPV по RT-qPCR (количественная полимеразная цепная реакция), как было описано выше.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение состоит из иммуногенного препарата против hMPV, содержащего рекомбинантный штамм BCG, выделяющий Р-белок из метапневмовируса человека. Этот препарат обеспечивает эффективную защиту против инфицирования hMPV и не вызывает воспалительной гиперреактивности.
Изобретенный препарат может быть введен отдельно или в смеси с другими вакцинами, например, с иммуномодулирующим препаратом против SRV респираторно-синцитиального вируса (РСВ) в смешанной дозе, которая будет обеспечивать защиту от инфекции и/или осложнений, связанных с hMPV и РСВ.
Иммуномодулирующий препарат, описанный в этом изобретении может быть использован для приготовления вакцины, содержащей живые ослабленные рекомбинантные бактерии, из стерильных культур в дозах от 1×104 КОЕ (колониеобразующая единица) до 1×1010 КОЕ на дозу, особенно предпочтительнее 1×108 КОЕ на дозу. Препарат будет представлен в виде восстановленного лиофилизированного раствора, который не требует вспомогательного вещества, поскольку в качестве этого вещества выступает состав клеточной оболочки рекомбинантных бактерий. Изобретенный лиофилизированный иммуномодулирующий препарат, должен храниться в пределе температур от 4° до 8°С, в месте защищенном от прямого и непрямого солнечного света, представлен в двух отдельных флаконах, один из которых содержит лиофилизированные рекомбинантные бактерии, другой содержит укрепляющий физиологический раствор, которые следует смешать перед введением.
С момента своего появления в 1921 году вакцина на основе Микобактерий bovis bacillus Кальметта-Герена (BCG) была использована для более одного миллиарда человек, и в настоящее время используется для лечения туберкулеза во всем мире.
Авторами настоящего изобретения было обнаружено, что способ изменить баланс иммунного ответа с Th2-типа противовоспалительного ответа, защита которого не стабильна со временем, на Th1-Тип клеточной реакции, в частности, CD8+ цитотоксических Т- и CD4+ Т-вспомогательных клеток, представляет собой использование вспомогательных веществ, таких как компоненты клеточной стенки микобактерий. В частности, выделяющие иммуномодулирующий белок из hMPV в Микобактериях bovis bacillus Кальметта-Герена (BCG).
F и G белков с hMPV находятся на поверхности вирусной частицы и, следовательно, доступны для циркулирующих антител. Таким образом, эти белки будут очевидным выбором для вакцины на основе антител, чтобы предотвратить инфицирование hMPV.
Несмотря на вышесказанное, в настоящем изобретении, мы решили использовать неэкспонированные капсидные белки в качестве иммуномодулятора, в частности, Р-белок, в сочетании с вспомогательным веществом, который способствует Th1-Типу реакции клеток, таких как ослабленные Микобактерий bovis bacillus (BCG). Было обнаружено, что капсидные белки hMPV М2.1 способствуют активации цитотоксических лимфоцитов (ЦТЛ). Удивительно, но в настоящем изобретении описано применение Р-белка, белка который не подвергся воздействию из вируса hMPV, который при использовании в качестве иммуномодулирующего белка выделяемого микобактериями позволяет разработать иммуномодулирующий препарат, который при использовании в качестве вакцины или иммуномодулирующего препарата обеспечивает эффективную защиту без нежелательных побочных эффектов, таких как воспалительная гиперреактивность.
Рекомбинантные белки выделяемые вектором бактерии, используемые в настоящем исследовании, получены путем клонирования генов, закодированных в той же группе вирусов hMPV в прокариотических векторах выделения, все находятся в свободной продаже. Геном метапневмовируса (hMPV) был описан ранее и имеется в базе данных Генетического банка, инвентарный номер: АВ503857.1, DQ843659.1, DQ843658.1, EF535506.1, GQ153651.1, AY297749.1, AY297748.1, AF371337.2, FJ168779.1, FJ168778.1, NC 004148.2 и AY525843.1. Получение рекомбинантного штамма бактерий, описанное в данном исследовании, включает гетерогенное выделение вирусных белков при репродукции бактерий в организме хозяина. Гетерогенные последовательности ДНК интегрированы в бактериальную хромосомную ДНК с помощью вектора выделения pMV361. Эти белки hMPV могут быть генетически модифицированы, например, путем включения пептидных последовательностей или гликозилированных доменов и/или последующего назначения эндоцитарных или фагоцитарных рецепторов антигенпредставляющих клеток путем их соединения с природными лигандами с использованием биотин-стрептавидин системы (с использованием коммерческих наборов биотинилирования и генетической модификации вирусных белков путем связывания с бактериальным белком стрептавидином, или путем введения генетической последовательности для кодирования аминокислотных последовательностей, описанных как биотинилирование сигналов в рекомбинантных белках или белковых фрагментах, с использованием методик, описанных выше для прокариотических и/или эукариотических гетерогенных систем выделения).
Изобретенный иммуномодулирующий препарат включает в себя выделение hMPV Р-белка либо полностью, либо его иммуногенного фрагмента, в виде штамма ослабленных микобактерий. Особенно предпочтительным является рекомбинантный штамм ослабленных микобактерий, полученных из штамма бактерий Кальметта-Герена (BCG). hMPV Р-белок может быть Р-белком из метапневмовируса подтипов А или В.
Рекомбинантный штамм ослабленных микобактерий изобретения может содержать последовательности нуклеиновой кислоты, закодированных для hMPV Р-белка или его иммуномодулирующего фрагмента встроенного в бактериальный геном или во внехромосомную плазмиду, в одном или нескольких экземплярах. Выделение белка может находиться под контролем основных или индуцируемых, эндогенных или экзогенных стимуляторов из микобактерий BCG.
hMPV Р-белок или его иммуномодулирующий фрагмент могут быть выражены в растворимой, цитоплазматической форме, выделяемого вне клетки или мембраносвязанного белка.
Изобретенный иммуномодулирующий препарат может содержать два или более рекомбинантных штаммов ослабленных микобактерий, в котором белки или иммуномодулирующие фрагменты hMPV Р-белка из штаммов выделяются для производства различного количества копий, выделяемых базово или индуцируемо, и/или расположены в разных местах клетки.
Описанный здесь иммуномодулирующий препарат, может быть использован в сочетании с другими иммуномодулирующими препаратами, содержащими дополнительные составы антигенов против различных вирусов hPCB и hMPV, с ослабленными штаммами BCG и сезонными вакцинами против гриппа А и В.
Вышеописанный иммуномодулирующий препарат можно применять для людей в субдермальной/подкожной форме в сочетании с буферным раствором (PBS, натрий-фосфатный буфер) или физиологическим раствором.
Для разработки рекомбинантной Микобактерии, выделяющей hMPV Р-белок, мы сначала должны сформировать вектор, выделяющий указанный белок. Можно использовать любой известный микобактериальный вектор выделения, кодирующий ген для Р-белка вируса hMPV, который должен быть внедрен вместе с его стимуляторной областью. В предпочтительном варианте выполняется обратное копирование с универсальными праймерами из РНК, выделенной из отдельного метапневмовируса человека. Впоследствии Р-белок гена усиливается специфическими праймерами (Рисунок 1А). Продукт усиления внедряется в вектор выделения. В настоящем изобретении мы использовали микобактериальный вектор выделения pMV361, формируя вектор pMV361-П-hMPV (Рисунок 1В).
Полученный вектор, используется для трансформации штамма микобактерий, таких как Микобактерии BCG. Для изобретения может быть использован любой известный штамм BCG, например, BCG Пастера или Датский BCG. Методом трансформации может выступать любой доступный метод, особенно предпочтительным является метод электротрансформации. В дальнейшем, должны быть выбраны трансформированные клетки, выделяющие hMPV Р-белок.
Эти рекомбинантные клетки являются иммуномодулирующим составом изобретения, которые предоставляются в количестве от 104 до 109 КОЕ/ на дозу в фармакологически соответствующем солевом буфере.
Кроме того, изобретенный препарат может быть приготовлен в сочетании с рекомбинантными штаммами BCG, выделяемыми иммуномодулирующими белками из респираторно-синцитиальный вируса (РСВ). В предпочтительном варианте рекомбинантные бактерии BCG выделяющие hMPV Р-белки представлены в сочетании с рекомбинантными бактериями BCG, выделяющими N, Р, М, F, М2 (ORF1 и 2), SH, G или L протеины из РСВ. В более предпочтительном варианте реализация изобретения иммуномодулирующего препарата используется в комбинации со штаммом рекомбинантного BCG для N гена из РСВ. В частности, предпочтительным является сочетание рекомбинантной BCG гена Р из hMPV подтипа А и рекомбинантной BCG для N гена РСВ подтипа А.
В другом варианте изобретения штамм BCG трансформируется вектором, выделяющим hMPV С-белок, а затем трансформированные клетки вновь трансформируются вектором, выделяя белок респираторно-синцитиального вируса (РСВ). Белок РСВ, выбранный из N, Р, М, F, м2 (ORF1 и 2), SH, G or L. В частности, во-первых, предпочтительнее трансформация вектором, выделяющим Р-белок из hMPV подтипа А, во-вторых подвергать эти трансформированные штаммы второго преобразования вектором, выделяющим N ген РСВ подтипа А, с получением вакцины штамма BCG, одновременно выделяющих Р-белок из hMPV подтипа А и N-белок из СРВ подтипа А.
Изобретенный иммуномодулирующий препарат может быть предоставлен в лиофилизированной, многодозовой форме готовой для разведения в 1 мл прилагаемого солевой раствора для получения 1×109 КОЕ/мл восстановленного раствора. Каждые 0,1 мл повторно суспендированного раствора будет содержать соответствующую дозу 1×108 КОЕ для введения.
Для приготовления лиофилизированного раствора трансформированных штаммов изобретенного препарата разведение можно произвести в любом подходящем растворе для лиофилизации. Например, можно использовать лиофильную добавку с буфером, содержащим 4% (вес/объем) маннитола, 0.05% (Вт/в) Тилоксапола, 0.25% сахарозы и 5 мМ гистидина. Затем он может быть лиофилизирован и должен храниться при 25°С.
Восстановительный раствор может быть создан любым доступным в своем виде способом. В одном из вариантов это разведение раствора Саутон ИСС предпочтительнее при -80°С (125 мг соли MgSO4, 125 мкг K2HPO4, 1 мг L - аспарагина, 12.5 мкг цитрата аммония железа, 18.4 мг 85% глицерина, 0,5 мг лимонной кислоты в 1 мл H2O). В другом варианте, изобретенный препарат может быть разведен в PBS (фосфатно-солевом буферном растворе) (137 мм NaCl; 2,7 мм Кcl; 4.3 мм Na2HPO4; 1,47 мм КН2РО4, рН 7,4) с добавлением 20% глицерина, 0.02% Твин-80 в конечной концентрации 108 бактерий на 100 мкл и сохранен при -80°С. Оба в присутствии неионного неионогенного очищающего средства, такого как 0,1% Твин-80 или 0,05% Тилксапола.
Изобретенный препарат должен храниться при температуре в пределах 4-8°С до и после восстановления, препарат постоянно держать вдали от прямого и непрямого солнечного света, после восстановления его следует выбросить в конце дня.
Следующие примеры создания и использования иммуномодулирующего состава против hMPV на основе рекомбинантных бактерий Микобактерии выделяющей белки вируса, являются лишь примерами и не предназначены для ограничения производства или сферы применения изобретения. Несмотря на то, что в следующих описаниях используются специфические термины, их использование носит лишь описательный характер, а не ограничительный.
ПРИМЕРЫ
Пример I: Создание рекомбинантного вектора, позволяющего выделение для hMPV Р-белка у микобактерии BCG.
Кодирующую область гена метапневмовируса Р усилили из РНК, с использованием следующих праймеров: P-hMPV_Fw: GAATTCATGTCATTCCCTGAAGGAAA (SEQ ID No 1) и P-hMPV_Rv: GAATTCCTACATAATTAACTGGTAAA (последовательность ID №2), где подчеркнутые последовательности включают участок EcoRI на обоих концах усиления продукта, Рисунок 1А. Микобактериальный вектор pMV361 был линеаризован в участок EcoRI, позволяя внедрить последовательность, соответствующую гену Р из hMPV:

Внедрение бескорпусного гена hMPV Р в участок EcoRI вектора pMV361 располагает его под контроль стимулятора hsp60 и ведет к построению pMV361-П-hMPV (Рисунок 1В).
Пример II: иммуногенный препарат, содержащий 10 доз 1×108 КОЕ каждой из BCG датского штамма рекомбинантного для гена Р HMPV подтипа А.
Ген Р HMPV подтипа А вводится в одном экземпляре в бактериальный геном при регуляции стимулятора эндогенных конститутивных БТШ 60 из микобактерий BCG для экспрессии белка.
Микобактериальная BCG датского штамма (АТСС 35733) была преобразована при помощи электротрансформации с плазмидой pMV361-P-HMPV, полученной из плазмиды pMV361 (Стовер и др., 1991), которая вводится один раз в бактериальный геном. Эта плазмида содержит ген, кодирующий Р-белок HMPV подтипа А, который экспрессируется под эндогенным конститутивным промотором гена hsp60 из BCG. Полученные рекомбинантные колонии выращивают (при 37°С в дополненной культуральной среде Миддлброка 7Н9 (4,9 г/л)) до НД600нм=1, центрифугируют при 4000 оборотах в минуту в течение 20 мин (в роторе Эппендорфа модели 5702/R А-4-38) и повторно суспендируют в фосфатно-солевом буферном растворе (137 мМ NaCl, 2,7 мМ KCl, 4,3 мМ Na2HPO4, 1,47 мМ KH2PO4, рН 7,4) с добавлением 20% глицерина и 0,02% Твина 80 до конечной концентрации 108 бактерий на 100 мкл, и сохраняют при температуре - 80°С.
Аналогичным образом штаммы можно вновь суспендировать в растворе объемом: 25% объема лактозы и среде Проскауэра-Бека с добавлением глюкозы и твина 80 (PBGT: 0,5 г аспарагина, 5,0 г первичного кислого фосфата, 1,5 г цитрата магния, 0,5 г сульфата калия, 0,5 мл твина 80 и 10,0 г глюкозы на литр дистиллированной воды) до лиофилизации, а затем сохранять при температуре 25°С.
С помощью Вестерн-блоттинга и антител для Р-белка HMPV можно заметить, что этот штамм BCG конститутивно экспрессирует Р-белок из HMPV подтипа А в цитоплазме (рис. 2А).
Иммунизация мышей инбредной линии BALB/c субдермальной дозой 1×108 колониеобразующих единиц (КОЕ) rBCG-P-HMPV путем вакцины обеспечивает защиту этих животных от интраназального заражения 106 бляшкообразующими единицами HMPV подтипа А (рисунок 3). Эффект вакцины по изобретению, rBCG-P-HMPV, сравнивали с вакциной rBCG, экспрессирующей еще один белок HMPV - белок М2, а также с нетрансформированными BCG; неиммунизированная группа использовалась для контроля, все группы были интраназально инфицированны HMPV. Также был включен контроль неиммунизированных и неинфицированных животных. Изменение веса животных после заражения были проанализированы, результаты показаны на рисунке 3А. Обе рекомбинантные вакцины BCG для Р ( ) и М2 (
) и М2 ( ) белков HMPV защитили животных от потери веса после заражения; их вес был аналогичен весу неинфицированных животных (
) белков HMPV защитили животных от потери веса после заражения; их вес был аналогичен весу неинфицированных животных ( ). Кроме того, неиммунизированные животные (
). Кроме того, неиммунизированные животные ( ) или животные, иммунизированные с помощью BCG дикого типа (WT-BCG) (
) или животные, иммунизированные с помощью BCG дикого типа (WT-BCG) ( ), живой вакцины HMPV (
), живой вакцины HMPV (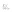 ) или ВВ-вакцины HMPV (
) или ВВ-вакцины HMPV ( ) понесли потери массы тела после заражения.
) понесли потери массы тела после заражения.
Также был проведен анализ инфильтрации иммунных клеток в дыхательные пути животных после заражения, которая является ориентировочным показателем развития заболевания. Анализ был проведен в виде подсчета количества клеток, проникших в дыхательные пути (рис 3В), и проникающих клеток, которые являются позитивными в отношении CD11b и Gr1 в соответствии с гранулоцитами (рис. 3С). Рисунок 3b показывает, что только вакцина rBCG-P-HMPV помешала инфильтрации лимфоцитов в дыхательные пути, что обеспечило инфильтрацию, как у незараженных животных. Кроме того, неиммунизированные животные или животные, иммунизированные с помощью BCG дикого типа (WT-BCG) или вакцины rBCG-M2-HMPV страдали от инфильтрации иммунных клеток в дыхательных путях после инфицирования. Вакцинация rBCG-M2 обеспечила неполную защиту дыхательных путей животных для инфильтрации иммунных клеток.
Кроме того было проанализировано количество копий гена РНК N-HMPV в легочных клетках различных групп исследуемых животных. Большее количество копий вируса HMPV РНК свидетельствует о большей инфекции, результаты нормализованы на копии β-актина. Результаты показаны на рисунке 3D. Следует понимать, что количество вируса HMPV, присутствующего в легких неиммунизированных инфицированных животных, аналогично количеству данного вируса у инфицированных животных, иммунизированных с помощью WT-BCG, живой вакцины HMPV или ВВ-вакцины HMPV, т.е. эти прививки не могут обеспечить защиту. Замечено, что иммунизация с помощью rBCG-M2 обеспечила неполную защиту. Кроме того, вирус практически отсутствует у инфицированных животных, иммунизированных вакциной rBCG-P; полученные результаты были аналогичны результатам, полученным в группе незараженных животных. Это доказывает, что препарат эффективно защищает от инфекции с HMPV.
Пример III: иммуногенная композиция, содержащая 5×107 бактерии Микобактериальной BCG датского штамма, рекомбинантной для гена Р HMPV подтипа A, и 5×107 бактерий Микобактериальной BCG датского штамма, рекомбинантной гена для N RSV подтипа А.
В каждой бактерии, входящей в состав иммуногенной композиции, гены из HMPV и RSV вводятся в бактериальный геном в одном экземпляре под регулированием при помощи эндогенного конститутивного промотора hsp60 из BCG. Экспрессия белка является цитоплазматической. Иммуногенная композиция сохраняется в фосфатно-солевом буферном растворе (137 мМ NaCl, 2.7 мМ KCl, 4.3 мМ Na2 НРО4, 1.47 мМ KH2PO4, рН 7.4) с добавлением 20% глицерина и 0,02% Твина 80 в конечной концентрации 108 бактерий на 100 мкл, при температуре -20°С.
BCG датского штамма (АТСС 35733) была преобразована при помощи электротрансформации с плазмидой pMV361-P HMPV с получением штамма rBCG-P-MPV; дополнительно вторая группа была преобразована с помощью pMV361-N SRV для получения трансформированного штамма rBCG-N СРВ. Эти плазмиды были получены из плазмиды pMV361 (Стовер и др., 1991), которая вводится один раз в бактериальный геном. Полученные рекомбинантные колонии выращивают при 37°С в дополненной культуральной среде Миддлброка 7Н9 до НД600нм=1, центрифугируют при 4000 оборотах в минуту в течение 20 мин (в роторе Эппендорфа модели 5702/R А-4-38) и повторно суспендируют в фосфатно-солевом буферном растворе (137 мМ NaCl, 2.7 мМ KCl, 4.3 мМ Na2HPO4, 1.47 мМ KH2PO4, рН 7.4) с добавлением 20% глицерина и 0,02% Твина 80 до конечной концентрации 107 бактерий на 100 мкл, и сохраняют при температуре - 20°С. Штаммы ресуспендировали в буфере LYO С, содержащем 4% (вес/объем) маннита, 0,05% (вес/объем) Тилоксапола, 0,25% сахарозы и 5 мМ гистидина, затем подвергали лиофилизации и сохраняли при температуре 4°С. С помощью Вестерн блоттинга и специфических антител для Р-белка HMPV или N-белка RSV было обнаружено, что датские штаммы BCG рекомбинантно экспрессировали - Р-белок HMPV или N-белок SRV подтипа А, соответственно (рисунок 2). Иммуногенная композиция, содержащая оба трансформированных штамма, одновременно приобрела иммунитет от HMPV и вируса RSV.
Пример IV: иммуногенной композиции 104 бактерий из BCG датского штамма рекомбинантного для гена Р от HMPV подтипа A.
BCG датского штамма был преобразован геном Р от HMPV подтипа. А таким образом, что ген был введен в бактериальный геном в одном экземпляре под регуляцией эндогенного индуцибельного ACR промотора из BCG, который активно реагирует на оксид азота, низкую концентрацию кислорода и стационарные фазы роста. Экспрессия белка является цитоплазматической. Иммуногенную композицию подвергли лиофилизации в буфере LYO С, содержащем 4% (вес/объем) маннита, 0,05% (вес/объем) тилоксапола, 0,25% сахарозы и 5 мМ гистидина, и сохраняется при температуре 25°С в разбавленном растворе Саутона SSI (125 мкг MgSO4, 125 мкг K2HPO4, 1 мг L-аспарагина, 12,5 мкг цитрата аммония трехвалентного железа, 18,4 мг 85% глицерина, 0,5 мг лимонной кислоты в 1 мл Н2О). В качестве альтернативы, трансформированные штаммы могут быть сохранены в фосфатно-солевом буферном растворе (137 мМ NaCl; 2.7 мМ KCl; 4.3 мМ Na2HPO4; 1.47 мМ KH2PO4, рН 7,4) с добавлением 20% глицерина и 0,02% Твина 80 до конечной концентрации 104 бактерий на 100 мкл.
BCG датского штамма (Американская коллекция типовых культур, www.atcc.org, номер АТСС 35733) была преобразована при помощи электротрансформации с плазмидой pMV361Pacr/P-HMPV, которая была получена из плазмиды pMV361 (Стовер и др., 1991), которая вводится один раз в бактериальный геном. Эта плазмида содержит ген, кодирующий Р-белок HMPV подтипа А, который экспрессируется под действием эндогенного индуцибельного ACR промотора BCG. Полученные рекомбинантные колонии выращивают (при 37°С в дополненной культуральной среде Миддлброка 7Н9) до НД600нм=1, центрифугируют при 4000 оборотах в минуту в течение 20 мин (в роторе Эппендорфа модели 5702/R А-4-38) и повторно суспендируют в Lyo С буферном растворе, состоящем из 4% (вес/объем) маннита, 0,05% (вес/объем) тилоксапола, 0,25% сахарозы и 5 мМ гистидина. И, наконец, 1 мл аликвот 104 бактерий лиофилизируют и сохраняют при температуре 25°С. Аналогичным образом, штаммы могут быть сохранены в фосфатно-солевом буферном растворе (137 мМ NaCl; 2.7 мМ KCl; 4.3 мМ Na2HPO4; 1.47 мМ KH2PO4, рН 7,4) с добавлением 0,02% Твина 80 и 20% глицерина в конечной концентрации 104 бактерий на 100 мкл. Эта иммуногенная композиция дает иммунитет против вируса HMPV.
Пример V: иммуногенная композиция, состоящая из 109 бактерий BCG датского штамма, рекомбинантной для гена Р HMPV подтипа А.
Ген вводят в бактериальный геном в единственном экземпляре, в соответствии с положением экзогенного Т7-фагового промотора для конститутивной экспрессии в штаммах BCG, что совместно экспрессируется Т7-фаговой полимеразой. Экспрессия белка является цитоплазматической. Иммуногенную композицию суспендируют в разбавленном растворе Саутона SSI (125 мкг MgSO4, 125 мкг K2HPO4, 1 мг L-аспарагина, 12,5 мкг цитрата аммония трехвалентного железа, 18,4 мг 85% глицерина, 0,5 мг лимонной кислоты в 1 мл H2O) и сохраняют при температуре 20°С. Также композицию можно лиофилизировать и сохранить при температуре 4°С. Аналогичным образом, штаммы могут быть сохранены в фосфатно-солевом буферном растворе (137 мМ NaCl; 2.7 мМ KCl; 4.3 мМ Na2HPO4; 1.47 мМ KH2PO4, рН 7.4) с добавлением 0,02% твина 80 и 20% глицерина до конечной концентрации 109 бактерий на 100 мкл.
BCG датского штамма АТСС 35733 была преобразована при помощи электротрансформации с плазмидой pMV361PT7/P-HMPV, которая была получена изплазмиды (Стовер и др., 1991), которая вводится один раз в бактериальный геном. Эта плазмида содержит ген, кодирующий Р-протеин HMPV подтипа А, который экспрессирует под действием Т7 промотора, активированного экспрессией Т7-фаговой полимеразы.
Полученный штамм BCG был преобразован при помощи электротрансформации с плазмидой pMV261Amp/PolT7, которая была получена из плазмиды pMV261 (Стовер и др., 1991), Полученный штамм BCG был преобразован при помощи электротрансформации с плазмидой pMV261Amp/PolT7, которая была получена из плазмиды pMV261 (Стовер и др., 1991), которая находится вне хромосомы в нескольких экземплярах внутри бактерии. В этой плазмиде резистентность по отношению к антибиотику канамицину была заменена устойчивостью к антибиотику гигромицину (Hygr). Т7-полимераза из фага Т7 находится под контролем конститутивного промотора гена hsp60 BCG. Полученные рекомбинантные колонии выращивают при 37°С в дополненной культуральной среде Миддлброка 7Н9 до НД600нм=1, центрифугируют при 4000 оборотах в минуту в течение 20 мин (в роторе Эппендорфа модели 5702/R А-4-38) и повторно суспендируют в разбавленном растворе Саутона SSI (125 мкг MgSO4, 125 мкг K2HPO4, 1 мг L-аспарагина, 12,5 мкг цитрата аммония трехвалентного железа, 18,4 мг 85% глицерина, 0,5 мг лимонной кислоты в 1 мл H2O) и сохраняют при температуре - 80°С.
Пример VI: Прививка 108 бактерий BCG датского штамма, рекомбинантных по гену hMPV-P в любой из иммуногенной композиций, которые обеспечивают защиту от иммунопатологических повреждений.
Прививка рекомбинантного штамма BCG, экспрессирующего Р-белок из метапневмовируса в любой из его композиций защищает от клинических признаков и симптомов заражения штаммами А и В HMPV. Уменьшает потерю аппетита, вызванную высокой температурой и недомоганием (рис. 3А), а также инфильтрацию дыхательных путей (рис. 3В и 3С). Также она уменьшает репликацию и распространение штаммов А и В HMPV (рис. 3D).
Прививка композиции в любом проявлении также значительно уменьшает гистопатологические проявления инфекции штаммов А и В HMPV. В легких животных, иммунизированных данной композицией, наблюдается гораздо меньший объем инфильтрации иммунных клеток, потери структуры и воспалений легочной ткани в сравнении с неиммунизированными животными или животными, иммунизированными штаммом дикого типа (Рисунок 4).
Прививка лекарственной формы с рекомбинантной BCG, экспрессирующей Р-белок HMPV в любом проявлении, создает клеточный иммунитет, который может быть передан лицам, ранее не подверженным экспериментам, путем выделения и очистки Т-лимфоцитов от иммунизированных доноров (Рисунок 6).
Приведенные выше примеры распространяются на иммунные препараты, содержащие рекомбинантный ослабленный штамм микобактерий, экспрессирующий Р-белок HMPV или его значительную часть, а также все комбинации с иммунологическими препаратами, содержащими рекомбинантный ослабленный штамм микобактерий, экспрессирующий любой из NS2, N, Р, М, SH, М2 (ORF1), М2 (ORF2), L, F или G белков RSV. Также примеры распространяются на иммунологические препараты, которые содержат один или несколько рекомбинантных ослабленных штаммов микобактерий; при этом указанная рекомбинантная бактерия содержит гены белка или иммуногенные фрагменты Р-белка HMPV, внедренного либо в бактериальный геном, либо в экстрахромосомную плазмиду (в одной или нескольких копиях), а его экспрессия управляется эндогенными или экзогенными, конститутивными или индуцируемыми промоторами, и это выражается в цитоплазматической растворимой внеклеточно-секретируемой форме или в качестве клеточных мембраносвязанных белков.
Использованная литература
Биачеси, С., Фам, К.Н., Скиадопулос, М.X., Мерфи, Б.Р., Коллинз, П.Л. и Бухгольц, У.Дж. (2005). Заражение низших приматов рекомбинантный человеческим метапневмовирусом, лишенным белков SH, G, или М2-2, каждый из которых классифицируется, как несущественный вспомогательный белок и определяет кандидатные вакцины. J Virol 79, 12608-12613.
Чеке, Г., Райт, Д.В., Толлефсон, С.Дж., Джонсон, Дж.Е., Кроув, Дж.Е. Младший и Вильямса, Дж.Б. (2007). Вакцинация человека слитым белком метапневмовируса, который является иммуногенным и защитным для хлопковых хомяков. J Virol 81, 698-707.
Денис Ф., Ален, С., Ханц, С. и Лагранж, П. (2005). [Противовирусная вакцинация и иммунитет слизистых оболочек органов дыхания: до сих пор разочаровывающие результаты соблазнительной идеи]. Presse Med 34, 1245-1253.
Хамелин, М.Е., Кутюр, К., Сэкетт, М., Кинер, П., Сузич, Дж., Ульбрандт, Н. и Буавен, Г. (2008). Профилактическое введение моноклонального антитела против человеческого метапневмовируса ослабляет вирусное заболевание дыхательных путей и гиперреактивность у мышей. Antivir Ther 13, 39-46.
Герфест, С., де-Грааф, М., Шраувен, Е.Дж., Спронг, Л., Хуссейн, К., ван ден Хуген, Б.Г., Остерхаусе, А.Д. и Фушье, Р.А. (2008а). Генерация чувствительных к температуре штаммов человеческих метапневмовирусов, которые обеспечивают защитный иммунитет у хомяков. J Gen Virol 89, 1553-1562.
Герфест, С., Шраувен, Е.Дж., де-Грааф, М., ван Амеронген Г., ван ден Хуген, Б.Г., де Сварт, Р.Л., Остерхаусе, А.Д. и Фушье, P.A. (2008b). Иммуногенность и эффективность двух кандидатных вакцин человеческого метапневмовируса у яванских макак. Вакцина 26, 4224-4230.
Каррон, Р.А., Райт, П.Ф., Белше, Р.Б. и другие авторы (2005). Идентификация рекомбинантной живой ослабленной дыхательной кандидатной вакцины синцитиального вируса, которая сильно ослаблена у детей раннего возраста. J Infect Dis 191, 1093-1104.
Колли, Д., Батаки, Е.Л., Спетч, Л., Герреро-Плата, А., Джуэлл, А.М., Пьедра, П.А., Миллиган, Г.Н., Гарофало, Р.П. и Касола, А. (2008). Т-лимфоциты способствуют противовирусному иммунитету и патогенезу при экспериментальном заражении человеческим метапневмовирусом. J Virol 82, 8560-8569.
Стовер, С.К., де-ла-Крус, В.Ф., Фюрст, Т.Р. и другие авторы (1991). Новое применение BCG для рекомбинантных вакцин. Nature 351, 456-460.
Иим, К.С., Крагин, Р.П., Бухалова, М.С., Бланко, Дж.С., Хэмлин, М.Е., Буавен, Г. Портер, Д.Д. и Принс Г.А. (2007). Человеческий метапневмовирус: усиление легочного заболевания у хлопковых крыс, иммунизированных вирусом вакцины, инактивированным формалином, в рамках контрольного лабораторного заражения. Вакцина 25, 5034-5040.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОТИВОТУБЕРКУЛЕЗНАЯ ВАКЦИНА С УЛУЧШЕННОЙ ЭФФЕКТИВНОСТЬЮ | 2004 |
|
RU2342400C2 |
| ВАКЦИНА MYCOBACTERIUM TUBERCULOSIS | 2009 |
|
RU2473365C1 |
| РЕКОМБИНАНТНАЯ BCG, СВЕРХЭКСПРЕССИРУЮЩАЯ PhoP-PhoR | 2017 |
|
RU2760580C2 |
| СОЧЕТАНИЕ РЕКОМБИНАНТНОЙ МИКРОБАКТЕРИИ И БИОЛОГИЧЕСКИ АКТИВНОГО СРЕДСТВА В КАЧЕСТВЕ ВАКЦИНЫ | 2005 |
|
RU2495677C2 |
| НОВЫЙ ОСЛАБЛЕННЫЙ ШТАММ ВИРУСА И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ ВАКЦИНЫ | 2019 |
|
RU2803068C2 |
| ПОЛИАНТИГЕННАЯ ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ И ВСПОМОГАТЕЛЬНОГО ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2019 |
|
RU2724896C1 |
| РЕКОМБИНАНТНЫЙ ВИРУС ГРИППА, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ПРОФИЛАКТИКИ COVID-19 И ГРИППА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2022 |
|
RU2802058C1 |
| Рекомбинантный штамм Mycobacterium bovis rBCG-1 на основе вакцинного штамма Mycobacterium bovis BCG strain Russia 368 | 2022 |
|
RU2807732C1 |
| Рекомбинантный штамм вируса гриппа A/PR8-NS124-TB10.4-2A-HspX и способ специфической профилактики туберкулеза легких с использованием вакцины мукозального применения на его основе | 2019 |
|
RU2726106C1 |
| РЕКОМБИНАНТНАЯ ПРОТИВОГРИППОЗНАЯ ВАКЦИНА С ШИРОКИМ СПЕКТРОМ ЗАЩИТЫ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2017 |
|
RU2757013C2 |


Группа изобретений относится к области биотехнологии. Предложена иммуногенная композиция, обеспечивающая защиту от HMPV подтипа А и/или ослабляющая патогенность, вызванную HMPV подтипа А, и содержащая один или более рекомбинантных ослабленных штаммов микобактерии, полученных из штамма Бациллы Кальметта-Герена (BCG), в количестве от 104 до 109 бактерий (КОЕ/доза) на штамм, и в которой каждый штамм экспрессирует Р-белок, который является Р-белком HMPV, в фармакологически соответствующем солевом буфере. Предложен способ защиты от HMPV инфекции или болезни, вызванной HMPV, включающий введение пациенту указанной иммуногенной композиции. Группа изобретений обеспечивает эффективную защиту против HPMV, не вызывая воспалительную гиперчувствительность. 2 н. и 6 з.п. ф-лы, 6 ил., 6 пр.
1. Иммуногенная композиция, которая обеспечивает защиту от инфекции метапневмовируса человека (HMPV) подтипа А и/или ослабляет патогенность, вызванную HMPV подтипа А, содержащая один или более рекомбинантных ослабленных штаммов микобактерии, которые являются штаммами, полученными из штамма Бациллы Кальметта-Герена (BCG), в количестве, которое находится в диапазоне от 104 до 109 бактерий (КОЕ/доза) на штамм, и в которой каждый штамм экспрессирует P-белок, который является Р-белком HMPV, в фармакологически соответствующем солевом буфере.
2. Иммуногенная композиция по п. 1, в которой последовательности нуклеиновых кислот, кодирующие Р-белок, вводятся в геном ослабленного штамма микобактерии или в экстрахромосомальную плазмиду в одном экземпляре или в большем количестве экземпляров так, чтобы вирусный белок экспрессировался из последовательностей нуклеиновых кислот.
3. Иммуногенная композиция по п. 1, отличающаяся тем, что белки получены путем экспрессии нуклеиновых кислот под контролем конститутивных или индуцируемых, эндогенных или экзогенных промоторов из микобактерий BCG.
4. Иммуногенная композиция по п. 1, содержащая два или более рекомбинантных ослабленных штамма микобактерии, в которой Р-белки HMPV экспрессируются из штаммов для генерации различного количества копий, конститутивно или индуцибельно выражены и/или расположены в разных клеточных локациях.
5. Иммуногенная композиция по п. 1, где композиция стабилизируется путем замораживания, сублимационной сушки или с помощью буферизованного солевого раствора для сохранения до использования.
6. Иммуногенная композиция по п. 1, в которой белок экспрессируется в виде растворимого цитоплазматического белка.
7. Способ защиты от HMPV инфекции или болезни, вызванной HMPV, включающий введение пациенту иммуногенной композиции по п. 1.
8. Способ по п. 7, в котором указанный препарат вводят подкожно или чрескожно.
| US 20040005545 A1, 08.01.2004 | |||
| WO 2005027825 A2, 31.03.2005 | |||
| US 20110200634 A1, 18.08.2011 | |||
| СПОСОБ ОБНАРУЖЕНИЯ РЕСПИРАТОРНЫХ ВИРУСНЫХ АГЕНТОВ В ОБРАЗЦЕ | 2009 |
|
RU2478718C2 |
Авторы
Даты
2018-09-04—Публикация
2014-09-30—Подача