Изобретение относится к области медицины, в частности к клинической микробиологии, и может быть использовано для преодоления устойчивости к карбапенемам у грамотрицательных бактерий вида Acinetobacter baumannii, продуцирующихметалло-β-лактамазу (МβЛ).
В настоящее время у пациентов, находящихся на стационарном лечении, увеличивается доля грамотрицательных аэробных бактерий как возбудителей инфекций [1]. Это Pseudomonas aeruginosa, Acinetobacter spp., Klebsiella spp., Stenotrophomonas maltophilia и др. Эти микроорганизмы, как правило, обладают низкой чувствительностью к различным классам антибиотиков, а также способностью приобретать резистентность в процессе лечения, что представляет существенные проблемы при проведении антибактериальной терапии, а именно, резко ограничивает арсенал применяемых для лечения больных антибактериальных препаратов, в том числе карбапенемов. Основным механизмом устойчивости к карбапенемам у грамотрицательных микроорганизмов является продукция металло-β-лактамаз.
Известна композиция и способы лечения, включающие цефтаролин [2], представляющий собой новый парентеральный цефалоспорин с широким спектром активности против клинически важных внебольничных и внутрибольничных грамотрицательных и грамположительных микроорганизмов. Однако, полученный авторами синергидный эффект применения композиции цефтаролина и антимикробных препаратов не описан в отношении резистентных грамотрицательных микроорганизмов, продуцирующих МβЛ.
Известна композиция [3], содержащая халконы в качестве усилителей антимикробных средств, действие которой направлено на предотвращение образования и разрушение сформированных микробных биопленок в полости рта. Синергидный эффект действия композиции халконов и антимикробных агентов авторы оценивали в средствах гигиены полости рта местного действия. Кроме того, авторы не оценивали данный эффект в отношении резистентных грамотрицательных микроорганизмов, продуцирующих МβЛ.
Известно изобретение [4] ингибиторов металло-β-лактамазы на основе малеиновой кислоты, которое демонстрирует эффект подавления МβЛ грамотрицательных бактерий и усиления действия бета-лактамных антибиотиков. В изобретении описаны способы синтеза различных производных малеиновой кислоты, показан их ингибирующий эффект в отношении МβЛ, а также восстановление действия бета-лактамных антибиотиков в отношении устойчивых к ним микроорганизмов. Однако такие производные малеиновой кислоты и их сочетания с антимикробными агентами не применяются в практической медицине в настоящее время.
Известна лекарственная композиция в отношении Acinetobacter baumannii, наиболее близкая к заявляемому изобретению по достижению технического результата и выбранная в качестве прототипа [5]. Изобретение представляет лекарственную композицию в отношении A. baumannii и ее применение. Лекарственная комбинация состоит из меропенема и сульбактама с весовым соотношением меропенема к сульбактаму 1:2-4. Дизайн исследования воспроизведен методом «шахматной доски». Синергидный антибактериальный эффект комбинированного применения меропенема и сульбактама в отношении карбапенем-чувствительных и лекарственно-устойчивых штаммов A. baumannii определяли методом микроразведений в бульоне. Как показано в результатах исследования, вне зависимости от того, какие были протестированы штаммы, меропенем-лекарственно-устойчивые или меропенем-чувствительные, большинство из них показали синергидный или частично синергидный эффект к комбинированному применению меропенема и сульбактама, и количество штаммов, продемонстрировавших синергидный эффект, насчитывало 25%.
Недостатком такой композиции является использование авторами сульбактама как ингибитора бета-лактамаз только у А. baumannii, так как по данным литературы известно, что сульбактам является ингибитором сериновых бета-лактамаз, но не ингибирует металло-β-лактамазы. При этом авторы изобретения-прототипа тестировали штаммы A. baumannii, не продуцирующие металло-β-лактамазы.
Заявляемое изобретение свободно от указанного недостатка.
Указанный технический результат достигается тем, что клодроновая или этидроновая кислоты из группы бисфосфонатов ингибируют стандартный реактив - металло-β-лактамазу P. aeruginosa рекомбинантную, экспрессированную в Escherichia coli. Достигнутый результат позволяет выявить антимикробный эффект комбинации клодроновой / этидроновой кислот с карбапенемами (имипенемом/меропенемом) в отношении референс-штамма A.baumannii АТСС ВАА 747, резистентного к карбапенемам в присутствии стандартного реактива МβЛ, инактивирующего эти антибиотики. Предложенное техническое решение позволяет моделировать получение штаммов грамотрицательных микроорганизмов с различным уровнем резистентности к карбапенемам и оценить эффективность ингибирования МβЛ.
Далее для достижения технического результата оценивают эффективность антимикробной комбинации карбапенемов (имипенема или меропенема) в сочетании с клодроновой или этидроновой кислотами методом «шахматной доски» [6]. В исследованиях используют микроразведения в бульоне в полистироловых 96-луночных планшетах.
В исследовании используют антибиотики имипенем и меропенем, разведенные стандартным титрованием в бульоне Мюллера-Хинтона [7] от 512 мкг/мл до 2 мкг/мл. Для данного исследования исходный концентрат клодроновой кислоты для приготовления раствора для внутривенного введения с содержанием 60 мг/мл разводят в среде Мюллера-Хинтона методом последовательных двукратных разведений. Этидроновую кислоту из исходного 20% концентрата разводят до 2% раствора в стерильной дистиллированной воде, и далее готовят двукратные разведения в среде Мюллера-Хинтона. В ячейки, содержащие по 95 мкл разведения соответствующего антибиотика, вносят по 95 мкл разведения клодроновой или этидроновой кислоты. Таким образом, объем смеси составляет 190 мкл.
Для получения инокулюма тест-штамма A.baumannii АТСС ВАА-747, готовят исходную суспензию суточной культуры микроба по стандарту 0,5 McFarland, далее суспензию разводят в 31 раз в бульоне Мюллер-Хинтон, при этом полученная взвесь содержит 5×106 КОЕ/мл. Далее во все ячейки вносят по 10 мкл микробной взвеси. Таким образом, в каждой ячейке конечная микробная нагрузка тест-штамма составляет 5×104 КОЕ в 200 мкл. Всегда присутствует контроль тест-культуры и контроль среды.
Значение минимальной подавляющей концентрации (МПК) тестируемого препарата оценивают в первой ячейке, содержимое которой прозрачное, где отсутствует видимый рост тест-штамма.
В табл. 1 представлены результаты инактивации антибиотика в присутствии стандартного реактива МβЛ. Показано, что фермент в ячейках 1-4 полностью инактивирует антибиотик в количестве от 1 мкг/мл до 512 мкг/мл, при этом в ячейках наблюдается рост тест-культуры A.baumannii АТСС ВАА-747. Начиная с 5-й ячейки, интенсивность инактивации фермента снижается, и в 8-й ячейке отмечается отсутствие роста тест-культуры на уровне референтного значения чувствительности к меропенему (МПК) - 2 мкг/мл (EUCAST 2015 г. [8]).

Примечание: «Р» - рост чувствительной к меропенему тест-культуры А. baumanniiATCC ВАА-747; «-» - отсутствие роста
В таб. 2 представлены результаты ингибирования МβЛ клодроновой кислотой в комбинации с имипенемом. В ячейках без клодроновой кислоты отмечается рост тест-культуры A.baumannii АТСС ВАА-747 за счет инактивации антибиотика МβЛ. Эффект ингибитора отмечен со 2-й ячейки, где он содержится в количестве 469 мкг. Отмечен эффект инактивации МβЛ и отсутствие роста тест-культуры в ячейке 5 с количеством антибиотика 4 мкг/мл и количеством клодроновой кислоты 3750 мкг/мл. Исходя из данных, представленных в ячейке 5 таблицы 2, предложена антимикробная комбинация в отношении A. baumannii, которая содержит имипенем и ингибитор МβЛ клодроновую кислоту в соотношении 4:3750 (1:938).

Примечание: «Р» - рост чувствительной к имипенему тест-культуры A.baumannii АТСС ВАА-747 в присутствии субстрата МβЛ;
«-» - отсутствие роста.
В таб. 3 представлены результаты ингибирования МβЛ этидроновой кислотой в комбинации с имипенемом. В ячейках без этидроновой кислоты отмечается рост тест-культуры A.baumannii АТСС ВАА-747 за счет инактивации антибиотика МβЛ. Эффект ингибитора отмечен со 2-й ячейки, где он содержится в количестве 1563 мкг. Отмечен эффект инактивации МβЛ и отсутствие роста тест-культуры в ячейке 8 с количеством антибиотика 2 мкг/мл и количеством этидроновой кислоты 100000 мкг/мл. Исходя из данных, представленных в ячейке 8 таблицы 3, предложена антимикробная комбинация в отношении A.baumannii, которая содержит имипенем и ингибитор МβЛ этидроновую кислоту в соотношении 2:100000 (1:50000).
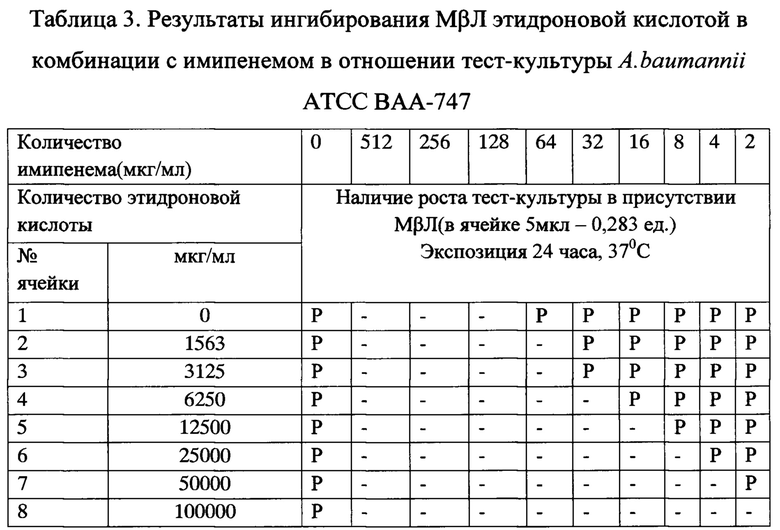
Примечание: «Р» - рост чувствительной к имипенему тест-культуры A.baumannii АТСС ВАА-747 в присутствии субстрата МβЛ;
«-» - отсутствие роста.
В таб. 4 представлены результаты ингибирования МβЛ этидроновой кислотой в комбинации с меропенемом. В ячейках без этидроновой кислоты отмечается рост тест-культуры A.baumannii АТСС ВАА-747 за счет инактивации антибиотика МβЛ. Эффект ингибитора отмечен со 2-й ячейки, где он содержится в количестве 1563 мкг. Отмечен эффект инактивации МβЛ и отсутствие роста тест-культуры в ячейке 8 с количеством антибиотика 2 мкг/мл и количеством этидроновой кислоты 100000 мкг/мл. Исходя из данных, представленных в ячейке 8 таблицы 4, предложена антимикробная комбинация в отношении A.baumannii, которая содержит меропенем и ингибитор МβЛ этидроновую кислоту в соотношении 2:100000 (1:50000).

Примечание: «Р» - рост чувствительной к меропенему тест-культуры A.baumannii АТСС ВАА-747 в присутствии субстрата МβЛ;
«-» - отсутствие роста.
В таб. 5 представлены результаты ингибирования МβЛ клодроновой кислотой в комбинации с меропенемом. В ячейках без клодроновой кислоты отмечается рост тест-культуры A.baumannii АТСС ВАА-747 за счет инактивации антибиотика МβЛ. Эффект ингибитора отмечен со 2-й ячейки, где он содержится в количестве 469 мкг. Отмечен эффект инактивации МβЛ и отсутствие роста тест-культуры в ячейке 5 с количеством антибиотика 2 мкг/мл и количеством клодроновой кислоты 3750 мкг/мл. Исходя из данных, представленных в ячейке 5 таблицы 5, предложена антимикробная комбинация в отношении A.baumannii, которая содержит меропенем и ингибитор МβЛ клодроновую кислоту в соотношении 2:3750 (1:1875).

Примечание: «Р» - рост чувствительной к меропенему тест-культуры A.baumannii АТСС ВАА-747 в присутствии субстрата МβЛ;
«-» - отсутствие роста.
Дозы бисфосфонатов, представленные в соотношениях с карбапенемами, составляют от 3% до 13% суточной дозы клодроновой кислоты и от 8% до 17% суточной дозы этидроновой кислоты.
Технико-экономическая эффективность заявленной антимикробной комбинации состоит в усилении действия антибиотика до уровня референтного значения чувствительности грамотрицательных микроорганизмов, продуцирующих МβЛ, вызывающих инфекционно-воспалительные заболевания у человека, что может улучшить терапевтический эффект проводимой антимикробной химиотерапии карбапенемами.
Использованные источники информации
1. Шевченко О.В., Эйдельштейн М.В., Степанова М.Н. Металло-β-лактамазы: значение и методы выявления у грамотрицательных неферментирующих бактерий. Клин. микробиол. антимикроб. химиотер. 2007; 9(3):211-19.
2. Композиции и способы лечения, включающие цефтаролин. Патент RU 2524665 С2.
3. Халконы в качестве усилителей антимикробных средств. Патент RU 2521252 С2.
4. Ингибиторы металло-β-лактамазы. Патент RU 2462450 С2.
5. Anti-Acinetobacterbaumannii drug combination and application thereof. Патент CN102475703.
6. Eliopoulos G.M., and R.C. Moellering. 1991. Antimicrobial combinations, p. 432-492. In V. Lorian (ed.), Antibiotics in laboratory medicine. The Williams & Wilkins Co., Baltimore, MD.
7. Определение чувствительности микроорганизмов к антимикробным препаратам (Методические указания МУК 4.2.1890-04).
8. EUCAST 2015 г. www.eucast.com
Изобретение относится к области медицины, а именно к клинической микробиологии, и предназначено для преодоления устойчивости грамотрицательных микроорганизмов вида Acinetobacter baumannii, продуцирующих металло-β-лактамазу (МβЛ), к карбапенемам. Антимикробная комбинация сочетанного применения карбапенемов и бисфосфонатов в отношении устойчивых к карбапенемам грамотрицательных бактерий вида Acinetobacter baumannii, продуцирующих МβЛ, которая приводит к инактивации МβЛ при следующем весовом соотношении компонентов:
1. Имипенем и клодроновая кислота 1:938 или
2. Меропенем и клодроновая кислота 1:1875 или
3. Имипенем и этидроновая кислота 1:50000 или
4. Меропенем и этидроновая кислота 1:50000.
Использование изобретения позволяет моделировать получение штаммов грамотрицательных микроорганизмов с различным уровнем резистентности к карбапенемам и оценивать эффективность ингибирования металло-β-лактамаз. 5 табл.
Антимикробная комбинация сочетанного применения карбапенемов и бисфосфонатов в отношении устойчивых к карбапенемам грамотрицательных бактерий вида Acinetobacter baumannii, продуцирующих металло-β-лактамазу (МβЛ), которая приводит к инактивации МβЛ при следующем весовом соотношении компонентов:
1. Имипенем и клодроновая кислота 1:938 или
2. Меропенем и клодроновая кислота 1:1875 или
3. Имипенем и этидроновая кислота 1:50000 или
4. Меропенем и этидроновая кислота 1:50000.
| ИНГИБИТОРЫ МЕТАЛЛО-β-ЛАКТАМАЗЫ | 2006 |
|
RU2462450C2 |
| КОМБИНИРОВАННЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2008 |
|
RU2488394C2 |
| ХАЛКОНЫ В КАЧЕСТВЕ УСИЛИТЕЛЕЙ АНТИМИКРОБНЫХ СРЕДСТВ | 2009 |
|
RU2521252C2 |
| WO 9847895 A1, 29.10.1998 | |||
| WALSH TR et al | |||
| Metallo-beta-lactamases: the quiet before the storm? Clin | |||
| Microbiol | |||
| Rev., 2005, 18(2), p.306-25. | |||
Авторы
Даты
2018-09-11—Публикация
2016-12-01—Подача