Настоящая заявка зависит от и претендует на приоритет предварительной заявки США №61/821,953, поданной 10 мая 2013 года, полное содержание которой включено в настоящую заявку посредством отсылки.
Изобретение по данному описанию может быть осуществлено, применено и лицензировано при поддержке или для правительства Соединенных Штатов.
Область техники
Изобретение, в общем смысле, относится к диагностике заболевания, а в частности - к способам обнаружения присутствия или отсутствия вируса гепатита С (HCV, ВГС) в биологическом образце или для диагностики, лечения или предупреждения HCV у пациента.
Уровень техники
Вирус гепатита С (HCV, ВГС) является основным возбудителем передающегося с кровью и спорадического гепатита "ни-А, ни-В". Связь хронических HCV инфекций с циррозом печени и печеночно-клеточной (гепатоцеллюлярной) карциномой делает HCV серьезной проблемой для здоровья во всем мире.
Для диагностики инфекции применяют преимущественно два основных теста на HCV: 1) ПЦР (PCR)- анализы; и 2) серологический метод обнаружения антител. Серологическое тестирование на антитела (Ab) к HCV представляет собой стандартный метод обнаружения HCV инфекции у человека. Однако первые серологические тесты имели значительные недостатки, а именно, слабую чувствительность, что давало неприемлемо завышенные ложноотрицательные результаты. Хотя чувствительность и специфичность иммуноанализов второго и третьего поколения с применением ферментных меток была значительно повышена, наличие "периода серонегативного окна" от инициирования HCV инфекции до наступления сероконверсии делает возможными ложноотрицательные результаты. Этот период варьируется от 2 месяцев у иммунокомпетентных субъектов до 6-12 месяцев у пациентов с иммунодефицитными состояниями.
Геном вируса HCV представлен однонитевой положительно-смысловой РНК с длиной цепи примерно 9,400 нуклеотидов. Следовательно, HCV инфекции можно также детектировать, применяя методы на основе нуклеиновых кислот с использованием полимеразной цепной реакции (ПЦР, PCR). Помимо скрининга на основе PCR (ПЦР) была предложена комбинация PCR-скрининга с серологическими тестами. Такой комбинированный метод снижает риск передачи HCV от инфицированных доноров во время "периода серонегативного окна" вследствие того, что метод на основе PCR позволяет осуществить детекцию до наступления сероконверсии. К сожалению, применение молекулярно-генетических тестов является значительной проблемой для здравоохранения и клинических лабораторий, связанной с необходимостью в специальном оборудовании и чувствительностью к перекрестному заражению.
В связи с этим существует потребность в композициях и способах, которые можно применять в качестве средства при скрининге с целью идентификации и проявления HCV инфекции у субъекта.
Сущность изобретения
Обнаружение HCV в биологическом образце часто ставит в тупик вследствие заражения источника образца. Например, требуется несколько недель, чтобы у HCV-инфицированного субъекта наступила сероконверсия в такой степени, когда в образце можно будет детектировать антитела к HCV. Это оставляет окно для возможного переноса инфекции от инфицированного субъекта, который не знает о своей инфицированности, вследствие неспособности имеющихся анализов обнаружить присутствие вируса. Хотя PCR анализы позволяют детектировать вирусный антиген до наступления сероконверсии, многие медицинские центры не имеют средств для проведения таких анализов. Кроме того, PCR анализы восприимчивы к перекрестному заражению вследствие их высокой чувствительности. Поэтому целью изобретения является предоставление композиции, которую можно эффективно применять в анализе для обнаружения (детекции) присутствия HCV как до, так и после сероконверсии, и не на основе методов PCR.
В изобретении предусматривается агент для обнаружения (детектирующий агент) HCV, который детектирует антитело, специфическое к ядерному (core, коровому, сердцевинному) белку вируса гепатита С (HCV) в образце, содержащий 5 или более последовательных (соседних) аминокислот, включающих остатки или расположенных между остатками 14-31, 50-91, или и те и другие, последовательности SEQ ID NO: 1, причем в этом детектирующем агенте исключены остатки 41-50 и 100-120 последовательности SEQ ID NO: 1. Согласно некоторым вариантам детектирующий агент содержит последовательность SEQ ID NO: 2. Необязательно, детектирующий агент содержит последовательность SEQ ID NO: 3. Согласно некоторым вариантам аминокислотная последовательность содержит последовательности SEQ ID NO: 2 и SEQ ID NO: 3, необязательно связанные между собой непосредственно или разделенные линкером Необязательно, линкер включает последовательность SEQ ID NO: 4.
В настоящем изобретении предусматривается также способ обнаружения (детекции) присутствия или отсутствия HCV в биологическом образце, применимый как до, так и после сероконверсии. На самом деле этот способ можно применять вне зависимости от того, когда субъект был инфицирован HCV или от его способности вырабатывать (продуцировать) антитела к HCV. Способ, необязательно, включает осуществление контакта биологического образца с детектирующим агентом, таким как любой из детектирующих агентов, описанных или заявляемых в данной заявке; и обнаружение присутствия или отсутствия в биологическом образце антитела к HCV-ядерному белку, которое специфически связывается с указанным детектирующим агентом, причем обнаружение антитела указывает на присутствие HCV в указанном образце. Необязательно, обнаружение антитела применяется для обнаружения присутствия или отсутствия HCV инфекции у субъекта. Согласно некоторым вариантам способ включает также осуществление контакта образца с антителом к HCV-ядерному белку, причем антитело не связывается с детектирующим агентом с аффинностью, достаточной для того, чтобы полученный результат анализа был ложноотрицательным. Антитело к HCV-ядерному белку, необязательно, является моноклональным или поликлональным. Необязательно, антитело к HCV-ядерному белку и детектирующий агент контактируют с образцом одновременно. Биологический образец, необязательно, представляет собой образец крови, плазмы или сыворотки крови. Биологический образец, необязательно, представляет собой клетку или клеточный экстракт.
В настоящем изобретении предусматриваются также наборы, пригодные для применения в способах обнаружения присутствия или отсутствия HCV-ядерного белка в биологическом образце. В набор, необязательно, входит детектирующий агент, включающий пептид, содержащий 5 или более последовательных (соседних) аминокислот, включающих остатки или расположенных между остатками 14-31, 50-91, или и те и другие, последовательности SEQ ID NO: 1, причем в этом детектирующем агенте исключены остатки 41-50 и 100-120 последовательности SEQ ID NO: 1. Согласно некоторым вариантам детектирующий агент содержит последовательность SEQ ID NO: 2. Необязательно, детектирующий агент содержит последовательность SEQ ID NO: 3. Согласно некоторым вариантам аминокислотная последовательность содержит последовательности SEQ ID NO: 2 и SEQ ID NO: 3, необязательно непосредственно связанные между собой или разделенные линкером Необязательно, линкер включает последовательность SEQ ID NO: 4. Набор, необязательно, включает фармацевтически приемлемый носитель, необязательно, воду или буферный водный раствор.
Композиции и способы по изобретению удовлетворяют назревшую потребность в быстрой, надежной, простой и недорогой системе для обнаружения HCV инфекции у субъекта, независимо от статуса сероконверсии субъекта.
Подробное описание
Нижеприведенное описание конкретного(-ых) варианта(-ов) изобретения по существу является лишь иллюстративным и никоим образом не претендует на ограничение объема изобретения, его приложения или применений, которые, естественно, могут меняться. Данное изобретение описано с использованием неограничивающих определений и терминов, включенных в настоящую заявку. Эти определения и термины предназначены не для ограничения объема или практического осуществления изобретения, но лишь с целью иллюстрации и наглядности. Хотя способ описан в виде последовательности отдельных стадий или использования конкретных элементов, следует принять во внимание, что описанные стадии или элементы могут быть взаимозаменяемыми, в результате чего описание изобретения включает несколько элементов или стадий, расположенных по-разному, и это легко поймет специалист в данной области техники.
В плазме HCV-инфицированных субъектов присутствуют вирусные частицы с физико-химическими, морфологическими и антигенными свойствами нуклеокапсидов безоболочечных вирусов гепатита С (HCV). Эти частицы имеют плавучую плотность 1.32-34 г/мл в CsCl, неоднородны по размеру и экспрессируют локализованные поверхностные эпитопы (антигенные детерминанты) HCV-ядерного (корового) белка. HCV ядерный антиген (белок) играет жизненно важную роль в капсидировании вируса. Он синтезируется только в гепатоцитах, реплицирующих РНК HCV и в силу этого может служить в качестве маркера активной HCV инфекции вместо PCR. Ядерный белок является весьма консервативным среди различных генотипов HCV. Обнаружить ядерный белок у HCV-инфицированных пациентов в период серонегативного окна довольно просто.
К сожалению, обнаружение ядерного белка самого по себе страдает недостатками вследствие сероконверсии. Когда в крови появляются антитела к ядерному белку, титр свободного ядерного белка снижается. Чтобы преодолеть это затруднение, авторы изобретения предусматривают композиции, которые делают возможным одновременное, в одной лунке, обнаружение молекул, которые присутствуют до сероконверсии, а также антител, которые присутствуют после сероконверсии. Одновременное обнаружение как ядерного антигена, так и антител, специфических к ядерному белку, представляет собой наилучший альтернативный вариант точной (чувствительной) диагностики гепатита С у доноров крови.
В изобретении предлагаются композиции и способы обнаружения HCV в биологическом образце. Композиция включает детектирующий агент, который представляет собой белковую молекулу. Детектирующий агент включает пептид, имеющий последовательность, представляющую одну или более областей ядерного белка HCV, в соответствии с определением в Genbank код доступа №АВ719482.1 и с SEQ ID NO. 1.
MSTNPKPQRK TKRNTNRRPQ DVKFPGGGQI VGGVYLLPRR GPRLGVRATR KTSERSQPRG RRQPIPKARQ PEGRAWAQPG YPWPLYGNEG LGWAGWLLSP RGSRPSWGPT DPRRRSRNLG (SEQ ID NO: 1).
Детектирующий агент включает пептид, представляющий по меньшей мере одну область ядерного белка HCV (ядерного белка вируса гепатита С). Область ядерного белка HCV охватывает 4 или более аминокислот, необязательно, 5 или более аминокислотных остатков, включающих остатки или находящихся между остатками 14-31, 50-91, или и те и другие, последовательности SEQ ID NO: 1. Необязательно, детектирующий агент включает 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69 или 70 аминокислот. Необязательно, детектирующий агент включает 70 или менее аминокислот, необязательно, 69 или менее аминокислот. Необязательно, детектирующий агент включает от 4 аминокислот до 41 аминокислоты, необязательно, от 4 до 18 аминокислот, необязательно, от 4 до 70 аминокислот. Необязательно, детектирующий агент включает от 5 до 17 аминокислот. Необязательно, детектирующий агент включает от 5 аминокислот до 41 аминокислоты. Приведенные выше значения длины аминокислотных последовательностей, необязательно, даются без учета метки (тега), линкера или другой аминокислоты или последовательности аминокислот, которые существенно не меняют способность детектирующего агента действовать нужным образом.
Следует принимать во внимание, что аминокислотная последовательность детектирующего агента во всех возможных вариантах изобретения необязательно включает одну(-о) или более аминокислотных замен, делеций, добавлений или модификаций последовательности, включающих остатки или находящихся между остатками 14-31, 50-91, или и те и другие, последовательности SEQ ID NO: 1, при условии, что такая область сохраняет свою функцию эпитопа, распознаваемого антителом к ядерному белку, образующимся к эпитопу, имеющему последовательность, идентичную последовательности SEQ ID NO: 1, остатки 14-31, 50-91, или ее релевантную часть. Для иллюстрации, детектирующий агент может включать одну(-о) или более аминокислотных замен, делеций, добавлений или модификаций последовательности остатков 14-31 или 50-91, которые не нарушают способность антитела, специфического к одной или более таких областей, или к ее участку, связываться с детектирующим агентом.
Согласно некоторым вариантам детектирующий агент включает область первого эпитопа. Область первого эпитопа, необязательно, включает 5 или более аминокислотных остатков 14-31 последовательности SEQ ID NO: 1. Область первого эпитопа, необязательно, включает последовательность NTNRRPQDVKFPGGGQIV (SEQ ID NO: 2). Детектирующий агент, необязательно, включает область второго эпитопа. Область второго эпитопа, необязательно, включает 5 или более аминокислот из остатков 50-91 последовательности SEQ ID NO: 1, необязательно, остатков 50-90 одной лишь последовательности SEQ ID NO: 1, или включая одну дополнительную аминокислоту на С-конце, необязательно M или L. Необязательно, область второго эпитопа включает последовательность RKTSERSQPRGRRQPIPKARQPEGRAWAQPGYPWPLYGNEGL (SEQ ID NO: 3). Необязательно, в области второго эпитопа исключен последний остаток L в последовательности SEQ ID NO: 3.
Детектирующий агент, необязательно, включает линкер. Линкер, необязательно, расположен между областью первого эпитопа и областью второго эпитопа. Линкер, необязательно, представляет собой пептид, содержащий 1 или более аминокислот, при этом линкер не совпадает с участком аминокислотной последовательности ядерного белка HCV. Необязательно, линкер включает от 2 до 50 аминокислот или любое число аминокислот в любом интервале между ними. Необязательно линкер включает 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, или более аминокислот. Необязательно, линкер включает последовательность SGGGGSGGGS (SEQ ID NO: 4).
Детектирующий агент, необязательно, не включает один или более последовательных (соседних) остатков аминокислот 1-13, 32-49, 41-49, 41-50, 91-120 или 100-120 последовательности SEQ ID NO: 1 или любую их комбинацию.
Детектирующий агент включает пептид или представляет собой исключительно пептид. Предполагается, что термины "пептид", "полипептид" и "белок" в данном контексте обозначают природное или синтетическое соединение, содержащее 4 или более аминокислот. Аминокислоты, которые могут присутствовать в пептиде, включают стандартные (широко распространенные) аминокислоты: аланин, цистеин, аспарагиновую кислоту, глутаминовую кислоту, фенилаланин, глицин, гистидин, изолейцин, лизин, лейцин, метионин, аспарагин, пролин, глутамин, аргинин, серии, треонин, валин, триптофан и тирозин, а также малораспространенные натуральные аминокислоты, модифицированные аминокислоты или синтетические соединения, такие как альфа-аспарагин, 2-аминобутановую или 2-аминомасляную кислоту, 4-аминомасляную кислоту, 2-аминокаприновую кислоту (2-аминодекановую кислоту), 6- аминокапроновую кислоту, альфа-глутамин, 2-аминогептановую кислоту, 6-аминогексановую кислоту, альфа-аминоизомасляную кислоту (2-аминоаланин), 3-аминоизомасляную кислоту, бета-аланин, алло-гидроксилизин, алло-изолейцин, 4-амино- 7-метилгептановую кислоту, 4-амино-5-фенилгептановую кислоту, 2-аминопимелиновую кислоту, гамма-амино-бета-гидроксибензолпентановую кислоту, 2-аминосубериновую кислоту, 2-карбоксиазетидин, бета-аланин, бета-аспарагиновую кислоту, бифенилаланин, 3,6-диаминогексановую кислоту, бутановую (масляную) кислоту, циклобутилаланин, циклогексилаланин, циклогексилглицин, N5-аминокарбонилорнитин, циклопентилаланин, циклопропилаланин, 3-сульфоаланин, 2,4-диаминобутановую кислоту, диаминопропионовой кислоту, 2,4-диаминомасляную кислоту, дифенилаланин, Ν,Ν-диметилглицин, диаминопимелиновую кислоту, 2,3-диаминопропановую кислоту, S-этилцистеин, N-этиласпарагин, N-этилглицин, 4-азафенилаланин, 4-фторфенилаланин, гамма-глутаминовую кислоту, гамма- карбоксиглутаминовую кислоту, гликолевую (оксиуксусную) кислоту, пироглутаминовую кислоту, гомоаргинин, гомоцистеиновую кислоту, гомоцистеин, гомогистидин, 2-гидроксиизовалериановую кислоту, гомофенилаланин, гомолейцин, гомопролин, гомосерин, 2-гидроксипентановую кислоту, 5-гидроксилизин, 4-гидроксипролин, 2-карбоксиоктагидроиндол, 3-карбоксиизохинолин, изовалин, 2-гидроксипропановую кислоту (молочную кислоту), меркаптоуксусную кислоту, меркаптобутановую кислоту, саркозин, 4-метил-3-гидроксипролин, меркаптопропановую кислоту, норлейцин, нипекотиновую кислоту, нортирозин, норвалин, омега-аминокислоту, орнитин, пеницилламин (3-меркаптовалин), 2-фенилглицин, 2-карбоксипиперидин, саркозин (N-метилглицин), 2-амино-3-(4-сульфенил)пропионовую кислоту, 1-амино-1-карбоксициклопентан, 3-тиенилаланин, эпсилон-N-триметиллизин, 3-тиазолилаланин, тиазолидин 4-карбоновую кислоту, альфа-амино -2,4-диоксопиримидинпропановую кислоту и 2-нафтилаланин. Таким образом, термин "пептид" в данном контексте может включать пептиды, содержащие от 5 и до примерно 200 аминокислот или любое число (аминокислот) или в любом интервале между ними.
В последовательности пептида можно сделать модификации и изменения по сравнению с последовательностью дикого типа SEQ ID NO: 1 или его области эпитопа и все еще получать молекулу, способную специфически связываться антителом к ядерному белку. Например, некоторые аминокислоты могут заменять другие аминокислоты в последовательности без заметной потери активности, где активность означает способность специфически связываться антителом к ядерному белку. Поскольку именно это представляет собой активность взаимодействия, а природа пептида определяет эту активность пептида, то в последовательности пептида можно делать некоторые (определенные) аминокислотные замены и тем не менее получать полипептид с подобными свойствами.
Осуществляя такие изменения, можно принимать во внимание индекс гидропатичности аминокислот. Вообще важность индекса гидропатичности аминокислот для придания полипептиду активности установлена в уровне техники. Известно, что некоторые аминокислоты могут заменять другие аминокислоты, имеющие аналогичный индекс или показатель гидропатичности, и все еще получать в результате полипептид с аналогичной биологической активностью. Каждой аминокислоте был присвоен индекс гидропатичности, исходя из его характеристик гидрофобности и заряда. Далее приводятся эти индексы: изолейцин (+4.5); валин (+4.2); лейцин (+3.8); фенилаланин (+2.8); цистеин/цистеин (+2.5); метионин (+1.9); аланин (+1.8); глицин (-0.4); треонин (-0.7); серии (-0.8); триптофан (-0.9); тирозин (-1.3); пролин (-1.6); гистидин (-3.2); глутамат (-3.5); глутамин (-3.5); аспартат (-3.5); аспарагин (-3.5); лизин (-3.9); и аргинин (-4.5).
Полагают, что относительная гидропатическая характеристика аминокислоты определяет вторичную структуру образующегося в результате полипептида, которая, в свою очередь, определяет взаимодействие полипептида с другими молекулами, такими как ферменты, субстраты, рецепторы, антитела, антигены и т.п. Из уровня техники известно, что аминокислоту можно заменить на другую аминокислоту, имеющую близкий (аналогичный) индекс гидропатичности, и тем не менее получить функционально эквивалентный полипептид. При таких изменениях возможно замена аминокислот, индексы гидропатичности которых находятся в пределах ± 2, в пределах0 ± 1 и в пределах ± 0.5.
Замену подобных аминокислот можно также осуществлять с учетом гидрофильное™, в частности, если предполагается получить при этом полипептид или пептид с эквивалентной активностью. Аминокислотные остатки имеют (им заданы) следующие величины гидрофильности: аргинин (+3.0); лизин (+3.0); аспартат (+3.0±1); глутамат (+3.0±1); серии (+0.3); аспарагин (+0.2); глутамин (+0.2); глицин (0); пролин (-0.5±1); треонин (-0.4); аланин (-0.5); гистидин (-0.5); цистеин (-1.0); метионин (-1.3); валин (-1.5); лейцин (-1.8); изолейцин (-1.8); тирозин (-2.3); фенилаланин (-2.5); триптофан (-3.4). Понятно, что аминокислоту можно ввести в качестве замены вместо другой аминокислоты, имеющей аналогичную (близкую) величину гидрофильности, и по-прежнему получить биологически эквивалентный и, в частности, имеющий эквивалентную или более высокую активность, пептид. В таких изменениях предпочтительными для замены являются аминокислоты, величина гидрофильности которых находится в пределах ± 2, особенно предпочтительны аминокислоты с величиной гидрофильности в пределах ± 1, и еще более предпочтительны аминокислоты с величиной гидрофильности в пределах ± 0.5.
Как подчеркивается выше, обычно аминокислотные замены осуществляют на основании сходства заместителей в боковой цепи аминокислот, например, их гидрофобности, гидрофильности, заряда, размера и т.п.Такие заместители обычно считаются консервативными заместителями. Типичные консервативные заместители, которые соответствуют различным вышеприведенным характеристикам, хорошо известны специалистам в данной области техники и включают (исходный остаток: типичная замена): (Ala: Gly, Ser), (Arg: Lys), (Asn: Gln, His), (Asp: Glu, Cys, Ser), (Gln: Asn), (Glu: Asp), (Gly: Ala), (His: Asn, Gln), (Ile: Leu, Val), (Leu: Ile, Val), (Lys: Arg), (Met: Leu, Tyr), (Ser: Thr), (Thr: Ser), (Tip: Tyr), (Tyr: Trp, Phe) и (Val: Ile, Leu). Поэтому в вариантах настоящего изобретения рассматриваются функциональные или биологические эквиваленты описанного выше пептида. В частности, варианты полипептидов могут включать варианты, последовательность которых примерно на 50%, 60%, 70%, 80%, 90% и 95% идентична последовательности рассматриваемого полипептида.
Пептид получают любым из различных методов, известных из уровня техники, включающих, например, выделение из клетки или из организма, химический синтез, экспрессию нуклеиновой кислоты и частичный гидролиз белков. Химические методы пептидного синтеза известны в уровне техники и включают, например, твердофазный пептидный синтез и пептидный синтез в растворе (жидкофазный пептидный синтез). Пептид, включенный в состав детектирующего агента, может представлять собой натуральный или ненатуральный пептид. Термин "натуральный (природный)" относится к эндогенному пептиду клетки, ткани или организма, и включает аллельные варианты. Ненатуральный (не природный) пептид представляет собой синтетический пептид или пептид, полученный вне организма, с которым он ассоциирован в природе, или модифицированный пептид, который отсутствует в немодифицированных клетке, ткани или организме.
Например, пептид является рекомбинантным пептидом. Пептид по изобретению может экспрессироваться совместно с ассоциированными метками (тегами), модификациями, другими белками, например, такими, которые входят в состав химерного пептида, или другими модификациями или комбинациями, известными в уровне техники. Типичные метки (теги) включают 6х His, FLAG, биотин, убиквитин, SUMO или другую метку, известную в уровне техники. В качестве иллюстрации, метка (тег) может отщепляться, например, путем связывания с пептидом с помощью последовательности расщепляющего фермента, который затем отщепляется с помощью фермента, известного в уровне техники, включающего, например, но без ограничения, Фактор Ха, тромбин, белок SUMOstar, получаемый от компании Lifesensors, Inc., Malvern, РА, или трипсин. Также следует принимать во внимание, что можно осуществлять химическое расщепление с использованием подходящего отщепляемого линкера.
Экспрессию пептида осуществляют, например, при использовании транскрипции нуклеотидной последовательности, кодирующей пептид, и трансляции РНК, транскрибированной с нуклеотидной последовательности. Экспрессию пептида, необязательно, проводят на клеточной системе, например, в клетках Е. coli, клетках Hela или клетках яичника китайского хомячка. Также применимы бесклеточные системы экспрессии.
Детектирующий агент, необязательно, выделяют или очищают. Предполагается, что термины "очищенный" или "выделенный" в данном контексте относятся к композиции, которую отделяют от других компонентов, причем композиция является очищенной в той или иной степени по сравнению с ее состоянием в природе или с состоянием после экспрессии в клетке или синтетической системе. Следовательно, выражение "очищенный пептид" относится также к пептиду, не содержащему примесей из окружающей среды, в которой он может находиться в природе.
Выделенный пептид можно подвергать фракционированию для удаления различных других компонентов. Если применяется выражение "по существу" очищенный, "практически" очищенный, то это пояснение (определение) относится к композиции, в которой белок или пептид является основным компонентом, например, составляющим примерно 50% или более всех белков, содержащихся в композиции.
С учетом настоящего раскрытия и данных из уровня техники специалистам в данной области техники будут понятны методы количественного определения степени чистоты белка или пептида. Эти методы включают, например, определение специфической активности активной фракции или определение количества полипептидов во фракции с помощью анализа SDS/PAGE (электрофорез в полиакриламидном геле с додецилсульфатом натрия). Предпочтительным способом определения чистоты фракции является количественное определение (расчет) специфической активности фракции и сравнение ее со специфической активностью исходного экстракта и тем самым вычисление степени чистоты, выражаемой в настоящей заявке как "-кратная степень очистки". Фактические числа, используемые для количественного изображения активности, естественно, будут зависеть от конкретного метода анализа, выбранного для того, чтобы следить за очисткой, и от того, обладает экспрессируемый белок или пептид детектируемой активностью или не обладает.
Специалистам в данной области техники хорошо известны различные методы, применимые для очистки белков. Эти методы включают, например, преципитацию (осаждение) с использованием сульфата аммония, полиэтиленгликоля, антител и т.п. или тепловой денатурацией с последующим центрифугированием; хроматографию, например, ионообменную хроматографию, гель-проникающую хроматографию (гель-фильтрацию), обращенно-фазовую, гидроксилапатитную и аффинную хроматографию; изоэлектрическое фокусирование; электрофорез в геле; и комбинации этих и других методов. Как известно из уровня техники, полагают, что порядок осуществления различных стадий очистки может меняться или что некоторые стадии можно исключить, и тем не менее осуществить адекватный способ получения практически (по существу) очищенного белка или пептида.
Общего требования, чтобы детектирующий агент всегда предоставлялся в особо чистом состоянии, нет. На самом деле в некоторых вариантах изобретения предполагается применение менее чистых продуктов. Частичную очистку можно осуществлять, применяя меньше стадий очистки в сочетании (друг с другом), или применяя различные формы той же самой общей схемы очистки. Например, катионообменная колоночная хроматография, проводимая на системе для ВЭЖХ (HPLC), обычно дает более многократную степень очистки, чем тот же способ с применением хроматографической системы, работающей под низким давлением. Преимущество методов, в которых достигается более низкая степень относительной очистки, может заключаться в сквозном извлечении белкового продукта или в сохранении активности экспрессированного белка.
Известно, что миграция пептида в геле может меняться, иногда значительно, в разных условиях SDS/PAGE (Capaldi et al., Biochem. Biophys. Res. Comm., 76:425, 1977). Поэтому следует принимать во внимание, что в различных условиях проведения электрофореза средняя (кажущаяся) молекулярная масса очищенного или частично очищенного экспрессированного продукта может меняться.
Некоторые варианты изобретения включают выделение детектирующего агента. Способы выделения пептидов включают, например, колоночную хроматографию, аффинную хроматографию, электрофорез в геле, фильтрацию или другие способы, известные из уровня техники. Согласно некоторым вариантам пептид экспрессируется с меткой, пригодной для аффинной очистки. Метка представляет собой, необязательно, метку (хвост) 6х His. Белок по изобретению, меченный тегом 6х His, очищают, например, Ni-NTA колоночной хроматографией или с использованием антитела к метке 6х His на твердой подложке (носителе) (Geneway Biotech, San Diego, CA). Также пригодны для такого применения другие метки и системы очистки.
Следует понимать, что пептид, не обязательно, не является меченым. Согласно таким вариантам очистку, необязательно, проводят способами, известными в уровне техники, включающими, например, ионообменную хроматографию, аффинную хроматографию, преципитацию (осаждение) солью, например, такой как сульфат аммония, стрептомицина сульфат или протамина сульфат, обращенно-фазовую хроматографию, эксклюзионную (по размеру) хроматографию, например, такую как высокоэффективная гель-проникающая хроматография (гель-фильтрация), ВЭЖХ (HPLC), металл-аффинную хелатную хроматографию или другие способы, известные в уровне техники. Специалист в данной области техники может выбрать наиболее подходящие методы выделения и очистки в объеме настоящего изобретения.
Детектирующий агент может быть рекомбинантным. Экспрессию белка можно осуществлять при использовании транскрипции нуклеотидной последовательности, кодирующей детектирующий агент, трансляции с матрицы РНК, транскрибируемой с этой нуклеотидной последовательности, ее модификаций или фрагментов. Экспрессию белка, необязательно, осуществляют на клеточной системе, например, в клетках Е. coli, клетках Hela или клетках яичника китайского хомячка. Следует принимать во внимание, что также применимы бесклеточные системы экспрессии.
Необязательно, пептид получают методами химического синтеза. Методами химического синтеза получают белки протяженностью более 600 аминокислот, включая или не включая модификации, такие как модификации, являющиеся результатом гликозилирования или фосфорилирования. Способы химического синтеза белков и пептидов включают, например, твердофазный химический синтез белков. Типичные способы химического синтеза белков представлены в обзорах Miranda, LP, Peptide Science, 2000, 55:217-26 и Kochendoerfer GG, Curr Opin DrugDiscov Devel. 2001; 4(2):205-14.
Детектирующий агент, необязательно, можно охарактеризовать, применяя такие методы анализа, как например, но без ограничения, вестерн-блоттинг, биофизические методы определения молекулярной массы макромолекул, SDS- PAGE/окрашивание, HPLC и т.п., методы распознавания антител, анализы жизнеспособности клеток, анализы апоптоза и анализы, позволяющие сделать заключение об иммунной защите или иммунной патологии путем адоптивного переноса клеток, белков или антител.
Также предусматриваются выделенные олигонуклеотиды, кодирующие детектирующий агент. Эти олигонуклеотиды можно применять для получения пептидов, включенных в детектирующий агент. Вырожденный генетический код понятен специалисту в данной области, поэтому специалист в полной мере и сразу поймет, какая нуклеотидная последовательность позволит продуцировать последовательность заданного пептида. По сути олигонуклеотид включает любой полинуклеотид, который кодирует детектирующий агент.
Предполагается, что термин "нуклеотид" означает комбинацию основание- сахар-фосфатная группа, либо натуральную, либо синтетическую, линейные, кольцевые и последовательные повторы нуклеотидов и нуклеозидов, например, кДНК, геномную ДНК, мРНК и РНК, олигонуклеотиды, олигонуклеозиды и их производные. Это определение охватывает также модифицированные нуклеотиды, которые включают добавления к сахар-фосфатным группам, а также к основаниям.
Термин "олигонуклеотид" относится к нескольким нуклеотидам, связанным в виде одно- или двунитевой (одно- или двухцепочечной) молекулы, которая может быть натуральной или полученной синтетическими, ферментативными методами или методами клонирования. Термин "олигонуклеотид" относится к полинуклеотиду, содержащему менее 2000 нуклеотидов.
Термин "олигонуклеотид" в данном контексте относится к одно- или двухцепочечным молекулам, которые могут представлять собой ДНК, включающую нуклеотидные основания А, Т, С и G, или РНК, состоящую из оснований A, U (введенное вместо Т), С и G. Олигонуклеотид может представлять собой кодирующую цепь или ее комплемент. Олигонуклеотиды могут иметь последовательность, идентичную природной (натуральной) последовательности, или может включать альтернативные кодоны, которые кодируют ту же самую аминокислоту, что и аминокислота в природной последовательности. Кроме того, олигонуклеотиды могут включать кодоны, представляющие консервативные замены аминокислот, хорошо известные в уровне техники.
Олигонуклеотид, кодирующий детектирующий агент по настоящему изобретению, может представлять собой часть рекомбинантной нуклеотидной конструкции, включающей любую комбинацию сайтов рестрикции и/или функциональных элементов, хорошо известных в уровне техники, которые способствуют молекулярному клонированию и другим манипуляциям с рекомбинантной ДНК. Поэтому в настоящем изобретении также предусматривается конструкция на основе рекомбинантного олигонуклеотида, включающая нуклеиновую кислоту, кодирующую пептид и/или полипептид по настоящему изобретению.
В настоящем изобретении предусматривается также вектор, содержащий последовательность нуклеиновой кислоты, кодирующей пептидную последовательность. Типичные векторы включают плазмидные векторы, космидные векторы, катионные липиды в качестве векторов, не-липосомальные катионные векторы, катионный циклодекстрин, вирусы с РНК- или ДНК- генетическим материалом, полиэтиленимины, гистидилированный полилизин или другие векторные системы, известные в уровне технике. Вектор, необязательно, представляет собой плазмиду. Подходящий вектор, необязательно, проявляет специфическую экспрессию в определенных типах клеток, или имеет другие регуляторные последовательности или последовательности, выполненные с возможностью стимулировать или ингибировать экспрессию гена или белка. Например, вектор содержит селективный маркер, такой как ген устойчивости к антибиотикам.
В изобретении предусматривается олигонуклеотид. Олигонуклеотид, необязательно, кодирует пептид, включающий последовательность SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, комбинацию SEQ ID NO: 2, SEQ ID NO: 4 и SEQ ID NO: 3, расположенных в любом другом или в перечисленном порядке. Генетический код представляет собой вырожденный код, в котором специфические нуклеотидные последовательности кодируют конкретные аминокислоты. По существу специалисты в данной области техники могут определить нуклеотидную последовательность, которая будет кодировать пептиды по изобретению.
Нуклеотидная последовательность по изобретению, необязательно, является выделенной из клеточных материалов, с которыми она связана в природе. В данном контексте термин "выделенная нуклеиновая кислота" обозначает нуклеиновую кислоту, выделенную из других компонентов или практически (по существу) не содержащую по меньшей мере некоторые из других компонентов природного (встречающегося в природе) организма, например, структурные компоненты клетки, обычно ассоциированные с нуклеиновыми кислотами в клеточной среде, и/или другие нуклеиновые кислоты. Выделение нуклеиновых кислот, необязательно, осуществляют такими методами, как лизис клеток с последующей экстракцией фенолом плюс хлороформ, а затем осаждением нуклеиновых кислот этанолом. Нуклеиновые кислоты по настоящему изобретению можно выделять из клеток методами выделения нуклеиновых кислот, хорошо известными в уровне техники. Или же нуклеиновые кислоты по настоящему изобретению можно синтезировать в соответствии со стандартными протоколами, хорошо описанными в литературе по синтезу нуклеиновых кислот. Также рассматриваются модификации нуклеиновых кислот по изобретению, при условии, что сохраняется базовая структура и функция пептида или полипептида, кодируемого нуклеиновой кислотой.
В уровне техники известно множество методов синтеза и продуцирования нуклеотидных последовательностей, включающих, например, клонирование и экспрессию в клетках, таких как Е. coli, клетках насекомых, таких как клетки Sf9, клетках дрожжей и клетках млекопитающих, таких как клетки Hela, клетки яичников китайского хомячка, или в других клеточных системах, известных в уровне техники как клетки, поддающиеся трансфекции и экспрессирующие нуклеиновые кислоты и/или белки. Аналогично, методы выделения олигонуклеотидов известны в уровне техники. Например, плазмидную ДНК, амплифицированную в Е. coli, расщепляют соответствующими рестриктазами, такими как NdeI и XhoI, чтобы линеаризовать ДНК. Затем ДНК выделяют с помощью электрофореза в геле, используя набор S.N.A.P.™ UV-Free Gel Purification Kit (Invitrogen, Carlsbad, CA) в соответствии с инструкциями производителя.
Многие агенты пригодны для того, чтобы способствовать трансфекции клеток, включая, например, синтетические или натуральные трансфецирующие агенты, такие как липофектин (LIPOFECTIN), бакуловирус, "голая" плазмидная или другая ДНК, или другие системы, известные в уровне техники.
Нуклеотидные последовательности по изобретению можно выделять традиционными методами полимеразной цепной реакции или клонирования, описанными в классических учебниках. Например, нуклеотидные последовательности по настоящему изобретению можно получать с использованием ДНК или выделять из ДНК, используя ДНК праймеры и зонды и методы ПЦР. Или же, нуклеотидную последовательность по изобретению можно получать из банков генов, полученных из целой геномной ДНК Bacillus anthracis. Эти последовательности, их фрагменты, их модификации и полноразмерные последовательности можно конструировать рекомбинантными методами, применяя традиционные методы генной инженерии или химического синтеза, или ПЦР и т.п.
Также предусматривается клетка-хозяин, трансформируемая при использовании соответствующего вектора или пептидной последовательности по изобретению. Типичные клетки-хозяева включают клетки Е. coli или Sf9. Необязательно, трансфекцию клеток осуществляют с помощью электропорации.
Термины "полученные методами генной инженерии" ("генно-инженерные") и "рекомбинантные" клетки являются синонимами термина клетки-"хозяева" и, как предполагается, относятся к клеткам, в которые введен сегмент экзогенной ДНК или экзогенный ген, например, кДНК или гена. Следовательно, рекомбинантные клетки отличаются от натуральных (природных) клеток, которые не содержат сегмента экзогенной ДНК или экзогенного гена, введенного методами рекомбинантной ДНК. Клетка-хозяин, необязательно, представляет собой натуральную клетку, которая трансформирована с помощью сегмента экзогенной ДНК или экзогенного гена, или клетку, которая не является модифицированной. Рекомбинантные клетки представляют собой клетки, содержащие ген или гены, введенные человеком. Рекомбинантные клетки включают клетки, содержащие введенную кДНК или геномную ДНК, а также включающие гены, прилегающие к промотору, который в естественном состоянии не связан с конкретным введенным геном.
Для экспрессии рекомбинантного кодированного пептида согласно настоящему изобретению надо приготовить экспрессионный вектор, который содержит олигонуклеотид под контролем одного или более промоторов. Чтобы взять кодирующую последовательность "под контроль" промотора, обычно помещают 5' конец сайта инициации трансляции рамки считывания примерно между нуклеотидами 1 и 50 "даунстрим (downstream)" (т.е. 3') от выбранного промотора. Промотор "апстрим (5', upstream)" стимулирует транскрипцию встроенной ДНК и промотирует экспрессию кодированного рекомбинантного белка. В данном контексте именно это означает "рекомбинантную экспрессию".
Существует множество стандартных методов конструирования экспрессионных векторов, содержащих подходящие нуклеиновые кислоты и последовательности регуляции (контроля) транскрипции/трансляции, для осуществления экспрессии белка или пептида в системах экспрессии на основе различных клеток-хозяев. Типы клеток, пригодных для экспрессии, включают, но без ограничения, бактерии, такие как Е. coli и В. Subtilis, трансформированные с использованием экспрессионных векторов на основе рекомбинантной фаговой ДНК, плазмидной ДНК или космидной ДНК.
Некоторые примеры прокариотических хозяев включают Е. coli штамм RR1, Е. coli LE392, Ε. coli В, Ε. coli .chi. 1776 (ATCC No. 31537), а также Ε. coli W3110 (F-, лямбда-, прототрофный-, ATCC No. 273325); бациллы (палочковидные бактерии, палочки, такие как Bacillus subtilis; и другие энтеробактерии, например, такие как Salmonella typhimurium, Serratia marcescens и различные виды Pseudomonas.
Как правило, плазмидные векторы, содержащие репликой и контрольные (регуляторные) последовательности, происходящие из видов, совместимых с клеткой-хозяином, применяются совместно с их хозяевами. Вектор обычно несет сайт репликации, а также маркирующие последовательности (метки), которые способны обеспечить отбор (фенотипическую селекцию) трансформированных клеток по фенотипу. Например, Е. coli часто трансформируют с использованием pBR322, плазмиды, полученной из препарата Е. coli. Плазмида pBR322 содержит гены устойчивости к ампициллину и тетрациклину и тем самым предоставляет простой способ идентификации трансформированных клеток. Плазмида pBR322, или другая плазмида микроба или фага должна также содержать, или должна быть модифицирована таким образом, чтобы содержать, промоторы, которые могут использоваться микроорганизмом для экспрессии его собственных белков. Необязательно, олигонуклеотид включен в pETitN вектор для экспрессии в Е. coli.
Кроме того, фаговые векторы, содержащие репликон и регуляторные последовательности, совместимые с микроорганизмом-хозяином, можно применять в качестве трансформирующих векторов вместе с этими хозяевами. Например, фаг лямбда можно применять для получения рекомбинантного фагового вектора, который можно использовать для трансформации клеток-хозяев, например, Е. coli LE392.
Другие векторы включают векторы pIN и векторы pGEX, их можно применять при получении растворимых (гибридных) белков, слитых с глутатион S- трансферазой (GST), для последующей очистки и выделения или расщепления. Другие подходящие гибридные белки включают β-галактозидазу, убиквитин и т.п.
Промоторы, которые чаще всего применяются для создания рекомбинантных ДНК, включают β-лактамазную (пенициллазную), лактозную и триптофановую (trp) промоторные системы. Хотя эти системы применяются наиболее часто, открыты и применяются другие промоторы микроорганизмов, и подробности, касающиеся их нуклеотидных последовательностей, опубликованы, что позволяет специалистам в данной области техники лигировать их к плазмидным векторам.
Для экспрессии в Saccharomyces обычно применяется, например, плазмида YRp7. Эта плазмида содержит ген trp1, который предоставляет селективный маркер для мутантного штамма дрожжей, который не способен расти в триптофане, например, АТСС No. 44076 или РЕР4-1. В дальнейшем повреждение по trp1 как характерный признак генома клеток хозяев-дрожжей обеспечивает эффективную среду для обнаружения трансформации с помощью выращивания в отсутствие триптофана.
Подходящие промоторные последовательности в дрожжевых векторах включают промоторы для 3-фосфоглицерат киназы или других гликолитических ферментов, таких как енолаза, глицеральдегид-3-фосфат дегидрогеназа, гексокиназа, пируватдекарбоксилаза, фосфофруктокиназа, глюкозо-6-фосфат-изомераза, 3-фосфоглицерат мутаза, пируваткиназа, триозофосфатизомераза, фосфоглюкозо-изомераза и глюкокиназа. При конструировании подходящих экспрессионных плазмид стоп-кодоны (терминирующие кодоны), ассоциированные с этими генами, также лигируют к экспрессионному вектору 3' от последовательности, которую надо экспрессировать, чтобы обеспечить полиаденилирование мРНК и терминацию.
Другие подходящие промоторы, дополнительным преимуществом которых является транскрипция, контролируемая условиями роста, включают промоторный участок алкогольдегидрогеназы 2, изоцитохрома С, кислой фосфатазы, деструктивных ферментов, ассоциированных с азотистым обменом веществ, и глицеральдегид-3- фосфат дегидрогеназы, и ферментов, отвечающих за утилизацию мальтозы и галактозы.
Помимо микроорганизмов, в качестве хозяев можно также применять культуры клеток многоклеточных организмов. В принципе любая такая культура работает, вне зависимости от того, являются многоклеточные организмы позвоночными или беспозвоночными. Помимо клеток млекопитающих, эти клетки включают системы клеток насекомых, инфицированных рекомбинантными вирусными экспрессионными векторами (например, бакуловирусом); и системы растительных клеток, инфицированных рекомбинантными вирусными экспрессионными векторами (например, вирусом мозаики цветной капусты, CaMV; вирусом табачной мозаики, TMV) или трансформированных с использованием рекомбинантных плазмидных экспрессионных векторов (например, Ti плазмидой), содержащих одну или более кодирующих последовательностей.
В эффективной клеточной системе насекомых в качестве вектора для экспрессии чужеродных генов применяется вирус Autographica califomica nuclear polyhedrosis (AcNPV). Вирус выращивают на клетках Spodoptera frugiperda. Выделенные нуклеотидные кодирующие последовательности клонируют в несущественные области (например, полиэдронный (многогранный) ген) вируса и помещают под контроль промотора AcNPV (например, полиэдронного (многогранного) промотора). Успешное встраивание (инсерция) кодирующих последовательностей приводит к инактивации полиэдронного гена и получению неокклюдированного рекомбинантного вируса (т.е. вируса, лишенного белковой оболочки, кодируемой полиэдронным геном). Эти рекомбинантные вирусы затем используют для инфицирования клеток Spodoptera frugiperda, в которых экспрессируется встроенный ген (см., например, патент США №4,215,051).
Примерами применимых линий клеток хозяев-млекопитающих являются клетки VERO и HeLa, клетки яичников китайского хомячка (СНО), линии клеток W138, ВНК, COS-7, 293, HepG2, NIH3T3, RIN и MDCK. Кроме того, можно выбрать клетку-хозяина, которая модулирует экспрессию встроенных последовательностей, или модифицирует и процессирует генный продукт конкретным желательным способом. Такие модификации (например, гликозилирование) и процессирование (например, расщепление) белковых продуктов может иметь большое значение для функции кодированного белка.
Механизмы посттрансляционного процессирования и модификации белков являются характеристическими и специфическими для различных клеток-хозяев. Чтобы гарантировать корректные модификацию и процессирование экспрессированного чужеродного белка, можно выбрать подходящие клеточные линии или системы клетки-хозяина. Экспрессионные векторы для применения в клетках млекопитающих обычно включают ориджин (точку начала) репликации (при необходимости), промотор, расположенный перед экспрессируемым геном, наряду с любыми необходимыми сайтами связывания рибосом, сайты сплайсинга РНК, сайт полиаденилирования и последовательности терминации транскрипции (стоп-кодоны). Ориджин репликации может быть предусмотрен либо конструкцией вектора, включающей экзогенный ориджин, например, такой, который может быть получен из вируса SV40 или из другого вирусного источника (например, вируса полиомы, аденовируса, VSV, BPV), или может быть предусмотрен механизмом репликации хромосом клетки-хозяина. Если вектор интегрирован в хромосому клетки-хозяина, последнего часто бывает достаточно.
Промоторы могут быть получены из генома клеток млекопитающих (например, металлотионеиновый промотор) или из вирусов млекопитающих (например, поздний промотор аденовируса; промотор 7.5К вируса коровьей оспы). Кроме того, возможно и может быть желательно использовать промоторные или регуляторные последовательности, обычно ассоциированные с последовательностью нужного гена, при условии, что эти регуляторные последовательности совместимы с системами клетки-хозяина.
Могут применяться многие экспрессионные системы на основе вирусов, например, часто используются промоторы вирусов полиомы, аденовируса 2, цитомегаловируса и вируса обезьян 40 (SV40). Могут применяться ранний и поздний промоторы вируса SV40, потому что их обоих можно легко получать из вируса в качестве фрагмента, который также содержит ориджин репликации вируса SV40. Можно также использовать фрагменты SV40 большего или меньшего размера при условии, что они включают последовательность протяженностью примерно 250 п. о. от сайта HindIII в направлении к сайту BglI, локализованную в ориджине репликации вируса.
В тех случаях, когда в качестве экспрессионного вектора используют аденовирус, кодирующие последовательности можно лигировать к комплексу регуляции транскрипции/трансляции аденовируса, например, к позднему промотору и трехкомпонентной лидерной последовательности. Этот химерный ген можно затем вставить в геном аденовируса с помощью рекомбинации in vitro или in vivo. Инсерция (вставка) в несущественную область вирусного генома (например, область E1 или Е3) дает в результате рекомбинантный вирус, который является жизнеспособным и делает возможной экспрессию белков в инфицированных клетках-хозяевах.
Для эффективной трансляции заявляемых выделенных нуклеотидных кодирующих последовательностей могут также потребоваться специфические сигналы инициации. Эти сигналы включают инициирующий кодон ATG и прилегающие последовательности. Могут дополнительно потребоваться экзогенные сигналы регуляции трансляции, включая инициирующий кодон ATG. Рядовой специалист в данной области техники сможет легко определить эту потребность и обеспечить необходимые сигналы. Общеизвестно, что инициирующий кодон должен быть в рамке (или в фазе) считывания заданной кодирующей последовательности, чтобы гарантировать трансляцию всей вставки (целого инсерта). Эти экзогенные сигналы регуляции трансляции и инициирующие ко доны могут иметь различное происхождение, могут быть как натуральными, так и синтетическими. Эффективность экспрессии можно повысить путем включения соответствующих энхансеров транскрипции или терминаторов транскрипции.
При экспрессии в эукариотических клетках обычно требуется вводить в единицу транскрипции соответствующий сайт полиаденилирования, если он не содержался в исходном клонированном сегменте. Как правило, добавленный сайт полиаденилирования (poly А) расположен на расстоянии примерно от 30 до 2000 нуклеотидов 3' ("даунстрим") от сайта терминации белка в положении перед сайтом терминации транскрипции.
Для долговременного продуцирования рекомбинантных белков с высоким выходом предпочтительной является стабильная экспрессия. Например, методами генной инженерии можно получить линии клеток, которые стабильно экспрессируют кодирующие белки. Скорее чем с применением экспрессионных векторов, которые содержат ориджины репликации вирусов, клетки-хозяева можно трансформировать с использованием векторов под контролем соответствующих элементов регуляции экспрессии (например, промоторных, энхансерных последовательностей, терминаторов транскрипции, сайтов аденилирования и т.п.) и селективного маркера. После введения чужеродной ДНК полученные клетки можно оставлять расти в течение 1-2 дней в обогащенной питательной среде, а затем сменить ее на селективную среду. Селективный маркер в рекомбинантной плазмиде сообщает резистентность к отбору и позволяет клеткам стабильно интегрировать плазмиду в свои хромосомы и расти с образованием центров (очагов), которые в свою очередь можно клонировать и распространять в линии клеток.
Можно использовать целый ряд систем отбора, включая, но без ограничения, гены тимидинкиназы вируса простого герпеса, гипоксантин-гуанин фосфорибозилтрансферазы и аденин фосфорибозилтрансферазы в клетках tk-, hgprt- или aprt-, соответственно. Также можно использовать резистентность к антиметаболитам как основу для отбора на dhfr, который сообщает устойчивость к метотрексату; gpt, который сообщает устойчивость к микофенольной кислоте; neo, который сообщает устойчивость к аминогликозиду G-418; и hygro, который сообщает устойчивость к гигромицину. Известно, что в уровне техники имеются многие другие системы отбора, которые также применимы по настоящему изобретению.
Предполагается, что выделенные олигонуклеотиды или детектирующие агенты могут "сверхэкспрессироваться", избыточно экспрессироваться, т.е. уровень их экспрессии превышает уровень их натуральной экспрессии в резидентных клетках организма, или даже уровень экспрессии других белков в рекомбинантной клетке-хозяине. Такую сверхэкспрессию можно определять различными методами, включая мечение радиоактивной меткой и/или очистку белка. Однако, предпочтительными являются простые и непосредственные методы определения, например, методы, включающие SDS/PAGE и окрашивание белка или иммуноблоттинг с последующим количественным анализом, таким как денситометрическое сканирование полученного геля или блота (пятна). Специфическое повышение уровня рекомбинантного белка или пептида по сравнению с уровнем в нормальных человеческих клетках является показателем сверхэкспрессии, как и относительная интенсивность конкретного белка по сравнению с другими белками, продуцируемыми в клетке-хозяине, например, наглядно наблюдаемая на геле.
Олигонуклеотид может быть в клетке, которая может представлять собой клетку, экспрессирующую олигонуклеотид, в соответствии с чем детектирующий агент продуцируется в клетке. Кроме того, вектор может быть в клетке, которая может представлять собой клетку, экспрессирующую олигонуклеотид, в результате чего детектирующий агент продуцируется в клетке. Предполагается также, что олигонуклеотиды и/или векторы могут присутствовать в организме хозяина-животного (например, трансгенного животного), которое экспрессирует олигонуклеотид и продуцирует детектирующий агент.
Олигонуклеотид, кодирующий детектирующий агент, может представлять собой олигонуклеотид, который функционально кодирует детектирующий агент. Чтобы функционально кодировать детектирующий агент (т.е. способствовать экспрессии олигонуклеотида), олигонуклеотид должен включать, например, последовательности регуляции экспрессии (регуляторные последовательности, последовательности, регулирующие экспрессию), например, такие как ориджин репликации, промотор, энхансер и сайты процессирования необходимой информации, такие как сайты связывания рибосом, сайты сплайсинга РНК, сайты полиаденилирования и последовательности терминации транскрипции.
Применимые последовательности, регулирующие экспрессию (регуляторные последовательности), включают промоторы генов металлотионеинов, генов актинов, генов иммуноглобулинов, CMV, SV40, аденовируса, вируса бычьей папилломы и т.д. Нуклеиновую кислоту, кодирующую выбранный пептид или полипептид, можно легко определить на основании генетического кода для аминокислотной последовательности выбранного пептида или полипептида, и любой выбранный пептид или полипептид кодируют многие нуклеиновые кислоты. Также рассматриваются модификации в нуклеотидной последовательности, кодирующей детектирующий агент. Модификации, которые могут применяться, представляют собой модификации последовательностей регуляции (регуляторных последовательностей) экспрессии детектирующего агента, чтобы сделать продуцирование детектирующего агента индуцируемым (индуцибельным) или репрессируемым под контролем соответствующего индуктора или репрессора. Такие способы являются стандартными в уровне техники. Олигонуклеотид можно получать способами, стандартными в уровне техники, такими как методы рекомбинантной ДНК и методы получения синтетических нуклеиновых кислот или in vitro ферментативный синтез.
Антитела, специфические к областям или связывающиеся с областями HCV ядерного белка, которые не представлены областями, включенными в детектирующий агент, применимы в качестве инструментов исследования, компонентов для клинических диагностических анализов или других целей. Антитело, необязательно, применяется в качестве агента для скрининга на присутствие HCV ядерного белка в образце путем связывания с эпитопом в области ядерного белка. Антитело для применения в способе или в наборе по изобретению, необязательно, не специфически, или неспецифически связывается с детектирующим агентом и в настоящем контексте называется детектирующим антителом. Таким образом, детектирующий агент и детектирующее антитело можно применять в одном биологическом образце одновременно для обнаружения либо одного ядерного белка, либо как ядерного белка, так и антител, специфических к ядерному белку в образце.
Термины "антитело" и "антитела" в данном контексте включают моноклональные, поликлональные, химерные, одноцепочечные, биспецифические, симианизированные (включающие участки обезьяньих антител) и гуманизированные антитела, а также фрагменты Fab, включая продукты экспрессионной библиотеки Fab-фрагментов иммуноглобулинов.
В данном контексте антитела могут представлять собой поликлональные или моноклональные антитела. Также может применяться интактное антитело, его фрагмент (например, Fab или F(ab')2), или его рекомбинантный (полученный генной инженерией) вариант (например, sFv). Такие антитела могут представлять собой антитела, относящиеся к любому классу иммуноглобулинов, включая IgG, IgM, IgE, IgA, IgD, и к любому подклассу.
Антитела в настоящей заявке могут представлять собой моноклональные или поликлональные антитела, необязательно, фрагмент F(ab)'2, не содержащий Fc участок антитела. Антитела можно получать путем генерации гибридом слиянием с В клетками, или при использовании лабораторных животных, таких как мышь, гуманизированная мышь, крыса, кролик или коза, иммунизированных детектирующим агентом или его пептидным эпитопом. Пептиды и/или полипептиды, необязательно, содержат мутации: делецию, инсерцию (вставку) и/или замену. Для идентификации антител, которые специфически связываются с детектирующим агентом, можно проводить скрининг.
Предполагается, что выражение "специфически связываемся)" в данном контексте означает, что антитело обладает достаточной аффинностью к последовательности эпитопа, чтобы его можно было использовать в иммунном анализе, и в то же время не связывается в детектируемой степени с неэпитопными последовательностями в биологическом образце, например, в сыворотке.
Моноклональные антитела получают методами, хорошо известными специалистам в данной области техники. Типичный метод представляет собой модифицированный вариант метода, описанного в публикации Kearney et al., J. Immunol. 123:1548-1558 (1979). Коротко говоря, животных, таких как мыши или кролики, инокулируют иммуногеном в адъюванте, и спленоциты (клетки селезенки) собирают и смешивают с клетками миеломной линии. Слияние клеток индуцируют, добавляя полиэтиленгликоль. Гибридомы отбирают химическим методом, засевая клетки в селективной среде, содержащей гипоксантин, аминоптерин и тимидин (HAT). Затем гибридомы подвергают скринингу на способность продуцировать антитела, которые специфически связывают детектирующий агент. Гибридомы, продуцирующие антитела, клонируют, размножают и хранят в замороженном виде до момента продуцирования в будущем.
Методы получения одноцепочечных антител известны специалистам в данной области техники и описаны в патенте США №4,946,778, и их можно применять для получения одноцепочечных антител к мотивам по данному описанию. Метод фагового дисплея можно применять для отбора генов антител, обладающих активностью связывания с целевыми пептидами.
Антитело, необязательно, модифицируют с тем, чтобы оно стало "гуманизированным", путем трансплантации областей, определяющих комплементарность (гипервариабельных областей) антитела, полученного с использованием гибридом, в человеческое моноклональное антитело, описанное в публикации Jones et al., Nature, 32: 1522-525 (1986).
Поликлональные антитела можно получать, иммунизируя доноров вакцинами или иммуногенами. Затем берут сыворотку у выбранных доноров и готовят препараты иммуноглобулинов.
Иммуноген, используемый для получения антитела по настоящему изобретению, необязательно модифицируют с целью повысить его иммуногенность. В неограничивающем примере иммуноген (антиген) можно связывать с химическими соединениями или с иммуногенными носителями, при условии, что связывание не нарушит заданную биологическую активность ни антигена, ни носителя. Обзор некоторых общих положений в стратегии связывания см. в Практикуме: Antibodies, А Laboratory Manual, Cold Spring Harbor Laboratory, ed. E. Harlow and D. Lane (1988). Применимые иммуногенные носители, известные в уровне техники, включают, но без ограничения, гемоцианин лимфы улитки (гемоцианин фиссуреллы) (KLH); альбумин бычьей сыворотки (ВSA), овальбумин (яичный белок), PPD (туберкулин, очищенный от белковых фракций питательной среды); эритроциты; столбнячный анатоксин; холерный анатоксин; агарозные гранулы; активированный уголь; или бентонит.Применимые для связывания химические соединения включают, но без ограничения, динитрофенольные группы и арсаниловую кислоту.
Иммуноген можно модифицировать также другими методами, включающими, например, тепловую денатурацию и/или SDS.
Иммуноген можно применять также в виде фармацевтически приемлемой соли. Подходящие кислоты и основания, которые способны образовывать соли с полипептидами по настоящему изобретению, хорошо известны специалистам в данной области техники и включают неорганические и органические кислоты и основания.
Иммуноген, необязательно, включает аминокислоты или состоит из аминокислот 1-13, 32-49 или с 91 до 120 последовательности SEQ ID NO: 1, или любую их комбинацию (или любой их комбинации). Иммуноген, необязательно, включает аминокислотную последовательность HCV ядерного белка, за исключением остатков 14- 31 или 51-90 последовательности SEQ ID NO: 1. Методы получения таких иммуногенов описаны в настоящей заявке и хорошо известны из уровня техники. Типичные примеры антител, которые не распознают детектирующий агент, включают антитела, описанные в публикации Barban, V., et al., J. Gen. Virol, 2000; 81:461-469.
В другом аспекте изобретения предусматривается набор, который включает детектирующий агент и подходящий носитель. Подходящие фармацевтически приемлемые носители облегчают применение пептида в системе для обнаружения или в способе обнаружения присутствия или отсутствия антитела, которое специфически связывает детектирующий агент. Носители может выбрать специалист в данной области техники. Типичные носители включают стерильную воду или физиологический солевой раствор, систему на основе водных буферов, например, такую как HEPES, TRIS, или фосфатно-солевой буферный раствор, лактозу, сахарозу, фосфат кальция, желатин, декстран, агар-агар, пектин, арахисовое масло, оливковое масло и кунжутное масло.
Необязательно, детектирующий агент или детектирующее антитело можно применять совместно (объединять) с обычными фармацевтическими ингредиентами, например, такими как консерванты или химические стабилизирующие вещества. Подходящие ингредиенты включают, например, казаминовые кислоты, сахарозу, желатин, феноловый красный (фенолрот), N-Z амин, монокалия дифосфат (?), лактозу, гидролизат лактальбумина и сухое молоко.
Также предусматривается способ обнаружения присутствия или отсутствия HCV у субъекта. Способ включает осуществление контакта образца с детектирующим агентом и обнаружение (детекцию) специфического связывания антитела, присутствующего в образце, с детектирующим агентом. В периоды HCV инфекции, когда антитело присутствует в достаточном количестве, антитела к ядерному антигену, а именно, в области остатков 14-31 или 50-91, можно детектировать по их специфическому связыванию с детектирующим агентом. Было найдено, что области HCV ядерного белка, охватывающие первый и второй эпитоп, представляют собой области, неожиданно важные для получения антител к HCV ядерному белку. Так, детектирующий агент, который включает все остатки или часть остатков 14-31 или 50-91, применим для обнаружения HCV инфекции у субъекта за счет присутствия антител к ядерному белку у субъекта. По существу способ включает осуществление контакта образца, или его части, с детектирующим агентом, чтобы обеспечить возможность его специфического связывания с антителом к ядерному белку. Если специфическое связывание удается обнаружить, это подтверждает наличие HCV инфекции. Если специфическое связывание не удается обнаружить, это указывает либо на отсутствие HCV инфекции, либо на то, что сероконверсия еще не наступила и у субъекта еще не выработались антитела.
Способ, решающий проблему обнаружения до наступления сероконверсии, включает осуществление контакта биологического образца как с детектирующим агентом, так и с детектирующим антителом, которое не связывается с какой-либо областью детектирующего агента. Таким образом детектирующий агент может применяться для обнаружения присутствия или отсутствия антител к ядерному белку, а детектирующее антитело может применяться для обнаружения присутствия или отсутствия ядерного белка либо до, либо после сероконверсии. Итак, предлагается надежная и полноценная (совершенная) аналитическая система. Подобные аналитические системы представлены в патенте США №7,316,905, методики, описанные в этом патенте, можно применять для работы с детектирующим агентом по настоящему изобретению и детектирующим антителом. Однако, пептиды и антитела, описанные в патенте США №7,316,905, не работают (непригодны) в заданных (вышеприведенных) процессах.
Термином "субъект" в данном контексте определяется любой организм, способный принимать, размещать в качестве хозяина вирусную инфекцию, например HCV инфекцию. Субъект включает, например: любое млекопитающее, например, человека, нечеловеческих приматов, лошадей, коз, коров, овец, свиней, собак, кошек, грызунов; а также клетки. Согласно некоторым вариантам субъект означает человека и исключает другие организмы. Согласно некоторым вариантам субъект означает клетку и исключает организм.
Термин "биологический образец" в данном контексте определяется как образец, полученный из биологического организма, ткани, клетки, клеточной культуральной среды или любой среды, пригодной для имитации биологических условий, или из окружающей среды. Неограничивающие примеры включают слюну, десневую (гингивальную) жидкость, спинномозговую жидкость (ликвор), желудочный и кишечный сок, выделения желез слизистой оболочки, урогенитальные выделения, синовиальную жидкость, кровь, сыворотку, плазму, мочу, содержимое кисты, лимфатическую жидкость, асцит, плевральный выпот, интерстициальную жидкость, внутриклеточную жидкость, внутриглазную жидкость, сперму, выделения молочной железы, витреальную жидкость, носовой (назальный) секрет, воду, воздух, газ, порошок, почву, биологические отходы, кал, клеточную культуральную среду, цитоплазму, клеточный секрет, клеточный лизат, буферы или любые другие жидкие или твердые среды.
Способ, необязательно, применяют для диагностики инфицирования субъекта вирусом HCV. Необязательно, способ применяют при лечении HCV инфекции, чтобы определить, выведен ли вирус из субъекта (освобожден ли организм субъекта от вируса) или требуется дальнейшее лечение.
В целом предлагаемые детектирующие агенты и способы обнаружения представляют надежную и полноценную систему для обнаружения HCV или для диагностики HCV инфекции у субъекта. Детектирующие агенты можно применять для обнаружения HCV инфекции после сероконверсии. Согласно некоторым вариантам полную информацию о масштабе HCV инфекции можно получить, объединив детектирующий агент с детектирующим антителом, чтобы обнаруживать HCV инфекцию вне зависимости от статуса сероконверсии у субъекта, тем самым исключаются ограничения, накладываемые периодом серонегативного окна, характерные для многих предыдущих диагностических процессов.
Различные аспекты настоящего изобретения иллюстрируются нижеприведенными неограничивающими примерами. Примеры даются с целью иллюстрации и ни в коей мере не ограничивают осуществление применения настоящего изобретения на практике. Следует понимать, что можно осуществлять варианты и модификации, не отступая от сущности и объема изобретения. Рядовой специалист в данной области техники без труда поймет, каким образом можно получить такие реагенты.
Примеры
Пример 1: Получение детектирующего агента.
Для анализа, включающего одновременное обнаружение антител (Ab's) и ядра, требуется применение рекомбинантного белка, который хотя и способен обнаруживать Ab's, специфические к ядру HCV, но не способен иммунологически реагировать с моноспецифическими Ab's, применяемыми для извлечения (захвата) ядра (ядерного белка) из сыворотки крови. В некоторых вариантах был создан ген, кодирующий области HCV ядерного белка 14-31 аа и 50-91 аа, разделенные линкером с аа последовательностью SGGGGSGGGS; этот ген экспрессировали в E.coli с применением вектора pETitN. Для того чтобы упростить очистку антигена методом металл-аффинной хроматографии на Ni-агарозе (Invitrogen, USA), была добавлена метка 6xHis на N-конце.
Пример 2: Иммобилизованное и детектирующее антитела
Продажное моноклональное Ab (Pierce Biotechnology, Rockford, IL) метили биотином и применяли для (обычного) обнаружения HCV ядерного (корового) белка. Моноспецифические моноклональные Ab's применяли для захвата HCV ядра. Протокол иммунизации и создание (разработка) моноспецифических поликлональных антител описаны в публикации Puffinbarger Ν, Hansen К, Resta R, Laurent A, Knudsen T, Madara J, Thompson L. Production and characterization of multiple antigenic peptide antibodies to the adenosine Агь receptor. Mol. Pharm. 1995; 47:1126-1132. Антитела (Ab's) очищали аффинной хроматографией, используя синтетические пептиды, содержащие области HCV ядра 1-30 аа и 28-58 аа.
Пример 3: Обнаружение антиядерных (антикоровых) антител или ядерного белка в сыворотке крови HCV- инфицированных субъектов.
Для обнаружения антител к ядру HCV использовали пять рекомбинантных HCV белков: (i) модифицированный рекомбинантный детектирующий агент из Примера 1, (ii) NS3 (аа положения 1356-1459) HCV генотипа 1a, (iii) NS3 (аа положения 1192-1459) HCV генотипа 1b, (iv) мозаичный белок, содержащий иммунодоминантные области белка NS4 (аа положения 1691-1710, 1712-1733 и 1921-1940) HCV генотипов 1, 2, 3 и 5, и (v) NS5 (аа положения 2061-2302) HCV генотипа 1а. Все белки, за исключением детектирующего агента, экспрессировались в Е. coli в виде химерных (гибридных) белков с глутатион S-трансферазой (GST) и очищались аффинной хроматографией (Pharmacia Biotech, Inc., Piscataway, NJ).
Детектирующие агенты и антиядерные антитела разводили в фосфатно-солевом буферном растворе (PBS). Индивидуальные лунки планшетов Nunc MaxiSorp (Nunc, Inc., Denmark) сенсибилизировали помощью 100 мкл смеси, содержащей 1 мкг/мл ядерного белка (детектирующего агента), 1 мкг/мл белка NS3 вируса генотипа 1a, 1 мкг/мл белка NS3 вируса генотипа 1b, 1 мкг/мл мозаичного белка NS4, 1 мкг/мл NS5 Ag и 2 мкг/мл антиядерных антител. Планшеты инкубировали в течение ночи при комнатной температуре, а затем блокировали, выдерживая в 150 мкл/лунка 10 мМ PBS, содержащего 1% BSA, 5% сахарозы, в течение 2 час при комнатной температуре. Блокирующий раствор отсасывали (аспирация) и планшеты сушили и упаковывали в пакеты из фольги с осушителем.
Девятнадцать продажных (серийно выпускаемых) сероконверсионных панелей, содержащих серийные образцы от отдельных доноров крови с HCV инфекцией, получали от компаний Zeptometrix (Buffalo, NY) и SeraCare Life Sciences, Inc. (Milford, MA). Bee панели тестировали с помощью EIA-HCV Ag/Ab.
Образцы анти-HCV-положительной сыворотки крови (n=374) получали от компаний SeraCare Life Sciences, Inc. и Diagnostic Systems (Nizhniy Novgorod, Russia). Образцы от SeraCare тестировали с применением тест-системы (набора) Ortho EIA Anti-HCV 3.0. Сыворотку, полученную от компании Diagnostic Systems, проверяли с использованием наборов DS-EIA-Anti-HCV (Diagnostic Systems, Nizhniy Novgorod, Russia) и Ortho RIBA HCV 3.0.
Образцы сыворотки (n=208), отрицательные маркеры HCV инфекции, получали от компаний Innovative Research (Novi, MI), Diagnostic Systems (Nizhniy Novgorod, Russia) и SeraCare Life Sciences, Inc. (Milford, MA); 23 из них были получены из больниц и имели отрицательные маркеры HCV инфекции, но положительные маркеры некоторых других вирусных инфекций. Все образцы тестировали с применением набора DS-EIA-Anti-HCV. Анализ EIA-HCV Ag/Ab представляет собой комбинацию "сэндвич" метода обнаружения HCV ядерного антигена и непрямого метода (формата) обнаружения антитела с использованием детектирующего агента из Примера 1. На первой стадии конъюгат 1, содержащий биотинилированное моноклональное Ab к HCV ядерному Ag, образцы и контрольные образцы добавляли в лунки и инкубировали при встряхивании в течение 30 мин при 37°С. После отмывки добавляли стрептавидин-пероксидазу и конъюгат 2 (меченные пероксидазой антитела к человеческому IgG). Планшеты инкубировали при встряхивании в течение 30 мин при 37°С. Несвязанный конъюгат удаляли на дополнительной стадии отмывки, и детектировали комплекс антиген-антитело, добавляя субстрат. После прекращения реакции определяли интенсивность поглощения (оптической плотности) при 450 нм. Образец считали положительным, если его оптическая плотность была выше предельного значения или равна предельному значению. Для расчета предельного (cut-off, СО) значения мы проверяли 208 HCV-отрицательных сывороточных образцов, используя анализ EIA-HCV-Ag/Ab. Среднее значение OD (оптической плотности) было 0.033, медианное - 0.025. Для установления СО применяли два метода. Первый метод был основан на вычислении 99.9й процентили значений OD для отрицательных образцов. В качестве второго метода использовали метод относительных операционных характеристик (ROC). Для отбора СО использовали сумму чувствительности и специфичности. Оба метода дали близкие значения СО.
Все положительные образцы на антитела к HCV- (n=374) были определены как положительные анализом EIA-HCV Ag/Ab, причем у 88% образцов значение OD/CO было >9.0. Отношение OD/CO варьировалось от 1.2 до 40.0. Среднее значение OD/CO составляло 22.9, а медианное значение было равно 24.5.
Методом EIA-HCV Ag/Ab определено, что все образцы (n=45) от пациентов, инфицированных вирусом HCV известных генотипов, являются положительными. Для этих образцов нет разницы между средним и медианным значением отношения OD/CO (Таблица 1).
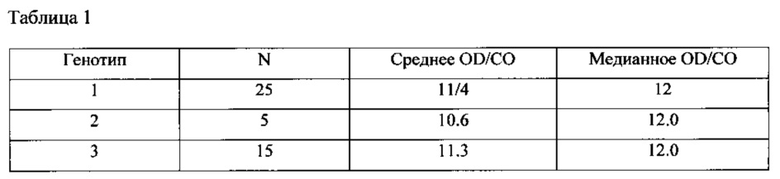
Серийные образцы с сероконверсионных панелей (n=19) проверяли при использовании EIA-HCV-Ag/Ab, чтобы оценить чувствительность раннего определения HCV и сравнить с другими анализами. Результаты представлены в Таблице 2.
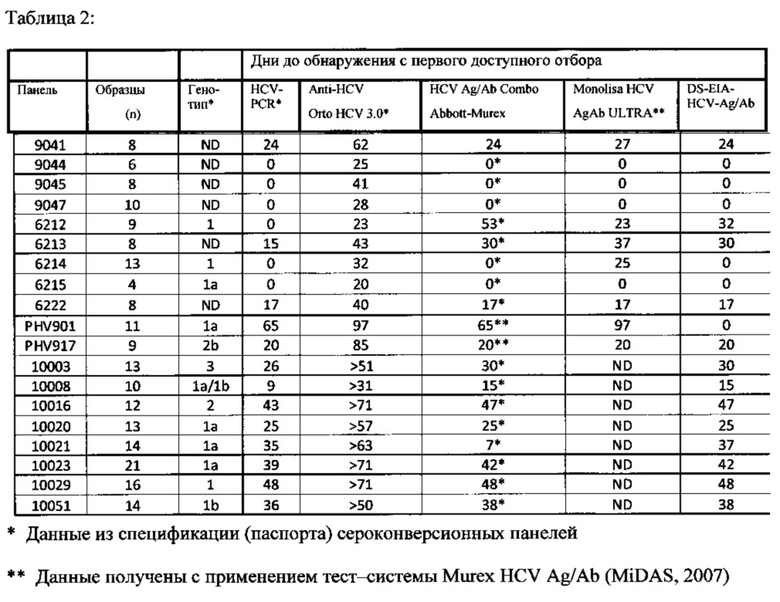
Анализ EIA-HCV-Ag/Ab позволил обнаруживать HCV инфекцию на 10 панелях так же быстро, как и PCR. На одной панели (PHV901) он обнаружил HCV инфекцию раньше, чем PCR. Анализ EIA-HCV-Ag/Ab обнаружил HCV инфекцию на 16 панелях так же рано, как тест на HCV Ag/Ab Combo Abbott-Murex, а на 2 панелях еще раньше. Чувствительность теста EIA-HCV-Ag/Ab была такой же, как чувствительность теста Monolisa HCV AgAb ULTRA BioRad на 6 из 11 панелей. Тест EIA-HCV-Ag/Ab обнаруживал HCV инфекцию раньше, чем Monolisa HCV AgAb ULTRA BioRad, на других 4 из 11 панелей.
Среднее значение задержки обнаружения сероконверсии определяли, сравнивая с HCV PCR. Результаты показаны в Таблицах 3 и 4.
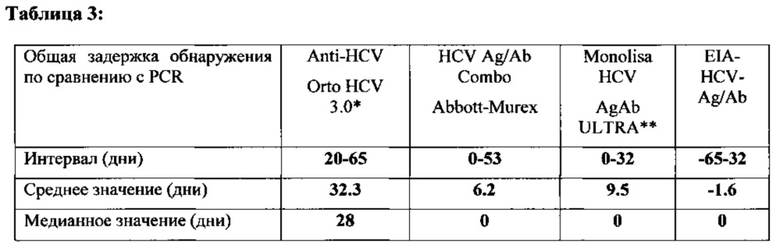

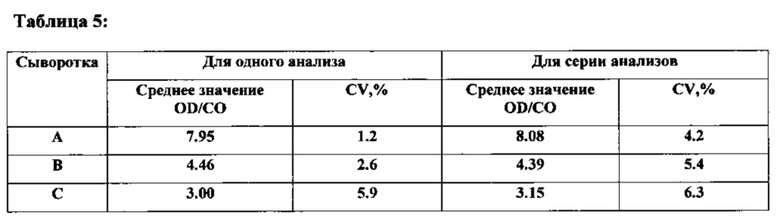
Коэффициенты вариации для одного анализа и для серии анализов рассчитывали, тестируя в 4 повторностях 3 сыворотки крови в одном и том же анализе (прогоне, цикле) и в 4 повторностях 3 сыворотки крови в 5 различных анализах (прогонах, циклах). Коэффициенты вариации для одного анализа и для серии анализов <8%. Результаты представлены в Таблице 5.
СПИСОК ЛИТЕРАТУРЫ
Velati С, Romano L, Baruffi L, Pappalettera M, carreri V, Zanetti A. Residual risk of transfusion-transmitted HCV and HIV infections by antibody-screened blood in Italy. Transfusion 2002;42:989-993
Van der Poel CL, Cuypers HT, Reesink HW. Hepatitis С virus six years on. Lancet 1994; 344: 1475-1479
Puffinbarger N, Hansen K, Resta R, Laurent A, Knudsen T, Madara J, Thompson L. Production and characterization of multiple antigenic peptide antibodies to the adenosine Агь receptor. Mol. Pharm. 1995;47:1126-1132
Busch M. Closing the windows on viral transmission by blood transfusion. In S.L. Stramer (ed.), Blood safety in the new millennium. American association of blood bunks. 2001; Bethesda, Md:33-54
Toyoda H, Sakamoto H, Mizuno T, Horiguchi Y, Nakano H. Eradication of hepatitis С virus lb by interferon in a health care worker with acute hepatitis following needlestick transmission from a patient with chronic hepatitis С unresponsive to interferon. Scand. J. Gastroenterol. 2000; 35:1117-1120
Sillanpaa M, Melen K, Porka P, Fagerlund R, Nevalainen K, Lappalainen M, Julkunen I. Hepatitis С virus core, NS3, NS4B and NS5A are the major immunogenic proteins in humoral immunity in chronic HCV infection. Virology J 2009; 6:84-96
Lefrere J, Guiramand S, Lefrere F et al. Full or partial seroconversion in patients infected by hepatitis С virus. J Infect Dis 1997; Vol 175: 316-322
Courouce A, Le Marrec N, Girault A, Ducamp S, Simon N. Anti-hepatitis С virus (anti-HCV) seroconversion in patients undergoing hemodialysis: comparison of second- and third-generation anti-HCV assays. Transfusion 1994; Vol 34; 790-795
Laperche S. Simultaneous detection of anti-HCV Ab and HCV core antigen. Roche infectious diseases symposium, Barselona, Spain, 2009; 8th Oct
Riabinina S, Baranova E, Sharipova I, Susekina M, Puzyrev V, Obriadina A, Burkov A, Ulano va T. Evaluation of diagnostic efficiency of the recombinant protein modeling immunodominant epitope V3 of envelope gpl20 for immunoenzyme detection for HIV-1 infection antibodies. Mol Gen Mikrobiol Virusol 2007; 3:33-36
Baranova E, Puzyrev V, Van'kova O, Pimenov V, Burkov A, Obriadina A, Ulanova T. Comparison of the diagnostic value of recombinant antigens and synthetic peptides that mimic the immunogenic epitopes of the envelop protein gp41 in the enzyme immunodetection of HIV-1 antibodies. Vopr Virusol. 2006 May-Jun;51(3):46-48
Yeh C-T, Han C-M, Lo S-Y, Ou J-H, Fan K-D, Sheen I-S, Chu C-M, Liaw Y-F. Early detection of anti-HCc antibody in acute hepatitis С virus (HCV) by western blot (immunoblot) using a recombinant HCV core protein fragment. J Clin Microbiol 1994;Sept: 2235-2241
Lin S, Arcángel Ρ, Medina-Selby A, Coit D, Ng P, Nguyen S, McCoin C, Gyenes A, Ни C, Tandeske L, Phelps B, Chien D. Design of novel conformational and genotype-specific antigens for improving sensitivity of immunoassays for hepatitis С virus-specific antibodies. J Clin Microbiol 2005; Aug: 3917-3924
Evaluation of Murex HCV Ag/Ab Combination. MiDAS, London 2007:1-18
В свете вышеприведенного описания различные модификации настоящего изобретения, помимо модификаций, показанных и описанных в настоящей заявке, будут очевидны для специалистов в данной области техники. Также предполагается, что такие модификации входят в объем прилагаемой Формулы изобретения.
Следует принимать во внимание, что, если не указано иное, все реагенты можно получать, используя источники, известные в области техники. Способы амплификации нуклеотидов, трансфекции клеток и экспрессии и очистки белков также в пределах компетенции специалистов в данной области техники.
Патенты и публикации, указанные в описании, показывают уровень специалистов в той области техники, к которой относится данное изобретение. Эти патенты и публикации включены в настоящее изобретение посредством отсылки в той же степени, как если бы в данной заявке конкретно и отдельно утверждалось, что каждая отдельная заявка или публикация включена в настоящее изобретение посредством отсылки во всей полноте идеи изобретения.
Предполагается, что вышеприведенное описание иллюстрирует конкретные варианты изобретения, но не ограничивает его практическое осуществление.


Изобретение относится к области биохимии, в частности к детектирующему агенту для обнаружения антитела, специфического к HCV-ядерному белку, причем указанный детектирующий агент может специфически связываться с указанным антителом, специфическим к HCV-ядерному белку. Указанный детектирующий агент включает пептид, который содержит область первого эпитопа, область второго эпитопа, и линкер, расположенный между указанной областью первого эпитопа и указанной областью второго эпитопа. Также раскрыт способ обнаружения присутствия или отсутствия HCV в биологическом образце с использованием вышеуказанного детектирующего агента. Изобретение также относится к набору для обнаружения HCV у субъекта, включающему вышеуказанный детектирующий агент. Изобретение позволяет эффективно обнаруживать HCV в образце до или после сероконверсии, делая надежным способ обнаружения и диагностики HCV. 4 н. и 11 з.п. ф-лы, 5 табл., 3 пр.
1. Детектирующий агент для обнаружения антитела, специфического к HCV-ядерному белку,
причем указанный детектирующий агент может специфически связываться c указанным антителом, специфическим к HCV-ядерному белку;
причем указанный детектирующий агент включает пептид, содержащий:
область первого эпитопа, состоящую из последовательности SEQ ID NO: 2; область второго эпитопа, состоящую из последовательности SEQ ID NO: 3 или последовательности SEQ ID NO: 3, в которой исключен С-концевой остаток; и линкер, расположенный между указанной областью первого эпитопа и указанной областью второго эпитопа, при этом в указанном линкере исключена любая часть последовательности SEQ ID NO: 1; и причем в указанном детектирующем агенте исключены последовательные аминокислоты 1-13, последовательные аминокислоты 32-49 и последовательные аминокислоты 100-120 последовательности SEQ ID NO: 1.
2. Детектирующий агент по п. 1, в котором указанный линкер представляет собой аминокислоту или аминокислотную последовательность длиной от 2 до 50 аминокислот.
3. Детектирующий агент по п. 2, в котором указанный линкер содержит 5 или более аминокислот.
4. Детектирующий агент по п. 3, в котором указанный линкер содержит последовательность SEQ ID NO: 4.
5. Способ обнаружения присутствия или отсутствия HCV в биологическом образце, включающий:
осуществление контакта биологического образца с детектирующим агентом, который может специфически связываться антителом, специфическим к HCV-ядерному белку, и включает пептид, содержащий область первого эпитопа, состоящую из последовательности SEQ ID NO: 2, область второго эпитопа, состоящую из последовательности SEQ ID NO: 3 или последовательности SEQ ID NO: 3, в которой исключен С-концевой остаток; и линкер, расположенный между указанной областью первого эпитопа и указанной областью второго эпитопа, при этом в указанном линкере исключена любая часть последовательности SEQ ID NO: 1; причем в указанном детектирующем агенте исключены последовательные аминокислоты 1-13, последовательные аминокислоты 32-49 и последовательные аминокислоты 100-120 последовательности SEQ ID NO: 1;
осуществление контакта указанного биологического образца с детектирующим антителом, причем указанное детектирующее антитело является поликлональным, способным специфически связываться с эпитопом в HCV-ядерном белке и не связывается специфически с указанным детектирующим агентом;
обнаружение в указанном биологическом образце присутствия или отсутствия указанного антитела, специфического к HCV-ядерному белку, при этом обнаружение в указанном биологическом образце специфического связывания указанного детектирующего агента с указанным антителом, специфическим к HCV-ядерному белку, указывает на присутствие HCV в указанном биологическом образце; и
обнаружение в указанном биологическом образце присутствия или отсутствия HCV-ядерного белка, при этом обнаружение в указанном биологическом образце специфического связывания указанного детектирующего антитела с HCV-ядерным белком указывает на присутствие HCV в указанном биологическом образце.
6. Способ по п. 5, в котором указанное детектирующее антитело получено к иммуногену, в котором исключены указанная область первого эпитопа и указанная область второго эпитопа.
7. Способ по п. 5, в котором указанный детектирующий агент представляет собой пептид, состоящий из последовательности SEQ ID NO: 2 и последовательности SEQ ID NO: 3, которые связаны линкером.
8. Способ по п. 5, в котором указанный биологический образец выбран из группы, состоящей из крови, плазмы крови и сыворотки крови.
9. Набор для обнаружения HCV у субъекта, содержащий детектирующий агент по п. 1 и фармацевтически приемлемый носитель.
10. Набор для обнаружения HCV у субъекта, содержащий детектирующий агент по п. 1 и детектирующее антитело, причем указанное детектирующее антитело является поликлональным, способным специфически связываться с эпитопом в HCV-ядерном белке и не связывается специфически с указанным детектирующим агентом.
11. Набор по п. 10, в котором указанное детектирующее антитело получено к иммуногену, у которого исключены указанная область первого эпитопа и указанная область второго эпитопа.
12. Набор по п. 10, в котором указанный иммуноген содержит одну или более последовательных аминокислот 1-13, последовательных аминокислот 32-49 и последовательных аминокислот 91-120 последовательности SEQ ID NO: 1.
13. Способ по п. 6, в котором указанный иммуноген содержит одну или более последовательных аминокислот 1-13, последовательных аминокислот 32-49 и последовательных аминокислот 91-120 последовательности SEQ ID NO: 1.
14. Детектирующий агент по п. 1, причем указанный детектирующий агент представляет собой пептид, состоящий из указанной области первого эпитопа и указанной области второго эпитопа, которые связаны линкером.
15. Детектирующий агент по п. 1, в котором указанный пептид имеет 70 или меньше аминокислот без учета указанного линкера.
| Электрический конденсатор | 1986 |
|
SU1394255A1 |
| US5574132 A, 12.11.1996 | |||
| US5350671 A, 27.09.1994 | |||
| Способ удаления экстрамедуллярных опухолей спинного мозга | 1979 |
|
SU1076092A1 |
| СПОСОБ ОБНАРУЖЕНИЯ АНТИТЕЛ К ЯДЕРНОМУ БЕЛКУ ВИРУСА ГЕПАТИТА С | 1997 |
|
RU2133622C1 |
Авторы
Даты
2018-09-19—Публикация
2014-05-12—Подача