ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к области фармацевтической химии и фармакотерапии, в частности, к соединениям 1-(3-аминопропил)-замещенного циклического амина, способу их получения, фармацевтическим композициям, содержащим такие соединения, и их применениям.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Синдром приобретенного иммунодефицита (СПИД) представляет собой такой синдром, при котором у людей после инфецирования вирусом иммунодефицита человека (ВИЧ) наступает дефицит иммунитета и запускается ряд оппортунистических инфекций и опухолей, при этом некоторые случаи могут привести к смерти. По данным Всемирной организации здравоохранения (ВОЗ) в 2011 г. во всем мире было 34 млн. носителей ВИЧ и пациентов со СПИД, 2,7 млн. человек были инфицированы повторно, и 1,8 млн. пациентов умерли. По оценкам китайского центра по контролю и профилактике заболеваний к концу 2011 года в Китае было 780000 носителей ВИЧ и пациентов со СПИД, 48000 человек были инфицированы повторно, и 28000 пациентов умерли. В настоящее время в Китае наблюдается высший пик заболеваемости и смертности от СПИД.
В настоящее время лекарственные средства для лечения СПИД в клинике разделены не следующие классы: ингибиторы обратной транскриптазы, включая нуклеозидные ингибиторы обратной транскриптазы и ненуклеозидные ингибиторы обратной транскриптазы; ингибиторы протеазы; ингибиторы интегразы и ингибиторы проникновения в клетку. Ингибиторы проникновения в клетку можно разделить на антагонисты рецептора хемокина CCR5, антагонисты рецептора хемокина CXCR4, ингибиторы адгезии и ингибиторы слияния в соответствии с различными мишенями в процессе проникновения ВИЧ в клетки-хозяева. До настоящего времени основной терапией при лечении СПИД является высокоактивная антиретровирусная терапия (ВААРТ), при которой рекомендована комбинация нескольких лекарственных препаратов, действующих на различных стадиях репликации ВИЧ для достижения эффективного действия против ВИЧ. За последнее десятилетие высокоактивная антиретровирусная терапия значительно уменьшила смертность ВИЧ-инфицированных пациентов. Тем не менее, режим дозирования при ВААРТ сложен, и комбинация лекарственных препаратов может вызывать долгосрочные тяжелые побочные эффекты. Поэтому очень важна разработка лекарственных препаратов против ВИЧ, обладающих новыми механизмами действия.
Хемокины представляют собой класс цитокинов, управляющих направленной миграцией лимфоцитов, и играют важную роль в воспалении, репарации тканей, иммунном надзоре, диапедезе, онкогенезе и эмбриональном развитии. Хемокины представляют собой белки, принадлежащие к семейству низкомолекулярных цитокинов, которое в настоящее время имеет приблизительно 45 членов. Их общие признаки заключаются в том, что они имеют небольшую молекулярную массу (приблизительно 8-10 кДа), и они содержат четыре позиционно-консервативных остатка цистеина (Cys), обеспечивающих их третичную структуру. В зависимости от того, какая из других аминокислот содержится между двумя Cys вблизи N-конца, семейство делится на четыре категории: СС, СХС, СХ3С и С хемокины, где СС хемокин и СХС хемокин представляют собой две самые важные категории.
Функции хемокина опосредованы in vivo рецептором хемокина. В настоящее время рецептору хемокина присваивают название в соответствии с характеристиками хемокина, с которым он специфично связывается (например, если его лиганд принадлежит к подсемейству СС хемокинов, его называют CCR). Рецепторы хемокинов, принадлежащие к семи трансмембранным рецепторам, сопряженным с G-белком (GPCR), селективно экспрессируются на поверхности клеток-мишеней, где их N-конец находится снаружи клетки, а С-конец находится в клетке, и они содержат семь высококонсервативных трансмембранных областей, состоящих из α-спирали. К настоящему времени обнаружено 19 рецепторов хемокинов. Они представляют собой CCR1-11, CXCR1-6, XCR1 и CX3CR1. Модуляторы рецепторов хемокинов можно применять при ряде заболеваний, таких как воспалительные или аллергические заболевания и тому подобное.
Исследования показали, что молекула CD4 на клетке Т-хелпере (Th) существенна для инвазии ВИЧ, но одной CD4 недостаточно для того, чтобы опосредовать слияние ВИЧ с клеткой. В дополнительных исследованиях обнаружено, что рецепторы хемокинов вовлечены в процесс инвазии ВИЧ, и они известны как корецепторы ВИЧ. Корецепторы можно разделить на две категории. Одна из них представляет собой корецептор CCR5, распределенный на поверхности макрофагов и вовлеченный во вхождение в клетки-хозяева ВИЧ по механизму тропизма к макрофагам (М-тропизма). Другая категория представляет собой корецептор CCR4, распределенный на поверхности Т клетки и вовлеченный во вхождение в клетки-хозяева ВИЧ по механизму тропизма к Т клеткам (Т-тропизма). На начальных стадиях инфекции почти все подтипы ВИЧ-1 используют CCR5 в качестве корецептора. Поэтому CCR5 играет очень важную роль в ВИЧ инфекции.
В экспериментах in vitro обнаружено, что хемокины RANTES, MIP-1α и MIP-1β, которые могут связываться с CCR5, могут ингибировать ВИЧ-инфекцию посредством ингибирования М-тропизма вхождения ВИЧ в клетку. В эксперименте за счет нокаутирования гена, экспрессирующего CCR5, у мышей были получены положительные результаты. Тем не менее, некоторые исследования указывают на то, что в некоторых моделях иммунная функция мыши может быть изменена. В 1996 г. сообщили, что существуют индивиды с естественным гомозиготным дефицитом гена CCR5, и такие индивиды могут быть хорошо защищены от ВИЧ инфекции в отсутствие каких-либо других проблем со здоровьем. Впоследствии было обнаружено, что по сравнению с ВИЧ-инфицированными пациентами, не имеющими дефицита по аллелю CCR5, у гетерозиготных индивидов, имеющих только один аллель CCR5, прогрессирование СПИД может явным образом замедляться. Поэтому CCR5 можно использовать в качестве хорошей мишени против ВИЧ.
Макромолекулярный антагонист к CCR5 может специфично связываться с определенным внеклеточным участком CCR5, в результате чего производит ингибиторные действия, при этом значительные токсические действия отсутствуют, но он нестабилен, легко расщепляется и разлагается, дорого стоит и не может быть введен перорально, поскольку в этом случае он не вызывает выработку организмом иммунного ответа, вызванного антителом. Поэтому основная масса эффективных исследований проведена компаниями и научно-исследовательскими институтами на непептидном низкомолекулярном антагонисте CCR5, и разработан ряд высокоактивных низкомолекулярных антагонистов CCR5, таких как ТАК-220, TBR652, викривирок и маравирок (торговое название Целзентри), утвержденные Управлением США по надзору за качеством пищевых продуктов и медикаментов (FDA) в 2007 г.
Подводя итог, существует неотложная необходимость в разработке соединений, имеющих потенциальное применение в данной области техники в качестве лекарственного препарата, являющегося антагонистом CCR5.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Объектом настоящего изобретения является обеспечение соединений 1-(3-аминопропил)-замещенного циклического амина, обладающих антагонистической активностью в отношении CCR5, представленных формулой (I), их фармацевтически приемлемых солей, энантиомеров, диастереоизомеров, рацематов или их смесей, и способа синтеза указанных соединений 1-(3-аминопропил)-замещенного циклического амина с использованием ароматического гетероциклического формальдегида в качестве сырьевого материала.
Дополнительным объектом настоящего изобретения является обеспечение фармацевтической композиции, содержащей вышеописанные соединения.
Дополнительным объектом настоящего изобретения является обеспечение применения вышеописанного соединения для получения лекарственных средств для лечения инфекции ВИЧ.
В одном аспекте настоящего изобретения предложено соединение 1-(3-аминопропил)-замещенного циклического амина формулы (I), его фармацевтически приемлемая соль, энантиомер, диастереоизомер, рацемат или их смесь:
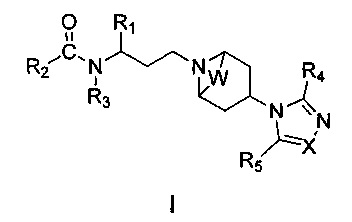
где
W отсутствует или представляет собой -СН2СН2-;
X представляет собой N или CR6;
R1 выбран из 5-7-членного гетероарила, незамещенного или замещенного от 1 до 3 заместителями, где указанный гетероарил содержит от 1 до 3 гетероатомов, выбранных из атома кислорода, серы или азота, и каждый из указанных заместителей независимо выбран из атома галогена, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 алкилокси, прямого или разветвленного С1-С4 галогеналкокси, -NR10R11, -C(=O)R12, прямого или разветвленного С1-С4 алканоилокси, циано, нитро и гидрокси, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7-членное кольцо;
каждый из R10 и R11 независимо выбран из группы, состоящей из Н, прямого или разветвленного С1-С4 алкила и -C(=O)R13;
R12 выбран из группы, состоящей из прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 алкилокси, гидроксила, амино (NH2) и прямого или разветвленного С1-С4 алкиламино;
R13 выбран из группы, состоящей из Н и прямого или разветвленного С1-С4 алкила;
R2 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С6 алкила, С3-С7 циклоалкила, 4-7-членной гетероциклической группы, С6-С12 арила или 5-7-членного гетероарила; где указанный заместитель выбран из группы, состоящей из атома галогена, гидрокси, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, С1-С4 прямого или разветвленного алкилокси, прямого или разветвленного С1-С4 алкилкарбонила, прямого или разветвленного С1-С4 галогеналкокси, прямого или разветвленного С1-С4 алкилсульфонила, прямого или разветвленного С1-С4 алкилсульфонилкарбамоила, тетразолила, циано, нитро, амино, карбокси, фенила и фенокси;
каждый из R3, R4 и R5 независимо выбран из группы, состоящей из атома водорода, прямого или разветвленного С1-С6 алкила и С3-С7 циклоалкила;
R6 выбран из группы, состоящей из Н и прямого или разветвленного С1-С6 алкила; альтернативно R5 и R6 могут связываться вместе с 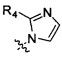 с образованием
с образованием 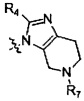 или
или 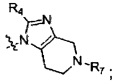
R7 выбран из группы, состоящей из Н, C(=O)R8, C(=O)OR8, C(=O)NR8R9, SO2R8 и следующих групп, замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С6 алкила, С3-С7 циклоалкила, 4-7-членной гетероциклической группы, бензила, С6-С12 арила и 5-7-членного гетероарила; где указанный заместитель выбран из атома галогена, гидрокси, прямого или разветвленного С1-С4 алкилокси, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 галогеналкокси, циано, нитро, амино и карбоксила;
каждый из R8 и R9 независимо выбран из группы, состоящей из атома водорода и следующих групп, незамещенных или замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С6 алкила, С3-С7 циклоалкила, 4-7-членной гетероциклической группы, бензила, С6-С12 арила и 5-7-членного гетероарила; где указанный заместитель выбран из группы, состоящей из атома галогена, гидрокси, прямого или разветвленного С1-С4 алкокси, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 галогеналкокси, циано, нитро, амино и карбоксила.
В другом предпочтительном воплощении изобретения соединение 1-(3-аминопропил)-замещенного циклического амина формулы (I) находится в S конфигурации или R конфигурации, предпочтительно в S конфигурации.
Предпочтительно R1 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: 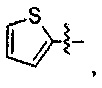
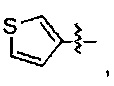
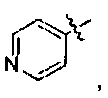
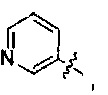
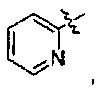

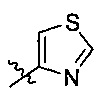 и
и 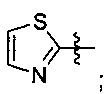 при этом указанный заместитель выбран из группы, состоящей из атома галогена, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 алкокси, -NR10R11, -C(=O)R12, прямого или разветвленного С1-С4 алкилкарбонилокси, прямого или разветвленного С1-С4 галогеналкокси, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7-членное кольцо; предпочтительно заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 галогеналкила, С1-С2 алкокси, NR10R11, -C(=O)R12, С1-С2 алкилкарбонилокси, С1-С2 галогеналкокси, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7 членный карбоцикл, 5-7-членное гетероарильное кольцо или 5-7-членный гетероцикл; и наиболее предпочтительно заместитель выбран из группы, состоящей из атома галогена, метила, метокси, этила, амино, гидроксила, циано, нитро, ацетила, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметилкарбамоила, формилокси, ацетокси, метоксикарбонила, трифторметила и трифторметокси, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо, циклопентеновое кольцо или диоксольное кольцо.
при этом указанный заместитель выбран из группы, состоящей из атома галогена, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 алкокси, -NR10R11, -C(=O)R12, прямого или разветвленного С1-С4 алкилкарбонилокси, прямого или разветвленного С1-С4 галогеналкокси, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7-членное кольцо; предпочтительно заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 галогеналкила, С1-С2 алкокси, NR10R11, -C(=O)R12, С1-С2 алкилкарбонилокси, С1-С2 галогеналкокси, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7 членный карбоцикл, 5-7-членное гетероарильное кольцо или 5-7-членный гетероцикл; и наиболее предпочтительно заместитель выбран из группы, состоящей из атома галогена, метила, метокси, этила, амино, гидроксила, циано, нитро, ацетила, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметилкарбамоила, формилокси, ацетокси, метоксикарбонила, трифторметила и трифторметокси, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо, циклопентеновое кольцо или диоксольное кольцо.
Предпочтительно каждый из R10 и R11 независимо выбраны из группы, состоящей из Н, С1-С2 алкила и -C(=O)R13.
Предпочтительно R12 выбран из группы, состоящей из С1-С2 алкила, С1-С2 алкокси, гидрокси, амино (NH2) и С1-С2 алкиламино.
Предпочтительно R13 выбран из группы, состоящей из Н и прямого или разветвленного С1-С2 алкила.
Предпочтительно R2 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С4 алкила, С3-С7 циклоалкила, 4-7-членной гетероциклической группы и фенила, где указанный заместитель выбран из группы, состоящей из атома галогена, гидрокси, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 алкокси, прямого или разветвленного С1-С4 алкилкарбонила, прямого или разветвленного С1-С4 галогеналкокси, прямого или разветвленного С1-С4 алкилсульфонила, прямого или разветвленного C1-C4 алкилсульфонилкарбамоила, тетразолила, циано, нитро, амино, карбоксила, фенила, галогенфенила, фенокси и галогенфенокси; более предпочтительно R2 выбран из прямого или разветвленного С1-С4 алкила, циклопропила, циклобутила, циклопентила, циклогексила, тетрагидропиран-4-ила, 1-метил пиперидин-4-ила, 1-ацетилпиперидин-4-ила, 1-метилсульфонилпиперидин-4-ила, 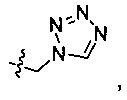
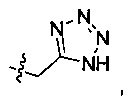

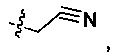 4-фторбензила, фенила, дифторциклогексила (предпочтительно 4,4-дифторциклогексила) (аналогично в данном документе ниже), этилциклогексила и феноксиметила.
4-фторбензила, фенила, дифторциклогексила (предпочтительно 4,4-дифторциклогексила) (аналогично в данном документе ниже), этилциклогексила и феноксиметила.
Предпочтительно каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н, прямого или разветвленного С1-С4 алкила и С3-С7 циклоалкила; более предпочтительно каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н, метила, этила, н-пропила, изопропила, н-бутила, втор-бутила, третичного бутила, циклопропила, циклобутила, циклопентила и циклогексила; наиболее предпочтительно каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н, метила, этила, н-пропила, изопропила, н-бутила, втор-бутила, трет-бутила и циклопропила.
Предпочтительно R6 выбран из группы, состоящей из Н и прямого или разветвленного С1-С4 алкила, более предпочтительно R6 выбран из группы, состоящей из Н, метила и этила.
Альтернативно R5 и R6 может связываться вместе с 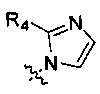 с образованием
с образованием 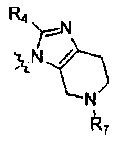 или
или 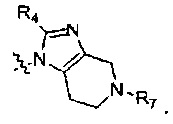
Предпочтительно R7 выбран из группы, состоящей из Н, C(=O)R8, C(=O)OR8, C(=O)NR8R9, SO2R8 и следующих групп, замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С4 алкила, С3-С7 циклоалкила, 4-7-членной гетероциклической группы, бензила и фенила, где указанный заместитель выбран из группы, состоящей из атома галогена, гидрокси, прямого или разветвленного С1-С4 алкокси, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 галогеналкокси, циано, нитро, амино и карбоксила; более предпочтительно R7 выбран из группы, состоящей из Н, C(=O)R8 и SO2R8;
каждый из R8 и R9 независимо выбран из группы, состоящей из Н и следующих групп, незамещенных или замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, С3-С7 циклоалкила, 4-7-членной гетероциклической группы, бензила, фенила и 5-7-членного гетероарила, где указанный заместитель выбран из группы, состоящей из атома галогена, гидрокси, прямого или разветвленного С1-С4 алкокси, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 галогеналкокси, циано, нитро, амино и карбоксила, где предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, гидрокси, метокси, этокси, метила, этила, трифторметила, трифторметокси, циано, нитро, амино и карбоксила; предпочтительно каждый из R8 и R9 независимо выбран из группы, состоящей из Н, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, С3-С7 циклоалкила, бензила и фенила; более предпочтительно каждый из R8 и R9 независимо выбран из группы, состоящей из метила, этила, н-пропила, циклопропила, изопропила, н-бутила, втор-бутила и трет-бутила.
В предпочтительном воплощении изобретения предложено соединение 1-(3-аминопропил)-замещенного циклического амина формулы (II), его фармацевтически приемлемая соль, энантиомер, диастереоизомер, рацемат или их смесь:
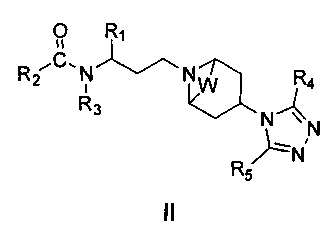
где R1, R2, R3, R4, R5 и W являются такими, как определено в формуле (I).
В формуле II предпочтительно R1 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: 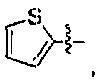

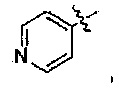
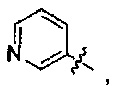
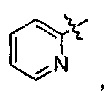
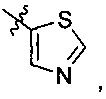
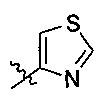 и
и 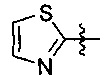 , где указанный заместитель выбран из группы, состоящей из атома галогена, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 алкокси, прямого или разветвленного С1-С4 алкилкарбонилокси, прямого или разветвленного С1-С4 галогеналкокси, NR10R11, -C(=O)R12, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7 членное кольцо; предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 галогеналкила, С1-С2 алкилкарбонилокси, С1-С2 алкокси, С1-С2 галогеналкокси, NR10R11, -C(=O)R12, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7-членный карбоцикл, 5-7-членное гетероарильное кольцо или 5-7-членный гетероцикл; наиболее предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, метила, трифторметила, трифторметокси, метокси, этила, амино, циано, нитро, ацетила, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметил карбамоила, ацетокси, формилокси и метоксикарбонила, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо, циклопентеновое кольцо или диоксольное кольцо;
, где указанный заместитель выбран из группы, состоящей из атома галогена, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 алкокси, прямого или разветвленного С1-С4 алкилкарбонилокси, прямого или разветвленного С1-С4 галогеналкокси, NR10R11, -C(=O)R12, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7 членное кольцо; предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 галогеналкила, С1-С2 алкилкарбонилокси, С1-С2 алкокси, С1-С2 галогеналкокси, NR10R11, -C(=O)R12, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7-членный карбоцикл, 5-7-членное гетероарильное кольцо или 5-7-членный гетероцикл; наиболее предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, метила, трифторметила, трифторметокси, метокси, этила, амино, циано, нитро, ацетила, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметил карбамоила, ацетокси, формилокси и метоксикарбонила, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо, циклопентеновое кольцо или диоксольное кольцо;
каждый из R10 и R11 независимо выбран из группы, состоящей из Н, прямого или разветвленного С1-С4 алкила и -C(=O)R13; предпочтительно каждый из R10 и R11 независимо выбран из группы, состоящей из Н, С1-С2 алкила и -C(=O)R13;
R12 выбран из группы, состоящей из прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 алкокси, гидрокси, амино (NH2) и прямого или разветвленного С1-С4 алкиламино; предпочтительно R12 выбран из группы, состоящей из С1-С2 алкила, С1-С2 алкокси, гидрокси, амино (NH2) и С1-С2 алкиламино;
R13 выбран из группы, состоящей из Н и прямого или разветвленного С1-С4 алкила; предпочтительно R13 выбран из группы, состоящей из Н и прямого или разветвленного С1-С2 алкила;
R2 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: фенила, прямого или разветвленного С1-С4 алкила и С3-С7 циклоалкила, где указанный заместитель выбран из группы, состоящей из атома галогена, гидрокси, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 алкокси, прямого или разветвленного С1-С4 алкилкарбонила, прямого или разветвленного С1-С4 галогеналкокси, прямого или разветвленного С1-С4 алкилсульфонил, прямого или разветвленного С1-С4 алкилсульфонилкарбамоила, тетразолила, амино, фенила, галогенфенила, фенокси и галогенфенокси; более предпочтительно R2 выбран из группы, состоящей из метила, этила, циклопропила, циклобутила, циклопентила, циклогексила, тетрагидропиран-4-ила, 1-метилпиперидин-4-ила, 1-ацетилпиперидин-4-ила, 1-метилсульфонилпиперидин-4-ила, 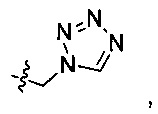
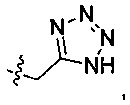
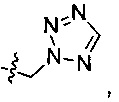
 4-фторбензила, фенила, этилциклогексила и дифторциклогексила;
4-фторбензила, фенила, этилциклогексила и дифторциклогексила;
каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н и прямого или разветвленного С1-С4 алкила; более предпочтительно каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н, метила, этила, н-пропила, изопропила, н-бутила, втор-бутила и трет-бутила; наиболее предпочтительно каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н, метила, этила, н-пропила и изопропила.
В другом предпочтительном воплощении изобретения предложено соединение 1-(3-аминопропил)-замещенного циклического амина формулы (III), его фармацевтически приемлемая соль, энантиомер, диастереоизомер, рацемат или их смесь:
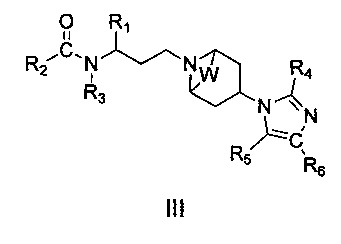
где R1, R2, R3, R4, R5, R6 и W являются такими, как определено в формуле I.
В формуле III предпочтительно R1 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: 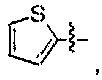
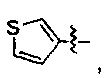

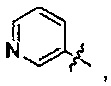
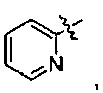
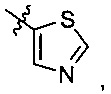
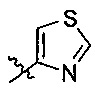 и
и 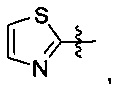 где указанный заместитель выбран из группы, состоящей из атома галогена, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 алкилкарбонилокси, прямого или разветвленного С1-С4 алкокси, прямого или разветвленного С1-С4 галогеналкокси, NR10R11, -C(=O)R12, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7-членное кольцо; предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 галогеналкила, С1-С2 алкокси, С1-С2 алкилкарбонилокси, С1-С2 галогеналкокси, NR10R11, -C(=O)R12, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7-членный карбоцикл, 5-7 членное гетероарильное кольцо или 5-7-членный гетероцикл; наиболее предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, метила, трифторметила, трифторметокси, метокси, этила, амино, циано, нитро, ацетила, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметилкарбамоила, формилокси, ацетокси и метоксикарбонила, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо, циклопентеновое кольцо или диоксольное кольцо;
где указанный заместитель выбран из группы, состоящей из атома галогена, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 алкилкарбонилокси, прямого или разветвленного С1-С4 алкокси, прямого или разветвленного С1-С4 галогеналкокси, NR10R11, -C(=O)R12, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7-членное кольцо; предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 галогеналкила, С1-С2 алкокси, С1-С2 алкилкарбонилокси, С1-С2 галогеналкокси, NR10R11, -C(=O)R12, циано, нитро и гидроксила, или два соседних заместителя вместе с присоединенным атомом углерода образуют 5-7-членный карбоцикл, 5-7 членное гетероарильное кольцо или 5-7-членный гетероцикл; наиболее предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, метила, трифторметила, трифторметокси, метокси, этила, амино, циано, нитро, ацетила, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметилкарбамоила, формилокси, ацетокси и метоксикарбонила, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо, циклопентеновое кольцо или диоксольное кольцо;
каждый из R10 и R11 независимо выбран из группы, состоящей из Н, прямого или разветвленного С1-С4 алкила и -C(=O)R13; предпочтительно каждый из R10 и R11 независимо выбран из группы, состоящей из Н, С1-С2 алкила и -C(=O)R13;
R12 выбран из группы, состоящей из прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 алкокси, гидрокси, амино (NH2) и прямого или разветвленного С1-С4 алкиламино; предпочтительно R12 выбран из группы, состоящей из С1-С2 алкила, С1-С2 алкокси, гидрокси, амино (NH2) и С1-С2 алкиламино;
R13 выбран из группы, состоящей из Н и прямого или разветвленного С1-С4 алкила; предпочтительно R13 выбран из группы, состоящей из Н и прямого или разветвленного С1-С2 алкила;
R2 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С4 алкила и С3-С7 циклоалкила, где указанный заместитель выбран из атома галогена, гидрокси, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 алкокси, прямого или разветвленного С1-С4 алкилкарбонила, прямого или разветвленного С1-С4 галогеналкокси, прямого или разветвленного С1-С4 алкилсульфонила, прямого или разветвленного С1-С4 алкилсульфонилкарбамоила, тетразолила, циано и амино; более предпочтительно R2 выбран из группы, состоящей из метила, этила, циклопропила, циклобутила, циклопентила, циклогексила, тетрагидропиран-4-ила, 1-метил пиперидин-4-ила, 1-ацетил пиперидин-4-ила, 1-метилсульфонил пиперидин-4-ила, 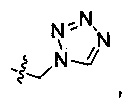
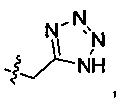
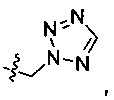
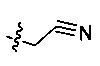 и дифторциклогексила;
и дифторциклогексила;
каждый из R3 и R4 независимо выбран из группы, состоящей из Н и прямого или разветвленного С1-С4 алкила; более предпочтительно каждый из R3 и R4 независимо выбран из группы, состоящей из Н, метила, этила, н-пропила, изопропила, н-бутила, втор-бутила и трет-бутила; наиболее предпочтительно каждый из R3 и R4 независимо выбран из группы, состоящей из Н, метила и этила;
R5 и R6 могут связываться вместе с 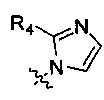 с образованием
с образованием 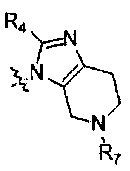 или
или 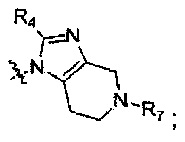
R7 выбран из группы, состоящей из Н, C(=O)R8, C(=O)OR8, C(=O)NR8R9 и SO2R8; более предпочтительно R7 выбран из группы, состоящей из Н, C(=O)R8 и SO2R8;
каждый из R8 и R9 независимо выбран из группы, состоящей из Н и следующих групп, незамещенных или замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, С3-С7 циклоалкила и бензила, где указанный заместитель выбран из группы, состоящей из атома галогена, гидрокси, прямого или разветвленного С1-С4 алкокси, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила, прямого или разветвленного С1-С4 галогеналкокси и амино; предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, гидрокси, метокси, этокси, метила, этила, трифторметила, трифторметокси и амино; предпочтительно каждый из R8 и R9 независимо выбран из группы, состоящей из Н, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 галогеналкила и С3-С7 циклоалкила; более предпочтительно каждый из R8 и R9 независимо выбран из группы, состоящей из метила, этила, н-пропила, циклопропила, изопропила, н-бутила, втор-бутила и трет-бутила.
В другом предпочтительном воплощении изобретения каждый из R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13, W и X в соединении формулы I по настоящему изобретению независимо и предпочтительно представляет собой соответствующую группу в соединениях 1-172, полученных в примерах.
Определения в настоящем изобретении перечислены ниже: атом галогена включает F, CI, Br и I; С3-С7 циклоалкил относится к циклоалкилу, содержащему от 3 до 7 атомов углерода на кольце, и включает (без ограничений) циклопропил, циклобутил, циклопентил, циклогексил и циклогептил; С6-С12 арил относится к ароматической кольцевой группе, содержащей от 6 до 12 атомов углерода на кольце без гетероатома, и включает (без ограничений) фенил и нафтил; 4-7-членная гетероциклическая группа относится к неароматической циклической группе, содержащей от 4 до 7 атомов и по меньшей мере один гетероатом, выбранный из О, N или S на кольце, и включает (без ограничений) азетидинил, тетрагидрофуранил, пиперазинил, морфолинил и пиперидинил; 5-7-членный гетероарил относится к ароматической циклической группе, содержащей от 5 до 7 атомов и по меньшей мере один гетероатом, который выбран из О, N или S на кольце, и включает (без ограничений) тиенил, тиазолил, пиридил, фурил, пирролил, пиразолил, имидазолил, оксазолил, пиримидинил и триазинил. 5-7-членное кольцо относится к кольцу, содержащему от 5 до 7 атомов на кольце с гетероатомом, который выбран из О, N или S, или без гетероатома, и включает 5-7-членный карбоцикл (насыщенное или ненасыщенное кольцо, содержащее только атомы углерода), 5-7-членное гетероарильное кольцо (ароматическое кольцо, содержащее от 5 до 7 атомов и по меньшей мере один гетероатом, который выбран из О, N или S на кольце) и 5-7-членный гетероцикл (неароматическое кольцо, содержащее от 5 до 7 атомов и по меньшей мере один гетероатом, который выбран из О, N или S на кольце), и включает (без ограничений) бензольное кольцо, циклопентеновое кольцо, циклогексеновое кольцо, циклогептеновое кольцо, диоксольное кольцо и тому подобное.
При использовании в настоящем документе термины «арил», «фенил», «фенокси», «гетероарил», «гетероароматическое кольцо» и «гетероцикл» включают замещенные или незамещенные формы, где замещенная форма может включать, например, от 1 до 5 идентичных или различных неводородных заместителей, и репрезентативный заместитель включает (без ограничений) С1-С4 алкил, С3-С4 циклоалкил, атом галогена (фтор, хлор, бром или йод), С1-С4 галогеналкил или их комбинации.
При использовании в настоящем документе термин «прямой или разветвленный С1-С4 алкиламино» включает моно- или дизамещенный амино, и для дизамещенного амино алкильные заместители могут быть идентичными или различными. Репрезентативный пример включает (без ограничений) -NH(СН3), -N(CH3)2, -N(CH3)(C2H5).
В частности, соединения 1-(3-аминопропил)-замещенного циклического амина согласно настоящему изобретению предпочтительно выбраны из любого из соединения 1-соединения 172, полученного в примерах, или их фармацевтически приемлемых солей.
В другом аспекте настоящего изобретения предложен способ получения соединения 1-(3-аминопропил)замещенного циклического амина формулы I. Соединение получают путем использования замещенного пиридилальдегида или замещенного тиофенкарбоксальдегида в качестве исходного вещества посредством ступенчатой реакции Манниха, удаления сульфинила, защиты ВОС, восстановления сложного эфира, окисления, восстановительного аминирования, удаления защиты и реакции конденсации. Способ осуществляют посредством описанного ниже процесса, где R1, R2, R4, R5, R6, X и W являются такими, как определено выше.
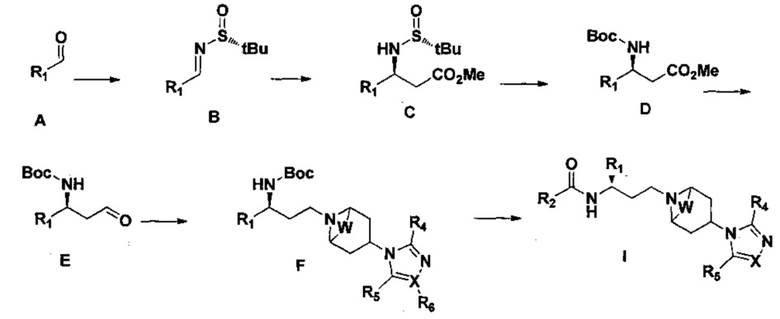
1) Соединение сульфинилимина В получают из соединения А посредством имидирования.
В качестве примера соединение А растворяют в тетрагидрофуране, замещенном тетрагидрофуране, метиленхлориде или диэтиловом эфире и перемешивают при комнатной температуре и последовательно добавляют к раствору (R)-трет-бутилсульфинамида и тетраэтилтитаната. После взаимодействия в течение от 3 до 6 часов под защитой азота добавляют воду и получают фильтрат посредством фильтрования. Соединение сульфинимина В получают путем экстракции органическим растворителем и разделения с помощью колоночной хроматографии.
2) Соединение С получают из соединения сульфинилимина В посредством реакции Манниха.
В качестве примера, N,N-диизопропилэтиламин или триэтиламин растворяют в тетрагидрофуране, замещенном тетрагидрофуране, метиленхлориде или диэтиловом эфире при температуре от -20 до 0°С, добавляют по каплям раствор н-бутиллития в гексане в атмосфере азота. После взаимодействия в течение от 30 до 120 минут смесь охлаждают до -78°С и добавляют метилацетат. После взаимодействия в течение от 30 до 120 минут добавляют триизопропоксид хлортитана. После взаимодействия в течение от 30 до 60 минут добавляют соединение В. После взаимодействия в течение от 3 до 6 часов реакцию гасят насыщенным раствором хлорида аммония. Получают фильтрат посредством фильтрования. Соединение С получают путем экстракции органическим растворителем и разделения колоночной хроматографией.
3) Соединение D получают из соединения С посредством удаления сульфинила и защиты трет-бутилоксикарбонила (ВОС).
В качестве примера, соединение С растворяют в метаноле или этаноле, добавляют раствор кислоты и перемешивают в течение от 2 до 5 часов при комнатной температуре. После концентрирования смесь растворяют в дихлорметане или этилацетате, добавляют основание и ди-трет-бутилдикарбонат и перемешивают в течение 2-5 часов при комнатной температуре. Систему концентрируют, экстрагируют органическим растворителем и разделяют колоночной хроматографией с получением соединения D.
4) Соединение Е получают из соединения D посредством восстановления сложного эфира и окисления.
В качестве одного из примеров, соединение растворяют в тетрагидрофуране, замещенном тетрагидрофуране или диэтиловом эфире при температуре от 0 до 20°С и медленно добавляют по каплям раствор алюмогидрид лития и перемешивают в течение от 2 до 4 часов при комнатной температуре. Реакцию гасят водой, промывают основным раствором и фильтруют. Органическую фазу промывают насыщенным соляным раствором, высушивают и концентрируют. Концентрат растворяют в дихлорметане, добавляют периодинан Десса-Мартина (DMP) и перемешивают в течение от 0,5 до 6 часов. Добавляют насыщенный раствор бикарбоната натрия, и соединение Е получают путем экстракции органическим растворителем и разделением колоночной хроматографией.
5) Соединение F получают из соединения Е и соединения 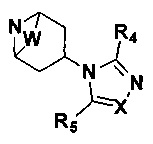 посредством реакции восстановительного аминирования.
посредством реакции восстановительного аминирования.
В качестве примера, соединение Е растворяют в тетрагидрофуране, дихлорметане или 1,2-дихлорэтане, и добавляют 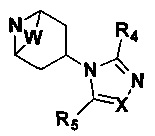 и триацетоксиборгидрид натрия и перемешивают в течение от 8 до 16 часов при комнатной температуре. Добавляют воду, и смесь экстрагируют органическим растворителем и разделяют колоночной хроматографией с получением соединения F.
и триацетоксиборгидрид натрия и перемешивают в течение от 8 до 16 часов при комнатной температуре. Добавляют воду, и смесь экстрагируют органическим растворителем и разделяют колоночной хроматографией с получением соединения F.
6) Соединение F подвергают удалению защиты и реакции конденсации с  с получением соединения I.
с получением соединения I.
В качестве примера, соединение F растворяют в метаноле или этаноле, добавляют раствор кислоты и перемешивают в течение от 2 до 5 часов при комнатной температуре. Реакционную смесь концентрируют и растворяют в N,N-диметилформамиде. Последовательно добавляют основание, 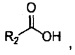 агент конденсации, такой как бензотриазол-1-илокси-трис(диметиламино)фосфония гексафторфосфат (ВОР) или соль гидрохлорид 1-этил-(3-диметиламинопропил)карбодиимида (EDCI) и т.д. и перемешивают при комнатной температуре в течение от 8 до 16 часов. Добавляют воду, и смесь экстрагируют органическим растворителем и разделяют колоночной хроматографией с получением соединения I.
агент конденсации, такой как бензотриазол-1-илокси-трис(диметиламино)фосфония гексафторфосфат (ВОР) или соль гидрохлорид 1-этил-(3-диметиламинопропил)карбодиимида (EDCI) и т.д. и перемешивают при комнатной температуре в течение от 8 до 16 часов. Добавляют воду, и смесь экстрагируют органическим растворителем и разделяют колоночной хроматографией с получением соединения I.
В описанном выше способе кислота, используемая на каждой стадии, может представлять собой органическую или неорганическую кислоту, органическая кислота может представлять собой уксусную кислоту, трифторуксусную кислоту, муравьиную кислоту, а неорганическая кислота может представлять собой хлорид водорода, серную кислоту или фосфорную кислоту; основание может представлять собой неорганические или органические основания, где неорганическое основание выбрано из группы, состоящей из карбоната натрия, карбоната калия, карбоната цезия, бикарбоната натрия, фосфата калия, однозамещенного фосфата калия, гидроксида натрия, гидроксида лития и гидроксида калия, а органическое основание выбрано из группы, состоящей из триэтиламина, пиридина, диазабицикло (DBU) и N,N-диизопропилэтиламина (DIPEA); органический растворитель может быть выбран группы, состоящей из тетрагидрофурана (ТГФ), ацетонитрила, ацетона, 1,4-диоксана, спиртов, диэтилового эфира, N,N-диметилформамида, диметилового эфира этиленгликоля, N,N-диметилформамида (ДМФ) и диметилсульфоксида (ДМСО); и агент конденсации, используемый на стадии 6), может представлять собой гидрохлорид 1-этил-(3-диметиламинопропил)карбодиимида (EDCI), бензотриазол-1-илокси-трис(диметиламино)фосфония гексафторфосфат (ВОР), 2-(7-азобензотриазол)-N,N,N',N'-тетраметилурония гексафторфосфат (HATU) или N,N'-дициклогексилкарбодиимид (DCC) и тому подобное.
В другом аспекте изобретения предложена фармацевтическая композиция, содержащая соединения 1-(3-аминопропил)-замещенного циклического амина согласно настоящему изобретению, его фармацевтически приемлемую соль, энантиомер, диастереоизомер, рацемат или смесь и необязательно фармацевтически приемлемый носитель. Фармацевтическую композицию может применяться в терапии in vivo и обладает биосовместимостью. Фармацевтическая композиция может быть получена в различных формах в зависимости от различных путей введения. Фармацевтическую композицию по настоящему изобретению можно применять в качестве антагониста CCR5 для лечения инфекции ВИЧ.
Фармацевтическая композиция по настоящему изобретению может быть представлена в различных формах, таких как таблетка, капсула, порошок, сироп, раствор, суспензия, аэрозоль и т.д., и может содержаться в подходящем твердом или жидком носителе или разбавителе и в подходящем дезинфицирующем контейнере для инъекции или инфузии. Фармацевтическая композиция может также содержать ароматизатор, и т.д., и желаемая доля соединения формулы I в качестве активного ингредиента составляет 65% или более в расчете на общую массу, а доля остальных ингредиентов составляет от 0,5 до 40%, предпочтительно от 1 до 20% или предпочтительно от 1 до 10% фармацевтически приемлемого носителя, разбавителя или растворителя, или раствора соли.
Соединение согласно настоящему изобретению, как описано выше, можно применять клинически для млекопитающих, включая людей и животных, через полость рта, нос, кожу, легкое или желудочно-кишечный тракт и т.д., и более предпочтительно через полость рта. Суточная доза предпочтительно составляет от 0,01 до 200 мг/кг массы тела при однократном введении или от 0,01 до 100 мг/кг массы тела в разделенных дозах. Независимо от способа введения оптимальную дозу для индивида следует определять на основании конкретного лечения. В обычных условиях сначала вводят небольшую дозу, и дозу постепенно повышают до нахождения наиболее подходящей дозы.
В другом аспекте изобретения предложено применение соединения 1-(3-аминопропил)-замещенного циклического амина согласно изобретению, его фармацевтически приемлемой соли, энантиомера, диастереоизомера, рацемата или их смеси для получения антагониста CCR5.
В следующем аспекте настоящего изобретения предложено применение соединения 1-(3-аминопропил)-замещенного циклического амина согласно настоящему изобретению, его фармацевтически приемлемой соли, энантиомера, диастереоизомера, рацемата или их смеси для получения лекарственного средства для лечения CCRS-опосредованного заболевания.
В следующем аспекте настоящего изобретения предложено применение соединения 1-(3-аминопропил)-замещенного циклического амина согласно настоящему изобретению, его фармацевтически приемлемой соли, энантиомера, диастереоизомера, рацемата или их смеси для получения лекарственного средства для лечения инфекции ВИЧ.
В следующем аспекте настоящего изобретения предложен способ лечения заболевания, опосредованного CCR5, включающий введение соединения 1-(3-аминопропил)-замещенного циклического амина по настоящему изобретению, его фармацевтически приемлемой соли, энантиомера, диастереоизомера, рацемата или их смеси или фармацевтической композиции, содержащей одно из соединений 1-(3-аминопропил)-замещенного циклического амина согласно настоящему изобретению, его фармацевтически приемлемую соль, энантиомер, диастереоизомер, рацемат или их смесь, пациенту, нуждающемуся в этом. В одном воплощении изобретения заболевание, опосредованное CCR5, представляет собой инфекцию ВИЧ.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение будет дополнительно проиллюстрировано следующими примерами. Эти примеры предназначены для иллюстрации настоящего изобретения, но никоим образом не ограничивают изобретение. Если не указано иное, все параметры, а также остальные описания в примерах приведены на основе массы.
Для экспериментальных способов в приведенных ниже примерах без конкретных условий их выполняют в обычных условиях, таких как условия, описанные в кн. Sambrook et al., Molecular Cloning: A Laboratory Manual, New York: Cold Spring Harbor Laboratory Press, 1989, или согласно инструкциям производителя.
Данные измерения проб получали с помощью следующих приборов. ЯМР измеряли с помощью спектрометров GEMINI-300, Bruker АМХ-400 и INVOA-600 ядерно-магнитного резонанса, где ТМС (тетраметилсилан) использовали в качестве внутреннего стандарта, единица химического сдвига представляла собой ppm, и единица константы спин-спинового взаимодействия представляла собой Гц. Масс-спектры снимали с помощью масс-спектрометра Finnigan МАТ-711, МАТ-95 и LCQ-DECA и масс-спектрометра lonSpec4.7 Тесла.
Колоночную хроматографию проводили на силикагеле 200-300 меш (Qingdao Marine Chemical Plant). Пластина для тонкослойной хроматографии (ТСХ) на силикагеле представляет собой пластину для тонкослойной хроматографии заводского изготовления HSGF-254, производимую компанией Yantai Chemical Plant. Диапазон температуры кипения петролейного эфира составлял от 60 до 90°С. Для проявления использовали ультрафиолетовый (УФ) свет и йодный цилиндр. Если не указано иное, традиционные реагенты и фармацевтические препараты, используемые в приведенных ниже примерах, приобретали у компании Sinopharm. Реагенты и растворители, используемые в экспериментах, обрабатывают в соответствии с конкретными условиями.
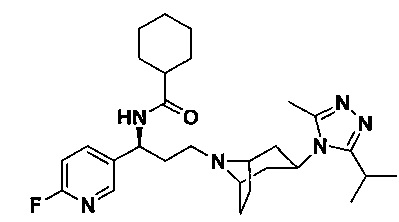
Пример 1. Синтез соединения 1
4,4-Дифтор-N-[3-[4-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(тиофен-2-ил)пропил]циклогексан-1-карбоксамид
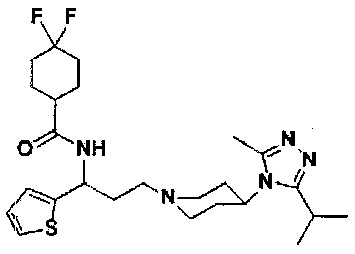
Путь синтеза:
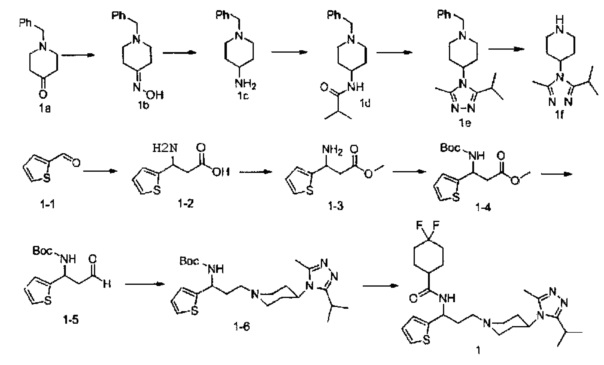
Синтез соединения 1b:
Соединение 1а (1,89 г, 10 ммоль) растворяли в 50 мл абсолютного этанола и последовательно добавляли карбонат калия (2,76 г, 20 ммоль) и гидрохлорид гидроксиламина (1,04 г, 15 ммоль) и перемешивали при комнатной температуре в течение 6 часов. После концентрирования смеси добавляли воду. Затем смесь экстрагировали этилацетатом, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия и концентрировали с получением белого твердого вещества 1b (2,04 г, выход 100%), МС: 205,0 [М+Н]+.
Синтез соединения 1с:
Соединение 1b (2,04 г, 10 ммоль) растворяли в 50 мл безводного н-амилового спирта и перемешивали при температуре образования флегмы, к этому раствору порциями добавляли натрий (2,76 г, 120 ммоль). Реакцию поддерживали в течение 2,5 часов. Затем реакционную смесь охлаждали, доводили 1 М соляной кислотой до рН 12 и экстрагировали водой. Объединенную водную фазу доводили 1 М гидроксидом натрия до рН 8. Затем смесь экстрагировали этилацетатом, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия и концентрировали с получением бесцветной жидкости 1 с (1,71 г, выход 90%), МС: 191,0 [М+Н]+.
Синтез соединения 1d:
Соединение 1с (1,90 г, 10 ммоль) растворяли в 30 мл дихлорметана, добавляли карбонат натрия (1,59 г, 15 ммоль) и перемешивали при комнатной температуре. Медленно добавляли по каплям изобутирилхлорид (1,6 г, 15 ммоль), и реакцию поддерживали в течение 2 часов. Затем реакционную смесь экстрагировали дихлорметаном, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия и концентрировали с получением белого твердого вещества 1d (2,60 г, выход 100%), МС: 191,0 [М+Н]+.
Синтез соединения 1е:
Соединение 1d (1,30 г, 5 ммоль) растворяли в 20 мл дихлорметана и медленно добавляли пентахлорид фосфора (1,248 г, 5 ммоль) в ледяной бане и перемешивали в течение 2 часов при комнатной температуре. Затем добавляли 5 мл трет-амилового спирта и гидразид уксусной кислоты (0,74 г, 10 ммоль) и перемешивали в течение 16 часов при комнатной температуре. Смесь концентрировали и повторно растворяли в 10 мл толуола и 10 мл диоксана. Затем 32 мг пара-толуолсульфоновой кислоты. Реакционную смесь кипятили с обратным холодильником в течение 5 часов и добавляли воду. Смесь доводили до рН 8, экстрагировали дихлорметаном, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия и разделяли колоночной хроматографией с получением белого твердого вещества 1е (0,99 г, выход 67%), МС: 299,0 [М+Н]+.
Синтез соединения 1f:
Соединение 1e (0,507 г, 1,7 ммоль) растворяли в 10 мл метанола и добавляли 20% гидроксид палладия (0,14 г, 0,7 ммоль) и формиат аммония (0,535 г, 8,5 ммоль). Реакционную смесь перемешивали при температуре образования флегмы в течение 2,5 часов, а затем фильтровали. Реакционную смесь концентрировали и разделяли колоночной хроматографией с получением белого твердого вещества 1f (0,336 г, выход 95%), МС: 209,0 [М+Н]+.
Синтез соединения 1-2:
Соединение 1-1 (2,00 г, 17,83 ммоль) растворяли в 5,5 мл этанола и последовательно добавляли к нему ацетат аммония (2,74 г, 35,58 ммоль) и малоновую кислоту (1,85 г, 17,78 ммоль). Реакционную смесь держали при перемешивании и кипятили с обратным холодильником в течение 7 часов. В прозрачной реакционной смеси появлялась белая мутность. Затем реакционную смесь фильтровали и промывали горячим этанолом (3×10 мл) с получением белого твердого вещества 1-2 (2,20 г, выход 72%), МС: 172,0 [М+Н]+.
Синтез соединения 1-3:
При комнатной температуре медленно добавляли тионилхлорид (4,0 мл) к раствору 1-1 (8,55 г, 50,0 ммоль) в безводном метаноле (30,0 мл) при перемешивании, и реакционную смесь перемешивали при температуре образования флегмы в течение 16 часов. Анализ показал, что реакция завершена. Затем реакционную смесь концентрировали, и к остатку добавляли насыщенный раствор карбоната калия для доведения рН до 8. Затем смесь экстрагировали этилацетатом, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия и концентрировали с получением белого твердого вещества 1-3 (8,78 г, выход 95%), МС: 185,9 [М+Н]+.
Синтез соединения 1-4:
Соединение 1-3 (6,72 г, 36,4 ммоль) растворяли в 50 мл метанола, последовательно добавляли триэтиламин (7,6 мл, 54,6 ммоль) и ди-трет-бутилдикарбонат (11,9 г, 54,6 ммоль) и перемешивали при комнатной температуре в течение 3 часов. Систему концентрировали, экстрагировали этилацетатом, промывали насыщенным раствором бикарбоната натрия и соляным раствором, высушивали над безводным сульфатом натрия и концентрировали с получением бесцветного маслянистого продукта 1-4 (10,16 г, выход 98%), МС: 286,1 [М+Н]+.
Синтез соединения 1-5:
В ледяной бане соединение 1-4 (285 мг, 1 ммоль) растворяли в 5 мл безводного тетрагидрофурана и медленно добавляли по каплям 1,0 М раствор алюмогидрида лития (1,1 мл, 1,1 ммоль). Смесь нагревали до комнатной температуры и перемешивали в течение 2 часов. Реакционную смесь гасили водой, и смесь промывали 15% водным раствором гидроксида натрия и фильтровали. Затем органическую фазу промывали соляным раствором, высушивали над безводным сульфатом натрия и концентрировали с получением бесцветной маслянистой жидкости. Эту бесцветную маслянистую жидкость растворяли в дихлорметане (5 мл), добавляли периодинан Десса-Мартина (466,4 мг, 1,1 ммоль) и перемешивали в течение 2 часов. Затем добавляли насыщенный раствор бикарбоната натрия, и смесь экстрагировали дихлорметаном, последовательно промывали насыщенным раствором бикарбоната натрия и насыщенным соляным раствором, высушивали над безводным сульфатом натрия, концентрировали и разделяли колоночной хроматографией с получением бесцветной маслянистой жидкости 1-5 (156 мг, выход 61%), МС: 256,1 [М+Н]+.
Синтез соединения 1-6:
Соединение 1-5 (512 мг, 2 ммоль) растворяли в 5 мл дихлорметана, последовательно добавляли соединение 1f (468 мг, 2 ммоль) и триацетоксиборгидрид натрия (466 мг, 2,2 ммоль) и перемешивали в течение 12 часов при комнатной температуре. Добавляли воду, и смесь экстрагировали дихлорметаном, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия, концентрировали и разделяли колоночной хроматографией с получением бледно-желтой маслянистой жидкости 1-6 (664 мг, выход 70%), МС: 474,3 [М+Н]+.
Синтез соединения 1:
Соединение 1-6 (47,4 мг, 0,1 ммоль) растворяли в 1 мл метанола, добавляли 1 мл раствора HCl в диоксане (4 М) и перемешивали в течение 2 часов при комнатной температуре. Реакционную смесь концентрировали, растворяли в 1 мл N,N-диметилформамида с последующим добавлением триэтиламина (28 мкл, 0,2 ммоль), 4,4-дифтор-циклогексанкарбоновой кислоты (18 мг, 0,11 ммоль), соли бензотриазол-1-илокси-трис(диметиламино)фосфония гексафторфосфата (ВОР) (46,4 мг, 0,11 ммоль) и перемешивали в течение 12 часов при комнатной температуре. Добавляли воду, затем смесь экстрагировали этилацетатом, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия, концентрировали и разделяли колоночной хроматографией с получением белого твердого вещества 1 (25,6 мг, выход 52%), МС: 494,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,28 (t, 1Н), 7,11 (d, 1Н), 6,97 (d, 1Н), 5,17 (m,1Н), 3,90 (m, 1Н), 3,00 (m, 1Н), 2,50 (s, 3Н), 2,43 (m, 2Н), 2,26-1,99 (m, 10Н), 1,99-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 2. Синтез соединения 2
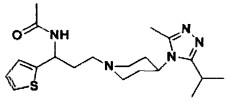
N-[3-[4-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(тиофен-2-ил)пропил]ацетамид
В соответствии со способом синтеза примера 1, уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 1 с получением соединения 2. МС: 390,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,26 (t, 1Н), 7,15 (d, 1Н), 6,99 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,10 (m, 1Н), 2,51 (s, 3Н), 2,43 (m, 2Н), 2,20-1,69 (m, 14Н), 1,35 (d, 6Н).
Пример 3. Синтез соединения 3
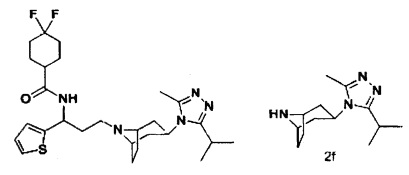
4,4-Дифтор-N-[3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]циклогексан-1-карбоксамид
Синтез соединения 2f
В соответствии со способом синтеза соединения 1f, в примере 1 N-бензилтропинон использовали вместо 1а в примере 1 с получением соединения 2f.
Синтез соединения 3
В соответствии со способом синтеза примера 1 соединение 2f использовали вместо 1f в примере 1 с получением соединения 3, МС: 520,3 [М+Н]+.1Н-ЯМР (400 Гц, CDCl3): δ 7,27 (t, 1Н), 7,14 (d, 1Н), 6,95 (d, 1Н), 5,14 (m, 1Н), 3,91 (m, 1Н), 3,03 (m, 1Н), 2,52 (s, 3H), 2,40 (m, 2Н), 2,27-1,93 (m, 12Н), 1,93-1,62 (m, 9Н), 1,32 (d, 6H).
Пример 4. Синтез соединения 4
N-[3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1] октан-8-ил]-1-(тиофен-2-ил)пропил]ацетамид
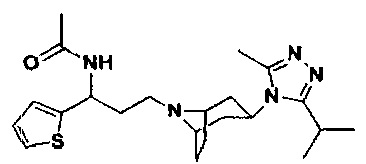
В соответствии со способом синтеза примера 1, уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 1, и соединение 2f использовали вместо 1f в примере 1 с получением соединения 4, МС: 416,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,23 (t, 1Н), 7,15 (d, 1Н), 6,99 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,03 (m, 1Н), 2,54 (s, 3H), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6H).
Пример 5. Синтез соединения 5
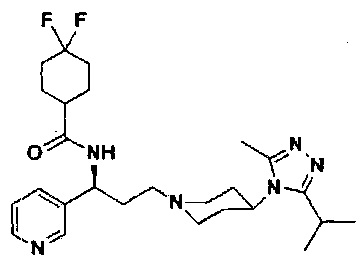
4,4-Дифтор-N-[(1S)-3-[4-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(пиридин-3-ил)пропил]циклогексан-1-карбоксамид
Путь синтеза:
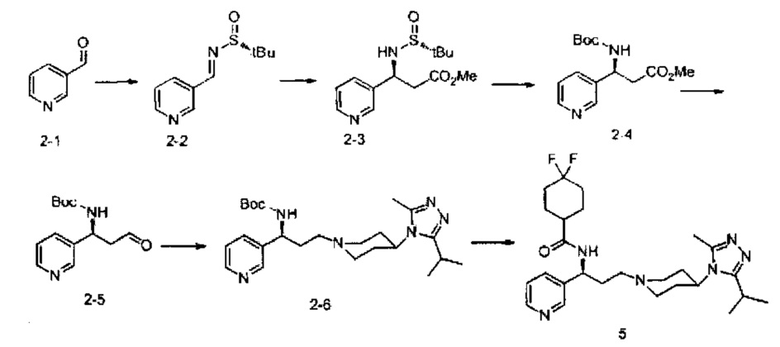
Синтез соединения 2-2:
Соединение 2-1 (1,07 г, 10 ммоль) растворяли в тетрагидрофуране (20 мл) и перемешивали при комнатной температуре, и к этому раствору последовательно добавляли (R)-трет-бутил сульфинамид (1,33 г, 11 ммоль) и тетраэтилтитанат (4,56 г, 20 ммоль). В атмосфере азота реакцию проводили в течение 3 часов. Затем добавляли воду, смесь фильтровали, и фильтрат экстрагировали этилацетатом, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия, концентрировали и разделяли колоночной хроматографией с получением бесцветной жидкости 2-2 (1,94 г, выход 92%), МС: 211,2 [М+Н]+.
Синтез соединения 2-3:
При 0°С N,N-диизопропиламин (1,13 мл, 8 ммоль) растворяли в 10 мл тетрагидрофурана и медленно добавляли по каплям 2,4 М раствор н-бутиллития (3,3 мл, 8 ммоль) в атмосфере азота. После взаимодействия в течение 30 минут смесь охлаждали до -78°С. Добавляли метилацетат (0,58 г, 8 ммоль) и подвергали взаимодействию в течение 45 минут. Добавляли 2 М раствор хлорида триизопропоксида титана (8 мл, 16 ммоль) и подвергали взаимодействию в течение 30 минут. Затем добавляли соединение 2-2 (0,84 г, 4 ммоль) и подвергали взаимодействию в течение 3 часов. Реакционную смесь гасили насыщенным раствором хлорида аммония, смесь фильтровали. Фильтрат экстрагировали этилацетатом, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия, концентрировали и разделяли колоночной хроматографией с получением бесцветной жидкости 2-3 (0,87 г, выход 74%), МС: 286,2 [М+Н]+.
Синтез соединения 2-4:
Соединение 2-3 (2,85 г, 10 ммоль) растворяли в 20 мл метанола, добавляли 10 мл 4 М HCl в диоксане и перемешивали в течение 2 часов при комнатной температуре. Реакционную смесь концентрировали, а затем последовательно добавляли триэтиламин (2,8 мл, 20 ммоль) и ди-трет-бутилд и карбонат (3,26 г, 15 ммоль) и перемешивали при комнатной температуре в течение 3 часов. Систему концентрировали, экстрагировали этилацетатом, промывали насыщенным раствором бикарбоната натрия и насыщенным соляным раствором, высушивали над безводным сульфатом натрия, концентрировали и разделяли колоночной хроматографией с получением продукта 2-4 (2,43 г, выход 87%) в виде бесцветного масла, МС: 281,1 [М+Н]+.
Синтез соединения 2-5:
В ледяной бане соединение 2-4 (280 мг, 1 ммоль) растворяли в 5 мл безводного тетрагидрофурана, медленно добавляли по каплям 1,0 М раствор алюмогидрида лития (1,1 мл, 1,1 ммоль), а затем смесь подогревали до комнатной температуры и перемешивали в течение 2 часов. Реакционную смесь гасили водой, промывали 15% водным раствором гидроксида натрия и фильтровали. Органическую фазу промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия и концентрировали с получением бесцветной маслянистой жидкости. Эту бесцветную маслянистую жидкость растворяли в дихлорметане (5 мл), а затем добавляли периодинан Десса-Мартина (466,4 мг, 1,1 ммоль) и перемешивали в течение 2 часов. Затем добавляли насыщенный раствор бикарбоната натрия, и смесь экстрагировали дихлорметаном, последовательно промывали насыщенным раствором бикарбоната натрия и насыщенным соляным раствором, высушивали над безводным сульфатом натрия, концентрировали и разделяли колоночной хроматографией с получением бесцветной маслянистой жидкости 2-5 (158 мг, выход 63%), МС: 251,1 [М+Н]+.
Синтез соединения 2-6:
Соединение 2-5 (502 мг, 2 ммоль) растворяли в 5 мл дихлорметана и последовательно добавляли соединение 1f (468 мг, 2 ммоль) и триацетоксиборгидрид натрия (466 мг, 2,2 ммоль) и перемешивали в течение 12 часов при комнатной температуре. Добавляли воду, а затем смесь экстрагировали дихлорметаном, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия, концентрировали и разделяли колоночной хроматографией с получением бледно-желтой маслянистой жидкости 2-6 (686 мг, выход 71%), МС: 469,3 [М+Н]+.
Синтез соединения 5:
Соединение 2-6 (46,8 мг, 0,1 ммоль) растворяли в 1 мл метанола, а затем добавляли 1 мл 4 М HCl в диоксане и перемешивали в течение 2 часов при комнатной температуре. Смесь концентрировали, а затем растворяли в 1 мл N,N-диметилформамида, после чего последовательно добавляли триэтиламин (28 мкл, 0,2 ммоль), 4,4-дифтор-циклогексанкарбоновую кислоту (18 мг, 0,11 ммоль), соль гексафторфосфат бензотриазол-1-илокси-трис(диметиламино)фосфония (ВОР) (46,4 мг, 0,11 ммоль). Смесь перемешивали в течение 12 часов при комнатной температуре, а затем добавляли воду. Смесь экстрагировали этилацетатом, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия, концентрировали и разделяли колоночной хроматографией (ДХМ:СН3ОН=8:1) с получением белого твердого вещества 5 (27,7 мг, выход 57%), МС: 89,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,58 (s, 1Н), 8,38 (d, 1Н), 7,81 (d, 1Н), 7,37 (t, 1Н), 5,17 (m, 1Н), 3,90 (m, 1Н), 3,00 (m, 1Н), 2,50 (s, 3H), 2,43 (m, 2Н), 2,26-1,99 (m, 10H), 1,99-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 6. Синтез соединения 6
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(пиридин-3-ил)пропил]циклогексан-1-карбокса мид
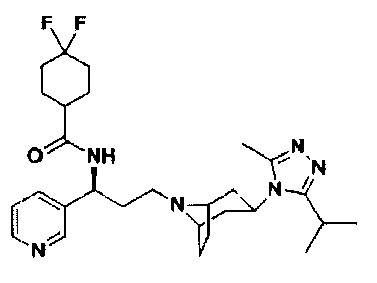
В соответствии со способом синтеза примера 5, соединение 2f использовали вместо 1f в примере 5 с получением соединения 6, МС: 514.9[М+Н]+. 1Н-ЯМР(400 Гц, CDCl3): δ 8,57 (s, 1Н), 8,39 (d, 1Н), 7,80 (d, 1Н), 7,37 (t, 1Н), 5,17 (m,1H), 3,90 (m, 1Н), 3,00 (m, 1Н), 2,50 (s, 3H), 2,43 (m,2H), 2,27-1,96 (m,12H), 1,96-1,60 (m, 9H), 1,34 (d, 6H).
Пример 7. Синтез соединения 7
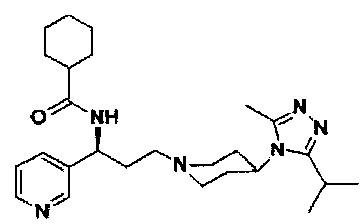
N-[(1S)-3-[4-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(пиридин-3-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 7, МС: 453,0 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,59 (s, 1Н), 8,37 (d, 1Н), 7,80 (d, 1Н), 7,35 (t, 1Н), 5,17 (m, 1Н), 3,90 (m, 1Н), 3,00 (m, 1Н), 2,50 (s, 3H), 2,43 (m, 2Н), 2,26-1,99 (m, 11Н), 1,99-1,61 (m, 10Н), 1,34 (d, 6H).
Пример 8. Синтез соединения 8
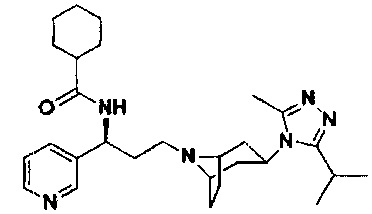
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(пиридин-3-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 8, МС: 479,0 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,59 (s, 1Н), 8,48 (d, 1Н), 7,86 (d, 1Н), 7,38 (t, 1Н), 5,17 (m, 1Н), 3,90 (m, 1Н), 3,00 (m, 1Н), 2,50 (s, 3H), 2,43 (m, 2Н), 2,27-1,96 (m, 12Н), 1,96-1,60 (m, 11Н), 1,34 (d, 6Н).
Пример 9. Синтез соединения 9
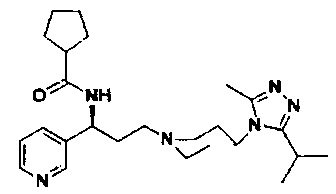
N-[(1S)-3-[4-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(пиридин-3-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5 циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 9, МС: 439,0 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,59 (s, 1Н), 8,37 (d, 1Н), 7,80 (d, 1Н), 7,35 (t, 1Н), 5,18 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,53 (s, 3H), 2,40 (m, 2Н), 2,25-1,97 (m, 10Н), 1,97-1,60 (m, 9Н), 1,33 (d, 6H).
Пример 10. Синтез соединения 10
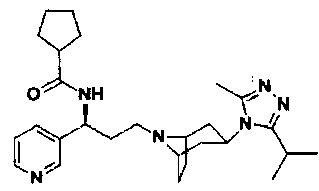
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(пиридин-3-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 10, МС: 464,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,59 (s, 1Н), 8,48 (d, 1Н), 7,86 (d, 1Н), 7,38 (t, 1Н), 5,16 (m, 1Н), 3,93 (m, 1Н), 3,07 (m, 1Н), 2,45 (s, 3H), 2,42 (m, 2Н), 2,27-1,96 (m, 12Н), 1,96-1,61 (m, 9Н), 1,35 (d, 6Н).
Пример 11. Синтез соединения 11
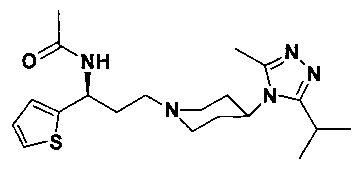
N-[(1S)-3-[4-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(тиофен-2-ил)пропил]ацетамид
В соответствии со способом синтеза примера 5 соединение 1-1 использовали вместо соединения 2-1 в примере 5, и уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 11, МС: 390,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,26 (t, 1Н), 7,15 (d, 1Н), 6,99 (d, 1Н), 5,21 (m, 1H), 3,95 (m, 1Н), 3,10 (m, 1Н), 2,51 (s, 3H), 2,43 (m,2H), 2,20-1,69 (m, 14H), 1,35 (d, 6H).
Пример 12. Синтез соединения 12
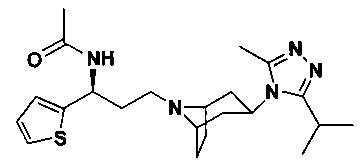
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]ацетамид
В соответствии со способом синтеза примера 5 соединение 1-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 12, МС: 416,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,23 (t, 1Н), 7,15 (d, 1Н), 6,99 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,03 (m, 1Н), 2,54 (s, 3H), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 13. Синтез соединения 13
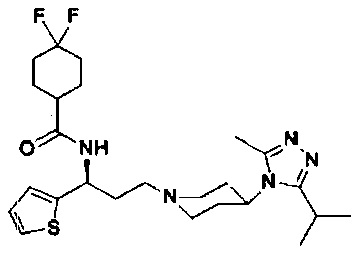
4,4-Дифтор-N-[(1S)-3-[4-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(тиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 1-1 использовали вместо соединения 2-1 в примере 5 с получением соединения 13, МС: 493,9 [M+H]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,27 (t, 1Н), 7,13 (d, 1Н), 6,95 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54(s, 3H), 2,43 (m, 2Н), 2,27-1,95 (m, 10Н), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 14. Синтез соединения 14
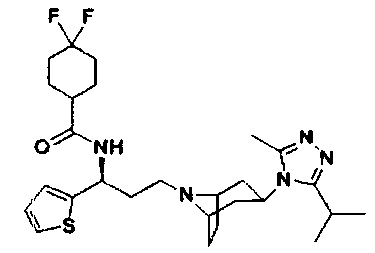
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 1-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 14, МС: 520,0 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,27 (t, 1Н), 7,14 (d, 1Н), 6,95 (d, 1Н), 5,14 (m, 1Н), 3,91 (m, 1Н), 3,03 (m, 1Н), 2,52 (s, 3H), 2,40 (m, 2Н), 2,27-1,93 (m, 12Н), 1,93-1,62 (m, 9Н), 1,32 (d, 6Н).
Пример 15. Синтез соединения 15
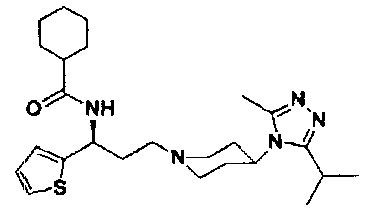
N-[(1S)-3-[4-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(тиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 1-1 использовали вместо соединения 2-1 в примере 5, и циклогексанкарбоновую кислоты использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 15, МС: 457,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,28 (t, 1Н), 7,13 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26-1,93 (m, 12Н), 1,93-1,61 (m, 9Н), 1,36 (d, 6Н).
Пример 16. Синтез соединения 16
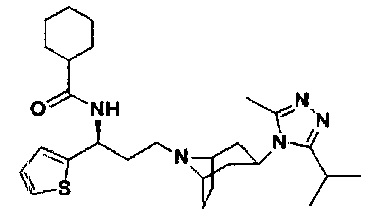
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-[(тиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 1-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 16, МС: 483,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,28 (t, 1Н), 7,13 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10Н), 1,36 (d, 6Н).
Пример 17. Синтез соединения 17
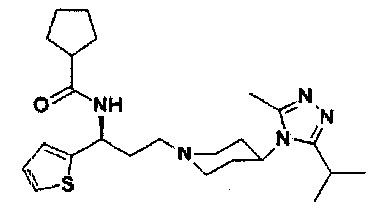
N-[(1S)-3-[4-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(тиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 1-1 использовали вместо соединения 2-1 в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 17, МС: 443,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,27 (t, 1Н), 7,13 (d, 1Н), 6,95 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,01 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,29-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,33 (d, 6Н).
Пример 18. Синтез соединения 18
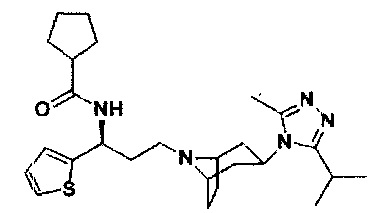
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 1-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 18, МС: 469,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,25 (t, 1Н), 7,13 (d, 1Н), 6,97 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 19. Синтез соединения 19

4-Этил-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 1-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и 4-метилциклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 19, МС: 511,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,25 (t, 1Н), 7,15 (d, 1Н), 6,97 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,29-1,93 (m, 15Н), 1,93-1,61 (m, 12Н), 1,33 (d, 6Н).
Пример 20. Синтез соединения 20
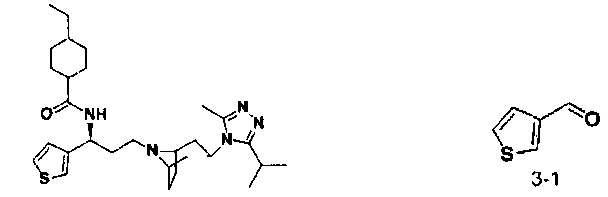
4-Этил-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-3-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 3-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и 4-метилциклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 20, МС: 511,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,25 (t, 1Н), 7,15 (s, 1Н), 6,97 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,29-1,93 (m, 15Н), 1,93-1,61 (m, 12Н), 1,33 (d, 6H).
Пример 21. Синтез соединения 21
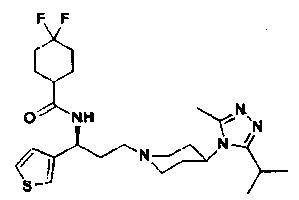
4,4-Дифтор-N-[(1S)-3-[4-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(тиофен-3-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 3-1 использовали вместо соединения 2-1 в примере 5 с получением соединения 21, МС: 493,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,26 (t, 1Н), 7,15 (s, 1Н), 6,97 (d, 1Н), 5,17 (m, 1Н), 3,94 (m, 1Н), 3,05 (m, 1Н), 2,53 (s, 3H), 2,43 (m, 2Н), 2,25-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 22. Синтез соединения 22
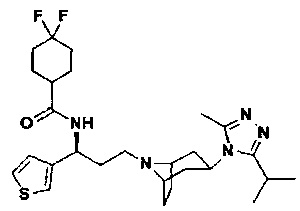
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-3-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 3-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 22, МС: 520,0 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,26 (d, 1Н), 7,14 (s, 1Н), 6,95 (d, 1Н), 5,14 (m, 1Н), 3,91 (m, 1Н), 3,03 (m, 1Н), 2,52 (s, 3H), 2,40 (m, 2Н), 2,28-1,93 (m, 12Н), 1,93-1,65 (m, 9Н), 1,35 (d, 6Н).
Пример 23. Синтез соединения 23
N-[(1S)-3-[4-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(тиофен-3-ил)пропил]циклогексан-1-карбоксамид

В соответствии со способом синтеза примера 5 соединение 3-1 использовали вместо соединения 2-1 в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 23, МС: 457,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7.27 (d, 1Н), 7,13 (s, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,05 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,25-1,93 (m, 12Н), 1,93-1,61 (m, 9Н), 1,35 (d, 6Н).
Пример 24. Синтез соединения 24
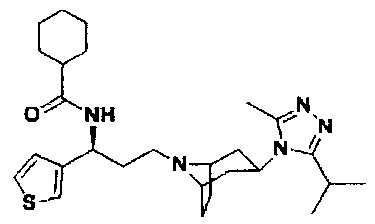
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-[(тиофен-3-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 3-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 24, МС: 483,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,23 (d, 1Н), 7,12 (s, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,34 (d, 6Н).
Пример 25. Синтез соединения 25
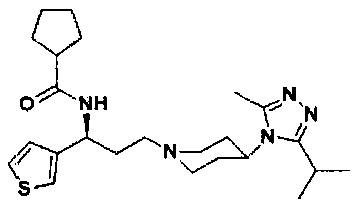
N-[(1S)-3-[4-(3-изоиропил-5-метил-4Н-1,2,4-триазол-4-ил)-пиперидин-1-ил]-1-(тиофен-3-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 3-1 использовали вместо соединения 2-1 в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 25, МС: 443,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,27 (d, 1Н), 7,13 (s, 1Н), 6,95 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,03 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,33 (d, 6Н).
Пример 26. Синтез соединения 26
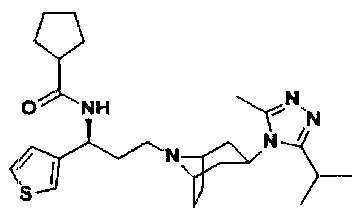
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-3-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 3-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 26, МС: 469,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,25 (d, 1Н), 7,13 (s, 1H), 6,97 (d, 1H), 5,19 (m, 1H), 3,91 (m, 1H), 3,02 (m, 1H), 2,54 (s, 3H), 2,43 (m, 2H), 2,25-1,93 (m, 11H), 1,93-1,61 (m, 10H), 1,35 (d, 6H).
Пример 27. Синтез соединения 27

4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(бензотиофен-3-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 4-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 27, МС: 570,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,36 (d, 1Н), 57,26 (d, 2Н), 7,14 (s, 1Н), 6,95 (d, 1Н), 5,14 (m, 1Н), 3,91 (m, 1Н), 3,03 (m, 1Н), 2,52 (s, 3H), 2,40 (m, 2Н), 2,28-1,93 (m, 12Н), 1,93-1,65 (m, 9Н), 1,35 (d, 6Н).
Пример 28. Синтез соединения 28
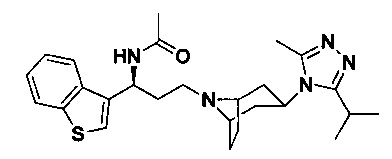
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(бензотиофен-3-ил)пропил]ацетамид
В соответствии со способом синтеза примера 5, соединение 5-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 28, МС: 520,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,35 (d, 1Н), 5 7,23 (t, 2Н), 7,15 (d, 1Н), 6,99 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,03 (m, 1Н), 2,54 (s, 3H), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 29. Синтез соединения 29
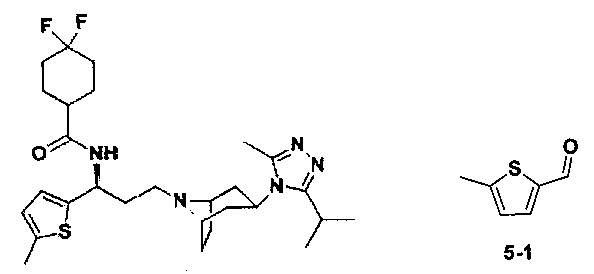
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 5-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 29, МС: 534,2 [М+Н]+. δ 7,27 (d, 1Н), 7,20 (d, 1Н), 5,14 (m,1Н), 3,91 (m, 1Н), 3,03 (m, 1Н), 2,52 (s, 3H), 2,40 (m, 5Н), 2,27-1,93 (m, 12Н), 1,93-1,62 (m, 9Н), 1,32 (d, 6Н).
Пример 30. Синтез соединения 30
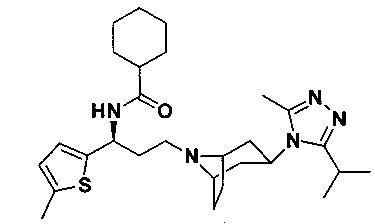
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 5-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 30, МС: 498,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,28 (d, 1Н), 7,21 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10Н), 1,36 (d, 6Н).
Пример 31. Синтез соединения 31
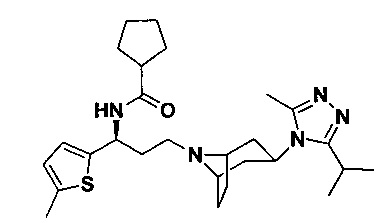
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метилтиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 5-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 31, МС: 484,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,25 (d, 1Н), 7,17 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 32. Синтез соединения 32
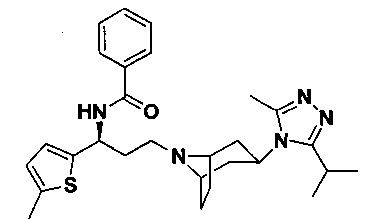
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метилтиофен-2-ил)пропил]бензамид
В соответствии со способом синтеза примера 5, соединение 5-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и бензойную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 32, МС: 492,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,70 (d, 2Н), 7,45 (d, 3H), 7,23 (t, 1Н), 7,15 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,03 (m, 1Н), 2,54 (s, 3H), 2,40 (m, 5Н), 2,25-1,67 (m, 11Н), 1,32 (d, 6Н).
Пример 33. Синтез соединения 33
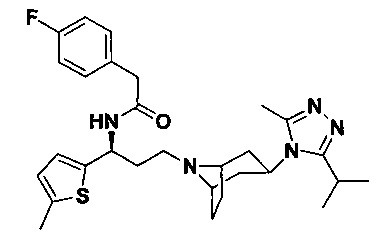
4-Фтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метилтиофен-2-ил)пропил]фенилацетамид
В соответствии со способом синтеза примера 5, соединение 5-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и лара-фторфенилуксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 33, МС: 524,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,50 (d, 2Н), 7,35 (d, 2Н), 7,23 (t, 1Н), 7,15 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,37 (s, 2Н), 3,03 (m, 1Н), 2,54 (s, 3H), 2,40 (m, 5Н), 2,25-1,67 (m, 11Н), 1,32 (d, 6Н).
Пример 34. Синтез соединения 34
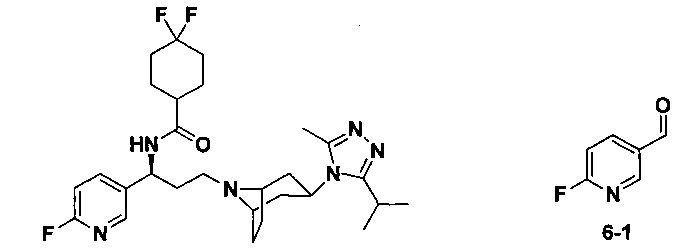
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(6-фторпиридин-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 6-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 34, МС: 533,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,19 (d, 1Н), 7,80 (d, 1Н), 7,37 (t, 1Н), 5,17 (m, 1Н), 3,90 (m, 1Н), 3,00 (m, 1Н), 2,50 (s, 3H), 2,43 (m, 2Н), 2,27-1,96 (m, 12Н), 1,96-1,60 (m, 9Н), 1,34 (d, 6Н).
Пример 35. Синтез соединения 35
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(6-фторпиридин-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 6-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 35, МС: 497,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,08 (d, 1Н), 7,66 (d, 1Н), 7,31 (t, 1Н), 5,17 (m, 1Н), 3,90 (m, 1Н), 3,00 (m, 1Н), 2,50 (s, 3H), 2,43 (m, 2Н), 2,27-1,96 (m, 12Н), 1,96-1,60 (m, 11H), 1,34 (d, 6H).
Пример 36. Синтез соединения 36

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(6-фторпиридин-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 6-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 36, МС: 483,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,29 (s, 1Н), 5 7,86 (d, 1Н), 7,48 (t, 1Н), 5,16 (m, 1Н), 3,93 (m, 1Н), 3,07 (m, 1Н), 2,45 (s, 3H), 2,42 (m, 2Н), 2,27-1,96 (m, 12H), 1,96-1,61 (m, 9H), 1,35 (d, 6H).
Пример 37. Синтез соединения 37
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-фтортиофен-2-ил)пропил]циклогексан-1-карбоксамид
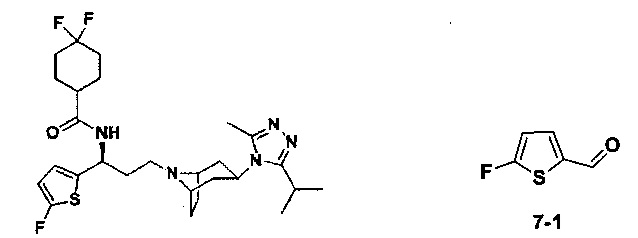
В соответствии со способом синтеза примера 5, соединение 7-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 37, МС: 538,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,07 (d, 1Н), 6,95 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6H).
Пример 38. Синтез соединения 38
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-фтортиофен-2-ил)пропил]циклогексан-1-карбоксамид

В соответствии со способом синтеза примера 5 соединение 7-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 38, МС: 502,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,13 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 39. Синтез соединения 39

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-фтортиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 7-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 39, МС: 488,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,10 (d, 1Н), 6,97 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 40. Синтез соединения 40
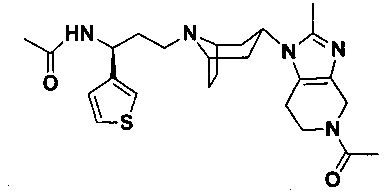
N-{(1S)-1-(тиофен-3-ил)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}ацетамид
Путь синтеза:
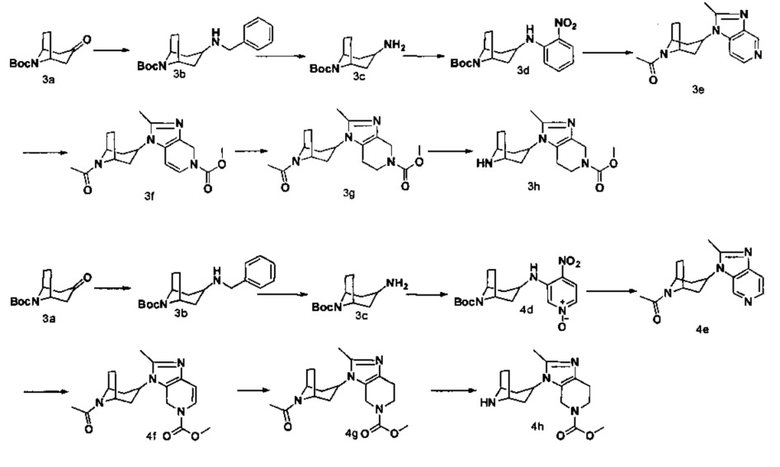
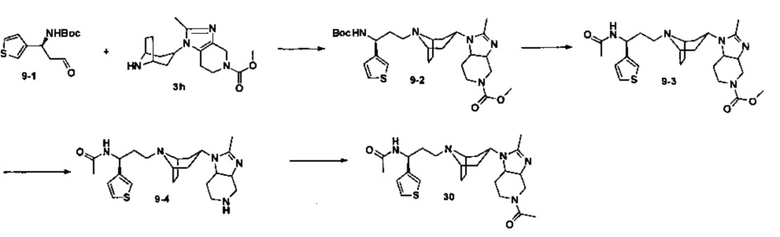
Синтез соединения 3b:
Соединение 3а (10,0 г, 44,4 ммоль), бензиламин (4,85 мл, 49,7 ммоль) и триацетилборгидрид натрия (14,11 г, 66,6 ммоль) растворяли в смешанном растворителе из уксусной кислоты и дихлорметана (1:9 об/об, 290 мл) и перемешивали в течение 16 часов при комнатной температуре. После удаления растворителя роторным выпариванием остаток растворяли в этилацетате, промывали насыщенным раствором карбоната натрия, высушивали над безводным сульфатом магния, выпаривали до сухого состояния в вакууме и разделяли колоночной хроматографией с получением соединения 3b (7,0 г, 50%), МС: 317,2 [М+Н]+.
Синтез соединения 3с:
Соединение 3b (7,0 г, 22,2 ммоль), формиат аммония (7,0 г, 111 ммоль) и 20% гидроксид палладия/углерод (0,7 г) диспергировали в этаноле (200 мл) и подвергали взаимодействию в течение 2 часов при 50°С. После охлаждения реакционный раствор фильтровали путем отсасывания. Затем фильтрат подвергали роторному выпариванию и разделению колоночной хроматографией с получением соединения 3с (4,7 г, 94%).
Синтез соединения 3d:
Соединение 3с (3,0 г, 13,2 ммоль), 4-этокси-3-нитропиридин (2,7 г, 13,2 ммоль) и DIPEA (1,89 г, 14,6 ммоль) растворяли в N-метилпирролидиноне (5 мл). Реакционную смесь нагревали до 120°С в течение 18 часов. Реакционный раствор охлаждали, экстрагировали этилацетатом, промывали водой, высушивали над сульфатом магния и концентрировали. Затем добавляли эфир для осаждения твердых веществ, и соединение 3d (1,5 г, 33%) было получено фильтрованием путем отсасывания. МС: 347,2 [М+Н]+.
Синтез соединения 3е:
Соединение 3d (4,4 г, 12,6 ммоль) и порошок железа (2,11 г, 37,8 ммоль) растворяли в уксусной кислоте (50 мл) и нагревали до 60°С в течение 2 часов. Затем добавляли уксусный ангидрид (8 мл) и нагревали до 140°С в течение 18 часов. После охлаждения реакционный раствор фильтровали путем отсасывания. Затем фильтрат подвергали роторному выпариванию, и остаток диспергировали в дихлорметане (200 мл) и воде (200 мл). Раствор доводили 2 н. гидроксидом натрия до рН 9, а затем фильтровали путем отсасывания. Затем фильтрат экстрагировали дихлорметаном, высушивали над сульфатом магния и выпаривали до сухого состояния в вакууме с получением соединения 3е (3,27 г, 91%). МС: 285,1 [М+Н]+.
Синтез соединения 3f:
Соединение 3е (10г, 35,2 ммоль) растворяли в этаноле (95 мл) и воде (5 мл), и в атмосфере азота медленно добавляли по каплям метилхлорформиат (3,3 мл, 42,2 ммоль) при -70°С. Смесь перемешивали в течение 45 минут, а затем добавляли порциями боргидрид натрия (4,0 г, 105,7 ммоль). Смесь медленно подогревали до комнатной температуры, добавляли колотый лед и перемешивали еще в течение 10 минут. Этанол удаляли роторным выпариванием, и остаток добавляли к 2 М водной соляной кислоте (100 мл) и промывали этилацетатом. Водный слой доводили твердым гидроксидом калия до рН 9, экстрагировали дихлорметаном, высушивали над сульфатом магния и разделяли колоночной хроматографией с получением соединения 3f (9 г, 74%), МС: 345,1 [М+Н]+.
Синтез соединения 3g:
Соединение 3f (6,75 г, 19,6 ммоль) растворяли в этаноле (60 мл) и добавляли 10% палладиевую чернь (Pd/C) (500 мг). Реакцию гидрогенизации проводили при 50°С в течение 5 ч. Реакционную смесь фильтровали путем отсасывания, и фильтрат выпаривали до сухого состояния в вакууме, а затем разделяли колоночной хроматографией с получением соединения 3g (6,2 г, 91%), МС: 346,2 [М+Н]+.
Синтез соединения 3h:
Соединение 3g (10,58 г, 30 ммоль) растворяли в 2М серной кислоте и нагревали до 100°С в течение 18 часов. Добавляли твердый гидроксид калия до доведения рН до 11-12. Смесь экстрагировали дихлорметаном и разделяли колоночной хроматографией с получением соединение 3h (7,4 г, 80%), МС: 304,1 [М+Н]+.
Синтез соединения 4h:
В соответствии со способом синтеза соединения 3h 3-фтор-4-нитропиридина N-оксид использовали вместо 4- этокси-3-нитропиридина в синтезе соединения 3h в примере 30.
Синтез соединения 9-2:
В соответствии со способом синтеза соединения 2-6, соединение 3-1 использовали вместо соединения 2-1 в примере 5, и соединение 3h использовали вместо 1f в примере 5 с получением соединения 9-2, МС: 545,3[М+Н]+.
Синтез соединения 9-3:
Соединение 9-2 (109 мг, 0,2 ммоль) растворяли в 1 мл метанола, добавляли 1 мл 4 М раствора HCl в диоксане и перемешивали в течение 2 часов при комнатной температуре. Смесь концентрировали и растворяли в 1 мл N,N-диметилформамида с последующим добавлением триэтиламина (30,3 мг, 0,3 ммоль), уксусной кислоты (49 мг, 0,3 ммоль), соли бензотриазол-1-илокси-трис(диметиламино)фосфония гексафторфосфата (ВОР) (126,5 мг, 0,3 ммоль) и перемешивали в течение 12 часов при комнатной температуре. Добавляли воду, а затем смесь экстрагировали этилацетатом, промывали насыщенным соляным раствором, высушивали над безводным сульфатом натрия, концентрировали и разделяли колоночной хроматографией с получением белого твердого вещества 9-3 (56,7 мг, выход 58%), МС: 487,2 [М+Н]+.
Синтез соединения 9-4:
Соединение 9-3 (85 мг, 0,17 ммоль) растворяли в изопропаноле (2 мл) и 2 М растворе гидроксида натрия (3 мл). Реакционную смесь нагревали при температуре образования флегмы в течение 48 часов, экстрагировали этилацетатом и разделяли колоночной хроматографией с получением соединения 9-4 (55 мг, 73%), МС: 429,1 [М+Н]+.
Синтез соединения 40:
Соединение 9-4 (55 мг, 0,13 ммоль) растворяли в 4 мл тетрагидрофурана и добавляли триэтиламин (17 мг, 0,17 ммоль). Затем добавляли по каплям ацетилхлорид (18 мг, 0,17 ммоль) и перемешивали в течение 2 часов при комнатной температуре. Смесь экстрагировали этилацетатом и разделяли колоночной хроматографией с получением соединения 40 (50 мг, 91%), МС: 500,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,25 (m, 1Н), 7,04 (m, 1Н), 6,97 (m, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 5Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 6Н), 1,69-1,53 (m, 4Н).
Пример 41. Синтез соединения 41
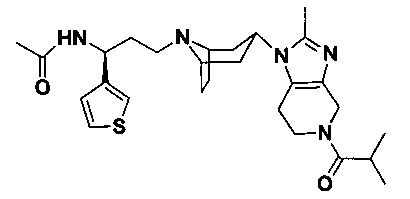
N-{(1S)-1-(тиофен-3-ил)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}ацетамид
В соответствии со способом синтеза соединения 40, изобутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 41, МС: 498,3 [М+Н]+.1Н-ЯМР (400 Гц, CDCl3): δ 7,14 (m, 1Н), 7,07 (m, 1Н), 6,97 (m, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 2Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 6Н), 1,69-1,53 (m, 4Н), 1,13-1,06 (m, 6Н).
Пример 42. Синтез соединения 42
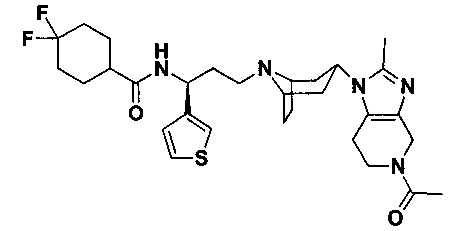
4,4-Дифтор-N-{(1S)-1-(тиофен-3-ил)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}циклогексан-1-карбоксамид
В соответствии со способом синтеза соединения 40 4,4-дифтор-циклогексанкарбоновую кислоту использовали вместо уксусной кислоты в примере 40 с получением соединения 42, МС: 574,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,14 (m, 1H), 7,07 (m, 1H), 6,97 (m, 1H), 5,17 (m, 1H), 4,65 (m, 1H), 4,43 (m, 2H), 4,09 (m, 2H), 3,43 (m, 2H), 3,07 (m, 1H), 2,83-2,69 (m, 5H), 2,51-2,39 (m, 2H), 2,36-1,84 (m, 9H), 1,69-1,53 (m, 9H).
Пример 43. Синтез соединения 43
4,4-Дифтор-N-{(1S)-1-(тиофен-3-ил)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}циклогексан-1-карбоксамид
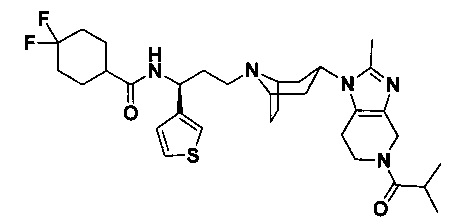
В соответствии со способом синтеза соединения 40, изобутирилхлорид использовали вместо ацетилхлорида в примере 40, и 4,4-дифтор-циклогексанкарбоновую кислоту использовали вместо уксусной кислоты в примере 40 с получением соединения 43, МС: 602,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,14 (m, 1Н), 7,03 (m, 1Н), 6,97 (m, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 2Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 8Н), 1,69-1,53 (m, 10H), 1,13-1,06 (m, 6Н).
Пример 44. Синтез соединения 44
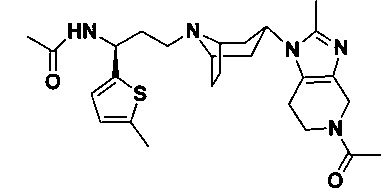
N-{(1S)-1-(5-метилтиофен-2-ил)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}ацетамид
В соответствии со способом синтеза соединения 40, соединение 5-1 использовали вместо 3-1 в примере 40 с получением соединения 44, МС: 470,3 [М+Н]+. 1Н-ЯМР (400 ГЦ, CDCl3): δ 7,10 (d, 1Н), 7,04 (d, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 5Н), 2,51-2,39 (m, 5Н), 2,36-1,84 (m, 6Н), 1,59-1,30 (m, 4Н).
Пример 45. Синтез соединения 45
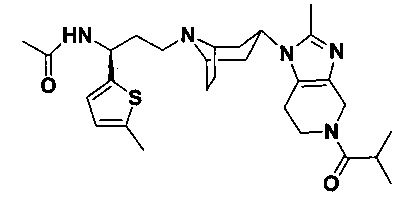
N-{(1S)-1-(5-метилтиофен-2-ил)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]про пил}ацетамид
В соответствии со способом синтеза соединения 40, изобутирилхлорид использовали вместо ацетилхлорида в примере 40, и соединение 5-1 использовали вместо 3-1 в примере 40 с получением соединения 45, МС: 498,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,14 (d, 1Н), 7,07 (d, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 2Н), 2,51-2,39 (m, 5Н), 2,36-1,84 (m, 6Н), 1,69-1,53 (m, 4Н), 1,13-1,06 (m, 6Н).
Пример 46. Синтез соединения 46
N-{(1S)-1-(5-метилтиофен-2-ил)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}циклогексан-1-карбоксамид
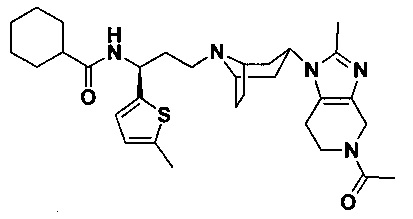
В соответствии со способом синтеза соединения 40, циклогексанкарбоновую кислоту использовали вместо уксусной кислоты в примере 40, и соединение 5-1 использовали вместо 3-1 в примере 40 с получением соединения 46, МС: 538,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,14 (d, 1Н), 7,03 (d, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 2Н), 2,51-2,39 (m, 5Н), 2,36-1,84 (m, 9Н), 1,69-1,53 (m, 11Н), 1,13-1,06 (m, 6H).
Пример 47. Синтез соединения 47

N-{(1S)-1-(5-метилтиофен-2-ил)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}циклогексан-1-карбоксамид
В соответствии со способом синтеза соединения 40, изобутирилхлорид использовали вместо ацетилхлорида в примере 40, соединение 5-1 использовали вместо 3-1 в примере 40, и циклогексанкарбоновую кислоту использовали вместо уксусной кислоты в примере 40 с получением соединения 47, МС: 566,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,14 (d, 1Н), 7,03 (d, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43(m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 2Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 8Н), 1,69-1,53 (m, 12Н), 1,13-1,06 (m, 6Н).
Пример 48. Синтез соединения 48
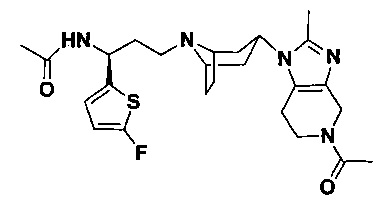
N-{(1S)-1-(5-фтортиофен-2-ил)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 7-1 использовали вместо 3-1 в примере 40 с получением соединения 48, МС: 488,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,10 (d, 1Н), 6,97 (d, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 5Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 6Н), 1,59-1,30 (m, 4Н).
Пример 49. Синтез соединения 49
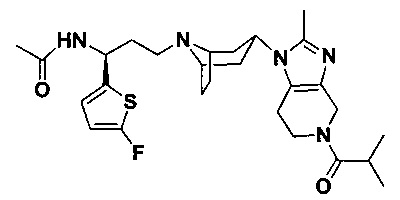
N-{(1S)-1-(5-фтортиофен-2-ил)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}ацетамид
В соответствии со способом синтеза соединения 40 изобутирилхлорид использовали вместо ацетилхлорида в примере 40, и соединение 7-1 использовали вместо 3-1 в примере 40 с получением соединения 49, МС: 516,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,07 (d, 1Н), 6,97 (d, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 2Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 6Н), 1,69-1,53 (m, 4Н), 1,13-1,06 (m, 6Н).
Пример 50. Синтез соединения 50

N-{(1S)-1-(5-фтортиофен-2-ил)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}циклогексан-1-карбоксамид
В соответствии со способом синтеза соединения 40 циклогексанкарбоновую кислоту использовали вместо уксусной кислоты в примере 40, и соединение 7-1 использовали вместо 3-1 в примере 30 с получением соединения 50, МС: 556,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,03 (m, 1Н), 6,97 (m, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,19 (m, 2Н), 3,63 (m, 2Н), 3,27 (m, 1Н), 2,83-2,69 (m, 2Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 9Н), 1,69-1,53 (m, 11Н), 1,13-1,06 (m, 6Н).
Пример 51. Синтез соединения 51
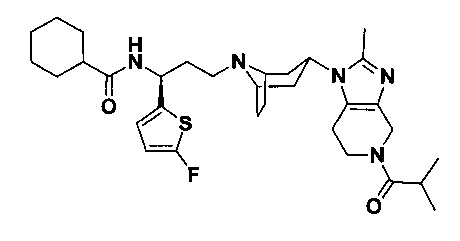
N-{(1S)-1-(5-фтортиофен-2-ил)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}циклогексан-1-карбоксамид
В соответствии со способом синтеза соединения 40 циклогексанкарбоновую кислоту использовали вместо уксусной кислоты в примере 40, соединение 7-1 использовали вместо 1-1 в примере 30, и изобутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 51, МС: 584,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,05 (m, 1Н), 6,97 (m, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,85-2,69 (m, 2Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 8Н), 1,69-1,53 (m, 12Н), 1,13-1,06 (m, 6Н).
Пример 52. Синтез соединения 52

4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-5-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 8-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо соединения 1f в примере 5 с получением соединения 52, МС: 520,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,27 (s, 1Н), 7,14 (s, 1Н), 5,14 (m, 1Н), 3,91 (m, 1Н), 3,03 (m, 1Н), 2,52 (s, 3H), 2,40 (m, 2Н), 2,27-1,93 (m, 12Н), 1,93-1,62 (m, 9Н), 1,32 (d, 6H).
Пример 53. Синтез соединения 53
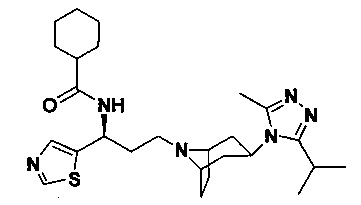
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-5-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 8-1 использовали вместо соединения 2-1 в примере 5 соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 53, МС: 484,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,28 (s, 1Н), 7,23 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2.26-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 54. Синтез соединения 54
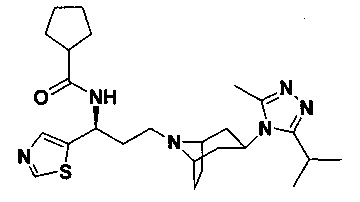
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-5-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 8-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 54, МС: 470,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,25 (s, 1Н), 7,33 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2.27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 55. Синтез соединения 55
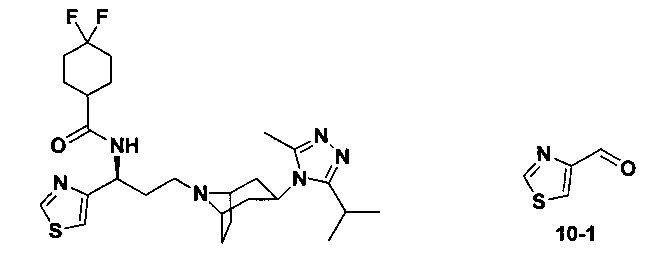
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-4-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 10-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо соединения 1f в примере 5 с получением соединения 55, МС: 520,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,20 (s, 1Н), 7,19 (s, 1Н), 5,14 (m, 1Н), 3,91 (m, 1Н), 3,03 (m, 1Н), 2,52 (s, 3H), 2,40 (m, 2Н), 2,27-1,93 (m, 12Н), 1,93-1,62 (m, 9H), 1,32 (d, 6H).
Пример 56. Синтез соединения 56
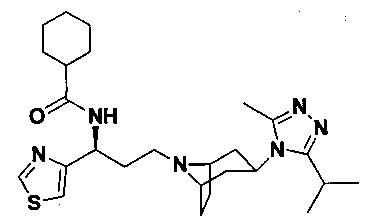
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-5-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 10-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 56, МС: 484,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,18 (s, 1Н), 7,23 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 57. Синтез соединения 57
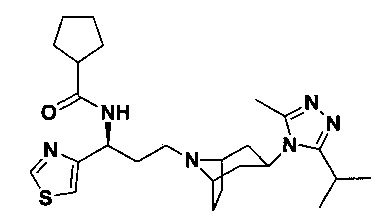
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-5-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 10-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 57, МС: 470,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,20 (s, 1Н), 7,33 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 58. Синтез соединения 58
N-{(1S)-1-(тиазол-5-ил)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}ацетамид
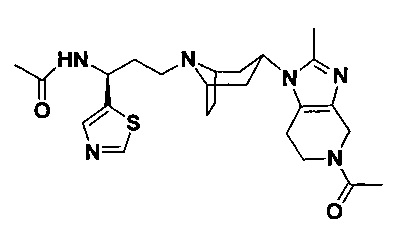
В соответствии со способом синтеза соединения 40 соединение 8-1 использовали вместо соединения 3-1 в примере 40 с получением соединения 58, МС: 471,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,10 (s, 1Н), 7,17 (s, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 5Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 6Н), 1,59-1,30 (m, 4Н).
Пример 59. Синтез соединения 59
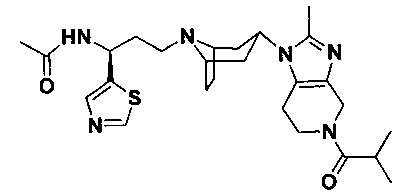
N-{(1S)-1-(тиазол-5-ил)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 8-1 использовали вместо соединения 3-1 в примере 40, и изобутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 59, МС: 499,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,87 (s, 1Н), 7,07 (s, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 2Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 6Н), 1,69-1,53 (m, 4Н), 1,13-1,06 (m, 6Н).
Пример 60. Синтез соединения 60
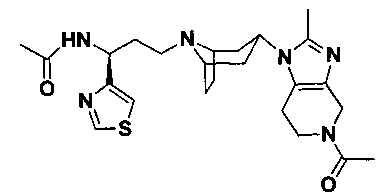
N-{(1S)-1-(тиазол-4-ил)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 10-1 использовали вместо соединения 3-1 в примере 40 с получением соединения 60, МС: 471,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8.13 (s, 1Н), 7.13 (s, 1Н), 5.17 (m, 1Н), 4.65 (m, 1Н), 4.43 (m, 2Н), 4.09 (m, 2Н), 3.43 (m, 2Н), 3.07 (m, 1Н), 2.83-2.69 (m, 5Н), 2.51-2.39 (m, 2Н), 2.36-1.84 (m, 6Н), 1.59-1.30 (m, 4Н).
Пример 61. Синтез соединения 61
N-{(1S)-1-(тиазол-4-ил)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}ацетамид

В соответствии со способом синтеза соединения 40, соединение 10-1 использовали вместо соединения 3-1 в примере 40, и изобутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 61, МС: 499,3 [M+H]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,07 (s, 1Н), 7,37 (s, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 2Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 6Н), 1,69-1,53 (m, 4Н), 1,13-1,06 (m, 6Н).
Пример 62. Синтез соединения 62
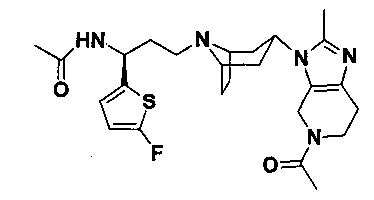
N-{(1S)-1-(5-фтортиофен-2-ил)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 7-1 использовали вместо соединения 3-1 в примере 40, соединение 4h использовали вместо соединения 3h в примере 40, и изобутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 62, МС: 488,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,13 (d, 1Н), 7,03 (d, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 5Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 6Н), 1,59-1,30 (m, 4Н).
Пример 63. Синтез соединения 63
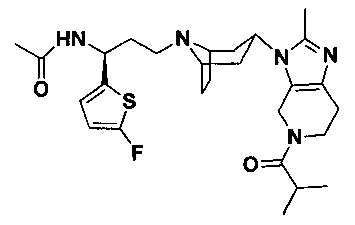
N-{(1S)-1-(5-фтортиофен-2-ил)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 7-1 использовали вместо соединения 3-1 в примере 40, и соединение 4h использовали вместо соединения 3h в примере 40 с получением соединения 63, МС: 516,3 [M+H]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,37 (d, 1Н), 7,01 (d, 1Н), 5,17 (m, 1Н), 4,65 (m, 1Н), 4,43 (m, 2Н), 4,09 (m, 2Н), 3,43 (m, 2Н), 3,07 (m, 1Н), 2,83-2,69 (m, 2Н), 2,51-2,39 (m, 2Н), 2,36-1,84 (m, 6Н), 1,69-1,53 (m, 4Н), 1,13-1,06 (m, 6Н).
Пример 64. Синтез соединения 64
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-этилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
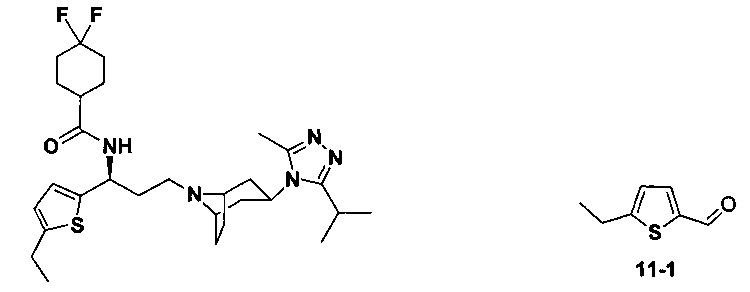
В соответствии со способом синтеза примера 5 соединение 11-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 64, МС: 548,2 [М+Н]+. δ 7,27 (d, 1Н), 7,20 (d, 1Н), 5,14 (m, 1Н), 3,91 (m, 1Н), 3,03 (m, 1Н), 2,52 (q, 2Н), 2,40 (m, 5Н), 2,27-1,93 (m,12Н), 1,93-1,62 (m, 9Н), 1,32 (m, 9Н).
Пример 65. Синтез соединения 65
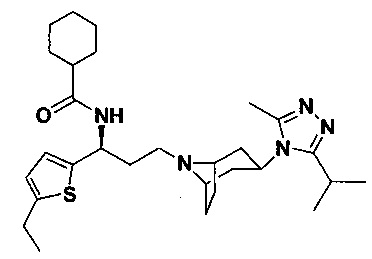
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-этилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 11-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 65, МС: 512,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,28 (d, 1Н), 7,21 (d, 1H), 5,19 (m, 1H), 3,91 (m, 1H), 3,02 (m, 1H), 2,54 (q, 2H), 2,43 (m, 5H), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10Н), 1,36 (m, 9H).
Пример 66. Синтез соединения 66
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метилтиофен-2-ил)пропил]циклопентан-1-карбоксамид
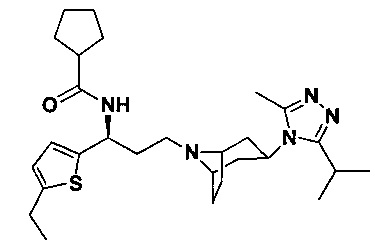
В соответствии со способом синтеза примера 5, соединение 11-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 66, МС: 498,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,25 (d, 1Н), 7,17 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (q, 2Н), 2,43 (m, 5Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (m, 9Н).
Пример 67. Синтез соединения 67
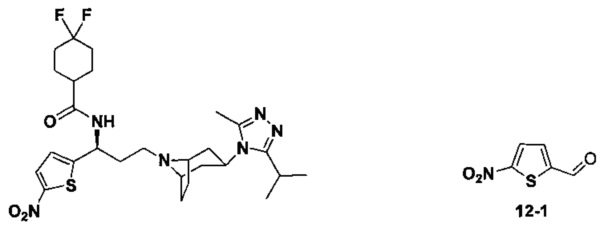
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-нитротиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 12-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 67, МС: 565,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,97 (d, 1Н), 7,05 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 68. Синтез соединения 68
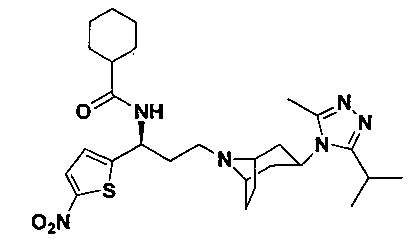
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-нитротиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 12-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 68, МС: 529,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,93 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6H).
Пример 69. Синтез соединения 69
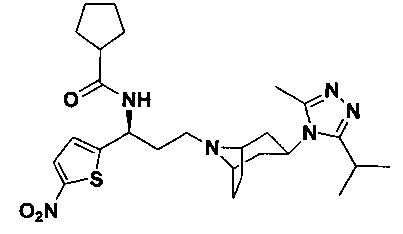
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-нитротиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 12-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 69, МС: 515.2[М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,90 (d, 1Н), 6,97 (d, 1Н), 5,19 (m, 1H), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m,2H), 2,27-1,93 (m, 11H), 1,93-1,61 (m, 10H), 1,35 (d, 6H).
Пример 70. Синтез соединения 70
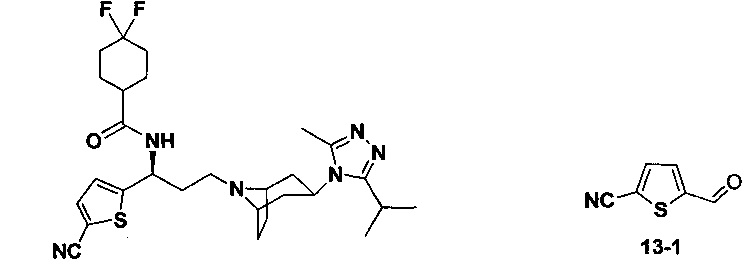
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-цианотиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 13-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 70, МС: 545,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,27 (d, 1Н), 6,95 (d, 1Н), 5,19 (m,1H), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2H), 2,27-1,95 (m, 10H), 1,95-1,61 (m, 9H), 1,34 (d, 6H).
Пример 71. Синтез соединения 71
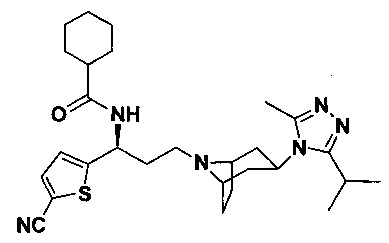
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-цианотиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 13-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 71, МС: 509,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,33 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 72. Синтез соединения 72
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-цианотиофен-2-ил)пропил]циклопентан-1-карбоксамид
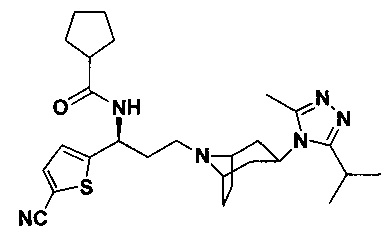
В соответствии со способом синтеза примера 5, соединение 13-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 72, МС: 495,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,30 (d, 1Н), 6,97 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 73. Синтез соединения 73

4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метоксикарбонилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 14-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 73, МС: 578,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,77 (d, 1Н), 6,95 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 74. Синтез соединения 74
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метоксикарбонилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 14-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 74.
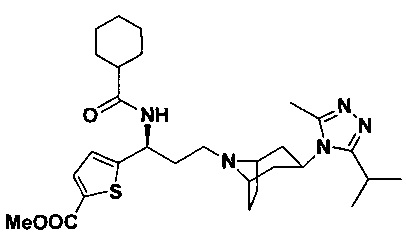
МС: 542,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,83 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6H).
Пример 75. Синтез соединения 75
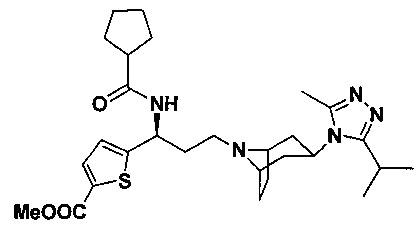
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метоксикарбонилтиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 14-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 75, МС: 528,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,80 (d, 1Н), 6,97 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 76. Синтез соединения 76
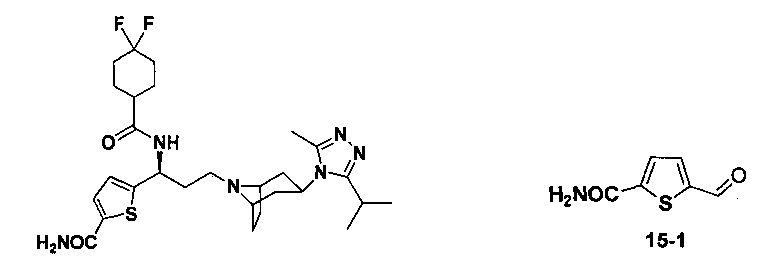
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-карбамоилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 15-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 76, МС: 563,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,87 (d, 2Н), 7,57 (d, 1Н), 6,95 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 77. Синтез соединения 77
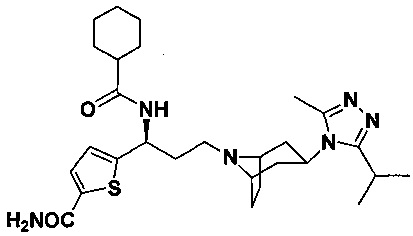
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-карбамоилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 15-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 77, МС: 528,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,87 (d, 2Н), 7,63 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 78. Синтез соединения 78

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-карбамоилтиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 15-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 78, МС: 513,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,87 (d, 2Н), 7,60 (d, 1Н), 6,97 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 79. Синтез соединения 79

4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-ацетилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 16-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 79, МС: 562,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,27 (d, 1Н), 6,95 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,27-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 80. Синтез соединения 80
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-ацетилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
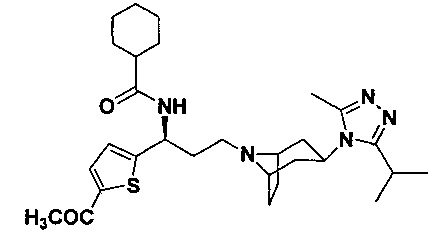
В соответствии со способом синтеза примера 5, соединение 16-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 80, МС: 526,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,23 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6H).
Пример 81. Синтез соединения 81
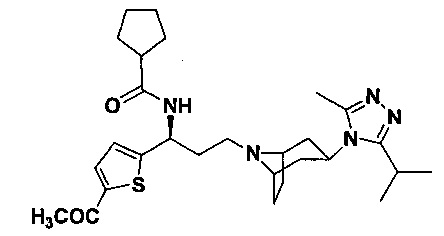
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-ацетилтиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 16-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 81, МС: 512,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,20 (d, 1Н), 6,97 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 82. Синтез соединения 82
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-формамидотиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 17-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 82.
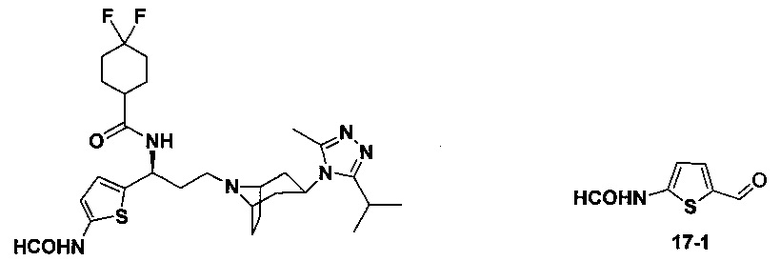
МС: 562,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,10 (s, 1Н), 7,07 (d, 1Н), 6,95 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 83. Синтез соединения 83
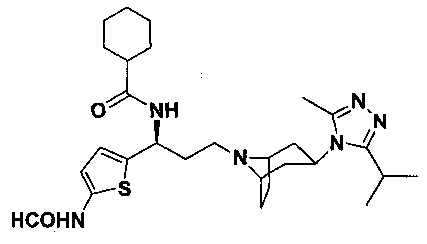
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-формамидотиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 17-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 83, МС: 527,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,10 (s, 1Н), 7,13 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 84. Синтез соединения 84
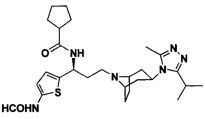
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-формамидотиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 17-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 84, МС: 513,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,10 (s, 1Н), 7,10 (d, 1Н), 6,97 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 85. Синтез соединения 85
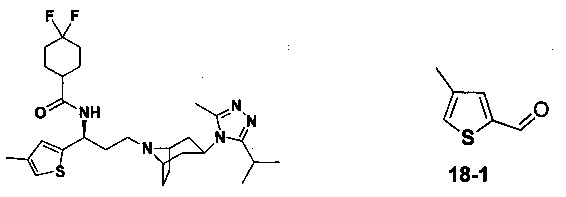
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(4-метилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 18-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 85, МС: 533,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,07 (s, 1Н), 6,95 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,27-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 86. Синтез соединения 86
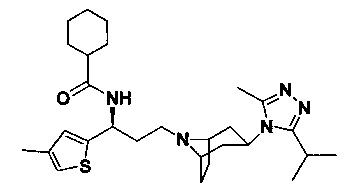
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(4-метилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 18-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 86, МС: 498,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,13 (s, 1Н), 6,94 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 87. Синтез соединения 87

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(4-метилтиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 18-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 87, МС: 484,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,10 (s, 1Н), 6,97 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 88. Синтез соединения 88
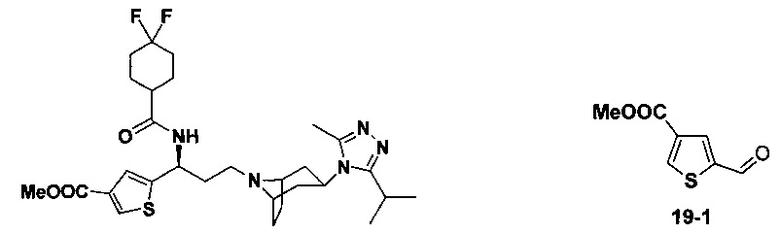
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метоксикарбонилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 19-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 88, МС: 578,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,17 (s, 1Н), 7,27 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 89. Синтез соединения 89
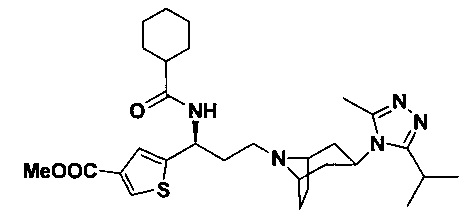
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метоксикарбонилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 19-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 89, МС: 542,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,13 (s, 1Н), 7,26 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 90. Синтез соединения 90
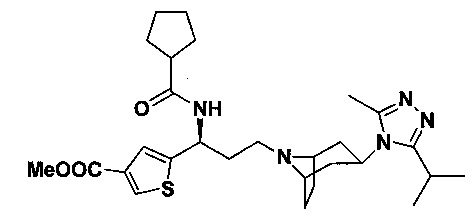
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метоксикарбонилтиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 19-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 90, МС: 528,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,10 (s, 1Н), 7,27 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 91. Синтез соединения 91
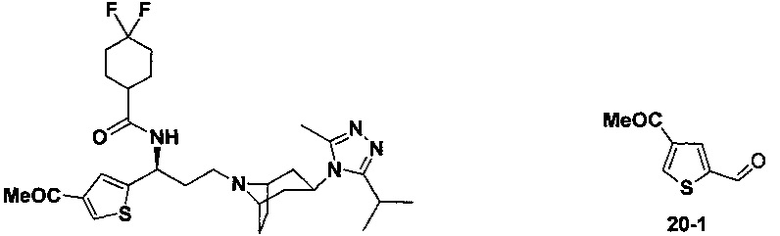
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(4-ацетилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 20-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 91, МС: 562,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,07 (s, 1Н), 7,15 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,27-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 92. Синтез соединения 92
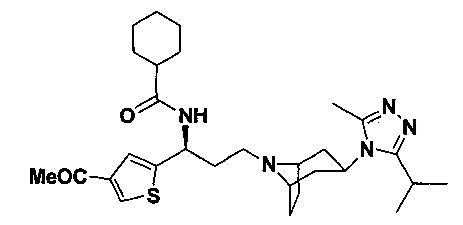
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(4-ацетилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 20-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 92, МС: 526,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,13 (s, 1Н), 7,14 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,26-1,93 (m, 13H), 1,93-1,61 (m, 10H), 1,36 (d, 6H).
Пример 93. Синтез соединения 93

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(4-ацетилтиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 20-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 93, МС: 512,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,10 (s, 1Н), 6,97 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,27-1,93 (m, 11Н), 1,93-1,61 (m, 10Н), 1,35 (d, 6Н).
Пример 94. Синтез соединения 94
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(4,5-диметилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
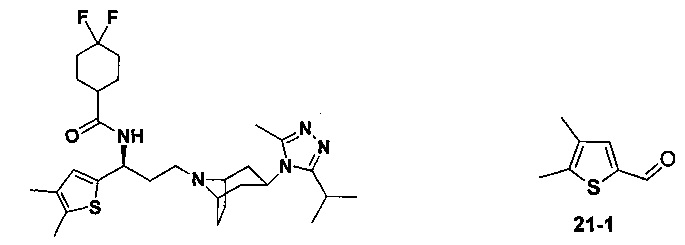
В соответствии со способом синтеза примера 5, соединение 21-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 94, МС: 548,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,05 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,25 (s, 6Н), 2,17-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 95. Синтез соединения 95
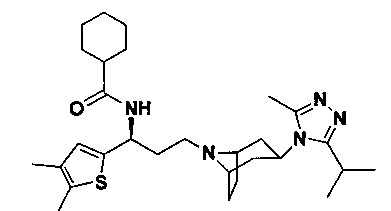
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(4,5-диметилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 21-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 95, МС: 512,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,04 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,25 (s, 6Н), 2,16-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 96. Синтез соединения 96

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(4,5-диметилтиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 21-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 96, МС: 498,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,07 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,25 (s, 6Н), 2,17-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 97. Синтез соединения 97
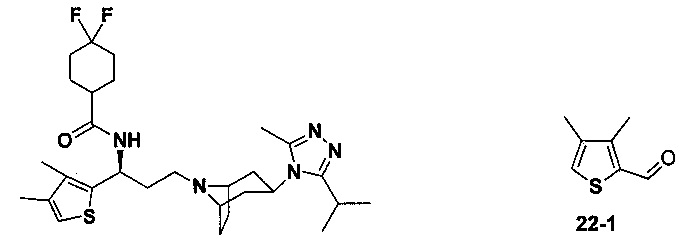
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(3,4-диметилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 22-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 97, МС: 548,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,05 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,25 (s, 6Н), 2,17-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 98. Синтез соединения 98
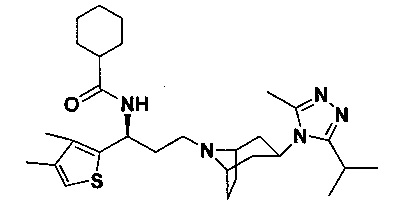
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(3,4-диметилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 22-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 98, МС: 512,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,04 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,25 (s, 6Н), 2,16-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 99. Синтез соединения 99
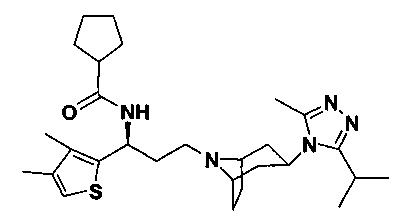
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(3,4-диметилтиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 22-1 использовали вместо 2-1 в примере 5, соединение 2f использовали вместо 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 99, МС: 498,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,07 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,25 (s, 6Н), 2,17-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 100. Синтез соединения 100
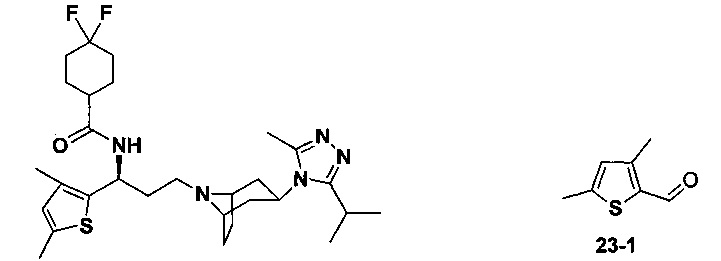
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(3,5-диметилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 23-1 использовали вместо 2-1 в примере 5, и соединение 2f использовали вместо 1f в примере 5 с получением соединения 100, МС: 548,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,15 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,29 (s, 6Н), 2,17-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d, 6Н).
Пример 101. Синтез соединения 101
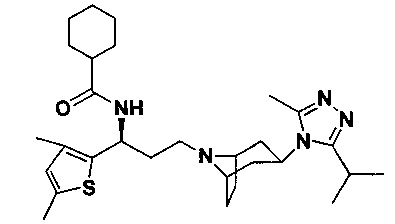
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(3,5-диметилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 23-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 101, МС: 512,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,14 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,29 (s, 6Н), 2.16-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 102. Синтез соединения 102
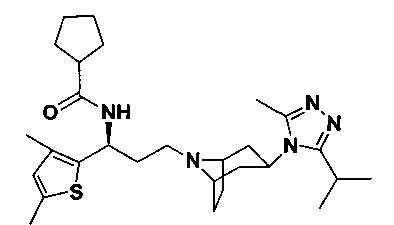
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(3,5-диметилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 23-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 102, МС: 498,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,17 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,29 (s, 6Н), 2.17-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 103. Синтез соединения 103

4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(3,4,5-триметилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 24-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо соединения 1f в примере 5 с получением соединения 103, МС: 562,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26 (s, 9Н), 2,17-1,95 (m, 10H), 1,95-1,61 (m, 9Н), 1,34 (d,6H).
Пример 104. Синтез соединения 104
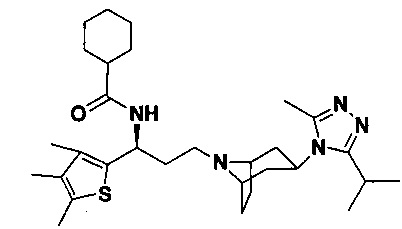
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(3,4,5-триметилтиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 24-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 104, МС: 526,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,27 (s, 9Н), 2,16-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 105. Синтез соединения 105
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(3,4,5-триметилтиофен-2-ил)пропил]циклопентан-1-карбоксамид
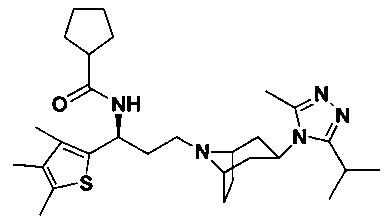
В соответствии со способом синтеза примера 5, соединение 24-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 105, МС: 512,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,29 (s, 9Н), 2,17-1,93 (m, 11Н), 1,93-1,61 (m, 10H), 1,35 (d, 6Н).
Пример 106. Синтез соединения 106

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5,6-дигидро-циклопентатиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 25-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 106, МС: 524,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,83 (s, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 5Н), 2,54 (s, 3H), 2,43 (m, 4Н), 2,16-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 107. Синтез соединения 107
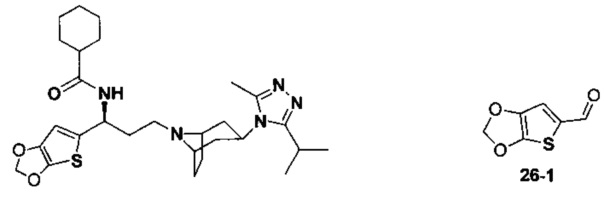
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиено[2,3-d][1,3]диоксол-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 26-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 107, МС: 528,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,03 (s, 2Н), 5,79 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,16-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 108. Синтез соединения 108
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метокситиофен-2-ил)пропил]циклопентан-1-карбоксамид
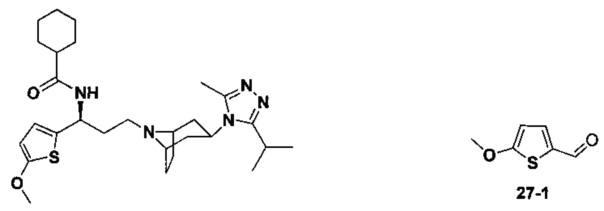
В соответствии со способом синтеза примера 5, соединение 27-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 108, МС: 514,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,43 (m, 2Н), 5,79 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,16-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 109. Синтез соединения 109

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]тетрагидропиран-4-карбоксамид
В соответствии со способом синтеза примера 5, соединение 1-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и тетрагидропиран-4-карбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 109, МС: 485,9 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,28 (t, 1Н), 7,13 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,61 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 2Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 6Н), 1,36 (d, 6Н).
Пример 110. Синтез соединения 110
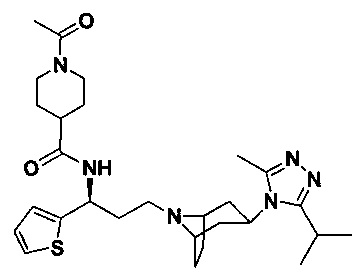
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]-1-ацетилпиперидин-4-карбоксамид
В соответствии со способом синтеза примера 5, соединение 1-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 1-ацетил-4-пиперидинкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 110, МС: 527,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,28 (t, 1Н), 7,13 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,31 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 6Н), 1,36 (d, 6Н).
Пример 111. Синтез соединения 111
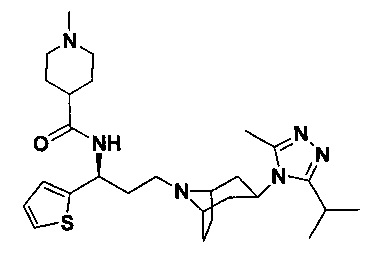
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]-1-метилпиперидин-4-карбоксамид
В соответствии со способом синтеза примера 5, соединение 1-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 1-метилпиперидин-4-карбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 111, МС: 499,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,28 (t, 1Н), 7,13 (d, 1Н), 6,94 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,51 (m, 7Н), 2,43 (m, 5Н), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 6Н), 1,36 (d, 6Н).
Пример 112. Синтез соединения 112

4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-хлортиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 28-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо соединения 1f в примере 5 с получением соединения 112, МС: 554,25 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,67 (m, 2Н), 4,78 (m, 1Н), 3,70 (m, 1Н), 3,18 (m, 1Н), 2,38-2,43 (m, 3H), 2,36 (s, 3H), 1,40-1,82 (m, 20Н), 1,26 (d, 6Н).
Пример 113. Синтез соединения 113
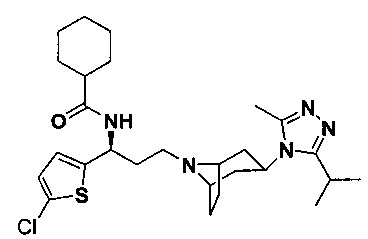
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-хлортиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 28-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 113, МС: 518,26 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,65-6,80 (m, 2Н), 4,78 (m, 1Н), 3,72 (m, 1Н), 3,20 (m, 1Н), 2,31-2,45 (m, 3H), 2,33 (s, 3H), 1,44-1,82 (m, 22Н), 1,36 (d, 6Н).
Пример 114. Синтез соединения 114
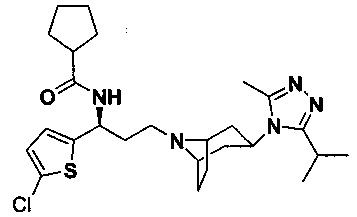
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-хлортиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 28-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 114, МС: 504,25 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,65-6,80 (m, 2Н), 4,78 (m, 1Н), 3,72 (m, 1Н), 3,20 (m, 1Н), 2,31-2,45(m, 3H), 2,33 (s, 3H), 1,44-1,82 (m, 20Н), 1,36 (d, 6H).
Пример 115. Синтез соединения 115
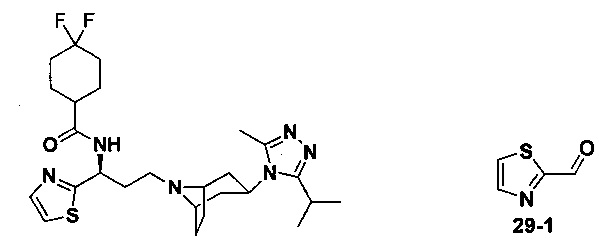
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 29-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо соединения 1f в примере 5 с получением соединения 115, МС: 521,28 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,67 (d, 1Н), 7,20 (d, 1Н), 4,78 (m, 1Н), 3,72 (m, 1Н), 3,20 (m, 1Н), 2,31-2,45 (m, 3H), 2,36 (s, 3H), 1,44-1,82 (m, 20Н), 1,36 (d, 6H).
Пример 116. Синтез соединения 116
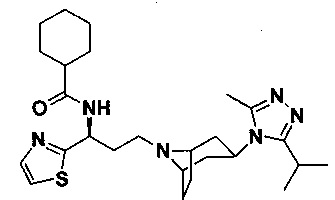
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 29-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 116, МС: 485,30 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,65 (d, 1Н), 7,23 (d, 1Н), 4,74 (m, 1Н), 3,71 (m, 1Н), 3,21 (m, 1Н), 2,31-2,45 (m, 3H), 2,33 (s, 3H), 1,34-1,83 (m, 22Н), 1,26 (d, 6Н).
Пример 117. Синтез соединения 117

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 29-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 117, МС: 471,28 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,62 (d, 1Н), 7,22 (d, 1Н), 4,73 (m, 1Н), 3,74 (m, 1Н), 3,22 (m, 1Н), 2,31-2,45 (m, 3H), 2,33 (s, 3H), 1,44-1,82 (m, 20Н), 1,33 (d, 6Н).
Пример 118. Синтез соединения 118
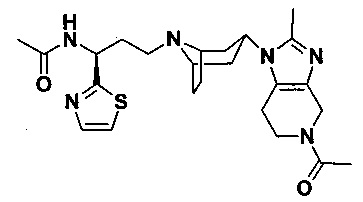
N-{(1S)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40, соединение 29-1 использовали вместо соединения 3-1 в примере 40 с получением соединения 118, МС: 471,25 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,65 (d, 1Н), 7,26 (d, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 2,32 (s, 3H), 1,44-2,12 (m, 15Н).
Пример 119. Синтез соединения 119
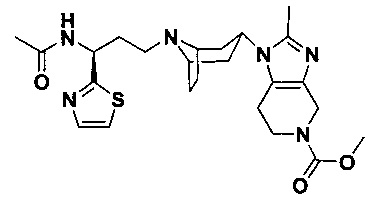
Метил-1-{(эндо)-8-[(S)-3-ацетамидо-3-(тиазол-2-ил)-пропил]-8-азабицикло[3.2.1]октан-3-ил}-2-метил-1,4,6,7-тетрагидро-5Н-имидазо[4,5-с]пиридин-5-карбоксилат
В соответствии со способом синтеза соединения 40, соединение 29-1 использовали вместо соединения 3-1 в примере 40, и метилхлорформиат использовали вместо ацетилхлорида в примере 40 с получением соединения 119, МС: 487,24 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,65 (d, 1Н), 7,26 (d, 1Н), 4,78 (t, 1Н), 4,18 (m, 2Н), 3,76 (s, 3H), 3,65-3,733 (m, 3H), 2,66 (m, 2Н), 2,43 (m, 2Н), 2,32 (s, 3H), 1,44-2,12 (m, 15Н).
Пример 120. Синтез соединения 120

N-{(1S)-3-[(3-эндо)-3-(5-пропионил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40, соединение 29-1 использовали вместо соединения 3-1 в примере 40, и пропионилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 120, МС: 485,26 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,65 (d, 1Н), 7,26 (d, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 2,27 (q, 2Н), 1,44-2,12 (m, 15Н), 1,21 (t, 3H).
Пример 121. Синтез соединения 121

N-{(1S)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40, соединение 29-1 использовали вместо соединения 3-1 в примере 40, и изобутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 121, МС: 499,28 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,65 (d, 1Н), 7,26 (d, 1Н), 4,78 (t, 1H), 4,38 (m, 2H), 3,86 (m, 2H), 3,74 (m, 1H), 2,66-2,69 (m, 3H), 2,53 (s, 3H), 2,43 (m, 2H), 1,44-2,12 (m, 15H), 1,10 (d, 6H).
Пример 122. Синтез соединения 122
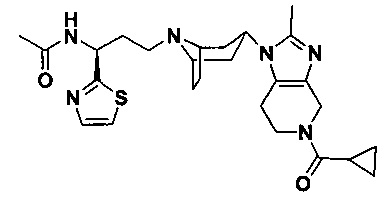
N-{(1S)-3-[(3-эндо)-3-(5-циклопропионил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40, соединение 29-1 использовали вместо соединения 3-1 в примере 40, циклопропионилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 122, МС: 497,26 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,65 (d, 1Н), 7,26 (d, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66-2,69 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 1,44-2,12 (m, 16Н), 0,53-0,78 (m, 4Н).
Пример 123. Синтез соединения 123
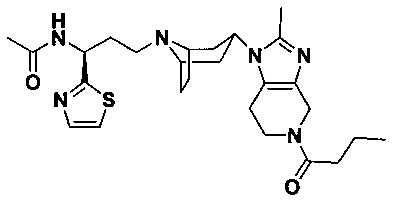
N-{(1S)-3-[(3-эндо)-3-(5-н-бутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 29-1 использовали вместо соединения 3-1 в примере 40, и н-бутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 123, МС: 499,28 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,65 (d, 1Н), 7,26 (d, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66-2,69 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2H), 2,34 (m, 2H), 1,44-2,12 (m, 17H), 0,96 (t, 3H).
Пример 124. Синтез соединения 124
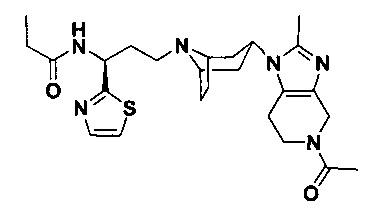
N-{(1S)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиазол-2-ил)-пропил}пропанамид
В соответствии со способом синтеза соединения 40, соединение 29-1 использовали вместо соединения 3-1 в примере 40, пропионовую кислоту использовали вместо уксусной кислоты в примере 40, и н-бутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 124, МС: 485,26 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,65 (d, 1Н), 7,26 (d, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 2,32 (s, 3H), 2,23 (q, 2Н), 1,44-1,96 (m, 12Н), 1,11 (t, 3H).
Пример 125. Синтез соединения 125

N-{(1S)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-хлортиофен-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40, соединение 28-1 использовали вместо соединения 3-1 в примере 40 с получением соединения 125, МС: 504,21 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,65 (d, 1Н), 6,26 (d, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 2,32 (s, 3H), 1,44-2,12 (m, 15Н).
Пример 126. Синтез соединения 126
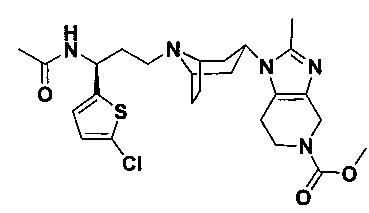
Метил-{(эндо)-8-[(S)-3-ацетамидо-3-(5-хлортиофен-2-ил)-пропил]-8-азабицикло[3.2.1]октан-3-ил}-2-метил-1,4,6,7-тетрагидро-5Н-имидазо[4,5-с]пиридин-5-карбоксилат
В соответствии со способом синтеза соединения 40 соединение 28-1 использовали вместо соединения 3-1 в примере 40, и метилхлорформиат использовали вместо ацетилхлорида в примере 40 с получением соединения 126, МС: 520,21 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,45 (d, 1Н), 6,16 (d, 1Н), 4,78 (t, 1Н), 4,18 (m, 2Н), 3,76 (s, 3H), 3,65-3,733 (m, 3H), 2,66 (m, 2Н), 2,43 (m, 2Н), 2,32 (s, 3H), 1,44-2,12 (m, 15Н).
Пример 127. Синтез соединения 127
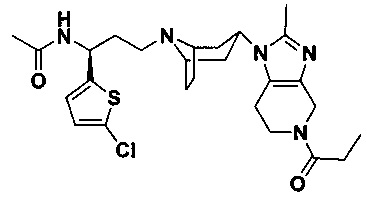
N-{(1S)-3-[(3-эндо)-3-(5-пропионил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-хлортиофен-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 28-1 использовали вместо соединения 3-1 в примере 40, и пропионилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 127, МС: 518,23 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,45 (d, 1Н), 6,16 (d, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 2,27 (q, 2Н), 1,44-2,12 (m, 15Н), 1,21 (t, 3H).
Пример 128. Синтез соединения 128
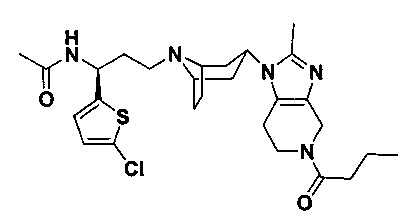
N-{(1S)-3-[(3-эндо)-3-(5-н-бутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-хлортиофен-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40, соединение 28-1 использовали вместо соединения 3-1 в примере 40, и н-бутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 128, МС: 532,24 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,48 (d, 1Н), 6,12 (d, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66-2,69 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 2,34 (m, 2Н), 1,44-2,12 (m, 17Н), 0,96 (t, 3H).
Пример 129. Синтез соединения 129
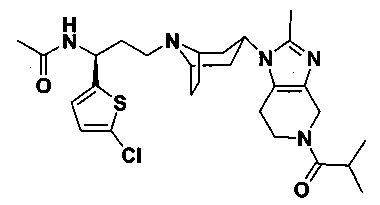
N-{(1S)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-хлортиофен-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 28-1 использовали вместо соединения 3-1 в примере 40, и изобутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 129, МС: 532,24 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,48 (d, 1Н), 6,12 (d, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66-2,69 (m, 3H), 2,53 (s, 3H), 2,43 (m, 2Н), 1,44-2,12 (m, 15Н), 1,10 (d, 6Н).
Пример 130. Синтез соединения 130
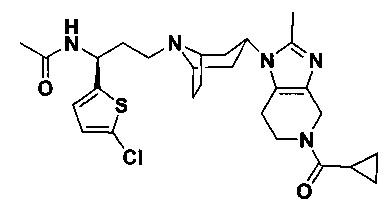
N-{(1S)-3-[(3-эндо)-3-(5-циклопропионил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-хлортиофен-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40, соединение 28-1 использовали вместо соединения 3-1 в примере 40, и циклопропионилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 130, МС: 530,23 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,78 (d, 1Н), 6,22 (d, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66-2,69 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 1,44-2,12 (m, 16Н), 0,53-0,78 (m, 4Н).
Пример 131. Синтез соединения 131

N-{(1S)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-фтортиофен-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 7-1 использовали вместо соединения 3-1 в примере 40 с получением соединения 131, МС: 488,24 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,46 (m, 1Н), 6,27 (m, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 2,32 (s, 3H), 1,44-2,12 (m, 15Н).
Пример 132. Синтез соединения 132
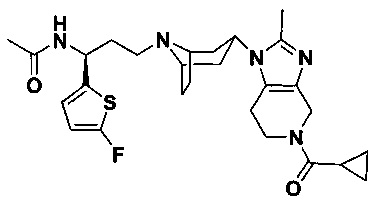
N-{(1S)-3-[(3-эндо)-3-(5-циклопропионил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-фтортиофен-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 7-1 использовали вместо соединения 3-1 в примере 40, и циклопропионилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 132, МС: 514,26 [M+H]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,36 (m, 1Н), 6,15 (m, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66-2,69 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 1,44-2,12 (m, 16Н), 0,53-0,78 (m, 4Н).
Пример 133. Синтез соединения 133
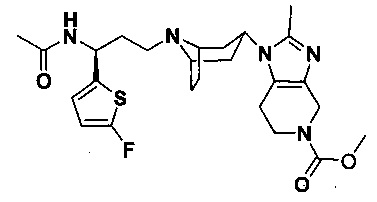
Метил-1-{(эндо)-8-[(S)-3-ацетамидо-3-(5-фтортиофен-2-ил)-пропил]-8-азабицикло[3.2.1]октан-3-ил}-2-метил-1,4,6,7-тетрагидро-5Н-имидазо[4,5-с]пиридин-5-карбоксилат
В соответствии со способом синтеза соединения 40 соединение 7-1 использовали вместо соединения 3-1 в примере 40, и метилхлорформиат использовали вместо ацетилхлорида в примере 40 с получением соединения 133, МС: 504,24 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,47 (m, 1Н), 6,25 (m, 1Н), 4,78 (t, 1Н), 4,18 (m, 2Н), 3,76 (s, 3H), 3,65-3,733 (m, 3H), 2,66 (m, 2Н), 2,43 (m, 2Н), 2,32 (s, 3H), 1,44-2,12 (m, 15Н).
Пример 134. Синтез соединения 134
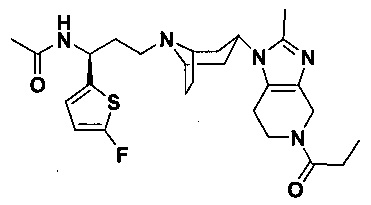
N-{(1S)-3-[(3-эндо)-3-(5-пропионил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-фтортиофен-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 7-1 использовали вместо соединения 3-1 в примере 40, и пропионилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 134, МС: 502,26 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,48 (m, 1Н), 6,23 (m, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 2,27 (q, 2Н), 1,44-2,12 (m, 15Н), 1,21 (t, 3H).
Пример 135. Синтез соединения 135 N-{(1S)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-фтортиофен-2-ил)-пропил}ацетамид

В соответствии со способом синтеза соединения 40 соединение 7-1 использовали вместо соединения 3-1 в примере 40, и изобутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 135, МС: 516,27 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,42 (m, 1Н), 6,13 (m, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66-2,69 (m, 3H), 2,53 (s, 3H), 2,43 (m, 2Н), 1,44-2,12 (m, 15Н), 1,10 (d, 6Н).
Пример 136. Синтез соединения 136
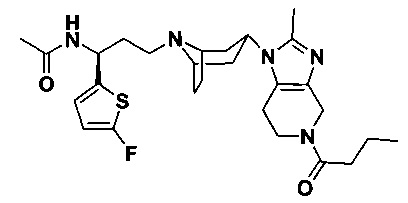
N-{(1S)-3-[(3-эндо)-3-(5-н-бутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-фтортиофен-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40 соединение 7-1 использовали вместо соединения 3-1 в примере 40, и н-бутирилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 136, МС: 516,27 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,41 (m, 1Н), 6,12 (m, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66-2,69 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2H), 2,34 (m, 2H), 1,44-2,12 (m, 17H), 0,96 (t, 3H).
Пример 137. Синтез соединения 137
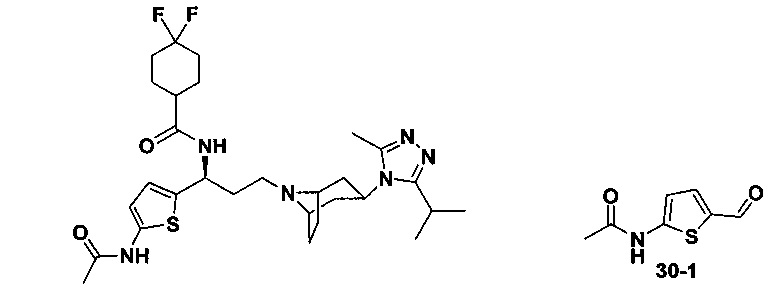
4,4-Дифтор-N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-ацетамидотиофен-2-ил)пропил]циклогексан -1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 30-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо соединения 1f в примере 5 с получением соединения 137, МС: 577,31 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,32 (d, 1Н), 7,07 (d, 1Н), 4,74 (m, 1Н), 3,71 (m, 1Н), 3,21 (m, 1Н), 2,31-2,45 (m, 6Н), 2,33 (s, 3H), 1,34-1,83 (m, 20Н), 1,26 (d, 6H).
Пример 138. Синтез соединения 138

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-ацетамидотиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 30-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 138, МС: 541,32 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,31 (d, 1H), 7,03 (d, 1H), 4,74 (m, 1H), 3,71 (m, 1H), 3,21 (m, 1H), 2,36-2,43 (m, 6H), 2,30 (s, 3H), 1,34-1,83 (m, 22H), 1,26 (d, 6H).
Пример 139. Синтез соединения 139
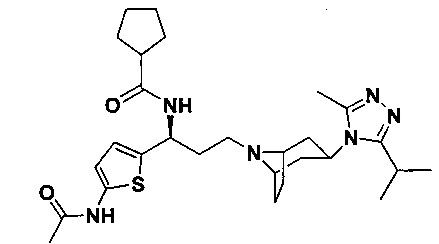
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-ацетамидотиофен-2-ил)пропил]циклопентан-1-карбоксамид
В соответствии со способом синтеза примера 5 соединение 30-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 139, МС: 527,31 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,31 (d, 1Н), 7,03 (d, 1Н), 4,74 (гл, 1Н), 3,71 (m, 1Н), 3,21 (m, 1Н), 2,36-2,43 (m, 6Н), 2,26 (s, 3H), 1,34-1,83 (m, 20Н), 1,26 (d, 6Н).
Пример 140. Синтез соединения 140
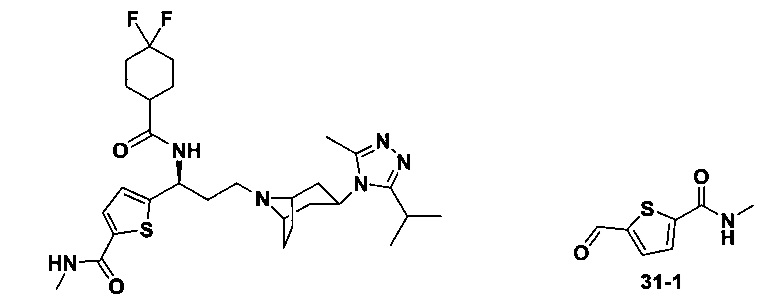
5-[(1S)-1-(4,4-дифторциклогексил-1-формамидо)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-пропил]-N-метилтиофен-2-карбоксамид
В соответствии со способом синтеза примера 5 соединение 31-1 использовали вместо соединения 2-1 в примере 5, и соединение 2f использовали вместо соединения 1f в примере 5 с получением соединения 140, МС: 577,31 [M+H]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,26 (d, 1Н), 7,07 (d, 1Н), 4,74 (m, 1Н), 3,71 (m, 1Н), 3,21 (m, 1Н), 2,86 (s, 3H), 2,39-2,45 (m, 3H), 2,33 (s, 3H), 1,34-1,83 (m, 20Н), 1,26 (d, 6Н).
Пример 141. Синтез соединения 141
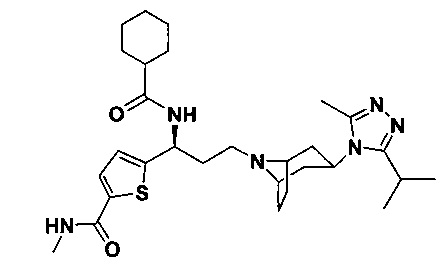
5-[(1S)-1-(циклогексанформамидо)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-пропил]-N-метилтиофен-2-карбоксамид
В соответствии со способом синтеза примера 5 соединение 31-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 141, МС: 541,32 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,14 (d, 1Н), 7,13 (d, 1Н), 4,74 (m, 1Н), 3,71 (m, 1Н), 3,21 (m, 1Н), 2,86 (s, 3H), 2,39-2,45 (m, 3H), 2,33 (s, 3H), 1,34-1,83 (m, 22Н), 1,26 (d, 6Н).
Пример 142. Синтез соединения 142
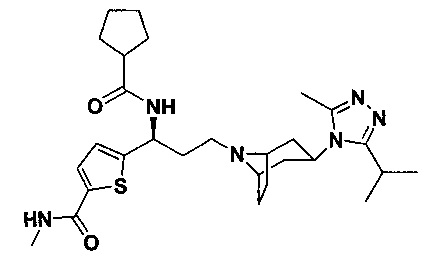
5-[(1S)-1-(циклопентанформамидо)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-пропил]-N-метилтиофен-2-карбоксамид
В соответствии со способом синтеза примера 5 соединение 31-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклопентанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 142, МС: 527,31 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,36 (d, 1Н), 7,13 (d, 1Н), 4,74 (m, 1Н), 3,71 (m, 1Н), 3,21 (m, 1Н), 2,86 (s, 3H), 2,39-2,45 (m, 3H), 2,33 (s, 3H), 1,34-1,83 (m, 20Н), 1,26 (d, 6Н).
Пример 143. Синтез соединения 143
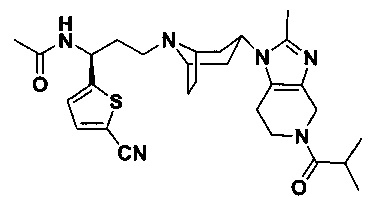
N-{(1S)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-цианотиофен-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40, соединение 13-1 использовали вместо соединения 3-1 в примере 40, и изопропионилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 143, МС: 523,28 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,44 (m, 1Н), 6,87 (m, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66-2,69 (m, 3H), 2,53 (s, 3H), 2,43 (m, 2Н), 1,44-2,12 (m, 15Н), 1,10 (d, 6Н).
Пример 144. Синтез соединения 144
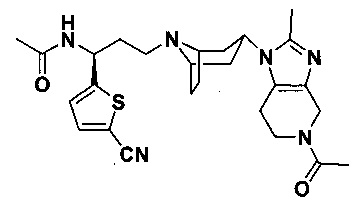
N-{(1S)-3-[(3-эндо)-3-(5-ацетил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-цианотиофен-2-ил)-пропил} ацетамид
В соответствии со способом синтеза соединения 40, соединение 13-1 использовали вместо соединения 3-1 в примере 40 с получением соединения 144, МС: 495,25 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,56 (m, 1Н), 6,93 (m, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66 (m, 2Н), 2,53 (s, 3H), 2,43 (m, 2Н), 2,32 (s, 3H), 1,44-2,12 (m, 15Н).
Пример 145. Синтез соединения 145
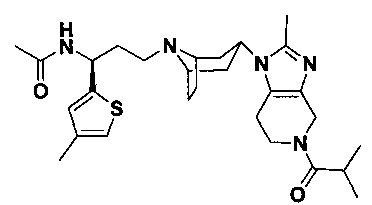
N-{(1S)-3-[(3-эндо)-3-(5-изобутирил-2-метил-4,5,6,7-тетрагидро-1Н-имидазо[4,5-с]пиридин-1-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(4-метилтиофен-2-ил)-пропил}ацетамид
В соответствии со способом синтеза соединения 40, соединение 18-1 использовали вместо соединения 3-1 в примере 40, и изопропионилхлорид использовали вместо ацетилхлорида в примере 40 с получением соединения 145, МС: 512,30 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,59 (m, 1Н), 6,91 (m, 1Н), 4,78 (t, 1Н), 4,38 (m, 2Н), 3,86 (m, 2Н), 3,74 (m, 1Н), 2,66-2,69 (m, 3H), 2,53 (s, 3H), 2,43 (m, 2Н), 1,44-2,12 (m, 15Н), 1,10 (d, 6Н).
Пример 146. Синтез соединения 146

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]-1-метилсульфонилпиперидин-4-карбоксамид
В соответствии со способом синтеза примера 5, соединение 1-1 использовали вместо соединения 2-1 в примере 5 соединение 2f использовали вместо соединения 1f в примере 5, и 1-метилсульфонил-4-пиперидинкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 146, МС: 563,3 [M+H]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7.28 (t, 1Н), 7.13 (d, 1Н), 6.94 (d, 1Н), 5.19 (m, 1Н), 3.91 (m, 1Н), 3.31 (m, 4Н), 3.02 (m, 1Н), 2.54 (s, 3H), 2.43 (m, 5Н), 2.26-1.93 (m, 13Н), 1.93-1.61 (m, 6Н), 1.36 (d, 6Н).
Пример 147. Синтез соединения 147

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]-1-метилсульфонилпиперидин-4-карбоксамид
В соответствии со способом синтеза примера 5 соединение 5-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 1-метилсульфонил-4-пиперидинкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 147, МС: 577,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,28 (t, 1Н), 7,13 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 1Н), 3,31 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,36 (s, 3H), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 6Н), 1,36 (d, 6Н).
Пример 148. Синтез соединения 148
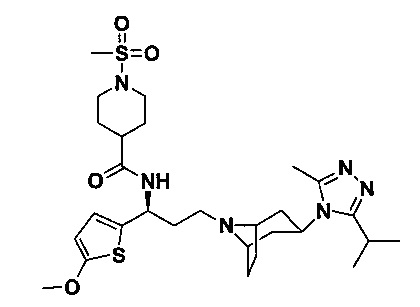
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метокситиофен-2-ил)пропил]-1-метилсульфонилпиперидин-4-карбоксамид
В соответствии со способом синтеза примера 5 соединение 27-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 1-метилсульфонил-4-пиперидинкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 148, МС: 593,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,28 (t, 1Н), 7,13 (d, 1Н) 5,19 (m, 1Н), 3,91 (m, 4Н), 3,31 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,36 (s, 3H), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 6Н), 1,36 (d, 6H).
Пример 149. Синтез соединения 149

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-цианотиофен-2-ил)пропил]-1-метилсульфонилпиперидин-4-карбоксамид
В соответствии со способом синтеза примера 5, соединение 13-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 1-метилсульфонил-4-пиперидинкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 149, МС: 588,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,38 (t, 1Н), 7,24 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 4Н), 3,31 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2,36 (s, 3H), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 6Н), 1,36 (d, 6Н).
Пример 150. Синтез соединения 150

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-хлортиофен-2-ил)пропил]-1-метилсульфонилпиперидин-4-карбоксамид
В соответствии со способом синтеза примера 5, соединение 28-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 1-метилсульфонил-4-пиперидинкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 150, МС: 597,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,38 (t, 1Н), 7,23 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 4Н), 3,31 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2.36 (s, 3H), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 6Н), 1,36 (d, 6Н).
Пример 151. Синтез соединения 151
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-фтортиофен-2-ил)пропил]-1-метилсульфонилпиперидин-4-карбоксамид
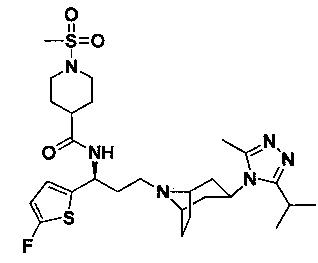
В соответствии со способом синтеза примера 5 соединение 7-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 1-метилсульфонил-4-пиперидинкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 151, МС: 581,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,48 (t, 1Н), 7,24 (d, 1Н), 5,19 (m, 1Н), 3,91 (m, 4Н), 3,31 (m, 4Н), 3,02 (m, 1Н), 2,54 (s, 3H), 2,43 (m, 5Н), 2.37 (s, 3H), 2,26-1,93 (m, 13Н), 1,93-1,61 (m, 6Н), 1,36 (d, 6Н).
Пример 152. Синтез соединения 152
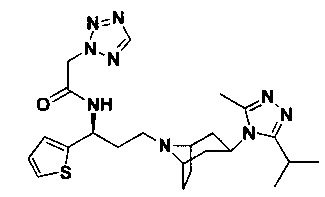
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]-2-(2Н-тетразол-2-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 1-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(2Н-тетразол-2-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 152, МС: 484,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,53 (s, 1Н), 7,23 (t, 1Н), 7,15 (d, 1Н), 6,99 (d, 1Н), 5,21 (m, 1Н), 4,62 (s, 2Н), 3,95 (m, 1Н), 3,03 (m, 1Н), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 153. Синтез соединения 153
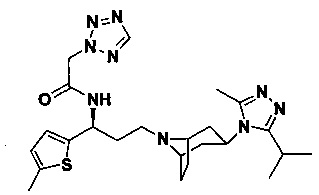
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метилтиофен-2-ил)пропил]-2-(2Н-тетразол-2-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 5-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(2H-тетразол-2-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 153, МС: 498,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,53 (s, 1Н), 7,23 (t, 1Н), 7,15 (d, 1Н), 6,99 (d, 1Н), 5,21 (m, 1Н), 4,62 (s, 2Н), 3,95 (m, 1Н), 3,03 (m, 1Н), 2,36 (s, 3H), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6H).
Пример 154. Синтез соединения 154
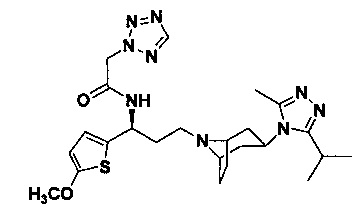
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метилтиофен-2-ил)пропил]-2-(2Н-тетразол-2-ил)ацетамид
В соответствии со способом синтеза примера 5, соединение 27-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(2Н-тетразол-2-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 154, МС: 514,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,53 (s, 1Н), 7,23 (t, 1Н), 5,21 (m, 1Н), 4,62 (s, 2Н), 3,95 (m, 1Н), 3,85 (s, 3H), 3,03 (m, 1Н), 2,36 (s, 3H), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 155. Синтез соединения 155
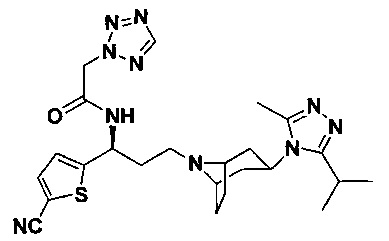
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-цианотиофен-2-ил)пропил]-2-(2Н-тетразол-2-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 13-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(2Н-тетразол-2-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 155, МС: 509,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,53 (s, 1Н), 7,23 (t, 1Н), 5,21 (m, 1Н), 4,62 (s, 2Н), 3,95 (m, 1Н), 3,03 (m, 1Н), 2,36 (s, 3H), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 156. Синтез соединения 156
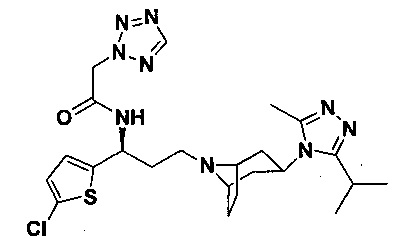
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-хлортиофен-2-ил)пропил]-2-(2H-тетразол-2-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 28-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(2Н-тетразол-2-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 156, МС: 518,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,03 (s, 1Н), 7,53 (t, 1Н), 5,21 (m, 1Н), 4,62 (s, 2Н), 3,95 (m, 1Н), 3,03 (m, 1Н), 2,36 (s, 3H), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6H).
Пример 157. Синтез соединения 157
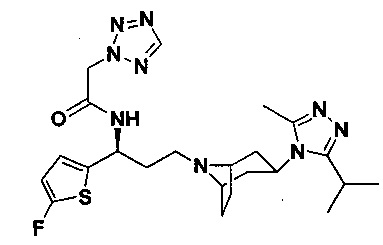
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-фтортиофен-2-ил)пропил]-2-(2H-тетразол-2-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 7-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(2H-тетразол-2-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 157, МС: 502,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,13 (s, 1Н), 7,23 (t, 1Н), 5,21 (m, 1Н), 4,62 (s, 2Н), 3,95 (m, 1Н), 3,03 (m, 1Н), 2,36 (s, 3H), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 158. Синтез соединения 158
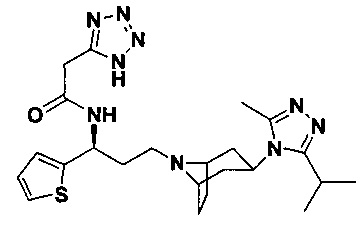
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]-2-(1Н-тетразол-5-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 1-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(1Н-тетразол-5-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 158, МС: 484,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7.23 (t, 1Н), 7.15 (d, 1Н), 6.99 (d, 1Н), 5.21 (m, 1Н), 3.95 (m, 1Н), 3.42 (s, 2Н), 3.03 (m, 1Н), 2.40 (m, 2Н), 2.25-1.67 (m,14H), 1.32 (d, 6Н).
Пример 159. Синтез соединения 159

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метилтиофен-2-ил)пропил]-2-(1H-тетразол-5-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 5-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(1H-тетразол-5-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 159, МС: 498,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,23 (t, 1Н), 7,15 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,42 (s, 2Н), 3,03 (m, 1Н), 2,40 (m, 2Н), 2,36 (s, 3H), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 160. Синтез соединения 160
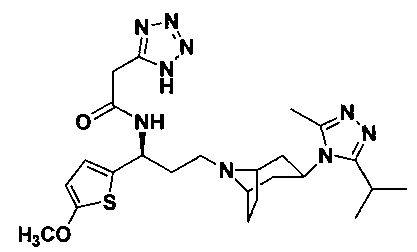
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метокситиофен-2-ил)пропил]-2-(1Н-тетразол-5-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 27-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(1H-тетразол-5-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 160, МС: 514,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,23 (t, 1Н), 7,15 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,42 (s, 2Н), 3,03 (m, 1Н), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 161. Синтез соединения 161
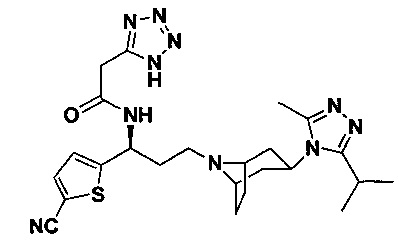
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-цианотиофен-2-ил)пропил]-2-(1Н-тетразол-5-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 13-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(1Н-тетразол-5-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 161, МС: 509,3 [M+HJ+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,43 (t, 1Н), 7,35 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,42 (s, 2Н), 3,03 (m, 1Н), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 162. Синтез соединения 162
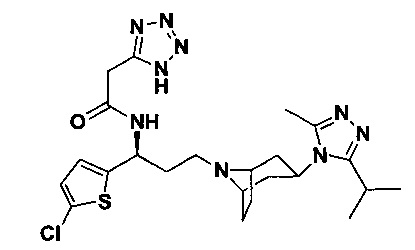
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-хлортиофен-2-ил)пропил]-2-(1Н-тетразол-5-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 28-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(1H-тетразол-5-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 162, МС: 518,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,53 (t, 1Н), 7,45 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,42 (s, 2Н), 3,03 (m, 1H), 2,40 (m, 2H), 2,25-1,67 (m, 14H), 1,32 (d, 6H).
Пример 163. Синтез соединения 163
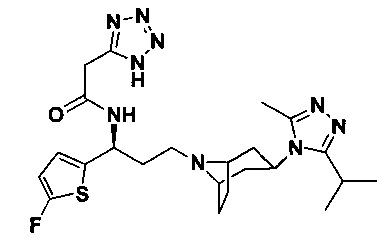
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-фтортиофен-2-ил)пропил]-2-(1Н-тетразол-5-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 7-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(1Н-тетразол-5-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 163, МС: 502,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,63 (t, 1Н), 7,55 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,42 (s, 2Н), 3,03 (m, 1Н), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 164. Синтез соединения 164
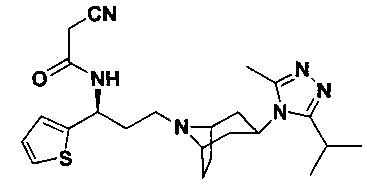
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]-2-цианоацетамид
В соответствии со способом синтеза примера 5 соединение 1-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-цианоуксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 164, МС: 441,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,23 (t, 1Н), 7,15 (d, 1Н), 6,99 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,32 (s, 2Н), 3,03 (m, 1Н), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 165. Синтез соединения 165
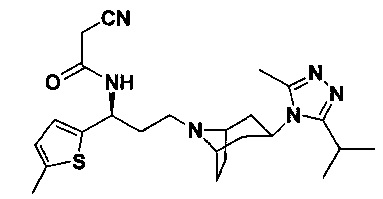
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метилтиофен-2-ил)пропил]-2-цианоацетамид
В соответствии со способом синтеза примера 5, соединение 5-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-цианоуксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 165, МС: 454,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,23 (t, 1Н), 7,15 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,32 (s, 2Н), 3,03 (m, 1Н), 2,37 (s, 3H), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 166. Синтез соединения 166
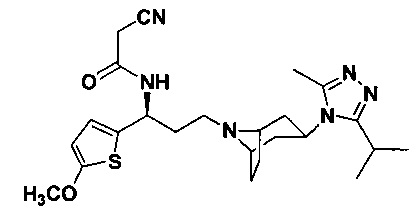
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-метокситиофен-2-ил)пропил]-2-цианоацетамид
В соответствии со способом синтеза примера 5 соединение 27-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-цианоуксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 166, МС: 471,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,23 (t, 1Н), 7,15 (d, 1H), 5,21 (m, 1H), 3,95 (m, 1H), 3,87 (s, 3H), 3,32 (s, 2H), 3,03 (m, 1H), 2,40 (m, 2H), 2,25-1,67 (m, 14H), 1,32 (d, 6H).
Пример 167. Синтез соединения 167
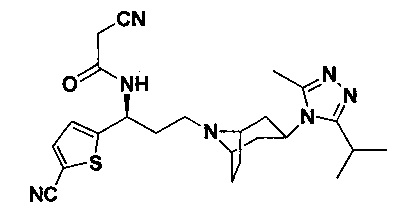
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3,2.1]октан-8-ил]-1-(5-цианотиофен-2-ил)пропил]-2-цианоацетамид
В соответствии со способом синтеза примера 5 соединение 13-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-цианоуксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 167, МС: 465,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,23 (t, 1Н), 7,15 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,32 (s, 2Н), 3,03 (m, 1Н), 2,40 (m,2H), 2,25-1,67 (m, 14Н), 1,32 (d, 6H).
Пример 168. Синтез соединения 168
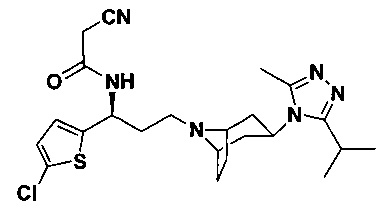
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]-2-цианоацетамид
В соответствии со способом синтеза примера 5, соединение 28-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-цианоуксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 167, МС: 465,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,43 (t, 1Н), 7,35 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,32 (s, 2Н), 3,03 (m, 1Н), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Пример 169. Синтез соединения 169

N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]-2-цианоацетамид
В соответствии со способом синтеза примера 5 соединение 7-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-цианоуксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 169, МС: 458,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 7,48 (t, 1Н), 7,37 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,32 (s, 2Н), 3,03 (m, 1Н), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6H).
Пример 170. Синтез соединения 170
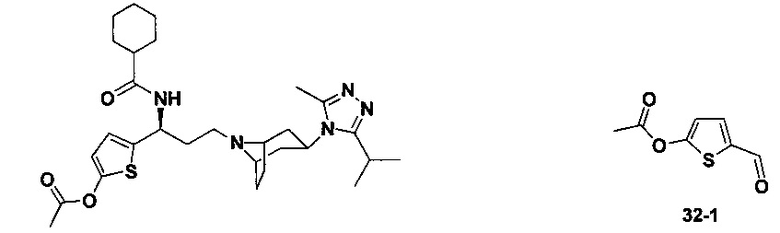
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(5-ацетокситиофен-2-ил)пропил]циклогексан-1-карбоксамид
В соответствии со способом синтеза примера 5, соединение 32-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 170, МС: 542,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,43 (m, 2Н), 5,79 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,43 (m, 5Н), 2,28 (s, 3H), 2,16-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 171. Синтез соединения 171

5-[(1S)-1-(циклогексанформамидо)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-пропил]-N,N-диметилтиофен-2-карбоксамид
В соответствии со способом синтеза примера 5 соединение 32-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и циклогексанкарбоновую кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 171, МС: 555,2 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 6,43 (m, 2Н), 5,79 (m, 1Н), 3,91 (m, 1Н), 3,02 (m, 1Н), 2,93 (s, 6Н), 2,85 (s, 6Н), 2,43 (m, 5Н), 2,16-1,93 (m, 13Н), 1,93-1,61 (m, 10H), 1,36 (d, 6Н).
Пример 172. Синтез соединения 172
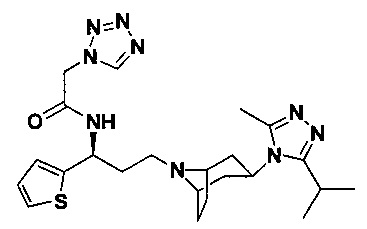
N-[(1S)-3-[экзо-3-(3-изопропил-5-метил-4Н-1,2,4-триазол-4-ил)-8-азабицикло[3.2.1]октан-8-ил]-1-(тиофен-2-ил)пропил]-2-(1Н-тетразол-1-ил)ацетамид
В соответствии со способом синтеза примера 5 соединение 1-1 использовали вместо соединения 2-1 в примере 5, соединение 2f использовали вместо соединения 1f в примере 5, и 2-(1Н-тетразол-1-ил)уксусную кислоту использовали вместо 4,4-дифтор-циклогексанкарбоновой кислоты в примере 5 с получением соединения 172, МС: 484,3 [М+Н]+. 1Н-ЯМР (400 Гц, CDCl3): δ 8,73 (s, 1Н), 7,23 (t, 1Н), 7,15 (d, 1Н), 6,99 (d, 1Н), 5,21 (m, 1Н), 3,95 (m, 1Н), 3,42 (s, 2Н), 3,03 (m, 1Н), 2,40 (m, 2Н), 2,25-1,67 (m, 14Н), 1,32 (d, 6Н).
Экспериментальный пример
Пример 1: Эксперимент по ингибированию притока кальция
Аппарат для эксперимента: FlexStation II
Материалы для эксперимента: линия клеток HEK293/CCR5-Gα16, краситель для кальция Fluo-4 (флуоресцентный-4 краситель на ион кальция) и прибор FlexStation.
Теория эксперимента: посредством основания линии клеток, котрансфицированных хемокиновым рецептором (CCR5) и Gα16, активация рецептора может вызвать активацию белка Gα16, в результате чего активируется фосфолипаза С (PLC) с образованием трис-фосфата инозита 3 (IP3) и диацилглицерина (DAG). IP3 может связываться с рецепторами IP3 на эндоплазматическом ретикулуме и митохондриях в клетке, что может вызывать высвобождение внутриклеточного кальция. Таким образом, изменения внутриклеточного кальция можно использовать как способ обнаружения состояния активации CCR5. Fluo-4/ацетоксиметил (AM) представляет собой индикатор флуоресцентного зонда для кальция, используемый для измерения иона кальция. Поскольку он является неполярным жирорастворимым соединением, после его проникновения в клетку группа AM диссоциирует с высвобождением Fluo-4 под действием фермента клеточного липолиза. Fluo-4 представляет собой полярную молекулу и с трудом проходит через липидную бислойную мембрану, поэтому он может оставаться внутри клеток в течение длительного времени. Наконец, уровень активированного белка Ga может отражаться путем измерения интенсивности возбужденной флуоресценции. Если соединение, подвергаемое скринингу, может активировать CCR5, оно может значительно усиливать реакцию притока кальция; напротив, если соединение, подвергаемое скринингу, может антагонизировать CCR5, оно может значительно уменьшить реакцию притока кальция.
Стадии эксперимента:
1. Клетки HEK293, способные стабильно экспрессировать CCR5, засевали в 96-луночный планшет и инкубировали в течение ночи.
2. Среду в каждой лунке, засеянной клетками, удаляли и добавляли 40 мкл/лунка свежеприготовленного красителя. Планшет помещали в термостат на 37°С и инкубировали в течение 40 минут при постоянной температуре.
3. Определяемое лекарственное средство разводили кальциевым буфером до восьми градиентов концентрации, составляющих 1×10-4M, 1×10-5М, 1×10-6M, 1×10-7М, 1×10-8М, 1×10-9M, 1×10-10М и 1×10-11М соответственно, и смешивали до однородного состояния.
4. Краситель удаляли. Свежеприготовленный кальциевый буфер использовали для однократной отмывки, добавляя 50 мкл кальциевого буфера.
5. Для обнаружения использовали прибор FlexStation II. 25 мкл кальциевого буфера, содержащего определяемое лекарственное средство, добавляли автоматически с 15й секунды. Считывали конечное значение флуоресценции при 525 нм.
Результаты эксперимента:


Примечание: В качестве положительных контрольных соединений использовали следующие структуры PF-232798 и маравирока (подобные приведенным в данном документе ниже):
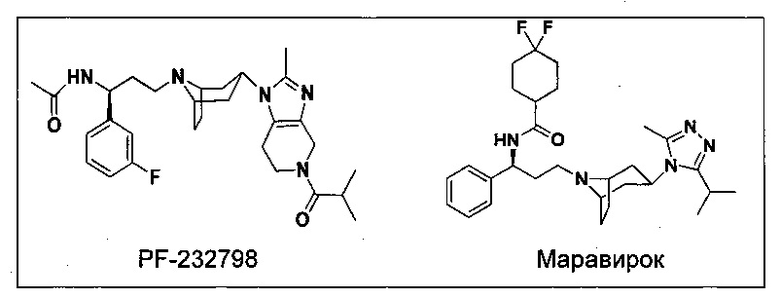
Заключение эксперимента: Из приведенных в таблице 1 данных видно, что все соединения обладают сильными действиями в качестве ингибиторов притока кальция, при этом соединение 3, 6, 13, 14, 16, 17, 18, 20, 22, 26, 29, 39, 64, 65, 66, 119, 123, 124, 131, 133, 146, 147, 148, 150, 151, 157, 160, 162, 164, 166, 168, 169, 170, 171 и 172 превосходят положительные контрольные соединения, и соединения 15, 21, 27, 31, 32, 37, 38, 135, 137, 138, 141, 142, 149, 152, 155, 156, 159, 161, 165 и 167 сравнимы с положительными контрольными соединениями.
Пример 2: Термостабильность белкового теста (количественное определение с помощью СРМ)
Теория эксперимента: в белковой последовательности CCR5 присутствуют многочисленные цистеины. Цистеины, расположенные в области петли, образуют дисульфидные связи, стабилизирующие третичную структуру белка. Некоторые свободные цистеины в восстановленном состоянии расположены в трансмембранной области. При возбуждении падающим светом 387 нм комбинация свободной сульфгидрильной группы и флуоресцентного красителя СРМ может испускать возбуждающий свет 436 нм. Если температуру постепенно повышать искусственно, третичная структура мембранного белка постепенно ослабевает по мере повышения температуры. Свободные сульфгидрильные группы, исходно расположенные в трансмембранной области, подвергают воздействию и объединяют с флуоресцентным красителем, а затем детектор обнаружит изменения усиления сигнала. Таким образом, термостабильность мембранных белков можно определять в соответствии с температурой (Tm) в средней точке изменений интенсивности сигнала.
Стадии эксперимента: После предварительной очистки полученный раствор белка переносили в небольшую пробирку для концентрирования (100 кДа, 500 мкл) для концентрирования (1000×g, 12 мин, 4°С). После центрифугирования пробирку для концентрирования извлекали и постукивали по ней, чтобы предотвратить коагуляцию белка за счет высокой локальной концентрации. Конечный объем концентрирования составлял приблизительно 50 мкл. В пробирку типа Эппендорф на 2 мл добавляли 117 мкл очищенного раствора (объем подходит для получения суммарного объема 120 мкл), 1 мкл флуоресцентного красителя СРМ (внутрифирменного приготовления) и 2 мкл концентрированного раствора белка (количество добавленного белка составляет 3-5 мкг в соответствии с расчетной концентрацией раствора белка и объемом концентрирования) и инкубировали при комнатной температуре в течение 20 мин, а затем смесь добавляли в кювету (Qwan) и помещали в оборудование для тестирования Cary, поверхностью замороженного стекла наружу. Температуру устанавливали в диапазоне от 4 до 90°С с повышением на 1°С в минуту и запускали программу. Значение Tm можно получить путем обработки данных и построения графика с помощью программного обеспечения для картирования, и данное значение можно использовать для сравнения различия термостабильности белка в различных условиях.
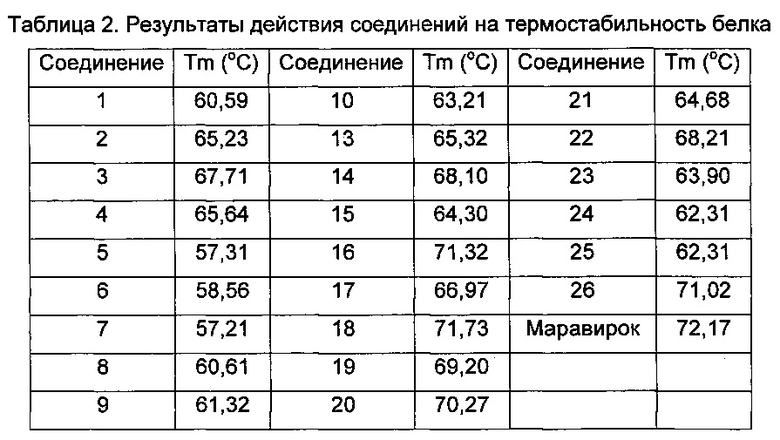
Из таблицы 2 видно, что все соединения обладают сильным действием на стабильность белка, при этом соединения 16, 18, 20 и 26 сравнимы с положительным контрольным соединением.
Пример 3: Предварительное скрининговое тестирование активности против ВИЧ-1 in vitro
1. Материалы эксперимента
Фосфатно-солевой буферный раствор (ФСБ), стрептомицина сульфат, ГЭПЭС (N-2(2-гидроксиэтил)пиперазин-N'-(2-этансульфоновая кислота), МТТ (3(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромид), пенициллин, глутамин, 2-меркаптоэтанол, RPMI-1640, полная среда RPMI-1640 с фетальной бычьей сывороткой (ФБС).
2. Титрование инфекционности ВИЧ-1
Вирус титровали в соответствии с модифицированным способом Johnson & Byington. Кратко, основной раствор ВИЧ-1 подвергали четырехкратному разведению в 96-луночном планшете (десять градиентов) в шести параллельных анализах для каждого градиента, при этом ставили шесть контрольных лунок. В каждую лунку добавляли 100 мкл (5*106/мл) стимулированных фитогемагглютинином (ФГА) мононуклеарных клеток периферической крови (МКПК), и конечный объем на лунку составлял 200 мкл. Клетки культивировали при 37°С с 5% СО2. На третьи сутки добавляли 100 мкл свежей полной среды RPMI-1640. На седьмые сутки инфицированный супернатант собирали и подвергали лизису 0,5% тритоном Х100. Антиген р24 определяли с помощью иммуноферментного анализа (ИФА), и 50% инфекционную дозу вируса в тканевой культуре (TCID50) вычисляли в соответствии со способом Reed & Muench (50% Tissue culture infection dose).
3. Тест на токсичность соединений на клетках HOS-CD4-CCR5, РМ1 и МКПК
Тестируемое соединение подвергали 5-кратному разведению в 96-луночном микротитрационном планшете полной средой RPMI-1640 или модифицированной Дульбекко средой Игла (DMEM) (содержащей 10% ФБС) (шесть разведений) в трех параллельных анализах для каждого разведения, и 100 мкл на каждую лунку. При этом лунки, не содержащие лекарственное средство, ставили в качестве контроля. В каждую лунку добавляли 100 мкл 4×105/мл клеток РМ1, HOS-CD4-CCR5 или 100 мкл 5×106/мл ФГА-стимулированных МКПК. Клетки культивировали при 37°С с 5% СО2 в течение трех суток (клетки МКПК культивировали в течение семи суток, и на третьи сутки добавляли 100 мкл свежей полной среды RPMI-1640). Цитотоксичность тестировали с помощью количественного анализа МТТ. Значения OD измеряли с помощью считывающего устройства для микропланшетов ELx800. Длина волны обнаружения составляла 570 нм, а опорная длина волны составляла 630 нм. Вычисляли значения СС50 (50% цитотоксическая концентрация).
4. Количественный анализ ингибирующего действия соединений на репликацию вируса в клетках HOS-CD4-CCR5, инфицированных ВИЧ-1SF162 или ВИЧ-1Ba-L
За сутки до теста 1×105/мл клетки HOS-CD4-CCR5 засевали в 96-луночные планшеты по 100 мкл в каждую лунку. Тестируемое соединение подвергали 5-кратному разведению в 96-луночном микротитрационном планшете полной средой DMEM (содержащей 10% ФБС). Исходная концентрация составляла 1 мкМ, и было получено шесть разведений. Ставили три параллельных анализа на каждое разведение, и каждая лунка содержала 100 мкл смеси. При этом лунки, не содержащие лекарственное средство, ставили в качестве контроля. Супернатант удаляли, добавляли 100 мкл лекарственного средства и инкубировали в течение 2 ч. Затем к разведенному супернатанту добавляли 100 мкл ВИЧ-1SF162 и ВИЧ-1Ba-L. Клетки инфицировали в течение 1 ч, свободный вирус вымывали и добавляли лекарственное средство в одинаковой конечной концентрации. В качестве положительного контроля использовали MVC. Клетки культивировали при 37°С с 5% СО2 в течение трех суток. Супернатант собирали, лизировалий инактивировали 0,5% тритоном Х-100. Ингибирующее действие лекарственного средства на репликацию ВИЧ-1 определяли с использованием способа ИФА с иммобилизующим антигеном р24.
5. Анализ ингибирующего действия соединений на репликацию вируса в клетках МКПК, инфицированных ВИЧ-1SF162, ВИЧ-1Ba-L или ВИЧ-1KM018.
Тестируемые соединения подвергали 5-кратному разведению в 48-луночной планшете полной средой RPMI-1640 (содержащей 10% ФБС). Исходная концентрация составляла 1 мкМ, было получено шесть разведений, и каждая лунка содержала 200 мкл смеси. При этом лунки, не содержащие лекарственное средство, ставили в качестве контроля. Вирус (множественность инфекции (MOI)=0,01) добавляли к 5×106/мл МКПК, которые были стимулированы ФГА в течение 72 ч. После перемешивания до однородного состояния смесь сразу добавляли в 48-луночный планшет, содержащий разведенное лекарственное средство, и в каждую лунку добавляли 200 мкл смеси. MVC использовали в качестве положительного контроля. Клетки культивировали при 37°С с 5% СО2 в течение семи суток (лекарственное средство такой же концентрации добавляли на третьи сутки). Супернатант собирали, подвергали лизису и инактивировали 0,5% тритоном Х-100. Ингибирующее действие лекарственного средства на репликацию ВИЧ-1 определяли, используя способ ИФА с иммобилизующим антигеном р24.
6. Результаты эксперимента:
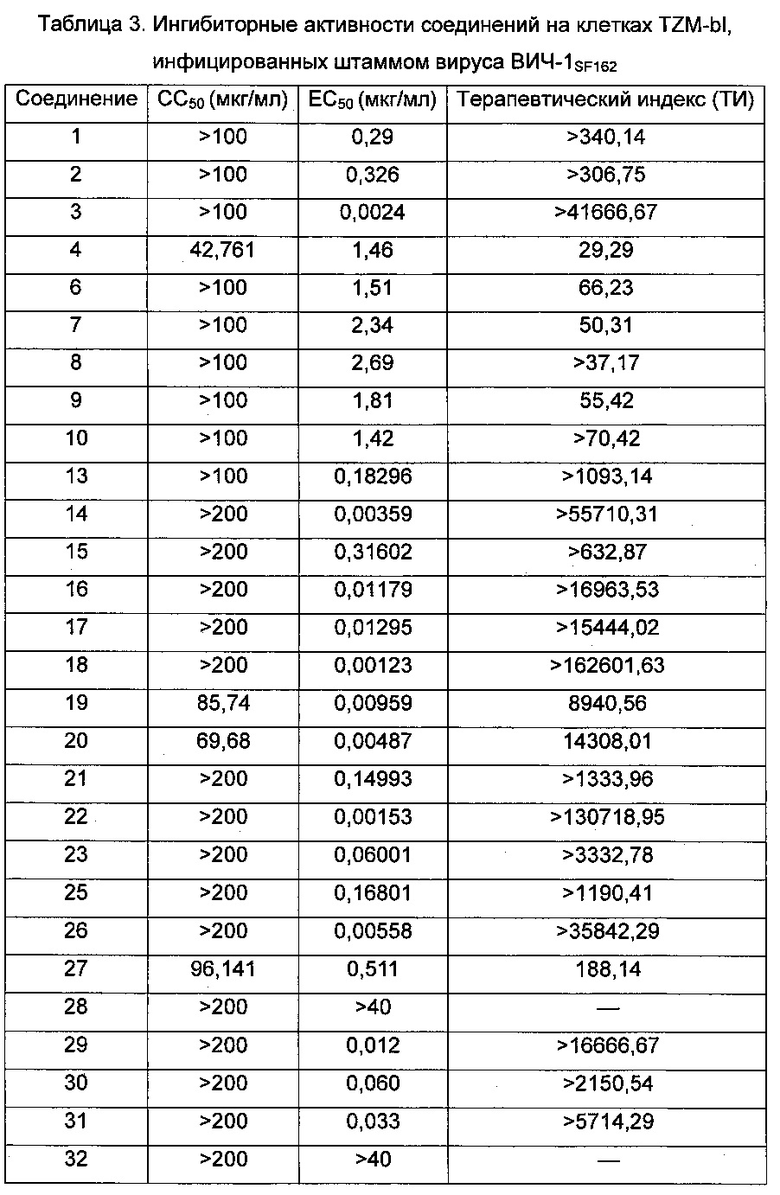
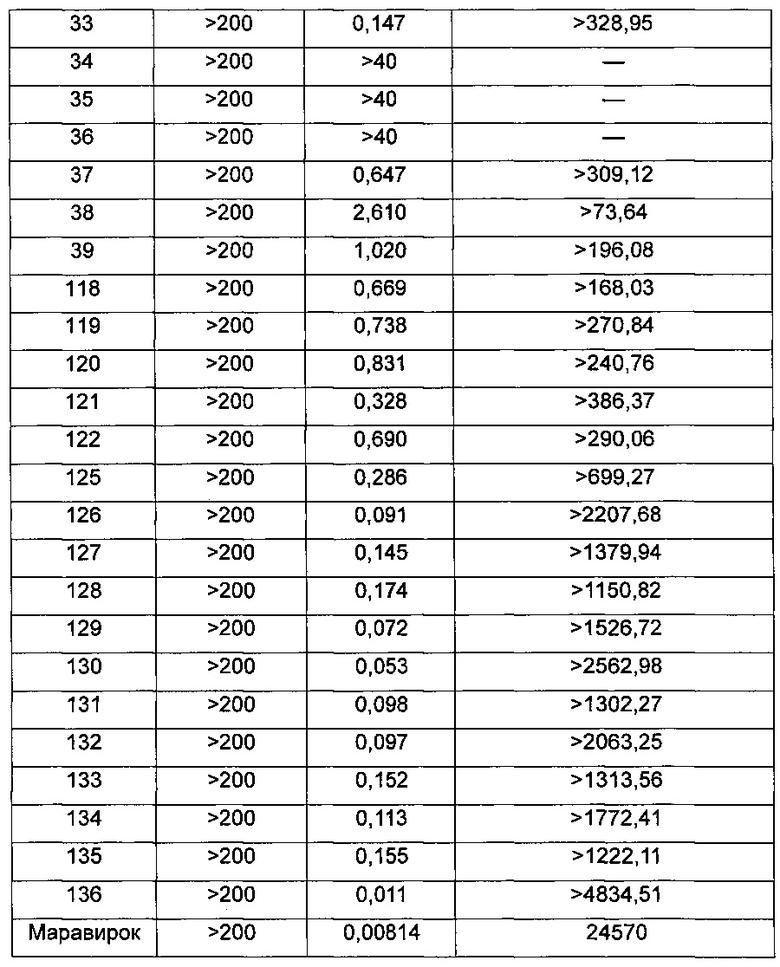
Вывод эксперимента: Из данных, приведенных в таблице выше, видно, что на клетках TZM-bl, инфицированных штаммом вируса ВИЧ-1SF162, соединения по настоящему изобретению проявляют более низкую цитотоксичность in vitro и более высокий терапевтический индекс, при этом соединения 3, 14, 18, 22 и 26 превосходят положительное контрольное соединение, а соединения 16, 17, 20 и 29 сравнимы с положительным контрольным соединением.
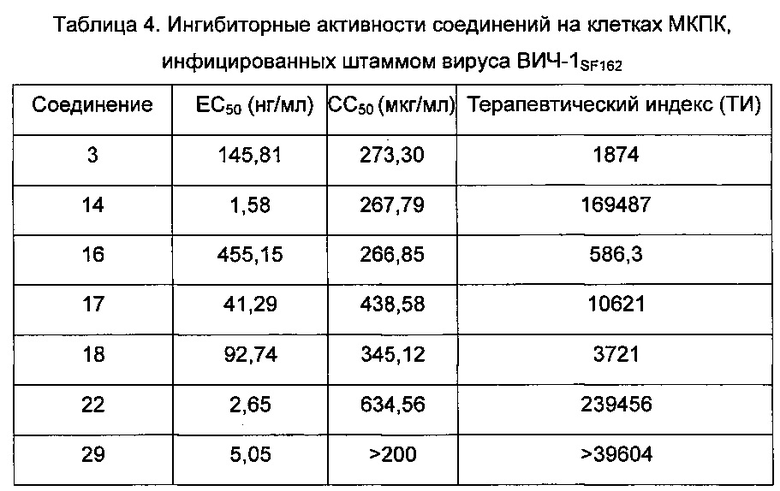
Вывод эксперимента: Из данных, приведенных в таблице выше, видно, что на клетках МКПК, инфицированных штаммом вируса ВИЧ-1SF162, соединения по настоящему изобретению проявляют более низкую цитотоксичность in vitro и более высокий терапевтический индекс, при этом соединения 14, 22 и 29 имеют более высокий терапевтический индекс, а терапевтический индекс соединения 22 даже достигает 239456.
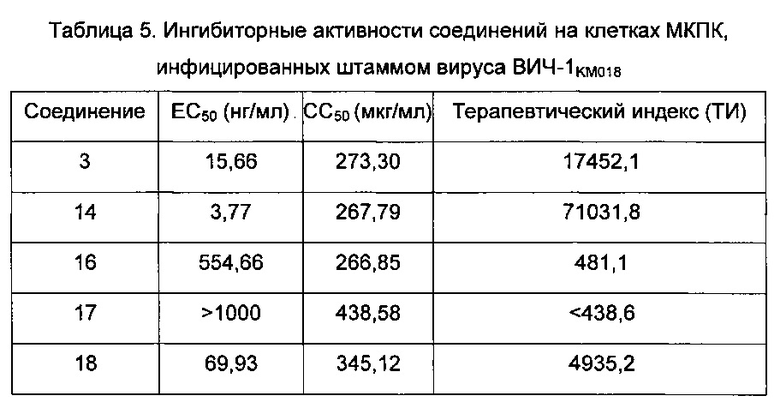

Вывод эксперимента: Из данных, приведенных в таблице выше, видно, что на клетках МКПК, инфицированных штаммом вируса ВИЧ-1KM018, соединения по настоящему изобретению проявляют более низкую цитотоксичность in vitro и более высокий терапевтический индекс, при этом соединения 3, 14 и 22 имеют относительно более высокий терапевтический индекс, и терапевтический индекс соединения 22 даже достигает 119054,4.
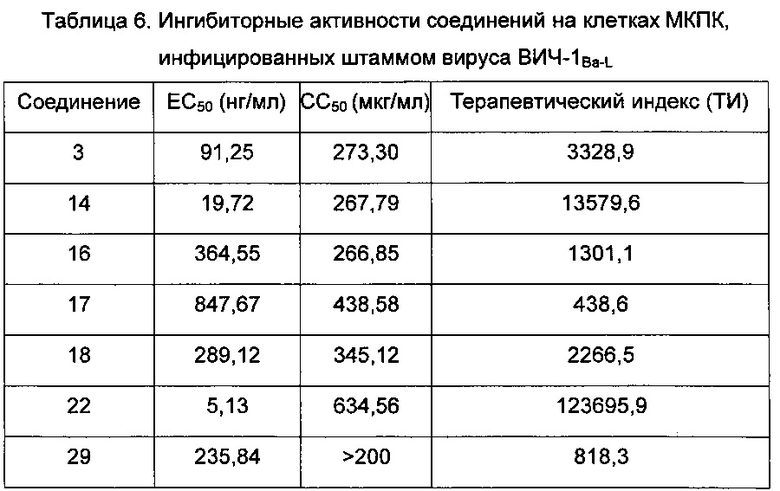
Вывод эксперимента: Из данных, приведенных в таблице выше, видно, что на клетках МКПК, инфицированных штаммом вируса ВИЧ-1Ba-L, соединения по настоящему изобретению проявляют более низкую цитотоксичность in vitro и более высокий терапевтический индекс, при этом соединения 14 и 22 имеют относительно более высокий терапевтический индекс, и терапевтический индекс соединения 22 даже достигает 123695,9.
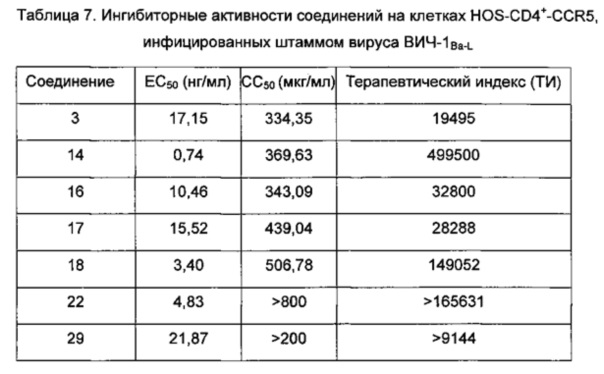
Вывод эксперимента: Из данных, приведенных в таблице выше, видно, что на клетках HOS-CD4+-CCR5, инфицированных штаммом вируса ВИЧ-1Ba-L, соединения по настоящему изобретению проявляют более низкую цитотоксичность in vitro и более высокий терапевтический индекс, при этом соединения 14, 16, 17, 18 и 22 имеют относительно более высокий терапевтический индекс, и терапевтический индекс соединения 14 даже достигает 499500.
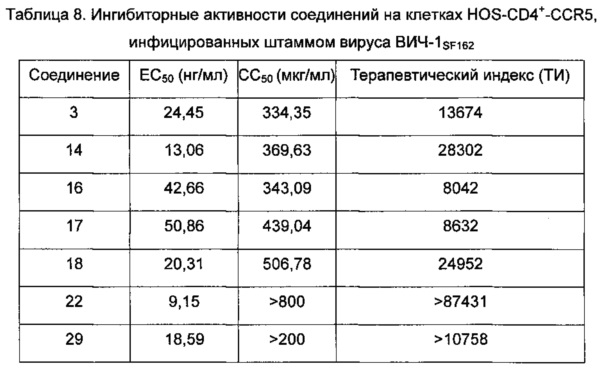
Вывод эксперимента: Из данных, приведенных в таблице выше, видно, что на клетках МКПК, инфицированных штаммом вируса ВИЧ-1Ba-L, соединения по настоящему изобретению проявляют более низкую цитотоксичность in vitro и более высокий терапевтический индекс, при этом соединения 3, 14, 18, 22 и 29 имеют относительно более высокий терапевтический индекс, и терапевтический индекс соединения 14 достигает даже 28302.
Пример 4: Анализ активности ингибирования hERG
1. Материалы эксперимента:
Фетальная телячья сыворотка (Gibco, № по каталогу 10099), гигромицин В (Invitrogen, № по каталогу В13871010), набор для анализа FluxOR™ (Invitrogen, № по каталогу F0017), 96-луночный планшет (Corning, № по каталогу 3894), положительные контроли: дофетилид, цизаприд и маравирок.
2. Стадии эксперимента:
1. К клеткам CHO-hERG, проинкубированным в течение ночи, добавляли буфер для пробы и инкубировали в течение 90 минут при комнатной температуре в темноте.
2. Буфер для пробы удаляли и добавляли аналитический буфер.
3. В планшет с клетками добавляли соединение и инкубировали в течение 20 минут в темноте.
4. Планшет с клетками помещали в прибор FDSS. Флуоресцентный сигнал регистрировали каждую секунду в течение 10 секунд. К клеткам добавляли возбуждающий буфер на 10й секунде, и флуоресцентный сигнал регистрировали каждую секунду в течение 180 секунд.
5. Проводили обработку данных.
3. Результаты эксперимента:

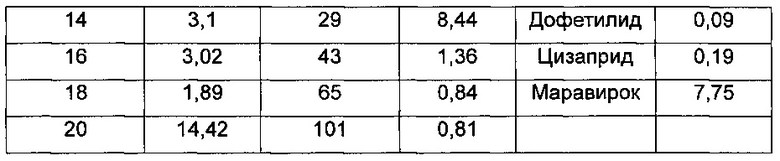
Вывод эксперимента: Из данных, приведенных в таблице выше, видно, что соединения по настоящему изобретению обладают более слабой ингибиторной активностью в отношении hERG, где ингибиторные активности соединений 8, 12, 20, 22, 29 и 107 в отношении hERG превосходят активности положительных контрольных соединений.
Пример 5. Эксперимент по фармакокинетике у крыс
1. Стадии эксперимента:
Шесть здоровых самцов крыс массой 150-200 г случайным порядком делили на 2 группы по 3 крысы для каждой группы. Крысам в каждой группе вводили соединения 14, 16, 17, 18, 22 и 29 соответственно через зонд или путем внутривенной инъекции. Объем введения составлял 10 мл/кг, и лекарственное средство включали в препарат ДМСО/Твин 80/физиологический раствор (5 : 5 : 90, об/об/об). Перед тестом крыс выдерживали натощак в течение 12 ч и давали возможность пить воду вволю. Через 2 ч после дозирования крысы питались вместе с остальными.
2. Моменты времени отбора проб крови и обработка пробы:
Внутрижелудочное введение: 0,25, 0,5, 1,0, 2,0, 4,0, 6,0, 8,0 и 24 ч после введения.
Внутривенное введение: 5 мин, 0,25, 0,5, 1,0, 2,0, 4,0, 6,0, 8,0 и 24 ч после введения.
В указанные выше моменты времени брали 0,3 мл венозной крови из ретробульбарного венозного сплетения крысы и вносили в антикоагулянтную пробирку ЭДТА (этилендиаминтетрауксусная кислота) -2К. После центрифугирования при 11000 об/мин в течение 5 мин плазму отделяли и замораживали при -20°С в морозильнике.
3. Тестирование пробы и анализ данных
Концентрацию каждого соединения в плазме крови крысы определяли с помощью жидкостной хроматографии с тандемной масс-спектрометрией (ЖХ/МС/МС).
Фармакокинетические параметры после введения вычисляли путем использования некомпартментной модели программного обеспечения WinNonlin 5.3 (Pharsight Corporation, США).
4. Результаты эксперимента:
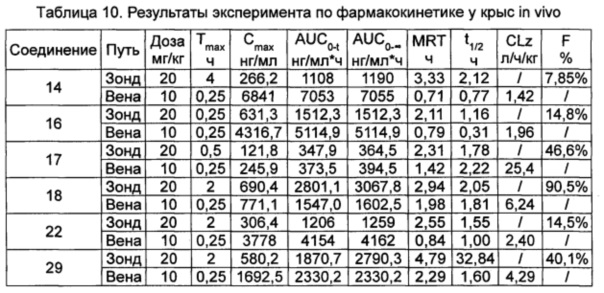
Соединение 14: После введения крысам 20 мг/кг соединения 14 через зонд Tmax (время достижения пика максимальной концентрации в плазме) составляет 4 ч, пиковая концентрация Cmax составляет 266,2 нг/мл, площадь под кривой лекарственного средства по времени AUC0-t составляет 1108 нг⋅ч/мл, и конечный период полувыведения t1/2 составляет 2,12 ч. После введения крысам 10 мг/кг соединения 14 через вену AUC0-t составляет 7053 нг⋅ч/мл. После нормализации дозы абсолютная биодоступность 20 мг/кг соединения 14, вводимого крысам через зонд, составляет 7,85%.
Соединение 16: После введения крысам 20 мг/кг соединения 16 через зонд Tmax (время достижения пика максимальной концентрации в плазме) составляет 0,25 ч, пиковая концентрация Cmax составляет 631,3 нг/мл площадь под кривой лекарственного средства по времени AUC0-t составляет 1512,3 нг⋅ч/мл, и конечный период полувыведения t1/2 составляет 1,16 ч. После введения крысам 10 мг/кг соединения 16 через вену AUC0-t составляет 5114,9 нг⋅ч/мл. После нормализации дозы абсолютная биодоступность 20 мг/кг соединения 16, вводимого крысам через зонд, составляет 14,8%.
Соединение 17: После введения крысам 20 мг/кг соединения 17 через зонд Tmax (время достижения пика максимальной концентрации в плазме) составляет 0,5 ч, пиковая концентрация Cmax составляет 121,8 нг/мл, площадь под кривой лекарственного средства по времени AUC0-t составляет 347,9 нг⋅ч/мл, и конечный период полувыведения t1/2 составляет 1,78 ч. После введения крысам 10 мг/кг соединения 17 через вену AUC0-t составляет 373,5 нг⋅ч/мл. После нормализации дозы абсолютная биодоступность 20 мг/кг соединения 17, вводимого крысам через зонд, составляет 46,6%.
Соединение 18: После введения крысам 20 мг/кг соединения 18 через зонд Tmax (время достижения пика максимальной концентрации в плазме) составляет 2 ч, пиковая концентрация Cmax составляет 690,4 нг/мл, площадь под кривой лекарственного средства по времени AUC0-t составляет 2801,1 нг⋅ч/мл, и конечный период полувыведения t1/2 составляет 2,05 ч. После введения крысам 10 мг/кг соединения 18 через вену AUC0-t составляет 1547,0 нг⋅ч/мл. После нормализации дозы абсолютная биодоступность 20 мг/кг соединения 18, вводимого крысам через зонд, составляет 90,5%.
Соединение 22: После введения крысам 20 мг/кг соединения 22 через зонд Tmax (время достижения пика максимальной концентрации в плазме) составляет 2 ч, пиковая концентрация Cmax составляет 306,4 нг/мл, площадь под кривой лекарственного средства по времени AUC0-t составляет 1206 нг⋅ч/мл, и конечный период полувыведения t1/2 составляет 1,55 ч. После введения крысам 10 мг/кг соединения 22 через вену AUC0-t составляет 4154 нг⋅ч/мл. После нормализации дозы абсолютная биодоступность 20 мг/кг соединения 22, вводимого крысам через зонд, составляет 14,5%.
Соединение 29: После введения крысам 20 мг/кг соединения 29 через зонд Tmax (время достижения пика максимальной концентрации в плазме) составляет 2 ч, пиковая концентрация Cmax составляет 580,2 нг/мл, площадь под кривой лекарственного средства по времени AUC0-t составляет 1870,7 нг⋅ч/мл, и конечный период полувыведения t1/2 составляет 32,84 ч. После введения крысам 10 мг/кг соединения 29 через вену AUC0-t составляет 2330,2 нг⋅ч/мл. После нормализации дозы абсолютная биодоступность 20 мг/кг соединения 29, вводимого крысам через зонд, составляет 40,1%.
Вывод эксперимента: Из приведенных выше результатов теста видно, что в эксперименте по фармакокинетике у крыс соединение 18 проявляет превосходную абсолютную биодоступность, достигающую 90,5%; и соединения 17 и 29 проявляет хорошую абсолютную биодоступность, достигающую 46,6% и 40,1% соответственно, значительно более высокую по сравнению с препаратом MVC Mara Calvino, имеющимся в продаже (по сообщениям только 5% биодоступность).
Пример 6: Эксперимент по фармакокинетике у собак породы бигль
1. Стадии эксперимента:
Шесть здоровых самцов собак породы бигль массой 9-11 кг делили случайным порядком на 2 группы по 3 в каждой группе. Собакам бигль в каждой группе вводили соединение 22 по настоящему изобретению через зонд или путем внутривенной инъекции. Объем введения составлял 2 мл/кг и 1 мл/кг соответственно. Для введения через зонд соединение суспендировали в 20% ПЭГ 400 (4:96), а для внутривенной инъекции включали в препарат ДМСО/Твин 80/физиологический раствор (5:1:94, об/об/об) для внутривенной инъекции. Перед тестом собак бигль выдерживали натощак в течение 12 ч и давали возможность пить воду вволю. Через 2 ч после дозирования собаки питались вместе с остальными.
2. Моменты времени отбора проб крови и обработка пробы:
Внутрижелудочное введение: 0,25, 0,5, 1,0, 2,0, 4,0, 6,0, 8,0 и 24 ч после введения.
Внутривенное введение: 5 мин, 0,25, 0,5, 1,0, 2,0, 4,0, 6,0, 8,0 и 24 ч после введения.
В указанные выше моменты времени брали 0,6 мл венозной крови из вены конечности и вносили в антикоагулянтную пробирку ЭДТА-2К. После центрифугирования при 11000 об/мин в течение 5 мин, плазму отделяли и замораживали при -20°С в морозильнике.
3. Тестирование пробы и анализ данных
Концентрацию каждого соединения в плазме крови крысы определяли с помощью жидкостной хроматографии с тандемной масс-спектрометрией (ЖХ/МС/МС).
Фармакокинетические параметры после введения вычисляли путем использования некомпартментной модели программного обеспечения WinNonlin 5.3 (Pharsight Corporation, США).
4. Результаты эксперимента:

Соединение 22: После введения собакам бигль 15 мг/кг соединения 22 через зонд Tmax (время достижения пика максимальной концентрации в плазме) составляет 0,8333 ч, пиковая концентрация Cmax составляет 4613 нг/мл, площадь под кривой лекарственного средства по времени AUC0-t составляет 5426 нг⋅ч/мл, и конечный период полувыведения t1/2 составляет 3,89 ч. После введения 3 мг/кг соединения 22 собакам бигль через вену AUC0-t составляет 10877 нг⋅ч/мл. После нормализации дозы абсолютная биодоступность 15 мг/кг соединения 22, вводимого собакам бигль через зонд, составляет 9,98%.
Из приведенных выше результатов теста видно, что в эксперименте по фармакокинетике у собак породы бигль соединение 22 проявляет хорошую абсолютную биодоступность.
Пример 7: Анализ на обратные мутации у бактерий
1. Схема эксперимента
Определяли мутагенные действия соединений 18 и 22 по настоящему изобретению на штаммах Salmonella typhimurium ТА98 и ТА100 в условиях неметаболической активации (-S9). Для анализа обратных мутаций у бактерий для соединений 18 и 22 были выбраны два штамма ТА98 и ТА100. В эксперименте ставили 9 доз, содержащих 1, 3, 10, 30, 100, 300, 1000, 3000 и 5000 мкг/чашка, отрицательные и положительные контроли. На каждую дозу использовали 3 чашки. Эксперимент проводили в условиях -S9.
2. Результаты эксперимента
Соединения 18 и 22 ни при одной дозе не увеличивали число колоний ревертантов ТА98 и ТА100, и ни при одной дозе не наблюдали значимой бактериальной токсичности. Заключили, что соединения 18 и 22 не обладают мутагенным действием на штаммы Salmonella typhimurium ТА98 и ТА100.

Заключение эксперимента: Из приведенных выше результатов теста видно, что соединения 18 и 22 не обладают мутагенным действием на штаммы Salmonella typhimurium ТА98 и ТА100 в условиях настоящего эксперимента. Пример 8: Количественное определение ингибиторной активности в отношении различных подсемейств фермента CYP450
1. Материалы эксперимента
Наборы для скрининга VividR CYP450 и считывающее устройство для микропланшетов Envision 2101 и т.д.
2. Теория эксперимента
Наборы для скрининга VividR CYP450 можно использовать для оценки действия на подтипы CYP450 (CYP1A2, CYP2D6, CYP2C9, CYP2C19, CYP3A4-T и CYP3A4-M), и субстрат VividR в наборе может метаболизироваться с образованием продукта, который может испускать сильную флуоресценцию в водном растворе посредством специфичных ферментов CYP450.
3. Стадии эксперимента
1. Тестируемые соединения и положительное соединение добавляли в соответствующие лунки, и в контрольные лунки добавляли ДМСО.
2. К тестируемым соединениям, положительному соединению и в контрольные лунки ДМСО добавляли фермент CYP450. В качестве контроля фона вместо фермента использовали разведение фермента и добавляли в лунки ДМСО. Смесь перемешивали с помощью вибрации в течение 1 минуты, а затем инкубировали при комнатной температуре в течение 20 минут.
3. Для инициации реакции добавляли систему регенерации никотинамиддинуклеотидфосфата (НАДФ+) и субстрат и инкубировали при комнатной температуре в течение 60 минут.
4. Для регистрации флуоресцентного сигнала использовали многофункциональное считывающее устройство Envision 2101 в условиях возбуждения 480 нм и испускания 530 нм.
4. Результаты эксперимента

Вывод эксперимента: Значения IC50 ингибиторной активности соединений 16, 17, 18, 22 и 29 в отношении шести подтипов CYP450 составляют более 10 мкМ. Ингибиторные активности соединений являются достаточно слабыми и лучшими по сравнению с Маравироком.
Пример 9: Четырехсуточный тест на острую токсичность у крыс
1. Цель эксперимента
После введения крысам линии Спрэг-Доули (SD) соединений 18 и 22 по настоящему изобретению через зонд в течение 4 последовательных суток токсическую реакцию предварительно оценивали для подтверждения возможного органа-мишени токсической реакции.
2. Схема эксперимента
Ставили четыре группы дозы 100 и 1000 мг/кг соединения 18, 100 и 1000 мг/кг соединения 22. Ставили одну контрольную группу носителя. Каждая группа дозы содержала четырех крыс, включающих двух самцов крыс и двух самок крыс. Во время стадии эксперимента ежесуточно проводили клинический осмотр животных. Регулярно измеряли массу тела. На 5-е сутки всех животных подвергали патологическому исследованию и проводили макроскопическое анатомическое исследование.
3. Результаты эксперимента
По сравнению с животными в контрольной группе носителя прибавление массы у некоторых самцов и самок животных в группе дозы соединения 18 (100 и 1000 мг/кг) и соединения 22 (100 и 1000 мг/кг) нарастало медленно или проявляло отрицательный рост. Клинические наблюдения, определение клинической патологии (гематология и биохимия сыворотки) и макроскопическое морфологическое обследование не показало значительных изменений, связанных с лекарственным средством.
Вывод эксперимента: Подводя итог, в данных условиях эксперимента уровень, не вызывающий видимых нежелательных явлений (NOAEL, No Observed Adverse Effect Level), составляет 1000 мг/кг для крыс SD, которым вводили соединение 18 через зонд в течение 4 суток, и NOAEL составлял 1000 мг/кг для крыс SD, которым вводили соединение 22 через зонд в течение 4 суток. Таким образом, соединения обладают высокой безопасностью.
Все документы, на которые ссылаются в настоящем изобретении, включены посредством ссылки, как если бы каждая ссылка цитировалась отдельно в настоящей заявке в виде ссылки. Кроме того, следует понимать, что по прочтении описанных выше положений настоящего изобретения специалистами в данной области техники могут быть проведены различные изменения или модификации изобретения, и данные эквивалентные формы также входят в объем, определенный прилагаемой формулой настоящей заявки.
Изобретение относится к соединению формулы I, в которой W представляет собой -СН2СН2-; X представляет собой N или CR6; R1 выбран из 5-6-членного гетероарила, незамещенного или замещенного от 1 до 3 заместителями, где указанный гетероарил содержит от 1 до 2 гетероатомов, выбранных из атома серы или азота, и каждый из указанных заместителей независимо выбран из атома галогена, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 алкокси, -NR10R11, -C(=O)R12, прямого или разветвленного С1-С4 алканоилокси, циано, нитро, или два соседних заместителя вместе с присоединенным атомом углерода образуют 6-членное ароматическое кольцо, 5-членное насыщенное кольцо или 5-членное гетероциклическое кольцо, содержащее 2 гетероатома, выбранных из атома кислорода; R2 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С6 алкила, С3-С7 циклоалкила, 6-членной гетероциклической группы, содержащей 1 гетероатом, выбранный из атома азота, С6-арила; где указанный заместитель выбран из группы, состоящей из атома галогена, прямого или разветвленного С1-С4 алкила, прямой или разветвленной С1-С4 алкилсульфонильной группы, тетразолила, циано; каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н, прямого или разветвленного С1-С6 алкила; значения остальных радикалов указаны в формуле изобретения. Изобретение также относится к способу получения, к фармацевтической композиции и к применениям соединения. Технический результат: получены новые соединения формулы I, которые обладают свойствами антагониста CCR5 и могут применяться для лечения инфекции вируса иммунодефицита человека (ВИЧ). 6 н. и 4 з.п. ф-лы, 13 табл., 181 пр.
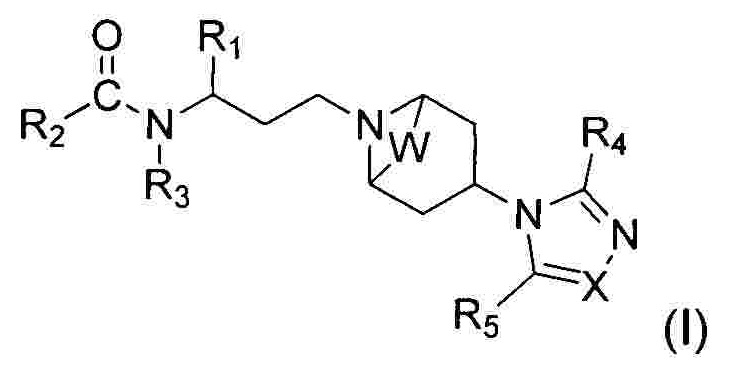
1. Соединение формулы I, его фармацевтически приемлемая соль, энантиомер или их смесь,

где
W представляет собой -СН2СН2-;
X представляет собой N или CR6;
R1 выбран из 5-6-членного гетероарила, незамещенного или замещенного от 1 до 3 заместителями, где указанный гетероарил содержит от 1 до 2 гетероатомов, выбранных из атома серы или азота, и каждый из указанных заместителей независимо выбран из атома галогена, прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 алкокси, -NR10R11, -C(=O)R12, прямого или разветвленного С1-С4 алканоилокси, циано, нитро, или два соседних заместителя вместе с присоединенным атомом углерода образуют 6-членное ароматическое кольцо, 5-членное насыщенное кольцо или 5-членное гетероциклическое кольцо, содержащее 2 гетероатома, выбранных из атома кислорода;
каждый из R10 и R11 независимо выбран из группы, состоящей из Н и -C(=O)R13;
R12 выбран из группы, состоящей из прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 алкокси, амино (NH2), прямого или разветвленного С1-С4 алкиламино и прямого или разветвленного диС1-С4 алкиламино;
R13 выбран из группы, состоящей из Н и прямого или разветвленного С1-С4 алкила;
R2 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С6 алкила, С3-С7 циклоалкила, 6-членной гетероциклической группы, содержащей 1 гетероатом, выбранный из атома азота, С6-арила; где указанный заместитель выбран из группы, состоящей из атома галогена, прямого или разветвленного С1-С4 алкила, прямой или разветвленной С1-С4 алкилсульфонильной группы, тетразолила, циано;
каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н, прямого или разветвленного С1-С6 алкила;
R5 и R6 могут связываться вместе с 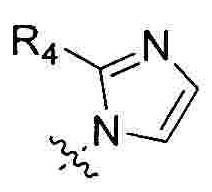 с образованием
с образованием 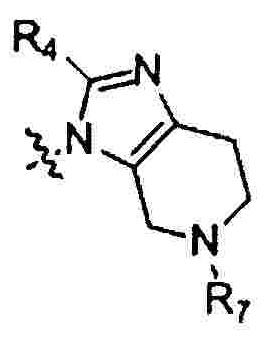 или
или 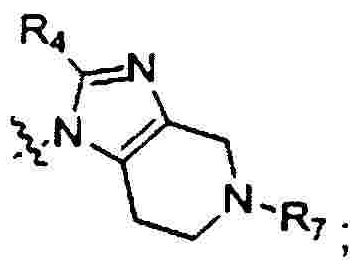
R7 выбран из группы, состоящей из C(=O)R8, C(=O)OR8;
R8 выбран из группы, состоящей из прямого или разветвленного С1-С6 алкила, С3-С7 циклоалкила.
2. Соединение по п. 1, его фармацевтически приемлемая соль, энантиомер или их смесь, где
R1 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: 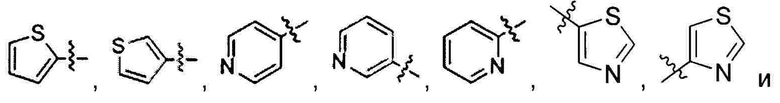
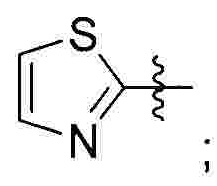 при этом указанный заместитель является таким, как определено в п. 1; предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 алкокси, NR10R11, -C(=O)R12, циано, нитро, или два соседних заместителя вместе с присоединенным атомом углерода образуют 6-членное ароматическое кольцо, 5-членное насыщенное кольцо или 5-членное гетероциклическое кольцо, содержащее 2 гетероатома, выбранных из атома кислорода; наиболее предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, метила, метокси, этила, амино, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметилкарбамоила, ацетокси, циано, нитро, ацетила, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо или диоксольное кольцо;
при этом указанный заместитель является таким, как определено в п. 1; предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 алкокси, NR10R11, -C(=O)R12, циано, нитро, или два соседних заместителя вместе с присоединенным атомом углерода образуют 6-членное ароматическое кольцо, 5-членное насыщенное кольцо или 5-членное гетероциклическое кольцо, содержащее 2 гетероатома, выбранных из атома кислорода; наиболее предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, метила, метокси, этила, амино, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметилкарбамоила, ацетокси, циано, нитро, ацетила, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо или диоксольное кольцо;
каждый из R10 и R11 независимо выбран из группы, состоящей из Н и -C(=O)R13;
R12 выбран из группы, состоящей из С1-С2 алкила, С1-С2 алкокси, амино (NH2), С1-С2 алкиламино и диС1-С2 алкиламино;
R13 выбран из группы, состоящей из Н и прямого или разветвленного С1-С2 алкила;
R2 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С4 алкила, С3-С7 циклоалкила, 6-членной гетероциклической группы, содержащей 1 гетероатом, выбранный из атома азота, и фенила, где указанный заместитель выбран из группы, состоящей из атома галогена, прямого или разветвленного С1-С4 алкила, прямой или разветвленной С1-С4 алкилсульфонильной группы, тетразолила, циано; более предпочтительно R2 выбран из прямого или разветвленного С1-С4 алкила, циклопропила, циклобутила, циклопентила, циклогексила, 1-метилпиперидин-4-ила, 1-метилсульфонилпиперидин-4-ила, 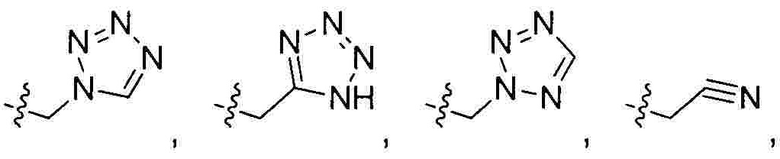 фенила, этилциклогексила;
фенила, этилциклогексила;
каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н, прямого или разветвленного С1-С4 алкила; более предпочтительно каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н, метила, этила, н-пропила, изопропила, н-бутила, втор-бутила и третичного бутила;
R5 и R6 могут связываться вместе с 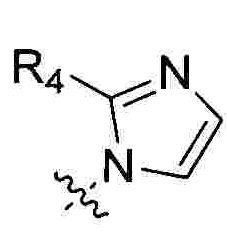 с образованием
с образованием 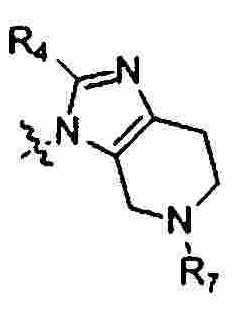 или
или 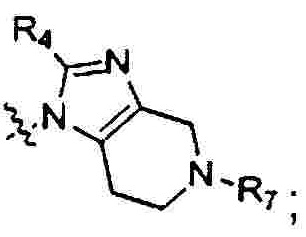
R7 выбран из группы, состоящей из C(=O)R8, С(=O)OR8; более предпочтительно R7 выбран из группы, состоящей из C(=O)R8;
R8 выбран из группы, состоящей из прямого или разветвленного С1-С4 алкила, С3-С7 циклоалкила; предпочтительно R8 выбран из группы, состоящей из метила, этила, н-пропила, циклопропила, изопропила, н-бутила, втор-бутила и трет-бутила.
3. Соединение по п. 1, его фармацевтически приемлемая соль, энантиомер или их смесь, где соединение формулы I выбрано из следующих соединений:
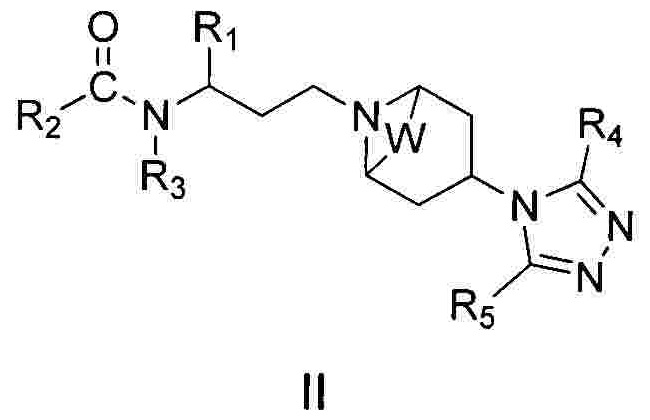
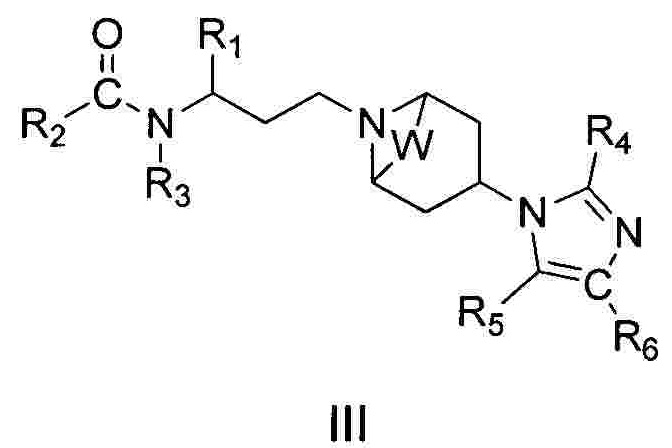
где R1, R2, R3, R4, R5, R6 и W являются такими, как определено в п. 1.
4. Соединение по п. 3, его фармацевтически приемлемая соль, энантиомер или их смесь, где в формуле (II)
R1 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: 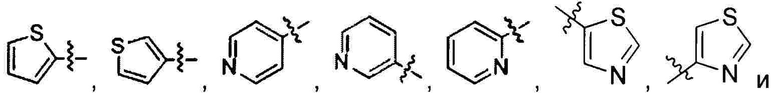
 при этом указанный заместитель является таким, как определено в п. 1; предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 алкокси, NR10R11, -C(=O)R12, циано, нитро, или два соседних заместителя вместе с присоединенным атомом углерода образуют 6-членное ароматическое кольцо, 5-членное насыщенное кольцо или 5-членное гетероциклическое кольцо; наиболее предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, метила, метокси, этила, амино, циано, нитро, ацетила, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметилкарбамоила, ацетокси, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо или диоксольное кольцо;
при этом указанный заместитель является таким, как определено в п. 1; предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 алкокси, NR10R11, -C(=O)R12, циано, нитро, или два соседних заместителя вместе с присоединенным атомом углерода образуют 6-членное ароматическое кольцо, 5-членное насыщенное кольцо или 5-членное гетероциклическое кольцо; наиболее предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, метила, метокси, этила, амино, циано, нитро, ацетила, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметилкарбамоила, ацетокси, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо или диоксольное кольцо;
каждый из R10 и R11 независимо выбран из группы, состоящей из Н и -C(=O)R13;
R12 выбран из группы, состоящей из прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 алкокси, амино (NH2), прямого или разветвленного С1-С4 алкиламино и прямого или разветвленного диС1-С4 алкиламино; предпочтительно R12 выбран из группы, состоящей из С1-С2 алкила, С1-С2 алкокси, амино (NH2), С1-С2 алкиламино и диС1-С2 алкиламино;
R13 выбран из группы, состоящей из Н и прямого или разветвленного С1-С4 алкила; предпочтительно R13 выбран из группы, состоящей из Н и С1-С2 прямого или разветвленного алкила;
R2 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: фенила, прямого или разветвленного С1-С4 алкила и С3-С7 циклоалкила, где указанный заместитель выбран из группы, состоящей из атома галогена, прямого или разветвленного С1-С4 алкила, прямой или разветвленной С1-С4 алкилсульфонильной группы, тетразолила; более предпочтительно R2 выбран из группы, состоящей из метила, этила, циклопропила, циклобутила, циклопентила, циклогексила, 1-метилпиперидин-4-ила, 1-метилсульфонилпиперидин-4-ила, 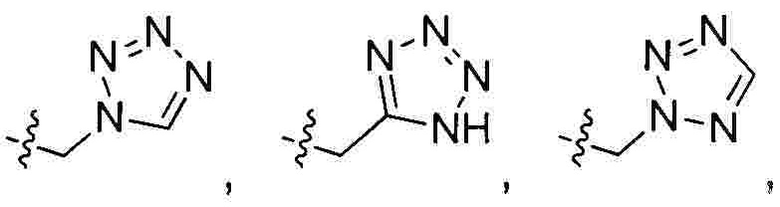 фенила, этилциклогексила;
фенила, этилциклогексила;
каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н и прямого или разветвленного С1-С4 алкила; более предпочтительно каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н и метила, этила, н-пропила, изопропила, н-бутила, втор-бутила и трет-бутила; наиболее предпочтительно каждый из R3, R4 и R5 независимо выбран из группы, состоящей из Н, метила, этила, н-пропила и изопропила;
в формуле (III) R1 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: 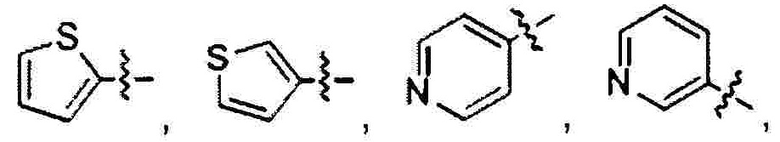
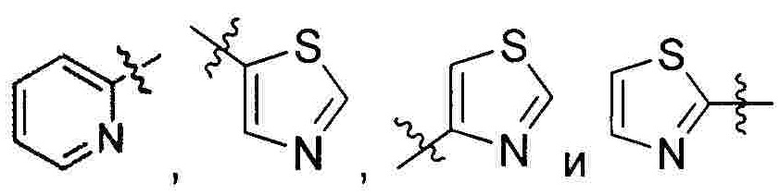 , где указанный заместитель является таким, как определено в п. 1; предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 алкокси, NR10R11, -C(=O)R12, циано, нитро, или два соседних заместителя вместе с присоединенным атомом углерода образуют 6-членное ароматическое кольцо, 5-членное насыщенное кольцо или 5-членное гетероциклическое кольцо; наиболее предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, метила, метокси, этила, амино, циано, нитро, ацетила, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметилкарбамоила, ацетокси, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо или диоксольное кольцо;
, где указанный заместитель является таким, как определено в п. 1; предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, С1-С2 алкила, С1-С2 алкокси, NR10R11, -C(=O)R12, циано, нитро, или два соседних заместителя вместе с присоединенным атомом углерода образуют 6-членное ароматическое кольцо, 5-членное насыщенное кольцо или 5-членное гетероциклическое кольцо; наиболее предпочтительно указанный заместитель выбран из группы, состоящей из атома галогена, метила, метокси, этила, амино, циано, нитро, ацетила, формамидо, ацетамидо, карбамоила, N-метилкарбамоила, N,N-диметилкарбамоила, ацетокси, или два соседних заместителя вместе с присоединенным атомом углерода образуют бензольное кольцо или диоксольное кольцо;
каждый из R10 и R11 независимо выбран из группы, состоящей из Н и -C(=O)R13;
R12 выбран из группы, состоящей из прямого или разветвленного С1-С4 алкила, прямого или разветвленного С1-С4 алкокси, амино (NH2), прямого или разветвленного С1-С4 алкиламино и прямого или разветвленного диС1-С4 алкиламино; предпочтительно R12 выбран из группы, состоящей из С1-С2 алкила, С1-С2 алкокси, амино (NH2), С1-С2 алкиламино и диС1-С2 алкиламино;
R13 выбран из группы, состоящей из Н и прямого или разветвленного С1-С4 алкила; предпочтительно R13 выбран из группы, состоящей из Н и прямого или разветвленного С1-С2 алкила;
R2 выбран из следующих групп, незамещенных или замещенных от 1 до 3 заместителями: прямого или разветвленного С1-С4 алкила и С3-С7 циклоалкила, где указанный заместитель выбран из атома галогена, прямого или разветвленного С1-С4 алкила, прямой или разветвленной С1-С4 алкилсульфонильной группы, тетразолила, циано; более предпочтительно R2 выбран из группы, состоящей из метила, этила, циклопропила, циклобутила, циклопентила, циклогексила, 1-метилпиперидин-4-ила, 1-метилсульфонилпиперидин-4-ила, 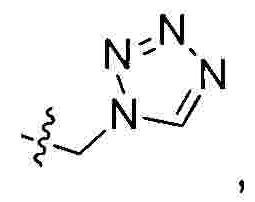
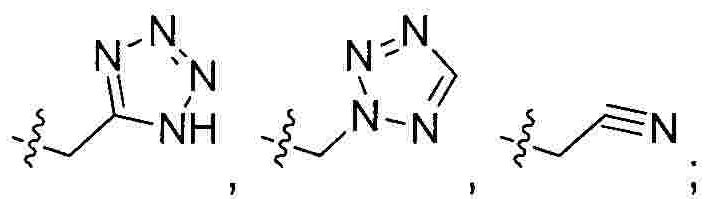
каждый из R3 и R4 независимо выбран из группы, состоящей из Н и прямого или разветвленного С1-С4 алкила; более предпочтительно каждый из R3 и R4 независимо выбран из группы, состоящей из Н и метила, этила, н-пропила, изопропила, н-бутила, втор-бутила и трет-бутила; наиболее предпочтительно каждый из R3 и R4 независимо выбран из группы, состоящей из Н, метила и этила;
R5 и R6 могут связываться вместе с 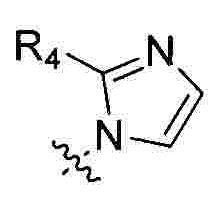 с образованием
с образованием 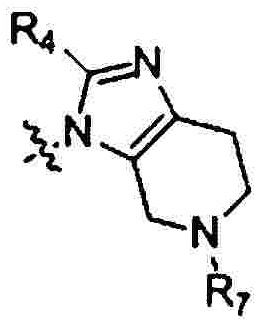 или
или 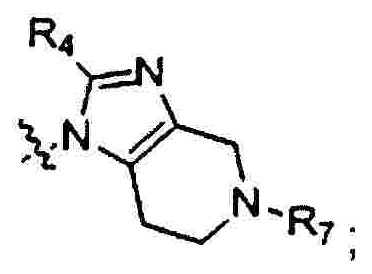
R7 выбран из группы, состоящей из C(=O)R8, C(=O)OR8; более предпочтительно R7 выбран из группы, состоящей из C(=O)R8;
R8 выбран из группы, состоящей из прямого или разветвленного С1-С4 алкила, С3-С7 циклоалкила; предпочтительно R8 выбран из группы, состоящей из метила, этила, н-пропила, циклопропила, изопропила, н-бутила, втор-бутила и трет-бутила.
5. Соединение по п. 1, его фармацевтически приемлемая соль, энантиомер или их смесь, где соединение формулы (I) выбрано из следующих соединений:
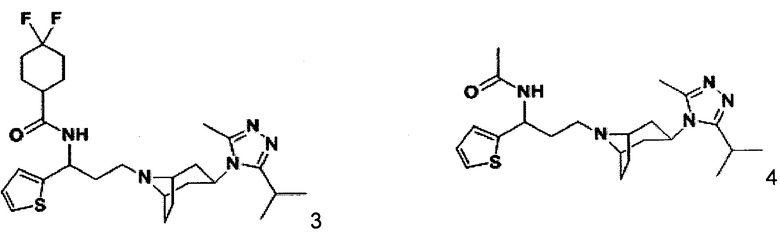
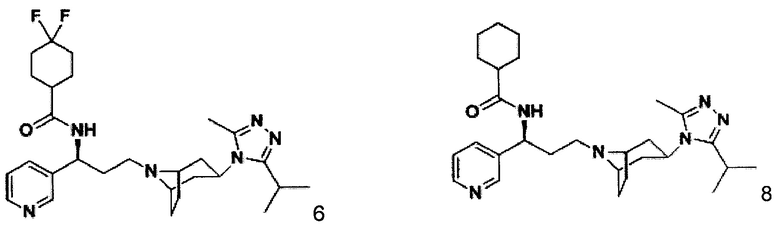
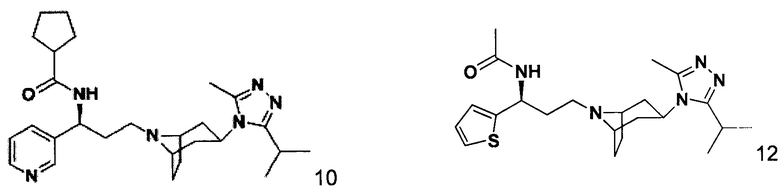
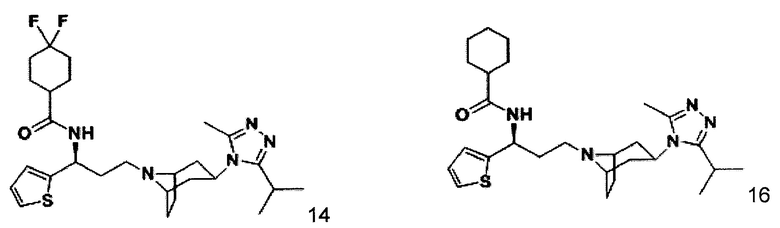
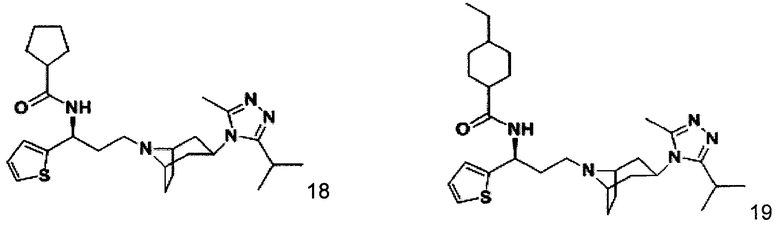
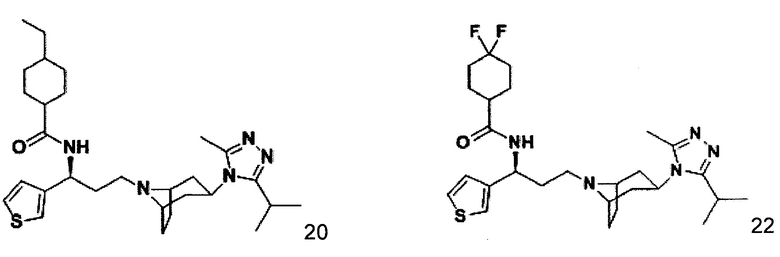

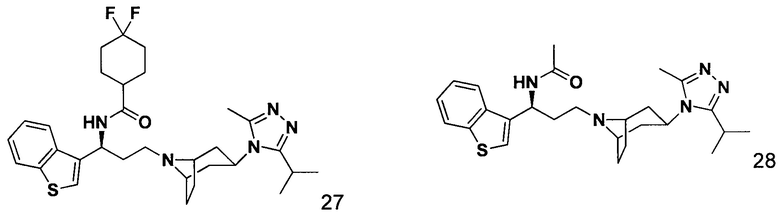


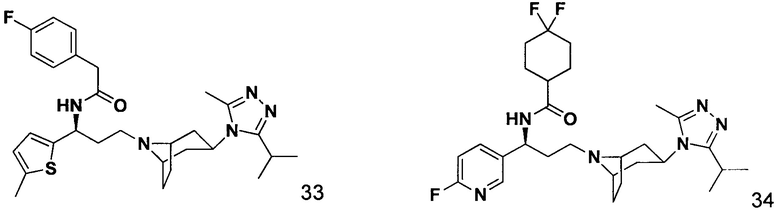
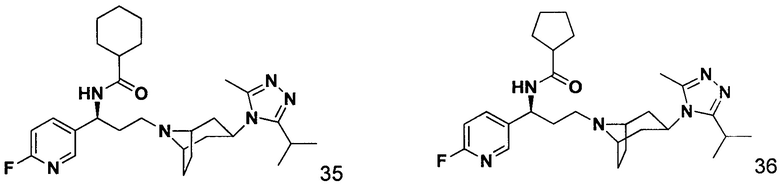

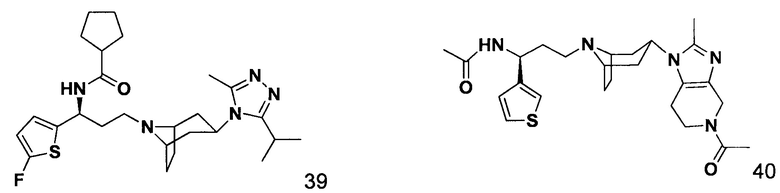
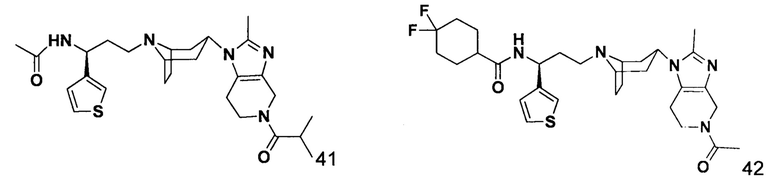

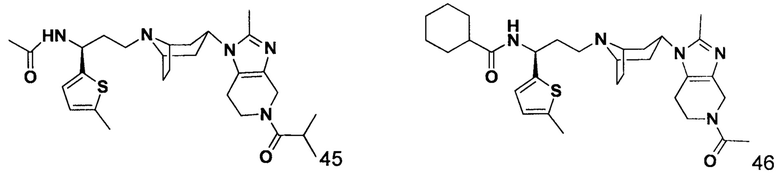
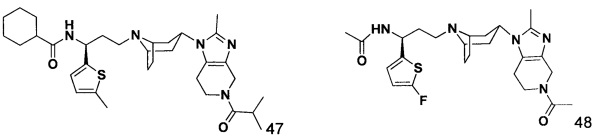
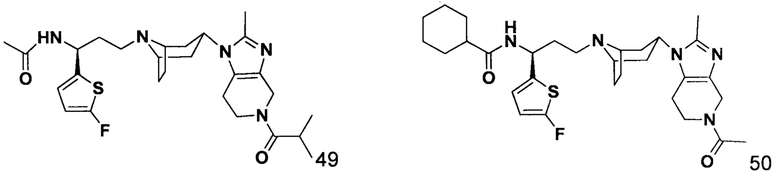
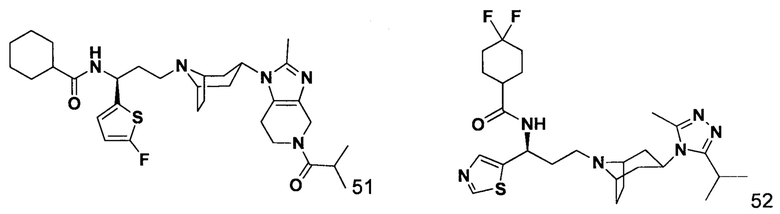

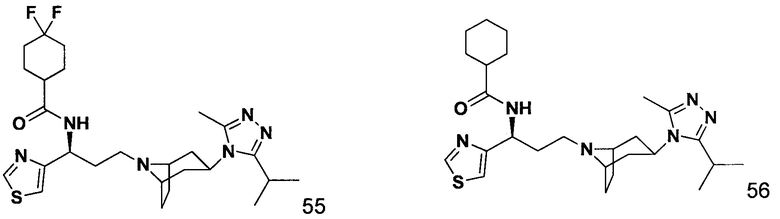

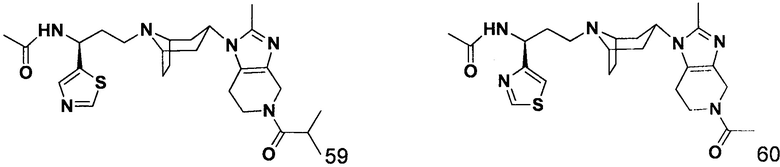
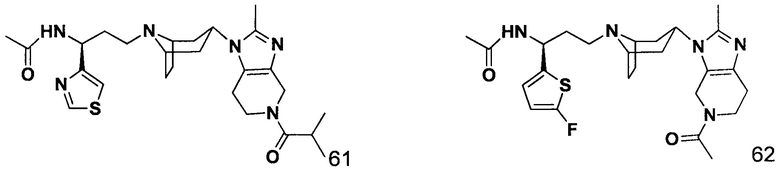
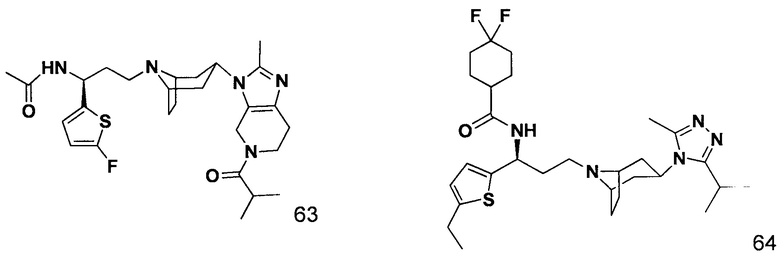
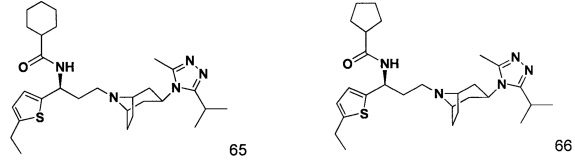
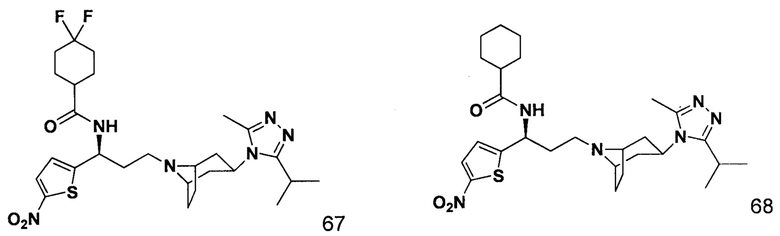
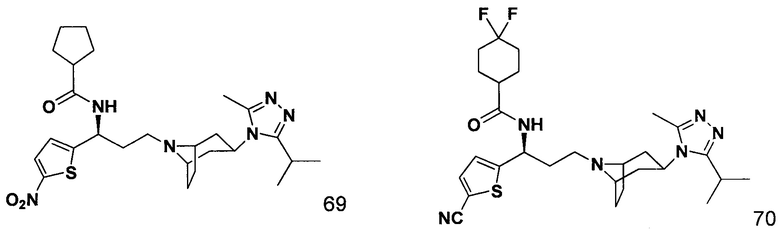
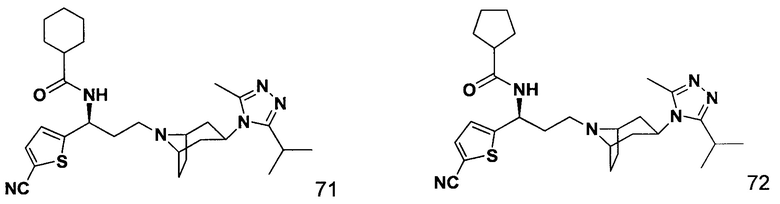
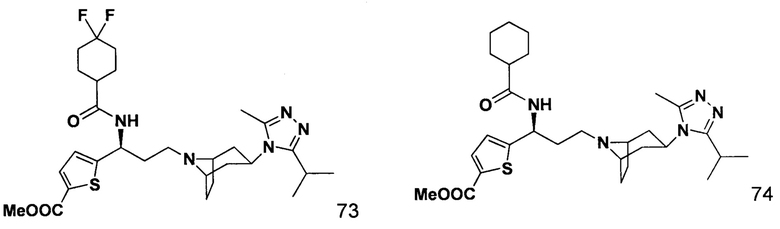
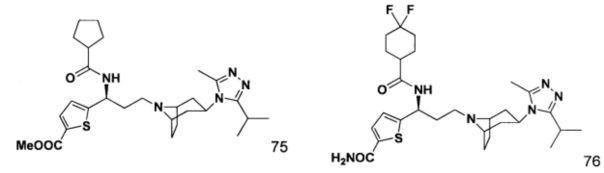
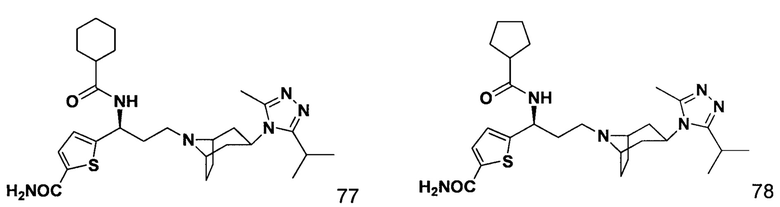

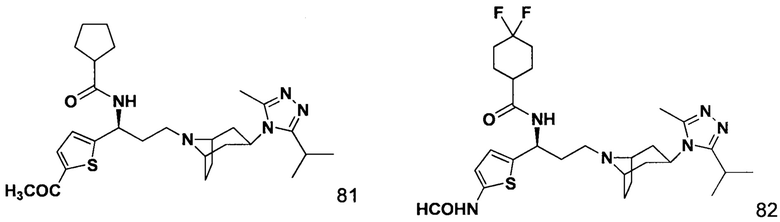
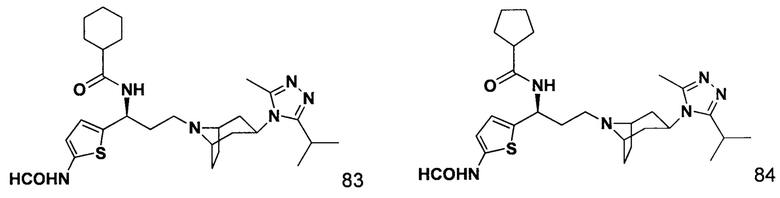

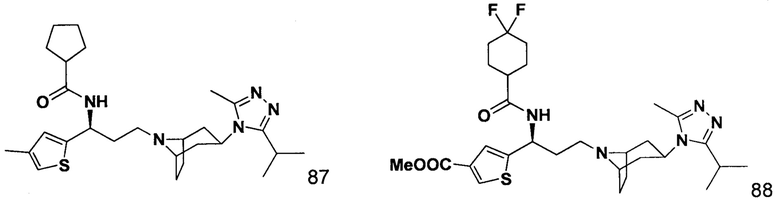

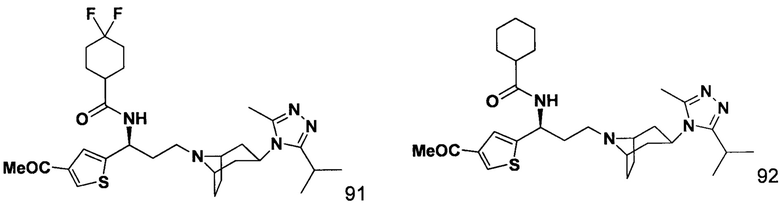
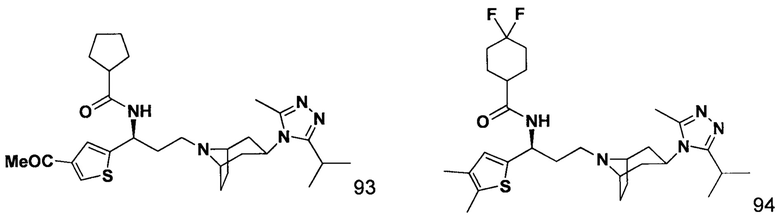
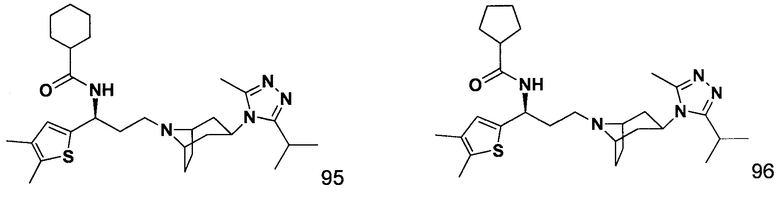
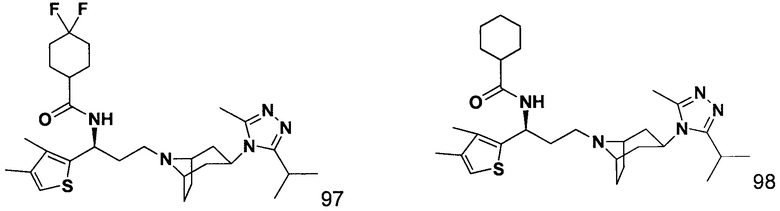
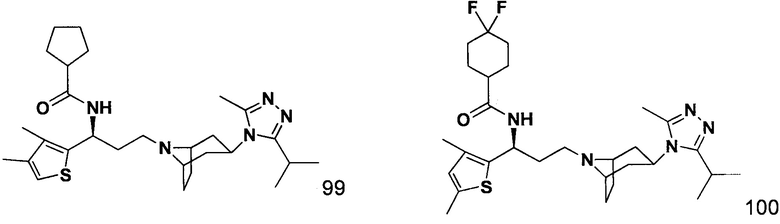
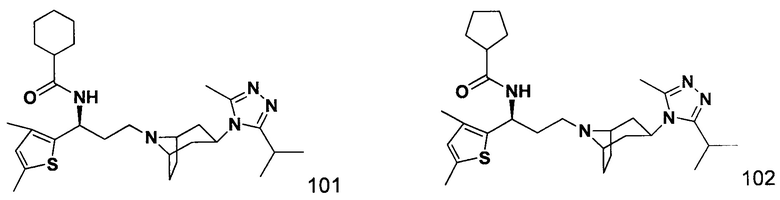
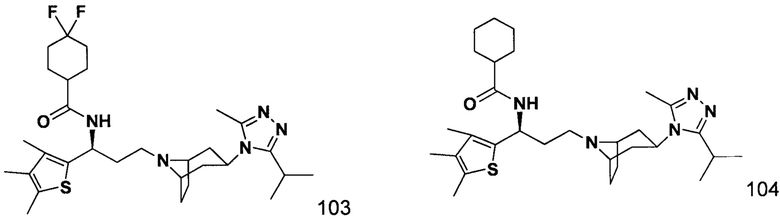
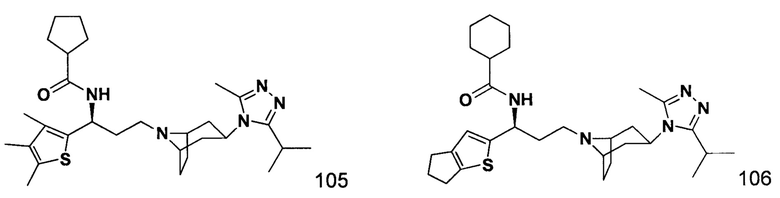
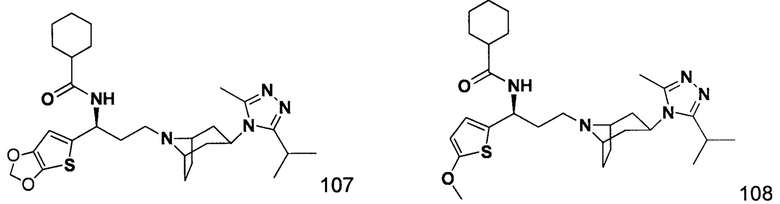
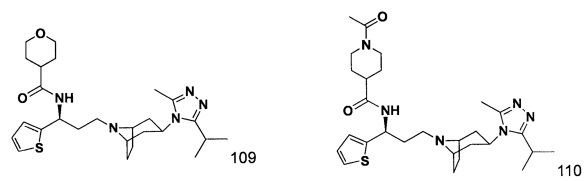
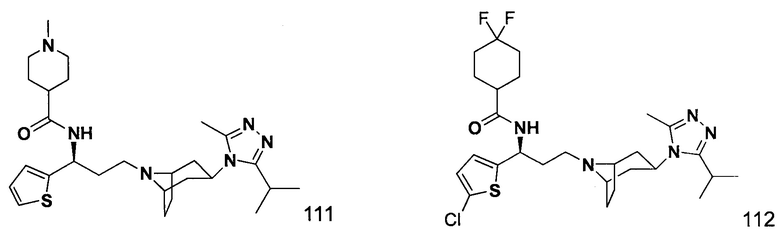
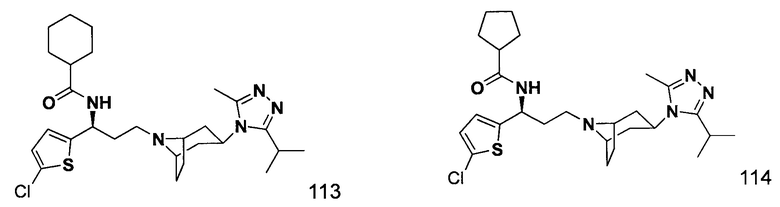
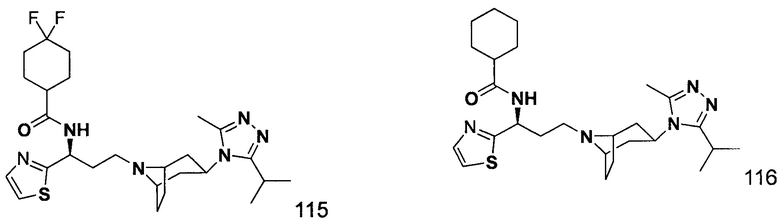
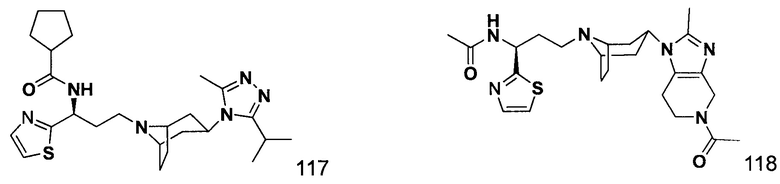
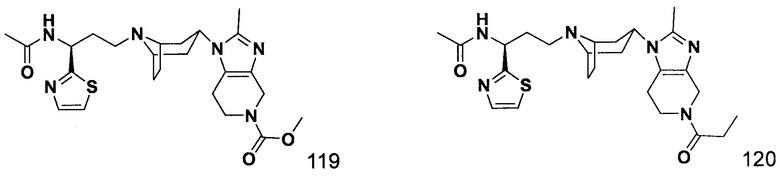
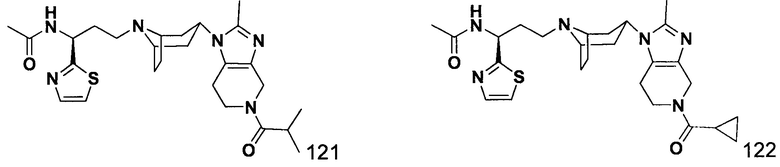
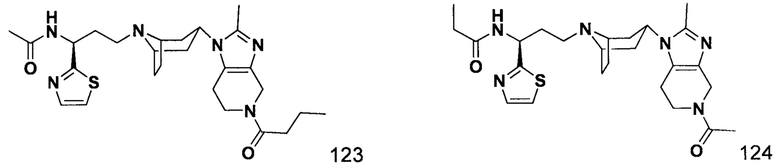
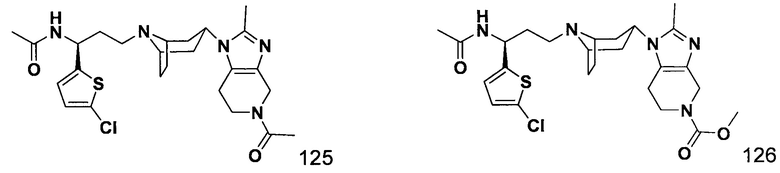
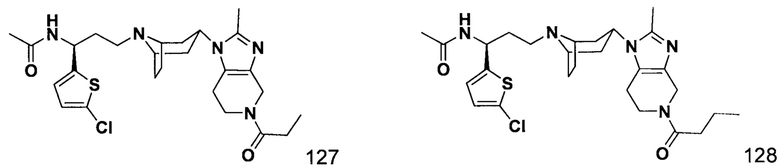
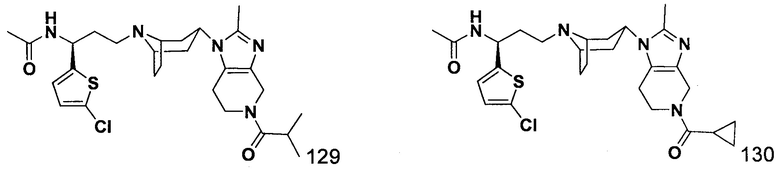
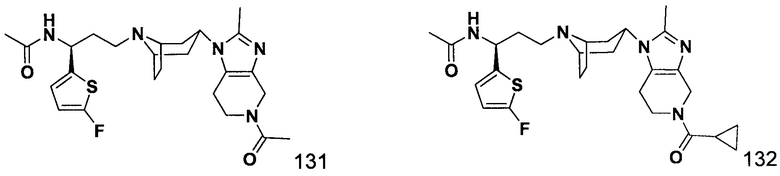
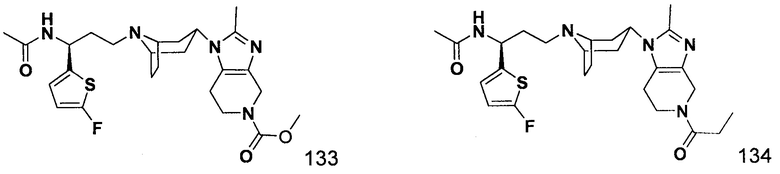

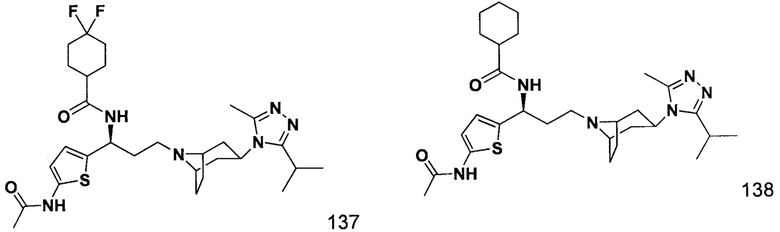
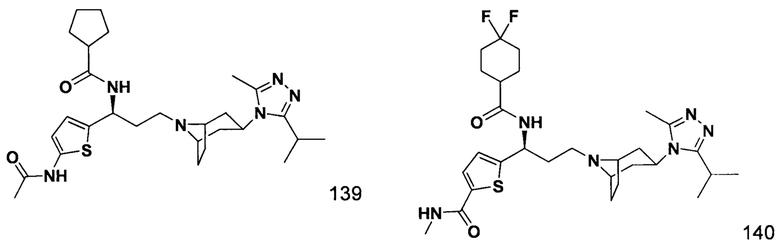
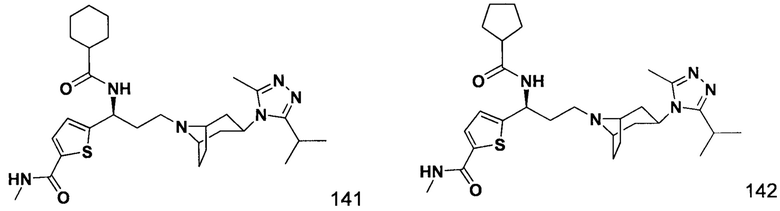
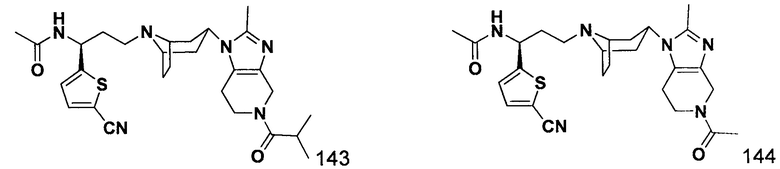
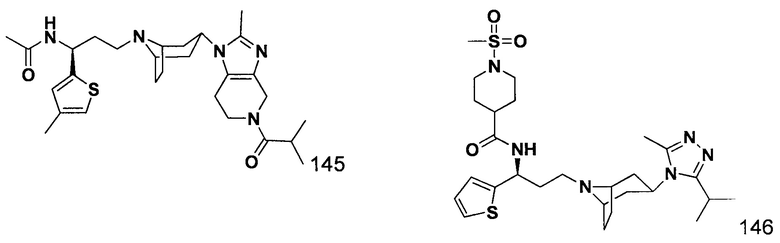

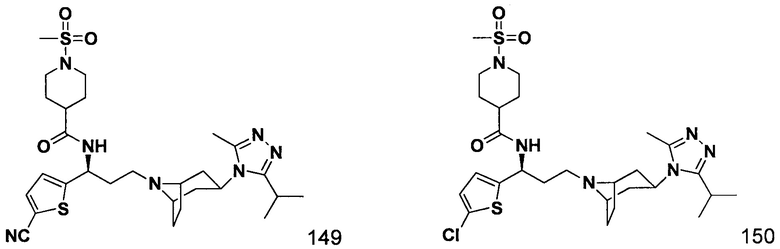
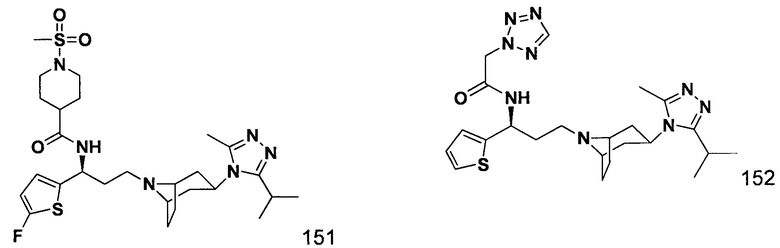
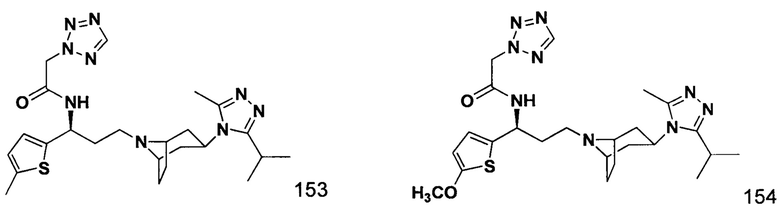
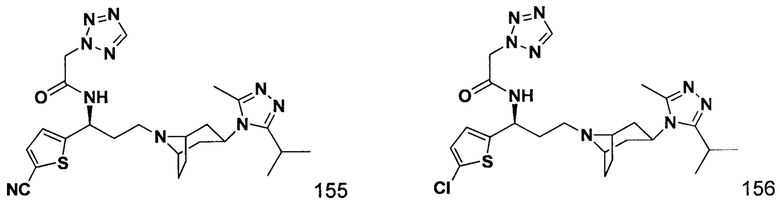
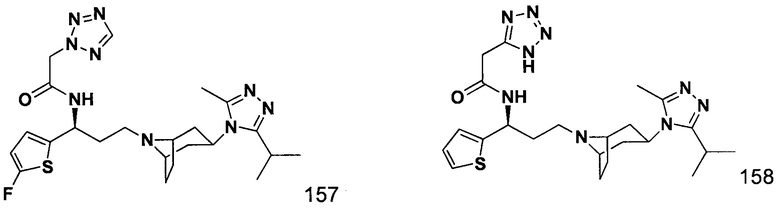


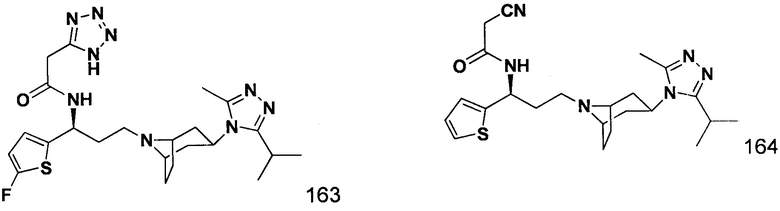
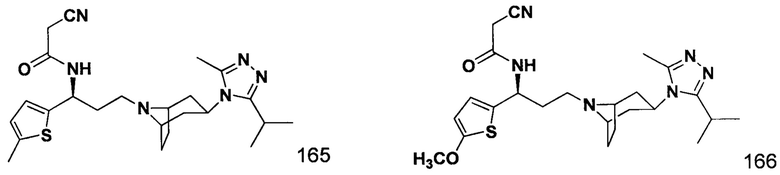
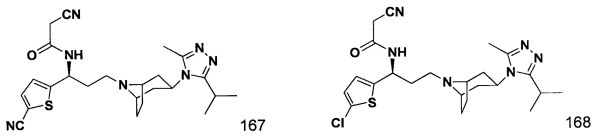
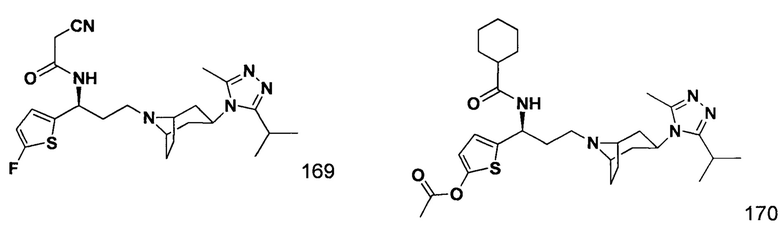
 или
или 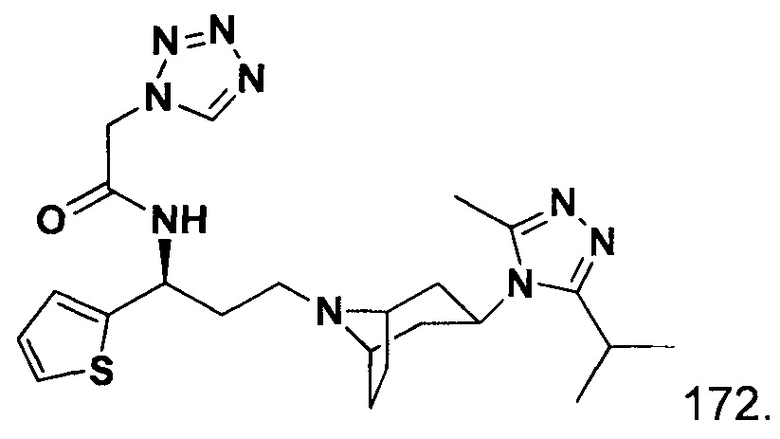
6. Способ получения соединения формулы I, включающий следующие стадии:
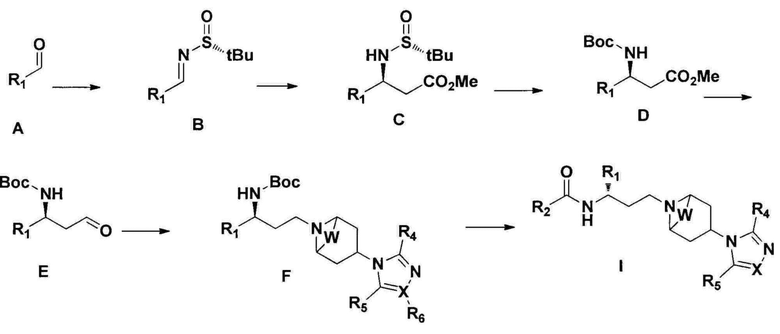
1) соединение сульфинилимина В получают из соединения А посредством имидирования;
2) соединение С получают из соединения сульфинилимина В посредством реакции Манниха;
3) соединение D получают из соединения С посредством удаления сульфинила и защиты трет-бутилоксикарбонила (ВОС);
4) соединение Е получают из соединения D посредством восстановления и окисления сложного эфира;
5) соединение F получают из соединения Е и 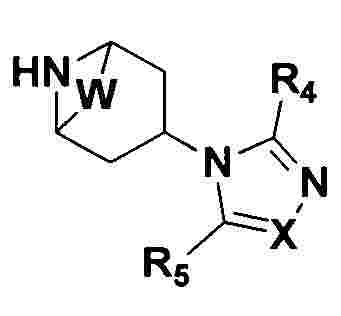 посредством реакции восстановительного аминирования;
посредством реакции восстановительного аминирования;
6) соединение F подвергают реакции удаления защиты и конденсации с 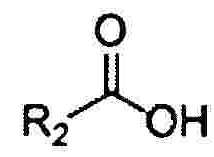 с получением соединения I,
с получением соединения I,
где в каждой формуле R1, R2, R4, R5, R6, X и W являются такими, как определено в п. 1.
7. Фармацевтическая композиция в качестве антагониста рецептора хемокина CCR5 или в качестве лекарственного средства для лечения CCR5-опосредованного заболевания, содержащая терапевтически эффективное количество одного из соединений по любому из пп. 1-5, его фармацевтически приемлемой соли, энантиомера или их смеси и фармацевтически приемлемый носитель.
8. Применение соединения по любому из пп. 1-5, его фармацевтически приемлемой соли, энантиомера или их смеси для получения антагониста рецептора хемокина CCR5.
9. Применение соединения по любому из пп. 1-5, его фармацевтически приемлемой соли, энантиомера или их смеси для получения лекарственного средства для лечения CCR5-опосредованного заболевания.
10. Применение соединения по любому из пп. 1-5, его фармацевтически приемлемой соли, энантиомера или их смеси для получения лекарственного средства для лечения инфекции вируса иммунодефицита человека (ВИЧ).
| ЕА 200100588 А1, 28.02.2002 | |||
| WO 03030898 A1, 17.04.2003 | |||
| WO 2006136917 A1, 28.12.2006 | |||
| WO 2007066201 A2, 14.06.2007 | |||
| C | |||
| G | |||
| Barber et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| WO 2005007656 A1, 27.01.2005. | |||
Авторы
Даты
2018-10-29—Публикация
2014-12-29—Подача