Ссылка на перечень последовательностей, поданный в электронном виде
Содержание перечня последовательностей, поданного в электронном виде в текстовом файле ASCII (имя - CTLA4101P1Sequencelisting.txt; размер: 107814 байт; и дата создания: 11 мая 2012 г.), представленного с заявкой, включено в данный документ во всей своей полноте посредством ссылки.
Область изобретения
Настоящее изобретение относится к композициям, содержащим варианты антигена 4 цитотоксических Т-лимфоцитов (CTLA-4), необязательно слитого с Fc IgG, и их терапевтическому применению для ингибирования активности Т-клеток, в частности, в контексте воспалительных состояний, таких как ревматоидный артрит (RA).
Предпосылки изобретения
Считается, что активация наивных T-клеток протекает с помощью двухсигнального механизма. При встрече с антигенпредставляющей клеткой (APC) T-клеточный рецептор (TCR) взаимодействует с пептидом, связанным с молекулами главного комплекса гистосовместимости (MHC) и таким образом доставляет первый сигнал активации T-клеткам. Этого исходного сигнала недостаточно для того, чтобы привести к активации Т-клеток, и обязательным требованием является второй сигнал от костимулирующих рецепторов. Одним из самых важных и наилучшим образом описанных костимулирующих рецепторов является CD28, который взаимодействует с CD80 (B7.1) и CD86 (B7.2) на поверхности макрофагов, дендритных клеток, а также В- и активированных Т-лимфоцитов.
Ген CD86 кодирует мембранный белок типа I (номер доступа в Swiss-Prot P33681). Альтернативный сплайсинг приводит к образованию двух вариантов транскриптов гена CD86, кодирующего различные изоформы. Описаны дополнительные варианты транскриптов, однако, их непроцессированные последовательности полной длины не были определены.
Соответствующий белок CD80 (номер доступа в Swiss-Prot P42081) имеет вторичную структуру, подобную CD86. CD80 имеет 26% и 46% идентичных и сходных аминокислотных остатков с CD86, соответственно. CD80 экспрессируется лишь в незначительных количествах в APC, находящихся в покое, однако после активации может происходить стимуляция их выработки. CD80 распознает одинаковые рецепторы на T-клетках, CD28 и CD152 (CTLA-4), однако связывается с последними с аффинностью, примерно в 2-4 раза большей, чем CD86.
Никакого линейного пептидного эпитопа, ответственного за связывание с CD28 и/или CTLA-4, обнаружено не было (Ellis et al., J Immunol., 156, 2700-2709), однако, были обнаружены консервативные остатки во вторичных структурах (слои IgV CD80 и CD86) в контакте с CTLA-4 (Swartz et al., Nature, 410, 604-608).
Передача сигнала от CD28 приводит к активации T-клеток и стимуляции выработки коингибиторного рецептора CTLA-4. CTLA-4 является членом иммуноглобулинового надсемейства. Он связывается с CD80 и CD86 с повышенной аффинностью и авидностью по сравнению с CD28 и эффективно подавляет сигналы активации.
По поводу относительной роли CD80 и CD86 в связывании CTLA-4 были выдвинуты различные теории. Slavik et al. (Immunol. Res. 19(1):1-24 1999) рассмотрели передачу сигналов и функционирование семейств CD28/CTLA-4 и CD80/CD86. Sansom (Immunology 101:169-177 2000) обобщил ряд исследований, в которых изучали различия между CD80 и CD86.
Odobasic et al. (Immunology 124:503-513 2008) изучали роль CD80 и CD86 в ответах эффекторных T-клеток. В этом исследовании изучали эффекты моноклональных антител к CD80 и CD86 в мышиной модели артрита, индуцированного антигеном. Сообщалось, что блокада CD80 и CD86 приводила к тенденции снижения тяжести заболевания по сравнению с таковой мышей, получавших контрольные антитела. На основании результатов лечения отдельными антителами авторы пришли к заключению, что CD80 обостряет артрит вследствие подавления выработки системного IL-4 и увеличения накопления T-клеток в суставах, тогда как CD86 увеличивает степень тяжести заболевания вследствие стимуляции выработки IL-17 и увеличения накопления эффекторных Т-клеток в суставах без воздействия на развитие Th1 или Th2. Однако в исследовании отмечается, что дальнейшего дополнительного уменьшения степени тяжести артрита не наблюдалось в случае блокады и CD80, и CD86, что свидетельствует о том, что ингибирование любой костимулирующей молекулы было достаточным для получения максимального облегчения заболевания. Эта модель была основана на вторичном ответе на антиген (в данном исследовании BSA), вводимый непосредственно в суставную щель.
В другом исследовании применяли мышиную модель артрита, индуцированного коллагеном, с нарушением толерантности к эндогенному антигену (коллагену). В этом исследовании было отмечено, что для максимальной эффективности требовалась блокада как CD80, так и CD86 (Webb et al. Eur J. Immunol 26(10):2320-2328 1996).
Показано, что рекомбинантный белок слияния, содержащий внеклеточный домен CTLA-4, связанный с модифицированным доменом Fc IgG1 (“CTLA-4 - Ig”), связывается с CD80 и CD86 in vivo и эффективно подавляет Т-клеточную активацию, опосредованную CD28 (Kliwinski et al., J Autoimmun. 2005; 25(3):165-71).
Белки слияния CTLA-4 разрабатывали в качестве терапевтических средств для лечения ревматоидного артрита (RA). RA является прогрессирующим дегенеративным заболеванием, ведущим к разрушению хрящевой и костной ткани. Существуют доказательства того, что в процессе воспаления, ведущем к повреждению суставов и разрушению хрящевой и костной ткани, опосредованным фибробластоподобными синовиоцитами и остеокластами, участвуют многие звенья иммунной системы. Многочисленные исследования показали повышенную активацию Т-клеток в синовиальной оболочке и то, что до 50% клеток, инфильтрующих воспаленный паннус, являются Т-лимфоцитами. Также T-клетки в синовиальной оболочке пациентов с RA характеризуются активированным эффекторным фенотипом, показывая повышенную экспрессию маркеров, связанных с активацией, таких как CD44, CD69, CD45RO, VLA-1 и CD27.
Показано, что активированные T-клетки играют основную роль в образовании и поддержании патологического воспалительного ответа, обнаруживаемого в синовиальной оболочке при RA. Активированные Т-клетки являются важным источником провоспалительных цитокинов, таких как IFNγ, IL-17 и TNFα. Эти факторы являются эффективными активаторами фибробластоподобных синовиоцитов (FLS) и макрофагоподобных синовиоцитов (MLS), вызывающими секрецию матриксных металлопротеаз (MMP), которые являются медиаторами разрушения хрящевой ткани, а также секреции медиаторов воспаления, таких как IL-6, IL-1 и TNFα. Активированные CD4+ клетки также могут предоставлять когнатную помощь B-лимфоцитам, приводя к выработке антител, таких как ревматоидный фактор (RF), которые также способствуют прогрессированию заболевания.
Абатацепт (Оренсия®) является белком слияния CTLA-4 с Ig, содержащим внеклеточный домен CTLA-4, слитый с Fc IgG1. Полученный растворимый белок является димером с молекулярной массой приблизительно 92 кДа. Показано, что при клиническом применении белок оказывал благоприятные эффекты в лечении пациентов с RA, показывая, что ингибирование костимулирующего пути, включающего CD80 и CD86, является практически осуществимым терапевтическим подходом для лечения RA. Терапию RA абатацептом проводят либо в виде внутривенной инъекции ежемесячно или подкожной инъекции еженедельно.
Абатацепт содержит в своей CDR3-подобной петле аминокислотный гексапептидный мотив MYPPPY, который является общим для CD28 и CTLA-4, и описано, что он необходим для связывания с лигандами B7. Мутация, приводящая к замене первой молекулы тирозина (Y) в этом мотиве на аланин (A), делает невозможным связывание с CD80, однако также приводит к пониженному связыванию с CD86, при этом замена на фенилаланин (F) способствует возврату полной аффинности к CD80 при полной утрате связывания с CD86 (Harris et al., J. Exp. Med. (1997) 185:177-182). Для взаимодействия абатацепта с его лигандами также важны другие остатки в CDR3-подобном и CDR1-подобном участках. Так, мутантная молекула с глутаминовой кислотой (E) вместо лейцина (L) в положении 104 и тирозином (Y) вместо аланина (A) в положении 29 характеризуется приблизительно в 2 раза большей авидностью связывания с CD80 (B7-1) и приблизительно в 4 раза большей авидностью связывания с CD86 (B7-2), чем абатацепт. Описано, что данное соединение, LEA-29Y (белатацепт, Nulojix®), имеет такую же аффинность связывания с CD80, что и связывания с CD86 (3,66 нМ и 3,21 нМ, соответственно). Белатацепт разрабатывался в качестве иммуносупрессора для трансплантации (Larsen et al., Am. J. Transplantation (2005) 5:443-453; Gupta & Womer Drug Des Develop Ther 4:375-382 2010) и недавно был одобрен для профилактики отторжения органов у взрослых пациентов, получающих трансплантат почки. Сам абатацепт показал ограниченную эффективность в отношении отторжения трансплантата, что было результатом его более низкого ингибирования CD86-зависимой, по сравнению с CD80-зависимой, костимуляции (Gupta & Womer, supra).
Составы абатацепта и белатацепта для подкожного введения описаны в WO 2007/07654.
Для выделения улучшенных вариантов CTLA-4 ранее выполняли отбор в отношении улучшенной аффинности и стабильности с помощью рибосомного дисплея. Для изменения белка успешным оказался как мутагенез на основе ПЦР сниженной точности для мутации полной генной последовательности, так и направленный мутагенез для направленных мутаций ключевых участков. Например, в WO 2008/047150 описаны варианты белка CTLA-4, проявляющие повышенную активность и повышенную стабильность по сравнению с диким типом.
Компанией Maxygen, Inc. описана терапевтическая молекула CTLA-4-Ig, обозначенная ASP2408, которую разрабатывала компания Perseid Therapeutics LLC в сотрудничестве с компанией Astellas Pharma Inc для лечения RA. Описано, что молекула CTLA-4-Ig проявляла повышенную эффективность по сравнению с Orencia® (абатацептом) (WO 2009/058564).
В патенте США 6750334 (Repligen Corporation) описан CTLA-4-Cγ4, растворимый белок слияния, содержащий CTLA-4, слитый с участком иммуноглобулина. Для снижения активации комплемента или взаимодействия Fc с рецептором константная область иммуноглобулина, содержащая шарнирную область и домены CH2 и CH3, модифицирована посредством замены, добавления или делеции по меньшей мере одного аминокислотного остатка.
Компанией Xencor, Inc. недавно была описана молекула CTLA4-Ig, содержащая участок варианта CTLA-4 и Fc-участок иммуноглобулина (WO 2011/103584). Для создания вариантов CTLA4-Ig с большей ингибиторной активностью Т-клеток был описан ряд аминокислотных замен в аминокислотной последовательности участка CTLA-4. В WO 2011/103584 также описаны модификации Fc, например, для улучшения связывания с FcγR путем усиления Fc-опосредованных эффекторных функций и/или увеличения in vivo периода полужизни CTLA4-Ig.
Краткое описание изобретения
В первом аспекте настоящее изобретение предлагает полипептиды CTLA-4, которые являются вариантами CTLA-4 дикого типа. Полипептиды CTLA-4 по настоящему изобретению могут иметь одно или несколько улучшенных свойств, таких как более высокая эффективность, более высокая аффинность к CD80 и/или CD86, более высокая селективность в отношении CD80 по сравнению с CD86, высокая кросс-реактивность и/или более высокая стабильность по сравнению с диким типом.
Улучшений CTLA-4 можно достичь с помощью мутации аминокислотной последовательности внеклеточного домена CTLA-4 человека дикого типа, также известного как растворимый CTLA-4. Как описано в данном документе, для получения улучшенного полипептида CTLA-4 в аминокислотную последовательность CTLA-4 можно вводить одну или несколько мутаций аминокислот, которыми могут быть аминокислотная замена, вставка или делеция. Полипептид может, например, характеризоваться повышенной эффективностью, аффинностью и/или стабильностью по отношению к CTLA-4 дикого типа.
Внеклеточный домен CTLA-4 содержит аминокислотную последовательность SEQ ID NO: 35 дикого типа. SEQ ID NO: 35 не является полным внеклеточным доменом, а представляет собой участок, использованный в абатацепте (Оренсия®).
Полипептиды CTLA-4 по настоящему изобретению также могут содержать или не содержать дополнительные остатки или последовательности CTLA-4 вне пределов участка, соответствующего SEQ ID NO: 35. Предпочтительно полипептид CTLA-4 по настоящему изобретению является растворимым. Как правило, в связи с этим он не содержит трансмембранный участок CTLA-4.
В данном документе определен ряд мутаций в аминокислотной последовательности CTLA-4, которые связаны с повышенной эффективностью, аффинностью и/или стабильностью или которые можно вводить с другими целями, такими как воздействие на димеризацию.
Примерами аминокислотных замен в CTLA-4 дикого типа являются: R, S, V или T в положении I16; T в положении A24; N или P в положении S25; S в положении G27; I в положении V 32; G в положении D41; G в положении S42; E в положении V44; K или V в положении M54; S или G в положении N56; A, G, S или P в положении L58; S или A в положении T59; T в положении F 60; Q или P в положении L61; G в положении D62; Y в положении D63; P в положении S64; N, D, V или T в положении I65; A, T, M или H в положении S70; R в положении Q80; Q, S, V, R, K или L в положении M85; S в положении T87; Q, H, T, E или M в положении K93; R, Q или E в положении L104; V в положении I106; D или S в положении N108; V или F в положении I115 и S в положении C120. Примером аминокислотной делеции является делеция T51. Нумерация остатков указана по отношению к последовательностям CTLA-4, показанным на фигуре 1A и фигуре 2, при этом первый остаток пронумерован как положение 1 “нумерации последовательности”. На фигуре 1 также для сравнения показана нумерация по Swiss Prot.
Вариант CTLA-4 может иметь, например, до двенадцати или до двадцати мутаций аминокислот в растворимом CTLA-4 человека дикого типа. Мутации могут включать любую или все из мутаций аминокислот, перечисленных выше, и необязательно одну или несколько различных мутаций, например, различные замены, в этих или других положениях остатков. Аминокислотная последовательность варианта может содержать последовательность CTLA-4 человека дикого типа SEQ ID NO: 35 с одной или несколькими, например, по меньшей мере пятью, шестью или семью из перечисленных мутаций аминокислот.
Полипептид CTLA-4 может содержать аминокислотную последовательность или состоять из аминокислотной последовательности, имеющей по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95%, 96%, 97%, 98% или 99% идентичности последовательности с SEQ ID NO: 35.
Примеры аминокислотных последовательностей варианта CTLA-4 в соответствии с настоящим изобретением включают аминокислотные последовательности SEQ ID NO: 36-55, показанные на фигуре 1A. Вариант CTLA-4 может содержать аминокислотную последовательность CTLA-4 “1299”, кодируемую нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948. Молекула под номером доступа в NCIMB 41948 кодирует полипептид CTLA-4 1299, слитый с Fc-участком иммуноглобулина. Кодируемый полипептид CTLA-4 1299, кодируемый Fc-участок и кодируемый полипептид, содержащий полипептид CTLA-4 1299, слитый с Fc-участком, все из которых кодируются нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948, все являются отдельными вариантами осуществления настоящего изобретения.
Предпочтительными мутациями являются аминокислотные замены, выбранные из следующих: R, S или V в положении I16; T в положении A24; N в положении S25; S в положении G27; K в положении M54; S в положении N56; A или G в положении L58; S в положении T59; T в положении F60; Q в положении L61; Y в положении D63; P в положении S64; N или D в положении I65; A в положении S70; R в положении Q80; Q или S в положении M85; Q или H в положении K93 и S в положении C120. Соответственно, аминокислотная последовательность варианта может содержать последовательность CTLA-4 человека дикого типа SEQ ID NO: 35 с аминокислотными остатками, замещенными в одном или нескольких, например, по меньшей мере пяти или шести или всех из этих положений другим определенным остатком.
Последовательность полипептида CTLA-4 предпочтительно содержит: R, I, S или V в положении 16; T или A в положении 24; N в положении 25; S или G в положении 27; M или K в положении 54; N или S в положении 56; A, L или G в положении 58; T или S в положении 59; F или T в положении 60; L или Q в положении 61; D или Y в положении 63; S или P в положении 64; I, N или D в положении 65; A или S в положении 70; Q или R в положении 80; Q, M или S в положении 85; Q или H в положении 93 и/или C или S в положении 120. Остатки в других положениях могут быть дикого типа человека или могут подвергаться одной или нескольким другим мутациям.
Полипептид CTLA-4 может содержать N в положении 25, представляя собой замену S дикого типа в этом положении. Полипептид может содержать Q или H в положении 93, представляя собой замену К дикого типа в этом положении. Предполагается, что эти замены в положении остатков 25 и 93, проиллюстрированные примерами, описанными далее, в значительной степени связаны с улучшениями аффинности, эффективности и/или стабильности CTLA-4.
Предпочтительным аминокислотным мотивом, наблюдавшимся в многочисленных вариантах с высокой эффективностью, является STQDYPN (SEQ ID NO: 69). Этот мотив, расположенный в положении остатков 59-65, находится в петлевом участке, который, по-видимому, находится в непосредственной близости к CD80 и CD86 в связанной структуре. Соответственно, в некоторых вариантах осуществления полипептид CTLA-4 содержит SEQ ID NO: 69 в положении остатков 59-65. Нумерация остатков представлена на фигуре 1A (верхний ряд нумерации, начиная с 1) и фигуре 2. Если присутствуют вставки или делеции, то фактическая нумерация остатков полипептида может отличаться от эталонной последовательности. На фигуре 1А также для сравнения показана нумерация по Swiss Prot.
Также может быть желательным вызвать мутацию С в положении 120, например, с помощью замены на S, для удаления дисульфидного мостика, образующегося между молекулами CTLA-4 в этом месте, и ингибирования димеризации CTLA-4. В других ситуациях желательным является сохранение или стимуляция димеризации или большей мультимеризации CTLA-4 (например, образование тетрамера). Этого можно достичь, например, посредством сохранения C120 и/или посредством добавления димеризирующих доменов, таких как полученные путем конъюгации CTLA-4 с Fc-участком IgG. Добавление таких доменов и образование макромолекул, содержащих CTLA-4, будет дополнительно рассмотрено далее.
Полипептид CTLA-4 может содержать аминокислотную последовательность SEQ ID NO: 68 или может содержать SEQ ID NO: 68 с одной или несколькими мутациями. Например, полипептид CTLA-4 может содержать SEQ ID NO: 68, содержащую до двенадцати мутаций, до десяти мутаций аминокислот или до пяти мутаций, например, одну, две или три мутации аминокислот. SEQ ID NO: 68 проиллюстрирована на фигуре 2 и является консенсусной последовательностью остатков, найденной в группе из шести полипептидов CTLA-4 с исключительно высокой функциональной активностью, которые были получены как описано в примерах. Шесть полипептидов имеют аминокислотные последовательности, показанные на фигуре 1A, со следующими SEQ ID NO: SEQ ID NO: 43 (вариант 1299), SEQ ID NO: 37 (вариант 1322), SEQ ID NO: 38 (вариант 1321), SEQ ID NO: 36 (вариант 1315), SEQ ID NO: 42 (вариант 1115) и SEQ ID NO: 47 (вариант 1227). Эти шесть последовательностей и варианты с одной или несколькими мутациями аминокислот, например, до двенадцати мутаций, например, до десяти мутаций аминокислот, например, до пяти мутаций, например, с одной, двумя или тремя мутациями аминокислот в любой из этих шести последовательностей, представляют примеры настоящего изобретения. Полипептид CTLA-4 может содержать последовательность полипептида CTLA-4 “1299”, депонированную под номером в NCIMB 41948, с одной или несколькими мутациями аминокислот, например, до двенадцати мутаций, например, до десяти мутаций аминокислот, например, до пяти мутаций, например, с одной, двумя или тремя мутациями аминокислот.
Полипептиды CTLA-4 в соответствии с настоящим изобретением могут содержать аминокислотную последовательность или состоять из аминокислотной последовательности, имеющей по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95%, 96%, 97%, 98% или 99% идентичности последовательности с SEQ ID NO: 68, с любой из SEQ ID NO: 36-55 или с последовательностью полипептида CTLA-4 “1299”, депонированной под номером доступа в NCIMB 41948.
Мутация или мутации могут содержать аминокислотные замены или состоять из аминокислотных замен и могут необязательно быть выбранными из следующих:
T в положении остатка 16; P в положении остатка 25; I в положении остатка 32; G в положении остатка 41; G в положении остатка 42; E в положении остатка 44; V в положении остатка 54; G в положении остатка 56; S или P в положении остатка 58; A в положении остатка 59; P в положении остатка 61; G в положении остатка 62; V или T в положении остатка 65; T, M или H в положении остатка 70; V, R, K или L в положении остатка 85; S в положении остатка 87; T, E или M в положении остатка 93; R, Q или E в положении остатка 104; V в положении остатка 106; D или S в положении остатка 108; V или F в положении остатка 115; S в положении остатка 120; делеция остатка 51.
Предпочтительно полипептид содержит N в положении 25 и/или содержит Q или H в положении 93. Полипептид может необязательно содержать S в положении 120.
Как отмечено ранее, полипептид предпочтительно содержит R, I, S или V в положении 16; T или A в положении 24; N в положении 25; S или G в положении 27; M или K в положении 54; N или S в положении 56; A, L или G в положении 58; T или S в положении 59; F или T в положении 60; L или Q в положении 61; D или Y в положении 63; S или P в положении 64; I, N или D в положении 65; A или S в положении 70; Q или R в положении 80; Q, M или S в положении 85; Q или H в положении 93 и/или C или S в положении 120. Так, полипептид содержит одну или несколько, например, по меньшей мере пять или шесть или все из следующих аминокислотных замен по отношению к SEQ ID NO: 35 CTLA-4 дикого типа: R, S или V в положении I16; T в положении A24; N в положении S25; S в положении G27; K в положении M54; S в положении N56; A или G в положении L58; S в положении T59; T в положении F 60; Q в положении L61; Y в положении D63; P в положении S 64; N или D в положении I65; A в положении S70; R в положении Q80; Q или S в положении M85; Q или H в положении K93.
Мутации в SEQ ID NO: 36-55 в сравнении с диким типом проиллюстрированы на фигуре 1A. Полипептид в соответствии с настоящим изобретением может содержать SEQ ID NO: 35 CTLA-4 дикого типа с одной или несколькими мутациями, показанными в качестве примера в этих вариантах, например, в комбинации с мутациями, присутствующими в любой из SEQ ID NO: 36-55. Полипептид может необязательно содержать дополнительные мутации, как рассматривалось ранее, например, необязательно одну или две дополнительные мутации.
Например, полипептид может содержать комбинацию мутаций, выбранных из:
- мутаций 1315, т.е. S в положении I16; N в положении S25; G в положении L58; A в положении S70; R в положении Q80; S в положении M85 и Q в положении K93;
- мутаций 1322, т.е. N в положении S25; S в положении G27; K в положении M54; S в положении N56; S в положении T59; T в положении F 60; Q в положении L61; Y в положении D63; P в положении S64; N в положении I65 и Q в положении K93;
- мутаций 1321, т.е. S в положении I16; N в положении S25; K в положении M54; G в положении L58; A в положении S70; R в положении Q80; S в положении M85 и Q в положении K93;
- мутаций 1115, т.е. V в положении I16; N в положении S25; G в положении L58; A в положении S70; Q в положении M85 и Q в положении K93;
- мутаций 1299, т.е. R в положении I16; T в положении A24; N в положении S25; S в положении G27; A в положении L58; A в положении S70; Q в положении M85 и Q в положении K93; и
- мутаций 1227, т.е. S в положении I16; N в положении S25; S в положении G27; A в положении L58; A в положении S70; Q в положении M85 и H в положении К93.
Соответственно, полипептид CTLA-4 может представлять собой полипептид, который содержит комбинацию замещенных остатков в любой из SEQ ID NO: 36-55 по отношению к дикому типу, например, он может содержать:
- S в положении остатка 16; N в положении остатка 25; G в положении остатка 58; A в положении остатка 70; R в положении остатка 80; S в положении остатка 85 и Q в положении остатка 93;
- N в положении остатка 25; S в положении остатка 27; K в положении остатка 54; S в положении остатка 56; S в положении остатка 59; T в положении остатка 60; Q в положении остатка 61; Y в положении остатка 63; P в положении остатка 64; N в положении остатка 65 и Q в положении остатка 93;
- S в положении остатка 16; N в положении остатка 25; K в положении остатка 54; G в положении остатка 58; A в положении остатка 70; R в положении остатка 80; S в положении остатка 85 и Q в положении остатка 93;
- V в положении остатка 16; N в положении остатка 25; G в положении остатка 58; A в положении остатка 70; Q в положении остатка 85 и Q в положении остатка 93;
- R в положении остатка 16; Т в положении остатка 24; N в положении остатка 25; S в положении остатка 27; A в положении остатка 58; A в положении остатка 70; Q в положении остатка 85 и Q в положении остатка 93;
- S в положении остатка 16; N в положении остатка 25; S в положении остатка 27; A в положении остатка 58; R в положении остатка 70; Q в положении остатка 85 и H в положении остатка 93.
Мутация предпочтительно является заменой и может быть консервативной заменой. Под “консервативной заменой” подразумевают замену первого аминокислотного остатка вторым, отличным аминокислотным остатком, где первый и второй аминокислотные остатки имеют боковые цепи, которые имеют сходные биофизические характеристики. Сходные биофизические характеристики включают гидрофобность, заряд, полярность или способность отдавать или принимать водородные связи. Примеры консервативных замен включают изменение серина на треонин или триптофан, глутамина на аспарагин, лизина на аргинин, аланина на валин, аспартата на глутамат, валина на изолейцин, аспарагина на серин.
Полипептиды в соответствии с настоящим изобретением могут включать одну или несколько мутаций аминокислотной последовательности (замену, делецию и/или вставку аминокислотного остатка) и менее чем приблизительно 15 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3 или 2.
Эти мутации обычно не приводят к потере функции, поэтому полипептид, содержащий измененную таким образом аминокислотную последовательность, может сохранять способность связываться с CD80 и/или CD86 человека. Он может сохранять ту же самую аффинность связывания или функцию что и полипептид, в котором не производили изменение, например, как измеряли в анализе, описанном в данном документе.
Мутация может включать замену одного или нескольких аминокислотных остатков на не встречающуюся в природе или нестандартную аминокислоту, модифицируя один или несколько аминокислотных остатков с получением не встречающейся в природе или нестандартной формы, или вставку одной или нескольких не встречающихся в природе или нестандартных аминокислот в последовательность. Примеры числа и местоположений изменений в последовательностях по настоящему изобретению описаны в других частях данного документа. Встречающиеся в природе аминокислоты включают 20 "стандартных" L-аминокислот, обозначаемых как G, A, V, L, I, M, P, F, W, S, T, N, Q, Y, C, K, R, H, D, E их стандартным однобуквенным кодом. Нестандартные аминокислоты включают любой другой остаток, который может быть внедрен в полипептидный скелет или который получен в результате модификации существующего аминокислотного остатка. Нестандартные аминокислоты могут быть встречающимися в природе или не встречающимися в природе. В данной области известен ряд встречающихся в природе нестандартных аминокислот, таких как 4-гидроксипролин, 5-гидроксилизин, 3-метилгистидин, N-ацетилсерин и др. [Voet & Voet, Biochemistry, 2nd Edition, (Wiley) 1995]. Аминокислотные остатки, дериватизированные по их N-альфа-положению, будут расположены только на N-конце аминокислотной последовательности. Как правило, в настоящем изобретении аминокислота представляет собой L-аминокислоту, однако она может представлять собой D-аминокислоту. Изменение может, таким образом, включать модификацию L-аминокислоты с получением D-аминокислоты или замену ее таковой. Метилированные, ацетилированные и/или фосфорилированные формы аминокислот также известны, и аминокислоты в настоящем изобретении могут быть подвергнуты таким модификациям.
Аминокислотные последовательности в полипептидах по настоящему изобретению могут содержать не встречающиеся в природе или нестандартные аминокислоты, описанные ранее. Нестандартные аминокислоты (например, D-аминокислоты) могут быть внедрены в аминокислотную последовательность во время синтеза или с помощью модификации или замены "первоначальных" стандартных аминокислот после синтеза аминокислотной последовательности.
Применение нестандартных и/или не встречающихся в природе аминокислот повышает структурное и функциональное разнообразие и может, таким образом, повышать возможность достижения желаемого связывания и нейтрализующих свойств. Также показано, что D-аминокислоты и аналоги имели отличные фармакокинетические профили по сравнению со стандартными L-аминокислотами в связи с in vivo разложением полипептидов с L-аминокислотами после введения животному, например, человеку, что означает, что D-аминокислоты являются предпочтительными для некоторых способов применения in vivo.
Варианты можно создавать с помощью случайного мутагенеза одного или нескольких выбранных генов VH и/или VL для создания мутаций во всем вариабельном домене. Такая методика описана Gram et al. [Gram et al., 1992, Proc. Natl. Acad. Sci., USA, 89:3576-3580], которые применяли ПЦР сниженной точности. Другим способом, который можно применять, является направленный мутагенез определенных участков или местоположений в полипептиде. Такие методики раскрыты Barbas et al. [Barbas et al., 1994, Proc. Natl. Acad. Sci., USA, 91:3809-3813] и Schier et al. [Schier et al., 1996, J. Mol. Biol. 263:551-567].
Все описанные выше методики известны как таковые в данной области, и специалист в данной области сможет применять такие методики для получения полипептидов по настоящему изобретению с помощью стандартной методологии в данной области.
Алгоритмы, которые можно применять для расчета % идентичности двух аминокислотных последовательностей, включают, например, BLAST [Altschul et al. (1990) J. Mol. Biol. 215: 405-410], FASTA [Pearson and Lipman (1988) PNAS USA 85: 2444-2448], или алгоритм Smith-Waterman [Smith and Waterman (1981) J. Mol Biol. 147: 195-197], например, применяя стандартные параметры.
В соответствии с настоящим изобретением могут быть предложены композиции, содержащие полипептиды CTLA-4, имеющие улучшенную биологическую активность, такую как повышенная селективность в отношении CD80 по сравнению с CD86, более высокая аффинность и/или более высокая эффективность, и/или они могут демонстрировать значительную перекрестную реактивность, повышенную стабильность и/или увеличенный период полужизни по сравнению с CTLA-4 дикого типа. Как подробно рассмотрено в данном документе, такие свойства могут способствовать большей терапевтической эффективности и могут обеспечивать возможность достижения благоприятных эффектов лечения при более низком или менее частом дозировании. Повышенная стабильность может облегчать производство и составление с получением фармацевтических композиций.
Полипептид CTLA-4 в соответствии с настоящим изобретением является необязательно конъюгированным с Fc-участком IgG, например, в виде белка слияния. Для повышения in vivo полужизни молекулы и придания общей стабильности композиции можно сконструировать Fc-участок, избегая при этом нежелательных эффекторных функций Fc. Повышенная стабильность облегчает составление препарата при высоких концентрациях, например, для подкожного введения.
Краткое описание графических материалов
Фигура 1. (A) Выравнивание последовательностей вариантов CTLA-4 (SEQ ID NO: 36-55) с CTLA-4 человека дикого типа (SEQ ID NO: 35). Мутации дикого типа показаны в серых рамках. Верхний ряд нумерации, начиная с 1, представляет собой нумерацию, на которую ссылаются в настоящем описании, если не указано иное. Для сравнения ниже показана нумерация по Swiss Prot. (В) Выравнивание последовательностей Fc IgG1 (SEQ ID NO: 56, SEQ ID NO: 57, SEQ ID NO: 58, SEQ ID NO: 59 и SEQ ID NO: 60. Верхний ряд нумерации, начиная с 1, представляет собой нумерацию, на которую ссылаются в настоящем описании, если не указано иное. Для сравнения ниже показана нумерация по Swiss Prot.
Фигура 2. Последовательность полипептида CTLA-4 SEQ ID NO: 68. При последовательной нумерации, начиная с Met в положении 1, SEQ ID NO: 68 имеет 124 остатка с вариабельностью в положении остатков 16, 24 27, 54, 56, 58, 59, 60, 61, 63, 64, 65, 70, 80, 85 и 93. Аминокислотный остаток в каждом из этих вариабельных положений выбран из группы остатков, указанных в каждом примере.
Фигура 3. Профили IC50 вариантов CTLA-4 и CTLA-4 дикого типа в формате слияния с Fc в: (A) двойном клеточном анализе на клетках Raji-Jurkat; (B) анализе первичных CD4+ T-клеток человека; (C) реакции смешанных лимфоцитов яванского макака.
Фигура 4. Специфичность вариантов CTLA-4 в отношении CD80 и CD86 по сравнению с другими родственными белковыми лигандами. (A) вариант 1299. (B) вариант 1322.
Фигура 5. Демонстрация нулевой эффекторной функции (ADCC и CDC) вариантов CTLA-4 с модификацией TM и YTE. (A) ADCC. (B) CDC.
Фигура 6. Улучшения моновалентной аффинности к CD80 и CD86 вариантов CTLA-4 по сравнению с CTLA-4 дикого типа в формате слияния с Fc.
Фигура 7. (A) Разработка конструкта для тетрамерного белка CTLA-4. (B) Сравнение эффективности в анализе Raji Jurkat CTLA-4 дикого типа в формате слияния с Fc по отношению к тетрамерному CTLA-4.
Подробное описание
Нумерация остатков CTLA-4, которая используется в настоящем описании, является такой, какая представлена на фигуре 1A (верхний ряд, нумерация последовательности), и фигуре 2, если не указано иное. CTLA-4 имеет лидерную последовательность, которая отщепляется, и возможны по меньшей мере две различные системы нумерации для зрелого белка. Последовательность CTLA-4 может начинаться, в числе прочего, с Ala в положении 1 (патент США 5434131) или с Met в положении 1 (Larsen et al., Am. J. Transplantation (2005) 5:443-453). Если в контексте четко не указано иное, система нумерации, используемая в данном документе, является такой, в которой в положении 1 находится Met. Она также соответствует нумерации, которая, как правило, используется для обозначения остатков препарата абатацепт.
Нумерация остатков Fc, которая используется в настоящем описании, является такой, какая представлена на фигуре 1B (верхний ряд, начиная с 1), если не указано иное.
Следующие пронумерованные пункты представляют собой аспекты настоящего изобретения:
1. Выделенный полипептид CTLA-4, имеющий большую аффинность связывания с CD80 человека, большую эффективность и/или большую стабильность по сравнению с SEQ ID NO: 35 CTLA-4 дикого типа, при этом полипептид содержит аминокислотную последовательность, которая является вариантом SEQ ID NO: 35, где вариант содержит пять или более из следующих мутаций аминокислот в SEQ ID NO: 35:
R, S, V или T в положении I16;
T в положении A24;
N или P в положении S25;
S в положении G27;
I в положении V32;
G в положении D41;
G в положении S42;
E в положении V44;
K в положении M54;
S или G в положении N56;
A, G, S или P в положении L58;
S или A в положении T59;
T в положении F 60;
Q или P в положении L61;
G в положении D 62;
Y в положении D63;
P в положении S 64;
N, D, V или T в положении I65;
A, T, M или H в положении S70;
R в положении Q80;
Q, S, V, R, K или L в положении M85;
S в положении T87;
Q, H, T, E или M в положении K93;
R, Q или E в положении L104;
V в положении I106;
D или S в положении N108;
V или F в положении I115;
S в положении C120;
делеция T51.
2. Полипептид CTLA-4 по пункту 1, где полипептид содержит аминокислотную последовательность, по меньшей мере на 70% идентичную SEQ ID NO: 35.
3. Полипептид CTLA-4 по пункту 1 или пункту 2, содержащий пять или более из следующих мутаций аминокислот:
R, S или V в положении I16;
T в положении A24;
N в положении S25;
S в положении G27;
K в положении M54;
S в положении N56;
A или G в положении L58;
S в положении T59;
T в положении F60;
Q в положении L61;
Y в положении D63;
P в положении S64;
N или D в положении I65;
A в положении S70;
R в положении Q80;
Q или S в положении M85;
Q или H в положении K93;
S в положении C120.
4. Полипептид CTLA-4 по пункту 1 или пункту 2, содержащий замену S25N или S25P.
5. Полипептид CTLA-4 по любому из пунктов 1-3, содержащий замену S25N, K93Q или K93H.
6. Полипептид CTLA-4 по любому из пунктов 1-5, содержащий аминокислотную последовательность, по меньшей мере на 70%, 80%, 90%, 95% или 98% идентичную любой из SEQ ID NO: 36-55, или аминокислотную последовательность, по меньшей мере на 70%, 80%, 90%, 95%, 98% или 99% идентичную аминокислотной последовательности CTLA-4, кодируемой нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948.
7. Полипептид CTLA-4 по любому из пунктов 1-6, содержащий аминокислотный мотив SEQ ID NO: 69 в положении остатков 59-65, при этом нумерация остатков указана по отношению к SEQ ID NO: 35.
8. Полипептид CTLA-4 по любому из пунктов 1-6, содержащий комбинацию мутаций, выбранных из:
- мутаций 1315, т.е. S в положении I16; N в положении S25; G в положении L58; A в положении S70; R в положении Q80; S в положении M85 и Q в положении K93;
- мутаций 1322, т.е. N в положении S25; S в положении G27; K в положении M54; S в положении N56; S в положении T59; T в положении F 60; Q в положении L61; Y в положении D63; P в положении S64; N в положении I65 и Q в положении K93;
- мутаций 1321, т.е. S в положении I16; N в положении S25; K в положении M54; G в положении L58; A в положении S70; R в положении Q80; S в положении M85 и Q в положении K93;
- мутаций 1115, т.е. V в положении I16; N в положении S25; G в положении L58; A в положении S70; Q в положении M85 и Q в положении K93;
- мутаций 1299, т.е. R в положении I16; T в положении A24; N в положении S25; S в положении G27; A в положении L58; A в положении S70; Q в положении M85 и Q в положении K93; и
- мутаций 1227, т.е. S в положении I16; N в положении S25; S в положении G27; A в положении L58; A в положении S70; Q в положении M85 и H в положении К93.
9. Полипептид CTLA-4 по любому из предыдущих пунктов, содержащий аминокислотную последовательность, выбранную из SEQ ID NO: 36-55, или содержащий аминокислотную последовательность CTLA-4, кодируемую нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948, или содержащий вариант любой из этих последовательностей, которые содержат до десяти мутаций аминокислот.
10. Полипептид CTLA-4 по любому из предыдущих пунктов, содержащий аминокислотную последовательность, выбранную из SEQ ID NO: 36-55, или содержащий аминокислотную последовательность CTLA-4, кодируемую нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948, или содержащий вариант любой из этих последовательностей, которые содержат до пяти мутаций аминокислот.
11. Полипептид CTLA-4 по пункту 10, содержащий аминокислотную последовательность, выбранную из SEQ ID NO: 36-55, или содержащий аминокислотную последовательность CTLA-4, кодируемую нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948, или содержащий вариант любой из этих последовательностей, которые содержат до трех мутаций аминокислот.
12. Полипептид CTLA-4 по пункту 1 или пункту 2, содержащий аминокислотную последовательность, выбранную из SEQ ID NO: 36-55, или содержащий аминокислотную последовательность CTLA-4, кодируемую нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948.
13. Полипептид CTLA-4 по пункту 12, содержащий аминокислотную последовательность, выбранную из SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42, SEQ ID NO: 47, или аминокислотную последовательность CTLA-4, кодируемую нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948.
14. Выделенный полипептид CTLA-4, имеющий большую аффинность связывания с CD80 человека, большую эффективность и/или большую стабильность по сравнению с SEQ ID NO: 35, где полипептид содержит:
(i) аминокислотную последовательность SEQ ID NO: 68, SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42 или SEQ ID NO: 47;
(ii) аминокислотную последовательность, которая является вариантом (i), содержащим до десяти мутаций аминокислот, где остаток 25 не мутирован и представляет собой N;
(iii) аминокислотную последовательность, которая является вариантом (i), содержащим одну или несколько мутаций аминокислот, где остаток 25 не мутирован и представляет собой N, при этом вариант имеет по меньшей мере 70% идентичности последовательности с (i); или
(iv) аминокислотную последовательность CTLA-4, кодируемую нуклеиновой кислотой, депонированной под номером в NCIMB 41948.
15. Полипептид CTLA-4 по пункту 14, содержащий SEQ ID NO: 68, SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42 или SEQ ID NO: 47 или вариант любой из этих последовательностей, которые содержат до пяти мутаций аминокислот.
16. Полипептид CTLA-4 по пункту 15, содержащий SEQ ID NO: 68, SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42 или SEQ ID NO: 47 или вариант любой из этих последовательностей, которые содержат до трех мутаций аминокислот.
17. Полипептид CTLA-4 по пункту 14, где полипептид содержит аминокислотную последовательность, имеющую по меньшей мере 80% идентичности последовательности с SEQ ID NO: 68, SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42 или SEQ ID NO: 47.
18. Полипептид CTLA-4 по пункту 17, где полипептид содержит аминокислотную последовательность, имеющую по меньшей мере 90%, 95%, 98% или 99% идентичности последовательности с SEQ ID NO: 68, SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42 или SEQ ID NO: 47.
19. Полипептид CTLA-4 по любому из предыдущих пунктов, имеющий аффинность связывания с CD80 человека 50 нМ или менее, где аффинность выражена Kd, определяемой с помощью поверхностного плазмонного резонанса.
20. Полипептид CTLA-4 по пункту 19, имеющий аффинность связывания с CD80 человека 20 нМ или менее, где аффинность выражена Kd, определяемой с помощью поверхностного плазмонного резонанса.
21. Полипептид CTLA-4 по любому из предыдущих пунктов, где полипептид имеет большую аффинность связывания с CD86 человека, чем CTLA-4 дикого типа (SEQ ID NO: 35).
22. Полипептид CTLA-4 по любому из пунктов 14-21, содержащий:
- S в положении остатка 16; N в положении остатка 25; G в положении остатка 58; A в положении остатка 70; R в положении остатка 80; S в положении остатка 85 и Q в положении остатка 93;
- N в положении остатка 25; S в положении остатка 27; K в положении остатка 54; S в положении остатка 56; S в положении остатка 59; T в положении остатка 60; Q в положении остатка 61; Y в положении остатка 63; P в положении остатка 64; N в положении остатка 65 и Q в положении остатка 93;
- S в положении остатка 16; N в положении остатка 25; K в положении остатка 54; G в положении остатка 58; A в положении остатка 70; R в положении остатка 80; S в положении остатка 85 и Q в положении остатка 93;
- V в положении остатка 16; N в положении остатка 25; G в положении остатка 58; A в положении остатка 70; Q в положении остатка 85 и Q в положении остатка 93;
- R в положении остатка 16; Т в положении остатка 24; N в положении остатка 25; S в положении остатка 27; A в положении остатка 58; A в положении остатка 70; Q в положении остатка 85 и Q в положении остатка 93 или
- S в положении остатка 16; N в положении остатка 25; S в положении остатка 27; A в положении остатка 58; R в положении остатка 70; Q в положении остатка 85 и H в положении остатка 93.
23. Полипептид CTLA-4 по любому из пунктов 14-22, содержащий аминокислотную последовательность SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42 или SEQ ID NO: 47, содержащую до трех мутаций аминокислот.
24. Полипептид CTLA-4 по любому из пунктов 14-18, содержащий: R, I, S или V в положении 16; T или A в положении 24; S или G в положении 27; M или K в положении 54; N или S в положении 56; A, L или G в положении 58; T или S в положении 59; F или T в положении 60; L или Q в положении 61; D или Y в положении 63; S или P в положении 64; I, N или D в положении 65; A или S в положении 70; Q или R в положении 80; Q, M или S в положении 85; Q или H в положении 93 и C или S в положении 120.
25. Полипептид CTLA-4 по любому из пунктов 14-18, где мутации аминокислот выбраны из следующих: замена T в положении остатка 16; замена I в положении остатка 32; замена G в положении остатка 41; замена G в положении остатка 42; замена E в положении остатка 44; замена G в положении остатка 56; замена S или P в положении остатка 58; замена A в положении остатка 59; замена P в положении остатка 61; замена G в положении остатка 62; замена V или T в положении остатка 65; замена T, M или H в положении остатка 70; замена V, R, K или L в положении остатка 85; замена S в положении остатка 87; замена T, E или M в положении остатка 93; замена R, Q или E в положении остатка 104; замена V в положении остатка 106; замена D или S в положении остатка 108; замена V или F в положении остатка 115; замена S в положении остатка 120; делеция остатка 51.
26. Полипептид CTLA-4 по пункту 14, содержащий аминокислотную последовательность SEQ ID NO: 68, SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42 или SEQ ID NO: 47 или содержащий аминокислотную последовательность CTLA-4, кодируемую нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948.
27. Выделенный полипептид CTLA-4, который имеет аффинность связывания с CD80, по меньшей мере в 10 раз превышающую аффинность связывания с CD86.
28. Полипептид CTLA-4 по пункту 27, который имеет аффинность связывания с CD80, по меньшей мере в 50 раз превышающую аффинность связывания с CD86.
29. Полипептид CTLA-4 по пункту 27 или пункту 28, где полипептид является таким, как определено в любом из пунктов 1-26.
30. Полипептид CTLA-4 по любому из предыдущих пунктов, конъюгированный с аминокислотной последовательностью Fc IgG.
31. Полипептид CTLA-4 по пункту 30, где Fc IgG представляет собой Fc IgG1 человека, модифицированный с целью снижения эффекторной функции Fc, и содержит нативную шарнирную область Fc IgG1 человека.
32. Полипептид CTLA-4 по пункту 30 или пункту 31, где аминокислотная последовательность Fc IgG содержит Fc-участок IgG1 человека, в котором одна или обе из следующих групп остатков замещены следующим образом:
F в положении остатка 20; E в положении остатка 21; S в положении остатка 117 и
Y в положении остатка 38, T в положении остатка 40, E в положении остатка 42,
при этом нумерация остатков определена по отношению к SEQ ID NO: 56.
33. Полипептид CTLA-4 по любому из пунктов 30-32, где аминокислотная последовательность Fc IgG содержит SEQ ID NO: 59.
34. Выделенный полипептид CTLA-4, содержащий аминокислотную последовательность CTLA-4-Ig 1299, кодируемую нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948.
35. Полипептид CTLA-4 по любому из предыдущих пунктов, где полипептид находится в мультимере.
36. Полипептид CTLA-4 по пункту 35, где полипептид CTLA-4 находится в димере.
37. Полипептид CTLA-4 по пункту 35, где полипептид CTLA-4 находится в тетрамере.
38. Полипептид CTLA-4 по пункту 37, где тетрамер содержит две пары полипептидов CTLA-4, при этом каждая пара включает полипептид CTLA-4, слитый с константной областью легкой цепи антитела, и полипептид CTLA-4, слитый с константной областью тяжелой цепи антитела.
39. Клетка-хозяин, содержащая нуклеиновую кислоту, где нуклеиновая кислота содержит последовательность нуклеиновой кислоты CTLA-4-Ig 1299, депонированную под номером доступа в NCIMB 41948.
40. Композиция, содержащая
полипептид CTLA-4 по любому из предыдущих пунктов и
один или несколько фармацевтических наполнителей.
41. Композиция, содержащая
полипептид CTLA-4, содержащий аминокислотную последовательность SEQ ID NO: 68, SEQ ID NO: 43, SEQ ID NO: 47, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42, SEQ ID NO: 47 или аминокислотную последовательность CTLA-4, кодируемую нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948, конъюгированную с аминокислотной последовательностью Fc IgG; и
один или несколько фармацевтических наполнителей.
42. Композиция по пункту 40 или пункту 41, где полипептид CTLA-4 конъюгирован с аминокислотной последовательностью Fc IgG, содержащей SEQ ID NO: 59.
43. Композиция по пункту 42, где полипептид CTLA-4, конъюгированный с Fc IgG, содержит аминокислотную последовательность SEQ ID NO: 13, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 14, SEQ ID NO: 15 или SEQ ID NO: 16.
44. Композиция, содержащая полипептид CTLA-4-Ig 1299, кодируемый нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948, и один или несколько фармацевтических наполнителей.
45. Композиция по любому из пунктов 40-44, содержащая полипептид CTLA-4 в концентрации по меньшей мере 70 мг/мл.
46. Композиция по пункту 45, содержащая полипептид CTLA-4 в концентрации по меньшей мере 100 мг/мл.
47. Полипептид CTLA-4 по любому из пунктов 1-38 или композиция по любому из пунктов 40-46 для применения в способе лечения пациента посредством подкожного или внутривенного введения.
48. Полипептид CTLA-4 по любому из пунктов 1-38 или композиция по любому из пунктов 40-46 для применения в способе лечения ревматоидного артрита, рассеянного склероза, астмы, болезни Крона, язвенного колита, системной красной волчанки или отторжения трансплантата.
49. Полипептид CTLA-4 по любому из пунктов 1-38 или композиция по любому из пунктов 40-46 для применения в способе лечения, включающем введение указанного полипептида CTLA-4 или указанной композиции пациенту с интервалами 28 дней.
50. Способ получения дополнительного полипептида CTLA-4 посредством мутации аминокислотной последовательности полипептида CTLA-4, выбранной из SEQ ID NO 36-55, или аминокислотной последовательности CTLA-4, кодируемой нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948, при этом способ включает:
обеспечение полипептида CTLA-4, содержащего или состоящего из аминокислотной последовательности SEQ ID NO 36-55 или аминокислотной последовательности CTLA-4, кодируемой нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948;
введение одной или нескольких мутаций в аминокислотную последовательность для обеспечения дополнительного полипептида CTLA-4;
исследование стабильности, аффинности и/или эффективности дополнительного полипептида CTLA-4 и
составление дополнительного полипептида CTLA-4 с получением композиции, содержащей один или несколько фармацевтических наполнителей.
51. Способ по пункту 50, отличающийся тем, что дополнительный полипептид CTLA-4 конъюгирован с Fc-участком.
Биологическая эффективность
Растворимый CTLA-4 конкурирует с CD28, экспрессируемым на поверхности T-лимфоцитов, ингибируя связывание лигандов CD80 (B7.1) и CD86 (B7.2) с CD28, которое в противном случае приведет к костимуляции и активации T-лимфоцитов. Таким образом, растворимый CTLA-4 ингибирует активацию T-лимфоцитов. Силу этого ингибирования с помощью экзогенного растворимого CTLA-4 можно определить в анализах in vitro. Полипептид CTLA-4 необязательно может быть конъюгирован с другой молекулой, например, в виде белка слияния. Например, может присутствовать Fc IgG, как описано в других частях данного документа. Анализ можно применять для качественного определения того, является ли полипептид CTLA-4 более или менее эффективным по сравнению с диким типом, применяя CTLA-4 дикого типа (необязательно конъюгированный с Fc, в зависимости от ситуации) в качестве контроля, и он также может давать количественную информацию касательно величины различия активности. В данной области известны способы выполнения таких анализов и анализа статистической значимости данных для получения достоверной качественной и количественной информации.
Связывание полипептида CTLA-4 можно измерить по выработке IL-2, поскольку связывание CTLA-4 с CD80 и CD86 уменьшает выработку IL-2. Подходящие анализы могут включать выявление количества выработанного IL-2, например, с помощью ELISA.
Снижение уровня выработки IL-2 может быть частичным или полным. Полипептид CTLA-4 может снижать выработку IL-2 по меньшей мере на 50%, 75% или 80%, более предпочтительно по меньшей мере на 85%, 90% или 95% при исследуемых концентрациях.
Для выявления полипептидов CTLA-4 с более высокой эффективностью по сравнению с таковой дикого типа можно применять двойной клеточный анализ. Анализ полипетидов CTLA-4 проводят для измерения ингибирования передачи сигналов. Совместное культивирование T-клеток, экспрессирующих CD28 (например, клеток Jurkat), и B-клеток, экспрессирующих CD80 и CD86 (например, клеток Raji) приводит к выработке IL-2 благодаря взаимодействию между CD28 и лигандами CD80 и CD86 в присутствии фитогемагглютинина (PHA). IL-2 затем выявляют с помощью ELISA. См. пример 3 в качестве подробного отработанного примера этого анализа.
Для дальнейшей оценки эффективности выбранных полипептидов можно применять анализ активации первичных Т-клеток человека. Полипептиды CTLA-4 можно распределить по их способности ингибировать опосредованную CD80/86 секрецию IL-2 первичными CD4+ Т-лимфоцитами человека. Полипептиды CTLA-4 также можно распределить по их способности ингибировать пролиферацию CD4+ лимфоцитов человека, стимулированную антителами к CD3, в присутствии клеток Raji, экспрессирующих CD80 и CD86. Оценить пролиферацию можно с помощью гомогенного люминесцентного анализа (ATP lite). Преимуществом этого анализа является то, что он позволяет измерять эффективность полипептидов CTLA-4 в отношении блокады активации первичных CD4+ лимфоцитов человека. См. пример 4 в качестве подробного отработанного примера этого анализа.
Показано, что в анализе, в котором измеряют активацию Т-клеток, определенные полипептиды CTLA-4 в соответствии с настоящим изобретением связываются с CD80 и CD86 с высокой эффективностью. Полипептиды CTLA-4 блокируют лиганды CD80 и CD86, предупреждая, таким образом, дополнительные сигналы активации от этих молекул, что приводит к снижению выработки IL-2.
Эффективность полипептидов CTLA-4 можно определить или измерить с помощью одного или нескольких анализов, известных специалисту в данной области и/или описанных или упоминаемых в данном документе. Эффективность является мерой активности, выраженной количеством, необходимым для получения эффекта. В клеточном анализе обычно сравнивают титрование пептида и регистрируют значения IC50. В функциональном анализе IC50 является концентрацией препарата, которая снижает биологический ответ на 50% от своего максимума. IC50 можно рассчитать, откладывая графически % максимального биологического ответа как функцию логарифма концентрации препарата и применяя компьютерную программу, такую как Prism (GraphPad), для подбора сигмоидальной функции к данным для получения значений IC50. Чем меньше значение IC50, тем более эффективным является препарат.
Полипептиды CTLA-4 можно описывать с точки зрения наличия как можно меньшей повышенной эффективности, необходимой, по сравнению с референтными (например, дикого типа) полипептидами CTLA-4, для ингибирования выработки IL-2. Это также отражено в регистрируемых значениях IC50. Предпочтительные полипептиды CTLA-4 имеют повышенную эффективность по сравнению с таковой CTLA-4 дикого типа (SEQ ID NO: 35).
Полипептид CTLA-4 в соответствии с настоящим изобретением может иметь большую эффективность, чем CTLA-4 дикого типа, содержащий SEQ ID NO: 35, где эффективность отражает снижение IC50 при анализе выработки IL-2 T-клетками, активированным B-клетками. Эффективность может по меньшей мере в 10 раз, по меньшей мере в 15 раз, по меньшей мере в 20 раз, по меньшей мере в 30 раз, по меньшей мере в 40 раз или по меньшей мере в 50 раз превосходить таковую дикого типа. Показано, что описанный в примерах в данном документе один полипептид с SEQ ID NO: 36 (вариант 1315) имел приблизительно в 120 раз большую эффективность, чем CTLA-4 дикого типа. Эффективность может, например, до 150 раз, до 130 раз, до 120 раз, до 100 раз, до 80 раз, до 70 раз или до 60 раз превосходить таковую дикого типа. Повышение эффективности может, например, превышать таковое дикого типа в диапазоне от 10 раз до 100 раз.
Эффективность полипептида CTLA-4 можно определять по отношению к последовательностям полипептида CTLA-4, показанным в качестве примера в данном документе, а не (или также) по отношению к дикому типу, например, эффективность можно сравнить с таковой любой из SEQ ID NO: 37 (вариант 1322), SEQ ID NO: 38 (вариант 1321), SEQ ID NO: 43 (вариант 1299), SEQ ID NO: 36 (вариант 1315), SEQ ID NO: 42 (вариант 1115), SEQ ID NO: 47 (вариант 1227) или варианта 1299, кодируемого нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948. Таким образом, один из этих вариантов CTLA-4 можно применять в качестве контроля в данном анализе. Полипептид CTLA-4 может быть по меньшей мере таким же эффективным, как один или несколько из этих вариантов, например, по меньшей мере таким же активным, как SEQ ID NO: 43 (вариант 1299) или SEQ ID NO: 47 (вариант 1227). Полипептид CTLA-4 может иметь эффективность, приблизительно такую же или ниже, чем эффективность SEQ ID NO: 36 (вариант 1315).
Аффинность
Аффинность связывания полипептида CTLA-4 с CD80 или CD86 можно определить как моновалентную аффинность, применяя поверхностный плазмонный резонанс для определения Kd. См. пример 8 в качестве отработанного примера применения поверхностного плазмонного резонанса для измерения аффинности связывания и определения Kd. Для определения относительной аффинности полученную Kd можно сравнить с Kd CTLA-4 дикого типа с SEQ ID NO: 35 или сравнить с Kd одного из полипептидов CTLA-4 с SEQ ID NO: 37 (вариант 1322), SEQ ID NO: 38 (вариант 1321), SEQ ID NO: 43 (вариант 1299), SEQ ID NO: 36 (вариант 1315), SEQ ID NO: 42 (вариант 1115), SEQ ID NO: 47 (вариант 1227) или варианта 1299, кодируемого нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948. Полипептид CTLA-4 может иметь большую аффинность связывания с CD86 человека и/или CD80 человека по сравнению с аффинностью CTLA-4 дикого типа.
Полипептид CTLA-4 может иметь аффинность связывания с CD80 человека, превосходящую аффинность связывания CTLA-4 дикого типа, например, по меньшей мере в 10 раз, по меньшей мере в 15 раз, по меньшей мере в 20 раз, по меньшей мере в 30 раз, по меньшей мере в 40 раз, по меньшей мере в 50 раз, по меньшей мере в 100 раз или по меньшей мере в 140 раз по сравнению с таковой дикого типа. Полипептид CTLA-4 может иметь по меньшей мере аффинность связывания CD80 человека с одной или несколькими из SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42 и SEQ ID NO: 47 или по меньшей мере аффинность варианта CTLA-4 1299, кодируемого нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948. Полипептид CTLA-4 может иметь аффинность связывания с CD80 человека, которая приблизительно такая же или ниже, чем аффинность SEQ ID NO: 37. Kd связывания с CD80 человека может составлять 50 нМ или менее, например, 25 нМ или менее, 20 нМ или менее или 10 нМ или менее. Например, Kd может находиться в диапазоне от 5 до 50 нМ.
Полипептид CTLA-4 может иметь аффинность связывания с CD86 человека, превосходящую аффинность связывания CTLA-4 дикого типа, например, по меньшей мере в 2 раза, по меньшей мере в 3 раза, по меньшей мере в 4 раза, по меньшей мере в 5 раз или меньшей мере в 10 раз по сравнению с таковой дикого типа. Полипептид CTLA-4 может иметь по меньшей мере аффинность связывания CD86 человека с одной или несколькими из SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42 и SEQ ID NO: 47 или по меньшей мере аффинность варианта CTLA-4 1299, кодируемого нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948. Полипептид CTLA-4 может иметь аффинность связывания с CD86 человека, которая приблизительно такая же или ниже, чем активность SEQ ID NO: 37. Kd связывания с CD86 человека может составлять 2 мкМ или менее, например, 1,5 мкМ или менее или 1 мкМ или менее. Например, Kd может находиться в диапазоне от 0,5 до 2 мкМ.
Селективность в отношении CD80 по сравнению с CD86
Полипептиды CTLA-4, описанные в данном документе, могут связываться с CD80 и CD86, однако могут селективно связываться с CD80 вместо CD86. Известно, что CTLA-4 дикого типа имеет более высокую аффинность связывания с CD80 по сравнению с CD86, и полипептид CTLA-4 в соответствии с настоящим изобретением может также иметь большую аффинность связывания с CD80, чем аффинность связывания с CD86. В то же время, полипептид CTLA-4 может иметь большую селективность связывания с CD80 вместо CD86 по сравнению с CTLA-4 дикого типа. Например, в анализах поверхностного плазмонного резонанса, описанных в данном документе, CTLA-4 дикого типа характеризовался аффинностью связывания с CD80, приблизительно в 4 раза превосходящей аффинность связывания с CD86. Напротив, полипептиды CTLA-4 могут характеризоваться аффинностью связывания с CD80, более чем в 10 раз, более чем в 20 раз, более чем в 30 раз, более чем в 40 раз или более чем в 50 раз превосходящей аффинность связывания с CD86. Например, полипептид CTLA-4 может характеризоваться аффинностью связывания с CD80, до 120 раз или 130 раз превосходящей аффинность связывания с CD86. Таким образом, по сравнению с аффинностью CTLA-4 дикого типа, полипептид CTLA-4 может характеризоваться большей аффинностью связывания с CD80, чем с CD86. Селективную предпочтительность по отношению к CD80 по сравнению с CD86 можно наблюдать в случае CD80 человека и CD86 человека.
Также такая же селективная предпочтительность может сохраняться в случае CD80 и CD86 яванского макака. Кратность различия аффинности связывания с CD80 по сравнению с CD86 может быть приблизительно одинаковой для CD80 и CD86 человека и яванского макака.
Повышение аффинности связывания с CD80 должно обеспечивать лучший биологический профиль для медицинского применения. Связываясь с CD80, выработка которого стимулируется на антигенпредставляющих клетках в рамках активного иммунного ответа, CTLA-4 ингибирует связывание CD80 с CD28 на T-клетках, блокируя, таким образом, сигнал активации к T-клетке. Таким образом, полипептид CTLA-4 можно применять для ослабления ответа T-клеток in vivo и лечения состояний, при которых это является благоприятным, как описано в других частях данного документа.
Разрабатывая полипептид CTLA-4, который селективно воздействует на CD80 по сравнению с CD86, можно получить очень существенное увеличение аффинности связывания с CD80. Хотя литературные данные не являются убедительными касательно относительной роли CD80 и CD86, полипептиды по настоящему изобретению селективно связываются с CD80 по сравнению с CD86 и характеризуются отличными биологическими профилями, подходящими для терапевтического применения, как показано в различных анализах. Не привязываясь к теории, характеристики полипептидов CTLA-4 по настоящему изобретению могут быть обусловлены по меньшей мере частично, высокой аффинностью связывания с CD80 и/или предпочтительным связыванием с CD80 по сравнению с CD86.
Различные данные указывают на роль CD80, передающих сигнал повышенной активации к Т-лимфоцитам. Например,
CD80-трансдуцированные клетки CHO индуцируют повышенную выработку IL-2 первичными Т-клетками человека по сравнению с CD86-трансдуцированными клетками CHO (Slavik et al. JBC 274(5):3116-3124 1999);
CD80 индуцирует повышенную активность NFκB и фактора транскрипции AP-1 по сравнению с CD86 в Т-клетках Jurkat (факторы, важные для выработки цитокинов, таких как IL-2) (Olsson et al. Int. Immunol. 10(4):499-506 1998);
CD80 индуцирует повышенную экспрессию CD25 в CD8+ T-клетках, взаимодействующих с дендритными клетками, инфицированными вирусом, по сравнению с CD86 (важно для выживания и пролиферации T-клеток) (Pejawar-Gaddy & Alexander-Miller J. Immunol. 177:4495-4502 2006); и
в мышиной модели аллергической астмы с применением мутированной молекулы CTLA-4 Ig обнаружено, что CD80, а не CD86, является основным фактором легочной эозинофилии (Harris et al. J. Exp. Med. 185(1) 1997).
Предпочтительно повышение аффинности CTLA-4 к CD80 может, таким образом, приводить к повышенному ингибированию активации T-клеток путем нацеливания на более эффективный путь активации Т-клеток с помощью CD80.
Также существует ряд доказательств того, что передача сигналов с помощью CD86 может оказывать благоприятное противовоспалительное действие в некоторых моделях заболеваний. Например, в мышиной модели сепсиса наблюдалось, что тяжесть заболевания и смертность были связаны со стимуляцией выработки CD80 и сопутствующим подавлением CD86 (Nolan et al. PLoS ONE 4(8):6600 2009). Таким образом, селективное связывание с CD80 по сравнению с CD86 может давать преимущество, поскольку при этом ингибируется связывание CD80 с CD28 наряду с меньшей степенью снижения взаимодействия с CD28.
CD80- и CD86-положительные клетки могут встречаться в суставах пациентов с ревматоидным артритом, и связывание этих обеих молекул B7 может способствовать терапевтической эффективности, в то время как селективность в отношении CD80 по сравнению с CD86 также может способствовать желаемым количественным и качественным эффектам в подавлении активации T-клеток. Соответственно, полипептиды CTLA-4 по настоящему изобретению могут связываться и с CD80, и с CD86, и могут иметь более высокую аффинность к CD80, чем CTLA-4 дикого типа, и также могут иметь более высокую аффинность к CD86, чем аффинность CTLA-4 дикого типа.
Перекрестная реактивность
Предпочтительно полипептиды CTLA-4 в соответствии с настоящим изобретением сохраняют профиль перекрестной реактивности CTLA-4 дикого типа.
Полипептид CTLA-4 может проявлять перекрестную реактивность связывания с CD80 и CD86 яванского макака и/или мыши, а также CD80 и CD86 человека. Различие аффинности к CD80 яванского макака и таковой к CD80 человека может составлять до 10 раз, до 5 раз, до 2 раз, до 1,5 раза или до 1,2 раза. Различие аффинности к CD86 яванского макака и таковой к CD86 человека может составлять до 10 раз, до 5 раз, до 2 раз, до 1,5 раза или до 1,2 раза. Различие аффинности CD80 мыши и таковой к CD80 человека может составлять до 10 раз, до 5 раз, до 2 раз, до 1,5 раза или до 1,2 раза. Различие аффинности CD86 мыши и таковой к CD86 человека может составлять до 10 раз, до 5 раз, до 2 раз, до 1,5 раза или до 1,2 раза.
Полипептид CTLA-4 может ингибировать активацию Т-лимфоцитов яванского макака, например, измеряемую по ингибированию выработки IL-2 в реакции смешанных лимфоцитов с применением мононуклеарных клеток периферической крови яванских макаков. Этот полипептид может проявлять большую эффективность, чем CTLA-4 дикого типа в анализе ингибирования активации Т-лимфоцитов яванского макака.
Данные по видовой перекрестной реактивности, например, полипептидов CTLA-4 по настоящему изобретению, показаны в примере 8.
Полипептид CTLA-4 может проявлять специфическое связывание с CD80 и CD86 вместо других белков семейства В7. Таким образом, может наблюдаться отсутствие перекрестной реактивности с PD-L2, B7-H1, B7-H2, B7-H3 и B7-H3B.
В данной области известны анализы для определения специфичности. Например, можно применять иммуноферментный анализ. См. пример 6 в качестве отработанного примера подходящего анализа.
Стабильность
Полипептид CTLA-4 предпочтительно сохраняет по меньшей мере стабильность CTLA-4 дикого типа и предпочтительно является более стабильным по сравнению с диким типом, например, при измерениях для CTLA-4 самого по себе или конъюгированного CTLA-4 (например, слитого) с Fc-участком, как описано далее.
Предполагается, что более стабильные конъюгаты CTLA-4 Fc (“CTLA-4 Ig”) смогут лучше переносить составление при высоких (например, ≥100 мг/мл) концентрациях, требуемых для подкожного введения.
Стабильного можно исследовать в анализе в отношении разложения. Как правило, анализ включает инкубацию препарата при фиксированной температуре (например, 5°C или 25°C) в течение периода времени, например, в течение месяца, и определение степени утраты чистоты (степень разложения) в течение этого месяца. Агрегация и/или фрагментация может способствовать утрате чистоты, и каждый процесс можно измерять отдельно для определения процента, и два значения в сумме дадут % утраты чистоты. Отработанные примеры анализов в отношении разложения представлены в примере 9 и примере 10.
Полипептид CTLA-4 с улучшенной стабильностью может быть пригодным в способах введения, таких как подкожное введение, в связи со сниженной агрегацией, которая не только повышает эффективность, но также снижает риск нейтрализации или связывания секретированных антител.
Конъюгация с Fc
В одном варианте осуществления настоящее изобретение предлагает молекулу CTLA-4 Ig с оптимизированной аффинностью, необязательно с увеличенным периодом полужизни (например, включающим мутацию YTE, также описанную в данном документе), для подкожного или внутривенного состава и для ежемесячного, с интервалом 28 дней или менее, дозирования для лечения RA от средней до тяжелой степени тяжести или других описанных состояний.
Настоящее изобретение предлагает полипептид, который состоит из последовательности полипептида CTLA-4 или который содержит или конъюгирован с пептидом или последовательностью полипептида, например, с молекулой антитела или частью молекулы антитела. Например, полипептид CTLA-4 может быть конъюгирован с аминокислотной последовательностью Fc антитела, например, Fc IgG. Fc-участок содержит шарнирную область, CH2- и CH3-участок. Предпочтительно, IgG является IgG человека, например, IgG1, IgG2 или IgG4.
Известны аллотипные варианты IgG1. Предпочтительно, Fc-участок IgG1 содержит E в положении остатка 142 и M в положении остатка 144 (нумерация соответствует SEQ ID NO: 56, начиная с 1, как показано на фигуре 1). Этот аллотип широко представлен в общей популяции. Альтернативный Fc-участок IgG1, представляющий другой аллотип, содержит D в положении остатка 142 и L в положении остатка 144. Этот аллотип используется в абатацепте.
Аминокислотная последовательность Fc IgG может содержать аминокислотную последовательность Fc IgG человека (например, IgG1 или IgG4) с определенными мутациями. Например, если IgG человека является IgG1, аминокислотная последовательность может быть мутированной с целью снижения или устранения эффекторных функций Fc, например, комплементзависимой цитотоксичности (CDC) и антителозависимой клеточноопосредованной цитотоксичности (ADCC). Устранение эффекторных функций Fc можно подтвердить в известных стандартных анализах. Иллюстративные анализы для определения ADCC и CDC см. в примере 7.
Известно, что эффекторную функцию IgG1 можно уменьшить с помощью мутации шарнирной области Fc IgG1. Примером этого является конструкт CTLA-4 - Fc IgG1 абатацепта, который внедряет мутированную шарнирную последовательность в Fc-участок IgG1, в котором C дикого типа мутирован в S. Участок IgG1 абатацепта включает аминокислотную последовательность SEQ ID NO: 71, которая соответствует аминокислотной последовательности Fc IgG1 дикого типа человека SEQ ID NO: 70 с С дикого типа, замещенным S. Замены происходят в положении остатков 6, 12 и 15 Fc-участка.
SEQ ID NO: 70 VEPKSCDKTHTCPPCPAPE
SEQ ID NO: 71 QEPKSSDKTHTSPPSPAPE
В контексте настоящего изобретения неожиданно было открыто, что эта мутация снижает стабильность Fc-домена, поэтому слияние CTLA4 - Fc IgG1 абатацепта имеет в целом более низкую стабильность, чем слияние CTLA-4 - Fc IgG1, в котором применяется последовательность Fc IgG1 дикого типа. Эта утрата стабильности является нежелательной, однако, несмотря на это, она важна для снижения или устранения эффекторной функции Fc IgG1.
Fc-участок, конъюгированный с полипептидом CTLA-4 по настоящему изобретению, предпочтительно не содержит SEQ ID NO: 71. Предпочтительно в положении остатка 6, 12 и/или 15 Fc сохраняется цистеин. Предпочтительно конъюгат CTLA-4 - Fc в соответствии с настоящим изобретением содержит шарнирную область Fc IgG1 человека дикого типа. Предпочтительно Fc-участок содержит SEQ ID NO: 70. Fc-участок может быть участком Fc полипептида CTLA-4 1299, кодируемого нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948.
Хотя реверсия Fc абатацепта к дикому типу устраняет нестабильность, вызванную мутацией Fc, она также восстанавливает эффекторные функции Fc IgG1, которые нежелательны во многих терапевтических областях применения. Соответственно, эта мутация улучшает стабильность Fc-домена абатацепта, но только за счет повторного введения нежелательной эффекторной функции.
Можно применять другие Fc-участки IgG с пониженной эффекторной функцией или без эффекторной функции, например, IgG2.
Настоящее изобретение предлагает способ применения Fc IgG1, не имеющего эффекторных функций, в то же время преодолевая проблему пониженной стабильности, свойственную мутации абатацепта. Fc-участок в соответствии с настоящим изобретением может представлять собой Fc IgG1, содержащий тройную мутацию (TM) L20F, L21E, P117S (Oganesyan et al 2008 Acta Crystallogr D Biol Crystallogr. 64:700-4). Эта мутация снижает эффекторную функцию Fc без снижения стабильности. Соответственно, такой Fc-домен облегчает составление конструктов CTLA-4 - Fc при высоких концентрациях, которые пригодны для получения композиций для подкожного введения.
Более того, благоприятных эффектов можно достичь посредством внедрения мутации “YTE” в Fc-участок (Dall’Acqua et al 2006 J Biol Chem. 281:23514-24). Мутация YTE обеспечивает увеличенный период полужизни in vivo, который может улучшить терапевтическую эффективность и/или может обеспечивать возможность достижения благоприятных эффектов лечения при сниженном или менее частом дозировании, таком как ежемесячное дозирование. Fc-домен, применяемый в продуктах по настоящему изобретению, может содержать Y в положении остатка 38, T в положении остатка 40 и E в положении остатка 42. Указанное представляет мутацию M38Y, S40T, T42E Fc IgG1 человека.
За исключением YTE и/или тройной мутации, отмеченных выше, предпочтительно, чтобы другими остатками Fc-домена были остатки IgG человека дикого типа. Известна некоторая вариация в Fc IgG1 человека, и Fc-участок может содержать любой IgG1 человека с YTE и/или тройной мутацией.
Предпочтительно полипептид CTLA-4 конъюгирован с аминокислотной последовательностью Fc IgG1 SEQ ID NO: 59. Она включает шарнирную область Fc IgG1 человека, не содержит мутацию с заменой C на S абатацепта, содержит тройную мутацию для снижения эффекторной функции и включает YTE для увеличения периода полужизни.
Улучшенные Fc-участки, описанные в данном документе, можно применять в связи с CTLA-4 дикого типа, однако, они дают еще большие благоприятные эффекты при конъюгации с полипептидом CTLA-4 в соответствии с настоящим изобретением. Полипептид CTLA-4 может быть конъюгирован по своему C-концу с N-концом Fc-участка, необязательно с помощью одной или нескольких связывающих аминокислот или линкерного пептида. Предпочтительно конъюгат является белком слияния CTLA-4 - Fc.
Например, полипептид CTLA-4, содержащий аминокислотную последовательность SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42 или SEQ ID NO: 47, может быть конъюгирован с аминокислотной последовательностью Fc IgG SEQ ID NO: 59 или с аминокислотной последовательностью Fc IgG SEQ ID NO: 60.
Белок слияния CTLA-4 - Fc IgG в соответствии с настоящим изобретением может содержать SEQ ID NO: 13, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 14, SEQ ID NO: 15 или SEQ ID NO: 16.
Полипептид CTLA-4 - Fc IgG 1299, кодируемый нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948, является вариантом осуществления настоящего изобретения. Полипептид CTLA-4 1299, кодируемый нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948, может, по желанию, альтернативно быть конъюгирован с другим Fc-участком.
Продукты полипептида CTLA-4
Полипептиды CTLA-4, включая CTLA-4 - Fc, могут быть мономерными или мультимерными, например, димерными, тримерными, тетрамерными или пентамерными. Как описано в других частях данного документа, CTLA-4 могут образовывать димеры. Эта естественная димеризация может активироваться конъюгацией CTLA-4 с Fc-доменом или другим димеризирующим доменом.
Полипептидные мультимеры, содержащие множество полипетидов CTLA-4, являются аспектом настоящего изобретения. Множество полипептидов CTLA-4 в мультимере могут быть идентичными или отличаться друг от друга. Мультимер может содержать некоторые идентичные полипептиды и/или некоторые различающиеся полипептиды. Мультимер может содержать один или несколько полипептидов CTLA-4 в соответствии с настоящим изобретением и один или несколько других полипептидов. Один или несколько других полипептидов могут включать, например, CTLA-4 дикого типа и/или полипептид, который не является полипептидом CTLA-4.
Мультимер может являться димером, содержащим два полипептида CTLA-4 в соответствии с настоящим изобретением, которые могут быть идентичными (гомодимер) или различными (гетеродимер).
Мультимер может являться тетрамером, содержащим четыре полипептида CTLA-4 в соответствии с настоящим изобретением, все из которых могут быть идентичными (гомотетрамер), или могут включать один или несколько различающихся полипептидов CTLA-4 в соответствии с настоящим изобретением (гетеротетрамер). Мультимер может являться тетрамером, содержащим два полипептида CTLA-4 в соответствии с настоящим изобретением (идентичные или отличающиеся друг от друга) и два других полипептида CTLA-4, таких как CTLA-4 дикого типа.
Если CTLA4 находится в мультимерной форме, полипептид CTLA-4 необязательно конъюгирован с Fc-участком иммуноглобулина и/или молекулой антитела. Конъюгат может включать или может не включать антиген-связывающий сайт антитела, VH-домен или VL-домен.
Одним аспектом настоящего изобретения является конъюгат, содержащий один или несколько, например, два, три, четыре или пять полипептидов CTLA-4 и молекулу антитела или домен антитела, предпочтительно, человека. Димеризованные домены CTLA-4 могут быть конъюгированы с парами тяжелых-легких цепей антитела. Молекула антитела может содержать две пары тяжелых-легких цепей антитела, каждая тяжелая цепь содержит VH-домен и один или несколько константных доменов тяжелой цепи (например, CH1, CH2 и CH3), и каждая легкая цепь содержит VL-домен и константный участок легкой цепи, где две пары тяжелой-легкой цепи связаны посредством димеризации константных доменов тяжелой цепи, и где четыре полипептида CTLA-4 конъюгированы с молекулой антитела, при этом один CTLA-4 соединен с каждым из четырех вариабельных доменов. Константный участок легкой цепи может быть лямбда- или каппа-легкой цепью. Пара молекул CTLA-4 может соединяться с каждой парой доменов VH-VL, где полипептид CTLA-4, присоединенный к VH-домену, образует димер с полипептидом CTLA-4, присоединенным к VL-домену. Предпочтительно, С-конец CTLA-4 слит с N-концом VH- или VL-домена. Предпочтительно, чтобы образование пары VH и VL не приводило к связыванию с известными антигенами человека.
Необязательно удаляют некоторые или все из VH- и/или VL-доменов антител для того, чтобы включить полипептид CTLA-4 вместо VH- и/или VL-домена или вместо его части. Димер может, соответственно, содержать пару полипептидов CTLA-4, один, слитый с константной областью легкой цепи антитела, и один, слитый с константной областью тяжелой цепи антитела. Тетрамер может, соответственно, содержать две пары полипептидов CTLA-4, при этом каждая пара включает полипептид CTLA-4, слитый с константной областью легкой цепи антитела, и полипептид CTLA-4, слитый с константной областью тяжелой цепи антитела. Как отмечалось ранее, константный участок тяжелой цепи содержит один или несколько константных доменов тяжелой цепи, например, CH1, CH2 и CH3, и константный участок легкой цепи может быть лямбда или каппа.
Настоящее изобретение также включает пентамеры CTLA4. Для образования пентамера могут объединяться пять полипетидов CTLA4, необязательно посредством пентамеризации присоединенных Fc-участков антител. Образование пентамера облегчается с помощью Fc-участка IgM, который обычно является пентамерным. Таким образом, пять полипептидов CTLA4-Fc, включая Fc-участок IgM, предпочтительно IgM человека, могут объединяться в виде пентамера. Описан пентамерный CTLA4 (Yamada et al. Microbiol. Immunol. 40(7):513-518 1996).
Полипептиды в мультимере могут быть связаны ковалентно, например, с помощью дисульфидных связей. Ковалентные связи могут присутствовать между полипептидом CTLA4 и/или между любым Fc-участком, связанным с полипептидом CTLA-4. Если применяются Fc-участки и/или другие домены антитела, полипептиды могут быть связаны таким же образом, как происходит в природных условиях для таких Fc-доменов и/или других доменов антитела. Образование дисульфидных связей между цистеиновыми остатками полипептидов CTLA-4 описано в других частях данного документа.
Такие мультимеры и конъюгаты можно применять в любом способе или для любого применения, описанного в данном документе для полипептидов CTLA-4. Мультимерная структура может способствовать биологической активности CTLA-4, например, ингибированию активации T-клеток. Показано, что ингибирование CTLA-4 дикого типа усиливается в тетрамерной форме (пример 11, фигура 7).
Полипептид CTLA-4 может быть меченым или немеченым. Метку можно добавлять к последовательности CTLA-4 или Fc-участку, конъюгированному с ней.
CTLA-4 и/или Fc-участок может быть гликозилированным или негликозилированным. Предпочтительно, CTLA-4 и/или Fc характеризуются обычным гликозилированием, свойственным таковым человека.
Полипептиды CTLA-4, описанные в данном документе, можно дополнительно модифицировать или усовершенствовать для получения улучшенных или измененных дополнительных вариантов. Например, аминокислотную последовательность полипептида CTLA-4 в соответствии с изобретением, описанным в данном документе, можно модифицировать введением одной или нескольких мутаций, например, замен, для получения дополнительного полипептида CTLA-4, который можно исследовать в отношении эффективности, аффинности (к CD80 и/или CD86) и/или стабильности, например, как описано в других частях данного документа.
Полипептиды CTLA-4 предпочтительно сохраняют одно или несколько желаемых функциональных свойств, описанных в данном документе. Такие свойства включают способность связываться с CD80 и/или CD86, способность связываться с CD80 и/или CD86 с аффинностью, большей, чем таковая CTLA-4 дикого типа, и/или эффективность, аффинность и/или стабильность, описанные в данном документе для полипептидов CTLA-4 по настоящему изобретению, например, Kd связывания с CD80 человека 50 нМ или менее, как определено с помощью поверхностного плазмонного резонанса. Описанный в данном документе полипептид CTLA-4 в соответствии с настоящим изобретением, как правило, имеет большую аффинность связывания с CD80 человека, большую эффективность и/или большую стабильность по сравнению с CTLA-4 дикого типа с SEQ ID NO: 35.
Полипептид CTLA-4 может содержать или состоять из аминокислотной последовательности, имеющей по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% с любой из SEQ ID NO: 36-55, например, с SEQ ID NO: 43, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 36, SEQ ID NO: 42 или SEQ ID NO: 47. Полипептид CTLA-4 может содержать или состоять из аминокислотной последовательности, имеющей, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% с SEQ ID NO: 68. Полипептид CTLA-4 может содержать аминокислотную последовательность или состоять из аминокислотной последовательности, имеющей по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% с аминокислотной последовательностью CTLA-4, кодируемой нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948.
Полипептид CTLA-4 может содержать любую из или состоять из любой из SEQ ID NO: 36-55, SEQ ID NO: 68, или аминокислотной последовательности CTLA-4, кодируемой нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948, с одной или несколькими аминокислотными мутациями. Например, он может содержать до двенадцати мутаций, например, до десяти мутаций аминокислот, например, до пяти мутаций, например, одну, две или три мутации аминокислот. Примеры мутаций описаны в других частях данного документа.
После введения одной или нескольких мутаций полипептид CTLA-4 можно исследовать в отношении желаемых функциональных свойств, таких как способность связываться с CD80 и/или CD86, способность связываться с CD80 и/или CD86 с аффинностью, большей, чем CTLA-4 дикого типа, и/или эффективность, аффинность и/или стабильность, описанные в данном документе для полипептидов CTLA-4 настоящего изобретения, например, Kd связывания с CD80 50 нМ или менее, как определено с помощью поверхностного плазмонного резонанса.
Одним аспектом настоящего изобретения является способ, включающий
получение полипептида CTLA-4, содержащего или состоящего из аминокислотной последовательности полипептида CTLA-4, описанной в данном документе;
введение одной или нескольких мутаций в аминокислотную последовательность для получения дополнительного полипептида CTLA-4 и
исследование стабильности, аффинности и/или эффективности дополнительного полипептида CTLA-4.
Аминокислотная последовательность полипептида CTLA-4 может содержать любую из или состоять, например, из любой из SEQ ID NO 36-55 или SEQ ID NO: 68, или аминокислотной последовательности CTLA-4, кодируемой нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948. Например, аминокислотной последовательностью может быть SEQ ID NO: 43, 37, 36, 38, 42 или 47.
Можно необязательно вводить от одной до двадцати мутаций включительно, и они могут включать замены, делеции, вставки или смесь любых из них. Например, можно ввести одну либо несколько замен, например, от одной до двадцати замен включительно.
Примеры анализов для исследования стабильности, аффинности и/или эффективности дополнительного полипептида CTLA-4 описаны в данном документе. Дополнительный полипептид может иметь стабильность, аффинность и/или эффективность, которые не являются значительно меньшими или которые превышают таковые полипептида CTLA-4, из которого он был получен.
Способ может включать определение того, что дополнительный полипептид CTLA-4 имеет эффективность, аффинность и/или стабильность, описанные в данном документе для полипептидов CTLA-4 по настоящему изобретению, например, что он имеет Kd связывания с CD80 человека 50 нМ или менее, как определено с помощью поверхностного плазмонного резонанса.
Дополнительный полипептид CTLA-4, определяемый как имеющий эффективность, аффинность и/или стабильность, описанные в данном документе для полипептидов CTLA-4 по настоящему изобретению, может тогда быть составлен с получением фармацевтической композиции или применяться в способах, включая терапевтические способы, описанные в данном документе.
Способ может включать составление дополнительного полипептида CTLA-4 с получением композиции, содержащей один или несколько фармацевтических наполнителей. Такие композиции, их применение и составление описаны более подробно в других частях данного документа. Полипептид CTLA-4 может быть получен в любом формате, описанном в данном документе, например, он может быть конъюгирован, как описано, с Fc-участком.
Можно получить молекулу нуклеиновой кислоты, кодирующую полипептид CTLA-4, например, конструкт CTLA-4 - Fc. Например, молекула нуклеиновой кислоты может кодировать любую аминокислотную последовательность полипептида CTLA-4 или аминокислотную последовательность CTLA-4 - Fc в соответствии с настоящим изобретением. Нуклеиновая кислота может содержать последовательность нуклеиновой кислоты, депонированную под номером доступа в NCIMB 41948, кодирующую полипептид CTLA-4-Ig 1299 или кодирующую по меньшей мере участок этого полипептида CTLA-4. Молекула нуклеиновой кислоты может быть выделенной или может содержаться в векторе, например, рекомбинантном векторе для экспрессии нуклеиновой кислоты в клетке. Клетка in vitro может содержать вектор и может применяться для экспрессии полипептида CTLA-4 или продукта CTLA-4 Fc. Полипептид может экспрессироваться клеточной линией E. coli, депонированной под номером доступа в NCIMB 41948.
Полипептид CTLA-4, описанный в данном документе, можно получать способом, включающим экспрессию полипептида из кодирующей нуклеиновой кислоты. Этого можно беспрепятственно достигнуть, выращивая клетку-хозяина в среде, содержащей такой вектор, в подходящих условиях, которые вызывают экспрессию или обеспечивают возможность экспрессии полипептида CTLA-4. Полипептиды CTLA-4 также могут экспрессироваться в in vitro системах, таких как лизат ретикулоцитов. После получения полипептида CTLA-4 в результате экспрессии можно по стандартной методике исследовать его активность, например, его способность связываться с CD86 или CD80.
Системы клонирования и экспрессии полипептида во множестве различных клеток-хозяев хорошо известны и могут применяться для экспрессии полипептидов CTLA-4, описанных в данном документе, включая полипептиды CTLA-4 - Fc. Пригодные клетки-хозяева включают бактерий, клетки эукариот, такие как клетки млекопитающих и дрожжей, и бакуловирусные системы. Клеточные линии млекопитающих, доступные в данной области для экспрессии гетерологичного пептида, включают клетки яичника китайского хомяка, клетки HeLa, клетки почки новорожденного хомяка, клетки COS и многие другие. Распространенным предпочтительным бактериальным хозяином является E. coli. Можно выбрать или сконструировать пригодные векторы, содержащие соответствующие регуляторные последовательности, включая промоторные последовательности, терминаторные фрагменты, последовательности полиаденилирования, энхансерные последовательности, маркерные гены и, по необходимости, другие последовательности. Векторами могут быть плазмиды, вирус, например, бактериофаг, или, по необходимости, фагмида. Известно много методик и протоколов для работы с нуклеиновой кислотой, например, при приготовлении конструктов нуклеиновых кислот, мутагенезе, секвенировании, введении ДНК в клетки и экспрессии генов и анализе белков.
Как правило, нуклеиновую кислоту, кодирующую полипептид CTLA-4 в соответствии с настоящим изобретением, получают в виде изолята, в выделенной и/или очищенной форме или без примесей или практически не содержащей примеси. Нуклеиновая кислота может быть полностью или частично синтетической и может включать геномную ДНК, кДНК или РНК.
Нуклеиновая кислота может быть получена как часть реплицируемого вектора, и также настоящим изобретением предлагаются вектор, включающий нуклеиновую кислоту, кодирующую полипептид CTLA-4 по настоящему изобретению, в частности, любой вектор экспрессии, из которого при соответствующих условиях может экспрессироваться кодируемый полипептид, и клетка-хозяин, содержащая любой такой вектор или нуклеиновую кислоту. Вектором экспрессии в данном контексте является молекула нуклеиновой кислоты, включая нуклеиновую кислоту, кодирующую полипептид, представляющий интерес, и соответствующие регуляторные последовательности для экспрессии полипептида, в системе экспрессии in vitro, например, лизате ретикулоцитов, или in vivo, например, в эукариотических клетках, таких как клетки COS или CHO, или в прокариотических клетках, таких как E. coli.
Клетка-хозяин может содержать нуклеиновую кислоту, раскрытую в данном документе. Нуклеиновая кислота по настоящему изобретению может быть интегрирована в геном (например, хромосому) клетки-хозяина. Интеграцию можно стимулировать с помощью включения последовательностей, которые стимулируют рекомбинацию с геномом, в соответствии со стандартными методиками. В клетке нуклеиновая кислота может находиться во внехромосомном векторе.
Нуклеиновая кислота может быть введена в клетку-хозяина. При введении, которое может (в частности, для введения in vitro) быть, как правило, названо, без ограничения, “трансформацией” или “трансфекцией”, можно применять любую доступную методику. Для эукариотических клеток пригодные методики могут включать трансфекцию с использованием фосфата кальция, DEAE-Dextran, электропорацию, трансфекцию, опосредованную липосомами, и трансдукцию с помощью ретровируса или другого вируса, например вакцинии, или для клеток насекомых - бакуловируса. Для бактериальных клеток подходящие методики могут включать трансформацию с хлористым кальцием, электропорацию и трансфекцию с применением бактериофага.
При выявлении клонов, содержащих изучаемую нуклеиновую кислоту, представляющую интерес, можно применять маркерные гены, такие как гены устойчивости или чувствительности к антибиотикам, как хорошо известно в данной области.
Введение может впоследствии обуславливать или обеспечивать возможность экспрессии из нуклеиновой кислоты, например, с помощью культивирования клеток-хозяев (которые могут включать клетки, фактически трансформированные, хотя более вероятно, клетки будут потомками трансформированных клеток) при условиях, пригодных для экспрессии гена, для продуцирования кодируемого белка. Если полипептид экспрессируется в паре с соответствующим сигнальным лидерным пептидом, он может секретироваться из клетки в среду для культивирования. После продуцирования в результате экспрессии полипептид можно выделять и/или очищать от клетки-хозяина и/или среды для культивирования, в зависимости от ситуации, и в последующем применять по желанию, например, при составлении композиции, которая может включать один или несколько дополнительных компонентов, таких так фармацевтическая композиция, которая включает один или несколько фармацевтически приемлемых наполнителей, сред или носителей (например, см. далее).
Полипептид CTLA-4 в соответствии с настоящим изобретением может быть выделенным и/или очищенным (например, с помощью антитела), например, после получения в результате экспрессии из кодирующей нуклеиновой кислоты. Таким образом, полипептид CTLA-4 может быть получен без примесей или практически без примесей. Полипептид CTLA-4 может быть получен без других полипептидов или практически не содержащим других полипептидов. Выделенный и/или очищенный полипептид CTLA-4 может применяться при составлении композиции, которая может включать по меньшей мере один дополнительный компонент, например, фармацевтическую композицию, включающую фармацевтически приемлемый наполнитель, среду или носитель. Композицию, включающую полипептид CTLA-4 в соответствии с настоящим изобретением, можно применять при профилактическом и/или терапевтическом лечении, как рассматривается в других частях данного документа.
Соответственно, одним аспектом настоящего изобретения является композиция, содержащая или состоящая из полипептида CTLA-4 по настоящему изобретению, необязательно, полипептида CTLA-4, конъюгированного с Fc IgG, и одного или нескольких фармацевтических наполнителей. Многочисленные примеры полипептидов CTLA-4 в соответствии с настоящим изобретением описаны в других частях данного документа, и любой может быть конъюгирован с Fc-участком.
Например, композиция может содержать или состоять из
полипептида CTLA-4, содержащего аминокислотную последовательность SEQ ID NO: 43 (вариант 1299), SEQ ID NO: 37 (вариант 1322), SEQ ID NO: 38 (вариант 1321), SEQ ID NO: 36 (вариант 1315), SEQ ID NO: 42 (вариант 1115) или SEQ ID NO: 47 (варианта 1227), конъюгированного с аминокислотной последовательностью Fc IgG SEQ ID NO: 59; и
одного или нескольких фармацевтических наполнителей.
Композиция может содержать или состоять из полипептида CTLA-4-Ig 1299, кодируемого нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948, и одного или нескольких фармацевтических наполнителей.
Например, полипептид CTLA-4 может содержать аминокислотную последовательность SEQ ID NO: 13, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 14, SEQ ID NO: 15 или SEQ ID NO: 16.
Композиция в соответствии с настоящим изобретением может содержать полипептид CTLA-4 в концентрации по меньшей мере 70 мг/мл, например, по меньшей мере 80 мг/мл, по меньшей мере 90 мг/мл или по меньшей мере 100 мг/мл. Концентрацию рассчитывают как массу полипептида, включая гликозилирование, и включает, при наличии, Fc-участок. Концентрацию полипептида можно определять с помощью стандартных способов спектрометрического измерения, применяя коэффициент экстинкции на основе рассчитанной массы полипептида, включая гликозилирование (при наличии). Если присутствует гликозилирование, можно предположить, что оно является полным. Пригодные способы проиллюстрированы в примерах. Например, коэффициент экстинкции 1,09 может применяться для определения концентрации, как показано в качестве примера для CTLA-4-Fc 1299.
Составление и медицинское применение
Полипептиды CTLA-4 по настоящему изобретению можно вводить посредством ежемесячного или менее частого введения. Низкая частота введения, как правило, желательна для снижения нагрузки на пациентов и на врачей, однако, может быть связана с риском пониженной терапевтической эффективности и/или необходимостью в повышенной дозе препарата. Улучшение эффективности, аффинности и/или периода полужизни в соответствии с настоящим изобретением снижает такие риски и обеспечивает возможность введения меньших доз или менее частого дозирования по сравнению с предыдущими схемами введения.
Для многих пациентов лечение будет необходимо в течение продолжительных периодов времени, например, в течение многих лет и возможно в течение всей жизни пациента. Таким образом, предусмотрено, что будут вводиться многократные дозы. Интервалы между дозами могут составлять порядка дней, недели или месяца. Предпочтительно введение осуществляют с интервалами по меньшей мере или приблизительно 14, 21 или 28 дней. Предпочтительно введение пациенту осуществляют посредством подкожного введения с интервалами дозирования 28 дней или больше, например, ежемесячного дозирования.
Введение может быть внутривенным или посредством любого другого пригодного пути введения. Например, полипептид CTLA-4 можно вводить посредством подкожной инъекции, что облегчает самостоятельное введение пациентами в домашних условиях и обеспечивает возможное преимущество снижения числа визитов пациента в клинику по сравнению со схемами внутривенного введения.
Для составления CTLA-4 при уменьшенных объемах, пригодных для подкожного введения, как правило, требуется более высокая концентрация препарата CTLA-4 по сравнению с составом для внутривенного введения. Для подкожного введения, как правило, предпочтительны концентрации по меньшей мере 70 мг/мл, более предпочтительно по меньшей мере 100 мг/мл. Повышенная стабильность композиций CTLA-4 в соответствии с настоящим изобретением облегчает составление при высоких концентрациях, например, для подкожного введения.
Фармацевтические композиции в соответствии с настоящим изобретением и для применения в соответствии с настоящим изобретением могут включать, в дополнение к активному ингредиенту, фармацевтически приемлемый наполнитель, носитель, буфер, стабилизатор или другие вещества, хорошо известные специалистам в данной области. Такие вещества должны быть нетоксичными и не должны оказывать противодействие эффективности активного ингредиента. Точная природа носителя или другого вещества будет зависеть от пути введения, которым может быть любой пригодный путь, однако, наиболее вероятно, инъекция (с иглой или без иглы), в частности, подкожная инъекция. Другие предпочтительные способы введения включают введение с помощью ингаляции или интраназальное введение.
Для внутривенной, подкожной или внутримышечной инъекции активный ингредиент будет находиться в форме приемлемого для парентерального введения водного раствора, который не содержит пирогены и имеет подходящий pH, изотоничность и стабильность. Специалисты в данной области могут получать пригодные растворы, используя, например, изотонические среды, такие как физиологический раствор для инъекций, раствор Рингера для инъекций или лактатный раствор Рингера для инъекций. Консерванты, стабилизаторы, буферы, антиоксиданты и/или другие добавки могут быть включены при необходимости.
Полипептид CTLA-4 в соответствии с настоящим изобретением можно применять в способе диагностики или лечения организма человека или животного, предпочтительно человека.
Способы лечения могут включать введение полипептида CTLA-4 в соответствии с настоящим изобретением, например, введение фармацевтической композиции, содержащей полипептид CTLA-4. Полипептид CTLA-4 или композиция, содержащая полипептид CTLA-4, как описано в данном документе, могут быть предназначены для применения в способе лечения пациента путем подкожного или внутривенного введения.
Полипептид CTLA-4 можно вводить индивиду предпочтительно путем введения в “эффективном для профилактики количестве” или “эффективном для терапии количестве" (в зависимости от ситуации, хотя профилактика может считаться терапией), при этом количество должно быть достаточным для оказания благоприятных эффектов для пациента. Реально вводимое количество и скорость и динамика введения будут зависеть от природы и тяжести состояния, лечение которого осуществляют. Назначение лечения, например, решения о дозах и т.д., находится в пределах компетенции врачей общей практики и других врачей.
Композицию можно вводить саму по себе или в комбинации с другими средствами для лечения либо одновременно, либо последовательно в зависимости от состояния, подлежащего лечению.
Полипептиды CTLA-4 пригодны для ослабления T-клеточного ответа, и в связи с этим их можно применять для лечения состояний, при которых ослабление ответа Т-клеток является целесообразным. Показания к применению, при которых полипептид CTLA-4 можно применять для получения благоприятных эффектов лечения, включают аутоиммунные заболевания и/или воспалительные заболевания. Примерами показаний к применению являются ревматоидный артрит (RA), ювенильный артрит, псориатический артрит, псориаз, рассеянный склероз, астма, болезнь Крона, люпус-нефрит, системная красная волчанка, анкилозирующий спондилит, отторжение трансплантата, сахарный диабет I типа, синдром Шегрена и язвенный колит, а также другие аутоиммунные состояния, такие как алопеция. Полипептиды CTLA-4 в соответствии с настоящим изобретением считаются особенно пригодными для пациентов с RA от средней до тяжелой степени тяжести.
Пациентами, получающими лечение полипептидами CTLA-4 или фармацевтическими композициями в соответствии с настоящим изобретением, могут быть пациенты с активным RA от средней до тяжелой степени тяжести, несмотря на предшествующее или текущее лечение синтетическими модифицирующими заболевание противоревматическими лекарственными средствами (DMARD) или биопрепаратами, кроме CTLA-4, например, кроме абатацепта. Полипептид CTLA-4 в соответствии с настоящим изобретением можно применять для лечения пациентов посредством монотерапии, в комбинации с традиционными DMARD у пациентов с недостаточным ответом на традиционные DMARD или у пациентов с отсутствием ответа на биопрепараты.
Можно отслеживать эффективность лечения и можно получать данные по прогрессированию повреждения суставов и/или функционального статуса пациента.
Примеры
Следующая последовательность CTLA4-Ig была внесена в NCIMB:
Escherichia coli DH5a вариант 1299 = NCIMB 41948
Дата регистрации = 13 марта 2012 г.
Стратегия, применяемая для оптимизации биологической эффективности молекулы слияния CTLA-4 Fc состояла из двух основных видов активности. Одна активность заключалась в применении рибосомного дисплея для осуществления направленного развития домена CTLA-4 для выбора улучшенной аффинности к лигандам CD80 и CD86, а также улучшенной стабильности этого домена. Продукты селекции рибосомного дисплея, состоящие из различных популяций вариантов CTLA-4, секвенировали, и продукты, кодирующие уникальные последовательности, экспрессировали со слитным партнером Fc для исследования непосредственно в анализе стимуляции Т-клеток in vitro. Преимуществом этого подхода было расположение множества разных вариантов CTLA-4 (было исследовано >1000) в формате, подобном лекарственному препарату, т.е. в отношении Fc-домена, который способствует димеризации, в биологически релевантном анализе. Дополнительной чертой этой стратегии было выполнение рекомбинаций тех мутаций CTLA-4, которые были связаны с улучшенной биологической функцией, для достижения дальнейших прибавок эффективности вследствие синергии.
В этом подходе было возможно одновременно проводить отбор на повышенную аффинность вариантов CTLA-4 и на стабильность белка. При отборе аффинности применяется снижение концентраций целевого лиганда, в данном случае CD80/86, для избирательного обогащения вариантов CTLA-4 с более высокой аффинностью. При отборе улучшенной стабильности применяется дестабилизирующее средство, такое как DTT, или бусины гидрофобной хроматографии (HIC) для удаления из селекционного пула тех вариантов, которые менее стабильны и более подвержены развертыванию. Таким образом, давление стабильности и аффинности могло бы применяться при одном отборе, а не при выполнении параллельных подходов.
Вторая активность заключалась в рациональной разработке инженерным путем Fc-домена с целью введения известных мутаций для устранения опосредованных Fc эффекторных функций, и для повышения периода полужизни молекулы в кровотоке in vivo. Различные участки варианта Fc готовили в виде слияний с CTLA-4 и изучали их в ускоренных исследованиях стабильности in vitro для отбора Fc-участка с оптимальным профилем стабильности.
После изучения этих двух параллельных видов активности и последующего скрининга самые эффективные домены CTLA-4, как было определено по ингибированию в многочисленных анализах стимуляции Т-клеток in vitro, объединяли с самым стабильным разработанным инженерным путем Fc-доменом, как было определено с помощью ускоренных исследований стабильности in vitro. Дальнейшее изучение биологической эффективности и стабильности белка in vitro способствовало относительному расположению молекул в конечном формате лекарственного препарата.
Пример 1. Создание библиотеки вариантов CTLA-4 и отбор рибосомного дисплея в отношении улучшенной эффективности и стабильности
Рибосомный дисплей выполняли на мономерном домене CTLA-4 человека, соответствующем входу P16410 системы Swiss-Prot, остаткам 38-161 внеклеточного домена, без прилагаемого Fc-участка. Эту последовательность (SEQ ID NO: 35) также обозначают как CTLA-4 дикого типа. Конструкт рибосомного дисплея CTLA-4 получали с помощью клонирования необходимого участка кДНК CTLA-4 человека в вектор, содержащий 5’ и 3’ регуляторные элементы, которые необходимы для рибосомного дисплея (Hanes et al, Meth. Enzymol. (2000) 328:404). Этот конструкт содержит последовательность промотора РНК-полимеразы T7 с последующим сайтом связывания прокариотической рибосомы (последовательность Shine-Dalgarno) в обратном направлении от кодирующей последовательности CTLA-4. Цистеин в аминокислоте 120 (или положении 157 в соответствии с нумерацией во входе P16410 системы Swiss-Prot) на границе димеризации CTLA-4 человека был мутирован в серин с целью предупреждения димеризации молекул CTLA-4 в формате рибосомного дисплея, который в противном случае мог помешать отбору улучшенных последовательностей CTLA-4. По направлению последовательности CTLA-4 был включен участок белка гена III нитевидного фага для выполнения роли спейсера для обеспечения дисплея вариантов CTLA4 рибосомного туннеля. Конструкт рибосомного дисплея CTLA-4 также содержал 5’ и 3’ последовательности "петля на стебле" на уровне мРНК для обеспечения стабилизации библиотек мРНК против разрушения нуклеазой.
Библиотеки сниженной точности
Конструкт рибосомного дисплея CTLA-4 человека, описанный выше, применяли в качестве матрицы, на которой создавали библиотеку случайных вариантов с помощью ПЦР сниженной точности. ПЦР сниженной точности применяли в отношении гена CTLA-4 с помощью набора Diversify PCR Random Mutagenesis Kit (Clontech) в соответствии с указаниями производителя. Реакции направляли на получение в среднем четырех мутаций аминокислот на молекулу и библиотеки из приблизительно 2,5×1010 молекул варианта. Эту процедуру случайного мутагенеза в дальнейшем внедряли в процесс отбора, в котором ее применяли в отношении продукта третьего цикла отбора для введения большего разнообразия в обогащенную популяцию связывающихся элементов перед дальнейшим отбором.
Библиотека, направленная на ‘петлю 4’
Конструкт рибосомного дисплея CTLA-4 человека также применяли в качестве матрицы, на которой создавали библиотеку вариантов с мутагенезом, направленным на участок молекулы CTLA-4 с потенциалом содействия взаимодействию с CD80 и CD86. Сокристаллическую структуру CTLA-4 человека:комплекса CD80 человека (Protein Data Bank (PDB): 1I8L) и CTLA-4 человека:комплекса CD86 человека (PDB: 1I85) изучали с целью визуализации связывающего взаимодействия между молекулами, в частности, боковыми цепями аминокислот CTLA-4 в непосредственной близости к лигандам. Было обнаружено, что участок белка CTLA-4 человека (SEQ ID 35), содержащий аминокислоты в положениях от 59 до 65 (или в положениях от 96 до 102 в соответствии с нумерацией системы SwissProt входа P16410 CTLA-4) образовывал петлю, расширяющуюся в направлении CD80 и CD86. Каждый из остатков в этом участке полностью рандомизировали с помощью насыщающего (NNS) мутагенеза для создания библиотеки из приблизительно 3,4×1010 молекул варианта. Данную библиотеку ‘петли 4’ создавали с помощью стандартных методик с применением накладывающихся олигонуклеотидов (SEQ ID NO: 33 и SEQ ID NO: 34).
Отбор в отношении улучшенной аффинности и стабильности
Отбор в отношении улучшенного связывания вариантов CTLA-4 человека с CD80 и CD86 проводили с помощью аффинности рибосомного дисплея, основанной на видах отбора, описанных в Hanes et al (Meth. Enzymol. (2000) 328:404). Вкратце, библиотеки ДНК варианта CTLA-4 транскрибировали и затем транслировали в бесклеточной прокариотической системе трансляции, и реакции трансляции останавливали для создания тройных комплексов для отбора рибосомного дисплея (мРНК-рибосома-белок), которые затем инкубировали с белками слияния CD80 Fc человека или CD86 Fc человека (R&D Systems). Комплексы, связанные с CD80 или CD86, захватывали с помощью инкубации с магнитными шариками, покрытыми белком G (Dynal), и связанные третичные комплексы извлекали с помощью магнитного разделения до тех пор, пока несвязанные комплексы не вымывались. мРНК, кодирующую варианты CTLA-4, извлекали с помощью обратной транскрипции и ПЦР. Для направления отбора вариантов CTLA-4 с улучшенным связыванием, процесс отбора повторяли путем снижения концентраций CD80 или CD86 в течение нескольких циклов.
Параллельно с отбором для улучшенной аффинности к CD80 и CD86, пулы варианта CTLA-4 одновременно отбирали с помощью рибосомного дисплея в отношении улучшенной стабильности. В ранних циклах отбора (циклы 1 и 3) применяли DTT для проведения давления отбора, которое благоприятствовало возврату более стабильных вариантов CTLA-4 (Jermutus et al., Proc Natl Acad Sci U S A. 2001 Jan 2;98(1):75-80). Конечную концентрацию DTT, равную 0,5 мМ, включали в реакцию трансляции, после чего реакционную смесь инкубировали с суспензией сефарозных бусин (GE Healthcare) гидрофобной хроматографии (HIC) также в присутствии 0,5 мМ DTT. Этап HIC применяли для захвата вариантов с недостаточным свертыванием и их удаления из реакционной смеси с помощью центрифугирования, перед инкубацией с CD80 и отбором аффинности, как описано ранее.
Библиотека горячих точек мутагенеза и рациональная рекомбинация ключевых мутаций
После исходного скрининга вариантов CTLA-4 из библиотек сниженной точности ПЦР и библиотек, направленных на петлю 4, для создания дополнительных вариантов CTLA-4 выявляли и применяли мутации, связанные с улучшенной активностью. В одной стратегии создавали библиотеку горячих точек мутагенеза, в которой положения 16, 25, 58, 70, 85 и 93 SEQ ID NO: 35 (или положения 53, 62, 95, 107, 122 и 130 в соответствии с нумерацией системы SwissProt входа P16410 CTLA-4) полностью рандомизировали в единой библиотеке с помощью насыщающего (NNS) мутагенеза. Библиотеку создавали с помощью накладывающихся и мутагенных олигонуклеотидов (с SEQ ID NO: 61 по SEQ ID NO: 67 включительно). Затем в этой библиотеке проводили отбор в отношении улучшенной аффинности, как описано выше.
В альтернативном подходе меньшее число мутаций, выявленных из библиотек сниженной точности, библиотек, направленных на петлю 4, и библиотек горячих точек мутагенеза, которые были связаны с улучшенной активностью, объединяли с помощью олигонуклеотид-направленного мутагенеза с целью создания рациональных рекомбинантов, которые затем непосредственно изучали в отношении биологической активности. Мутациями, выбранными для этой стратегии, были: I16S, S25N, S25P, G27S, M54K, N56S, L58G, T59S, F60T, L61Q, L61P, D62G, D63Y, S64P, I65N, I65V, S70A, Q80R, M85S и K93Q (или, пронумерованные в соответствии с системой SwissProt входа P16410 CTLA-4: I53S, S62N, S62P, G64S, M91K, N93S, L95G, T96S, F97T, L98Q, L98P, D99G, D100Y, S101P, I102N, I102V, S107A, Q117R, M122S и K130Q).
Пример 2. Экспрессия CTLA-4 дикого типа и вариантов CTLA-4 в качестве белков слияния Fc
Гены варианта CTLA-4 из отбора рибосомного дисплея клонировали в вектор pEU7.1. Этот вектор способствует экспрессии гена CTLA-4 в виде слияния внутри рамки с Fc-участком IgG1 (SEQ ID NO: 56). Продукты рибосомного дисплея амплифицировали с помощью ПЦР и клонировали в pEU7.1 перед трансформацией в клетки DH5-альфа E.coli. Олигонуклеотиды, применяемые для клонирования с помощью ПЦР, также разрабатывали с целью обращения серина в положении 120 (остаток 157 в соответствии с нумерацией во входе P16410 системы Swiss-Prot) назад в аминокислоту дикого типа цистеин. После секвенирования отдельных трансформантов для экспрессии белка всего было отобрано более 1000 вариантов с уникальными аминокислотными последовательностями CTLA-4. В сериях из 88 вариантов кодирующую плазмидную ДНК очищали в соответствии с протоколами поставщика (Qiagen) и количественно определяли с помощью спектрофотометрии при 260 нм с тем, чтобы концентрацию ДНК можно было бы применять для расчета точного количества ДНК для трансфекции.
Экспрессия, очистка и количественное определение белков CTLA-4 из 24-луночных планшетов
3 мл клеток (ECACC) яичников китайского хомяка (CHO) засевали при концентрации 1 миллион клеток на мл в отдельные лунки в 24-луночный планшет (Whatman 734-2558) в среде CD-CHO (Invitrogen 10743-029), содержащей 25 мкМ L-метионина сульфоксимина (Sigma M5379). 24-луночные планшеты, содержащие клетки, запечатывали воздухопроницаемой трехслойной крышкой (Applikon biotechnology, Z365001224) и помещали в зажим для планшетов с глубокими лунками (Applikon biotechnology, Z365001700). Клетки встряхивали при 250 об/мин, влажности 80%, 5% CO2 и температуре 37°C. Для трансфекции 50 мкл NaCl 150 мМ, содержащие 3 мкг плазмидной ДНК, смешивали с 50 мкл, содержащими 21 мкг 25 кДА линейного PEI (Polysciences, 23966). Образованный комплекс DNA-PEI добавляли к клеткам, с учетом не более чем 15 минут между началом образования комплекса и добавлением к клеткам. Через 16-24 ч после трансфекции клеткам подавали питание, добавляя 300 мкл/лунку среды CD-CHO Efficient Feed B (Invitrogen A10240). Планшеты встряхивали при 250 об/мин, влажности 80%, 5% CO2 и температуре 37°C в течение дополнительных 5-6 дней для обеспечения экспрессии белка в среде для роста. После экспрессии отработанную культуральную среду, содержащую белок, очищали с помощью центрифугирования при 3000 об/мин в течение 10 мин. Очищенные супернатанты (1,2 мл) перераспределяли в 96-луночный фильтровальный планшет (3M Empore, 12146036) с помощью роботизированной раскапывающей станции Freedom Evo® (Tecan). Оставшиеся клеточные остатки удаляли фильтрованием с помощью вакуумного насоса и вакуумного коллектора QIAvac 6S (Qiagen). 1,8 мл очищенного отфильтрованного супернатанта обрабатывали для очистки, выполняемой на роботизированной раскапывающей станции (Perkin Elmer) Minitrack (RTM) с помощью аффинных колонок для белка А PhyTip (RTM) (Phynexus, PTP-92-20-01), с объемом 20 μмкл ионообменной смолы). Колонки PhyTip (RTM) увлажняли с помощью 500 мкл NaP 20 мМ pH 7,0. Затем колонки PhyTip (RTM) нагружали прохождением через необработанные супернатанты в сериях 6×300 мкл, отмытые с помощью 200 мкл D-PBS, 200 мкл NaP 20 мМ pH 7,0, элюированные с помощью 120 мкл 100 мМ HEPES 140 мМ NaCl pH 3 и нейтрализованные с помощью 20 мкл 1M HEPES pH 8,0.
Очищенные белки затем переносили в 96-луночный черный полипропиленовый планшет (Greiner, 655209) с последующим добавлением 145 мкл PBS, 0,02% Tween20, 1 мг/мл BSA, 0,05% буфера азида натрия (буфер Octet). Стандартную кривую создавали с помощью предварительно очищенного белка слияния CTLA-4 дикого типа и Fc в идентичном буфере. Ряд концентраций готовили в черном полипропиленовом планшете в объеме 150 мкл с исходной концентрацией 500 мкг/мл и 3-х-кратными разведениями. С помощью Octet RED с биосенсорами, покрытыми белком А (ForteBio Inc, 18-0004), выполняли количественное определение со временем считывания 120 секунд при скорости потока 200 об/мин. Для каждого 96-луночного планшета образцов применяли одну колонку из 8 биосенсоров. Биосенсоры восстанавливали добавлением 200 мкл 10 мМ глицина pH 1,7 (Sigma, G-7403) в 96-луночный планшет. Биосенсоры нейтрализовали перед обработкой следующих образцов добавлением 200 мкл буфера Octet. Выполняли 3 цикла восстановления/нейтрализации со временем 30 с и скоростью потока 200 об/мин. Концентрации неизвестных образцов определяли путем сравнения скорости связывания между неизвестными образцами и стандартной кривой с помощью пакета компьютерной программы по анализу данных Octet RED.
Экспрессия, очистка и количественное определение белков CTLA-4 в более крупных масштабах
Для получения отдельных белков CTLA-4 в виде слияний с Fc осуществляли те же самые общие этапы, которые применяли для способа с 24-луночным планшетом. Плазмиды, содержащие ген варианта CTLA-4 в виде слияния внутри рамки с Fc IgG1 готовили из клеток E.coli. Для приготовления белков в количестве >100 мг, весь конструкт, содержащий ген CTLA-4 непосредственно внутри рамки с геном Fc IgG1 готовили с помощью синтеза гена. Во всех случаях плазмидную ДНК, кодирующую изучаемый белок, готовили и трансфицировали для экспрессии в клетки CHO. В случае 24-луночных планшетов перед очисткой супернатантов культуры в колбах для культуры тканей или одноразовых биореакторах фирмы WAVE выращивали большие объемы клеток. Выращенные клетки объединяли и фильтровали перед очисткой путем хроматографии с помощью белка А. Супернатанты культуры загружали на колонку соответствующего размера из Ceramic Protein A (BioSepra) и отмывали 50 мМ Tris-HCl pH 8,0, 250 мМ NaCl. Связанный IgG элюировали из колонки с помощью 0,1 M цитрата натрия (pH 3,0) и нейтрализовали добавлением Tris-HCl (pH 9,0). В элюированном веществе осуществляли замену буфера на PBS, применяя колонки Nap10 (GE, 17-0854-02), и концентрацию IgG определяли спектрофотометрическим путем с применением коэффициента экстинкции на основе аминокислотной последовательности белка. Очищенные белки анализировали на предмет агрегации и разложения с помощью эксклюзионной ВЭЖХ (SEC-HPLC) и SDS-PAGE.
Пример 3. Биологическая активность вариантов CTLA-4 в двойном клеточном анализе на клетках Raji (B-клетки) и клетках Jurkat (T-клетки)
Стратегия скрининга, описанная в данном документе, включала измерение биологической активности свыше 1000 вариантов CTLA-4, экспрессирующихся с партнером слияния Fc, в анализе стимуляции Т-клеток in vitro. Варианты CTLA-4 из всех различающихся стратегий мутагенеза (включая ПЦР сниженной точности, направленный мутагенез, рекомбинацию горячих точек и рациональную рекомбинацию) исследовали в отношении биологической активности и располагали в соответствии с их биологической активностью по отношению к CTLA-4 дикого типа (SEQ ID NO: 35), также экспрессирующемся в формате слияния с Fc.
Для определения биологической активности вариантов CTLA-4 в двойном клеточном анализе добавляли образцы, состоящие из клеток Raji (B-клетки) и Jurkat (T-клетки). Взаимодействие CD28, экспрессируемого клетками Jurkat, с лигандами CD80 (B7-1) и CD86 (B7-2), экспрессирующимися на клетках Raji, совместно с сигналом коактивации рецептора Т-клеток (таким как PHA (фитогемагглютинин)) приводит к выделению интерлейкина-2 (IL-2) клетками Jurkat. Растворимый CTLA-4 может связываться с лигандами CD80 и CD86, блокируя их взаимодействие с CD28 и ослабляя этот ответ. Таким образом, эффективность клонов CTLA-4 Ig определяют по ингибированию выделения IL-2 T-клетками, определяемому в анализе с помощью IL-2 HTRF (CisBio 64IL2PEC).
384-луночные планшеты для незначительного связывания белков (Greiner # 781280) применяли для выполнения одиннадцати серийных разведений 1 к 3 исследуемых образцов, которые были приготовлены в полной среде для роста (RPMI 1640 Glutamax, Invitrogen # 61870, 10% FBS, 1% пенициллин/стрептомицин, Invitrogen # 15140). Все разведения образцов выполняли дважды, начиная с высшей концентрации образца 5-30 мкг/мл, действующей на клетки.
Клетки суспензий Raji и Jurkat переносили из колб в пробирки для центрифуги и центрифугировали при 240 g в течение 5 минут. Обе клеточные линии ресуспендировали при концентрации 750000 клеток/мл в среде для роста и клетки каждой линии размещали при концентрации 0,02 мл/лунку (=15000 клеток/клеточную линию/лунку) в 384-луночный планшет Maxisorp (Nunc 464718). Переносили 0,02 мл из планшетов с разведенными образцами в клеточные планшеты и добавляли 0,02 мл 40 мкг/мл PHA (Sigma # L-1668) (или 0,02 мл среды для лунок с отрицательным контролем) во все другие лунки для получения окончательной концентрации 10 мкг/мл, и инкубировали при температуре 37°C с 5% CO2.
Через 20-24 часа собирали супернатанты клеток и измеряли секрецию IL-2 с помощью коммерческого набора IL-2 HTRF (CisBio 64IL2PEC). Вкратце, ‘мастер-микс’ криптата к IL-2 человека (донорный флуорофор) и d2 к IL-2 человека (акцепторный флуорофор) готовили разведением 1/200 в свежеприготовленном конъюгатном буфере (0,2% BSA/0,8M KF/PBS). Стандартную кривую из восьми точек создавали с помощью IL-2 (NIBSC # 96/504), разведенного 1 к 2 в среде с наибольшей концентрацией 2 нг/мл. Равные объемы реагентов мастер-микса и образцов смешивали в 384-луночном планшете для анализа малых объемов (Costar 3676) и инкубировали в течение 3-168 часов при комнатной температуре. Планшеты сканировали на аппарате Envision (Perkin Elmer) при длине волны возбуждающего света 320 нм и длинах волны излучения 620 нм и 665 нм.

Лунки только со средой (минимальное значение/неспецифическое связывание (NSB)) применяли в качестве фоновых, и лунки только с PHA (максимальное значение/общее) применяли для определения максимального сигнала при анализах. Результаты анализировали с помощью компьютерной программы Graphpad Prism (v5.01), и концентрации IC50 определяли с помощью модели нелинейной регрессии подбора кривой (Log [ингибитора] по отношению к ответу при различном угле наклона) с помощью метода подбора наименьших квадратов.
Следующая таблица обобщает число молекул вариантов CTLA-4, упорядоченных по наличию значительного улучшения биологической эффективности по отношению к CTLA-4 дикого типа (SEQ ID NO: 35), также экспрессирующемся в формате слияния с Fc.
После повторного исследования этих 107 вариантов CTLA-4 проводили точные измерения IC50 и рассчитывали кратность улучшения по отношению к CTLA-4 дикого типа (SEQ ID NO: 35) в формате слияния с Fc. Таблица, представленная далее, обобщает эти данные для некоторых наиболее эффективных вариантов CTLA-4 из каждой стратегии мутагенеза.
Jurkat (нМ)
Последовательности этих вариантов CTLA-4 представлены на фигуре 1A.
Профили IC50 6 наиболее эффективных вариантов CTLA-4 и CTLA-4 дикого типа (SEQ ID NO: 35) в формате слияния с Fc в двойном клеточном анализе Raji-Jurkat представлены на фигуре 3A.
Пример 4. Биологическая активность вариантов CTLA-4 в двойном клеточном анализе на клетках Raji (B-клетки) и первичных CD4+ T-клетках человека
Кровь человека собирали в пробирку-сборник CPT Vacutainer (BD Biosciences) и добавляли 400 мкл очищающего реагента CD4+ RosetteSep (Stem Cell Technologies). Через 20 минут после инкубации пробирки центрифугировали при 1700 g в течение 25 минут. Клетки собирали и переносили в 50 мл коническую трубку и осаждали центрифугированием при 350 g в течение 10 минут. Эритроциты лизировали путем ресуспендирования в 20 мл реагента Vitalize и инкубировали от 30 минут до 1 часа. Затем клетки осаждали центрифугированием при 350 g в течение 10 минут и отмывали однократно с среде T-клеток (среда Xvivo-15 (Lonza) с добавлением 1% Anti/Anti (Invitrogen)). Один миллион клеток Raji и первичных CD4+ T-клеток человека на мл суспензии готовили в полной среде Т-клеток и содержали отдельно вплоть до добавления в 96-луночный планшет для анализа. В отдельном 96-луночном планшете (незначительное связывание белков), разведения молекул вариантов CTLA-4 выполняли в полной среде Т-клеток, начиная с исходной концентрации 100 мкг/мл и выполняя двенадцать серийных разведений 1:5. 100 мкл варианта CTLA-4 при каждой концентрации распределяли в культуру ткани при обработке 96-луночного планшета для анализа. Суспензию клеток Raji и CD4+ T-клеток человека смешивали в соотношении 1:1 и добавляли антитело к CD3 (клон UCHT1 (BD Bioscience)) до конечной концентрации 10 мкг/мл. 100 мкл клеточной суспензии распределяли в каждую лунку, содержащую варианты CTLA-4, и инкубировали в течение 18-24 часов. Затем содержимое планшетов собирали центрифугированием при 350 g в течение 5 минут и супернатанты переносили в новый 96-луночный планшет. Секрецию IL-2 измеряли с помощью набора Duoset для определения IL-2 человека в соответствии с протоколом изготовителя (R&D Systems).
Сравнение эффективности по отношению к CTLA-4 дикого типа (SEQ ID NO: 35) в формате слияния с Fc в клеточном анализе на первичных CD4+ T клетках человека для 6 наиболее эффективных вариантов CTLA-4 показано на фигуре 3B.
Пример 5. Биологическая активность вариантов CTLA-4 в смешанной реакции лимфоцитов с применением мононуклеарных клеток периферической крови яванского макака
Кровь яванского макака от двух разных животных собирали в пробирку-сборник CPT Vacutainer (BD Biosciences) и осаждали центрифугированием при 1700 g в течение 25 минут. Клетки собирали и переносили в коническую трубку на 50 мл и осаждали центрифугированием при 350 g в течение 10 минут. Эритроциты лизировали путем ресуспендирования в 20 мл реагента Vitalize и инкубировали от 30 минут до 1 часа. Затем клетки осаждали центрифугированием при 350 g в течение 10 минут и отмывали однократно в среде T-клеток (среда Xvivo-15 (Lonza) с добавлением 1% Anti/Anti (Invitrogen)). В отдельном 96-луночном планшете (незначительное связывание белков), разведения молекул вариантов CTLA-4 выполняли в полной среде Т-клеток, начиная с исходной концентрации 100 мкг/мл и выполняя двенадцать серийных разведений 1:5. 100 мкл разведений CTLA-4 Ig распределяли в культуру ткани при обработке 96-луночного планшета для анализа. Суспензию клеток PBMC от каждого животного смешивали в соотношении 1:1 и 100 мкл суспензии клеток распределяли во все лунки, содержащие разведения CTLA-4 Ig, и инкубировали в течение 24 часов. Затем содержимое планшетов собирали центрифугированием при 350 g в течение 5 минут и супернатанты переносили в новый 96-луночный планшет. Секрецию IL-2 измеряли с помощью набора ELISA для определения IL-2 яванского макака в соответствии с протоколом изготовителя (MABTech).
Сравнение эффективности по отношению к CTLA-4 дикого типа (SEQ ID NO: 35) в формате слияния с Fc в реакции смешанных лимфоцитов яванского макака для двух наиболее эффективных вариантов CTLA-4 показано на фигуре 3С.
Пример 6. Специфичность связывания вариантов с CD80 и CD86
Варианты CTLA-4 метили пероксидазой хрена с помощью набора для маркировки активированной HRP (Pierce). Белок слияния Fc внеклеточных доменов членов семейства B7 (R&D Systems) покрывали на ночь при концентрации 5 мкг/мл в PBS на планшете Maxisorp (Nunc). Планшеты блокировали 1% BSA и при разных концентрациях добавляли варианты CTLA-4, меченые HRP, и определяли количество связанного белка с помощью колориметрического субстрата (субстрат BD OptEIA, BD Biosciences).
Специфичность двух наиболее эффективных вариантов CTLA-4 по отношению к CD80 и CD86 по сравнению с другими родственными белковыми лигандами показана на фигуре 4.
Пример 7. Анализ Fc-опосредованных эффекторных функций
Анализ антителозависимой клеточноопосредованной цитотоксичности (ADCC)
Кровь человека собирали в пробирку-сборник CPT Vacutainer (BD Biosciences) и осаждали центрифугированием при 1700 g в течение 25 минут. Клетки собирали и переносили в коническую трубку на 50 мл и осаждали центрифугированием при 350g в течение 10 минут. Эритроциты лизировали путем ресуспендирования в 20 мл реагента Vitalize и инкубировали от 30 минут до 1 часа. Затем клетки осаждали центрифугированием при 350 g в течение 10 минут и отмывали однократно в среде T-клеток (среда Xvivo-15 (Lonza) с добавлением 1% Anti/Anti (Invitrogen)). 500000 PBMC помещали в 200 мкл среды Xvivo-15 в присутствии различных антител и белков слияния с Fc. Через 24 часа после инкубации определяли жизнеспособность B-лимфоцитов с помощью проточной цитометрии по окрашиванию антителами к CD19 (BD Biosciences) и 7-AAD (Molecular Probes). Число жизнеспособных B-клеток рассчитывали для каждого образца умножением 500000 на процент клеток в жизнеспособном выходе, определяемых свойствами прямого/бокового рассеивания, которые также являлись CD19+ и 7-AAD-.
Анализ комплементзависимой цитотоксичности (CDC)
Сыворотку человека собирали в пробирки для отделения сыворотки и добавляли среду Xvivo-15 до конечной концентрации 10% масса/объем. 100000 В-клеток Raji инкубировали в течение 18 часов в среде, содержащей различные антитела и белки слияния с Fc. Жизнеспособность клеток Raji определяли с помощью проточной цитометрии по окрашиванию 7-AAD (Molecular Probes). Число жизнеспособных клеток рассчитывали для каждого образца умножением 100000 на процент клеток в жизнеспособном выходе, определяемых свойствами прямого/бокового рассеивания, которые также являлись 7-AAD-. Среду, содержащую сыворотку человека, которую предварительно инактивировали нагреванием в течение 30 минут при температуре 56oC, применяли в качестве контроля для подтверждения комплементзависимой цитотоксичности. Демонстрация нулевой эффекторной функции (ADCC и CDC) двух наиболее эффективных вариантов CTLA-4 с модификацией TM показана на фигуре 5.
Пример 8. Анализ кинетики связывания вариантов CTLA-4 с CD80 и CD86 человека, яванского макака и мыши
Клонирование и экспрессия реагентов CD80 и CD86
Молекулы кДНК, кодирующие внеклеточные домены (ECD) CD80 и CD86 человека и мыши, синтезировали клонированием с помощью ПЦР с удлинением праймера и клонировали в pDONR221 (Invitrogen, номер по каталогу 12536-017). Применяли последовательности из базы данных для CD80 и CD86 человека и мыши (см. таблицу 1). Последовательности яванского макака были недоступны, поэтому, основываясь на прогнозированной высокой гомологии между яванским макаком и макаком резус, для создания праймеров, способных к амплификации кодирующей последовательности гена яванского макака, применяли последовательности CD80 (номер доступа группы ENSMMUG00000016367) и CD86 (номер доступа группы ENSMMUG00000000912) макака резус.
Фрагменты кДНК, кодирующие внеклеточные домены, затем переносили в вектор экспрессии млекопитающих pDEST12.2 (Invitrogen) с помощью фермента клоназы II LR Gateway в соответствии с инструкциями изготовителя (Invitrogen, номер по каталогу 12538-120). Вектор pDEST12.2 модифицировали таким образом, чтобы он содержал метку FLAG 10×his (DYKDDDDKAAHHHHHHHHHH) внутри рамки во вставленном изучаемом гене, и также с помощью вставки точки начала репликации oriP из вектора pCEP4 (Invitrogen, номер по каталогу V044-50), способствуя репликации эписомной плазмиды при трансфекции в клеточные линии, экспрессирующие продукт гена EBNA-1 (такие как клетки HEK293-EBNA). Экспрессируемый белок в супернатанте HEK293-EBNA очищали с помощью аффинной хроматографии Ni-NTA (колонка Histrap HP (GE Healthcare, номер по каталогу 17-5248-02)) с последующей эксклюзионной хроматографией (колонка Superdex 200 (GE Healthcare, номер по каталогу 17-1069-01)).
Внеклеточные домены CD80
Внеклеточные домены CD86
Анализ аффинности связывания с помощью поверхностного плазмонного резонанса (SPR)
Анализ взаимодействий CTLA-4:CD80 и CD86 с помощью SPR проводили на аппарате SPR Biacore 2000. Приблизительного 200 RU вариантов CTLA4 ковалентно связывались посредством первичных аминных групп с чипом CM5 Biacore (GE healthcare, номер по каталогу BR-1000-14) с помощью набора связывания аминов (GE healthcare, номер по каталогу BR-1000-50). Титрование CD80 и CD86 в буфере HBS-EP (GE healthcare, номер по каталогу BR-1001-88) проводили поверх неподвижных вариантов CTLA-4. Все остатки вычитали в двойном размере по отношению к референтному веществу. Анализ выполняли в компьютерной программе оценки Biacore, применяя модель Langmuir 1:1 для приведения в соответствие констант ассоциации и диссоциации. Если варианты имели очень быструю кинетику, то выполняли равновесный анализ.
Моновалентная аффинность (Kd в нМ) выбранных вариантов CTLA-4 и CTLA-4 дикого типа (SEQ ID NO: 35) в формате слияния с Fc для лигандов человека, яванского макака и мыши показана далее.
типа
1322
1321
1299
1315
1227
1115
1114
Улучшение аффинности (кратность улучшения по сравнению с CTLA-4 дикого типа в формате слияния с Fc) выбранных вариантов CTLA-4 для лигандов человека, яванского макака и мыши показано далее.
яванского макака
яванского макака
дикого
типа
1322
1321
1299
1315
1227
1115
Было отмечено, что все эти варианты, которые были наиболее эффективными вариантами в анализах биологической активности, проявляли более высокие прибавки аффинности к лиганду CD80 человека, чем к лиганду CD86 человека (как представлено в обобщенном виде на фигуре 6). Подобный вариант более высокой прибавки аффинности в отношении CD80 по сравнению с CD86 наблюдали при применении лигандов яванского макака.
Пример 9. Ускоренные исследования стабильности CTLA-4 дикого типа с мутациями Fc
Экспрессия, очистка и количественное определение белков CTLA-4
Кодирующую нативный внеклеточный домен CTLA4, слитый с вариантами 1-4 Fc, кДНК клонировали в pEE 12.4 (Lonza) и экспрессировали в клетках CHO. Вкратце, 1×106 клеток CHOK1SV (Lonza) трансфицировали нуклеофекцией (Lonza) с помощью программ U-024 и Solution V с 5 мкг линеризованной плазмидной ДНК. После трансфекции клетки культивировали в CD-CHO (Invitrogen), добавки 1×GS и 50 мкМ MSX. Клетки начинали расти приблизительно через 2 недели после трансфекции, при этом их переносили во встряхиваемые колбы для выработки белков. Для очистки применяли ряд этапов, начиная с этапа захвата и отбора Mab, с последующим этапом обменной полировки SuperQ аниона и с последующим SEC для удаления агрегатов. Белки хранили в фосфатно-солевом буферном растворе (PBS) pH 7,2.
Исследования стабильности
Исследования стабильности выполняли на молекулах CTLA-4, слитых с различными вариантами Fc для сравнения их стабильности и определения наиболее стабильной конфигурации Fc. Исследуемые молекулы включали: вариант-1 CTLA-4 Fc (SEQ ID NO: 7); вариант-2 CTLA-4 Fc (SEQ ID NO: 8); вариант-3 CTLA-4 Fc (SEQ ID NO: 9); и вариант-4 CTLA4 Fc (SEQ ID NO: 10). Аминокислотные различия в Fc-участке выделены на фигуре 1B для варианта-1 Fc (SEQ ID NO: 57); варианта-2 Fc (SEQ ID NO: 58); варианта-3 Fc (SEQ ID NO: 59) и варианта-4 Fc (SEQ ID NO: 60).
Вариант-1 CTLA-4 Fc (SEQ ID NO: 7) является молекулой абатацепта, содержащей CTLA-4 дикого типа (SEQ ID NO: 35), слитый с Fc-участком IgG1 с модифицированным шарниром (SEQ ID NO: 57).
Вариант-2 CTLA-4 Fc (SEQ ID NO: 8) является молекулой абатацепта, модифицированной для внедрения мутации YTE в Fc-участок, и содержит CTLA-4 дикого типа (SEQ ID NO: 35), слитый с Fc IgG1 с модифицированным шарниром и мутацией YTE (SEQ ID NO: 58).
Вариант-3 CTLA-4 Fc (SEQ ID NO: 9) содержит CTLA-4 дикого типа (SEQ ID NO: 35), слитый с Fc IgG1, в котором мутации C>S, обнаруженные в абатацепте, обращены, содержащим шарнир дикого типа и также включающий тройную мутацию (TM) и мутацию YTE (SEQ ID NO: 59).
Вариант-4 CTLA-4 Fc (SEQ ID NO: 10) содержит CTLA-4 дикого типа (SEQ ID NO: 35), слитый с Fc IgG4, содержащим мутацию YTE и мутацию шарнирной области, содержащей пролин в положении 111 (SEQ ID NO: 60).
Положение 111 в нумерации по Swiss Prot соответствует остатку 14 соответствующей последовательности IgG1 SEQ ID NO: 56, как показано на фигуре 1, или остатку 228 в полноразмерном константном участке IgG4. Известно, что введение мутации замены пролина серином в этом положении стабилизирует дисульфидное взаимодействие внутри цепи и, таким образом, минимизирует образование половины молекул IgG4 (Aalberse and Schuurman, Immunology 105(1):9-19 2002; Van der Neut Kolfschoten et al, Science 307(5844):1554-7 2007; Angal et al, Mol Immunol 30(1):105-8 1993; Schuurman et al Mol Immunol 38(1):1-8 2001), минимизируя, таким образом, сложности, связанные с разработкой кандидатных лекарственных препаратов. Также в связи с тем, что этот остаток пролина находится в соответствующем положении IgG1, возникновения сложностей, связанных с иммуногенностью, не предвидится.
Молекулы получали в жидкой форме при ~10 мг/мл в буфере PBS. Эти 4 молекулы концентрировали с помощью центрифугальных фильтров Amicon μltra, с предельной величиной 30000 MW. Молекулы центрифугировали при 4200 g до достижения целевого объема (30-60 минут). Концентрации измеряли спектрофотометрически с помощью стандартного коэффициента экстинкции антител 1,4. Были рассчитаны конечные концентрации, находящиеся в диапазоне 71-85 мг/мл. Хотя в этом примере применяли коэффициент экстинкции антитела, равный 1,4, впоследствии был определен фактический коэффициент экстинкции полипептида, составивший приблизительно 1,1. Таким образом, эти рассчитанные концентрации в действительности представляют диапазон концентраций 91-108 мг/мл. При желании можно достичь более высокой концентрации путем продолжения ультрафильтрации, с учетом ограничений объема.
Образцы каждого варианта Fc инкубировали при температуре 5°C и 25°C в течение 1 месяца. Эксклюзионная высокоэффективная жидкостная хроматография (SE-HPLC) представляла собой анализ, указывающий на стабильность, применяемый для определения и сравнения скоростей разложения 4 молекул. SE-HPLC проводили в соответствии с SOP DV-9525 со скоростью потока 1 мл/мин. Любой пик, который элюирует перед пиком мономера (при времени элюирования менее чем для одного мономера) в хроматограмме ВЭЖХ, определяют как пик агрегата. Любой пик, который элюирует после пика мономера (при времени элюирования более чем для одного мономера), определяют как пик фрагмента. Общий процент агрегатов и фрагментов определяют по площади пика(пиков) агрегатов и пика(пиков) фрагментов в виде доли всех общей площади всех пиков белка в хроматограмме. Перед инкубацией SE-HPLC проводили на всех образцах для времени точки замера 0. Впоследствии данные SE-HPLC собирали каждую неделю для исследования стабильности при температуре 25°C и каждые 2 недели для исследования стабильности при температуре 5°C. Общая продолжительность обоих исследований составила 1 месяц. Далее показаны скорости агрегации, фрагментации и разрушения, рассчитанные с помощью линейного соответствия данным 1 месяца.
Скорости через 1 месяц при температуре 5°C
Скорости через 1 месяц при температуре 25°C
На основании этих данных вариант-3 Fc (SEQ ID NO: 59) был выбран в качестве оптимального партнера слияния на основании наименьших скоростей утраты чистоты при температуре 5°C и 25°C.
Пример 10. Ускоренные исследования стабильности вариантов CTLA-4, слитых с вариантом-3 Fc
Исследования стабильности выполняли на 6 из наиболее эффективных молекул вариантов CTLA-4, слитых с вариантом-3 Fc (SEQ ID NO: 59) для определения наиболее стабильного варианта CTLA-4. Молекулами, которые исследовали в этом формате, были: вариант 1115 (SEQ ID NO: 15), вариант 1227 (SEQ ID NO: 16), вариант 1299 (SEQ ID NO: 13), вариант 1315 (SEQ ID NO: 14), вариант 1321 (SEQ ID NO: 12), вариант 1322 (SEQ ID NO: 11).
Молекулы получали в жидкой форме при ~10 мг/мл в буфере PBS. Эти 6 молекулы концентрировали с помощью центрифугальных фильтров Amicon μltra, с предельной величиной 30000 MW. Молекулы центрифугировали при 4200 g до достижения целевого объема (30-60 минут). Коэффициенты экстинкции рассчитывали с помощью аминокислотных последовательностей. Рассчитанные коэффициенты экстинкции составили 1,10 для 1315 и 1321; и 1,09 для 1115, 1227, 1299 и 1322. Концентрации измеряли с помощью соответствующего коэффициента экстинкции. Конечные концентрации находились в диапазоне 94,6-101,6 мг/мл.
Исследования стабильности выполняли при температуре 5°C и 25°C в соответствии с теми же указаниями, описанными в предыдущем разделе, за исключением сбора только во временные точки месяца 0 и 1 для исследования стабильности при температуре 5°C. Общая продолжительность обоих исследований составила 1 месяц. Далее показаны скорости агрегации, фрагментации и разрушения, рассчитанные с помощью линейного соответствия данным 1 месяца.
Скорости через 1 месяц при температуре 25°C
Скорости через 1 месяц при температуре 5°C
Было обнаружено, что варианты 1299 и 1322 имеют наименьшие уровни утраты чистоты в исследованиях в течение 1 месяца при температуре 5°C и 25°C. В связи с этим, исследования стабильности были продлены до 6 месяцев при температуре 5°C для вариантов 1299 и 1322. Далее приведены результаты, полученные по ежемесячным временным точкам.
Данные стабильности 1299 при температуре 5°C
% утраты чистоты/год, рассчитанный исходя из линейного соответствия данных, равен 3,6%.
Данные стабильности 1322 при температуре 5°C
% утраты чистоты/год, рассчитанный, исходя из линейного соответствия данных, равен 2,6%.
Пример 11. Создание тетравалентной молекулы CTLA-4
Разработка и конструирование векторов экспрессии тетравалентного CTLA-4
С помощью связывающегося с нитрофенолом IgG NIP 74 (тяжелая цепь SEQ ID NO: 17; легкая цепь SEQ ID NO: 18) в качестве каркаса создавали тетравалентный CTLA-4 путем слияния CTLA-4 с аминоконцом обеих цепей антитела VH и VL (фигура 7A). Конструкты экспрессии создавали путем слияния CTLA-4 с VH и VL с помощью 2-х-этапной стратегии ПЦР и затем субклонирования продуктов ПЦР в векторы экспрессии IgG, содержащие константные домены антитела. В процессе первичной ПЦР амплифицировали CTLA-4 и IgG VH и VL с ген-специфическими праймерами (SEQ ID NO: 21-28), которые добавляли гибкий линкер на 3’ конце CTLA-4 и 5’ конце VH и VL. В процессе вторичной ‘протягивающей’ ПЦР CTLA-4 прикрепляли к 5’ концу VH и VL путем отжига комплементарных линкерных последовательностей. Конечный конструкт CTLA-4-VH амплифицировали с помощью праймеров, которые вводили BssHII в 5’ конец и сайт BstEII в 3’ конец (SEQ ID NO: 29-30). Конечный конструкт CTLA-4-VL амплифицировали с помощью праймеров, которые вводили ApaLI в 5’ конец и сайт PacI в 3’ конец (SEQ ID NO: 31-32). Продукты ПЦР затем расщепляли соответствующими ферментами рестрикции до их сшивки непосредственно в предрасщепленные векторы экспрессии IgG, pEU1.4 для кассеты CTLA-4-VH и pEU3.4 для кассеты CTLA-4-VL, и применяли для трансформации химически компетентных клеток DH5-альфа E.coli. Точные клоны, соответствующие SEQ ID NO: 19 и 20, затем идентифицировали с помощью анализа последовательностей для исследований экспрессии.
Экспрессия и очистка тетрамерного CTLA-4
Для обеих плазмид, необходимых для трансфекции, одной, кодирующей слияние CTLA-4 с тяжелой цепью, и одной, кодирующей слияние CTLA-4 с легкой целью, применяли одну колонию для инокуляции 100 мл 2xTY бульона, содержащего 100 мкг/мл ампициллина. Культуры инкубировали на ночь (16 часов) при температуре 37°C и 300 об/мин. Плазмидную ДНК выделяли из бактериального осадка с помощью набора EndoFree Plasmid Maxi (QIAGEN; 12362) в соответствии с инструкциями изготовителя. На следующее утро после трансфекции клетки CHO засевали при концентрации один миллион клеток на мл в среде CD-CHO (Invitrogen; 10743-029), содержащей 25 мкМ L-метионина сульфоксимина (Sigma; M5379). Клетки культивировали в объеме 500 мл и инкубировали при температуре 37°C, 140 об/мин, 80% влажности и 5% CO2. С целью образования комплексов ДНК-PEI для трансфекции 250 мкг каждого вектора смешивали и разводили в 150 мМ NaCl для получения 500 мкг ДНК в конечном объеме 1 мл. Затем ДНК смешивали с 1 мл 5 мг/мл PEI (Polysciences; 23966), разведенного в 150 мМ NaCl, и инкубировали при комнатной температуре в течение 1 минуты. Затем смесь DNA-PEI осторожно добавляли к культуре CEP6, которую затем инкубировали в течение 24 часов перед добавлением 150 мл CD-CHO среды Efficient Feed B (Invitrogen; A10240). После этого культуру инкубировали в течение еще шести дней.
Затем культуру центрифугировали при 2000 g в течение 30 минут; после этого очищенный супернатант культуры отфильтровывали с помощью 500 мл Stericup (Millipore; SCGVU05RE). Очистку тетравалентного CTLA-4 из очищенного супернатанта культуры выполняли с помощью системы ÄKTApurifier 10 (GE Healthcare; 28-4062-64) и аффинной хроматографии с последующей гельфильтрационной хроматографией. Колонку 5 мл MabSelect Sure (GE Healthcare; 11-0034-94) уравновешивали десятью объемами D-PBS колонки (Invitrogen; 14040-174). Очищенный супернатант культуры пропускали через колонку перед отмывкой колонки дополнительными десятью объемами D-PBS колонки. Связанный белок элюировали 0,1 M глицином, pH 2,7, и фракции собирали по 1 мл. Каждую фракцию нейтрализовали 100 мкл 1M Tris, pH 10, и фракции, содержащие элюированный белок, объединяли и концентрировали до 2 мл с помощью Vivaspin, фильтра 10000 MWCO (Sartorius Stedim; VS2002) в соответствии с инструкциями изготовителя. 2 мл концентрированного образца загружали в HiLoad Superdex 200, 16/60 гельфильтрационную колонку (GE Healthcare; 17-1069-01), которую уравновешивали в D-PBS. В результате этого способа собирали фракции по 1,2 мл. Эти фракции, содержащие целевой белок точной молекулярной массы (объем возврата 56 мл), объединяли, концентрировали до 1 мл с помощью Vivaspin, фильтров 10000 MWCO и хранили при температуре -80°C.
Профиль очищенного тетрамерного CTLA-4 сравнивали с CTLA-4 дикого типа (SEQ ID NO: 35) в формате слияния с Fc в двойном клеточном анализе Raji-Jurkat и данные представлены на фигуре 8. Значения IC50 в этом анализе тетрамерного CTLA-4 и CTLA-4 дикого типа (SEQ ID NO: 35) в формате слияния с Fc составили 1,93 нМ и 11,39 нМ, соответственно. Результат указывает на возрастание эффективности в 5,9 раз при превращении из димерного формата слияния Fc в тетрамерный формат, подобный IgG.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОСУПРЕССОРНЫЕ ПОЛИПЕПТИДЫ И НУКЛЕИНОВЫЕ КИСЛОТЫ | 2008 |
|
RU2506275C2 |
| ВЫДЕЛЕННАЯ НУКЛЕИНОВАЯ КИСЛОТА, КОДИРУЮЩАЯ ЛИГАНД CD86 КОШКИ, ДИАГНОСТИЧЕСКИЙ ОЛИГОНУКЛЕОТИД, КЛОНИРУЮЩИЙ ВЕКТОР, ВАКЦИНА, СПОСОБЫ ИНДУКЦИИ ИЛИ ПОДАВЛЕНИЯ ИММУНИТЕТА У КОШКИ | 1999 |
|
RU2263145C2 |
| НУКЛЕИНОВЫЕ КИСЛОТЫ, КОДИРУЮЩИЕ РЕЦЕПТОР CTLA-4 КОШКИ, ВЕКТОР, КЛЕТКИ-ХОЗЯЕВА, ВАКЦИНЫ, ОЛИГОНУКЛЕОТИДЫ, ПОЛИПЕПТИДЫ CTLA-4 КОШКИ И СПОСОБЫ ИНДУКЦИИ И ПОДАВЛЕНИЯ ИММУННОГО ОТВЕТА У КОШКИ | 1999 |
|
RU2377302C2 |
| ИНГИБИТОРЫ Т-КЛЕТОЧНОЙ АКТИВАЦИИ | 2012 |
|
RU2657440C2 |
| M2-ДЕФЕКТНЫЙ ПОКСВИРУС | 2019 |
|
RU2819245C2 |
| РЕКОМБИНАНТНЫЙ ВИРУС, ЭКСПРЕССИРУЮЩИЙ ЧУЖЕРОДНУЮ ДНК, КОДИРУЮЩУЮ КОШАЧИЙ CD80, КОШАЧИЙ CTLA-4 ИЛИ КОШАЧИЙ CD86, И ЕГО ИСПОЛЬЗОВАНИЕ | 1999 |
|
RU2244006C2 |
| ОДНОЦЕПОЧЕЧНЫЕ БЕЛКИ-АГОНИСТЫ РЕЦЕПТОРА CD40 | 2016 |
|
RU2745801C2 |
| НОВЫЕ БИСПЕЦИФИЧЕСКИЕ АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, ОБЛАДАЮЩИЕ СПОСОБНОСТЬЮ СПЕЦИФИЧЕСКИ СВЯЗЫВАТЬСЯ С CD40 И FAP | 2018 |
|
RU2766234C2 |
| СПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ АГЕНТЫ ПРОТИВ В7-Н1 | 2010 |
|
RU2571204C2 |
| СПОСОБ ОТБОРА И ПОЛУЧЕНИЯ ВЫСОКОСЕЛЕКТИВНЫХ И МУЛЬТИСПЕЦИФИЧНЫХ НАЦЕЛИВАЮЩИХ ГРУПП С ЗАДАННЫМИ СВОЙСТВАМИ, ВКЛЮЧАЮЩИХ ПО МЕНЬШЕЙ МЕРЕ ДВЕ РАЗЛИЧНЫЕ СВЯЗЫВАЮЩИЕ ГРУППИРОВКИ, И ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2639287C2 |



























































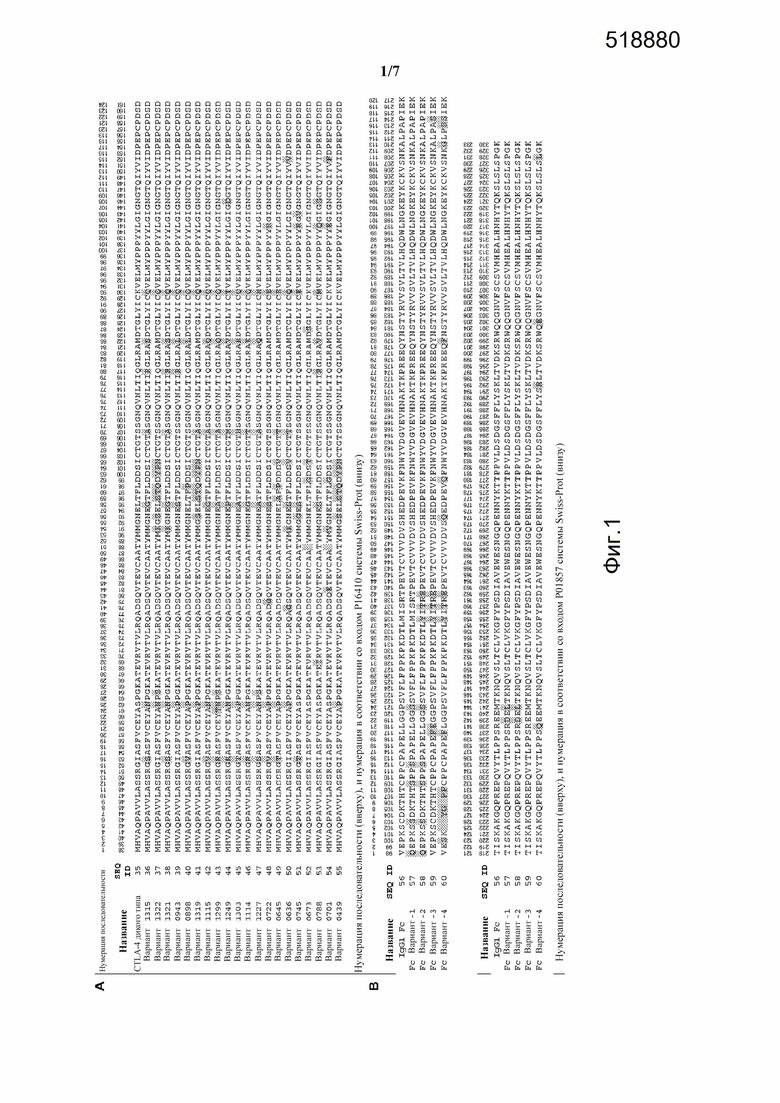

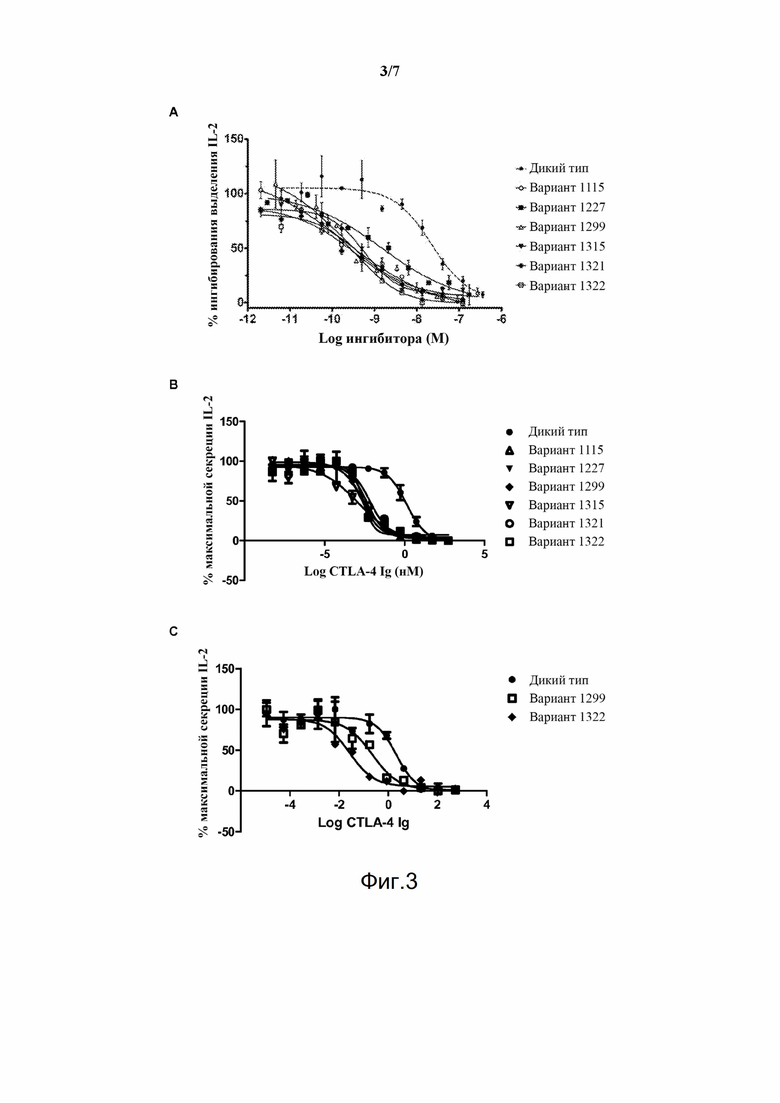
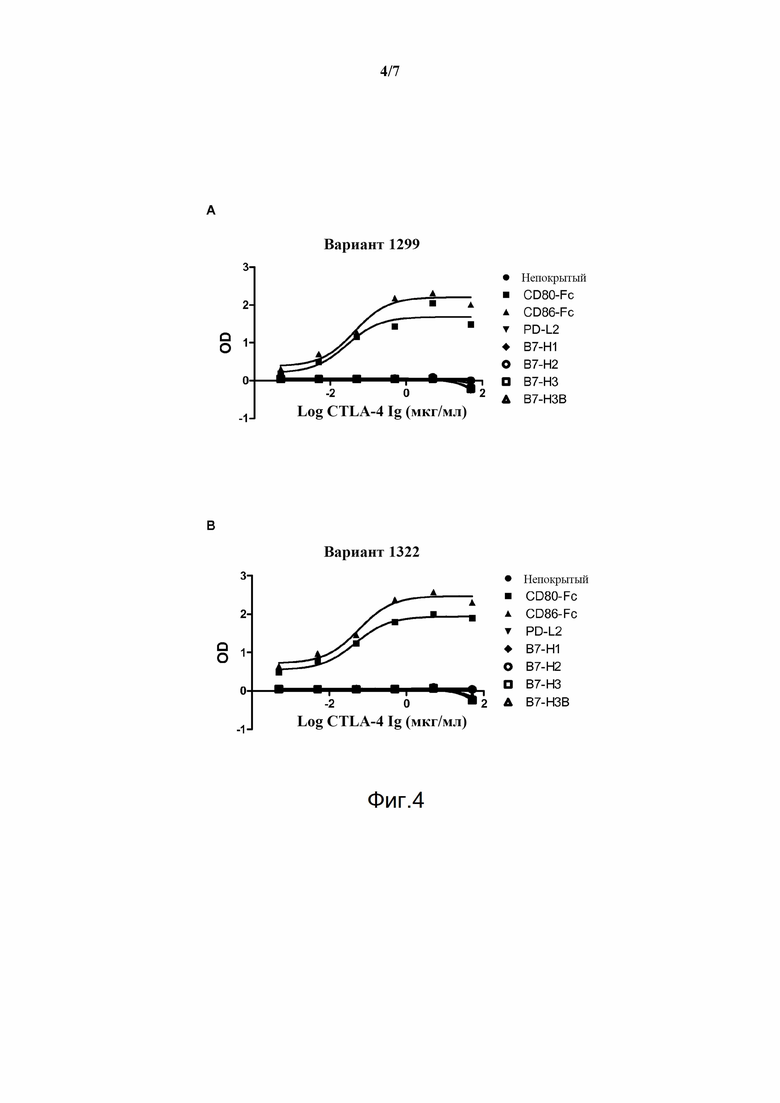
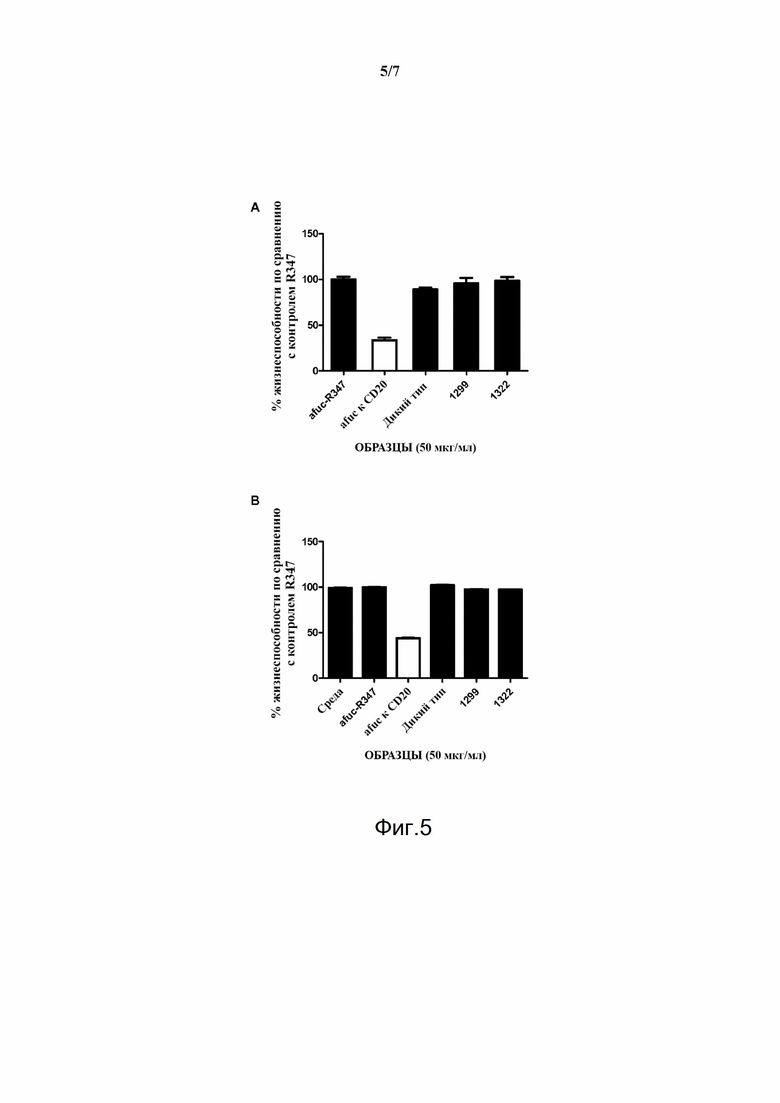
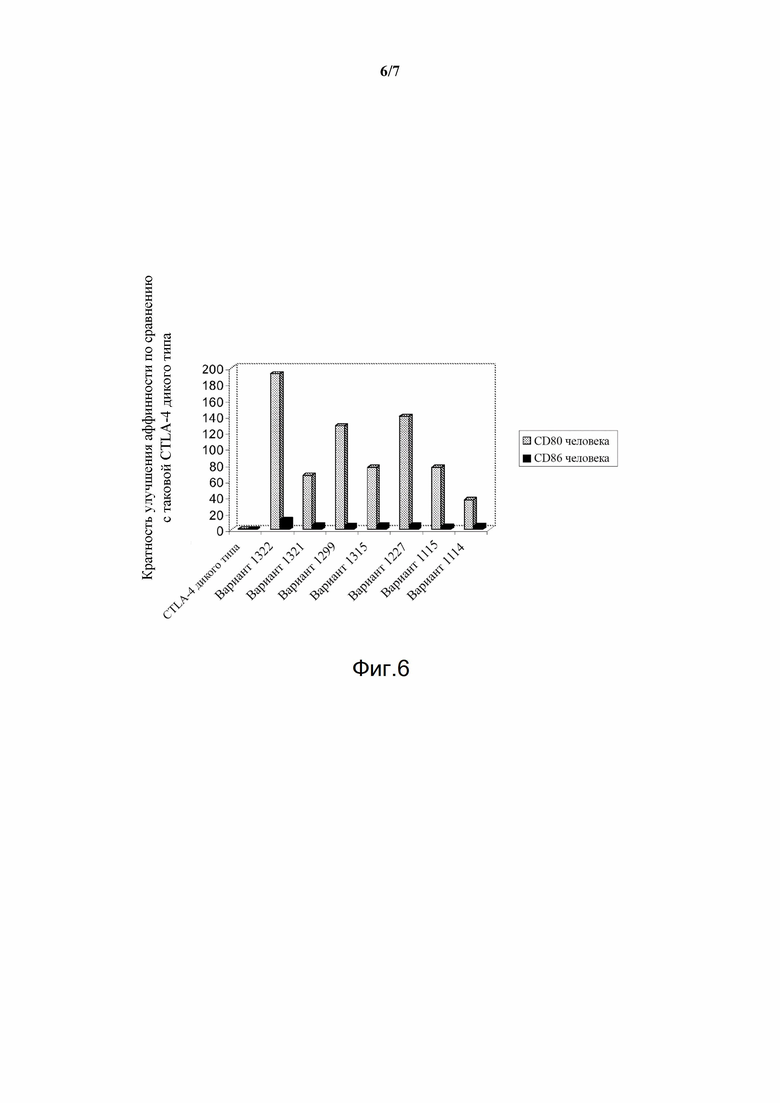
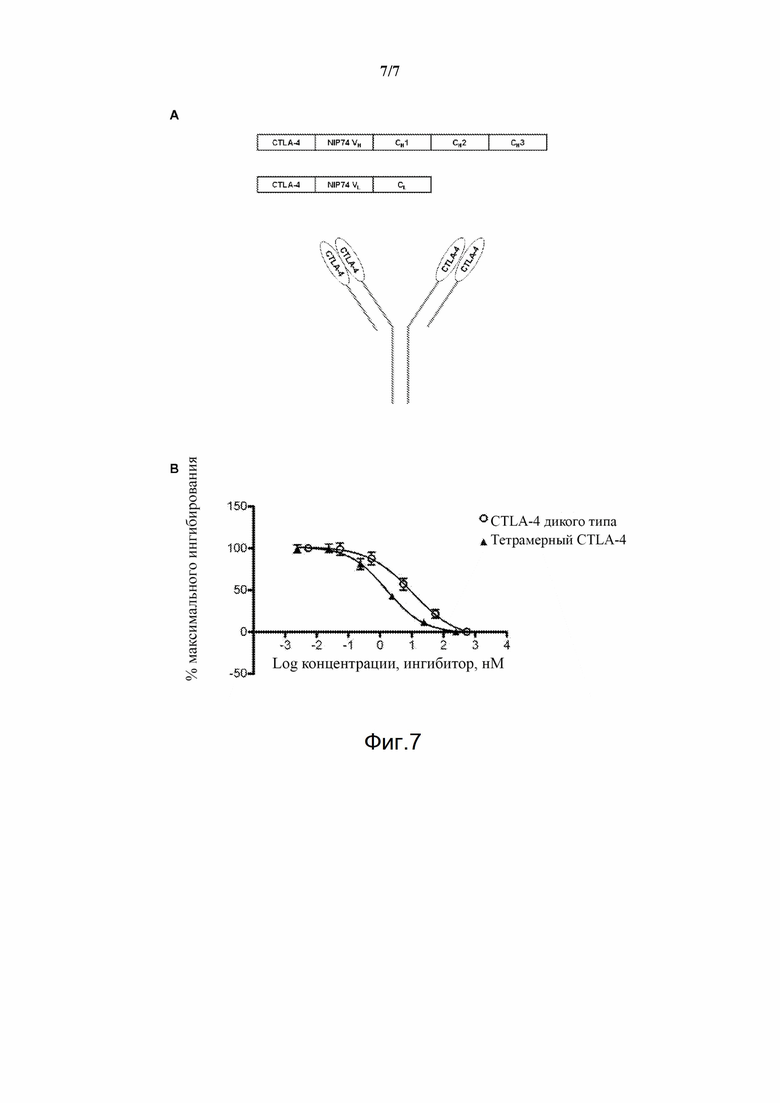
Изобретение относится к области биотехнологии, конкретно к вариантам антигена 4 цитотоксических Т-лимфоцитов (CTLA-4), что может быть использовано в медицине. Получают полипептид CTLA-4 с мутациями, его конъюгат с Fc IgG, клетку-хозяина для получения полипептида, композицию, содержащую полипептид, которые применяются для лечения аутоиммунного заболевания и/или ослабления ответа Т-клеток у пациента. Изобретение позволяет за счет высокой аффинности и стабильности полипептида увеличить эффективность лечения аутоиммунного заболевания и/или ослабления ответа Т-клеток у пациента, например, ревматоидного артрита. 6 н. и 18 з.п. ф-лы, 7 ил., 12 табл., 11 пр.
1. Выделенный полипептид CTLA-4, содержащий комбинацию мутаций, выбранных из:
- мутаций 1315, т.е. S в положении I16; N в положении S25; G в положении L58; A в положении S70; R в положении Q80; S в положении M85 и Q в положении K93 (SEQ ID NO: 36);
- мутаций 1322, т.е. N в положении S25; S в положении G27; K в положении M54; S в положении N56; S в положении T59; T в положении F 60; Q в положении L61; Y в положении D63; P в положении S64; N в положении I65 и Q в положении K93 (SEQ ID NO: 37);
- мутаций 1321, т.е. S в положении I16; N в положении S25; K в положении M54; G в положении L58; A в положении S70; R в положении Q80; S в положении M85 и Q в положении K93 (SEQ ID NO: 38);
- мутаций 1115, т.е. V в положении I16; N в положении S25; G в положении L58; A в положении S70; Q в положении M85 и Q в положении K93 (SEQ ID NO: 42);
- мутаций 1299, т.е. R в положении I16; T в положении A24; N в положении S25; S в положении G27; A в положении L58; A в положении S70; Q в положении M85 и Q в положении K93 (SEQ ID NO: 43); и
- мутаций 1227, т.е. S в положении I16; N в положении S25; S в положении G27; A в положении L58; A в положении S70; Q в положении M85 и H в положении К93 (SEQ ID NO: 47).
2. Полипептид CTLA-4 по п.1, имеющий аффинность связывания с CD80 человека 50 нМ или менее, где аффинность выражена Kd, определяемой с помощью поверхностного плазмонного резонанса.
3. Полипептид CTLA-4 по п.2, имеющий аффинность связывания с CD80 человека 20 нМ или менее, где аффинность выражена Kd, определяемой с помощью поверхностного плазмонного резонанса.
4. Полипептид CTLA-4 по п.1, где полипептид имеет большую аффинность связывания с CD86 человека, чем CTLA-4 дикого типа (SEQ ID NO: 35).
5. Полипептид CTLA-4 по п. 1, который имеет аффинность связывания с CD80, по меньшей мере в 10 раз превышающую аффинность связывания с CD86.
6. Полипептид CTLA-4 по п.5, который имеет аффинность связывания с CD80, по меньшей мере в 50 раз превышающую аффинность связывания с CD86.
7. Конъюгат полипептида CTLA-4, обладающий активностью полипептида CTLA-4, где полипептид CTLA-4 по п.1 конъюгирован с аминокислотной последовательностью Fc IgG.
8. Конъюгат олипептида CTLA-4 по п.7, где Fc IgG представляет собой Fc IgG1 человека, модифицированный с целью снижения эффекторной функции Fc, и содержит нативную шарнирную область Fc IgG1 человека.
9. Конъюгат полипептида CTLA-4 по п.7, где аминокислотная последовательность Fc IgG содержит Fc-участок IgG1 человека, в котором одна или обе из следующих групп остатков замещены следующим образом:
F в положении остатка 20; E в положении остатка 21; S в положении остатка 117 и
Y в положении остатка 38, T в положении остатка 40, E в положении остатка 42,
при этом нумерация остатков определена по отношению к SEQ ID NO: 56.
10. Конъюгат полипептида CTLA-4 по п.7, где аминокислотная последовательность Fc IgG содержит SEQ ID NO: 59.
11. Конъюгат полипептида CTLA-4 по п. 7, где полипептид CTLA-4 содержит SEQ ID NO: 43 и где аминокислотная последовательность Fc IgG содержит SEQ ID NO: 59.
12. Конъюгат полипептида CTLA-4 по п. 10, где аминокислотная последовательность Fc CTLA-4-IgG представляет собой аминокислотную последовательность CTLA-4-Ig, кодируемую нуклеиновой кислотой, депонированной под номером доступа в NCIMB 41948.
13. Полипептид CTLA-4 по п.1, где полипептид находится в мультимере.
14. Полипептид CTLA-4 по п.13, где полипептид CTLA-4 находится в димере.
15. Полипептид CTLA-4 по п.13, где полипептид CTLA-4 находится в тетрамере.
16. Полипептид CTLA-4 по п.15, где тетрамер содержит две пары полипептидов CTLA-4, при этом каждая пара включает полипептид CTLA-4, слитый с константной областью легкой цепи антитела, и полипептид CTLA-4, слитый с константной областью тяжелой цепи антитела.
17. Клетка-хозяин для получения полипептида CTLA-4 по п.1, содержащая нуклеиновую кислоту, кодирующую полипептид CTLA-4 по п. 1.
18. Композиция, содержащая
эффективное количество полипептида CTLA-4 по п. 1, конъюгированного с аминокислотной последовательностью Fc IgG; и
один или несколько фармацевтических наполнителей,
причем композиция предназначена для лечения аутоиммунного заболевания и/или ослабления ответа T-клеток.
19. Композиция по п.18, отличающаяся тем, что полипептид CTLA-4 конъюгирован с аминокислотной последовательностью Fc IgG, содержащей SEQ ID NO: 59.
20. Композиция по п. 18, где полипептид CTLA-4 содержит SEQ ID NO: 43 и где аминокислотная последовательность Fc IgG содержит SEQ ID NO: 59.
21. Композиция по п.18, содержащая полипептид CTLA-4 в концентрации по меньшей мере 70 мг/мл.
22. Композиция по п.21, содержащая полипептид CTLA-4 в концентрации по меньшей мере 100 мг/мл.
23. Применение полипептида CTLA-4 по п. 1, конъюгата полипептида CTLA-4 по п. 7 или композиции по п. 18 в способе лечения аутоиммунного заболевания и/или ослабления ответа T-клеток у пациента посредством подкожного или внутривенного введения.
24. Применение полипептида CTLA-4 по п. 1, конъюгата полипептида CTLA-4 по п. 7 или композиции по п. 18 в способе лечения аутоиммунного заболевания и/или ослабления ответа T-клеток, включающем введение указанного полипептида CTLA-4, конъюгата полипептида CTLA-4 или композиции пациенту с интервалами 28 дней.
| MORTON P.A | |||
| et al., Differential effects of CTLA-4 substitutions on the binding of human CD80 (B7-1) and CD86 (B7-2), J | |||
| Immunol., 1996, v.156, is.3, p.1047-1054 | |||
| WO 2009058564 A2, 07.05.2009 | |||
| WO 1997047732 A2, 18.12.1997 | |||
| RUDERMAN E.M | |||
| et al., The evolving clinical profile of abatacept (CTLA4-Ig): a novel co-stimulatory modulator for the treatment of rheumatoid arthritis, Arthritis Res | |||
| Ther., 2005, v.7, is.2, p.21-25 | |||
| МОНОВАЛЕНТНЫЕ КОМПОЗИЦИИ ДЛЯ СВЯЗЫВАНИЯ CD40L И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2005 |
|
RU2364420C2 |
Авторы
Даты
2018-10-31—Публикация
2013-03-11—Подача