ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к китайской лекарственной композиции для предотвращения или лечения сердечно-сосудистых и цереброваскулярных заболеваний или деменции, а также способу получения и применению указанной китайской лекарственной композиции.
УРОВЕНЬ ТЕХНИКИ
Сердечно-сосудистые и цереброваскулярные заболевания являются основными заболеваниями, которые угрожают жизни и здоровью людей, и характеризуются высоким уровнем заболеваемости, высоким уровнем смертности, высокой частотой инвалидизации и высокой частотой рецидивов. Согласно статистическим данным последних лет, случаи смерти, вызванной сердечнососудистыми и цереброваскулярными заболеваниями, ежегодно в Китае составляют примерно половину от всех случаев смерти. Распространенность сердечнососудистых и цереброваскулярных заболеваний тесно связана с развитием общества и повышением уровня жизни, и причинами таких заболеваний являются высокое давление, неправильное питание, недостаток физической активности, чрезмерное потребление табака и алкоголя и ожирение. Сердечно-сосудистые и цереброваскулярные заболевания включают коронарную болезнь сердца, стенокардию, инфаркт миокарда, гемодинамически зависимое сердечно-легочное заболевание (blood addicted pulmonary heart disease), ишемическую энцефалопатию, тромбоз сосудов головного мозга, гипертензию, гиперлипидемию, и основными причинами, вызывающими эти заболевания, является атеросклероз; они приводят к стенозу сосудов, закупорке протоков, что влечет за собой недостаточное кровоснабжение сердца и головного мозга, вызывая ощущение тяжести в голове, головокружение, головную боль, чувство сдавленности в груди и другие симптомы, а в тяжелых случаях могут привести к инсульту и инфаркту миокарда. Сердечнососудистая ишемия оказывает влияние на энергетический метаболизм с последующими многочисленными изменениями, такими как накопление молочной кислоты, кальциевая перегрузка, свободно-радикальные повреждения. Таким образом, сердечно-сосудистые и цереброваскулярные заболевания причиняют серьезный вред здоровью человека, и раннее их предотвращение и своевременное лечение имеют чрезвычайно важное значение.
Деменция представляет собой приобретенный устойчивый синдром умственного расстройства, вызванный органическими поражениями головного мозга. Деменцию, встречающуюся у людей пожилого возраста, подразделяют на: А. первичную дегенеративную деменцию, а именно болезнь Альцгеймера (сокращенно БА); В. сосудистую деменцию (СД); С. смешанную деменцию (сочетание БА и СД); D. другие типы деменции (болезнь Пика, деменцию с тельцами Леви). БА и СД представляют собой два основных типа деменции.
Сосудистая деменция связана с однократным или повторными инсультами и высоким артериальным давлением, высоким уровнем холестерина, диабетом, курением, потреблением алкоголя и т.д., и она проявляется в виде нарушений памяти, способности к счету, ориентации и способности к рассуждению, аффективных расстройств и патологического поведения, и даже потери жизнеспособности при достижении поздней стадии.
Данные исследований указывают на то, что вероятность возникновения деменции вследствие церебрального инфаркта связана в основном с размером, количеством и локализацией очаговых поражений, возникающих при церебральном инфаркте. Исследования показали, что очаговое поражение при инфаркте объемом более 50 мл может сопровождаться деменцией, объемом более 100 мл - часто сопровождается деменцией; в результате исследований также было обнаружено, что среди пациентов с СД большая площадь очаговых поражений при инфаркте составляет 11,2% случаев, малая площадь очаговых поражений при инфаркте составляет 88,8% случаев, множественные очаговые поражения составляли 97,6% случаев, и отмечается, что деменция также может возникать, даже если объем очаговых поражений мал - в частности, чем больше количество очаговых поражений при инфаркте, тем выше частота возникновения деменции. Также существуют исследования, подтверждающие, что локализация церебрального инфаркта является ключевым фактором, приводящим к деменции; в большинстве сообщений упоминалось, что инфаркты, приводящие к очаговым изменениям перивентрикулярного белого вещества, обнаруживаемым с помощью КТ, значительно увеличивали частоту возникновения деменции. Павикс (Pavics) изучал изменения мозгового кровотока у пациентов и обнаружил, что у пациентов с сосудистой деменцией усредненный кровоток в полушарии был значительно снижен, перфузия в области инфаркта значительно снижена по сравнению с нормальными тканями, полностью неперфузируемые области редки; в исследованиях, сопоставляющих шкалу оценки когнитивных функций с мозговым кровотоком, была обнаружена положительная корреляция между усредненным кровотоком в полушарии и степенью деменции, что позволяет предположить, что снижение кровотока при СД тесно связано с умственной деятельностью. В исследованиях последних лет было отмечено, что мозговой кровоток и интенсивность метаболизма глюкозы в некоторых участках, таких как лобная доля, височная доля, в частности таламус, базальные ганглии, у пациентов с СД были значительно снижены по сравнению с мозговым кровотоком и интенсивностью метаболизма глюкозы в других участках, что свидетельствует о возможной ассоциированности СД с разрывом связей между корой головного мозга и подкорковыми структурами, т.е. неполной связью между неврологическими функциями головного мозга. Сопротивление сосудов головного мозга, вязкость крови и нейрогуморальные факторы могут оказывать прямое или косвенное влияние на поддержание постоянного мозгового кровотока.
Исследования показали, что ишемическое поражение головного мозга представляет собой каскадный процесс, и в каждом секторе происходит индукция различных молекулярных сетей, вызывающих дегенеративное повреждение нейронов; после возникновения церебрального инфаркта происходят нарушение мозгового кровотока и реперфузия, что вызывает энергетический дефицит ткани головного мозга, повышение уровня нейромедиатора, в частности, возбуждающей аминокислоты, вызывает дальнейшее снижение кровотока и поток или высвобождение ионов кальция из внутриклеточных запасов кальция, вызывает активацию большого количества сигнальных каскадов, запускаемых ферментами, активность некоторых ферментов приводит к образованию радикалов кислорода, которые сами по себе также играют роль вторичного мессенджера, повреждают клеточные белки, сахара, жирные кислоты, дополнительно вызывают периинфарктную деполяризацию, допускают распространение области инфаркта до области ишемической полутени; свободные радикалы и другие мессенджеры активируют воспалительные цитокины и ферменты, приводят к активации клеток микроглии с развитием воспаления, таким образом происходит увеличение проницаемости сосудов, повреждение нейронального скелета, тогда как вторичное повреждение приводит к деменции. Исследования показали, что после состояния ишемии уровни нейромедиаторов сначала повышаются, а затем снижаются, такие нейромедиаторы как ацетилхолин, катехоламин, нейропептид тесно связаны со снижением когнитивных способностей. Данные нейромедиаторы участвуют в патофизиологическом процессе развития СД и могут стать важным индикатором, отражающим тяжесть СД.
В последние годы традиционная китайская медицина показала уникальные преимущества при лечении сердечно-сосудистых и цереброваскулярных заболеваний, сенильной деменции, в частности, сосудистой деменции; традиционная китайская медицина является эффективной, долгосрочной, характеризуется меньшим количеством неблагоприятных реакций, особенно удовлетворяет требованию долгосрочной эффективности и, таким образом, широко используется в клинической практике. Результаты многочисленных исследований и применений в клинической практике доказали, что традиционная китайская медицина имеет уникальные преимущества, поскольку она характеризуется хорошей переносимостью и незначительными побочными эффектами, и, соответственно, она подходит для длительного применения пациентами.
Женьшень является «теплым» по своей природе и имеет сладкий и немного горький вкус и выполняет функцию питания сердца и почек, благоприятен для энергии ци и повышения интеллекта; листья гинкго являются «нейтральными» по своей природе и имеют горький и вяжущий вкус и выполняют функцию стимулирования кровообращения с устранением закупорки кровеносных сосудов. Рыльца шафрана являются «нейтральными» по своей природе, имеют сладкий вкус и выполняют функцию стимулирования кровообращения с устранением закупорки кровеносных сосудов, что приводит к уменьшению закупорки и растворению тромбов. Современные фармакологические исследования подтвердили, что женьшень содержит различные сапонины, которые могут значительно облегчить реперфузионное повреждение и нарушение памяти при ишемии головного мозга при изучении многих экспериментальных животных, эти сапонины могут улучшать способность к обучению и запоминанию у нормальных животных и обладать эффектами увеличения поглощения нейромедиаторов синаптосомами и усиления экспрессии фактора роста нервов; экстракт листьев гинкго может ингибировать перекисное окисление липидов клеточных мембран и может способствовать расширению кровеносных сосудов, увеличивать кровоток, снижать вязкость крови, ингибировать тромбоз и противодействовать агрегации тромбоцитов, что обеспечивает улучшение метаболизма в головном мозге и защиту нервных клеток; рыльца шафрана обладают эффектами блокирования притока внеклеточного кальция и высвобождения кальция из эндоплазматического ретикулума, антиоксидантной активностью, антигипертензивной активностью, действием против атеросклероза, отека головного мозга и т.д., они также могут улучшать парциальное давление кислорода в кровотоке млекопитающих, а в последние годы также было обнаружено, что они действенны против нарушений памяти и способности к познанию, вызванных употреблением алкоголя.
В патенте ZL 02131435.7 раскрыта китайская лекарственная композиция, содержащая терапевтически эффективное количество женьшеня, листьев гинкго и рылец шафрана для лечения ишемического цереброваскулярного заболевания и сосудистой деменции, сенильной деменции и т.д. На основании вышеуказанного патента заявитель разработал «капсулу Sailuotong» (оригинальное торговое наименование «Weinaokang»), и в настоящее время препарат проходит клинические испытания.
В заявке WO 2007118363 A1 раскрыта сходная китайская лекарственная композиция для лечения ишемического цереброваскулярного заболевания и сенильной деменции, приготовленная из женьшеня, листьев гинкго, рылец шафрана и соевых бобов.
При систематическом изучении вышеупомянутых патентов авторы настоящего изобретения обнаружили, что могут быть достигнуты лучшие результаты в случае применения конкретного компонентного состава и содержаний компонентов.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения провели систематическое экспериментальное исследование эффектов компонентов композиций, указанных в патенте ZL 02131435.7 и заявке WO 2007118363 A1, по предотвращению или лечению сердечно-сосудистых и цереброваскулярных заболеваний и деменции и обнаружили, что эффект соевых бобов, содержащихся в композиции, не является очевидным. В ходе оптимизационного исследования состава лекарственного средства авторы настоящего изобретения обнаружили, что можно достичь лучшего по сравнению с композицией согласно WO 2007118363 A1 фармакологического эффекта с применением лишь трех ингредиентов, использующихся в китайской медицине: женьшеня, листьев гинкго и рылец шафрана.
Кроме того, авторы настоящего изобретения также обнаружили, что композиция, которая получена при конкретном массовом соотношении женьшеня, листьев гинкго и рылец шафрана, обладает улучшенным действием в отношении лечения или предотвращения сердечно-сосудистых и цереброваскулярных заболеваний и деменции, в частности, при лечении ишемического цереброваскулярного заболевания, ишемической болезни сердца, стенокардии и сенильной деменции. В частности, указанная композиция обладает улучшенным действием в отношении лечения заболеваний, ассоциированных с сосудистой деменцией. Согласно данному исследованию, дозы композиции, приготовленной из женьшеня, листьев гинкго и рылец шафрана, в лекарстве дополнительно могут быть уменьшены, и, таким образом, могут быть обеспечены экономия энергии и уменьшение стоимости, и дополнительно могут быть уменьшены побочные эффекты, вызванные долгосрочным применением композиции.
Таким образом, задачей настоящего изобретения является обеспечение китайской лекарственной композиции для предотвращения или лечения сердечнососудистого заболевания или деменции с повышенной эффективностью и способа ее получения и применения.
Задача настоящего изобретения решена с помощью следующих технических решений:
Китайская лекарственная композиция для предотвращения или лечения сердечно-сосудистого и цереброваскулярного заболевания или деменции, сырье для получения которой представляет собой лекарственное сырье со следующим массовым соотношением ингредиентов: 1 часть женьшеня, 0,8-1,5 части листьев гинкго, 0,018-0,030 части рылец шафрана.
Предпочтительно, сырье для получения китайской лекарственной композиции представляет собой лекарственное сырье со следующим массовым соотношением ингредиентов: 1 часть женьшеня, 1 часть листьев гинкго, 0,018-0,030 части рылец шафрана.
Более предпочтительно, сырье для получения китайской лекарственной композиции представляет собой лекарственное сырье со следующим массовым соотношением ингредиентов: 1 часть женьшеня, 0,9-1,2 части листьев гинкго, 0,020-0,025 части рылец шафрана.
Еще более предпочтительно, сырье для получения китайской лекарственной композиции представляет собой лекарственное сырье со следующим массовым соотношением ингредиентов: 1 часть женьшеня, 1 часть листьев гинкго, 0,020-0,025 части рылец шафрана.
Наиболее предпочтительно, сырье для получения китайской лекарственной композиции представляет собой лекарственное сырье со следующим массовым соотношением ингредиентов: 1 часть женьшеня, 1 часть листьев гинкго, 0,022 части рылец шафрана.
Согласно настоящему изобретению также предложен способ получения вышеуказанной китайской лекарственной композиции.
Китайская лекарственная композиция согласно настоящему изобретению может быть получена различными способами.
В одном варианте реализации настоящего изобретения взвешивание трех видов китайского лекарственного сырья: женьшеня, листьев гинкго и рылец шафрана в соответствии с вышеуказанным соотношением, смешивание, затем измельчение или измельчение, далее смешивание с получением композиции.
В другом варианте реализации настоящего изобретения взвешивание трех видов китайского лекарственного сырья: женьшеня, листьев гинкго и рылец шафрана в соответствии с вышеуказанным соотношением, смешивание, затем экстрагирование с получением композиции.
В предпочтительном варианте реализации настоящего изобретения способ получения китайской лекарственной композиции включает следующие стадии: стадию взвешивания трех видов китайского лекарственного сырья: женьшеня, листьев гинкго и рылец шафрана в соответствии с вышеуказанным соотношением, стадию получения экстракта женьшеня, стадию получения экстракта листьев гинкго, стадию получения экстракта рылец шафрана, стадию смешивания указанных экстракта женьшеня, экстракта листьев гинкго и экстракта рылец шафрана.
Предпочтительно, на стадии получения экстракта женьшеня основной получаемый компонент представляет собой общую фракцию гинзенозидов; на стадии получения экстракта листьев гинкго основной получаемый компонент представляет собой общую фракцию флавоноидов и общую фракцию лактонов, содержащихся в листьях гинкго; на стадии получения экстракта рылец шафрана основной получаемый компонент представляет собой общую фракцию гликозидов, содержащихся в рыльцах шафрана.
Экстракты трех вышеупомянутых компонентов могут быть получены обычными способами экстракции для экстрагирования вышеуказанных компонентов, способ получения компонентов путем экстракции представляет собой отработанный способ, например, общая фракция гинзенозидов, общая фракция флавоноидов и общая фракция лактонов, содержащихся в листьях гинкго, могут быть получены с применением способов экстракции, описанных в фармакопее, способ экстракции общей фракции гликозидов, содержащихся в рыльцах шафрана, может заимствовать способ экстракции, описанный в литературном источнике «Chinese modern applied Pharmacy» (August 2011, Vol. 28 No. 8, page 729-731).
В одном варианте реализации настоящего изобретения способ получения экстракта женьшеня является следующим: женьшень измельчают в порошок, затем его 2 раза подвергают экстракции с этанолом при нагревании с обратным холодильником, фильтруют, снижают давление в полученном фильтрате с регенерацией растворителя до достижения относительной плотности 1,12-1,14 при 70°С, добавляют воду в количестве, в 2-6 раз превышающем количество неочищенного лекарственного средства, для гомогенного перемешивания, затем смесь охлаждают для осаждения, супернатант наносят на макропористую адсорбирующую смолу, указанную смолу, которая содержит лекарственное средство, сначала промывают дистиллированной водой, затем элюируют этанолом, этанольный элюент собирают и концентрируют досуха с получением экстракта женьшеня.
В одном варианте реализации настоящего изобретения способ получения экстракта листьев гинкго является следующим: к крупнодисперсному порошку листьев гинкго добавляют теплый этанол для обеспечения погружения, порошок фильтруют, и остаток на фильтре погружают в теплый этанол, затем фильтруют, фильтраты, полученные в результате двукратного погружения, объединяют, концентрируют при пониженном давлении до достижения относительной плотности 1,12-1,14 при 70°С, добавляют воду в количестве, в 2-6 раз превышающем количество неочищенного лекарственного средства, смесь перемешивают до гомогенного состояния, затем ее охлаждают для осаждения, фильтруют, фильтрат наносят на макропористую адсорбирующую смолу, указанную смолу, которая содержит лекарственное средство, сначала промывают дистиллированной водой, затем элюируют этанолом, этанольный элюент собирают и концентрируют до достижения относительной плотности 1,02-1,04 при 70°С, его подвергают экстракции смесью этилацетат : н-бутиловый спирт, экстракты объединяют и снижают в них давление с регенерацией растворителя с получением экстракта листьев гинкго.
В одном варианте реализации настоящего изобретения способ получения экстракта рылец шафрана является следующим: к неочищенному лекарственному сырью рылец шафрана добавляют холодный этанол для погружения, затем фильтруют, к остаткам добавляют холодный этанол для погружения, далее фильтруют, фильтраты, полученные в результате двукратного погружения, объединяют, концентрируют при пониженном давлении до достижения относительной плотности 1,12-1,14 при 70°С, добавляют воду, затем смесь наносят на макропористую адсорбирующую смолу, указанную смолу, которая содержит лекарственное средство, сначала промывают дистиллированной водой, затем элюируют этанолом, этанольный элюент концентрируют до достижения относительной плотности 1,02-1,04 при 70°С, его концентрируют досуха с получением экстракта рылец шафрана.
Согласно настоящему изобретению также предложена китайская лекарственная композиция для предотвращения или лечения сердечно-сосудистых и цереброваскулярных заболеваний и/или деменции, которая состоит из вышеуказанной китайской лекарственной композиции и по меньшей мере одного фармацевтически приемлемого вспомогательного вещества.
Состав согласно настоящему изобретению может представлять собой твердый состав или полутвердый состав, жидкий состав или газообразный состав.
Твердый или полутвердый состав выбран из одного из следующих составов: таблетки, пилюли, мази, сублимированные препараты, мелкие порошки, гранулы, суппозитории, порошки, эмульсии, жевательные препараты, капсулы.
Жидкий состав выбран из одного из следующих составов: жидкость для перорального введения, суспензии, сиропы, составы для инъекций, лекарственный раствор и настойки.
Газообразный состав представляет собой аэрозоль или состав для ингаляции.
Согласно настоящему изобретению также предложено применение китайской лекарственной композиции или состава для предотвращения или лечения сердечнососудистых и цереброваскулярных заболеваний и/или деменции.
Предпочтительно, сердечно-сосудистое и цереброваскулярное заболевание выбрано из по меньшей мере одного из следующих заболеваний: ишемического цереброваскулярного заболевания, ишемической болезни сердца или стенокардии.
Предпочтительно, деменция выбрана из сенильной деменции, в частности, сосудистой деменции.
По сравнению с предшествующим уровнем техники китайская лекарственная композиция согласно настоящему изобретению обладает следующими техническими эффектами:
(1) Китайские лекарственные композиции и составы согласно настоящему изобретению более эффективны для предотвращения или лечения сердечнососудистого и цереброваскулярного заболевания или деменции.
(2) В лекарстве используется меньшее количество китайской лекарственной композиции согласно настоящему изобретению, что, таким образом, обеспечивает экономию затрат и энергии.
(3) Побочные эффекты китайской лекарственной композиции согласно настоящему изобретению незначительны, и указанная композиция обладает хорошими характеристиками безопасности, поэтому она может применяться в течение длительного времени и имеет хорошие перспективы для применения в медицине.
ВАРИАНТЫ РЕАЛИЗАЦИИ
Настоящее изобретение далее будет проиллюстрировано с помощью комбинации последующих примеров, сравнительных примеров и соответствующих тестовых примеров, однако эти примеры и тестовые примеры должны использоваться исключительно для иллюстрации настоящего изобретения, но они не ограничивают объем настоящего изобретения. В последующих примерах и тестовых примерах методы проведения эксперимента, описанные без указания конкретных условий эксперимента, были выполнены в соответствии с обычными условиями или в соответствии с условиями, рекомендованными производителями.
Часть 1: Получение китайской лекарственной композиции и состава согласно настоящему изобретению
Пример 1
женьшень 1 часть
листья гинкго 0,8 части
рыльца шафрана 0,018 части
Экстракт женьшеня, экстракт листьев гинкго, экстракт рылец шафрана получали в соответствии со способами, описанными в примере 1 патента ZL 02131435.7, указанные три экстракта смешивали и далее готовили в виде гранул, капсул и препаратов для инъекций в соответствии с обычными способами.
Пример 2
женьшень 1 часть
листья гинкго 1,5 части
рыльца шафрана 0,030 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 1 настоящего изобретения.
Пример 3
женьшень 1 часть
листья гинкго 1 часть
рыльца шафрана 0,018 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 1 настоящего изобретения.
Пример 4
женьшень 1 часть
листья гинкго 1 часть
рыльца шафрана 0,030 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 1 настоящего изобретения.
Пример 5
женьшень 1 часть
листья гинкго 0,9 части
рыльца шафрана 0,020 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 1 настоящего изобретения.
Пример 6
женьшень 1 часть
листья гинкго 1,2 части
рыльца шафрана 0,025 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 1 настоящего изобретения.
Пример 7
женьшень 1 часть
листья гинкго 1 часть
рыльца шафрана 0,20 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 1 настоящего изобретения.
Пример 8
женьшень 1 часть
листья гинкго 1 часть
рыльца шафрана 0,025 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 1 настоящего изобретения.
Пример 9
женьшень 1 часть
листья гинкго 1 часть
рыльца шафрана 0,022 части
Экстракт женьшеня и экстракт листьев гинкго экстрагировали в соответствии со способами, описанными в фармакопее Китая (издание 2010 г., часть первая), стр. 367-368 и стр. 392-393, соответственно, экстракт рылец шафрана экстрагировали в соответствии со способом, описанным в литературном источнике «Chinese modern applied Pharmacy» (August 2011, Vol. 28 No. 8, page 729-731), указанные три экстракта смешивали и далее готовили в виде гранул, капсул и препаратов для инъекций в соответствии с обычными способами.
Пример 10
женьшень 1 часть
листья гинкго 0,8 части
рыльца шафрана 0,030 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 9 настоящего изобретения.
Пример 11
женьшень 1 часть
листья гинкго 1,5 части
рыльца шафрана 0,018 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 9 настоящего изобретения.
Пример 12
женьшень 1 часть
листья гинкго 0,9 части
рыльца шафрана 0,025 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 9 настоящего изобретения.
Пример 13
женьшень 1 часть
листья гинкго 1,2 части
рыльца шафрана 0,02 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 9 настоящего изобретения.
Часть 2: Получение китайской лекарственной композиции и состава согласно сравнительным примерам
Сравнительный пример 1
женьшень 1 часть
листья гинкго 1 часть
рыльца шафрана 0,1 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 1 настоящего изобретения.
Сравнительный пример 2
женьшень 1 часть
листья гинкго 1 часть
рыльца шафрана 0,015 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 1 настоящего изобретения.
Сравнительный пример 3
женьшень 1 часть
листья гинкго 1,5 части
рыльца шафрана 0,4 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 1 настоящего изобретения.
Сравнительный пример 4
женьшень 1 часть
листья гинкго 1,9 части
рыльца шафрана 0,05 части
Смесь экстрактов и препарат получали в соответствии со способами согласно примеру 9 настоящего изобретения.
Сравнительный пример 5
Смесь экстрактов и соответствующий состав получали в соответствии с композицией и способом получения согласно примеру 1 патента ZL 02131435.7.
Сравнительный пример 6
Смесь экстрактов и соответствующий состав получали в соответствии с композицией и способом получения согласно примеру 2 патента ZL 02131435.7.
Сравнительный пример 7
Смесь экстрактов и соответствующие капсулы получали в соответствии с назначением композиции и способом получения согласно примеру 1 заявки WO 2007/118363.
Сравнительный пример 8
Смесь экстрактов и соответствующие капсулы получали в соответствии с назначением композиции согласно примеру 2 заявки WO 2007/118363 и способом получения согласно примеру 1 заявки WO 2007/118363.
Часть 3: Фармакодинамические эксперименты
Тестовый пример 1. Защитное действие на ишемический миокард экспериментальных крыс
Материалы для проведения эксперимента
Здоровые самцы крыс Wastar с массой тела 180~220 г, чистая линия, были предоставлены Центром проведения экспериментов на животных Vital River.
Китайскую лекарственную композицию согласно настоящему изобретению и китайскую лекарственную композицию согласно сравнительным примерам (смесь трех экстрактов была получена самостоятельно в соответствии со способами, описанными в примерах и сравнительных примерах согласно настоящему изобретению) готовили в ходе эксперимента, используя дистиллированную воду, с получением концентрации 0,15 г/мл (расчет на основе исходной дозы китайской лекарственной композиции).
Реагенты: уретан, гидрохлорид изопротеренола, хлорид натрия для инъекций, набор для определения креатинкиназы (КК) и ее изофермента креатинкиназы-МВ (КК-МВ).
Приборы: регистратор физиологических параметров, система сбора физиологического сигнала BL-420, центрифуги, полуавтоматический биохимический анализатор.
Метод проведения эксперимента
а) Формирование групп и создание модели:
Перед исследованием и до введения лекарств осуществляли обследование крыс с помощью ЭКГ, не принимали во внимание сегмент ST, наблюдали аномальные изменения и аномальные сердечные ритмы в зубце Т. Крыс случайным образом разделяли на не получавшую лекарства контрольную группу и модельную группу, по 10 крыс в каждой группе, каждая часть животных получала с помощью желудочного зонда каждый день соответственно следующее: контрольной группе вводили физиологический раствор, группе китайской лекарственной композиции согласно настоящему изобретению (композицию согласно примеру 1, примеру 2, примеру 5, примеру 6, примеру 9, примеру 11 вводили в дозе 3 г/кг/день, дозу рассчитывали на основе исходной дозы женьшеня, листьев гинкго и рылец шафрана), группе композиций согласно сравнительным примерам (при этом лекарства согласно сравнительному примеру 1, сравнительному примеру 2, сравнительному примеру 3, сравнительному примеру 4, сравнительному примеру 5, сравнительному примеру 6 вводили в дозе 3 г/кг/день, дозу рассчитывали на основе исходной дозы женьшеня, листьев гинкго, рылец шафрана; лекарства согласно сравнительному примеру 7, сравнительному примеру 8 вводили в дозе 3 г/кг/день, причем дозу рассчитывали на основе исходной дозы женьшеня, листьев гинкго, рылец шафрана, соевых бобов), лекарства вводили непрерывно в течение 10 дней, на 10-й день, через 30 мин после перфузии, создавали модель в соответствии со следующим способом: крысам из каждой группы вводили посредством внутрибрюшинной инъекции 20% уретан в дозе 5 мл/кг, затем крыс подвергали легкой анестезии, спины крыс фиксировали, вводили гидрохлорид изопротеренола посредством подкожной инъекции с несколькими проколами, нормальной контрольной группе вводили равный объем физиологического раствора, крыс подключали к электрокардиографам, скорость перемещения бумаги составляла 50 см/с, стандартное напряжение составляло 10 мм/мВ, были зарегистрированы изменения ЭКГ после создания модели. Регистрировали ЭКГ, наблюдали изменения сегмента ST. Одно из следующих состояний считали положительным признаком ишемии миокарда: 1) горизонтальная элевация или депрессия сегмента ST≥0,1 мВ; 2) зубец Т выше 1/2 зубца R; 3) высокий зубец Т и смещение сегмента ST. Стандартными отрицательными признаками являлись: 1) косонисходящее или горизонтальное смещение сегмента ST<0,1 мВ; 2) зубец Т сглажен и снижен или двухфазный. Элевацию сегмента ST≥0,1 мВ на ЭКГ крыс в модельной группе считали признаком успешного создания модели.
b) Метод проведения эксперимента:
Лекарства непрерывно вводили в течение 10 дней, через 30 мин после последнего введения с помощью желудочного зонда создавали модель, регистрировали ЭКГ с применением регистратора физиологических параметров непосредственно и через 5 мин, 10 мин, 20 мин, 30 мин до создания модели и после создания модели, и через 6 ч осуществляли забор крови, собирали сыворотку после центрифугирования, проводили анализы уровней КК, КК-МВ.
c) Статистический анализ:
Данные эксперимента выражали как среднее значение ± стандартное отклонение, для статистического анализа использовали t-критерий.
3 Результаты
а) Влияние на смещение точки J
Были обнаружены значительные различия между контрольной группой и модельной группой (Р<0,01); группы китайской лекарственной композиции согласно настоящему изобретению демонстрировали значительные эффекты смещения точки J в различные моменты времени (Р<0,05-0,01) по сравнению с модельной группой, и эффекты китайских лекарственных композиций были лучше, чем для каждой из сравнительных групп. См. таблицу 1.
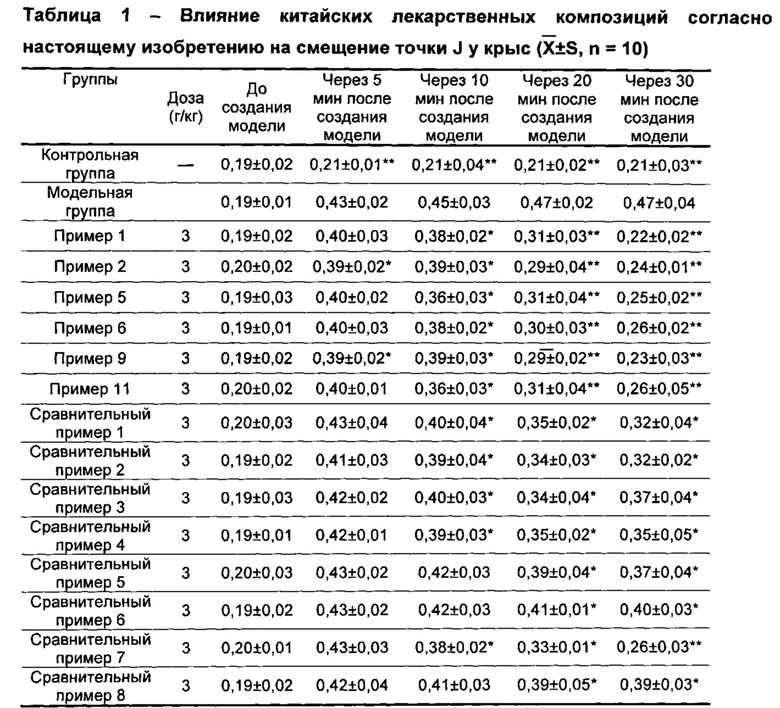
PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
b) Влияние на уровни КК, КК-МВ в сыворотке у крыс с индуцированной изопротеренолом острой ишемией миокарда
Группы китайской лекарственной композиции согласно настоящему изобретению демонстрировали очень значительные различия по сравнению с контрольной группой; по сравнению с модельной группой, уровни креатинкиназы КК, изофермента креатинкиназы КК-МВ через 6 ч после создания модели были значительно снижены; и по сравнению со сравнительной группой эффекты композиций согласно настоящему изобретению были лучшими. Китайские лекарственные композиции согласно настоящему изобретению показали лучший защитный эффект при индуцированном изопротеренолом ишемическом повреждении миокарда у крыс. См. таблицу 2.
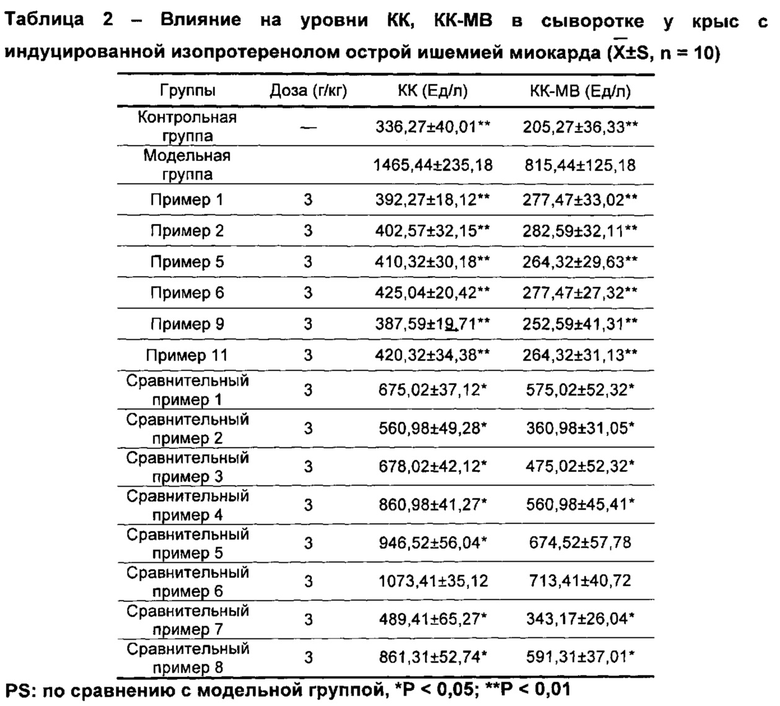
Краткий вывод: ишемия миокарда относится к патологическому состоянию, сопровождающемуся снижением перфузии тканей сердца кровью, что приводит к уменьшению доставки кислорода в ткани сердца, аномальному энергетическому метаболизму миокарда и отсутствию поддержки нормальной работы сердца. Ишемическая болезнь сердца является основной причиной и наиболее распространенной причиной ишемии миокарда. По сравнению с китайскими лекарственными композициями согласно сравнительным примерам, китайские лекарственные композиции согласно настоящему изобретению были способны к значительному смещению точки J у крыс с индуцированной изопротеренолом ишемией миокарда в различные моменты времени (Р<0,05~0,01), были способны к значительному снижению уровней КК, КК-МВ в сыворотке, что свидетельствовало о том, что китайские лекарственные композиции согласно настоящему изобретению обладали значительным защитным эффектом против ишемии миокарда, и их эффекты были лучше, чем аналогичные эффекты китайских лекарственных композиций согласно сравнительным примерам.
Тестовый пример 2. Эксперименты по снижению уровня липидов
Материалы для проведения эксперимента
Мыши Kunming, масса тела 18~22 г, поровну самцы и самки, были предоставлены Центром проведения экспериментов на животных Vital River.
Китайские лекарственные композиции согласно настоящему изобретению и китайские лекарственные композиции согласно сравнительным примерам (смесь соответствующих экстрактов была получена самостоятельно в соответствии со способами, описанными в примерах и сравнительных примерах согласно настоящему изобретению) готовили в ходе эксперимента, используя дистиллированную воду, с получением концентрации 0,2 г/мл (расчет на основе исходной дозы композиции).
Реагенты: набор для определения общего холестерина (ОХ); набор для определения триглицеридов (ТГ).
Приборы: водяная баня-термостат В-260; низкоскоростная центрифуга 80-2В; устройство для прочтения микропланшетов МК3 от компании THERMO LABSYSTEM.
Метод проведения эксперимента
Мышей Kunming случайным образом разделяли на контрольную группу (16), модельную группу, получавшую питание с высоким содержанием жира (16), группы композиций согласно настоящему изобретению (10 в каждой группе), группы композиций согласно сравнительным примерам (10 в каждой группе), в каждой группе самцов и самок было поровну. Нормальная контрольная группа получала обычное питание, другие группы получали питание с высоким содержанием жира (ингредиенты были следующими: 77,5% основное питание, 2% холестерин, 10% свиной жир, 10% сухой яичный желток, 0,5% дезоксихолат натрия). Мышей взвешивали один раз в неделю, питание обеспечивали в течение пяти недель. Через пять недель отбирали случайным образом 3 самок и самцов мышей из нормальной сравнительной группы и группы, получавшей питание с высоким содержанием жира, осуществляли забор крови из глазных яблок, измеряли уровни ОХ и ТГ в сыворотке. Уровни ОХ и ТГ в сыворотке в нормальной сравнительной группе были ниже соответствующих уровней для модельной группы, получавшей питание с высоким содержанием жира, различие результатов было значимым, что свидетельствовало о том, что была создана модель гиперлипидемии на мышах, и указанных мышей можно было применять для формального исследования. Затем мышам из каждой группы вводили в желудок равный объем перфузионного раствора в соответствии с дозой, указанной в таблице 4 (где китайскую лекарственную композицию согласно настоящему изобретению (композицию согласно примеру 1, примеру 2, примеру 5, примеру 6, примеру 9, примеру 11 вводили в дозе 4 г/кг/день, дозу рассчитывали в соответствии с исходной дозой женьшеня, листьев гинкго, рылец шафрана), сравнительная группа (где композицию согласно сравнительному примеру 1, сравнительному примеру 2, сравнительному примеру 3, сравнительному примеру 4, сравнительному примеру 5, сравнительному примеру 6 вводили в дозе 4 г/кг/день, дозу рассчитывали на основе исходной дозы женьшеня, листьев гинкго, рылец шафрана; композицию согласно сравнительному примеру 7, сравнительному примеру 8 вводили в дозе 3 г/кг/день, дозу рассчитывали в соответствии с исходной дозой женьшеня, листьев гинкго, рылец шафрана и соевых бобов). Лекарство для каждой группы готовили в виде суспензии, содержащей 1% карбоксиметилцеллюлозы натрия. После 3 недель введения лекарств всех животных лишали пищи на 12 ч, взвешивали и удаляли их глазные яблоки для забора крови, образцы крови центрифугировали при 3000 об/мин в течение 10 мин, сыворотки отделяли, анализ проводили в соответствии с инструкцией к наборам для определения общего холестерина и триглицеридов, измеряли уровни ОХ и ТГ. Полученные данные обрабатывали с применением программного обеспечения для статистических расчетов SPSS10.0, данные выражали в виде X±S.
Результаты
а) Влияние лекарства для каждой группы на увеличение массы тела мышей, имеющих высокий уровень липидов
В начале эксперимента масса тела мышей в каждой группе составляла примерно 18-20 г, после создания модели с применением питания с высоким содержанием жира в течение пяти недель изменения массы тела мышей в каждой группе были различными. Можно видеть, что: по сравнению с нормальной контрольной группой, изменения массы тела в модельной группе, получавшей питание с высоким содержанием жира, в группах композиций согласно настоящему изобретению и в группах композиций согласно сравнительным примерам значительно увеличивались, после 3 недель введения масса тела животных в модельной группе увеличивалась до наибольшего значения, что указывало на функционирование модельной группы, получавшей питание с высоким содержанием липидов, китайские лекарственные композиции согласно настоящему изобретению и китайские лекарственные композиции согласно сравнительным примерам обладали способностью значительно уменьшать массу тела животных в модельной группе, получавшей питание с высоким содержанием жира (Р<0,05). Также лекарственные композиции согласно настоящему изобретению демонстрировали лучший эффект по снижению массы тела. См. таблицу 3.
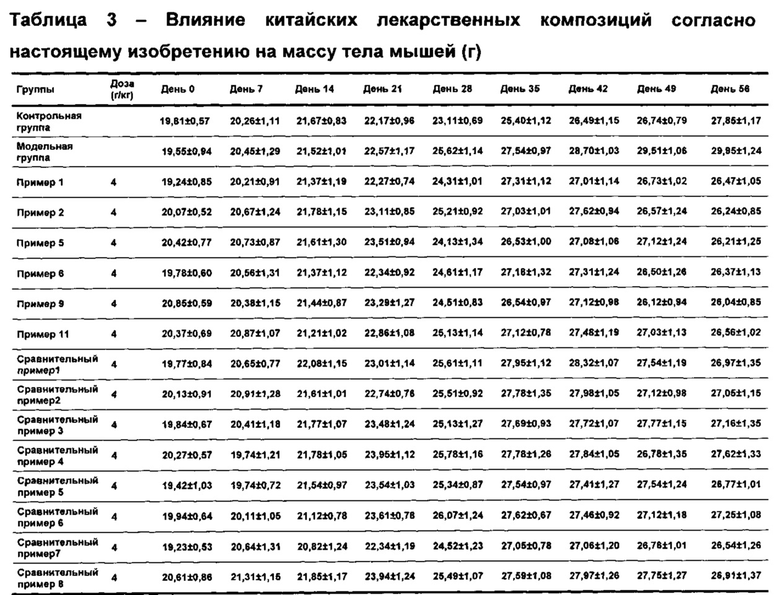
PS: по сравнению с модельной группой, *Р<0,05
b) Влияние лекарства в каждой группе на уровни ОХ, ТГ в сыворотке мышей с гиперлипидемией
После 3 недель введения лекарств измеряли уровни общего холестерина (ОХ) и триглицеридов (ТГ) в сыворотке мышей в каждой группе. Результаты представлены в таблице 4.
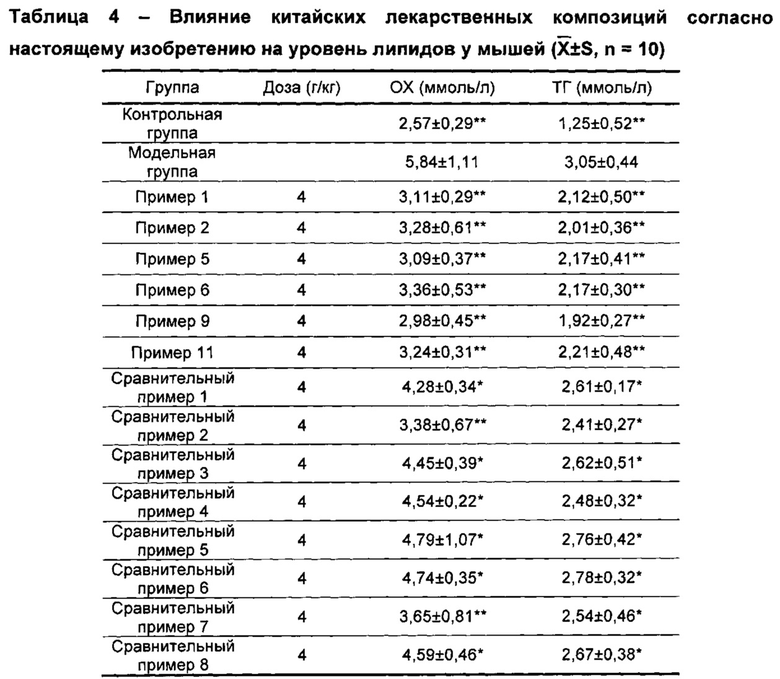
PS: по сравнению с модельной группой, *Р<0,05;**Р<0,01
Из данных таблицы 4 можно видеть, что уровни ОХ и ТГ в модельной группе, получавшей питание с высоким содержанием липидов, были значительно повышены по сравнению с нормальной контрольной группой, что свидетельствовало об успешном создании модели мышей с высоким уровнем липидов. По сравнению с модельной группой, в группах китайских лекарственных композиций согласно настоящему изобретению и в группах композиций согласно сравнительным примерам могло наблюдаться значительное снижение уровней ОХ и ТГ у мышей, а эффекты китайских лекарственных композиций согласно настоящему изобретению были лучше, чем эффекты композиций согласно сравнительным примерам, что указывало на то, что эффекты по снижению уровня липидов для композиций согласно настоящему изобретению были лучше, чем аналогичные эффекты композиций согласно сравнительным примерам.
Краткий вывод: гиперлипидемия ассоциирована с повышенными уровнями холестерина или триглицеридов в плазме. Гиперлипидемия в основном связана с уровнем холестерина, причем повышение уровня холестерина является одним из наиболее важных факторов риска, которые вызывают повышение смертности от сердечно-сосудистых и цереброваскулярных заболеваний, таких как ишемическая болезнь сердца. Дислипидемия, особенно увеличение концентрации холестерина, способна легко приводить к «сгущению крови» и может вызывать образование отложений на стенках сосудов и постепенное образование небольших бляшек (процесс, который мы часто называем «атеросклерозом»), количество и размер этих «бляшек» увеличиваются, что приводит к постепенной закупорке кровеносных сосудов, является причиной замедления кровотока, который может даже прерываться, если ситуация становится серьезной; если эта ситуация возникает в сердце, она вызывает ишемическую болезнь сердца; если она возникает в головном мозге, она вызывает сердечно-сосудистые и цереброваскулярные заболевания, такие как инсульт. По сравнению с модельной группой, китайские лекарственные композиции согласно настоящему изобретению сильно различались по эффекту снижения уровней ОХ и ТГ в сыворотке мышей с гиперлипидемией (**Р<0,01), что свидетельствовало о том, что китайские лекарственные композиции согласно настоящему изобретению демонстрировали лучший эффект для лечения и предотвращения сердечно-сосудистых и цереброваскулярных заболеваний, чем китайские лекарственные композиции согласно сравнительным примерам.
Тестовый пример 3. Эксперимент по снижению уровня глюкозы в крови
Материалы для проведения эксперимента
Мыши Kunming, масса тела 18~22 г, самцы, были предоставлены Центром проведения экспериментов на животных Vital River.
Китайские лекарственные композиции согласно настоящему изобретению и китайские лекарственные композиции согласно сравнительным примерам (смесь соответствующих экстрактов была получена самостоятельно в соответствии со способами, описанными в примерах и сравнительных примерах согласно настоящему изобретению) готовили в ходе эксперимента, используя дистиллированную воду, с получением концентрации 0,2 г/мл (расчет на основе исходной дозы композиции).
Реагенты: аллоксан, набор для определения инсулина посредством радиоиммуноанализа.
Приборы: прибор и входящие в его комплект тест-полоски для определения уровня глюкозы/кетонов в крови, водяная баня-термостат с электрическим нагревом, электронные весы, низкоскоростная центрифуга с охлаждением, счетчик излучения для радиоиммуноанализа.
Метод проведения эксперимента
Получение модельных мышей с диабетом:
Самцы мышей получали адаптивное питание в течение одной недели. 10 животных были выбраны случайным образом в качестве нормального контроля, а остальных мышей лишали пищи (не ограничивая доступ к воде) на 24 часа, готовили свежий раствор 2% аллоксана на физиологическом растворе и вводили посредством внутрибрюшинной инъекции в дозе 200 мг/кг, через 72 часа надрезали хвосты для забора крови и определения уровня глюкозы в крови, мыши с уровнем глюкозы в крови, составляющим 11,1 ммоль/л, являлись модельными мышами с диабетом и были включены в эксперимент.
b) Формирование групп и введение лекарств:
Модельных мышей с диабетом случайным образом разделяли на группы, по 10 в каждой группе. Уровни глюкозы в крови были близкими в данных группах, при этом одна группа представляла собой модельную контрольную группу, 6 групп представляли собой группы композиций согласно настоящему изобретению, 8 групп представляли собой группы композиций согласно сравнительным примерам. Мыши из указанных групп получали соответствующие лекарства с помощью желудочного зонда (дозы были такими же, как в тестовом примере 2), соответствующее количество физиологического раствора вводили нормальной контрольной группе и модельной контрольной группе, регулярно измеряли массу тела для корректировки количества вводимых лекарств, введение лекарств продолжали в течение 21 дня.
c) Определение индикаторов диабета:
В ходе эксперимента хвосты надрезали на 0-й день, 7-й день, 14-й день, 21-й день для забора крови и определения уровня глюкозы в крови. Пероральный тест на толерантность к глюкозе проводили после окончания введения лекарств с помощью желудочного зонда и определения уровня глюкозы в крови, мышам вводили глюкозу посредством перфузии в дозе 2,5 г/кг и определяли уровень глюкозы в крови через 0 мин, 30 мин, 60 мин, 120 мин. На 22-й день забирали кровь из глазницы мышей, сыворотку отделяли при 4°С, центрифугировали в течение 10 мин при 3000 об/мин, измеряли уровень инсулина в сыворотке в соответствии с инструкцией к наборам.
Данные эксперимента подвергали статистическому анализу с применением программного обеспечения SPSS, результаты определения индикаторов диабета выражали как среднее значение ± стандартное отклонение, сравнение между двумя группами выполняли с применением t-критерия.
Результаты
а) Влияние на уровень глюкозы в крови у модельных мышей с индуцированной аллоксаном гипергликемией
После инъекции аллоксана уровень глюкозы в крови мышей был значительно повышен, уровень глюкозы в крови мышей, которым вводили аллоксан в течение 7 дней и 14 дней, был высоким и сильно отличался от нормальной группы, что указывало на успешное создание модели индуцированного аллоксаном диабета, и уровень глюкозы в крови этих мышей оставался высоким в течение эксперимента. Через 7 дней после введения аллоксана уровень глюкозы в крови мышей, которым вводили лекарства, начинал снижаться, после введения лекарств в течение 14 дней уровень глюкозы в крови мышей из группы композиций согласно настоящему изобретению значительно снижался по сравнению с модельной группой, полученные различия были значимыми. После введения лекарств с помощью желудочного зонда в течение 21 дня результаты для групп композиций согласно настоящему изобретению значительно отличались (Р<0,01), результаты для групп композиций согласно сравнительным примерам значительно отличались (Р<0,05). Данные результаты показали, что композиции согласно настоящему изобретению обладали лучшим эффектом снижения уровня глюкозы в крови, и эффект снижения уровня глюкозы в крови для композиций согласно настоящему изобретению был лучше, чем аналогичный эффект в группе композиций согласно сравнительным примерам.
Тест на толерантность к глюкозе показал, что китайские лекарственные композиции согласно настоящему изобретению в значительной степени улучшали толерантность экспериментальных мышей к глюкозе (Р<0,01), композиции согласно сравнительным примерам были способны значительно улучшать толерантность экспериментальных мышей к глюкозе (Р<0,05). Результаты позволили предположить, что эффект снижения уровня глюкозы в крови для китайских лекарственных композиций согласно настоящему изобретению был лучше, чем аналогичный эффект в сравнительных группах. См. таблицу 5.
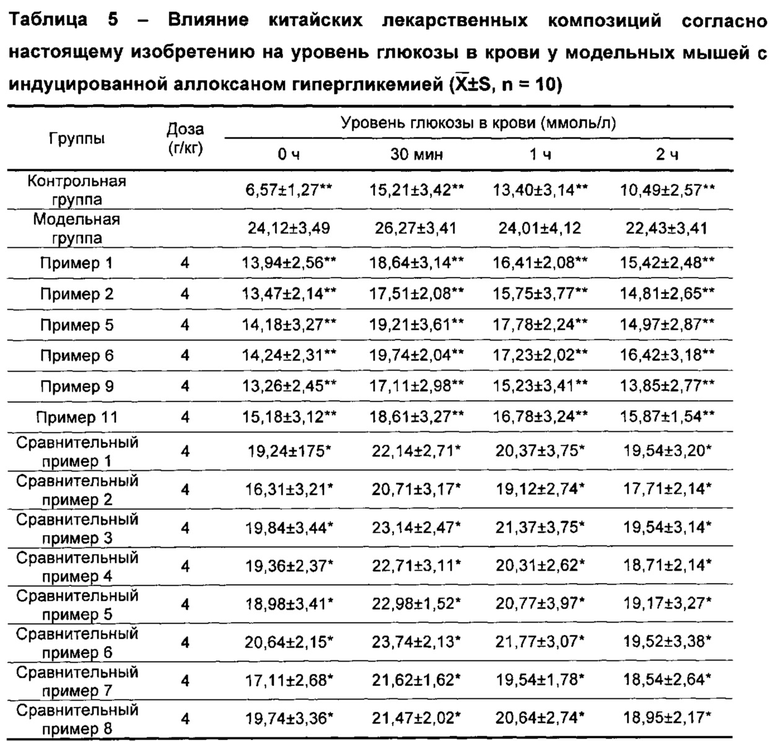
PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
b) Влияние на уровень инсулина в сыворотке у модельных мышей с индуцированным аллоксаном диабетом
По сравнению с нормальными парами, уровень инсулина в сыворотке модельных мышей был значительно снижен, что указывало на нарушение функции В-клеток этих мышей после внутрибрюшинной инъекции аллоксана, и это свидетельствовало об успешном создании модели; по сравнению с модельной группой, уровни инсулина в сыворотке в группе китайских лекарственных композиций согласно настоящему изобретению и в группе композиций согласно сравнительным примерам были повышены в различной степени, причем результаты для групп китайских лекарственных композиций согласно настоящему изобретению имели очень значительные отличия (Р<0,01), тогда как результаты для групп композиций согласно сравнительным примерам 1, 2, 4, 7, 8, имели значительные отличия (Р<0,05), в группах композиций согласно другим сравнительным примерам уровни инсулина в сыворотке были повышены, но результаты не были статистически значимыми, что позволило предположить, что для композиций согласно настоящему изобретению эффект повышения уровня инсулина в сыворотке у мышей с индуцированным аллоксаном диабетом был лучше, чем аналогичный эффект в группе композиций согласно сравнительным примерам. Результаты представлены в таблице 6.
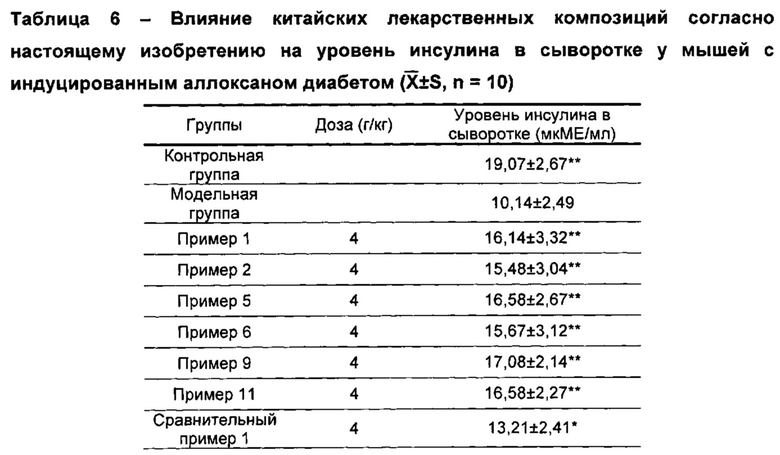
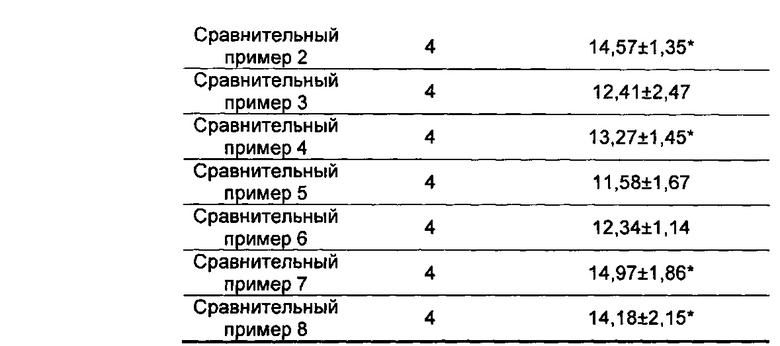
PS: по сравнению с модельной группой, *Р<0,05, **Р<0,01
Краткий вывод: в результате повышения уровня жизни людей и воздействия факторов окружающей среды, аномальный метаболизм глюкозы все чаще появляется у пациентов с сердечно-сосудистыми и цереброваскулярными заболеваниями, если у пациентов с такими заболеваниями одновременно наблюдается аномальный метаболизм глюкозы, прогноз развития их состояния может быть неблагоприятным. Риски рецидива инфаркта миокарда у больных диабетом, которые однажды перенесли инфаркт миокарда, превышают 40%. Кроме того, аномальный уровень глюкозы может вызывать патологический процесс, такой как эндотелиальная дисфункция, уменьшение эластичности аорты, гипертрофия левого желудочка, образование атеросклеротических бляшек в сонной артерии, микроальбуминурия, и в конечном итоге приводить к развитию атеросклероза. Китайские лекарственные композиции согласно настоящему изобретению могут значительно снижать уровень глюкозы в крови модельных мышей с индуцированной аллоксаном гипергликемией, улучшать уровень инсулина в сыворотке мышей с индуцированным аллоксаном диабетом, что указывает на то, что китайские лекарственные композиции согласно настоящему изобретению обладают полезным эффектом для лечения и предотвращения сердечно-сосудистых и цереброваскулярных заболеваний.
Тестовый пример 4. Исследование антитромботической активности
1. Материалы для проведения эксперимента
Крысы Спрег-Доули (SD), масса тела 180,0-220,0 г, самцы и самки, были предоставлены Центром проведения экспериментов на животных Vital River, крысы получали адаптивное питание в течение недели при содержании в виварии (с контролем температуры) перед проведением эксперимента.
Китайские лекарственные композиции согласно настоящему изобретению и китайские лекарственные композиции согласно сравнительным примерам (смесь соответствующих экстрактов была получена самостоятельно в соответствии со способами, описанными в примерах и сравнительных примерах согласно настоящему изобретению) готовили в ходе эксперимента, используя дистиллированную воду, с получением концентрации 0,15 г/мл (расчет на основе исходной дозы композиции).
Аспирин: белые таблетки, 50 мг/шт., был предоставлен компанией Shanghai Branch группы компаний China Pharmaceutical. Пентобарбитал натрия: белый порошок, предоставленный компанией Shanghai Chemical Reagent (группа компаний China Pharmaceutical), был приготовлен в виде 0,8% водного раствора на физиологическом растворе для использования в качестве стокового раствора. Гепарин: белый порошок, 125 ед/мг, предоставленный компанией Shanghai Chemical Reagent (группа компаний China Pharmaceutical), был приготовлен в виде 0,1% раствора на физиологическом растворе для использования в качестве стокового раствора. Цитрат натрия: был предоставлен компанией China Pharmaceutical Industry, фабрика Southwest Pharmaceutical, был приготовлен в виде 3,8% раствора на физиологическом растворе. АДФ: производство компании Sigma, был приготовлен в виде раствора с концентрацией 200 мкмоль/л на фосфатном буфере, рН 7,4 для использования в качестве стокового раствора.
Устройство для подсчета тромбоцитов MK4/НС (производство компании USA Baker Instruments), двухканальное устройство для измерения агрегации тромбоцитов Labor aggregometer-153 (компания German Labor GmbHHanburg).
2. Метод проведения эксперимента
Крыс случайным образом разделяли на группы, каждая из которых состояла из 15 крыс, а именно, не получавшую лекарств контрольную группу, группу аспирина (измельчали и готовили в виде суспензии с концентрацией 0,88 мг/мл в 1% растворе карбоксиметилцеллюлозы натрия (CMC-Na), вводили в дозе 0,0044 г/кг/день), группы китайских лекарственных композиций согласно настоящему изобретению (6 групп, дозы были такими же, как в тестовом примере 1), группы композиций согласно сравнительным примерам (8 групп, дозы были такими же, как в тестовом примере 1). Равный объем физиологического раствора вводили не получавшей лекарств контрольной группе. Введение осуществляли один раз в день в течение 7 дней.
Эксперименты по тромбообразованию in vivo: через 1 ч после введения в течение 7 дней крыс из указанных групп подвергали наркозу с помощью внутрибрюшинной инъекции, содержащей 0,8% пентобарбитал натрия в дозе 40 мг/кг в соответствии со способом моделирования тромбообразования, включающим применение артериовенозного шунта [Zhang Jun Tian. Modern pharmacology experimental methods. Beijing: Beijing Medical University Press, 1998; 1216-1217], разделяли правую общую сонную артерию и левую наружную яремную вену. Брали три секции полиэтиленовой пластиковой трубки, диаметр средней секции составлял 2 мм, длина составляла примерно 8,5 см, диаметр двух пластиковых трубок с двух концов составлял 1,5 мм, длина составляла 10 см, соответственно. Взвешенную ранее хирургическую шелковую нить №4 длиной примерно 7 см помещали в пластиковую трубку в средней части, при этом один конец нити длиной 0,5 см выставляли в трубку для фиксации положения нити, и шелковую нить длиной 6,5 см оставляли в трубке, указанную полиэтиленовую пластиковую трубку заполняли раствором гепарина, один конец пластиковой трубки вставляли в левую наружную яремную вену, другой конец пластиковой трубки вставляли в правую общую сонную артерию, тогда сразу начинался ток крови. Через 20 минут после начала тока крови указанный ток быстро прекращали и быстро извлекали шелковую нить из средней части, шелк взвешивали и указанную массу считали общей массой. Разность общей массы и массы нити составляла массу влажного тромба. Скорость ингибирования тромбоза рассчитывали по следующей формуле:
Скорость ингибирования = (масса влажного тромба в контрольной группе - масса влажного тромба в экспериментальной группе) / масса влажного тромба в контрольной группе × 100%. Массу влажного тромба в каждой группе оценивали статистически.
Тест ингибирования агрегации тромбоцитов: через 1 ч после 7 дней введения крысам, разделенным на группы, крыс подвергали наркозу в соответствии с указанным выше способом, в общую сонную артерию вводили трубку для сбора крови, в кровь добавляли 3,8% цитрата натрия в качестве антикоагулянта в отношении 1:9, проводили центрифугирование в течение 5 минут при 500 об/мин, верхнюю часть плазмы отбирали в качестве обогащенной тромбоцитами плазмы (англ.: platelet-rich plasma, PRP), оставшуюся часть снова центрифугировали в течение 15 минут при 3500 об/мин, супернатант представлял собой обедненную тромбоцитами плазму (англ.: platelet poor plasma, РРР), количество тромбоцитов в PRP подсчитывали с помощью прибора для подсчета тромбоцитов, количество тромбоцитов PRP регулировали с помощью РРР до примерно 3×105/мм2. Температуру пробирки для образцов поддерживали на уровне 37°С в течение 3 минут, затем добавляли 5 мкл АДФ (конечная концентрация 5 мкмоль/л), скорость перемешивания мешалки составляла 500 об/мин, отмечали пространство между рядами движения записывающего пера после добавления, и скорость агрегации рассчитывали по следующей формуле:
Скорость агрегации (%) = путь при добавлении АДФ × 100% / 0 ~ 100% пути.
Для каждой экспериментальной группы вычисляли средние скорости накопления и стандартные отклонения, а скорости ингибирования агрегации тромбоцитов для каждой экспериментальной группы рассчитывали по следующей формуле:
Степень ингибирования агрегации (%) = (скорость агрегации в контрольной группе - скорость агрегации в экспериментальной группе) / скорость агрегации в контрольной группе × 100%.
3. Результаты
а) Влияние на экспериментальное тромбообразование
По сравнению с не получавшей лекарств контрольной группой, в группах, которые получали лекарства, наблюдали значительные эффекты ингибирования тромбообразования по сравнению с контрольной группой, массы влажных тромбов у крыс из групп китайской лекарственной композиции согласно настоящему изобретению и групп китайских лекарственных композиций согласно сравнительному примеру 2 и примеру 7 значительно отличались (Р<0,01), массы влажных тромбов у крыс из групп китайских лекарственных композиций согласно сравнительному примеру 1, сравнительному примеру 3, сравнительному примеру 4, сравнительному примеру 5, сравнительному примеру 6 и сравнительному примеру 8 (Р<0,05) значительно отличались (Р<0,05), что указывало на то, что эффекты ингибирования тромбообразования у крыс, получавших китайскую лекарственную композицию согласно настоящему изобретению, были лучше, чем аналогичные эффекты в группе композиций согласно сравнительным примерам. Результаты представлены в таблице 7.
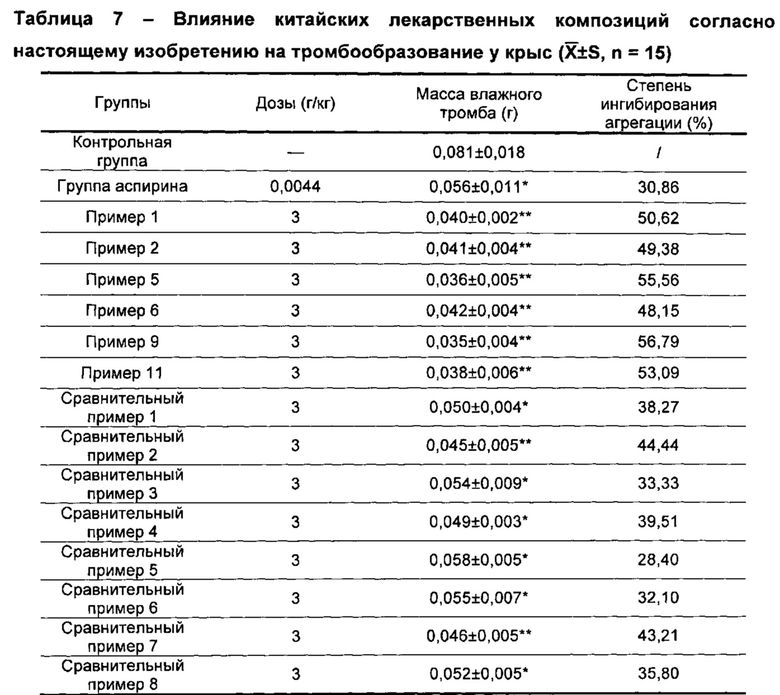
PS: по сравнению с контрольной группой, *Р<0,05; **Р<0,01
(2) Влияние на агрегацию тромбоцитов
В процессе эксперимента количество тромбоцитов в образцах крови, собранных в исследуемых группах животных, составляло примерно 3×105/мм2, значимого отличия обнаружено не было. Результаты представлены в таблице 8.
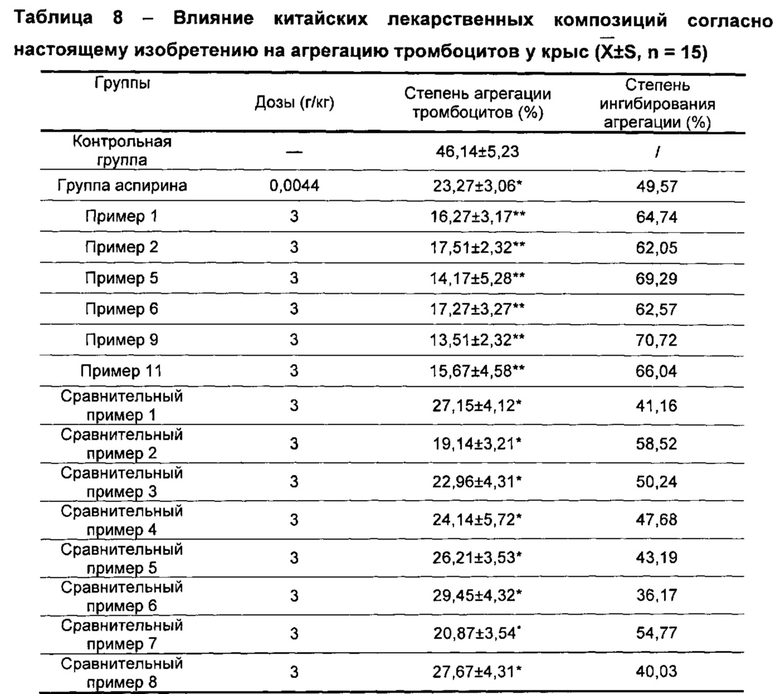
PS: по сравнению с контрольной группой, *Р<0,05; **Р<0,01
Из приведенной выше таблицы можно видеть, что, по сравнению с не получавшей лекарств контрольной группой, в группах, которые получали лекарства, наблюдали ингибирование АДФ-индуцированной агрегации тромбоцитов у крыс. Значения степени ингибирования агрегации в группах китайских лекарственных композиций согласно настоящему изобретению (по сравнению с контрольной группой, **Р<0,01) были выше, чем в группах композиций согласно сравнительным примерам (по сравнению с контрольной группой *Р<0,05), что указывало на то, что эффекты, противодействующие агрегации тромбоцитов, в группах китайских лекарственных композиций согласно настоящему изобретению были лучше, чем аналогичные эффекты в группах композиций согласно сравнительным примерам.
Краткий вывод: тромбообразование представляет собой агрегацию некоторых компонентов крови с образованием сгустков, которая влияет на кровоток. Причинами появления тромбов являются, в основном, изменение компонентного состава крови, повреждение эндотелия сосудов и изменение скорости кровотока. Тромбы могут блокировать коронарные кровеносные сосуды, что приводит к резкому снижению или прерыванию кровотока, которое вызывает тяжелую и стойкую острую ишемию соответствующих сердечных мышц, приводящую к ишемическому некрозу миокарда; кроме того, некоторые части кровеносных сосудов головного мозга подвержены спонтанному тромбозу, что приводит к блокированию кровеносных сосудов головного мозга, недостаточному кровообращению, образованию «мозгового тромба», после тромбоза сосудов головного мозга тромбы отрываются и затем вызывают блокирование кровеносных сосудов и, таким образом, приводят к церебральному инфаркту. По сравнению с китайскими лекарственными композициями согласно сравнительным примерам, китайские лекарственные композиции согласно настоящему изобретению обладали лучшим эффектом уменьшения размера тромба, ингибирования тромбообразования и снижения степени агрегации тромбоцитов, что позволило предположить, что китайские лекарственные композиции согласно настоящему изобретению обладали лучшими эффектами для лечения и предотвращения сердечно-сосудистых и цереброваскулярных заболеваний.
Тестовый пример 5. Влияние на индуцированное скополамина гидробромидом приобретенное нарушение памяти в модели на мышах
1. Материалы для проведения эксперимента
Мыши ICR, 18-22 г, поровну самцы и самки, были предоставлены Beijing Vital River Laboratory Animal Technology Development Company Ltd.
Китайские лекарственные композиции согласно настоящему изобретению и китайские лекарственные композиции согласно сравнительным примерам (смесь соответствующих экстрактов была получена самостоятельно в соответствии со способами, описанными в примерах и сравнительных примерах согласно настоящему изобретению) готовили в ходе эксперимента, используя дистиллированную воду, с получением концентрации 0,2 г/мл (расчет на основе исходной дозы композиции).
Гуперзин (таблетки гуперзина А), 50 мкг/шт., были произведены компанией Henan Zhu Lin Zhong Sheng Pharmaceutical Co., Ltd., и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 4 мкг/мл; таблетки танакана (танакан), стандартизованный экстракт листьев гинкго (Egb761), 40 мг/таблетка, были произведены компанией France Beaufort - Ipsen pharmaceutical industry Co., Ltd., и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 1,5 мг/мл; скополамина гидробромид, 0,6 мг/мл, был произведен компанией Shanghai Hefeng pharmaceutical Co.
Автоматический программируемый регулятор прыжков для мышей ТТ-2, разработанный в Институте фармакологии Китайской академии медицинских наук.
2. Метод проведения эксперимента
Животных, самцов и самок поровну, случайным образом разделяли на группы: не получавшую лекарств контрольную группу, модельную группу, группу, получавшую гуперзин в дозе 0,08 мг/кг, группу, получавшую танакан в дозе 30 мг/кг, группы китайских лекарственных композиций согласно настоящему изобретению (6 групп, дозы были такими же, как в тестовом примере 2), группы композиций согласно сравнительным примерам (8 групп, дозы были такими же, как в тестовом примере 2).
Животным вводили лекарства внутрижелудочно один раз в день в дозе 20 мл/кг, не получавшей лекарств контрольной группе и модельной группе вводили дистиллированную воду один раз в день, введение продолжали в течение 15 дней, через 50 минут после введения на 14-й день мышам из не получавшей лекарств контрольной группы вводили физиологический раствор посредством внутрибрюшинной инъекции в объеме 10 мл/кг, остальным животным вводили скополамин посредством инъекции (6 мг/кг). Через 10 минут мышей помещали на автоматический программируемый регулятор прыжков для адаптации в течение 3 минут, затем включали питание, мышей стимулировали электрошоком 5 раз, когда мышей стимулировали, они прыгали на погружную платформу, чтобы избежать электрошока, мышей обучали в течение 5 минут для приобретения памяти. Через 60 минут после введения на 15-й день животных помещали на автоматический программируемый регулятор прыжков, определяли количество раз, которое мыши покидали платформу для прыжков и получали электрошок (количество ошибок), и время покидания платформы (инкубационный период). Результаты анализировали с применением статистического метода (t-критерий). См. таблицу 9.
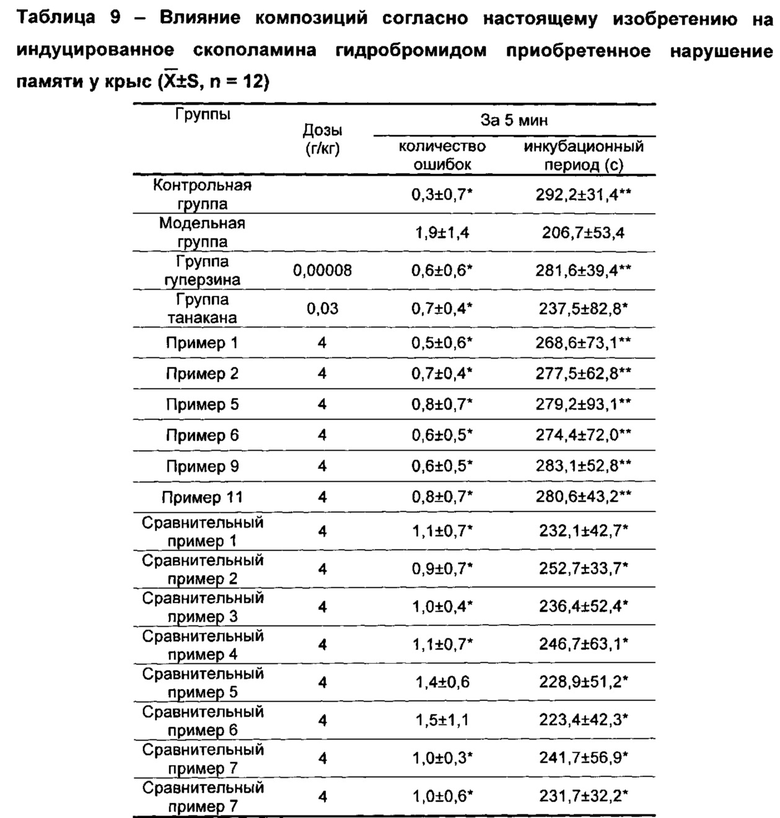
PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
Результаты: по сравнению с модельной группой, количество ошибок за 5 минут у мышей из не получавшей лекарств контрольной группы было значительно уменьшено (Р<0,05), инкубационный период был значительно увеличен (Р<0,01), что свидетельствовало об успешном создании моделей. По сравнению с модельной группой, количество ошибок за 5 минут у мышей из группы гуперзина было значительно уменьшено (Р<0,05), инкубационный период был значительно увеличен (Р<0,01); количество ошибок за 5 минут у мышей из групп китайских лекарственных композиций согласно настоящему изобретению было значительно уменьшено (Р<0,05), инкубационные периоды были значительно увеличены (Р<0,01); количество ошибок за 5 минут у мышей из группы танакана и групп китайских лекарственных композиций согласно сравнительным примерам 1-4, 7, 8 было значительно уменьшено (Р<0,05), инкубационные периоды были значительно увеличены (Р<0,01). Количество ошибок в группах китайских лекарственных композиций согласно сравнительным примерам 5, 6 имели тенденцию к уменьшению, а инкубационные периоды для указанных групп имели тенденцию к увеличению, результаты не были статистическая значимыми.
Краткий вывод: перед обучением мышам вводили антагонист М-рецептора скополамина, который может вызывать снижение содержания ацетилхолина в головном мозге, что вызывает приобретенное нарушение памяти. В данном эксперименте тест с применением платформы выполняли с расчетом на это химическое повреждение, при этом в качестве индикаторов нарушения памяти использовали количество ошибок у мышей за 5 минут и инкубационные периоды, наблюдали эффекты композиций согласно настоящему изобретению и композиций согласно сравнительным примерам на созданной модели. Результаты показали, что китайские лекарственные композиции согласно настоящему изобретению значительно облегчали индуцированные скополамином приобретенные нарушения памяти у мышей, причем эффекты были лучше, чем в сравнительных группах, что позволило предположить, что китайские лекарственные композиции согласно настоящему изобретению могли обладать эффектами повышения содержания ацетилхолина в головном мозге, и эти эффекты были выражены сильнее, чем аналогичные эффекты в сравнительных группах.
Тестовый пример 6. Влияние на индуцированное резерпином приобретенное нарушение памяти в модели на мышах
1. Материалы для проведения эксперимента
Мыши ICR, 25-32 г, поровну самцы и самки, были предоставлены Beijing Vital River Laboratory Animal Technology Development Company Ltd.
Китайские лекарственные композиции согласно настоящему изобретению и китайские лекарственные композиции согласно сравнительным примерам (смесь соответствующих экстрактов была получена самостоятельно в соответствии со способами, описанными в примерах и сравнительных примерах согласно настоящему изобретению) готовили в ходе эксперимента, используя дистиллированную воду, с получением концентрации 0,2 г/мл (расчет на основе исходной дозы композиции).
Гуперзин (таблетки гуперзина А), 50 мкг/шт., были произведены компанией Henan Zhu Lin Zhong Sheng Pharmaceutical Co., Ltd., и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 4 мкг/мл; таблетки танакана (танакан), стандартизованный экстракт листьев гинкго (Egb761), 40 мг/таблетка, были произведены компанией France Beaufort - Ipsen pharmaceutical industry Co., Ltd., и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 1,5 мг/мл; резерпин для инъекций, 1 мг/мл, фармацевтическая фабрика Hong Qi Шанхайского медицинского университета, и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 0,05 мг/мл.
Автоматический программируемый регулятор прыжков для мышей ТТ-2, разработанный в Институте фармакологии Китайской академии медицинских наук.
2. Метод проведения эксперимента.
Экспериментальные группы были такими же, как в тестовом примере 5.
Животным вводили лекарства внутрижелудочно один раз в день в дозе 20 мл/кг, не получавшей лекарств контрольне группе, и модельной группе вводили дистиллированную воду один раз в день, введение продолжали в течение 15 дней. После введения на 14-й день мышам из не получавшей лекарств контрольной группы незамедлительно вводили физиологический раствор посредством подкожной инъекции в область спины и шеи в объеме 10 мл/кг, остальные животные получали гидрохлорид резерпина (0,5 мг/кг) посредством подкожной инъекции в область спины и шеи. Через 60 минут после инъекции мышей помещали на автоматический программируемый регулятор прыжков для адаптации в течение 3 минут, затем включали питание, мышей стимулировали электрошоком 5 раз, когда мышей стимулировали, они прыгали на погружную платформу, чтобы избежать электрошока, мышей обучали в течение 5 минут для приобретения памяти. Через 60 минут после введения на 15-й день животных помещали на автоматический программируемый регулятор прыжков, определяли количество ошибок и инкубационный период для мышей за 5 минут. Результаты анализировали с применением статистического метода (t-критерий).
3. Результаты
По сравнению с модельной группой количество ошибок за 5 минут у мышей из не получавшей лекарств контрольной группы было значительно уменьшено (Р<0,05), инкубационный период был значительно увеличен (Р<0,01), что свидетельствовало об успешном создании модели. По сравнению с модельной группой, количество ошибок за 5 минут у мышей из группы китайских лекарственных композиций согласно настоящему изобретению было значительно уменьшено (Р<0,05), инкубационный период был значительно увеличен (Р<0,05). Количество ошибок за 5 минут у мышей из группы, получавшей лекарства согласно сравнительным примерам, группы гуперзина и группы танакана было значительно уменьшено (Р<0,05), инкубационный период имел тенденцию к увеличению, однако результаты не были статистически значимыми. См. таблицу 10.
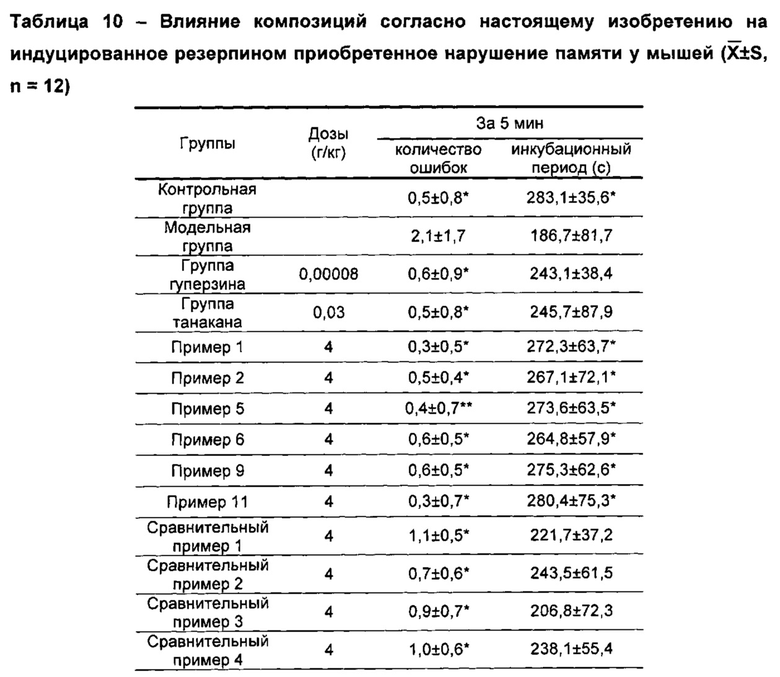

PS: по сравнению с модельной группой, Р<0,05; **Р<0,01
Краткий вывод: данное исследование подтвердило, что резерпин может вызывать дефицит моноаминового нейромедиатора в головном мозге, нарушать процесс запоминания и обучения, введение мышам резерпина до обучения может вызывать у них нарушение памяти, касающееся получения или сохранения информации. Количество ошибок и инкубационный период за 5 минут использовали в качестве индикатора для настоящего эксперимента, наблюдали эффекты китайских лекарственных композиций согласно настоящему изобретению и композиций согласно сравнительным примерам на созданной модели. После введения мышам с помощью желудочного зонда китайских лекарственных композиций согласно настоящему изобретению и композиций согласно сравнительным примерам, два вышеуказанных индикатора улучшались в различной степени, и улучшения в группах китайских лекарственных композиций согласно настоящему изобретению были намного лучше, чем в группах композиций согласно сравнительным примерам, что указывало на то, что китайские лекарственные композиции согласно настоящему изобретению обладали эффектами облегчения приобретенного нарушения памяти у животных, это позволило предположить, что данные эффекты связаны с механизмом, заключающимся в том, что китайские лекарственные композиции согласно настоящему изобретению могли увеличивать содержание катехоламинового нейромедиатора, и эффекты китайских лекарственных композиций согласно настоящему изобретению были лучше, чем аналогичные эффекты композиций согласно сравнительным примерам.
Тестовый пример 7. Влияние на индуцированное нитритом натрия приобретенное нарушение консолидированной памяти в модели на мышах
1. Материалы для проведения эксперимента
Мыши ICR, 18-22 г, поровну самцы и самки, были предоставлены Beijing Vital River Laboratory Animal Technology Development Company Ltd.
Китайские лекарственные композиции согласно настоящему изобретению и китайские лекарственные композиции согласно сравнительным примерам (смесь соответствующих экстрактов была получена самостоятельно в соответствии со способами, описанными в примерах и сравнительных примерах согласно настоящему изобретению) готовили в ходе эксперимента, используя дистиллированную воду, с получением концентрации 0,2 г/мл (расчет на основе исходной дозы композиции).
Гуперзин (таблетки гуперзина А), 50 мкг/шт., были произведены компанией Henan Zhu Lin Zhong Sheng Pharmaceutical Co., Ltd., и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 4 мкг/мл; таблетки танакана (танакан), стандартизованный экстракт листьев гинкго (Egb761), 40 мг/таблетка, были произведены компанией France Beaufort - Ipsen pharmaceutical industry Co., Ltd., и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 1,5 мг/мл; нитрит натрия, был произведен компанией Beijing Yili fine chemicals Co., и с помощью дистиллированной воды в ходе эксперимента была получена его дозировка 12 мг/мл.
Автоматический программируемый регулятор прыжков для мышей ТТ-2, разработанный в Институте фармакологии Китайской академии медицинских наук.
2. Метод проведения эксперимента
Экспериментальные группы были такими же, как в тестовом примере 5.
Животным вводили лекарства внутрижелудочно один раз в день в дозе 20 мл/кг, животным из не получавшей лекарств контрольной группы и модельной группы вводили дистиллированную воду один раз в день, введение продолжали в течение 15 дней. Через 60 минут после введения на 14-й день мышей помещали на автоматический программируемый регулятор прыжков для адаптации в течение 5 минут, и мышей стимулировали электрошоком 5 раз. После обработки мышам из сравнительной группы незамедлительно вводили физиологический раствор посредством подкожной инъекции в область спины и шеи в объеме 10 мл/кг, остальным животным вводили посредством инъекции нитрит натрия (120 мг/кг). Через 60 минут после введения на 15-й день животных из ислледуемых групп помещали на автоматический программируемый регулятор прыжков, определяли количество ошибок и инкубационный период за 5 мин. Результаты анализировали с применением статистического метода (t-критерий).
3. Результаты
По сравнению с модельной группой, количество ошибок у мышей из не получавшей лекарств контрольной группы за 5 минут было значительно уменьшено (Р<0,05), инкубационный период был значительно увеличен (Р<0,01), что свидетельствовало об успешном создании моделей. По сравнению с модельной группой, количество ошибок за 5 минут у мышей из группы китайских лекарственных композиций согласно настоящему изобретению, группы гуперзина и группы танакана было значительно уменьшено (Р<0,05), инкубационный период был значительно увеличен (Р<0,01~0,05). Количество ошибок за 5 минут у мышей из группы китайской лекарственной композиции согласно сравнительному примеру 7 было значительно уменьшено (Р<0,05), инкубационный период был значительно увеличен (Р<0,05). Количество ошибок за 5 минут у мышей из группы китайской лекарственной композиции согласно сравнительному примеру 2 было значительно уменьшено (Р<0,05), инкубационный период имел тенденцию к увеличению, однако результаты не были статистически значимыми. Количество ошибок в других сравнительных группах имело тенденции к уменьшению, инкубационный период имел тенденцию к увеличению, результаты не были статистически значимыми. Результаты представлены в таблице 11.
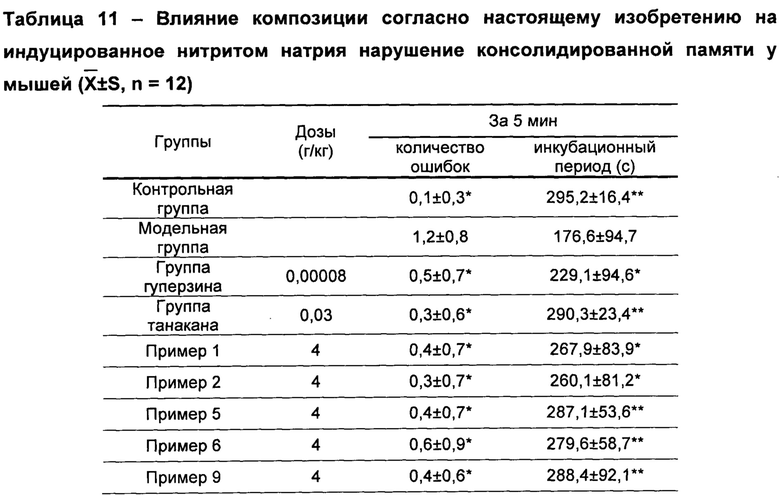
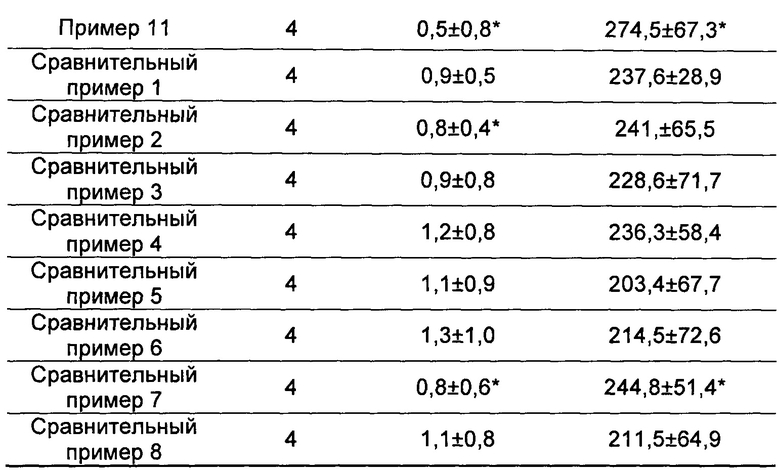
PS: по сравнению с модельной группой *Р<0,05; **Р<0,01
Данное исследование подтвердило, что нитрит натрия может вызывать денатурацию гемоглобина, что приводит к ишемии и гипоксии тканей головного мозга, нарушает процесс обучения и запоминания, введение мышам нитрита натрия незамедлительно после обучения вызывало у мышей нарушение консолидированной памяти или нарушение сохранения информации. Принимая во внимание это химическое повреждение, используя количество ошибок и инкубационный период в качестве индикаторов для настоящего эксперимента, наблюдали эффекты композиций согласно настоящему изобретению и композиций согласно сравнительным примерам на созданных моделях. После введения мышам с помощью желудочного зонда композиций согласно настоящему изобретению и композиций согласно сравнительным примерам, два вышеуказанных индикатора улучшались в различной степени, и улучшения в группах композиций согласно настоящему изобретению были намного лучше, чем в группах композиций согласно сравнительным примерам, что указывало на то, что композиции согласно настоящему изобретению обладали эффектами облегчения нарушения консолидированной памяти у животных, это позволило предположить, что китайские лекарственные композиции согласно настоящему изобретению могут улучшать процесс запоминания путем улучшения мозгового кровотока и облегчения ишемии и гипоксии тканей головного мозга, и эффекты китайских лекарственных композиций согласно настоящему изобретению были лучше, чем аналогичные эффекты композиций согласно сравнительным примерам.
Тестовый пример 8. Влияние на СД, вызванное постоянной перевязкой двусторонней общей сонной артерии крыс
1. Материалы для проведения эксперимента
(1) Животные: крысы SD, масса тела 250~270 г, самцы, были предоставлены Beijing Vital River Laboratory Animal Technology Development Company Ltd.
(2) Лекарства:
Китайские лекарственные композиции согласно настоящему изобретению и китайские лекарственные композиции согласно сравнительным примерам (смесь соответствующих экстрактов была получена самостоятельно в соответствии со способами, описанными в примерах и сравнительных примерах согласно настоящему изобретению) готовили в ходе эксперимента, используя дистиллированную воду, с получением концентрации 0,3 г/мл (расчет на основе исходной дозы композиции).
Гуперзин (таблетки гуперзина А), 50 мкг/шт., были произведены компанией Henan Zhu Lin Zhong Sheng Pharmaceutical Co., Ltd., и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 6 мкг/мл; таблетки танакана (танакан): стандартизованный экстракт листьев гинкго (Egb761), 40 мг/таблетка, были произведены компанией France Beaufort - Ipsen pharmaceutical Co., Ltd., и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 2 мг/мл.
(3) Реагенты:
Жидкость для высокоэффективной жидкостной хроматографии: хлорид ацетилхолина (AXCl), гидрофосфат натрия (Na2HPO4), хлорид, хлорид тетраметиламмония (TMACl), октаносульфонат натрия (OSA), тиосульфат натрия (Na2S2O5), тетранатриевая соль этилендиаминтетрауксусной кислоты (EDTA) все класса ВЭЖХ, производство Sigma, США; фосфорная кислота (H3PO4, 85%), хлорная кислота (HClO4), все класса ВЭЖХ, производство компании Fisher Scientific, США; реагент МВ, производство компании ESA, США.
Биохимические измерения: набор для определения ацетилхолинэстеразы (ТСНЕ); набор для определения супероксиддисмутазы (СОД); набор для определения малондиальдегида (МДА); набор для количественного определения белка (биуретовым методом); все предоставлены Институтом биоинженерии Яньчэн в Нанкине (Jiancheng Institute of Bioengineering of Nanjing); набор для определения нейропептидов Y (NPY), предоставлен Радиоиммунологическим центром развития науки и технологий Госпиталя Народно-освободительной армии (RIA center of Science and technology development center of PLA General Hospital); набор для определения β-эндорфина (β-EP), предоставлен Морским радиоиммунологическим технологическим центром.
(4) Прибор:
Водный лабиринт Морриса производства Института лекарственных средств Китайской академии медицинских наук (Institute of Medicines of Chinese Academy of Medical Sciences). Счетчик FT-630Gy производства Пекинской атомной электростанции. Спектрофотометр UV-120-02 производства компании Shimadzu, Япония. 16-канальная рабочая станция Coularray Cullen для высокоэффективной жидкостной хроматографии и хроматографии с электрохимическим детектором, 582 насосов, электрохимический детектор 5600А, автоматический пробоотборник 542, твердый пористый электрод типа 5040 (платиновый электрод, твердые палладиевые электроды), колоночный термостат типа СН150, реактор с иммобилизованным ферментом перед колонками, реактор с иммобилизованным ферментом после колонок, все продукты из компании ESA, США; колонки (С18150×3 мм (внутренний диаметр)), продукция компании ESA, США; ультрацентрифуга 55Р-72, продукт компании HITACHI, Япония; криогенные холодильники, продукты компании JOUAN, Франция; шприц с микропористым мембранным фильтром: водная мембрана (0,22 мкм), продукт фабрики фильтров Тяньцзинь Тенгда (Tianjin Tengda).
(5) Условия определения содержания ацетилхолина (АХ)
Подвижная фаза: Na2HPO4 (100 ммоль/л), TMACl (0,5 ммоль/л), OSA (2,0 ммоль/л), реагент МВ (0,005% об./об.), разбавление бидистиллированной водой, 85% рН доводили до 8,00 посредством H3PO4, фильтровали через водную мембрану с размером пор 0,22 мкм.
Условия проведения хроматографии: насосная система типа ESA582 для двухкомпонентных смесей, колонка ESA АСН-3 (150×3 мм, внутренний диаметр 5 мкм), первый реактор ESA с иммобилизованным ферментом перед колонками (ESA ACH-SPR, 3 см), скорость потока, 0,35 мл/мин, температура колонки 35°С.
Условия проведения эксперимента: электрохимический детектор 5600А; твердый пористый электрод типа 5040 (платиновый рабочий электрод, твердотельный палладиевый электрод сравнения), потенциал: + 300 мВ
2. Метод проведения эксперимента
Ложнооперированная группа, модельная группа, группа гуперзина, группа танакана, группы китайской лекарственной композиции согласно настоящему изобретению (шесть групп, дозы были такими же, как в тестовом примере 1), группы композиций согласно сравнительным примерам (8 групп, дозы были такими же, как в тестовом примере 1).
Крыс подвергали анестезии с помощью хлоральгидрата (350 мг/кг), делали разрезы в середине шеи, отделяли двусторонние общие сонные артерии и осуществляли их перевязку (в ложнооперированной группе артерии только отделяли, но не перевязывали), образовавшиеся у крыс раны зашивали, затем крыс кормили в клетках, крысам проводили противоинфекционную терапию пенициллином в течение 4 дней. Через месяц проводили испытание на плавание в водном лабиринте Морриса, отбирали крыс с тенденцией к снижению обучаемости и ухудшению памяти по показателю времени пребывания в лабиринте, и случайным образом группировали крыс следующим образом: модельная группа; группа гуперзина 60 мкг/кг; группа танакана 20 мг/кг; группа китайских лекарственных композиций согласно настоящему изобретению и группа китайских лекарственных композиций согласно сравнительным примерам (дозы те же, что и в экспериментальном примере 1), введение крысам проводили внутрижелудочно один раз в сутки (10 мл/кг) в течение 2 месяцев. Ложнооперированной группе и модельной группе вводили через желудочный зонд дистиллированную воду того же объема. Через 2 месяца, 3 месяца после создания моделей (1 месяц и 2 месяца после введения) определяли время пребывания в водном лабиринте Морриса. После последнего измерения брали кровь из брюшной аорты, быстро отбирали головной мозг, и его левое полушарие отвердевали жидким азотом. На ледяной бане гомогенаты в 0,15 М HClO4 (на 100 мг головного мозга добавляли 1 мл) центрифугировали в условиях 14000×g, 4°С в течение 20 мин, отбирали супернатант, фильтровали через мембрану с размером пор 0,22 мкм, 10 мкл подавали в автоматический пробоотборник, определяли содержание АХ с применением ВЭЖХ; правое полушарие, 4 для каждой группы, отвердевали формалином, дегидратировали, внедряли, нарезали, окрашивали НЕ для определения патологии, получали гомогенаты шести тканей головного мозга, определяли активность АХЭ, активность СОД и содержание МДА (колориметрический метод); определяли такие показатели, как нейропептид Y, β-ЕР в плазме (посредством радиоиммуноанализа). Результаты анализировали с применением статистического метода (t-критерий).
3. Результаты
3.1. Влияние на продолжительность пребывания крыс в водном лабиринте
Через месяц после перевязки двух общих сонных артерий крыс, хотя тенденция к снижению обучаемости и ухудшению памяти и проявилась, по сравнению с ложнооперированной группой больших отличий не было. Спустя два месяца, через три месяца после перевязки, время пребывания крыс в водном лабиринте Морриса у ложнооперированной группы было значительно меньше, чем у модельной группы (Р<0,01). Это указывало на то, что модели были созданы успешно. Во время от 2 до 3 месяцев после введения способность к обучению и запоминанию у крыс, получавших китайскую лекарственную композицию согласно настоящему изобретению, была значительно улучшена по сравнению с модельной группой, время пребывания в лабиринте было значительно сокращено (Р<0,01); такие же эффекты были обнаружены для сравнительной группы, получавшей лекарство гуперзин, и группы китайских лекарственных композиций согласно сравнительному примеру 2, сравнительному примеру 3, сравнительному примеру 6 и сравнительному примеру 7 (Р<0,05~0,01); через 3 месяца после введения способность к обучению и запоминанию у крыс сравнительной группы, получавшей лекарство танакан, имели тенденцию к улучшению, однако результаты не были статистически значимыми. Результаты представлены в таблице 12.
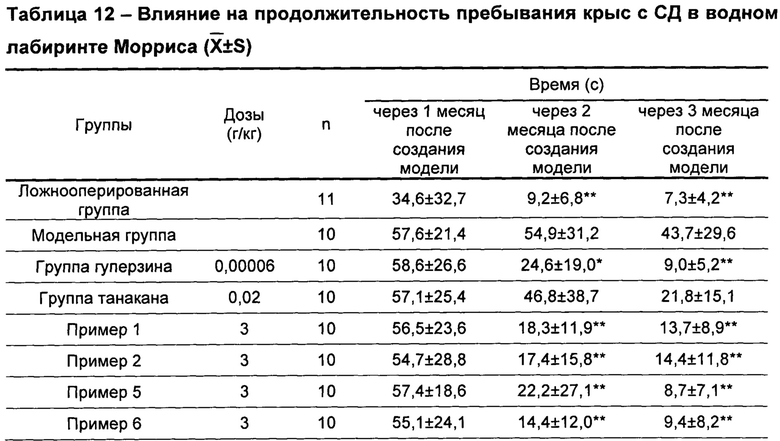
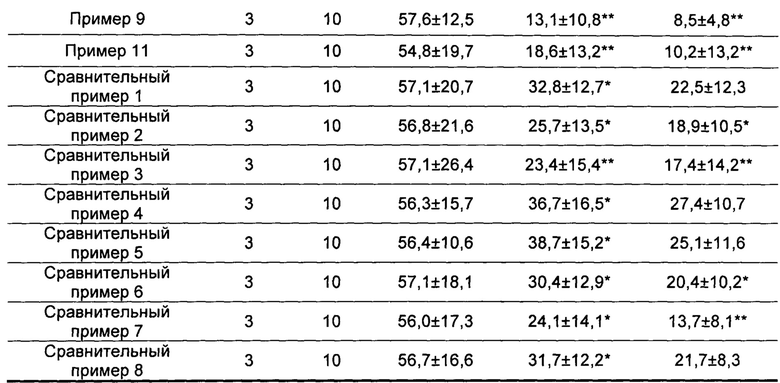
PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
3.2. Влияние на активность АХЭ и содержание АХ в головном мозге крыс
Через 3 месяца после перевязки двусторонних общих сонных артерий у крыс активность АХЭ в головном мозге была повышена, а содержание АХ было снижено, наблюдали значительные различия между ложнооперированной группой и модельной группой (Р<0,01); через 2 месяца после введения активность АХЭ в головном мозге крыс группы китайских лекарственных композиций согласно настоящему изобретению была значительно снижена (Р<0,05), содержание АХ во всем мозге крыс было значительно повышено (Р<0,01); тот же эффект наблюдали в сравнительной группе, получавшей лекарство гуперзин, и группе китайской лекарственной композиции согласно сравнительному примеру 7 (Р<0,05~0,01), для других групп китайских лекарственных композиций согласно сравнительным примерам и группы танакана изменения активности АХЭ были незначимыми, содержание АХ было значительно повышено (Р<0,05). Результаты представлены в таблице 13.
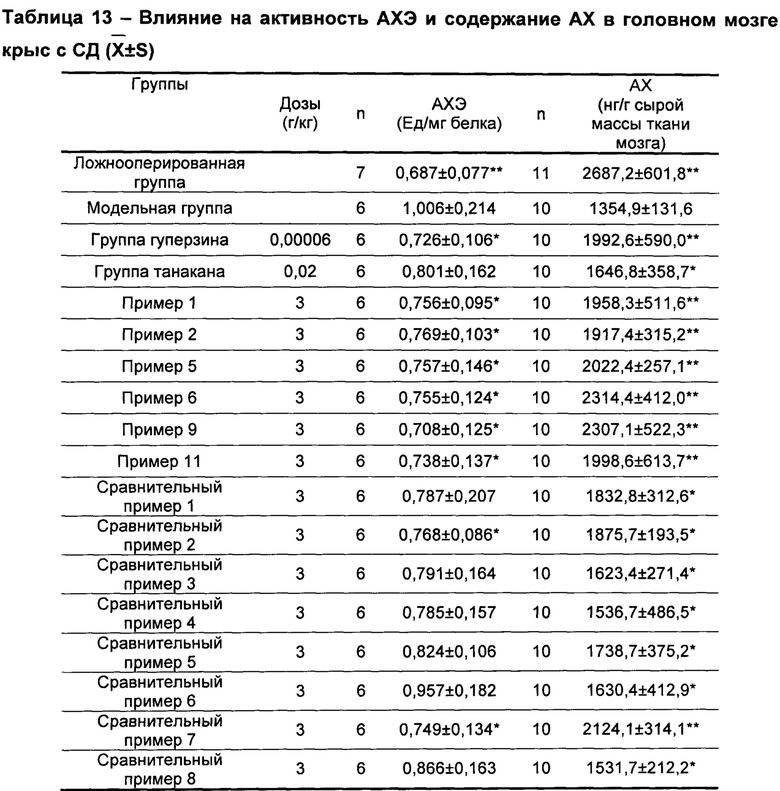
PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
3.3. Влияние на активность СОД, содержание МДА в ткани головного мозга
Через 3 месяца после перевязки двусторонних общих сонных артерий крыс активность СОД в головном мозге значительно снижалась, наблюдались значительные различия между ложнооперированной группой и модельной группой (Р<0,01), значительных изменений в содержании МДА не было; по сравнению с модельной группой активность СОД в группах китайских лекарственных композиций согласно настоящему изобретению была значительно повышена (Р<0,05), значительных изменений активности СОД для остальных групп не было. По сравнению с модельной группой значительных изменений в содержании МДА в головном мозге крыс указанных групп не было. Результаты представлены в таблице 14.
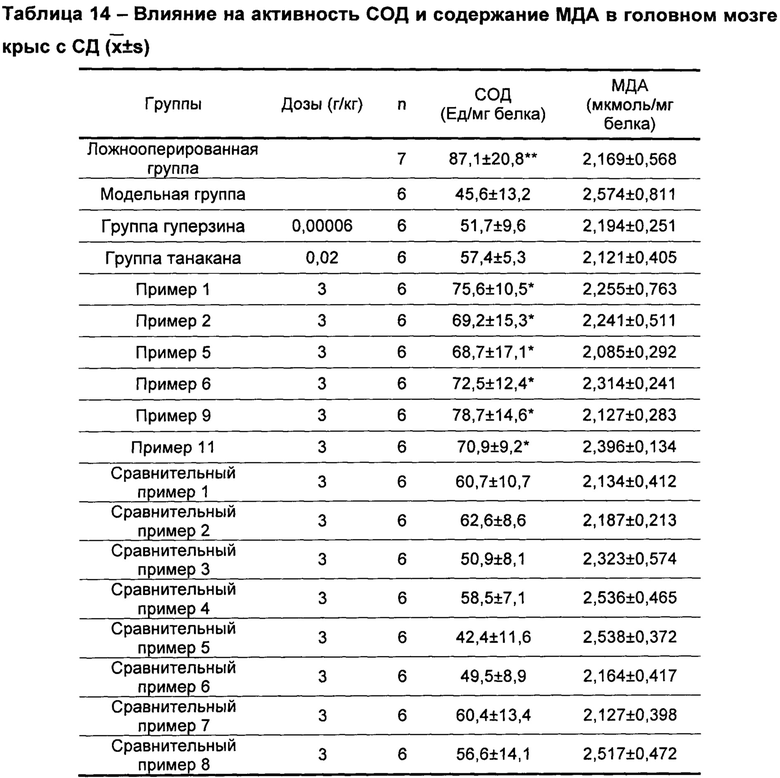
PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
3.4. Влияние на уровни NPY, β-ЕР в плазме крыс
Через 3 месяца после перевязки двусторонних общих сонных артерий крыс содержание NPY в плазме было значительно снижено, содержание β-ЕР было значительно повышено, наблюдались значительные различия между ложнооперированной и модельной группой (Р<0,01); через 2 месяца после введения содержание NPY у крыс из группы китайской лекарственной композиции согласно настоящему изобретению, группы китайской лекарственной композиции согласно сравнительному примеру 2 и группы китайской лекарственной композиции согласно сравнительному примеру 7 были значительно повышены, содержание β-ЕР в каждой группе было значительно снижено (Р<0,01 для всех), содержание NPY у крыс из групп китайских лекарственных композиций согласно другим сравнительным примерам было значительно повышено, содержание β-ЕР для каждой группы было значительно снижено (Р<0,05 для всех), указанные эффекты не были очевидны для сравнительных групп, получавших лекарства гуперзин и танакан. Результаты можно увидеть в таблице 15.
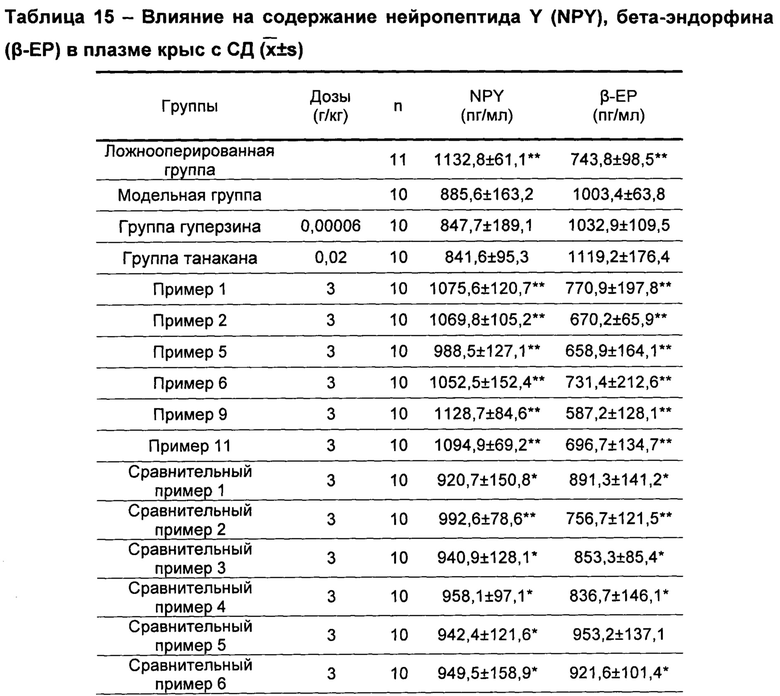

PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
3.5 Исследование по определению патологии
Исследование по определению патологии показало, что расположение пирамидного клеточного слоя гиппокампа ложнооперированной группы было почти регулярным, структура была компактной и имела несколько слоев, клеточная ядерная мембрана была свежей и гладкой. Расположение некоторых частей большей части пирамидных клеток гиппокампа в модельной группе было рыхлым, на ядерной мембране клеток были «морщины», ядрышко было относительно небольшим, структуры части пирамидных клеток были нечеткими, окрашенными, они представляли собой треугольники или агломераты, вокруг были видимые промежутки, ядро исчезло. Расположение пирамидной клетки гиппокампа в группе гуперзина было слегка рыхлым, большинство мембран ядер клеток можно было увидеть, небольшая часть ядрышка была относительно небольшой, часть ядрышка исчезла. В группе танакана и группах китайских лекарственных композиций согласно сравнительным примерам 1-3 и 7 расположение пирамидной клетки гиппокампа было четким, размеры клеток были приемлемыми, мембраны ядер были прозрачными, часть ядрышка можно было увидеть. Расположение большинства пирамидных клеток гиппокампа группы китайской лекарственной композиции согласно настоящему изобретению было упорядоченным, структуры между клетками были компактными, мембраны ядер клеток были относительно свежими и ядрышко было приемлемым, они были рассеяны в области, с видимыми «морщинами», окрашенными пирамидными клетками. Расположение пирамидных клеток гиппокампа группы китайской лекарственной композиции согласно сравнительному примеру 4 было относительно рыхлым, клетки были относительно небольшими, часть клеток были окрашенными с неясными нечеткими границами, у каждой клетки были «морщины», клетки представляли собой треугольники и агломераты. Расположение пирамидных клеток гиппокампа групп китайских лекарственных композиций согласно сравнительным примерам 5-6 и 8 было приемлемым, можно было видеть слои, границы между пирамидными клетками были нечеткими, мембрана ядер была обесцвечена, ядрышко было небольшим, они находились в денатурированном состоянии, а часть их исчезла.
Краткий вывод:
Хроническая церебральная ишемия представляет собой распространенный патологический процесс развития многих заболеваний, таких как сосудистая деменция (СД), болезнь Альцгеймера (AD) и подкорковая артериосклеротическая энцефалопатия (болезнь Бинсвангера) и другие заболевания. Исследование подтвердило, что после перевязки двухсторонней общей сонной артерии (2VO) у крыс кровоток может продолжать снижаться, через три недели начинается хроническая фаза, через месяц она все еще ниже, чем в нормальной группе; нейроны, которые были задействованы в обучении и памяти, такие как кора и гиппокамп, были атрофированы, вырождены, депигментированы, что означает, что состояние постепенно усугубляется; через 3 месяца после 2VO адгезия между М-ацетилхолиновым рецептором коры и гиппокампа снижалась; были значительные проблемы в поведении, таком как обучение и запоминание.
Многие исследования показали, что после церебральной ишемии может возникать перегрузка Са2+ в клетках, экзотоксичность и воспалительные реакции, что дополнительно приводит к нарушению функции и структуры нейронов. Церебральная ишемия и гипоксия также могут вызывать нарушение окислительного метаболизма митохондрий, приводя к избыточной выработке активных кислородных радикалов, включая О-2, НО-2, ОН-, Н2О2 и тому подобное. Эти активные кислородные радикалы могут взаимодействовать с белками, липидами, молекулами нуклеиновых кислот в нейронах и разрушать их молекулярную структуру, происходят супероксидные изменения, которые могут дополнительно вызывать повреждение структуры и функции клеток головного мозга и обеспечивать избыточную выработку продуктов перекисного окисления, таких как малондиальдегид (МДА). Нейроны гиппокампа, префронтальной коры, височной доли и коры головного мозга чувствительны к ишемии, и эти области представляют собой области головного мозга, которые тесно связаны со способностью к обучению и запоминанию. Нарушение функции и структуры этих нейронов в головном мозге после церебральной ишемии вызовет нарушение нейромедиаторов, связанных с обучением и памятью, приведет к снижению способности к обучению и запоминанию и даже к деменции.
Полученные посредством 2VO модели СД, использованные в настоящем эксперименте, подтвердили вышеуказанные биохимические, патологические и поведенческие изменения процесса, и было отмечено, что китайские лекарственные композиции согласно настоящему изобретению могут значительно ингибировать активность АХЭ, увеличивая содержание АХ в головном мозге модельных животных, вызывая улучшения при нарушении обучаемости и запоминания, указанное лекарство также может в значительной степени увеличить активность DOS в головном мозге, устраняя свободные кислородные радикалы для защиты тканей мозга, при этом было показано, что группы китайских лекарственных композиций согласно настоящему изобретению имеют значительные терапевтические эффекты в отношении СД, и эти эффекты намного лучше, чем эффекты китайских лекарственных композиций согласно сравнительным примерам.
Сообщается, что в плазме пациентов с СД содержание нейропептида Y снижается, содержание β-ЕР увеличивается, заявитель определял содержание нейропептида Y и β-ЕР в полученных посредством 2VO моделях на животных, полученные данные согласуются с изложенным, и отмечается, что в группе китайских лекарственных композиций согласно настоящему изобретению содержание нейропептида Y в плазме может быть в значительной степени увеличено, а содержание β-ЕР в плазме может быть значительно уменьшено.
Исследование по определению патологии показало, что некоторые области гиппокампа в модельной группе были расположены свободно, на ядерных мембранах можно наблюдать видимые сжатые участки, ядрышки были относительно небольшими, структура части пирамидных клеток была нечеткой, окрашенной, они представляли собой треугольники или агломераты, видимые промежутки рядом, ядрышко исчезло. Большая часть пирамидных клеток гиппокампа в группах китайских лекарственных композиций согласно настоящему изобретению была упорядочена, структуры между клетками были компактными, ядерная мембрана была свежей и степень поражений была значительно снижена.
Тестовый пример 9. Влияние на ишемическую реперфузию и нарушение способности к обучению и памяти у мышей, индуцированное подкожной инъекцией D-галактозы
1. Материалы для проведения эксперимента
(1) Животные: мыши ICR, 25-32 г, поровну самцы и самки. Предоставлены Beijing Vital River Laboratory Animal Technology Development Company Ltd.
(2) Лекарства:
Китайские лекарственные композиции согласно настоящему изобретению и китайские лекарственные композиции согласно сравнительным примерам (смесь соответствующих экстрактов была получена самостоятельно в соответствии со способами, описанными в примерах и сравнительных примерах согласно настоящему изобретению) готовили в ходе эксперимента, используя дистиллированную воду, с получением концентрации 0,2 г/мл (расчет на основе исходной дозы композиции).
Гуперзин (таблетки гуперзина А), 50 мкг/шт., были произведены компанией Henan Zhu Lin Zhong Sheng Pharmaceutical Co., Ltd., и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 4 мкг/мл; таблетки танакана (танакан): стандартизованный экстракт листьев гинкго (Egb761), 40 мг/таблетка, были произведены компанией France Beaufort - Ipsen pharmaceutical Co., Ltd., и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 1,5 мг/мл. D-галактоза, была произведена компанией Shanghai Hengxin chemical reagent со., LTD; набор для определения ацетилхолинэстеразы (ТСНЕ); набор для определения супероксиддисмутазы (СОД); набор для определения малондиальдегида (МДА); набор для определения глутатионпероксидазы (GSH-Px); набор для определения оксида азота (NO); набор для количественного определения белка (биуретовым методом); все предоставлены Институтом биоинженерии Яньчэн в Нанкине (Jiancheng Institute of Bioengineering of Nanjing).
(3) Приборы:
Водный лабиринт Морриса производства Института лекарственных средств Китайской академии медицинских наук (Institute of Medicines of Chinese Academy of Medical Sciences). Спектрофотометр UV-120-02 производства компании Shimadzu, Япония.
2. Метод проведения эксперимента
Мышей случайным образом разделяли на группы, самцов и самок было поровну: ложнооперированную группу, группу комбинированной модели, группу D-галактозы, группу ишемии и реперфузии, группу гуперзина, группу танакана, группы китайских лекарственных композиций согласно настоящему изобретению (шесть групп, дозы были такими же, как в тестовом примере 2), группы композиций согласно сравнительным примерам (8 групп, дозы были такими же, как в тестовом примере 2).
Мышей подвергали анестезии с помощью хлоральгидрата, делали разрезы в области шеи, применяли операцию для моделирования ишемии и реперфузии: отделяли двусторонние общие сонные артерии, зажимали на 20 минут с помощью зажима типа "бульдог", ослабляли зажим на 2 минуты, затем снова зажимали на 20 минут, затем ослабляли, в то же время надрезали хвосты мышей, забирали 0,5 мл крови, при этом развивалось поражение головного мозга вследствие повторной ишемии-реперфузии, образовавшиеся у крыс раны зашивали, затем крыс кормили в клетках. Через 7 дней после операции мышам вводили D-галактозу (100 мг/кг, 10 мл/кг) посредством подкожной инъекции в область спины, и одновременно мышам вводили внутрижелудочно лекарства (20 мл/кг) один раз в день, введение продолжали в течение 8 недель; для ложнооперированной группы общие сонные артерии отделяли без установки зажима, такой же объем физиологического раствора вводили посредством подкожной инъекции в область спины; в группе D-галактозы общие сонные артерии отделяли без установки зажима, D-галактозу (100 мг/кг, 10 мл/кг) вводили посредством подкожной инъекции в область спины; группа ишемии и реперфузии была подвергнута операции, вызывающей развитие ишемии и реперфузии, и ей вводили такой же объем физиологического раствора посредством подкожной инъекции в область спины. Ложнооперированной группе, группе комбинированной модели, группе D-галактозы вводили с помощью желудочного зонда такой же объем дистиллированной воды.
После 8 недель введения лекарств мышей обучали в течение 3 дней в водном лабиринте Морриса два раза в день, параметры, характеризующие обучаемость и память, определяли на 4-й день, на 5-й день животных декапитировали для забора головного мозга, готовили препараты тканей мозга в виде 10% гомогенатов на физиологическом растворе, определяли активность АХЭ, СОД, GSH-Px и содержание биохимических индикаторов, таких как МДА, NO, в тканях головного мозга (колориметрическими методами). Результаты анализировали с применением статистического метода (t-критерий).
3. Результаты
3.1. Влияние на обучаемость и память у мышей в тесте водного лабиринта Морриса
Через 8 недель после введения в состояние ишемии-реперфузии и подкожной инъекции D-галактозы продолжительность пребывания и длина траектории движения мышей в водном лабиринте Морриса увеличивались, были значительные различия по сравнению с ложнооперированной группой (Р<0,01); стратегии поиска выхода в основном представляли собой тип «край лабиринта» или тип «случайный поиск». По сравнению с ложнооперированной группой и модельной группой, не было значительных различий в продолжительности пребывания и длине траектории движения для группы, которую подвергали только ишемии-реперфузии, по сравнению с группой комбинированной модели, были значительные различия в стратегии поиска (Р<0,05); по сравнению с группой комбинированной модели не было значительных различий в продолжительности пребывания, длине траектории движения и стратегии поиска для группы, которая получала только D-галактозу посредством подкожной инъекции; это указывало на то, что нарушение обучения и памяти у мышей может быть вызвано только подкожной инъекцией D-галактозы и только повреждениями вследствие ишемии и реперфузии, но степень нарушений была не такой значительной, как при комбинации этих двух воздействий; по сравнению с группой комбинированной модели была уменьшена длина траектории движения в сравнительной группе лекарства гуперзина, стратегия поиска была значительно улучшена (Р<0,05-0,01); продолжительность пребывания и длина траектории движения в группе танакана были значительно уменьшены (Р<0,05~0,01), стратегия поиска не была значительно улучшена; продолжительность пребывания и длина траектории движения у мышей из групп китайских лекарственных композиций согласно настоящему изобретению были значительно уменьшены (Р<0,05~0,01), стратегии поиска были значительно улучшены (Р<0,01); продолжительность пребывания и длина траектории движения в группах композиций согласно сравнительным примерам 2, 3, 7, 8 были значительно уменьшены (Р<0,05~0,01), стратегии поиска были значительно улучшены (Р<0,05~0,01); продолжительность пребывания и длина траектории движения в группах композиций согласно сравнительным примерам 1, 4, 5, 6 были значительно уменьшены (Р<0,05), стратегии поиска были значительно улучшены. Результаты представлены в таблице 16.
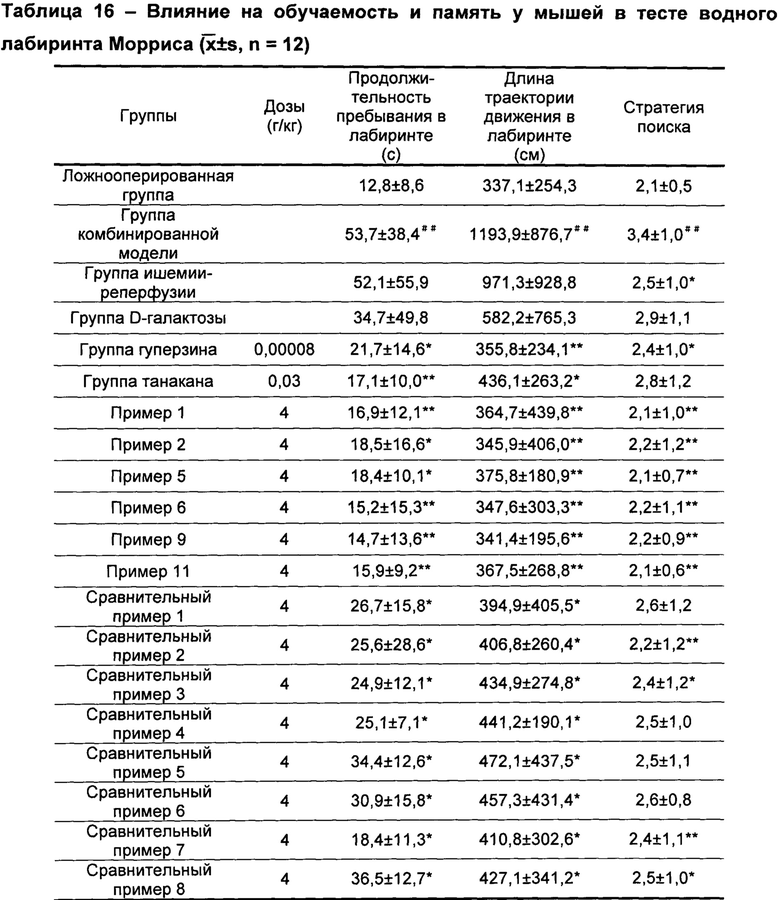
Р5:  стратегия поиска: тип «прямая линия», 1 балл; тип «направление», 2 балла; тип «край», 3 балла; тип «случайный поиск», 4 балла;
стратегия поиска: тип «прямая линия», 1 балл; тип «направление», 2 балла; тип «край», 3 балла; тип «случайный поиск», 4 балла;  по сравнению с ложнооперированной группой, *Р<0,05, **Р<0,01;
по сравнению с ложнооперированной группой, *Р<0,05, **Р<0,01;  по сравнению с модельной группой, *Р<0,05, **Р<0,01.
по сравнению с модельной группой, *Р<0,05, **Р<0,01.
3.2. Влияние на активность СОД, GSH-Px и содержание МДА и NO в головном мозге
Через 8 недель после введения в состояние ишемии-реперфузии и подкожной инъекции D-галактозы активность СОД, GSH-Px в ткани головного мозга мышей (группа комбинированной модели) была снижена, а содержание МДА, NO было повышено, наблюдались значимые отличия по сравнению с ложнооперированной группой (Р<0,05~0,01); в группе, которая получала только D-галактозу посредством подкожной инъекции, активность СОД, GSH-Px в ткани головного мозга была снижена, а содержание МДА, NO было повышено, наблюдались значительные изменения по сравнению с ложнооперированной группой (Р<0,05~0,01 для всех), не было обнаружено значительных изменений по сравнению с группой комбинированной модели; в группе, которую подвергали только ишемии-реперфузии, активность СОД, GSH-Px и содержание МДА, NO в ткани головного мозга по сравнению с ложнооперированной группой были снижены (Р<0,05), по сравнению с ложнооперированной группой, не наблюдали значительных изменений содержания МДА. По сравнению с группой комбинированной модели, не наблюдали значительных изменений для активности СОД, GSH-Px и содержания МДА, NO в сравнительной группе лекарства гуперзина; в группе танакана активность СОД, GSH-Px была значительно повышена, а содержание МДА, NO было значительно снижено (Р<0,05~0,01); в группе китайских лекарственных композиций согласно настоящему изобретению активность СОД, GSH-Px была значительно повышена, а содержание МДА, NO было значительно снижено (Р<0,05~0,01); в группах китайской лекарственной композиции согласно сравнительным примерам 1~3, 7 активность СОД в ткани головного мозга мышей была значительно повышена, содержание NO было значительно снижено (Р<0,05 для всех), не было обнаружено значительных изменений активности GSH-Px и содержания МДА; в группах композиций согласно сравнительным примерам 4~6, 8 содержание NO было значительно снижено (Р<0,05 для всех), не было обнаружено значительных изменений активности СОД, GSH-Px и содержания МДА. Результаты представлены в таблице 17.
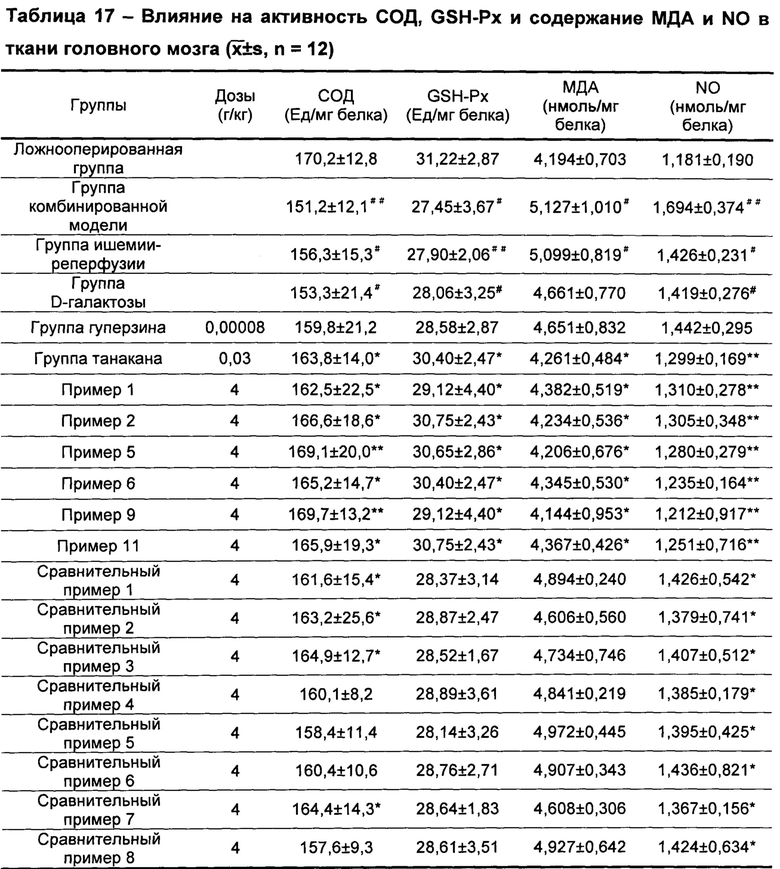
PS: по сравнению с ложнооперированной группой, *Р<0,05, **Р<0,01; по сравнению с группой комбинированной модели, *Р<0,05, **Р<0,01
3.3. Влияние на активность АХЭ в ткани головного мозга
Через 8 недель после введения в состояние ишемии-реперфузии и подкожной инъекции D-галактозы активность АХЭ в ткани головного мозга мышей (группа комбинированной модели) была значительно повышена, наблюдались значимые отличия по сравнению с ложнооперированной группой (Р<0,01); в группе, которая получала только подкожную инъекцию D-галактозы, и в группе, которую подвергали только ишемии-реперфузии, активность АХЭ в тканях головного мозга была повышена, наблюдались значимые отличия по сравнению с ложнооперированной группой (Р<0,05), не было обнаружено значительных различий по сравнению с группой комбинированной модели. По сравнению с группой комбинированной модели, активность АХЭ в группах китайских лекарственных композиций согласно настоящему изобретению, в группах китайских лекарственных композиций согласно сравнительным примерам 1-3, 7 (Р<0,05); не было обнаружено значительных изменений активности АХЭ в группах китайских лекарственных композиций согласно сравнительным примерам 4~6, 8. Результаты представлены в таблице 18.
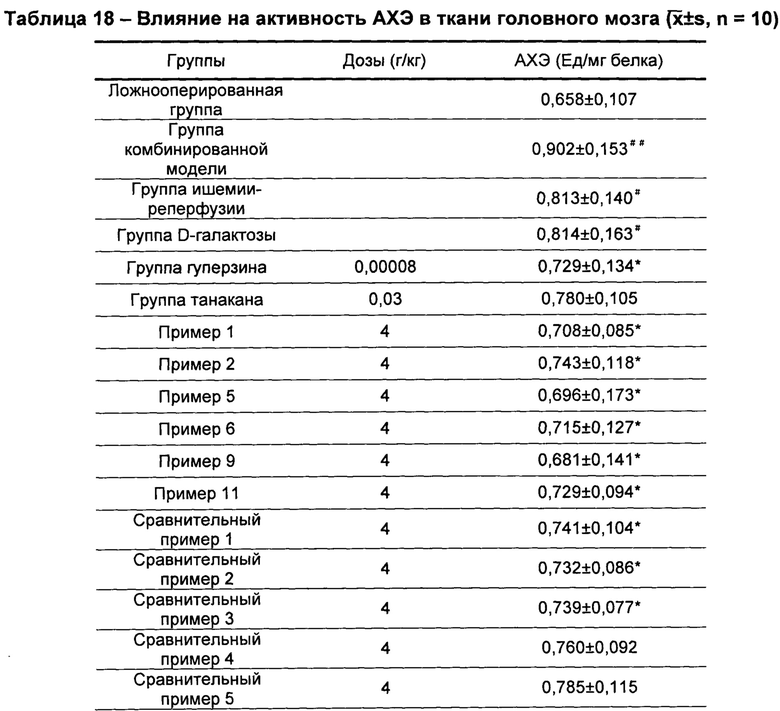
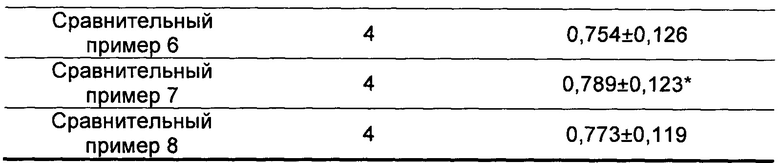
PS: по сравнению с ложнооперированной группой, *Р<0,05, **Р<0,01; по сравнению с группой комбинированной модели, *Р<0,05, **Р<0,01
Краткий вывод: Точный механизм ишемически-реперфузионного повреждения головного мозга неясен, большинство ученых полагают, что оно связано с каскадной реакцией, вызванной увеличением числа свободных кислородных радикалов. В нормальных условиях образуется очень небольшое количество свободных кислородных радикалов и время их существования невелико, поэтому они не вызывают опасности для организма, и при этом поглотители эндогенных свободных кислородных радикалов играют очень важную роль. Глутатионпероксидаза (GSH-Px) является важным ферментом, разлагаемым каталитическими гидроксильными свободными радикалами; СОД является представителем поглотителей эндогенных свободных кислородных радикалов, в определенной степени ее активность отражает активность по поглощению эндогенных свободных кислородных радикалов; основной метаболит МДА, образуемый при расщеплении липидов мембраны, обычно используется в качестве индикатора перекисного окисления липидов, NO является чрезвычайно важным мессенджером организма и играет двойную роль в процессе церебральной ишемии: с одной стороны, он может уменьшить площадь инфаркта, увеличить кровоснабжение коры, а с другой стороны он может действовать синергически со свободными кислородными радикалами, вызванными ишемией, приводя к повреждению нервных клеток. Мониторинг уровня СОД, GSH-Px, МДА и NO в ткани головного мозга важен для изучения ишемически-реперфузионного повреждения головного мозга.
D-галактозная подострая модель старения построена следующим способом: мышам давали большие дозы D-галактозы непрерывно посредством подкожной инъекции, чтобы вызвать нарушение метаболизма глюкозы у животных. При катализе D-галактозооксидазой D-галактоза может обеспечить выработку свободных кислородных радикалов, таких как супероксидный анион. Свободные кислородные радикалы являются высокореакционноспособными, могут атаковать ненасыщенные жирные кислоты, белки, ферменты мембранных фосфолипидов и ДНК в ядре и т.д.; свободные радикалы также могут обеспечить перикисное окисление липидов с образованием пероксида липидов (ПОЛ), МДА образуется в кислой среде после осаждения ПОЛ белком, МДА является активным сшивающим агентом, он может быстро образовывать флуоресцентный краситель с фосфатидилэтаноламином, а затем образовать пластинчатый липофусцин (ПЛ) с белками, пептидами, липидами. При непрерывной инъекции D-галактозы мыши могут продуцировать изменения ряда биохимических показателей, таких как увеличение МДА в головном мозге, содержание ПЛ; снижение активности СОД в головном мозге, активности GSH-Px в крови, активности эритроцитарного CAT, и эти изменения согласуются с естественными изменениями, происходящими при старении, что указывает на то, что D-галактоза может вызывать старение клеток и организмов. Активности СОД, GSH-Px и CAT косвенно отражают способность организма устранять свободные кислородные радикалы; а уровни МДА и ПЛ косвенно отражают тяжесть атак свободных радикалов на клетки.
В этом эксперименте у мышей с реперфузионно-ишемическим повреждением головного мозга в сочетании с подкожной инъекцией D-галактозы вызывали повреждение головного мозга, затем активность АХЭ значительно увеличивали, вследствие чего появлялись когнитивные нарушения, уменьшалась способность к пространственному обучению; при тестировании также наблюдали что для мозговой ткани мышей комплексной модели активности СОД, GSH-Px были значительно снижены, содержание МДА и NO не было значительно увеличено. После того, как мышам давали через желудочный зонд китайские лекарственные композиции согласно настоящему изобретению, в мозговой ткани мышей активность АХЭ была снижена, активности СОД и GSH-Px были значительно повышены, содержания МДА и NO были значительно снижены, способность к пространственному обучению была значительно улучшена, что указывало на то, что китайские лекарственные композиции согласно настоящему изобретению подавляли эффекты выработки реакционноспособного кислорода и перекисного окисления липидов, вызванные ишемией-реперфузией, тем самым предотвращая необратимое повреждение нервных клеток, и следовательно улучшая способность к обучению и запоминанию, и эффективность китайских лекарственных композиций согласно настоящему изобретению была выше, чем эффективность китайских лекарственных композиций согласно сравнительным примерам.
Тестовый пример 10. Влияние на модель мультиинфарктной деменции (МИД) на крысах
1. Материалы для проведения эксперимента
(1) Животные: крысы SD, самцы, масса тела 260-280 г, были предоставлены Beijing Vital River Laboratory Animal Technology Development Company Ltd.
(2) Лекарства:
Китайские лекарственные композиции согласно настоящему изобретению и китайские лекарственные композиции согласно сравнительным примерам (смесь соответствующих экстрактов была получена самостоятельно в соответствии со способами, описанными в примерах и сравнительных примерах согласно настоящему изобретению) готовили в ходе эксперимента, используя дистиллированную воду, с получением концентрации 0,15 г/мл (расчет на основе исходной дозы композиции).
Таблетки танакана (танакан), стандартизированный экстракт листьев гинкго (Egb761) 40 мг/таблетка, были произведены компанией France Beaufort - Ipsen pharmaceutical Co., и с помощью дистиллированной воды в ходе эксперимента была получена их концентрация 2,0 мг/мл. Агент для эмболизации сосудов на основе микросфер альгината натрия (KMG), размер: 100~200 мкм, Beijing Sheng Yi Yao Technology Development Co., Ltd.; набор для радиоиммунологического определения соматостатина (СС), нейропептид Y (NPY), были предоставлены Морским радиоиммунологическим технологическим центром; набор для радиоиммунологического определения пептида, связанного с геном кальцитонина (CGRP), биоинженерная компания Beijing Furui, эндотелии (ЭТ), был предоставлен Институтом биотехнологии Пекина Бей Миан Донг (Beijing Bei Mian Dong Ya Institute of biotechnology), норепинефрин (NE), допамин (DA), 3,4-дигидроксифенилуксусная кислота (DOPAC), гомованиловая кислота (HVA), 5-гидрокситриптамин (5-HT), 5-гидроксииндолуксусная кислота (5-HIAA), дигидрофосфат натрия (NaH2PO4), лимонная кислота, тиосульфат натрия (Na2S2O5), этилендианаттетрауксусная кислота, тетранатриевая соль (ЭДТА), все чистоты для анализа; октаносульфонат натрия (OSA), класс ВЭЖХ, все продукты компании Sigma, США; ацетонитрил (ACN), хлорная кислота (HClO4), все класса ВЭЖХ, продукты компании Fisher Scientific, США.
(3) Прибор:
Ультрацентрифуга (Япония, HITACHI 55Р-72); 16-канальная рабочая станция Coularray Cullen для высокоэффективной жидкостной хроматографии и хроматографии с электрохимическим детектором, 580 насосов, электрохимический детектор 5600А, автоматический пробоотборник 542, продукт компании ESA, США; колонки (С1815×4,6 мм 5 мкм), продукт компании WATERS, США. криогенные холодильники, продукты компании JOUAN, Франция; шприц с микропористым мембранным фильтром: водный (0,22 мкм), продукт фабрики фильтров Тяньцзинь Тенгда. Водный лабиринт Морриса производства Института лекарственных средств Китайской академии медицинских наук. Счетчик FT-630Gy производства Пекинской атомной электростанции.
(4) Условия проведения хроматографии:
Состав подвижной фазы: дигидрофосфат натрия 90 ммоль/л, лимонная кислота 50 ммоль/л, октансульфонат натрия 1,7 ммоль/л, тетранатриевая соль этилендиаминтетрауксусной кислоты (ЭДТА) 0,05 мкмоль/л. Раствор фильтровали через водную мембрану с размером пор 0,2 мкм. К фильтрату добавляли ацетонитрил (10%). Скорость потока подвижной фазы составляла 0,6 мкл/мин, рабочий электрод 1: -150 мВ, рабочий электрод 2: 450 мВ, рабочий электрод 3: 500 мВ, рабочий электрод 4: 550 мВ.
Получение стандартного раствора: исходный раствор (100 мкг/мл) готовили с 0,1 моль/л хлорной кислоты и стандартным веществом, полученный раствор хранили в холодильнике при -70°С. Данный исходный раствор разбавляли до 10 мкг/мл разбавителем. Готовили последовательные разведения с получением растворов, которые использовали в качестве стандартных. В качестве рабочей жидкости использовали 0,15 моль/л хлорной кислоты (0,04% метабисульфита натрия и 0,04% ЭДТА).
2. Метод проведения эксперимента
Крысы получали внутрибрюшинную анестезию хлоральгидратом (350 мг/кг), волосы на шее выбривали, проводили дезинфекцию, крысам делали разрез в середине шеи, отделяли общую сонную артерию, внутреннюю сонную артерию и наружную сонную артерию. Наружную сонную артерию перевязывали, общую сонную артерию пережимали зажимом типа «бульдог», вводили 0,1 мл KMG во внутреннюю сонную артерию шприцом из наружной сонной артерии, зажим типа «бульдог» удаляли, наружную сонную артерию перевязывали, образовавшиеся у крыс раны зашивали, затем крыс кормили в клетках. Для ложнооперированной группы только отделяли общую сонную артерию, внутреннюю сонную артерию и наружную сонную артерию, микросферы не вводили. Для предотврашения инфекции вводили пенициллин натрия для инъекций в течение 4 дней. На следующий день после операции наблюдали поведение животных, если были изменения поведения передних конечностей, тогда модели были успешно созданы (если нет - крыс не использовали в исследовании), и полученных крыс разделяли на модельную группу, группу танакана 20 мг/кг, группы китайских лекарственных композиций согласно настоящему изобретению (6 групп, дозы были такими же, как и в примере 1), группы, получавшие композиции согласно сравнительным примерам (8 групп, дозы были такими же, как в тестовом примере 1).
Через 10 дней после операции крысам производили внутрижелудочное введение (ложнооперированная группа и модельная группа получали через зонд дистиллированную воду того же объема) один раз в день в течение 90 дней. Через 40, 100 дней создания моделей (через 30, 90 дней после введения) определяли время пребывания и длину пути крыс для поиска платформы в водном лабиринте Морриса, через 60 минут после последнего введения крысы получали внутрибрюшинную анестезию с помощью хлоралгидрата, брали кровь из брюшной аорты, обрабатывали антикоагулянтом, плазму отделяли, и быстро отрезали головы для извлечения головного мозга, кору, гиппокамп и полосатое тело, взвешивали, взвешивали, отвердевали жидким азотом, хранящемся в холодильнике при температуре -70°С. К каждым 100 мг ткани головного мозга добавляли 1 мл холодной рабочей жидкости, полученные комбинации гомогенизировали с помощью электронного гомогенизатора в течение 15 с на ледяной бане (11000 оборотов в минуту), центрифугировали при 0-4°С со скоростью 14000 об/мин в течение 20 минут, супернатант подврергали экстракции, фильтровали через мембрану с размером пор 0,22 мкм фильтр шприцевого типа, полученный фильтрат отделяли, хранили в холодильнике при -20°С. Отбирали 10 мкл каждого образца с помощью автоматического пробоотборника, определяли содержание моноаминовых нейромедиаторов, таких как 5-НТ, 5-HIAA, NE, DA и тому подобное посредством ВЭЖХ (метод ВЭЖХ с электрохимическим детектированием). Определяли содержание ЕТ, NPY, SS, CGRP в плазме (посредством радиоиммуноанализа). Результаты анализировали с применением статистического метода (t-критерий).
3. Результаты
3.1. Влияние на массу коры головного мозга, полосатого тела и гиппокампа После инъекции биомикросферы микросферы попадали в кровь головного мозга с кровотоком, через 24 часа они могут образовывать в головном мозге множественные очаги омертвения разных размеров, и указанные очаги в основном находятся в области коры, гиппокампа и полосатого тела. Через 100 дней для модельной группы указанные очаги были более жидкими и произошел некроз таких очагов, появились полости, ткань мозга была сжата, гиппокамп был меньше, кора была тоньше, масса уменьшилась по сравнению с модельной группой, были обнаружены значительные различия для ложнооперированной группы (Р<0,05~0,01) по сравнению с модельной группой, для групп, получавших китайские лекарственные композиции согласно настоящему изобретению и китайские лекарственные композиций согласно сравнительным примерам, масса коры головного мозга крыс была увеличена, но отсутствовала статистическая значимость для групп, получавших китайские лекарственные композиции согласно настоящему изобретению, массы полосатого тела и гиппокампа были значительно увеличены (Р<0,05); для группы, получавшей леакрство танакан, и групп, получавших китайские лекарственные композиции согласно сравнительным примерам были увеличены массы коры головного мозга, полосатого тела, гиппокампа крыс, но статистическая значимость отсутствала. См. таблицу 19.
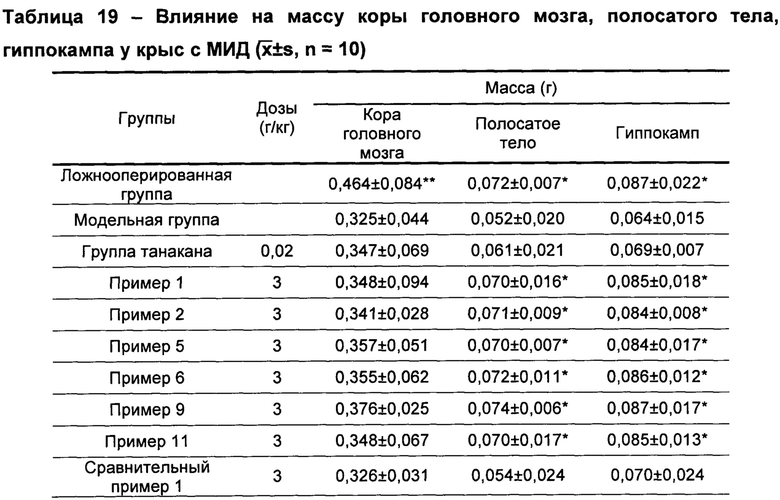
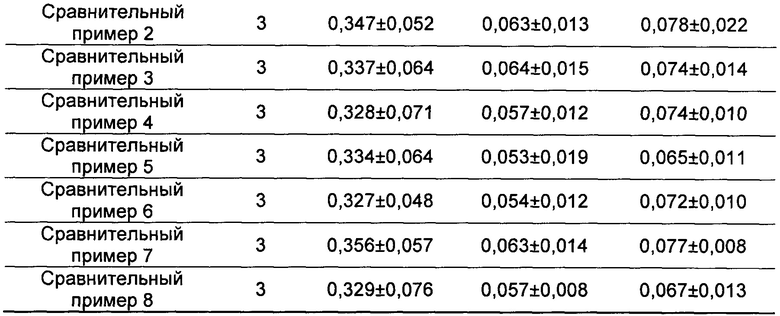
PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
3.2. Влияние на время пребывания в водном лабиринте Морриса
По сравнению с модельной группой, для ложнооперированной модельной группы время пребывания в водном лабиринте было значительно уменьшено (Р<0,05); через 30 дней после введения, по сравнению с модельной группой, для групп китайских лекарственных композиций согласно настоящему изобретению время пребывания в водном лабиринте было значительно уменьшено (Р<0,05), для других групп значительных изменений не наблюдалось; через 90 дней после введения для групп китайских лекарственных композиций согласно настоящему изобретению время пребывания в водном лабиринте было значительно уменьшено (Р<0,05~0,01), по сравнению с модельной группой, для групп композиций согласно сравнительным примерам 1~3 и 7 время пребывания в водном лабиринте было значительно уменьшено (Р<0,05), для других групп значительных изменений не наблюдалось. См. таблицу 20.
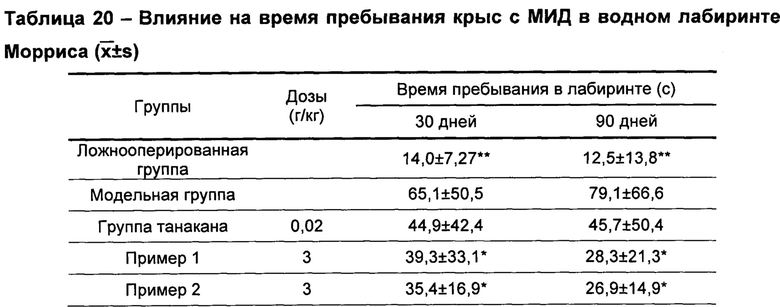
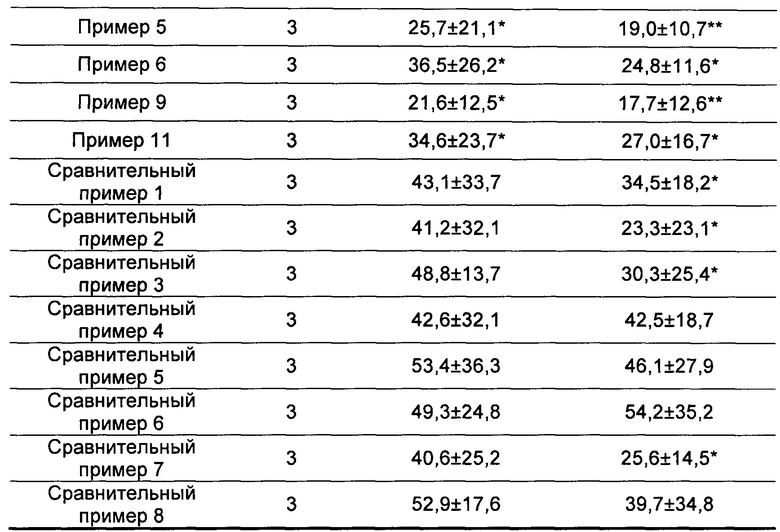
PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
3.3. Влияние на содержание ЕТ, NPY, SS, CGRP в плазме
Через 100 дней после создания моделей, по сравнению с модельной группой, для ложнооперированной группы содержание NPY в плазме животных было значительно повышено, содержание ЕТ было значительно снижено (Р<0,01 для всех), содержание SS и CGRP было повышено, но статистическая значимость отсутствовала (Р<0,01); через 100 дней после создания моделей (через 90 дней после введения), по сравнению с модельной группой, для групп китайских лекарственных композиций согласно настоящему изобретению содержание NPY и SS было значительно повышено (Р<0,01), содержание ЕТ было значительно снижено (Р<0,05), значительных изменений содержания CGRP не наблюдалось; для групп китайских лекарственных композиций согласно сравнительным примерам 1~3 и 7 содержание NPY и SS было значительно повышено (Р<0,05~0,01), содержание ЕТ имело тенденцию к уменьшению, значительных изменений содержания CGRP не наблюдалось; для групп китайских лекарственных композиций согласно сравнительным примерам 4~6 и 8 содержание NPY и SS имело тенденцию к увеличению, содержание ЕТ имело тенденцию к уменьшению, значительных изменений содержания CGRP не наблюдалось; для сравнительной группы лекарства танакана содержание NPY и SS было значительно повышено (Р<0,01), содержание ЕТ было значительно снижено (Р<0,01), значительных изменений содержания CGRP не наблюдалось. См. таблицу 21.

PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
3.4. Влияние на содержание моноаминовых нейромедиаторов в головном мозге
(1) Влияние на содержание моноаминовых нейромедиаторов коры головного мозга
Через 100 дней после создания моделей, по сравнению с модельной группой, для ложнооперированной группы содержание 5-НТ, 5-HIAA в коре головного мозга крыс было значительно повышено (Р<0,05), содержание NE и DA было повышено, но статистическая значимость отсутствовала; для групп китайских лекарственных композиций согласно настоящему изобретению содержание 5-НТ было значительно повышено (Р<0,01), содержание DA и 5-HIAA было значительно повышено (Р<0,05); для групп китайских лекарственных композиций согласно сравнительным примерам 1~3 и 7 содержание DA и 5-НТ было значительно повышено (Р<0,05); для групп китайских лекарственных композиций согласно сравнительным примерам 4~6 и 8 содержание 5-НТ было значительно повышено, но статистическая значимость отсутствовала; для сравнительной группы лекарства танакана содержание 5-НТ и 5-HIAA было значительно повышено (Р<0,01), значительных различий для других показателей не наблюдалось. См. таблицу 22.
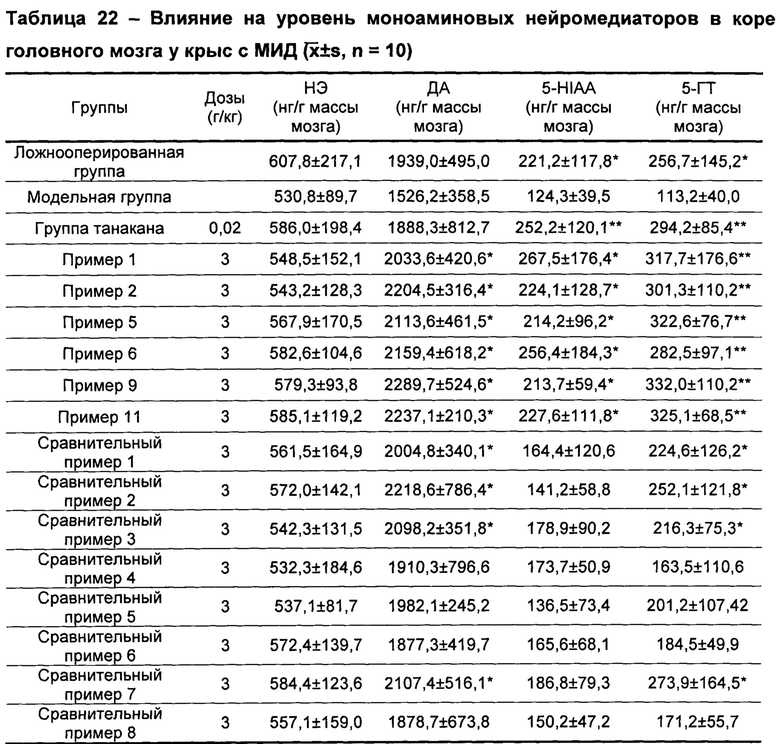
PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
(2) Влияние на содержание моноаминовых нейромедиаторов полосатого тела
Через 100 дней после создания моделей, по сравнению с модельной группой, для ложнооперированной группы содержание 5-НТ и 5-HIAA в полосатом теле головного мозга крыс было значительно повышено (Р<0,05), что свидетельствовало об успешном создании моделей; через 100 дней после создания моделей (через 90 дней после введения), по сравнению с модельной группой, для групп композиций согласно примерам 5 и 9 настоящего изобретения содержание 5-НТ было значительно повышено (Р<0,05), для групп композиций согласно примерам 1, 2, 6 и 11 настоящего изобретения содержание 5-HIAA было значительно повышено (Р<0,05); для групп китайских лекарственных композиций согласно сравнительным примерам и сравнительной группы лекарства танакана значительных различий для содержания 5-НТ и 5-HIAA не наблюдалось. См. таблицу 23.
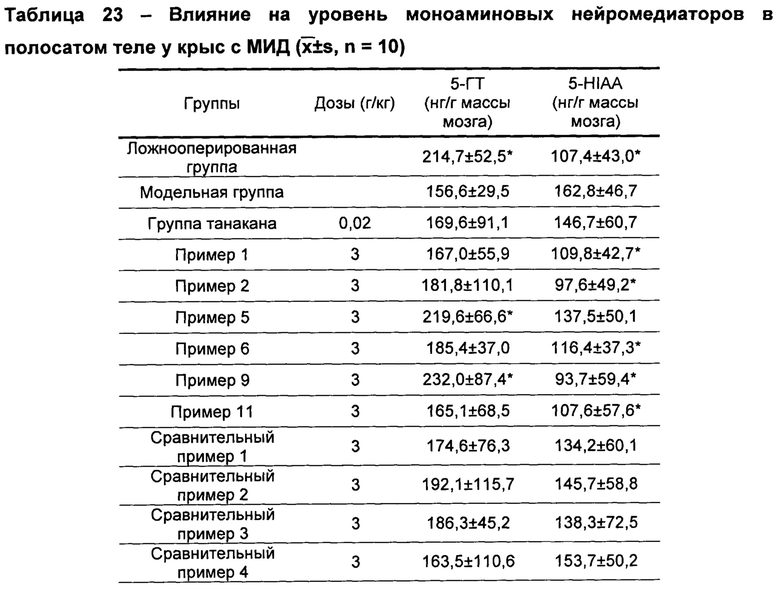
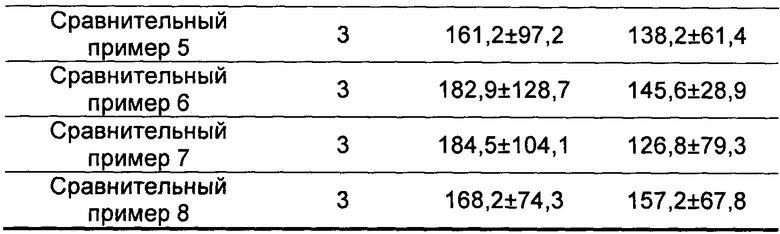
PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
(3) Влияние на содержание моноаминовых нейромедиаторов гиппокампа
Через 100 дней после создания моделей (через 90 дней после введения), по сравнению с модельной группой, для ложнооперированной группы содержание DA, 5-НТ и 5-HIAA в гиппокампе крыс было значительно повышено (Р<0,05~0,01), содержание NE было повышено, но статистическая значимость отсутствовала; для групп китайских лекарственных композиций согласно настоящему изобретению содержание NE, DA и 5-НТ было значительно повышено (Р<0,05~0,01); для групп китайских лекарственных композиций согласно сравнительным примерам содержание 5-НТ было значительно повышено (Р<0,05); для сравнительной группы лекарства танакана значительных различий для каждого из показателей не наблюдалось. См. таблицу 24.

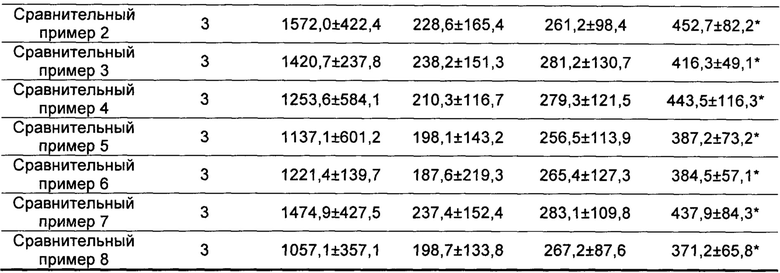
PS: по сравнению с модельной группой, *Р<0,05; **Р<0,01
Краткий вывод:
Исследования подтверждают, что возможность возникновения деменции вследствие церебрального инфаркта связана в основном с размером, количеством и локализацией очаговых поражений, возникающих при церебральном инфаркте. Исследования показали, что, если объем очагового поражения при инфаркте превышает 50 мл, он может сочетаться с деменцией, если этот объем превышает 100 мл, он часто сочетается с деменцией; в результате исследований также было обнаружено, что среди пациентов с СД, пациенты с большой площадью очаговых поражений при инфаркте составляли 11,2% случаев, пациенты с малой площадью очаговых поражений при инфаркте составляли 88,8% случаев, пациенты с множественными очаговыми поражениями при инфаркте составляли 97,6% случаев, и это позволяет предположить, что малый объем очаговых поражений также может вызывать деменцию, в частности, чем больше количество очаговых поражений при инфаркте, тем выше частота возникновения деменции. Также существуют исследования, подтверждающие, что локализация церебрального инфаркта является ключевым фактором, приводящим к деменции; в большинстве сообщений упоминалось, что инфаркты, приводящие к очаговым изменениям перивентрикулярного белого вещества, обнаруживаемым с помощью КТ, значительно увеличивали частоту возникновения деменции. Исследования, основанные на модели мультиинфарктной деменции (МИД), содержат рекомендации по определению эффективности лечения СД с применением лекарственных средств.
Механизмы обучения и памяти в головном мозге в основном включают нейрофизиологические механизмы и нейрохимические механизмы, причем нейрофизиологические механизмы фокусируются на локализации памяти в головном мозге и сопутствующих процессах биоэлектрической активности, а нейрохимический механизм в основном объясняет влияние нейромедиаторов, нейропептидов и биологических макромолекул на обучение и память и их связь. Нейропептид обычно относится к эндогенному активному веществу, он присутствует в нервной ткани и участвует в функционировании нервной системы, являясь своего рода специфическим информационным веществом. Нейропептид характеризуется низким содержанием, высокой активностью, обширным и сложным эффектом, регулирующим самые разнообразные физиологические функции организма, такие как боль, сон, настроение, обучение и память, а также дифференцировку и развитие самой нервной системы; все эти процессы регулируются нейропептидом. Соматостатин (SS) является нейроактивным пептидом, который широко распространен в нервной системе, наивысшее содержание SS обнаружено в гипоталамусе и коре головного мозга и гиппокампе, такое распределение связано с его регуляцией когнитивной функции. SS в тканях головного мозга обладает положительной регуляторной ролью для обучения и памяти, сигнальные пути SS, регулирующие обучение и память, представляют собой: первый, прямой путь, опосредован возбуждением SS-чувствительных нервов, что вызывает увеличение притока кальция, а второй возможно опосредован другими нервными путями. SS-нейроны и холинергические нейроны очень близки и имеют синаптические связи, что свидетельствует об их функциональном контакте: SS может способствовать высвобождению ацетилхолина, который влияет на функции обучения и памяти. Эндотелии (эндотелин-1, ЕТ) является результатом недавнего углубленного изучения вазоактивного пептида, он является нейромедиатором и обладает сильными сосудосуживающими свойствами, широко распространен в различных органах тела, кроме способности вызывать сужение сосудов, ЕТ также способен вызывать прямое повреждение нейронов и глиальных клеток, у пациентов с геморрагическим, ишемическим цереброваскулярным заболеванием концентрации ЕТ в плазме были значительно повышены, наблюдается значительная положительная корреляция между уровнями ЕТ и размерами очаговых поражений при церебральном инфаркте. ЕТ действует на нервные клетки, вызывает кальциевую перегрузку нервных клеток и способствует образованию свободных радикалов, что еще больше усугубляет повреждение головного мозга. Нейропептид Y (NPY) является активным полипептидом, состоящим из 36 аминокислот, в центральной нервной системе он в основном локализуется в коре головного мозга, гиппокампе, таламусе, гипоталамусе и стволе головного мозга, самая высокая концентрация NPY обнаружена в гиппокампе, и гиппокамп представляет собой ключевой участок головного мозга, который регулирует обучение и память. NPY первоначально синтезируется внутри нервных клеток, затем транспортируется к нервным окончаниям и хранится в везикулах, и он сосуществует с классическими нейромедиаторами, такими как норэпинефрин, эпинефрин, y-аминомасляная кислота и соматостатин. NPY не только тесно связан с долговременной памятью, но также оказывает влияние на кратковременную память. NPY выполняет свою биологическую роль главным образом посредством своих рецепторов, и современные исследования позволяют предположить, что экспрессия мРНК рецептора Y2 в гиппокампе наиболее распространена, регулирование рецепторов при обучении и запоминании может представлять собой механизм долговременной потенциации передачи (long-transfer potentiation, LTP). По причине наличия вышеуказанной корреляции между уровнями нейропептидов и способностями к обучению и запоминанию и их корреляцией с уровнями холинергических и адренергических нейромедиаторов, авторы настоящего изобретения исследовали содержание нейропептидов в плазме, уровни моноаминовых нейромедиаторов в коре головного мозга, полосатом теле, гиппокампе и эффекты лекарственных средств в модели МИД на крысах.
В проведенном эксперименте в сонную артерию вводили микросферы для создания модели мультиинфарктной деменции (МИД) на крысах. Результаты показали, что через 24 часа у модельных животных возникало нейроповеденческое расстройство, развивался множественный инфаркт, через 10 дней происходил разжижающий некроз тканей головного мозга в очагах инфарктического поражения, уменьшалась толщина коры головного мозга, происходила атрофия гиппокампа, массы коры головного мозга, стриатума, гиппокампа значительно уменьшались, появлялись нарушения процессов обучения и памяти, содержание 5-НТ, 5-HIAA в коре головного мозга и гиппокампе значительно снижалось, содержание DA имело тенденцию к уменьшению, но статистическая значимость отсутствовала (Р<0,01), содержание NPY в плазме было значительно снижено, содержание ЕТ было значительно повышено, содержание SS и CGRP имело тенденцию к уменьшению.
После 30~90 дней введения крысам с помощью желудочного зонда китайских лекарственных композиций согласно настоящему изобретению (через 40~100 дней после создания моделей), по сравнению с модельной группой, время пребывания в водном лабиринте Морриса крыс группы китайских лекарственных композиций согласно настоящему изобретению было значительно уменьшено, способности к обучению и памяти были значительно увеличены; после 90 дней введения масса гиппокампа была значительно увеличена (Р<0,05), содержание 5-НТ, 5-HIAA и DA в коре головного мозга, содержание 5-НТ, 5-HIAA в полосатом теле и содержание NE, DA, 5-НТ в гиппокампе было значительно повышено (Р<0,05~0,01), содержание NPY и SS в плазме было значительно повышено, содержание ЕТ было значительно снижено. Следует указать, что содержание нейромедиаторов, связанных с обучением и памятью, в головном мозге крыс с МИД может быть увеличено путем применения китайских лекарственных композиций согласно настоящему изобретению, таким образом, китайские лекарственные композиции согласно настоящему изобретению обладают терапевтическим эффектом при сосудистой деменции. Кроме того, по данным сравнительных экспериментов можно видеть, что эффекты китайских лекарственных композиций согласно настоящему изобретению были лучше, чем аналогичные эффекты китайских лекарственных композиций согласно сравнительным примерам, и результаты были статистически значимыми.
Изобретение относится к фармацевтической промышленности, а именно к композиции для предотвращения или лечения сердечно-сосудистых и цереброваскулярных заболеваний и/или деменции. Китайская лекарственная композиция для предотвращения или лечения сердечно-сосудистых и цереброваскулярных заболеваний и/или деменции, полученная из лекарственного сырья, состоящего из ингредиентов со следующим массовым соотношением: 1 часть женьшеня, 0,8-1,5 части листьев гинкго, 0,018-0,030 части рылец шафрана. Способ получения китайской лекарственной композиции. Китайский лекарственный состав для предотвращения или лечения сердечно-сосудистых и цереброваскулярных заболеваний и/или деменции. Применение китайской лекарственной композиции или китайского лекарственного состава для получения лекарственного средства для предотвращения или лечения сердечно-сосудистых и цереброваскулярных заболеваний и/или деменции. Вышеописанная композиция обладает повышенным эффектом для предотвращения или лечения сердечно-сосудистых и цереброваскулярных заболеваний и/или деменции. 4 н. и 9 з.п. ф-лы, 24 табл., 10 пр.
1. Китайская лекарственная композиция для предотвращения или лечения сердечно-сосудистых и цереброваскулярных заболеваний и/или деменции, полученная из лекарственного сырья, состоящего из ингредиентов со следующим массовым соотношением: 1 часть женьшеня, 0,8-1,5 части листьев гинкго, 0,018-0,030 части рылец шафрана.
2. Китайская лекарственная композиция по п. 1, отличающаяся тем, что сырье для получения указанной китайской лекарственной композиции представляет собой лекарственное сырье со следующим массовым соотношением ингредиентов: 1 часть женьшеня, 1 часть листьев гинкго, 0,018-0,030 части рылец шафрана.
3. Китайская лекарственная композиция по п. 2, отличающаяся тем, что сырье для получения указанной китайской лекарственной композиции представляет собой лекарственное сырье со следующим массовым соотношением ингредиентов: 1 часть женьшеня, 0,9-1,2 части листьев гинкго, 0,020-0,025 части рылец шафрана.
4. Китайская лекарственная композиция по п. 3, отличающаяся тем, что сырье для получения указанной китайской лекарственной композиции представляет собой лекарственное сырье со следующим массовым соотношением ингредиентов: 1 часть женьшеня, 1 часть листьев гинкго, 0,020-0,025 части рылец шафрана.
5. Китайская лекарственная композиция по п. 4, отличающаяся тем, что сырье для получения указанной китайской лекарственной композиции представляет собой лекарственное сырье со следующим массовым соотношением ингредиентов: 1 часть женьшеня, 1 часть листьев гинкго, 0,022 части рылец шафрана.
6. Способ получения китайской лекарственной композиции по любому из пп. 1-5, включающий стадию взвешивания женьшеня, листьев гинкго и рылец шафрана в массовом соотношении 1: 0,8-1,5: 0,018-0,030, стадию получения экстракта женьшеня, стадию получения экстракта листьев гинкго, стадию получения экстракта рылец шафрана, стадию смешивания указанных экстракта женьшеня, экстракта листьев гинкго и экстракта рылец шафрана.
7. Способ по п. 6, отличающийся тем, что на стадии получения экстракта женьшеня основной получаемый компонент представляет собой общую фракцию гинзенозидов; на стадии получения экстракта листьев гинкго основной получаемый компонент представляет собой общую фракцию флавоноидов и общую фракцию лактонов, содержащихся в листьях гинкго; на стадии получения экстракта рылец шафрана основной получаемый компонент представляет собой общую фракцию гликозидов, содержащихся в рыльцах шафрана.
8. Способ по п. 7, отличающийся тем, что стадии получения экстракта женьшеня следующие: женьшень измельчают в порошок, затем 2 раза подвергают экстракции с этанолом при нагревании с обратным холодильником, фильтруют, снижают давление в полученном фильтрате с извлечением растворителя до достижения относительной плотности 1,12-1,14 при 70°С, добавляют воду в количестве, в 2-6 раз превышающем количество неочищенного лекарственного средства, для гомогенного перемешивания, затем смесь охлаждают с образованием осадка, супернатант выгружают на макропористую адсорбирующую смолу, и указанную смолу, содержащую лекарственное средство, сначала промывают дистиллированной водой, затем элюируют этанолом, этанольный элюент собирают и концентрируют досуха с получением экстракта женьшеня;
стадии получения экстракта листьев гинкго следующие: к крупнодисперсному порошку листьев гинкго добавляют теплый этанол, покрывая порошок, фильтруют, и остаток с фильтра погружают в теплый этанол, повторно фильтруют, полученные фильтраты объединяют и концентрируют при пониженном давлении до достижения относительной плотности 1,12-1,14 при 70°С, добавляют воду в количестве, в 2-6 раз превышающем количество неочищенного лекарственного средства, перемешивают до гомогенного состояния, затем охлаждают с образованием осадка, фильтруют, фильтрат выгружают на макропористую адсорбирующую смолу, и указанную смолу, содержащую лекарственное средство, сначала промывают дистиллированной водой, затем элюируют этанолом, этанольный элюент собирают и концентрируют до достижения относительной плотности 1,02-1,04 при 70°С, его подвергают экстракции смесью этилацетат:н-бутиловый спирт, экстракты объединяют и сбрасывают давление с извлечением растворителя с получением экстракта листьев гинкго;
стадии получения экстракта рылец шафрана следующие: к лекарственному сырью в виде рылец шафрана добавляют холодный этанол с покрытием рылец шафрана, затем фильтруют, к остаткам повторно добавляют холодный этанол с покрытием, далее фильтруют, полученные фильтраты объединяют, концентрируют при пониженном давлении до достижения относительной плотности 1,12-1,14 при 70°С, добавляют воду, затем смесь выгружают на макропористую адсорбирующую смолу, и указанную смолу, содержащую лекарственное средство, сначала промывают дистиллированной водой, затем элюируют этанолом, этанольный элюент концентрируют до достижения относительной плотности 1,02-1,04 при 70°С и концентрируют досуха с получением экстракта рылец шафрана.
9. Китайский лекарственный состав для предотвращения или лечения сердечно-сосудистых и цереброваскулярных заболеваний и/или деменции, состоящий из китайской лекарственной композиции по любому из пп. 1-5 или китайской лекарственной композиции, полученной по способу по любому из пп. 6-8, и по меньшей мере одного фармацевтически приемлемого вспомогательного вещества.
10. Применение китайской лекарственной композиции по любому из пп. 1-5, китайской лекарственной композиции, полученной по способу по любому из пп. 6-8, или китайского лекарственного состава по п. 9 для получения лекарственного средства для предотвращения или лечения сердечно-сосудистых и цереброваскулярных заболеваний и/или деменции.
11. Применение по п. 10, отличающееся тем, что указанные сердечно-сосудистое и цереброваскулярное заболевание выбраны из по меньшей мере одного из следующих заболеваний: ишемического цереброваскулярного заболевания, коронарной болезни сердца или стенокардии.
12. Применение по п. 10, отличающееся тем, что указанная деменция выбрана из сенильной деменции.
13. Применение по п. 10, отличающееся тем, что указанная деменция представляет собой сосудистую деменцию.
| Устройство для приема и обнаружения комбинации двоичных сигналов | 1987 |
|
SU1413656A1 |
| Противоблокировочная тормозная система транспортного средства | 1988 |
|
SU1562186A1 |
| WO 2007118363 A1, 25.10.2007 | |||
| КИТАЙСКИЙ ЛЕКАРСТВЕННЫЙ СОСТАВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2006 |
|
RU2408384C2 |
Авторы
Даты
2018-12-06—Публикация
2015-12-29—Подача