Настоящее изобретение относится к области биотехнологии, а именно к технологии создания тканей, органов, тканеинженерных конструкций. Также настоящее изобретение относится к области медицины, а именно к биотрансплантатам для регенерации костной ткани при хирургическом лечении деструктивных, дегенеративно-дистрофических, травматических или врожденных поражений костной ткани.
В ряде случаев заболевания или пороки развития приводят к потере костной ткани в связи с развитием различных патологических процессов [Григорьян А.С., Топоркова А.В. Проблемы интеграции имплантатов в костную ткань (теоретические аспекты). М.: Техносфера, 2007, 130 с.]. Хирургическое лечение дефицита и дефектов костной ткани направлено на восстановление утраченных тканей в их оригинальной гистоархитектонике и функции. В настоящее время, в широкой клинической практике распространены имплантационные материалы для направленной костной регенерации. Эффективность восстановления костной ткани в таком случае при хирургическом лечении, главным образом, зависит от свойств имплантационных материалов, которыми замещается дефект.
Известны материалы для имплантации в ткани на основе резорбируемых и нерезорбируемых остеоиндуктивных веществ, которые могут быть минерального или биологического происхождения. Так, известна имплантация в поднадкостничную область материалов на основе коллагена, содержащих костный порошок гидроксиапатитов, трикальцийфосфатов с применением лекарственных средств гликозаминогликанов [RU 2159101 С1, 25.03.99].
Известен биосовместимый материал для стоматологии, включающий неорганические соли, коллаген, сульфатированные гликозаминогликаны и воду [RU 2155024 C1, 25.11.2000].
Также широко используются различные виды костных ауто-, алло- и ксенотрансплантатов. Известно использование различного вида культур клеток, чаще фибробластов, в качестве оптимизаторов раневого заживления в хирургической пародонтологии [Fang В, Song Y, Lin Q, Zhang Y, Cao Y, Zhao R C, Ma Y. Human adipose tissue derived mesenchymal stromal cells as salvage therapy for treatment of severe refractory acute grafts vs. host disease in two children. Pediatr Transplant. 2007 Nov; 11(7): 8147].
Ближайшим аналогом заявленного изобретения является биотрансплантат для восстановления объема костной ткани при дегенеративных заболеваниях и травматических повреждениях костей [RU 2530622]. Изобретение характеризуется тем, что содержит аутологичные мультипотентные мезенхимальные стромальные клетки пациента и матрицу-носитель, имеющую в основе своей структуры коллаген-минеральный комплекс, идентичный по составу натуральному костному материалу, отличающийся тем, что содержит смесь мультипотентных мезенхимальных стромальных клеток (ММСК), культивированных в стандартных условиях, и мультипотентных мезенхимальных стромальных клеток, дифференцированных в остеогенном направлении, взятых в соотношении 1:1 и в количестве 10 клеток на 1 г веса матрицы-носителя. В аспекте способа получения, данное изобретение характеризуется тем, что подготавливают жировую ткань, полученную у пациента, измельчают, ферментативно дезагрегируют; полученную суспензию фильтруют, центрифугируют и ресуспендируют в культуральной среде; суспензию ММСК высевают на чашки Петри диаметром 100 мм, инкубируют при 37°C в атмосфере 5% CO2 до первого пассажа, дифференцируют в остеогенной культуральной среде с добавлением аскорбиновой кислоты и Дексаметазона; культивирование осуществляют в конфлюентном монослое в течение 2 недель, меняя среду на свежую каждые 3 дня; матрицу-носитель, представляющую собой коллаген-минеральный комплекс, размягчают и перемешивают с суспензией клеток, отличающийся тем, что подготавливают аутологичную сыворотку крови пациента, после центрифугирования суспензию клеток высаживают в количестве 1×103 клеток на чашку Петри в стандартную среду культивирования AdvanceSTEMTM /Antibiotic/Antimycotic Solution 100х с добавлением 10% аутологичной сыворотки крови пациента; после первого пассажа клетки снимают с подложки и разделяют на 2 равные части: одну часть ММСК продолжают культивировать в стандартных условиях, а другую дифференцируют в остеогенном направлении в течение 2 недель, затем клетки снимают с подложек и смешивают в соотношении 1:1; после чего их смешивают с матрицей-носителем в количестве 107 клеток на 1 г веса матрицы-носителя и инкубируют в течение суток при 37°C в атмосфере 5% CO2.
Недостатком данного изобретения является низкая эффективность регенерации поврежденных тканей, обусловленная низким уровнем ангиогенеза и, как следствие, остеогенеза мультипотентных мезенхимальных стромальных клеток, находящихся в составе биотрансплантата. Причиной этого является низкая плотность заселения биотрансплантата клетками, культивированными в виде монослоя.
Таким образом, задачей заявленного изобретения является повышение уровня ангиогенеза мультипотентных мезенхимальных стромальных клеток, а также повышение эффективности регенерации поврежденных тканей при использовании биотрансплантатов для регенерации костной ткани при хирургическом лечении деструктивных, дегенеративно-дистрофических, травматических или врожденных поражений костной ткани, содержащих мультипотентные мезенхимальные стромальные клетки и матрицу-носитель в виде биокомпозиционного материала.
Решение поставленной задачи обеспечивается тем, что клеточная культура для создания тканей, органов, тканеинженерных конструкций содержит мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов, а также тем, что биотрансплантат для регенерации костной ткани при хирургическом лечении деструктивных, дегенеративно-дистрофических, травматических или врожденных поражений костной ткани содержит мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов и матрицу-носитель в виде биокомпозиционного материала.
Мультипотентные мезенхимальные стромальные клетки (ММСК) - мультипотентные стволовые клетки, способные дифференцироваться в остеобласты (клетки костной ткани), хондроциты (хрящевые клетки) и адипоциты (жировые клетки) [Pittenger et al., 1999; Caplan, 1991]. Данные клетки претерпевают ассиметричное деление, в результате которого одна дочерняя клетка переходит на новую ступень дифференцировки, а вторая - остается копией материнской клетки и сохраняет способность к самообновлению. После рождения и на протяжении всей жизни ММСК остаются клеточным резервом, участвующим в физиологическом обновлении тканей и патологической репарации, и присутствуют в костном мозге, жировой ткани, пульпе зуба. Во многих работах в области тканевой инженерии такие клетки были использованы в качестве источника клеток, обеспечивающих начало процесса регенерации. Первое успешное выделение ММСК костного мозга относится к 1970 году [Friedenstein et al., 1970]. В основе выделения авторы использовали принцип адгезии клеток к пластику, в данный момент наиболее точной методикой является выделение с помощью проточного цитофлуориметра или магнитного сортинга на основании экспрессии определенных поверхностных антигенов [Lee et al., 2006; Smith et al., 2004]. Фенотипически ММСК отличаются отсутствием экспрессии маркеров гемопоэтических клеток: CD34, CD45, CD14, glycophorin А и CD133. Также в ММСК отсутствует секреция МНС II, Т-клеточных костимулирующих факторов (В7-1, В7-2, CD40, CD40L), рецепторов к матриксу (CD65L, CD65P), к факторам роста (CD1200A, TGFbIIR), маркеров предшественников остеогенных клеток - STRO-1, щелочная фосфатаза, остеонектин, остеокальцин. ММСК идентифицируются по экспрессии Thy-1 (CD90), CD105, VCAM-1, CD44. Также ММСК экспрессируют CD29, CD51 (интегрины) и характерные для МСК SH2, SH3. Характерными для ММСК являются виментин, фибронектин, коллаген I и III, VI типов и т.н. osteoblast-specific factor. Таким образом, ММСК могут служить привлекательным источником клеток для тканевой инженерии и при регенерации костной ткани [Мао, 2005].
Комитет по мезенхимальным и стромальным стволовым клеткам Международного общества клеточной терапии установил следующие стандартные критерии ММСК для научных и доклинических исследований:
1. Клетки должны обладать адгезией к стандартному пластику для культивирования in vitro при стандартных условиях культивирования.
2. Более 95% клеточной популяции должны демонстрировать экспрессию специфических поверхностных маркеров: CD105, CD73, CD90, но не CD45, CD34, CD14 или CD11b, CD79a или CD 19 и HLA class II (положительная экспрессия данных маркеров допустима в количестве менее 2%).
3. Клетки должны обладать способностью к дифференцировке по остеогенному, хондрогенному и адипогенному пути.
Способность клеток к адгезии к стандартному пластику является важным свойством ММСК и уравнивает уникальные субпопуляции ММСК, так как характерна для всех их типов. Протоколы, в которых описывали ММСК, не обладающие адгезией к пластику, предлагали использование очень специфических условий культивирования. В таких случаях требуется культивирование клеток в стандартных условиях, чтобы доказать их принадлежность к популяции ММСК.
Определение экспрессии поверхностных антигенов - быстрый и точный способ идентифицировать клеточную популяцию. Для идентификации ММСК предлагают исследовать экспрессию следующих маркеров: CD 105 - эндоглин, распознается Mab SH2; CD 73-5'нуклеотидаза, распознается Mab SH3 или SH4, и CD90, известного также как Thy-1. Чтобы не получить гетерогенную популяцию клеток, стоит проверить их на предмет экспрессии маркеров гемопоэтического ряда клеток: CD45, CD34, CD14 или CD11b, CD79a или CD19 и HLA class II (последний может экспрессироваться только при обработке культуры ММСК интерфероном-γ).
Наиболее уникальным свойством ММСК является способность к дифференцировке в трех направлениях: остеогенном, хондрогенном и адипогенном. Таким образом, клетки должны демонстрировать in vitro дифференцировку при культивировании их в стандартных условиях для дифференцировки по одному из этих путей. Дифференцировка в остеобласты может быть продемонстрирована с помощью окраски клеток ализариновым красным или по методу ван Косса. Адипогенная дифференцировка может быть показана окрашиванием Oil Red О. Дифференцировка в хондробласты может быть продемонстрирована с помощью окрашивания альциановым синим, или с помощью антител к коллагену II типа [Minimal criteria for defining multipotent mesenchymal stromal cells. The International Society for Cellular Therapy position statement. Dominici, M. et al. Cytotherapy, Volume 8, Issue 4,315-317].
Адгезивная культура мультипотентных мезенхимальных стромальных клеток представляет собой клетки, растущие двумерным монослоем на плоской поверхности. Такая культура обладает низким уровнем стабильности по той причине, что клетки, прикрепленные к подложке или матрице, контактируют с другими клетками с образованием межклеточных контактов только в одной плоскости. При длительном культивировании в монослое мультипотентные мезенхимальные стромальные клетки теряют одно из важнейших свойств - эпителио-мезенхимную пластичность [Сабурина И.Н. Эпителио-мезенхимальная пластичность мультипотентных мезенхимальных стромальных клеток в норме и патологии (экспериментальное исследование). Диссертация на соискание степени д.б.н. 2010. М. 195 с], что приводит к снижению эффективности ангиогенеза и, как следствие, остеогенеза мультипотентных мезенхимальных стромальных клеток, находящихся в составе биотрансплантата. Это, в свою очередь, приводит к снижению эффективности регенерации поврежденных тканей при использовании биотрансплантатов, содержащих мультипотентные мезенхимальные стромальные клетки для регенерации костной ткани при хирургическом лечении деструктивных, дегенеративно-дистрофических, травматических или врожденных поражений костной ткани.
Органы и ткани имеют трехмерную клеточную организацию, в рамках которой клетки образуют сложные комплексы контактов с другими клетками и внеклеточным матриксом, формируя уникальное микроокружение. Подобные структуры могут быть получены в виде клеточных сфероидов. Наличие сформированных контактов и элементов внеклеточного матрикса, а также высокая плотность клеток в сфероидах приближает их к нативным тканям. Этим и обусловлена повышенная стабильность мультипотентных мезенхимальных стромальных клеток, культивированных в виде сфероидов, по сравнению с двухмерными клеточными культурами. Культивирование мультипотентных мезенхимальных стромальных клеток в виде сфероидов поддерживает их эпителио-мезенхимную пластичность. Это, в свою очередь, повышает эффективность ангиогенеза и, как следствие, остеогенеза мультипотентных мезенхимальных стромальных клеток, находящихся в составе биотрансплантата. Повышается эффективность регенерации поврежденных тканей при использовании биотрансплантатов, содержащих мультипотентные мезенхимальные стромальные клетки для регенерации костной ткани при хирургическом лечении деструктивных, дегенеративно-дистрофических, травматических или врожденных поражений костной ткани.
Как вариант осуществления изобретения, мультипотентные мезенхимальные стромальные клетки могут быть культивированы в виде сфероидов со средним размером 50-200 мкм.
Как вариант осуществления изобретения, мультипотентные мезенхимальные стромальные клетки могут быть культивированы в виде сфероидов с гладкой поверхностью.
Как вариант осуществления изобретения, мультипотентные мезенхимальные стромальные клетки на поверхности сфероидов могут находиться в виде эпителиального фенотипа.
Настоящее изобретение также обеспечивает способ получения клеточной культуры для создания тканей, органов, тканеинженерных конструкций, содержащей мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов, который включает в себя следующие стадии:
- изолирование фрагмента ткани донора,
- перенос фрагмента ткани донора в среду, содержащую культуральную среду, аминокислоту и антибиотик, механическое измельчение фрагмента ткани донора с получением гомогената,
- инкубирование полученного гомогената в растворе протеолитических ферментов при 37°С до момента получения клеточной суспензии,
- добавление питательной среды, содержащей культуральную среду, аминокислоту, антибиотик, сыворотку крови,
- центрифугирование клеточной суспензии до момента полного осаждения клеток,
- удаление супернатанта,
- ресуспендирование выделенных клеток в питательной среде, содержащей культуральную среду, аминокислоту, антибиотик, сыворотку крови,
- культивирование выделенных клеток в монослойной культуре при 37°С в среде 5% СО2 как минимум 2 пассажа,
- дезагрегация монослоя,
- культивирование в неадгезивных условиях клеток как минимум 2-го пассажа в концентрации от 1×106 кл/мл до 5×106 кл/мл в питательной среде, содержащей культуральную среду, аминокислоту, антибиотик, сыворотку крови, фактор индукции ангиогенеза с получением клеточной культуры, содержащей мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов.
Как вариант осуществления изобретения, культивирование клеток в питательной среде, содержащей культуральную среду, аминокислоту, антибиотик, сыворотку крови, фактор индукции ангиогенеза осуществляется до момента образования гладкой поверхности сфероидов.
Как вариант осуществления изобретения, в качестве ткани донора используется жировая ткань.
Как вариант осуществления изобретения, в качестве ткани донора используется ткань пупочного канатика.
Как вариант осуществления изобретения, в качестве ткани донора используется ткань костного мозга.
Как вариант осуществления изобретения, в качестве культуральной среды используется среда DMEM.
Как вариант осуществления изобретения, в качестве культуральной среды используется среда F12.
Как вариант осуществления изобретения, в качестве культуральной среды используется смесь культуральной среды DMEM и культуральной среды F12 в соотношении 1 к 1 по объему.
Как вариант осуществления изобретения, в качестве культуральной среды используется смесь культуральной среды DMEM и культуральной среды F12 в соотношении 2 к 1 по объему.
Как вариант осуществления изобретения, в качестве культуральной среды используется среда α-МЕМ.
Как вариант осуществления изобретения, в качестве аминокислоты используется L-глутамин.
Как вариант осуществления изобретения, в качестве антибиотика используется гентамицин.
Как вариант осуществления изобретения, в качестве антибиотика используется смесь пенициллина со стрептомицином.
Как вариант осуществления изобретения, в качестве антибиотика используется амфотерицин В.
Как вариант осуществления изобретения, в качестве раствора протеолитических ферментов используется раствор коллагеназы первого типа и диспазы.
Как вариант осуществления изобретения, в качестве раствора протеолитических ферментов используется раствор коллагеназы первого типа.
Как вариант осуществления изобретения, в качестве раствора протеолитических ферментов используется раствор диспазы.
Как вариант осуществления изобретения, в качестве раствора протеолитических ферментов используется раствор трипсина.
Как вариант осуществления изобретения, в качестве раствора протеолитических ферментов используется раствор коллагеназы второго типа и диспазы.
Как вариант осуществления изобретения, в качестве раствора протеолитических ферментов используется раствор коллагеназы второго типа.
Как вариант осуществления изобретения, в качестве сыворотки крови используется эмбриональная телячья сыворотка.
Как вариант осуществления изобретения, в качестве сыворотки крови используется аутологичная сыворотка крови пациента.
Как вариант осуществления изобретения, в качестве фактора индукции ангиогенеза используется фактор роста эндотелия сосудов.
Как вариант осуществления изобретения, в качестве фактора индукции ангиогенеза используется кондиционированная среда от эндотелиальных клеток вены пупочного канатика.
Как вариант осуществления изобретения, в качестве фактора индукции ангиогенеза используется основной фактор роста фибробластов.
Настоящее изобретение также обеспечивает способ получения биотранплантата для регенерации костной ткани при хирургическом лечении деструктивных, дегенеративно-дистрофических, травматических или врожденных поражений костной ткани, который включает в себя следующие стадии:
- стерилизация матрицы-носителя в виде биокомпозиционного материала,
- нанесение клеточной культуры, содержащей мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов, на поверхность матрицы-носителя в виде биокомпозиционного материала,
- инкубирование биокомпозиционного материала с нанесенной на его поверхность клеточной культурой, содержащей мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов, не менее 1 суток с получением биотрансплантата.
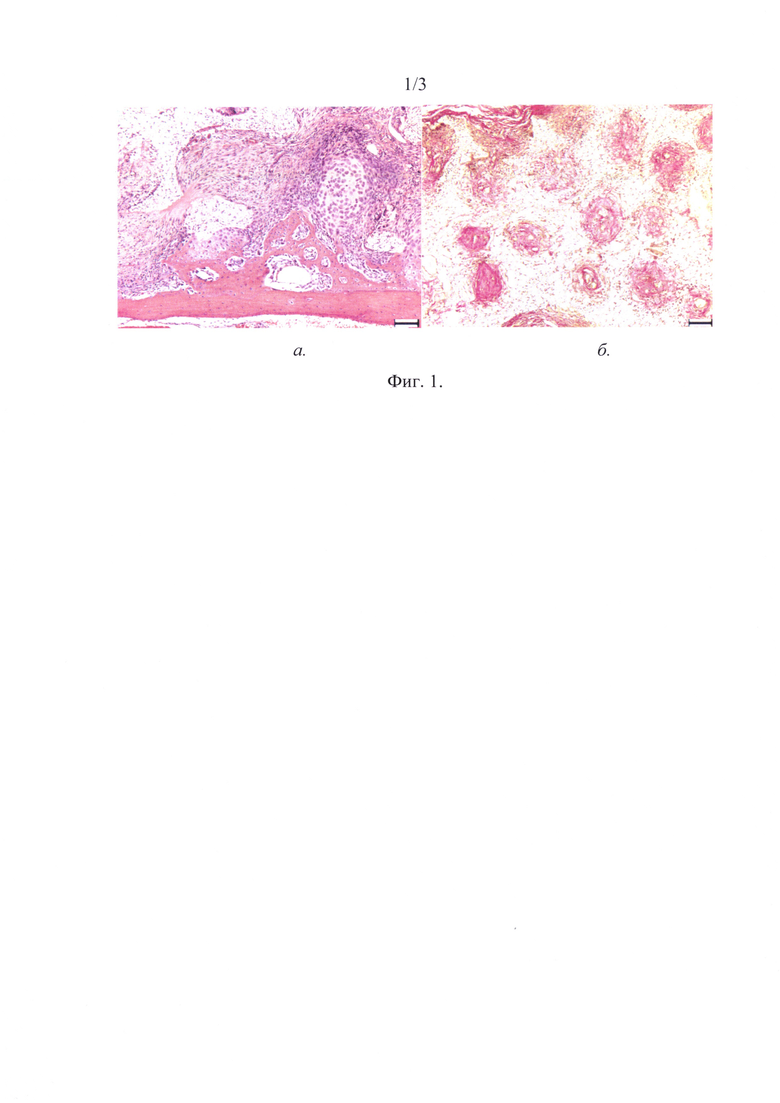
На фиг. 1 представлена фотография среза фрагмента нижней челюсти животного опытной группы на 21-ые сутки после остеоабразии и трансплантации биотрансплантата.
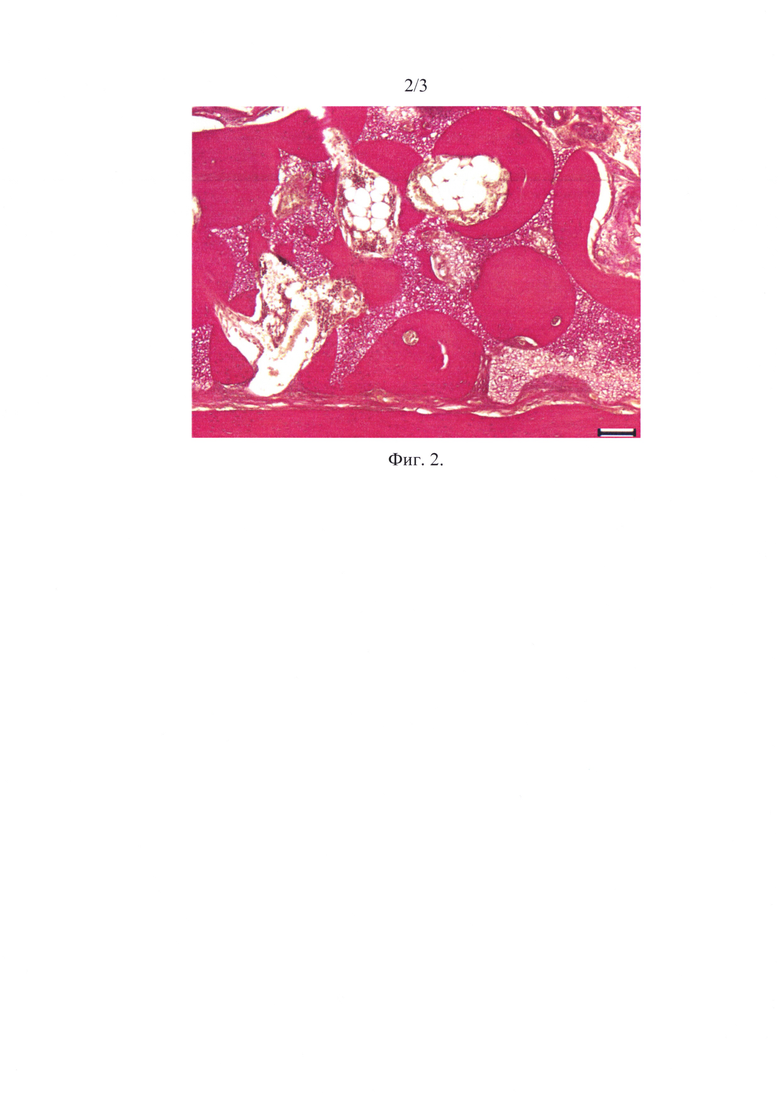
На фиг. 2 представлена фотография среза фрагмента нижней челюсти животного опытной группы на 120 - е сутки после остеоабразии и трансплантации биотрансплантата.
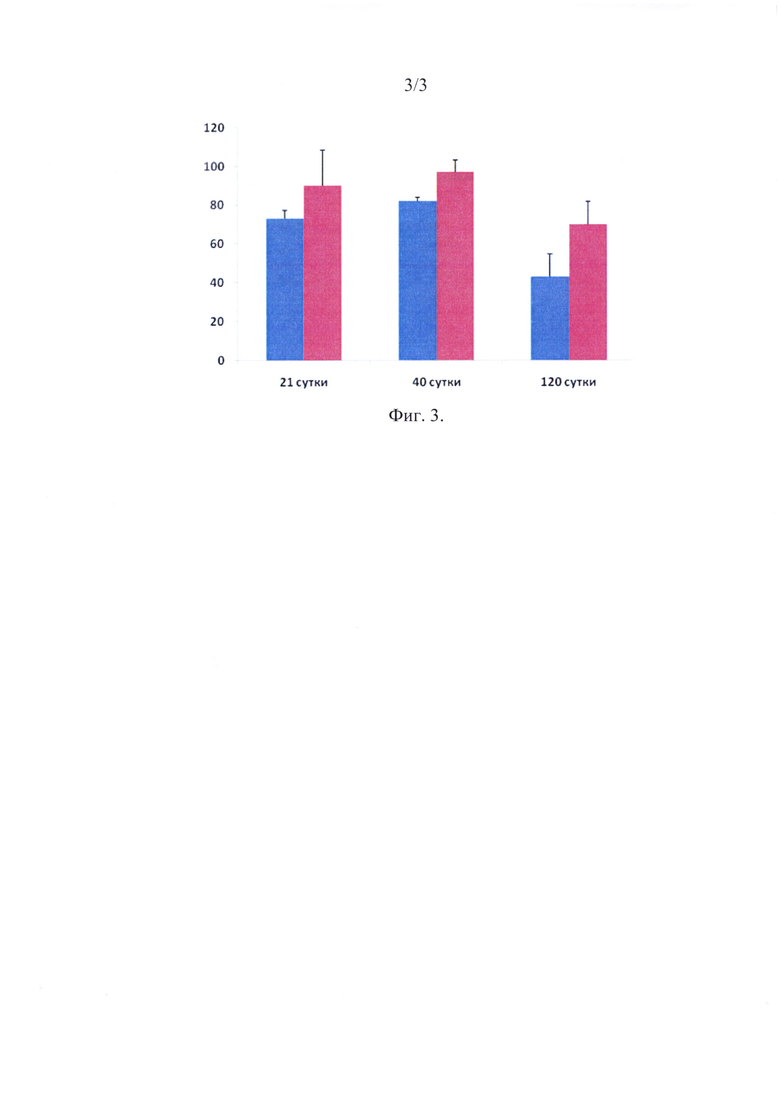
На фиг. 3 приведена диаграмма динамики изменения количества сосудов после трансплантации в группе положительного контроля (синий) и в опытной группе (красный) на разных сроках исследования.
Настоящее изобретение проиллюстрировано далее посредством следующих примеров.
Пример 1. Получение клеточной культуры для создания тканей, органов, а также тканеинженерных конструкций, содержащей мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов.
Выделение и монослойное культивирование аутологичных клеток.
Для выделения клеток стромально-сосудистой фракции у животных в процессе операции брали фрагменты ткани подкожного жира из области нижней части живота и выделяли по стандартному протоколу. Для этого, под общей анестезией рассекали кожу, отделяли гиподерму от мышц брюшной стенки, отрезали фрагмент подкожного жира и помещали его в среду для культивирования клеток, кожу зашивали. Полученную ткань в стерильных условиях измельчали, получив суспензию мелких фрагментов проводили их инкубацию в растворах коллагеназы 1-го типа (0,07%) и диспазы (0,025%) в течение 30 минут. После окончания инкубации в раствор с ферментами и тканью добавляли полную среду культивирования и центрифугировали в течение 5 мин при 1000 об/мин. Затем, слив супернатант, полученный осадок ресуспендировали в полной среде и пропускали через нейлоновый фильтр, для того чтобы избавиться от крупных фрагментов ткани. Полученную суспензию клеток помещали на чашки Петри и культивировали в течение 10 дней. Среду меняли каждые 3 дня, рассев осуществляли на 4-й и 8-й дни после выделения. Полная среда культивирования имеет следующий состав: DMEM/F12 с глутамином (ПанЭко), 1% пенициллин-стрептомицин (ПанЭко), 10% FCS (Fetal Calf Serum).
Получение клеточных сфероидов.
Из охарактеризованных монослойных 2D культур 4-ого пассажа получали 3D культуры - клеточные сфероиды с использованием специальных агарозных планшетов с лунками (Microtissue, США), посевная концентрация клеток составила 3×106 кл/мл. Агарозные планшеты помещали в 12-луночный культуральный планшет и культивировали в течение 7 суток в стандартных условиях (37°С, 5%СО2) в полной ростовой среде вышеуказанного состава с добавлением фактора роста эндотелия сосудов VEGF (10 нг/мл) для стимуляции эндотелиальных предшественников.
Характеристика полученных сфероидов. Получение полутонких срезов.
Сфероиды, зафиксированные в 3% растворе глутарового альдегида на фосфатно-солевом буфере (pH=7,4), дофиксировали 2 часа с помощью 1% OsO4 на фосфатно-солевом буфере (pH=7,4). Отмывали от фиксатора в растворе фосфатно-солевого буфера (pH=7,4), проводили по ряду восходящих спиртов: 50° (2 смены по 5 мин), 70° (ночь при +4°C), 96° (4 смены по 20 мин); обезвоживали в пропилен оксиде (5 мин), переносили в смеси пропилен оксид : аралдит 1 : 1 (60 мин), чистый аралдит (60 мин) и инкубировали в чистой смоле при +60°C до полной полимеризации. Полученные блоки серийно резали на ультратоме Leica ЕМ UC6 (Leica, Германия) (толщина среза 1 мкм). Срезы окрашивали 15 мин смесью толуидинового синего с бурой. При необходимости проводили дифференцировку окрашенных препаратов в воде и фоторегистрировали в видимом световом диапазоне под микроскопом Axiovert 25 {Carl Zeiss, Германия) с помощью цифровой камеры AxioCam HRC {Carl Zeiss, Германия).
Характеристика полученных сфероидов. Проточная цитофлуориметрия.
Полученные сфероиды ферментировали с применением 0.25% раствора трипсина для получения суспензии отдельных клеток. Полученную суспензию инкубировали с антителами к CD1 lb, CD14, CD19, CD29, CD31, CD45, CD90 и CD105 (Beckman Coulter). Анализ экспрессии проводили на проточном цитофлуориметре FC500 (Beckman Coulter, США) с помощью программного обеспечения СХР System.
Иммуноцитохимическое окрашивание
Для проведения иммуноцитохимического анализа сфероиды фиксировали в 4%-ном растворе параформальдегида (20 мин, 4°C), отмывали от фиксатора в растворе фосфатного-солевого буфера (pH=7,4; 3 смены по 5 минут) и инкубировали в течение ночи при 4°C с первичными антителами к маркерам эндотелиальных клеток CD31, Flk-1, vWF, VEGF. Затем сфероиды тщательно отмывали в растворе фосфатного-солевого буфера (pH=7,4) и инкубировали 1 час в темноте со вторичными антителами, конъюгированными с флуоресцентными метками. Ядра на препаратах докрашивали красителем бис-бензимид (Hoechst 33258, Serva). Препараты анализировали под лазерным сканирующим конфокальным микроскопом Olympus Fluoview FV10I (Olympus, Япония).
Результаты
Наблюдение за процессом формирования сфероидов при помощи прижизненной цейтраферной съемки показало, что уже в первые часы клетки формировали рыхлую структуру, которая в дальнейшем компактизировалась, и к седьмым суткам формировался плотный компактный сфероид с гладкой поверхностью. Гистологический анализ показал, что поверхность сфероидов представлена плотно упакованными уплощенными клетками, центральная зона состояла из рыхло расположенных клеток полигональной формы.
Проточная цитофлуориметрия показала, что клетки в составе сфероидов сохраняли экспрессию характерных для ММСК маркеров, в то же время повышалось количество CD34 + клеток - эндотелиальных прогениторов. Иммуноцитохимический анализ показал, что добавление в культуральную среду фактора роста эндотелия сосудов (VEGF) стимулировало появление в сфероидах ММСК, экспрессирующих маркеры эндотелиальных клеток: CD31, Flk-1, vWF, VEGF. При помещении индуцированных фактором роста эндотелия сосудов (VEGF) сфероидов в гель эндотелиальные прогениторные клетки формировали тубулоподобные ветвящиеся структуры, что доказывает ангиогенный потенциал полученных сфероидов. Таким образом, культивирование сфероидов в присутствии фактора роста эндотелия сосудов (VEGF) способствует поддержанию и активации популяции эндотелиальных прогениторов.
В результате была получена и охарактеризована клеточная культура для создания тканей, органов, а также тканеинженерных конструкций, содержащая мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов.
Пример 2. Получение биотрансплантата для регенерации костной ткани при хирургическом лечении деструктивных, дегенеративно-дистрофических, травматических или врожденных поражений костной ткани, содержащего клеточную культуру для создания тканей, органов, а также тканеинженерных конструкций, состоящую из мультипотентных мезенхимальных стромальных клеток, культивированных в виде сфероидов.
Для получения биоинженерной конструкции брали микропористый каркас из силикатной матрицы, в которой диспергирована биоактивная фаза (гидроксиапатит) в сочетании с трехкальциевым фосфатом Ca3(P04)2 в форме блоков неправильной формы размером примерно 0.5×0.5 см. Блоки помещали по два в каждую лунку четырехлуночного стерильного планшета и насыщали сфероидами по 250 сфероидов на блок в 150 мкл среды. Планшет помещали в инкубатор на 30 мин для обеспечения адгезии сфероидов к матрице. Через 40 мин в каждую лунку осторожно добавляли полную ростовую среду, пока она не покроет края матрицы со сфероидами, биотрансплантат использовали через 3 суток после заселения.
Для получения биоинженерных конструкций использован стерильный ячеистый биосовместимый остеокондуктивный апатитосиликатный композиционный материал с пористостью 60%, размером пор 50-500 мкм, по минеральному составу близкий к минеральному матриксу губчатой костной ткани. Материал имеет микропористый каркас из силикатной основы, в которой диспергирована биоактивная фаза - гидроксиапатит Са10(РО4)6(ОН)2 или гидроксиапатит в сочетании с трехкальциевым фосфатом Са3(РО4)2.
Исследование показало, что используемый материал не цитотоксичен, адгезивен и не влияет на пролиферативную активность клеток. При заселении матрицы сфероидами к 7 суткам наблюдали лишь единичные выселившиеся клетки. На самой матрице, как на поверхности, так и в порах, к 7 суткам формировался плотный слой клеток, которые экспрессировали остеопонтин и остеокальцин - маркеры остеогенной дифференцировки. При заселении матрицы сфероидами наблюдали также появление тубулоподобных структур.
В результате был получен биотрансплантат для регенерации костной ткани при хирургическом лечении деструктивных, дегенеративно-дистрофических, травматических или врожденных поражений костной ткани, содержащий клеточную культуру для создания тканей, органов, а также тканеинженерных конструкций, состоящую из мультипотентных мезенхимальных стромальных клеток, культивированных в виде сфероидов.
Пример 3. Исследование эффективности биотрансплантата для регенерации костной ткани при хирургическом лечении деструктивных, дегенеративно-дистрофических, травматических или врожденных поражений костной ткани, содержащего клеточную культуру для создания тканей, органов, а также тканеинженерных конструкций, состоящую из мультипотентных мезенхимальных стромальных клеток, культивированных в виде сфероидов.
Используемый в исследовании биотрансплантат
Используемый в исследовании биотрансплантат представляет собой биокомпозиционный материал, содержащий в своей матрице мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов с гладкой поверхностью и средним размером - 100 мкм.
Экспериментальные группы для трансплантации биоинженерной конструкции.
Исследование выполнено на 36 самцах крыс линии Sprague Dawley в возрасте 3-4 месяцев со средним весом 400 гр. Животных разделили на 3 группы: в первой группе (опытная группа) проводили пересадку биотрансплантата, содержащего мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов, и матрицу-носитель в виде биокомпозиционного материала (12 животных). Во второй группе (положительный контроль) проводили пересадку биотрансплантата на основе матрицы - носителя в виде биокомпозиционного материала, содержащего смесь мультипотентных мезенхимальных стромальных клеток, культивированных в стандартных условиях, и мультипотентных мезенхимальных стромальных клеток, дифференцированных в остеогенном направлении. Клетки взяты в соотношении 1:1 и в количестве 107 клеток на 1 г веса матрицы-носителя (12 животных). При этом клетки в составе биоинженерной конструкции культивированы в виде монослоя. В третьей группе (отрицательный контроль) проводили операцию по остеоабразии передней поверхности нижней челюсти без применения биотрансплантатов (12 животных).
Для определения влияния используемого биотрансплантата, аутологичные образцы, соответствующие номеру экспериментального животного, пересаживали в область угла нижней челюсти, также поступали при имплантации образцов в группе положительного контроля. Для контроля вклада собственных клеток надкостницы, закрывающей костную ткань нижней челюсти, в процесс репаративного остеогенеза проводили операцию остеоабразии без внесения биотрансплантатов (отрицательный контроль). Животных выводили из эксперимента помещением в СО2-камеру. Образцы фиксировались в 10% нейтральном формалине на 7, 21, 40 и 120 сутки. Для каждой экспериментальной группы на одну временную точку приходилось по три животных.
Операции по остеоабразии передней поверхности нижней челюсти и имплантации образцов.
Под общим наркозом рассекали кожу в области левой щеки, отсепаровывали мышцу, обнажали поверхность угла нижней челюсти, скальпелем проводили абразию данной поверхности вплоть до глубины 0,1-0,2 мм. Поверхность санировали стерильным марлевым тампоном, потом аккуратно прижимая соответствующий аутологичный образец пинцетом, фиксировали его к челюсти посредством титановой проволоки, рану обрабатывали антибиотиком и послойно ушивали.
Гистологический анализ фрагментов нижней челюсти после трансплантации биоинженерной конструкции или матрицы.
Зафиксированный в 10% нейтральном формалине фрагмент нижней челюсти с трансплантированным материалом подвергали декальцификации в Трилоне Б по общепринятой методике [Саркисова, Перова, 1996]. После декальцификации из каждого образца вырезали фрагмент ткани с участком имплантата толщиной примерно 5 мм, помещали его в одноразовую кассету и подвергали обработке в автомате для гистологической обработки тканей (STP 120, MICROM INTERNATIONAL GmbH, Германия). Производили заливку в парафин и формирование блоков с использованием станции для заливки в парафин, нарезали срезы толщиной 5 мкм, которые окрашивали гематоксилин-эозином и пикрофуксином по Ван-Гизону по стандартным методикам [Саркисова, Перова, 1996].
Результаты
В опытной группе, а также в группе положительного контроля на 7 сутки после травматического повреждения контакт биокомпозиционного материала с поверхностью кости нижней челюсти животного отсутствовал, в области дефекта уже не было выявлено гематомы, но присутствовали признаки воспалительной реакции. Во всех случаях в области остеобразии над костной поверхностью в области воспалительного инфильтрата на поверхности кости были отмечены признаки репаративного остеогенеза. Различия между опытной и контрольными группами в скорости репаративных процессов, то есть в динамике увеличения доли костной части регенерата и уменьшения доли рыхлой соединительной ткани на данном этапе не зафиксированы.
В группе отрицательного контроля признаков регенерации костной ткани не обнаружено.
На 21 сутки эксперимента в опытной группе, а также в группе положительного контроля отмечена высокая активность репаративных процессов. Между костной поверхностью нижней челюсти и остеопластическим материалом сформировалась тонкая прослойка волокнистой соединительной ткани, представляющая собой тяжи коллагеновых волокон.
В опытной группе на 21 сутки признаки остеогенеза отмечены в двух независимых областях: на поверхности кости и в ячейках матрицы, расположенных в отдалении от костной поверхности, ближе к мышечному пласту (фиг. 1а). Между костной поверхностью нижней челюсти и биотрансплантатом на 21 сутки формировалась прослойка волокнистой соединительной ткани, в которой было много сосудов различного диаметра (фиг. 1б), а также умеренное количество лимфоцитов. В прилежащих к мышечной ткани ячейках отмечена высокая плотность заполнения коллагеновыми волокнами.
В группе положительного контроля в некоторых ячейках матрицы было отмечено формирование костной ткани, источниками развития которой являлись края дефекта, содержащие элементы периоста, эндоста.
В группе отрицательного контроля признаков регенерации костной ткани не обнаружено.
На 40 сутки после пересадки у животных опытной группы в центральных ячейках матрицы отмечено большое количество кровеносных сосудов различного диаметра, а также много коллагеновых волокон, местами формирующих массивные тяжи коллагена. В ячейках со стороны мышечной ткани отмечено формирование плотной волокнистой соединительной ткани, большое количество незрелых клеток.
На 40 сутки после пересадки у животных группы положительного контроля между остеопластическим материалом и костной поверхностью нижней челюсти сформировалась прослойка из волокнистой ткани, пронизанная кровеносными сосудами. В области плотного контакта пластины с костной поверхностью нижней челюсти отмечены многочисленные среднего размера костные бугорки и гребешки, а также оссификация (кальцинирование) материала между ячейками. В ячейках, контактирующих с костной поверхностью, отмечена хорошо сформированная новообразованная костная ткань. Большинство ячеек матрицы заполнены кровеносными сосудами различного диаметра, в отдельных ячейках, преимущественно центральной локализации в пластине, отмечено небольшое количество жировой ткани.
В группе отрицательного контроля на 40 сутки после операции признаков регенерации костной ткани не обнаружено.
На 120 сутки после пересадки у животных опытной группы шло активное замещение биотрансплантата сформированной и функционально активной новообразованной костной тканью: костная часть регенерата состояла из ретикулофиброзной и компактной кости (фиг. 2). Ретикулофиброзная кость была образована массивными костными трабекулами с узкими щелевидными межтрабекулярными пространствами, заполненными соединительной тканью или костным мозгом. Между матрицей и костной поверхностью нижней челюсти сформировалась прослойка из волокнистой соединительной ткани, пронизанная кровеносными сосудами.
На 120 сутки после пересадки у животных группы положительного контроля между остеопластическим материалом и костной поверхностью нижней челюсти сформировалась прослойка из волокнистой соединительной ткани, пронизанная кровеносными сосудами. Репаративные процессы кости на этих сроках наблюдения можно охарактеризовать как перестройку ретикулофиброзной (незрелой кости) в компактную (зрелую). Скорость репаративных процессов снизилась, на первый план выступали процессы минерализации и ремоделирования костной ткани в соответствии с функциональной нагрузкой костного органа.
В группе отрицательного контроля на 120 сутки практически не шел остеогенез, в большей степени сохранялись участки рыхлой соединительной ткани.
При иммуногистохимическом окрашивании срезов в опытной группе на 21, 40 и 120 сутки на всех трех сроках после трансплантации была зафиксирована экспрессия маркера зрелого сосудистого русла - фактора Фон Виллебранда и синтезируемого зрелыми остеоцитами и участвующего в минерализации костной ткани остеокальцина. В большинстве случаев, остеокальцин - позитивные клетки локализовались внутри ячеек носителя, вследствие чего предполагается, что остеокальцин экспрессировали клетки сфероидов, ранее заселенных на матрицу. На всех трех сроках исследования интенсивность синтеза остеокальцина в группе после пересадки заявленного биотрансплантата была выше по сравнению с группой положительного контроля.
Дополнительно на гистологических препаратах после трансплантации в опытной группе, а также в группе положительного контроля был произведен подсчет сосудов. Результаты приведены на фиг. 3. Количество крупных, мелких и средних сосудов достоверно выше в опытной группе, на поздних сроках происходит значительное уменьшение количества сосудов в обеих группах, однако в опытной группе данный феномен менее выражен.
Выводы.
Полученные данные, свидетельствуют о выраженном положительном влиянии клеточных сфероидов в биотрансплантате на репаративный остеогенез после абразии костной ткани за счет значимого улучшения кровоснабжения биотрансплантата. Инициацию репаративного остеогенеза на границе «трансплантат-кость» обеспечивали именно клеточные взаимодействия между привнесенными с биотрансплантатом клеточными сфероидами и реципиентным ложем.
Исходя из вышеуказанных результатов, можно сделать вывод о повышении уровня ангиогенеза мультипотентных мезенхимальных стромальных клеток, а также о повышении эффективности регенерации поврежденных тканей при использовании биотрансплантата, содержащего клеточную культуру, состоящую из мультипотентных мезенхимальных стромальных клеток, культивированных в виде сфероидов.
Список использованной литературы
1. Zuk Р.А., Zhu М., Mizimo Н., Huang J.I., Futrell W.J., Katz A.J., Benhaim P., Lorenz H.P., Hedrick M.H. Multilineage cells from human adipose tissue: implications for cell-based therapies. // Tissue Eng. - 2001. - V. 7. - P. 211-226.
2. Rehman J., Traktuev D., Li J., Merfeld-Clauss S., Temm-Grove C.J., Bovenkerk J.E., Pell C.L., Johnstone B.H., Considine R.V., March K.L. Secretion of angiogenic and antiapoptotic factors by human adipose stromal cells. // Circulation. - 2004. V. 109. - №10. - P. 1292-1298.
3. Микроскопическая техника Руководство для врачей и лаборантов под ред. Д.С. Саркисова и Ю.Л. Перова, Москва «Медицина» 1996, 542 С.
| название | год | авторы | номер документа |
|---|---|---|---|
| Клеточная культура и биотрансплантат для регенерации костной ткани на ее основе | 2018 |
|
RU2721532C1 |
| БИОТРАНСПЛАНТАТ ДЛЯ ВОССТАНОВЛЕНИЯ ОБЪЕМА КОСТНОЙ ТКАНИ ПРИ ДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЯХ И ТРАВМАТИЧЕСКИХ ПВОРЕЖДЕНИЯХ КОСТЕЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2530622C2 |
| Тканеинженерная конструкция для восполнения объема костной ткани челюстно-лицевой области | 2019 |
|
RU2729365C1 |
| Биокомпозитный сфероид для восстановления костей и способ его получения | 2020 |
|
RU2744732C1 |
| БИОТРАНСПЛАНТАТ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНЫХ И ТРАВМАТИЧЕСКИХ ЗАБОЛЕВАНИЙ КОСТНОЙ ТКАНИ ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ | 2008 |
|
RU2380105C1 |
| Тканебиоинженерная конструкция для восполнения объема костной ткани челюстных костей | 2022 |
|
RU2809154C1 |
| БИОТРАНСПЛАНТАТ НА ОСНОВЕ ПЕНОКЕРАМИЧЕСКИХ НОСИТЕЛЕЙ СИСТЕМЫ ОКСИД ЦИРКОНИЯ - ОКСИД АЛЮМИНИЯ И МУЛЬТИПОТЕНТНЫХ СТРОМАЛЬНЫХ КЛЕТОК КОСТНОГО МОЗГА ЧЕЛОВЕКА ДЛЯ ВОССТАНОВЛЕНИЯ ПРОТЯЖЕННЫХ ДЕФЕКТОВ КОСТНОЙ ТКАНИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2386453C1 |
| Способ трансплантации биокомпозитных сфероидов для обеспечения возможности восстановления целостности кости при дефектах, размеры которых превышают критические | 2020 |
|
RU2744756C1 |
| Восстановление диафиза трубчатых костей клеточными технологиями с применением способа аутотрансплантации сосуда | 2020 |
|
RU2757157C1 |
| Способ наращивания объема костной ткани гребня альвеолярного отростка челюсти | 2016 |
|
RU2645963C2 |
Изобретение относится к области биотехнологии, в частности к получению мультипотентных мезенхимальных стромальных клеток, культивированных в виде сфероидов и индуцированных в ангиогенном направлении. Способ включает изолирование фрагмента ткани донора, содержащей мультипотентные мезенхимальные стромальные клетки, перенос фрагмента ткани донора в среду, содержащую культуральную среду, аминокислоту и антибиотик, механическое измельчение фрагмента ткани донора с получением гомогената, инкубирование полученного гомогената в растворе протеолитических ферментов при 37°С до момента получения клеточной суспензии. Далее добавляют питательную среду, содержащую культуральную среду, аминокислоту, антибиотик, сыворотку крови; осуществляют центрифугирование клеточной суспензии до момента полного осаждения клеток, удаление супернатанта, ресуспендирование выделенных клеток в питательной среде, содержащей культуральную среду, аминокислоту, антибиотик, сыворотку крови, культивирование выделенных клеток в монослойной культуре при 37°С в среде 5% СО2 как минимум 2 пассажа, дезагрегация монослоя, культивирование в неадгезивных условиях клеток как минимум 2-го пассажа в концентрации от 1×106 кл/мл до 5×106 кл/мл в питательной среде, содержащей культуральную среду, аминокислоту, антибиотик, сыворотку крови, фактор индукции ангиогенеза с получением клеточной культуры, содержащей мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов. Изобретение позволяет получить мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов и индуцированные в ангиогенном направлении. 24 з.п. ф-лы, 3 ил, 3 пр.
1. Способ получения мультипотентных мезенхимальных стромальных клеток, культивированных в виде сфероидов и индуцированных в ангиогенном направлении, включающий в себя следующие стадии:
- изолирование фрагмента ткани донора, содержащей мультипотентные мезенхимальные стромальные клетки.
- перенос фрагмента ткани донора в среду, содержащую культуральную среду, аминокислоту и антибиотик, механическое измельчение фрагмента ткани донора с получением гомогената,
- инкубирование полученного гомогената в растворе протеолитических ферментов при 37°С до момента получения клеточной суспензии,
- добавление питательной среды, содержащей культуральную среду, аминокислоту, антибиотик, сыворотку крови,
- центрифугирование клеточной суспензии до момента полного осаждения клеток,
- удаление супернатанта,
- ресуспендирование выделенных клеток в питательной среде, содержащей культуральную среду, аминокислоту, антибиотик, сыворотку крови,
- культивирование выделенных клеток в монослойной культуре при 37°С в среде 5% СО2 как минимум 2 пассажа,
- дезагрегация монослоя,
- культивирование в неадгезивных условиях клеток как минимум 2-го пассажа в концентрации от 1×106 кл/мл до 5×106 кл/мл в питательной среде, содержащей культуральную среду, аминокислоту, антибиотик, сыворотку крови, фактор индукции ангиогенеза с получением клеточной культуры, содержащей мультипотентные мезенхимальные стромальные клетки, культивированные в виде сфероидов.
2. Способ по п. 1, отличающийся тем, что культивирование клеток в питательной среде, содержащей культуральную среду, аминокислоту, антибиотик, сыворотку крови, фактор индукции ангиогенеза, осуществляется до момента образования гладкой поверхности сфероидов.
3. Способ по п. 1, отличающийся тем, что в качестве ткани донора используется жировая ткань.
4. Способ по п. 1, отличающийся тем, что в качестве ткани донора используется ткань пупочного канатика.
5. Способ по п. 1, отличающийся тем, что в качестве ткани донора используется ткань костного мозга.
6. Способ по п. 1, отличающийся тем, что в качестве культуральной среды используется среда DMEM.
7. Способ по п. 1, отличающийся тем, что в качестве культуральной среды используется среда F12.
8. Способ по п. 1, отличающийся тем, что в качестве культуральной среды используется смесь культуральной среды DMEM и культуральной среды F12 в соотношении 1 к 1 по объему.
9. Способ по п. 1, отличающийся тем, что в качестве культуральной среды используется смесь культуральной среды DMEM и культуральной среды F12 в соотношении 2 к 1 по объему.
10. Способ по п. 1, отличающийся тем, что в качестве культуральной среды используется среда α-МЕМ.
11. Способ по п. 1, отличающийся тем, что в качестве аминокислоты используется L-глутамин.
12. Способ по п. 1, отличающийся тем, что в качестве антибиотика используется гентамицин.
13. Способ по п. 1, отличающийся тем, что в качестве антибиотика используется смесь пенициллина со стрептомицином.
14. Способ по п. 1, отличающийся тем, что в качестве антибиотика используется амфотерицин В.
15. Способ по п. 1, отличающийся тем, что в качестве раствора протеолитических ферментов используется раствор коллагеназы первого типа и диспазы.
16. Способ получения по п. 1, отличающийся тем, что в качестве раствора протеолитических ферментов используется раствор коллагеназы первого типа.
17. Способ по п. 1, отличающийся тем, что в качестве раствора протеолитических ферментов используется раствор диспазы.
18. Способ по п. 1, отличающийся тем, что в качестве раствора протеолитических ферментов используется раствор трипсина.
19. Способ по п. 1, отличающийся тем, что в качестве раствора протеолитических ферментов используется раствор коллагеназы второго типа и диспазы.
20. Способ по п. 1, отличающийся тем, что в качестве раствора протеолитических ферментов используется раствор коллагеназы второго типа.
21. Способ по п. 1, отличающийся тем, что в качестве сыворотки крови используется эмбриональная телячья сыворотка.
22. Способ по п. 1, отличающийся тем, что в качестве сыворотки крови используется аутологичная сыворотка крови пациента.
23. Способ по п. 1, отличающийся тем, что в качестве фактора индукции ангиогенеза используется фактор роста эндотелия сосудов.
24. Способ по п. 1, отличающийся тем, что в качестве фактора индукции ангиогенеза используется кондиционированная среда от эндотелиальных клеток вены пупочного канатика.
25. Способ по п. 1, отличающийся тем, что в качестве фактора индукции ангиогенеза используется основной фактор роста фибробластов.
| Cesarz Z., et al | |||
| "Spheroid Culture of Mesenchymal Stem Cells", Stem Cell Int | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| БИОТРАНСПЛАНТАТ ДЛЯ ВОССТАНОВЛЕНИЯ ОБЪЕМА КОСТНОЙ ТКАНИ ПРИ ДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЯХ И ТРАВМАТИЧЕСКИХ ПВОРЕЖДЕНИЯХ КОСТЕЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2530622C2 |
| ВЕЧКАНОВ Е.М., и др | |||
| Основы клеточной инженерии: Учебное пособие | |||
| - Ростов-на-Дону, 2012 | |||
| Регулятор для ветряного двигателя в ветроэлектрических установках | 1921 |
|
SU136A1 |
| КОЖУХАРОВА И.В | |||
| УСТРОЙСТВО ДЛЯ ИЗМЕНЕНИЯ ВЕЛИЧИНЫ УСИЛЕНИЯ КАТОДНОГО РЕЛЕ В КАТОДНЫХ МУЗЫКАЛЬНЫХ ПРИБОРАХ | 1922 |
|
SU612A1 |
| Цитология | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
Авторы
Даты
2018-12-25—Публикация
2017-07-21—Подача