Изобретение относится к медицине, в частности к экспериментальной фармакологии.
Известно, что тремор, брадикинезия и ригидность мышц возникают в следствие гибели 70%-80% дофаминергических нейронов черной субстанции [Liangqin Shi, Chao Huang, Qihui Luo et al. Pilot study: molecular risk factors for diagnosing sporadic Parkinson's disease based on gene expression in blood in MPTP-induced rhesus monkeys 2017; 8(62): 105606–105614. doi: 10.18632/oncotarget.22348]. Сегодня присутствует целый ряд существенных достижений в области лечения паркинсонизма. Однако все существующие препараты направлены на симптоматическую и патогенетическую терапию, поскольку этиологического лечения этого заболевания не разработано [Протокол ведения больных. Болезнь Паркинсона // Проблемы стандартизации в здравоохранении. 2005. № 3. С. 74–166].
В течение последних 40 лет использование леводопы для паркинсонических пациентов считается наиболее эффективным симптоматическим лечением [Fahn S. The history of dopamine and levodopa in the treatment of Parkinson's disease. Mov Disord 2008; 23 Suppl 3:S497-508].
При наличии моторных нарушений, мешающих повседневной жизни, согласно рекомендациям Национального института здоровья и клинического совершенствования, лечение следует начинать с одного из трех препаратов первой линии: леводопа, агонисты дофамина, или ингибиторов моноамино-оксидазы-B [Clarke CE. Clinical Review Parkinson's disease, professor of clinical neurology, University of Birmingham. BMJ. 2007; 335(7617): 441–445. doi:10.1136/bmj.39289.437454].
Данные рандомизированных контролируемых исследований и систематические обзоры подтверждают эффективность каждого из этих классов препаратов [Parkinson’s disease: diagnosis and management in primary and secondary care. NICE guideline Second draft for consultation. 2006; 37 https://www.nice.org.uk/guidance/cg35/documents/parkinsons-disease-nice-guideline-second-consultation2].
Однако лечение леводопой вызывает ряд побочных эффектов, например, аномальные непроизвольные движения, синдром истощения эффекта (временное ухудшение состояния незадолго до приема очередной дозы препарата) и акинетические пароксизмы [Национальный институт здравоохранения и клинического совершенствования. Болезнь Паркинсона: диагностика и лечение первичной и вторичной помощи Лондон: NICE, 2006].
Таким образом, вполне очевидным становится изыскание новых высокоэффективных и безопасных препаратов для лечения данной патологии. Актуальным явилось исследование субстанции лекарственного средства Рапиталам для коррекции тремора в эксперименте, являющегося модулятором mGluR4 рецепторов. Рапиталам представляет собой N-[(4-chlorophenyl)methyl]-1,6-dihydro-4-methoxy-1-(2-methylphenyl)-6-oxo-3-pyridazinecarboxamide и имеет химическую форму С20Н18ClN3O3 (Авдеева, Н.В. Исследование некоторых аспектов мутагенного действия фармацевтической субстанции лекарственного средства – Рапиталам. Авдеева Н.В., Корокин М.В., Покровский М.В.. Современные проблемы науки и образования. 2017. № 3. С. 136).
Известен способ коррекции тремора с использованием ботулинического токсина типа А BoNT-A, путем его инъекционного введения в мышцы, с последующим проведением кинематического анализа согласно протокола клинического исследования [Fariborz Rahimi, Olivia Samotus, Jack Lee and Mandar Jog Monitoring Editor: Elan D. Louis. Effective Management of Upper Limb Parkinsonian Tremor by IncobotulinumtoxinA Injections Using Sensor-based Biomechanical Patterns. Tremor Other Hyperkinet Mov (NY). 2015; 5: 348. doi: 10.7916/D8BP0270].
Основным недостатком способа является сложность дозирования и определения места введения ботулинического токсина, что приводит к мышечной слабости, а, следовательно, в некоторых случаях невозможности осуществления моторной функции. Несмотря на то, что максимальная сила тремора уменьшилась на 25% после первого введения, у 57% участников наблюдалась слабость пальцев, которая оценивалась как побочное действие [Brin MF, Lyons KE, Doucette J, et al. A randomized, double masked, controlled trial of botulinum toxin type A in essential hand tremor. Neurology. 2001; 56:1523–1528]. При этом, в ходе исследования 21% пациентов испытывали выраженную мышечную слабость, требующую отмены исследования после трех введений [Fariborz Rahimi, Olivia Samotus, Jack Lee and Mandar Jog Monitoring Editor: Elan D. Louis. Effective Management of Upper Limb Parkinsonian Tremor by IncobotulinumtoxinA Injections Using Sensor-based Biomechanical Patterns. Tremor Other Hyperkinet Mov (N Y). 2015; 5: 348. doi: 10.7916/D8BP0270].
Известен способ доставки вирусных векторов, в частности рекомбинантного аденоассоциированного вируса (rAAV), в центральную нервную систему (ЦНС). Вирионы rAAV включают последовательность нуклеотидов, кодирующую терапевтический полипептид. Этот метод может быть использован для лечения расстройств ЦНС, таких как лечение болезни Паркинсона [US 09320171].
В данном случае явным недостатком, помимо сложности осуществления введения вирусных частиц, является невозможность их равномерного распределения в полосатом теле, что подтверждается гистологией, представленной в самом патенте. Помимо этого, невозможно использование данной терапии у пациентов с высоким титром антител к AAV. А также есть ряд побочных эффектов, связанных с проведением процедуры, а именно головная боль, внутричерепное кровоизлияние, у некоторых пациентов увеличение количества дискинезий [Li Rebekah Feng, Kathleen A. Gene Therapy in Parkinson’s Disease: Rationale and Current Status. 2010. CNS Drugs. 24(3): 177–192. doi: 10.2165/11533740-000000000-00000].
Наиболее близким к заявленному решению является способ коррекции тремора на модели оксотреморин-индуцированного тремора у крыс (Е.А. Катунина, Е.А. Малыхина, Н.В. Кузнецов и др.. Антиоксиданты в комплексной терапии болезни Паркинсона. Журнал неврологии и психиатрии, 9, 2006). Введение мексидола в течение 5 дней животным не сопровождалось изменением двигательной активности и координации. Значимых изменений нейрофизиологических параметров также отмечено не было. Оксотреморин вводили животным однократно внутрибрюшинно на пятый день эксперимента. Введение мексидола способствовало уменьшению выраженности тремора, вызванного введением оксотреморина. Уменьшались длительность тремора (с 30-40 до 20-25 мин) на фоне введения мексидола.
Недостатком данного решения является то, что препарат мексидол обладает рядом побочных эффектов, такими как появление тошноты и сухости слизистой оболочки ротовой полости, аллергические реакции, сонливость [Сидоров A.M., Борисова В.А. Клиническая эффективность препарата Мексидол в терапии цереброваскулярной патологии. Методические рекомендации для бригад скорой помощи г. Москва 2005 год]. В дозе 300 мг/кг у крыс побочные эффекты Мексидола выражаются главным образом в угнетении двигательной активности и нарушении координации движений [Т.А. Воронина Отечественный препарат нового поколения Мексидол основные эффекты, механизм действия, применение Москва 2005. http://www.voed.ru/mexidol.htm]. Помимо этого, существенным недостатком проведенного исследования является отсутствие указания дозы оксотреморина, используемого для моделирования патологии.
Задачей предлагаемого изобретения является создание эффективного способа коррекции тремора в эксперименте с использованием субстанции лекарственного средства Рапиталам модулятора mGluR4 рецепторов, лишенного побочных эффектов прототипа и аналогов за счет его направленного влияния на mGluR4 рецепторы.
Техническим результатом предлагаемого изобретения является эффективный способ коррекции тремора в эксперименте с использованием субстанции лекарственного средства Рапиталам модулятора mGluR4 рецепторов, лишенного побочных эффектов прототипа и аналогов за счет направленного механизма действия.
Поставленная задача достигается тем, что предложен способ коррекции тремора в эксперименте, включающий однократное ежедневное введение крысам корригирующего агента и однократное внутрибрюшинное введение оксотреморина в последний день эксперимента, причем в качестве корригирующего агента крысам вводят субстанцию лекарственного средства Рапиталам модулятор mGluR4 рецепторов внутрижелудочно через зонд в дозе 10 мг/кг в течение 10 дней, а оксотреморин вводят в последний день эксперимента в дозе 1,5 мг/кг в объеме 5 мл/кг через 30 минут после введения Рапиталама.
Основным преимуществом предлагаемого способа является то, что введение субстанции лекарственного средства Рапиталам модулятор mGluR4 рецепторов в дозе 10 мг/кг приводит к выраженной коррекции оксотреморин-индуцированного тремора, подтверждаемой длительностью латентного периода и тремора, суммарной оценкой выраженности тремора в баллах, и процентом животных с тремором в группе, с учетом его длительности.
СПОСОБ ОСУЩЕСТВЛЯЕТСЯ СЛЕДУЮЩИМ ОБРАЗОМ
Исследование проведено на модели оксотреморин-индуцированного тремора. Исследование фармакологической активности лекарственного средства рапиталам проводили на самцах крыс линии Sprague Dawley. Перед исследованием животные проходили карантинные процедуры. По завершении карантина животные осмотрены ветеринаром, в эксперимент допущены животные без выявленных признаков патологии. Все животные содержались в стандартных условиях согласно руководству Guide for the care and use of laboratory animals (Washington, 2011) и правилам, утвержденным ГОСТ 33044-2014 «Принципы надлежащей лабораторной практики».
Характеристика тест-системы:
Вид: крысы
Линия: SD
Пол: самцы
Источник: «Питомник лабораторных животных», Филиала Института биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова, г. Пущино.
Возраст к введению: 12-14 недель.
Противопаркинсонические свойства субстанции лекарственного средства Рапиталам модулятор mGluR4 рецепторов (Рапиталам) исследовали в дозе 10 мг/кг, Леводопа в дозе 50 мг/кг вводили крысам внутрижелудочно (в/ж) один раз в сутки в течение 10 дней. Препарат Мексидол в дозе 1 мг/кг вводили один раз в сутки внутрибрюшинно в течение, 5 дней и 10 дней. Через 30 мин после введения рапиталама, Леводопа, Мексидола внутрибрюшинно (в/б) вводили раствор оксотреморина в дозе 1,5 мг/кг в объеме 5 мл/кг. Животным интактной группы (контроль 1) вводили физраствор в эквивалентном объеме. Животным группы контроль 2 вводили оксотреморин в соответствующей концентрации и в эквивалентном объеме что и другим группам.
Коррекция оценивали по выраженности в баллах и по продолжительности, регистрируя время начала и окончания тремора. По локализации и амплитуде тремор выражают в баллах:
0 – отсутствие;
1 – локальный мелкоамплитудный тремор головы, передних лап или хвоста;
2 – локальный среднеамплитудный тремор;
3 – генерализованный мелко- или среднеамплитудный тремор всего тела.
Также проводили процентный расчёт количества крыс с тремором и без.
Межгрупповое статистическое сравнение проводили при помощи критерия Крускалл-Уоллиса с постанализом по критерию Дана. Для статистического сравнения повторяющихся измерений был использован Repeated measures ANOVA, в случае выявления отличий между группами, применяли критерий Бонферони. Различия были определены при 0,05 уровне значимости (GraphPad Prism 5.0).
ПРИМЕР КОНКРЕТНОГО ВЫПОЛНЕНИЯ
В результате исследования установлено, что субстанция рапиталам дозе 10 мг оказывает выраженное противопаркинсоническое действие на модели оксотреморин индуцированного тремора. Латентный период и длительность тремора в группах представлена в таблице 1.
Таблица 1 - Латентный период (мин) и длительность (мин) тремора в группах крыс, средн. ± ст. ош.
Примечание: * р<0,05 в сравнении с группой Контроль 1, # р<0,05 в сравнении с группой Контроль 2 (непараметрический критерий Крускалл-Уоллиса, постанализ Данна).
Оксотреморин при внутрибрюшинном введении крысам из группы Контроль 2 вызывал нарастающую степень выраженности тремора с 10-й по 20-ю минуты после введения. Через 40 мин после введения оксотреморина степень выраженности тремора у контрольных крыс начала снижаться, и, начиная с 80-й мин после введения оксотреморина, проявлений тремора у животных не регистрировали.
В группе, которой вводили препарат Леводопа в дозе 50 мг/кг, по сравнению с группой Контроль 2, было отмечено достоверное уменьшение выраженности тремора через 20, 30 и 50 мин, после введения оксотреморина. Через 60 мин в данной группе было отмечено значимое уменьшение % крыс с тремором.
В группах, которым вводили препарат Мексидол в дозе 1 мг/кг 5 дней и 10 дней, по сравнению с группой Контроль 2, не было отмечено достоверного уменьшение выраженности тремора через 20, 30 и 50 мин, после введения оксотреморина. Через 60 мин в данной группе было отмечено значимое уменьшение % крыс с тремором.
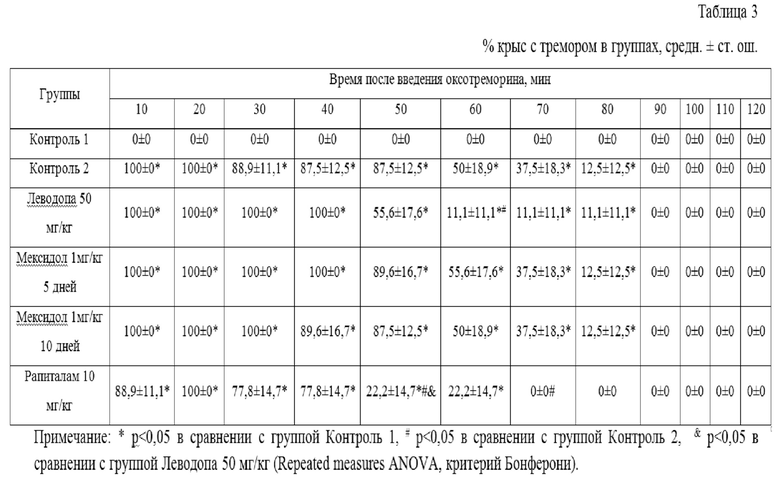
Рапиталам в дозе 10 мг/кг приводит к уменьшению выраженности тремора у крыс с 30-й мин и уменьшению % крыс в группе с проявлениями тремора через 50 мин и далее.
Таким образом, введение субстанции лекарственного средства Рапиталам модулятор mGluR4 рецепторов в дозе 10 мг/кг, как и препарат Леводопа в дозе 50 мг/кг, снижало проявления оксотреморин-индуцированного тремора у крыс, при этом, Рапиталам в дозе 10 мг/кг превосходит по эффективности препарат Леводопа дозе 50 мг/кг и Мексидол в дозе 1 мг/кг. Описанные выше результаты представлены в таблицах 2, 3.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ коррекции ишемии головного мозга субстанцией рапиталама в эксперименте | 2019 |
|
RU2711906C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ, ОКАЗЫВАЮЩАЯ ВЛИЯНИЕ НА ФУНКЦИОНИРОВАНИЕ ЦНС, СПОСОБ КОРРЕКЦИИ СОСТОЯНИЙ, СВЯЗАННЫХ С НАРУШЕНИЯМИ ФУНКЦИОНИРОВАНИЯ ЦНС; ФАРМАЦЕВТИЧЕСКИЙ НАБОР; СРЕДСТВО, СПОСОБСТВУЮЩЕЕ ПРОНИКНОВЕНИЮ ЧЕРЕЗ ГЕМАТОЭНЦЕФАЛИЧЕСКИЙ БАРЬЕР ЛЕКАРСТВЕННЫХ СУБСТАНЦИЙ И МЕТАБОЛИТОВ; ФАРМАЦЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЭНДОНАЗАЛЬНОГО ПРИМЕНЕНИЯ | 2004 |
|
RU2253461C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ СУБСТАНЦИИ ИЗ СЫВОРОТКИ КРОВИ | 2000 |
|
RU2236238C2 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2014 |
|
RU2545734C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2006 |
|
RU2324492C1 |
| ПРИМЕНЕНИЕ КАРБАМАТНОГО СОЕДИНЕНИЯ ДЛЯ ПРОФИЛАКТИКИ, ОБЛЕГЧЕНИЯ ИЛИ ЛЕЧЕНИЯ ТРЕМОРОВ ИЛИ СИНДРОМА ТРЕМОРА | 2017 |
|
RU2776368C2 |
| НОВОЕ ПРОИЗВОДНОЕ ОКСИМА ХРОМОНА И ЕГО ИСПОЛЬЗОВАНИЕ В КАЧЕСТВЕ АЛЛОСТЕРИЧЕСКОГО МОДУЛЯТОРА МЕТАБОТРОПНЫХ РЕЦЕПТОРОВ ГЛУТАМАТА | 2015 |
|
RU2672569C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОИНСУЛИТНЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2521404C1 |
| ИНЪЕКЦИОННАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА, СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ И ПРИМЕНЕНИЕ | 2011 |
|
RU2520758C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГИПОКСИЧЕСКИМ, ПРОТИВОИНСУЛЬТНЫМ, УЛУЧШАЮЩИМ ПАМЯТЬ ДЕЙСТВИЕМ | 2007 |
|
RU2326665C1 |
Изобретение относится к медицине, в частности к экспериментальной фармакологии, и может быть использовано для коррекции тремора в эксперименте. Способ включает однократное ежедневное внутрижелудочное введение крысам корригирующего агента в дозе 10 мг/кг в течение 10 дней, а в последний день эксперимента однократное внутрибрюшинное введение оксотреморина в дозе 1,5 мг/кг в объёме 0,5 мл/кг через 30 минут после введения корригирующего агента. При этом в качестве корригирующего агента используют субстанцию лекарственного средства Рапиталам, который является модулятором mGluR4 рецепторов. Изобретение приводит к выраженной коррекции оксотреморин-индуцированного тремора, подтверждаемой длительностью латентного периода и тремора, суммарной оценкой выраженности тремора в баллах и процентом животных с тремором в группе, с учетом его длительности. 3 табл.
Способ коррекции тремора в эксперименте, включающий однократное ежедневное введение крысам корригирующего агента и однократное внутрибрюшинное введение оксотреморина в последний день эксперимента, отличающийся тем, что в качестве корригирующего агента крысам вводят субстанцию лекарственного средства Рапиталам модулятор mGluR4 рецепторов внутрижелудочно через зонд в дозе 10 мг/кг в течение 10 дней, а оксотреморин вводят в последний день эксперимента в дозе 1,5 мг/кг в объеме 5 мл/кг через 30 минут после введения Рапиталама.
| НОВОЕ СОЕДИНЕНИЕ И ЕГО ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2011 |
|
RU2570900C2 |
| АВДЕЕВА Н.В., ПОКРОВСКИЙ М.В., КОРОКИН М.В | |||
| Изучение острой токсичности фармацевтической субстанции лекарственного средства, являющегося модулятором mGluR4 рецепторов, Рапиталам // Современные проблемы науки и образования, 2017, N4 [он-лайн], [найдено 01.11.2018] | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| ТИТОВА Н.В., БОГОМАЗОВА М.А | |||
| Возможности применения антиоксидантной терапии при болезни Паркинсона | |||
| Экспериментально-клиническое исследование // Вестник РГМУ, 2005, N3(42), с.27 | |||
| OLIVIA SAMOTUS | |||
| Characterization and personalization of botulinum toxin type A therapy for upper limb tremor in Parkinson disease and Essential tremor patients using multi-sensor kinematic technology, 2016, Electronic Thesis and Dissertation Repository, 4035, https:// ir.lib.uwo.ca/etd/4035. | |||
Авторы
Даты
2019-02-05—Публикация
2018-04-12—Подача