Изобретение относится к биотехнологии, генной инженерии, микробиологической и медицинской промышленности и касается новых генетических конструкций и продуцентов, обеспечивающих в промышленных масштабах синтез рекомбинантного гранулоцитарного колониестимулирующего фактора человека.
Гранулоцитарный колониестимулирующий фактор (далее Г-КСФ) регулирует пролиферацию клеток-предшественников нейтрофилов и их дифференцировку на гранулоциты и функционально активирует зрелые нейтрофилы. Он продуцируется в ответ на специфическую стимуляцию различными клетками, включая макрофаги, фибробласты, эндотелиальные клетки и клетки костного мозга. В настоящее время Г-КСФ используется в клинике для восстановления гемопоэза после трансплантации костного мозга, химиотерапии рака и других заболеваниях, приводящих к нейтропении.
Белок Г-КСФ представляет собой гликопротеин 20,0 кДа, который имеет 5 цистеиовых остатков, а также 2 внутримолекулярные дисульфидные связи, которые необходимы для его биологической активности.
Ген Г-КСФ локализован на 17 хромосоме, кодирует два белковых продукта в результате альтернативного сплайсинга: изоформа А, состоит из 177 аминокислот, а изоформа В из 174 аминокислот. Природная изоформа Г-КСФ гликозилирована по аминокислоте Thr133. Изоформа А содержит дополнительные три остатка (Val-Ser-Gln), расположенные после Leu35 в изоформы В. Изоформа В обладает большей биологической активностью и устойчивостью по сравнению с изоформа А. Вследствие этого факта, изоформа В Г-КСФ человека была использована для создания фармацевтического препарата.
Известны два основных принципа получения Г-КСФ для терапевтических целей: 1) получение полного аналога "природного" Г-КСФ из рекомбинантных клеток яичника китайского хомяка (СНО), имеющий международное непатентованное название ленограстим (гликозилированный Г-КСФ, lenograstim, Chugai Pharma UK Ltd) и 2) получение Г-КСФ по технологии рекомбинантной ДНК из рекомбинантных клеток Escherichia coli, имеющий международное непатентованное название Г-КСФ (негликозилированный Г-КСФ, Г-КСФ, Neupogen, Amgeri).
Рекомбинантный человеческий Г-КСФ или фиглграстим (далее рч Г-КСФ), имеет молекулярную массу 18,8 кДа, состоит из 175 аминокислот, содержит 5 цистеиовых остатков, а также 2 внутримолекулярные дисульфидные связи, которые необходимы для его биологической активности, обладает такой же биологической активностью, что и «нативный» белок, но отличается тем, что он содержит N-концевой остаток метионина и не является гликозилированным.
Ленограстим, "природный" Г-КСФ, полученный in vitro из рекомбинантных клеток яичника китайского хомяка (СНО), является абсолютным аналогом Г-КСФ по структуре и свойствам изоформы В Г-КСФ человека, который синтезируется в человеческом организме. Выделение, очистка, структура, свойства и технология получения ленограстим описана во многих работах (WO 8604605, 1989; ЕР 215126, 1987 Chugai, Н. Nomura et.al., 1986, "Purification and characterization of human granulocyte colony-stimulation factor (G-CSF)", The EMBO Journal, vol. 5, no. 5, pp. 871-876, N. Kubota, et. al., 1990, "Structural characterization of natural and recombinant human granulocyte colony-stimulating factors", J. Biochem., 107, 486-492, C. J. Holloway, 1994, "Application of recombinant DNA technology in the production of glycosylated recombinant human granulocyte colony stimulating factor", European J. Cancer, vol. 30A, Suppl., 3, pp. 82-56").
Основными недостатками получения Г-КСФ из рекомбинантных клеток яичника китайского хомяка (СНО) являются низкий выход целевого продукта, вероятность контаминации конечного продукта вирусами из клеточной линии и из продуктов животного происхождения используемых при культивировании рекомбинантной линии клеток яичника китайского хомяка (СНО) и высокая себестоимость.
В настоящее время производство Г-КСФ основано, главным образом, на использовании в качестве продуцентов микроорганизмов различной видовой принадлежности, созданных с помощью технологии рекомбинантных ДНК.
Существует достаточно много разнообразных рекомбинантных экспрессионных плазмидных векторов и сконструированных на их основе бактериальных и дрожжевых штаммов, синтезирующих рч Г-КСФ.
Например, известен ряд продуцентов из рекомбинантных дрожжей видов Saccharomyces cerevisiae (Robinson А., 1995, "Constitutive overexpression of secreted heterologous proteins decreases extractable BiP and protein disulfide isomerase levels in Saccharomyces cerevisiae", Biotechnol Prog., vol. 11, n. 2, pp.171-177,), Pichia pastoris (A. Bahrami et. al., 2007, "Production of recombinant human granulocyte-colony stimulating factor by Phichia pastoris", Iranian J. Microbiology, vol. 5, n. 3, pp. 162-168, A. Saeedinia, et. al., 2008, "Heterologous expression of human granulocyte-colony stimulating factor in Pichia pastoris", Biotechnology, vol. 7, n. 3, pp. 569-573) и Hancenula polymorpha, (Y. Talebkhan, et. al., 2015, "Expression of granulocyte colony stimulating factor (GCSF) in Hansenula polymorpha", Iranian J. Microbiology, vol. 8, n. 1, pp. 21-28), а также бактерий вида Escherichia coli (US 4810643, 1989, US 5849883, 1998, US 2005/0283000 A1, RU 96113021, 1996, RU 2260049, 2003, RU 2326169, 2006, RU 2321424, 2006), и др. (Krasevec N, et. al., 2014, Human granulocyte colony stimulating factor (G CSF) produced in the filamentous fungus Aspergillus niger"., Acta Chim. Slov., vol. 61, pp. 709-717.).
Существенными недостатками дрожжевых продуцентов является, во-первых, существование процесса гликозилирования и гипергликозилирования (для Saccharomyces cerevisiae) синтезированных белков специфичный для дрожжевых клеток, что приводит к пострансляционной модификации целевого продукта, во-вторых, продолжительное время процесса ферментации, занимающее до 5 суток (для Pichia pastoris), в-третьих, в связи с тем, что целевой продукт находится длительное время растворенной форме, он подвергается процессу деградации внутриклеточными протеазами, что приводит к значительному снижению выхода продукта. Кроме того, дрожжевые продуценты требуют крайне сложных условий ферментации, связанных с использованием сложных рецептур ферментационных сред, многостадийностью самого процесса ферментации, необходимостью строго поддерживать в процессе биосинтеза концентрацию субстратов/индуктора, например, концентрацию метанола/глицерина при использовании метилотрофных дрожжей, таких как Hansenula polimorpha и Pichia pastorius. В следствие этого, известны только два фармацевтических продукта, разрешенных к применению, субстанции которых получены в дрожжевых продуцентах - рекомбинантный инсулин и вакцина против вируса гепатит Б человека (Melmer Р, "Biopharmaceuticals and the industrial environment". In "Production of recombinant proteins: novel microbial and eukaryotic expression systems", Ed, Gellissen G, Wiley-VCH, Weinheim, pp. 361-383).
Рекомбинантные продуценты Г-КСФ, полученные на основе бактерий вида Escherichia coli (Е. coli) позволяют получить целевой продукт со значительно более высоким выходом, по сравнению с технологией получения ленограстима (US 4810643, 1989, US 5849883, 1998, US 2005/0283000 A1, RU 96113021, 1996, RU 2260049, 2003, RU 2326169, 2006, RU 2321424, 2006). Но многие известные штаммы имеют значительные недостатки по некоторым параметрам таким как, стабильность штамма продуцента, уровень экспрессии рч Г-КСФ, использование дорогих богатых сред и индукторов, что является препятствием для промышленного производства.
В патенте RU 2113483 описан штамм E.coli SG20050/pGGF8, содержащий рекомбинантную плазмиду pGGF8, кодирующую рч Г-КСФ человека, экспрессия которого находится под контролем тандема триптофанового промотора E.coli и синтетический участок - усилитель трансляции (TREN) гена 10 бактериофага 7, синтетический ген Г-КСФ, терминатор транскрипции фага лямбда и генетический маркер - ген бета-лактамазы, детерминирующий устойчивость клеток рекомбинантного штамма к антибиотику ампициллин. Основным недостатками известной плазмиды и штамма, полученного на ее основе, является использование в плазмиде селективного гена β-лактамазы, детерминирующего устойчивость штамма к антибиотику ампициллин, использование богатой среды для ферментации и низкие выходы целевого продукта. При культивировании штамма β-лактамаза секретируется из бактериальной клетки и разрушает антибиотик. В результате чего в процессе ферментации происходит постоянное неконтролируемое снижение селективного давления для плазмидосодержащих клеток штамма, накопление бесплазмидных клеток. Выход целевого продукта составляет не выше 40 мг с литра культуры клеток (RU 2201962, RU 2278870).
В патенте RU 2326169 описан штамм продуцент E.coli SGK/pA3GF, содержащий рекомбинантную плазмиду ДНК pA3GF, кодирующая Г-КСФ человека, экспрессия которого находится под контролем конститутивного промотора A3 из ранней области бактериофага T7 и синтетический участок - усилитель трансляции (TREN) гена 10 бактериофага 7, синтетический ген рч Г-КСФ (как в RU 2113483), терминатор транскрипции фага лямбда и генетический маркер - ген бета-лактамазы, детерминирующий устойчивость клеток рекомбинантного штамма к антибиотику ампициллин. Плазмиды pGGF8 и pA3GF отличаются только тем, что первая плазмида кодирует экспрессию рч Г-КСФ под контролем тандемом триптофанового промотора E.coli, а вторая плазмида кодирует экспрессию рч Г-КСФа под контролем конститутивного промотора A3 из ранней области бактериофага 77. Основными недостатками изобретения, описанном в патенте RU 2326169 является так же использование на плазмиде селективного гена β-лактамазы, но и сильного конститутивного, не регулируемого промотора. Оба эти фактора приводят резкому снижению селективного давления для плазмидосодержащих клеток штамма, накопление безплазмидных клеток и, как следствие, снижение выхода Г-КСФа. Следствием этого, культура при ферментации переходит в стационарную фазу роста при низких значениях оптической плотности 3,0-3,5 (при 560 нм). Недостатком этой технологии является так же использование т.н. богатой комплексной среды (SB) при ферментации. И, как следствие, приводит к резкому повышению себестоимости целевого продукта.
В патенте RU 2260049 описан штамм E.coli BL21(DE3)PES3-7, содержащий рекомбинантную плазмиду pES3-7, кодирующую рч Г-КСФ человека. ДНК плазмиды pES3-7, представляет собой ДНК векторной плазмиды рЕТ22b(+), содержащий промотор и терминатор транкрипции T7-РНК-полимеразы, усилитель трансляции гена 10 фага Т7 экспрессия которого находится под контролем T7 промотора, селективный ген β-лактамазы в которую по сайтам NdeI/NotI клонирован синтетический ген Г-КСФ с максимально широким набором кодонов, являющиеся оптимальными для продукции белка в клетках E.coli, расположение которых в синтетическом гене устраняет возможность образования на синтезируемой мРНК протяженных «шпилек», потенциально ингибирующих трансляцию. Недостатками этого изобретения является также использование селективного гена β-лактамазы, богатых сред для ферментации и индуктора ИПТГ (изопропилтио-β-D-галактозид), что в конечном счете приводит к удорожанию производства.
Наиболее близким аналогом по технической сущности к предлагаемому изобретению является способ, описанный в патенте RU2321424. В патенте описан штамм E.coli SX70 и рекомбинантная плазмида pSX70, размером 4305 пар оснований, содержащая триптофановый промотор Рtrp, синтетический ген, кодирующий полипептид рч Г-КСФ (описанный в патентах RU 2113483, RU 2326169, Кашьян С.П., Быстров Н.С., Болдырева Е.Ф., Полякова И.А., Северцова И.В., Коробко В.Г. // Биорганическая химия, Том 18, №1, с. 71-77, 1992 г.), терминатор транскрипции rrnBT1T2 из плазмиды pSX50 (RU 2242516), последовательность векторной плазмиды pUC19, в ген β-лактомазы встроен полный ген kan из векторной плазмиды pUC4K, обеспечивающий устойчивость к антибиотику канамицин. Выход Г-КСФ в результате применения описанного штамма составляет не менее 200 мг чистого белка с 1 л культуральной среды. Основным недостатком этого изобретения является необходимость использовать специальную богатую среду с низким содержанием триптофана, включающую дорогостоящий компонент кислотный гидролизат казеина, являющийся продуктом животного происхождения.
Предлагаемое изобретение решает задачу конструирования бактериального штамма-продуцента, позволяющего получать чистый рекомбинантный Г-КСФ человека с более высоким выходом (до 2-3 г с 1 л культуральной среды) при ферментации на синтетических средах, не содержащих продуктов животного происхождения и по упрощенной технологии.
Технический результат изобретения заключается в упрощении технологии получения рч Г-КСФ человека за счет создания рекомбинантной плазмидной ДНК pFM-GCSF-5, и создания на ее основе высокопродуктивного стабильного штамма Escherichia coli FM-GCS, способного культивироваться на синтетических средах до высоких плотностей (до 50-60 о.е. и выше) и высоких значениях синтеза целевого продукта (до 2-3 г с 1 л культуральной среды).
Изобретение поясняется следующими рисунками.
На фиг. 1 представлена нуклеотидная последовательность синтетического гена kan.
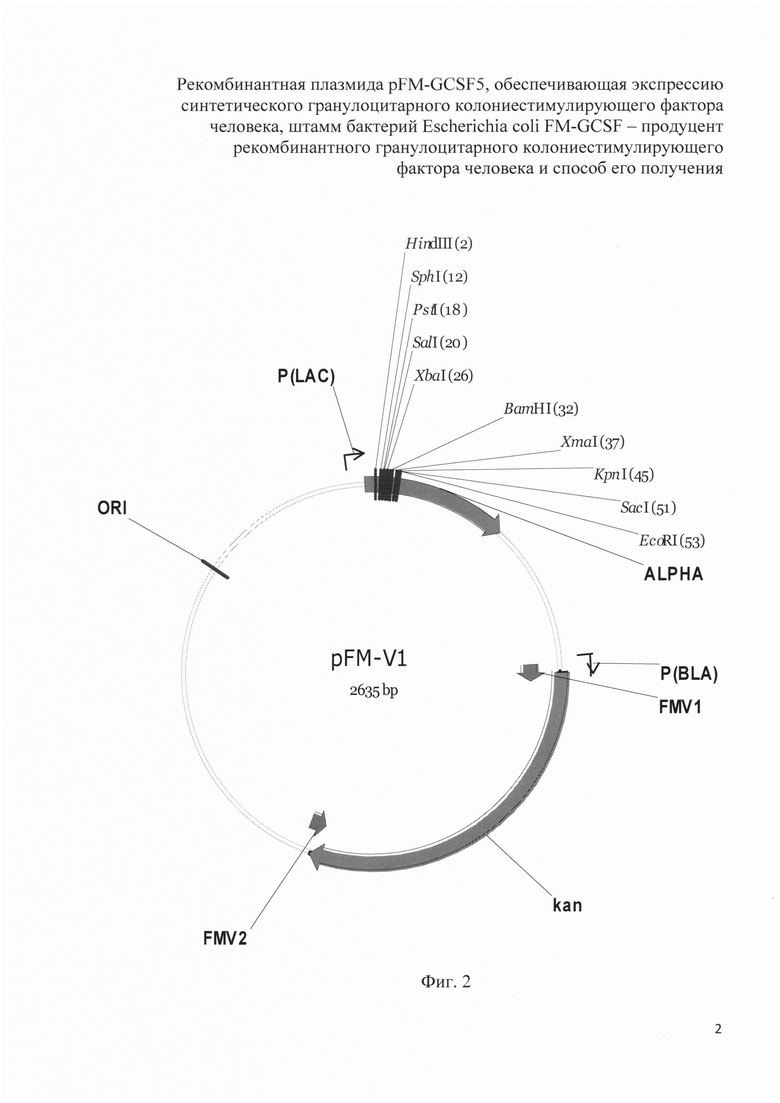
На фиг. 2 изображена рестрикционная карта рекомбинантной плазмиды pFM-V1.
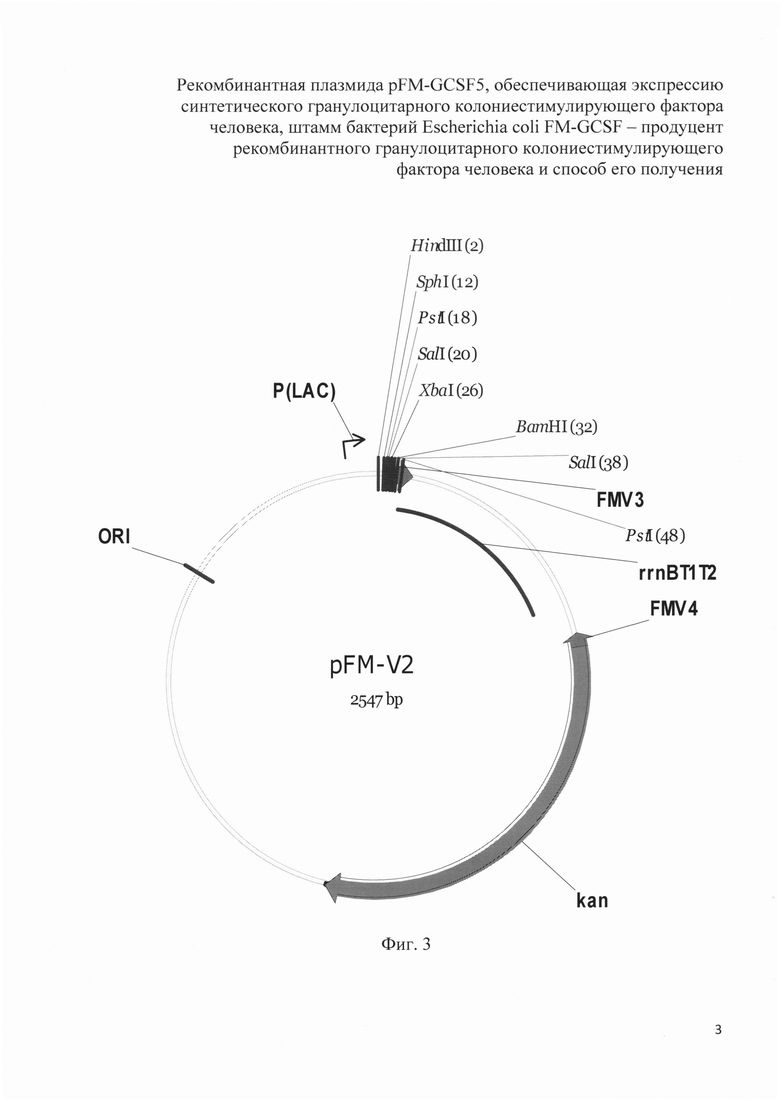
Фиг.3 показывает рестрикционную карту рекомбинантной плазмиды pFM-V2.
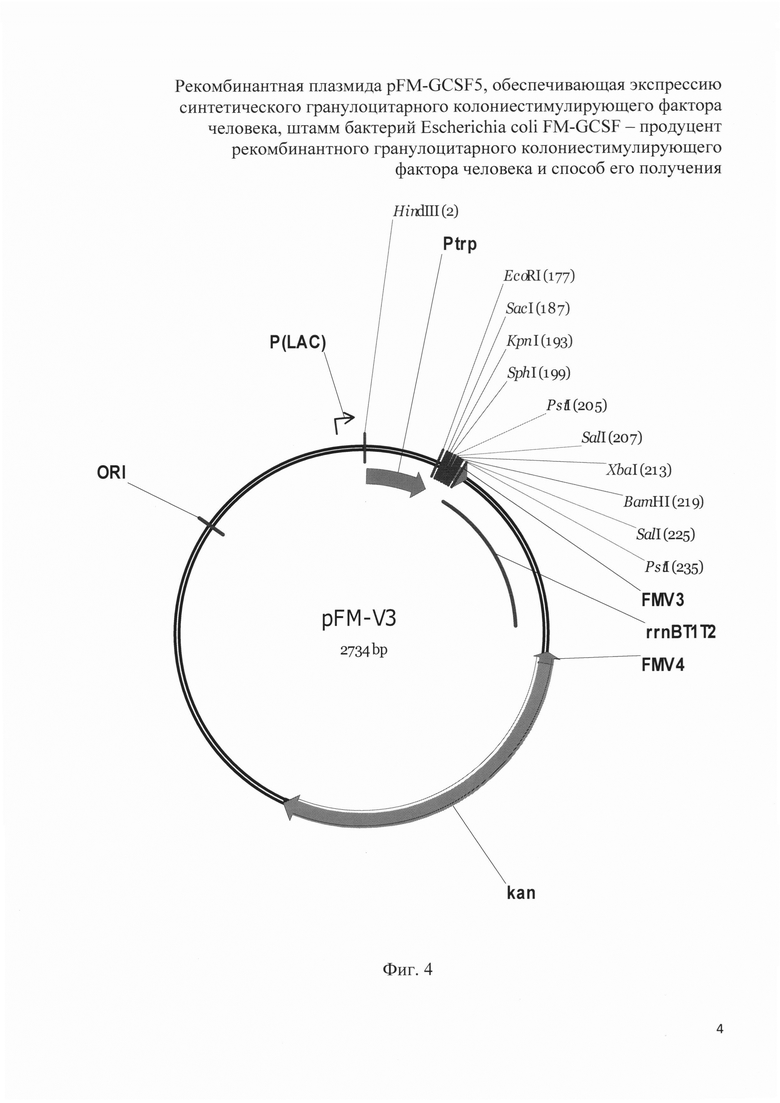
На фиг. 4 показана рестрикционная карта рекомбинантной плазмиды pFM-V3.
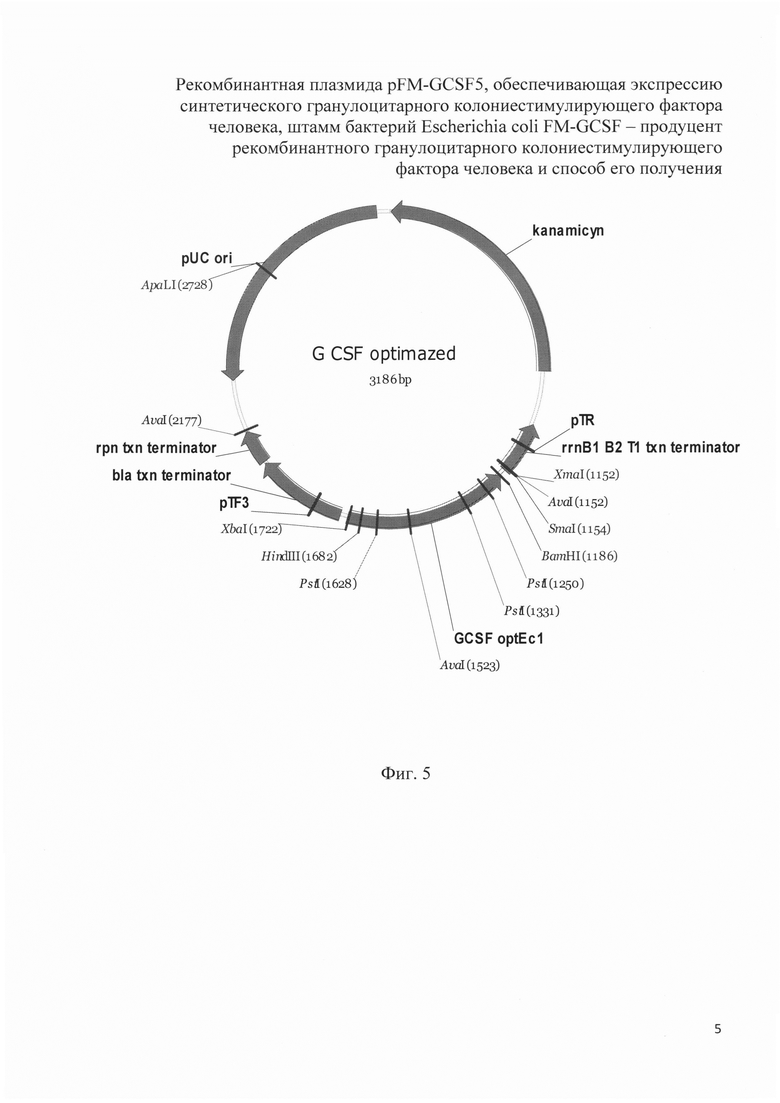
На фиг. 5 представлена рестрикционная карта рекомбинантной плазмиды pG CSF optimized.
На фиг. 6 представлена нуклеотидная последовательность синтетического гена филграстима человека.
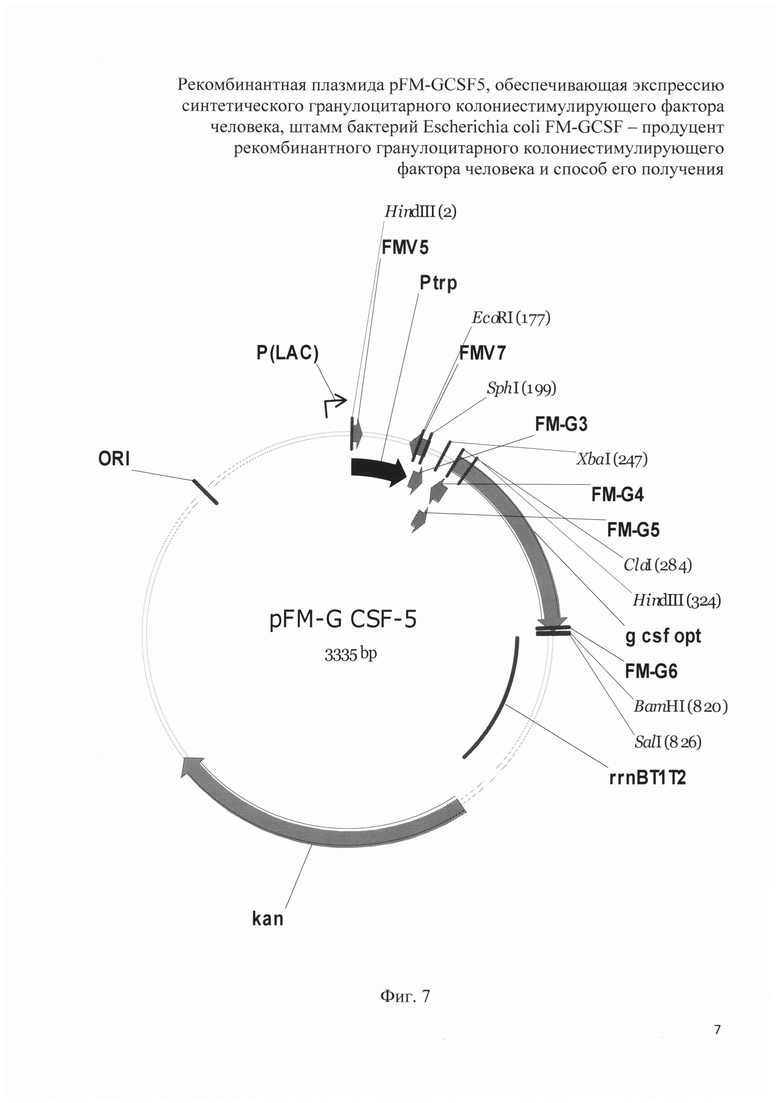
На фиг. 7 изображена рестрикционная карта рекомбинантной плазмиды pFM-GCSF-5.
Сущность изобретения заключается в следующем.
Рекомбинантная плазмидная ДНК pFM-GCSF-5 кодирует синтез Г-КСФ человека под контролем триптофанового и лактозного промоторов и терминатора транскрипции rrnВТ1Т2, содержит в качестве генетического маркера синтетический ген kan, детерминирующий устойчивости к канамицину. Моноплазмидный штамм E.coli BL21, содержащий рекомбинантную плазмиду pFM-GCSF-5, обладает высоким уровнем экспрессии Г-КСФ (2-3 г с 1 л культуральной среды).
Плазмида pFM-GCSF-5 имеет 3335 пар оснований (п.о.), и характеризуется наличием следующих фрагментов:
- фрагмент ДНК размером 287 п.о., включающий триптофановый промотор E.coli и последовательность Шайн Дельгарно, ответственную за инициацию трансляции;
- синтетический фрагмента ДНК размером 531 п.о., включающий «оптимизированную» кодирующую часть гена гранулоцитарного колониестимулирующего фактора человека; при оптимизации гена Г КСФ из последовательности были удалены внутренние TATA-boxes, chi-sites, RBS последовательности, AT-богатые и GC-богатые последовательности, повторяющиеся последовательности и потенциальные вторичные структуры мРНК; codon usage был адаптирован для Е. coli, при этом параметр CAI (codon adaptation index) = 0,99;
- фрагмент ДНК плазмиды рKK223-3 размером 534 п.о, включающий последовательность строгого терминатора транскрипции rrnВТ1Т2, последовательности промотора и SD последовательность гена бета-лактамазы
- синтетический фрагмент ДНК размером 810 п.о., включающий синтетический ген kan, обеспечивающий устойчивость к канамицину - аналога гена kan из транспозона Tn903, в котором удалены сайты рестрикции AvaI, ClaI, SmaI, HindIII
- фрагмент ДНК размером 1173 п.о. плазмиды pUC19, включающий последовательности ответственную за репликацию плазмиды (ori) и лактозный промотор.
Физическая карта плазмиды pFM-GCSF-5 представлена на фиг. 7. Нуклеотидная последовательность синтетического гена Г-КСФ человека, встроенного в плазмиду pFM-GCSF-5, приведена на фиг. 6.
Рекомбинантный штамм бактерий E.coli FM-GCSF получен путем трансформации клеток штамма Е. coli BL21 рекомбинантной плазмидной ДНК pFM-G-CSF-5.
Штамм E.coli FM-GCSF характеризуется следующими признаками:
Культурально-морфологические признаки.
Штамм обладает свойствами типичного представителя вида Escherichia coli. Клетки мелкие, прямые, утолщенной палочковидной формы, грамотрицательные, неспороносные.
Штамм хорошо растет на простых питательных средах. Колонии при росте штамма на L агаре - круглые, гладкие, выпуклые, мутные, блестящие, серые, с ровными краями. В жидких средах (в минимальной среде с глюкозой или в L-бульоне) штамм образует интенсивную ровную муть.
Физиолого-биохимические признаки.
Штамм растет в аэробных условиях, при температуре в пределах от 4 до 42°С. Оптимум рН для роста составляет 6,5-7,5.
В качестве источника азота клетки штамма используют минеральные соли в аммонийной или нитратной формах; органические соединения, в частности, аминокислоты, пептон, триптон, дрожжевой экстракт и т.д.
В качестве источника углерода клетки штамма могут использовать аминокислоты, глицерин, углеводы.
Устойчивость к антибиотикам.
Штамм проявляет устойчивость к канамицину (100 мкг/мл).
Особенность штаммов.
Продуцирует Г-КСФ.
Условия хранения штаммов.
Штаммы хранится: под маслом в L-агаре с добавлением канамицина до концентрации 100 мкг/мл; криоконсервированным в L-бульоне, содержащем 15% глицерина и антибиотик канамицин 100 мкг/мл, в ампулах при температуре минус 40°-70°С; или в лиофилизированном состоянии в ампулах при температуре плюс 4°С.
Штамм E.coli FM-GCSF стабильно синтезируют Г-КСФ с высоким уровнем экспрессии (2-3 г с 1 л культуральной жидкости). Штамм технологичен и для достижения высокой продуктивности не требуют особых условий для культивирования, специальных индукторов экспрессии целевого продукта, а также применения сложных питательных сред, включающих компоненты животного происхождения.
Целевой продукт накапливается в количестве более 20-30% суммарного белка клетки в виде тел включения Использование нового продуцента, содержащий плазмиду pFM-GCSF-5, позволит значительно повысить выход целевого продукта, а также упростить технологический процесс получения Г-КСФ за счет упрощения стадии культивирования штаммов.
Изобретение иллюстрируется, но не ограничивается следующими примерами.
Пример 1. Конструирование рекомбинантной плазмиды pFM-GCSF-5, обеспечивающей экспрессию синтетического гена Г-КСФ.
Способ получения рекомбинантной плазмиды pFM-GCSF-5 включает несколько последовательных этапов:
- конструирование векторной плазмиды pFM-V1 (2635 п.о.);
- конструирование векторной плазмиды pFM-V2 (2547 п.о.);
- конструирование рекомбинантной плазмиды pFM-V3 (2734 п.о.);
- конструирование рекомбинантной плазмиды pFM-GCSF-5 (3335 п.о.);
1.1. Конструирование векторной плазмиды pFM-V1.
Исходным вектором при получении векторной плазмиды pFM-V1 служит вектор pUC19, в котором кодирующая последовательность гена бета-лактамазы, обеспечивающего устойчивость к ампициллину, заменена на кодирующую последовательность синтетического гена кап, обеспечивающего устойчивость к канамицину. Для получения векторной плазмиды pFM-V1 проводят 2 раунда амплификации ДНК. Для первого раунда реакции амплификации используют два синтетических олигонуклеотида FMV1 и FMV2:
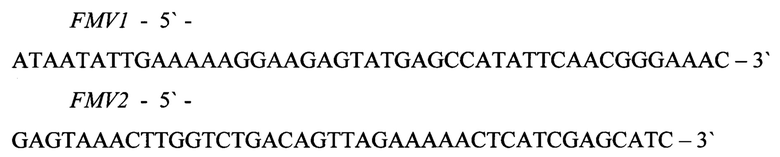
и в качестве матрицы ДНК - рекомбинантная плазмида pGCSF optimized, содержащая синтетический ген kan - аналог гена кап из транспозона Тп903, в котором удалены сайты рестрикции AvaI, ClaI, SmaI, HindIII. Нуклеотидная последовательность синтетического гена кап, приведена на рис. 1. Рестрикционная карта рекомбинантной плазмиды pGCSF optimized приведена на фиг. 5
Амплификацию и все последующие проводят в ДНК-амплификаторе в буферном растворе, содержащем: 20 mM Tis - HCl, рН 8.8, 10 mM (NH4)2SO4, 10 mM KCl, 2 mM MgCl2, 0.1% Triton X100, 0.1 mg/ml BSA, 0.2 mM каждого dNTP, 1.25 ед. Pfu ДНК полимеразы, 100 нг ДНК матрицы при следующих режимах: прогревание - 5 мин при 96°С, далее 35 циклов ПЦР (режимы одного цикла: 30 с при 96°С, 30 с при 58°С, 1 мин при 72°С и затем финальная элонгация - 10 мин при 72°С). В результате ПЦР получают фрагмент размером 852 п.о., который электрофоретически очищают.
Для второго раунда амплификации используют векторную ДНК плазмиды pUC19 и полученный фрагмент ДНК, полученный в первом раунде амплификации в эквимолярных количествах при следующих режимах: прогревание - 5 мин при 96°С, далее 6 циклов ПЦР (режимы одного цикла: 30 с при 96°С, 30 с при 58°С, 3 мин при 72°С и затем финальная элонгация - 10 мин при 72°С). Полученной ДНК во втором раунде ПЦР трансформируют в клетки штамма E.coli DH5α и высевают на среду LA, содержащую 100 мкг/мл канамицина. После инкубирования в течение 12 ч при 37°С, клоны отсевают, выделяют плазмидную ДНК, проводят рестрикционный анализ и определяют первичную структуру ДНК. В результате получают плазмиду pFM-V1 размером 2635 п.о. Рестрикционная карта рекомбинантной плазмиды pFM-V1 приведена на фиг. 2.
1.2. Конструирование векторной плазмиды pFM-V2.
Векторная плазмида pFM-V2 представляет собой плазмиду pFM-V1, в которой после сайта BamHI последовательность ДНК, кодирующая альфа LacZ пептид и промотор бета-лактомазы заменена на последовательность ДНК, кодирующая терминатор транскрипции rrnВТ1Т2 и промотор бета-лактомазы из ДНК вектора рKK223-3. Генетическое конструирование плазмиды pFV-V-2 осуществляют в два раунда амплификации ДНК с помощью полимеразной цепной реакции (ПЦР). Для первого раунда реакции амплификации используют два синтетических олигонуклеотида FMV3 и FMV4:
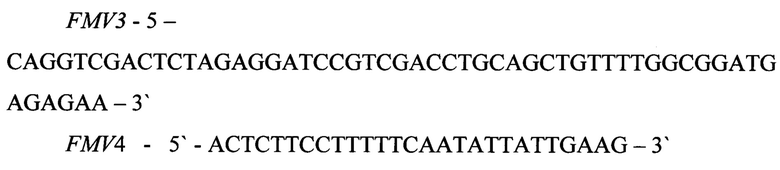
и в качестве матрицы ДНК плазмиды рKK223-3. ПЦР проводят при следующих режимах: прогревание - 5 мин при 96°С, далее 35 циклов ПЦР (режимы одного цикла: 30 с при 96°С, 30 с при 58°С, 1 мин при 72°С и затем финальная элонгация - 10 мин при 72°С). В результате ПЦР получают фрагмент размером 549 п.о., который электрофоретически очищают.
Для второго раунда амплификации используют векторную ДНК плазмиды pFM-V1 и, полученный фрагмент ДНК в первом раунде амплификации, в эквимолярных количествах при следующих режимах: прогревание - 5 мин при 96°С, далее 6 циклов ПЦР (режимы одного цикла: 30 с при 96°С, 30 с при 58°С, 3 мин при 72°С и затем финальная элонгация - 10 мин при 72°С). Полученной ДНК во втором раунде ПЦР трансформируют в клетки штамма E.coli DH5α и высевают на среду LA, содержащую 100 мкг/мл канамицина, IPTG, X-gal. После инкубирования в течение 12 ч при 37°С, белые колонии пересевают, выделяют плазмидную ДНК, проводят рестрикционный анализ и определяют первичную структуру ДНК. В результате получают плазмиду pFM-V2 размером 2547 п.о. Рестрикционная карта рекомбинантной плазмиды pFM-V2 приведена на фиг. 3.
1.3. Конструирование векторной плазмиды pFM-V3.
Векторная плазмида pFM-V-3 представляет собой плазмидуpFM-V2, в которой между сайтами HindIII и SphI клонирован фрагмент ДНК, кодирующий бактериальный триптофановый промотор Е. coli размером 187 п.о. Генетическое конструирование плазмиды pFM-V3 осуществляют, используя один раунд амплификации ДНК, с помощью полимеразной цепной реакции (ПЦР). Для этого используют два синтетических олигонуклеотида FMV5 и FMV7, а в качестве матрицы тотальную ДНК E.coli.

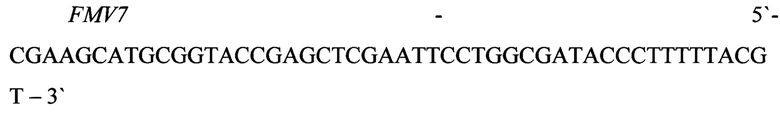
ПЦР фрагмент ДНК размером 199 п.о. и ДНК плазмиды pFM-V2 обрабатывают ферментами рестрикции HindIII и SphI. Полученные ПЦР фрагмент ДНК размером 187 п.о. и фрагмент ДНК плазмиды pFM-V2 размером 2547 п.о. очищают с помощью электрофореза в 1%-ном агарозном геле, лигируют ферментом лигазой фага Т4, трансформируют в компетентые клетки штамма E.coli DH5α и высевают на среду LA, содержащую 100 мкг/мл канамицина. После инкубирования в течение 12 ч при 37°С, клоны отсевают, выделяют плазмидную ДНК, проводят рестрикционный анализ и определяют первичную структуру ДНК.
В результате получают плазмиду pFM-VS размером 2734 п.о. Рестрикционная карта рекомбинантной плазмиды pFM-V3 приведена на фиг. 4.
1.4. Конструирование векторной плазмиды pFM-G CSF-5.
Плазмида pFM-G CSF-5 представляет собой плазмиду pFM-V3, в которую по сайтам рестрикции SphI и BamHI клонирован фрагмент ДНК размером 637 п.о., кодирующий SD последовательность из векторной плазмиды pRSET-A и синтетический ген G CSF. Синтетический ген G CSF был получен стандартным методом химико-ферментативного синтеза и клонирован в составе рекомбинантной плазмиды pGCSF optimazed, размером 3186 п.о. Рестрикционная карта рекомбинантной плазмиды pGCSF optimazed приведена на фиг. 5. Нуклеотидная последовательность синтетического гена G CSF человека приведена на фиг. 6.
Конструирование рекомбинантной плазмиды pFM-G CSF-5 проводят следующим образом.
На первом этапе получают фрагмент фрагмент ДНК размером 637 п.о., кодирующий SD последовательность из векторной плазмиды pRSET-A и синтетический ген G CSF фланкированный сайтами рестрикции EcoRI и BamHI. Этот фрагмент ДНК получают в результате трех раундов ПЦР.
В первом раунде ПЦР используя праймеры FM-G3 и FM-G4, а в качестве матрицы ДНК векторной плазмиды pREST-A, получают фрагмент ДНК размером 111 п.о., кодирующий SD последовательность и N-конец гена G CSF.
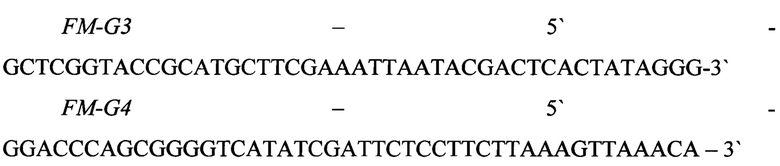
Во втором раунде ПЦР используя праймеры FM-G5 и FM-G6, а в качестве матрицы ДНК плазмиды G CSF optimazed, получают фрагмент ДНК размером 564 п.о., кодирующий полный синтетический ген G CSF.

В третьем раунде ПЦР используя праймеры FM-G3 и FM-G6, а в качестве матриц ДНК фрагментов первых двух раундов ПЦР, получают объединенный фрагмент ДНК размером 631 п.о., кодирующий SD последовательность и синтетический ген G CSF, фланкированный сайтами рестрикции EcoRI и BamHI.
На втором этапе полученный фрагмент ДНК клонируют в векторную плазмиду pFM-V3 по сайтам рестрикции EcoRI и BamHI. Для этого полученный фрагмент ДНК в третьем раунде ПЦР и ДНК векторной плазмиды pFM-V3 обрабатывают ферментами рестрикции EcoRI и BamHI. Полученные фрагменты EcoRI-BamHI фрагмент ДНК размером 2698 п.о. из плазмиды pFM-V3 и фрагмент ДНК размером 637 п.о. от третьего раунда ПЦР очищают с помощью электрофореза в 1%-ном агарозном геле. Далее электрофоретически очищенные фрагменты объединяют, лигируют ферментом лигазой фага Т4.
ДНК трансформируют в клетки штамма E.coli DH5α и высевают на среду LA, содержащую 100 мкг/мл канамицина. После инкубирования в течение 12 ч при 37°С, клоны отсевают, выделяют плазмидную ДНК, проводят рестрикционный анализ и определяют первичную структуру ДНК.
В результате получают плазмиду pFM-GCSF-5 размером 3335 п.о., содержащая синтетический ген G CSF человека. Рестрикционная карта рекомбинантной плазмиды pFM-GCSF-5 приведена на фиг. 7.
Пример 2. Конструирование рекомбинантного штамма Escherichia coli FM-GCSF.
Путем трансформации клеток штамма Е. coli BL21 рекомбинантной плазмидой pFM-GCSF-5 получают штаммы Escherichia coli FM-GCSF. Трансформанты высевают на среду LA, содержащую 100 мкг/мл канамицина.
Пример 3. Культивирование штамма Е. coli FM-GCSF.
Посевной материал штамма Е. coli FM-GCSF культивируют в течение 12 ч при 28°С в 3 л синтетической минерально-солевой среды, содержащей 2хМ9, 1% глюкозы, следовые количества металлов и 100 мг/мл канамицина и асептически вносят в ферментер, содержащий 27 л этой же стерильной синтетической минерально-солевой среды.
Культивирование в ферментере проводят при температуре 28±1°С, поддерживая рН 6,9±0,15 до оптической плотности 10-12 о.е., после чего температуру поднимают до 38°С и культивирование продолжают до достижения стационарной фазы. Концентрацию растворенного кислорода в диапазоне (30±0,5) % от насыщения поддерживают путем изменения скорости оборотов мешалки от 100 до 800 об/мин и подачи воздуха от 1 до 15 л/мин. Концентрацию субстратов, в частности глюкозы, поддерживают в течение ферментации путем подачи концентрированного 40% раствора глюкозы перистальтическим насосом.
Накопление рч Г-КСФ в виде нерастворимой формы - "телец включений" контролируют с помощью фазово-контрастной микроскопии. Ферментацию останавливают по достижении максимальной оптической плотности (~50-60 о.е.). Содержание рч Г-КСФ в биомассе клеток, получаемой с 1 л культуры, составляет 2-3 г рч Г-КСФ.
По окончании ферментации культуральную жидкость сепарируют центрифугированием, бактериальную биомассу фасуют в полиэтиленовые пакеты и замораживают при температуре минус 70°С.
Пример 4. Способ получения Г-КСФ человека из биомассы штамма Е. coli FM-GCSF.
Получение Г-КСФ проводят в три этапа:
1 этап. Выделение и очистка нерастворимой формы Г-КСФ человека.
2 этап. Растворение и ренатурация Г-КСФ человека.
3 этап. Хроматографическая очистка Г-КСФ человека.
1 этап. Выделение и очистка нерастворимой формы Г-КСФ человека.
Выделение и очистка нерастворимой формы Г-КСФ (в виде "телец включений" или "inclusion bodies") проводят по стандартной схеме, используемой для выделения и очистки большинства inclusion bodies (RU 610173, US 5849883, US 5789551, RU 2165455, RU 2242516). В конце процесса выделения и очистки нерастворимой формы Г-КСФ (тельца включений или т.вкл.) из 1,00-1,5 кг биомассы полученный материал суспендируют в 1,0 л буфера (20 мМ Tris/HCl, рН 8.0).
2 этап. Растворение и ренатурация Г-КСФ человека.
Тельца включений растворяют добавлением мочевины до 8 М и дитиотреитол до концентрации 5 мМ в конечном объеме 2,0 литров, инкубируют 2 час при комнатной температуре, центрифугируют (20000 g) и фильтруют (0,22 микрон). Полученный раствор Г-КСФ вливают в емкость, содержащая 30 литров буфера - 20 мМ Tris/HCl, рН 8.0, 1,0 М мочевины, 50 μM CuSO4 при температуре 15°С. Далее добавляют PMSF до концентрации 0,2 мМ. Ренатурацию проводят в течение 10-12 часов при 15°С. Процесс ренатурации останавливают, добавляя ЭДТА до концентрации 0,5 мМ. Далее раствор Г-КСФ фильтруют через мембранный фильтр с диаметром пор 0,22 микрона, проводят замену буфера на буфер - 20 мМ Tris/HCl, рН 7.0, 0.1 мМ ЭДТА диафильтрацией на тангенциальных касетах (диаметр пор 10К) и окончательно концентрируют до объема 20 л. Далее добавляют концентрированный раствор ацетата натрия 2,5 М рН 4,5 до концентрации 25 мМ и инкубируют 10-12 часов при 4°С. Раствор Г-КСФ фильтруют через мембранный фильтр с диаметром пор 0,22 микрон.
3 этап. Хроматографическая очистка Г-КСФ человека.
1. Полученный раствор рч Г-КСФ очищают на катионообменной смоле Toyopearl СМ-650М (Tosoh Bioscience). Г-КСФ элюируют градиентом создаваемый буфером 20 мМ Na цитрат, рН 5.0, 0.1 мМ ЭДТА и буфером 20 мМ Na цитрат, рН 5.0, 0.1 мМ ЭДТА, 0,2 M NaCl.
2. Далее Г-КСФ очищают на анионообменнике Toyopearl DEAE-650M (Tosoh Bioscience) или Macro-Prep DEAE (Bio-Rad). Г-КСФ элюируют градиентом создаваемый буферами 20 мМ Tris/HCl, рН 8.0, 0.1 мМ ЭДТА и 20 мМ Tris/HCl, рН 8.0, 0.1 мМ ЭДТА, 0.5 М NaCl.
3. Полученный раствор Г-КСФ очищают на катионообменной смоле Toyopearl SP-650M (Tosoh Bioscience) или Nuvia HR-S (Bio-Rad). Г-КСФ элюируют градиентом создаваемый буфером 20 мМ Na цитрат, рН 5.0, 0.1 мМ ЭДТА и буфером 20 мМ Na цитрат, рН 5.5, 0.1 мМ ЭДТА, 0,2 M NaCl.
4. Окончательно Г-КСФ очищают методом колоночной гель-фильтрации на смоле Sephacryl S200 (GE Healthcare). Хроматографию проводят в буфере 10 мM Na цитрат, рН 3,8.
Описанный способ выделения и очистки рекомбинантного Г-КСФ человека дает возможность получать примерно 0,5-1,0 грамма субстанции фармакопейного качества за один цикл, получаемой с 1,0 л ферментационной среды. Полученный в результате использования указанной технологии конечный продукт сохраняет свои свойства в течение более 2 лет при хранении при температуре минус 4-10°С.


Изобретение относится к биотехнологии, в частности к рекомбинантной плазмиде pFM-GCSF5, кодирующей экспрессию гранулоцитарного колониестимулирующего фактора человека (далее Г-КСФ), к рекомбинантному штамму Escherichia coli FM-GCSF - продуценту рекомбинантного Г-КСФ человека, а также к способу получения рекомбинантного Г-КСФ человека. Рекомбинантный штамм бактерий E.coli FM-GCSF получают путем трансформации клеток штамма Е. coli BL21 рекомбинантной плазмидной ДНК pFM-GCSF-5. Рекомбинантная плазмидная ДНК pFM - GCSF-5, размером 3335 п.о., кодирует синтез Г-КСФ человека под контролем лактозного и триптофанового промотора и терминатора транскрипции ггпВТ1Т2 и содержит в качестве генетического маркера синтетический ген kan, детерминирующий устойчивости к канамицину. Изобретение позволяет получать рекомбинантный Г-КСФ человека с высоким выходом и по упрощенной технологии. 3 н.п. ф-лы, 7 ил.
1. Рекомбинантная плазмида pFM-GCSF5, обеспечивающая экспрессию синтетического гена гранулоцитарного колониестимулирующего фактора человека, имеющая размер 3335 п.о. и состоящая из следующих элементов: фрагмент ДНК размером 194 п.о., включающий триптофановый промотор E.coli и последовательность Шайн Дельгарно, ответственную за инициацию трансляции; синтетический фрагмент ДНК размером 503 п.о., включающий «оптимизированную» кодирующую часть гена Г-КСФ человека; при оптимизации гена Г-КСФ из последовательности были удалены внутренние TATA-boxes, chi-sites, RBS последовательности, AT-богатые и GC-богатые последовательности, повторяющиеся последовательности и потенциальные вторичные структуры мРНК; codon usage был адаптирован для Е. coli, при этом параметр CAI (codon adaptation index)=0,99; фрагмент ДНК плазмиды pKK223-3 размером 534 п.о., включающий последовательность строгого терминатора транскрипции rrnBT1T2, последовательности промотора и SD последовательность гена бета-лактамазы; синтетический фрагмент ДНК размером 810 п.о., включающий синтетический ген kan, обеспечивающий устойчивость к канамицину - аналогу гена kan из транспозона Tn903, в котором удалены сайты рестрикции AvaI, ClaI, SmaI, HindIII; фрагмент ДНК размером 1173 п.о. плазмиды pUC19, включающий последовательность, ответственную за репликацию плазмиды (ori), и лактозный промотор.
2. Штамм бактерий Escherichia coli FM-G-CSF, полученный путем трансформации клеток штамма Е. coli BL21 рекомбинантной плазмидной ДНК pFM-GCSF-5 по п. 1, - продуцент рекомбинантного Г-КСФ человека.
3. Способ получения рекомбинантного Г-КСФ человека, включающий культивирование штамма бактерий Escherichia coli FM-G-CSF по п. 2 на синтетической минерально-солевой среде, содержащей 2xМ9, 1% глюкозы, следовые количества металлов, 100 мг/мл канамицина, и, необязательно, выделение и очистку нерастворимой формы Г-КСФ человека, растворение и ренатурацию Г-КСФ человека и хроматографическую очистку Г-КСФ человека.
Авторы
Даты
2019-02-28—Публикация
2018-05-25—Подача