Заявление о федеральном финансировании исследования или разработки
[0001] Часть этой работы финансировалась за счет средств федерального бюджета по контракту DOE/NETL № DE-FE0001259.
Предпосылки создания изобретения
Область техники, к которой относится изобретение
[0002] Настоящее изобретение относится к производству жидких топлив, в частности, к конверсии (переработке) угля в жидкость в пласте (in-situ) или вне пласта (ex-situ).
Уровень техники
[0003] Угли могут также конвертироваться в жидкие топлива, такие как бензин или дизельное топливо, посредством нескольких различных процессов. При разработке промышленного процесса уголь сначала конвертируют в газ, а затем в жидкость с применением процесса Фишера-Тропша (ФТ). В ФТ-процессе, представляющем собой непрямой путь производства топлива, уголь сначала газифицируют, получая сингаз (синтез-газ), очищенную смесь СО и газа Н2. Затем ФТ-катализаторы используют для конверсии сингаза в легкие углеводороды, такие как этан, которые затем перерабатывают в пригодные для дальнейшей переработки жидкие топлива. Помимо создания топлива, сингаз можно также конвертировать в метанол, который может использоваться в качестве топлива или топливной присадки.
[0004] Альтернативно, уголь может конвертироваться непосредственно в жидкие топлива посредством процессов гидрогенизации. Например, применяют способ Бергиуса, в котором уголь ожижают, смешивая его с наводороженным газом и нагревая систему. Было разработано несколько других процессов прямого ожижения, таких как процессы рафинирования угля в процессе гидрогенизации, который привел к созданию нескольких опытно-промышленных объектов. Помимо этого, подсушенная угольная пыль, смешанная с приблизительно 1% масс. молибденовых катализаторов, может быть гидрогенизирована, при этом может быть получен синтез-газ под давлением. Однако сингаз должен быть получен в отдельном газификаторе.
[0005] В то же время, процессы переработки угля в жидкое топливо включают в себя добычу угля из-под земли. Как документально доказано, добыча угля представляет собой опасный процесс, и многие угольные шахты приходится закрывать, прежде чем будут извлечены все пригодные для использования продукты. Кроме того, в тех шахтах, которые эксплуатируются безопасным способом, остаются столбы угля, поддерживающие потолок, и остатки угля в стенах шахты. Эти источники угля представляют значительное количество энергии, которое остается неиспользованным после горнодобывающих работ. Кроме того, эти нетронутые ресурсы могут быть конвертированы в жидкое топливо для последующей транспортировки. В связи с этим, в отрасли существует потребность в извлечении брошенного, низкокачественного или остаточного угля горнодобывающих работ для использования при производстве жидкости на основе угля.
Сущность изобретения
[0006] В настоящей заявке раскрыт способ получения жидкого углеводородного продукта, включающий в себя измельчение источника углеводородов; предварительный нагрев измельченного источника углеводородов; солюбилизацию измельченного источника углеводородов с образованием суспензии, содержащей молекулу реактанта источника углеводородов; подмешивание биохимического раствора к суспензии, причем биохимический раствор содержит по меньший мере один фермент конверсии с возможностью содействия селективно-связывающей фотофрагментации указанной молекулы реактанта источника углеводородов с образованием жидких углеводородов с помощью катализируемой ферментом селективно-связывающей фотофрагментации, причем указанный фермент конверсии содержит реакционноспособные центры с возможностью ограничения указанной молекулы реактанта таким образом, чтобы фотофрагментация благоприятно воздействовала на заранее выбранную внутреннюю связь указанной молекулы реактанта; отделение жидких углеводородов от суспензии, причем загрязняющие примеси остаются в суспензии; и обогащение жидких углеводородов с образованием жидкого углеводородного продукта.
[0007] В одном из вариантов осуществления измельчение источника углеводородов включает в себя раздробление источника углеводородов. В одном из вариантов осуществления раздробление включает в себя размалывание. В одном из вариантов осуществления раздробление включает в себя гидротермальную обработку под давлением. В одном из вариантов осуществления предварительный нагрев измельченного источника углеводородов включает в себя предварительную химическую обработку, предварительную тепловую обработку, окисление источника углеводородов или их комбинацию.
[0008] В одном из вариантов осуществления солюбилизация с помощью измельченного источника углеводородов включает в себя обработку измельченного источника углеводородов с помощью по меньшей мере одного фермента. В одном из вариантов осуществления подмешивание биохимического раствора включает в себя подмешивание по меньшей мере одного дополнительного фермента. В одном из вариантов осуществления подмешивание по меньшей мере одного дополнительного фермента дополнительно включает в себя подмешивание фермента для конверсии источника углеводородов в более низкомолекулярные углеводороды.
[0009] В одном из вариантов осуществления отделение жидких углеводородов (сепарация) включает в себя процесс осаждения суспензии из жидкого углеводорода. В одном из вариантов осуществления отделение жидких углеводородов включает в себя процесс осаждения загрязняющих примесей из жидкого углеводорода. В одном из вариантов осуществления обогащение жидкого углеводорода включает в себя подмешивание к жидкому углеводороду по меньшей мере одного фермента.
[0010] В одном из вариантов осуществления биохимический раствор содержит модифицированный фермент. В одном из вариантов осуществления модифицированный фермент содержит генетически модифицированный фермент. В одном из вариантов осуществления модифицированный фермент содержит химически модифицированный фермент.
[0011] В одном из вариантов осуществления способ осуществляется в пласте в угольной шахте или вне пласта на угле, добытом шахтным способом. В одном из вариантов осуществления обогащение жидких углеводородов включает в себя улучшение качеств жидкого углеводородного продукта до перегонки. В одном из вариантов осуществления жидкий углеводородный продукт содержит по меньшей мере одно вещество, выбранное из группы, состоящей из бензина, дизельного топлива, керосина и их дистиллятов. В одном из вариантов осуществления источник углеводородов содержит по меньшей мере одно вещество, выбранное из группы, состоящей из угля, антрацитового угля, битуминозного угля, лигнита, полубитуминозного угля, угля низких сортов, кокса, нефтеносного песка и горючего сланца.
[0012] В настоящей заявке раскрыт способ конверсии в пласте угля в жидкий углеводород, включающий в себя: определение местоположения подземного угольного пласта; бурение по меньшей мере одной скважины, находящейся в контакте с подземным угольным пластом и имеющей средства для циркуляции жидкостей через нее; повышение давления в подземном угольном пласте с помощью пара; циркуляцию реагентов через подземный угольный пласт, причем реагенты содержат по меньшей мере один фермент, с образованием суспензии; извлечение части суспензии; переработку суспензии для получения жидкого углеводорода; отделение жидкого углеводорода от суспензии; и возвращение суспензии в угольный пласт для дальнейшей переработки.
[0013] В одном из вариантов осуществления по меньшей мере одна скважина сообщается по текучей среде с потоком реактантов. В одном из вариантов осуществления по меньшей мере одна скважина сообщается по текучей среде с потоком обработки суспензии.
[0014] В одном из вариантов осуществления циркуляция реактантов с образованием суспензии дополнительно включает в себя солюбилизацию угля с образованием суспензии; конверсию угля с образованием жидких углеводородов; отделение загрязняющих соединений от жидких углеводородов, причем загрязняющие соединения содержат загрязнители окружающей среды; осаждение суспензии из жидких углеводородов, причем жидкие углеводороды пригодны для жидких топлив; и переработку жидких углеводородов в жидкие топлива.
[0015] В одном из вариантов осуществления этап солюбилизации угля включает в себя обработку угля с помощью по меньшей мере одного фермента. В одном из вариантов осуществления этап конверсии угля включает в себя обработку угля с помощью по меньшей мере одного фермента. В одном из вариантов осуществления этап отделения загрязняющих соединений включает в себя обработку жидких углеводородов с помощью по меньшей мере одного фермента.
[0016] Дополнительно раскрыт способ применения фермента для получения жидких топлив, содержащий выбор микроорганизма, производящего фермент; генетическую модификацию микроорганизма для увеличения производства фермента; структурную модификацию микроорганизма для изменения активности фермента с образованием модифицированного фермента; сбор модифицированного фермента с образованием биохимического раствора, содержащего по меньшей мере один модифицированный фермент; и подвергание источника углеводородов воздействию биохимического раствора с образованием прекурсора жидкого топлива.
[0017] В одном из вариантов осуществления этап выбора микроорганизма содержит выбор по меньшей мере одного микроорганизма, выбираемого из группы, состоящей из гиполитов, эндолитов, криптолитов, ацидофилов, алкалофилов, термофилов, литоавтотрофов, галофилов, пьезофилов и их комбинаций. В одном из вариантов осуществления модификация микроорганизма включает в себя введение вектора нуклеиновой кислоты. В одном из вариантов осуществления генетическая модификация организма включает в себя направленный мутагенез. В одном из вариантов осуществления модификация фермента включает в себя структурное изменение фермента. В одном из вариантов осуществления подвергание источника углеводородов воздействию биохимического раствора дополнительно содержит направленную фрагментацию с помощью проходящего излучения.
[0018] В одном из вариантов осуществления способ получения жидких углеродных продуктов включает в себя измельчение источника углеводородов, химическую обработку измельченного источника углеводородов, солюбилизацию измельченного источника углеводородов, подмешивание биохимического раствора, причем биохимический раствор содержит по меньший мере один фермент для образования жидких углеводородов, отделение жидких углеводородов и обогащение жидких углеводородов с образованием жидкого углеродного продукта.
[0019] В другом варианте осуществления способ конверсии в пласте угля в жидкий углеводород, включает в себя: определение местоположения подземного угольного пласта; бурение по меньшей мере одной скважины, находящейся в контакте с подземным угольным пластом; повышение давления в подземном угольном пласте с помощью пара; циркуляцию реактантов через подземный угольный пласт, причем реактанты содержат по меньшей мере один фермент, с образованием суспензии; извлечение части суспензии; переработку суспензии, причем жидкий углеводород отделен от суспензии; и возвращение суспензии в угольный пласт для дальнейшей переработки.
[0020] В дополнительных вариантах осуществления способ применения фермента для получения жидких топлив содержит выбор микроорганизма, производящего фермент; генетическую модификацию микроорганизма для увеличения производства фермента; структурную модификацию микроорганизма для изменения активности фермента с образованием модифицированного фермента; сбор модифицированного фермента с образованием биохимического раствора, содержащего по меньшей мере один модифицированный фермент; и подвергание источника углеводородов воздействию биохимического раствора с образованием прекурсора жидкого топлива.
[0021] Выше в довольно общих чертах описаны признаки и технические преимущества изобретения, чтобы обеспечить лучшее понимание следующего далее подробного описания изобретения. Различные описанные выше характеристики, а также другие признаки, будут очевидными для специалистов в данной области техники после прочтения нижеследующего подробного описания предпочтительных вариантов осуществления и обращения к прилагаемым чертежам.
Краткое описание чертежей
[0022] Для подробного описания предпочтительных вариантов осуществления изобретения обратимся теперь к прилагаемым чертежам изобретения.
[0023] На фиг. 1 изображена общая схема технологического процесса для конверсии угля в жидкость.
[0024] На фиг. 2 изображен один вариант осуществления процесса вне пласта для конверсии угля в жидкость.
[0025] На фиг. 3 изображен один вариант осуществления процесса в пласте для конверсии угля в жидкость.
[0026] На фиг. 4 изображена типовая схема каталитического антитела.
[0027] На фиг. 5 изображена типовая схема активированного каталитического антитела.
[0028] На фиг. 6 изображена типовая схема фермента дикого типа.
[0029] На фиг. 7 изображена типовая схема активированного комплекса фермента.
[0030] На фиг. 8 изображена типовая схема направленной эволюции активированного комплекса фермента.
[0031] На фиг. 9 изображена типовая схема сайт-направленного мутагенеза активированного комплекса фермента.
[0032] На фиг. 10 изображена типовая схема аллостерического направленного мутагенеза активированного комплекса фермента.
[0033] На фиг. 11 изображена типовая схема редизайна активного центра (сайта) активированного комплекса фермента.
[0034] На фиг. 12 изображена типовая схема рационального дизайна активного центра активированного комплекса фермента.
[0035] На фиг. 13 изображена типовая схема кофактор-направленного редизайна активного центра активированного комплекса фермента.
[0036] На фиг. 14 изображена схема фотофрагментации.
[0036] На фиг. 15 изображена схема лазерной фотофрагментации.
[0038] На фиг. 16 показаны результаты рабочего цикла механического размола, выполненного на струйной мельнице JET-O-MIZER 630 для уменьшения крупности частиц, модель 0101 Fluid Energy.
[0039] На фиг. 17 показаны результаты, полученные с помощью комплектной мельницы угольно-топливной системы (УТС).
[0040] На фиг. 18А-18С показаны микрофотографии продукта в воде; 18А - при 125-кратном увеличении; 18В - при 430-кратном увеличении; 18С - при 1000-кратном увеличении.
[0041] На фиг. 19А представлены результаты предварительной обработки угля 3% Н202 (перекисью водорода) при ферментативной солюбилизации и конверсии.
[0042] На фиг. 19В представлены результаты предварительной обработки угля 3% Н202 при химической солюбилизации и конверсии.
[0043] На фиг. 19С представлены результаты предварительной обработки угля 3% Н202 в картофельно-декстрозной (PD) питательной среде, содержащей P. chrysosporium.
[0044] На фиг. 19D представлены результаты предварительной обработки угля 3% Н202 в сабуро-декстрозной (SD) питательной среде с 0,1 пептона, содержащей P. chrysosporium.
[0045] На фиг. 19Е представлены результаты предварительной обработки угля 15% Н202 при ферментативной солюбилизации и конверсии.
[0046] На фиг. 19F представлены результаты предварительной обработки угля 15% Н202 при химической солюбилизации и конверсии.
[0047] На фиг. 19G представлены результаты предварительной обработки угля 15% Н202 в картофельно-декстрозной (PD) питательной среде, содержащей Р. chrysosporium.
[0048] На фиг. 19Н представлены результаты предварительной обработки угля 15% Н202 в сабуро-декстрозной (SD) питательной среде с 0,1 пептона, содержащей P. chrysosporium.
[0049] На фиг. 19I представлены результаты предварительной обработки угля 30% Н202 при ферментативной солюбилизации и конверсии.
[0050] На фиг. 19J представлены результаты предварительной обработки угля 30% Н202 при химической солюбилизации и конверсии.
[0051] На фиг. 19K представлены результаты предварительной обработки угля 30% Н202 в картофельно-декстрозной (PD) питательной среде, содержащей P. chrysosporium.
[0052] На фиг. 19L представлены результаты предварительной обработки угля 30% Н202 в сабуро-декстрозной (SD) питательной среде с 0,1 пептона, содержащей P. chrysosporium.
[0053] На фиг. 19М представлены результаты, полученные для нагретого угля, предварительно обработанного 30% Н202, при ферментативной солюбилизации и конверсии.
[0054] На фиг. 20А представлены результаты, полученные для нагретого угля в картофельно-декстрозной (PD) питательной среде, содержащей P. chrysosporium.
[0055] На фиг. 20В представлены результаты, полученные для нагретого угля в сабуро-декстрозной (SD) питательной среде с 0,1 пептона, содержащей P. chrysosporium.
[0056] На фиг. 21А представлены результаты, полученные для угля, предварительно обработанного шахтной водой при ферментативной солюбилизации и конверсии.
[0057] На фиг. 21В представлены результаты, полученные для угля, предварительно обработанного шахтной водой при химической солюбилизации и конверсии.
[0058] На фиг. 21С представлены результаты, полученные для угля, предварительно обработанного шахтной водой, в картофельно-декстрозной питательной среде, содержащей P. chrysosporium.
[0059] На фиг. 21D представлены результаты, полученные для угля, предварительно обработанного шахтной водой, в сабуро-декстрозной (SD) питательной среде с 0,1 пептона, содержащей P. chrysosporium.
[0060] На фиг. 22А представлены результаты, полученные для угля, предварительно обработанного HN03 (pH 1) (неконцентрированной азотной кислотой), при ферментативной солюбилизации и конверсии.
[0061] На фиг. 22В представлены результаты, полученные для угля, предварительно обработанного HN03 (pH 1), в картофельно-декстрозной питательной среде, содержащей P. chrysosporium.
[0062] На фиг. 22С представлены результаты, полученные для угля, предварительно обработанного HN03 (рН 1), в сабуро-декстрозной (SD) питательной среде с 0,1 пептона, содержащей P. chrysosporium.
[0063] На фиг. 23 (известный уровень техники) представлена упрощенная схема, показывающая микробиологическое расщепление фенола.
[0064] На фиг. 24 (известный уровень техники) показаны спектры УФ-излучения для расщепления фенола.
Подробное раскрытие предпочтительных вариантов осуществления
[0065] Раскрыт процесс конверсии угля в жидкие топлива. Уголь представляет собой любой уголь, найденный или извлеченный из угольной шахты, пласта или копи. Уголь может также представлять собой антрацитовые угли или кокс битуминозного угля. В некоторых случаях уголь представляет собой лигнит, полубитуминозный уголь, другие виды угля низких сортов и/или другой источник углеводородов, такой как нефтеносные пески, без ограничений. Альтернативно, уголь представляет собой выветрелый, состаренный, выщелоченный или расщепленный уголь, без ограничений.
[0066] В некоторых случаях уголь конвертируют в жидкие топлива с помощью двухстадийного процесса. Этот процесс включает в себя катализируемые ферментами реакции. Первая стадия (стадия I) включает в себя предварительную обработку и конверсию угля в жидкие продукты с помощью ферментов. В вариантах осуществления на стадии I угольное сырье конвертируется в жидкие углеводороды. Угольное сырье представляет собой уголь, остающийся в угольных шахтах, или сырье в пласте. Альтернативно, угольное сырье представляет собой уголь, извлеченный из угольной шахты, или сырье вне пласта. В некоторых случаях источник углеводородов может представлять собой любой источник, такой как нефтеносные пески, не являющийся предпочтительным для других отраслей.
[0067] Вторая стадия (стадия II) включает в себя обогащение жидких углеводородных продуктов. Обогащение или улучшение жидкого углеводородного продукта включает в себя дополнительные катализируемые ферментами реакции. Кроме того, реакции представляют собой этапы ферментно-опосредованной обработки. Стадия II дополнительно включает в себя улучшение свойств жидкого продукта для использования в топливе. Катализируемые ферментами процессы на стадии II изменяют характеристики топлива. В иллюстративных примерах обработка на стадии II может изменять цетановое число дизельного топлива или октановое число бензина.
[0068] По сравнению с существующими методиками обработки ферментно-опосредованный двухстадийный процесс требует меньше энергии. Помимо этого, условия реакции мягче, так как в гомеостатических условиях микроорганизма-продуцента ферменты функционируют оптимальным образом. Кроме того, могут быть внедрены дополнительные ферменты или микроорганизмы, чтобы секвестировать загрязняющие вещества, регулируемые в жидких топливах. Например, сера и азот могут быть количественно уменьшены или удалены из жидких топлив до перегонки конечного продукта. Заблаговременное удаление загрязняющих окружающую среду веществ делает процесс регулируемым в соответствии с существующими и будущими нормами по выбросам в атмосферу. Помимо этого, ферментно-опосредованный двухстадийный процесс является адаптируемым к ранее недоступным типам сырья, например, столбы угля в шахте слишком опасны для извлечения путем обратной отработки.
[0069] Микроорганизмы. В раскрытом процессе ферменты, продуцируемые микроорганизмами, опосредуют конверсию. В некоторых вариантах осуществления микроорганизмы представляют собой бактерии, водоросли или грибки. В некоторых случаях микроорганизмы представляют собой гетеротрофы, которые секретируют ферменты для каталитического расщепления углеводородов. Микроорганизмы используют углеводороды в качестве источников углерода для процессов жизнедеятельности. Микроорганизмы отбирают из горючих сланцев, нефтеносных песков, битумных ям или угольных пещер, без ограничения. Например, микроорганизмы могут быть получены из найденных на ранчо Ла-Брея. Кроме того, микроорганизмы могут быть собраны из геотермальных источников, грязевых вулканов, заполненных водой впадин сольфатары, фумарол, гейзеров, грязевых котлов и т.п., без ограничения. Микроорганизмы могут также представлять собой экстремофилы, такие как, без ограничений, гиполиты, эндолиты, криптолиты, ацидофилы, алкалофилы, термофилы, литоавтотрофы, галофилы, пьезофилы. В примерах вариантов осуществления микроорганизмы представляют собой архебактерии. Альтернативно, подходящие микроорганизмы включают в себя найденные в родах Poria, Polyporus, Thiobacillus, Candida, Streptomyces, Psuedomonas, Penicillium, или Trichoderma. Как понятно специалисту в данной области техники, могут быть выявлены не названные конкретно альтернативные организмы, подходящие для применения в раскрытой системе, которые не имеют значительных отличий в структуре и функционировании. Кроме того, можно предположить, что эти микроорганизмы определяются в качестве средств изменения, улучшения или модификации настоящего описания.
[0070] В некоторых случаях микроорганизмы подвергают воздействию ранее добытого шахтным способом угля, остатков угля или остатков угля, менее подходящих для производства электроэнергии, с целью отбора ферментов. В некоторых случаях микроорганизм продуцирует ферменты естественным образом. Как понятно специалисту в данной области техники, продолжительное воздействие субстрата, такого как уголь, приведет к возросшей экспрессии и продуцированию ферментов для производства жидких углеводородов.
[0071] Ферменты. Ферменты, используемые в раскрытом процессе, получают из микроорганизмов, которые продуцируют эти ферменты с высоким выходом. В дополнительных вариантах осуществления микроорганизмы генетически изменяют для продуцирования ферментов с высоким выходом. Предпочтительно ферменты секретируются внеклеточно и/или микроорганизмы высвобождают ферменты в свою среду. Альтернативно, клетки разрушаются, и ферменты захватываются для использования при переработке угля. В вариантах осуществления ферменты отделяют от микроорганизмов до использования при переработке угля. Для уменьшения воздействия, высвобождения или загрязнения окружающей среды микроорганизмы отделяют от процессов переработки. Никакие микроорганизмы не включены непосредственно в варианты осуществления процесса производства жидкого топлива. Кроме того, устройства, используемые для выращивания этих организмов, обладают достаточными средствами для изоляции организмов-хозяев от окружающей природной среды.
[0072] Альтернативно, микроорганизмы подвергают сайт-направленному мутагенезу для активирования, сверхэкспрессирования и/или увеличения продуцирования ферментов. Сайт-направленный мутагенез представляет собой мутацию ДНК-молекулы в конкретной последовательности пар оснований нуклеиновых кислот. Сайт-направленный мутагенез может происходить в хромосомной ДНК или внехромосомной ДНК из вектора. Кроме того, сайт-направленный мутагенез может представлять собой делецию/исключение гена, праймер-опосредованный мутагенез, кассетный мутагенез, дополнительный мутагенез, мутагенез на основе ошибочного спаривания, конверсию генов, топологическое манипулирование, специфическую рекомбинацию или ПЦР-опосредованный мутагенез. Кроме того, мутагенез и сверхэкспрессирование гена могут быть индуцированы любым мутагеном. Например, могут использоваться, без ограничения, ионизирующее излучение, УФ облучение, дезаминирование, интеркаляция, алкилирование, вставка аналога, транспозонное умножение и другие методы молекулярной биологии. В некоторых случаях воздействие мутагена индуцирует захват микроорганизмом вектора, такого как плазмида. Кроме того, мутагенез может индуцировать инкорпорацию векторной ДНК в хромосомную ДНК. В контексте настоящего описания методика направленного мутагенеза может быть реализована, чтобы индуцировать дополнительное продуцирование фермента. Кроме того, мутагенез может использоваться для увеличения активности фермента.
[0073] В некоторых случаях ферменты химически модифицируют после продуцирования. Ферменты могут быть модифицированы до или после сбора из микроорганизмов. Может быть реализован любой процесс, известный специалисту в данной области техники, например, без ограничения, добавление функциональных групп, добавление других пептидов, изменение химической природы и/или структурные изменения. Например, предполагается, что в настоящем изобретении могут найти применение такие процессы, как ацилирование, гликозилирование, убиквитинирование, дезаминирование и/или расщепление, без ограничения.
[0074] Продуцированные и модифицированные ферменты используются в биохимическом растворе. Биохимический раствор содержит жидкую смесь белков, ферментов, неорганических катализаторов и органических и неорганических соединений. Биохимический раствор дополнительно содержит соли, электролиты, металлы и/или другие молекулы, которые способствуют, улучшают или изменяют действие ферментативного бульона или биохимического раствора. Биохимический раствор представляет собой смесь, состоящую по меньшей мере из одной из каждой вышеупомянутой группы, без ограничения. Биохимический бульон может быть суспендирован в любом известном растворителе; предпочтительны органические растворители. В примерах осуществления растворителем является вода.
[0075] Процесс. Как показано на фиг. 1, процесс включает в себя прохождение потока угля через последовательность отдельных этапов обработки. На СТАДИИ I процесс включает в себя по меньшей мере один этап предварительной обработки. Уголь затем подвергается солюбилизации, которая может быть включена в этапы предварительной обработки. Предварительно обработанный, солюбилизированный угольный материал конвертируют в жидкие углеводороды. Одновременно или вслед за этим материал может повергаться конверсии серы и азота. Удаление серы и азота из продукта улучшает характеристики топлива после обработки, такой как сепарация (расслоение). Различные топлива расслаиваются так, чтобы реактанты водной фазы рециркулировали и/или жидкие стоки обрабатывались для возвращения в систему. На СТАДИИ II продукты углеводородной фазы с этапа конверсии подвергаются дополнительному очищению. Очищение продуктов включает в себя очищение, обогащение и перегонку топлива для улучшения качеств продукта.
[0076] Предварительная обработка. Этап предварительной обработки включает в себя физическое и химическое расщепление угля для получения расщепленного угля. Для увеличения эффективности раскрытого процесса предпочтительно увеличить площадь поверхности материала. Площадь поверхности угля может быть увеличена путем уменьшения объема частиц, например, в процессе раздробления. Например, уголь открытой добычи, уголь, добываемый шахтным способом, угольные отвалы или остатки угля механически разламывают или дробят, получая мелкие твердые частицы. Остатки угля могут включать в себя, без ограничения, уголь, поступающий из любой отрасли, в которой он был отбракован. Твердые частицы могут включать в себя, без ограничения, каменную крошку, пыль, порошок и т.п.
[0077] В некоторых случаях, уголь обрабатывают в пласте, например, в подземном угольном пласте паром высокого давления. Пар подают к угольной шахте по подземным скважинам, каналам и/или другим линиям. Пар может быть находящимся под давлением, перегретым или представляющим собой комбинацию этих видов воздействия для повышения степени проникновения в пласт. Пар может применяться для растрескивания каменноугольного пласта под землей до предварительной обработки. Кроме того, пар высокого давления механически отделяет уголь от окружающих горных пород.
[0078] Кроме того, уголь подвергается химической обработке. Химическая обработка угля повышает его реакционную способность. Помимо этого, химическая обработка предназначена для удаления, выпаривания или исключения неугольных материалов из угольных продуктов. Кроме того, химическая обработка может увеличивать площадь поверхности угля после стимулирования образования пор, пустот, ямок и т.п. Химическая обработка может включать в себя окислительное вещество. В некоторых вариантах осуществления для окисления угля применяют мягкий ионный, кислотный, основной или свободно-радикальный растворы. В одном из вариантов осуществления раствор представляет собой мягкий кислотный раствор. В примере осуществления химическая обработка включает в себя перекись водорода. Перекись водорода находится в концентрациях между приблизительно 10% и приблизительно 50%; альтернативно, между приблизительно 20% и приблизительно 40%; и предпочтительно, составляет приблизительно 30%.
Как описано выше, растворы вводят в угольные шахты с паром или водой, поэтому водные растворы предпочтительны. В некоторых случаях может осуществляться неорганическая химическая обработка.
[0079] Солюбилизация. Кроме того, этапы предварительной обработки включают в себя солюбилизацию расщепленного угля. После механического измельчения и химического окисления вводят первый набор ферментов для разрыва поперечных связей в угле. В некоторых случаях первые ферменты могут быть извлечены из ферментов, найденных, например, в видах Peoria, Polypores, родов Poria, Polyporus, без ограничений. Первые ферменты позволяют частицам угля растворяться в жидкой среде. В вариантах осуществления жидкая среда та же, что используется для доставки ферментов. В некоторых случаях среда представляет собой описанный выше биохимический раствор. Кроме того, жидкая среда содержит водную среду. Солюбилизированные частицы угля суспендированы в жидкой среде, образуя угольную суспензию; альтернативно, угольную пульпу, угольную смесь, угольный коллоид или угольный раствор, без ограничения. Угольная суспензия улучшает доступность угольных частиц для ферментов из биохимического раствора. Суспендирование частиц в среде может улучшать реакционную кинетику на последующих ферментно-опосредованных этапах. Угольная суспензия дополнительно улучшает передачу угля между этапами обработки.
[0080] Конверсия. После солюбилизации уголь перерабатывают на этапах конверсии. В некоторых случаях солюбилизированный уголь в угольной суспензии конвертируют в меньшие или более легкие углеводороды. Более легкие углеводороды могут включать в себя любой углеводород, например, углеводороды, содержащие от приблизительно 24 атомов углерода до приблизительно 2 атомов углерода. Второй фермент или второй ферментный раствор поддерживается в биохимическом бульоне. Второй ферментный раствор может быть извлечен из ферментов, полученных с помощью микроорганизмов для видов Thiobacillus, Candida, Streptomyces, Psuedomonas, Penicillium, Trichoderma, например, без ограничения. Второй фермент может быть введен в угольную суспензию в процессе конверсии. В некоторых случаях воздействие на угольную суспензию второго фермента включает в себя конверсию угля в более низкомолекулярные углеводородные фракции. Альтернативно, второй фермент представляет собой конвертирующий фермент. Конвертирующие ферменты представляют собой ферменты, выбранные, сконструированные или модифицированные для каталитической конверсии макромолекул углеводородов, находящихся в угле, в более низкомолекулярные углеводороды. На этапе конверсии углеводороды подвергаются насыщению и конверсии серы, азота и других загрязнителей. На этапе конверсии образуется реакционная суспензия, или углеводородная суспензия с биохимическим раствором.
[0081] Реакции ферментативной конверсии успешно разделяют частицы природного, исходного или солюбилизированного, угля, на меньшие молекулы углеводородов, которые остаются в реакционной суспензии. Реакции ферментативной конверсии превращают высокомолекулярные компоненты угля в более низкомолекулярные смеси углеводородных жидкостей и углеводородных газов.
[0082] Во время конверсии из процесса удаляют некоторые отходы, загрязняющие вещества и потенциальные загрязнители окружающей среды. В некоторых случаях удаление этих продуктов опосредовано третьим ферментом, добавленным к реакционной суспензии. Третий фермент или третий ферментный раствор вступает в реакцию с продуктами каталитической конверсии, высвобождая серу из углеводородных комплексов и образуя разнообразные более простые серосодержащие соединения, которые растворимы в реакционной суспензии. Растворимые серосодержащие соединения могут отфильтровываться из реакционной суспензии и перерабатываться для других продуктов.
[0083] Помимо этого, для удаления других отходов, загрязняющих веществ и потенциальных загрязнителей окружающей среды, к реакционной суспензии может быть добавлен четвертый фермент. В некоторых случаях для специальной ликвидации, секвестрации или расщепления нежелательных соединений может применяться любой количество удаляющих отходы ферментов. В некоторых вариантах осуществления четвертый фермент или четвертый ферментный раствор вступает в реакцию с продуктами каталитической конверсии, высвобождая азот и образуя разнообразные более простые азотсодержащие соединения, которые растворимы в реакционной суспензии.
[0084] Переработанные отходы могут содержать газы, солюбилизированные в реакционной суспензии. Газы могут включать в себя азот, оксиды азота, серу, оксиды серы, окись углерода, двуокись углерода и другие газы, без ограничения. Некоторые отходы используются для дальнейших процессов, таких как производство сингаза или катализированный синтез жидких топлив. Кроме того, катализируемые ферментами реакции превращают комплексные соединения серы и азота, находящиеся в угле, в более простые формы, которые удаляют при сепарации продукта.
[0085] Как понятно специалисту в данной области техники, реакционные свойства, такие как температура, давление, рН и время пребывания выборочно контролируются и регулируются для максимального увеличения производства. В некоторых случаях реакционные свойства регулируют для получения распределения молекулярных весов углеводорода в потоке продукта. Кроме того, так как реакционная суспензия содержит биохимический раствор, изменение условий позволяет оптимизировать конверсию.
[0086] Как указано выше, биохимический раствор содержит любое число ферментов. Как понятно специалисту в данной области техники, каждый фермент имеет предпочтительные условия эффективного катализа. В связи с этим предусматривается циклическое изменение условий реакции, таких как температура и давление, для максимального увеличения эффективности любой части процесса или действия любой части ферментов. В других вариантах осуществления этап конверсии состоит из отдельных реакционных сосудов для солюбилизации, каталитического крекинга и реакций конверсии азота и серы. Такая схема расположения позволяет применять различные условия работы в каждом сосуде, такие как температура и степени рециркуляции реактора, для оптимизации катализируемых ферментами реакций.
[0087] Разделение продуктов. После конверсии углеводородную смесь направляют в отстойные чаны. В вариантах осуществления отстойный чан может представлять собой любой сосуд, выполненный с возможностью отделения углеводородной жидкости от водоугольной суспензии. В некоторых случаях отстойный чан может включать в себя динамический осадитель, в который постоянный поток реакционной суспензии вводят в малом объеме или при низкой скорости для разделения водной и углеводородной фаз. Альтернативно, отстойный чан включает в себя статический осадитель, угольная суспензия жидкой фазы осаждается из более легких углеводородов под действием силы тяжести. В некоторых вариантах осуществления оставшиеся серные и азотные соединения распределяются в водную фазу. Водородную фазу отделяют вытягиванием более легко углеводородного слоя из более плотного водного слоя. Альтернативно, водная фаза по трубе отводится со дна чана.
[0088] Обогащение продуктов. Углеводородный слой, который уже содержит бензин, керосин, дизельное топливо и горючие масла, направляют на стадию II, где он дополнительно обогащается путем конверсии низкокачественных фракций, нафты, дизельного топлива, топливных масел, парафинов и т.п. в высококачественные фракции, такие как бензин или керосин. В вариантах осуществления обогащение продукта может включать в себя ферментативную конверсию, молекулярную фотофрагментацию, конверсию и молекулярную фотофрагментационную конверсию с помощью ферментов. В некоторых случаях обогащение продукта включает в себя пятый фермент или пятый ферментный раствор, вводимый в углеводородные продукты с этапа отделения. После обогащения углеводородная смесь разделяется на конечные продукты путем традиционной перегонки.
[0089] Переработка вне пласта. На фиг. 2 изображен вариант осуществления для непрерывной переработки вне пласта угольного сырья, или ЕХ-система 10. В ЕХ-системе 10 процессы предварительной обработки, конверсии и переработки продуктов являются сообщающимися по текучей среде. В ЕХ-системе 10 уголь сначала размалывают до мелких частиц механическими средствами 12. Как указано выше, механические средства 12 создают поток 14 продукта, состоящего из частиц. Поток продукта, состоящего из частиц, вводят в систему 16 химической обработки, содержащую, например, слабокислотный раствор. В некоторых случаях механические средства 12 и система 16 химической обработки могут содержать единственный сосуд или единственную установку по переработке. Уголь и кислотный раствор образуют угольную суспензию, в которой уголь подвергается предварительному окислению. Степень предварительному окисления определяется временем пребывания суспензии в системе 16 химической обработки. Кроме того, в комбинированных вариантах осуществления окисление угля в угольной суспензии может регулироваться, по меньшей мере частично, по степени перемешивания, обеспечиваемого смесителями 18.
[0090] Поток 20 суспензионного продукта затем перекачивают из сырьевого резервуара в реакционную ступень 22. Реакционная ступень 22 предусматривает реакцию солюбилизации. В некоторых случаях поток 24 первого фермента с ферментами, выбранными для солюбилизации угля, вводят в поток 20 суспензионного продукта. Альтернативно, поток 24 первого фермента вводят непосредственно в реакционную ступень 22. Без привязки к какой-либо конкретной теории, может оказаться целесообразным ввести поток 24 первого фермента в поток 20 суспензионного продукта до ввода в реакционную ступень 22.
[0091] Реакционная ступень 22 предусматривает ферментно-опосредованную каталитическую реакцию конверсии. Поток 26 второго фермента вводят в реакционную ступень 22. Ферменты вступают в реакцию каталитически, осуществляют конверсию макромолекул углеводородов и создают поток 30 продукта. Кроме того, в реакционную ступень 22 добавляют поток 27 третьего фермента для конверсии серных соединений и поток 28 четвертого фермента для конверсии азотных соединений. Поток 27 третьего фермента и поток 28 четвертого фермента выполняют конверсию соответствующих загрязняющих веществ, находящихся в угольной суспензии 20, в более простые водорасторимые формы. Стоки 23 реакционной ступени непрерывно разделяются между рециркуляционным потоком 25, который закачивается обратно в реакционную ступень 22, и потоком 30 продукта.
[0092] В других вариантах осуществления реакционная ступень 22 состоит из отдельных реакционных сосудов для солюбилизации, каталитической конверсии и реакций конверсии азота и серы. Такая многореакторная схема расположения позволяет применять различные условия работы в каждом сосуде, такие как температура и степени рециркуляции реактора, для оптимизации различных наборов реакций.
[0093] Поток 30 продукта перекачивается в сепарационную ступень 32. Сепарационная ступень 32 может содержать газовый выход 33 для отведения газов и летучих соединений во время сепарации. В некоторых случаях через газовый выход 33 выпускаются некоторые газы, которые были растворены в потоке 30 продукта. Сепарационная ступень 32 предусматривает этап, на котором водная фаза 36 осаждается под углеводородной фазой 34. Сепарационная ступень 32 включает в себя осадитель или осадочную камеру. Альтернативно, сепарационная ступень представляет собой фильтр или другой аппарат для разделения жидкой и углеводородной фаз из потока 30 продукта. Сепарационная ступень 32 содержит сепаратор нефти непрерывного действия. Водная фаза 36 отводится из сепарационной ступени 32 и направляется с помощью рециркуляционного потока 39 к реакционной ступени 22. Рециркуляционный поток предусматривает наличие системы очистки сточных вод. Система очистки сточных вод представляет собой любую систему, выполненную для обработки кислой воды с возможностью удаления кубового остатка, а также побочных продуктов в виде азота и серы. Очищенная вода затем рециркулирует обратно в реакционную секцию (секцию реактора).
[0094] В некоторых случаях углеводородная фаза 34 может отводиться с верха осадителя в качестве углеводородного потока 38 для обогащения и/или перегонки с целью получения транспортного топлива. Углеводородный поток 38 перекачивают в ступень обогащения продукта.
[0095] Переработка в пласте. Другой вариант осуществления включает в себя непрерывную переработку угля в пласте, или IN-систему 100, которая показана на фиг. 3. В этом варианте осуществления IN-система 100 содержит отработанное, разрушенное, недоступное или по иной причине трудное для разработки месторождение угля, или подземный угольный пласт 101. В вариантах осуществления по меньшей мере одну скважину 102 бурят в угольном пласте 101. Скважины 102 обычно выполняют с возможностью транспортировки жидкостей и суспензий между подземным угольным пластом 101 и перерабатывающим центром 120. Кроме того, скважины 102 могут быть выполнены с возможностью непрерывного циркулирования технологических текучих сред в подземный угольный пласт 101 и из него. Можно предположить, что множество скважин 102 улучшают выход продукции, время переработки и общие экономические показатели IN-системы 100, без ограничения.
[0096] Процесс в IN-системе 100 начинается с закачки пара в обсадные трубы скважины 102 с целью вызвать разрыв подземного угольного пласта 101. Этот этап 105 разрыва выполнен с возможностью разделения угольного пласта на частицы угля, угольный щебень и т.п.В некоторых случаях пар высокого давления используют в соответствии с традиционными методами, применяемыми в отрасли подземной добычи угля.
[0097] После завершения этапа 105 разрыва пар высокого давления отводят. Этап 106 окисления включает в себя нагнетание кислотного раствора для предварительного окисления раздробленного угля. В вариантах осуществления кислотный раствор непрерывно рециркулирует с образованием циркулирующего технологического потока 150 так, чтобы кислоты закачивалась в скважину 102А с одной стороны пласта и выкачивалась из скважины 102В с другой стороны пласта. Для завершения цикла кислотный раствор транспортируется обратно и закачивается в первую скважину 102А. Циркулирующий технологический поток 150 может повторяться до тех пор, пока не будет достигнут требуемый уровень предварительного окисления.
[0098] Как раскрыто выше, этап 107 солюбилизации может включать в себя введение раствора первого фермента в подземный угольный пласт 101. Раствор первого фермента вводится в циркулирующий технологический поток 150 для солюбилизации подвергаемого воздействию угля в циркулирующем технологическом растворе.
[0100] После того, как будет достигнут достаточный уровень растворимого угля, последовательно или одновременно добавляются дополнительные ферменты для создания угольной суспензии в циркулирующем технологическом потоке 150 В определенных случаях в циркулирующий технологический поток 150 добавляют растворы второго фермента 106, третьего фермента 107 и четвертого фермента 108. Как описано выше в настоящем документе, поток 106 второго фермента выбирают для каталитического крекинга углеводородов. Растворы третьего фермента 107 и четвертого фермента 108 выбирают для удаления серо- и азотсодержащих соединений и/или отходов из циркулирующего технологического потока 150. В вариантах осуществления в циркулирующий технологический поток 150 могут вводиться дополнительные потоки ферментов.
[0101] Часть циркулирующего технологического потока 150 затем отделяется, принимается в качестве потока 160 исходного продукта и направляется в ступень 120 переработки. Ступень 120 переработки аналогична используемой в вариантах осуществления процесса вне пласта, рассмотренных выше. Сепарационная емкость 162 предусматривает этап, на котором водная фаза 163 осаждается под углеводородной фазой 164. Сепарационная емкость 162 включает в себя осадитель или осадочную камеру. Водная фаза 163 отводится из сепарационной емкости 162 и направляется с помощью рециркуляционного потока 170 в циркулирующий технологический поток 150. Рециркуляционный поток 170 предусматривает наличие системы очистки сточных вод. Система очистки сточных вод представляет собой любую систему, выполненную для обработки кислой воды с возможностью удаления кубового остатка, а также побочных продуктов в виде азота и серы. В некоторых случаях углеводородная фаза 164 может отводиться с верха осадителя в качестве углеводородного потока 168 для обогащения и/или перегонки с целью получения транспортного топлива. Углеводородный поток 38 перекачивают в ступень обогащения продукта.
[0102] Мутагенез. Способы, используемые при получении подходящих ферментов для реализации на стадии II с целью обогащения топлива включает в себя применение каталитических антител. Как показано на фиг. 4, биологические ферменты идентифицируют для требуемых каталитических процессов. В определенных случаях биологические ферменты извлекают из микроорганизмов, описанных выше в настоящем документе. В дополнительных вариантах осуществления ферменты представляют собой ферменты только естественного происхождения (ТЕП). Ферменты ТЕП являются фенотипическими экспрессиями немодифицированных генетических последовательностей в микроорганизмах. Альтернативно, ферменты ТЕП являются ферментами дикого типа. В дополнительных случаях, показанных на фиг. 5, ферменты ТЕП выбирают из тех, которые содержат активированный фермент. В определенных случаях проводится скрининг активированных ферментов посредством анализа антител. Альтернативно, любой подходящий способ скрининга может включать в себя любой подходящий протокол для идентификации ферментов ТЕП дикого типа, как дополнительно показано на фиг. 6 и 7.
[0103] Выбранные ферменты ТЕП образуются путем направленной эволюции, как показано на фиг. 8. Выбранные ферменты ТЕП подвергают сайт-направленному и случайному мутагенезу, охватывая весь фермент, а не ограничиваясь только активным центром. В некоторых случаях ферменты являются объектом мутагенеза в аллостерических центрах и на участках, удаленных от активных и/или аллостерических центров. Мутагенез на нескольких участках включает в себя средства, как способствующие, так и ограничивающие получение потенциальных продуктов, как показано на фиг. 9 и 10. В определенных случаях мутагенез включает в себя химический редизайн активного центра, как показано на фиг. 11. Предпочтительно, результаты включают в себя рациональный дизайн фермента или ферментной структуры.
[0104] Структура синтезируется, проектируется с помощью вычислительных средств с мотивами, связанными с каркасами ферментов. Ферменты представляют собой довольно большие молекулы, имеющие сотни аминокислот, с молекулярными массами, достигающими десятков килодальтонов (кДа), и размерами, составляющими тысячи кубических ангстремов, при этом они могут считаться пространственно малоэффективными. В определенном случае большие молекулы ферментов содержат небольшие активные центры. Ферментные реакционноспособные центры сравнительно невелики, при этом другие свернутые аминокислоты служат в качестве поддерживающих каркасов для создания объема реакционноспособного центра. Эти «другие аминокислоты» могут быть, вообще говоря, довольно далеко от активного центра фермента, как показано на фиг. 12. Помимо этого, ферменты могут включать в себя редизайн центра прикрепления кофактора, показанный на фиг. 13. Чтобы индуцировать редизайн центра прикрепления кофактора, реализацию сайт-направленного мутагенеза повторяют, как описано выше, например, в параграфе 21.
[0105] Как показывает график на фиг. 14, фемтосекундный лазерный импульс определенной формы в ИК-диапазоне воздействует на ферментный комплекс, индуцируя фрагментацию реактанта. Кроме того, можно предположить, что любое конкретное воздействующее излучение, известное специалисту в данной области техники, может быть способно к такой же фрагментации реактанта, без ограничения. Лазерный импульс для направленной фрагментации реактантов/конверсии в продукты может способствовать образованию реакционных продуктов. Как понятно специалисту в данной области техники, может быть образовано несколько реакционных продуктов фрагментации. В определенных случаях несколько продуктов фрагментации могут быть предпочтительными для образования целого ряда реакционных фрагментов. Альтернативно, фемтосекундные лазерные импульсы определенной формы в ИК-диапазоне вместе с вышеупомянутыми методами использования ферментов применяются, чтобы способствовать селективной фрагментации реактантов в ферментных активных центрах, аллостерических центрах и на участках, удаленных от связывающих и/или аллостерических центров, как показано на фиг. 15. Как понятно специалисту в данной области техники, связывание водородного реактанта на молекулярном уровне с реакционноспособным центром фермента может включать в себя ковалентную, нековалентную, водородную, ионную, ван-дер-ваальсову связь, взаимодействие, соединение или ассоциацию, без ограничения. Кроме того, реакционноспособный центр фермента выполнен с возможностью ограничения молекулы реактанта и диапазона ее перемещения. Помимо этого, реакционноспособный центр ограничивает внутренние степени свободы, чтобы удобно было нацеливать фемтосекундные лазерные импульсы на заранее выбранную внутреннюю связь. В определенных случаях реакционноспособный центр фермента уменьшает внутренние степени свободы так, что предотвращается перегруппировка под действием внутренних вибраций, и энергия лазера фокусируется на заранее выбранной внутренней связи.
[0106] Конверсия угля в жидкие углеводороды. В варианте осуществления процесс конверсии угля в жидкие углеводороды включает в себя механическую предварительную обработку и/или химическую предварительную обработку, солюбилизацию и конверсию (из угля в жидкие углеводороды). Механическая предварительная обработка включает в себя размол на молотковой мельнице или размол на струйной вихревой мельнице. В некоторых случаях струйная вихревая мельница способна размалывать уголь с получением мелких частиц размером 5 мкм или меньше. Например, может применяться струйная мельница JET-O-MIZER 630 для уменьшения крупности частиц, модель 0101.
[0107] В одном из вариантов осуществления солюбилизацию и конверсию выполняют для различных видов предварительной обработки угля. В некоторых случаях уголь предварительно обрабатывается посредством ферментативного процесса, например, с использованием внеклеточных лакказы и марганецпероксидазы (MnP). В некоторых случаях уголь предварительно обрабатывается посредством химического процесса, например, с использованием тартрата аммония и марганецпероксидазы. В некоторых случаях уголь предварительно обрабатывается посредством ферментативного процесса, например, с использованием живых организмов Phanerochaete chrysosporium.
Пример
[0108] Общие сведения. Разложение угля осуществляется с помощью трех различных подходов: (1) ферментативный процесс - использование внеклеточных лакказы и марганецпероксидазы (MnP); (2) химический процесс - использование тартрата аммония и марганецпероксидазы; и (3) ферментативный процесс - использование живых организмов Phanerochaete chrysosporium. Для определения степени эффективности каждого из этих способов при разложении битуминозного угля применялся спектральный анализ. После анализа результатов и других факторов, таких как затраты и воздействия на окружающую среду, было решено, что ферментативные подходы, в противоположность химическим подходам с использованием хелаторов, были более эффективными при разложении угля. Представлены и сопоставлены результаты экспериментов с использованием лакказы/MnP и результаты экспериментов с использованием Phanerochaete chrysosporium.
[0109] Спектры обоих ферментативных способов показывают пики поглощения в диапазоне от 240 до 300 нм. Эти пики соответствуют ароматическим промежуточным соединениям, образующимся при разрушении структуры угля. Пики затем демонстрируют уменьшение поглощения с течением времени в соответствии с расходованием ароматических промежуточных соединений в то время, как они подвергаются разрыву кольца. Как показывают результаты, этот процесс происходит в течение 1 часа при использовании внеклеточных ферментов, но занимает несколько дней при использовании живых организмов. В дополнение к этому, живые организмы требуют особых условий культивирования, регулирования загрязнителей и фунгицидов для эффективного продуцирования внеклеточных ферментов, которые расщепляют уголь. Таким образом, при сравнении двух ферментативных способов результаты показывают, что процесс использования внеклеточных ферментов, расщепляющих лигнин, таких как лакказа и марганецпероксидаза, представляется более эффективным способом разложения битуминозного угля.
[0110] Механическая предварительная обработка. Процесс механической предварительной обработки включает в себя размол частиц угля до меньшего размера перед химической предварительной обработкой и проведением экспериментов. Этот процесс обеспечивает увеличение площади поверхности для химической предварительной обработки угля, а также большую площадь поверхности для последующей ферментативной конверсии угля в жидкие углеводороды.
[0111] Использовался битуминозный уголь из угольного пласта Нижний Киттанинг, большой удельный объем - №5, от компании Rosebud Mining Company, г. Киттанинг, штат Пенсильвания.
[0112] В первом квартиле (Q1) использовались три различные степени помола угля: частицы размеров 1 мм, 400 мкм и 40 мкм. Все три степени помола угля были получены посредством размола на молотковой мельнице. Частицы размером 1 мм были получены от компании Rosebud Coal, г. Киттанинг, штат Пенсильвания. Частицы размером 400 мкм и 40 мкм поступили от Pulva Corporation, г. Валенсия, штат Пенсильвания (хотя исходным материалом для помолов микронного размера служит также 1 мм уголь от Rosebud). Во втором квартиле (Q2) процесса механической предварительной обработки размол на молотковой мельнице был заменен размолом на струйной мельнице. Он был выполнен компанией Fluid Energy, Inc., г. Телфорд, штат Пенсильвания. В качестве применявшегося оборудования служила система уменьшения крупности частиц JET-O-MIZER. Фактический размол производился в герметических условиях, исключающих поступление кислорода или воздуха. Это было сделано по соображениям безопасности, чтобы обеспечить защиту от самовоспламенения или взрыва. Дальнейшие работы по механическому размолу выполнялись в третьем квартиле (Q3) с использованием струйной размольной мельницы (например, мельницы JET-O-MIZER 630 для уменьшения крупности частиц, модель 0101 компании Fluid Energy). На вход мельницы JET-O-MIZER 630 для уменьшения крупности частиц, модель 0101 Fluid Energy, поступают частицы угля размером 3 мм. Частицы этого размера легко доступны у производителей угля. При удельном потреблении энергии, составлявшем 1000 кВт*ч/т, и использовании пара в качестве движущегося газа, были получены средние размеры частиц меньше 5 микрон.
[0113] Результаты и обсуждение. На фиг. 16 показаны результаты рабочего цикла механического размола, выполненного на мельнице JET-O-MIZER 630 для уменьшения крупности частиц, модель 0101 Fluid Energy. Как видно из этого чертежа, 25% частиц меньше 1,7 микрон, и 50% меньше 4 микрон. Средний диаметр Саутера D (3,2) составляет только 2,128 микрон, удельная площадь поверхности превышает 28000 см2 на см3. Эти маленькие размеры частиц приводят к увеличению площади поверхности, а значит, и к росту числа функциональных групп угля, которые подвергаются воздействию ферментов во время процесса солюбилизации и конверсии углеводородов (см. таблицу 1 ниже).
[0114] Лабораторная мельница JET-O-MIZER CFS, модель 0101, название которой сокращается до «мельница УТС», была оснащена паровым интерфейсом для измельчителя. Размеры мельницы УТС составляют приблизительно 7×6×3 фута. Позади панели управления справа находятся 2 нагревателя для пара. Уголь из угольного бункера подается в секцию размола (снабженный кожухом куб слева от бункера). Размолотый угольный продукт подается в контейнер позади снабженного кожухом измельчителя.

[0115] На фиг. 17 показаны окончательные результаты, полученные с помощью комплектной мельницы УТС.Статические данные по угольному продукту взяты для жидкого продукта. Эти результаты получены с помощью анализатора стандартного диапазона размеров частиц MICROTRAC. Как видно из фиг. 17, размол на мельнице УТС выполняется при скорости подачи угля 27 фунтов в час. Движущийся пар имеет температуру 450° и давление 110 фунт/кв. дюйм изб. Диапазон размеров частиц составляет приблизительно от 0,5 микрон до 25 микрон. Среднее значение равно 5,769 микрон.
[0116] В дополнение к статистическим результатам, уголь из мельницы УТС исследовали под микроскопом. Из следующих микрофотографий очевидны несколько характеристик угольного помола и частиц.
[0117] На фиг. 18А показана микрофотография продукта в воде. Используется 125-кратное увеличение. Предметное стекло микроскопа с нанесенной сеткой разделено на десятые доли (0,1 мм) миллиметра, как показано делениями 0-0,5. Деления величиной 0,1 мм дополнительно снова подразделяются на десятые доли (0,01 мм) в пределах малого деления от 0,0 до 0,1 мм. Деления величиной 0,01 мм выглядят как «гитарные струны». Большая частица в середине «гитарных струн» составляет приблизительно 30 микрон в диаметре. Это самая большая частица в поле зрения. Некоторые частицы гораздо меньше, как можно видеть на следующих 2 микрофотографиях.
[0118] На фиг. 18В показано 430-кратное увеличение. Гитарные струны представляют собой деления 10-5 мкм. Как можно видеть между струнами и вокруг центрального поля, имеются частицы, составляющие 0,1 «струнных» делений или около 1 микрон. Фиг. 18С представляет собой микрофотографию того же центрального поля, что на фиг. 18А-18В. Используется 1000-кратное увеличение. При этом увеличении обратите внимание на частицу, обведенную оранжевым кружком. Она составляет около 10 микрон в диаметре. Естественно, вокруг частиц такого размера наблюдается дифракция видимого света. Однако обратите внимание на то, что в середине частицы, по-видимому, имеет место некоторая прозрачность. Это явление также наблюдается во всех других частицах с этой стороны, а также на других, не показанных микрофотографиях.
[0119] В этом примере применялись несколько различных подходов к механической предварительной обработке. В конечном счете, было решено использовать размол на струйной мельнице (в противоположность размолу на молотковой мельнице), который позволяет размалывать частицы угля до размера 5 мкм или меньше. Как видно по результатам, мельница JET-O-MIZER 630 для уменьшения крупности частиц, модель 0101 Fluid Energy, может функционировать в соответствии с необходимыми техническими характеристиками и размалывать частицы угля до размеров 5 мкм или меньше. Процесс размалывания угля чрезвычайно важен, поскольку при размерах частиц 5 мкм или меньше резко возросшая площадь поверхности обеспечивает дополнительное внешнее воздействие на функциональные группы, которые затем которые подвергаются воздействию ферментов. Это практически значимо, поскольку возросшие скорости реакций и объемы продукта сильно зависят от доступа (или внешнего воздействия) к этим функциональным группам.
[0120] Размеры частиц и дисперсия частиц угля близки к определению «растворимости». Частицы имеют порядка 800-1200 бензольных колец. Это вполне удобный размер для «подачи» к ряду ферментов с целью получения жидких топлив.
[0121] Солюбилизация и конверсия. Использовался битуминозный уголь (угольный пласт Нижний Киттанинг, большой удельный объем - №5, от компании Rosebud Mining Company, г. Киттанинг, штат Пенсильвания). Для размалывания угля перед проведением экспериментов применялся механический измельчитель. Как упоминалось в разделе, посвященном механической предварительной обработке, использовалось несколько различных размеров частиц, но большинство экспериментов проводились с использованием частиц угля размером около 5 мкм. Анализировались результаты экспериментов с использованием частиц угля размером 5 мкм.
[0122] Химическая предварительная обработка применяется для «выветривания» или окисления угля, что, в свою очередь, способствует растворимости угля в процессе ферментативной конверсии. В экспериментах применялись несколько различных способов предварительной обработки, включая: перекись водорода, Н202 (3% рН 5, 15% рН 4,5 и 30% рН 4), компания PBS, шахтная H2O (округ Сомерсет, РА рН 2.2), азотная кислота, HN03 (рН 1, рН 2, рН 3, рН 4 и 15М), дистиллированная H2O и предварительно нагретый уголь, в котором частицы угля 5 мкм предварительно нагревались при температуре 120°С в течение приблизительно 36 часов. Все предварительно нагретые образцы высушивались, прежде чем уголь использовался для экспериментов.
[0123] В дополнение к экспериментам с различными типами предварительно обработанного угля проводились также эксперименты с необработанным углем. Результаты экспериментов по предварительной обработке угля анализировались для определения наиболее эффективных способов предварительной обработки. Исходя из этих результатов было определено, что наиболее эффективными способами для предварительной обработки являются применение перекиси водорода (3%>, 15%> и 30%), нагретого угля, шахтной воды и азотной кислоты. Ниже рассматриваются результаты экспериментов с использованием этих специальных предварительно обработанных проб угля.
[0124] Ферментативный подход: лакказа и марганецпероксидаза
[0125] Ферментативные эксперименты в этом примере проводились с использованием лакказы из Trametes versicolor и марганецпероксидазы (MnP) из Phanerochaete chrysosporium, обе из которых были приобретены у компании Sigma-Aldrich. Лакказа и MnP внеклеточных ферментов продуцируются возбуждающими белую гниль грибками. Они рассматриваются в качестве двух из основных групп лигнолитических ферментов и способны с эффективному расщеплению лигнина. Лакказу использовали для первого этапа процесса, ферментативной солюбилизации, а MnP - на втором этапе процесса, конверсии углеводородов. Детальная методика проведения эксперимента при этом подходе показана ниже.
[0126] Методика использования лакказы и MnP
[0127] Этап 1: лакказа
Растворы:
 лакказный буфер - 100 мМ цитрат-100 мМ натрий-фосфатный буфер, рН 4,5;
лакказный буфер - 100 мМ цитрат-100 мМ натрий-фосфатный буфер, рН 4,5;
 лакказный раствор - лакказа (Т. versicolor) была растворена в лакказном буфере.
лакказный раствор - лакказа (Т. versicolor) была растворена в лакказном буфере.
Методика
1) 0,1 г сухого, предварительно обработанного угля объединяли с 3 мл лакказного буфера в пробирке.
2) 2 мл лакказного раствора добавляли к каждой пробирке, содержавшей уголь и лакказный буфер.
3) Каждую пробирку встряхивали с помощью орбитального встряхивателя шейкерной лабораторной линии на протяжении ночи.
4) Продукты, полученные в результате экспериментов, измеряли с помощью спектрофотометра Genesys 10 UV-VIS (диапазон 190 нм-1100 нм), приобретенного у компании Fisher Scientific. Концентрации (число капель), измеренные в спектрофотометре, регулировали так, чтобы значения интенсивности поглощения были относительно одинаковыми.
[0128] Этап 2: марганецпероксидаза (MnP)
Растворы:
 буфер MnP - 160 мМ раствора малоновой кислоты, рН 4,5;
буфер MnP - 160 мМ раствора малоновой кислоты, рН 4,5;
 раствор MnP - раствор окислителя MnP перемешивали в буфере MnP для образования малонового комплекса марганца (комплекс описан в методике количественного анализа). Методика
раствор MnP - раствор окислителя MnP перемешивали в буфере MnP для образования малонового комплекса марганца (комплекс описан в методике количественного анализа). Методика
1) 2,5 мл раствора MnP добавляли в кювету спектрофотометра.
2) Несколько капель каждого продукта из экспериментов с лакказой добавляли в кювету для проведения конверсии углеводородов. Концентрации (число капель) регулировали так, чтобы значения интенсивности поглощения были относительно одинаковыми.
3) Продукты, полученные в результате экспериментов, измеряли немедленно, а затем каждые 15 минут (до 1 часа) с помощью спектрофотометра Genesys 10 UV-VIS (диапазон 190 нм-1100 нм), приобретенного у компании Fisher Scientific.
[0129] Химический подход: хелаторы
[0130] В этом примере применялся также химический подход с использованием хелаторов. Действие хелаторов позволяет удалять комплексные ионы из угольной структуры для стабилизации угля. Применялись три различных хелатора, однако тартрат аммония представляется наиболее эффективным. Для экспериментов тартрат аммония применялся на этапе солюбилизации, а MnP применялась затем на этапе конверсии углеводородов. Более детальная методика при этом подходе показана ниже.
[0131] Методика применения хелатора
[0132] Этап 1: тартрат аммония
Раствор
 Раствор хелатора - 1,00 г тартрата аммония смешивали с 250 мл Н20.
Раствор хелатора - 1,00 г тартрата аммония смешивали с 250 мл Н20.
Методика
1) Уголь - 0,10 г каждой пробы предварительно обработанного сухого угля использовали для каждого эксперимента.
2) 0,1 г угля объединяли с 10 мл раствора хелатора в каждой пробирке.
3) Каждую пробирку встряхивали с помощью орбитального встряхивателя шейкерной лабораторной линии на протяжении ночи.
4) Продукты, полученные в результате экспериментов, измеряли с помощью спектрофотометра Genesys 10 UV-VIS (диапазон 190 нм-1100 нм), приобретенного у компании Fisher Scientific. Концентрации (число капель) продукта, измеренные в спектрофотометре, регулировали так, чтобы значения интенсивности поглощения были относительно одинаковыми.
[0133] Этап 2: марганецпероксидаза.
Растворы:
 буфер MnP - 160 мМ раствора малоновой кислоты, рН 4,5;
буфер MnP - 160 мМ раствора малоновой кислоты, рН 4,5;
 раствор MnP - раствор окислителя MnP перемешивали в буфере MnP для образования малонового комплекса марганца (комплекс описан в методике количественного анализа).
раствор MnP - раствор окислителя MnP перемешивали в буфере MnP для образования малонового комплекса марганца (комплекс описан в методике количественного анализа).
Методика
1) 2,5 мл раствора MnP добавляли в кювету спектрофотометра.
2) Несколько капель каждого продукта из экспериментов с тартратом (продукт с этапа 1) добавляли в кювету для проведения конверсии углеводородов. Концентрации (число капель) регулировали так, чтобы значения интенсивности поглощения были относительно одинаковыми.
3) Продукты, полученные в результате экспериментов, измеряли немедленно, а затем каждые 15 минут (до 1 часа) с помощью спектрофотометра Genesys 10 UV-VIS (диапазон 190 нм-1100 нм), приобретенного у компании Fisher Scientific.
[0134] Ферментативный подход: Phanerochaete Chrysosporium
[0135] В дополнение к использованию внеклеточных ферментов, эксперименты проводили с использованием живых организмов, позволяющих, как известно, продуцировать ферменты, расщепляющие лигнин. Эти эксперименты были направлены на обеспечение среды для живого организма, экскретирующего такие внеклеточные ферменты для расщепления предварительно нагретого угля. Применявшийся организм, Phanerochaete chrysosporium (P. chrysosporium), представляет собой возбуждающие белую гниль грибки, которые экскретируют внеклеточные ферменты для расщепления лигнина. Этот организм был приобретен в Американской коллекции клеточных культур (АТСС) (АТСС #24725). Для выращивания использовали две различные питательные среды: картофельную декстрозу (PD) и сабуро с декстрозой (SD). Более детальная методика эксперимента при этом подходе показана ниже.
[0136] Методика применения P. Chrysosporium
1) 0,2 г сухого, предварительного нагретого угля взвешивали и помещали в колбу Эрленмейера объемом 50 мл.
2) 30 мл бульона из питательных сред (с внесенным P. chrysosporium) добавляли к углю в колбах.
3) Каждую пробирку встряхивали с помощью орбитального встряхивателя шейкерной лабораторной линии непрерывно в течение 14 дней.
4) Пробы брали из каждой колбы спустя первые 2 часа в качестве начального отсчета, а также один раз в сутки в дни 1-7, день 10 и день 14. Эти образцы измеряли с помощью спектрофотометра Genesys 10 UV-VIS (диапазон 190 нм-1100 нм), приобретенного у компании Fisher Scientific.
[0137] Результаты. Как указано выше, при проведении экспериментов по солюбилизации и конверсии были приняты три различных подхода: (1) лакказа и MnP, (2) тартрат аммония и MnP и (3) живой организм P. Chrysosporium с использованием двух различных питательных сред. Первые два подхода включали в себя этап солюбилизации с использованием как ферментов, так и хелаторов, для начального разложения структуры угля; разложившийся уголь поступал на этап конверсии углеводородов с использованием дополнительных ферментов для дальнейшего крекинга молекул углеводородов с образованием меньших молекул углеводородов. В подходе на основе живого организма P. Chrysosporium использовался для экскретирования некоторого количества внеклеточных ферментов как для разложения, так и для дальнейшего крекинга угольной структуры.
[0138] После проведения экспериментов с ферментами и хелаторами во втором и третьем квартилях, было определено что ферментативный подход является более эффективным при расщеплении битуминозного угля, чем химический (хелаторный) подход. Кроме того, хелаторы дороги и могут оказывать вредные воздействия на окружающую среду. Исходя из этих экспериментальных результатов и экологических соображений было решено, что хелаторный подход не является оптимальным.
[0139] Эксперименты с живым P. Chrysosporium проводили с использованием различных типов питательных сред. Результаты этих экспериментов показали, что оптимальные условия роста создавали питательная среда PD и питательная среда SD, обе с наименьшим количеством добавляемого пептона.
[0140] Успешные результаты расщепления угля были получены как при ферментативном подходе (лакказа и MnP), так и при подходе с использованием живого организма (P. Chrysosporium). Поэтому представлены и проанализированы только результаты спектральных измерений при этих подходах. На фиг. 19А-22С показаны результаты этих экспериментов.
[0141] Каждая кривая показывает длину волны (нм) в сопоставлении с относительным поглощением (А), где относительное поглощение (А) связано с пропусканием: А=Iog10 (1/Т). Пояснительные надписи на графиках следует читать слева направо, в соответствии с порядком, в котором производились измерения проб.
[0142] Результаты разбиты на группы в соответствии с типом применявшейся предварительной обработки. Представлены только результаты спектральных измерений по наиболее эффективным способам предварительной обработки. Этими способами являются предварительная обработка с помощью перекиси водорода (3%, 15% и 30%), нагретого угля, шахтной воды и азотной кислоты. После сравнения этих результатов будет определен лучший общий подход к расщеплению битуминозного угля.
[0143] Уголь, предварительно обработанный 3% H2O2
[0144] На фиг. 19А представлены результаты экспериментов по предварительной обработке угля с помощью 3% перекиси водорода (Н202) с использованием растворов лакказы и MnP. Спектр для предварительно обработанного угля в лакказном буфере имеет пик приблизительно при 215 нм и поглощение, составляющее приблизительно 1,0 А (красная кривая). Этот спектр может сравниваться со спектром предварительно обработанного угля в лакказном растворе, который имеет пик приблизительно при 215 нм и поглощение, составляющее приблизительно 2,0 А (синяя кривая).
[0145] Эта два спектра показывают, что предварительная обработка угля с помощью 3% Н202 оказывает некоторое воздействие на солюбилизацию угля, но лакказа дополнительно окисляет и солюбилизирует его. Спектры на фиг. 19А также иллюстрируют сдвиг пиков с 215 нм до 244 нм и уменьшение поглощения с 2,0 А до 1,74 А, что происходит при добавлении лакказного продукта к раствору MnP (зеленая кривая - 0 мин). Поглощение (зеленая кривая - 0 мин) продолжает уменьшаться с течением времени до приблизительно 1,45 А (розовая кривая - 15 мин, бирюзовая кривая - 30 мин, желтая кривая - 45 мин, серая кривая - 1 час).
[0146] На фиг. 19В показаны результаты экспериментов по предварительной обработке угля с помощью 3% перекиси водорода (Н202). Спектр для необработанного угля в тартратном растворе не демонстрирует каких-либо резко выраженных пиков поглощения в спектрах (красная кривая). Однако предварительно обработанный уголь в тартратном буфере имеет пик приблизительно при 225 нм и поглощение, составляющее приблизительно 0.634А (синяя кривая). Это говорит о том, что предварительная обработка оказывает очень существенное воздействие на химическую солюбилизацию угля при использовании тартратного раствора. Спектры на фиг. 19В также иллюстрируют сдвиг пиков с 225 нм до приблизительно 243 нм, что происходит при добавлении тартратного продукта к раствору MnP (зеленая кривая - 0 мин). Это поглощение (зеленая кривая - 0 мин) продолжает уменьшаться с течением времени до приблизительно 0,286А (розовая кривая - 15 мин, бирюзовая кривая - 30 мин, желтая кривая - 45 мин, серая кривая - 1 час).
[0147] На фиг. 19С представлены результаты экспериментов по предварительной обработке угля 3% Н202 в питательной среде PD, содержащей P. chrysosporium. Спектр для предварительно обработанного угля в этих условиях роста первоначально показывает пик приблизительно при 245 нм с поглощением, составляющим приблизительно 1,30 А, и пик приблизительно при 290 нм с поглощением, составляющим приблизительно 2,10 А (красная кривая). Эти пики не сдвигаются по длине волны (нм) с течением времени, но поглощение (А) каждый день проявляет тенденцию к небольшому изменению. В день 1 поглощение уменьшается до приблизительно 0,52 А при 245 нм и 1,60 А при 290 нм (синяя кривая), но увеличивается до приблизительно 1,45 А при 245 нм и 2,20 А при 290 нм в день 2 (зеленая кривая). После дня 2, поглощение снова увеличивается в день 3 до 1,28 А при 245 нм и 1,35 А при 290 нм (розовая кривая). Поглощение затем продолжает увеличиваться в течение оставшихся дней. День 4: 1,36 А при 245 нм и 1,58 А при 290 нм (бирюзовая кривая); день 5: 1,51 А при 245 нм и 2,02 А при 290 нм (желтая кривая); день 6: 1,56 А при 245 нм и 2,48 А при 290 нм (серая кривая); день 7: 1, 52 А при 245 нм и 2,63 А при 290 нм (черная кривая).
[0148] На фиг. 19D представлены результаты эксперимента для угля, предварительно обработанного 3% Н202, в питательной среде SD с пептоном в количестве одна десятая (0, 1), содержащей P. chrysosporium. Спектр для предварительно обработанного угля в этих условиях роста первоначально показывает пик приблизительно при 245 нм и поглощение, составляющее приблизительно 2.73А (красная кривая). Этот пик при 245 нм не сдвигается по длине волны и не демонстрирует значительно увеличения или уменьшения поглощения со дня 1 по день 10. День 1: 2,52 А (синяя кривая); день 2: 2,57 А (зеленая кривая); день 3: 2,42 А (розовая кривая); день 4: 2,39 А (бирюзовая кривая); день 5: 2,71 А (желтая кривая); день 6: 2,66 А (серая кривая); день 7: 2.52А (черная кривая); день 10: 2,60 А (оранжевая кривая). Поглощение при 245 нм затем уменьшается в день 14 до 2,02 А (бежевая кривая).
[0149] Уголь, предварительно обработанный 15% H2O2
[0150] На фиг. 19Е представлены результаты экспериментов по предварительной обработке угля с помощью 15% перекиси водорода (Н202). Спектр для предварительно обработанного угля в лакказном буфере имеет пик приблизительно при 230 нм и поглощение, составляющее только приблизительно 0,877 А (красная кривая). Этот спектр может сравниваться со спектром предварительно обработанного угля в лакказном растворе, который имеет пик приблизительно при 224 нм и поглощение, составляющее приблизительно 3,20 А (синяя кривая). При сравнении этих спектров можно увидеть, что предварительная обработка влияет на солюбилизацию угля, но для дальнейшей солюбилизации необходима лакказа. Спектры на фиг.19Е также иллюстрируют сдвиг пиков с 224 нм до приблизительно 249 нм и небольшое снижение поглощения с 3,20 А до 1,99 А, что происходит при первоначальном добавлении лакказного продукта к раствору MnP (зеленая кривая - 0 мин). Это поглощение (зеленая кривая - 0 мин) продолжает уменьшаться с течением времени до приблизительно 1,63 А (розовая кривая - 15 мин, бирюзовая кривая - 30 мин, желтая кривая - 45 мин, серая кривая - 1 час).
[0151] На фиг. 19F представлены результаты экспериментов по предварительной обработке угля с помощью 15% перекиси водорода (Н202). Спектр для необработанного угля в тартратном растворе не демонстрирует каких-либо резко выраженных пиков поглощения в спектрах (красная кривая). Однако предварительно обработанный уголь в тартратном буфере имеет пик приблизительно при 227 нм и поглощение, составляющее приблизительно 1,21 А (синяя кривая). Это указывает на то, что предварительная обработка оказывает очень существенное воздействие на химическую солюбилизацию угля при использовании тартратного раствора. Спектры на фиг.19F также иллюстрируют сдвиг пиков с 227 нм до приблизительно 245 нм и небольшое снижение поглощения с 1,21 А до 1,14 А, что происходит при добавлении тартратного продукта к раствору MnP (зеленая кривая - 0 мин). Это поглощение (зеленая кривая - 0 мин) продолжает уменьшаться с течением времени до приблизительно 0,52А (розовая кривая - 15 мин, бирюзовая кривая - 30 мин, желтая кривая - 45 мин, серая кривая - 1 час).
[0152] На фиг. 19G представлены результаты эксперимента по предварительной обработке угля с помощью 15% Н202, в питательной среде PD, содержащей Р. chrysosporium. Спектр (красная кривая) для предварительно обработанного угля в этих условиях роста первоначально показывает два пика: один пик при длине волны 245 нм с поглощением 1,00 А и один пик при длине волны 290 нм с поглощением 2,20 А. Пики на фиг. 19G, по-видимому, не сдвигаются по длине волны, но демонстрирует изменения поглощения день за днем. После первого дня пиковое поглощение уменьшается от начального пика до приблизительно 0,69 А при 245 нм и 1,80 А при 290 нм (синяя кривая). Это поглощение затем увеличивается в день 2 до 1,56 А при 245 нм и 2,30 А при 290 нм (зеленая кривая) и уменьшается в день 3 до 1,31 А при 245 нм и 1,35 А при 290 нм (розовая кривая). После дня 3 кривые затем демонстрируют увеличение поглощения в течение оставшихся дней. День 4: 1.38 А при 245 нм и 1,58 при 290 нм (бирюзовая кривая); день 5: 1,53 А при 245 нм и 2,13 А при 290 нм (желтая кривая); день 6: 1,62 А при 245 нм и 2,22 А при 290 нм (серая кривая); день 7: 1,74 А при 245 нм и 2,69 А при 290 нм (черная кривая); день 10: 1,75 А при 245 нм и 2,76 А при 290 нм (оранжевая кривая).
[0153] На фиг. 19Н представлены результаты эксперимента для угля, предварительно обработанного 15% Н202, в питательной среде SD с пептоном в количестве одна десятая (0,1), содержащей P. chrysosporium. Спектр для предварительно обработанного угля в этих условиях роста первоначально показывает пик приблизительно при 245 нм и поглощение, составляющее 2,78 А (красная кривая). Этот пик при 245 не сдвигается по длине волны, но демонстрирует небольшое уменьшение поглощения с дня 1 по день 14. День 1: 2,64 А (синяя кривая); день 2: 2,45 А (зеленая кривая); день 3: 2,38 А (розовая кривая); день 4: 2.39 А (бирюзовая кривая); день 5: 2,02 А (желтая кривая); день 6: 2,09 А (серая кривая); день 7: 2,12 А (черная кривая); день 10: 2,13 А (оранжевая кривая); день 14: 1,50 А (бежевая кривая).
[0154] Уголь, предварительно обработанный 30% H2O2
[0155] На фиг. 19I представлены результаты экспериментов по предварительной обработке угля с помощью 30% перекиси водорода (Н202). Спектр для предварительно обработанного угля в лакказном буфере имеет пик приблизительно при 224 нм и поглощение, составляющее приблизительно 1,99 А (красная кривая). Этот спектр может сравниваться со спектром предварительно обработанного угля в лакказном растворе, который имеет пик приблизительно при 211 нм и поглощение, составляющее приблизительно 2,58 А (синяя кривая). Сравнение этих спектров показывает, что предварительная обработка с помощью 30% Н202 сама по себе почти также эффективна, как лакказа при солюбилизации угля. Спектры на фиг. 19I также иллюстрируют сдвиг пиков с 211 нм до приблизительно 249 нм и снижение поглощения с 2,58 А до 1,77 А, что происходит при первоначальном добавлении лакказного продукта к раствору MnP (зеленая кривая). Поглощение (зеленая кривая) также продолжает уменьшаться с течением времени до приблизительно 1,13 А (розовая кривая - 15 мин, бирюзовая кривая - 30 мин, желтая кривая - 45 мин, серая кривая - 1 час).
[0156] На фиг. 19J представлены результаты экспериментов по предварительной обработке угля с помощью 30% перекиси водорода (Н202). Спектр для необработанного угля в тартратном растворе не демонстрирует каких-либо резко выраженных пиков поглощения в спектрах (красная кривая). Однако предварительно обработанный уголь в тартратном буфере имеет пик приблизительно при 228 нм и поглощение, составляющее приблизительно 1,52 А (синяя кривая). Разность между этими пиками показывает, что предварительная обработка необходима для химической солюбилизации угля в тартратном растворе. Спектры на фиг.19J также иллюстрируют сдвиг пиков с 228 нм до приблизительно 245 нм и снижение поглощения с 1,52 А до 1,18 А, что происходит при первоначальном добавлении тартратного продукта к раствору MnP (зеленая кривая- 0 мин). Это поглощение (зеленая кривая - 0 мин) продолжает уменьшаться с течением времени до приблизительно 0,87 А (розовая кривая - 15 мин, бирюзовая кривая - 30 мин, желтая кривая - 45 мин, серая кривая - 1 час).
[0157] На фиг. 19K представлены результаты эксперимента по предварительной обработке угля с помощью 30% Н202, в питательной среде PD, содержащей Р. chrysosporium. Спектр для этого конкретного предварительно обработанного угля первоначально имеет пик приблизительно при 245 нм с поглощением, составляющим приблизительно 0,86 А, и пик приблизительно при 295 нм с поглощением, составляющим 1,89 А (красная кривая). После первого дня поглощение снижается до приблизительно 0,59 А при 245 нм, но остается равным приблизительно 0,86 А при 295 нм (синяя кривая). Со дня 2 по день 5 поглощение при 245 нм не изменяется значительно, тогда как пик при 295 нм немного изменяется каждый день. День 2: 1,54 А при 245 нм и 2,56 А при 295 нм (зеленая кривая); день 3: 1,38 А при 245 нм и 2,22 А при 295 нм (розовая кривая); день 4: 1,57 А при 245 нм и 2,26 А при 295 нм (бирюзовая кривая); день 5: 1,76 А при 245 нм и 2,83 А при 295 нм (желтая кривая). В день 6 поглощение увеличивается в обоих пиках до приблизительно 2,29 А при 245 нм и 3,46 А при 295 нм (серая кривая).
[0158] На фиг. 19L представлены результаты эксперимента для угля, предварительно обработанного 30% Н202, в питательной среде SD с пептоном в количестве одна десятая (0,1), содержащей P. chrysosporium. Спектр для предварительно обработанного угля в этих условиях роста первоначально показывает пик приблизительно при 243 нм и поглощение, составляющее приблизительно 1,56 А (красная кривая). Этот пик при 245 нм не сдвигается по длине волны, но демонстрирует небольшое уменьшение поглощения со дня 1 по день 7, за исключением дней 3 и 10, когда поглощение увеличивается. День 1: 1,47 А (синяя кривая); день 2: 1,39 А (зеленая кривая); день 3: 2,09 А (розовая кривая); день 4: 1,30 А (бирюзовая кривая); день 5: 1,07 А (желтая кривая); день 6: 0,93 А (серая кривая); день 7: 0,93 А (черная кривая). В день 10 поглощение при 245 нм увеличивается до 2,58 А (оранжевая кривая).
[0159] Предварительная обработка нагретого угля
[0160] На фиг. 19М представлены результаты экспериментов по предварительной обработке нагретого угля с помощью 30% перекиси водорода (Н202). Спектр для предварительно обработанного угля в лакказном буфере имеет пик приблизительно при 237 нм и поглощение, составляющее только приблизительно 1,41 А (красная кривая). Этот спектр может сравниваться со спектром предварительно обработанного угля в лакказном растворе, который имеет пик приблизительно при 227 нм и поглощение, составляющее приблизительно 3,09 А (синяя кривая). Сравнение этих спектров показывает, что предварительная обработка угля оказывает некоторое воздействие на солюбилизацию угля, но лакказа дополнительно окисляет уголь и солюбилизирует его спектры на фиг. 19М также иллюстрируют сдвиг пиков с 227 нм до приблизительно 247 нм и небольшое снижение поглощения с 3,09 А до 2,31 А, что происходит при первоначальном добавлении лакказного продукта к раствору MnP (зеленая кривая - 0 мин). Эта кривая также продолжает уменьшаться с течением времени (розовая кривая - 15 мин, бирюзовая кривая - 30 мин, желтая кривая - 45 мин, серая кривая - 1 час).
[0161] На фиг. 20А представлены результаты эксперимента по нагреванию угля. Спектр для этой предварительной обработки в питательной среде PD с Р. chrysosporium не показывает первоначально резко выраженный пик в день 0 (красная кривая) или день 1 (синяя кривая). Пик затем начинает образовываться в день 2 приблизительно при 240 нм с поглощением 1,39 А (зеленая кривая). Этот пик при 240 нм затем демонстрирует уменьшение поглощения в день 3 до 0,68 А (розовая кривая) и день 4 до 0,23 А (бирюзовая кривая). Наконец, пик демонстрирует увеличение поглощения при 240 нм за последние 2 дня. День 5: 1,39 А при 245 нм (желтая кривая) и день 6: 1,93 А при 240 нм (серая кривая).
[0162] На фиг. 20В представлены результаты эксперимента по нагреванию угля в питательной среде SD с пептоном в количестве одна десятая (0,1), содержащей Р. chrysosporium. Спектр для предварительно обработанного угля в этих условиях роста первоначально имеет пик приблизительно при 240 нм и поглощение, составляющее 0,61 А (красная кривая). Этот пик при 240 нм демонстрирует увеличение поглощения до приблизительно 0,78 А в день 1 (синяя кривая). Со дня 2 по день 5 поглощение при этой длине волны продолжает изменяться. День 2: 0,73 А (зеленая кривая); день 3: 0,56 А (розовая кривая); день 4: 0,78 А (бирюзовая кривая); день 5: 0,44 А (желтая кривая). В день 6 пик, по-видимому, сдвигается по длине волны до приблизительно 260 нм и остается на той же длине волны в день 7 и день 10. День 6: 0.66А (серая кривая); день 7: 0,55 А (черная кривая) и день 10: 0,95 А (оранжевая кривая).
[0163] Уголь, предварительно обработанный шахтной водой
[0164] На фиг. 21А представлены результаты экспериментов по предварительной обработке угля с помощью шахтной воды. Спектр для предварительно обработанного угля в лакказном буфере имеет пик приблизительно при 245 нм и поглощение, составляющее приблизительно 0,71 А (красная кривая). Этот спектр может сравниваться со спектром предварительно обработанного угля в лакказном растворе, который имеет пик приблизительно при 217 нм и поглощение, составляющее приблизительно 2,34 А (синяя кривая). Сравнение этих спектров показывает, что предварительная обработка способствует первоначальному окислению и разложению угля, но что лакказа необходима для дальнейшего разложения. Спектры на фиг. 21А также иллюстрируют сдвиг пиков с 227 нм до приблизительно 249 нм и небольшое снижение поглощения с 2,58 А до 2,25 А, что происходит при первоначальном добавлении лакказного продукта к раствору MnP (зеленая кривая - 0 мин). Это поглощение (зеленая кривая - 0 мин) продолжает уменьшаться с течением времени до приблизительно 1,83 А (розовая кривая - 15 мин, бирюзовая кривая - 30 мин, желтая кривая - 45 мин, серая кривая - 1 час).
[0165] На фиг. 21В представлены результаты экспериментов по предварительной обработке угля с помощью шахтной воды. Спектр для необработанного угля в тартратном растворе не демонстрирует каких-либо резко выраженных пиков поглощения в спектрах (красная кривая). Однако предварительно обработанный уголь в тартратном буфере имеет пик приблизительно при 228 нм и поглощение, составляющее приблизительно 1,43 А (синяя кривая). Сравнение этих двух кривых показывает, что предварительная обработка необходима для химической солюбилизации угля в тартратном растворе. Спектры на фиг. 21В также иллюстрируют сдвиг пиков с 228 нм до приблизительно 245 нм, что происходит при добавлении тартратного продукта к раствору MnP (зеленая кривая - 0 мин). Это поглощение (зеленая кривая - 0 мин) продолжает уменьшаться с течением времени до приблизительно 0,87 А (розовая кривая - 15 мин, бирюзовая кривая - 30 мин, желтая кривая - 45 мин, серая кривая - 1 час).
[0166] На фиг. 21С представлены результаты экспериментов по предварительной обработке угля в питательной среде PD, содержащей P. chrysosporium. Спектр для этого предварительно обработанного угля имеет 2 пика: один пик при приблизительно 245 нм и один пик при приблизительно 305 нм. Пик при 245 нм имеет поглощение 1,17 А (красная кривая) и сохраняет поглощение равным 1,17 А после дня 1 (синяя кривая). Пик при 245 нм демонстрирует увеличение поглощения в день 2 до приблизительно 2,00 А (зеленая кривая) и лишь небольшое изменение поглощения в оставшиеся дни. День 4: 1,84 А (розовая кривая); день 5: 1,89 А (бирюзовая кривая); день 6: 1,87 А (желтая кривая); день 7: 1,78 А (серая кривая); день 10: 1,82 А (черная кривая). Пик при 305 нм имеет первоначальное поглощение, составляющее 2,97 А (красная кривая) и также лишь немного изменяется за весь период времени. День 1: 3,06 А (синяя кривая); день 2: 3,51 А (зеленая кривая); день 4: 3,49А (розовая кривая); день 5: 3,12А (бирюзовая кривая); день 6: 3,31 А (желтая кривая); день 7: 3.24А (серая кривая); день 10: 3,06А (черная кривая).
[0167] На фиг. 21D представлены результаты эксперимента для угля, предварительно обработанного 30% Н202, в питательной среде SD с пептоном в количестве одна десятая (0,1), содержащей P. chrysosporium. Спектр для предварительно обработанного угля в этих условиях первоначально имеет широкий пик приблизительно при 297 нм с поглощением, составляющим приблизительно 3,94 А (красная кривая). Спектры со дня 1 по день 5 остаются относительно неизменными при 297 нм. День 1: 3,95 А (синяя кривая); день 2: 3,96 А (зеленая кривая); день 3: 3,89 А (розовая кривая); день 4: 3,97 А (бирюзовая кривая); день 5: 3,82 А (желтая кривая). В день 6 поглощение начинает немного уменьшаться при 297 нм и продолжает немного уменьшаться в день 7 и день 10. День 6: 3,70 А (серая кривая); день 7: 3,60 А (черная кривая); день 10: 3,45 А (оранжевая кривая). В день 14 поглощение увеличивается до 3,76 А (бежевая кривая).
[0168] Уголь, предварительно обработанный HNO3 (рН 1)
[0169] На фиг. 22А представлены результаты экспериментов для угля, предварительно обработанного неконцентрированной азотной кислотой HN03 (рН 1). Спектр для предварительно обработанного угля в лакказном буфере имеет пик приблизительно при 210 нм и поглощение, достигающее только приблизительно 0,47 А (красная кривая) и может сравниваться со спектром для предварительно обработанного угля в лакказном растворе, имеющим пик приблизительно при 213 нм и поглощение, достигающее приблизительно 1,68 А (синяя кривая). Сравнение этих кривых показывает, что предварительная обработка оказывает воздействие на солюбилизацию угля, но лакказный раствор дополнительно окисляет и разлагает уголь. Спектры на фиг. 22А также иллюстрируют сдвиг пиков с 213 нм до приблизительно 244 нм и снижение поглощения с 1,68 А до 1,35 А, что происходит при первоначальном добавлении лакказного продукта к раствору MnP (зеленая кривая - 0 мин). Это поглощение (зеленая кривая - 0 мин) продолжает уменьшаться с течением времени до приблизительно 0,99 А (розовая кривая - 15 мин, бирюзовая кривая - 30 мин, желтая кривая - 45 мин, серая кривая - 1 час).
[0170] На фиг. 22В представлены результаты эксперимента по предварительной обработке угля с помощью HN03 (рН 1) в питательной среде PD, содержащей Р. chrysosporium. Спектр для этого эксперимента имеет пик приблизительно при 260 нм с относительным поглощением -0,52 А (красная кривая). Это поглощение при 260 нм увеличивается до -0.32А в день 1 (синяя кривая). В день 2 пик сдвигается и начинает формироваться при 240 нм с поглощением 0,794 А (зеленая кривая). Этот пик при 240 нм немного увеличивается в день 3 до 0,93 А (розовая кривая), но затем демонстрирует уменьшение поглощения со дня 4 по день 7. День 4: 0,80 А (бирюзовая кривая); день 5: 0,49 А (желтая кривая); день 6: 0,44 А (серая кривая); день 7: 0,003 А (черная кривая).
[0171] На фиг. 22С представлены результаты эксперимента для угля, предварительно обработанного неконцентрированной азотной кислотой HN03 (рН 1), в питательной среде SD с пептоном в количестве одна десятая (0,1), содержащей P. chrysosporium. Спектр для предварительно обработанного угля в этих условиях первоначально показывает поглощение, составляющее -0,23 А приблизительно при 235 нм (красная кривая). Поглощение на этой длине волны затем продолжает уменьшаться со дня 1 по день 7. День 1: -0,35 А (синяя кривая); день 2: -0,44 А (зеленая кривая); день 3: -0,34 А (розовая кривая); день 4: -0,33А (бирюзовая кривая); день 5: -0.55А (желтая кривая); день 6: -0,70А (серая кривая); день 7: -0.78А (черная кривая). Наконец, в день 10 поглощение при 245 нм увеличивается до -0,30 А (оранжевая кривая).
[0172] Работа в этом примере направлена на конверсию битуминозного угля в жидкие топлива. Этот процесс включает в себя одни и те же действия, выполняемые природными микроорганизмами для расщепления молекулярных структур, находящихся в угле, до пригодных для использования форм, которые могут вступать в свои метаболические пути, высвобождая углерод и энергию. Одним из примеров такого метаболического пути является расщепление фенола, показанное на фиг. 23.
[0173] Фенолы представляют собой важный класс функциональных групп, поскольку 40-75% углерода в битуминозном угле относятся к ароматическому ряду, при этом фенолы и фенольные фрагменты представляют собой предпочтительную входную точку для бактериального разрыва ароматического кольца.
[0174] Раскрытие ароматических кольцевых структур является также необходимым первым этапом при конверсии угля в жидкие топлива в процессе УТС. В качестве справочной информации, временные последовательности спектров УФ-излучения для расщепления фенола приведены на фиг.24. Хотя эти результаты не были получены в биологической системе, они обеспечивают качественный показатель переходов в спектрах УФ-излучения, которые можно ожидать при направлении реакции, показанном выше.
[0175] Как видно из графиков, поглощение на переднем краю спектров УФ-излучения возрастает на начальных стадиях расщепления, соответствующих образованию ароматических промежуточных соединений. По мере формирования промежуточных соединений концентрация фенола уменьшается, что показано уменьшением поглощения для фенола при 268 нм. Оба пика затем начинают снижаться по мере того, как фенол расходуется и ароматические промежуточные соединения подвергаются разрыву кольца. В конечном счете, поглощение приближается к нулю по мере того, как расщепляемые ароматические промежуточные соединения преобразуются в органические кислоты.
[0176] Спектры, представленные в данном примере, показывают, что используемые в нем способы обеспечивают один и тот же тип расщепления, как показано спектрами УФ-излучения для расщепления фенола. Очевидно также, что степень, до которой уголь подвергается конверсии, значительно изменяется в зависимости от способа предварительной обработки угля.
[0177] Как указано выше, были приняты три различных подхода для расщепления битуминозного угля: (1) лакказа и MnP, (2) тартрат аммония и MnP и (3) живой организм P. Chrysosporium с использованием двух различных питательных сред. Результаты экспериментов с лакказой и MnP и живым P. chrysosporium оказались лучшими и сравнивались между собой.
[0178] Эти спектры показаны на фиг. 19А-22С. Как видно из фиг. 19А-22С, спектры для этих подходов с использованием различных способов предварительной обработки угля имеют пики в области от 240 нм до 300 нм. Эти пики соответствуют меньшим ароматическим кольцевым промежуточным соединениям и органическим кислотам, образующимся при расщеплении битуминозного угля. Из этих спектров становится ясным, что оба способа действительно позволяют расщеплять уголь.
[0179] Первые эксперименты по ферментативной солюбилизации и конверсии проводились с использованием лакказы и MnP и показаны на фиг. 19А, 19Е, 191, 19М, 21А и 22А. Спектры имеют пики приблизительно при 245 нм - 250 нм. Пики в этих спектрах затем начинают демонстрировать уменьшение поглощения в течение 1 часа в соответствии с расходованием ароматических промежуточных соединений в то время, как они подвергаются разрыву кольца.
[0180] Живой P. chrysosporium использовался в качестве другого способа расщепления битуминозного угля. Он выращивался в двух различных питательных средах для обеспечения удовлетворительных условий роста организма, экскретирующего внеклеточные ферменты для расщепления угля. Спектры для картофельно-декстрозной (PD) питательной среды, содержащей P. chrysosporium, имели пики в области от 240 нм до 300 нм, показанной на фиг. 19С, 19G, 19K, 20А, 21С и 22В. В этих экспериментах показано, что пиковое поглощение уменьшается за период с 7 по 10 день.
[0181] P. chrysosporium также выращивался в сабуро-декстрозной (SD) питательной среде. Спектры, соответствующие этим экспериментам, показаны на фиг. 19D, 19Н, 19L, 20В, 2 ID и 22С. Большинство пиков спектра видны в диапазоне от 235 нм до 245 нм. Уменьшение пика поглощения наблюдается в период с 10 по 14 день.
[0182] Основными параметрами, сравниваемыми между спектрами в УФ- и видимой области для двух различных ферментативных способов, были местоположение пиков (нм) и уменьшение пика поглощения (А). Как упоминалось выше, пики в экспериментах приходятся на диапазон от 240 нм до 300 нм, что соответствует ароматическим промежуточным соединениям, образующимся при разрушении структуры угля. Кривые, полученные для лакказы + MnP и Р. chrysosporium в питательной среде S.D., имеют аналогичные пики в области от 235 нм до 250 нм. Кривые, полученные для P. chrysosporium в питательной среде P.D., имеют два различных пика, в области 245 нм и в области 290 нм.
[0183] Из сравнения значений уменьшения пика поглощения видно, что поглощение в экспериментах, проводившихся с лакказой и MnP, уменьшается за период времени 1 час. Однако в экспериментах с живым P. chrysosporium уменьшение пика поглощения наблюдается в период с 10 по 14 день. Это значительное различие во времени, требующемся для образования ароматических промежуточных соединений и разрыва кольца, иллюстрирует одно из основных различий между применением внеклеточных ферментов и живых организмов.
[0184] Из сравнения спектров различных типов предварительной обработки видно, что наиболее непротиворечивые результаты наблюдаются в случаях предварительной обработки 3%, 15% и 30% перекисью водорода. Эти спектры имеют пики в области от 235 нм до 240 нм для всех проб предварительно обработанного угля. В случае спектров для нагретого угля значения пиков для экспериментов с использованием живого P. chrysosporium не являются такими же непротиворечивыми, как для экспериментов с использованием внеклеточных ферментов. Для угля, предварительно обработанного шахтной водой, пики поглощения не уменьшаются со временем в экспериментах с использованием живого P. chrysosporium, как это происходит в экспериментах с использованием внеклеточных ферментов. Наконец, спектры для угля, обработанного азотной кислотой, демонстрируют отрицательное поглощение в экспериментах с использованием живого P. chrysosporium, что не согласуется с пиками, полученными при использовании внеклеточных ферментов.
[0185] В этом примере было показано, что как внеклеточные ферменты, так и живые организмы можно использовать для разложения битуминозного угля. Спектры, полученные в этих экспериментах, имеют пики в области от 240 нм до 300 нм, соответствующей меньшим ароматическим кольцевым промежуточным соединениям и органическим кислотам, образующимся при расщеплении угля. Однако при сравнении этих различных способов становится понятно, что наиболее эффективным способом является разрушение структуры угля с помощью ферментов. Этот процесс имеет несколько преимуществ по сравнению с использованием живых организмов.
[0186] Одним из основных преимуществ использования внеклеточных ферментов вместо живых организмов является время, необходимое для разложения. Как видно из спектров, результаты экспериментов с использованием лакказы и марганецпероксидазы показали уменьшение поглощения в течение первого часа проведения экспериментов. Аналогичные величины уменьшения поглощения также видны из результатов для P. chrysosporium. Однако эти результаты были зарегистрированы в течение дней, а не минут. Очевидно, что живому организму требуется больше времени для экскретирования подходящих внеклеточных ферментов для измельчения угля.
[0187] В дополнение к этому, как упоминалось выше, работать с организмами сложно, поскольку они живые, и количество неизвестных факторов очень велико. Сюда входит поддержание идеальных условий культивирования для организма, а также регулирование загрязнителей и фунгицидных побочных продуктов, что может препятствовать росту организма или экскретированию внеклеточных ферментов для разрушения угля.
[0188] Для расщепления битуминозного угля могут также использоваться лигнолитические ферменты, такие как лигнинпероксидаза. В дополнение к этому, возбуждающие белую гниль грибки, такие как Trametes Versicolor, могут выращиваться и подвергаться воздействию битуминозного угля. Различные условия культивирования могут также воздействовать на то, как организмы экскретируют внеклеточные ферменты, расщепляя уголь.
[0189] Хотя были показаны и описаны предпочтительные варианты осуществления настоящего изобретения, специалистом в данной области техники могут быть выполнены его модификации без отступления от объема и принципов настоящего изобретения. Описанные в настоящем документе варианты осуществления и приведенные примеры рассмотрены только в качестве иллюстрации и не имеют ограничительного характера. Многие изменения и модификации изобретения, раскрытого в настоящем документе, возможны и включены в объем изобретения.
Соответственно, объем правовой охраны не ограничивается приведенным выше описанием, а ограничивается только нижеследующей формулой изобретения, при этом объем включает в себя все эквиваленты предмета формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЛИГНИНОЛИТИЧЕСКИХ ФЕРМЕНТОВ | 1992 |
|
RU2021371C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ЛИГНОЦЕЛЛЮЛОЗНОЙ БУМАГИ И БУМАЖНЫХ ПРОДУКТОВ | 2016 |
|
RU2728098C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДАЗ ГРИБА MICROTHIELAVIA OVISPORA VKM F-1735, ОБЕСЦВЕЧИВАЮЩИХ ПРОМЫШЛЕННЫЕ КРАСИТЕЛИ БЕЗ МЕДИАТОРА | 2021 |
|
RU2773712C1 |
| ШТАММ RHIZOCTONIA SOLANI F-895 - ПРОДУЦЕНТ АЛКАЛОФИЛЬНЫХ ЛАККАЗ, АКТИВНЫХ С ФЕНИЛПРОПАНОИДАМИ | 2015 |
|
RU2647767C2 |
| Способ получения лакказ гриба Myrothecium verrucaria ВКМ F-3851, трансформирующие фенольные соединения в нейтрально - щелочных условиях среды | 2016 |
|
RU2663342C2 |
| ТЕРМОСТАБИЛЬНАЯ ЛАККАЗА III ГРИБА Steccherinum ochraceum LE (BIN) 1833 D И СПОСОБ ПОЛУЧЕНИЯ ЛАККАЗ | 2008 |
|
RU2385930C1 |
| СИСТЕМЫ И СПОСОБЫ ОТБОРА РАСТВОРИТЕЛЕЙ ДЛЯ РАСТВОРЕНИЯ ДОННОГО ОСАДКА В РЕЗЕРВУАРЕ | 2014 |
|
RU2673608C1 |
| Способ получения оксидаз Curvularia geniculata ВКМ F-3561, активных с фенольными соединениями в нейтральных условиях среды | 2017 |
|
RU2664483C2 |
| Способ определения индивидуальных полициклических ароматических углеводородов в техническом углероде | 1983 |
|
SU1254359A1 |
| СОЛЮБИЛИЗАЦИЯ УГЛЕРОДСОДЕРЖАЩИХ МАТЕРИАЛОВ И КОНВЕРСИЯ ИХ В УГЛЕВОДОРОДЫ И ДРУГИЕ ПОЛЕЗНЫЕ ПРОДУКТЫ | 2011 |
|
RU2560158C2 |
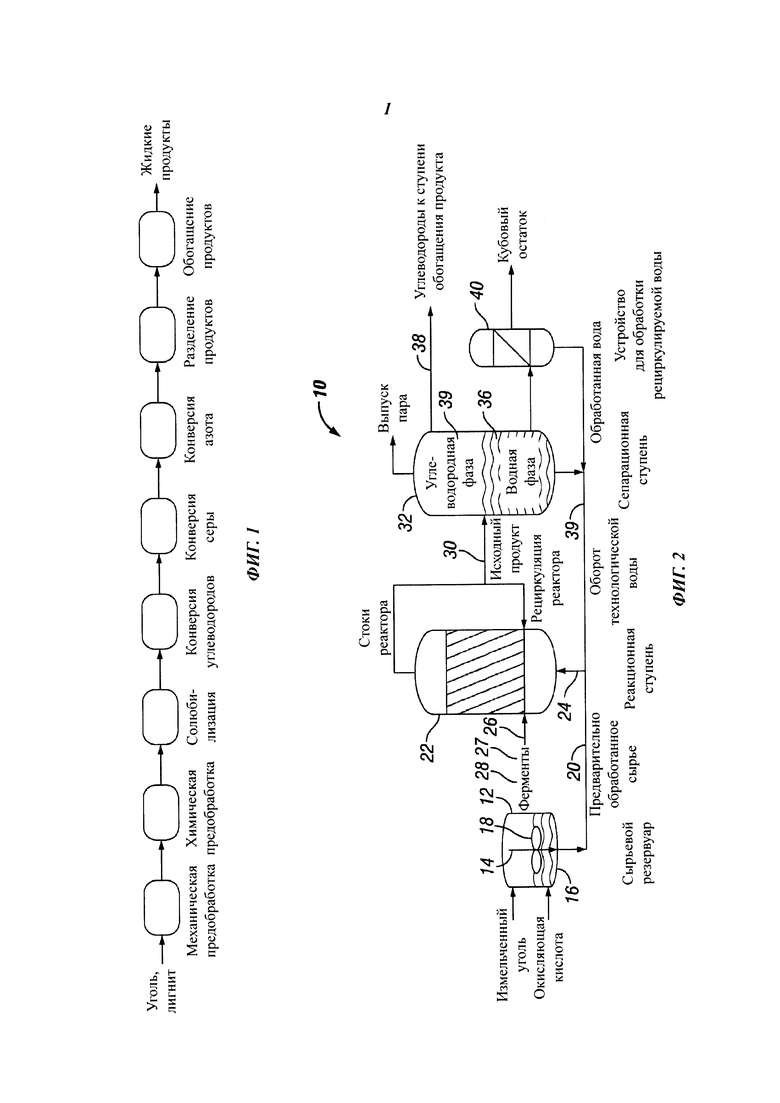
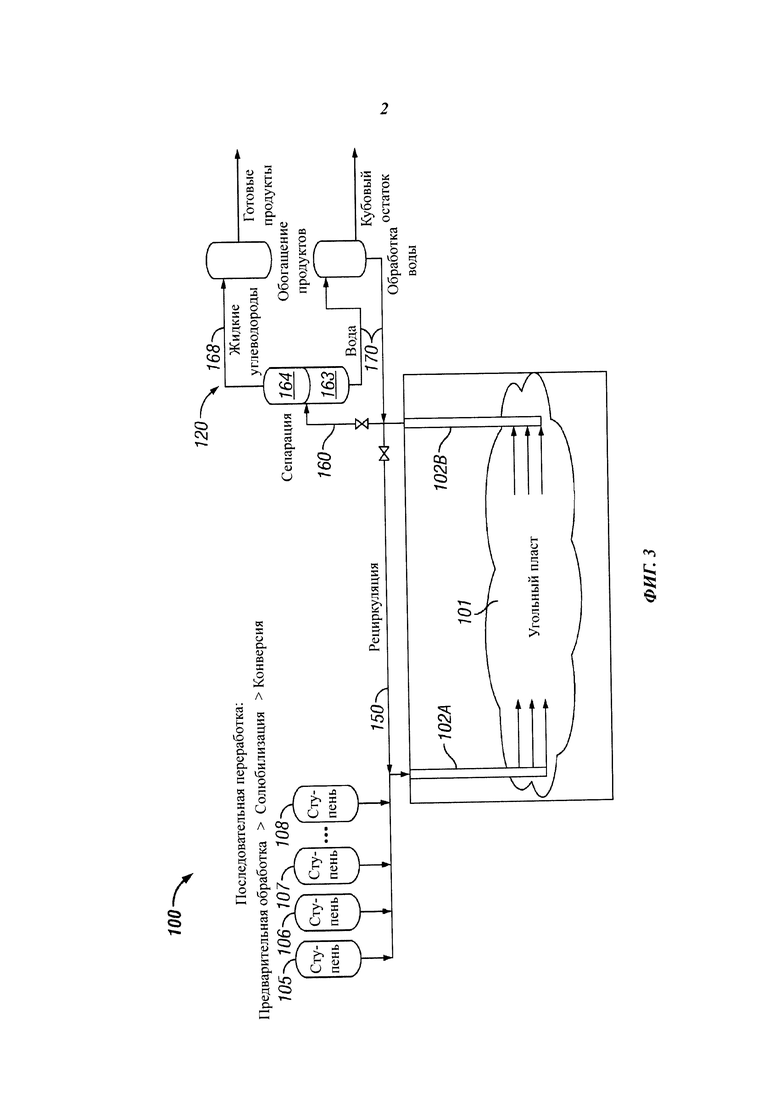
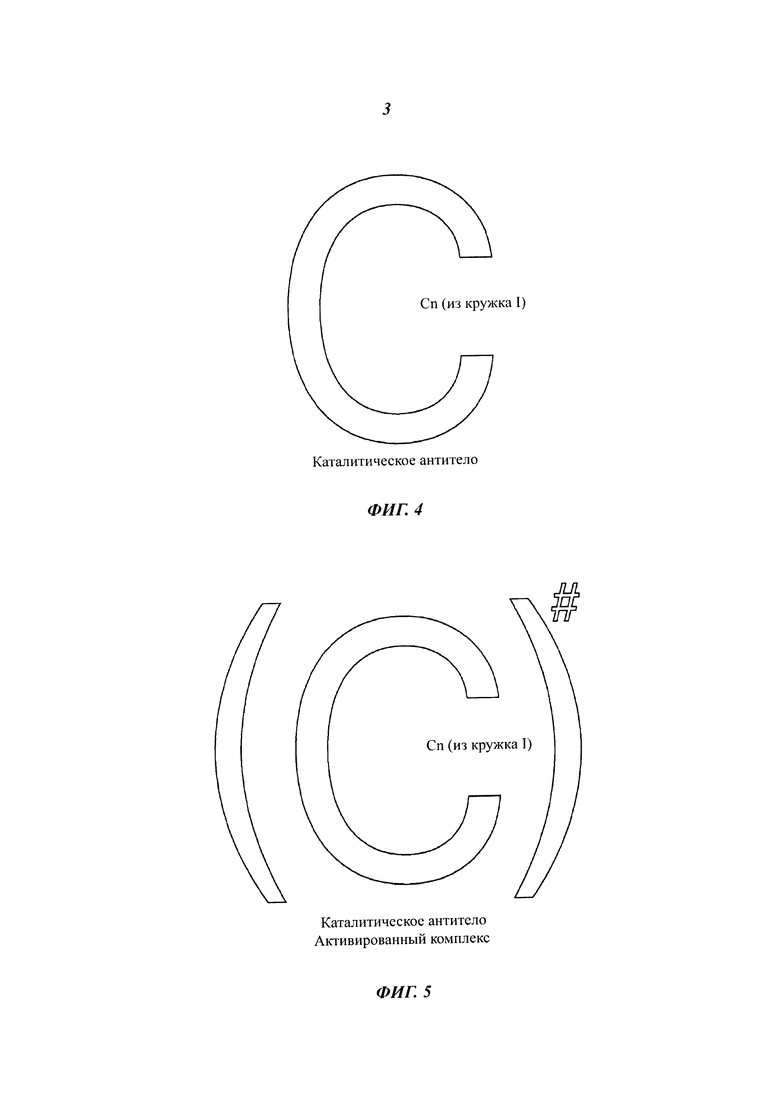
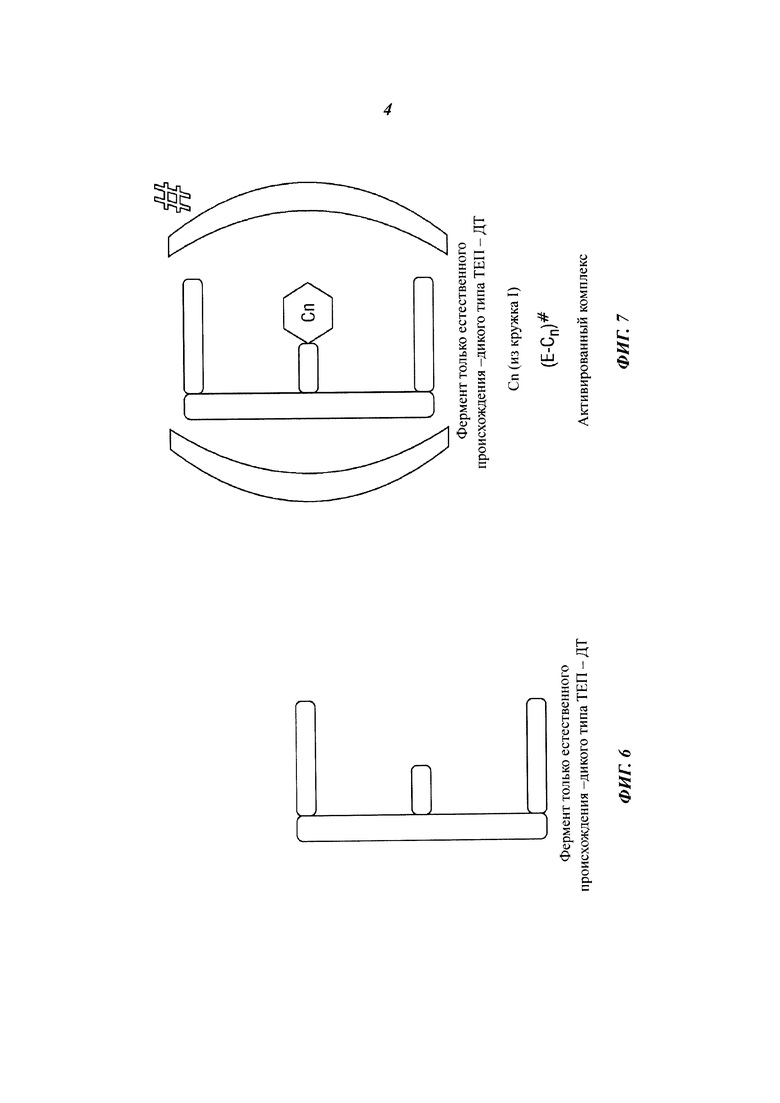
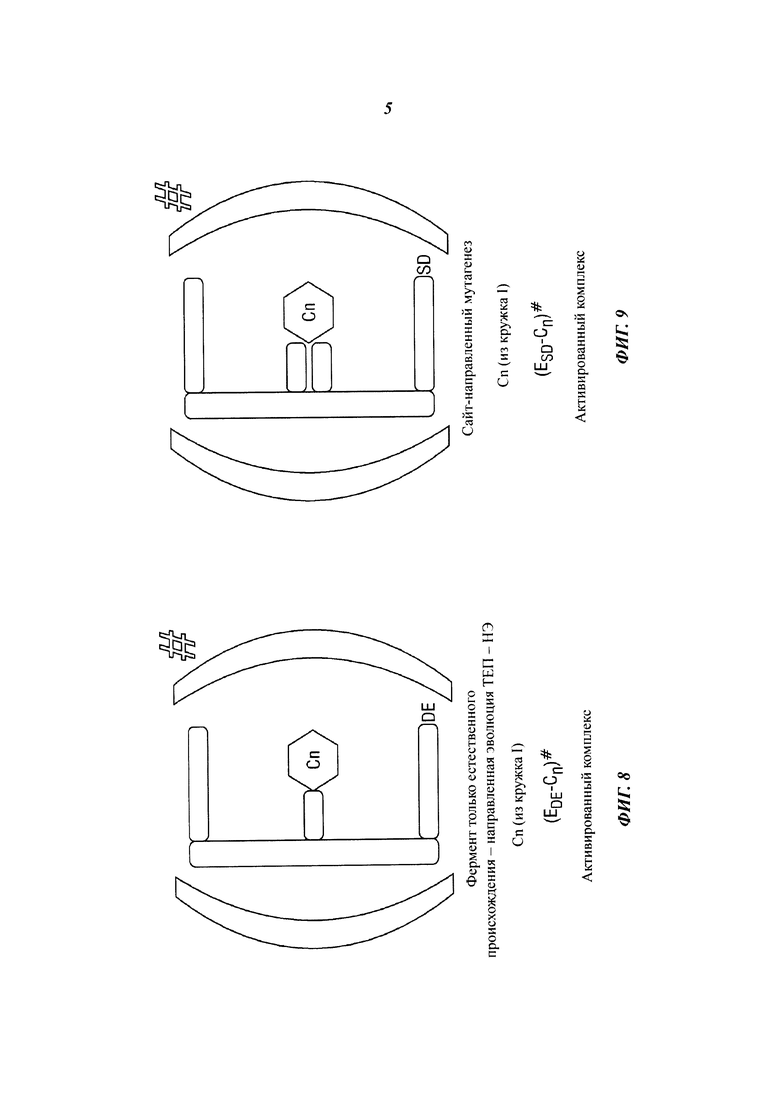
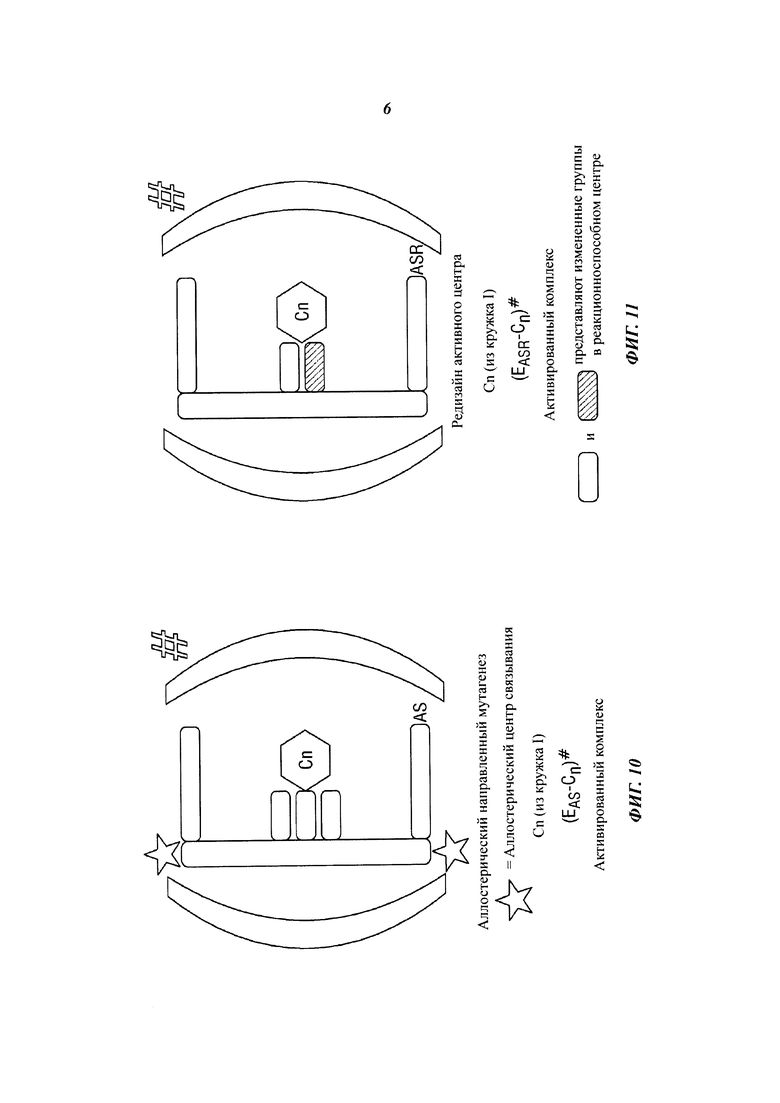
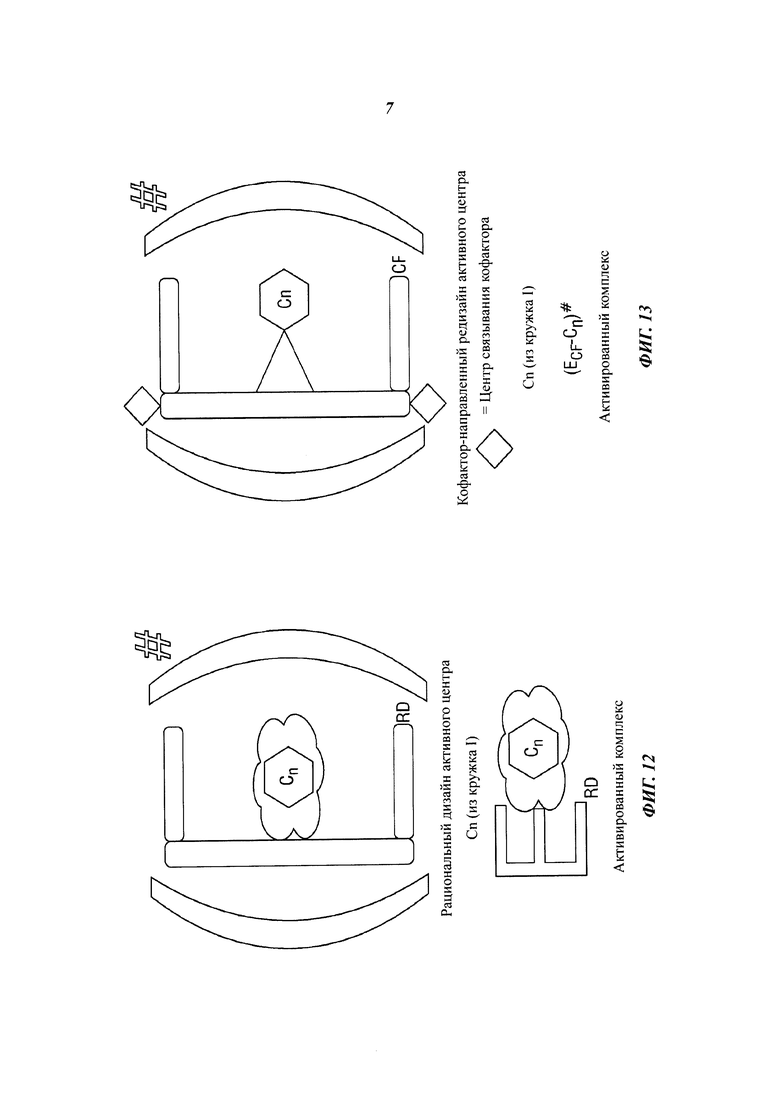
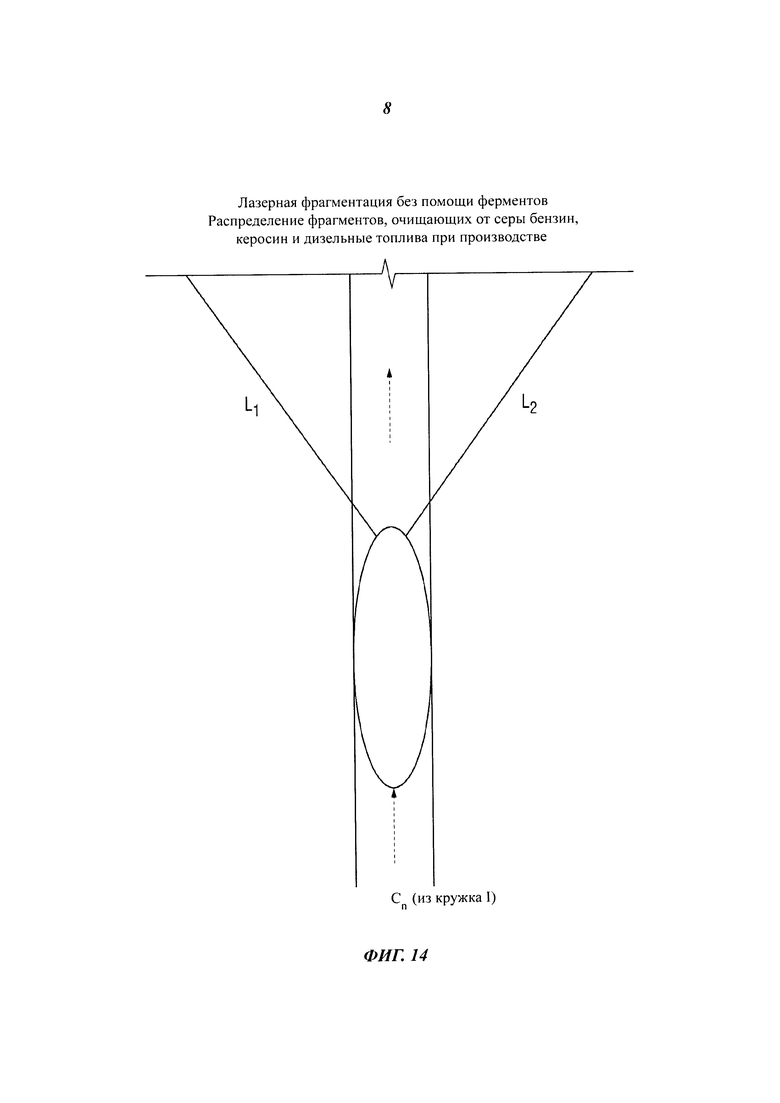
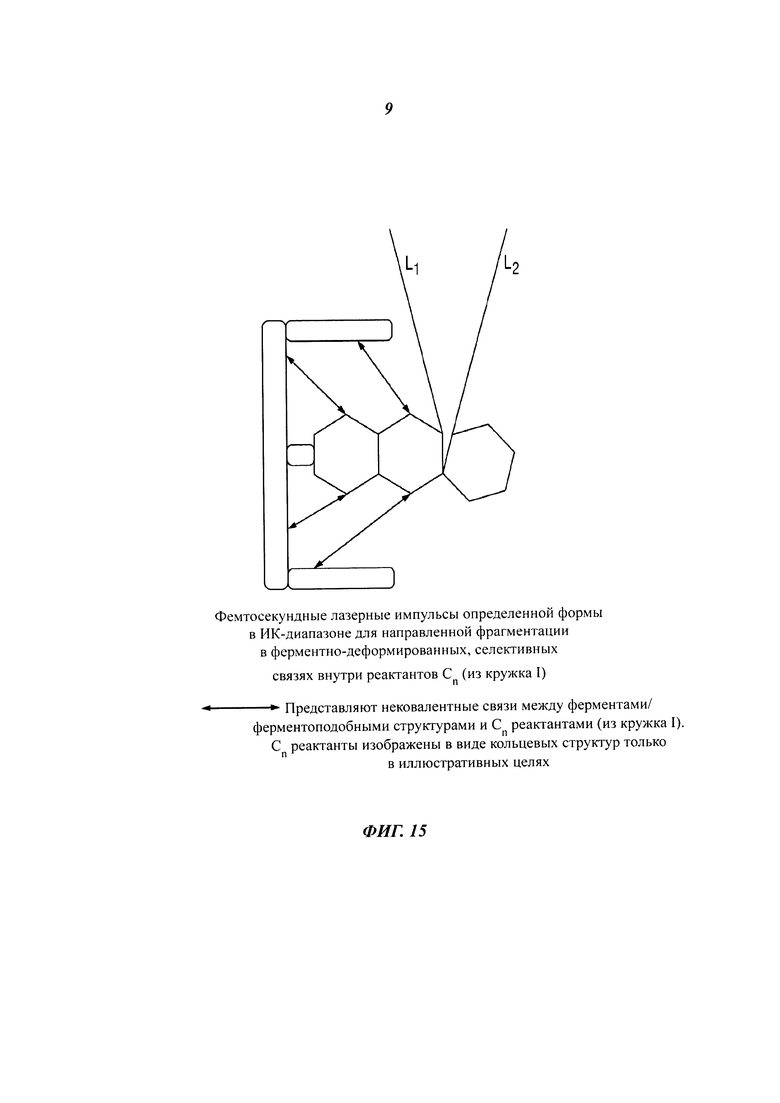
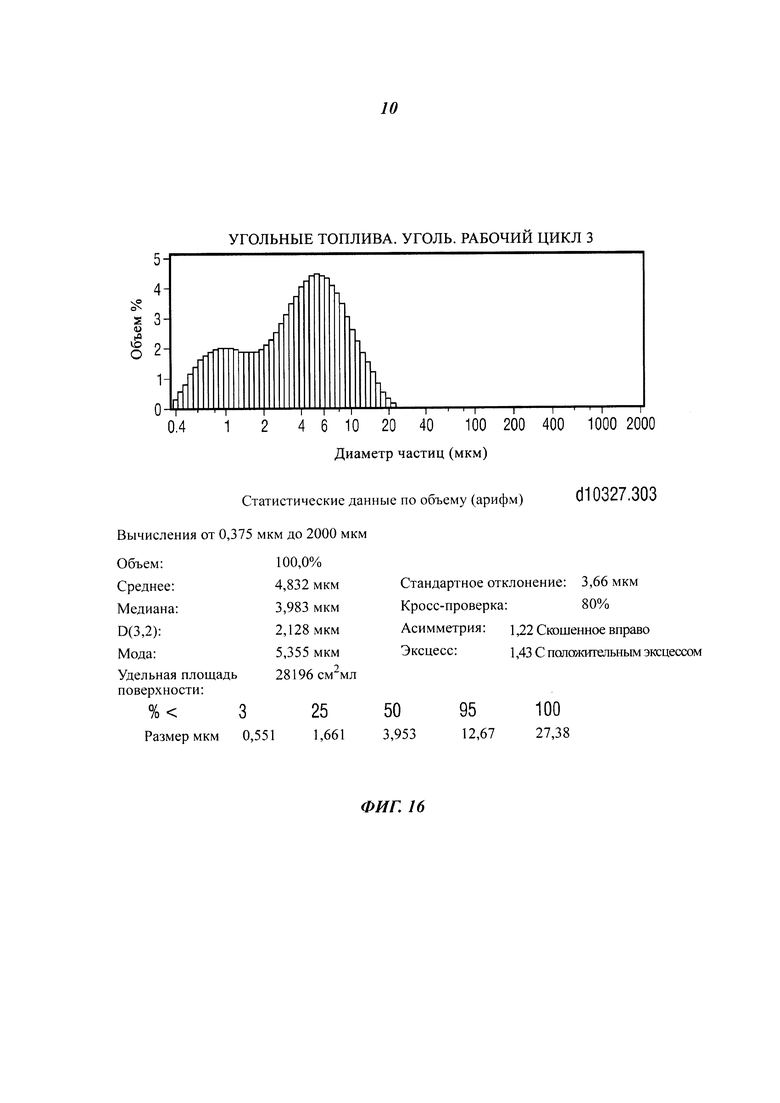
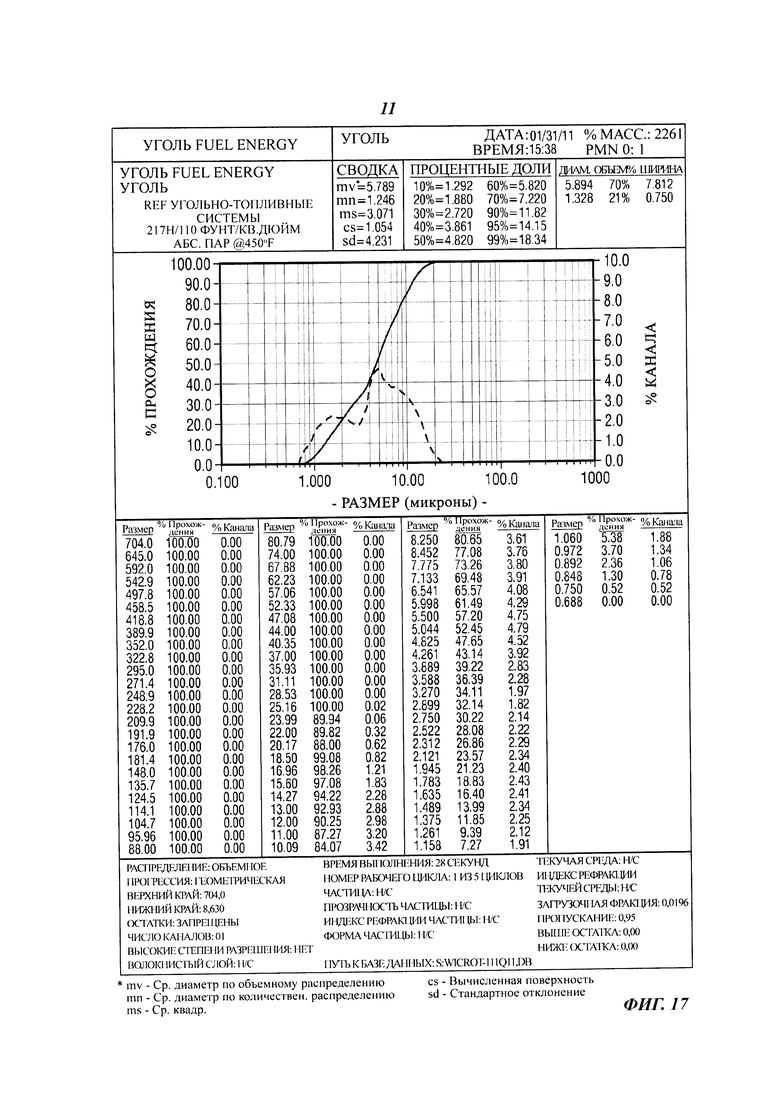
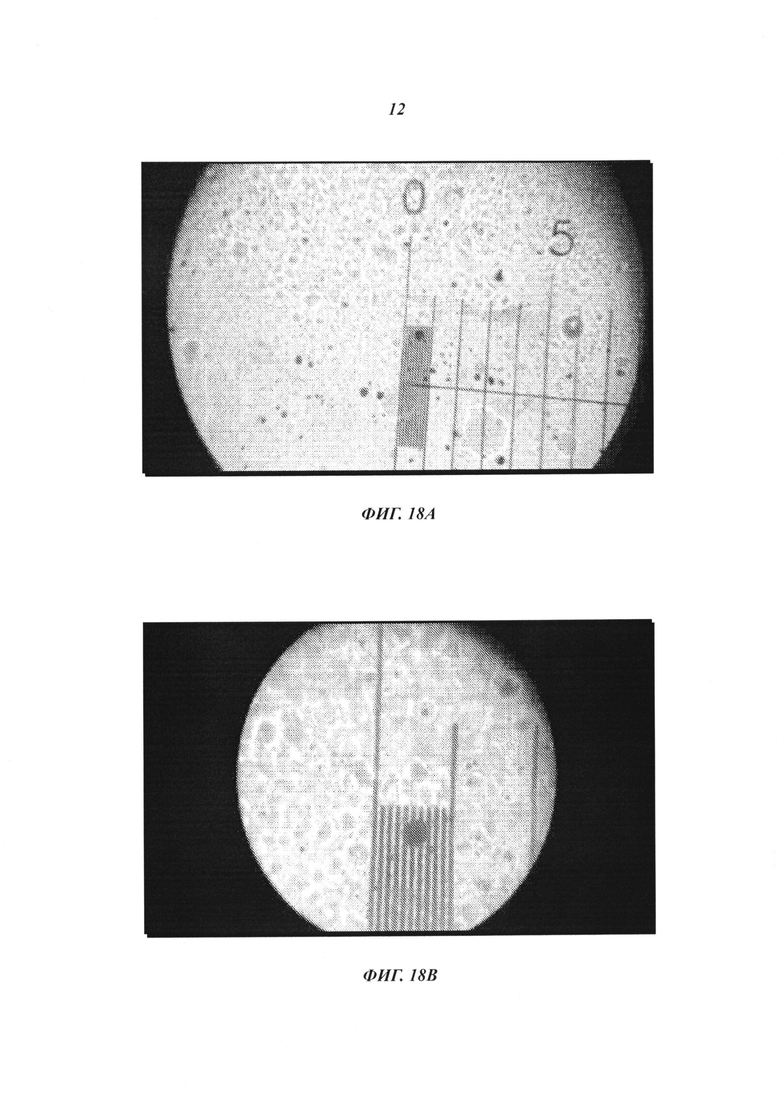
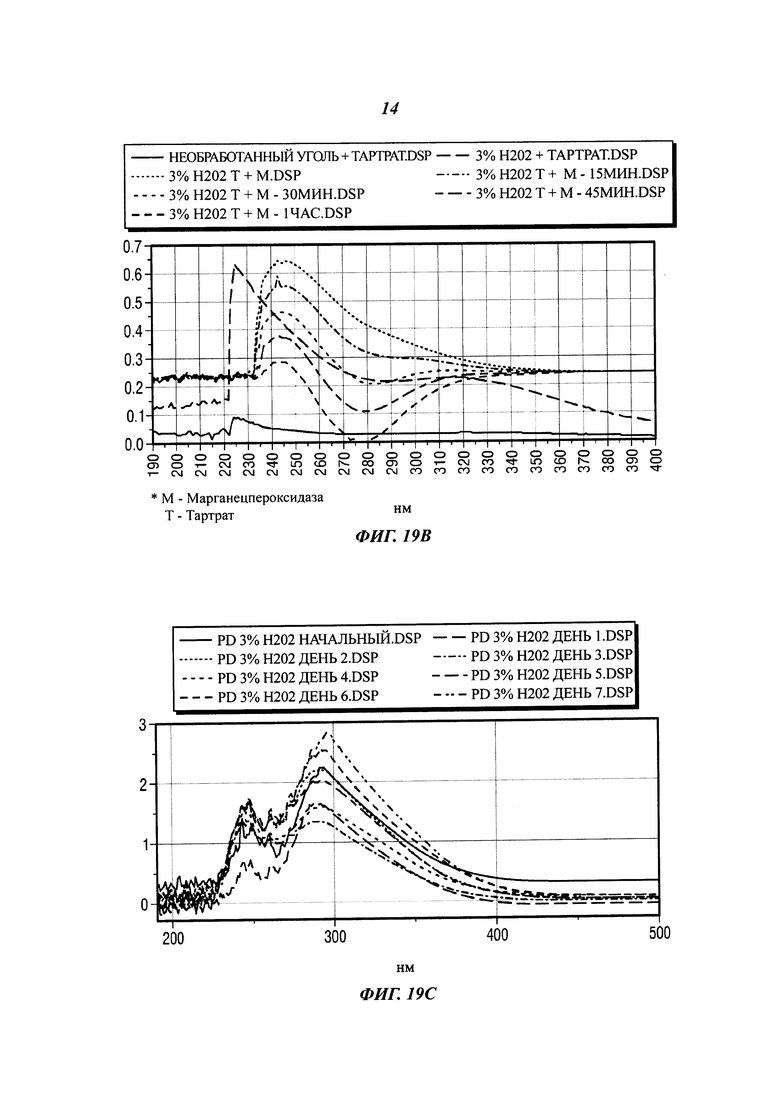
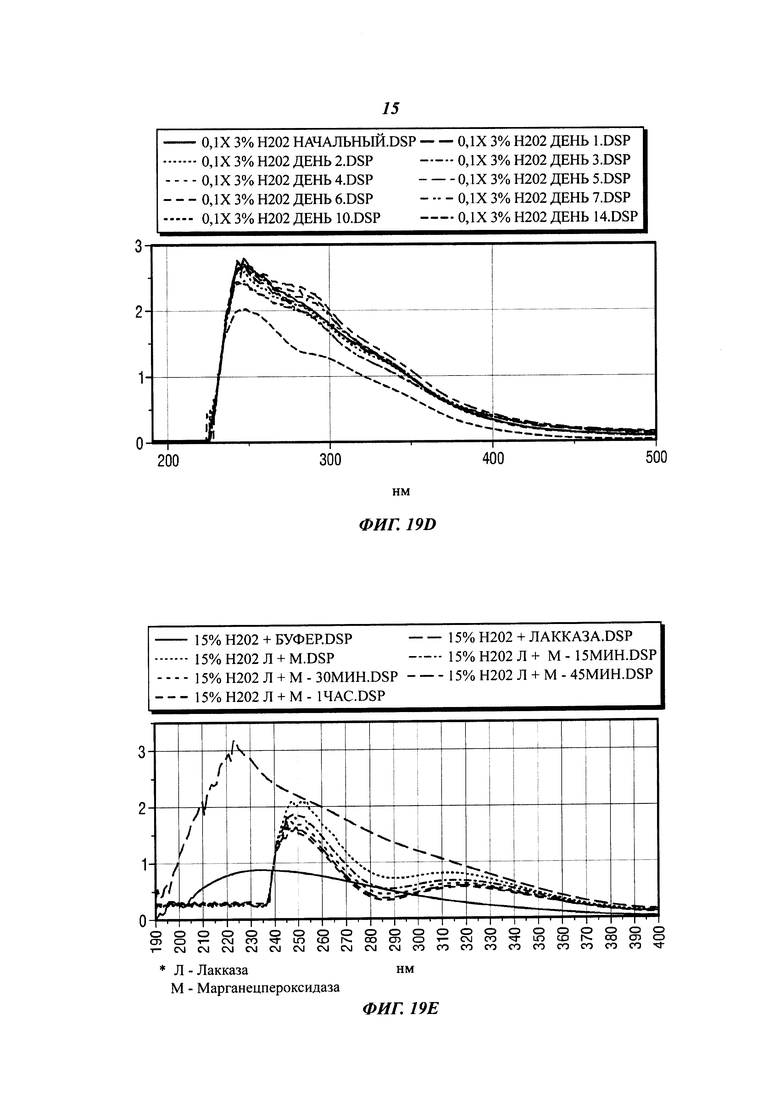
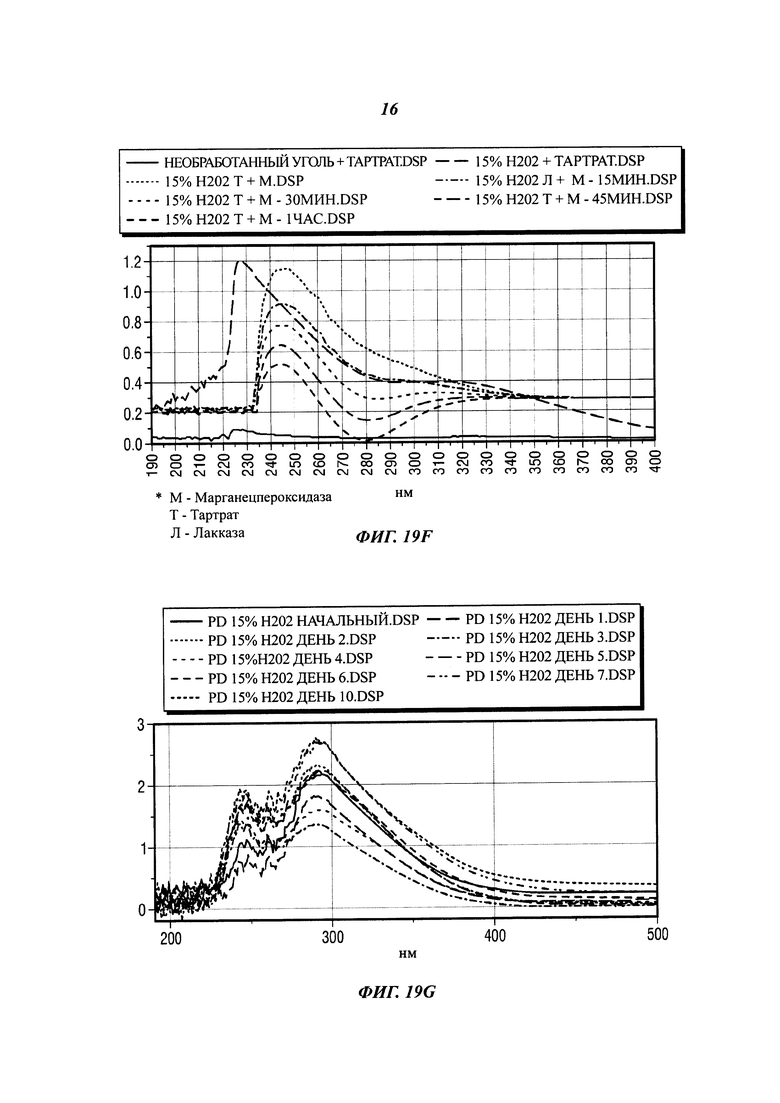
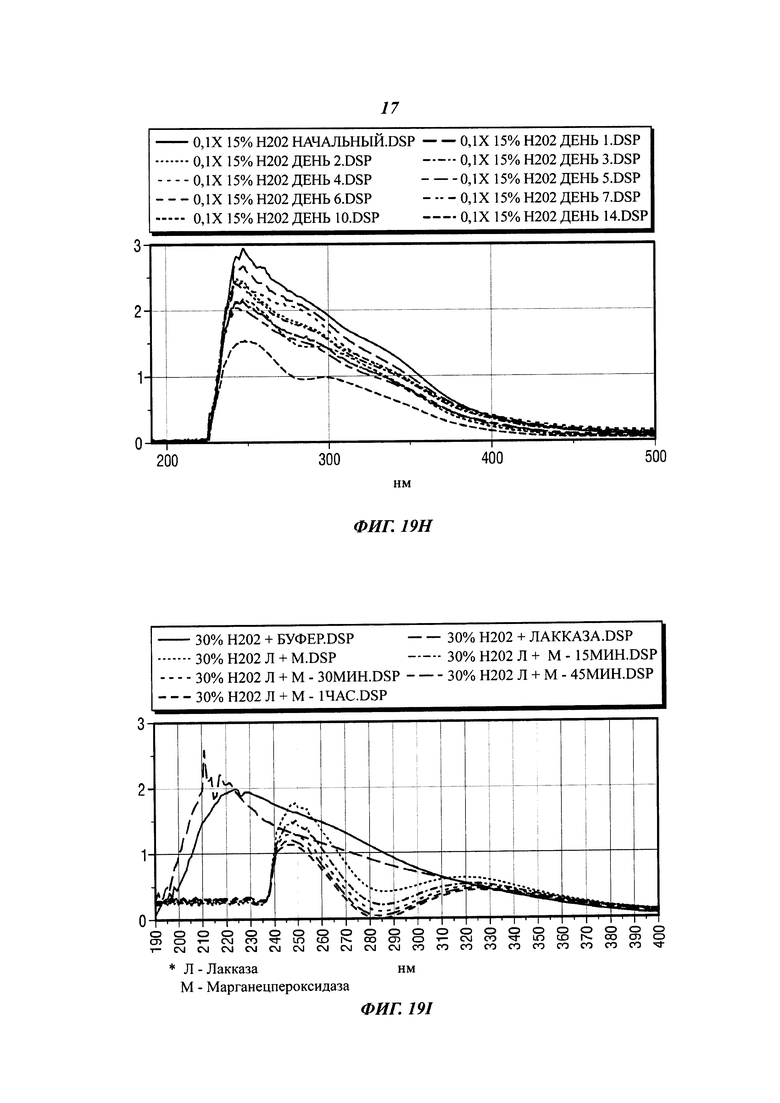
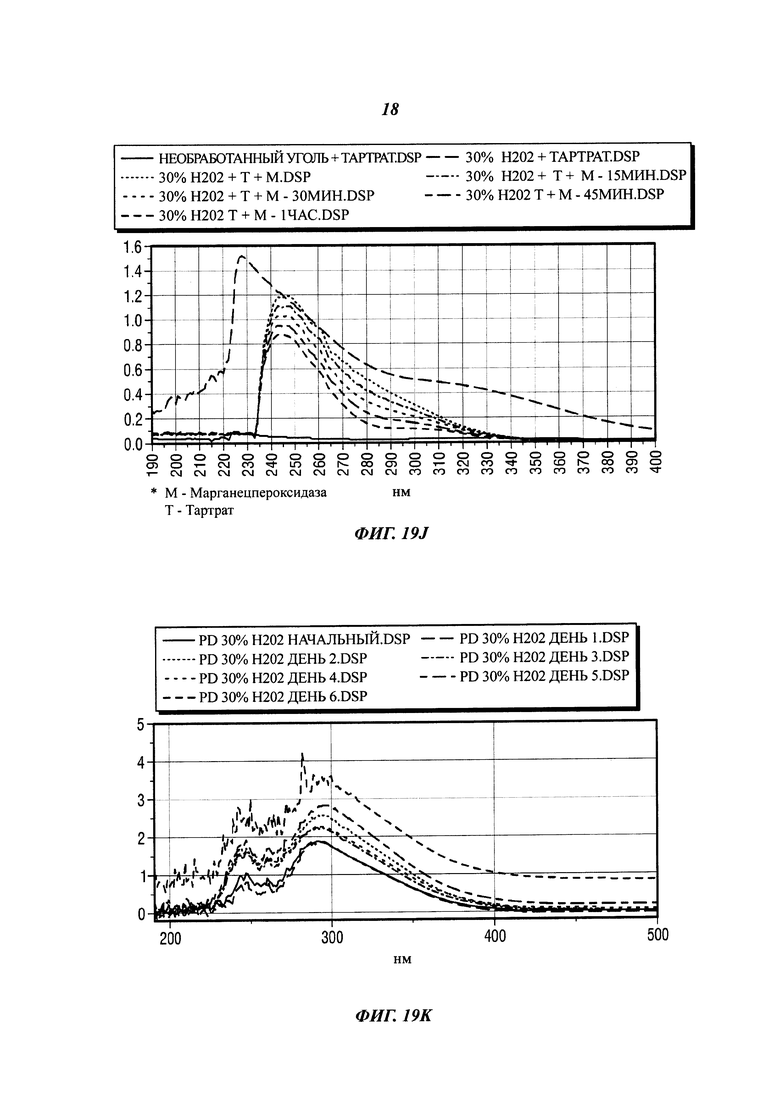
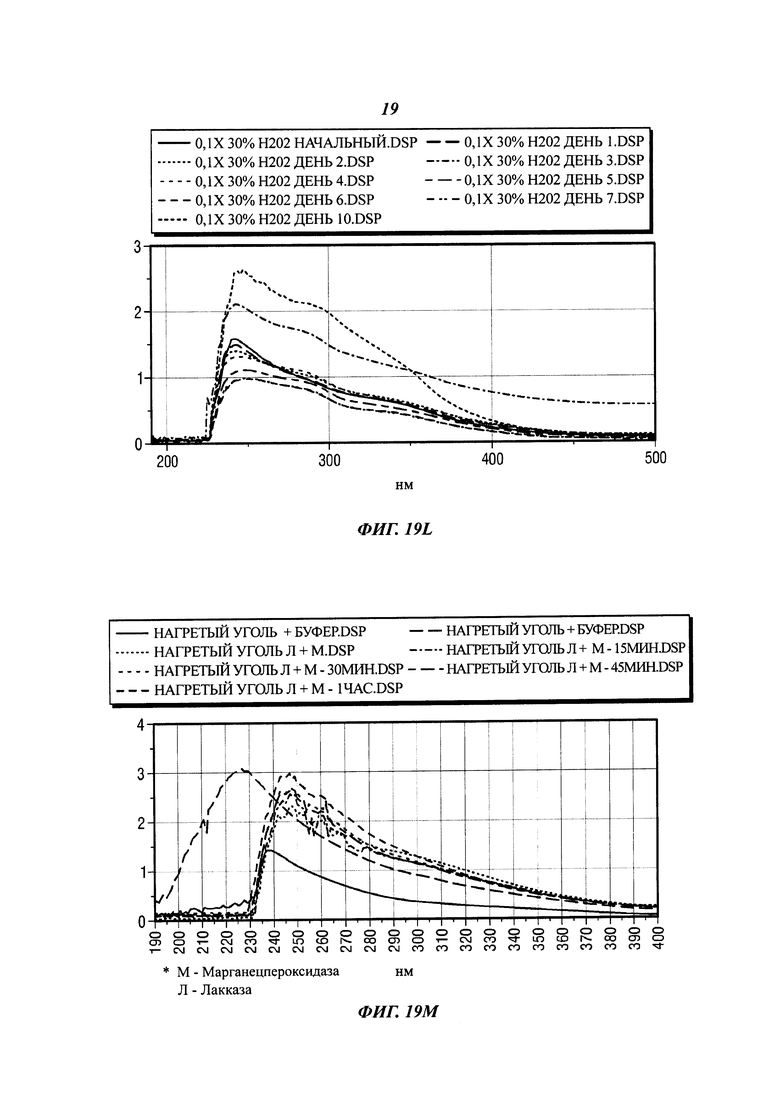
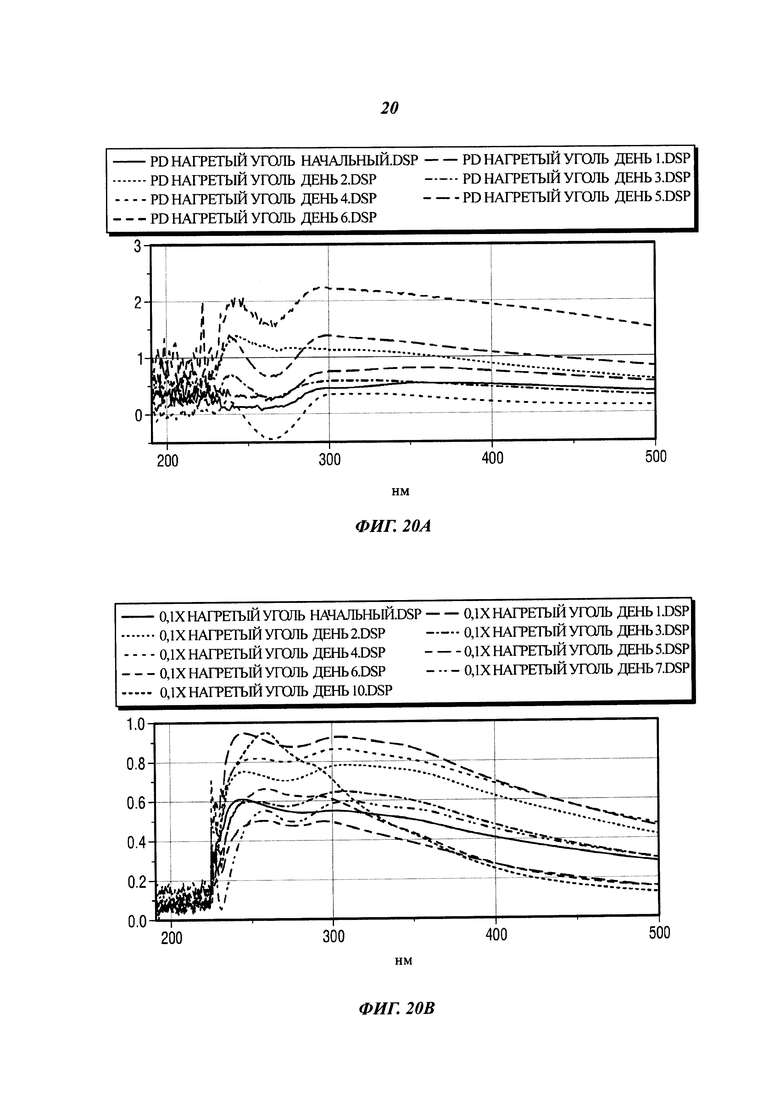
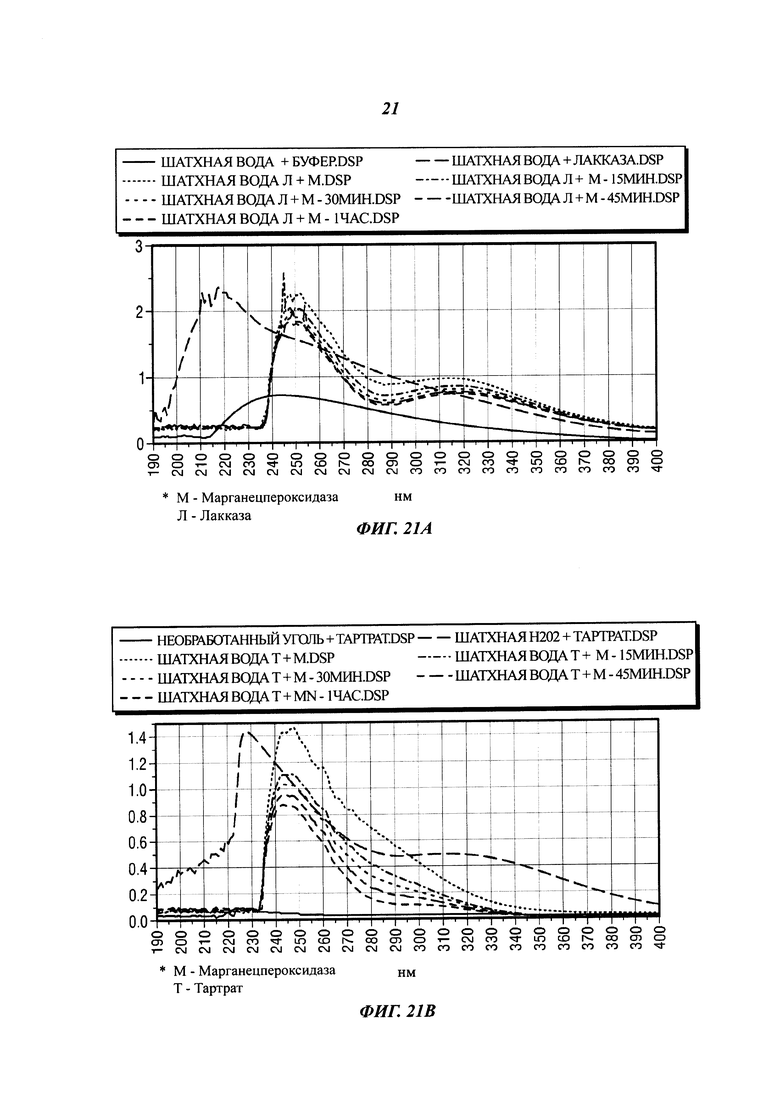
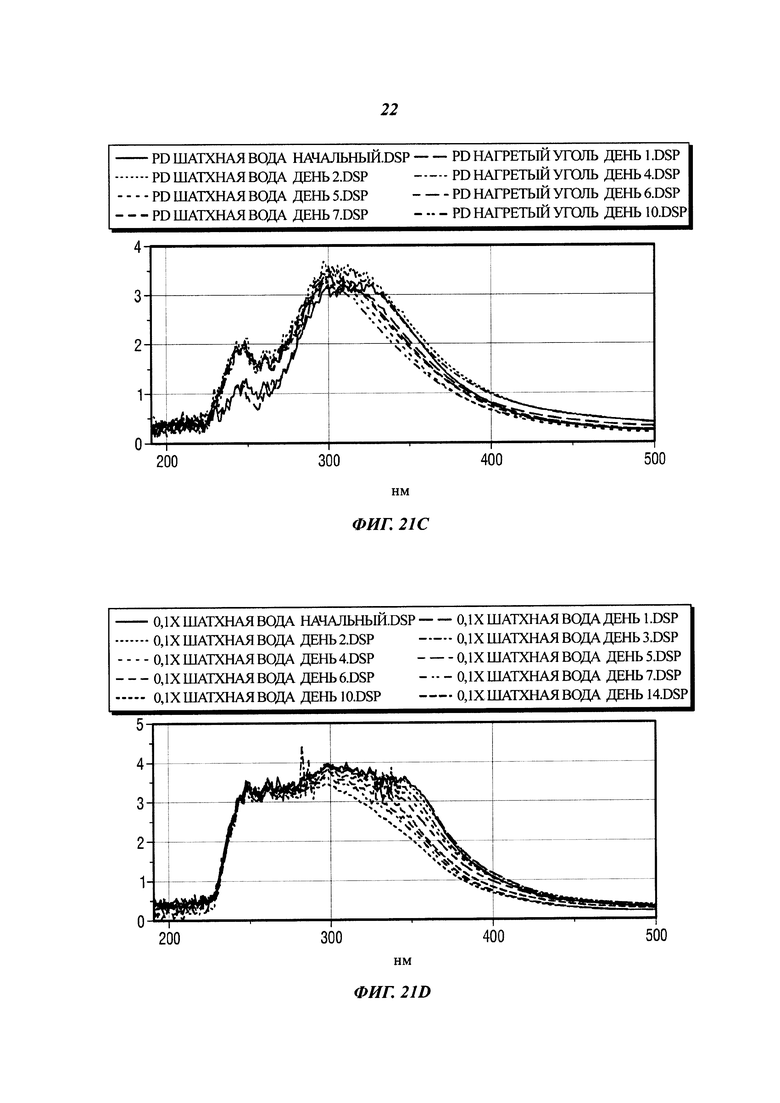
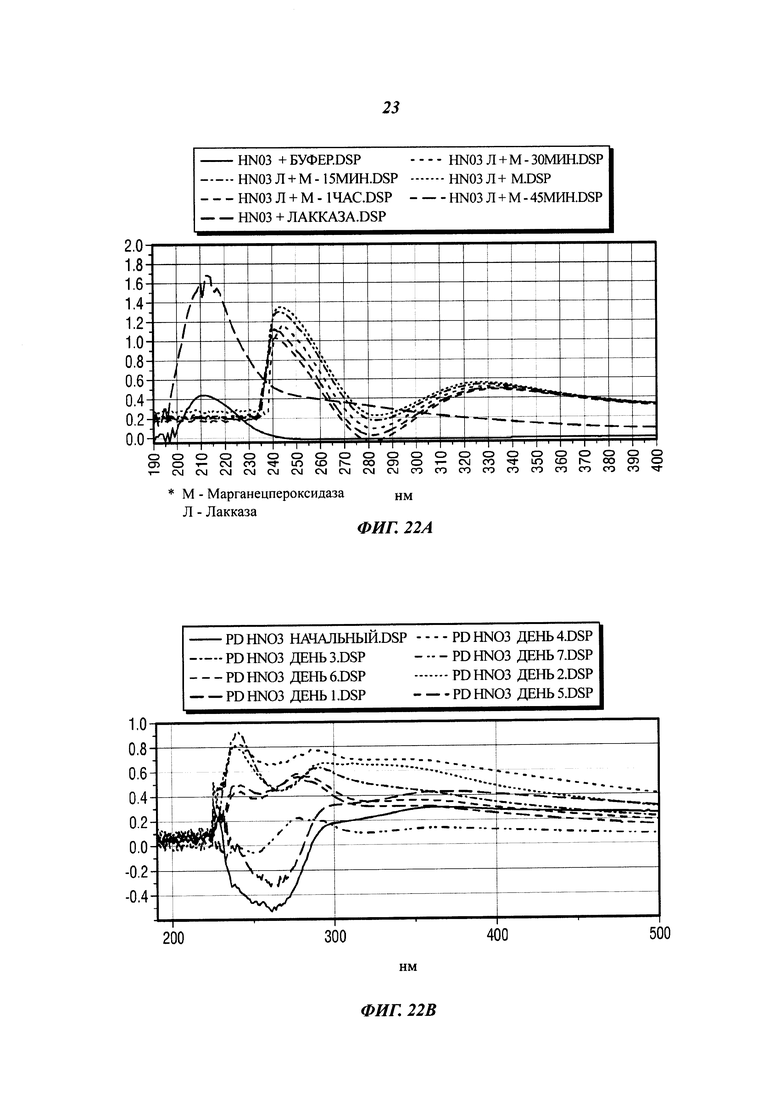
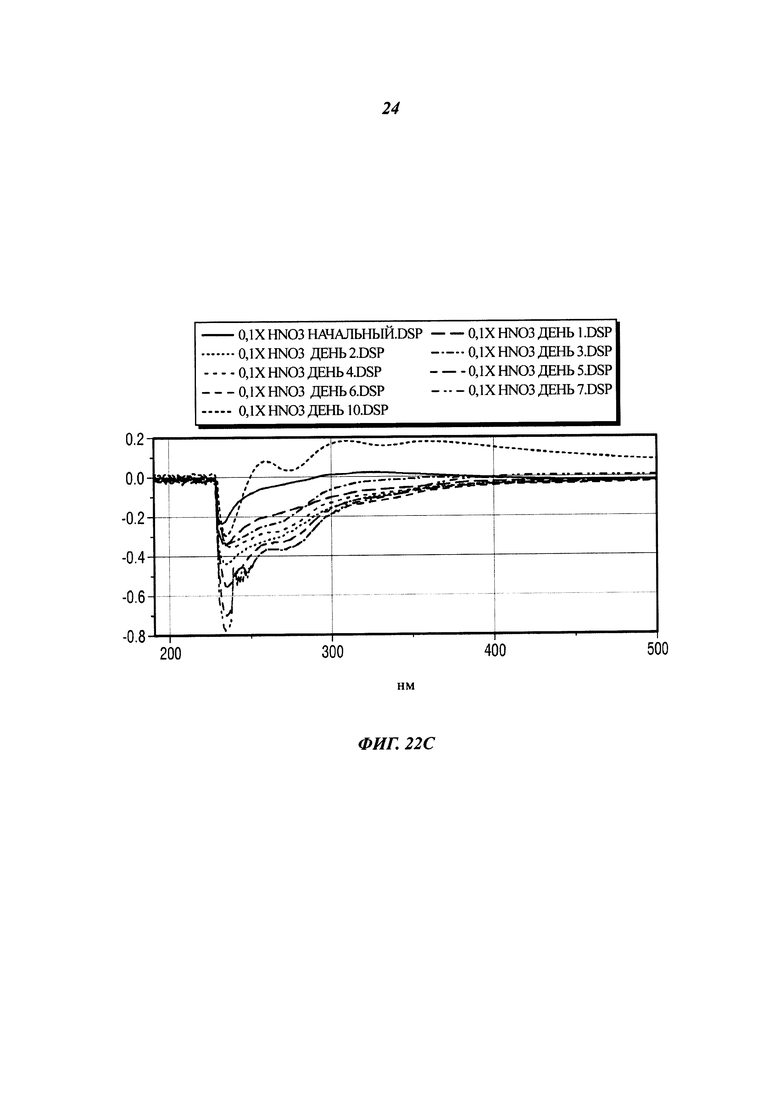
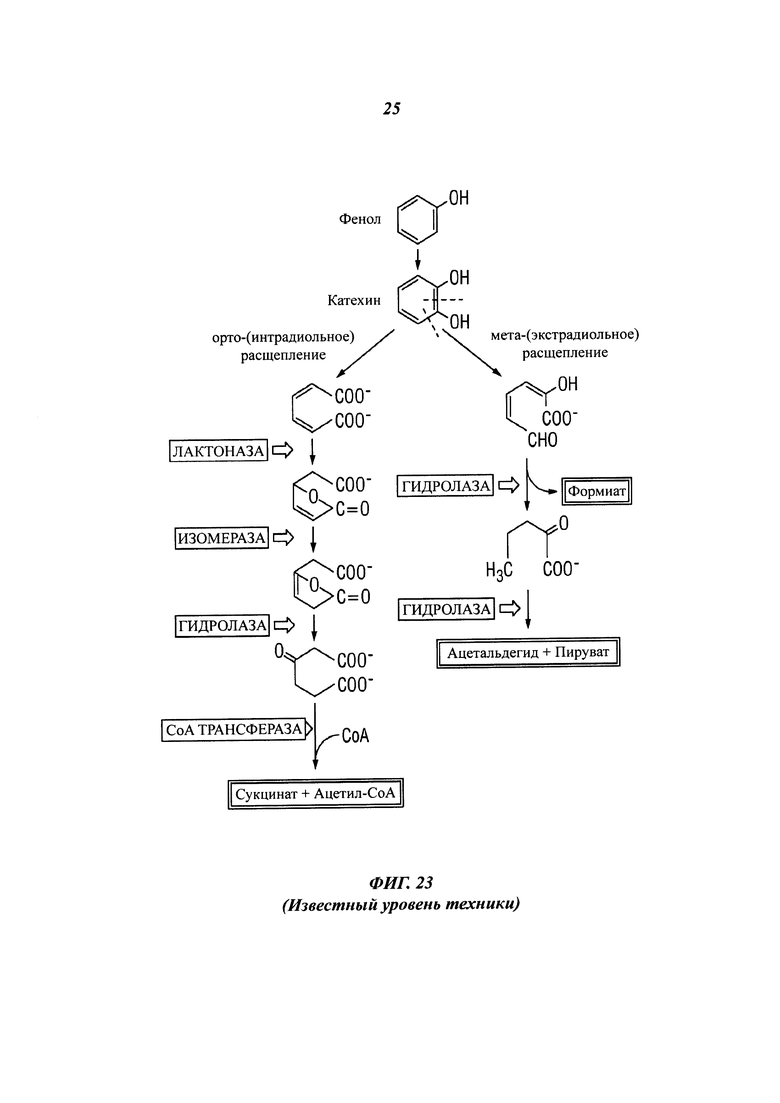
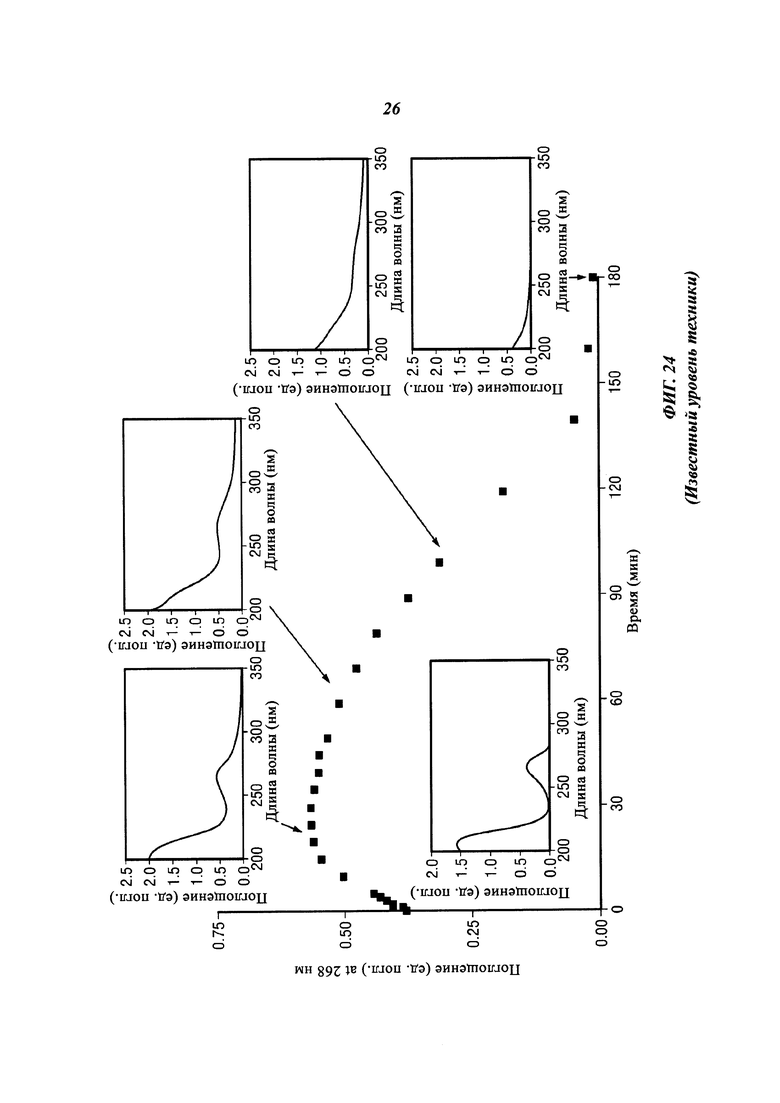
Изобретение относится к производству жидких топлив при переработке источника углеводородов. Способ получения жидкого углеводородного продукта включает следующее: измельчают источник углеводородов, где источник углеводородов содержит по меньшей мере одно, выбранное из группы, состоящей из угля, антрацитового угля, битуминозного угля, лигнита, полубитуминозного угля, угля низких сортов, кокса, нефтеносного песка и горючего сланца; предварительно обрабатывают измельченный источник углеводородов, где предварительная обработка измельченного источника углеводородов включает химическую предварительную обработку, тепловую предварительную обработку, окисление источника углеводородов или их комбинацию; солюбилизируют измельченный источник углеводородов, получая суспензию, содержащую участвующие в реакции молекулы источника углеводородов, где солюбилизация измельченного источника углеводородов включает в себя обработку измельченного источника углеводородов с помощью по меньшей мере одного фермента для разрыва поперечных связей в измельченном источнике углеводородов; подмешивают в суспензию биохимический раствор, содержащий по меньшей мере один фермент конверсии, предназначенный для содействия селективной фотофрагментации связей участвующих в реакции молекул источника углеводородов, где по меньшей мере один фермент конверсии содержит марганецпероксидазу; индуцируют фрагментацию участвующих в реакции молекул, получая жидкие углеводороды, с помощью катализируемой ферментом селективной фотофрагментации связей; отделяют жидкие углеводороды от суспензии, причем загрязняющие примеси остаются в суспензии; и обогащают жидкие углеводороды, получая жидкий углеводородный продукт, где жидкий углеводородный продукт содержит по меньшей мере одно, выбранное из группы, состоящей из бензина, дизельного топлива и керосина. Технический результат – расширение ассортимента способов производства жидких топлив и обеспечение меньшей энергоемкости. 12 з.п. ф-лы, 44 ил., 1 табл.
1. Способ получения жидкого углеводородного продукта, включающий следующее:
измельчают источник углеводородов, где источник углеводородов содержит по меньшей мере одно, выбранное из группы, состоящей из угля, антрацитового угля, битуминозного угля, лигнита, полубитуминозного угля, угля низких сортов, кокса, нефтеносного песка и горючего сланца;
предварительно обрабатывают измельченный источник углеводородов, где предварительная обработка измельченного источника углеводородов включает химическую предварительную обработку, тепловую предварительную обработку, окисление источника углеводородов или их комбинацию;
солюбилизируют измельченный источник углеводородов, получая суспензию, содержащую участвующие в реакции молекулы источника углеводородов, где солюбилизация измельченного источника углеводородов включает в себя обработку измельченного источника углеводородов с помощью по меньшей мере одного фермента для разрыва поперечных связей в измельченном источнике углеводородов;
подмешивают в суспензию биохимический раствор, содержащий по меньшей мере один фермент конверсии, предназначенный для содействия селективной фотофрагментации связей участвующих в реакции молекул источника углеводородов, где по меньшей мере один фермент конверсии содержит марганецпероксидазу;
индуцируют фрагментацию участвующих в реакции молекул, получая жидкие углеводороды, с помощью катализируемой ферментом селективной фотофрагментации связей;
отделяют жидкие углеводороды от суспензии, причем загрязняющие примеси остаются в суспензии; и
обогащают жидкие углеводороды, получая жидкий углеводородный продукт, где жидкий углеводородный продукт содержит по меньшей мере одно, выбранное из группы, состоящей из бензина, дизельного топлива и керосина.
2. Способ по п. 1, в котором измельчение источника углеводородов включает в себя раздробление источника углеводородов.
3. Способ по п. 2, в котором раздробление включает в себя размалывание.
4. Способ по п. 2, в котором раздробление включает в себя гидротермальную обработку под давлением.
5. Способ по п. 1, в котором подмешивание биохимического раствора включает в себя подмешивание по меньшей мере одного дополнительного фермента для конверсии источника углеводородов в более низкомолекулярные углеводороды.
6. Способ по п. 1, в котором отделение жидких углеводородов включает в себя процесс осаждения суспензии из жидкого углеводорода.
7. Способ по п. 1, в котором отделение жидких углеводородов включает в себя процесс осаждения загрязняющих примесей из жидкого углеводорода.
8. Способ по п. 1, в котором обогащение жидкого углеводорода включает в себя подмешивание к жидкому углеводороду по меньшей мере одного фермента для конверсии низкокачественных фракций в высококачественные фракции.
9. Способ по п. 1, в котором биохимический раствор дополнительно содержит модифицированный фермент.
10. Способ по п. 9, в котором модифицированный фермент содержит генетически модифицированный фермент.
11. Способ по п. 9, в котором модифицированный фермент содержит химически модифицированный фермент.
12. Способ по п. 1, в котором способ осуществляется в пласте (in-situ) в угольной шахте или вне пласта (ex-situ) на добытом угле.
13. Способ по п. 1, в котором обогащение жидких углеводородов включает в себя улучшение качеств жидкого углеводородного продукта до перегонки.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| МИКРОБИОЛОГИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УГЛЕВОДОРОДОВ НЕФТИ И ОТДЕЛЬНЫХ УГЛЕВОДОРОДНЫХ ФРАКЦИЙ ИЗ ТВЕРДЫХ ГОРЮЧИХ ИСКОПАЕМЫХ | 2000 |
|
RU2180919C1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| МНОГОКОМПОНЕНТНАЯ СИСТЕМА ДЛЯ ФЕРМЕНТАТИВНОГО ОКИСЛЕНИЯ СУБСТРАТОВ И СПОСОБ ФЕРМЕНТАТИВНОГО ОКИСЛЕНИЯ | 2000 |
|
RU2224061C2 |
| СПОСОБ ИЗМЕНЕНИЯ, ДЕСТРУКЦИИ ИЛИ ОТБЕЛИВАНИЯ ЛИГНИНА, ЛИГНИНСОДЕРЖАЩЕГО МАТЕРИАЛА ИЛИ ПОДОБНЫХ ВЕЩЕСТВ | 1994 |
|
RU2121025C1 |
Авторы
Даты
2019-03-28—Публикация
2014-12-12—Подача