Предлагаемое изобретение относится к медицине, а именно к хирургии, и может быть использовано для лечения гнойных ран, в частности, гнойных ран после вскрытия клетчаточных пространств при флегмоне шеи и лица, которые имеют сложное топографо-анатомическое строение («карманы», затеки и др.), приводящее к неравномерной смене фаз раневого процесса на разных участках раневой поверхности.
Вопрос о патогенетических принципах лечения гнойных ран относится к одному из важных и интенсивно изучаемых разделов современной гнойной хирургии [1, 2]. Особенно это актуально в лечении пациентов с обширными гнойными поражениями клетчаточных пространств, в частности, флегмонами лица и шеи. В этих случаях положительные результаты в лечении таких больных во многом зависят не только от хирургического (вскрытие, некрэктомия и т.д.), но и от местного лечения самой гнойной раны [3, 4].
Заживление раны - это сложный комплекс реакций, развивающихся в организме в ответ на повреждение тканей. Согласно большинству классификаций [5] в процессе заживления ран различают три фазы:
- Фаза воспаления или гнойно-некротическая фаза (I фаза), характеризующаяся наличием некротических тканей и гнойного содержимого в ране (в среднем 3-5 дней);
- фаза регенерации/грануляции (II фаза) - очищение раны от гнойно-некротического содержимого и образование в ней грануляционной ткани, постепенно восполняющей полость раны (начиная с 6-х суток до 21 дня);
- фаза эпителизации раневой поверхности и реорганизация рубца (III фаза) от 21 дней до 2 лет.
В настоящее время предложено большое количество способов местного лечения, включающих применение повязок из различного материала, пропиток и мазей, обладающих гидрофильными, сорбционными, противомикробными или протеолитическими свойствами, а также с использованием методов лечения, основанных на физических принципах (ультразвук, лазеро-, свето- и магнитотерапия, гипербарическая оксигенация, озонотерапия, активное дренирование и др.). Среди всех предложенных способов применение повязок является более доступным, простым и экономически выгодным лечением гнойной раны, по мнению большинства авторов, раневые покрытия в зависимости от стадии раневого процесса должны соответствовать следующим требованиям [2]:
- поглощать раневое отделяемое, микроорганизмы и токсины;
- обладать антибактериальным действием;
- поддерживать оптимальную среду в ране путем водо-, воздухо- и теплообмена между раной и внешней средой;
- изолировать рану от внешней среды, предотвращая реинфицирование;
- не вызывать травматизацию подлежащих тканей;
- активно стимулировать процессы заживления раны.
Широко известны способы лечения гнойных ран с учетом фаз раневого процесса, включающие хирургическую обработку раневой поверхности и последующее наложение на раневую поверхность марлевых повязок, пропитанных лекарственными средствами. При этом, в гнойно-некротическую фазу (I фазу) применяют препараты, обладающие дегидратационными, антимикробными, некролитическими, сорбционными свойствами («Левомеколь», «Левосин», «Диоксиколь», «Бетадин» и др.), а в фазы регенерации и эпителизации - препараты трофического, стимулирующего регенерацию, антиадгезивного действия, поддерживающие влажность в ране (метилурациловая мазь, «Эксальб», «Метилдоксициллин» и др.) [6]. Однако, применение таких традиционных повязок (марлевых, синтетических) имеет ряд недостатков:
- повязки быстро высыхают, прилипают к ране;
- снятие повязки травмирует подлежащие ткани и вызывает выраженную болезненность;
- необходимость частых повторных перевязок, либо постоянного орошения повязки раствором антисептика.
Известен способ лечения гнойных ран по патенту РФ №2466720, заключающийся в том, что вначале гнойник вскрывают хирургическим путем и выполняют хирургическую обработку раневой поверхности, а в последующем проводят перевязки с лекарственными средствами, накладывая на раневую поверхность повязку, пропитанную мазью следующего состава: кремний органический глицерогидрогель - 95,25%, ципрофлоксацин - 0,2%, окситоцин - 4,35%.
Используя этот способ лечения, удается за счет потенцирования антиперсистентного и регенеративного действия препаратов предотвратить возникновение персистирующей инфекции и ускорить регенеративные процессы во II и III фазах раневого процесса.
Недостатками данного способа лечения являются:
- сложное приготовление повязок, требующих пропитывания повязочного материала дозированными смесями лекарственных средств;
- необходимость частых повторных перевязок, либо постоянного орошения повязки раствором антисептика;
- отсутствие сорбционной способности по отношению к раневому отделяемому;
- использование для лечения традиционных марлевых повязок с присущими им недостатками в виде быстрого высыхания, прилипания к раневой поверхности;
- болезненность и травматизация раневой поверхности при снятии;
- применимость только для одной фазы раневого процесса.
Важной же особенностью обширных гнойных процессов, к которым относят флегмоны лица и шеи является то, что в силу обширности распространения, сложной топографии (варьирующая глубина поражения, наличие труднодоступных полостей, «карманов» и складок), неравномерности воспалительных изменений в разных местах поражения, воспалительные и восстановительные раневые процессы не имеют строгой последовательности и протекают одновременно на разных участках раны, накладываясь один на другой [7].
Большинство современных способов лечения не учитывают этой особенности, основываясь на представлении о дискретной смене фаз (I, II и III) в течение раневого процесса.
Таким образом, учитывая одновременное существование процессов воспаления и регенерации в разных участках раны, способ местного лечения гнойных ран должен предусматривать одновременное применение лекарственных средств, воздействующих на все фазы раневого процесса (воспаления, репарации, эпителизации и реорганизации).
Таким образом разработка способа лечения, учитывающего указанные выше особенности течения обширных и сложных ран является актуальным, перспективным и рациональным направлением в гнойной хирургии.
Наиболее близким аналогом является способ лечения гнойных ран по патенту РФ 2185781, который заключается в одновременном осуществлении дегидратационного, неполитического, антимикробного, трофического, антиадгезивного и обезболивающего воздействия на гнойную рану с учетом характера раны и фазности раневого процесса имеющимися в производстве и доступными лекарственными средствами. Эта задача решается тем, что в первой фазе раневого процесса до и после операции на раневую поверхность накладывают многослойную медицинскую марлевую повязку с комбинированными лекарственными средствами, где I-й слой пропитан протеолитическим ферментом, растворенным в 30%-ном водном растворе мочевины, II-й слой - многокомпонентной мазью на водорастворимой основе, III-й слой полностью гидрофобизированной нафталанной мазью, а во второй фазе - осуществляют свободную кожную пластику или накладывают вторичные швы с дренированием остаточной полости с использованием 30% водного раствора мочевины.
Способ по прототипу осуществляют следующим образом. В первой фазе раневого процесса, до и после вторичной хирургической обработки гнойной раны, когда одномоментно закрыть ее не представляется возможным, или при наличии противопоказаний, на раневую поверхность накладывают многокомпонентную трехслойную медицинскую марлевую повязку с комбинацией лекарственных средств. Первый слой состоит из марлевых салфеток, смоченных протеолитическим ферментом, в частности террилитином, растворенном в 30%-ном водном растворе мочевины (в концентрации, согласно инструкции - 200 ИЕ террилитина на 10 мл 30% водного раствора мочевины). Второй слой повязки из марлевых салфеток пропитывают подогретой до жидкого состояния многокомпонентной мазью на водорастворимой основе (левонорсин, левомеколь, левосин, мафенид-ацетат и т.д.) и накладывают его на первый слой повязки. Наружный, т.е. третий слой из марлевых салфеток предварительно гидрофобизируют нафталанной мазью, или какой-либо другой гидрофобной мазью на масляной основе, например, мазью Вишневского. Лечение продолжают до полного очищения раневой поверхности от некротических тканей, купирования явлений острого воспалительного процесса. Во второй фазе раневого процесса осуществляют кожную пластику или накладывают вторичные швы на гранулирующую рану с последующим ирригационным дренированием остаточной раневой полости 30% водным раствором мочевины.
Однако, данный способ имеет следующие недостатки:
- обеспечивает распределение компонентов лишь по глубине раны, что делает эффективным его применение лишь для ран простой конфигурации, где смена фаз процесса происходит по глубине, т.е. от дна раны к поверхности;
- не учитывает особенности ран, имеющих участки замедленной смены раневых фаз (например, раны со сложной топографией, поражением затеками поверхностных и глубоких фасциальных футляров, наличием труднодоступными «карманов» и затеков, локальными различиями кровоснабжения, неравномерным по глубине и выраженности некротическим или воспалительным поражением), в которых неизбежно разные участки поверхности раны будут находиться в разных фазах раневого процесса;
- необходимость ручного приготовления повязок из различных компонентов, что повышает трудоемкость и делает невозможным их стандартизацию;
- использование для лечения традиционных марлевых повязок с присущими им недостатками (прилипание к поверхности раны, травматичность, болезненность при снятии, необходимость частой смены.
Для успешного лечения обширных гнойных ран все шире и шире используют биологически активные раневые покрытия, обладающие разнонаправленным действием и обеспечивающие комплексное аппликационно-сорбционное, антибактериальное и репаративное воздействие [1, 2]. В настоящее время широко распространены повязки «Аквасель Ag+ повязка Гидрофайбер», импрегнированные ионами серебра в виде ленты шириной 2 см и повязка «Аквасель Ag Фоум повязка Гидрофайбер» на пенной основе неадгезивная, с серебром и внутренним абсорбирующим слоем. Данные виды покрытий практически не вызывают травматизацию подлежащих тканей, обладают антимикробным и выраженным абсорбционным свойством, одновременно поддерживая влажную среду в ране. Для стимулирования процессов неоангиогенеза и регенерации гранулирующей раны широко используют гидроколлоидную повязку «Грануфлеке». При этом нигде в доступной нам литературе и рекомендациях производителя мы не встретили метода совместного их применения.
Задачей предлагаемого изобретения является повышение эффективности лечения гнойных ран сложной конфигурации, в том числе с участками, находящимися в разных фазах раневого процесса.
Сущность предлагаемого способа заключается в том, что в глубокие труднодоступные клетчаточные пространства с воспалением I фазы укладывают абсорбирующую повязку в виде ленты «Аквасель Ag+ повязка Гидрофайбер» с абсорбционными, антимикробными, гиперосматическими и протеолитическими свойствами, поверх нее повязку «Аквасель Ag Фоум повязка Гидрофайбер» на пенной основе неадгезивную, с внутренним абсорбирующим слоем, с антимикробными, абсорбирующими, дегидратационными, некролическими, гиперосматическими, протеолитическими свойствами; на участки раны II-III фаз накладывают повязку «Грануфлекс» со стимулирующими, заживляющими, антиадгезивными, гидроколлоидными, трофическими свойствами, при этом повязки меняют через 1-2 дня с обработкой раны раствором хлоргексидина биглюконат 0,02%, причем при очищении раны, выполнении ее грануляционной тканью и появлении краевой эпителизации, последнюю ушивают. Процесс очищения и заживления раны контролируют в динамике с учетом макроскопической картины раны, клинико-лабораторных показателей и с помощью микробиологического, цитологического, морфологического исследований.
Новым в предложении является то, что в отличии от прототипа, в предлагаемом изобретении выделяют участки поверхности раны с разными фазами раневого процесса, определяют их границы, а затем укладывают перевязочные материалы в соответствии с фазой раневого процесса и границами выделенных участков. На участки, находящиеся в I фазе раневого процесса - воспаление накладывают повязки с выраженными абсорбционными, антимикробными, гиперосмотическими и протеолитическими свойствами: «Аквасель Ag+ повязка Гидрофайбер», «Аквасель Ag Фоум повязка Гидрофайбер», а на участки раны, находящиеся во II-III фазе раневого процесса накладывают повязки «Грануфлекс» с выраженными стимулирующими заживление свойствами. Как известно, при очищении раны, выполнении ее грануляционной тканью и появлении краевой эпителизации, последнюю ушивают.
В качестве перевязочных материалов используют современные неприлипающие, атравматические повязки с сорбционными и антимикробными свойствами: «Аквасель Ag+ повязка Гидрофайбер», «Аквасель Ag Фоум повязка Гидрофайбер», гидроколлоидные - «Грануфлекс», которые позволяют поддерживать оптимальную среду в ране, не вызывают травматизацию подлежащих тканей, обеспечивают полную конгруэнтность с раневой поверхностью и не вызывают болевых ощущений у пациентов.
Достигаемый при осуществлении изобретения технический результат состоит в том, что заявляемый способ за счет одновременного, но «адресного» распределения на участках раневой поверхности в соответствии с фазами течения раневого процесса разных по фармакологическому действию повязок, достигают скорейшее «созревание» и переход раны в стадии репарации и эпителизации, предотвращают возникновение персистирующей инфекции и, следовательно, снижают время выздоровления больного. Использование раневых покрытий с различными свойствами, накладываемых дифференцированно и адресно, в зависимости от фазы раневого процесса на каждом из участков неравномерно заживающей раны позволяет поддерживать оптимальную среду в ране, не вызывает травматизацию подлежащих тканей, при этом обеспечивают полную конгруэнтность с раневой поверхностью, не вызывают болевых ощущений у пациентов. Учитывая выраженное антимикробное и абсорбционное свойства раневых покрытий, данный способ обеспечивает эффективное дренирование, снижение микробной обсемененности в ране, более быстрое купирование гнойного воспалительного процесса, ускорение созревания грануляций и эпителизации и позволяет избежать распространение воспалительного процесса на смежные клетчаточные пространства.
После адекватной хирургической обработки, выполняют осмотр всей поверхности раны, обращая особое внимание на выявление «карманов», затеков, «скрытых» полостей и поверхностей, т.е. плохо дренируемых мест, где раневой процесс длительное время сохраняется в фазе воспаления. Определяют расположение и границы участков раневой поверхности, находящихся в разных фазах развития раневого процесса. Визуальный осмотр дополняют цитологическими, морфологическими исследованиями и бактериальными посевами с разных участков раневой поверхности.
После этого покрывают участки повязками, патогенетически обоснованными для лечения соответствующей фазы. На участки раневой поверхности, находящиеся в I фазе (воспаление) накладывают повязки с препаратами, абсорбирующими, дегидратационными, некролитическими и антимикробными свойствами. А участки раневой поверхности, находящиеся во II или III фазе (пролиферации, эпителизации) покрывают повязками с препаратами, трофического, антиадгезивного действия, гидроколлоидными свойствами.
Способ осуществляют следующим образом. После хирургической обработки гнойной раны, флегмоны лица и шеи, в глубокие, труднодоступные клетчаточные пространства лица и шеи (I фаза раневого процесса) укладывают абсорбирующую повязку в виде ленты с серебром «Аквасель Ag+ повязка Гидрофайбер», поверх нее накладывают «Аквасель Ag Фоум повязка Гидрофайбер» на пенной основе, не адгезивная, с серебром, с внутренним абсорбирующим слоем, с антимикробными, абсорбирующими, дегидратационными, некролическими, гиперосматическими, протеолитическими свойствами. При появлении участков грануляций, краевой эпителизации (II, III фазы раневого процесса) для стимулирования процессов неоангиогенеза и регенерации, поверхность этих участков покрывают гидроколлоидными повязками «Грануфлекс» со стимулирующими, заживляющими, антиадгезивными, гидроколлоидными, трофическими свойствами, в то время как на участках, где продолжается процесс очищения раны от некротизированных тканей и экссудация (I фаза раневого процесса) продолжают использовать повязки, содержащие серебро «Аквасель Ag + повязка Гидрофайбер». Перевязки производят один раз в 1-2 дня с предварительной обработкой раны раствором хлоргексидина биглюконат 0,02%. При очищении раны, выполнении ее грануляционной тканью и появлению краевой эпителизации последнюю ушивают.
Заявителями проведено лечение 40 больных с флегмонами лица и шеи в возрасте от 20 до 50 лет, с вовлечением в гнойно-воспалительный процесс 3 и более клетчаточных пространств без тяжелой сопутствующей патологии.
Для оценки эффективности использования комбинации раневых покрытий, проводили рандомизированное исследование пациентов, разделенных случайным образом на 2 группы:
I группа - основная, 20 человек с флегмонами лица и шеи, которым после хирургической обработки флегмоны, в глубокие, труднодоступные клетчаточные пространства лица и шеи укладывали абсорбирующую повязку «Аквасель Ag + повязка Гидрофайбер», импрегнированную ионами серебра в виде ленты шириной 2 см. Поверх нее накладывали «Аквасель Ag Фоум повязка Гидрофайбер» на пенной основе, не адгезивную, с серебром, с внутренним абсорбирующим слоем. При очищении раны и появлении грануляций, для стимулирования процессов неоангиогенеза и регенерации, на гранулирующую поверхность раны накладывали стерильную гидроколлоидную повязку «Грануфлекс», а на участках, где продолжался процесс очищения раны от некротизированных тканей и экссудация, продолжали использовать повязки, содержащие серебро «Аквасель Ag + повязка Гидрофайбер». Перевязки производили в фазу экссудации 1 раз в сутки, в фазу регенерации один раз в 1-2 дня с обработкой раны раствором хлоргексидина биглюконат 0,02%.
II группа - сравнения, 20 человек с флегмонами лица и шеи, которым после хирургической обработки и дренирования флегмоны, послеоперационную гнойную рану ежедневно обрабатывали не менее 2 раз в сутки раствором хлоргексидина биглюконат 0,02%, с наложением повязки с мазью «Левомеколь».
Больные обеих групп получали адекватное антибактериальное, противовоспалительное и дезинтоксикационное лечение.
Для оценки динамики гнойного раневого процесса и общего состояния больных, изучали ряд клинических признаков: сроки очищения раны, появление грануляций, эпителизации, сроки наложения вторичных швов, длительность пребывания в стационаре, «синдром системного воспалительного ответа» (ССВО), который включает следующие симптомы - частоту дыхания, частоту пульса, величину артериального давления, температуру тела, наличие лейкоцитоза или лейкопении с появлением юных форм. Измерение площади воспалительного инфильтрата до начала эпителизации раны проводили по методу В.Я. Кушнира. Оценку лабораторных показателей проводили до операции, на 1-е, 3-е, 5-е, 10-е, 15-е и 20-е сутки и включали исследования: OAК, лейкоцитарного индекса интоксикации (ЛИИ), С-реактивного белка. Динамику микробиологической обсемененности раны оценивали в день оперативного лечения, на 5-е и 8-е сутки после вскрытия флегмоны. Так же проводили цитологическую (в день оперативного лечения, на 3-тьи, 5-е, 7-е, 10-е, 15-е сутки) и морфологическую оценку заживления раны (в день оперативного лечения, на 3-тьи, 5-е, 7-е, 10-е, 13-е и 15-е сутки лечения). Статистическая обработка данных проведена с использованием параметрических и непараметрических методов статистики. Достоверными признаны различия при р<0,05.
Общее состояние пациентов в момент госпитализации было расценено как тяжелое и крайне тяжелое. Эндогенная интоксикация по показателям лейкоцитарного индекса интоксикации (ЛИИ) соответствовала 6,7± 0,96 ед. у 92% (37 больных), а у 8% (3 больных) ЛИИ (лейкоцитарный индекс интоксикации) достигал 9,4±0,67, что свидетельствовало о значительной степени выраженности эндогенной интоксикации при наличии бактериального инфекции. Тяжесть ССВО (синдром системного воспалительного ответа) у всех пациентов при поступлении соответствовала «тяжелой», температура тела достигала 39,6±0,4 С0, тахикардия 109±1,6 уд в мин, ЧДД>16 в мин, лейкоцитоз 21,6±6,8×109, отмечалась лимфопения - 0,5±0,1%, количество сегментоядерных лейкоцитов - 9,5±3,6%. Локально определяли плотный и резко болезненный инфильтрат, зачастую не имеющий четких границ, во всех случаях отмечалось наличие симптома флюктуации, а у 36% больных - симптом крепитации (при анаэробной инфекции). Кожные покровы над инфильтратом были гиперемированы, кожа в складку не собиралась. При вскрытии и ревизии гнойного очага отмечалось обильное гнойное отделяемое.
При анализе динамики лабораторных показателей были отмечены значительные различия в исследуемых группах. Достоверно уже к 3 суткам после оперативного вмешательства у пациентов основной группы отмечалось снижение общего количества лейкоцитов и палочкоядерных нейтрофилов с увеличением общего количества лимфоцитов. С-реактивный белок достигал нормальных значений к 10 суткам. У больных группы сравнения положительная динамика лабораторных показателей наблюдали лишь на 5 сутки, а у 2 пациентов наблюдалось распространение гнойно-воспалительного процесса на смежные клетчаточные пространства со значительными ухудшениями общего состояния и лабораторных показателей, число лимфоцитов -менее 0,5, снижение тромбоцитов - менее 50×109, что свидетельствовало о развитии септического состояния.
Клинический анализ крови с подсчетом лейкоцитарного индекса интоксикации (ЛИИ), биохимические показатели крови, коагулограмма в динамике не выявили статистически достоверных различий в группах. В основной группе по сравнению с группой сравнения, получавшей традиционную терапию, достоверно отмечалась более быстрая нормализация показателей крови.
Анализ данных, полученный при лечении больных с флегмонами лица и шеи, показал, что между группами имелись достоверные различия в клиническом течении гнойно-воспалительного процесса. На фоне проводимой терапии у больных основной группы к 5 суткам от начала лечения температура тела нормализовалась, а в группе сравнения нормализация температурной кривой наступало только на 7 сутки (р<0,05), сроки купирования болевого синдрома в основной группе отмечалось на 4,24±0,12, а в группе сравнения к 5,62±0,26 (р<0,05). Сроки окончания экссудации у больных I группы составили 6,74±1,10, в отличии от пациентов II группы - 10,81±1,3 (р<0,03), появление грануляции наступало на 5,60±1,1 и на 10,46±0,98 соответственно (р<0,05). Сроки наложения вторичных швов составляли у основной группы 10,6±1,4 сутки, в группе сравнения - 14,4±1,30 сутки (р<0,05). Количество дней в стационаре составило 15,26±2,62 в основной группе, а в группе сравнения 21,64±2,89 суток (р<0,03).
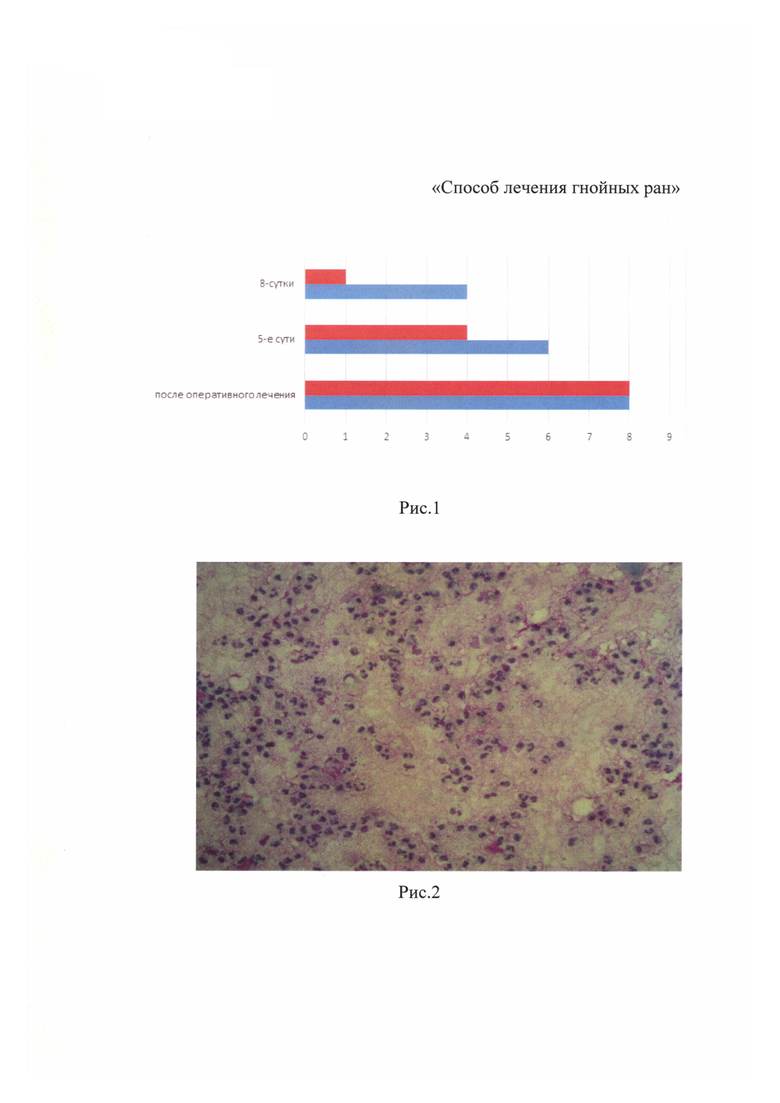
Количественная обсемененность в ране после оперативного лечения варьировала от 106 до 108 КОЕ, у 93% больных составляла 108 КОЕ. В основной группе на фоне применения комбинации повязок «Аквасель Ag + повязка Гидрофайбер», «Аквасель Ag Фоум повязка Гидрофайбер» и «Грануфлекс», на 5-е сутки микробная обсемененности достоверно снижалась до 104 КОЕ, микробиологический пейзаж представлен условно патогенной аэробной и факультативно-анаэробной микрофлорой. Выявлено, что на 8-е сутки у 76% пациентов наблюдалась полная деконтоминация, у остальных больных обнаруживались лишь единичные колонии. В группе сравнения выявлено снижение микробной обсемененности исследуемого материала доЮ4 КОЕ лишь к 8 суткам. Комбинация покрытий «Аквасель Ag + повязка Гидрофайбер», «Аквасель Ag Фоум Гидрофайбер» и «Грануфлекс» проявила высокую антибактериальную активность по отношению к грамположительным коккам, грамотрицательным палочкам и условно патогенным анаэробам и частичную эффективность по отношению к S. aureus, Streptococcus spp., Acinetobacter baumannii, Corynebacterium striatum, Streptococcus oralis, Acinetobacter spp. Данные изменения динамики микробиологической обсемененности раневого отделяемого по группам сравнения представлены на рисунке 1. - динамика микробиологической обсемененности раневого отделяемого у больных флегмонами лица и шеи по группам сравнения.
При анализе цитограмм в динамике в 1-е и 3-е сутки у больных обеих групп достоверной разницы в картине мазков-отпечатков не отмечалось, наблюдались массивные скопления детрита и лейкоцитарная реакция, которая соответствовала ранней стадии воспалительного процесса, в мазках преобладали сегментоядерные нейтрофилы.
Начиная с 5 суток у больных основной группы, среди нейтрофилов наблюдалось появление дегенеративно-измененных форм, увеличение количества макрофагов. У пациентов группы сравнения аналогичные изменения происходили лишь на 7-е сутки. В группе с применением раневого покрытия в мазках отпечатках на 7 сутки отмечалось появление фибробластов, что является признаком формирования грануляционной ткани, а к 10 суткам в препаратах наблюдались молодые эпителиальные клетки с базофильной цитоплазмой, что клинически соответствовало появлению краевой эпителизации в ране. В группе сравнения появление фибробластов отмечалось лишь к 10 суткам, молодые эпителиальные клетки с базофильной цитоплазмой обнаруживались к 15 суткам. Результаты цитологического исследования у больных флегмонами лица и шеи показали, что регенераторные процессы в ране на фоне традиционной терапии достоверно наступали в более позднем периоде.
При анализе в динамике гистологических препаратов, в день оперативного лечения у больных обеих групп достоверной разницы в микроскопической картине не отмечалось. Морфологическая картина соответствовала ранней стадии воспалительного процесса, в ране выражен диффузный гнойный воспалительный инфильтрат, детрит из полиморфоядерных лейкоцитов, воспалительный отек окружающих мягких тканей и их расплавление. У больных второй группы аналогичная гистологическая картина сохранялась на 3-е сутки.
У большинства больных первой группы на 3-е сутки в микроскопической картине на фоне гнойно-некротической деструкции мягких тканей отмечалось формирование единичных поверхностных сосудистых петель, что свидетельствует о начале процесса формирования в ране грануляционной ткани. Аналогичная картина у больных второй группы отмечалась к 7-м суткам.
Начиная с 5 суток у больных основной группы, среди лейкоцитарной инфильтрации наблюдалось появление хорошо выраженного поверхностного слоя сосудистых петель грануляционной ткани, а также появление макрофагов и фибробластов, что свидетельствует о формировании молодой грануляционной ткани в ране и о быстром очищении ее. У пациентов группы сравнения аналогичные изменения происходили лишь на 10-е сутки.
В группе с применением раневых покрытий на 7 сутки микроскопическая морфологическая картина соответствовала созреванию грануляционной ткани с хорошо выраженными вертикальными сосудами и клеточными элементами: макрофагами и фибробластами. В группе сравнения созревание грануляционной ткани отмечалось лишь к 15 суткам.
К 10 суткам у пациентов основной группы в гистологических препаратах визуализировалась гомогенизация коллагеновых волокон, появление плазматических клеток в большом количестве. Микроскопическая и клиническая картины соответствовали заполнению всей раневой поверхности зрелой грануляционной тканью в сочетании с краевой эпителизацией. В группе сравнения аналогичная картина появлялась к 15 суткам.
Таким образом, доказана высокая эффективность одновременного «адресного» применения раневых покрытий «Аквасель Ag + повязка Гидрофайбер», «Аквасель Ag Фоум повязка Гидрофайбер» и «Грануфлекс» для лечения I фазы и II фазы раневого процесса в комплексном лечении пациентов с флегмонами лица и шеи. Применение современных раневых покрытия существенно облегчают выполнение перевязок, поскольку легко снимаются с раневой поверхности, не вызывают болевых ощущений и повреждения тканей у пациентов. В тоже время повязки «Аквасель Ag + повязка Гидрофайбер», «Аквасель Ag Фоум повязка Гидрофайбер» обеспечивают эффективное дренирование раны и обладают выраженным антимикробным действием.
Пример. Пациентка Я, 35 лет, находилась на стационарном лечении с диагнозом: Одонтогенная флегмона дна полости рта, крыло-челюстного, окологлоточного пространств справа, шеи.
Жалобы при поступлении: на болезненную припухлость в подчелюстной и подподбородочной областях с обеих сторон, шеи, ограниченное, болезненное открывание рта, боли при глотании справа, повышение температуры тела до 39,0 С.
Из анамнеза: появились боли в разрушенном зубе на нижней челюсти справа, через несколько дней появилась болезненнаяя припухлость, которая увеличивалась, появились боли при глотании справа, последние сутки отмечает болезненное, ограниченное открывание рта. Ранее за медицинской помощью не обращалась, госпитализирована на 7 сутки от начала заболевания.
Объективно: конфигурация лица изменена за счет коллатерального отека мягких тканей нижней зоны лица, шеи, разлитого резко болезненного инфильтрата мягких тканей подчелюстных областей с обеих сторон, подподбородочной области, верхней третьи. Симптом флюктуации положительный. Открывание рта болезненное, ограничено до 1,0 см. В полости рта отек слизистой передней небной дужки, язычка, со смещением последнего, боковой стенки глотки справа. Крыло-челюстная складка, боковая стенка глотки справа гиперемированы, при пальпации плотный, болезненный инфильтрат крыло-челюстной складки справа. 48 коронковаяя часть разрушена, в цвете изменена. В анализах крови лейкоцитоз до 24 *109/л (нейтрофилы 59,80%, лимфоциты 32,70%, моноциты 7,5%). Лейкоцитарный индекс интоксикации (ЛИИ) составил 6,2. Синдром системного воспалительного ответа (ССВО) оценено, как тяжелое.
В день поступления под общим обезболиванием по средствам назо-трахеальной интубации после 3-х кратной обработки операционного поля раствором йодопирон, хлоргексидина биглюконат, произведена экстракция 48 зуба, согласно интраоперационной разметке произведено вскрытие, ревизия, санация флегмоны дна полости рта, крыло-челюстного, окологлоточного пространств справа, шеи. Эвакуировано обильное гнойное отделяемое. Рана обработана раствором хлоргексидина биглюконат 0,02%. Заинтересованные глубокие труднодоступные клетчаточные пространства (находящиеся в I фазе - воспаление) дренированы абсорбирующей повязкой «Аквасель Ag + повязка Гидрофайбер», импрегнированная ионами серебра в виде ленты шириной 2 см. Поверх нее наложена повязка «Аквасель Ag Фоум повязка Гидрофайбер» на пенной основе не адгезивная, с серебром, с внутренним абсорбирующим слоем. Фиксировано бинтом Peha-Haft.
Интраоперационно взят посев, мазок-отпечаток из раны, участок тканей на патогистологическое исследование (ПГИ).
Данные микробиологического исследования: Staphylococcus aureus, Streptococcus anginosus, Streptococcus pyogenes 108 КОЕ.
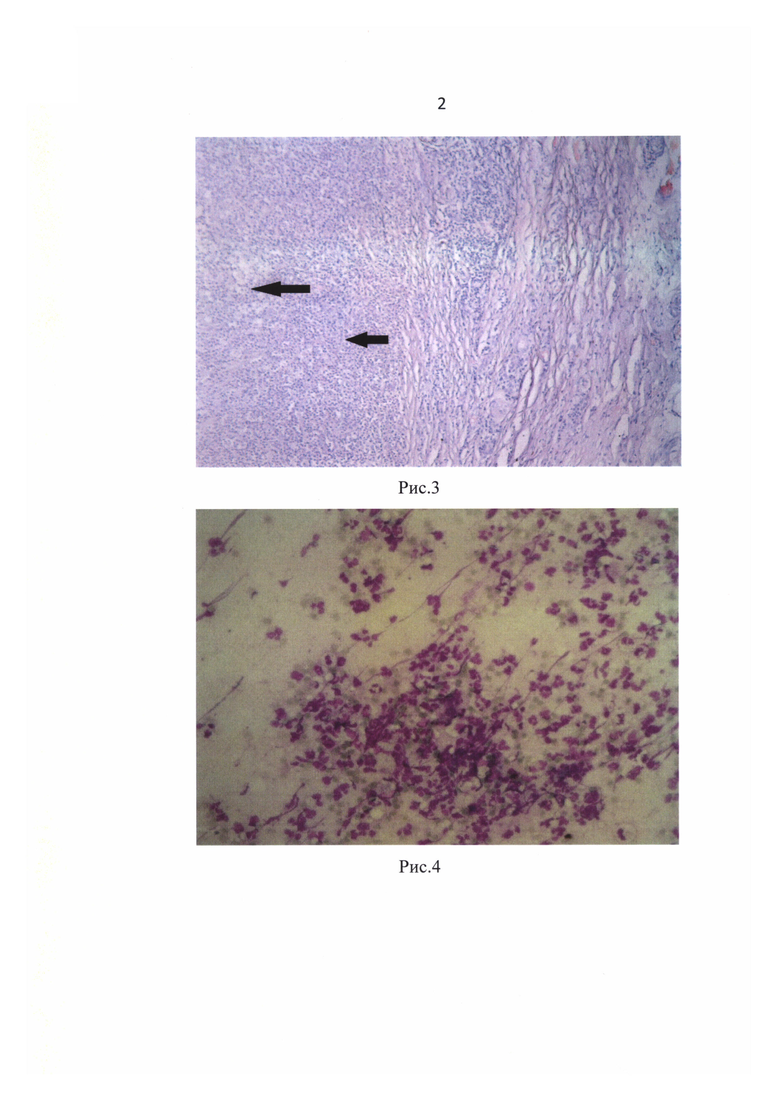
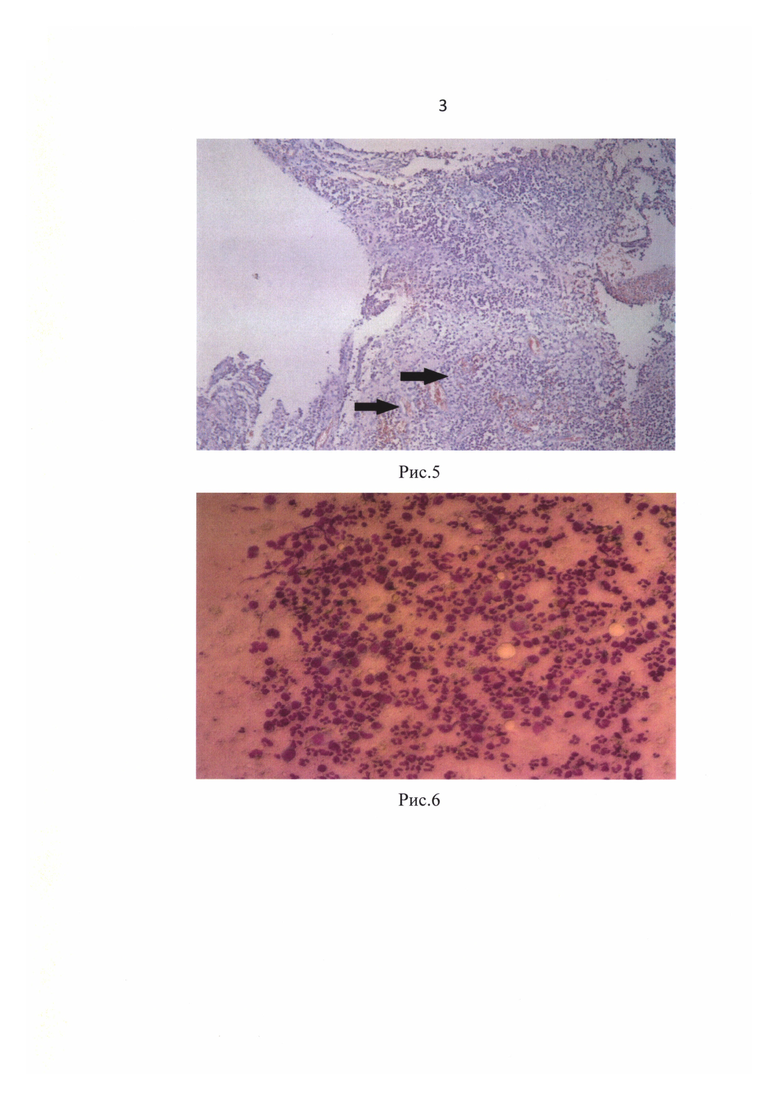
Данные цитологического (рис. 2 - выраженная лейкоцитарная реакция вмазке-отпечатке с раневой поверхности: нейтрофильные лейкоциты. Окраска по Романовскому-Гимзе, об. 20х) и морфологического исследования (рис. 3 - диффузный гнойный воспалительный инфильтрат из полиморфноядерных лейкоцитов с расплавлением мягких тканей. Окраска гематоксилин-эозином, ув. 200х) в день оперативного лечения.
Пациентка получала комплексное медикаментозное лечение. Со вторых суток лечения проводили ежедневные перевязки с раствором хлоргексида биглюконат 0,02% в сочетании с повязками «Аквасель Ag + повязка Гидрофайбер» и «Аквасель Ag Фоум повязка Гидрофайбер».
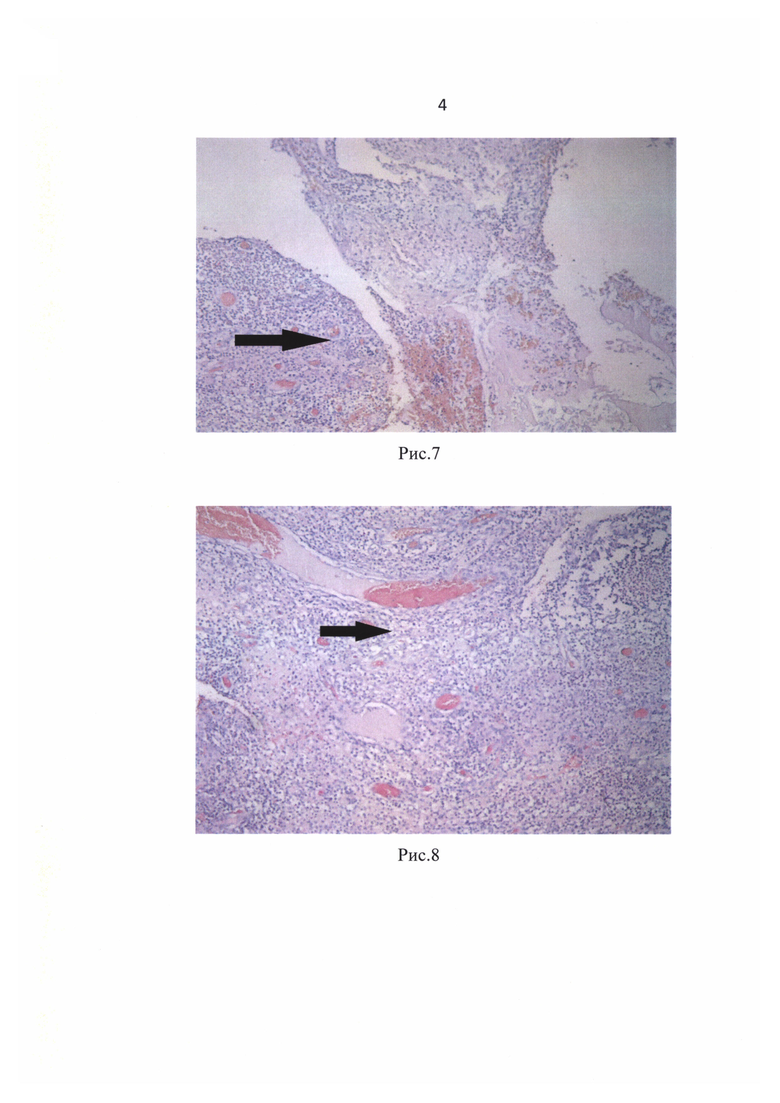
На 3-е сутки отмечена незначительная положительная динамика в общеклинических показателях и локальном статусе больной. Достоверной разницы в картине мазков-отпечатков в сравнении с 1-й сутками не наблюдалось (рис. 4 - дегенеративно измененные формы нейтрофильных лейкоцитов, детрит в мазке-отпечатке с раневой поверхности. Окраска по Романовскому-Гимзе, об. 20х).
В данных морфологического исследования (рис. 5 - на фоне гнойно-некротической деструкции отмечается формирование единичных поверхностных сосудистых петель. Окраска гематоксилин-эозином, ув. 200х).
К 3-м суткам отмечена нормализация температуры тела. В OAК: эритроциты 3,87 *1012 /л, гемоглобин 130 г/л, лейкоциты 8,6* 109 /л, нейтрофилы 64,8%, лимфоциты 19,10%), моноциты 13,2%, эозинофилы 2,9%, лейкоцитарный индекс интоксикации снизился до 0,92. В локальном статусе наблюдали исчезновение инфильтрации мягких тканей, отека, краевой инфильтрации, гиперемии кожных покровов, очищение раны от некротических масс. В ране определяли появления грануляции по периферии раны и сохранение фазы экссудации в области дна раны. Микробная обсемененность достоверно снижена до 104 КОЕ, микробиологический пейзаж представлен Staphylococcus aureus.
Цитологическая (рис. 6 - макрофаги на фоне лейкоцитов в мазке-отпечатке с раневой поверхности у больной с одонтогенной флегмоной дна полости рта, шеи, крыло-челюстного, окологлоточного пространств справа, об. 20х) и морфологическая (рис. 7 - хорошо выраженный поверхностный слой сосудистых петель грануляционной ткани. Окраска гематоксилин-эозином, ув. 200х; рис. 8 - среди рыхловолокнистой соединительной ткани видны скопления макрофагов и молодых фибробластов. Окраска гематоксилин-эозином, ув. 200х) картины на 5-е сутки.
С 5-х суток перевязки проводили 1 раз в 2 суток, рану обратывали раствором хлоргексидина биглюконат 0,02%. На дно раны, где продолжалась I фаза раневого процесса продолжали использовать повязки, содержащие серебро «Аквасель Ag + повязка Гидрофайбер», а на участки, выполненные грануляциями (II фаза раневого процесса), начинали укладывать гидроколлоидную повязку «Грануфлекс».
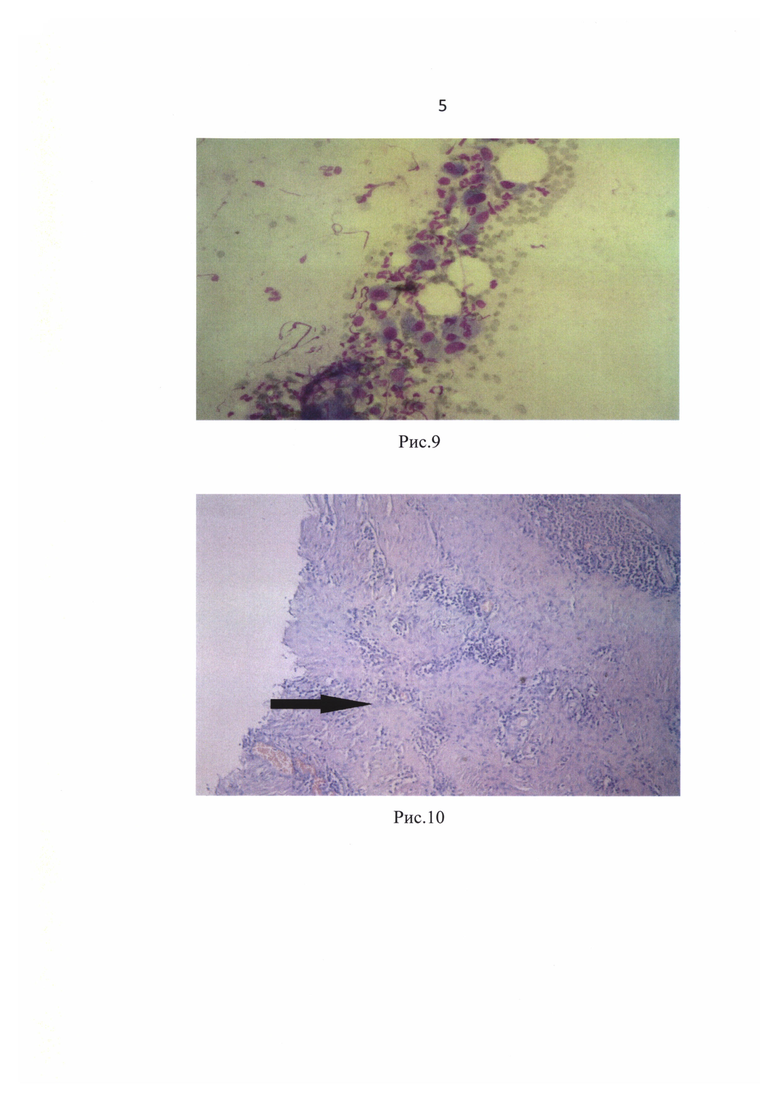
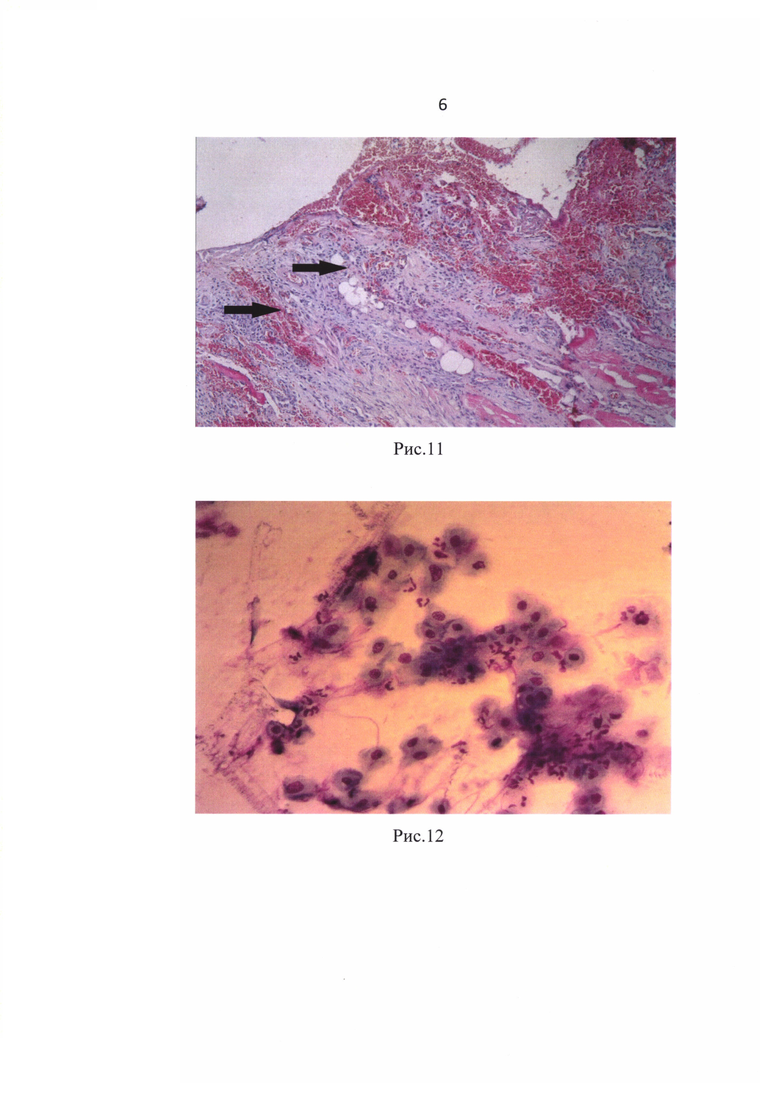
На 7-е сутки положительная динамика локального статуса раны, что отражено в цитологической (рис.9 - фибробласты и нейтрофильные лейкоциты в мазке-отпечатке с раневой поверхности у больных флегмонами лица и шеи, об. 20х) и морфологической картинах (рис. 10 - созревающий слой грануляционной периваскулярной воспалительной лимфо-гранулоцитарной инфильтрацией. Окраска гематоксилин-эозином, ув. 200х; рис. 11 - созревающий слой с пучками горизонтально расположенных фибробластов. Окраска гематоксилин-эозином, ув. 200х).
На 8-е сутки в посеве из раны наблюдали полную деконтоминацию микробной обсемененности.
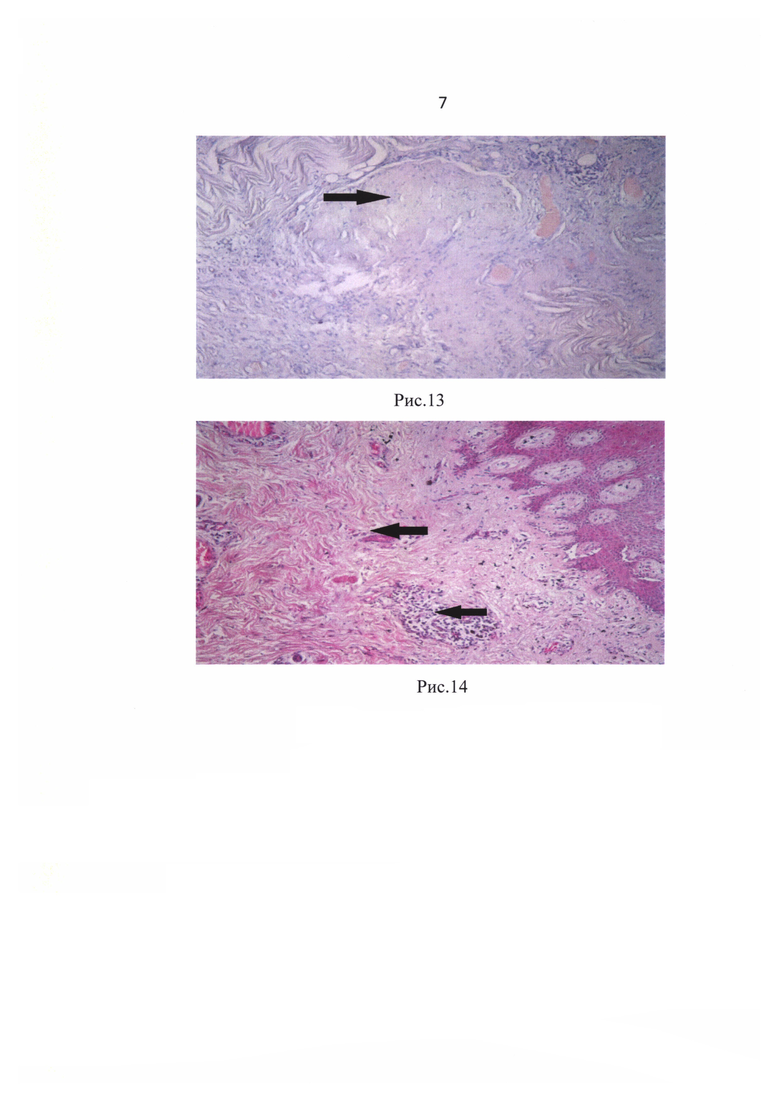
К 10-м суткам рана уменьшилась в размерах, выполнена грануляциями, наблюдалась краевая эпителизация, что подтверждено цитологической (рис.12 - молодые эпителиальные клетки с базофильной цитоплазмой в мазке-отпечатке с раневой поверхности у больной с одонтогенной флегмоной дна полости рта, шеи, крыло-челюстного, окологлоточного пространств справа, об. 20х) и морфологической картинами (рис. 13 - гомогенизация коллагеновых волокон (фиброзный слой). Окраска гематоксилин-эозином, ув. 200х; рис. 14 - формирование краевой эпителизации раны с замещением грубоволокнистым коллагеном дермы. Окраска гематоксилин-эозином, ув. 200х).
Пациентке на 10-е сутки в условиях операционной, под местной инфильтрационной анестезией наложены вторичные швы. Интраоперационно взят мазок-отпечаток и материал на патогистологическое исследование (ПГИ).
Послеоперационный период без осложнений. Пациентка выписана на дальнейшее амбулаторное лечение на 15 сутки.
Литература:
1. Винник Ю.С., Маркелова Н.М., Шишацкая Е.И., Кузнецов М.Н., Соловьева Н.С., Зуев А.П. К вопросу о выборе раневых покрытий в лечении гнойных ран // Фундаментальные исследования. - 2015. - №1-5. - С. 1061-1064.
2. Абаев Ю.К. Перевязочные материалы и средства в хирургии / Ю.К. Абаев // Вестн. хирургии. - 2004. - №3. - С. 83-87.
3. Андреев Д.Ю. Современные раневые покрытия Ч. I / Д.Ю. Андреев, Б.А. Парамонов, A.M. Мухтарова // Вестн. хирургии им. И.И. Грекова. - 2009. - Т. 168, №3. - С. 98-102.
4. Винник Ю.С. Современные методы лечения гнойных ран / Ю.С. Винник, Н.М. Маркелова, B.C. Тюрюмин // Сибирское медицинское обозрение. - 2013. - №1. - С. 18-24.
5. Раны и раневая инфекция. Под ред. М.И. Кузина, Б.М. Костюченко. М., Медицина, изд. 2-е перераб. и доп., 1991. - 608 с.
6. Блатун Л.А. Флегмоны и абсцессы - современные возможности лечения. // Лечащий врач, 2002. - №2. - С. 30-40.
7. Кузнецов Н.А., Никитин В.Г. Щадящие хирургические вмешательства и интерактивные повязки в лечении инфицированных ран. Consilium medicum. Хирургия. 2006; 8; 2.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения ран мягких тканей с использованием измельченных слайсов пантов марала | 2024 |
|
RU2831889C1 |
| Способ лечения гнойных ран | 2021 |
|
RU2775878C1 |
| СПОСОБ ЛЕЧЕНИЯ ГНОЙНЫХ РАН | 2023 |
|
RU2817920C1 |
| СПОСОБ ЛЕЧЕНИЯ ФЛЕГМОН ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ | 2007 |
|
RU2328292C1 |
| Способ лечения одонтогенных флегмон челюстно-лицевой области и устройство для его осуществления | 2024 |
|
RU2829258C1 |
| Способ лечения флегмон шеи в послеоперационном периоде | 2024 |
|
RU2832448C1 |
| СПОСОБ КОМПЛЕКСНОГО ЛЕЧЕНИЯ ФЛЕГМОН ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ СРЕДНЕЙ СТЕПЕНИ ТЯЖЕСТИ | 2007 |
|
RU2320329C1 |
| РАНЕВОЕ ПОКРЫТИЕ | 2006 |
|
RU2314834C1 |
| Способ комбинированного лечения пролежней у пациентов в хроническом критическом состоянии | 2021 |
|
RU2777483C1 |
| КЛЕЙ ХИРУРГИЧЕСКИЙ АНТИСЕПТИЧЕСКИЙ "АРГАКОЛ" | 2005 |
|
RU2284824C1 |
Изобретение относится к медицине, а именно к хирургии, и может использовано для лечения гнойных ран. Для этого в I фазе раневую поверхность покрывают повязкой «Аквасель Ag повязка Гидрофайбер» и «Аквасель Ag Фоум повязка Гидрофайбер» с антимикробными, абсорбционными свойствами, а участки раны во II или III фазе покрывают гидроколлоидными повязками «Грануфлекс». Повязки меняют через 1-2 дня после обработки раны раствором хлоргексидина биглюконат 0,02%, при этом при очищении раны, выполнении ее грануляционной тканью и появлении краевой эпителизации последнюю ушивают. Способ позволяет быстро достичь переход раны в стадии репарации и эпителизации, предотвратить возникновение персистирующей инфекции и ускорить выздоровление больного за счет дифференцированного использования раневых покрытий в зависимости от фазы раневого процесса при поддержании оптимальной среды в ране, отсутствии боли, травматизации подлежащих тканей и полной конгруэнтности повязок с раневой поверхностью. 14 ил.
Способ лечения гнойных ран, включающий медикаментозное воздействие, хирургическую обработку раны, отличающийся тем, что в глубокие труднодоступные клетчаточные пространства с воспалением I фазы укладывают абсорбирующую повязку в виде ленты «Аквасель Ag повязка Гидрофайбер» с абсорбционными, антимикробными, гиперосматическими и протеолитическими свойствами, поверх нее - повязку «Аквасель Ag Фоум повязка Гидрофайбер» на пенной основе неадгезивную, с внутренним абсорбирующим слоем, с антимикробными, абсорбирующими, дегидратационными, некролическими, гиперосматическими, протеолитическими свойствами; на участки раны II-III фаз накладывают повязку «Грануфлекс» со стимулирующими, заживляющими, антиадгезивными, гидроколлоидными, трофическими свойствами, при этом повязки меняют через 1-2 дня после обработки раны раствором хлоргексидина биглюконат 0,02%, при этом при очищении раны, выполнении ее грануляционной тканью и появлении краевой эпителизации последнюю ушивают, причем процесс очищения и заживления раны контролируют в динамике по макроскопической картине раны, клинико-лабораторным показателям и с помощью микробиологического, цитологического, морфологического исследований.
| СПОСОБ ЛЕЧЕНИЯ ГНОЙНЫХ РАН | 1998 |
|
RU2185781C2 |
| WO 2014016157 A1, 30.01.2014 | |||
| КУЗИН М.Н | |||
| под ред | |||
| Раны и раневая инфекция | |||
| Руководство для врачей// М.: "Медицина", 1990, с | |||
| ПАРОПЕРЕГРЕВАТЕЛЬ ДЛЯ ТРУБЧАТЫХ ПАРОВЫХ КОТЛОВ С ЭЛЕМЕНТАМИ, СОСТОЯЩИМИ ИЗ ДВУХ ПЕТЕЛЬ, ВВОДИМЫХ В ПРОГАРНЫЕ ТРУБЫ КОТЛА | 1916 |
|
SU281A1 |
| AVETIKOV D.S | |||
| et al | |||
| Dinamics of clinical changes and healing of purulent wounds in application of nanocapsules of phosphatidylcholine in complex of treatment of patients, sufferingthe oral cavity floor phlegmon// Klin | |||
| Khir | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
Авторы
Даты
2019-04-09—Публикация
2018-04-18—Подача