ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новой гидробромидной соли N-{4-хлор-2-гидрокси-3-[(3S)-3-пиперидинилсульфонил]фенил}-N'-(3-фтор-2-метилфенил)мочевины, композициям, комбинациям и лекарственным средствам, содержащим указанные соединения, и способам их получения. Изобретение также относится к применению указанных соединений, комбинаций, композиций и лекарственных средств в лечении заболеваний или состояний, при которых показан антагонист CXCR2.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
CXCR2 является хорошо описанным связанным с G-белками рецептором ряда хемокинов, содержащих мотив Glu-Leu-Arg (ELR), включая интерлейкин-8 (IL-8, CXCL8) и регулируемые ростом онкогены альфа, бета и гамма (GROα, β, γ или CXCL1, 2, 3), о которых известно, что они вовлечены в рекрутинг нейтрофилов к месту повреждения [Reutershan, J. (2006) Drug News Perspect 19: 615-623]. CXCR2 экспрессирован преимущественно на нейтрофилах (PMN), но может также быть экспрессирован на других лейкоцитах, таких как моноциты. Показано, что антагонизм в отношении CXCR2 эффективно блокирует рекрутинг PMN в легкие в ответ на такие стимулы, как воздействие LPS (липополисахарид), сигаретным дымом или озоном, как доклинически, так и у людей [Thatcher ТН (2005) Am Jour Phys Lung Cell Mol Phys 289:L322-L328; Reutershan J (2006) J Clin Invest 116: 695-702]. Holz O, Khalilieh S, Ludwig-Sengpiel A, Watz H, Stryszak P, Soni P, Tsai M, Sadeh J, Magnussen H. SCH527123, a novel CXCR2 antagonist, inhibits ozone-induced neutrophilia in healthy subjects. Eur Respir J 2010; 35: 564-570 Lazaar AL, Sweeney LE, MacDonald AJ, Alexis NE, Chen C, Tal-Singer R. SB-656933, a novel CXCR2 selective antagonist, inhibits ex vivo neutrophil activation and ozone-induced airway inflammation in humans. Br. J. Clin. Pharmacol. 72: 282-293 (2011). Селективный антагонизм в отношении взаимодействия CXCR2 и его различных хемокиновых лигандов обеспечивает потенциальную стратегию для уменьшения лежащего в основе воспаления, способствующего прогрессированию множества заболеваний [Chapman RW, Phillipsa JE, Hipkina RW, Currana AK, Lundella D, Fine JS. CXCR2 antagonists for the treatment of pulmonary disease. Pharmacol. Ther. 2009; 121 (1): 55-68], как показано в предварительных исследованиях у пациентов с респираторными заболеваниями (Nair Р, Gaga М, Zervas Е, Alagha К, Hargreave FE, O'Byrne РМ, Stryszak Р, Gann L, Sadeh J, Chanez P; Study Investigators. Safety and efficacy of a CXCR2 antagonist in patients with severe asthma and sputum neutrophils: a randomized, placebo-controlled clinical trial. Clin Exp Allergy 2012; 42:1097-2103) Rennard SI, Dale DC, Donohure JF, Kanniess F, Magnussen H, Sutherland ER, Watz H, Lu S, Stryszak P, Rosenberg E, Staudinger H. CXCR2 antagonist MK-7123 - a phase 2 proof-of-concept trial for chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2013; 187: A6071.
СХС-хемокины, обладающие мотивом ELR (например, CXCL1/GROα, CXCL8/IL-8), важны для рекрутинга воспалительных клеток, опосредующего патологию многих органов. Патология связана, например, с неправильным высвобождением гидролитических ферментов и активных форм кислорода из активированных нейтрофилов. С другой стороны, при большинстве бактериальных инфекций этот хемокиновый ответ является первой критической линией защиты, но даже в таких условиях ELR+-СХС-хемокиновые ответы могут, ввиду их способности активировать воспалительные клетки, обладающие рецепторами CXCR1 и CXCR2, усугублять патологию. Несмотря на критическую важность этих хемокиновых ответов во многих ситуациях, воспалительные клеточные ответы в достаточной степени вредны, чтобы идентификация терапевтических инструментов для блокирования ELR+-хемокинов представляла интерес.
ELR-хемокины являются хемоаттрактантами и активаторами воспалительных клеток через их рецепторы CXCR1 и CXCR2. CXCR1 специфичен в отношении CXCL8 и CXCL6, в то время как CXCR2 связывает CXCL8 с высокой аффинностью, но также связывает CXCL1, CXCL5 и CXCL6 с несколько меньшей аффинностью. CXCL8 - сигнализация в клеточных линиях, трансфицированных человеческим CXCR1 или CXCR2, индуцирует равносильные хемотактические ответы. Изменения свободного Са++ в цитозоле нейтрофилов и дегрануляция клеток в ответ на CXCL8 также опосредованы обоими рецепторами, но, согласно сообщениям, респираторный взрыв и активация фосфолипазы D зависят исключительно от CXCR1. С другой стороны, есть сообщения о том, что непептидный антагонист CXCR2, но не CXCR1, противодействует опосредованному CXCL8 хемотаксису нейтрофилов, но не активации клеток. В завершение, существует множество данных, согласно которым хемокины чаще всего сверхэкспрессированы при воспалительных ответах.
В WO 2007/124424 раскрыты соединения, полезные в лечении болезненных состояний, опосредованных IL-8, включая соединение N-{4-хлор-2-гидрокси-3-[3-пиперидинилсульфонил]фенил}-N'-(3-фтор-2-метилфенил)мочевину и энантиомер N-{4-хлор-2-гидрокси-3-[(3S)-3-пиперидинилсульфонил]фенил}-N'-(3-фтор-2-метилфенил)мочевину.
В данной области сохраняется потребность в лечении и соединениях, способных противодействовать CXCR2.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В одном аспекте предложена новая гидробромидная соль N-{4-xлop-2-гидрокси-3-[3-пиперидинилсульфонил]фенил}-N'-(3-фтор-2-метилфенил)мочевины, в частности гидробромидная соль энантиомера N-{4-хлор-2-гидрокси-3-[(3S)-3-пиперидинилсульфонил]фенил}-N'-(3-фтор-2-метилфенил)мочевины (настоящее соединение).
В другом аспекте настоящего изобретения предложено настоящее соединение для использования в терапии, в частности в лечении заболевания или состояния, при котором показан антагонист CXCR2.
В другом аспекте настоящего изобретения предложена фармацевтическая композиция, содержащая настоящее соединение и один или более чем один фармацевтически приемлемый носитель, разбавитель и эксципиент.
В другом аспекте настоящего изобретения предложен способ лечения заболевания или состояния, при котором показан антагонист CXCR2, включающий введение терапевтически эффективного количества настоящего соединения.
В другом аспекте настоящего изобретения предложено применение настоящего соединения в изготовлении лекарственного средства для использования в лечении заболевания или состояния, при котором показан антагонист CXCR2.
В другом аспекте предложена комбинация, содержащая настоящее соединение и по меньшей мере один другой терапевтический агент.
В другом аспекте предложена фармацевтическая композиция, содержащая настоящее соединение, по меньшей мере один другой терапевтический агент и один или более чем один фармацевтически приемлемый носитель, разбавитель и эксципиент.
В другом аспекте предложена комбинация, содержащая настоящее соединение и по меньшей мере один другой терапевтический агент, для использования в терапии, в частности для лечения заболевания или состояния, при котором показан антагонист CXCR2.
В другом аспекте предложен способ лечения заболевания или состояния, при котором показан антагонист CXCR2, включающий введение человеку, нуждающемуся в этом, терапевтически эффективного количества комбинации, содержащей настоящее соединение и по меньшей мере один другой терапевтический агент.
В другом аспекте предложено применение комбинации, содержащей настоящее соединение и по меньшей мере один другой терапевтический агент, в изготовлении лекарственного средства для лечения заболевания или состояния, при котором показан антагонист CXCR2.
В другом аспекте предложен способ ингибирования связывания IL-8 с его рецепторами у млекопитающего, в частности человека, включающий введение терапевтически эффективного количества настоящего соединения.
ПЕРЕЧЕНЬ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
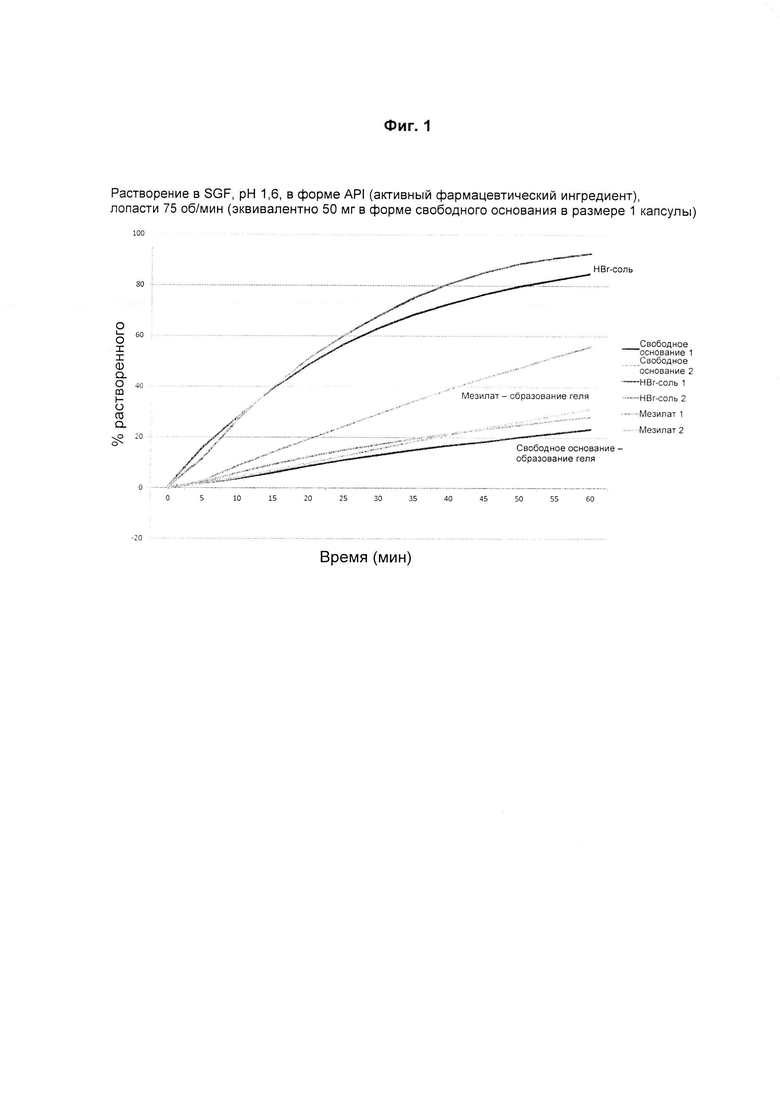
Фиг. 1: HBr-соль демонстрирует повышенную скорость растворения без гелеобразования при низком желудочном pH.
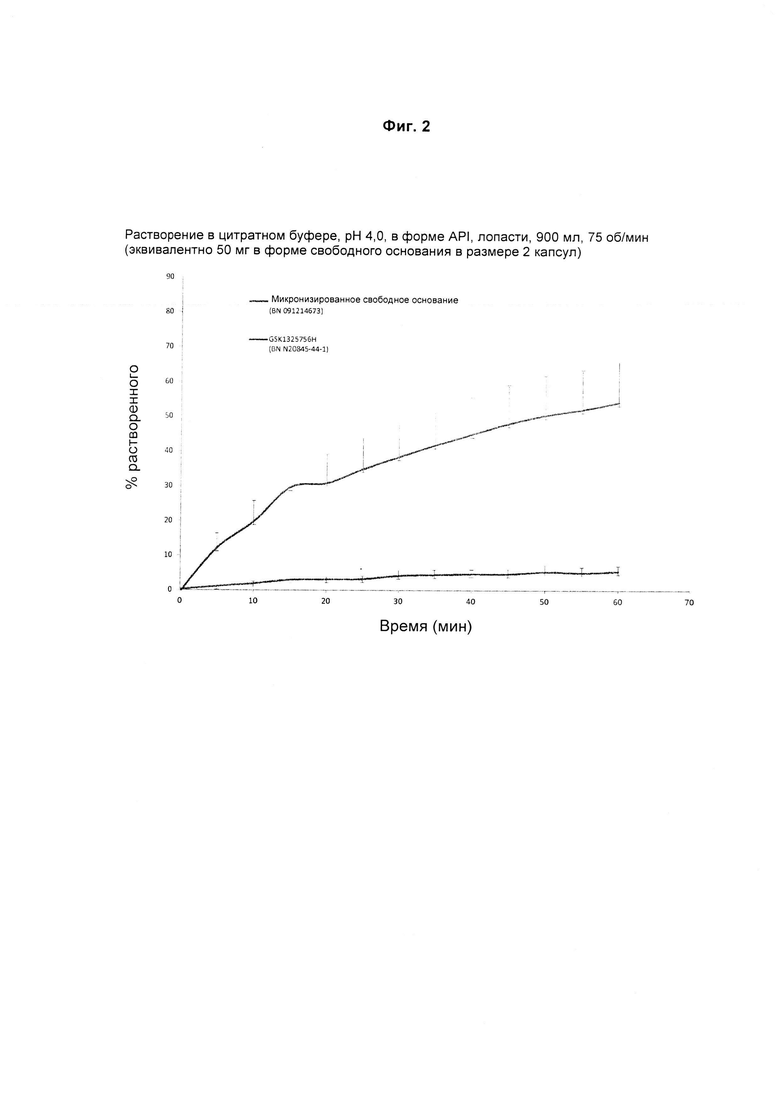
Фиг. 2: HBr-соль обеспечивает наибольшую скорость растворения при повышенном желудочном pH.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Обнаружено, что гидробромидная соль демонстрирует преимущества по сравнению со свободным основанием, что делает ее особенно подходящей для использования в лечении заболеваний или состояний, при которых показан антагонист CXCR2, например хронической обструктивной болезни легких (COPD).
Конкретно, гидробромидная соль демонстрирует улучшенную растворимость и профили растворения при более высоком pH по сравнению со свободным основанием. Многие пациенты с COPD также принимают ингибиторы протонных помп и, таким образом, могут иметь желудочный pH выше среднего. У таких пациентов свободное основание не будет оказывать такого же действия, как y в остальном здоровых пациентов, и, таким образом, повышенная растворимость и растворение гидробромидной соли усиливает действие у таких пациентов.
При использовании здесь термин «эффективное количество» означает такое количество лекарственного средства или фармацевтического агента, которое вызовет биологический или медицинский ответ ткани, системы, животного или человека, желаемый с точки зрения, например, исследователя или врача. Кроме того, термин «терапевтически эффективное количество» означает любое количество, которое, по сравнению с соответствующим субъектом, не получившим такого количества, приводит к улучшению лечения, излечения, предотвращения или облегчения заболевания, расстройства или побочного эффекта, или снижению темпов прогрессирования заболевания или расстройства. Объем данного термина также включает количества, эффективные для усиления нормальной физиологической функции.
При использовании здесь термин «фармацевтически приемлемый» относится к таким соединениям, веществам, композициям и лекарственным формам, которые, с медицинской точки зрения, являются подходящими для использования в контакте с тканями людей и животных без чрезмерной токсичности, раздражения или другой проблемы или осложнения, при разумном соотношении пользы и риска.
Настоящее соединение может существовать в сольватированных и несольватированных формах. При использовании здесь термин «сольват» относится к комплексу с различной стехиометрией, образованному растворенным веществом (в данном изобретении соединением формулы (I) или солью) и растворителем. Такие растворители для задач изобретения не должны мешать биологической активности растворенного вещества. Специалисту в данной области будет ясно, что могут быть получены фармацевтически приемлемые сольваты кристаллических соединений, где молекулы растворителя включены в кристаллическую решетку во время кристаллизации. Включенные молекулы растворителя могут представлять собой молекулы воды или неводные молекулы, такие как молекулы этанола, изопропанола, DMSO (диметилсульфоксид), уксусной кислоты, этаноламина и этилацетата. Кристаллическую решетку с включенными молекулами воды обычно называют «гидратами». Гидраты включают стехиометрические гидраты, а также композиции, содержащие различные количества воды. В одном воплощении настоящее соединение представляет собой гемигидрат.
Настоящее соединение может обладать способностью к кристаллизации в более чем одной форме, данное свойство известно как полиморфизм, и подразумевают, что объем изобретения включает такие полиморфные формы («полиморфы»). Полиморфизм обычно возникает в ответ на изменения температуры и/или давления и может также быть результатом изменений в процессе кристаллизации. Полиморфы можно различать по разнообразным физическим свойствам, известным в данной области, таким как картины дифракции рентгеновских лучей, растворимость и точка плавления.
Несмотря на то, что для использования в терапии настоящее соединение может быть введено в форме необработанного химического вещества, активный ингредиент может быть представлен как фармацевтическая композиция. Соответственно, согласно изобретению также предложены фармацевтические композиции, содержащие настоящее соединение и один или более чем один фармацевтически приемлемый носитель, разбавитель или эксципиент. Носител(и), разбавител(и) или эксципиент(ы) должен(ы) быть приемлем(ы) в смысле совместимости с другими ингредиентами композиции и безвредности для ее реципиента. Согласно другому аспекту изобретения также предложен способ изготовления фармацевтической композиции, содержащей агент или его фармацевтически приемлемые соли с одним или более чем одним фармацевтически приемлемым носителем, разбавителем или эксципиентом. Фармацевтическая композиция может быть предназначена для использования в лечении и/или профилактике любых из описанных здесь состояний.
Фармацевтические композиции могут быть представлены в стандартных лекарственных формах, содержащих предопределенное количество активного ингредиента на стандартную дозу. Предпочтительные стандартные композиции представляют собой композиции, содержащие суточную дозу активного ингредиента, или субдозу, или ее подходящую часть. Таким образом, такие стандартные дозы можно вводить один раз или более чем один раз в сутки. Такие фармацевтические композиции могут быть изготовлены любым из способов, хорошо известных в области фармацевтики.
Фармацевтические композиции могут быть адаптированы для введения любым подходящим способом введения, например пероральным (включая трансбуккальный или сублингвальный), ректальным, ингаляционным, интраназальным, местным (включая трансбуккальный, сублингвальный или трансдермальный), вагинальным или парентеральным (включая подкожный, внутримышечный, внутривенный или внутрикожный) способом введения. Такие композиции могут быть изготовлены любым способом, известным в области фармацевтики, например посредством объединения активного ингредиента с носителем(ями) или эксципиентом(ами).
Фармацевтические композиции, адаптированные для перорального введения, могут быть представлены в форме дискретных единиц, таких как капсулы или таблетки; порошки или гранулы; растворы или суспензии в водных или неводных жидкостях; съедобные пены или муссы; или жидкие эмульсии типа «масло в воде» или жидкие эмульсии типа «вода в масле».
Например, для перорального введения в форме таблетки или капсулы активный компонент лекарственного средства можно комбинировать с нетоксичным фармацевтически приемлемым инертным носителем для перорального введения, таким как этанол, глицерин, вода и тому подобное. Порошки получают путем измельчения соединения до подходящего мелкого размера и смешивания его с подготовленным сходным образом фармацевтическим носителем, таким как съедобный углевод, такой как, например, крахмал или маннит. Также могут присутствовать корригент, консервант, диспергирующий агент и краситель.
Капсулы изготавливают путем приготовления порошковой смеси, как описано выше, и наполнения формованных желатиновых оболочек. Перед наполнением к порошковой смеси могут быть добавлены скользящие и смазывающие агенты, такие как коллоидный диоксид кремния, тальк, стеарат магния, стеарат кальция или твердый полиэтиленгликоль. Также может быть добавлен разрыхлитель или солюбилизирующий агент, такой как агар-агар, карбонат кальция или карбонат натрия, для улучшения доступности лекарственного средства при проглатывании капсулы.
Более того, если это желательно или необходимо, в смесь могут также быть включены подходящие связывающие, скользящие, смазывающие агенты, подсластители, корригенты, разрыхлители и красители. Подходящие связывающие агенты включают крахмал, желатин, природные сахара, такие как глюкоза или бета-лактоза, кукурузные подсластители, природные и синтетические камеди, такие как аравийская камедь, трагакантовая камедь или альгинат натрия, карбоксиметилцеллюлоза, полиэтиленгликоль, воски и тому подобное. Смазывающие агенты, используемые в этих лекарственных формах, включают олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и тому подобное. Разрыхлители включают, без ограничения, крахмал, метил целлюлозу, агар, бентонит, ксантановую камедь и тому подобное. Таблетки изготавливают, например, путем получения порошковой смеси, гранулирования или комкования, добавления смазывающего агента и разрыхлителя и прессования в таблетки. Порошковую смесь получают путем смешивания соединения, измельченного подходящим образом, с разбавителем или основанием, как описано выше, и возможно со связывающим агентом, таким как карбоксиметилцеллюлоза, альгинат, желатин или поливинилпирролидон, замедлителем растворения, таким как парафин, усилителем всасывания, таким как четвертичная соль, и/или абсорбирующим агентом, таким как бентонит, каолин или гидрофосфат кальция. Порошковую смесь можно гранулировать путем смачивания связывающим агентом, таким как сироп, крахмальная паста, аравийская камедь или растворы целлюлозных или полимерных веществ, и пропускания через сито. В качестве альтернативы гранулированию, порошковую смесь можно пропускать через таблетировочную машину с получением комков неправильной формы, распадающихся на гранулы. Гранулы можно смазать для предотвращения прилипания к таблетировочным штампам посредством добавления стеариновой кислоты, стеаратной соли, талька или минерального масла. Смазанную смесь затем прессуют в таблетки. Соединения по настоящему изобретению можно также объединять со свободнотекучим инертным носителем и прессовать в таблетки сразу, без осуществления стадий гранулирования или комкования. Можно обеспечить прозрачное или непрозрачное защитное покрытие, состоящее из изолирующего покрытия из шеллака, покрытия из сахара или полимерного вещества и полирующего покрытия из воска. Для различения разных лекарственных форм в эти покрытия могут быть добавлены красители.
При использовании здесь настоящее соединение включает все сольваты, комплексы, полиморфы, меченные радиоактивными изотопами производные гидробромидной соли N-{4-хлор-2-гидрокси-3-[(3S)-3-пиперидинилсульфонил]фенил}-N'-(3-фтор-2-метилфенил)мочевины.
Могут быть изготовлены стандартные лекарственные формы в виде жидкостей для перорального применения, такие как растворы, сиропы и эликсиры, таким образом, чтобы заданное количество содержало предопределенное количество соединения. Сиропы могут быть получены путем растворения соединения в водном растворе с подходящими корригентами, в то время как эликсиры получают, используя нетоксичный спиртовой носитель. Суспензии могут быть получены путем диспергирования соединения в нетоксичном носителе. Могут также быть добавлены солюбилизаторы и эмульгаторы, такие как этоксилированные изостеариловые спирты и эфиры полиоксиэтиленсорбита, консерванты, корригенты, такие как масло мяты перечной, или природные подсластители, или сахарин, или другие искусственные подсластители и тому подобное.
Там, где это уместно, стандартные лекарственные композиции для перорального введения могут быть микроинкапсулированными. Композиция может также быть изготовлена для продления или поддержания высвобождения, например, посредством покрытия или заключения вещества в форме частиц в полимеры, воск или тому подобное.
Соединения по изобретению можно также вводить в форме липосомных систем доставки, таких как малые однослойные везикулы, большие однослойные везикулы и многослойные везикулы. Липосомы можно получать из множества фосфолипидов, таких как холестерин, стеариламин или фосфатидилхолины.
Фармацевтические композиции, адаптированные для трансдермального введения, могут быть представлены в форме отдельных пластырей, предназначенных для сохранения тесного контакта с эпидермисом реципиента в течение длительного периода времени.
Фармацевтические композиции, адаптированные для местного применения, могут быть изготовлены в форме мазей, кремов, суспензий, лосьонов, порошков, растворов, паст, гелей, спреев, аэрозолей или масел.
Для обработки глаз или других наружных тканей, например рта и кожи, композиции предпочтительно применяют в форме мази или крема для местного применения. При изготовлении в форме мази активные ингредиенты могут быть использованы с парафиновой или водорастворимой мазевой основой. Альтернативно, активный ингредиент может быть включен в крем с кремовой основой типа «масло в воде» или основой типа «вода в масле».
Фармацевтические композиции, адаптированные для местного введения в глаз, включают глазные капли, где активный ингредиент растворен или суспендирован в подходящем носителе, в частности водном растворителе.
Фармацевтические композиции, адаптированные для местного введения в рот, включают леденцы, пастилки и жидкости для полоскания рта.
Фармацевтические композиции, адаптированные для ректального введения, могут быть представлены в форме суппозиториев или в форме клизм.
Лекарственные формы для назального или ингаляционного введения могут быть подходящим образом изготовлены в форме аэрозолей, растворов, суспензий, капель, гелей или сухих порошков.
Фармацевтические композиции, адаптированные для вагинального введения, могут быть представлены в виде композиций в форме пессариев, тампонов, кремов, гелей, паст, пен или спреев.
Фармацевтические композиции, адаптированные для парентерального введения, включают водные и неводные стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактериостатические агенты и растворенные вещества, придающие композиции изотоничность относительно крови предполагаемого реципиента; и водные и неводные стерильные суспензии, которые могут содержать суспендирующие агенты и загустители. Композиции могут быть представлены в контейнерах на одну дозу или на несколько доз, например в герметичных ампулах и флаконах, и их можно хранить в сублимированном (лиофилизированном) состоянии, требующем только добавления стерильного жидкого носителя, например воды для инъекций, непосредственно перед применением. Растворы и суспензии для инъекций непосредственно после приготовления могут быть получены из стерильных порошков, гранул и таблеток.
Следует понимать, что в дополнение к ингредиентам, конкретно упомянутым выше, композиции могут содержать другие агенты, обычные для данной области, относящиеся к рассматриваемому типу композиций, например агенты, подходящие для перорального введения, могут включать корригенты.
Терапевтически эффективное количество настоящего соединения будет зависеть от ряда факторов, включая, например, возраст и массу тела субъекта, конкретное состояние, требующее лечения, и его тяжесть, тип композиции и путь введения, и, в конечном счете, его будет определять лечащий врач или ветеринар. В частности, субъект, подлежащий лечению, представляет собой млекопитающее, в частности человека.
Агент можно вводить в суточной дозе. Это количество можно давать как одну дозу в сутки или несколько (например, две, три, четыре, пять или шесть) субдоз в сутки, таким образом, чтобы общая суточная доза была такой же.
Для всех способов применения, раскрытых здесь для соединения по изобретению, суточная доза для перорального введения будет предпочтительно составлять от приблизительно 0,01 до приблизительно 80 мг/кг общей массы тела. Суточная доза для парентерального введения от приблизительно 0,0001 до приблизительно 80 мг/кг общей массы тела. Суточная доза для местного применения будет предпочтительно составлять от 0,1 мг до 150 мг для применения от одного до четырех раз в сутки, предпочтительно два или три раза в сутки. Суточная доза для ингаляционного введения будет предпочтительно составлять от приблизительно 0,01 мг/кг до приблизительно 1 мг/кг в сутки. Специалисту в данной области также будет ясно, что оптимальное количество отдельных доз соединения по изобретению и интервалы между ними будут определены природой и степенью состояния, подлежащего лечению, формой, путем и местом введения и конкретным пациентом, получающим лечение, и что такие оптимальные параметры можно определить посредством обычных методик. Специалисту в данной области также будет ясно, что оптимальный курс лечения, то есть число доз соединения по изобретению, вводимых за сутки на протяжении определенного числа суток, может быть определен специалистом в данной области с использованием обычных тестов для определения курса лечения. Все указанное выше относится к количествам свободного основания.
Настоящее изобретение полезно для изготовления лекарственного средства для профилактического или терапевтического лечения любого болезненного состояния у человека или другого млекопитающего, при котором показан антагонист CXCR2.
Соответственно, согласно настоящему изобретению предложен способ лечения заболевания или состояния, при котором показан антагонист CXCR2, включающий введение эффективного количества настоящего соединения.
Существует много болезненных состояний, при которых показан антагонист CXCR2. Заболевания, опосредованные хемокинами, включают псориаз, атопический дерматит, остеоартрит, ревматоидный артрит, астму, хроническую обструктивную болезнь легких, респираторный дистресс-синдром взрослых, воспалительное заболевание кишечника, болезнь Крона, язвенный колит, инсульт, септический шок, эндотоксический шок, грамотрицательный сепсис, синдром токсического шока, реперфузионное повреждение сердца и почек, гломерулонефрит, тромбоз, реакцию «трансплантат против хозяина», болезнь Альцгеймера, отторжение аллотрансплантата, малярию, рестеноз, ангиогенез, атеросклероз, остеопороз, гингивит, вирусные заболевания, такие как риновирусные, или нежелательное высвобождение гемопоэтических стволовых клеток. В частности, соединение по настоящему изобретению полезно в лечении астмы, хронической обструктивной болезни легких и респираторного дистресс-синдрома взрослых.
Предпочтительно, настоящее соединение полезно для лечения хронической обструктивной болезни легких.
Заболевания по настоящему изобретению характеризуются главным образом сильной нейтрофильной инфильтрацией, Т-клеточной инфильтрацией или ростом новых сосудов и ассоциированы с усиленным образованием IL-8, GROα, GROβ, GROγ, NAP-2 (нейтрофил-активирующий белок-2) или ENA-78 (эпителиальный нейтрофил-активирующий пептид-78), отвечающим за хемотаксис нейтрофилов к очагу воспалителения или направленный рост эндотелиальных клеток. В отличие от других воспалительных цитокинов (IL-I, TNF (фактор некроза опухоли) и IL-6), IL-8, GROα, GROβ, GROγ, NAP-2 или ENA-78 обладают уникальным свойством стимулирования хемотаксиса нейтрофилов и высвобождения ими ферментов, включая, без ограничения, высвобождение эластазы, а также образования и активации супероксидов, а-хемокины, но в особенности GROα, GROβ, GROγ, NAP-2 или ENA-78, действующие через рецепторы IL-8 I или II типа, могут способствовать неоваскуляризации опухолей посредством стимулирования направленного роста эндотелиальных клеток. Таким образом, ингибирование хемотаксиса или активации, индуцированных IL-8, будет приводить к непосредственному уменьшению нейтрофильной инфильтрации. Недавние данные также указывают на роль хемокинов в лечении ВИЧ (вирус иммунодефицита человека)-инфекции, Littleman et al., Nature 381, pp. 661 (1996) и Koup et al., Nature 381, pp. 30 667 (1996).
Согласно современным данным, применение ингибиторов IL-8 также показано при лечении атеросклероза. В первом источнике, Boisvert et al., 1. Clin. Invest, 1998, 101: 353-363, показано, посредством трансплантации костного мозга, что отсутствие рецепторов IL-8 на стволовых клетках (и, следовательно, на моноцитах/макрофагах) приводит к уменьшению развития атеросклеротических бляшек у мышей с дефектом рецептора LDL (липопротеинов низкой плотности).
Согласно настоящему изобретению также предложено средство лечения повреждений ЦНС (центральная нервная система). Такое лечение предложено для острых ситуаций, а также для предотвращения повреждения у тех индивидов, которых считают подверженными повреждению. Повреждения ЦНС, как определено здесь, включают как открытую или проникающую травму головы, такую как при хирургическом вмешательстве, так и закрытую травму/повреждение головы, такую как при повреждении области головы. Это определение также включает ишемический инсульт, в частности в области головного мозга. Ишемический инсульт можно определить как очаговое неврологическое расстройство, являющееся результатом недостаточного кровоснабжения определенной области головного мозга, обычно вследствие эмбола, тромба или локального атероматозного закрытия кровеносного сосуда. Роль воспалительных цитокинов в этой области была установлена, и согласно настоящему изобретению предложено средство потенциального лечения этих повреждений. При таких острых повреждениях было доступно относительно небольшое количество вариантов лечения.
TNF-α представляет собой цитокин с провоспалительным действием, включающим экспрессию эндотелиальной молекулы адгезии лейкоцитов. Лейкоциты инфильтрируют ишемические поражения в головном мозге, и поэтому соединения, ингибирующие или снижающие уровни TNF, будут полезны для лечения ишемичнеского повреждения головного мозга. См. статью Liu et al., Stroke, Vol. 25., No. 7, pp. 1481-88 (1994), содержание которой включено сюда посредством ссылки.
Модели закрытых травм головы и лечение смешанными 5-LO/СО-агентами обсуждены в Shohami et al., 1. Vaisc & Clinical Physiology and Pharmacology, Vol.3, No.2, pp.99-107 (1992). Было обнаружено, что лечение, уменьшающее развитие отека, улучшало функциональный исход у животных, получавших лечение.
При использовании здесь термин «цитокин» относится к любому секретируемому полипептиду, влияющему на функции клеток и представляющему собой молекулу, модулирующую взаимодействия между клетками при иммунном, воспалительном или гемопоэтическом ответе. Цитокины включают, без ограничения, монокины и лимфокины, независимо от того, какими клетками они образованы. Например, считают, что монокины обычно продуцируются и секретируются мононуклеарными клетками, такими как макрофаги и/или моноциты. Тем не менее, многие другие клетки также продуцируют монокины, например естественные клетки-киллеры, фибробласты, базофилы, нейтрофилы, эндотелиальные клетки, астроциты головного мозга, стромальные клетки костного мозга, эпидермальные кератиноциты и В-лимфоциты.
Соединения по настоящему изобретению могут быть использованы в комбинации с одним или более чем одним другим терапевтическим агентом или включать один или более чем один другой терапевтический агент, и их можно вводить последовательно или одновременно любым подходящим путем введения в раздельных или комбинированных фармацевтических композициях.
Таким образом, в другом аспекте изобретение включает комбинацию, содержащую настоящее соединение вместе с по меньшей мере одним другим терапевтически активным агентом.
Количества соединения(ий) по изобретению и другого(их) фармацевтически активного(ых) агента(ов) и относительное время введения будут выбраны для достижения желаемого комбинированного терапевтического эффекта.
Соединения по настоящему изобретению и другой(ие) терапевтический(ие) агент(ы) могут быть использованы в комбинации посредством одновременного введения в одной фармацевтической композиции, содержащей оба соединения. Альтернативно, комбинацию можно вводить по отдельности в раздельных фармацевтических композициях, каждая из которых содержит одно из соединений, последовательным образом, где, например, соединение по изобретению вводят первым, а другое соединение - вторым, и наоборот. Такое последовательное введение может быть близким по времени (например, одновременным) или отдаленным по времени. Кроме того, неважно, вводят ли соединения в одной и той же лекарственной форме, например одно соединение можно вводить местно, а другое можно вводить перорально.
Комбинации могут быть представлены в форме комбинированного набора. При использовании здесь термин «комбинированный набор» или «набор» обозначает фармацевтическую композицию или композиции, используемые для введения комбинации по изобретению. Когда оба соединения вводят одновременно, комбинированный набор может содержать оба соединения в одной фармацевтической композиции, такой как таблетка, или в раздельных фармацевтических композициях. Когда соединения вводят не одновременно, комбинированный набор будет содержать каждое соединение либо в раздельных фармацевтических композициях в одной упаковке, либо в раздельных фармацевтических композициях в раздельных упаковках.
Комбинированный набор может также быть снабжен инструкцией, такой как инструкции по дозированию и введению. Такие инструкции по дозированию и введению могут представлять собой инструкции, предоставляемые врачу, например инструкции по применению лекарственного средства, или они могут представлять собой инструкции, предоставляемые врачом, например инструкции для пациента.
При раздельном введении комбинации последовательным образом, где одно вводят первым, а другое - вторым или наоборот, такое последовательное введение может быть близким по времени или отдаленным по времени. Например, включено введение другого агента в интервале от нескольких минут до нескольких дюжин минут после введения первого агента и введение другого агента в интервале от нескольких часов до нескольких суток после введения первого агента, при этом промежуток времени не ограничен, например один агент можно вводить один раз в сутки и другой агент можно вводить 2 или 3 раза в сутки, или один агент можно вводить один раз в неделю и другой агент можно вводить один раз в сутки, и тому подобное.
Специалисту в данной области будет ясно, что там, где это уместно, другой(ие) терапевтический(ие) ингредиент(ы) можно использовать в форме солей, например в форме солей щелочных металлов или аминов, или в форме солей присоединения кислоты, или пролекарств, или в форме сложных эфиров, например низших алкиловых эфиров, или в форме сольватов, например гидратов, для оптимизации активности и/или стабильности, и/или физических свойств терапевтического ингредиента, таких как растворимость. Также будет ясно, что там, где это уместно, терапевтические ингредиенты можно использовать в оптически чистой форме.
При сочетании в одной композиции будет ясно, что два соединения должны быть стабильны и совместимы друг с другом и другими компонентами композиции и могут быть включены в композицию для введения. При включении в раздельные композиции они могут быть подходящим образом представлены в любой подходящей композиции, так, как известно для таких соединений в данной области.
При использовании соединения по изобретению в комбинации со вторым терапевтическим агентом, активным в отношении того же заболевания, состояния или расстройства, доза каждого соединения может отличаться от используемой при применении соединения в отдельности. Специалист в данной области легко определит подходящие дозы.
Настоящее соединение может быть использовано в комбинации с одним или более чем одним другим агентом, которые могут быть полезны для предотвращения или лечения аллергического заболевания, воспалительного заболевания, аутоиммунного заболевания, например антигенной иммунотерапией, антигистаминными агентами, кортикостероидами (например пропионатом флутиказона, фуроатом флутиказона, дипропионатом беклометазона, будесонидом, циклесонидом, фуроатом мометазона, триамцинолоном, флунизолидом), NSAID (нестероидными противовоспалительными средствами), модуляторами лейкотриенов (например монтелукастом, зафирлукастом, пранлукастом), ингибиторами iNOS (индуцируемой синтазы оксида азота), ингибиторами триптазы, ингибиторами IKK2 (киназной субъединицы бета ядерного фактора каппа-В), ингибиторами р38, ингибиторами Syk (селезеночной тирозинкиназы), ингибиторами эластазы, антагонистами бета-2-интегрина, А2А-агонистами аденозина, антагонистами хемокинов, такими как антагонисты CCR3 (хемокиновый рецептор 3) или антагонисты CCR4, ингибиторами высвобождения медиаторов, такими как кромогликат натрия, ингибиторами 5-липоксигеназы (зифло), антагонистами DP1, антагонистами DP2, ингибиторами рI3K (фосфоинозитид 3-киназы) дельта, ингибиторами ITK (интерлейкин-2-индуцибельной Т-клеточной киназы), LP (лизофосфатидными) ингибиторами или ингибиторами FLAP (белка, активирующего 5-липоксигеназу) (например 3-(3-(трет-бутилтио)-1-(4-(6-этоксипиридин-3-ил)бензил)-5-((5-метилпиридин-2-ил)метокси)-1Н-индол-2-ил)-2,2-диметилпропаноатом натрия), бронхорасширяющими агентами (например бета-2-агонистами, адренергическими агонистами, антихолинергическими агентами, теофиллином), метотрексатом и сходными агентами; терапией моноклональными антителами, например против IgE (иммуноглобулина Е), против TNF, против IL-5, против IL-6, против IL-12, против IL-1, и сходными агентами; рецепторной терапией, например этанерцептом и сходными агентами; антиген-неспецифической иммунотерапией (например интерфероном или другими цитокинами/хемокинами, модуляторами рецепторов цитокинов/хемокинов, агонистами или антагонистами цитокинов, агонистами TLR (Toll-подобных рецепторов) и сходными агентами).
Настоящее соединение может быть получено способами, известными в области органического синтеза, как изложено в конкретных Примерах, описанных ниже. Хорошо известно, что во всех способах могут по необходимости быть использованы защитные группы для чувствительных или реакционноспособных групп в соответствии с общими принципами химии. Защитные группы используют согласно стандартным способам органического синтеза (Т.W. Green, P.G.М. Wuts (1999) Protective Groups in Organic Synthesis, 3rd edition, John Wiley & Sons). Эти группы удаляют на подходящей стадии синтеза соединения с применением способов, хорошо известных специалистам в данной области. Выбор способов, а также условий взаимодействия и порядок их проведения должны соответствовать получению соединений по изобретению.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез гидробромидной соли N-(4-хлор-2-гидрокси-3-[(3S)-3-пиперидинилсульфонил]фенил}-N'-(3-фтор-2-метилфенил)мочевины
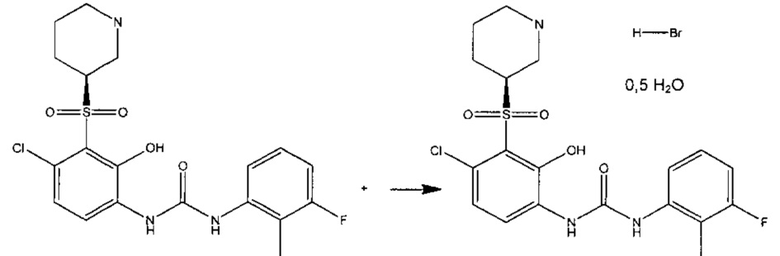
N-{4-хлор-2-гидрокси-3-[(3S)-3-пиперидинилсульфонил]фенил}-N'-(3-фтор-2-метилфенил)мочевину (которая может быть получена, как описано в WO 2007/124424) суспендировали в IРА (изопропиловый спирт) при 50±3°C перед добавлением 48 масс. % HBr в воде на протяжении по меньшей мере 30 минут и промывали водой. Реакционную смесь выдерживали при 50±3°C в течение по меньшей мере 180 минут перед нагреванием до 75±3°C. Полученный раствор осветляли путем переноса в чистый сосуд с последующими 10 масс. % воды в IPA при 75±3°C. Полученный раствор охлаждали до 40±3°C перед внесением затравки гидробромидной соли, суспендировали в 10 масс. % воды в IPA, обработанной ультразвуком в течение по меньшей мере 2 минут. Полученную суспензию затем выдерживали при 40±3°C в течение по меньшей мере 48 часов перед охлаждением до 0±3°C со скоростью 0,2°C в минуту. Полученную суспензию затем выдерживали при 0±3°C в течение по меньшей мере 24 часов перед сбором твердого вещества посредством фильтрации и промывали 10 масс. % воды в IPA. Затравку получали, добавляя сHBr к суспензии свободного основания в IPA и затем использовали ее в качестве затравки в последующих и более крупных партиях.
Продукт сушили под вакуумом при 50±5°C. HBr-соль представляет собой гемигидрат.
Растворимость
Растворимость HBr-соли выше, чем у свободного основания при более высоких pH и в искусственных желудочных жидкостях (см. таблицы ниже). Растворимость в искусственных желудочных жидкостях снижается со временем, но все равно намного выше растворимости эквивалентного свободного основания. 
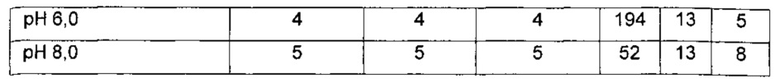
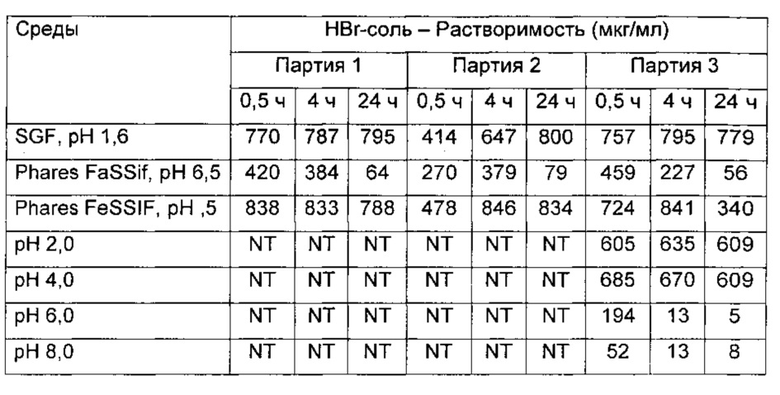
Растворение
Профили растворения HBr-соли (50 мг в свободной форме) в капсуле сравнивали со свободным основанием в искусственной желудочной жидкости, pH 1,6, и цитратном буфере, pH 4. HBr-соль лучше. Мезилат образовывал гель, и было признано, что HBr-соль превосходит как мезилатную соль, так и свободное основание. См. Фиг. 1 и 2.
Изобретение относится к соединению, представляющему собой гидробромидную соль N-{4-хлор-2-гидрокси-3-[(3S)-3-пиперидинилсульфонил]фенил}-N'-(3-фтор-2-метилфенил) мочевины, композиции, содержащей указанное соединение, и способам к применению указанного соединения для лечения заболевания или состояния, при котором показан антагонист CXCR2. 4 н. и 3 з.п. ф-лы, 2 ил., 2 табл.
1. Соединение, представляющее собой гидробромидную соль N-{4-хлор-2-гидрокси-3-[(3S)-3-пиперидинилсульфонил]фенил}-N'-(3-фтор-2-метилфенил)мочевины.
2. Соединение по п. 1 для использования в лечении заболевания или состояния, при котором показан антагонист CXCR2.
3. Соединение для использования по п. 2, где заболевание или состояние представляет собой COPD (хроническую обструктивную болезнь легких).
4. Фармацевтическая композиция, обладающая активностью антагониста CXCR2, содержащая эффективное количество соединения по п. 1 и один или более чем один фармацевтически приемлемый носитель, разбавитель и эксципиент.
5. Способ лечения заболевания или состояния, при котором показан антагонист CXCR2, у субъекта, включающий введение терапевтически эффективного количества соединения по п. 1.
6. Способ по п. 5, где заболевание или состояние представляет собой COPD.
7. Применение соединения по п. 1 в изготовлении лекарственного средства для использования в лечении заболевания или состояния, при котором показан антагонист CXCR2.
| EA 200870465 A1, 28.04.2009 | |||
| STEPHEN M BERGE et al | |||
| "Pharmaceutical salts", JOURNAL OF PHARMACEUTICAL SCIENCES, vol.66, no.1, pp.1-19, 1977, DOI: 10.1002/JPS.2600660104. |
Авторы
Даты
2019-04-18—Публикация
2014-11-11—Подача