Настоящее изобретение относится к новым изоиндолиновым или изохинолиновым соединениям, к способу их получения и к фармацевтическим композициям, содержащим их.
Соединения настоящего изобретения являются новыми и обладают очень ценными фармакологическими характеристиками в области апоптоза и онкологии.
Апоптоз, или запрограммированная гибель клеток, является физиологическим процессом, который имеет решающее значение для эмбрионального развития и поддержания тканевого гомеостаза.
Гибель клеток по типу апоптоза вовлекает морфологические изменения, такие как конденсация ядра, фрагментация ДНК, а также биохимический феномен, такой как активация каспаз, что вызывает повреждение ключевых структурных компонентов клетки, таким образом вызывая ее разборку и смерть. Регуляция процесса апоптоза является комплексной и задействует активацию или репрессию нескольких внутриклеточных путей передачи сигналов (Cory S. и др., Nature Review Cancer, 2002, 2, 647-656).
Дерегулирование апоптоза вовлечено в определенные патологии. Повышенный апоптоз связан с нейродегенеративными заболеваниями, такими как болезнь Паркинсона, болезнь Альцгеймера и ишемия. Наоборот, недостаточности осуществления апоптоза играют важную роль в развитии злокачественных новообразований и их резистентности к химиотерапии, при аутоиммунных заболеваниях, воспалительных заболеваниях и вирусных инфекциях. Следовательно, отсутствие апоптоза является одним из характерных фенотипических признаков злокачественного новообразования (Hanahan D. и др., Cell 2000, 100, 57-70).
Антиапоптотические белки семейства Вс1-2 связаны с многочисленными патологиями. Задействование белков семейства Вс1-2 описано для многочисленных типов злокачественных новообразований, таких как рак ободочной кишки, рак молочной железы, мелкоклеточный рак легкого, немелкоклеточный рак легкого, рак мочевого пузыря, рак яичников, рак предстательной железы, хронический лимфоидный лейкоз, фолликулярная лимфома, миелома и т.д. Сверхэкспрессия антиапоптотических белков семейства Вс1-2 связана с онкогенезом, с устойчивостью к химиотерапии и с клиническим прогнозом пациентов, страдающих злокачественным новообразованием. Таким образом, существует терапевтическая потребность в соединениях, которые ингибируют антиапоптотическую активность белков семейства Вс1-2.
Помимо того, что соединения настоящего изобретения являются новыми, соединения настоящего изобретения обладают проапоптотическими свойствами, что позволяет их применение при патологиях, в которые вовлечен дефект апоптоза, как, например, для лечения злокачественного новообразования и аутоиммунных заболеваний и заболеваний иммунной системы.
Более конкретно, настоящее изобретение относится к соединениям формулы (I):
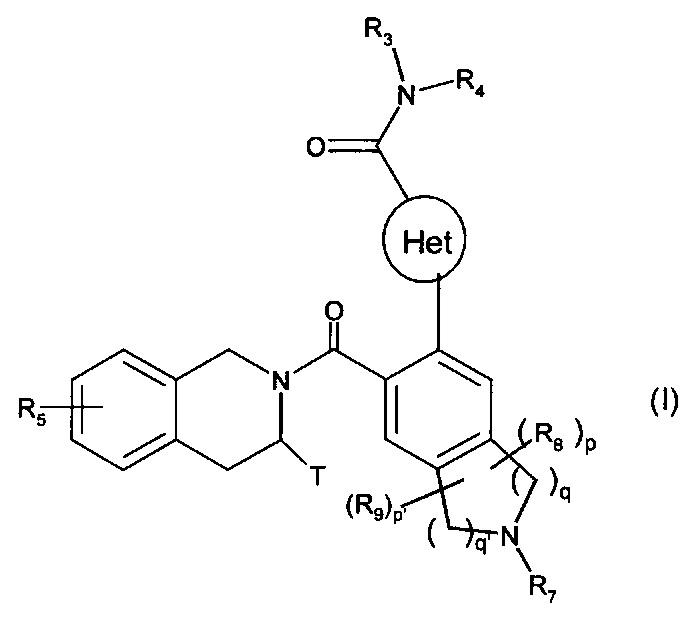
в которой:
 Het представляет собой гетероарильную группу,
Het представляет собой гетероарильную группу,
 Т представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, необязательно замещенную одним - тремя атомами галогена, группу алкил(С1-С4)-NR1R2 или группу алкил(С1-С4)-OR6,
Т представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, необязательно замещенную одним - тремя атомами галогена, группу алкил(С1-С4)-NR1R2 или группу алкил(С1-С4)-OR6,
 R1 и R2 независимо друг от друга представляют собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
R1 и R2 независимо друг от друга представляют собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
или R1 и R2 вместе с атомом азота, несущим их, образуют гетероциклоалкильную группу,
 R3 представляет собой линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C2-C6)алкенильную группу, линейную или разветвленную (C2-C6)алкинильную группу, циклоалкильную группу, (C3-C10)циклоалкил-(С1-С6)алкильную группу, в которой алкильная группа может быть линейной или разветвленной, гетероциклоалкильную группу, арильную группу или гетероарильную группу, при этом предполагается, что один или несколько атомов углерода из групп, определенных выше, или атомов углерода их возможных заместителей могут быть дейтерированы,
R3 представляет собой линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C2-C6)алкенильную группу, линейную или разветвленную (C2-C6)алкинильную группу, циклоалкильную группу, (C3-C10)циклоалкил-(С1-С6)алкильную группу, в которой алкильная группа может быть линейной или разветвленной, гетероциклоалкильную группу, арильную группу или гетероарильную группу, при этом предполагается, что один или несколько атомов углерода из групп, определенных выше, или атомов углерода их возможных заместителей могут быть дейтерированы,
 R4 представляет собой арильную, гетероарильную, циклоалкильную или линейную или разветвленную (С1-С6)алкильную группу, при этом предполагается, что один или несколько атомов углерода из групп, определенных выше, или атомов углерода их возможных заместителей могут быть дейтерированы,
R4 представляет собой арильную, гетероарильную, циклоалкильную или линейную или разветвленную (С1-С6)алкильную группу, при этом предполагается, что один или несколько атомов углерода из групп, определенных выше, или атомов углерода их возможных заместителей могут быть дейтерированы,
 R5 представляет собой атом водорода или атом галогена, линейную или разветвленную (С1-С6)алкильную группу, или линейную или разветвленную (C2-C6)алкокси группу,
R5 представляет собой атом водорода или атом галогена, линейную или разветвленную (С1-С6)алкильную группу, или линейную или разветвленную (C2-C6)алкокси группу,
 R6 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
R6 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
 R7 представляет собой группу, выбранную из R'7, R'7-CO-, R'7-О-СО-, NR'7R''7-CO-, R'7'SO2-, R'7NR''7-SO2-, где R'7 и R''7 независимо друг от друга представляют собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С2-С6)алкенильную группу, линейную или разветвленную (С2-С6)алкинильную группу, циклоалкил, гетероциклоалкил, арильную группу, или гетероарил,
R7 представляет собой группу, выбранную из R'7, R'7-CO-, R'7-О-СО-, NR'7R''7-CO-, R'7'SO2-, R'7NR''7-SO2-, где R'7 и R''7 независимо друг от друга представляют собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С2-С6)алкенильную группу, линейную или разветвленную (С2-С6)алкинильную группу, циклоалкил, гетероциклоалкил, арильную группу, или гетероарил,
 R8 и R9 независимо друг от друга представляют собой оксо группу или атом галогена,
R8 и R9 независимо друг от друга представляют собой оксо группу или атом галогена,
 p и p' независимо друг от друга означают целые числа, равные 0, 1, 2, 3 или 4,
p и p' независимо друг от друга означают целые числа, равные 0, 1, 2, 3 или 4,
 q и q' независимо друг от друга означают целые числа, равные 1, 2 или 3,
q и q' независимо друг от друга означают целые числа, равные 1, 2 или 3,
при этом предполагается, что когда соединение формулы (I) содержит гидрокси группу, эта последняя группа может быть необязательно замещена одной из следующих групп: -PO(OM)(OM'), -PO(OM)(O-M1+), -PO(OM1+)(OM2+), -PO(O-)(O-)М32+, -PO(OM)(O[CH2CH2O]nCH3), или -PO(O-М1+)(O[CH2CH2O]nCH3), где М и М' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C2-C6)алкенильную группу, линейную или разветвленную (C2-C6)алкинильную группу, циклоалкил или гетероциклоалкил, которые оба состоят из 5-6 кольцевых членов, тогда как M1+ и М2+ независимо друг от друга представляют собой фармацевтически приемлемый одновалентный катион, M32+ представляет собой фармацевтически приемлемый двухвалентный катион и n означает целое число от 1 до 5,
при этом также предполагается, что:
- "арил" означает фенильную, нафтильную, бифенильную или инденильную группу,
- "гетероарил" означает любую моно- или бициклическую группу, состоящую из 5-10 кольцевых членов, содержащую по меньшей мере один ароматический фрагмент, и содержащую от 1 до 4 гетероатомов, выбранных из кислорода, серы и азота (включая четвертичный азот),
- "циклоалкил" означает любую моно- или бициклическую, неароматическую, карбоциклическую группу, содержащую от 3 до 10 кольцевых членов, которая может включать конденсированные, мостиковые или спирокольцевые системы,
- "гетероциклоалкил" означает любую моно- или бициклическую, неароматическую, карбоциклическую группу, состоящую из 3-10 кольцевых членов, и содержащую от 1 до 3 гетероатомов, выбранных из кислорода, серы, SO, SO2 и азота, при этом предполагается, что бициклическая группа может быть конденсированного или спирокольцевого типа,
причем арильные, гетероарильные, циклоалкильные и гетероциклоалкильные группы, определенные таким образом, и алкильные, алкенильные, алкинильные и алкокси группы могут быть замещены 1-3 группами, выбранными из необязательно замещенной линейной или разветвленной (С1-С6)алкильной группы; необязательно замещенной линейной или разветвленной (C2-C6)алкенильной группы; необязательно замещенной линейной или разветвленной (C2-C6)алкинильной группы; (C3-C6)спиро; необязательно замещенного линейного или разветвленного (С1-С6)алкокси; (C1-C6)алкил-S-; гидроксила; оксо (или N-оксида, в соответствующих случаях); нитро; циано; -COOR'; -OCOR'; -NR'R''; R'CONR''-; NR'R''CO-; линейного или разветвленного (С1-С6)полигалогеналкила; трифторметокси; (C1-C6)алкилсульфонила; галогена; необязательно замещенного арила; необязательно замещенного гетероарила; необязательно замещенного арилокси; необязательно замещенного арилтио; необязательно замещенного циклоалкила или необязательно замещенного гетероциклоалкила, при этом предполагается, что R' и R'' независимо друг от друга представляют собой атом водорода, необязательно замещенную линейную или разветвленную (С1-С6)алкильную группу или арильную группу,
их энантиомерам и диастереоизомерам, и их солям присоединения с фармацевтически приемлемой кислотой или основанием.
Более предпочтительно, настоящее изобретение относится к соединениям формулы (IA):
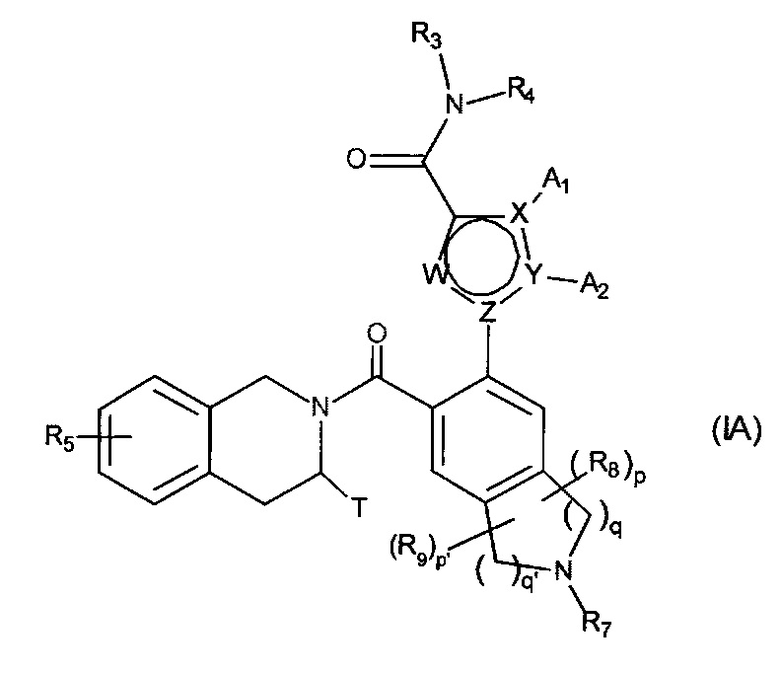
в которой:
 W представляет собой группу C-A3 или атом азота,
W представляет собой группу C-A3 или атом азота,
 X, Y и Z представляют собой атом углерода или атом азота, при этом предполагается, что только один из них представляет собой атом азота, тогда как две другие представляют собой атомы углерода,
X, Y и Z представляют собой атом углерода или атом азота, при этом предполагается, что только один из них представляет собой атом азота, тогда как две другие представляют собой атомы углерода,
 A1, А2 и A3 независимо друг от друга представляют собой атом водорода или атом галогена, линейную или разветвленную (C1-C6)полигалогеналкильную группу, линейную или разветвленную (C1-C6)алкильную группу или циклоалкильную группу,
A1, А2 и A3 независимо друг от друга представляют собой атом водорода или атом галогена, линейную или разветвленную (C1-C6)полигалогеналкильную группу, линейную или разветвленную (C1-C6)алкильную группу или циклоалкильную группу,
или A3 представляет собой атом водорода (когда W представляет собой группу C-A3), тогда как A1 и А2 вместе с атомами, несущими их, образуют необязательно замещенное, ароматическое или неароматическое кольцо Су, состоящее из 5, 6 или 7 кольцевых членов, которое может содержать от 1 до 4 гетероатомов, выбранных независимо из кислорода, серы и азота, при этом предполагается, что рассматриваемый азот может быть замещен группой, представляющей собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу или группу -C(O)-O-Alk, где Alk означает линейную или разветвленную (С1-С6)алкильную группу,
или W представляет собой атом азота, тогда как A1 и A2 вместе с атомами, несущими их, образуют необязательно замещенное, ароматическое или неароматическое кольцо Су, состоящее из 5, 6 или 7 кольцевых членов, которое может содержать от 1 до 4 гетероатомов, выбранных независимо из кислорода, серы и азота, при этом предполагается, что рассматриваемый азот может быть замещен группой, представляющей собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу или группу -C(O)-O-Alk, где Alk означает линейную или разветвленную (С1-С6)алкильную группу,
 Т представляет собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, необязательно замещенную одним - тремя атомами галогена, группу алкил(C1-C4)-NR1R2, или группу алкил(С1-C4)-OR6,
Т представляет собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, необязательно замещенную одним - тремя атомами галогена, группу алкил(C1-C4)-NR1R2, или группу алкил(С1-C4)-OR6,
 R1 и R2 независимо друг от друга представляют собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
R1 и R2 независимо друг от друга представляют собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
или R1 и R2 вместе с атомом азота, несущим их, образуют гетероциклоалкил,
 R3 представляет собой линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C2-C6)алкенильную группу, линейную или разветвленную (C2-C6)алкинильную группу, циклоалкильную группу, (C3-C10)циклоалкил-(С1-С6)алкильную группу, в которой алкильная группа может быть линейной или разветвленной, гетероциклоалкильную группу, арильную группу или гетероарильную группу, при этом предполагается, что один или несколько атомов углерода из групп, определенных выше, или атомов углерода их возможных заместителей могут быть дейтерированы,
R3 представляет собой линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C2-C6)алкенильную группу, линейную или разветвленную (C2-C6)алкинильную группу, циклоалкильную группу, (C3-C10)циклоалкил-(С1-С6)алкильную группу, в которой алкильная группа может быть линейной или разветвленной, гетероциклоалкильную группу, арильную группу или гетероарильную группу, при этом предполагается, что один или несколько атомов углерода из групп, определенных выше, или атомов углерода их возможных заместителей могут быть дейтерированы,
 R4 представляет собой арильную, гетероарильную, циклоалкильную или линейную или разветвленную (С1-С6)алкильную группу, при этом предполагается, что один или несколько атомов углерода из групп, определенных выше, или атомов углерода их возможных заместителей могут быть дейтерированы,
R4 представляет собой арильную, гетероарильную, циклоалкильную или линейную или разветвленную (С1-С6)алкильную группу, при этом предполагается, что один или несколько атомов углерода из групп, определенных выше, или атомов углерода их возможных заместителей могут быть дейтерированы,
 R5 представляет собой атом водорода или атом галогена, линейную или разветвленную (С1-С6)алкильную группу, или линейную или разветвленную (С1-С6)алкокси группу,
R5 представляет собой атом водорода или атом галогена, линейную или разветвленную (С1-С6)алкильную группу, или линейную или разветвленную (С1-С6)алкокси группу,
 R6 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
R6 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
 R7 представляет собой группу, выбранную из R'7, R'7-СО-, R'7-О-СО, NR'7R''7-CO-, R'7-SO2-, R'7-NR''7-SO2-, где R'7 и R''7 независимо друг от друга представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C2-C6)алкенильную группу, линейную или разветвленную (C2-C6)алкинильную группу, циклоалкил, гетероциклоалкил, арильную группу, или гетероарил,
R7 представляет собой группу, выбранную из R'7, R'7-СО-, R'7-О-СО, NR'7R''7-CO-, R'7-SO2-, R'7-NR''7-SO2-, где R'7 и R''7 независимо друг от друга представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C2-C6)алкенильную группу, линейную или разветвленную (C2-C6)алкинильную группу, циклоалкил, гетероциклоалкил, арильную группу, или гетероарил,
 R8 и R9 независимо друг от друга представляют собой оксо группу или атом галогена,
R8 и R9 независимо друг от друга представляют собой оксо группу или атом галогена,
 p и p' независимо друг от друга означают целые числа, равные 0, 1, 2, 3 или 4,
p и p' независимо друг от друга означают целые числа, равные 0, 1, 2, 3 или 4,
 q и q' независимо друг от друга означают целые числа, равные 1, 2 или 3,
q и q' независимо друг от друга означают целые числа, равные 1, 2 или 3,
при этом предполагается, что когда соединение формулы (I) содержит гидрокси группу, эта последняя группа может быть необязательно замещена одной из следующих групп: -PO(OM)(OM'), -PO(OM)(O-M1+), -PO(O-M1+)(O-M2+), -PO(O-)(O-)М32+, -PO(OM)(O[CH2CH2O]nCH3), или -PO(O-М1+)(O[CH2CH2O]nCH3), где М и М' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C2-C6)алкенильную группу, линейную или разветвленную (C2-C6)алкинильную группу, циклоалкил или гетероциклоалкил, которые оба состоят из 5-6 кольцевых членов, тогда как M1+ и М2+ независимо друг от друга представляют собой фармацевтически приемлемый одновалентный катион, М32+ представляет собой фармацевтически приемлемый двухвалентный катион и n означает целое число от 1 до 5,
при этом также предполагается, что:
- "арил" означает фенильную, нафтильную, бифенильную или инденильную группу,
- "гетероарил" означает любую моно- или бициклическую группу, состоящую из 5-10 кольцевых членов, содержащую по меньшей мере один ароматический фрагмент, и содержащую от 1 до 4 гетероатомов, выбранных из кислорода, серы и азота (включая четвертичный азот),
- "циклоалкил" означает любую моно- или бициклическую, неароматическую, карбоциклическую группу, содержащую от 3 до 10 кольцевых членов, которая может включать конденсированные, мостиковые или спирокольцевые системы,
- "гетероциклоалкил" означает любую моно- или бициклическую, неароматическую, карбоциклическую группу, состоящую из 3-10 кольцевых членов, и содержащую от 1 до 3 гетероатомов, выбранных из кислорода, серы, SO, SO2 и азота, при этом предполагается, что бициклическая группа может быть конденсированного или спирокольцевого типа,
причем арильные, гетероарильные, циклоалкильные и гетероциклоалкильные группы, определенные таким образом, и алкильные, алкенильные, алкинильные и алкокси группы могут быть замещены 1-3 группами, выбранными из необязательно замещенной линейной или разветвленной (С1-С6)алкильной группы; необязательно замещенной линейной или разветвленной (C2-C6)алкенильной группы; необязательно замещенной линейной или разветвленной (C2-C6)алкинильной группы; (C3-C6)спиро; необязательно замещенного линейного или разветвленного (С1-С6)алкокси; (C1-C6)алкил-S-; гидроксила; оксо (или N-оксида, в соответствующих случаях); нитро; циано; -COOR'; -OCOR''; -NR'R''; R'CONR''-; NR'R''CO-; линейного или разветвленного (С1-С6)полигалогеналкила; трифторметокси; (C1-С6)алкилсульфонила; галогена; необязательно замещенного арила; необязательно замещенного гетероарила; необязательно замещенного арилокси; необязательно замещенного арилтио; необязательно замещенного циклоалкила или необязательно замещенного гетероциклоалкила, при этом предполагается, что R' и R'' независимо друг от друга представляют собой атом водорода, необязательно замещенную линейную или разветвленную (С1-С6)алкильную группу или арильную группу,
причем фрагмент Су, определенный для формулы (IA), может быть замещен 1-3 группами, выбранными из линейного или разветвленного (C1-C6)алкила, линейного или разветвленного (С1-С6)полигалогеналкила, гидрокси, линейного или разветвленного (С1-С6)алкокси, СООН, NR1'R1'' и галогена, при этом предполагается, что R1' и R1'' имеют те же определения, что и группы R' и R'' упомянутые выше,
их энантиомерам и диастереоизомерам, и их солям присоединения с фармацевтически приемлемой кислотой или основанием.
Соединения формулы (IA-1), их энантиомеры и диастереоизомеры, и их соли присоединения с фармацевтически приемлемой кислотой или основанием являются более предпочтительными:
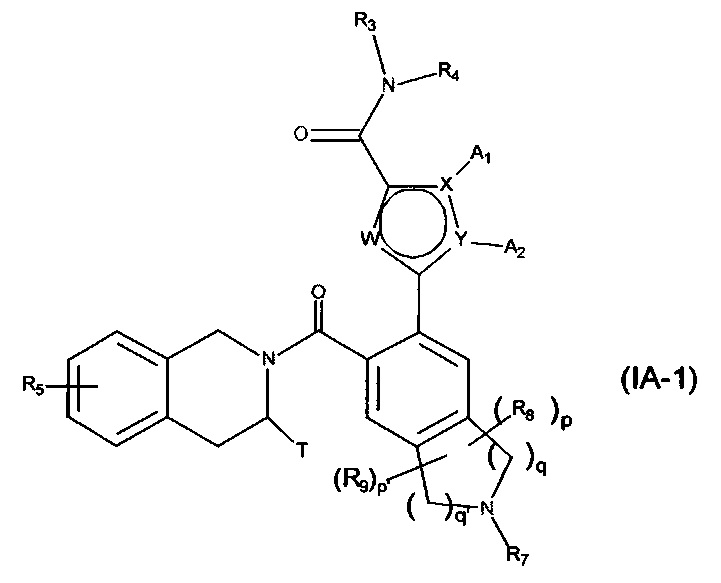
в которой X, Y, W, А1, А2, R3, R4, R5, R7, R8, R9, Т, p, p', q и q' являются такими, как определено для формулы (IA).
Соединения формулы (IA-2), их энантиомеры и диастереоизомеры, и их соли присоединения с фармацевтически приемлемой кислотой или основанием, являются еще более предпочтительными:
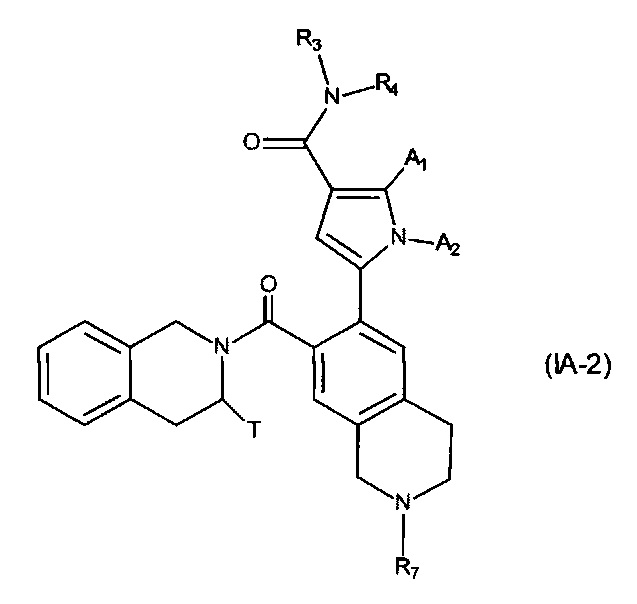
в которой A1, А2, R3, R4, R7 и T являются такими, как определено для формулы (IA).
Из числа фармацевтически приемлемых кислот могут быть упомянуты, без какого-либо ограничения, хлористоводородная кислота, бромистоводородная кислота, серная кислота, фосфоновая кислота, уксусная кислота, трифторуксусная кислота, молочная кислота, пировиноградная кислота, малоновая кислота, янтарная кислота, глутаровая кислота, фумаровая кислота, винная кислота, малеиновая кислота, лимонная кислота, аскорбиновая кислота, щавелевая кислота, метансульфоновая кислота, камфорная кислота и т.д.
Из числа фармацевтически приемлемых оснований могут быть упомянуты, без какого-либо ограничения, гидроксид натрия, гидроксид калия, триэтиламин, трет-бутиламин и т.д.
В предпочтительном варианте осуществления изобретения R4 представляет собой фенил, замещенный в пара-положении группой формулы -OРО(OM)(OM'), -OPO(OM)(O-M1+), -OPO(O-M1+)(OM2+), -ОРО(O-)(O-)М32+, -ОРО(OM)(O[CH2CH2O]nCH3), или -OРО(O-М1+)(O[CH2CH2O]nCH3), где М и М' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (C2-C6)алкенильную группу, линейную или разветвленную (C2-C6)алкинильную группу, циклоалкил или гетероциклоалкил, которые оба состоят из 5-6 кольцевых членов, тогда как M1+ и М2+ независимо друг от друга представляют собой фармацевтически приемлемый одновалентный катион, М32+ представляет собой фармацевтически приемлемый двухвалентный катион и n означает целое число от 1 до 5, при этом предполагается, что фенильная группа может быть необязательно замещена одним или несколькими атомами галогена.
Группа Het предпочтительно представляет собой одну из следующих групп: тетрагидроиндолизин, индолизин или 1,2-диметил-1H-пиррол. Группа 1,2-диметил-1H-пиррол является более предпочтительной. Альтернативно, группа 5,6,7,8-тетрагидроиндолизин является более предпочтительной.
В предпочтительных соединениях изобретения, q=1 и q'=1. Альтернативно, q=2 и q'=1.
Предпочтительно Т представляет собой атом водорода, метильную группу, (морфолин-4-ил)алкильную группу, диметиламинометильную группу, или (алкилпиперазин-1-ил)алкильную группу. Более предпочтительно Т представляет собой метильную группу, (морфолин-4-ил)метильную группу, 3-(морфолин-4-ил)пропильную группу или (4-метилпиперазин-1-ил)метильную группу. Еще более предпочтительно T представляет собой метильную группу. Альтернативно, Т более предпочтительно представляет собой (морфолин-4-ил)метильную группу.
В предпочтительных соединениях изобретения R3 представляет собой линейную или разветвленную (С1-С6)алкильную группу, арильную группу или гетероарильную группу. Более конкретно, R3 означает группу, выбранную из фенила, метила, этила, пропила, бутила, 1-метил-1H-пирроло[2,3-b]пиридина или 5-циано-1,2-диметил-1H-пиррола. Более предпочтительно R3 представляет собой метильную, пропильную или бутильную группу. Еще более предпочтительно R3 представляет собой метильную группу.
Предпочтительно R4 представляет собой линейную или разветвленную (C1-C6)алкильную группу (более конкретно бутил) или арильную группу. R4 предпочтительно представляет собой необязательно замещенную фенильную группу.
Предпочтение отдают группе R4, представляющей собой 4-гидроксифенил.
Предпочтительно R7 представляет собой группу R'7-СO- или R'7-О-СO-.
В предпочтительных соединениях изобретения R'7 представляет собой необязательно замещенный арил, необязательно замещенный циклоалкил или необязательно замещенный алкил. Более предпочтительно R'7 представляет собой необязательно замещенную нафталиновую, фенильную или индольную группу. Наиболее предпочтительными заместителями для фенильной группы являются необязательно замещенный алкил, циано, алкинил, галоген, необязательно замещенный алкокси, или -NR'R''. Еще более предпочтительными заместителями для фенильной группы являются метил, этил, метокси, хлор, бром, циано, 2-диметиламиноэтиламино, этинил, 2-диметиламиноэтокси, 2-(диметиламино)этил(метил)амино, диметилкарбамоилэтил.
В предпочтительном варианте, p=p'=0.
В частности, изобретение относится к следующим соединениям:
• N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид;
• Фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• Гидрохлорид фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата;
• Гидрохлорид фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата;
• Гидрохлорид 4-метилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата;
• 2-Метилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-Метоксифенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-Хлорфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-Этилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-Цианофенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 2-Метоксифенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-Метилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-Хлорфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-Цианофенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-Цианофенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-{[2-(Диметиламино)этил]амино}фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• Фенил 6-{4-[(4-гидроксифенил)(пропил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• Фенил 6-{4-[бутил(4-гидроксифенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• N-Бутил-N-(4-гидроксифенил)-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид;
• 3-[2-(Диметиламино)этокси]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-{[2-(Диметиламино)этил](метил)амино}фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-Этинилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• Нафталин-2-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 1H-Индол-5-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 3-[2-(Диметилкарбамоил)этил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-Бромфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• (1r,4r)-4-{[(трет-Бутокси)карбонил]амино}циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• 4-[2-(Диметилкарбамоил)этил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
• Циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат.
Изобретение также относится к способу получения соединений формулы (I), который отличается тем, что в качестве исходного вещества применяют соединение формулы (II):
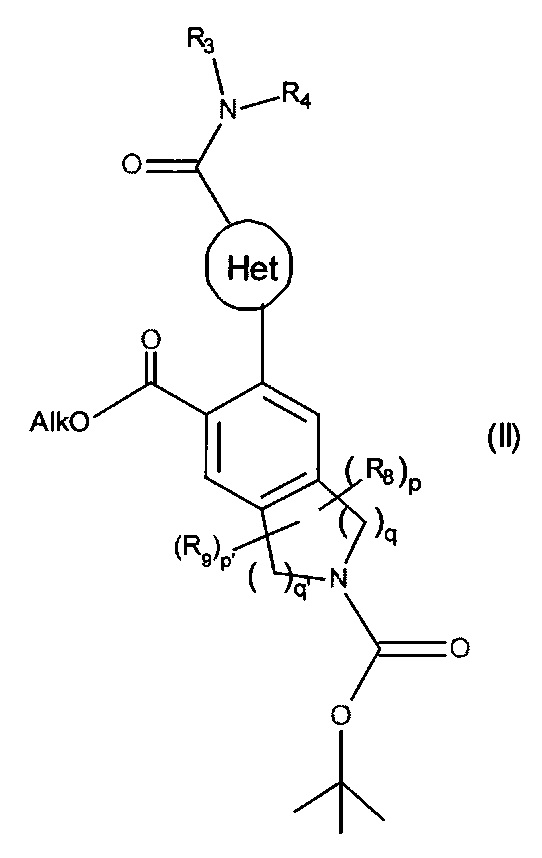
в которой Het, R3, R4, R8, R9, p, p', q и q' являются такими, как определено для формулы (I) и Alk представляет собой линейную или разветвленную (C1-C6)алкильную группу,
причем сложноэфирную функцию соединения формулы (II) гидролизуют с получением соответствующей карбоновой кислоты, которую затем подвергают пептидному сочетанию с соединением формулы (III):
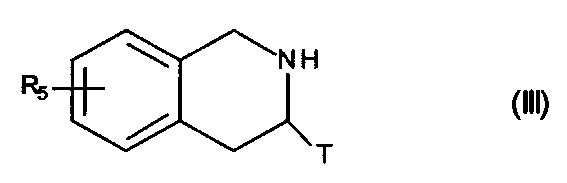
в которой R5 и T являются такими, как определено для формулы (I),
с получением соединения формулы (IV):
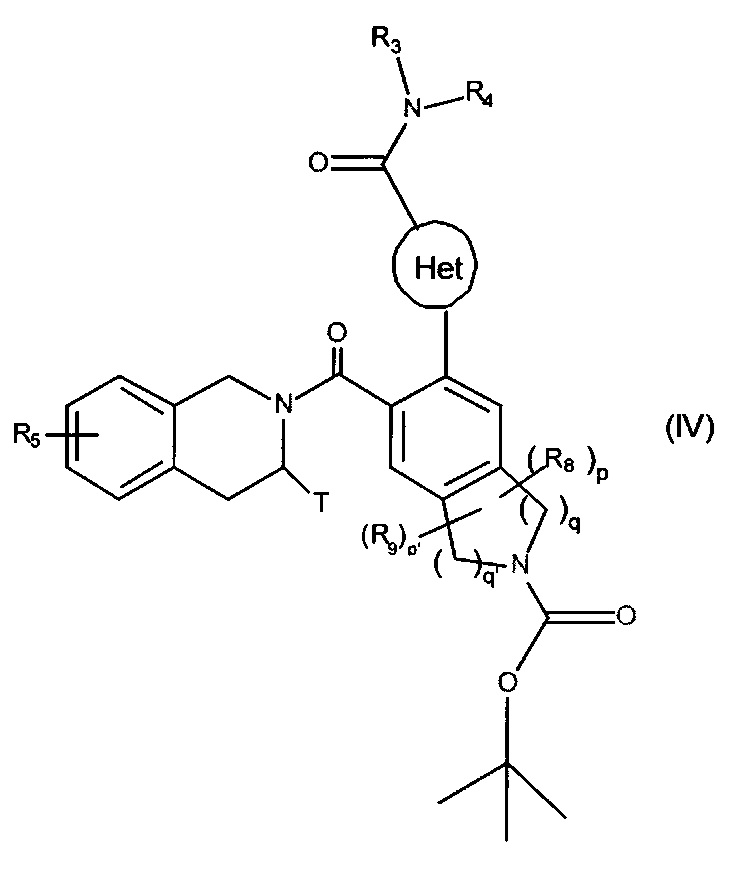
в которой Het, R3, R4, R5, R8, R9, Т, p, p', q и q' являются такими, как определено для формулы (I),
с соединения формулы (IV) снимают защиту и подвергают реакции ацилирования или сульфонилирования, и необязательно подвергают действию пирофосфатного или фосфонатного производного в основных условиях с получением соединения формулы (I),
которое можно очистить в соответствии с обычными методиками разделения, которое превращают, при необходимости, в его соли присоединения с фармацевтически приемлемой кислотой или основанием и которое необязательно разделяют на его изомеры в соответствии с обычными методиками разделения,
при этом предполагается, что в любое время, признанное подходящим в ходе описанного выше способа, некоторые группы (гидрокси, амино…) исходных реагентов или промежуточных соединений синтеза можно защитить и затем снять с них защиту в соответствии с требованиями синтеза.
Более конкретно, изобретение также относится к способу получения соединений формулы (IA-1), который отличается тем, что в качестве исходного вещества применяют соединение формулы (V):
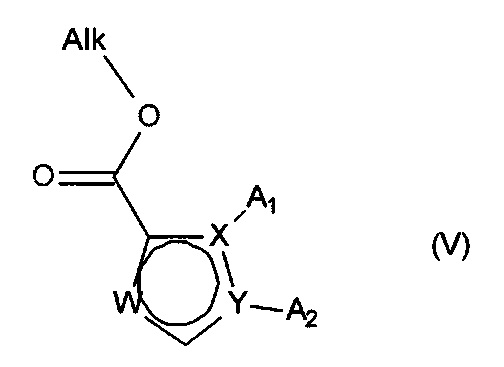
в которой X, Y, W, A1 и А2 являются такими, как определено для формулы (IA), и Alk представляет собой линейную или разветвленную (C1-C6) алкильную группу,
причем сложноэфирную функцию соединения формулы (V) гидролизуют с получением карбоновой кислоты или соответствующего карбоксилата, которую(-ый) можно превратить в производное кислоты, такое как ацилхлорид или соответствующий ангидрид, и затем подвергают сочетанию с амином NHR3R4, где R3 и R4 имеют те же значения, что и в случае формулы (IA), с получением соединения формулы (VI):
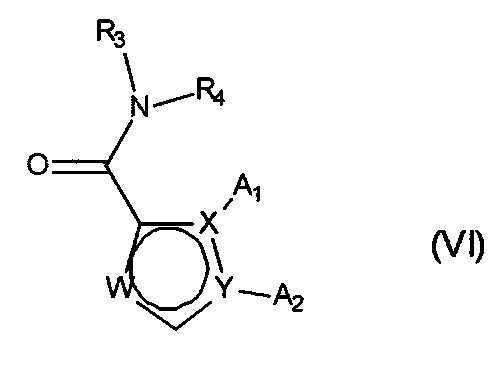
в которой X, Y, W, A1, A2, R3 и R4 являются такими, как определено для формулы (IA),
соединение формулы (VI) затем галогенируют и далее превращают в соответствующее борогидридное производное формулы (VII):
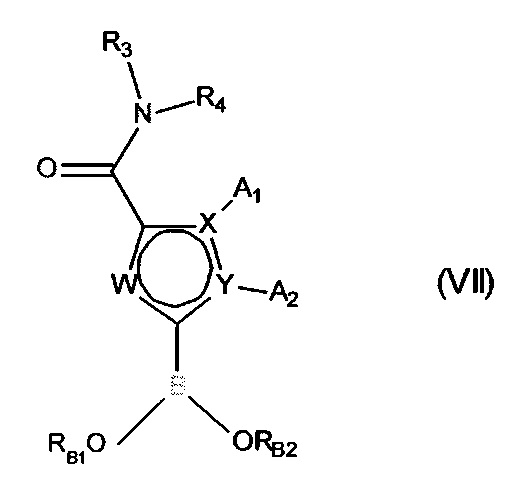
в которой X, Y, W, A1, A2, R3 и R4 являются такими, как определено для формулы (IA), и
RB1 и RB2 представляют собой водород, линейную или разветвленную (C1-C6) алкильную группу, или RB1 и RB2 вместе с атомами кислорода, несущими их, образуют необязательно метилированное кольцо,
соединение формулы (VII) далее подвергают сочетанию с соединением формулы (VIII):
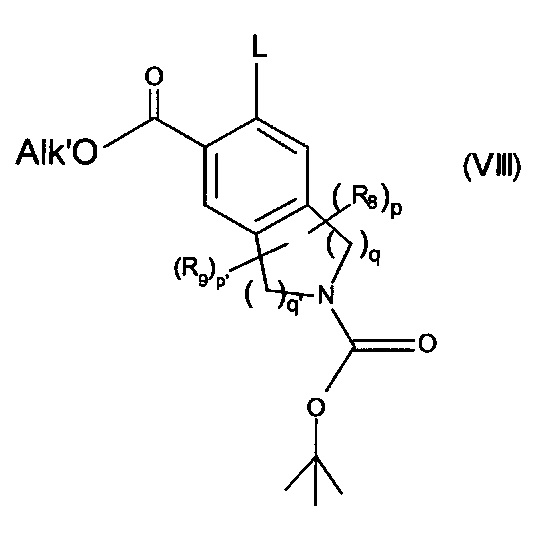
в которой R8, R9, p, p', q и q' являются такими, как определено для формулы (IA), и
Alk' представляет собой линейную или разветвленную (C1-C6) алкильную группу, и
L представляет собой уходящую группу, выбранную из галогена или сульфоната,
с получением соединения формулы (IIА-1):
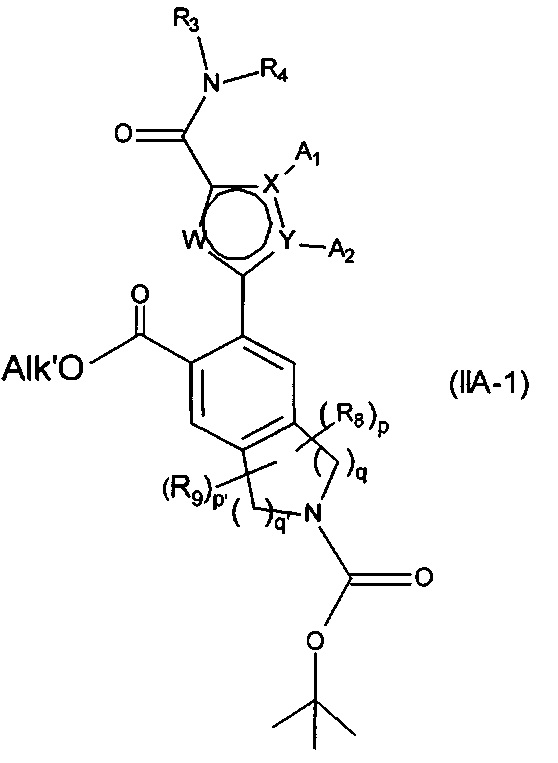
в которой X, Y, W, A1, А2, R3, R4, R8, R9, p, p', q, и q' являются такими, как определено для формулы (IA), и Alk' является таким, как определено ранее,
сложноэфирную функцию соединения формулы (IIА-1) гидролизуют с получением соответствующей карбоновой кислоты, которую затем подвергают пептидному сочетанию с соединением формулы (III):
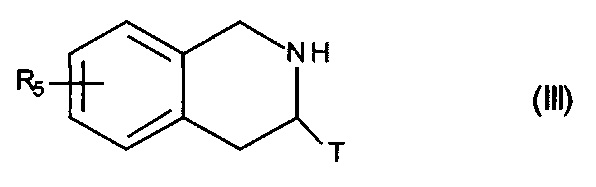
в которой R5 и T являются такими, как определено для формулы (IA), с получением соединения формулы (IVA-1):
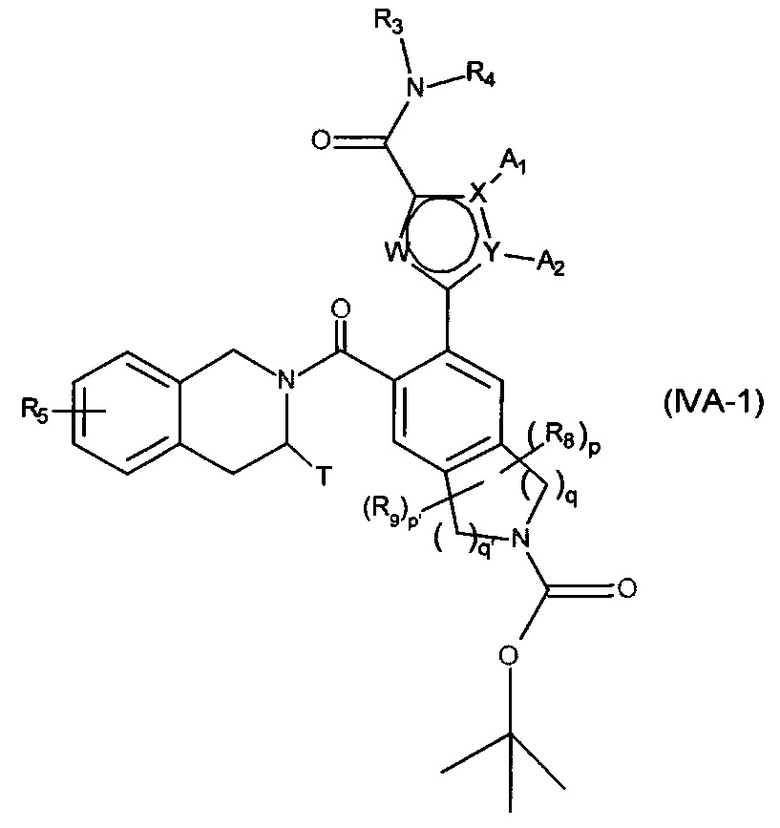
в которой X, Y, W, A1, А2, R3, R4, R5, R8, R9, T, p, p', q, q' являются такими, как определено для формулы (IA),
с соединения формулы (IVA-1) снимают защиту и подвергают реакции ацилирования или сульфонилирования, и необязательно подвергают действию пирофосфатного или фосфонатного производного в основных условиях с получением соединения формулы (IA-1):
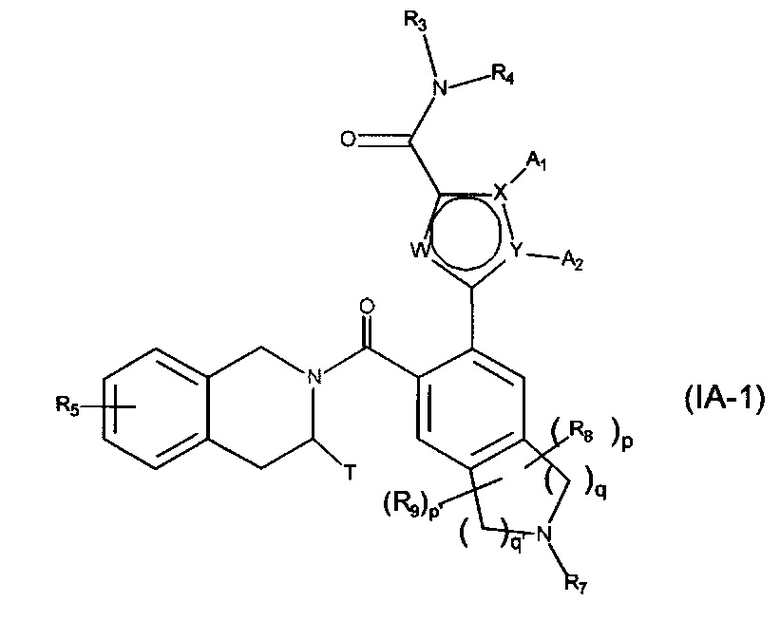
в которой X, Y, W, A1, А2, R3, R4, R5, R7, R8, R9, Т, p, р', q и q' являются такими, как определено для формулы (IA),
которое можно очистить в соответствии с обычными методиками разделения, которое превращают, при необходимости, в его соли присоединения с фармацевтически приемлемой кислотой или основанием и которое необязательно разделяют на его изомеры в соответствии с обычными методиками разделения,
при этом предполагается, что в любое время, признанное подходящим в ходе описанного выше способа, некоторые группы (гидрокси, амино...) исходных реагентов или промежуточных соединений синтеза можно защитить и затем снять с них защиту в соответствии с требованиями синтеза.
В частности, когда одна из групп R3 или R4 амина NHR3R4 замещена гидрокси функцией, последнюю можно подвергнуть реакции защиты заблаговременно перед сочетанием с карбоновой кислотой, образованной из соединения формулы (V), или с соответствующим производным таковой кислоты, где полученную в результате защищенную функцию затем подвергают реакции снятия защиты на последней стадии способа.
Соединения формул (III), (V), (VIII) и амин NHR3R4 либо доступны для приобретения, либо могут быть получены специалистом в данной области техники с использованием обычных химических реакций, описанных в литературе.
Фармакологическое исследование соединений изобретения показало, что они обладают проапоптотическими свойствами. Способность реактивировать апоптотический процесс в раковых клетках представляет большой терапевтический интерес для лечения злокачественных новообразований и аутоиммунных заболеваний и заболеваний иммунной системы.
Более конкретно, соединения в соответствии с изобретением будут полезны для лечения хемо- или радиорезистентных злокачественных новообразований, и в случае злокачественных заболеваний крови, и в случае мелкоклеточного рака легкого.
Из числа намеченных противоопухолевых терапий могут быть упомянуты, без какого-либо ограничения, терапия рака мочевого пузыря, головного мозга, молочной железы и матки, хронических лимфоидных лейкозов, рака ободочной кишки, пищевода и печени, лимфобластных лейкозов, неходжкинских лимфом, меланом, злокачественных заболеваний крови, миелом, рака яичников, немелкоклеточного рака легкого, рака предстательной железы и мелкоклеточного рака легкого. Из числа неходжкинских лимфом предпочтительно могут быть упомянуты фолликулярные лимфомы, лимфомы из клеток мантийной зоны, диффузные В-крупноклеточные лимфомы, мелкоклеточные лимфоцитарные лимфомы и В-клеточные лимфомы из клеток маргинальной зоны.
Настоящее изобретение также относится к фармацевтическим композициям, содержащим по меньшей мере одно соединение формулы (I) в комбинации с одним или несколькими фармацевтически приемлемыми наполнителями.
Из числа фармацевтических композиций в соответствии с изобретением могут быть упомянуты более конкретно те, которые подходят для перорального, парентерального, назального, чрес- или транскожного, ректального, перлингвального, офтальмологического или респираторного введения, в особенности таблетки или драже, сублингвальные таблетки, саше, пакеты, капсулы, глоссеты, пастилки, суппозитории, кремы, мази, гели для кожи и питьевые или инъекционные ампулы.
Дозировка варьируется в зависимости от пола, возраста и веса пациента, пути введения, природы терапевтического показания, или каких-либо сопутствующих лечений, и находится в диапазоне от 0.01 мг до 1 г в 24 часа за одно или несколько введений.
Кроме того, настоящее изобретение также относится к ассоциации соединения формулы (I) с противоопухолевым средством, выбранным из генотоксичных средств, митотических ядов, антиметаболитов, ингибиторов протеасом, ингибиторов киназ и антител, и также к фармацевтическим композициям, содержащим такой тип ассоциации, и их применению для изготовления лекарственных средств для применения для лечения злокачественного новообразования.
Соединения изобретения также можно применять в ассоциации с радиотерапией для лечения злокачественного новообразования.
В конечном счете, соединения изобретения могут быть связаны с моноклональными антителами или их фрагментами, или связаны с каркасными белками, которые могут относиться или не относиться к моноклональным антителам.
Фрагменты антител следует понимать как фрагменты Fv, scFv, Fab, F(ab')2, F(ab'), scFv-Fc типа или диатела, которые обычно имеют такую же специфичность связывания, что и антитело, из которого они происходят. В соответствии с настоящим изобретением, фрагменты антител изобретения могут быть получены исходя из антител с помощью методов, таких как переваривание ферментами, такими как пепсин или папаин, и/или посредством расщепления дисульфидных мостиков с помощью химического восстановления. Другим путем, фрагменты антител, включенных в настоящее изобретение, могут быть получены с использованием методик генетической рекомбинации, также хорошо известных специалисту в данной области техники или даже посредством пептидного синтеза с помощью, например, автоматических пептидных синтезаторов, таких как те, которые поставляются компанией Applied Biosystems, и т.д.
Под каркасными белками, которые могут относиться или не относиться к моноклональным антителам, понимают белок, который содержит или не содержит укладку цепи иммуноглобулинов и который обеспечивает способность к связыванию, такую же, как и у моноклонального антитела. Специалисту в данной области техники известно, каким образом выбрать каркас белка. В частности, известно, что должен быть выбран такой каркас, который будет демонстрировать несколько следующих отличительных признаков (Skerra A., J. Mol. Recogn., 13, 2000, 167-187): хорошая филогенетическая консервативность, прочная архитектура с хорошо известной трехмерной молекулярной организацией (как, например, на основании кристаллографии или ЯМР), небольшой размер, отсутствие или лишь низкая степень посттрансляционных модификаций, простота получения, экспрессии и очистки. Таким каркасным белком может быть, без ограничения перечисленным, структура, выбранная из группы, состоящей из фибронектина и предпочтительно 10-го домена фибронектина типа III (FNfn10), липокалина, антикалина (Skerra A., J. Biotechnol., 2001, 74 (4): 257-75), белка Z, производного из домена B стафилококкового белка A, тиоредоксина A или любого белка с повторяющимся доменом, таким как "анкириновый повтор" (Kohl и др., PNAS, 2003, т. 100, №4, 1700-1705), "армадилло повтор", "богатый лейцином повтор" или "тетратрикопептидный повтор". Также можно упомянуть каркас, производный из токсинов (как, например, токсины скорпионов, насекомых, растений или моллюсков) или белковых ингибиторов нейрональной синтазы оксида азота (PIN).
Следующие Синтезы и Примеры иллюстрируют изобретение, но не ограничивают его каким-либо образом.
Общие методики
Все реагенты, полученные из коммерческих источников, использовали без дополнительной очистки. Безводные растворители получали из коммерческих источников и использовали без дополнительной сушки. Флэш-хроматографию выполняли на приборе ISCO CombiFlash Rf 200i с предварительно набитыми силикагелевыми картриджами (SiliaSep™ F60 (40-63 мкм, 60Å). Тонкослойную хроматографию проводили на 5×10 см пластинах, покрытых силикагелем Merck Туре 60 F254. Нагрев микроволновым излучением выполняли в приборе СЕМ Discover® SP.
Аналитическая ЖХ-МС
Соединения настоящего изобретения характеризовали с помощью жидкостной хроматографии высокого разрешения-масс-спектроскопии (ЖХВР-МС) либо на приборе Agilent HP 1200 Rapid Resolution Mass detector 6140, многомодовый источник, m/z диапазон 150-1000 а.е.м., либо на приборе Agilent HP 1100 Mass detector 1946D, ESI источник, m/z диапазон 150-1000 а.е.м. Условия и методы, перечисленные ниже, идентичны для обоих приборов.
Детектирование: УФ детектирование на длине волны 230, 254 и 270 нм.
Объем введенной пробы: 2 мкл
Подвижные фазы: А - Вода + 10 мМ / формиат аммония + 0.08% (об./об.) муравьиной кислоты при рН прибл. 3.5; В - 95% Ацетонитрил + 5% А + 0.08% (об./об.) муравьиной кислоты
Метод А (3.75 мин; ионизация либо в режиме положительных ионов (положит.), либо в режиме положительных и отрицательных ионов (положит./отриц.))
Колонка: Gemini 5 мкм, С18, 30 мм×4.6 мм (Phenomenex).
Температура: 35°C.
Градиент:
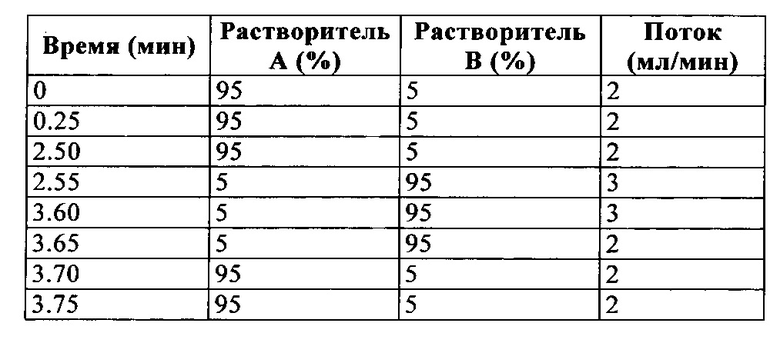
Метод В (1.9 мин; ионизация либо в режиме положительных ионов (положит.), либо в режиме положительных и отрицательных ионов (положит./отриц.))
Колонка: Gemini 5 мкм, С18, 30 мм×4.6 мм (Phenomenex).
Температура: 35°C.
Градиент:
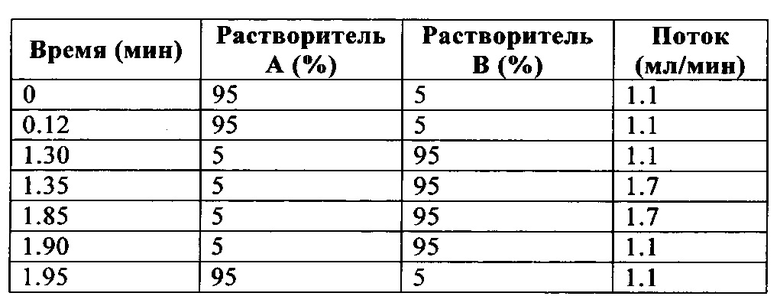
Препаративная ЖХВР
Некоторые соединения изобретения очищали с помощью препаративной ЖХВР. Очистку выполняли на системе автоочистки Waters FractionLynx MS, с колонкой Gemini® 5 мкм C 18(2), 100 мм×20 мм в.д. от Phenomenex, работая с расходом 20 см3 мин-1 с УФ детектированием на диодной матрице (210-400 нм) и сбором веществ по массе. Используемые для каждого соединения градиенты показаны в таблице 1.
При рН 4: растворитель А=10 мМ ацетат аммония в воде квалификации «для ЖХВР» + 0.08% об./об. муравьиной кислоты. Растворитель В=95% об./об. ацетонитрила квалификации «для ЖХВР» + 5% об./об. растворителя А + 0.08% об./об. муравьиной кислоты.
При pH 9: растворитель А=10 мМ ацетат аммония в воде квалификации «для ЖХВР» + 0.08% об./об. раствора аммиака. Растворитель В=95% об./об. ацетонитрила квалификации «для ЖХВР» + 5% об./об. растворителя А + 0.08% об./об. раствора аммиака.
Масс-спектрометр представлял собой спектрометр Waters Micromass ZQ2000, работающий в режиме электрораспылительной ионизации с генерированием положительных и отрицательных ионов, и с диапазоном сканирования молекулярных масс от 150 до 1000.
Синтез 1а: 2-трет-Бутил 7-метил 6-[(нонафторбутансульфонил)окси]-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
Стадия A: трет-Бутил 7-формил-6-гидрокси-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
трет-Бутил 6-гидрокси-3,4-дигидро-1H-изохинолин-2-карбоксилат (15.0 г, 0.06 моль) растворяют в 96 мл 7% раствора диметоксимагния в метаноле (0.06 моль) и перемешивают в течение 30 минут при комнатной температуре. Затем реакционную смесь концентрируют и упаривают совместно с толуолом с получением порошка, который затем суспендируют в толуоле (300 мл). Добавляют параформальдегид (6.32 г, 0.21 моль) и суспензию нагревают с обратным холодильником. Добавляют еще 6.32 г параформальдегида (0.21 моль) и смеси дают перемешиваться в течение 48 ч. Реакционную смесь охлаждают до комнатной температуры, разбавляют этилацетатом и промывают 1 н. HCl. Органическую фазу отделяют, а водную фазу промывают этилацетатом. Органику объединяют, фильтруют через набивку целита и фильтрат промывают солевым раствором, сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Сырое вещество вносят в дихлорметан, загружают на изолют и очищают на CombiFlash (220 г, силикагель, дихлорметан - 3% метанол/дихлорметан) с получением нежелательного региоизомера прямо в виде масла. Оставшиеся фракции объединяют, концентрируют до твердого вещества, и повторно очищают на CombiFlash (220 г, силикагель, изогексан - 30% этилацетат/изогексан). Продукт получают в виде смеси с соотношением компонентов 2:1 в пользу требуемого региоизомера.
ЖХ/МС (C15H19NO4) 177 [М-Вос+Н]+; RT 1.29 (Метод B)
Стадия B: 2-трет-Бутил 7-метил 6-гидрокси-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
К перемешиваемому раствору 6.4 г смеси региоизомеров альдегида, полученного на Стадии A, (приблиз. 4.22 г, 15.23 ммоль) в метаноле (250 мл) добавляют цианид натрия (0.75 г, 0.02 моль). Через 1 минуту добавляют активированный диоксид марганца (10.03 г, 115.4 ммоль) и реакционную смесь перемешивают при температуре окружающей среды в течение ночи. Реакционную смесь фильтруют через набивку целита и концентрируют. Сырое вещество очищают на CombiFlash (220 г, силикагель, изогексан - 20% этилацетат/изогексан) и сушат в вакууме с получением твердого вещества.
ЖХ/МС (C16H21NO5) 208 [М-Вос+Н]+; RT 1.40 (Метод В)
Стадия С: 2-трет-Бутил 7-метил 6-[(нонафторбутансульфонил)окси]-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
К раствору фенола, полученного на Стадии B, (5.97 г, 19.41 ммоль) в дихлорметане (10 мл), охлажденному до 0°C, добавляют триэтиламин (8.1 мл, 58.23 ммоль) и, далее, нонафторбутансульфонилфторид (10.46 мл, 58.23 ммоль). После завершения добавления смесь оставляют нагреться до комнатной температуры и перемешивают в течение 1 дня, после чего добавляют еще 10.46 мл сульфонилирующего реагента и перемешивание продолжают в течение дополнительного дня. Затем добавляют 20.92 мл реагента и реакционную смесь перемешивают в течение еще 4-5 дней. Реакционную смесь охлаждают до 0°C и добавляют воду (100 мл). Смесь экстрагируют дихлорметаном и органические слои сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Сырое вещество вносят в дихлорметан, загружают на изолют и очищают на CombiFlash (120 г, силикагель, изогексан - 10% этилацетат/изогексан) и сушат в вакууме с получением масла, которое медленно кристаллизуется в твердое вещество.
ЖХ/МС (C20H20NO7F9S) нет ионизации; RT 1.62 (Метод В)
Синтез 1b: 2-трет-Бутил 7-метил 6-(трифторметансульфонилокси)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
К раствору фенола из Стадии B Синтеза 1а (2.06 г, 6.70 ммоль) и пиридина (1.27 мл, 20.1 ммоль) в дихлорметане (75 мл) добавляют трифторметансульфоновый ангидрид (1.69 мл, 10.05 ммоль) при -10-0°C в течение 30 мин. Смесь перемешивают при 0°C в течение 2 ч, затем добавляют воду со льдом (50 мл) и смесь подкисляют разбавленной водной соляной кислотой до достижения pH 2-3. Смесь экстрагируют этилацетатом и органические экстракты промывают последовательно солевым раствором и насыщенным водным сульфатом меди, сушат над сульфатом магния, и концентрируют в вакууме с получением продукта.
Синтез 1с: трет-Бутил 7-формил-6-(трифторметансульфонилокси)-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору продукта из Стадии A Синтеза 1а (3.1 г, 11.2 ммоль) в безводном дихлорметане (50 мл), охлажденному на бане со льдом, добавляют пиридин (4.52 мл, 56 ммоль) с последующим медленным добавлением трифторметансульфонового ангидрида (2.75 мл, 16.8 ммоль). Смеси дают нагреться до температуры окружающей среды и оставляют перемешиваться в течение прибл. 16 ч.
Реакционную смесь разбавляют водой со льдом, подкисляют разбавленной HCl до ~pH 3 и затем экстрагируют в этилацетат, и промывают насыщенным водным раствором сульфата меди. Органическую фазу сушат над сульфатом магния, фильтруют и упаривают. Сырое вещество очищают с помощью колоночной хроматографии на силикагеле, элюируя градиентом изогексан - 25% этилацетат/изогексан с получением целевого продукта в виде смеси с соответствующим региоизомером (трет-бутил 5-формил-6-(трифторметансульфонилокси)-1,2,3,4-тетрагидроизохинолин-2-карбоксилатом).
Синтез 1d: 2-трет-Бутил 5-метил 6-бром-2,3-дигидро-1Н-изоиндол-2,5-дикарбоксилат
Стадия A: 5-Бромбензол-1,2,4-трикарбоновая кислота
Бромтриметил бензол (40.7 г, 205 ммоль) добавляют к смеси воды (3.25 л), перманганата калия (232 г, 1.468 моль) и карбоната натрия (28.5 г, 206 ммоль). Смесь перемешивают при нагревании с обратным холодильником в течение 60 ч. По каплям добавляют этанол (820 мл), и получаемую смесь фильтруют в горячем состоянии через целит, и затем дают охладиться до температуры окружающей среды. Фильтрат подкисляют концентрированной водной HCl, и органический растворитель удаляют в вакууме. Твердый продукт выделяют путем фильтрования.
Стадия B: 6-Бром-1,3-диоксо-2,3-дигидро-1Н-изоиндол-5-карбоновая кислота
Продукт из Стадии A (42.8 г, 148 ммоль) и бромид аммония (43.5 г, 444 ммоль) тонко измельчают и гомогенизируют. Полученную в результате твердую смесь нагревают при 230-240°C в течение 2 ч при тщательном перемешивании каждые 15 мин. Смеси дают охладиться до температуры окружающей среды, затем добавляют к воде (230 мл), подкисляют до pH 1-2 концентрированной водной HCl, и экстрагируют рядом порций этилацетата. Объединенные органические экстракты упаривают, и получаемое твердое вещество растирают с минимальным количеством этилацетата, и затем с этанолом с получением целевого продукта в виде твердого вещества.
Стадия С: (4-Метоксифенил)метил 6-бром-2-[(4-метоксифенил)метил]-1,3-диоксо-2,3-дигидро-1Н-изоиндол-5-карбоксилат
Продукт из Стадии B (40 г, 148 ммоль), 1-(хлорметил)-4-метоксибензол (48.7 г, 311 ммоль) и карбонат калия (61.3 г, 444 ммоль) добавляют к ДМФА (760 мл) и смесь нагревают при 45°C в течение прибл. 16 ч. Добавляют воду (1140 мл), и получаемый осадок выделяют путем фильтрования, растворяют в хлороформе (1100 мл) и сушат (сульфат натрия). Упаривание дает целевой продукт в виде твердого вещества.
Стадия D: {6-Бром-2-[(4-метоксифенил)метил]-2,3-дигидро-1Н-изоиндол-5-ил}метанол
Продукт из Стадии C (55.4 г, 108.5 ммоль) суспендируют в сухом ТГФ (165 мл) и по каплям в атмосфере аргона добавляют боран-ТГФ (1 М в ТГФ; 542 мл, 542 ммоль). Через 30 мин смесь нагревают до 60°C в течение 6 ч. По каплям добавляют метанол (244.5 мл) (выделение газа) и получаемый раствор упаривают при пониженном давлении до объема 300 мл. Добавляют метанол (170 мл) и 10% водную HCl (220 мл) и получаемую смесь нагревают при 70°C в течение 3.5 ч. Раствор упаривают при пониженном давлении, и остаток распределяют между насыщенным водным карбонатом калия и дихлорметаном. Водную фазу экстрагируют дихлорметаном, и объединенные органические экстракты концентрируют в вакууме и очищают с помощью колоночной флэш-хроматографии, элюируя градиентом 5-60% этилацетат/гексан с получением целевого продукта.
Стадия E: трет-Бутил 5-бром-6-(гидроксиметил)-2,3-дигидро-1Н-изоиндол-2-карбоксилат
Раствор соединения из Стадии D (11.3 г, 32.5 ммоль) в трифторуксусной кислоте (145 мл) нагревают как можно быстрее при 200°C при микроволновом облучении в течение 7 мин. Трифторуксусную кислоту удаляют в вакууме, добавляют 10% водный гидроксид натрия (185 мл), и получаемую смесь тщательно растирают/гомогенизируют, затем экстрагируют несколькими порциями дихлорметана. Объединенные органические экстракты упаривают, затем растворяют в смеси 1:1 метанол/дихлорметан (210 мл) и добавляют ди-трет-бутилдикарбонат (1.2 экв.). Через 40 мин растворитель удаляют в вакууме и сырое вещество очищают с помощью колоночной флэш-хроматографии на силикагеле, элюируя смесью 1:1 гексан/этилацетат с получением продукта.
Стадия F: трет-Бутил 5-бром-6-формил-2,3-дигидро-1Н-изоиндол-2-карбоксилат
Продукт из Стадии E (5 г, 15.2 ммоль) растворяют в дихлорметане (63.5), и порциями добавляют перйодинан Десса-Мартина (8.4 г, 19.8 ммоль). Через 1 ч смесь концентрируют в вакууме и сырое вещество очищают с помощью колоночной флэш-хроматографии на силикагеле, элюируя градиентом 2%-15% этилацетат/гексан с получением целевого продукта.
Стадия G: 2-трет-Бутил 5-метил 6-бром-2,3-дигидро-1Н-изоиндол-2,5-дикарбоксилат
Соединение из Стадии F (1.63 г, 5.0 ммоль), диоксид марганца (8.69 г, 100 ммоль), цианид натрия (1.47 г, 30 ммоль) и уксусную кислоту (601 мг, 10.0 ммоль) суспендируют в метаноле (50 мл) и смесь перемешивают в течение прибл. 16 ч. Реакционную смесь фильтруют через целит, концентрируют в вакууме, и остаток распределяют между этилацетатом и водой. Органическую фазу концентрируют в вакууме и очищают с помощью колоночной флэш-хроматографии на силикагеле, элюируя градиентом 0%-10% этилацетат/гексан с получением целевого продукта.
Синтез 1е; трет-Бутил 5-бром-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-Дигидро-1H-изоиндол-2-карбоксилат
Стадия А: 6-Бром-2-[(трет-бутокси)карбонил]-2,3-дигидро-1Н-изоиндол-5-карбоновая кислота
К раствору продукта из Синтеза 1d (1 г, 2.81 ммоль) в диоксане (5 мл) добавляют раствор моногидрата гидроксида лития (236 мг, 5.62 ммоль) в воде (5 мл), и реакционную смесь нагревают до 90°C. Через 40 мин реакционной смеси дают охладиться, и разбавляют водой и подкисляют до ~рН 2 с помощью 2 н. водной HCl. Смесь экстрагируют этилацетатом, и органические экстракты сушат и упаривают при пониженном давлении с получением продукта в виде твердого вещества.
ЖХ/МС (C14H16BrNO4) 342 [М+Н]+; RT 2.30 (Метод А)
Стадия B: трет-Бутил 5-бром-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксилат
К раствору продукта из Стадии A (933 мг, 2.73 ммоль) в ДМФА (10 мл) добавляют триэтиламин (1.33 мл, 9.55 ммоль), HBTU (1.04 г, 2.73 ммоль) и, далее, продукт из Синтеза 2а (832 мг, 2.73 ммоль) и смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь разбавляют водой и полученный в результате осадок отфильтровывают и промывают водой. Твердое вещество вносят в этилацетат, сушат над сульфатом магния, фильтруют и упаривают. Сырое вещество очищают с помощью колоночной хроматографии на силикагеле, элюируя градиентом изогексан - 1:1 этилацетат/изогексан с получением продукта в виде пены.
ЖХ/МС (С28Н34BrN3O4) 556 [М+Н]+; RT 2.35 (Метод А)
Синтез 1f: трет-Бутил 5-бром-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-Дигидро-1H-изоиндол-2-карбоксилат
Методика соответствует методике Синтеза 1е с заменой продукта из Синтеза 2а, используемого на Стадии C, на гидрохлорид (3R)-3-метил-1,2,3,4-тетрагидроизохинолина, полученный из Синтеза 2b.
ЖХ/МС (C24H27BrN2O3) 471 [М+Н]+; RT 2.76 (Метод А)
Синтез 1g: 6-Бром-2-(трифторацетил)-1,2,3,4-тетрагидроизохинолин-7-карбоновая кислота
Стадия А: 2-(3-Бром-4-метоксифенил)этанамин
К раствору 2-(4-метоксифенил)этанамина (25.0 г, 0.165 моль) в ледяной уксусной кислоте (300 мл) по каплям добавляют раствор брома (31.7 г, 0.198 моль) в ледяной уксусной кислоте (200 мл). Сразу образуется белый осадок, и реакционную смесь перемешивают при к.т. в течение 48 ч. Белое твердое вещество отфильтровывают и промывают гексаном с получением гидробромида. Маточный раствор упаривают и остаток промывают небольшим количеством уксусной кислоты и гексаном. Данные соли растворяют в воде и рН доводят до 8. Суспензию экстрагируют с помощью ДХМ и сушат, и концентрируют при пониженном давлении. Сырой продукт используют на следующей стадии без дополнительной очистки.
Стадия B: N-[2-(3-Бром-4-метоксифенил)этил]-2,2,2-трифторацетамид
2-(3-бром-4-метоксифенил)этанамин (600 мг) растворяют в 6 мл TFAA и 6 мл ДХМ и смесь перемешивают в течение 1 ч. Смесь охлаждают на бане со льдом и добавляют 24 мл воды. Органическую фазу несколько раз промывают водой, сушат и концентрируют при пониженном давлении. Сырой продукт используют на следующей стадии без дополнительной очистки.
Стадия С: 1-(6-Бром-7-метокси-3,4-дигидроизохинолин-2(1Н)-ил)-2,2,2-трифторэтанон
К раствору 40% серной кислоты в уксусной кислоте (150 мл) добавляют N-[2-(3-бром-4-метоксифенил)этил]-2,2,2-трифторацетамид (15.5 г, 52.4 ммоль) и параформальдегид (2.4 г, 80 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 18 ч, выливают в холодную воду и экстрагируют этилацетатом. Объединенный органический слой промывают раствором гидрокарбоната натрия, сушат и концентрируют при пониженном давлении. Сырой продукт очищают с помощью флэш-хроматографии (элюент: градиент н-гексан: EtOAc).
Стадия D: 1-(6-Бром-7-гидрокси-3,4-дигидроизохинолин-2(1Н)-ил)-2,2,2-трифторэтанон
В атмосфере аргона раствор 1-(6-бром-7-метокси-3,4-дигидроизохинолин-2(1H)-ил)-2,2,2-трифторэтанона (1 ммоль) в 20 мл ДХМ медленно добавляют к предварительно охлажденному раствору трибромида бора (1 ммоль) в 30 мл ДХМ при -30°C. Полученный в результате раствор медленно нагревают до -12°C и перемешивают в течение 16 ч. Реакцию гасят путем добавления льда и продукт экстрагируют с помощью EtOAc. Органическую фазу промывают водой и насыщенным водным NaCl и сушат, сырой продукт очищают с помощью флэш-хроматографии (элюент: градиент н-гексан:ДХМ).
Стадия E: 6-Бром-2-(трифторацетил)-1,2,3,4-тетрагидроизохинолин-7-ил трифторметансульфонат
1-(6-бром-7-гидрокси-3,4-дигидроизохинолин-2(1H)-ил)-2,2,2-трифторэтанон (5.72 г, 17.7 ммоль) и 2.2 мл пиридина (2.12 г, 26.5 ммоль) растворяют в ДХМ (130 мл). При 0°C по каплям добавляют 21.2 мл (21.2 ммоль) трифторметансульфонового ангидрида (1М в ДХМ) и температуре дают подняться до к.т. Когда реакция достигает соответствующей степени превращения, смесь разбавляют солевым раствором. Слои разделяют и органический слой сушат Na2SO4, фильтруют и концентрируют при пониженном давлении. Сырой продукт очищают с помощью флэш-хроматографии, используя гептан и этилацетат в качестве элюентов, с получением 6-бром-2-(трифторацетил)-1,2,3,4-тетрагидроизохинолин-7-ил трифторметансульфоната.
Стадия F: 6-Бром-2-(трифторацетил)-1,2,3,4-тетрагидроизохинолин-7-карбоновая кислота
6-бром-2-(трифторацетил)-1,2,3,4-тетрагидроизохинолин-7-ил трифторметансульфонат (912 мг, 2.0 ммоль) и 146 мг (dppf)PdCl2 (0.2 ммоль) растворяют в 15 мл ДМФА и 5 мл Н2О. Добавляют 560 мкл TEA (404 мг, 4.0 ммоль) и смесь перемешивают при 75°C в атмосфере СО (1 бар). Когда реакция достигает соответствующей степени превращения, смесь разбавляют ДХМ, экстрагируют 0.2 М HClводн. Слои разделяют, органический слой сушат Na2SO4, фильтруют и концентрируют при пониженном давлении. Сырой продукт очищают с помощью флэш-хроматографии, используя ДХМ и метанол в качестве элюентов с получением 6-бром-2-(трифторацетил)-1,2,3,4-тетрагидроизохинолин-7-карбоновой кислоты.
Синтез 1ha: 1-{6-Бром-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-ил}-2,2,2-трифторэтан-1-он
К раствору кислоты из Синтеза 1g (2 г, 0.01 моль) в N,N-диметилформамиде (15 мл) добавляют N,N-диизопропилэтиламин (1.98 мл, 11.36 ммоль), амин из Синтеза 2а (1.39 г, 5.96 ммоль) и HBTU (2.15 г, 5.68 ммоль), и смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь концентрируют в вакууме, затем повторно растворяют в этилацетате, и промывают водой и солевым раствором. Органический экстракт сушат над сульфатом магния, концентрируют в вакууме, и очищают с помощью колоночной флэш-хроматографии (40 г, силикагель, дихлорметан - 3% метанол в дихлорметане).
ЖХ/МС (C26H27BrF3N3О3) 566 [М+Н]+; RT 1.26 (Метод В)
Синтез 1hb: 1-{6-Бром-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-ил}-2,2,2-трифторэтан-1-он
Методика соответствует методике Синтеза 1ha с заменой амина из Синтеза 2а на амин из Синтеза 2b.
ЖХ/МС (C22H20BrF3N2O2) 481 [М+Н]+; RT 1.46 (Метод В)
Синтез 2а: Дигидрохлорид (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина
Стадия А: Бензил (3S)-3-(4-морфолинилкарбонил)-3,4-дигидро-2(1Н)-изохинолин карбоксилат
К раствору 5 г (3S)-2-[(бензилокси)карбонил]-1,2,3,4-тетрагидро-3-изохинолинкарбоновой кислоты (16 ммоль) в 160 мл дихлорметана добавляют 1.5 мл морфолина (17.6 ммоль) и затем 9 мл N,N-триэтиламина (64 ммоль), 3.3 г 1-этил-3-(3'-диметиламинопропил)-карбодиимида (EDC) (19.2 ммоль) и 2.6 г гидроксибензотриазола (НОВТ) (19.2 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение ночи и затем вливают в раствор хлорида аммония и экстрагируют этилацетатом. Органическую фазу потом сушат над сульфатом магния, и затем фильтруют и упаривают досуха. Полученный таким способом сырой продукт затем очищают с помощью хроматографии на силикагеле (градиент дихлорметан/метанол). Продукт получают в виде пены.
1H-ЯМР: δ (400 МГц; ДМСО-d6; 353°K): 7.30 (m, 5Н бензил); 7.15 (m, 4Н ароматические); 5.2-5.0 (m, 3Н, 2Н бензил, 1Н дигидроизохинолин); 4.75-4.5 (2d, 2Н дигидроизохинолин); 3.55-3.3 (m, 8Н морфолин); 3.15-2.9 (2dd, 2Н дигидроизохинолин)
ИК: ν:>С=O: 1694;1650 см-1
Стадия В: Бензил (3S)-3-(4-морфолинилметил)-3,4-дигидро-2(1Н)-изохинолин карбоксилат
К раствору 5.3 г продукта, полученного на Стадии A, (13.9 ммоль) в 278 мл тетрагидрофурана добавляют 14 мл BH3Ме2S (27.8 ммоль) при температуре окружающей среды. Все количество нагревают в течение 4 часов при 80°C. Температуре смеси дают вернуться к температуре окружающей среды, и затем добавляют 7 мл (14 ммоль) ВН3Ме2S. Реакционную смесь снова нагревают при 80°C в течение 2 часов. Затем упаривают тетрагидрофуран и медленно добавляют метанол и затем 5.6 мл 5 н. соляной кислоты (27.8 ммоль). Смесь перемешивают при температуре окружающей среды в течение ночи и затем при 80°C в течение одного часа. Затем к реакционной смеси добавляют насыщенный раствор NaHCO3 при 0°C до достижения рН 8, и затем осуществляют экстрагирование этилацетатом. Органическую фазу потом сушат над сульфатом магния, и затем фильтруют и упаривают досуха. Указанный в заголовке продукт получают в виде масла.
1Н-ЯМР: δ (400 МГц; ДМСО-d6; 353°K): 7.43-7.30 (неразрешенный пик, 5Н бензил); 7.19 (m, 4Н ароматические); 5.16 (m, 2Н, 2Н бензил); 4.79-4.29 (d, 2Н дигидроизохинолин); 4.58 (m, 1Н дигидроизохинолин); 3.50 (m, 4Н морфолин); 3.02-2.80 (dd, 2Н дигидроизохинолин); 2.42-2.28 (неразрешенный пик, 5Н, 4Н морфолин, 1Н морфолин); 2.15 (dd, 1Н морфолин)
ИК: ν: >СН: 2810 см-1; ν: >С=O: 1694 см-1; ν: >С-O-С<: 1114 см-1; ν: >СН-Ar: 751; 697 см-1
Стадия C: (3S)-3-(4-Морфолинилметил)-1,2,3,4-тетрагидроизохинолин
К раствору 4.9 г соединения Стадии B (13.4 ммоль) в 67 мл этанола добавляют 0.980 г дигидроксида палладия (20 мас. %) при температуре окружающей среды. Реакционную смесь помещают под давление водорода 1.2 бар при температуре окружающей среды на 4 часа. Смесь затем пропускают через фильтр Ватмана, и затем палладий несколько раз промывают этанолом. Фильтрат упаривают досуха. Указанный в заголовке продукт получают в виде масла.
1H-ЯМР: δ (400 МГц; ДМСО-d6; 300°K): 7.12-7.0 (неразрешенный пик, 4Н ароматические); 3.92 (s, 2Н тетрагидроизохинолин); 3.60 (t, 4Н морфолин); 2.98 (m, 1Н тетрагидроизохинолин); 2.68 (dd, 1Н тетрагидроизохинолин); 2.5-2.3 (неразрешенный пик, 8Н, 1Н тетрагидроизохинолин, 6Н морфолин, 1Н NH)
ИК: ν: >NH: 3322 см-1; ν: >C-O-C<: 1115 см-1; ν: >СН-Ar: 742 см-1
Стадия D: Дигидрохлорид (3S)-3-(4-морфолинилметил)-1,2,3,4-тетрагидроизохинолина
Свободное основание, полученное на Стадии C, растворяют в минимальном объеме дихлорметана. К перемешиваемому раствору при комнатной температуре добавляют 1 М раствор HCl в диэтиловом эфире (3 экв.). Реакционную смесь перемешивают в течение 15 минут, после чего добавляют диэтиловый эфир. Полученный в результате осадок отфильтровывают, промывают диэтиловым эфиром, затем сушат в вакууме с получением продукта.
Синтез 2b: (3R)-3-Метил-1,2,3,4-тетрагидроизохинолин
Стадия A: 3-Метил-1,2,3,4-тетрагидроизохинолин
К раствору 3-метилизохинолина и NiCl2*6H2O (1.2 экв.) в метаноле (3 мл/ммоль), охлажденному до 0°C, порциями добавляют борогидрид натрия (12 экв.) в течение 1 ч. Реакционную смесь перемешивают при температуре окружающей среды в течение 1 ч, затем гасят путем добавления воды. Растворитель удаляют при пониженном давлении, и остаток распределяют между этилацетатом и водой. Органическую фазу сушат над сульфатом натрия и упаривают с получением сырого продукта.
Стадия B: (3R)-3-Метил-1,2,3,4-тетрагидроизохинолин Продукт из Стадии A (4.5 г) растворяют в смеси 1:9 изопропанол/гептан (55 мл), и получаемый раствор повторно вводят в колонку для ИХ (50×500 мм, размер частиц 20 мкм), элюируя смесью 5:95 2-пропанол/гептан, содержащей 0.05% диэтиламина, со скоростью потока 50 мл/мин при температуре окружающей среды. При этих условиях (R)-изомер элюируется в виде второй фракции.
Синтез 2с: трет-Бутил [(3S)-1,2,3,4-тетрагидроизохинолин-3-илметил]карбамат
Стадия A: Бензил (3S)-3-(гидроксиметил)-3,4-дигидро-1Н-изохинолин-2-карбоксилат
Это соединение получают, используя протокол из литературы (R.В. Kawthekar и др. South Africa Journal of Chemistry 63, 195, 2009), исходя из 15 г (3S)-1,2,3,4-тетрагидроизохинолин-3-илметанола (91.9 ммоль) в присутствии бензилхлорформиата и триэтиламина, растворенных в дихлорметане. После очистки на силикагеле (градиент петролейный эфир/AcOEt) указанный в заголовке продукт получают в виде масла.
1Н ЯМР: δ (300 МГц; ДМСО-d6; 300K): 7.33 (m, 5Н, ароматические Н, О-бензил); 7.15 (s, 4Н, ароматические Н, Н тетрагидроизохинолин); 5.13 (s, 2Н, CH2-Ph); 4.73 (d, 1Н, Н тетрагидроизохинолин); 4.47 (m, Н, CH2ОН); 4.36 (m, 1Н, Н тетрагидроизохинолин); 4.28 (d, 1Н, Н тетрагидроизохинолин); 3.39 (dd, 1Н, CH2ОН); 3.23 (dd, 1H, CH2ОН); 2.93 (dd, 1Н, Н тетрагидроизохинолин); 2.86 (dd, 1Н, Н тетрагидроизохинолин).
ИК: ν ОН: 3416 см-1; ν <С=O 1694 см-1; ν ароматическая >С-Н: 754 см-1
Стадия В: Бензил (3S)-3-(азидометил)-3,4-дигидроизохинолин-2(1Н)-карбоксилат
Это соединение получают, используя протокол из литературы (D. Page и др. J. Med. Chem, 44, 2387, 2001), исходя из 23 г соединения, полученного на Стадии A, (77.3 ммоль) в присутствии дифенилфосфорилазида и трифенилфосфина, растворенных в ТГФ. После очистки на силикагеле (градиент петролейный эфир/AcOEt) указанный в заголовке продукт получают в виде масла.
1Н ЯМР: δ (400 МГц; ДМСО-d6; 300K): 7.36 (m, 5Н, ароматические Н, О-бензил); 7.19 (m, 4Н, ароматические Н, Н тетрагидроизохинолин); 5.16 (s, 2Н, CH2-Ph); 4.76 (d, 1Н, Н тетрагидроизохинолин); 4.53 (m, 1Н, Н тетрагидроизохинолин); 4.30 (m, 1Н, Н тетрагидроизохинолин); 3.28 (m, 2Н, CH2N3); 3.06 (dd, 1Н, H тетрагидроизохинолин); 2.78 (dd, 1Н, H тетрагидроизохинолин)
ИК: ν N3: 2095 см-1; ν <С=O: 1694 см-1; ν ароматическая >С-Н: 754 см-1
Стадия С: Бензил (3S)-3-(аминометил)-3,4-дигидроизохинолин-2(1Н)-карбоксилат
К раствору 20.9 г (64.5 ммоль) азидосоединения, полученного на Стадии B, в 650 мл ТГФ последовательно добавляют 25.5 г (97.2 ммоль) трифенилфосфина и 157 мл воды. Полную загрузку нагревают с обратным холодильником в течение 2 часов 30 минут. Затем реакционную смесь концентрируют досуха и оставшееся масло затем вносят в изопропиловый эфир. Образуется белый осадок, который отфильтровывают и промывают изопропиловым эфиром. Фильтрат затем концентрируют досуха и затем очищают с помощью хроматографии на силикагеле (градиент CH2Сl2/МеОН). Указанный в заголовке продукт получают в виде масла.
1H ЯМР: δ (400 МГц; ДМСО-d6; 300K): 7.40 (m, 5Н, ароматические Н, O-бензил); 7.20 (m, 4Н, ароматические Н, Н тетрагидроизохинолин); 5.15 (s, 2Н, CH2-Ph); 4.75-4.3 (m, 2Н, Н тетрагидроизохинолин); 4.30 (d, 1Н, Н тетрагидроизохинолин); 2.90 (m, 2Н, CH2NH2); 2.45 (m, 2Н, Н тетрагидроизохинолин); 1.40 (m, 2Н, NH2)
ИК: ν NH2: 3400-3300 см-1; ν <С=O: 1688 см-1
Стадия D: Бензил (3S)-3-{[(трет-бутоксикарбонил)амино]метил}-3,4-дигидроизохинолин-2(1Н)-карбоксилат
К раствору 18.4 г (62.1 ммоль) соединения, полученного на Стадии С, в 630 мл дихлорметана последовательно добавляют 17.5 мл (124 ммоль) триэтиламина и, порциями, 14.9 г (68.3 ммоль) ди-/трет-бутилдикарбоната. Полную загрузку перемешивают при температуре окружающей среды в течение 2 часов. Затем реакционную смесь концентрируют, и затем добавляют этилацетат. Органическую фазу последовательно промывают 1 М раствором HCl, насыщенным раствором NaCl, насыщенным раствором NaHCO3 и затем насыщенным раствором NaCl. После сушки, концентрирования досуха и очистки с помощью хроматографии на силикагеле (градиент петролейный эфир/AcOEt), указанный в заголовке продукт получают в виде масла.
1Н ЯМР: δ (400 МГц; ДМСО-d6; 300K): 7.35 (m, 5Н, ароматические Н, О-бензил); 7.15 (m, 4Н, ароматические Н, Н тетрагидроизохинолин); 6.51 (m, 1Н, NHBoc); 5.12 (s, 2Н, CH2-Ph); 4.76 (d, 1Н, H тетрагидроизохинолин); 4.51 (m, 1Н, H тетрагидроизохинолин); 4.36 (d, 1Н, H тетрагидроизохинолин); 2.95 (m, 3Н, Н тетрагидроизохинолин + CH2NHBoc); 2.71 (d, 1Н, Н тетрагидроизохинолин); 1.34 (s, 9Н, NHBoc)
ИК: ν NH: 3351 см-1; ν <С=O: 1686 см-1
Стадия Е: трет-Бутил [(3S)-1,2,3,4-тетрагидроизохинолин-3-илметил]карбамат
К раствору 21 г (53 ммоль) соединения, полученного на Стадии D, в 600 мл этилацетата добавляют 2.1 г,10%-ного палладия на угле. Полную загрузку перемешивают при температуре окружающей среды под давлением водорода 1.3 бар в течение 5 часов. Затем реакционную смесь фильтруют, и затем концентрируют досуха. Указанный в заголовке продукт получают в виде твердого вещества.
1Н ЯМР: δ (400 МГц; ДМСО-d6; 300K): 7.15 (m, 4Н, ароматические Н, Н тетрагидроизохинолин); 6.85 (t, 1Н, NHBoc); 3.90 (m, 2Н, Н тетрагидроизохинолин); 3.00 (m, 2Н, CH2NHBoc); 2.80 (m, 1Н, Н тетрагидроизохинолин); 2.65 (dd, 1Н, Н тетрагидроизохинолин); 2.40 (dd, 1Н, Н тетрагидроизохинолин); 1.40 (s, 9Н, NHBoc)
ИК: ν NH: 3386-3205 см-1 (NH амид); ν <С=O: 1688 см-1; ν NH: 1526 см-1 (NH амин)
Синтез 2d: Гидрохлорид (3S)-3-[2-(морфолин-4-ил)этил]-1,2,3,4-тетрагидроизохинолина
Стадия A: трет-Бутил (3S)-3-(2-морфолино-2-оксоэтил)-3,4-дигидро-1Н-изохинолин-2-карбоксилат
К раствору 3 г (10.30 ммоль) [(3S)-2-(трет-бутоксикарбонил)-1,2,3,4-тетрагидроизохинолин-3-ил]уксусной кислоты в 100 мл дихлорметана по каплям добавляют 1.10 мл (11.32 ммоль) морфолина и по каплям, в случае каждого вещества, - 4.3 мл (30.9 ммоль) триэтиламина, 2.20 г (12.40 ммоль) 1,2-дихлорметана и 1.70 г (1.68 ммоль) гидроксибензотриазола. Полную загрузку перемешивают при температуре окружающей среды в течение 15 часов. Затем реакционную смесь разбавляют дихлорметаном и последовательно промывают 1 М раствором HCl, насыщенным раствором NaHCO3 и затем насыщенным раствором NaCl до нейтральной реакции среды. Органическую фазу затем сушат над MgSO4, фильтруют и концентрируют досуха. После очистки с помощью колоночной хроматографии на силикагеле (дихлорметан /МеОН) указанный в заголовке продукт получают в виде масла.
1Н ЯМР: δ (400 МГц; ДMCO-d6; 300K): 7.20-7.10 (m, 4Н, ароматические Н, тетрагидроизохинолин); 4.70 (m, 1Н, алифатический Н, СН тетрагидроизохинолин); 4.75-4.20 (2m, 2Н, алифатические Н, CH2 альфа к N тетрагидроизохинолина); 3.60 (m, 8Н, алифатические Н, морфолин); 3.00 и 2.70 (2dd, 2Н, алифатические Н, тетрагидроизохинолин); 2.50-2.20 (2d, 2Н, алифатические Н, CH2СО); 1.40 (s, 9Н, tBu)
ИК: ν С=O: 1687; 1625 см-1
Стадия В: Гидрохлорид 1-(морфолин-4-ил)-2-[(3S)-1,2,3,4-тетрагидроизохинолин-3-ил]этанона
К раствору 2.88 г (7.18 ммоль) соединения, полученного на Стадии A, в 16 мл дихлорметана по каплям добавляют 80 мл (80 ммоль) 1 М эфирного раствора HCl. Полную загрузку перемешивают при температуре окружающей среды в течение 15 часов, суспензию затем фильтруют и осадок промывают эфиром. После сушки указанный в заголовке продукт получают в виде твердого вещества.
1H ЯМР: δ (400 МГц; ДМСО-d6; 300K): 9.80-9.50 (m, 2Н, NH2+); 7.30-7.10 (m, 4Н, ароматические Н, тетрагидроизохинолин); 4.30 (m, 2Н, алифатические Н, CH2 альфа к N тетрагидроизохинолина); 3.80 (m, 1Н, алифатический Н, СН тетрагидроизохинолин); 3.70-3.40 (2m, 8Н, алифатические Н, морфолин); 3.15 и 2.8 (m, 4Н, алифатический Н, CH2 тетрагидроизохинолин и CH2СО)
ИК: ν -NH2+: 2800-1900 см-1; ν С=O: 1620 см-1
Стадия С: Гидрохлорид (3S)-3-[2-(морфолин-4-ил)этил]-1,2,3,4-тетрагидроизохинолина
Приготавливают раствор 2.2 г (7.44 ммоль) соединения, полученного на Стадии B, в 22 мл МТВЕ и 5 мл дихлорметана. После охлаждения на бане со льдом при 0°C по каплям добавляют 15 мл (15 ммоль) 1 М раствора LiAlH4 в тетрагидрофуране. Полную загрузку затем перемешивают при температуре окружающей среды в течение 6 часов. Смесь охлаждают до 0°C, и затем по каплям добавляют 1 мл 5 М раствора NaOH. Полную загрузку перемешивают при температуре окружающей среды в течение 45 минут. Твердое вещество затем отфильтровывают и промывают с помощью МТВЕ и затем дихлорметаном, и фильтрат концентрируют досуха. Полученное таким образом масло разбавляют дихлорметаном и по каплям добавляют 6.3 мл 1 М эфирного раствора HCl. Полную загрузку перемешивают при температуре окружающей среды в течение 1 часа и затем фильтруют. Полученные таким образом кристаллы промывают этиловым эфиром. После сушки указанный в заголовке продукт получают в виде твердого вещества.
1Н ЯМР: δ (400 МГц; ДМСО-d6; 300K): 11.35+9.80 (2m, 2Н, NH2+); 10.00 (m, Н, NH+); 7.20 (m, 4Н, ароматические Н, тетрагидроизохинолин); 4.30 (s, 2Н, алифатические Н, CH2 альфа к N тетрагидроизохинолина); 4.00+3.85 (2m, 4Н, алифатические Н, CH2 альфа к N морфолина); 3.70 (m, 1Н, алифатический Н, СН тетрагидроизохинолин); 3.55-3.30 (m, 4Н, алифатические Н, СН альфа к O морфолина и CH2 морфолин); 3.15 (dd, 1Н, алифатический Н, CH2 тетрагидроизохинолин); 3.10 (m, 2Н, алифатические Н, СН альфа к O морфолина); 2.90 (dd, 1Н, алифатический Н, CH2 тетрагидроизохинолин); 2.30+2.15 (2m, 2Н, алифатические Н, CH2 тетрагидроизохинолин)
ИК: ν NH+/-NH2+: между 3500 и 2250 см-1; ν С=C: слабый 1593 см-1; ν ароматический С-Н: 765 см-1
Синтез 2е: трет-Бутил {2-[(3S)-1,2,3,4-тетрагидроизохинолин-3-ил]этил} карбамат
Стадия А: Бензил (3S)-3-(2-гидроксиэтил)-3,4-дигидроизохинолин-2(1Н)-карбоксилат
Указанное в заголовке соединение получают исходя из (3S)-2-[(бензилокси)карбонил]-1,2,3,4-тетрагидроизохинолин-3-карбоновой кислоты, на основании протокола из литературы (Jinlong Jiang и др. Bioorganic & Medicinal Chemistry Letters, 14, 1795, 2004).
Стадия В: Бензил (3S)-3-{2-[(метилсульфонил)окси]этил}-3,4-дигидроизохинолин-2(1Н)-карбоксилат
К раствору 10.6 г соединения Стадии A (35.6 ммоль) в 350 мл безводного CH2Cl2, охлажденному до 0°C, последовательно добавляют триэтиламин 10.1 мл (71.2 ммоль) и затем, по каплям, метансульфонилхлорид 3.1 мл (39 ммоль). Затем реакционную смесь перемешивают при температуре окружающей среды в течение 2 часов. Затем осуществляют гидролиз путем медленного добавления воды. Продукт экстрагируют несколько раз с помощью CH2Cl2. Органические фазы затем объединяют и последовательно промывают 1 н. раствором HCl, насыщенным раствором NaCl, насыщенным раствором NaHCO3 и насыщенным раствором NaCl до нейтральной реакции среды. Их затем сушат над MgSO4 и концентрируют досуха. После очистки с помощью хроматографии на силикагеле (градиент петролейный эфир/AcOEt) ожидаемый продукт получают в виде пены.
ЖХ/МС: m/z=(М+Н)+=375
Стадия С: Бензил (3S)-3-(цианометил)-3,4-дигидроизохинолин-2(1Н)-карбоксилат
К раствору 15.4 г соединения, полученного на Стадии B, (41.02 ммоль) в 250 мл безводного ДМСО добавляют 22 г (449 ммоль) цианида натрия. Полную загрузку затем нагревают при 60°C в течение 12 часов. Реакционной смеси дают охладиться и затем разбавляют путем добавления этилацетата. Затем осуществляют гидролиз, используя насыщенный раствор NaHCO3. Затем вновь дважды осуществляют экстрагирование этилацетатом, органические фазы объединяют, промывают H2O, сушат над MgSO4 и концентрируют досуха. После очистки с помощью хроматографии на силикагеле (гексан/AcOEt 7/3) ожидаемый продукт получают в виде масла.
ЖХ/МС: m/z=[М+Н]+=307.1
Стадия D: Бензил (3S)-3-(2-аминоэтил)-3,4-дигидроизохинолин-2(1Н)-карбоксилат
К раствору 15.4 г соединения, полученного на Стадии C, (50.3 ммоль) в 300 мл безводного ТГФ, охлажденному до 0°C, по каплям добавляют 1 н. раствор BH3-ТГФ. Температуре реакционной смеси дают понемногу вернуться к температуре окружающей среды, и затем полную загрузку перемешивают в течение 14 часов. Затем реакционную смесь гидролизуют путем медленного добавления насыщенного раствора NH4Cl. Затем дважды осуществляют экстрагирование этилацетатом, органические фазы объединяют и сушат над MgSO4. После концентрирования досуха ожидаемый продукт получают в виде пены, которую используют непосредственно, без очистки, на следующей стадии защиты.
Стадия Е: Бензил (3S)-3-{2-[(трет-бутоксикарбонил)амино]этил}-3,4-дигидроизохинолин-2(1Н)-карбоксилат
К раствору 15.6 г соединения, полученного на Стадии D, (50.3 ммоль) в 670 мл CH2Cl2, последовательно порциями добавляют 13.2 г (60.36 ммоль) Boc2O, 14 мл (100.6 ммоль) триэтиламина, и DMAP в каталитическом количестве. Полную загрузку перемешивают при температуре окружающей среды в течение 5 часов. Затем реакционную смесь гидролизуют водой и два раза экстрагируют с помощью CH2Cl2. Органические фазы объединяют, промывают водой и сушат над MgSO4. После концентрирования досуха и очистки с помощью хроматографии на силикагеле (градиент гептан/AcOEt) ожидаемый продукт получают в виде масла.
ЖХ/МС: m/z=(М+Н)+=411
Стадия F: трет-Бутил {2-[(3S)-1,2,3,4-тетрагидроизохинолин-3-ил]этил}карбамат
К раствору 10.4 г соединения, полученного на Стадии E, (25.5 ммоль) в 210 мл безводного МеОН добавляют 2.71 г (2.55 ммоль) Pd/C 10%. Полную загрузку дегазируют в течение 30 минут и затем перемешивают в атмосфере водорода в течение 16 часов. Затем реакционную смесь фильтруют и концентрируют досуха. Ожидаемый продукт получают в виде твердого вещества, которое вносят в смесь пентан/Et2O (90/10), растирают и отфильтровывают. После сушки продукт получают в виде твердого вещества.
1Н ЯМР: δ (400 МГц; ДМСО-d6; 300K): 7.1-6.98 (m, 4Н, ароматические Н, тетрагидроизохинолин); 6.83 (m, 1Н, CH2NHBoc); 3.85 (s, 2Н, алифатические Н, тетрагидроизохинолин); 3.09 (q, 2Н, CH2NHBос); 2.73 (m, 1Н, алифатический Н, тетрагидроизохинолин); 2.70 и 2.39 (2m, 2Н, алифатические Н, тетрагидроизохинолин); 1.63 (m, 2Н, алифатические Н); 1.38 (s, 9Н, NHCOOtBu)
ИК: ν: >NH: 3378, -3201 см-1 (амин, амид); ν: >С=O: 1683 см-1 (амид); ν: >NH: 1524 см-1 (амид); ν: >С=O: 1168 см-1
ЖХ/МС: m/z=[М+Н]+=277
Синтез 2f: Дигидрохлорид (3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолина
Стадия А: {(3S)-2-[(4-Метилфенил)сульфонил]-1,2,3,4-тетрагидроизохинолин-3-ил}метил 4-метилбензолсульфонат
Методика является точно такой же, как и методика Стадии A Синтеза 1'.
Стадия В: трет-Бутил 2-({(3R)-2-[(4-метилфенил)сульфонил]-1,2,3,4-тетрагидроизохинолин-3-ил}метил)-3-(морфолин-4-ил)-3-оксопропаноат
К суспензии 1 г NaH (60%) (25.08 ммоль) в 30 мл МТВЕ по каплям добавляют раствор 5 г трет-буткп 3-морфолино-3-оксопропаноата (21.81 ммоль) в 20 мл безводного МТВЕ. Эту суспензию перемешивают при температуре окружающей среды в течение 1 часа и затем добавляют соединение, полученное на Стадии A, в виде порошка. Загрузку перемешивают при 60°C в течение 30 часов. Добавляют 100 мл насыщенного раствора хлорида аммония. Полученный в результате раствор экстрагируют дихлорметаном. Органическую фазу затем сушат над MgSO4, фильтруют и концентрируют досуха. После очистки с помощью колоночной хроматографии на силикагеле (дихлорметан/МеОН) ожидаемый продукт получают в виде масла.
ЯМР 1H (500 МГц, ДМСО-d6) δ м.д.: 7.63/7.59 (2d, 2 Н), 7.3/7.26 (2d, 2 Н), 7.13 (m, 2 Н), 7.09/6.97 (2t, 2 Н), 4.64/4.55/4.36/4.28 (2АВ, 2 Н), 4.25/4.11 (2m, 1 Н), 3.81 (m, 1 Н), 3.73-3.48 (m, 4 Н), 3.57-3.32 (m, 4 Н), 2.51 (m, 2 Н), 2.32/2.31 (2s, 3 Н), 1.88/1.79 (2 m, 2 Н), 1.39/1.38 (2s, 9 Н)
ИК (ATR) см-1 ν: >С=O: 1731 (сложный эфир); ν: >С=O: 1644 (амид); ν: -SO2: 1334-1156; ν: >C-O-C<: 1115; γ: >СН-Ar: 815-746-709
Стадия С: 2-({(3R)-2-[(4-Метилфенил)сульфонил]-1,2,3,4-тетрагидроизохинолин-3-ил}метил)-3-(морфолин-4-ил)-3-оксопропановая кислота
К раствору 9.5 г (17.97 ммоль) соединения, полученного на Стадии B, в 40 мл диоксана по каплям добавляют 20 мл 4 М раствора HCl в диоксане. Загрузку перемешивают при температуре окружающей среды в течение 48 часов и затем раствор концентрируют досуха. После сушки ожидаемый продукт получают в виде масла.
ЯМР 1Н (400 МГц, ДМСО-d6) δ м.д.: 12.75 (m, 1 Н), 7.6 (2*d, 2 Н), 7.3 (2*d, 2 Н), 7.1/6.95 (2*m, 4 Н), 4.7-4.2 (d, 2 Н), 4.25/4.12 (2*m, 1 Н), 3.9-3.3 (m, 9 Н), 2.55 (d, 2 Н), 2.3 (2*s, 3 Н), 1.8 (t, 2 Н)
ИК (ATR) см-1: ν >C-Н: 3500-2000; ν: >С=O: 1727 (кислота); ν: >С=O: 1634 (амид); ν: -SO2: 1330-1155
Стадия D: 3-{(3R)-2-{(4-Метилфенил)сульфонил]-1,2,3,4-тетрагидроизохинолин-3-ил}-1-(морфолин-4-ил)пропан-1-он
К раствору 7.80 г (16.51 ммоль) соединения, полученного на Стадии C, в 100 мл ДМСО добавляют 1.16 г (19.83 ммоль) твердого хлорида натрия и затем, по каплям, 5 мл воды. Загрузку перемешивают при 130°C в течение 1 часа и затем раствор концентрируют до %. Затем реакционную смесь разбавляют дихлорметаном и последовательно промывают насыщенным раствором хлорида лития и затем насыщенным раствором NaCl. Органическую фазу затем сушат над MgSO4, фильтруют и концентрируют досуха. После очистки с помощью колоночной хроматографии на силикагеле (циклогексан/этилацетат) ожидаемый продукт получают в виде масла.
ЯМР 1Н (400 МГц, ДMCO-d6) δ м.д.: 7.65 (d, 2 Н), 7.3 (d, 2 Н), 7.15/7 (2 m, 4 Н), 4.6 (d, 1 Н), 4.25 (d, 1 Н), 4.2 (m, 1 Н), 3.5 (ш, 4 Н), 3.4 (2 m, 4 Н), 2.6 (2 dd, 2 Н), 2.35 (s, 3 Н), 2.3 (m, 2 Н), 1.5 (quad., 2 Н)
ИК (АТR) см-1: ν: >С=O: 1639; ν: -SO2: 1331-1156; γ: >CH-Ar: 815-675
Стадия E: (3R)-2-[(4-Метилфенил)сульфонил]-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолин
К раствору 6.0 г (14.0 ммоль) соединения, полученного на Стадии D, в 60 мл МТВЕ и 14 мл дихлорметана порциями добавляют 1.06 г (28 ммоль) LAH в течение 5 минут. Загрузку перемешивают при температуре окружающей среды в течение 15 часов. По каплям добавляют 1.5 мл воды и перемешивание осуществляют в течение 15 минут. Затем по каплям добавляют 1.5 мл 5М раствора гидроксида натрия и перемешивание осуществляют в течение 15 минут. Затем реакционную смесь разбавляют МТВЕ и дихлорметаном. Суспензию затем фильтруют и осадок промывают с помощью МТВЕ и дихлорметаном. Органическую фазу затем сушат над MgSO4, фильтруют и концентрируют досуха. После очистки с помощью колоночной хроматографии на силикагеле (дихлорметан/ЕtOH/NH4OH) ожидаемый продукт получают в виде масла.
ЯМР 1Н (400 МГц, ДМСО-d6) δ м.д.: 7.68 (d, 2 Н), 7.32 (d, 2 Н), 7.1 (массив, 4 Н), 4.65/4.23 (АВ, 2 Н), 4.2 (m, 1 Н), 3.55 (t, 4 Н), 2.7/2.6 (АВх, 2 Н), 2.35 (s, 3 Н), 2.25 (t, 4 Н), 2.2 (t, 2 Н), 1.4/1.3 (2 m, 4 Н)
ИК (ATR) см-1: ν: -SO2: 1333-1158
Стадия F: (3R)-3-[3-(Морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолин
К раствору 1.50 г (3.62 ммоль) соединения, полученного на Стадии E, в 20 мл безводного метанола порциями добавляют 2.0 г (82.3 ммоль) магниевых стружек. Загрузку перемешивают при обработке ультразвуком в течение 96 часов. Затем реакционную смесь фильтруют, твердое вещество промывают несколько раз метанолом, и фильтрат концентрируют досуха. После очистки с помощью колоночной хроматографии на силикагеле (дихлорметан/EtOH/NH4OH) ожидаемый продукт получают в виде масла.
ЯМР 1Н (400 МГц, ДМСО-d6) δ м.д.: 7.3 (d, 2 Н), 7.1 (t, 2 Н), 7.1 (d+t, 3 Н), 7 (d, 2 Н), 3.9 (s, 2 Н), 3.55 (t, 4 Н), 2.75 (m, 1 Н), 2.72/2.45 (dd, 2 Н), 2.35 (t, 4 Н), 2.25 (t, 2 Н), 1.6 (m, 2 Н), 1.45 (m, 2 Н)
ИК (ATR) см-1: ν: >NH2+/NH+: 3500-2300; ν: >C-O-C<: 1115
Масс-спектроскопия высокого разрешения (ESI+-/FIA/BF):
Брутто-формула: C16Н24N2О
[М+Н]+ рассчитано: 261.1961
[М+Н]+ найдено: 261.1959
Стадия G: Дигидрохлорид (3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолина
Свободное основание, полученное на Стадии F, растворяют в минимальном объеме дихлорметана. К перемешиваемому раствору при комнатной температуре добавляют 1 М раствор HCl в диэтиловом эфире (3 экв.). Реакционную смесь перемешивают в течение 15 минут, после чего добавляют диэтиловый эфир. Полученный в результате осадок отфильтровывают, промывают диэтиловым эфиром, затем сушат в вакууме с получением продукта.
Синтез 2g: Дигидрохлорид N,N-диметил[(3S)-1,2,3,4-тетрагидроизохинолин-3-илметил]амина
Методика соответствует методике Синтеза 2а с заменой морфолина, используемого на Стадии A, на N,N-диметиламин.
Синтез 2h: Тригидрохлорид (3S)-3-[(4-Метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолина
Методика соответствует методике Синтеза 2а с заменой морфолина, используемого на Стадии A, на 1-метилпиперазин и с использованием 4.5 эквивалентов 1 М раствора HCl в диэтиловом эфире на Стадии D (стадия образование соли).
Синтез 3а: 4-[(трет-Бутилдиметилсилил)окси]-N-метиланилин
К раствору 3.69 г 4-метиламинофенола (30 ммоль) и 3.20 г имидазола (47 ммоль) в 65 мл дихлорметана, содержащего 1% этанола, добавляют 5.88 г трет-бутилдиметилсилилхлорида (39 ммоль) при быстром перемешивании при температуре окружающей среды. Через 30 минут смесь выливают в 160 мл воды. Органическую фазу отделяют и водную фазу экстрагируют 50 мл дихлорметана. Объединенные органические фазы потом сушат над сульфатом магния, и затем фильтруют и упаривают досуха. Полученный таким способом сырой продукт затем очищают с помощью хроматографии на силикагеле (гексан/этилацетат 100:1) с получением продукта (6.2 г, 87%) в виде масла.
Синтез 3b: 4-(Бензилокси)-N-фениланилин
Бензилбромид (1.79 мл, 15.08 ммоль) добавляют к смеси 4-гидроксидифениламина (2.54 г, 13.71 ммоль), карбоната цезия (5.58 г, 1.25 экв.) и йодида калия (283 мг, 0.1 экв.) в ацетоне (20 мл).
Смесь перемешивают и нагревают при 50°C в течение 1.25 ч. По прошествии этого времени добавляют дополнительную порцию бензилбромида (0.2 экв.) и карбоната цезия (0.2 экв.) и смесь нагревают в течение 45 мин. Реакционной смеси дают охладиться до температуры окружающей среды, затем разбавляют этилацетатом, фильтруют, и растворитель удаляют в вакууме. Остаток очищают с помощью флэш-хроматографии (Combiflash; 120 г SilaSep силикагелевая колонка), элюируя градиентом 0-20% этилацетата в гексане с получением целевого продукта в виде твердого вещества.
ЖХ/МС (C19H17NO) 276 [М+Н]+; RT 1.48 (Метод В)
Синтез 3с: 4-(Бензилокси)-N-этиланилин
Стадия A: трет-Бутил-N-[4-(бензилокси)фенил]карбамат
К смеси трет-бутил-N-(4-гидроксифенил)карбамата (25 г, 0.12 моль) и карбоната калия (24.77 г, 0.18 моль) в ДМФА (400 мл) добавляют бензилбромид (22.48 г, 0.13 ммоль) и реакционную смесь нагревают при 50°C в течение 16 ч. Реакционной смеси дают охладиться до температуры окружающей среды, и добавляют воду (100 мл), вызывая осаждение белого твердого вещества. Добавляют дополнительное количество воды (500 мл) и получаемую суспензию перемешивают в течение 30 мин. Твердое вещество выделяют путем фильтрования, промывают водой и сушат в вакууме. Твердое вещество затем растворяют в дихлорметане (250 мл), сушат над сульфатом магния и концентрируют в вакууме с получением целевого продукта (32.05 г, 0.11 ммоль) в виде белого кристаллического твердого вещества.
ЖХ/МС (C18H21NO3) 200 [М-Вос+Н]+; RT 1.45 (Метод В)
Стадия В: трет-Бутил-N-[4-(бензилокси)фенил]-N-этилкарбамат
К охлажденному раствору соединения, полученного на Стадии A, (5 г, 16.7 ммоль) в ТГФ (50 мл) порциями добавляют гидрид натрия (1.34 г, 33.4 ммоль), и получаемой смеси дают перемешиваться в течение 40 мин. Добавляют йодэтан (2.69 мл, 33.4 ммоль) и реакционной смеси дают перемешиваться при температуре окружающей среды в течение 1 ч и затем при 40°C в течение прибл. 16 ч. Реакционную смесь охлаждают, гасят водой и затем экстрагируют этилацетатом. Органическую фазу последовательно промывают водным раствором тиосульфата натрия, водным раствором бикарбоната натрия, и солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме, и затем адсорбируют на изолют и очищают с помощью хроматографии (CombiFlash Rf, 80 г RediSep™ силикагелевый картридж) при элюировании в градиенте изогексан - 15% этилацетат в изогексане с получением целевого продукта (5.37 г, 16.4 ммоль).
ЖХ/МС (C20H25NO3) 228 [М-Вос+Н]+; RT 1.52 (Метод В)
Стадия C: 4-(Бензилокси)-N-этиланилин
К раствору соединения, полученного на Стадии B (5.37 г, 16.4 ммоль, 1 экв.) в дихлорметане (50 мл) добавляют трифторуксусную кислоту (5 мл) и смесь перемешивают при температуре окружающей среды в течение 2 часов. Реакционную смесь разбавляют водой и подщелачивают водным 1 М гидроксидом натрия. Органический экстракт сушат над сульфатом магния, фильтруют, концентрируют в вакууме и затем адсорбируют на изолют и очищают с помощью хроматографии (CombiFlash Rf, 40 г RediSep™ силикагелевый картридж) при элюировании в градиенте изогексан - 25% этилацетат в изогексане с получением продукта в виде желтого масла (3.24 г, 14.25 ммоль).
ЖХ/МС (C15H17NO) 228 [М+Н]+; RT 1.03 (Метод В)
Синтез 3d: 4-(Бензилокси)-N-пропиланилин
Методика соответствует методике Синтеза 3с с заменой йодэтана, используемого на Стадии B, на 1-йодпропан.
ЖХ/МС (C16H19NO) 242 [М+Н]+; RT 1.21 (Метод В)
Синтез 3е: 4-(Бензилокси)-N-бутиланилин
Методика соответствует методике Синтеза 3с с заменой йодэтана, используемого на Стадии B, на 1-йодбутан.
ЖХ/МС (C17H21NO) 256 [М+Н]+; RT 1.56 (Метод В)
Синтез 3f: 4-({4-[(трет-Бутилдиметилсилил)окси]фенил}амино)-1,5-диметил-1H-пиррол-2-карбонитрил
Стадия A: 4-Бром-1,5-диметил-1 Н-пиррол-2-карбонитрил
Раствор брома (6.58 мл, 0.13 моль) в уксусной кислоте (60 мл) добавляют по каплям с помощью капельной воронки к раствору 1,5-диметил-1H-пиррол-2-карбонитрила (15.0 г, 0.12 моль) в уксусной кислоте (300 мл). Все количество перемешивают при температуре окружающей среды в течение 24 часов. Затем реакционную смесь выливают в лабораторный стакан, содержащий 300 мл воды. Образовавшееся твердое вещество отфильтровывают и промывают водой. Вещество затем растворяют в дихлорметане (300 мл) и органическую фазу промывают солевым раствором, сушат над сульфатом натрия, фильтруют и концентрируют в вакууме с получением ожидаемого продукта в виде твердого вещества.
1H ЯМР (CDCl3) δ м.д.: 2.25 (s, 3 Н), 3.67 (s, 3 Н), 6.74 (s, 1 Н)
Стадия В: 4-({4-[(трет-Бутилдиметилсилил)окси]фенил}амино)-1,5-диметил-1Н-пиррол-2-карбонитрил
Раствор соединения предшествующей стадии (1.5 г, 7.53 ммоль), 4-[(трет-бутилдиметилсилил)окси]анилина (2.02 г, 9.04 ммоль), трет-бутилата натрия (1.45 г, 15.06 ммоль) и 2-ди-трет-бутилфосфино-2',4',6'-триизопропилбифенила (0.13 г, 0.30 ммоль) в толуоле (20 мл) продувают азотом. Добавляют трис(дибензилиденацетон)дипалладий(0) (0.28 г, 0.30 ммоль), и затем реакционную смесь нагревают при 90°C до тех пор, пока реакция не завершится (контролируют с помощью ТСХ). Нагревание прекращают и температуре смеси дают вернуться к температуре окружающей среды. Добавляют воду (75 мл) и смесь экстрагируют этилацетатом (3×75 мл). Объединенные органические фазы промывают солевым раствором и затем концентрируют. Сырой продукт абсорбируют на силикагеле и очищают с помощью флэш-хроматографии на силикагеле смесью этилацетата и гептана (0-30%). Полученный таким способом продукт растворяют в горячем гептане и дают осесть при перемешивании при температуре окружающей среды и затем при 0°C. Твердое вещество отфильтровывают и операцию повторяют на фильтрате с получением ожидаемого соединения в виде твердого вещества.
1Н ЯМР (400 МГц, CDCl3) δ м.д.: 0.15 (s, 6 Н), 0.97 (s, 9 Н), 2.13 (s, 3 Н), 3.66 (s, 3 Н), 4.68 (br. s, 1 Н), 6.49 (d, J=8.5 Гц, 2 Н), 6.64 (s, 1 Н), 6.66 (d, J=8.7 Гц, 2 Н)
13С ЯМР (100 МГц, CDCl3) δ м.д.: 4.34, 9.72, 18.30, 25.88, 32.94, 101.27, 114.37, 114.70, 116.41, 120.73, 124.52, 131.23, 141.54, 148.27
MS (ESI+): [М+Н]+ найдено: 342.3
Синтез 4а: N-[4-(Бензилокси)фенил]-N-метил-3-(тетраметил-1,3,2-диоксаборолан-2-ил)-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия A: 1-Формилпиперидин-2-карбоновая кислота
К смеси DL-пипеколиновой кислоты (33.45 г, 259 ммоль) в муравьиной кислоте (250 мл), охлажденной до 0°C, по каплям добавляют ангидрид уксусной кислоты (171 мл, 1.81 моль) в течение прибл. 60 минут. Реакционной смеси дают нагреться до комнатной температуры, перемешивают в течение прибл. 16 часов и затем охлаждают на бане с водой и льдом. Добавляют воду (250 мл), смесь перемешивают в течение 10 минут и затем концентрируют в вакууме. Для азеотропного удаления воды и уксусной кислоты добавляют и упаривают в вакууме толуол (3×50 мл), и затем остаток растворяют в дихлорметане (60 мл), фильтруют через гидрофобную фритту и фильтрат упаривают в вакууме с получением продукта в виде масла.
Стадия B: Метил 5,6,7,8-тетрагидроиндолизин-1-карбоксилат
К перемешиваемому раствору формилированной пипеколиновой кислоты, полученной на Стадии A, (13.26 г, 84.48 ммоль) в дихлорэтане (100 мл) добавляют тозилхлорид (17.69 г, 92.8 ммоль) и, далее, метил-альфа-хлоракрилат (15.4 мл, 151.86 ммоль). Затем по каплям добавляют триэтиламин (23.52 мл, 168.74 ммоль). Реакционную смесь перемешивают в течение 10 минут, и затем нагревают с обратным холодильником. Через 3 часа реакционную смесь охлаждают до комнатной температуры и добавляют дополнительную порцию метил-альфа-хлоракрилата (6.0 мл, 59.1 ммоль) с последующим добавлением по каплям триэтиламина (11 мл, 78.9 ммоль), и реакционную смесь нагревают с обратным холодильником в течение прибл. 16 ч. Реакционной смеси дают охладиться до комнатной температуры, распределяют между дихлорметаном и 1 М HCl, фильтруют через набивку целита и фазы разделяют. Органическую фазу промывают последовательно 1 н. HCl, насыщенным раствором NaHCO3 и затем солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме и затем адсорбируют на силикагель и очищают с помощью хроматографии (CombiFlash Rf, 220 г RediSep™ силикагелевый картридж) при элюировании в градиенте изогексан - 30% этилацетат в изогексане с получением масла.
ЖХ/МС (C10H13NO2) 180 [М+Н]+; RT 1.13 (Метод В)
Стадия C: 5,6,7,8-Тетрагидроиндолизин-1-карбоновая кислота
К раствору сложного эфира, полученного на Стадии B, (2 г, 11.2 ммоль) в диоксане (15 мл) добавляют раствор LiOH (936 мг, 22.3 ммоль) в воде (15 мл) и реакционную смесь перемешивают при 100°C в течение 5 часов. Реакционную смесь охлаждают, разбавляют водой, подкисляют до ~рН 2 с помощью 2 М HCl и полученный в результате осадок отфильтровывают и промывают водой и затем сушат в вакууме с получением продукта в виде порошка.
ЖХ/МС (C9H11NO2) 166 [М+Н]+; RT 1.72 (Метод А)
Стадия D: N-[4-(Бензилокси)фенил]-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Кислоту, полученную на Стадии C, (1 г, 6.05 ммоль) подвергают азеотропной перегонке с минимальным объемом толуола и затем растворяют в безводном дихлорметане (50 мл). Раствор охлаждают до -10°C в атмосфере азота и по каплям добавляют оксалилхлорид (2М в дихлорметане, 3 мл, 6.05 ммоль) и затем смесь перемешивают в течение часа, поддерживая температуру при -10°C. К реакционной смеси по каплям добавляют раствор пиридина (0.73 мл, 9.08 ммоль) и 4-(бензилокси)-N-метиланилина (1.42 г, 6.7 ммоль) в дихлорметане (3 мл) при -10°C и затем дают нагреться до температуры окружающей среды. Через 4 часа добавляют дополнительное количество пиридина (0.24 мл, 3 ммоль) и перемешивание продолжают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь загружают на предварительно набитую силикагелем колонку и очищают в градиенте изогексан - 40% этилацетат/изогексан с получением целевого продукта в виде порошка.
ЖХ/МС (C23H24N2O2) 361 [М+Н]+; RT 2.68 (Метод А)
Стадия E: N-[4-(Бензилокси)фенил]-3-бром-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору соединения, полученного на Стадии D, (3.49 г, 9.68 ммоль) в тетрагидрофуране (35 мл), охлажденному до -78°C, в атмосфере азота порциями добавляют N-бромсукцинимид (1 экв.) и затем получаемую смесь перемешивают в течение 1 часа. Реакционной смеси дают нагреться до температуры окружающей среды, затем разбавляют этилацетатом и промывают 10% раствором тиосульфата натрия, насыщенным раствором бикарбоната натрия и солевым раствором. Органическую фазу затем сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Сырой продукт очищают с помощью хроматографии на силикагеле в градиенте изогексан - 1:1 этилацетат/изогексан, затем растирают с эфиром и фильтруют с получением порошка.
ЖХ/МС (C23H23N2O2Br) 439 [М+Н]+; RT 2.74 (Метод А)
Стадия F: N-[4-(Бензилокси)фенил]-N-метил-3-(тетраметил-1,3,2-диоксаборолан-2-ил)-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору бромида, полученного на Стадии Е, (6.47 г, 14.73 ммоль) в безводном тетрагидрофуране (83 мл), охлажденному до -78°C, по каплям добавляют раствор «-бутиллития в гексанах (2.17 М, 7.47 мл, 16.20 ммоль) в течение прибл. 20 минут. Еще через 15 минут, по каплям добавляют 2-изопропил-4,4,5,5-тетраметил-1,3,2-диоксаборолан (3.61 мл, 17.67 ммоль) и перемешивание продолжают в течение 15 мин. Реакционную смесь гасят при -78°C путем добавления 20 мл насыщенного раствора хлорида аммония, и затем дают нагреться до температуры окружающей среды. Реакционную смесь распределяют между водой и этилацетатом и фазы разделяют. Органическую фазу промывают водой, насыщенным раствором NaCl, затем сушат над сульфатом магния, фильтруют и фильтрат концентрируют в вакууме до твердого вещества. Твердое вещество затем растирают с диэтиловым эфиром, отфильтровывают, промывают холодным эфиром и сушат в вакууме с получением продукта в виде порошка.
ЖХ/МС (C29H35BN2O4) 487 [М+Н]+; RT 1.59 (Метод В)
Синтез 4b: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-(тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол-3-карбоксамид
Стадия A: Этил 1,2-диметил-1Н-пиррол-3-карбоксилат
К охлажденному раствору 2-метил-7H-пиррол-3-карбоксилата (5 г, 32.64 ммоль) в ТГФ (50 мл) добавляют 60% NaH в минеральном масле (2.61 г, 65.28 ммоль) и получаемую смесь перемешивают при 0°C в течение 40 минут. Затем добавляют метилйодид (4.07 мл, 65.28 ммоль) и смеси дают перемешиваться в течение 1 часа. Реакцию гасят путем добавления по каплям воды (20 мл) и затем экстрагируют этилацетатом (20 мл×2). Органические экстракты промывают последовательно 10% водным раствором тиосульфата и солевым раствором, затем сушат над сульфатом магния, фильтруют и концентрируют. Сырой продукт вносят в дихлорметан и загружают на изолют для очистки на CombiFlash (120 г, силикагель, Hex - 20% EtOAc/Hex) с получением целевого продукта в виде масла.
ЖХ/МС (C9H13NO2) 168 [М+Н]+; RT 1.11 (Метод В)
Стадия B: 1,2-Диметил-1Н-пиррол-3-карбоновая кислота
К раствору продукта из Стадии A (5.3 г, 31.7 ммоль) в 1,4-диоксане (60 мл) добавляют 1 М LiOH (2.66 г, 63.4 ммоль) в воде (60 мл) и реакционную смесь перемешивают при 100°C в течение прибл. 16 ч. Реакционной смеси дают охладиться до температуры окружающей среды, разбавляют водой и подкисляют с помощью 2 М HCl. Полученный в результате осадок собирают путем вакуумного фильтрования с получением целевого продукта. Фильтрат экстрагируют этилацетатом и органические экстракты сушат над сульфатом магния, фильтруют и концентрируют с получением дополнительной порции целевого продукта.
ЖХ/МС (C7H9NO2) нет ионизации; RT 0.71 (Метод В)
Стадия C: N-[4-(Бензилокси)фенил]-N,1,2-триметил-1Н-пиррол-3-карбоксамид
Кислоту, полученную из Стадии B (1 г, 7.19 ммоль) растворяют в дихлорметане (20 мл), к раствору добавляют 1-хлор-N,N,2-триметил-1-пропениламин (1.15 г, 8.62 ммоль) и перемешивают при температуре окружающей среды в течение 2 часов. Смесь концентрируют до масла, которое повторно растворяют в толуоле (50 мл). Добавляют раствор 4-(бензилокси)-N-метиланилина (1.84 г, 8.62 ммоль) в толуоле (10 мл) и получаемую смесь перемешивают при нагревании с обратным холодильником в течение 2 часов. Реакционной смеси дают охладиться до температуры окружающей среды и оставляют стоять в течение прибл. 16 ч. Реакционную смесь распределяют между этилацетатом и водой, разделяют, и органику промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Сырой продукт очищают на CombiFlash (80 г, силикагель, Hex - 60% EtOAc) с получением целевого продукта в виде твердого вещества.
ЖХ/МС (C21H22N2O2) 335 [М+Н]+; RT 1.33 (Метод В)
Стадия D: N-[4-(Бензилокси)фенил]-5-бром-N,1,2-триметил-1Н-пиррол-3-карбоксамид
Продукт из Стадии C (1.74 г, 5.19 ммоль) растворяют в ТГФ (20 мл) и охлаждают до -78°C. Затем, порциями до добавления всего количества, добавляют N-бромсукцинимид (924 мг, 5.19 ммоль) и смесь затем перемешивают в течение 15 минут. Реакционной смеси дают нагреться до температуры окружающей среды, разбавляют этилацетатом и промывают последовательно 10% раствором тиосульфата натрия, насыщенным раствором бикарбоната натрия и солевым раствором. Органику затем сушат над сульфатом магния, фильтруют и концентрируют. Сырое вещество вносят в дихлорметан, загружают на изолют и очищают на CombiFlash (80 г, силикагель, Hex - 70% EtOAc/Hex) с получением продукта в виде твердого вещества.
ЖХ/МС (C21H21N2O2Br) 413 [М+Н]+; RT 1.42 (Метод В)
Стадия E: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-(тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиррол-3-карбоксамид
Бромид из Стадии D (1,74 g, 4.21 ммоль) и 2-изопропокси-4,4,5,5-тетраметил-1,3,2-диоксаборолан (0.94 г, 5.05 ммоль) объединяют и растворяют в безводном ТГФ (20 мл). Реакционную смесь охлаждают до - 78°C в атмосфере азота с последующим добавлением по каплям 2 М n-BuLi (2.13 мл, 4.25 ммоль) в течение 50 минут. Реакцию затем гасят путем добавления насыщенного водного раствора хлорида аммония, и смеси дают нагреться до температуры окружающей среды, разбавляют этилацетатом и затем промывают водой и, далее, солевым раствором. Органику сушат над сульфатом магния, фильтруют и концентрируют до масла, которое отвердевает при добавлении эфира. Повторное упаривание и сушка в вакууме дает целевой продукт.
ЖХ/МС (C27H33BN2O4) 461 [М+Н]+; RT 1.51 (Метод В)
Синтез 4с: N,1,2-Триметил-N-фенил-5-(тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол-3-карбоксамид
Методика соответствует методике Синтеза 4b с заменой 4-(бензилокси)-N-метиланилина, используемого на Стадии C, на N-метиланилин.
ЖХ/МС (C20H27BN2O3) 355 [М+Н]+; RT 1.39 (Метод В)
Синтез 4d: N,N-Дибутил-1,2-диметил-5-(тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол-3-карбоксамид
Методика соответствует методике Синтеза 4b с заменой 4-(бензилокси)-N-метиланилина, используемого на Стадии C, на дибутиламин.
ЖХ/МС (C21H37BN2O3) 377 [М+Н]+; RT 1.55 (Метод В)
Синтез 4е: N-{4-[(трет-Бутилдиметилсилил)окси]фенил}-N-метил-3-(тетраметил-1,3,2-диоксаборолан-2-ил)-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Синтеза 4а с заменой 4-(бензилокси)-N-метиланилина на Стадии D на 4-[(трет-бутилдиметилсилил)окси]-N-метиланилин из Синтеза 3а.
Синтез 4f: N-[4-(Бензилокси)фенил]-N-фенил-3-(тетраметил-1,3,2-диоксаборолан-2-ил)-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Синтеза 4а с заменой 4-(бензилокси)-N-метиланилина на Стадии D на 4-(бензилокси)-N-фениланилин из Синтеза 3b.
Синтез 4g: N-[4-(Бензилокси)фенил]-N-этил-1,2-диметил-5-(тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол-3-карбоксамид
Методика соответствует методике Синтеза 4b с заменой 4-(бензилокси)-N-метиланилина, используемого на Стадии C, на 4-(бензилокси)-N-этиланилин из Синтеза 3с.
ЖХ/МС (C28H35BN2O4) 475 [М+Н]+; RT 1.49 (Метод В)
Синтез 4h: N-[4-(Бензилокси)фенил]-1,2-диметил-N-пропил-5-(тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол-3-карбоксамид
Методика соответствует методике Синтеза 4b с заменой 4-(бензилокси)-N-метиланилина, используемого на Стадии C, на 4-(бензилокси)-N-пропиланилин из Синтеза 3d.
ЖХ/МС (C29H37BN2O4) 489 [М+Н]+; RT 1.57 (Метод В)
Синтез 4i: N-[4-(Бензилокси)фенил]-N-бутил-1,2-диметил-5-(тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол-3-карбоксамид
Методика соответствует методике Синтеза 4b с заменой 4-(бензилокси)-N-метиланилина, используемого на Стадии C, на 4-(бензилокси)-N-бутиланилин из Синтеза 3е.
ЖХ/МС (C30H39BN2O4) 503 [М+Н]+; RT 1.55 (Метод В)
Синтез 5а: 6-(1-{[4-(Бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-2-[(трет-бутокси)карбонил]-1,2,3,4-тетрагидроизохинолин-7-карбоновая кислота
Стадия А: 2-трет-Бутил 7-метил 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
Бороновую кислоту, полученную в Синтезе 4а (1.22 г, 2.50 ммоль) и трифлат, полученный в Синтезе 1b (1.1 г, 2.50 ммоль) суспендируют в 15 мл безводного N,N-диметилформамида и смесь дегазируют (барботирование N2) в течение 45 минут. Добавляют Cs2CO3 (1.63 г, 5 ммоль) и бис(ди-трет-бутил(4-диметиламинофенил)-фосфин)дихлорпалладий(II) (88.5 мг, 0.13 ммоль) и получаемую смесь герметизируют и немедленно нагревают в микроволновой печи при 130°C в течение 30 минут. Реакционную смесь концентрируют и повторно растворяют в этилацетате, промывают солевым раствором, сушат над сульфатом магния, фильтруют и концентрируют. Сырой продукт очищают с помощью флэш-хроматографии на CombiFlash (120 г, силикагель, дихлорметан -20% метанол/дихлорметан) с получением целевого продукта.
ЖХ/МС (C39H43N3O6) 650 [М+Н]+; RT 1.54 (Метод В)
Стадия В: 6-(1-{[4-(Бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-2-[(трет-бутокси)карбонил]-1,2,3,4-тетрагидроизохинолин-7-карбоновая кислота
К раствору сложного эфира, полученного на Стадии A, (730 мг, 1.12 ммоль) в диоксане (10 мл) добавляют раствор LiOH (94 мг, 2.24 ммоль) в воде (5 мл). Затем реакционную смесь нагревают при 90°C в течение прибл. 16 ч. Добавляют еще 94 мг LiOH (2.24 ммоль) в воде (5 мл) и смесь перемешивают в течение 1 часа для завершения реакции. Смесь охлаждают, разбавляют водой и подкисляют до ~pH 4 разбавленной водной HCl. Образованный осадок перемешивают в течение 30 минут и затем отфильтровывают, промывают холодной водой и сушат в вакууме с получением целевого продукта.
ЖХ/МС (C38H41N3O6) 636 [М+Н]+; RT 1.46 (Метод В)
Синтез 5b: 2-трет-Бутил 7-литио 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1H-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
Стадия А: 2-трет-Бутил 7-метил 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
Бороновую кислоту из Синтеза 4b (1 г, 1.7 ммоль) и нонафлат из Синтеза 1а (0.94 г, 2.04 ммоль) растворяют в ДМФА (20 мл) и дегазируют (барботирование азота) в течение 20 минут. Добавляют карбонат цезия (1.3 г, 4.04 ммоль) и бис(ди-трет-бутил(4-диметиламинофенил)фосфин)дихлорпалладий(II) (60 мг, 0.085 ммоль) и получаемую смесь немедленно нагревают в микроволновой печи при 130°C в течение 30 минут. ДМФА упаривают, и остаток, растворенный в этилацетате, промывают солевым раствором, затем сушат над сульфатом магния, фильтруют и концентрируют. Сырое вещество вносят в дихлорметан, загружают на изолют и очищают на CombiFlash (120 г, силикагель, Hex - 70% EtOAc/Hex) с получением продукта в виде пены.
ЖХ/МС (C37H41N3O6) 624 [М+Н]+; RT 1.55 (Метод В)
Стадия В: 2-трет-Бутил 7-литио 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
К раствору сложного эфира, полученного на Стадии A, (2.17 г, 3.48 ммоль) в диоксане (20 мл) добавляют водный раствор LiOH (2 М; 3.48 мл, 6.96 ммоль), и получаемую смесь нагревают с обратным холодильником в течение прибл. 16 ч. Реакционной смеси дают охладиться до температуры окружающей среды и твердые вещества удаляют путем фильтрования. Раствор концентрируют с получением целевого продукта в виде твердого вещества.
ЖХ/МС (C36H39N3O6) 610 [М+Н]+; RT 1.47 (Метод В)
Синтез 5с: 2-[(трет-Бутокси)карбонил]-6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-1,2,3,4-тетрагидроизохинолин-7-карбоновая кислота
Стадия А: 2-трет-Бутил 7-метил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
Методика соответствует методике Стадии A Синтеза 5b с заменой N-[4-(бензилокси)фенил]-N,1,2-триметил-5-(тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол-3-карбоксамида на продукт из Синтеза 4с.
Стадия В: 2-[(трет-Бутокси)карбонил]-6-{1,5-диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-1,2,3,4-тетрагидроизохинолин-7-карбоновая кислота
Методика соответствует методике Стадии B из Синтеза 5а с заменой 2-трет-бутил 7-метил 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилата на продукт из Стадии A.
Синтез 5d: 2-трет-Бутил 7-литио 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
Методика соответствует методике Синтеза 5b с заменой N-[4-(бензилокси)фенил]-N,1,2-триметил-5-(тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол-3-карбоксамида на продукт из Синтеза 4d.
Синтез 5е: 2-[(трет-Бутокси)карбонил]-6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-1,2,3,4-тетрагидроизохинолин-7-карбоновая кислота
Стадия А: трет-Бутил 6-[1-({4-[(трет-бутилдиметилсилил)окси]фенил}(метил)карбамоил)-5,6,7,8-тетрагидроиндолизин-3-ил]-7-формил-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Трифлат из Синтеза 1с (610 мг, 1.49 ммоль), бороновую кислоту из Синтеза 4е (910 мг, 1.79 ммоль) и карбонат калия (412 мг, 2.98 ммоль) растворяют в смеси ТГФ/вода и дегазируют (барботирование азота) в течение 15 минут. К смеси добавляют тетракис(трифенилфосфин)палладий(0) (5 мол.%) и получаемую смесь перемешивают при комнатной температуре в течение 45 мин. Реакционную смесь разбавляют этилацетатом, промывают водой и, далее, солевым раствором, и органику сушат над сульфатом магния и упаривают при пониженном давлении. Таким образом полученный сырой продукт очищают на CombiFlash (40 г, силикагель; изогексан - этилацетат) с получением целевого продукта.
ЖХ/МС (C37H49N3O5Si) 644 [М+Н]+; RT 1.71 (Метод В)
Стадия В: 2-трет-Бутил 7-метил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
Методика соответствует методике Стадии B
Синтеза 1а с заменой 2:1 смеси изомеров - трет-бутил 7-формил-6-гидрокси-1,2,3,4-тетрагидроизохинолин-2-карбоксилата и трет-бутил 5-формил-6-гидрокси-1,2,3,4-тетрагидроизохинолин-2-карбоксилата - на трет-бутил 6-[1-({4-[(трет-бутилдиметилсилил)окси]фенил}(метил)карбамоил)-5,6,7,8-тетрагидроиндолизин-3-ил]-7-формил-1,2,3,4-тетрагидроизохинолин-2-карбоксилат. Реакционную смесь нагревают при внешней температуре 45°C в течение 24 ч для содействия завершению наблюдаемого частичного десилилирования.
Стадия С: 2-[(трет-Бутокси)карбонил]-6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-1,2,3,4-тетрагидроизохинолин-7-карбоновая кислота
Методика соответствует методике Стадии B Синтеза 5а с заменой 2-трет-бутил 7-метил 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилата на 2-трет-бутил 7-метил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат.
Синтез 5f: 2-трет-Бутил 7-литио 6-(4-{[4-(бензилокси)фенил](этил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
Методика соответствует методике Синтеза 5b с заменой N-[4-(бензилокси)фенил]-N,1,2-триметил-5-(тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол-3-карбоксамида на продукт из Синтеза 4g.
ЖХ/МС (C37H41N3O6) 624 [М+Н]+; RT 1.50 (Метод В)
Синтез 5g: 2-трет-Бутил 7-литио 6-(4-{[4-(бензилокси)фенил](пропил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат
Методика соответствует методике Синтеза 5b с заменой N-[4-(бензилокси)фенил]-N,1,2-триметил-5-(тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол-3-карбоксамида на продукт из Синтеза 4h.
ЖХ/МС (C38H43N3O6) 638 [М+Н]+; RT 1.54 (Метод В)
Синтез 6аа: N-[4-(Бензилокси)фенил]-N-метил-3-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид, бис-соль с трифторуксусной кислотой
Стадия А: трет-Бутил 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору кислоты, полученной в Синтезе 5а, (150 мг, 0.24 ммоль) в N,N-диметилформамиде (2 мл) добавляют триэтиламин (0.13 мл, 0.96 ммоль), HBTU (91 мг, 0.24 ммоль) и дигидрохлорид (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина, полученный в Синтезе 2а (72 мг, 0.24 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 15 минут и затем разбавляют водой, и полученную в результате суспензию перемешивают. Продукт затем экстрагируют этилацетатом и органический экстракт сушат над сульфатом магния, фильтруют и концентрируют. Сырое вещество очищают на CombiFlash (12 г, силикагель, дихлорметан - 4% метанол/дихлорметан) и затем сушат в вакууме с получением продукта в виде стеклообразного твердого вещества.
ЖХ/МС (C52H59N5O6) 850 [М+Н]+; RT 1.49 (Метод В)
Стадия B: N-[4-(Бензилокси)фенил]-N-метил-3-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид, бис-соль с трифторуксусной кислотой
Вос-защищенное вещество, полученное на Стадии A, (173 мг, 0.2 ммоль) растворяют в дихлорметане (10 мл) и к раствору добавляют трифторуксусную кислоту (1 мл). Реакционной смеси дают перемешиваться в течение 1 часа при температуре окружающей среды и затем концентрируют в вакууме. Остаток растирают в диэтиловом эфире с получением осадка, который отфильтровывают и сушат в вакууме.
ЖХ/МС (C47H51N5O4) 750 [М+Н]+; RT 1.10 (Метод В)
Синтез 6ab: N-[4-(Бензилокси)фенил]-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид; соль с трифторуксусной кислотой
Стадия А: трет-Бут ил 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К перемешиваемому раствор кислоты, полученной из Синтеза 5а, (0.87 г, 1.36 ммоль) в ДМФА (10 мл) добавляют диизопропилэтиламин (0.47 мл, 2.72 ммоль) и (3R)-3-метил-1,2,3,4-тетрагидроизохинолин из Синтеза 2b (210 мг, 1.43 ммоль) и, далее, HBTU (516 мг, 1.36 ммоль). Реакционную смесь перемешивают в течение 1 ч, затем разбавляют водой и экстрагируют этилацетатом. Органические экстракты последовательно промывают водным бикарбонатом натрия и солевым раствором, затем сушат над сульфатом магния и упаривают в вакууме. Сырой продукт вносят в дихлорметан, загружают на изолют и очищают на CombiFlash (40 г, силикагель, градиент изогексан - этилацетат) с получением целевого продукта в виде пены.
ЖХ/МС (C48H52N4O5) 765 [М+Н]+; RT 1.62 (Метод В)
Стадия B: N-[4-(Бензилокси)фенил]-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид; соль с трифторуксусной кислотой
Вос-защищенный продукт из Стадии A (0.90 г, 1.18 ммоль) растворяют в дихлорметане (10 мл) и к раствору добавляют ТФУ (1 мл). Реакционную смесь перемешивают в течение 1 ч, затем растворитель удаляют при пониженном давлении, и остаточный растворитель удаляют в высоком вакууме. Добавление эфира к получаемому маслу вызывало его отверждение. Смесь перемешивают в течение 45 мин, затем охлаждают, фильтруют и промывают холодным эфиром с получением целевого продукта. Концентрирование фильтрата дает дополнительное количество твердого продукта. Объединенные твердые вещества сушат в вакууме с получением продукта.
ЖХ/МС (C43H44N4O3) 665 [М+Н]+; RT 1.24 (Метод В)
Синтез 6ba: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид; бис-соль с трифторуксусной кислотой
Стадия А: трет-Бутил 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Соль лития из Синтеза 5b (1.07 г, 1.74 ммоль) вносят в ДМФА (10 мл) и к раствору добавляют триэтиламин (0.97 мл, 6.96 ммоль), HBTU (660 мг, 1.74 ммоль), и дигидрохлорид (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина, полученный в Синтезе 2а (0.58 г, 1.91 ммоль) и получаемую смесь затем перемешивают в течение 15 минут при температуре окружающей среды. Реакционную смесь разбавляют водой и экстрагируют этилацетатом. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют. Сырое вещество вносят в дихлорметан, загружают на изолют и очищают на CombiFlash (40 г силикагель, дихлорметан - 5% МеОН/дихлорметан) с получением целевого продукта.
ЖХ/МС (C50H57N5O6) 824 [М+Н]+; RT 1.44 (Метод В)
Стадия B: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1Н-пиррол-3-карбоксамид; бис-соль с трифторуксусной кислотой
Вос-защищенный продукт из Стадии A (705 мг, 0.86 ммоль) растворяют в дихлорметане и к раствору добавляют трифторуксусную кислоту (1.33 мл). Получаемой смеси затем дают перемешиваться при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь концентрируют в вакууме и остаток растирают с эфиром с получением осадка, который фильтруют и сушат в вакууме с получением целевого продукта.
ЖХ/МС (C45H49N5O4) 724 [М+Н]+; RT 1.07 (Метод В)
Синтез 6bb: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид; соль с трифторуксусной кислотой
Методика соответствует методике Синтеза 6bа с заменой дигидрохлорида (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина на Стадии A на (3R)-3-метил-1,2,3,4-тетрагидроизохинолин из Синтеза 2b.
ЖХ/МС (C41H42N4O3) 639 [М+Н]+; RT 1.18 (Метод В)
Синтез 6bс: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-{7-[(3S)-3-[2-(морфолин-4-ил)этил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид; бис-соль с трифторуксусной кислотой
Методика соответствует методике Синтеза 6bа с заменой дигидрохлорида (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина на Стадии A на дигидрохлорид (3S)-3-[2-(морфолин-4-ил)этил]-1,2,3,4-тетрагидроизохинолина, полученный из Синтеза 2d.
ЖХ/МС (C46H51N5O4) 738 [М+Н]+; RT 1.07 (Метод В)
Синтез 6bd: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-{7-[(3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Методика соответствует методике Синтеза 6bа с заменой дигидрохлорида (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина на Стадии A на дигидрохлорид (3S)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолина из Синтеза 2f. Промежуточное соединение выделяют в виде свободного основания.
ЖХ/МС (C47H53N5O4) 752 [М+Н]+; RT 1.03 (Метод В)
Синтез 6bе: N-[4-(Бензилокси)фенил]-5-{7-[(3S)-3-[(диметиламино)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N,1,2-триметил-1H-пиррол-3-карбоксамид; бис-соль с трифторуксусной кислотой
Методика соответствует методике Синтеза 6bа с заменой дигидрохлорида (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина на Стадии A на дигидрохлорид диметил[(3S)-1,2,3,4-тетрагидроизохинолин-3-илметил]амина из Синтеза 2g.
ЖХ/МС (C43H47N5O3) 682 [М+Н]+; RT 1.02 (Метод В)
Синтез 6bf: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-{7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид; трис-соль с трифторуксусной кислотой
Методика соответствует методике Синтеза 6bа с заменой дигидрохлорида (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина на Стадии A на тригидрохлорид (3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолина из Синтеза 2h.
ЖХ/МС (C46H52N6O3) 737 [М+Н]+; RT 1.04 (Метод В)
Синтез 6са: N,1,2-Триметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-7H-фенил-1H-пиррол-3-карбоксамид; бис-соль с трифторуксусной кислотой
Методика соответствует методике Синтеза 6bа с заменой 2-трет-бутил 7-литио 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1H-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилата на Стадии A на 2-[(трет-бутокси)карбонил]-6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-1,2,3,4-тетрагидроизохинолин-7-карбоновую кислоту из Синтеза 5с.
ЖХ/МС (C38H43N5О3) 618 [М+Н]+; RT 0.93 (Метод В)
Синтез 6cb: N,1,2-Триметил-5-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-фенил-1H-пиррол-3-карбоксамид; соль с трифторуксусной кислотой
Методика соответствует методике Синтеза 6bа с заменой дигидрохлорида (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина на Стадии A на (3R)-3-метил-1,2,3,4-тетрагидроизохинолин из Синтеза 2b; и с заменой 2-трет-бутил 7-литио 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилата на Стадии A на 2-[(трет-бутокси)карбонил]-6-{1,5-диметил-4-[метил (фенил)карбамоил]-1H-пиррол-2-ил}-1,2,3,4-тетрагидроизохинолин-7-карбоновую кислоту из Синтеза 5с.
Синтез 6cd: N,1,2-Триметил-5-{7-[(3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-фенил-1H-пиррол-3-карбоксамид
Методика соответствует методике Синтеза 6bа с заменой дигидрохлорида (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина на Стадии A на дигидрохлорид (3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолина из Синтеза 2f; и с заменой 2-трет-бутил 7-литио 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1H-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилата на Стадии A на 2-[(трет-бутокси)карбонил]-6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-1,2,3,4-тетрагидроизохинолин-7-карбоновую кислоту из Синтеза 5с. Промежуточное соединение выделяют в виде свободного основания.
ЖХ/МС (C40H47N5O3) 646 [М+Н]+; RT 0.91 (Метод В)
Синтез 6ее: N,1,2-триметил-5-{7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-фенил-1H-пиррол-3-карбоксамид; трис-соль с трифторуксусной кислотой
Методика соответствует методике Синтеза 6bа с заменой дигидрохлорида (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина на Стадии A на тригидрохлорид (3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолина из Синтеза 2h, и с заменой 2-трет-бутил 7-литио 6-(4-{[4-(бензилокси)фенил] (метил)карбамоил}-1,5-диметил-1H-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилата на Стадии A на 2-[(трет-бутокси)карбонил]-6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-1,2,3,4-тетрагидроизохинолин-7-карбоновую кислоту из Синтеза 5с.
ЖХ/МС (C39H46N6O2) 631 [М+Н]+; RT 0.91 (Метод В)
Синтез 6da: N,N-Дибутил-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид; бис-соль с трифторуксусной кислотой
Методика соответствует методике Синтеза 6bа с заменой 2-трет-бутил 7-литио 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1H-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилата на Стадии A на 2-трет-бутил 7-литио 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат из Синтеза 5d.
ЖХ/МС (C39H53N5O3) 640 [М+Н]+; RT 1.10 (Метод В)
Синтез 6db: N,N-Дибутил-1,2-диметил-5-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид; соль с трифторуксусной кислотой
Методика соответствует методике Синтеза 6bа с заменой дигидрохлорида (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина на Стадии A на (5R)-3-метил-1,2,3,4-тетрагидроизохинолин из Синтеза 2b; и с заменой 2-трет-бутил 7-литио 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилата на Стадии A на 2-трет-бутил 7-литио 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат из Синтеза 5d.
Синтез 6dc: N,N-Дибутил-1,2-диметил-5-[7-(1,2,3,4-тетрагидроизохинолин-2-карбонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Методика соответствует методике Синтеза 6bа с заменой дигидрохлорида (3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолина на Стадии A на тетрагидроизохинолин; и с нейтрализацией раствора продукта на Стадии B разбавленным водным раствором гидроксида натрия.
ЖХ/МС (C34H44N4O2) 541 [М+Н]+; RT 1.14 (Метод В)
Синтез 6е: Дигидрохлорид N-(4-гидроксифенил)-N-метил-3-{7-[(3R)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Стадия А: трет-Бутил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии A Синтеза баа с заменой 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-2-[(трет-бутокси)карбонил]-1,2,3,4-тетрагидроизохинолин-7-карбоновой кислоты на Стадии A на 2-[(трет-бутокси)карбонил]-6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-1,2,3,4-тетрагидроизохинолин-7-карбоновую кислоту из Синтеза 5е.
ЖХ/МС (C45H53N5O6) 760 [М+Н]+; RT 1.25 (Метод В)
Стадия B: Дигидрохлорид N-(4-гидроксифенил)-N-метил-3-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Соединение, полученное на Стадии A, (135 мг, 0.18 ммоль) растворяют в этилацетате (6.75 мл) и к раствору добавляют концентрированную HCl (148 мкл, 1.78 ммоль) и смеси дают перемешиваться в течение 30 минут. Для содействия осаждению затем по каплям добавляют минимальное количество IPA. Твердое вещество затем отфильтровывают, промывают этилацетатом и сушат в вакууме в течение ночи с получением твердого вещества.
ЖХ/МС (C40H45N5O4) 660 [М+Н]+; RT 0.89 (Метод В)
Синтез 6f: N-[4-(Бензилокси)фенил]-N-этил-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Методика соответствует методике Синтеза 6bа с заменой 2-трет-бутил 1-литио 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1H-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилата на Стадии A на 2-трет-бутил 7-литио 6-(4-{[4-(бензилокси)фенил](этил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат из Синтеза 5f; и с нейтрализацией раствора продукта на Стадии B разбавленным водным раствором гидроксида натрия.
ЖХ/МС (C46H51N5O4) 738 [М+Н]+; RT 1.08 (Метод В)
Синтез 6g: N-[4-(Бензилокси)фенил]-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-пропил-1H-пиррол-3-карбоксамид
Методика соответствует методике Синтеза 6bа с заменой 2-трет-бутил 1-литио 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1H-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилата на Стадии A на 2-трет-бутил 7-литио 6-(4-{[4-(бензилокси)фенил](пропил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-1,2,3,4-тетрагидроизохинолин-2,7-дикарбоксилат из Синтеза 5g; и с нейтрализацией раствора продукта на Стадии B разбавленным водным раствором гидроксида натрия.
ЖХ/МС (C47H53N5O4) 752 [М+Н]+; RT 1.17 (Метод В)
Синтез 6h: N-[4-(Бензилокси)фенил]-N-бутил-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3?4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Стадия A: N-[4-(бензилокси)фенил]-N-бутил-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(трифторацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1Н-пиррол-3-карбоксамид
Раствор тетрагидрофуран/вода (5:1, 7 мл) дегазируют в течение 20 мин. К смеси боронатного сложного эфира из Синтеза 4i (246 мг, 0.49 ммоль) и бромида из Синтеза 1ha (332.78 мг, 0.59 ммоль) добавляют 7 мл основного раствора. Раствор дегазируют в течение еще 5 мин и к нему добавляют карбонат цезия (319.05 мг, 0.98 ммоль, 2 экв.) и бис(ди-трет-бутил(4-диметиламинофенил)фосфин) дихлорпалладий(II) (17.33 мг, 0.02 ммоль, 0.05 экв.), и затем нагревают до 95°C в микроволновой печи в течение 40 мин. Реакционную смесь разбавляют этилацетатом и промывают солевым раствором. Органический экстракт сушат над сульфатом магния и концентрируют в вакууме, и адсорбируют на изолют и очищают на CombiFlash (12 г, силикагель, дихлорметан - 4% метанол в дихлорметане).
ЖХ/МС (C50H54F3N5O5) 862 [М+Н]+; RT 1.53 (Метод В)
Стадия B: N-[4-(Бензилокси)фенил]-N-бутил-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1Н-пиррол-3-карбоксамид
К раствору продукта из Стадии A (138 мг, 0.16 ммоль) в этаноле (6 мл) добавляют раствор карбоната калия (132.75 мг, 0.96 ммоль) в воде (1.2 мл) и смеси дают перемешиваться при нагревании с обратным холодильником в течение 1 ч. Реакционной смеси дают охладиться до температуры окружающей среды и органический растворитель концентрируют в вакууме. Отстоявшийся раствор промывают этилацетатом. Органическую фазу промывают водой и насыщенным хлоридом натрия. Органический экстракт сушат над сульфатом магния и концентрируют в вакууме. Продукт непосредственно используют на следующей стадии, предполагая количественное превращение.
ЖХ/МС (C48H55N5O4) 766 [М+Н]+; RT 1.23 (Метод В)
Синтез 7аа: N-[4-(Бензилокси)фенил]-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия А: трет-Бутил 5-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксилат
Смесь бромида из Синтеза 1е (845 мг, 1.45 ммоль), бороновой кислоты из Синтеза 4а (886 мг, 1.82 ммоль) и карбоната цезия (991 мг, 3.04 ммоль) в ТГФ (9.0 мл) и воде (3.6 мл) дегазируют с помощью продувки азотом с последующим барботированием азота через смесь в течение 5 мин. Смесь нагревают до температуры 60°C, при которой добавляют катализатор PdCl2(Ata-Phos)2 (54 мг, 0.08 ммоль) и реакционной смеси дают перемешиваться в течение 3 ч.
Смеси дают охладиться до температуры окружающей среды, затем разбавляют этилацетатом, и промывают последовательно водой и солевым раствором. Органическую фазу сушат над сульфатом магния, и концентрируют в вакууме.
Сырое вещество очищают с помощью колоночной флэш-хроматографии (40 г, силикагель; дихлорметан - 5% МеОН/дихлорметан) с получением продукта в виде стеклообразного твердого вещества.
ЖХ/МС (C51H57N5O6) 836 [М+Н]+; RT 1.53 (Метод В)
Стадия B: N-[4-(Бензилокси)фенил]-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К перемешиваемому раствору продукта из Стадии A (850 мг, 1.02 ммоль) в дихлорметане (20 мл) добавляют трифторуксусную кислоту (5 мл) и смесь перемешивают в течение 1 ч. Добавляют воду и, далее, 2 н. водный раствор гидроксида натрия до тех пор, пока водная фаза не становилась основной. Органическую фазу затем разделяют, сушат над сульфатом магния, и концентрируют в вакууме с получением продукта в виде твердого вещества.
ЖХ/МС (C46H49N5O4) 736 [М+Н]+; RT 1.12 (Метод В)
Синтез 7ab: N-[4-(Бензилокси)фенил]-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид; соль с трифторуксусной кислотой
Стадия А: трет-Бутил 5-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксилат
Смесь ТГФ (20 мл) и воды (8 мл) дегазируют путем многократного выполнения циклов вакуумирование/продувка азотом и барботирования азота через смесь. Затем 20 мл этой смеси добавляют с помощью шприца к смеси бромида из Синтеза If (0.88 г, 1.87 ммоль), бороновой кислоты из Синтеза 4а (1.09 г, 2.25 ммоль) и карбоната цезия (1.22 г, 3.74 ммоль) в атмосфере азота. Затем добавляют PdCl2(Ata-Phos)2 (66 мг, 0.09 ммоль) и реакционную смесь незамедлительно нагревают при микроволновом облучении при 95°C в течение 20 мин.
Реакционную смесь разбавляют этилацетатом (100 мл) и промывают последовательно водой (2×50 мл), затем насыщенным NaCl (водн.) (2 х 50 мл), сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Сырой продукт очищают с помощью флэш-хроматографии (Combiflash, 80 г, элюируя градиентом 0 - 80% этилацетата в гексане) с получением продукта в виде пены.
ЖХ/МС (C47H50N4O5) 751 [М+Н]+; RT 1.61 (Метод В)
Стадия В: N-[4-(Бензилокси)фенил]-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид; соль с трифторуксусной кислотой
К раствору продукта из Стадии A (152 мг, 0.20 ммоль) в дихлорметане (3 мл) добавляют трифторуксусную кислоту (0.7 мл) и реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Растворитель удаляют в вакууме и полученное в результате твердое вещество растирают с эфиром и собирают с помощью фильтрования.
ЖХ/МС (C42H42N4O3) 651 [М+Н]+; RT 2.39 (Метод А)
Синтез 7bа: Гидрохлорид N-(4-бензилоксифенил)-N,1,2-триметил-5-[6-[(3S)-3-(морфолинометил)-3,4-дигидро-1H-изохинолин-2-карбонил]изоиндолин-5-ил]пиррол-3-карбоксамида
Стадия А: трет-Бутил 5-бром-6-[(3S)-3-(морфолинометил)-3,4-дигидро-1Н-изохинолин-2-карбонил]изоиндолин-2-карбоксилат
6-Бром-2-трет-бутоксикарбонилизоиндолин-5-карбоновую кислоту (0.70 г), TBTU (0.823 г) и DMAP (25 мг) растворяют дихлорметане (35 мл) и добавляют диизопропилэтиламин (1.75 мл). Через 3 минуты перемешивания при комнатной температуре добавляют гидрохлорид 4-[[(3S)-1,2,3,4-тетрагидроизохинолин-3-ил]метил]морфолина (0.656 г) и перемешивают в течение 1 ч. После завершения реакции смесь разбавляют дихлорметаном (100 мл) и промывают водой (50 мл), сушат над сульфатом натрия и упаривают. Сырой продукт очищают с помощью флэш-хроматографии на силикагеле (дихлорметан/метанол, градиент 1-10%) с получением указанного в заголовке соединения.
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: С28H34BrN3O4
[М+Н]+ рассчитано: 556.1813
[М+Н]+ найдено: 556.1790
ИК ν: С-Н: 2930 см-1; >С=O: 1697, 1635 см-1; С-О-С: 1113 см-1
Стадия В: трет-Бутил 5-[4-[(4-бензилоксифенил)-метилкарбамоил]-1,5-диметилпиррол-2-ил]-6-[(3S)-3-(морфолинометил)-3,4-дигидро-1Н-изохинолин-2-карбонил]изоиндолин-2-карбоксилат
Продукт из Стадии A (284 мг, 0.51 ммоль) и N-(4-бензилоксифенил)-N,1,2-триметилпиррол-3-карбоксамид (205 мг, 0.61 ммоль) из Стадии C Синтеза 4b растворяют в диметилацетамиде (5 мл), затем через раствор в течение 5 мин барботируют азот. К смеси добавляют ацетат калия (0.11 г, 1.12 ммоль) и дихлорид бис(трифенилфосфин)палладия(II) (20 мг), затем ее нагревают до 140°C, и затем, после 20 мин перемешивания, добавляют воду (20 мкл). Перемешивание при 140°C в атмосфере азота продолжают в течение дополнительных 16 часов. Реакционной смеси дают охладиться до комнатной температуры и затем упаривают. Остаток распределяют между дихлорметаном (50 мл) и водой (10 мл). Органическую фазу промывают водой (10 мл), сушат над Na2SO4 и упаривают. Сырой продукт очищают с помощью флэш-хроматографии на силикагеле (дихлорметан/метанол, градиент 1-10%) с получением указанного в заголовке соединения.
Стадия С: Гидрохлорид N-(4-бензилоксифенил)-N,1,2-триметил-5-[6-[(3S)-3-(морфолинометил)-3,4-дигидро-1Н-изохинолин-2-карбонил]изоиндолин-5-ил]пиррол-3-карбоксамида
Продукт из Стадии B (140 мг) перемешивают в 4 М растворе HCl в диоксане (15 мл) в течение 30 мин при комнатной температуре. После завершения реакции все растворители удаляют с получением 170 мг указанного в заголовке продукта.
Синтез 7bb: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-1H-пиррол-3-карбоксамид
Стадия А: трет-Бутил 5-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксилат
Смесь N-[4-(бензилокси)фенил]-N,1,2-триметил-1H-пиррол-3-карбоксамида из Стадии С Синтеза 4b (150 мг, 0.45 ммоль), бромида из Синтеза 1f (317 мг, 0.67 ммоль) и ацетата калия (88 мг, 0.9 ммоль) в диметилацетамиде (2 мл) дегазируют путем барботирования газообразного азота в течение 20 мин. Добавляют дихлорид бис(трифенилфосфин)палладия (31.5 мг, 0.04 ммоль), и реакционную смесь нагревают при 144°C. В течение следующих 8 часов добавляют 2 дополнительные порции дихлорида бис(трифенилфосфин)палладия по 0.1 экв. Затем реакционную смесь оставляют перемешиваться в течение прибл. 16 ч. Реакционной смеси дают охладиться до температуры окружающей среды, и концентрируют в вакууме. Остаток распределяют между этилацетатом и водой, разделяют, и органическую фазу промывают водой, сушат (сульфат магния), и концентрируют в вакууме. Сырое вещество очищают с помощью колоночной флэш-хроматографии (24 г силикагель, градиент изогексан-этилацетат) с получением целевого продукта.
ЖХ/МС (C45H48N4O5) 725 [М+Н]+; RT 1.57 (Метод В)
Стадия B: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил}-1Н-пиррол-3-карбоксамид
К раствору продукта из Стадии A (260 мг, 0.36 ммоль) в дихлорметане (5 мл) добавляют трифторуксусную кислоту (1 мл) и смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Смесь распределяют между водой и дихлорметаном, и подщелачивают 1 М водным гидроксидом натрия. Органическую фазу сушат (сульфат магния), упаривают, и очищают на CombiFlash (12 г, силикагель, дихлорметан - 5% метанол/дихлорметан) с получением продукта в виде стеклообразного твердого вещества.
ЖХ/МС (C40H40N4O3) 625 [М+Н]+; RT 1.20 (Метод В)
Синтез 7fa: Гидрохлорид N-(4-бензилоксифенил)-N-метил-3-[6-[(3S)-3-(морфолинометил)-3,4-дигидро-1H-изохинолин-2-карбонил]изоиндолин-5-ил]индолизин-1-карбоксамида
Стадия A: N-(4-Бензилоксифенил)-N-метилиндолизин-1-карбоксамид
Индолизин-1-карбоновую кислоту (0.4 г, 5.6 ммоль) растворяют в смеси дихлорметан/ТГФ (40/40 мл), затем добавляют 1-хлор-N,N,2-триметил-1-пропениламин (0.8 мл) и смесь перемешивают при комнатной температуре в течение 10 минут. После завершения образования ацилхлорида смесь упаривают и повторно растворяют в сухом дихлорметане (50 мл). Добавляют гидрохлорид 4-бензилокси-N-метиланилина (1.67 г, 6.7 ммоль) и триэтиламин (2.34 мл, 16.75 ммоль) и реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Раствор промывают насыщенным водным раствором NaHCO3 и солевым раствором, затем сушат над Na2SO4 и упаривают. Сырой продукт очищают с помощью флэш-хроматографии на силикагеле (дихлорметан/метанол, градиент 1-10%) с получением целевого вещества.
Стадия В: трет-Бутил 5-[1-[(4-бензилоксифенил)-метил-карбамоил]индолизин-3-ил]-6-[(3S)-3-(морфолинометил)-3,4-дигидро-1Н-изохинолин-2-карбонил]изоиндолин-2-карбоксилат
Соединение Синтеза 1е (278 мг, 0.5 ммоль) и продукт из Стадии A (240 мг, 0.70 ммоль) растворяют в диметилацетамиде (5 мл), затем через раствор в течение 5 мин барботируют азот. К смеси добавляют ацетат калия (0.11 г, 1.12 ммоль) и дихлорид бис(трифенилфосфин)палладия(II) (20 мг), смесь нагревают до 110°C и затем, после перемешивания в течение 20 мин, добавляют воду (20 мкл). Перемешивание при 110°C в атмосфере азота продолжают в течение дополнительных 5 часов. Реакционной смеси дают охладиться до температуры окружающей среды и затем упаривают. Остаток растворяют в ТГФ, фильтруют через набивку целита и после удаления растворителя путем упаривания сырой продукт очищают с помощью препаративной ЖХВР (H2O-ТФУ/ацетонитрил; градиентное элюирование). pH соответствующих объединенных фракций доводят до 10 с помощью Na2CO3, и затем ацетонитрил удаляют при пониженном давлении. Осажденное твердое вещество отфильтровывают, затем сушат с получением указанного в заголовке соединения.
Стадия С: Гидрохлорид N-(4-Бензилоксифенил)-N-метил-3-[6-[(3S)-3-(морфолинометил)-3,4-дигидро-1Н-изохинолин-2-карбонил]изоиндолин-5-ил]индолизин-1-карбоксамида
Продукт из Стадии B (167 мг) перемешивают в 4 М растворе HCl в диоксане (15 мл) в течение 30 мин при комнатной температуре. После завершения реакции все растворители удаляют с получением целевого продукта.
Синтез 7fb: Гидрохлорид N-(4-бензилоксифенил)-N-метил-3-[6-[(3R)-3-метил-3,4-дигидро-1H-изохинолин-2-карбонил]изоиндолин-5-ил]индолизин-1-карбоксамида
Стадия А: трет-Бутил 5-[1-[(4-бензилоксифенил)-метил-карбамоил]индолизин-3-ил]-6-[(3R)-3-метил-3,4-дигидро-1Н-изохинолин-2-карбонил/изоиндолин-2-карбоксилат
Методика соответствует методике Стадии B Синтеза 7fa с заменой трет-бутил 5-бром-6-[(3S)-3-(морфолинометил)-3,4-дигидро-1H-изохинолин-2-карбонил]изоиндолин-2-карбоксилата на соединение Синтеза If. Продукт очищают с помощью препаративной ЖХВР (H2O-ТФУ/ацетонитрил; градиентное элюирование).
Стадия В: Гидрохлорид N-(4-бензилоксифенил)-N-метил-3-[6-[(3R)-3-метил-3,4-дигидро-1Н-изохинолин-2-карбонил]изоиндолин-5-ил]индолизин-1-карбоксамида
Методика соответствует методике Стадии С Синтеза 7fa с заменой трет-бутил 5-[1-[(4-бензилоксифенил)-метилкарбамоил]индолизин-3-ил]-6-[(3R)-3-(морфолинометил)-3,4-дигидро-1H-изохинолин-2-карбонил]изоиндолин-2-карбоксилата на продукт из Стадии A.
Следующие примеры получают с использованием соединений соответствующих Синтезов, описанных выше. В случае, если конкретная методика не раскрыта подробно, соответствующий Пример можно получить путем повторения методики, описанной для Примеров - аналогов (т.е. примеров, структура которых близка), подробно раскрытых в другом месте в описании, выбирая соответствующие исходные вещества и используя базовые знания специалиста в данной области техники.
Пример 1: трет-Бутил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике, описанной на Стадии A Синтеза 6е.
ЖХ/МС (C45H53N5O6) 760 [М+Н]+; RT 1.25 (Метод В)
Пример 2: Дигидрохлорид N-(4-гидроксифенил)-N-метил-3-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Методика соответствует методике, описанной на Стадии B Синтеза 6е.
ЖХ/МС (C40H45N5O4) 660 [М+Н]+; RT 0.89 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C40H45N5O4
[М+Н]+ рассчитано: 660.3544
[М+Н]+ найдено: 660.3522
Пример 3: 3-[2-(Бензолсульфонил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия А: 4-{N-метил 3-[2-(бензолсульфонил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-5,6,7,8-тетрагидроиндолизин-1-амидо}фенилбензолсульфонат
К раствору продукта из Синтеза 6е (35 мг, 0.05 ммоль) в дихлорметане (1 мл) добавляют триэтиламин (52 мкл, 0.375 ммоль) и смесь охлаждают до 0°C. По каплям добавляют бензолсульфонилхлорид (17 мкл, 0.13 ммоль), и получаемую смесь перемешивают при 0°C в течение 1 ч. Реакционную смесь разбавляют дихлорметаном, промывают 1 М водным раствором гидроксида натрия и, далее, солевым раствором и сушат над сульфатом магния. Растворитель удаляют в вакууме, и сырой продукт очищают на CombiFlash (4 г, силикагель; дихлорметан - 5% МеОН/дихлорметан).
ЖХ/МС (C52H53N5O8S2) 798 [M-C6H5SO2]-; RT 1.41 (Метод В) Стадия B: 3-[2-(Бензолсульфонил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Продукт из Стадии A растворяют в метаноле (2 мл), добавляют гидроксид калия (10 экв.), и получаемой смеси дают перемешиваться при температуре окружающей среды в течение 7 ч. Концентрирование в вакууме и очистка на CombiFlash (4 г, силикагель; дихлорметан - 5% метанол/дихлорметан) дают целевой продукт в виде твердого вещества.
ЖХ/МС (C46H49N5O6S) 800 [М+Н]+; RT 1.21 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O6S
[М+Н]+ рассчитано: 800.3476
[М+Н]+ найдено: 800.3485
Пример 4: N-(4-Гидроксифенил)-N-метил-3-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-фенилметансульфонил-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 3 с заменой бензолсульфонилхлорида на Стадии A на фенилметансульфонилхлорид.
ЖХ/МС (C47H51N5O6S) 814 [М+Н]+; RT 1.23 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H51N5O6S
[М+Н]+ рассчитано: 814.3633
[М+Н]+ найдено: 814.3602
Пример 5: N-(4-Гидроксифенил)-N-метил-3-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(нафталин-2-сульфонил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 3 с заменой бензолсульфонилхлорида на Стадии A на нафталин-2-сульфонилхлорид.
ЖХ/МС (C50H51N5O6S) 850 [М+Н]+; RT 1.31 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C50H51N5O6S
[М+Н]+ рассчитано: 850.3633
[М+Н]+ найдено: 850.3624
Пример 6: трет-Бутил 5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Раствор продукта из Стадии A Синтеза 7аа (16 мг, 0.02 ммоль) в этаноле (10 мл) добавляют к 10% Pd/C (каталитическое количество) и смесь встряхивают в атмосфере водорода в течение прибл. 16 ч. Смесь фильтруют через целит с дальнейшим элюированием метанолом и удалением растворителей при пониженном давлении.
ЖХ/МС (C44H51N5O6) 746 [М+Н]+; RT 1.25 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H51N5O6
[М+Н]+ рассчитано: 746.3912
[М+Н]+ найдено: 746.3909
Пример 7: N-(4-Гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид; дигидрохлорид
Пример 6 (45 мг, 0.05 ммоль) растворяют в минимальном количестве метанола и к раствору добавляют 4 М раствор HCl в 1,4-диоксане (1 мл), и смеси дают перемешиваться при температуре окружающей среды в течение прибл. 1 ч. Затем реакционную смесь разбавляют сухим диэтиловым эфиром (прибл. 5 мл) и осадок собирают путем фильтрования и промывают минимальным количеством холодного диэтилового эфира с получением продукта.
ЖХ/МС (C39H43N5O4) 646 [М+Н]+; RT 0.89 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C39H43N5O4
[М+Н]+ рассчитано: 646.3388
[М+Н]+ найдено: 646.3385
Пример 8: N-(4-Гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид; гидрохлорид
Стадия А: N-(4-Гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта, полученного из Синтеза 7аа (50 мг, 0.07 ммоль) в дихлорметане (2 мл) добавляют N,N-диизопропилэтиламин (0.1 ммоль) и смесь охлаждают до 0°C. К получаемому раствору по каплям добавляют 2-фенилацетилхлорид (0.102 ммоль) и через 5 минут реакционную смесь разбавляют дихлорметаном и промывают последовательно 1 М водным гидроксидом натрия и солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме, адсорбируют на изолют, и очищают с помощью хроматографии (CombiFlash Rf, 40 г RediSep™ силикагелевый картридж) при элюировании в градиенте изогексан - 25% этилацетат. Остаток затем растворяют в этаноле (5 мл) и к раствору добавляют 10% Pd/C (каталитическое количество) и смесь перемешивают в атмосфере водорода в течение прибл. 16 ч. Смесь фильтруют через целит с дальнейшим элюированием метанолом, и растворитель удаляют при пониженном давлении. Остаток адсорбируют на изолют и очищают с помощью хроматографии (CombiFlash Rf, 4 г RediSep™ силикагелевый картридж) при элюировании в градиенте дихлорметан - 5% метанол в дихлорметане с получением целевого продукта.
ЖХ/МС (C47H49N5O5) 764 [М+Н]+; RT 1.18 (Метод В)
Стадия B: N-(4-Гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид; гидрохлорид
Продукт из Стадии A растворяют в изопропиловом спирте (0.5 мл) и добавляют эфирный раствор HCl (1 М; 0.13 мл). Смесь перемешивают в течение 30 мин, затем концентрируют в вакууме. Растирание остатка с эфиром дает целевой продукт в виде твердого вещества.
ЖХ/МС (C47H49N5O5) 764 [М+Н]+; RT 1.16 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H49N5O5
[М+Н]+ рассчитано: 764.3806
[М+Н]+ найдено: 764.3807
Пример 9: Гидрохлорид N-(4-гидроксифенил)-N-метил-3-{6-[(3SR)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(3-фенилпропаноил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Методика соответствует методике Примера 8 с заменой 2-фенилацетилхлорида на Стадии A на 3-фенилпропаноилхлорид.
ЖХ/МС (C48H51N5O5) 778 [М+Н]+; RT 1.19
(Метод В) Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H51N5O5
[М+Н]+ рассчитано: 778.3963
[М+Н]+ найдено: 778.3973
Пример 10: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной в Примере 7, с заменой Примера 6 на продукт из Синтеза 7ab.
ЖХ/МС (C35H36N4O3) 561 [М+Н]+; RT 1.04
Пример 11: Гидрохлорид N-(4-гидроксифенил)-N-метил-3-{6-[(3R)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-пропаноил-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Стадия A: N-[4-(Бензилокси)фенил]-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-пропаноил-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору соединения из Синтеза 7аа (50 мг, 0.068 ммоль) в дихлорметане (2 мл) добавляют DIPEA (17 мкл, 0.10 ммоль) и смесь охлаждают до 0°C. По каплям добавляют пропионилхлорид (9 мкл, 0.10 ммоль), и через 30 мин смесь разбавляют дихлорметаном, промывают последовательно 1 М водным NaOH и солевым раствором, сушат над сульфатом магния, и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (4 г, силикагель; дихлорметан - 5% МеОН/дихлорметан) дает продукт в виде стеклообразного твердого вещества.
ЖХ/МС (C49H53N5O5) 792 [М+Н]+; RT 1.30 (Метод В)
Стадия B: N-(4-Гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-пропаноил-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Раствор продукта из Стадии A (18.7 мг, 0.024 ммоль) в этаноле (5 мл) добавляют к 10% Pd/C (каталитическое количество) и смесь встряхивают в атмосфере водорода в течение прибл. 16 ч. Смесь фильтруют через целит с дальнейшим элюированием метанолом, и удалением растворителей при пониженном давлении. Сырой продукт очищают с помощью колоночной флэш-хроматографии (4 г, силикагель; дихлорметан - 5% МеОН/дихлорметан) с получением целевого продукта в виде стеклообразного твердого вещества.
ЖХ/МС (C42H47N5O5) 702 [М+Н]+; RT 1.08 (Метод В)
Стадия C: Гидрохлорид N-(4-гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-пропаноил-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Продукт из Стадии B растворяют в изопропиловом спирте (0.5 мл) и добавляют эфирный раствор HCl (1 М; 0.13 мл). Смесь перемешивают в течение 30 мин, затем концентрируют в вакууме. Растирание остатка с эфиром дает целевой продукт в виде твердого вещества.
ЖХ/МС (C42H47N5O5) 702 [М+Н]+; RT 1.10 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H47N5O5
[М+Н]+ рассчитано: 702.3650
[М+Н]+ найдено: 702.3684
Пример 12: Гидрохлорид 3-{2-бензоил-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Методика соответствует методике Примера 8 с заменой 2-фенилацетилхлорида на Стадии A на бензоилхлорид.
ЖХ/МС (C46H47N5O5) 750 [М+Н]+; RT 1.17 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H47N5O5
[М+Н]+ рассчитано: 750.3650
[М+Н]+ найдено: 750.3648
Пример 13: трет-Бутил 5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Методика соответствует методике, описанной в Примере 6, с заменой продукта, полученного на Стадии A Синтеза 7аа, на продукт, полученный на Стадии A Синтеза 7ab.
ЖХ/МС (C40H44N4O5) 661 [М+Н]+; RT 1.42 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C40H44N4O5
[М+Н]+ рассчитано: 661.3384
[М+Н]+ найдено: 661.3352
Пример 14: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 7ab.
ЖХ/МС (C43H42N4O4) 679 [М+Н]+; RT 1.31 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H42N4O4
[М+Н]+ рассчитано: 679.3279
[М+Н]+ найдено: 679.3298
Пример 15: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(3-фенилпропаноил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 7ab, и с заменой 2-фенилацетилхлорида на Стадии A на 3-фенилпропаноилхлорид.
ЖХ/МС (C44H44N4O4) 693 [М+Н]+; RT 2.57 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H44N4O4
[М+Н]+ рассчитано: 693.3435
[М+Н]+ найдено: 693.3441
Пример 16: Гидрохлорид фенил 5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилата
Методика соответствует методике Примера 8 с заменой 2-фенилацетилхлорида на Стадии A на фенилхлорформиат.
ЖХ/МС (C46H47N5O6) 766 [М+Н]+; RT 1.24 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H47N5O6
[М+Н]+ рассчитано: 766.3599
[М+Н]+ найдено: 766.3602
Пример 17: Гидрохлорид N-трет-бутил-5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксамида
Стадия A: 5-(1-{[4-(Бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-N-трет-бутил-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксамид
К раствору соединения Синтеза 7аа (30 мг, 0.04 ммоль) в дихлорметане (2 мл) добавляют DIPEA (10 мкл, 0.06 ммоль) и смесь охлаждают до 0°C. Добавляют трет-бутил изоцианат (7 мкл, 0.06 ммоль) и реакционную смесь перемешивают в течение 10 мин, затем разбавляют дихлорметаном и промывают последовательно 1 М водным NaOH и солевым раствором. Органическую фазу сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Сырое вещество вносят в дихлорметан, загружают на изолют и очищают на CombiFlash (4 г, силикагель, дихлорметан - 5% метанол/дихлорметан) с получением целевого продукта в виде стеклообразного твердого вещества, которое непосредственно применяют на следующей стадии.
Стадия В: N-трет-Бутил-5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксамид
Продукт из Стадии A (25 мг) растворяют в EtOH и к раствору добавляют 10% Pd/C (каталитическое количество) и смеси дают перемешиваться в атмосфере водорода в течение прибл. 16 ч. Реакционную смесь фильтруют через целит, элюируя метанолом, и концентрируют в вакууме с получением целевого продукта.
ЖХ/МС (C44H52N6O5) 745 [М+Н]+; RT 2.20 (Метод А)
Стадия С: Гидрохлорид N-трет-бутил-5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксамида
К раствору продукта из Стадии B в изопропиловом спирте (0.5 мл) добавляют эфирный раствор HCl (1 М; 0.17 мл, 0.17 ммоль) и смесь перемешивают в течение 30 мин. Растворитель удаляют в вакууме и растирание с эфиром дает целевой продукт в виде твердого вещества.
ЖХ/МС (C44H52N6O5) 745 [М+Н]+; RT 1.10 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H52N6O5
[М+Н]+ рассчитано: 745.4072
[М+Н]+ найдено: 745.4081
Пример 18: Гидрохлорид 3-[2-(этансульфонил)-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Методика соответствует методике Примера 8 с заменой 2-фенилацетилхлорида на Стадии A на этансульфонилхлорид.
ЖХ/МС (C41H47N5O6S) 738 [М+Н]+; RT 1.07 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H47N5O6S
[М+Н]+ рассчитано: 738.3320
[М+Н]+ найдено: 738.3316
Пример 19: Гидрохлорид 3-[2-(бензолсульфонил)-6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Методика соответствует методике Примера 8 с заменой 2-фенилацетилхлорида на Стадии A на бензолсульфонилхлорид.
ЖХ/МС (C45H47N5O6S) 786 [М+Н]+; RT 1.16 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H47N5O6S
[М+Н]+ рассчитано: 786.3320
[М+Н]+ найдено: 786.3339
Пример 20: 3-{2-Циклопропанкарбонил-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A и Стадии B Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 7ab, и с заменой 2-фенилацетилхлорида на Стадии A на циклопропанкарбонилхлорид.
ЖХ/МС (C39H40N4O4) 629.7 [М+Н]+; RT 2.41 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C39H40N4O4
[М+Н]+ рассчитано: 629.3122
[М+Н]+ найдено: 629.3129
Пример 21: Гидрохлорид N-(4-гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилэтансульфонил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Методика соответствует методике Примера 8 с заменой 2-фенилацетилхлорида на Стадии A на 2-фенилэтан-1-сульфонилхлорид.
ЖХ/МС (C47H51N5O6S) 814 [М+Н]+; RT 1.21 (Метод В)
Пример 22: Гидрохлорид N-(4-гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(пиридин-3-сульфонил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Методика соответствует методике Примера 8 с заменой 2-фенилацетилхлорида на Стадии A на пиридин-3-сульфонилхлорид.
ЖХ/МС (C44H46N6O6S) 787 [М+Н]+; RT 1.09 (Метод В)
Масс-спектроскопия высокого разрешения (EST+):
Эмпирическая формула: C44H46N6O6S
[М+Н]+ рассчитано: 787.3272
[М+Н]+ найдено: 787.3243
Пример 23: 3-[2-(2-Бензилпропаноил)-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия А: N-[4-(бензилокси)фенил]-3-[2-(2-бензилпропаноил)-6-[(311)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил]-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта из Синтеза 7ab (52 мг, 0.07 ммоль) в тетрагидрофуране (3 мл) добавляют. N,N-диизопропилэтиламин (37 мкл, 0.21 ммоль) и HBTU (27 мг, 0.07 ммоль) и, далее, 2-метил-3-фенилпропановую кислоту (17 мг, 0.10 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч, затем распределяют между этилацетатом и водой, сушат над сульфатом магния, и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (силикагель; градиент изогексан - этилацетат) дает целевой продукт.
ЖХ/МС (C52H52N4O4) 797 [М+Н]+; RT 2.91 (Метод А)
Стадия B: 3-[2-(2-Бензилпропаноил)-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Продукт из Стадии A растворяют в этаноле (10 мл) и к раствору добавляют 10% Pd/C (каталитическое количество) и смеси дают перемешиваться в атмосфере водорода в течение прибл. 16 ч. Реакционную смесь фильтруют через целит, элюируя метанолом и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (силикагель; градиент изогексан - этилацетат) дает целевой продукт.
ЖХ/МС (C45H46N4O4) 707 [М+Н]+; RT 2.64 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H46N4O4
[М+Н]+ рассчитано: 707.3592
[М+Н]+ найдено: 707.3600
Пример 24: 3-(2-{2-[(4-Хлорфенил)метил]пропаноил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил)-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта из Примера 10 (20 мг, 0.03 ммоль) в дихлорметане (3 мл) добавляют TEA (13 мкл, 0.09 ммоль), HATU (12 мг, 0.03 ммоль) и 3-(4-хлорфенил)-2-метилпропановую кислоту (6 мг, 0.03 ммоль), и смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь разбавляют дихлорметаном и промывают водой, сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Сырое вещество очищают с помощью колоночной хроматографии в градиенте дихлорметан - 10% метанол/дихлорметан.
ЖХ/МС (C45H45N4O4Cl) 741 [М+Н]+; RT 2.71 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H45N4O4Cl
[М+Н]+ рассчитано: 741.3202
[М+Н]+ найдено: 741.3246
Пример 25: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[(4-метилфенил)метил]пропаноил}-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной в Примере 23, с заменой 2-метил-3-фенилпропановой кислоты на Стадии A на 2-метил-3-(4-метилфенил)пропановую кислоту.
ЖХ/МС (C46H48N4O4) 721 [М+Н]+; RT 2.70 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H48N4O4
[М+Н]+ рассчитано: 721.3748
[М+Н]+ найдено: 721.3740
Пример 26: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[4-(трифторметокси)фенил]ацетил}-2,3-Дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной в Примере 23, с заменой 2-метил-3-фенилпропановой кислоты на Стадии A на 2-[4-(трифторметокси)фенил]уксусную кислоту.
ЖХ/МС (C44H41N4O5F3) 763 [М+Н]+; RT 2.70 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H41N4O5F3
[М+Н]+ рассчитано: 763.3102
[М+Н]+ найдено: 763.3102
Пример 27: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид; соль с трифторуксусной кислотой
Стадия A: трет-Бутил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Продукт из Синтеза 6ab (95 мг, 0.12 ммоль) растворяют в этаноле (5 мл) и к раствору добавляют 10% Pd/C (каталитическое количество) и смеси дают перемешиваться в атмосфере водорода в течение прибл. 6 ч. Реакционную смесь фильтруют через целит, элюируя метанолом, и концентрируют в вакууме с получением целевого продукта.
ЖХ/МС (C41H46N4O5) 675 [М+Н]+; RT 1.43 (Метод В)
Стадия B: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид; соль с трифторуксусной кислотой
Продукт из Стадии A растворяют в дихлорметане (2 мл) и добавляют трифторуксусную кислоту (0.1 мл). После перемешивания в течение прибл. 16 ч при температуре окружающей среды реакционную смесь концентрируют в вакууме и подвергают азеотропной перегонке с толуолом (×3) с получением целевого продукта в виде соли с трифторуксусной кислотой.
ЖХ/МС (C36H38N4O3) 575 [М+Н]+; RT 1.00 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C36H38N4O3
[М+Н]+ рассчитано: 575.3017
[М+Н]+ найдено: 575.2998
Пример 28: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(пиридин-2-илметил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии B Примера 29 с заменой соединения из Стадии A на Пример 10, и с заменой циклогексилацетальдегида на пиридин-2-карбальдегид.
ЖХ/МС (C41H41N5O3) 652 [М+Н]+; RT 1.06 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H41N5O3
[М+Н]+ рассчитано: 652.3282
[М+Н]+ найдено: 652.3269
Пример 29: 3-[2-(2-Циклогексилэтил)-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия A: N-[4-(Бензилокси)фенил]-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору соединения Стадии A Синтеза 7ab (150 мг, 0.20 ммоль) в дихлорметане (5 мл) добавляют трифторуксусную кислоту (0.5 мл) и реакционную смесь перемешивают в течение прибл. 16 ч. Смесь разбавляют дихлорметаном, промывают 1 н. водным гидроксидом натрия, сушат (сульфат магния) и упаривают при пониженном давлении. Очистка на CombiFlash (4 г, силикагель, дихлорметан - 10% метанол/дихлорметан) дает целевой продукт в виде смолы.
ЖХ/МС (C42H42N4O3) 651 [М+Н]+; RT 1.2 (Метод В)
Стадия В: N-[4-(Бензилокси)фенил]-3-[2-(2-циклогексилэтил)-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил]-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К перемешиваемому раствору продукта из Стадии A (57.5 мг, 0.088 ммоль) в ТГФ (2 мл) добавляют циклогексилацетальдегид (13.4 мг, 0.11 ммоль) и, далее, триацетоксиборогидрид натрия (22.5 мг, 0.106 ммоль) и реакционную смесь перемешивают в течение прибл. 16 ч. Смесь концентрируют при пониженном давлении, и очищают на CombiFlash (4 г, силикагель, дихлорметана - смесь 3% метанол/дихлорметан) с получением целевого продукта в виде смолы.
ЖХ/МС (C50H56N4O3) 761 [М+Н]+; RT 1.37 (Метод В)
Стадия C: 3-[2-(2-Циклогексилэтил)-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта из Стадии B (13 мг, 0.019 ммоль) в дихлорметане (2 мл), охлажденному до 0°C, добавляют трихлорид бора (2 М раствор в дихлорметане; 0.1 мл, 0.2 ммоль). Через 5 ч реакцию гасят путем добавления метанола, и концентрируют в вакууме. Очистка с помощью препаративной ЖХВР дает целевой продукт.
ЖХ/МС (С43Н50N4O3) 671 [М+Н]+; RT 1.16 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: С43Н50N4O3
[М+Н]+ рассчитано: 671.3956
[М+Н]+ найдено: 671.3955
Пример 30: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(3-фенилпропил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии B Примера 29 с заменой соединения из Стадии A на Пример 10, и с заменой циклогексилацетальдегида на 3-фенилпропаналь.
ЖХ/МС (C44H46N4O3) 679 [М+Н]+; RT 1.16 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H46N4O3
[М+Н]+ рассчитано: 679.3643
[М+Н]+ найдено: 679.3612
Пример 31: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[2-(пиразин-2-ил)-1,3-тиазол-4-ил]ацетил}-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия A: N-[4-(бензилокси)фенил]-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[2-(пиразин-2-ил)-1,3-тиазол-4-ил]ацетил}-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта из Синтеза 7ab (50 мг, 0.07 ммоль) в дихлорметане (3 мл) добавляют триэтиламин (29.2 мкл, 0.21 ммоль) и HATU (27 мг, 0.07 ммоль) и, далее, 2-[2-(пиразин-2-ил)-1,3-тиазол-4-ил]уксусную кислоту (14.46 мг, 0.07 ммоль), и смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь разбавляют дихлорметаном и промывают водой. Органическую фазу сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (силикагель; градиент дихлорметан - 5% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C51H47N7O4S) 854 [М+Н]+; RT 2.77 (Метод А)
Стадия B: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[2-(пиразин-2-ил)-1,3-тиазол-4-ил]ацетил}-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Раствор продукта из Стадии A (1 экв., 46 мг) в дихлорметане (5 мл) охлаждают до 0°C и к раствору добавляют трихлорид бора (1 M в дихлорметане, 100 мкл). Реакционной смеси дают нагреться до температуры окружающей среды в течение прибл. 16 ч, и затем гасят метанолом и распределяют между дихлорметаном и водой. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (силикагель; градиент дихлорметан - 10% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C44H41N7O4S) 764 [М+Н]+; RT 2.44 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H41N7O4S
[М+Н]+ рассчитано: 764.3014
[М+Н]+ найдено: 764.2994
Пример 32: 3-[2-(3-Циклогексилпропаноил)-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия A: N-[4-(Бензилокси)фенил]-3-[2-(3-циклогексилпропаноил)-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил]-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору соединения из Синтеза 7ab (52 мг, 0.066 ммоль) в ТГФ (3 мл) добавляют DIPEA (37 мкл, 0.21 ммоль) и HBTU (27 мг, 0.07 ммоль) и, далее, 3-циклогексилпропионовую кислоту (18 мкл, 0.10 ммоль) и смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч.
Реакционную смесь распределяют между водой и этилацетатом, разделяют, и органическую фазу сушат (сульфат магния) и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии на силикагеле с элюированием градиентом изогексан - этилацетат дает продукт в виде смолы.
ЖХ/МС (C51H56N4O4) 789 [М+Н]+; RT 3.00 (Метод А)
Стадия B: 3-[2-(3-Циклогексилпропаноил)-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Раствор продукта из Стадии A (50 мг, 0.06 ммоль) в этаноле (10 мл) добавляют к Pd/C (каталитическое количество), и смесь встряхивают в атмосфере водорода в течение прибл. 16 ч. Смесь фильтруют через целит, элюируя метанолом, и затем концентрируют в вакууме. Сырое вещество очищают с помощью колоночной флэш-хроматографии на силикагеле, элюируя градиентом дихлорметан - 5% метанол/дихлорметан с получением продукта в виде твердого вещества.
ЖХ/МС (C44H50N4O4) 699 [М+Н]+; RT 2.76 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H50N4O4
[М+Н]+ рассчитано: 699.3905
[М+Н]+ найдено: 699.3926
Пример 33: 3-{2-Бензил-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии B Примера 29, с заменой соединения из Стадии A на соединение из Примера 10, и с заменой циклогексилацетальдегида на бензальдегид.
ЖХ/МС (C42H42N4O3) 651 [М+Н]+; RT 1.11 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H42N4O3
[М+Н]+ рассчитано: 651.3330
[М+Н]+ найдено: 651.3300
Пример 34: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-пропаноил-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6ab, и с заменой 2-фенилацетилхлорида на Стадии A на пропаноилхлорид.
ЖХ/МС (C39H42N4O4) 631 [М+Н]+; RT 1.24 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C39H42N4O4
[М+Н]+ рассчитано: 631.3279
[М+Н]+ найдено: 631.3252
Пример 35: 3-{2-Бензоил-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6ab, и с заменой 2-фенилацетилхлорида на Стадии A на бензоилхлорид.
ЖХ/МС (C43H42N4O4) 679 [М+Н]+; RT 1.31 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H42N4O4
[М+Н]+ рассчитано: 679.3279
[М+Н]+ найдено: 679.3331
Пример 36: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6ab.
ЖХ/МС (C44H44N4O4) 693 [М+Н]+; RT 1.32 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H44N4O4
[М+Н]+ рассчитано: 693.3435
[М+Н]+ найдено: 693.3447
Пример 37: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(3-фенилпропаноил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6ab, и с заменой 2-фенилацетилхлорида на Стадии A на 3-фенилпропаноилхлорид.
ЖХ/МС (C45H46N4O4) 707 [М+Н]+; RT 1.36 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H46N4O4
[М+Н]+ рассчитано: 707.3592
[М+Н]+ найдено: 707.3557
Пример 38: N-(4-Гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-фенилметансульфонил-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой 2-фенилацетилхлорида на Стадии A на фенилметансульфонилхлорид.
ЖХ/МС (C46H49N5O6S) 800 [М+Н]+; RT 1.15 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O6S
[М+Н]+ рассчитано: 800.3476
[М+Н]+ найдено: 800.3487
Пример 39: 3-[2-(Бензолсульфонил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на продукт из Синтеза 6ab, и с заменой 2-фенилацетилхлорида на Стадии A на бензолсульфонилхлорид.
ЖХ/МС (C42H42N4O5S) 715 [М+Н]+; RT 1.37 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H42N4O5S
[М+Н]+ рассчитано: 715.2949
[М+Н]+ найдено: 715.2937
Пример 40: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-фенилметансульфонил-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на продукт из Синтеза 6ab, и с заменой 2-фенилацетилхлорида на Стадии A на фенилметансульфонилхлорид.
ЖХ/МС (C43H44N4O5S) 729 [М+Н]+; RT 1.37 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H44N4O5S
[М+Н]+ рассчитано: 729.3105
[М+Н]+ найдено: 729.3135
Пример 41: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(нафталин-2-сульфонил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на продукт из Синтеза 6ab, и с заменой 2-фенилацетилхлорида на Стадии A на нафталин-2-сульфонилхлорид.
ЖХ/МС (C46H44N4O5S) 765 [М+Н]+; RT 1.44 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H44N4O5S
[М+Н]+ рассчитано: 765.3105
[М+Н]+ найдено: 765.3140
Пример 42: N-(4-Гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(пиридин-3-ил)ацетил]-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия А: N-[4-(бензилокси)фенил]-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(пиридин-3-ил)ацетил]-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта из Синтеза 7аа (40 мг, 0.05 ммоль) в ДМФА (2 мл) добавляют триэтиламин (28 мкл, 0.2 ммоль) и HBTU (19 мг, 0.05 ммоль) и, далее, гидрохлорид 2-(пиридин-3-ил)уксусной кислоты (9.4 мг, 0.05 ммоль), и смесь перемешивают при температуре окружающей среды в течение 1 ч. Реакционную смесь концентрируют в вакууме и непосредственно используют на следующей стадии.
ЖХ/МС (C53H54N6O5) нет ионизации; RT 1.20 (Метод В)
Стадия B: N-(4-Гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(пиридин-3-ил)ацетил]-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Продукт из Стадии A (25 мг, 0.03 ммоль) растворяют в дихлорметане (2 мл) и раствор охлаждают до 0°C. К раствору добавляют трихлорид бора (1 М; 0.15 мл, 0.15 ммоль) и смесь перемешивают при температуре окружающей среды в течение 2 ч. Реакционную смесь выливают на смесь лед/вода и экстрагируют дихлорметаном. Органический экстракт промывают солевым раствором, сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (4 г, силикагель; дихлорметан - 5% метанол/дихлорметан) дает целевой продукт.
ЖХ/МС (C46H48N6O5) 765 [М+Н]+; RT 0.95 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H48N6O5
[М+2Н]2+ рассчитано: 383.1916
[М+2Н]2+ найдено: 383.1952
Пример 43: трет-Бутил 5-{1-[(4-гидроксифенил)(фенил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Методика соответствует методике, описанной на Стадиях A и В Примера 44.
ЖХ/МС (C45H46N4O5) 723 [М+Н]+; RT 1.47 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H46N4O5
[М+Н]+ рассчитано: 723.3541
[М+Н]+ найдено: 723.3546
Пример 44: N-(4-Гидроксифенил)-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-фенил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия А: трет-Бутил 5-(1-{[4-(бензилокси)фенил](фенил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксилат
Смесь ТГФ (20 мл) и воды (8 мл) дегазируют путем многократного выполнения циклов вакуумирование/продувка азотом и барботирования азота через смесь. 4 мл этой смеси добавляют с помощью шприца к смеси сложного эфира бороновой кислоты из Синтеза 4f (117 мг, 0.28 ммоль), бромида из Синтеза 1f (169 мг, 0.36 ммоль) и карбоната цезия (182 мг, 0.56 ммоль). Азот барботируют через смесь в течение еще 3-х минут. Добавляют бис(ди-трет-бутил(4-диметиламинофенил)фосфин)дихлорпалладий(II) (10 мг, 5 мол.%) и реакционную смесь сразу же нагревают при 95°C при микроволновом облучении в течение 30 минут.
Реакционную смесь разбавляют этилацетатом (30 мл) и промывают последовательно водой (2×30 мл) и насыщенным NaCl (водн.) (1×50 мл), сушат над сульфатом магния, фильтруют и упаривают. Сырое вещество очищают с помощью флэш-хроматографии (Combiflash, 12 г, силикагель, элюируя градиентом 0-100% этилацетата в гексане) с получением продукта в виде масла.
ЖХ/МС (C52H52N4O5) 813 [М+Н]+; RT 1.66 (Метод В)
Стадия В: трет-Бутил 5-{1-[(4-гидроксифенил)(фенил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксилат
Раствор продукта из Стадии A (94 мг, 0.12 ммоль) в этаноле (5 мл) гидрируют над катализатором 10% Pd/C в атмосфере водорода в течение прибл. 16 ч. Смесь фильтруют через целит, элюируя этанолом, и концентрируют в вакууме. Очистка с помощью флэш-хроматографии на силикагеле (CombiFlash Rf, 4 г SiO2, силикагелевая колонка) с элюированием 0-100% этилацетата в гексане дает продукт в виде твердого вещества.
ЖХ/МС (C45H46N4O5) 723 [М+Н]+; RT 1.47 (Метод В)
Стадия C: N-(4-Гидроксифенил)-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил}-N-фенил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта из Стадии B (40 мг, 0.055 ммоль) в безводном дихлорметане (4 мл) в атмосфере азота добавляют трифторуксусную кислоту (180 мкл, 2.33 ммоль) и реакционную смесь перемешивают в течение прибл. 16 ч. Смесь разбавляют дихлорметаном (25 мл) и промывают последовательно 1 М NaOH (водн.) раствором (20 мл) и насыщенным раствором NaCl (водн.) (20 мл). Органическую фазу сушат над сульфатом натрия, фильтруют и упаривают. Сырое вещество очищают с помощью флэш-хроматографии на силикагеле (CombiFlash Rf, 4 г, колонка SilaSep), элюируя 0-15% метанола в дихлорметане с получением стеклообразного твердого вещества. Растиранием с диэтиловым эфиром и упаривание дает целевой продукт в виде твердого вещества.
ЖХ/МС (C40H38N4O3) 623 [М+Н]+; RT 1.08 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C40H38N4O3
[М+Н]+ рассчитано: 623.3017
[М+Н]+ найдено: 623.3028
Пример 45: Фенил 5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Методика соответствует методике Стадии A Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 7ab, и с заменой 2-фенилацетилхлорида на фенилхлорформиат.
ЖХ/МС (C42H40N4O5) 681 [М+Н]+; RT 1.36 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H40N4O5
[М+Н]+ рассчитано: 681.3071
[М+Н]+ найдено: 681.3057
Пример 46: Фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии A Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 6ab, и с заменой 2-фенилацетилхлорида на фенилхлорформиат.
ЖХ/МС (C43H42N4O5) 695 [М+Н]+; RT 1.41 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H42N4O5
[М+Н]+ рассчитано: 695.3228
[М+Н]+ найдено: 695.3193
Пример 47: трет-Бутил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия А: трет-Бутил 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике, описанной на Стадии A Синтеза 6ab.
ЖХ/МС (C48H52N4O5) 765 [М+Н]+; RT 1.62 (Метод В)
Стадия В: трет-Бутил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Раствор продукта из Стадии A (50 мг, 0.07 ммоль) в этаноле (5 мл) добавляют к Pd/C (каталитическое количество), и смесь встряхивают в атмосфере водорода в течение прибл. 16 ч. Смесь фильтруют через целит, элюируя метанолом, и затем концентрируют в вакууме. Сырое вещество очищают с помощью колоночной флэш-хроматографии на силикагеле, элюируя градиентом дихлорметан - 5% метанол/дихлорметан с получением продукта в виде твердого вещества.
ЖХ/МС (C41H46N4O5) 675 [М+Н]+; RT 1.42 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H46N4O5
[М+Н]+ рассчитано: 675.3541
[М+Н]+ найдено: 675.3571
Пример 48: N-трет-Бутил-6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
Методика соответствует методике Стадии A Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 6ab, и с заменой 2-фенилацетилхлорида на 2-изоцианато-2-метилпропан.
ЖХ/МС (C41H47N5O4) 674 [М+Н]+; RT 1.33 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H47N5O4
[М+Н]+ рассчитано: 674.3701
[М+Н]+ найдено: 674.3706
Пример 49: 3-{2-[2-(4-Хлорфенокси)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия A: N-[4-(Бензилокси)фенил]-3-{2-[2-(4-хлорфенокси)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил}-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Стадии A Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 7ab, и с заменой 2-фенилацетилхлорида на 2-(4-хлорфенокси)ацетилхлорид.
ЖХ/МС (C50H47N4O5Cl) 819 [М+Н]+; RT 1.56 (Метод В)
Стадия В: 3-{2-[2-(4-Хлорфенокси)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Стадии B Примера 42 с заменой продукта из Стадии A Примера 42 на продукт из Стадии A Примера 49.
ЖХ/МС (C43H41N4O5Cl) 729 [М+Н]+; RT 1.37 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H41N4O5Cl
[М+Н]+ рассчитано: 729.2838
[М+Н]+ найдено: 729.2809
Пример 50: 3-{2-[2-(3-Хлорфенокси)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 49 с заменой 2-(4-хлорфенокси)ацетилхлорида на Стадии A на 2-(3-хлорфенокси)ацетилхлорид.
ЖХ/МС (C43H41N4O5Cl) 729 [М+Н]+; RT 1.37 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H41N4O5Cl
[М+Н]+ рассчитано: 729.2838
[М+Н]+ найдено: 729.2871
Пример 51: N-(4-Гидроксифенил)-3-{2-[2-(4-метоксифенил)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H44N4O5
[М+Н]+ рассчитано: 709.3392
[М+Н]+ найдено: 709.3382
Пример 52: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-феноксиацетил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 7ab, и с заменой 2-фенилацетилхлорида на Стадии A на 2-феноксиацетилхлорид.
ЖХ/МС (C43H42N4O5) 695 [М+Н]+; RT 1.31 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H42N4O5
[М+Н]+ рассчитано: 695.3228
[М+Н]+ найдено: 695.3252
Пример 53: 3-{2-[2-(4-Цианофенил)ацетил]-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 24 с заменой продукта из Примера 10 на продукт из Примера 27, и с заменой 3-(4-хлорфенил)-2-метилпропановой кислоты на 2-(4-цианофенил)уксусную кислоту.
ЖХ/МС (C45H43N5O4) 718 [М+Н]+; RT 1.29
Пример 54: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(4-метилфенил)ацетил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
ЖХ/МС (C45H46N4O4) 707 [М+Н]+; RT 2.65 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: С45Н46N4O4
[М+Н]+ рассчитано: 707.3592
[М+Н]+ найдено: 707.3556
Пример 55: 5-{1-[(4-Гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-N-метил-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксамид
Стадия А: трет-Бутил 5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксилат
К раствору соединения Стадии A Синтеза 7ab (400 мг, 0.53 ммоль) в этаноле (10 мл) добавляют 10% Pd/C (каталитическое количество), и смесь перемешивают в атмосфере водорода в течение прибл. 16 ч. Смесь фильтруют через целит, концентрируют при пониженном давлении, и очищают с помощью колоночной флэш-хроматографии на силикагеле с получением продукта в виде стеклообразного твердого вещества.
ЖХ/МС (C40H44N4O5) 661 [М+Н]+; RT 1.41 (Метод В)
Стадия B: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид; соль трифторуксусной кислоты
К раствору продукта из Стадии A (300 мг) в дихлорметане (5 мл) добавляют трифторуксусную кислоту (избыток) и смеси дают перемешиваться при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь концентрируют в вакууме и растирают с эфиром с получением продукта в виде твердого вещества.
ЖХ/МС (C35H36N4O3) 561 [М+Н]+; RT 1.01 (Метод В)
Стадия С: 5-{1-[(4-Гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбонилхлорид
К раствору продукта из Стадии B (100 мг, 0.15 ммоль) в дихлорметане (2 мл), охлажденному до 0°C, добавляют DIPEA (61 мкл, 0.37 ммоль) с последующим добавлением порциями трифосгена (44 мг, 0.15 ммоль). Реакционной смеси дают нагреться до температуры окружающей среды и перемешивают в течение 1 ч, затем распределяют между дихлорметаном и 1 М водной HCl. Органическую фазу сушат над сульфатом магния и концентрируют в вакууме с получением продукта в виде смеси трихлорметил 5-{1-[(4-гидpoкcифeнил)(мeтил)кapбaмoил]-5,6,7,8-тeтpaгидpoиндoлизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксилата и 5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбонилхлорида, которую непосредственно используют на следующей стадии без дополнительной очистки.
ЖХ/МС (C37H35Cl3N4O5) 721 [М+Н]+; RT 1.44, (C36H35ClN4O4) 623 [М+Н]+; RT 1.32 (Метод В)
Стадия D: 5-{1-[(4-Гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-N-метил-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксамид
К раствору продукта из Стадии C (50 мг, 0.07 ммоль) в ацетонитриле (2 мл) добавляют метиламин (2 М в ТГФ; 346 мкл, 0.69 ммоль) и DIPEA (61 мкл, 0.31 ммоль) и смесь перемешивают в течение прибл. 16 ч. Растворитель удаляют в вакууме и остаток распределяют между этилацетатом и водой, органическую фазу сушат над сульфатом магния, и растворитель удаляют в вакууме. Остаток растворяют в 1,4-диоксане (2 мл) и по каплям добавляют 1 М водный раствор NaOH (5 мл). Через 1 ч смесь разбавляют водой, подкисляют 1 М водной HCl, и экстрагируют этилацетатом. Органические экстракты сушат над сульфатом магния и концентрируют при пониженном давлении. Очистка на CombiFlash (4 г, силикагель, дихлорметан - 5% МеОН/дихлорметан) дает целевой продукт в виде твердого вещества.
ЖХ/МС (C37H39N5O4) 618 [М+Н]+; RT 2.27 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C37H39N5O4
[М+Н]+ рассчитано: 618.3075
[М+Н]+ найдено: 618.3069
Пример 56: 3-[2-(Этансульфонил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной на Стадии A и Стадии B Примера 8 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6ab, и с заменой 2-фенилацетилхлорида на Стадии A на этансульфонилхлорид.
ЖХ/МС (C38H42N4O5S) 667 [М+Н]+; RT 1.27 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C38H42N4O5S
[М+Н]+ рассчитано: 667.2949
[М+Н]+ найдено: 667.2935
Пример 57: 3-{2-Этил-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
ЖХ/МС (C38H42N4О3) 603 [М+Н]+; RT 1.05 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C38H42N4О3
[М+Н]+ рассчитано: 603.3330
[М+Н]+ найдено: 603.3270
Пример 58: 4-Аминофенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия А: 4-Нитрофенил 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору продукта из Синтеза 7ab (43 мг, 0.07 ммоль) в дихлорметане (5 мл) добавляют 4-нитрофенилхлорформиат (18 мг, 0.09 ммоль) и дают перемешиваться при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь разбавляют дихлорметаном и промывают 1 н. HCl, NaHCO3 и солевым раствором. Органическую фазу сушат над сульфатом магния, фильтруют и концентрируют в вакууме, и непосредственно применяют на следующей стадии, предполагая количественное превращение.
ЖХ/МС (C50H47N5O7) 830 [М+Н]+; RT 1.58 (Метод В)
Стадия В: 4-Аминофенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору соединения Стадии A (54 мг, 0.07 ммоль) в этаноле (10 мл) добавляют 10% Pd/C (каталитическое количество), и смесь перемешивают в атмосфере водорода в течение прибл. 16 ч. Реакционную смесь фильтруют через целит и концентрируют при пониженном давлении.
ЖХ/МС (C43H43N5O5) 708 [М-Н]-; RT 1.26 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H43N5O5
[М+Н]+ рассчитано: 710.3337
[М+Н]+ найдено: 710.3302
Пример 59: 4-Ацетамидофенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
4-Аминофенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат [Пример 58] (23 мг, 0.03 ммоль) растворяют в дихлорметане (5 мл) с последующим добавлением DIPEA (0.17 мл, 1 ммоль) и охлаждением до 0°C. Добавляют ацетилхлорид (3 мкл, 0.04 ммоль) и реакционную смесь перемешивают в течение прибл. 16 ч при температуре окружающей среды. Добавляют аммиак в метаноле (7 н.; 1 мл), и получаемую смесь промывают насыщенным раствором NaHCO3 и солевым раствором, сушат над сульфатом магния, фильтруют и концентрируют. Продукт очищают с помощью FlashChrom (24 г, силикагель, дихлорметан - 5% метанол/дихлорметан).
ЖХ/МС (C45H45N5O6) 752 [М+Н]+; RT 1.25 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H45N5O6
[М+Н]+ рассчитано: 752.3443
[М+Н]+ найдено: 752.3461
Пример 60: 5-{1-[(4-Гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-N-фенил-2,3-дигидро-1H-изоиндол-2-карбоксамид
Методика соответствует методике, описанной на Стадии A и Стадии B Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 7ab, и с заменой 2-фенилацетилхлорида на Стадии A на фенилизоцианат.
ЖХ/МС (C42H41N5O4) 680 [М+Н]+; RT 1.29 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H41N5O4
[М+Н]+ рассчитано: 680.3231
[М+Н]+ найдено: 680.3225
Пример 61: N-Бензил-5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксамид
Методика соответствует методике, описанной на Стадии A и Стадии B Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 7ab, и с заменой 2-фенилацетилхлорида на Стадии A на бензилизоцианат.
ЖХ/МС (C43H43N5O4) 694 [М+Н]+; RT 1.28 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H43N5O4
[М+Н]+ рассчитано: 694.3388
[М+Н]+ найдено: 694.3392
Пример 62: Бензил 5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Раствор продукта, полученного в Примере 10, (53 мг, 0.08 ммоль) в дихлорметане (5 мл) охлаждают до 0°C и к раствору добавляют N,N-диизопропилэтиламин (0.18 ммоль) и бензилхлорформиат (14.7 мг, 0.09 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение 15 мин, затем разбавляют дихлорметаном и последовательно промывают 1 М водным гидроксидом натрия и солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 4 г RediSep™ силикагелевый картридж; градиент дихлорметан - 5% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C43H42N4O5) 695 [М+Н]+; RT 1.40 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H42N4O5
[М+Н]+ рассчитано: 695.3228
[М+Н]+ найдено: 695.3241
Пример 63: Фенил 5-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 7bb, и с заменой 2-фенилацетилхлорида на Стадии A на фенилхлорформиат.
ЖХ/МС (C40H38N4O5) 655 [М+Н]+; RT 1.33 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C40H38N4O5
[М+Н]+ рассчитано: 655.2915
[М+Н]+ найдено: 655.2897
Пример 64: 1H-Пирроло[2,3-b]пиридин-5-илметил 5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Стадия A: 4-Нитрофенил 1Н-пирроло[2,3-b]пиридин-5-илметилкарбонат
К раствору 1H-пирроло[2,3-b]пиридин-5-илметанола (148 мг, 1 ммоль) и N,N-диизопропилэтиламина (261 мкл, 1.5 ммоль) в ДХМ (10 мл) добавляют 4-нитрофенилхлорформиат (202 мг, 1 ммоль) и смесь перемешивают при температуре окружающей среды. После концентрирования в вакууме, очистка с помощью колоночной флэш-хроматографии (силикагель; этилацетат) дает целевое вещество.
ЖХ/МС (C15H11N3O5) 314 [М+Н]+; RT 1.19 (Метод В)
Стадия В: 1Н-Пирроло[2,3-b]пиридин-5-илметил 5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксилат
К раствору продукта из Примера 10 (10 мг, 0.02 ммоль) в тетрагидрофуране (1 мл) добавляют N,N-диизопропилэтиламин (11 мкл, 0.06 ммоль) и, далее, продукт из Стадии A (6 мг, 0.02 ммоль), и смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. По прошествии этого времени добавляют еще N,N-диизопропилэтиламин (11 мкл, 0.06 ммоль) и продукт из Стадии A (6 мг, 0.02 ммоль) для обеспечения полного превращения. Очистка с помощью колоночной флэш-хроматографии (силикагель; градиент изогексан - этилацетат) с последующим упариванием и растиранием с диэтиловым эфиром дает целевой продукт.
ЖХ/МС (C44H42N6O5) 735 [М+Н]+; RT 2.48 (Метод А)
Пример 65: 5-{1-[(4-Гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-N-[4-(4-метилпиперазин-1-ил)фенил]-2,3-дигидро-1H-изоиндол-2-карбоксамид
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 7ab, и с заменой 2-фенилацетилхлорида на Стадии A на 1-(4-изоцианатофенил)-4-метилпиперазин.
ЖХ/МС (C47H51N7O4) 776 [М-Н]-; RT 2.18 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H51N7O4
[М+2Н]2+ рассчитано: 389.7074
[М+2Н]2+ найдено: 389.7107
Пример 66: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(3-фенилпирролидин-1-карбонил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия A: 3-Фенилпирролидин-1-карбонилхлорид
Раствор гидрохлорида 3-фенилпирролидина (50 мг, 0.27 ммоль) и N,N-диизопропилэтиламина (0.14 мл, 0.81 ммоль) в дихлорметане (2 мл) охлаждают до 0°C. К раствору добавляют трифосген (81 мг, 0.27 ммоль) и смесь перемешивают при температуре окружающей среды. Затем реакционную смесь разбавляют водой и продукт экстрагируют в дихлорметан, сушат над сульфатом магния и очищают с помощью колоночной флэш-хроматографии (силикагель; градиент изогексан - 10% этилацетат в изогексане) с получением целевого продукта.
ЖХ/МС (C11H12NOCl) 210 [М+Н]+; RT 2.56 (Метод А)
Стадия B: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(3-фенилпирролидин-1-карбонил)-2,3-дигидро-1Н-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 7ab, и с заменой 2-фенилацетилхлорида на хлорангидрид кислоты, полученный на Стадии A Примера 66.
ЖХ/МС (C46H47N5O4) 734 [М+Н]+; RT 2.68 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H47N5O4
[М+Н]+ рассчитано: 734.3701
[М+Н]+ найдено: 734.3673
Пример 67: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(3-фенилпирролидин-1-карбонил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Стадии A Примера 11 с заменой продукта из Синтеза 7аа на продукт из Примера 27, и с заменой пропионилхлорида на хлорангидрид кислоты, полученный на Стадии A Примера 66.
ЖХ/МС (C47H49N5O4) 748 [М+Н]+; RT 2.71 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H49N5O4
[М+Н]+ рассчитано: 748.3857
[М+Н]+ найдено: 748.3815
Пример 68: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 6bb, и с заменой 2-фенилацетилхлорида на Стадии A на фенилхлорформиат.
ЖХ/МС (C41H40N4O5) 669 [М+Н]+; RT 1.35 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H40N4O5
[М+Н]+ рассчитано: 669.3071
[М+Н]+ найдено: 669.3045
Пример 69: Гидрохлорид фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата
Стадия А: Дигидрохлорид N-[4-(бензилокси)фенил]-N-метил-3-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Продукт из Стадии A Синтеза 6аа (549 мг, 0.65 ммоль) растворяют в метаноле (5 мл), затем добавляют раствор HCl в диоксане (4 М; 10 мл) и смеси дают перемешиваться в течение прибл. 16 ч. Добавляют эфир, в результате чего происходило осаждение твердого вещества, которое собирают путем фильтрования и промывают эфиром с получением целевого продукта.
ЖХ/МС (C47H51N5O4) 750[М+Н]+; RT 1.09 (Метод В)
Стадия В: Фенил 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Продукт из Стадии A (100 мг, 0.12 ммоль) растворяют в дихлорметане (5 мл) и к раствору добавляют DIPEA (174 мкл, 1 ммоль), и раствор охлаждают до 0°C. Добавляют фенилхлорформиат (18 мкл, 0.14 ммоль) и смесь перемешивают в течение 30 минут, и затем разбавляют дихлорметаном, промывают последовательно 1 М NaOH и солевым раствором, и сушат над сульфатом магния. Растворитель удаляют в вакууме, и остаток вносят в дихлорметан и очищают на CombiFlash (12 г, силикагель; дихлорметан - 5% метанол/дихлорметан) с получением продукта в виде твердого вещества.
ЖХ/МС (C54H55N5O6) 870[М+Н]+; RT 1.45 (Метод В)
Стадия C: Гидрохлорид фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата
Раствор продукта из Стадии B (96.6 мг, 0.11 ммоль) в этаноле (5 мл) добавляют к каталитическому количеству 10% Pd/C, и смесь встряхивают в атмосфере газообразного водорода в течение прибл. 16 ч. Смесь фильтруют через целит и упаривают, полученный остаток растворяют в минимальном количестве изопропилового спирта. К получаемому раствору добавляют эфирный раствор HCl (1 М, 0.5 мл) и, далее, эфир, и твердый продукт собирают путем вакуумного фильтрования.
ЖХ/МС (C47H49N5O6) 780 [М+Н]+; RT 1.21 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H49N5O6
[М+Н]+ рассчитано: 780.3756
[М+Н]+ найдено: 780.3791
Пример 70: N-(4-Гидроксифенил)-N-метил-3-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза баа.
ЖХ/МС (C48H51N5O5) 778 [М+Н]+; RT 1.14 (Метод В)
Пример 71: 6-{1-[(4-Гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-N-фенил-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
Методика соответствует методике Стадии A Примера 8 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6аа, и с заменой 2-фенилацетилхлорида на фенилизоцианат.
ЖХ/МС (C43H43N5O4) 694 [М+Н]+; RT 1.31 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H43N5O4
[М+Н]+ рассчитано: 694.3388
[М+Н]+ найдено: 694.3356
Пример 72: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилэтил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
ЖХ/МС (C43H44N4O3) 665 [М+Н]+; RT 1.10 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H44N4O3
[М+Н]+ рассчитано: 665.3486
[М+Н]+ найдено: 665.3477
Пример 73: N-Бензил-6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6аа, и с заменой 2-фенилацетилхлорида на бензилизоцианат.
ЖХ/МС (C44H45N5O4) 708 [М+Н]+; RT 1.3 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H45N5O4
[М+Н]+ рассчитано: 708.3544
[М+Н]+ найдено: 708.3556
Пример 74: 6-{1-[(4-Гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-N-метил-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-N-фенил-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
Стадия А: 6-(1-{[4-(Бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилхлорид
Раствор продукта из Синтеза 6ab (50 мг, 0.08 ммоль) в дихлорметане (5 мл) охлаждают до 0°C и к раствору добавляют N,N-диизопропилэтиламин (0.3 ммоль) и, далее, трифосген (22.3 мг, 0.08 ммоль), и смеси дают перемешиваться при температуре окружающей среды в течение 1 ч. Реакционную смесь распределяют между дихлорметаном и 1 М водной HCl, и органический экстракт сушат над сульфатом магния. После концентрирования в вакууме вещество непосредственно применяют на следующей стадии, предполагая количественное превращение.
ЖХ/МС (C44H43N4O4Cl) 727 [М+Н]+; RT 1.54 (Метод В)
Стадия В: 6-(1-{[4-(Бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-N-метил-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-N-фенил-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
К раствору продукта, полученного на Стадии A, (62 мг, 0.08 ммоль) в ацетонитриле (5 мл) добавляют N,N-диизопропилэтиламин (0.40 ммоль) и N-метиланилин (80.4 мг, 0.75 ммоль), и смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь разбавляют этилацетатом и промывают последовательно водным бикарбонатом натрия и солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют, и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (4 г, силикагель, дихлорметан - 5% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C51H51N5O4) 798 [М+Н]+; RT 1.56 (Метод В)
Стадия С: 6-{1-[(4-Гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-N-метил-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-N-фенил-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
К раствору продукта, полученного на Стадии B, (60 мг, 0.08 ммоль) в этаноле (5 мл) добавляют 10% Pd/C (каталитическое количество) и смесь встряхивают в атмосфере водорода в течение прибл. 16 ч. Смесь фильтруют через целит с дальнейшим элюированием метанолом, и растворитель удаляют в вакууме. Очистка с помощью колоночной флэш-хроматографии (4 г, силикагель; дихлорметан - 5% метанол в дихлорметане) дает целевой продукт в виде твердого вещества.
ЖХ/МС (C44H45N5O4) 708 [М+Н]+; RT 1.35 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H45N5O4
[М+Н]+ рассчитано: 708.3544
[М+Н]+ найдено: 708.3543
Пример 75: N-(4-Гидроксифенил)-N,1,2-триметил-5-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1Н-пиррол-3-карбоксамид
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6bb.
ЖХ/МС (C42H42N4O4) 667 [М+Н]+; RT 1.27 (Метод В)
Пример 76: N-трет-Бутил-5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксамид
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 7ab, и с заменой 2-фенилацетилхлорида на трет-бутил изоцианат.
ЖХ/МС (C40H45N5O4) 660 [М+Н]+; RT 1.29 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C40H45N5O4
[М+Н]+ рассчитано: 660.3544
[М+Н]+ найдено: 660.3529
Пример 77: 6-{1-[(4-Гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-N-фенил-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 6аа, и с заменой 2-фенилацетилхлорида на фенилизоцианат.
ЖХ/МС (C47H50N6O5) 779 [М+Н]+; RT 1.12
Пример 78: N-Бензил-6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 6аа, и с заменой 2-фенилацетилхлорида на бензилизоцианат.
ЖХ/МС (C48H52N6O5) 793 [М+Н]+; RT 1.12
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H52N6O5
[М+Н]+ рассчитано: 793.4072
[М+Н]+ найдено: 793.4067
Пример 79: 6-{1-[(4-Гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-N-метил-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
Методика соответствует методике Примера 74 с заменой N-метиланилина на Стадии B на N-бензилметиламин.
ЖХ/МС (C38H41N5O4) 632 [М+Н]+; RT 1.16 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C38H41N5O4
[М+Н]+ рассчитано: 632.3231
[М+Н]+ найдено: 632.3232
Пример 80: N-(4-Гидроксифенил)-N,1,2-триметил-5-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-2,3-дигидро-1H-изоиндол-5-ил}-1H-пиррол-3-карбоксамид
Стадия A: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-2,3-дигидро-1Н-изоиндол-5-ил}-1Н-пиррол-3-карбоксамид
К раствору соединения из Синтеза 7bb (50 мг, 0.08 ммоль) в дихлорметане (2 мл), охлажденному до 0°C, добавляют DIPEA (28 мкл, 0.16 ммоль) и фенилацетилхлорид (13 мкл, 0.10 ммоль). После перемешивания в течение 10 минут реакционную смесь разбавляют дихлорметаном, промывают последовательно 1 М водным NaOH и солевым раствором, сушат (сульфат магния), и концентрируют в вакууме. Сырое вещество очищают на CombiFlash (4 г, силикагель, дихлорметан - смесь 3% метанол/дихлорметан) с получением продукта.
ЖХ/МС (C48H46N4O4) 743 [М+Н]+; RT 1.47 (Метод В)
Стадия В: N-(4-Гидроксифенил)-N,1,2-триметил-5-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-2,3-дигидро-1Н-изоиндол-5-ил}-1Н-пиррол-3-карбоксамид
Раствор продукта из Стадии A (59 мг, 0.08 ммоль) в этаноле добавляют к 10% Pd/C (каталитическое количество) и смесь встряхивают при температуре окружающей среды в атмосфере водорода в течение прибл. 16 ч. Фильтрование через целит, упаривание растворителей в вакууме, и очистка на CombiFlash (4 г, силикагель, дихлорметан - 5% метанол/дихлорметан) дает целевой продукт.
ЖХ/МС (C41H40N4O4) 653 [М+Н]+; RT 1.25 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H40N4O4
[М+Н]+ рассчитано: 653.3122
[М+Н]+ найдено: 653.3137
Пример 81: N-трет-Бутил-5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-N-метил-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксамид
Методика соответствует методике Примера 74 с заменой продукта из Синтеза 6ab на Стадии A на продукт из Синтеза 7ab, и с заменой N-метиланилина на Стадии B на N-трет-бутилметиламин.
ЖХ/МС (C41H47N5O4) 674 [М+Н]+; RT 1.38 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H47N5O4
[М+Н]+ рассчитано: 674.3701
[М+Н]+ найдено: 674.3720
Пример 82: 5-{1-[(4-Гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-N-метил-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-N-фенил-2,3-дигидро-1H-изоиндол-2-карбоксамид
Методика соответствует методике Примера 74 с заменой продукта из Синтеза 6ab на продукт из Синтеза 7ab.
ЖХ/МС (C43H43N5O4) 694 [М+Н]+; RT 1.33 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H43N5O4
[М+Н]+ рассчитано: 694.3388
[М+Н]+ найдено: 694.3395
Пример 83: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(3-фенилазетидин-1-карбонил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 74 с заменой продукта из Синтеза 7аа на продукт из Синтеза 7ab, и с заменой N-метиланилина на гидрохлорид 3-фенилазетидина.
ЖХ/МС (C45H45N5O4) 720 [М+Н]+; RT 2.62 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H45N5O4
[М+Н]+ рассчитано: 720.3544
[М+Н]+ найдено: 720.3536
Пример 84: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(3-фенилазетидин-1-карбонил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 74 с заменой продукта из Синтеза 7аа на продукт из Синтеза 6ab, и с заменой N-метиланилина на гидрохлорид 3-фенилазетидина.
ЖХ/МС (C46H47N5O4) 734 [М+Н]+; RT 2.66 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H47N5O4
[М+Н]+ рассчитано: 734.3701
[М+Н]+ найдено: 734.3668
Пример 85: N-Бензил-5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-N-метил-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксамид
Стадия A: N-Бензил-5-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-N-метил-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксамид
Методика соответствует методике Стадии A и Стадии B Примера 74 с заменой продукта из Синтеза 6ab на Стадии A на продукт из Синтеза 7ab, и с заменой N-метиланилина на Стадии B на N-бензилметиламин.
ЖХ/МС (C51H51N5O4) 798 [М+Н]+; RT 1.55 (Метод В)
Стадия B: N-Бензил-5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-N-метил-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-2-карбоксамид
Продукт из Стадии A (46 мг, 0.06 ммоль) растворяют в дихлорметане (5 мл) и охлаждают до 0°C. К раствору по каплям добавляют трихлорид бора (1 М в дихлорметане; 0.18 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение 1 ч, затем гасят путем добавления метанола (5 мл) и концентрируют в вакууме. Сырое вещество распределяют между этилацетатом и водой, и органический экстракт промывают солевым раствором, сушат (сульфат магния) и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (4 г, силикагель, дихлорметан - 5% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C44H45N5O4) 708 [М+Н]+; RT 1.36 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H45N5O4
[М+Н]+ рассчитано: 708.3544
[М+Н]+ найдено: 708.3542
Пример 86: 3-{2-[2-(2-Хлорфенокси)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия A: N-[4-(Бензилокси)фенил]-3-{2-[2-(2-хлорфенокси)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил}-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Стадии A Примера 11 с заменой продукта из Синтеза 7аа на продукт из Синтеза 7ab, и с заменой пропионилхлорида на 2-(2-хлорфенокси)ацетилхлорид.
ЖХ/МС (C50H47N4O5Cl) 819 [М+Н]+; RT 1.53 (Метод В)
Стадия В: 3-{2-(2-(2-Хлорфенокси)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1Н-изоиндол-5-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Стадии B Примера 85 с заменой продукта на Стадии A Примера 85 на продукт Стадии A Примера 86.
ЖХ/МС (C43H41N4O5Cl) 729 [М+Н]+; RT 1.35 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H41N4O5Cl
[М+Н]+ рассчитано: 729.2838
[М+Н]+ найдено: 729.2820
Пример 87: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(фениламино)ацетил]-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной в Примере 23, с заменой 2-метил-3-фенилпропановой кислоты на Стадии A на 2-(фениламино)уксусную кислоту.
ЖХ/МС (C43H43N5O4) 694 [М+Н]+; RT 2.58 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H43N5O4
[М+Н]+ рассчитано: 694.3388
[М+Н]+ найдено: 694.3357
Пример 88: Гидрохлорид фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата
Методика соответствует методике, описанной в Примере 69, с заменой соединения из Синтеза 6аа на соединение из Синтеза 6bа.
ЖХ/МС (C45H47N5O6) 754 [М+Н]+; RT 1.17 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H47N5O6
[М+Н]+ рассчитано: 754.3599
[М+Н]+ найдено: 754.3598
Пример 89: N-(4-Гидроксифенил)-N,1,2-триметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на продукт из Синтеза 6аа.
ЖХ/МС (C46H49N5O5) 752 [М+Н]+; RT 1.10 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O5
[М+Н]+ рассчитано: 752.3806
[М+Н]+ найдено: 752.3797
Пример 90: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[(2S)-2-фенилпропаноил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной в Примере 23, с заменой продукта из Синтеза 7ab на продукт из Синтеза 6ab, и с заменой 2-метил-3-фенилпропановой кислоты на Стадии A на (2S)-2-фенилпропановую кислоту.
ЖХ/МС (C45H46N4O4) 707 [М+Н]+; RT 2.65 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H46N4O4
[М+Н]+ рассчитано: 707.3592
[М+Н]+ найдено: 707.3589
Пример 91: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[(2R)-2-фенилпропаноил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной в Примере 23, с заменой продукта из Синтеза 7ab на продукт из Синтеза 6ab, и с заменой 2-метил-3-фенилпропановой кислоты на Стадии A на (2R)-2-фенилпропановую кислоту.
ЖХ/МС (C45H46N4O4) 707 [М+Н]+; RT 2.66 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H46N4O4
[М+Н]+ рассчитано: 707.3592
[М+Н]+ найдено: 707.3589
Пример 92: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[(фенилкарбамоил)метил]-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 8 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 7ab, и с заменой 2-фенилацетилхлорида на Стадии A на 2-хлор-N-фенилацетамид
ЖХ/МС (C43H43N5O4) 694 [М+Н]+; RT 1.18 (Метод В)
Пример 93: Бензил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 62 с заменой продукта из Примера 10 на продукт из Примера 27.
ЖХ/МС (C44H44N4O5) 709 [М+Н]+; RT 1.41 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H44N4O5
[М+Н]+ рассчитано: 709.3384
[М+Н]+ найдено: 709.3387
Пример 94: Бензил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия A: N-(4-Гидроксифенил)-N-метил-3-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид, соль с трифторуксусной кислотой
К раствору продукта из Стадии A Синтеза 6аа (43 мг, 0.065 ммоль) в дихлорметане (5 мл) добавляют трифторуксусную кислоту (0.4 мл), и смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Растворитель удаляют в вакууме с получением целевого продукта, который непосредственно используют на следующей стадии без дополнительной очистки.
ЖХ/МС (C40H45N5O4) 660 [М+Н]+; RT 0.87 (Метод В)
Стадия В: Бензил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Продукт из Стадии A (43 мг, 0.06 ммоль) растворяют в дихлорметане (2 мл) и охлаждают до 0°C. К раствору добавляют триэтиламин (42 мкл, 0.3 ммоль) и, далее, бензилхлорформиат (9 мкл) и смесь перемешивают в течение 15 минут. Реакционную смесь разбавляют дихлорметаном и промывают последовательно 1 М водным NaOH, и солевым раствором. Органику сушат над сульфатом магния, фильтруют и концентрируют, и остаток вносят в метанол. К метанольному раствору добавляют 1М водный NaOH и смесь нагревают в течение 2 часов при 50°C. Реакционную смесь концентрируют в вакууме, распределяют между этилацетатом и солевым раствором, и органику сушат над сульфатом магния. После упаривания сырой продукт очищают с помощью колоночной флэш-хроматографии на силикагеле (4 г), элюируя градиентом дихлорметан - 5% метанол/дихлорметан.
ЖХ/МС (C48H51N5O6) 794 [М+Н]+; RT 1.21 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H51N5O6
[М+Н]+ рассчитано: 794.3912
[М+Н]+ найдено: 794.3908
Пример 95: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилбутаноил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной в Примере 23, с заменой продукта из Синтеза 7ab на продукт из Синтеза 6ab, и с заменой 2-метил-3-фенилпропановой кислоты на Стадии A на 1-фенилциклопропан-1-карбоновую кислоту.
ЖХ/МС (C46H48N4O4) 721 [М+Н]+; RT 2.72 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H48N4O4
[М+Н]+ рассчитано: 721.3748
[М+Н]+ найдено: 721.3740
Пример 96: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(4-{[2-(морфолин-4-ил)этил]амино}фенил)ацетил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия А: Этил 2-(4-{[2-(морфолин-4-ил)этил]амино}фенил)ацетат
В толстостенную пробирку добавляют этил 2-(4-бромфенил)ацетат (317 мг, 1.3 ммоль), 2-(морфолин-4-ил)этан-1-амин (257 мкл, 1.96 ммоль), ортофосфат калия (386 мг, 1.82 ммоль) и (2-бифенил)ди-трет-бутилфосфин (0.1 мол.%) и, далее, толуол (6 мл). Реакционную смесь дегазируют азотом с последующим добавлением бис(дибензилиденацетон)палладия(0) (0.05 мол.%). Затем реакционную смесь нагревают при 100°C в атмосфере азота в течение прибл. 6 ч. Реакционную смесь разбавляют дихлорметаном и промывают водой. Органический экстракт сушат над сульфатом магния, фильтруют и загружают на колонку для очистки на силикагеле в градиенте изогексан - этилацетат.
ЖХ/МС (C16H24N2O3) 293 [М+Н]+; RT 1.74 (Метод А)
Стадия В: 2-(4-{[2-(Морфолин-4-ил)этил]амино}фенил)ацетат натрия
К раствору продукта, полученного на Стадии A, (61 мг, 0.21 ммоль) в метаноле (5 мл) добавляют 2 М NaOH (21 мкл, 0.42 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Затем реакционную смесь фильтруют через набивку из хлопковой ваты и концентрируют в вакууме, затем растирают с эфиром, фильтруют и растворители удаляют в вакууме.
ЖХ/МС (C14H20N2O3) 265 [М+Н]+; RT 0.50 (Метод А)
Стадия C: N-[4-(Бензилокси)фенил]-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(4-{[2-(морфолин-4-л)этил]амино}фенил)ацетил] -1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта из Синтеза 6ab (40 мг, 0.05 ммоль) в дихлорметане (3 мл) добавляют N,N-диизопропилэтиламин (20 мкл, 0.15 ммоль) и HBTU (20 мг, 0.5 ммоль) и, далее, натриевую соль из Стадии B (23 мг, 0.8 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь разбавляют дихлорметаном и промывают водой. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (силикагель; дихлорметан - 5% метанол в дихлорметане) с последующим растиранием с эфиром дает целевой продукт в виде кремового порошка.
ЖХ/МС (C57H62N6O5) 911 [М+Н]+; RT 2.51 (Метод А)
Стадия D: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(4-{[2-(морфолин-4-ил)этил]амино}фенил)ацетил]-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Раствор продукта из Стадии C (68 мг, 0.07 ммоль) в этаноле (5 мл) добавляют к 10% Pd/C (каталитическое количество) и смесь встряхивают при температуре окружающей среды в атмосфере водорода в течение прибл. 16 ч. Фильтрование через целит, упаривание растворителей в вакууме, и очистка на CombiFlash (4 г, силикагель, дихлорметан - 5% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C50H56N6O5) 819 [М-Н]-; RT 2.21 (Метод А)
Пример 97: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[4-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 96 с заменой 2-(морфолин-4-ил)этан-1-амина на Стадии A на 1-метилпиперазин.
ЖХ/МС (C49H54N6O4) 791 [М+Н]+; RT 2.20 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C49H54N6O4
[М+Н]+ рассчитано: 791.4279
[М+Н]+ найдено: 791.4268
Пример 98: Гидрохлорид 4-метилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата
Методика соответствует методике, описанной в Примере 99, с заменой 3-метилфенола на Стадии B на 4-метилфенол.
ЖХ/МС (C48H51N5O6) 794 [М+Н]+; RT 1.25 (Метод В)
Пример 99: 3-Метилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия A: 6-(1-{[4-(Бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилхлорид
К раствору соединения из Синтеза 6аа (150 мг, 0.17 ммоль) в дихлорметане (5 мл), охлажденному до 0°C, добавляют DIPEA (89 мкл, 0.51 ммоль) с последующим добавлением порциями трифосгена (52 мг, 0.17 ммоль). После перемешивания в течение 1 ч реакционную смесь распределяют между дихлорметаном и 1 М водной HCl, и органическую фазу сушат над сульфатом магния, фильтруют и концентрируют с получением смеси трихлорметил 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата и 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилхлорида, которую используют непосредственно на следующей стадии без дополнительной очистки и предполагая количественное превращение.
Стадия В: 3-Метилфенил 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору продукта из Стадии A (30 мг) в ацетонитриле (5 мл) добавляют карбонат калия (17 мг, 0.123 ммоль) и 3-метилфенол (13 мкл, 0.123 ммоль) и смесь нагревают при 65°C в течение 2 часов. Реакционную смесь охлаждают до комнатной температуры, разбавляют этилацетатом и промывают солевым раствором. Органику сушат над сульфатом магния, фильтруют и концентрируют. Сырое вещество вносят в дихлорметан, загружают на изолют и очищают на CombiFlash (4 г, силикагель, дихлорметан - 5% метанол/дихлорметан).
Стадия С: 3-Метилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Раствор продукта из Стадии B (30 мг, 0.03 ммоль) в этаноле добавляют к 10% Pd/C (каталитическое количество) и смесь встряхивают в атмосфере водорода в течение прибл. 16 ч. Фильтрование через целит, упаривание, и очистка на CombiFlash (4 г, силикагель, дихлорметан - 5% МеОН/дихлорметан) дает целевой продукт. Соответствующие фракции объединяют и концентрируют с получением целевого продукта.
ЖХ/МС (C48H51N5O6) 794 [М+Н]+; RT 1.25 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H51N5O6
[М+Н]+ рассчитано: 794.3912
[М+Н]+ найдено: 794.3925
Пример 100: 2-Метилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике, описанной в Примере 99 с заменой 3-метилфенола на Стадии B на 2-метилфенол.
ЖХ/МС (C48H51N5O6) 794 [М+Н]+; RT 1.25 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H51N5O6
[М+Н]+ рассчитано: 794.3912
[М+Н]+ найдено: 794.3877
Пример 101: N-(4-Гидроксифенил)-5-{2-[2-(4-метоксифенил)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N,1,2-триметил-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H42N4O5
[М+Н]+ рассчитано: 683.3235
[М+Н]+ найдено: 683.3213
Пример 102: 5-{2-[2-(4-Фторфенил)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H39FN4O4
[М+Н]+ рассчитано: 671,3035
[М+Н]+ найдено: 671.3039
Пример 103: N-(4-Гидроксифенил)-N,1,2-триметил-5-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-феноксиацетил)-2,3-дигидро-1H-изоиндол-5-ил}-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H40N4O5
[М+Н]+ рассчитано: 669.3079
[М+Н]+ найдено: 669.3084
Пример 104: N-(4-Гидроксифенил)-N,1,2-триметил-5-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-феноксипропаноил)-2,3-дигидро-1H-изоиндол-5-ил}-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H42N4O5
[М+Н]+ рассчитано: 683.3235
[М+Н]+ найдено: 683.3210
Пример 105: 4-Хлорфенил 5-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C40H37ClN4O5
[М+Н]+ рассчитано: 689.2532
[М+Н]+ найдено: 689.2539
Пример 106: 4-Фторфенил 5-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C40H37FN4O5
[М+Н]+ рассчитано: 673.2828
[М+Н]+ найдено: 673.2832
Пример 107: 4-Метилфенил 5-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H40N4O5
[М+Н]+ рассчитано: 669.3079
[М+Н]+ найдено: 669.3065
Пример 108: Гидрохлорид 3-{2-[2-(4-{[2-(диметиламино)этил]амино}фенил)ацетил]-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамида
Методика соответствует методике Примера 96 с заменой 2-(морфолин-4-ил)этан-1-амина на Стадии A на (2-аминоэтил)диметиламин.
ЖХ/МС (C48H54N6O4) 777 [М-Н]-; RT 2.20 (Метод А)
Пример 109: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(1-фенилциклопропанкарбонил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия A: N-[4-(бензилокси)фенил]-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(1-фенилциклопропанкарбонил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта из Синтеза 6ab (43 мг, 0.06 ммоль) в дихлорметане (5 мл) добавляют основание Хюнига (32 мкл, 0.18 ммоль) и HBTU (23 мг, 0.06 ммоль) и, далее, 1-фенилциклопропан-1-карбоновую кислоту (9 мг, 0.06 ммоль), и перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь разбавляют дихлорметаном и промывают водой, и, далее, водной 1 М HCl и затем солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют и загружают на колонку и очищают в этилацетате с получением целевого продукта.
ЖХ/МС (C53H52N4O4) 809 [М+Н]+; RT 2.92 (Метод А)
Стадия B: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(1-фенилциклопропанкарбонил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Раствор продукта из Стадии A (47.6 мг, 0.06 ммоль) в безводном дихлорметане (5 мл) охлаждают до 0°C и к раствору добавляют трихлорид бора (1 М в ДХМ, 120 мкл, 0.12 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакцию гасят метанолом (5 мл), и реакционную смесь разбавляют дихлорметаном. Органическую фазу промывают водой, сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Сырой продукт очищают с помощью колоночной хроматографии в градиенте дихлорметан - 5% метанол в дихлорметане с последующим растиранием с эфиром и сушат в вакууме.
ЖХ/МС (C46H46N4O4) 719 [М+Н]+; RT 2.65 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H46N4O4
[М+Н]+ рассчитано: 719.3592
[М+Н]+ найдено: 719.3556
Пример 110: N-Этил-5-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C36H39N5O4
[М+Н]+ рассчитано: 606.3082
[М+Н]+ найдено: 606.3078
Пример 111; N-Бензил-5-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H41N5O4
[М+Н]+ рассчитано: 668.3239
[М+Н]+ найдено: 668.3203
Пример 112: 5-{2-Ацетил-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C35H36N4O4
[М+Н]+ рассчитано: 577.2817
[М+Н]+ найдено: 577.2782
Пример 113: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-{4-[(4-метилпиперазин-1-ил)метил]фенил}ацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия A: 2-{4-[(4-метилпиперазин-1-ил)метил]фенил}уксусная кислота
К суспензии 4-(бромметил)фенилуксусной кислоты (100 мг, 0.44 ммоль) в ацетонитриле (2 мл) добавляют карбонат калия (126 мг, 0.88 ммоль) и N-метилпиперазин (100 мкл, 0.88 ммоль), и реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь фильтруют и промывают этилацетатом. Фильтрат подщелачивают метанольным раствором гидроксида натрия и затем концентрируют в вакууме. Сырое вещество растворяют в метаноле и загружают на РЕ-AX колонку, которую предварительно смачивают дихлорметаном. Колонку затем промывают дихлорметаном и метанолом, и продукт элюируют смесью 10% муравьиная кислота/дихлорметан.
ЖХ/МС (C14H20N2O2) 249 [М+Н]+; RT 0.42 (Метод А)
Стадия В: N-[4-(Бензилокси)фенил]-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-{4-[(4-метилпиперазин-1-ил)метил]фенил}ацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта из Синтеза 6ab (50 мг, 0.08 ммоль) в дихлорметане (3 мл) добавляют триэтиламин (56 мкл, 0.4 ммоль) и HBTU (30 мг, 0.08 ммоль) и, далее, кислоту, полученную на Стадии A, (30 мг, 0.1 ммоль) в дихлорметане (2 мл). Реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 2 ч. Реакционную смесь разбавляют дихлорметаном и промывают водой, сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Реакционную смесь очищают с помощью колоночной хроматографии на 10 г силикагелевой колонке в градиенте дихлорметан - 5% метанол в дихлорметане.
ЖХ/МС (C57H62N6O4) 448 [М+2Н]2+; RT 2.51 (Метод А)
Стадия C: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-{4-[(4-метилпиперазин-1-ил)метил]фенил}ацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Раствор продукта из Стадии B (44 мг, 0.05 ммоль) в этаноле (10 мл) добавляют к 10% Pd/C (каталитическое количество) и смесь встряхивают в атмосфере водорода в течение прибл. 16 ч. Фильтрование через целит, упаривание, и очистка с помощью колоночной хроматографии (4 г, силикагель, дихлорметан - 5% метанол в дихлорметане) дает целевой продукт. Растирание с диэтиловым эфиром дает целевой продукт.
ЖХ/МС (C50H56N6O4) 803 [М-Н]-; RT 2.20 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C50H56N6O4
[М+2Н]2+ рассчитано: 403.2254
[М+2Н]2+ найдено: 403.2252
Пример 114: Фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Продукт, полученный из Синтеза 6cb, (50 мг, 0.08 ммоль) и N,N-диизопропилэтиламин (70 мкл, 0.4 ммоль) растворяют в дихлорметане (5 мл) и раствор охлаждают до 0°C. К раствору добавляют фенилхлорформиат (11 мкл, 0.09 ммоль), и смесь перемешивают при температуре окружающей среды в течение 15 мин. Реакционную смесь разбавляют дихлорметаном, затем промывают 1 М водным гидроксидом натрия и солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (4 г, силикагель, дихлорметан - 4% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C41H40N4O4) 653 [М+Н]+; RT 1.48 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H40N4O4
[М+Н]+ рассчитано: 653.3122
[М+Н]+ найдено: 653.3159
Пример 115: Фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 114 с заменой продукта из Синтеза 6cb на продукт из Синтеза 6са.
ЖХ/МС (C45H47N5O5) 738 [М+Н]+; RT 1.28 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H47N5O5
[М+Н]+ рассчитано: 738.3650
[М+Н]+ найдено: 738.3655
Пример 116: N-(4-Гидроксифенил)-5-{2-[3-(4-метоксифенил)пропил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N,1,2-триметил-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H46N4O4
[М+Н]+ рассчитано: 683.3599
[М+Н]+ найдено: 683.3608
Пример 117: N,1,2-триметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-N-фенил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 114 с заменой продукта из Синтеза 6cb на продукт из Синтеза 6са, и с заменой фенилхлорформиата на фенилацетилхлорид.
ЖХ/МС (C46H49N5O4) 736 [М+Н]+; RT 1.23 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O4
[М+Н]+ рассчитано: 736.3857
[М+Н]+ найдено: 736.3828
Пример 118: N,1,2-Триметил-5-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-N-фенил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 114 с заменой фенилхлорформиата на фенилацетилхлорид.
ЖХ/МС (C42H42N4O3) 651 [М+Н]+; RT 1.40 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H42N4O3
[М+Н]+ рассчитано: 651.3330
[М+Н]+ найдено: 651.3344
Пример 119: Гидрохлорид N,1,2-триметил-5-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-фенил-1H-пиррол-3-карбоксамида
Продукт из Синтеза 6cb (22 мг, 0.03 ммоль) растворяют в этилацетате (10 мл) и промывают насыщенным бикарбонатом натрия (10 мл). Органическую фазу отделяют, сушат над сульфатом магния и концентрируют в вакууме. Твердое вещество затем растворяют в метаноле (2 мл) и к раствору добавляют 1 М HCl в диэтиловом эфире (0.15 мл, 5 экв.), перемешивают в течение 30 мин, и затем концентрируют в вакууме. Твердое вещество затем растирают в небольшом количестве диэтилового эфира и твердые вещества выделяют фильтрованием. Вещества промывают холодным эфиром и затем сушат в вакууме в течение 1 ч.
ЖХ/МС (C34H36N4O2) 533 [М+Н]+; RT 1.08 (Метод В)
Пример 120: 4-Фторфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6аа, и с заменой 2-фенилацетилхлорида на Стадии A на 4-фторфенилхлорформиат.
ЖХ/МС (C47H48N5O6F) 798 [М+Н]+; RT 1.22 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H48N5O6F
[М+Н]+ рассчитано: 798.3661
[М+Н]+ найдено: 798.3663
Пример 121: 4-Метоксифенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике, описанной на Стадии A Примера 8, с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6аа, и с заменой 2-фенилацетилхлорида на Стадии A на 4-метоксифенилхлорформиат.
ЖХ/МС (C48H51N5O7) 810 [М+Н]+; RT 1.21 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H51N5O7
[М+Н]+ рассчитано: 810.3861
[М+Н]+ найдено: 810.3826
Пример 122: 4-Хлорфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия А: 4-Хлорфенил 6-(1-{[4-(бензилокси)фенил](метил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии A Примера 11 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6аа, и с заменой пропионилхлорида на 4-хлорфенилхлорформиат.
ЖХ/МС (C54H54ClN5O6) 904 [М+Н]+; RT 1.51 (Метод В)
Стадия В: 4-Хлорфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии B Примера 85 с заменой продукта Стадии A Примера 85 на продукт Стадии A Примера 122.
ЖХ/МС (C47H48ClN5O6) 814 [М+Н]+; RT 1.27 (Метод В)
Пример 123: 3-{2-[2-(3-{[2-(Диметиламино)этил]амино}фенил)ацетил]-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 96 с заменой 2-(морфолин-4-ил)этан-1-амина на Стадии A на (2-аминоэтил)диметиламин, и с заменой этил 2-(4-бромфенил)ацетата на Стадии A на метил 2-(3-бромфенил)ацетат.
ЖХ/МС (C48H54N6O4) 777 [М-Н]-; RT 2.23 (Метод А)
Пример 124: 4-(Трифторметил)фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 74 с заменой продукта из Синтеза 6ab на Стадии A на продукт из Синтеза 6аа, и с заменой N-метиланилина на Стадии B на 4-(трифторметил)фенол.
ЖХ/МС (C48H48N5O6F3) 848 [М+Н]+; RT 1.31 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H48N5O6F3
[М+Н]+ рассчитано: 848.3629
[М+Н]+ найдено: 848.3615
Пример 125: 4-(Трифторметокси)фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 74 с заменой продукта из Синтеза 6ab на Стадии A на продукт из Синтеза 6аа, и с заменой N-метиланилина на Стадии B на 4-(трифторметокси)фенол.
ЖХ/МС (C48H48N5O7F3) 864 [М+Н]+; RT 1.31 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H48N5O7F3
[М+Н]+ рассчитано: 864.3579
[М+Н]+ найдено: 864.3576
Пример 126: 4-Этилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 74 с заменой продукта из Синтеза 6ab на Стадии A на продукт из Синтеза 6аа, и с заменой N-метиланилина на Стадии B на 4-этилфенол.
ЖХ/МС (C49H53N5O6) 808 [М+Н]+; RT 1.32 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C49H53N5O6
[М+Н]+ рассчитано: 808.4069
[М+Н]+ найдено: 808.4026
Пример 127: 4-Цианофенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 74 с заменой продукта из Синтеза 6ab на Стадии A на продукт из Синтеза 6аа, и с заменой N-метиланилина на Стадии B на 4-гидроксибензонитрил.
ЖХ/МС (C48H48N6O6) 805 [М+Н]+; RT 1.18 (Метод В)
Пример 128: 2-Метоксифенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии A Примера 8 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6аа, и с заменой 2-фенилацетилхлорида на 2-метоксифенилхлорформиат.
ЖХ/МС (C48H51N5O7) 810 [М+Н]+; RT 1.20 (Метод В)
Пример 129: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[4-(морфолин-4-илметил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия A: N-[4-(Бензилокси)фенил]-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[4-(морфолин-4-илметил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Стадий A и B Примера 113 с заменой N-метилпиперазина на Стадии A на морфолин.
ЖХ/МС (C56H59N5O5) 882 [М+Н]+; RT 2.51 (Метод А)
Стадия B: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[4-(морфолин-4-илметил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Раствор продукта из Стадии A (49 мг, 0.06 ммоль) в безводном дихлорметане (5 мл) охлаждают до 0°C и к раствору добавляют трихлорид бора (1 М в ДХМ, 170 мкл, 0.17 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакцию гасят метанолом (5 мл), и реакционную смесь разбавляют дихлорметаном. Органическую фазу промывают водой, сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Сырой продукт очищают с помощью колоночной хроматографии в градиенте дихлорметан - 7% метанол в дихлорметане с последующим растиранием с эфиром и сушат в вакууме.
ЖХ/МС (C49H53N5O5) 792 [М+Н]+; RT 2.20 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C49H53N5O5
[М+2Н]2+ рассчитано: 396.7096
[М+2Н]2+ найдено: 396.7104
Пример 130: N-(4-Гидроксифенил)-N,1,2-триметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(3-фенилпропаноил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 23 с заменой продукта из Синтеза 7ab на Стадии A на продукт из Синтеза 6bа, и с заменой 2-метил-3-фенилпропановой кислоты на Стадии A на 3-фенилпропановую кислоту.
ЖХ/МС (C47H51N5O5) 766 [М+Н]+; RT 1.14 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H51N5O5
[М+Н]+ рассчитано: 766.3963
[М+Н]+ найдено: 766.3955
Пример 131: N-(4-Гидроксифенил)-N,1,2-триметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[(2E-)-3-фенилпроп-2-еноил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 109 с заменой продукта из Синтеза 6ab на продукт из Синтеза 6bа, и с заменой 2-метил-3-фенилпропановой кислоты на (2E)-3-фенилпроп-2-еновую кислоту.
ЖХ/МС (C47H49N5O5) 764 [М+Н]+; RT 1.15 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H49N5O5
[М+Н]+ рассчитано: 764.3806
[М+Н]+ найдено: 764.3779
Пример 132: 5-[2-(3-Циклогексилпропаноил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 23 с заменой продукта из Синтеза 7ab на Стадии A на продукт из Синтеза 6bа, и с заменой 2-метил-3-фенилпропановой кислоты на Стадии A на 3-циклогексилпропановую кислоту.
ЖХ/МС (C47H57N5O5) 772 [М+Н]+; RT 1.25 (Метод В)
Пример 133: Фенил 5-{1-[(4-гидроксифенил)(фенил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H43N4O5
[М+Н]+ рассчитано: 743.3228
[М+Н]+ найдено: 743.3234
Пример 134: N-(4-гидроксифенил)-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-N-фенил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C49H47N4O4
[М+Н]+ рассчитано: 755.3592
[М+Н]+ найдено: 755.3595
Пример 135: N-(4-Гидроксифенил)-5-{2-[3-(3-метоксифенил)пропаноил]-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N,1,2-триметил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 23 с заменой продукта из Синтеза 7ab на Стадии A на продукт из Синтеза 6bа, и с заменой 2-метил-3-фенилпропановой кислоты на Стадии A на 3-(2-метоксифенил)пропановую кислоту.
ЖХ/МС (C48H53N5O6) 796 [М+Н]+; RT 1.14 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H53N5O6
[М+Н]+ рассчитано: 796.4069
[М+Н]+ найдено: 796.4068
Пример 136: N-(4-Гидроксифенил)-5-{2-[(2E)-3-(3-метоксифенил)проп-2-еноил]-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N,1,2-триметил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 109 с заменой продукта из Синтеза 6ab на продукт из Синтеза 6bа, и с заменой 2-метил-3-фенилпропановой кислоты на (2E)-3-(2-метоксифенил)проп-2-еновую кислоту.
ЖХ/МС (C48H51N5O6) 794 [М+Н]+; RT 1.16 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H51N5O6
[М+Н]+ рассчитано: 794.3912
[М+Н]+ найдено: 794.3908
Пример 137: 5-{2-[(2E)-3-(3,4-дихлорфенил)проп-2-еноил]-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 109 с заменой продукта из Синтеза 6ab на продукт из Синтеза 6bа, и с заменой 2-метил-3-фенилпропановой кислоты на (2E)-3-(3,4-дихлорфенил)проп-2-еновую кислоту.
ЖХ/МС (C47H47N5O5Cl2) 832 [М+Н]+; RT 1.27 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H47N5O5Cl2
[М+Н]+ рассчитано: 832.3027
[М+Н]+ найдено: 832.3000
Пример 138: 3-{2-[3-(4-{[2-(Диметиламино)этил]амино}фенил)пропаноил]-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике, описанной в Примере 96 с заменой 2-(морфолин-4-ил)этан-1-амина на Стадии A на (2-аминоэтил)диметиламин, и с заменой этил 2-(4-бромфенил)ацетата на Стадии A на метил 3-(4-бромфенил)пропаноат.
ЖХ/МС (C49H56N6O4) 791 [М-Н]-; RT 2.22 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C49H56N6O4
[М+Н]+ рассчитано: 793.4436
[М+Н]+ найдено: 793.4411
Пример 139: 4-Метилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 11 с заменой продукта из Синтеза 7аа на продукт из Синтеза 6bа, и с заменой пропионилхлорида на 4-метилфенилхлорформиат.
ЖХ/МС (C46H49N5O6) 768 [М+Н]+; RT 1.22 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O6
[М+Н]+ рассчитано: 768.3756
[М+Н]+ найдено: 768.3723
Пример 140: 4-Хлорфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия A: 4-Хлорфенил 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии A Примера 11 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6bа, и с заменой пропионилхлорида на 4-хлорфенилхлорформиат.
ЖХ/МС (C52H52N5O6Cl) 878[М+Н]+; RT 1.48 (Метод В)
Стадия В: 4-Хлорфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии B Примера 85 с заменой продукта на Стадии A Примера 85 на продукт Стадии A Примера 140.
ЖХ/МС (C45H46N5O6Cl) 788 [М+Н]+; RT 1.24 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H46N5O6Cl
[М+Н]+ рассчитано: 788.3209
[М+Н]+ найдено: 788.3191
Пример 141: 4-Карбамоилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 74 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6аа, и с заменой N-метиланилина на 4-гидроксибензамид.
ЖХ/МС (C48H50N6O7) 823 [М+Н]+; RT 1.06 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H50N6O7
[М+Н]+ рассчитано: 823.3814
[М+Н]+ найдено: 823.3788
Пример 142: 4-(Диметилкарбамоил)фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 74 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6аа, и с заменой N-метиланилина на 4-гидрокси-N,N-диметилбензамид.
ЖХ/МС (C50H54N6O7) 851 [М+Н]+; RT 1.11 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C50H54N6O7
[М+Н]+ рассчитано: 851.4127
[М+Н]+ найдено: 851.4094
Пример 143: 4-(1H-Имидазол-1-ил)фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 74 с заменой продукта из Синтеза 7аа на Стадии A на продукт из Синтеза 6аа, и с заменой N-метиланилина на 4-(1H-имидазол-1-ил)фенол.
ЖХ/МС (C50H51N7O6) 846 [М+Н]+; RT 1.03 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C50H51N7O6
[М+2Н]2+ рассчитано: 423.7023
[М+2Н]2+ найдено: 423.7023
Пример 144: 3-[2-(2-{4-[(Диметиламино)метил]фенил}ацетил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Методика соответствует методике Примера 113 с заменой N-метилпиперазина на Стадии A на диметиламин.
ЖХ/МС (C47H51N5O4) 748 [М-Н]-; RT 2.18 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H51N5O4
[М+Н]+ рассчитано: 750.4014
[М+Н]+ найдено: 750.3984
Пример 145: 5-{2-[2-(4-Цианофенил)ацетил]-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 109 с заменой продукта из Синтеза 6ab на Стадии A на продукт из Синтеза 6bb, и с заменой 1-фенилциклопропан-1-карбоновой кислоты на Стадии A на 2-(4-цианофенил)уксусную кислоту.
ЖХ/МС (C43H41N5O4) 692 [М+Н]+; RT 1.24 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H41N5O4
[М+Н]+ рассчитано: 692.3231
[М+Н]+ найдено: 692.3199
Пример 146: 4-Цианофенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 573 с заменой 3,4-дихлорфенола на Стадии B на 4-гидроксибензонитрил.
ЖХ/МС (C46H46N6O6) 779 [М+Н]+; RT 1.14 (Метод В)
Пример 147: 4-Цианофенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 573 с заменой продукта из Синтеза 6bа на продукт из Синтеза 6bb, и с заменой 3,4-дихлорфенола на Стадии B на 4-гидроксибензонитрил.
ЖХ/МС (C42H39N5O5) 694 [М+Н]+; RT 1.29 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H39N5O5
[М+Н]+ рассчитано: 694.3024
[М+Н]+ найдено: 694.3044
Пример 148: 4-Циано-2-метоксифенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 573 с заменой продукта из Синтеза 6bа на продукт из Синтеза 7аа, и с заменой 3,4-дихлорфенола на Стадии B на 4-гидроксибензонитрил.
ЖХ/МС (C49H50N6O7) 835 [М+Н]+; RT 1.19 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C49H50N6O7
[М+Н]+ рассчитано: 835.3814
[М+Н]+ найдено: 835.3833
Пример 149: 5-{2-[2-(4-{[2-(Диметиламино)этил]амино}фенил)ацетил]-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 96 с заменой 2-(морфолин-4-ил)этан-1-амина на Стадии A на (2-аминоэтил)диметиламин, и с заменой продукта из Синтеза 6bа на Стадии C на продукт, полученный в Синтезе 6cb.
ЖХ/МС (C46H52N6O3) 737 [М+Н]+; RT 1.13 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H52N6O3
[М+Н]+ рассчитано: 737.4174
[М+Н]+ найдено: 737.4173
Пример 150: 5-{2-[2-(4-Цианофенил)ацетил]-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 109 с заменой продукта из Синтеза 6ab на Стадии A на продукт из Синтеза 6cb, и с заменой 1-фенилциклопропан-1-карбоновой кислоты на Стадии A на 2-(4-цианофенил)уксусную кислоту.
ЖХ/МС (C43H41N5O3) 676 [М+Н]+; RT 1.36 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H41N5O3
[М+Н]+ рассчитано: 676.3282
[М+Н]+ найдено: 676.3249
Пример 151: 5-{2-[2-(4-Цианофенил)ацетил]-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 109 с заменой продукта из Синтеза 6ab на Стадии A на продукт из Синтеза 6са, и с заменой 1-фенилциклопропан-1-карбоновой кислоты на Стадии A на 2-(4-цианофенил)уксусную кислоту.
ЖХ/МС (C47H48N6O4) 761 [М+Н]+; RT 1.19 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H48N6O4
[М+Н]+ рассчитано: 761.3810
[М+Н]+ найдено: 761.3811
Пример 152: 4-Цианофенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадий A и B Пример 573 с заменой 3,4-дихлорфенола на Стадии B на 4-гидроксибензонитрил.
ЖХ/МС (C46H46N6O5) 763 [М+Н]+; RT 1.26 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H46N6O5
[М+Н]+ рассчитано: 763.3602
[М+Н]+ найдено: 763.3572
Пример 153: 4-{[2-(Диметиламино)этил]амино}фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 489 с заменой продукта из Синтеза 6cb на продукт из Синтеза 6ab.
ЖХ/МС (C47H52N6O5) 779 [М-Н]-; RT 2.27 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H52N6O5
[М+2Н]2+ рассчитано: 391.2072
[М+2Н]2+ найдено: 391.2081
Пример 154: 3-[2-(2-{4-[2-(Диметиламино)этокси]фенил}ацетил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия А: Метил 2-{4-[2-(диметиламино)этокси]фенил}ацетат
К раствору метил 4-гидроксифенилацетата (50 мг, 0.3 ммоль) в ацетоне (5 мл) добавляют карбонат цезия (196 мг, 0.6 ммоль) и, далее, гидрохлорид 2-диметиламиноэтилхлорида (45 мг, 0.31 ммоль), и реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. К смеси добавляют йодид натрия (45 мг, 0.3 ммоль) и смесь нагревают при 60°C в течение прибл. 48 ч. Реакционную смесь охлаждают до температуры окружающей среды, разбавляют дихлорметаном и промывают водой, сушат над сульфатом магния, фильтруют и концентрируют в вакууме и загружают на предварительно набитую 10 г силикагелевую колонку и очищают с помощью колоночной хроматографии в градиенте дихлорметан - 10% метанол в дихлорметане с получением целевого продукта.
ЖХ/МС (C13H19NO3) 238 [М+Н]+; RT 1.49 (Метод А)
Стадия В: 2-{4-[2-(Диметиламино)этокси]фенил}ацетат натрия
К раствору метил 2-{4-[2-(диметиламино)этокси]фенил}ацетата (19 мг, 0.08 ммоль) в метаноле (3 мл) добавляют гидроксид натрия (2 М, 80 мкл, 0.16 ммоль) и реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 48 ч. Реакционную смесь концентрируют в вакууме с получением целевого продукта и используют далее, предполагая количественное превращение.
ЖХ/МС (C12H17NO3) 224 [М+Н]+; RT 0.53 (Метод А)
Стадия C: N-[4-(Бензилокси)фенил]-3-[2-(2-{4-[2-(диметиламино)этокси]фенил}ацетил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К суспензии продукта из Стадии B (16 мг, 0.06 ммоль) в дихлорметане (5 мл) добавляют продукт из Синтеза 6ab (50 мг, 0.06 ммоль) и, далее, триэтиламин (27 мкл, 0.19 ммоль) и HBTU (24 мг, 0.06 ммоль), и реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь разбавляют дихлорметаном и промывают водой, сушат над сульфатом магния, фильтруют и концентрируют в вакууме и загружают в дихлорметане на предварительно набитую 10 г силикагелевую колонку и очищают с помощью колоночной хроматографии в градиенте дихлорметан - 10% метанол в дихлорметане.
ЖХ/МС (C55H59N5O5) 435.5 [М+2Н]2+; RT 2.54 (Метод А)
Стадия D: 3-[2-(2-{4-[2-(Диметиламино)этокси]фенил}ацетил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта, полученного на Стадии C, (51.8 мг, 0.04 ммоль, 1 экв.) в этаноле (5 мл) добавляют 10% Pd/C (каталитическое количество). Реакционную смесь перемешивают в атмосфере водорода в течение прибл. 48 ч. Реакционную смесь фильтруют через картридж с целитом и промывают метанолом, концентрируют в вакууме и очищают с помощью обращеннофазовой препаративной ЖХВР (H2O-ТФУ/ацетонитрил; градиентное элюирование).
ЖХ/МС (C48H53N5O5) 778 [М-Н]-; RT 2.20 (Метод А)
Пример 155: 4-[2-(Диметилкарбамоил)этил]фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 786 с заменой продукта из Синтеза 6cb на Стадии A на продукт из Синтеза 6ab, и 4-гидроксибензонитрила на Стадии B на 3-(4-гидроксифенил)-N,N-диметилпропанамид.
ЖХ/МС (C48H51N5O6) 794 [М+Н]+; RT 2.57 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H51N5O6
[М+Н]+ рассчитано: 794.3912
[М+Н]+ найдено: 794.3950
Пример 156: N-(4-Гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-феноксиацетил)-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H49N5O6
[М+Н]+ рассчитано: 780.3763
[М+Н]+ найдено: 780.3759
Пример 157: 1,1-Диоксо-1λ-тиолан-3-ил 5-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C38H40N4O7S
[М+Н]+ рассчитано: 697.2698
[М+Н]+ найдено: 697.2696
Пример 158: N-(4-Гидроксифенил)-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-феноксиацетил)-2,3-дигидро-1H-изоиндол-5-ил}-N-{1-метил-1H-пирроло[2,3-b]пиридин-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Пример 159: N-(4-Гидроксифенил)-N,1,2-триметил-5-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-феноксиацетил)-2,3-дигидро-1Н-изоиндол-5-ил}-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H47N5O6
[М+Н]+ рассчитано: 754.3606
[М+Н]+ найдено: 754.3574
Пример 160: 5-{2-[2-(Бензилокси)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H42N4O5
[М+Н]+ рассчитано: 683.3235
[М+Н]+ найдено: 683.3238
Пример 161: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-(1,2,3,4-тетрагидроизохинолин-2-карбонил)-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Продукт из Синтеза 6dc (81 мг, 0.15 ммоль, 1 экв.) в дихлорметане (5 мл) охлаждают до 0°C. К нему добавляют N,N-диизопропилэтиламин (52 мкл, 0.3 ммоль) и, далее, фенилхлорформиат (21 мкл, 0.16 ммоль) и смеси дают перемешиваться в течение 15 мин. Реакционную смесь разбавляют дихлорметаном и промывают последовательно 1М водным NaOH, и солевым раствором. Органические экстракты сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 12 г RediSep™ силикагелевый картридж; градиент дихлорметан - 5% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C41H48N4O4) 661 [М+Н]+; RT 1.57 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H48N4O4
[М+Н]+ рассчитано: 661.3748
[М+Н]+ найдено: 661.3769
Пример 162: N,N-Дибутил-1,2-диметил-5-[2-(2-фенилацетил)-7-(1,2,3,4-тетрагидроизохинолин-2-карбонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 161 с заменой фенилхлорформиата на фенилацетилхлорид.
ЖХ/МС (C42H50N4O3) 659 [М+Н]+; RT 1.52 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H50N4O3
[М+Н]+ рассчитано: 659.3956
[М+Н]+ найдено: 659.3969
Пример 163: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 161 с заменой продукта из Синтеза 6dc на продукт из Синтеза 6db.
ЖХ/МС (C42H50N4O4) 675 [М+Н]+; RT 1.52 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H50N4O4
[М+Н]+ рассчитано: 675.3905
[М+Н]+ найдено: 675.3900
Пример 164: N,N-Дибутил-1,2-диметил-5-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 161 с заменой продукта из Синтеза 6dc на продукт из Синтеза 6db, и с заменой фенилхлорформиата на фенилацетилхлорид.
ЖХ/МС (C43H52N4O3) 673 [М+Н]+; RT 1.51 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H52N4O3
[М+Н]+ рассчитано: 673.4112
[М+Н]+ найдено: 673.4087
Пример 165: N,N-Дибутил-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
К раствору продукта из Синтеза 6da (112 мг, 0.13 ммоль) в дихлорметане (5 мл) добавляют N,N-диизопропилэтиламин (112 мкл, 0.64 ммоль) и, далее, фенилацетилхлорид (17 мкл, 0.14 ммоль), и смеси дают перемешиваться в течение 15 мин. Реакционную смесь разбавляют дихлорметаном и промывают последовательно 1М водным гидроксидом натрия и солевым раствором. Органические экстракты сушат над сульфатом магния, фильтруют и концентрируют. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 12 г RediSep™ силикагелевый картридж) с элюированием градиентом дихлорметан - 5% метанол в дихлорметане дает целевой продукт.
ЖХ/МС (C47H59N5O4) 758 [М+Н]+; RT 1.40 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H59N5O4
[М+Н]+ рассчитано: 758.4640
[М+Н]+ найдено: 758.4648
Пример 166: N-(4-Гидроксифенил)-N-метил-3-{6-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-феноксиацетил)-2,3-дигидро-1N-изоиндол-5-ил}индолизин-1-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H45N5O6
[М+Н]+ рассчитано: 776.3450
[М+Н]+ найдено: 776.3430
Пример 167: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-феноксиацетил)-2,3-дигидро-1H-изоиндол-5-ил}индолизин-1-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H38N4O5
[М+Н]+ рассчитано: 691.2922
[М+Н]+ найдено: 691.2913
Пример 168: 4-Метилфенил 5-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксилат
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H42N4O5
[М+Н]+ рассчитано: 695.3235
[М+Н]+ найдено: 695.3230
Пример 169: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[3-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Стадия А: Метил 2-[3-(4-метилпиперазин-1-ил)фенил]ацетат
В толстостенную пробирку добавляют метил 2-(3-бромфенил)ацетат (250 мг, 1.09 ммоль), 1-метилпиперазин (0.18 мл, 1.64 ммоль), ди-трет-бутил(2-фенилфенил)фосфан, (32.57 мг, 0.11 ммоль) и ортофосфат калия (463.32 мг, 2.18 ммоль), которые затем суспендируют в толуоле (5 мл) и дегазируют путем барботирования азота в течение 5 мин. Затем к реакционной смеси добавляют трис(дибензилиденацетон)дипалладий(0) (49.97 мг, 0.05 ммоль) и перемешивают при 90°C в атмосфере азота в течение прибл. 16 ч. Реакционную смесь фильтруют, твердые вещества промывают дихлорметаном, и фильтрат концентрируют в вакууме, и затем загружают в дихлорметане на предварительно набитую 10 г силикагелевую колонку и очищают с помощью колоночной хроматографии в градиенте дихлорметан - 5% метанол в дихлорметане.
ЖХ/МС (C14H20N2O2) 249 [М+Н]+; RT 1.56 (Метод В)
Стадия В: 2-[3-(4-Метилпиперазин-1-ил)фенил]ацетат натрия
К раствору продукта из Стадии A (39.3 мг, 0.16 ммоль) в метаноле (5 мл) добавляют гидроксид натрия (2 М, 0.16 мл, 0.32 ммоль) и реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь концентрируют в вакууме и растирают с диэтиловым эфиром с получением целевого продукта.
ЖХ/МС (C13H18N2O2) 235 [М+Н]+; RT 0.69 (Метод В)
Стадия C: N-[4-(Бензилокси)фенил]-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[3-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта из Синтеза 6ab (50 мг, 0.06 ммоль) в дихлорметане (3 мл) добавляют HBTU (24.35 мг, 0.06 ммоль) и триэтиламин (26.79 мкл, 0.19 ммоль) и, далее, продукт из Стадии B (24.68 мг, 0.1 ммоль), и реакционную смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь разбавляют дихлорметаном и промывают водой и солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме, и загружают в дихлорметане на предварительно набитую 5 г силикагелевую колонку и очищают с помощью колоночной хроматографии в градиенте дихлорметан - 5% метанол в дихлорметане.
ЖХ/МС (C56H60N6O4) 881 [М+Н]+; RT 2.52 (Метод В)
Стадия D: N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[3-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
К раствору продукта из Стадии C (45 мг, 0.05 ммоль) в этаноле (10 мл) добавляют 10% Pd/C (каталитическое количество), и перемешивают в атмосфере водорода при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь фильтруют через картридж с целитом, который промывают метанолом, и фильтрат концентрируют в вакууме, и загружают в дихлорметане на предварительно набитую 5 г силикагелевую колонку и очищают с помощью колоночной хроматографии в градиенте дихлорметан - 5% метанол в дихлорметане.
ЖХ/МС (C49H54N6O4) 791 [М+Н]+; RT 2.21 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C49H54N6O4
[М+2Н]2+ рассчитано: 396.2176
[М+2Н]2+ найдено: 396.2176
Пример 170: 5-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-N-метил-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-2-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: С33H37N5O4
[М+Н]+ рассчитано: 592.2926
[М+Н]+ найдено: 592.2925
Пример 171: N-(4-Гидроксифенил)-N-метил-3-{6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(фенилсульфанил)ацетил]-2,3-дигидро-1H-изоиндол-5-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H42N4O4S
[М+Н]+ рассчитано: 711.3007
[М+Н]+ найдено: 711.3001
Пример 172: 5-{2-[2-(2H-1,3-Бензодиоксол-5-ил)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H40N4O6
[М+Н]+ рассчитано: 697.3028
[М+Н]+ найдено: 697.2994
Пример 173: 5-(2-[(2S)-2-Амино-2-фенилацетил]-6-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2,3-дигидро-1H-изоиндол-5-ил)-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H41N5O4
[М+Н]+ рассчитано: 668.3239
[М+Н]+ найдено: 668.3238
Пример 174; 5-(2-[(2R)-2-Амино-2-фенилацетил]-6-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2,3-дигидро-1H-изоиндол-5-ил)-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H41N5O4
[М+Н]+ рассчитано: 668.3239
[М+Н]+ найдено: 668.3247
Пример 175; N-(4-Гидроксифенил)-5-(2-[(2R)-2-гидрокси-2-фенилацетил]-6-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2,3-дигидро-1N-изоиндол-5-ил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H40N4O5
[М+Н]+ рассчитано: 669.3079
[М+Н]+ найдено: 669.3063
Пример 176: 5-{2-[2-(1-Пиперидил)ацетил]-6-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2,3-дигидро-1H-изоиндол-5-ил}-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C40H45N5O4
[М+Н]+ рассчитано: 660.3552
[М+Н]+ найдено: 660.3512
Пример 177: 5-[2-[2-(1,3-Бензодиоксол-5-ил)ацетил]-6-[(3R)-3-метил-3,4-дигидро-1H-изохйнолин-2-карбонил]изоиндолин-5-ил]-N,1,2-триметил-N-(1-метилпирроло[2,3-b]пиридин-5-ил)пиррол-3-карбоксамид
Пример 178: 5-[2-[2-(1,3-Бензодиоксол-5-ил)ацетил]-6-[(3R)-3-метил-3,4-дигидро-1H-изохинолин-2-карбонил]изоиндолин-5-ил]-N-(4-гидроксифенил)-1,2-диметил-N-(1-метил-1H-пиразол-4-ил)пиррол-3-карбоксамид
Пример 179: N-(4-Гидроксифенил)-N,1,2-триметил-5-[6-[(3R)-3-метил-3,4-дигидро-1H-изохинолин-2-карбонил]-2-[(2R)-2-фенилпропаноил]изоиндолин-5-ил]пиррол-3-карбоксамид
Пример 180: N-(4-Гидроксифенил)-N,1,2-триметил-5-[6-[(3R)-3-метил-3,4-дигидро-1N-изохинолин-2-карбонил]-2-[2-(3-тиенил)ацетил]изоиндолин-5-ил]пиррол-3-карбоксамид
Пример 181: N-(4-Гидроксифенил)-N,1,2-триметил-5-[6[(3R)-3-метил-3,4-дигидро-1H-изохинолин-2-карбонил]-2-[(2S)-2-фенилпропаноил]изоиндолин-5-ил]пиррол-3-карбоксамид
Пример 182: 5-[2-[3-(4-Хлорфенокси)пропаноил]-6-[(3R)-3-метил-3,4-дигидро-1H-изохинолин-2-карбонил]изоиндолин-5-ил]-N-(4-гидроксифенил)-N,1,2-триметилпиррол-3-карбоксамид
Пример 183: N-(4-Гидроксифенил)-N,1,2-триметил-5-[6-[(3R)-3-метил-3,4-дигидро-1H-изохинолин-2-карбонил]-2-(2-пиррол-1-илацетил)изоиндолин-5-ил]пиррол-3-карбоксамид
Пример 184: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1Н)-ил]карбонил}-3,4-дигидроизохинолин-2(1Н)-карбоксилат
Пример 185: Фенил 6-{4-[этил(4-гидроксифенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на продукт из Синтеза 6f, и с заменой фенилацетилхлорида на Стадии A на фенилхлорформиат.
ЖХ/МС (C46H49N5O6) 768 [М+Н]+; RT 1.21 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O6
[М+Н]+ рассчитано: 768.3756
[М+Н]+ найдено: 768.3741
Пример 186: Фенил 6-{4-[(4-гидроксифенил)(пропил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 777 с заменой продукта из Синтеза 6bе на Стадии A на продукт из Синтеза 6g, и с заменой фенилацетилхлорида на Стадии A на фенилхлорформиат.
ЖХ/МС (C47H51N5O6) 782 [М+Н]+; RT 1.24 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H51N5O6
[М+Н]+ рассчитано: 782.3912
[М+Н]+ найдено: 782.3927
Пример.187: Фенил 6-{4-[бутил(4-гидроксифенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 777 с заменой продукта из Синтеза 6bе на Стадии A на продукт из Синтеза 6h, и с заменой фенилацетилхлорида на Стадии A на фенилхлорформиат.
ЖХ/МС (C48H53N5O6) 796 [М+Н]+; RT 1.29 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H53N5O6
[М+2Н]2+ рассчитано: 398.7071
[М+2Н]2+ найдено: 398.7075
Пример 188: Фенил 6-{4-[(4-гидроксифенил)(фенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 189: Фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 190: Фенил 6-{4-[этил(фенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 191: Фенил 6-{1,5-диметил-4-[фенил(пропил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 192: Фенил 6-{4-[бутил(фенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 193: Фенил 6-[4-(дифенилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 194: Фенил 6-{4-[бутил(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 195: Фенил 6-{4-[бутил(этил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 196: Фенил 6-{4-[бутил(пропил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 197: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 165 с заменой фенилацетилхлорида на фенилхлорформиат.
ЖХ/MG (C46H57N5O5) 760 [М+Н]+; RT 1.40 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H57N5O5
[М+Н]+ рассчитано: 760.4432
[М+Н]+ найдено: 760.4449
Пример 198: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 199: Фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-днгидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 200: Фенил 6-{4-[(4-гидроксифенил)(фенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 201: Фенил 6-[4-(дифенилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 202: Фенил 6-{4-[бутил(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 203: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 204: Фенил 7-(3,4-дигидроизохинолин-2(1H)-илкарбонил)-6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 205: Фенил 7-(3,4-дигидроизохинолин-2(1H)-илкарбонил)-6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 206; Фенил 7-(3,4-дигидроизохинолин-2(1H)-илкарбонил)-6-{4-[(4-гидроксифенил)(фенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 207: Фенил 7-(3,4-дигидроизохинолин-2(1H)-илкарбонил)-6-[4-(дифенилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 208: Фенил 6-{4-[бутил(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-(3,4-дигидроизохинолин-2(1H)-илкарбонил)-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 209: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-(3,4-дигидроизохинолин-2(1H)-илкарбонил)-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 210: Фенил 7-{[(3S)-3-(аминометил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 211: Фенил 7-[(3S)-3-[(диметиламино)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия А: Фенил 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-7-[3S}-3-[(диметилимино)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии A Примера 777 с заменой фенилацетилхлорида на фенилхлорформиат.
ЖХ/МС (C50H51N5O5) 802 [М+Н]+; RT 1.34 (Метод В)
Стадия В: Фенил 7-[(3S)-3-[(диметиламино)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии B Примера 777, но очистку осуществляют с помощью препаративной ЖХВР (Н2O-ТФУ/ацетонитрил; градиентное элюирование).
ЖХ/МС (C43H45N5O5) 712 [М+Н]+; RT 1.13 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H45N5O5
[М+Н]+ рассчитано: 712.3493
[М+Н]+ найдено: 712.3496
Пример 212: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(пирролидин-1-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 213: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(пиперидин-1-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 214: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия А: Фенил 6-(4-{14-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии A Примера 777 с заменой соединения из Синтеза 6bе на соединение из Синтеза 6bf, и с заменой фенилацетилхлорида на фенилхлорформиат.
ЖХ/МС (C53H56N6O5) 857 [М+Н]+; RT 1.34 (Метод В)
Стадия В: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии B Примера 777, но очистку осуществляют с помощью препаративной ЖХВР (H2O-ТФУ/ацетонитрил; градиентное элюирование).
ЖХ/МС (C46H50N6O5) 767 [М+Н]+; RT 1.14 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H50N6O5
[М+2Н]2+ рассчитано: 384.1994
[М+2Н]2+ найдено: 384.1995
Пример 215: Фенил 7-{[(3S)-3-[2-(диметиламино)этил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 216: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-7-[(3S)-3-[2-(морфолин-4-ил)этил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на продукт из Синтеза 6bс, и с заменой фенилацетилхлорида на Стадии A на фенилхлорформиат.
ЖХ/МС (C46H49N5O6) 768 [М+Н]+; RT 1.14 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O6
[М+Н]+ рассчитано: 768.3756
[М+Н]+ найдено: 768.3756
Пример 217: Фенил 7-{[(3S)-3-(аминометил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 218: Фенил 7-{[(3S)-3-[(диметиламино)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 219: Фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(пирролидин-1-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 220: Фенил 6-{1,5-диметил-4~[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(пиперидин-1-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 221: Фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 222: Фенил 7-{[(3S)-3-[2-(диметиламино)этил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 223: Фенил 6-{1,5-диметил-4-|метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-[2-(морфолин-4-ил)этил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 224: Фенил 7-{[(3S)-3-(аминометил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 225: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-[(диметиламино)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 226: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(пирролидин-1-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 227: фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(пиперидин-1-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 228: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 229: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-[2-(диметиламино)этил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 230: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-[2-(морфолин-4-ил)этил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 231: N-(4-Гидроксифенил)-N,1,2-триметил-5[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 232: N-Бутил-N-(4-гидроксифенил)-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 777 с заменой продукта из Синтеза 6bе на Стадии A на продукт из Синтеза 6h.
ЖХ/МС (C49H55N5O5) 794 [М+Н]+; RT 1.23 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C49H55N5O5
[М+2Н]2+ рассчитано: 397.7174
[М+2Н]2+ найдено: 397.7178
Пример 233: N-(4-Гидроксифенил)-1,2-диметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацегил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 234: N,1,2-Триметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 235: N-Бутил-1,2-диметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 236: 1,2-Диметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N,N-дифенил-1H-пиррол-3-карбоксамид
Пример 237: N-Бутил-N,1,2-триметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 238: N,N-Дибутил-1,2-диметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 239: N-(4-Гидроксифенил)-N,1,2-триметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 240: N,1,2-Триметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 241: N-(4-Гидроксифенил)-1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 242: 1,2-Диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N,N-дифенил-1H-пиррол-3-карбоксамид
Пример 243: N-Бутил-N,1,2-триметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 244: N,N-Дибутил-1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 245: 6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-N-фенил-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bа, и с заменой фенилацетилхлорида на бензилизоцианат.
ЖХ/МС (C45H48N6O5) 753 [М+Н]+; RT 1.14 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H48N6O5
[М+Н]+ рассчитано: 753.3740
[М+Н]+ найдено: 753.3759
Пример 246: 6-{4-[Бутил(4-гидроксифенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 247: 6-{4-[(4-Гидроксифенил)(фенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 248: 6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 249: 6-{4-[Бутил(фенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 250: 6-[4-(Дифенилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 251: 6-{4-[Бутил(метил)карбамоил]-1,5-диметил-1N-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 252: 6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 253: 6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-N-фенил-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bb, и с заменой фенилацетилхлорида на бензилизоцианат.
ЖХ/МС (C41H41N5O4) 668 [М+Н]+; RT 1.31 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H41N5O4
[М+Н]+ рассчитано: 668.3231
[М+Н]+ найдено: 668.3211
Пример 254: 6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 255: 6-{4-[(4-Гидроксифенил)(фенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 256: 6-[4-(Дифенилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 257: 6-{4-[Бутил(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 258: 6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 259: N-(4-Гидроксифенил)-N,1,2-триметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(2-фенилэтил)-1,2,3,4-гетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 260: Бензил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 261: N-(4-Гидроксифенил)-N,1,2-триметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(феноксиацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 262: N-(4-Гидроксифенил)-N,1,2-триметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-[2-оксо-2-(фениламино)этил]-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 263: 5-(2-Бензоил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 264: N-(4-Гидроксифенил)-N,1,2-триметил-5-(7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-[(2E)-3-фенилпроп-2-еноил]-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 265: N-(4-Гидроксифенил)-N,1,2-триметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(3-фенилпропаноил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 266: 6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-N-метил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 267: 6-{4-[Бутил(4-гидроксифенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-N-метил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 268: 6-{4-[(4-Гидроксифенил)(фенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-N-метил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 269: 6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-N-метил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 270: 6-{4-[Бутил(фенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-N-метил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроиз6хинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 271: 6-[4-(Дифенилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-N-метил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 272: 6-{4-[Бутил(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-N-метил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 273: 6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-N-метил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 274: 6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-N-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 275: 6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-N-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 276: 6-{4-[(4-Гидроксифенил)(фенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-N-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 277: 6-[4-(Дифенилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-N-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 278: 6-{4-[Бутил(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-N-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 279: 6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-N-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-N-фенил-3,4-дигидроизохинолин-2(1H)-карбоксамид
Пример 280: 5-[2-(Бензилсульфонил)-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1N-пиррол-3-карбоксамид
Пример 281: 5-[2-(Бензилсульфонил)-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 282: 5-[2-(Бензилсульфонил)-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-1,2-диметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 283: 5-[2-(Бензилсульфонил)-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,N-дибутил-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 284: 5-[2-(Бензилсульфонил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 285: 5-[2-(Бензилсульфонил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 286: 5-[2-(Бензилсульфонил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-4-гидроксифенил)-1,2-диметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 287: 5-[2-(Бензилсульфонил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,N-дибутил-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 288: N-(4-Гидроксифенил)-N,1,2-триметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфамоил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 289: N,1,2-Триметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфамоил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 290: N-(4-Гидроксифенил)-1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфамоил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 291: N,N-Дибутил-1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфамоил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 292: N-(4-Гидроксифенил)-N,1,2-триметил-5-(2-[метил(фенил)сульфамоил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 293: N,1,2-Триметил-5-(2-[метил(фенил)сульфамоил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-фенил-1H-пиррол-3-карбоксамид
Пример 294: N-(4-Гидроксифенил)-1,2-диметил-5-(2-[метил(фенил)сульфамоил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-фенил-1H-пиррол-3-карбоксамид
Пример 295: N,N-Дибутил-1,2-диметил-5-(2-[метил(фенил)сульфамоил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 296: N-(4-Гидроксифенил)-N,1,2-триметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-[метил(фенил)сульфамоил]-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 297: N,1,2-Триметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-[метил(фенил)сульфамоил]-1,2,3,4-тетрагидроизохинолин-6-ил)-N-фенил-1H-пиррол-3-карбоксамид
Пример 298: N-(4-Гидроксифенил)-1,2-диметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-[метил(фенил)сульфамоил]-1,2,3,4-тетрагидроизохинолин-6-ил)-N-фенил-1H-пиррол-3-карбоксамид
Пример 299: N,N-Дибутил-1,2-диметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-[метил(фенил)сульфамоил]-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 300: N-(4-Гидроксифенил)-N,1,2-триметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 301: N,1,2-Триметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 302: N-(4-Гидроксифенил)-1,2-диметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 303: N,N-Дибутил-1,2-диметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 304: N-(4-Гидроксифенил)-N,1,2-триметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 305: N,1,2-Триметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 306: N-(4-Гидроксифенил)-1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 307: N,N-Дибутил-1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилсульфонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 308: Фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 309: Фенил 6-{1-[метил(фенил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 310: Фенил 6-{1-[(4-гидроксифенил)(фенил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 311: Фенил 6-[1-(дифенилкарбамоил)-5,6,7,8-тетрагидроиндолизин-3-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 312: Фенил 6-{1-[бутил(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 313: Фенил 6-[1-(дибутилкарбамоил)-5,6,7,8-тетрагидроиндолизин-3-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 314: Фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 315: Фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]индолизин-3-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 316: Фенил 6-{1-[метил(фенил)карбамоил]индолизин-3-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 317: Фенил 6-{1-[(4-гидроксифенил)(фенил)карбамоил]индолизин-3-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 318: Фенил 6-[1-(дифенилкарбамоил)индолизин-3-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 319: Фенил 6-{1-[бутил(метил)карбамоил]индолизин-3-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 320: Фенил 6-[1-(дибутилкарбамоил)индолизин-3-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 321: Фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]индолизин-3-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 322: Фенил 6-{3-[(4-гидроксифенил)(метил)карбамоил]-1H-индол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 323: Фенил 6-{3-[метил(фенил)карбамоил]-1H-индол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1Н)-ил]карбонил}-3,4-дигидроизохинолин-2(1Н)-карбоксилат
Пример 324: Фенил 6-{3-[(4-гидроксифенил)(фенил)карбамоил]-1H-индол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 325: Фенил 6-[3-(дифенилкарбамоил)-1H-индол-1-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 326: Фенил 6-{3-[бутил(метил)карбамоил]-1N-индол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 327: Фенил 6-[3-(дибутилкарбамоил)-1H-индол-1-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 328: Фенил 6-{3-[(4-гидроксифенил)(метил)карбамоил]-1H-индол-1-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 329: Фенил 6-{3-[(4-гидроксифенил)(метил)карбамоил]-1H-индазол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 330: Фенил 6-{3-[метил(фенил)карбамоил]-1H-индазол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 331: Фенил 6-{3-[(4-гидроксифенил)(фенил)карбамоил]-1H-индазол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 332: Фенил 6-[3-(дифенилкарбамоил)-1H-индазол-1-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 333: Фенил 6-{3-[бутил(метил)карбамоил]-1H-индазол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 334: Фенил 6-[3-(дибутилкарбамоил)-1H-индазол-1-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 335: Фенил 6-{3-[(4-гидроксифенил)(метил)карбамоил]-1H-индазол-1-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 336: Фенил 6-{4-хлор-3-[(4-гидроксифенил)(метил)карбамоил]-5-метил-1H-пиразол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 337: Фенил 6-{4-хлор-5-метил-3-[метил(фенил)карбамоил]-1H-индол-1-ил}-7-{[(3R)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 338: Фенил 6-{4-хлор-3-[(4-гидроксифенил)(фенил)карбамоил]-5-метил-1H-пиразол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 339: Фенил 6-[4-хлор-3-(дифенилкарбамоил)-5-метил-1H-пиразол-1-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 340: Фенил 6-{3-[бутил(метил)карбамоил]-4-хлор-5-метил-1H-пиразол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 341: Фенил 6-[4-хлор-3-(дибутилкарбамоил)-5-метил-1H-пиразол-1-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 342: Фенил 6-{4-хлор-3-[(4-гидроксифенил)(метил)карбамоил]-5-метил-1H-пиразол-1-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 343: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-2,3-диметил-1H-пиррол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 344: Фенил 6-{2,3-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 345: Фенил 6-{4-[(4-гидроксифенил)(фенил)карбамоил]-2,3-диметил-1H-пиррол-1-ил}-7-{[(3S)-3-(морфолин-4-илметйл)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 346: Фенил 6-[4-(дифенилкарбамоил)-2,3-диметил-1H-пиррол-1-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 347: Фенил 6-{4-[бутил(метил)карбамоил]-2,3-диметил-1H-пиррол-1-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 348: Фенил 6-[4-(дибутилкарбамоил)-2,3-диметил-1H-пиррол-1-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 349: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-2,3-диметил-1H-пиррол-1-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 350: Фенил 6-{2-[(4-гидроксифенил)(метил)карбамоил]-5-метил-1,3-тиазол-4-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 351: Фенил 6-{5-метил-2-[метил(фенил)карбамоил]-1,3-тиазол-4-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 352: Фенил 6-{2-[(4-гидроксифенил)(фенил)карбамоил]-5-метил-1,3-тиазол-4-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 353: Фенил 6-[2-(дифенилкарбамоил)-5-метил-1,3-тиазол-4-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 354: Фенил 6-{2-[бутил(метил)карбамоил]-5-метил-13-тиазол-4-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 355: Фенил 6-[2-(дибутилкарбамоил)-5-метил-1,3-тиазол-4-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 356: Фенил 6-{2-[(4-гидроксифенил)(метил)карбамоил]-5-метил-1,3-тиазол-4-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 357: Фенил 5-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-6-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,3-дигидро-2H-изоиндол-2-карбоксилат
Пример 358: Фенил 7-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-8-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,3,4,5-тетрагидро-2H-2-бензазепин-2-карбоксилат
Пример 359: Фенил 7-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-8-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,4,5-тетрагидро-3H-3-бензазепин-3-карбоксилат
Пример 360: N-(4-Гидроксифенил)-N,1,2-триметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1-оксо-2-(2-фенилэтил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 361: N-(4-Гидроксифенил)-N,1,2-триметил-5-[6-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1-оксо-2-(2-фенилэтил)-2,3-Дигидро-1H-изоиндол-5-ил]-1H-пиррол-3-карбоксамид
Пример 362: Фенил 1,1-дифтор-6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-5-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,3-дигидро-2H-изоиндол-2-карбоксилат
Пример 363: Фенил 1,1,3,3-тетрафтор-5-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-6-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,3-дигидро-2H-изоиндол-2-карбоксилат
Пример 364: 5-[3,3-Дифтор-6-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1-оксо-2-(2-фенилэтил)-2,3-дигидро-1H-изоиндол-5-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 365: Фенил 6-(4-{[2-(диметиламино)этил](4-гидроксифенил)карбамоил}-1,5-диметил-1H-пиррол-2-ил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 366: Фенил 6-(4-{(4-гидроксифенил)[2-(морфолин-4-ил)этил]карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 367: N-[2-(Диметиламино)этил]-N-(4-гидроксифенил)-1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 368: N-(4-Гидроксифенил)-1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-[2-(морфолин-4-ил)этил]-1H-пиррол-3-карбоксамид
Пример 369: Фенил 6-(4-{[2-(диметиламино)этил](фенил)карбамоил}-1,5-диметил-1H-пиррол-2-ил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 370: Фенил 6-(1,5-диметил-4-{[2-(морфолин-4-ил)этил](фенил)карбамоил}-1N-пиррол-2-ил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 371: N-[2-(Диметиламино)этил]-1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 372: 1,2-Диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-[2-(морфолин-4-ил)этил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 373: Фенил 6-(4-{бутил[2-(диметиламино)этил]карбамоил}-1,5-диметил-1H-пиррол-2-ил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 374: Фенил 6-(4-{бутил[2-(морфолин-4-ил)этил]карбамоил}-1,5-диметил-1H-пиррол-2-ил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 375: N-Бутил-N-[2-(диметиламино)этил]-1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 376: N-Бутил-1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1Н)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-[2-(морфолин-4-ил)этил]-1H-пиррол-3-карбоксамид
Пример 377: Фенил 6-{1-[2-(диметиламино)этил]-4-[(4-гидроксифенил)(метил)карбамоил]-5-метил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 378: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-5-метил-1-[2-(морфолин-4-ил)этил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 379: 1-[2-(Диметиламино)этил]-N-(4-гидроксифенил)-N,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 380: N-(4-Гидроксифенил)-N,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1-[2-(морфолин-4-ил)этил]-1H-пиррол-3-карбоксамид
Пример 381: Фенил 6-{1-[2-(диметиламино)этил]-5-метил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 382: Фенил 7-{[(3R)-3-метил-3,4-ДИГидроизохинолин-2(1H)-ил]карбонил}-6-{5-метил-4-[метил(фенил)карбамоил]-1-[2-(морфолин-4-ил)этил]-1H-пиррол-2-ил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 383: 1-[2-(Диметиламино)этил]-N,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 384: N,2-Диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1-[2-(морфолин-4-ил)этил]-N-фенил-1H-пиррол-3-карбоксамид
Пример 385: Фенил 6-{4-(дибутилкарбамоил)-1-[2-(диметиламино)этил]-5-метил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 386: Фенил 6-{4-(дибутилкарбамоил)-5-метил-1-[2-(морфолин-4-ил)этил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 387: N,N-Дибутил-1-[2-(диметиламино)этил]-2-метил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-карбоксамид
Пример 388: N,N-Дибутил-2-метил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1-[2-(морфолин-4-ил)этил]-1H-пиррол-3-карбоксамид
Пример 389: 2-(4-Метилпиперазин-1-ил)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1N-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 390: 2-{[2-(Диметиламино)этил](метил)амино}фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 391: 2-{[2-(Диметиламино)этил]амино}фенил 6-{4-|(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 392: 2-[2-(Диметиламино)этокси]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 709 с заменой продукта из Синтеза 6bа на Стадии A на продукт из Синтеза 6bb, и с заменой бензил 3-гидроксибензоата из Стадии B на 3-[2-(диметиламино)этокси]фенол.
ЖХ/МС (C45H49N5O6) 754 [М-Н]-; RT 2.27 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H49N5O6
[М+2Н]2+ рассчитано: 378.6914
[М+2Н]2+ найдено: 378.6926
Пример 393: 2-[2-(Диметиламино)этил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 394: 2-[(Диметиламино)метил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 395: 2-[3-(Диметиламино)проп-1-ин-1-ил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 396: N-(4-Гидроксифенил)-N,1,2-триметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-{[2-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 397: 5-(2-[(2-{[2-(Диметиламино)этил](метил)амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 398: 5-(2-[(2-{[2-(Диметиламино)этил]амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 399: 5-[2-({2-[2-(Диметиламино)этокси]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 400: 5-[2-({2-[2-(Диметиламино)этил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 401: 5-[2-({2-[(Диметиламино)метил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 402: 5-[2-({2-[3-(Диметиламино)проп-1-ин-ил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 403: 2-(4-Метилпиперазин-1-ил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 404: 2-{[2-(Диметиламино)этил](метил)амино}фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 405: 2-{[2-(Диметиламино)этил]амино}фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 406: 2-[2-(Диметиламино)этокси]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 407: 2-[2-(Диметиламино)этил]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 408: 2-[(Диметиламино)метил]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 409: 2-[3-(Диметиламино)проп-1-ин-1-ил]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 410: N,1,2-Триметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-{[2-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-фенил-1H-пиррол-3-карбоксамид
Пример 411: 5-(2-[(2-{[2-(Диметиламино)этил](метил)амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 412: 5-(2-[(2-{[2-(Диметиламино)этил]амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 413: 5-[2-({2-[2-(Диметиламино)этокси]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 414: 5-|2-({2-[2-(Диметиламино)этил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1N-пиррол-3-карбоксамид
Пример 415: 5-[2-({2-[(Диметиламино)метил]фенил}ацетил)-7-{[(3R)-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 416: 5-[2-({2-[3-(Диметиламино)проп-1-ин-1-ил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил 1H-пиррол-3-карбоксамид
Пример 417: 2-(4-Метилпиперазин-1-ил)фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 418: 2-{[2-(Диметиламино)этил](метил)амино}фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 419: 2-{[2-(Диметиламино)этил]амино}фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 420: 2-[2-(Диметиламино)этокси]фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 421: 2-[2-(Диметиламино)этил]фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 422: 2-[(Диметиламино)метил]фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 423: 2-[3-(Диметиламино)проп-1-ин-1-ил]фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 424: N,N-Дибутил-1,2-диметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-{[2-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 425: N,N-Дибутил-5-(2-[(2-{[2-(диметиламино)этил](метил)амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 426: N,N-Дибутил-5-(2-[(2-{[2-(диметиламино)этил]амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 427: N,N-Дибутил-5-[2-({2-[2-(диметиламино)этокси]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 428: N,N-Дибутил-5-[2-({2-[2-(диметиламино)этил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 429: N,N-Дибутил-5-[2-({2-[(диметиламино)метил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 430: N,N-Дибутил-5-[2-({2-[3-(диметиламино)проп-1-ин-1-ил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 431: 3-(4-Метилпиперазин-1-ил)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 432: 3-{[2-(Диметиламино)этил](метил)амино}фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 433: 3-{[2-(Диметиламино)этил]амино}фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 434: 3-[2-(Диметиламино)этокси]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 709 с заменой продукта из Синтеза 6bа на Стадии A на продукт из Синтеза 6bb, и с заменой бензил 3-гидроксибензоата из Стадии B на 3-[2-(диметиламино)этокси]фенол.
ЖХ/МС (C45H49N5O6) 754 [М-Н]-; RT 2.24 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H49N5O6
[М+2Н]2+ рассчитано: 378.6914
[М+2Н]2+ найдено: 378.6918
Пример 435: 3-[2-(Диметиламино)этил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 436: 3-[(Диметиламино)метил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 437: 3-[3-(Диметиламино)проп-1-ин-1-ил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 438: N-(4-Гидроксифенил)-N,1,2-триметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-{[3-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 439: 5-(2-[(3-{[2-(Диметиламино)этил](метил)амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 440: 5-(2-[(3-{[2-(Диметиламино)этил]амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 441: 5-[2-({3-[2-(Диметиламино)этокси]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 442: 5-[2-({3-[2-(Диметиламино)этил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 443: 5-[2-({3-[(Диметиламино)метил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидрошохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 444: 5-[2-({3-[3-(Диметиламино)проп-1-ин-1-ил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 445: 3-(4-Метилпиперазин-1-ил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 446: 3-{[2-(Диметиламино)этил](метил)амино}фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(31?)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 786 с заменой 4-гидроксибензонитрила на Стадии B на 3-{[2-(диметиламино)этил](метил)амино}фенол.
ЖХ/МС (C46H52N6O4) нет ионизации; RT 2.44 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H52N6O4
[М+2Н]2+ рассчитано: 377.2098
[М+2Н]2+ найдено: 377.2100
Пример 447: 3-{[2-(Диметиламино)этил]амино}фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 448: 3-[2-(Диметиламино)этокси] фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидройзохинолин-2-карбоксилат
Методика соответствует методике Примера 786 с заменой 4-гидроксибензонитрила на Стадии B на 3-[2-(диметиламино)этокси]фенол.
ЖХ/МС (C45H49N5O5) 740 [М+Н]+; RT 1.20 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H49N5O5
[М+2Н]2+ рассчитано: 370.6940
[М+2Н]2+ найдено: 370.6954
Пример 449: 3-[2-(Диметиламино)этил]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 450: 3-[(Диметиламино)метил]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 451: 3-[3-(Диметиламино)проп-1-ин-1-ил]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 452: N,1,2-Триметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-{[3-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-фенил-1H-пиррол-3-карбоксамид
Пример 453: 5-(2-[(3-{[2-(Диметиламино)этил](метил)амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 454: 5-(2-[(3-{[2-(Диметиламино)этил]амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 455: 5-[2-({3-[2-(Диметиламино)этокси]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 456: 5-[2-({3-[2-(Диметиламино)этил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 457: 5-[2-({3-[(Диметиламино)метил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 458: 5-[2-({3-[3-(Диметиламино)проп-1-ин-1-ил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 459: 3-(4-Метилпиперазин-1-ил)фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 460: 3-{[2-(Диметиламино)этил](метил)амино}фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 461: 3-{[2-(Диметиламино)этил]амино}фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 462: 3-[2-(Диметиламино)этокси]фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 463: 3-[2-(Диметиламино)этил]фенил 6-14-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 464: 3-[(Диметиламино)метил]фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 465: 3-[3-(Диметиламино)проп-1-ин-1-ил]фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3.1?)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 466: N,N-Дибутил-1,2-диметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-{[3-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 467: N,N-Дибутил-5-(2-[(3-{[2-(диметиламино)этил](метил)амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 468: N,N-Дибутил-5-(2-[(3-{[2-(диметиламино)этил]амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 469: N,N-Дибутил-5-[2-({3-[2-(диметиламино)этокси] фенил }ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 470: N,N-Дибутил-5-[2-({3-[2-(диметиламино)этил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 471: N,N-Дибутил-5-[2-({3-[(диметиламино)метил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 472: N,N-Дибутил-5-[2-({3-[3-(диметиламино)проп-1-ин-1-ил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 473: 4-(4-Метилпиперазин-1-ил)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 474: 4-{[2-(Диметиламино)этил](метил)амино}фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 709 с заменой продукта из Синтеза 6bа на Стадии A на продукт из Синтеза 6bb, и с заменой бензил 3-гидроксибензоата из Стадии B на 4-{[2-(диметиламино)этил](метил)амино}фенол.
ЖХ/МС (C46H52N6O5) 767 [М-Н]-; RT 2.26 (Метод А)
Пример 475: 4-{[2-(Диметиламино)этил]амино}фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 476: 4-[2-(Диметиламино)этокси]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 709 с заменой продукта из Синтеза 6bа на Стадии A на продукт из Синтеза 6bb, и с заменой бензил 3-гидроксибензоата из Стадии B на 4-[2-(диметиламино)этокси]фенол.
ЖХ/МС (C45H49N5O6) 754 [М-Н]-; RT 2.21 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H49N5O6
[М+2Н]2+ рассчитано: 378.6914
[М+2Н]2+ найдено: 378.6926
Пример 477: 4-|2-(Диметиламино)этил]фенил 6-(4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 478: 4-[(Диметиламино)метил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 479: 4-[3-(Диметиламино)проп-1-ин-1-ил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 480; N-(4-Гидроксифенил)-]-N,1,2-триметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-{[4-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 481: 5-(2-[(4-{[2-(Диметиламино)этил](метил)амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 482: 5-(2-[(4-{[2-(Диметиламино)этил]амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 483: 5-[2-({4-[2-(Диметиламино)этокси]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 484: 5-[2-({4-[2-(Диметиламино)этил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 485: 5-[2-({4-[(Диметиламино)метил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 486: 5-{2-({4-[3-(Диметиламино)проп-1-ин-1-ил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 487: 4-(4-Метилпиперазин-1-ил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 488: 4-{[2-(Диметиламино)этил](метил)амино}фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия А: 6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилхлорид
Методика соответствует методике Стадии A Примера 573 с заменой продукта из Синтеза 6bа на продукт из Синтеза 6cb.
ЖХ/МС (C35H35ClN4O3) 595 [М+Н]+; RT 2.73 (Метод А)
Стадия В: 4-{[2-(Диметиламино)этил](метил)амино}фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору карбамоилхлорида, полученного на Стадии A, (55 мг, 0.09 ммоль) в ацетонитриле (5 мл) добавляют карбонат калия (128 мг, 0.92 ммоль) и 4-(диметиламино)этил](метил)амино}фенол (22 мг, 0.11 ммоль), и реакционную смесь перемешивают при 60°C в течение прибл. 16 ч. Реакционной смеси дают охладиться до температуры окружающей среды, разбавляют дихлорметаном и промывают водой. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (силикагель; дихлорметан - 10% метанол/дихлорметан) дает целевой продукт в виде кремового твердого вещества.
ЖХ/МС (C46H52N6O4) 753 [М+Н]+; RT 2.42 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H52N6O4
[М+2Н]2+ рассчитано: 377.2098
[М+2Н]2+ найдено: 377.2102
Пример 489: 4-{[2-(Диметиламино)этил]амино}фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия А: 6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-7-1(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилхлорид
Методика соответствует методике Стадии A Примера 573 с заменой продукта из Синтеза 6bа на продукт из Синтеза 6cb.
ЖХ/МС (С35Н35СlH4O3) 595 [М+Н]+; RT 2.73 (Метод А)
Стадия В: 4-{[(трет-Бутокси)карбонил][2-(диметиламино)этил]амино}фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Стадии B Примера 573 с заменой продукта Стадии A Примера 573 на продукт Стадии A Примера 489, и с заменой 3,4-дихлорфенола на трет-бутил N-[2-(диметиламино)этил]-N-(4-гидроксифенил)карбамат.
ЖХ/МС (C50H58N6O6) нет ионизации; RT 2.54 (Метод А)
Стадия С: 4-{[2-(Диметиламино)этил]амино}фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору продукта, полученного на Стадии B, (31 мг, 0.04 ммоль, 1 экв.) в дихлорметане (5 мл) добавляют трифторуксусную кислоту (0.5 мл) и смесь перемешивают при температуре окружающей среды в течение прибл. 4 ч. Реакционную смесь разбавляют водой и подщелачивают 2М водным гидроксидом натрия. Фазы разделяют и водную фазу экстрагируют дихлорметаном. Объединенные органические фазы сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (10 г, силикагель; дихлорметан - 10% метанол в дихлорметане) дает целевой продукт в виде белого порошка.
ЖХ/МС (C45H50N6O4) нет ионизации; RT 2.38 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H50N6O4
[М+2Н]2+ рассчитано: 370.2020
[М+2Н]2+ найдено: 370.2038
Пример 490: 4-[2-(Диметиламино)этокси]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1N-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 491: 4-[2-(Диметиламино)этил]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 492: 4-[(Диметиламино)метил]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 493: 4-[3-(Диметиламино)проп-1-ин-1-ил]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 494: N,1,2-Триметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-{[4-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-фенил-1H-пиррол-3-карбоксамид
Пример 495: 5-(2-[(4-{[2-(Диметиламино)этил](метил)амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 496: 5-(2-[(4-{[2-(Диметиламино)этил]амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 497: 5-[2-({4-[2-(Диметиламино)этокси]фенил}ацетил)-7-{[(3R)-3-метид-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 498: 5-[2-({4-[2-(Диметиламино)этил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 499: 5-[2-({4-[(Диметиламино)метил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 500: 5-[2-({4-[3-(Диметиламино)проп-1-ин-1-ил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 501: 4-(4-Метилпиперазин-1-ил)фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 502: 4-{[2-(Диметиламино)этил](метил)амино}фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 503: 4-{[2-(Диметиламино)этил]амино}фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 504: 4-[2-(Диметиламино)этокси]фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 505: 4-[2-(Диметиламино)этил]фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 506: 4-[(Диметиламино)метил]фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 507: 4-[3-(Диметиламино)проп-1-ин-1-ил]фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 508: N,N-Дибутил-1,2-диметил-5-(7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-{[4-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1H-пиррол-3-карбоксамид
Пример 509: N,N-Дибутил-5-(2-[(4-{[2-(диметиламино)этил](метил)амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 510: N,N-Дибутил-5-(2-[(4-{[2-(диметиламино)этил]амино}фенил)ацетил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 511: N,N-Дибутил-5-[2-({4-[2-(диметиламино)этокси]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 512: N,N-Дибутил-5-[2-({4-[2-(диметиламино)этил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 513: N,N-Дибутил-5-[2-({4-[(диметиламино)метил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 514: N,N-Дибутил-5-[2-({4-[3-(диметиламино)проп-1-ин-1-ил]фенил}ацетил)-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 515: Динатрий 4-[({1,2-диметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(феноксикарбонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-ил}карбонил)(метил)амино]фенилфосфат
Пример 516: Динатрий 4-[({1,2-диметил-5-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-ил}карбонил)(метил)амино]фенилфосфат
Пример 517: Динатрий 4-[метил({3-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(феноксикарбонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-5,6,7,8-тетрагидроиндолизин-1-ил}карбонил)амино]фенилфосфат
Пример 518: Динатрий 4-[метил({3-[7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-5,6,7,8-тетрагидроиндолизин-1-ил}карбонил)амино]фенилфосфат.
Пример 519: Динатрий 4-[({1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(феноксикарбонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-ил}карбонил)(метил)амино]фенилфосфат
Пример 520: Динатрий 4-[({1,2-диметил-5-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1H-пиррол-3-ил}карбонил)(метил)амино]фенилфосфат
Пример 521: Динатрий 4-[метил({3-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(феноксикарбонил)-1,2,3,4-тетрагидроизохинолин-6-ил]-5,6,7,8-тетрагидроиндолизин-1-ил}карбонил)амино]фенилфосфат
Пример 522: Динатрий 4-[метил({3-[7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-5,6,7,8-тетрагидроиндолизин-1-ил}карбонил)амино]фенилфосфат
Пример 523: Фенил 6-{1-этил-4-[(4-гидроксифенил)(метил)карбамоил]-5-метил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 524: Фенил 6-{1-(2-гидроксиэтил)-4-[(4-гидроксифенил)(метил)карбамоил]-5-метил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 525: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1-(2-метоксиэтил)-5-метил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 526: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-5-метил-1-(2,2,2-трифторэтил)-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 527: Фенил 6-{1-этил-5-метил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 528: Фенил 6-{1-(2-гидроксиэтил)-5-метил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 529: Фенил 6-{1-(2-метоксиэтил)-5-метил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 530: Фенил 6-{5-метил-4-[метил(фенил)карбамоил]-1-(2,2,2-трифторэтил)-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 531: Фенил 6-[4-(дибутилкарбамоил)-1-этил-5-метил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 532: Фенил 6-[4-(дибутилкарбамоил)-1-(2-гидроксиэтил)-5-метил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 533: Фенил 6-[4-(дибутилкарбамоил)-1-(2-метоксиэтил)-5-метил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 534: Фенил 6-[4-(дибутилкарбамоил)-5-метил-1-(2,2,2-трифторэтил)-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 535: 2-Метилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 536: 3-Метилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 537: 4-Метилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 538: 2-Хлорфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 539: 3-Хлорфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 540: 4-Хлорфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 541: 2-Гидроксифенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1/7)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 542: 3-Гидроксифенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 543: 4-Гидроксифенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1N-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 544: 2-Метоксифенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 545: 3-Метоксифенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 546: 4-Метоксифенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 547: 2-(Метиламино)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 548: 3-(Метиламино)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 549: 4-(Метиламино)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 550: 2-(Диметиламино)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 551: 3-(Диметиламино)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 552: 4-(Диметиламино)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 553: 2-(Ацетиламино)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 554: 3-(Ацетиламино)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 555: 4-(Ацетиламино)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 556: 2-(Трифторметил)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 557: 3-(Трифторметил)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 558: 4-(Трифторметил)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 559: 2-Цианофенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 560: 3-Цианофенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 573 с заменой 3,4-дихлорфенола на Стадии B на 3-гидроксибензонитрил.
ЖХ/МС (C46H46N6O6) 779 [М+Н]+; RT 1.14 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H46N6O6
[М+Н]+ рассчитано: 779.3552
[М+Н]+ найдено: 779.3515
Пример 561: 4-Цианофенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 562: 2-Этинилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 563: 3-Этинилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 564: 4-Этинилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору продукта, полученного в Примере 784, (53 мг, 0.06 ммоль, 1 экв.) и триэтиламина (10 мкл, 0.1 ммоль) в ТГФ (1 мл) добавляют дихлорид бис(трифенилфосфин)палладия(II) (5 мг, 0.01 ммоль, 0.12 экв.), йодид меди(I) (0.7 мг, 3.84 мкмоль), и триметилсилилацетилен (36 мкл, 0.26 ммоль, 4 экв.) и смесь нагревают при 60°C в течение прибл. 16 ч. Реакционной смеси дают охладиться до температуры окружающей среды, затем упаривают и очищают с помощью препаративной ЖХВР (H2O-ТФУ/ацетонитрил; градиентное элюирование) с получением целевого продукта.
ЖХ/МС (C47H47N5O6) 778 [М+Н]+; RT 1.24 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H47N5O6
[М+Н]+ рассчитано: 778.3599
[М+Н]+ найдено: 778.3635
Пример 565: 2,3-Дихлорфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(H)-карбоксилат
Пример 566: Нафталин-1-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 567: 1H-Индол-7-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 568: 1-Метил-1H-индол-7-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 569: 1H-Индол-4-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 570: 1-Метил-1H-индол-4-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 571: 1H-Пирроло[2,3-b]пиридин-4-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 572: 1-Метил-1H-пирроло[2,3-b]пиридин-4-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 573: 3,4-Дихлорфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия A: 6-(4-{[4-(Бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилхлорид
К раствору соединения из Синтеза 6bа (450 мг, 0.47 ммоль) и N,N-диизопропилэтиламина (0.41 мл, 2.36 ммоль) в дихлорметане (45 мл), охлажденному до 0°C, добавляют трифосген (139 мг, 0.47 ммоль) и смесь перемешивают в течение 1 ч при температуре окружающей среды. Реакционную смесь разбавляют дихлорметаном и промывают 1 М водной HCl. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме с получением желтого, твердого вещества, которое непосредственно используют на следующей стадии без дополнительной очистки и предполагая количественное превращение.
ЖХ/МС (C46H48ClN5O5) 786 [М+Н]+; RT 1.33 (Метод В)
Стадия В: 3,4-Дихлорфенил 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору соединения из Стадии A (41 мг, 0.05 ммоль) в ацетонитриле (5 мл) добавляют карбонат калия (72 мг, 0.52 ммоль), DMAP (0.052 ммоль) и 3,4-дихлорфенол (0.52 ммоль) и смесь нагревают при 60°C в течение прибл. 16 ч. Реакционную смесь разбавляют этилацетатом и промывают насыщенным водным бикарбонатом натрия и солевым раствором. Органический экстракт сушат над сульфатом магния и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 4 г RediSep™ силикагелевый картридж; дихлорметан - 5% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C52H51Cl2N5O6) 912 [М+Н]+; RT 1.48 (Метод В)
Стадия С: 3,4-Дихлорфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору соединения из Стадии A в дихлорметане (5 мл), охлажденному до 0°C, по каплям добавляют трихлорид бора ( 1M в дихлорметане; 5 экв.). Затем реакционной смеси дают нагреться до температуры окружающей среды и перемешивание продолжают в течение прибл. 16 ч. Реакцию гасят путем добавления воды (10 мл) и фазы разделяют. Органическую фазу, последовательно промывают водным бикарбонатом натрия и солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 4 г RediSep™ силикагелевый картридж; дихлорметан - 5% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C45H45Cl2N5O6) 822 [М+Н]+; RT 1.28 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H45N5O6Cl2
[М+Н]+ рассчитано: 822.2820
[М+Н]+ найдено: 822.2832
Пример 574: Нафталин-2-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 573 с заменой 3,4-дихлорфенола на Стадии B на нафталин-2-ол.
ЖХ/МС (C49H49N5O6) 804 [М+Н]+; RT 1.24 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C49H49N5O6
[М+Н]+ рассчитано: 804.3756
[М+Н]+ найдено: 804.3767
Пример 575: 1H-Индол-6-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 573 с заменой 3,4-дихлорфенола на Стадии B на 3H-индол-6-ол.
ЖХ/МС (C47H48N6O6) 793 [М+Н]+; RT 1.15 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H48N6O6
[М+Н]+ рассчитано: 793.3708
[М+Н]+ найдено: 793.3690
Пример 576: 1-Метил-1H-индол-6-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 577: 1H-Индол-5-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 573 с заменой 3,4-дихлорфенола на Стадии B на 1H-индол-5-ол.
ЖХ/МС (C47H48N6O6) 793 [М+Н]+; RT 1.13 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H48N6O6
[М+2Н]2+ рассчитано: 397.1890
[М+2Н]2+ найдено: 397.1879
Пример 578: 1-Метил-1H-индол-5-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 579: 1H-Пирроло[2,3-b]пиридин-5-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 573 с заменой 3,4-дихлорфенола на Стадии B на 1H-пирроло[2,3-b]пиридин-5-ол.
ЖХ/МС (C46H47N7O6) 794 [М+Н]+; RT 1.07 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H47N7O6
[М+2Н]2+ рассчитано: 397.6867
[М+2Н]2+ найдено: 397.6880
Пример 580: 1-Метил-1H-пирроло[2,3-b]пиридин-5-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 581: 1H-Пирроло[2,3-b]пиридин-4-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 582: 1H-Пирроло[2,3-b]пиридин-5-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 583: 2-(Метилсульфанил)фенил 6-{4-((4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 584: 3-(Метилсульфанил)фенил 6-{4-|(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 585: 4-(Метилсульфанил)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 586: 2-(Диметилкарбамоил)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 587: 3-(Диметилкарбамоил)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 588: 4-(Диметилкарбамоил)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 589: 2-Метилфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 590: 3-Метилфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 591: 4-Метилфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 785 с заменой продукта из Синтеза 6cb на продукт из Синтеза 6са.
ЖХ/МС (C46H49N5O5) 752 [М+Н]+; RT 1.34 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O5
[М+Н]+ рассчитано: 752.3806
[М+Н]+ найдено: 752.3836
Пример 592: 2-Хлорфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 593: 3-Хлорфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 594: 4-Хлорфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 595: 2-Гидроксифенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 596: 3-Гидроксифенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 597: 4-Гидроксифенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 598: 2-Метоксифенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 599: 3-Метоксифенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 600: 4-Метоксифенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 601: 2-(Метиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 602: 3-(Метиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 603: 4-(Метиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 604: 2-(Диметиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 605: 3-(Диметиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 606: 4-(Диметиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 607: 2-(Ацетиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 608: 3-(Ацетиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 609: 4-(Ацетиламино)фенил 6-(1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 610: 2-(Трифторметил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 611: 3-(Трифторметил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 612: 4-(Трифторметил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 613: 2-Цианофенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 614: 3-Цианофенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 615: 4-Цианофенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 616: 2-Этинилфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 617: 3-Этинилфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 618: 4-Этинилфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 619: 2,3-Дихлорфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 620: Нафталин-1-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 621: 1H-Индол-7-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 622: 1-Метил-1H-индол-7-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 623: 1H-Индол-4-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 624: 1-Метил-1H-индол-4-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 625: 1H-Пирроло[2,3-b]пиридин-4-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 626: 1-Метил-1H-пирроло[2,3-b]пиридин-4-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 627: 3,4-Дихлорфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 628: Нафталин-2-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 629: 1H-Индол-6-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия A: 6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилхлорид и
Трихлорметил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору продукта из Синтеза 6са (200 мг, 0.32 ммоль) и N,N-диизопропилэтиламина (0.17 мл, 0.97 ммоль) в дихлорметане (10 мл), охлажденному до 0°C, добавляют трифосген (96 мг, 0.32 ммоль) и смесь перемешивают при температуре окружающей среды в течение 1 ч. Реакционную смесь разбавляют дихлорметаном и промывают 1 М водной HCl. Органический экстракт сушат сульфатом магния, фильтруют и концентрируют в вакууме с получением целевых продуктов виде смеси.
ЖХ/МС (C39H42ClN5O4) 680 [М+Н]+; RT 1.27, и (C40H42Cl3N5O5) 778 [М+Н]+; RT 1.36 (Метод В)
Стадия В: 1H-Индол-6-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору вещества из Стадии A (50 мг, 0.06 ммоль) в ацетонитриле (5 мл) добавляют карбонат калия (44 мг, 0.32 ммоль) и, далее, 1H-индол-6-ол (1.5 экв.) и смесь нагревают при 60°C в течение прибл. 16 ч. Реакционной смеси дают охладиться до температуры окружающей среды, и разбавляют этилацетатом (20 мл) и последовательно промывают 1 М водным гидроксидом натрия и солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 4 г RediSep™ силикагелевый картридж; дихлорметан - 10% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C47H48N6O5) 777 [М+Н]+; RT 1.26 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H48N6O5
[М+Н]+ рассчитано: 777.3759
[М+Н]+ найдено: 777.3795
Пример 630: 1-Метил-1H-индол-6-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 631: 1H-Индол-5-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 629 с заменой 1H-индол-6-ола на Стадии B на 1H-индол-5-ол и очисткой с помощью препаративной ЖХВР (H2O-ТФУ/ацетонитрил; градиентное элюирование).
ЖХ/МС (C47H48N6O5) 777 [М+Н]+; RT 1.28 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H48N6O5
[М+Н]+ рассчитано: 777.3759
[М+Н]+ найдено: 777.3742
Пример 632: 1-Метил-1H-индол-5-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 633: 1H-Пирроло[2,3-b]пиридин-5-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 629 с заменой 1H-индол-6-ола на Стадии B на 1H-пирроло[2,3-b]пиридин-5-ол.
ЖХ/МС (C46H47N7O5) 778 [М+Н]+; RT 1.18 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H47N7O5
[М+2Н]2+ рассчитано: 389.6892
[М+2Н]2+ найдено: 389.6874
Пример 634: 1-Метил-1H-пирроло[2,3-b]пиридин-5-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 629 с заменой 1H-индол-6-ола на Стадии B на 1-метил-1H-пирроло[2,3-b]пиридин-5-ол и очисткой с помощью препаративной ЖХВР (Н2O-ТФУ/ацетонитрил; градиентное элюирование).
ЖХ/МС (C47H49N7O5) 792 [М+Н]+; RT 1.25 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H49N7O5
[М+2Н]2+ рассчитано: 396.6970
[М+2Н]2+ найдено: 396.6978
Пример 635: 1H-Пирроло[2,3-b]пиридин-4-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 636: 1H-Пирроло[2,3-b]пиридин-5-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 786 с заменой 4-гидроксибензонитрила на Стадии B на 1H-пирроло[2,3-b]пиридин-5-ол.
ЖХ/МС (C42H40N6O4) 693 [М+Н]+; RT 1.34 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H40N6O4
[М+2Н]2+ рассчитано: 347.1628
[М+2Н]2+ найдено: 347.1639
Пример 637: 2-(Метилсульфанил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 638: 3-(Метилсульфанил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 639: 4-(Метилсульфанил)фенил 6-{1,5-диметил-4-{метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 640; 2-(Диметилкарбамоил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 641: 3-(Диметилкарбамоил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 642: 4-(Диметилкарбамоил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 643: 2-Метилфенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 644: 3-Метилфенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 645: 4-Метилфенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 646: 2-Хлорфенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 647: 3-Хлорфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 648: 4-Хлорфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 649: 2-Гидроксифенил 6-{1,5-диметил-4-(метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 650: 3-Гидроксифенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 651: 4-Гидроксифенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 652: 2-Метоксифенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 653: 3-Метоксифенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 654: 4-Метоксифенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 655: 2-(Метиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 656: 3-(Метиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 657: 4-(Метиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 658: 2-(Диметиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 659: 3-(Диметиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 660: 4-(Диметиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 661: 2-(Ацетиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 662: 3-(Ацетиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 663: 4-(Ацетиламино)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 664: 2-(Трифторметил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 665: 3-(Трифторметил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 666: 4-(Трифторметил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 667: 2-Цианофенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 668: 3-Цианофенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 669: 4-Цианофенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 670: 2-Этинилфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 671: 3-Этинилфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 672: 4-Этинилфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 673: 2,3-Дихлорфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 674: Нафталин-1-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 675: 1H-Индол-7-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 676: 1-Метил-1H-индол-7-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 677: 1H-Индол-4-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 678: 1-Метил-1H-индол-4-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 679: 1H-Пирроло[2,3-b]пиридин-4-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 680: 1-Метил-1H-пирроло[2,3-b]пиридин-4-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 681: 3,4-Дихлорфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 682: Нафталин-2-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 683: 1H-Индол-6-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 684: 1-Метил-1H-индол-6-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 685: 1H-Индол-5-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 686: 1-Метил-1H-индол-5-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 687: 1H-Пирроло[2,3-b]пиридин-5-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 688: 1-Метил-1H-пирроло[2,3-b]пиридин-5-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 689: 1H-Пирроло[2,3-b]пиридин-4-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 690: 1H-Пирроло[2,3-b]пиридин-5-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 691: 2-(Метилсульфанил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 692: 3-(Метилсульфанил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 693: 4-(Метилсульфанил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 694: 2-(Диметилкарбамоил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 695: 3-(Диметилкарбамоил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 696: 4-(Диметилкарбамоил)фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 697: Фенил 7-{[(3S)-3-(гидроксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 698: 5-[7-{[(3S)-3-(Гидроксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 699: Фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(гидроксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 700: 5-[7-{[(3S)-3-(Гидроксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 701: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(гидроксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 702: N,N-Дибутил-5-[7-{[(3S)-3-(гидроксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 703: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(метоксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 704: N-(4-Гидроксифенил)-5-[7-{[(3S)-3-(метоксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 705: Фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(метоксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 706: 5-[7-{[(3S)-3-(Метоксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-N,1,2-триметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 707: Фенил 6-[4-(дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(метоксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 708: N,N-Дибутил-5-[7-{[(3S)-3-(метоксиметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2-(фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил]-1,2-диметил-1H-пиррол-3-карбоксамид
Пример 709: 3-(6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилокси)бензойная кислота
Стадия A: 6-(4-{[4-(Бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилхлорид
К раствору продукта из Синтеза 6bа (450 мг, 0.47 ммоль, 1 экв.) в дихлорметане (45 мл), охлажденному до 0°C, добавляют N,N-диизопропилэтиламин (0.41 мл, 2.36 ммоль, 5 экв.) и трифосген (139 мг, 0.47 ммоль, 0.99 экв.), и смесь перемешивают в течение 1 ч при температуре окружающей среды. Реакционную смесь разбавляют дихлорметаном и промывают 1 М водной HCl. Органическую фазу сушат над сульфатом магния и концентрируют в вакууме с получением желтого твердого вещества, которое непосредственно используют на следующей стадии без дополнительной очистки и предполагая количественное превращение.
ЖХ/МС (C46H48ClN5O5) 786 [М+Н]+; RT 1.33 (Метод В)
Стадия В: 3-[(Бензилокси)карбонил]фенил 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору продукта, полученного на Стадии A, (41 мг, 0.05 ммоль) в ацетонитриле (5 мл) добавляют карбонат калия (71.87 мг, 0.52 ммоль), DMAP (0.052 ммоль) и бензил 3-гидроксибензоат (0.52 ммоль) и смесь нагревают при 60°C в течение 16 ч.
Реакционную смесь разбавляют этилацетатом, й последовательно промывают водным бикарбонатом натрия и солевым раствором. Органические экстракты сушат (MgSO4) и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (4 г, силикагель; дихлорметан - 5% МеОН/дихлорметан) дает целевой продукт.
ЖХ/МС (C60H59N5O9) нет ионизации; RT 1.46 (Метод В)
Стадия С: 3-(6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилокси)бензойная кислота
К раствору продукта, полученного на Стадии B, (42 мг, 0.04 ммоль, 1 экв.) в этаноле (8 мл) добавляют 10% Pd/C (50 мг) и смесь встряхивают в атмосфере водорода в течение прибл. 4 ч. Реакционную смесь фильтруют через целит с дальнейшим элюированием метанолом, и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (4 г, силикагель; дихлорметан - 5% метанол/дихлорметан) дает целевой продукт в виде твердого вещества.
ЖХ/МС (C46H47N5O8) 798 [М+Н]+; RT 1.07 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H47N5O8
[М+Н]+ рассчитано: 798.3497
[М+Н]+ найдено: 798.3438
Пример 710: 3-{2-[6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 711: 3-({[6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]карбонил}окси)бензойная кислота
Пример 712: 3-{2-[6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 713: 3-[({6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}карбонил)окси]бензойная кислота
Пример 714: 3-(2-{6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}-2-оксоэтил)бензойная кислота
Пример 715: 3-(6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилокси)бензойная кислота
Методика соответствует методике Примера 709 с заменой продукта из Синтеза 6bb на продукт из Синтеза 6bf, на Стадии A.
ЖХ/МС (C42H40N4O7) 711 [М-Н]-; RT 1.27 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H40N4O7
[М+2Н]2+ рассчитано: 713.2970
[М+2Н]2+ найдено: 713.2962
Пример 716: 3-{2-[6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 717: 3-({[6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]карбонил}окси)бензойная кислота
Пример 718: 3-{2-[6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1N-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 719; 3-[({6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}карбонил)окси]бензойная кислота
Пример 720: 3-(2-{6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}-2-оксоэтил)бензойная кислота
Пример 721: 4-(6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилокси)бензойная кислота
Методика соответствует методике Примера 709 с заменой бензил 3-гидроксибензоата из Стадии B на бензил 4-гидроксибензоат.
ЖХ/МС (C46H47N5O8) 798 [М+Н]+; RT 1.07 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H47N5O8
[М+Н]+ рассчитано: 798.3497
[М+Н]+ найдено: 798.3475
Пример 722; 4-{2-[6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 723: 4-({[6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]карбонил}окси)бензойная кислота
Пример 724: 4-{2-[6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 725: 4-[({6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}карбонил)окси]бензойная кислота
Пример 726: 4-(2-{6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}-2-оксоэтил)бензойная кислота
Пример 727: 4-({[6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]карбонил}окси)бензойная кислота
Пример 728: 4-{2-[6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 729: 4-({[6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]карбонил}окси)бензойная кислота
Пример 730: 4-{2-[6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 731: 4-[({6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}карбонил)окси]бензойная кислота
Пример 732: 4-(2-{6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}-2-оксоэтил)бензойная кислота
Пример 733: 3-(6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилокси)бензойная кислота
Методика соответствует методике Примера 709 с заменой продукта из Синтеза 6bа на продукт из Синтеза 6bf, на Стадии A.
ЖХ/МС (C47H50N6O7) 811 [М+Н]+; RT 2.16 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H50N6O7
[М+2Н]2+ рассчитано: 406.1943
[М+2Н]2+ найдено: 406.1944
Пример 734: 3-{2-[6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 735: 3-(6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилокси)бензойная кислота
Методика соответствует методике Примера 709 с заменой продукта из Синтеза 6bа на продукт из Синтеза 6cе, на Стадии A.
ЖХ/МС (C47H50N6O6) 795 [М+Н]+; RT 1.4 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H50N6O6
[М+2Н]2+ рассчитано: 398.1969
[М+2Н]2+ найдено: 398.1985
Пример 736: 3-{2-[6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 737: 3-[({6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}карбонил)окси]бензойная кислота
Пример 738: 3-(2-{6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}-2-оксоэтил)бензойная кислота
Пример 739: 4-({[6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]карбонил}окси)бензойная кислота
Пример 740: 4-{2-[6-{4-[(4-Гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 741: 4-({[6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]карбонил}окси)бензойная кислота
Пример 742: 4-{2-[6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил]-2-оксоэтил}бензойная кислота
Пример 743: 4-[({6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}карбонил)окси]бензойная кислота
Пример 744: 4-(2-{6-[4-(Дибутилкарбамоил)-1,5-диметил-1H-пиррол-2-ил]-7-{[(3S)-3-[(4-метилпиперазин-1-ил)метил]-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-ил}-2-оксоэтил)бензойная кислота
Пример 745: 5-(2-Ацетил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-1,2-диметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 746: 5-(2-Ацетил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-1,2-диметил-N-фенил-1H-пиррол-3-карбоксамид
Пример 747: N-4-Гидроксифенил)-1,2-диметил-5-(2-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-фенил-1H-пиррол-3-карбоксамид
Пример 748: 5-(2-Ацетил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-1,2-диметил-N-(1-метил-1H-пирроло[2,3-b]пиридин-5-ил)-1H-пиррол-3-карбоксамид
Пример 749: 5-(2-Ацетил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-1,2-диметил-N-(1-метил-1H-пирроло[2,3-b]пиридин-5-ил)-1H-пиррол-3-карбоксамид
Пример 750: N-(4-Гидроксифенил)-1,2-диметил-5-(2-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(1-метил-1H-пирроло[2,3-b]пиридин-5-ил)-1H-пиррол-3-карбоксамид
Пример 751: 5-(2-Ацетил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-1,2-диметил-N-(пиридин-4-ил)-1H-пиррол-3-карбоксамид
Пример 752: 5-(2-Ацетил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(4-гидроксифенил)-1,2-диметил-N-(пиридин-4-ил)-1H-пиррол-3-карбоксамид
Пример 753: N-(4-Гидроксифенил)-1,2-диметил-5-(2-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(пиридин-4-ил)-1H-пиррол-3-карбоксамид
Пример 754: 5-(2-Ацетил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1,2-диметил-N,N-дифенил-1H-пиррол-3-карбоксамид
Пример 755: 5-(2-Ацетил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1,2-диметил-N,N-дифенил-1H-пиррол-3-карбоксамид
Пример 756: 1,2-Диметил-5-(2-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N,N-дифенил-1H-пиррол-3-карбоксамид
Пример 757: 5-(2-Ацетил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1,2-диметил-N-(1-метил-1H-пирроло[2,3-b]пиридин-5-ил)-N-фенил-1H-пиррол-3-карбоксамид
Пример 758: 5-(2-Ацетил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,23,4-тетрагидроизохинолин-6-ил)-1,2-диметил-N-(1-метил-1H-пирроло[2,3-b]пиридин-5-ил)-N-фенил-1H-пиррол-3-карбоксамид
Пример 759: 1,2-Диметил-5-(2-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-(1-метил-1H-пирроло[2,3-b]пиридин-5-ил)-N-фенил-1N-пиррол-3-карбоксамид
Пример 760: 5-(2-Ацетил-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1,2-диметил-N-фенил-N-(пиридин-4-ил)-1H-пиррол-3-карбоксамид
Пример 761: 5-(2-Ацетил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-1,2-диметил-N-фенил-N-(пиридин-4-ил)-1H-пиррол-3-карбоксамид
Пример 762: 1,2-Диметил-5-(2-метил-7-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,2,3,4-тетрагидроизохинолин-6-ил)-N-фенил-N-(пиридин-4-ил)-1H-пиррол-3-карбоксамид
Пример 763: 4-Метилфенил 6-{4-[(4-гидроксифенил)(1-метил-1N-пиразол-4-ил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 764: 4-Метилфенил 6-{1-[(4-гидроксифенил)(1-метил-1H-пиразол-4-ил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 765: 4-Метилфенил 6-{4-[(4-гидроксифенил)(пиридин-4-ил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 766: 4-Метилфенил 6-{1-[(4-гидроксифенил)(пиридин-4-ил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 767; 4-Метилфенил 6-{4-[(4-гидроксифенил)(1-метил-1H-пирроло[2,3-b]пиридин-5-ил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 768: 4-Метилфенил 6-{1-[(4-гидроксифенил)(1-метил-1H-пирроло[2,3-b]пиридин-5-ил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 769: 4-Метилфенил 6-(1,5-диметил-4-{(1-метил-1H-пиразол-4-ил)[4-(фосфонокси)фенил]карбамоил}-1H-пиррол-2-ил)-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 770: 4-Метилфенил 6-(1-{(1-метил-1H-пиразол-4-ил)[4-(фосфонокси)фенил]карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 771: 4-Метилфенил 6-(1,5-диметил-4-{[4-(фосфонокси)фенил](пиридин-4-ил)карбамоил}-1H-пиррол-2-ил)-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 772: 4-Метилфенил 7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-6-(1-{[4-(фосфонокси)фенил](пиридин-4-ил)карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 773: 4-Метилфенил 6-(1,5-диметил-4-{(1-метил-1H-пирроло[2,3-b]пиридин-5-ил)[4-(фосфонокси)фенил]карбамоил}-1H-пиррол-2-ил)-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 774: 4-Метилфенил 6-(1-{(1-метил-1H-пирроло[2,3-b]пиридин-5-ил)[4-(фосфонокси)фенил]карбамоил}-5,6,7,8-тетрагидроиндолизин-3-ил)-7-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-3,4-дигидроизохинолин-2(1H)-карбоксилат
Пример 775: 2-[2-(Диметилкарбамоил)этил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 709 с заменой продукта из Синтеза 6bа на Стадии A на продукт из Синтеза 6bb, и с заменой бензил 3-гидроксибензоата из Стадии B на 3-(2-гидроксифенил)-N,N-диметилпропанамид.
ЖХ/МС (C46H49N5O6) 768 [М+Н]+; RT 2.51 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O6
[М+2Н]2+ рассчитано: 384.6914
[М+2Н]2+ найдено: 384.6929
Пример 776: 3-[2-(Диметилкарбамоил)этил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 709 с заменой продукта из Синтеза 6bа на Стадии A на продукт из Синтеза 6bb, и с заменой бензил 3-гидроксибензоата из Стадии B на 3-(3-гидроксифенил)-N,N-диметилпропанамид.
ЖХ/МС (C46H49N5O6) 768 [М+Н]+; RT 2.50 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O6
[М+2Н]2+ рассчитано: 384.6914
[М+2Н]2+ найдено: 384.6913
Пример 777: 5-{7-[(3S)-3-[(Диметиламино)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Стадия A: N-[4-(Бензилокси)фенил]-5-{7-[(3S)-3-[(диметиламино)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-N,1,2-триметил-1Н-пиррол-3-карбоксамид
Раствор соединения из Синтеза 6bе (50 мг, 0.05 ммоль) и N,N-диизопропилэтиламина (48 мкл, 0.27 ммоль) в дихлорметане (5 мл) охлаждают до 0°C. К раствору добавляют фенилацетилхлорид (8 мкл, 0.06 ммоль) и затем реакционную смесь перемешивают при температуре окружающей среды в течение 1 ч. Реакционную смесь разбавляют дихлорметаном, промывают 1 М водным гидроксидом натрия, и затем солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 4 г RediSep™ силикагелевый картридж; дихлорметан - 10% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C51H53N5O4) 800 [М+Н]+; RT 1.26 (Метод В)
Стадия В: 5-{7-[(3S)-3-[(диметиламино)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N,1,2-триметил-1Н-пиррол-3-карбоксамид
К раствору вещества из Стадии A (30 мг, 0.04 ммоль) в этаноле (5 мл) добавляют 10% Pd/C (каталитическое количество) и смесь встряхивают в атмосфере водорода в течение прибл. 16 ч. Смесь фильтруют через целит с дальнейшим элюированием метанолом, и концентрируют при пониженном давлении. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 4 г RediSep™ силикагелевый картридж; дихлорметан - 7% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C44H47N5O4) 710 [М+Н]+; RT 1.07 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H47N5O4
[М+Н]+ рассчитано: 710.3701
[М+Н]+ найдено: 710.3702
Пример 778: N-(4-Гидроксифенил)-N,1,2-триметил-5-{7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bf.
ЖХ/МС (C47H52N6O4) 765 [М+Н]+; RT 1.08 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H52N6O4
[М+Н]+ рассчитано: 765.4123
[М+Н]+ найдено: 765.4141
Пример 779: N-(4-Гидроксифенил)-N,1,2-триметил-5-{7-[(3S)-3-[2-(морфолин-4-ил)этил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на продукт из Синтеза 6bс.
ЖХ/МС (C47H51N5O5) 766 [М+Н]+; RT 1.08 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H51N5O5
[М+Н]+ рассчитано: 766.3963
[М+Н]+ найдено: 766.3982
Пример 780: N-Этил-N-(4-гидроксифенил)-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на продукт из Синтеза 6f.
ЖХ/МС (C47H51N5O5) 766 [М+Н]+; RT 1.15 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C47H51N5O5
[М+Н]+ рассчитано: 766.3963
[М+Н]+ найдено: 766.3967
Пример 781: N-(4-Гидроксифенил)-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-N-пропил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 777 с заменой продукта из Синтеза 6bе на Стадии A на продукт из Синтеза 6g.
ЖХ/МС (C48H53N5O5) 780 [М+Н]+; RT 1.19 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H53N5O5
[М+Н]+ рассчитано: 780.4119
[М+Н]+ найдено: 780.4101
Пример 782: 5-{7-[(3S)-3-[(Диметиламино)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(трифторацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
ЖХ/МС (C38H40F3N5O4) 688 [М+Н]+; RT 1.07 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C38H40N5O4F3
[М+Н]+ рассчитано: 688.3105
[М+Н]+ найдено: 688.3094
Пример 783: N-(4-Гидроксифенил)-N,1,2-триметил-5-{7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(трифторацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
ЖХ/МС (C41H45N6O4F3) 743 [М+Н]+; RT 1.09 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H45N6O4F3
[М+2Н]2+ рассчитано: 372.1800
[М+2Н]2+ найдено: 372.1801
Пример 784: 4-Бромфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия A: 4-Бромфенил 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору соединения из Синтеза 6bа (108 мг, 0.11 ммоль) и N,N-диизопропилэтиламина (0.1 мл, 0.57 ммоль) в дихлорметане (15 мл), охлажденному до 0°C, добавляют трифосген (34 мг, 0.11 ммоль) и смесь перемешивают в течение 1 ч при температуре окружающей среды. Реакционную смесь разбавляют дихлорметаном и промывают 1 М водной HCl. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме с получением желтого твердого вещества. К раствору этого твердого вещества в ацетонитриле (10 мл) добавляют карбонат калия (152 мг, 1.1 ммоль), DMАР (13 мг, 0.11 ммоль) и 4-бромфенол (98 мг, 0.57 ммоль) и смесь нагревают при 60°C в течение прибл. 16 ч. Реакционную смесь разбавляют этилацетатом и последовательно промывают насыщенным водным бикарбонатом натрия и солевым раствором. Органический экстракт сушат над сульфатом магния и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 4 г RediSep™ силикагелевый картридж; дихлорметан - 5% метанол в дихлорметане) дает целевой продукт (79 мг, 0.09 ммоль).
ЖХ/МС (C52H52BrN5O6) 922 [М+Н]+; RT 1.50 (Метод В)
Стадия В: 4-Бромфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Продукт из Стадии A растворяют в дихлорметане (10 мл) и раствор охлаждают до 0°C. К раствору по каплям добавляют трихлорид бора (5 экв.). Затем реакционной смеси дают нагреться до температуры окружающей среды в течение 1 ч. Реакционную смесь адсорбируют на изолют и очищают с помощью хроматографии (CombiFlash Rf, 12 г RediSep™ силикагелевый картридж) при элюировании в градиенте дихлорметан - 5% метанол в дихлорметане с получением целевого продукта.
ЖХ/МС (C45H46BrN5O6) 832 [М+Н]+; RT 1.24 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: С45Н46N6О6Br
[М+2Н]2+ рассчитано: 416.6388
[М+2Н]2+ найдено: 416.6374
Пример 785: 4-Метилфенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору продукта из Синтеза 6cb (50 мг, 0.09 ммоль) и N,N-диизопропилэтиламина (38 мкл, 0.19 ммоль) в дихлорметане (5 мл), охлажденному до 0°C, добавляют 4-метилфенилхлорформиат (15 мкл, 0.1 ммоль) и смесь перемешивают при температуре окружающей среды в течение 1 ч. Реакционную смесь разбавляют дихлорметаном, затем последовательно промывают 1 М водным гидроксидом натрия и солевым раствором. Органический экстракт сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 12 г RediSep™ силикагелевый картридж; дихлорметан - 5% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C42H42N4O4) 667 [М+Н]+; RT 1.50 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H42N4O4
[М+Н]+ рассчитано: 667.3279
[М+Н]+ найдено: 667.3287
Пример 786: 4-Цианофенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия А: 6-{1,5-Диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбонилхлорид
К раствору продукта из Синтеза 6cb (300 мг, 0.56 ммоль) и N,N-диизопропилэтиламина (0.29 мл, 1.69 ммоль) в дихлорметане (10 мл), охлажденному до 0°C, добавляют трифосген (167 мг, 0.56 ммоль) и смеси дают нагреться до температуры окружающей среды в течение 1 ч. Реакционную смесь разбавляют дихлорметаном, промывают 1 М водной HCl и сушат над сульфатом магния. Концентрирование в вакууме дает желтое твердое вещество, которое непосредственно используют на следующей стадии без дополнительной очистки и предполагая количественное превращение.
ЖХ/МС (C35H35ClN4O3) 595 [М+Н]+; RT 1.41 (Метод В)
Стадия В: 4-Цианофенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1Н-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору карбамоилхлорида из Стадии A (50 мг, 0.072 ммоль) в ацетонитриле (5 мл) добавляют карбонат калия (50 мг, 0.36 ммоль) и 4-гидроксибензонитрил (10 мг, 0.086 ммоль). После нагревания при 60°C в течение прибл. 16 ч реакционной смеси дают охладиться до температуры окружающей среды, затем разбавляют этилацетатом и последовательно промывают 1 М водным гидроксидом натрия и солевым раствором. Органический экстракт сушат над сульфатом магния, концентрируют в вакууме, и очищают с помощью препаративной ЖХВР с получением целевого продукта.
ЖХ/МС (C42H39N5O4) 678 [М+Н]+; RT 1.41 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H39N5O4
[М+Н]+ рассчитано: 678.3075
[М+Н]+ найдено: 678.3086
Пример 787: 3-[2-(Диметилкарбамоил)этил]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-{(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 786 с заменой 4-гидроксибензонитрила на Стадии B на 3-(3-гидроксифенил)-N,N-диметилпропанамид.
ЖХ/МС (C46H49N5O5) 752 [М+Н]+; RT 1.39 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O5
[М+2Н]2+ рассчитано: 376.6940
[М+2Н]2+ найдено: 376.6930
Пример 788: 4-[2-(Диметилкарбамоил)этил]фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 786 с заменой 4-гидроксибензонитрила на Стадии B на 3-(4-гидроксифенил)-N,N-диметилпропанамид.
ЖХ/МС (C46H49N5O5) 752 [М+Н]+; RT 1.38 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O5
[М+2Н]2+ рассчитано: 376.6940
[М+2Н]2+ найдено: 376.6926
Пример 789: 1H-Индол-5-ил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 786 с заменой 4-гидроксибензонитрила на Стадии B на 1H-индол-5-ол.
ЖХ/МС (C43H41N5O4) 692 [М+Н]+; RT 1.41 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H41N5O4
[М+Н]+ рассчитано: 692.3231
[М+Н]+ найдено: 692.3210
Пример 790: Циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bb, и с заменой фенилацетилхлорида на циклогексилхлорформиат.
ЖХ/МС (C41H46N4O5) 675 [М+Н]+; RT 1.45 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H46N4O5
[М+Н]+ рассчитано: 675.3541
[М+Н]+ найдено: 675.3548
Пример 791: Циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bа, и с заменой фенилацетилхлорида на циклогексилхлорформиат.
ЖХ/МС (C45H53N5O6) нет ионизации; RT 1.28 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H53N5O6
[М+Н]+ рассчитано: 760.4069
[М+Н]+ найдено: 760.4078
Пример 792: N-Циклогексил-6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bb, и с заменой фенилацетилхлорида на циклогексилизоцианат.
ЖХ/МС (C41H47N5O4) 674 [М+Н]+; RT 1.34 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H47N5O4
[М+Н]+ рассчитано: 674.3701
[М+Н]+ найдено: 674.3696
Пример 793: N-Циклогексил-6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксамид
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bа, и с заменой фенилацетилхлорида на циклогексилизоцианат.
ЖХ/МС (C45H54N6O5) нет ионизации; RT 1.18 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C45H54N6O5
[М+Н]+ рассчитано: 759.4228
[М+Н]+ найдено: 759.4192
Пример 794: 5-[2-(2-Циклогексилацетил)-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bа, и с заменой фенилацетилхлорида на 2-циклогексилацетилхлорид.
ЖХ/МС (C46H55N5O5) нет ионизации; RT 1.24 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H55N5O5
[М+Н]+ рассчитано: 758.4276
[М+Н]+ найдено: 758.4247
Пример 795: 5-[2-(2-Циклогексилацетил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bb, и с заменой фенилацетилхлорида на 2-циклогексилацетилхлорид.
ЖХ/МС (C42H48N4O4) 673 [М+Н]+; RT 1.24 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C42H48N4O4
[М+Н]+ рассчитано: 673.3748
[М+Н]+ найдено: 673.3741
Пример 796: Циклопентил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bа, и с заменой фенилацетилхлорида на циклопентилхлорформиат.
ЖХ/МС (C44H51N5O6) 746 [М+Н]+; RT 1.24 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C44H51N5O6
[М+Н]+ рассчитано: 746.3912
[М+Н]+ найдено: 746.3891
Пример 797: (1R,2S,5R)-5-Метил-2-(пропан-2-ил)циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bа, и с заменой фенилацетилхлорида на (1R,2S,5R)-5-метил-2-(пропан-2-ил)циклогексилхлорформиат.
ЖХ/МС (C49H61N5O6) 816 [М+Н]+; RT 1.47 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C49H61N5O6
[М+Н]+ рассчитано: 816.4695
[М+Н]+ найдено: 816.4717
Пример 798: 5-(2-[2-(Адамантан-1-ил)анетил]-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил}-N-(4-гидроксифенил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bа, и с заменой фенилацетилхлорида на 2-(адамантан-1-ил)ацетилхлорид.
ЖХ/МС (C50H59N5O5) 810 [М+Н]+; RT 1.32 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C50H59N5O5
[М+Н]+ рассчитано: 810.4589
[М+Н]+ найдено: 810.4586
Пример 799: N-(4-Гидроксифенил)-N,1,2-триметил-5-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(пиперидин-1-ил)ацетил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид
Стадия A: N-[4-(Бензилокси)фенил]-N,1,2-триметил-5-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(пиперидин-1-ил)ацетил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1Н-пиррол-3-карбоксамид
К раствору соединения из Синтеза 6bb (50 мг, 0.08 ммоль) в ДМФА (2 мл) добавляют гексафторфосфат 2-(1H-бензотриазол-1-ил)-1,1,3,3-тетраметилурония (30 мг; 0.08 ммоль), N,N-диизопропилэтиламин (41 мкл, 0.23 ммоль, 3 экв.), и 2-(пиперидин-1-ил)уксусную кислоту (13 мг, 0.09 ммоль), и смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакционную смесь концентрируют в вакууме и распределяют между этил ацетатом и водой. Органическую фазу промывают солевым раствором, сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 4 г RediSep™ силикагелевый картридж; дихлорметан - 10% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C48H53N5O4) нет ионизации; RT 1.29 (Метод В)
Стадия B: N-(4-Гидроксифенил)-N,1,2-триметил-5-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-[2-(пиперидин-1-ил)ацетил]-1,2,3,4-тетрагидроизохинолин-6-ил}-1Н-пиррол-3-карбоксамид
К раствору продукта из Стадии A (30 мг, 0.04 ммоль) в этаноле (5 мл) добавляют 10% Pd/C (каталитическое количество) и смесь встряхивают в атмосфере водорода в течение прибл. 16 ч. Смесь фильтруют через целит, элюируют метанолом, и фильтрат концентрируют в вакууме. Очистка с помощью препаративной ЖХВР (H2O-ТФУ/ацетонитрил; градиентное элюирование) дает целевой продукт.
ЖХ/МС (C41H47N5O4) 674 [М+Н]+; RT 1.09 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H47N5O4
[М+2Н]2+ рассчитано: 337.6887
[М+2Н]2+ найдено: 337.6887
Пример 800: (1r,4r)-4-{[(трет-Бутокси)карбонил]амино}циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Стадия А: (1r,4r)-4-{[(трет-Бутокси)карбонил]амино}циклогексилхлорформиат
Трифосген (69 мг, 0.23 ммоль) растворяют в дихлорметане (3 мл) и раствор охлаждают до 0°C. К раствору по каплям добавляют раствор трет-бутил N-(4-гидроксициклогексил)карбамата (100 мг, 0.46 ммоль) и триэтиламина (0.06 мл, 0.46 ммоль, 2 экв.) в дихлорметане (1 мл). После перемешивания в течение 2 ч при температуре окружающей среды реакционную смесь концентрируют в вакууме, затем повторно растворяют/суспендируют в дихлорметане и фильтруют. Фильтрат (2 мл) непосредственно применяют на следующей стадии, предполагая количественное превращение.
Стадия В: (1r,4r)-4-{[(трет-Бутокси)карбонил]амино}циклогексил 6-(4-{[4-(бензилокси)фенил](метил)карбамоил}-1,5-диметил-1Н-пиррол-2-ил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Раствор продукта из Синтеза 6bb (50 мг, 0.08 ммоль) в дихлорметане (3 мл) охлаждают до 0°C. К раствору добавляют триэтиламин (54 мкл, 0.39 ммоль) и раствор продукта из Стадии A (0.49 ммоль) и смесь перемешивают в течение 30 минут при температуре окружающей среды. Реакционную смесь разбавляют дихлорметаном, затем промывают последовательно 1 М водным гидроксидом натрия и солевым раствором. Органическую фазу сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 4 г RediSep™ силикагелевый картридж; дихлорметан - 3% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C53H61N5O7) 780 [М-Вос+Н]+; RT 1.60 (Метод В)
Стадия С: (1r,4r)-4-{[(трет-Бутокси)карбонил]амино}циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору продукта из Стадии B (96 мг, 0.11 ммоль) в этаноле (5 мл) добавляют 10% Pd/C (каталитическое количество) и смесь встряхивают в атмосфере водорода в течение прибл. 16 ч. Смесь фильтруют через целит, элюируют метанолом, и фильтрат концентрируют в вакууме. Очистка с помощью колоночной флэш-хроматографии (CombiFlash Rf, 4 г RediSep™ силикагелевый картридж; дихлорметан - 5% метанол в дихлорметане) дает целевой продукт.
ЖХ/МС (C46H55N5O7) 790 [М+Н]+; RT 1.43 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H55N5O7
[М+Н]+ рассчитано: 790.4174
[М+Н]+ найдено: 790.4166
Пример 801: Гидрохлорид (1r,4r)-4-аминоциклогексил 6-{4-[(4-гидроксифеннл)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата
Продукт из Примера 800 (48 мг, 0.06 ммоль) растворяют в 4 М HCl в 1,4-диоксане (5 мл) и перемешивают при температуре окружающей среды в течение прибл. 15 мин. Реакционную смесь концентрируют в вакууме с получением твердого вещества, которое суспендируют в эфире и перемешивают в течение 1 ч при 0°C. Твердое вещество фильтруют, промывают эфиром и сушат в вакууме с получением целевого продукта.
ЖХ/МС (C41H47N5O5) 690 [М+Н]+; RT 1.10 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C41H47N5O5
[М+2Н]2+ рассчитано: 345.6861
[М+2Н]2+ найдено: 345.6864
Пример 802: (1r,4r)-4-(Диметиламино)циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
К раствору продукта из Примера 801 (20 мг, 0.03 ммоль, 1 экв.) в метаноле (2 мл) добавляют параформальдегид (4 мг, 0.14 ммоль), уксусную кислоту (8 мкл, 0.14 ммоль, 5 экв.) и цианоборогидрид натрия (9 мг, 0.14 ммоль), и смесь перемешивают при температуре окружающей среды в течение прибл. 16 ч. Реакцию гасят путем добавления воды (1 мл) и экстрагируют дихлорметаном. Органический экстракт промывают последовательно водой, и солевым раствором, и затем сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Очистка с помощью препаративной ЖХВР (H2O-ТФУ/ацетонитрил; градиентное элюирование) дает целевой продукт
ЖХ/МС (C43H51N5O5) 718 [М+Н]+; RT 1.10 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C43H51N5O5
[М+2Н]2+ рассчитано: 359.7018
[М+2Н]2+ найдено: 359.7017
Пример 803: 4-(N-Метилацетамидо)фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 709 с заменой бензил 3-гидроксибензоата из Стадии B на N-(4-гидроксифенил)-N-метилацетамид.
ЖХ/МС (C48H52N6O7) 825 [М+Н]+; RT 1.07 (Метод В)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C48H52N6O7
[М+2Н]2+ рассчитано: 413.2022
[М+2Н]2+ найдено: 413.2031
Пример 804: 4-[2-(Диметилкарбамоил)этил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 709 с заменой продукта из Синтеза 6bа на Стадии A на продукт из Синтеза 6bb, и с заменой бензил 3-гидроксибензоата из Стадии B на 3-(4-гидроксифенил)-N,N-диметилпропанамид.
ЖХ/МС (C46H49N5O6) 384 [М+2Н]2+; RT 2.49 (Метод А)
Масс-спектроскопия высокого разрешения (ESI+):
Эмпирическая формула: C46H49N5O6
[М+2Н]2+ рассчитано: 384.6914
[М+2Н]2+ найдено: 384.6933
Пример 805: Гидрохлорид толил 6-[4-[(5-циано-1,2-диметил-1H-пиррол-3-ил)-(4-гидроксифенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил]-7-[(3S)-3-(морфолинометил)-3,4-дигидро-1H-изохинолин-2-карбонил]-3,4-дигидро-1H-изохинолин-2-карбоксилата
Стадия A: Бензил 7-формил-6-(4-этоксикарбонил-1,5-диметил-1Н-пиррол-2-ил)-3,4-дигидро-1Н-изохинолин-2-карбоксилат
К раствору 1.3 г этил 1,2-диметил-1H-пиррол-3-карбоксилата (7.97 ммоль) в 15 мл N,N-диметилацетамида последовательно добавляют 2.5 г бензил 6-бром-7-формил-3,4-дигидро-1H-изохинолин-2-карбоксилата (6.64 ммоль), 1.3 г ацетата калия (13.3 ммоль), и затем загрузку перемешивают в атмосфере аргона в течение 20 минут. Затем добавляют 0.2 г палладиевого катализатора PbCl2(PPh3)2 (0.33 ммоль). Затем реакционную смесь нагревают при 85°C в течение 4.5 часов. Температуре смеси дают вернуться к температуре окружающей среды и затем смесь разбавляют этилацетатом. После фильтрования органическую фазу промывают насыщенным водным раствором хлорида натрия, сушат над сульфатом магния, фильтруют и концентрируют досуха. Полученный таким образом сырой продукт очищают с помощью хроматографии на силикагеле (градиент петролейный эфир/этил ацетат). Указанный в заголовке продукт получают в виде желтой пены.
1Н ЯМР (400 МГц, ДМСО-d6) δ м.д.: 9.78 (s, 1 Н), 7.78 (s, 1 Н), 7.45-7.3 (m, 5 Н), 7.32 (s, 1 Н), 6.39 (s, 1 Н), 5.14 (s, 2 Н), 4.72 (m, 2 Н), 4.18 (q, 2 Н), 3.68 (m, 2 Н), 3.31 (s, 3 Н), 2.93 (t, 2 Н), 2.55 (s, 3 Н), 1.25 (t, 3 Н)
Стадия В: 2-Бензилоксикарбонил-6-(4-этоксикарбонил-1,5-диметил-1Н-пиррол-2-ил)-3,4-дигидро-1Н-изохинолин-7-карбоновая кислота
Приготавливают раствор, содержащий 1.3 г соединения, полученного на Стадии A, (2.82 ммоль) и 2.4 мл (22.6 ммоль) 2-метил-2-бутена в смеси, состоящей из 2.5 мл ацетона и 2.5 мл тетрагидрофурана. По каплям при 0°C добавляют 20 мл водного раствора, содержащего смесь 0.64 г NaClO2 (7.05 ммоль) и 1.4 г NaHPO4 (9.88 ммоль). Загрузку затем энергично перемешивают при температуре окружающей среды в течение 16 часов. Затем реакционную смесь концентрируют для удаления ацетона и тетрагидрофурана. Добавляют этилацетат и органическую фазу промывают водой и затем насыщенным водным раствором хлорида натрия, сушат над сульфатом магния, фильтруют и концентрируют досуха. Полученную желтую пену затем используют без очистки каким-либо иным способом.
1H ЯМР (400 МГц, ДМСО-d6) δ м.д.: 12.75 (m, 1 Н), 7.69 (s, 1 Н), 7.44-7.3 (m, 5 Н), 7.14 (s, 1 Н), 6.2 (s, 1 Н), 5.14 (s, 2 Н), 4.67 (m, 2 Н), 4.15 (q, 2 Н), 3.67 (m, 2 Н), 3.21 (s, 3 Н), 2.86 (m, 2 Н), 2.49 (s, 3 Н), 1.24 (t, 3 Н)
Стадия C: Бензил 6-(4-этоксикарбонил-1,5-диметил-1Н-пиррол-2-ил)-7-[(3S)-3-(морфолинометил)-3,4-дигидро-1Н-изохинолин-2-карбонил]-3,4-дигидро-1Н-изохинолин-2-карбоксилат
К раствору 1.5 г соединения, полученного на Стадии B, (2.49 ммоль) в 13 мл дихлорметана добавляют 0.636 г 4-[[(3S)-1,2,3,4-тетрагидроизохинолин-3-ил]метил]морфолина (2.74 ммоль), 1.1 мл N,N,N-триэтил амина (7.47 ммоль), 0.51 г 1-этил-3-(3'-диметиламинопропил)-карбодиимида (EDC) (2.99 ммоль) и затем 0.4 г гидроксибензотриазола (НОВТ) (2.99 ммоль).. Реакционную смесь перемешивают при температуре окружающей среды в течение 16 часов и затем разбавляют смесью дихлорметана и насыщенного раствора гидрокарбоната натрия. После разделения фаз органическую фазу сушат над сульфатом магния, фильтруют и упаривают досуха. Полученный таким образом сырой продукт затем очищают с помощью хроматографии на силикагеле (градиент дихлорметан/этилацетат). Продукт получают в виде белой пены.
1H ЯМР (500 МГц, ДМСО-d6) δ м.д.: 7.4-7.3 (m, 5 Н), 7.25-7.15 (4*s, 2 Н), 7.2-6.9 (m, 4 Н), 6.32/6.28/6.1 (3*bs, 1 Н), 5.15 (3*s, 2 Н), 5.15/4.85/3.7 (3*m, 1 Н), 5-4 (m, 2 Н), 4.7 (m, 2 Н), 4.1 (m, 2 Н), 3.78/3.6 (2*m, 2 Н), 3.6-3.4 (m, 4 Н), 3.45/3.39/3.2 (3*s, 3 Н), 3-2.45 (m, 2 Н), 2.9 (m, 2 Н), 2.5-1.9 (4*m, 4 Н), 2.5/2.41/2.05 (4*bs, 3 Н), 2.35-1.7 (m, 2 Н), 1.2/1.1 (3*t, 3 Н)
13С ЯМР (500 МГц, ДМСО-d6) δ м.д.: 130/125, 129-126, 128, 110, 66.5, 66.5, 59, 57.5, 53.5, 49.5/44.5/43, 45.5, 44.5/41, 41.5, 31.5, 30/29, 28, 15, 11.5
Стадия D: 1,2-Диметил-5-[7-[(3S)-3-(морфолинометил)-3,4-дигидро-1Н-изохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-1Н-пиррол-3-карбоновая кислота
К раствору 1.1 г соединения, полученного на Стадии C, (1.59 ммоль) в 8 мл этанола добавляют 0.9 мл 5 н. водного раствора гидроксида натрия (4.77 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение 24 часов при 80°C и выполняют второе добавление 0.9 мл 5 н. водного раствора гидроксида натрия. После выдерживания смеси в течение 24 часов при такой же температуре, эту операцию осуществляют второй раз. Затем этанол упаривают и реакционную смесь разбавляют водой, и затем добавляют 1 н. водный раствор соляной кислоты до достижения pH 7. После экстрагирования водной фазы дихлорметаном органические фазы объединяют и концентрируют досуха с получением указанного в заголовке продукта в виде желтой пены.
1Н ЯМР (500 МГц, ДМСО-d6) δ м.д.: 7.2-6.9 (т, 4 Н), 7.05/7 (2*s, 2 Н), 6.31/6.25/6.1 (3*s, 1 Н), 5.1/4.85/3.7 (3*m, 1 Н), 4.15/4.1 (m, 2 Н), 3.91/3.81 (bs+dd, 2 Н), 3.6-3.4 (m, 4 Н), 3.4/3.35/3.15 (3*s, 3 Н), 3-2.9 (m, 2 Н), 2.9-1.9 (m, 2 Н), 2.75 (m, 2 Н), 2.5/2.4/1.98 (3*s, 3 Н), 2.5-1.9 (m, 6 Н)
13С ЯМР (500 МГц, ДМС-d6) δ м.д.: 130/125, 129-126, 110.5, 66.5, 57/54, 49.5/44.5/43, 47.5, 44, 43.5, 32, 30, 29, 11.5
Стадия Е: 1,2-Диметил-5-[2-(4-метилфенокси)карбонил-7-[(3S)-3-(морфолинометил)-3,4-дигидро-1Н-изохинолин-2-карбонил]-3,4-дигидро-1Н-изохинолин-6-ил]-1Н-пиррол-3-карбоновая кислота
К раствору 0.35 г соединения, полученного на Стадии D, (0.66 ммоль) в 1 мл диоксана при 0°C добавляют 0.33 мл 2 н. водного раствора гидроксида натрия (0.66 ммоль) и, несколькими порциями каждого, 0.106 мл n-толилхлорформиата (0.73 ммоль) и 0.36 мл 2 н. водного раствора гидроксида натрия (0.73 ммоль). Реакционную смесь перемешивают в течение 2 часов при температуре окружающей среды и затем разбавляют водой и экстрагируют дихлорметаном. Водную фазу подкисляют и затем экстрагируют дихлорметаном. Органические фазы объединяют, сушат над сульфатом магния, фильтруют и концентрируют.
Полученный остаток вносят в 12 мл метанола и 3.2 мл 1 н. водного раствора гидроксида калия (3.26 ммоль) и затем реакционную смесь перемешивают при температуре окружающей среды в течение 20 минут. После добавления 0.1 н. водного раствора соляной кислоты до достижения pH 4 смесь экстрагируют дихлорметаном. Органические фазы объединяют, промывают насыщенным водным раствором хлорида натрия, сушат над сульфатом магния, фильтруют и концентрируют. Остаток затем вносят в смесь дихлорметана и изопропилового эфира. Затем полученное твердое вещество отфильтровывают и промывают эфиром. Указанный в заголовке продукт получают в виде твердого вещества, которое затем используют без очистки каким-либо иным способом.
1H ЯМР (500 МГц, ДМСО-d6) δ м.д; 11.5 (bs, 1 Н), 7.28 (bs, 1 Н), 7.2-6.9 (m, 4 Н), 7.2 (bd, 2 Н), 7.02 (bd, 2 Н), 6.88 (bs, 1 Н), 6.35/6.28/6.12 (3*s, 1 Н), 5.11/4.85/3.7 (3*m, 1 Н), 4.85-4.65 (m, 2 Н), 4.8-4.1 (m, 2 Н), 4.2-3.6 (m, 2 Н), 3.6-3.4 (m, 4 Н), 3.45/3.4/3.18 (3*s, 3 Н), 3-1.8 (m, 2 Н), 2.97 (мл, 2 Н), 2.5/2.41/1.99 (4*s, 3 Н), 2.5-1.9 (4*m, 4 Н), 2.35/2.18 (2*m, 2 Н), 2.25 (bs, 3 Н)
13С ЯМР (500 МГц, ДMCO-d6) δ м.д.: 130, 129, 129-126, 125, 122, 110.5, 66.5, 58, 54, 49.5/44/43, 45.5, 44.5/41.5, 41.5, 32, 30-29, 28, 20.5, 11
Стадия F: Гидрохлорид толил 6-[4-[(5-циано-1,2-диметил-1Н-пиррол-3-ил)-(4-гидроксифенил)карбамоил]-1,5-диметил-1Н-пиррол-2-ил]-7-[(3S)-3-(морфолинометил)-3,4-дигидро-1Н-изохинолин-2-карбонил]-3,4-дигидро-1Н-изохинолин-2-карбоксилата
К раствору 0.232 г соединения, полученного на Стадии E, (0.35 ммоль) в 9 мл дихлорэтана добавляют 0.05 мл 1-хлор-N,N,2-триметилпроп-1-ен-1-амина (0.385 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение 2 часов и затем добавляют 0.131 г 4-[4-[трет-бутил(диметил)силил]оксианилино]-1,5-диметил-1H-пиррол-2-карбонитрила (0.385 ммоль, продукт из Синтеза 3f). Загрузку перемешивают при 80°C в течение ночи. Реакционную смесь разбавляют смесью дихлорметана и насыщенного водного раствора гидрокарбоната натрия. После разделения фаз органическую фазу сушат над сульфатом магния, фильтруют и концентрируют досуха. Полученный таким образом сырой продукт затем используют без очистки каким-либо иным способом.
К раствору полученного таким образом соединения в 1.8 мл тетрагидрофурана добавляют 0.53 мл 1 н. раствора фторида тетрабутиламмония в тетрагидрофуране (13.5 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение 1 часа и затем разбавляют смесью дихлорметана и насыщенного водного раствора гидрокарбоната натрия. Водную фазу экстрагируют дихлорметаном и затем органические фазы объединяют, сушат над сульфатом магния, фильтруют и концентрируют. Сырой продукт затем очищают с помощью хроматографии на силикагеле (градиент дихлорметан/метанол). Полученное таким образом твердое вещество превращают в форму гидрохлорида, растворенную в смеси ацетонитрила и воды, фильтруют и затем лиофилизуют для выделения указанного в заголовке продукта.
Масс-спектроскопия высокого разрешения (ESI/FIA/BP и МС/МС):
Эмпирическая формула: C52H53N7O6
[М+Н]+ рассчитано: 872.4130
[М+Н]+ найдено: 872.4130
Элементный микроанализ: (%, теоретическое значение: найдено)
%С=68.75:68.07; %Н=5.99:5.90; %N=10.79:10.68; %Cl-=3.90:3.84
Пример 806: N-(4-Гидроксифенил)-5-(2-[(2S)-2-гидрокси-2-фенилацетил]-6-{[(3R)-3-метил-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-2,3-дигидро-1H-изоиндол-5-ил)-N,1,2-триметил-1H-пиррол-3-карбоксамид
Пример 807: Циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-[2-(морфолин-4-ил)этил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bс, и с заменой фенилацетилхлорида на циклогексилхлорформиат.
ЖХ/МС (C46H55N5O6) 774 [М+Н]+; RT 1.22 (Метод В)
Пример 808: Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3)4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на продукт из Синтеза 6bd; и с заменой фенилацетилхлорида на Стадии A на фенилхлорформиат.
ЖХ/МС (C47H51N5O6) 782 [М+Н]+; RT 1.15 (Метод В)
Пример 809: Циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 777 с заменой соединения из Синтеза 6bе на Стадии A на соединение из Синтеза 6bd, и с заменой фенилацетилхлорида на циклогексилхлорформиат.
ЖХ/МС (C47H57N5O6) 788 [М+Н]+; RT 1.21 (Метод В)
Пример 810: Фенил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Пример 811: Циклогексил 6-{1,5-диметил-4-[метил(фенил)карбамоил]-1H-пиррол-2-ил}-7-[(3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат
Методика соответствует методике Примера 114 с заменой продукта из Синтеза 6cb на продукт из Синтеза 6cd, и с заменой фенилхлорформиата на циклогексилхлорформиат.
ЖХ/МС (C47H57N5O5) 772 [М+Н]+; RT 1.33 (Метод В)
ФАРМАКОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ
ПРИМЕР А: Ингибирование Всl-2 с использованием методики поляризации Флуоресценции
Исследования с применением поляризации флуоресценции осуществляют на микропланшетах (384 луночных). Меченый белок Bcl-2 (histag-Bcl-2 такой, что Bcl-2 соответствует UniProtKB® первичному номеру доступа: Р10415), в конечной концентрации 2.50×10-8 М, смешивают с флуоресцентным пептидом (Fluorescein-REIGAQLRRMADDLNAQY) в конечной концентрации 1.00×10-8 М в буферном растворе (Hepes 10 мМ, NaCl 150 мМ, Tween20 0.05%, pH 7.4), в присутствии или отсутствии возрастающих концентраций исследуемых соединений. После инкубирования в течение 2 часов измеряют поляризацию флуоресценции.
Результаты выражены в IC50 (концентрация соединения, которая ингибирует поляризацию флуоресценции на 50%) и приведены в таблице 1 ниже.
Результаты показывают, что соединения изобретения ингибируют взаимодействие между белком Bcl-2 и флуоресцентным пептидом, описанным выше.
ПРИМЕР B: In vitro цитотоксичность
Исследования цитотоксичности осуществляют на линии клеток лейкозной опухоли RS4;11 и на линии клеток мелкоклеточной карциномы легких Н146. Клетки распределяют на микропланшетах и подвергают воздействию исследуемых соединений в течение 48 часов. Жизнеспособность клеток затем определяют количественно путем колориметрического анализа, анализа микрокультур с использованием тетразолия (Cancer Res., 1987, 47, 939-942).
Результаты выражены в IC50 (концентрация соединения, которая ингибирует жизнеспособность клеток на 50%) и приведены в таблице 1 ниже.
Результаты показывают, что соединения изобретения являются цитотоксичными.
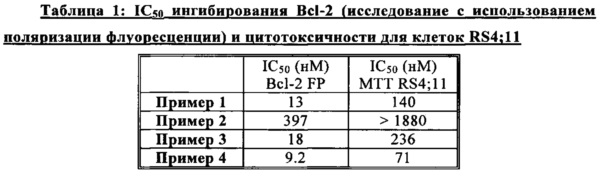
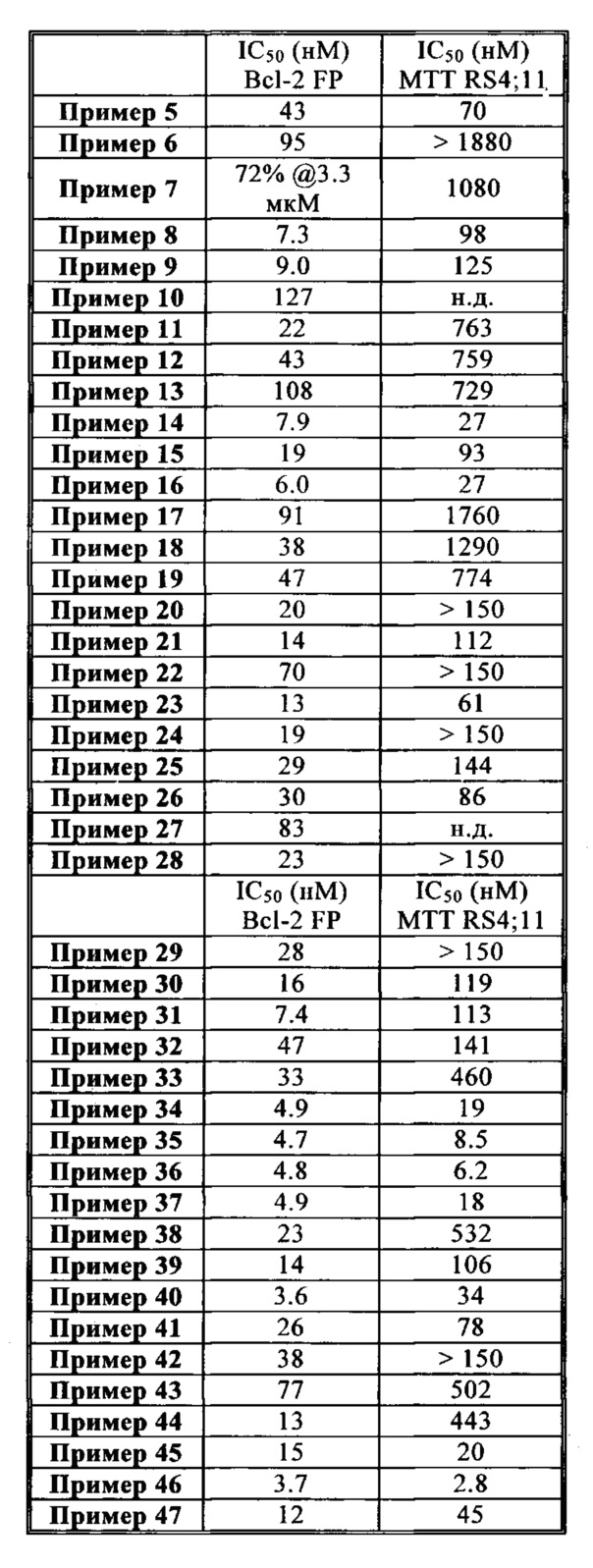
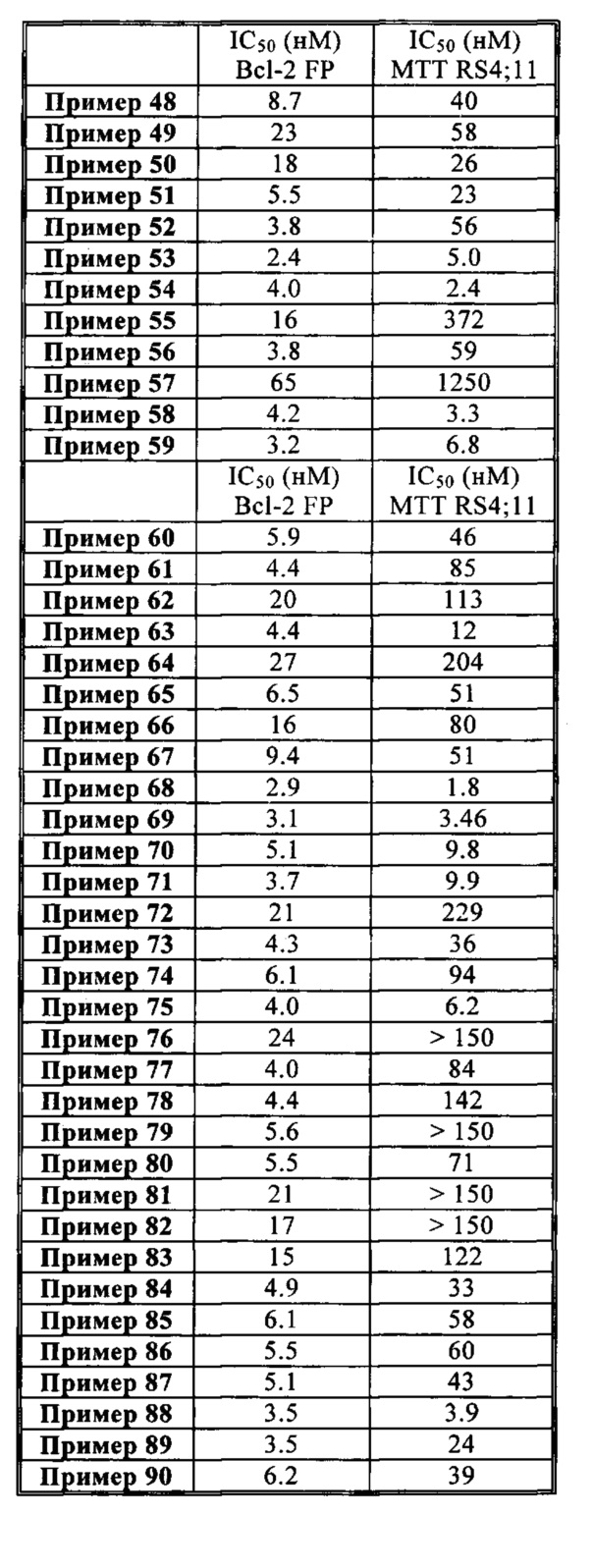
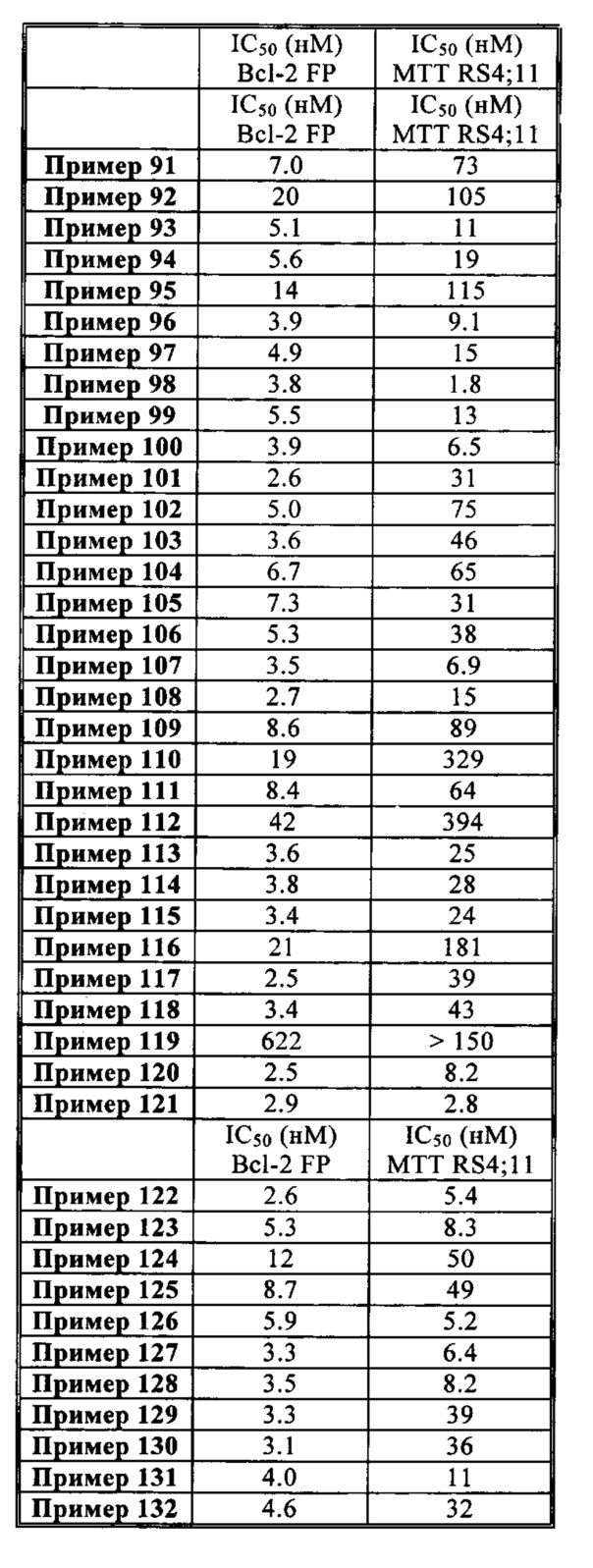
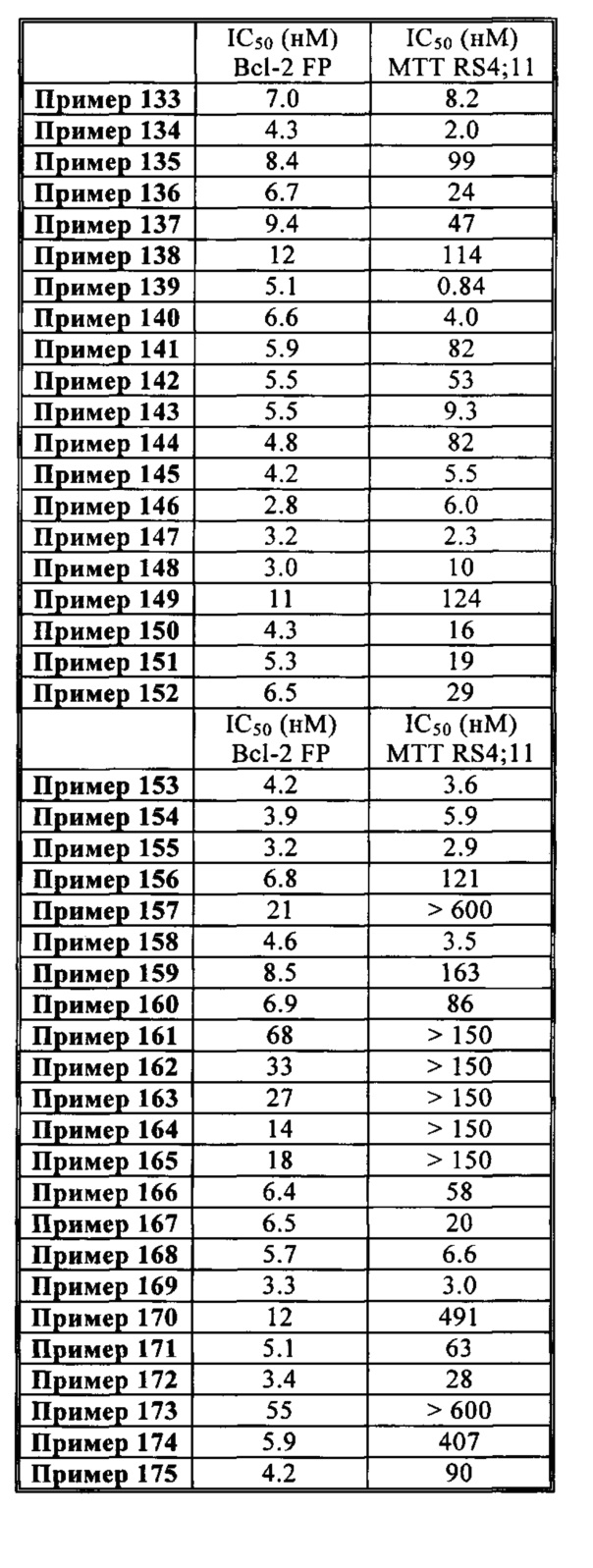
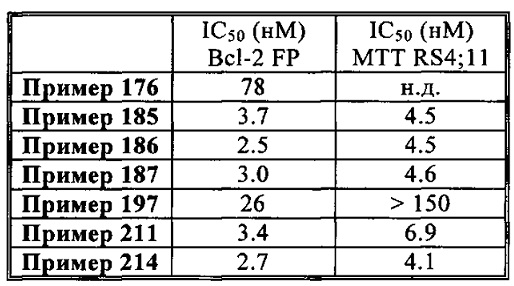
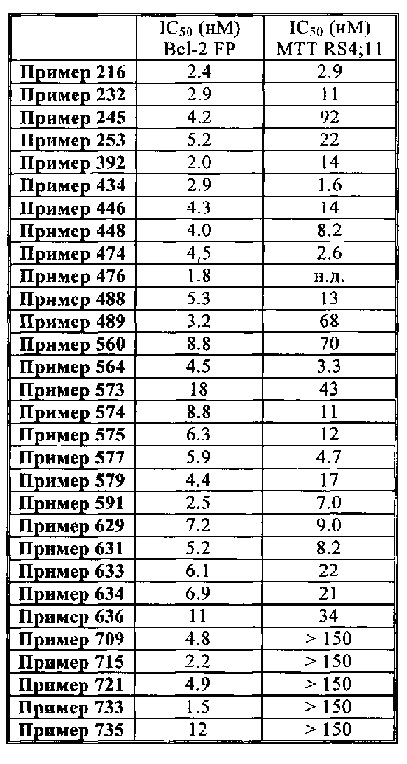
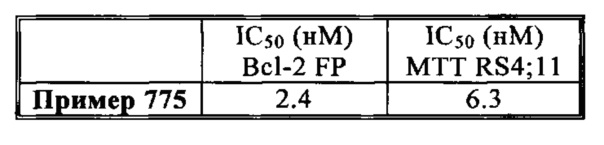
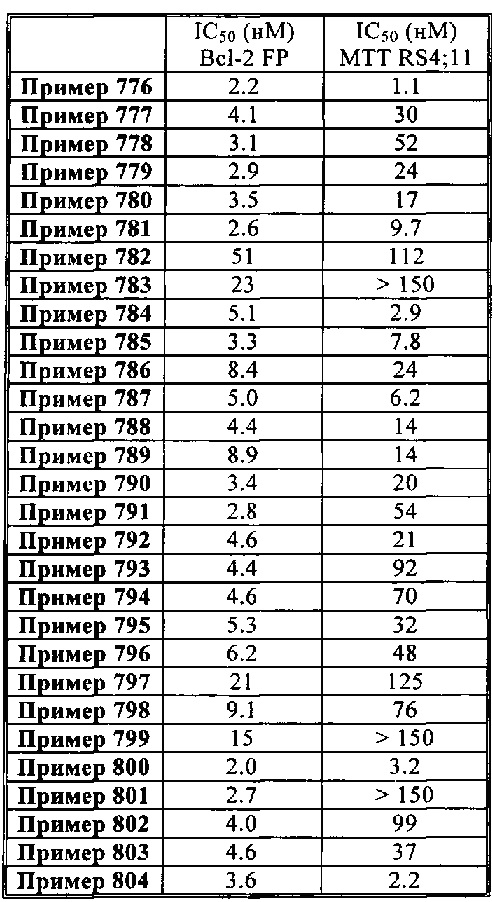
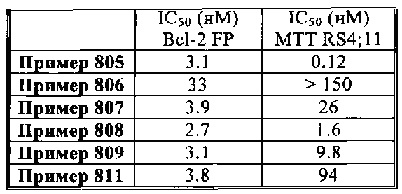
н.д.: не определено.
Для частичных ингибиторов указано процентное значение ингибирования поляризации флуоресценции для приведенной концентрации исследуемого соединения. Соответственно, 72% 3.3 мкМ означает, что 72%-ное ингибирование поляризации флуоресценции наблюдается для концентрации исследуемого соединения, равной 3.3 мкМ.
ПРИМЕР С: Индукция активности каспазы in vivo
Способность соединений изобретения активировать каспазу 3 оценивают на ксенотрансплантатной модели лейкозных клеток RS4;11.
1×107 клеток RS4;11 трансплантируют под кожу иммуносупрессивным мышам (штамм SCID). Через 25-30 дней после трансплантации животные перорально получают лечение различными соединениями. Через шестнадцать часов после введения опухолевые массы извлекают и лизируют, и в опухолевых лизатах измеряют активность каспазы 3.
Данное ферментативное измерение осуществляют путем анализа появления флуоригенного продукта расщепления (DEVD-азная активность, Promega). Оно выражается в виде фактора активации, который равняется соотношению между двумя активностями каспазы: активности у мышей, получающих лечение, деленной на активность у контрольных мышей.
Результаты показывают, что соединения изобретения способны индуцировать апоптоз in vivo в опухолевых клетках RS4;11.
ПРИМЕР D: Количественное определение расщепленной формы каспазы 3 in vivo
Способность соединений изобретения активировать каспазу 3 оценивают на ксенотрансплантатной модели лейкозных клеток RS4; 11.
1×107 клеток RS4;11 трансплантируют под кожу иммуносупрессивным мышам (штамм SCID). Через 25-30 дней после трансплантации животные перорально получают лечение различными соединениями. После лечения опухолевые массы извлекают и лизируют, и количественно определяют расщепленную (активированную) форму каспазы 3 в опухолевых лизатах.
Количественное определение осуществляют с использованием исследования "Meso Scale Discovery (MSD) ELISA platform", которое предназначено для проведения специфического анализа на расщепленную форму каспазы 3. Оно выражается в виде фактора активации, который равняется соотношению между количеством расщепленной каспазы 3 у мышей, получающих лечение, и количеством расщепленной каспазы 3 у контрольных мышей.
Результаты показывают, что соединения изобретения способны индуцировать апоптоз in vivo в опухолевых клетках RS4;11.
ПРИМЕР Е: Антиопухолевая активность in vivo
Антиопухолевую активность соединений изобретения оценивают на ксенотрансплантатной модели лейкозных клеток RS4;11.
1×107 клеток RS4;11 трансплантируют под кожу иммуносупрессивным мышам (штамм SCID). Через 25-30 дней после трансплантации, когда опухолевая масса достигнет приблизительно 150 мм3, мышей лечат пероральным путем различными соединениями в двух различных режимах (ежедневное введение в течение пяти дней в неделю в течение двух недель, или два введения в неделю в течение двух недель). Опухолевую массу измеряют дважды в неделю с начала лечения.
Полученные результаты, следовательно, показывают, что соединения изобретения способны индуцировать значительную регрессию опухолей в течение периода лечения.
ПРИМЕР F: Фармацевтическая композиция: Таблетки

| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПИРРОЛЬНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2607788C2 |
| НОВЫЕ ИНДОЛИЗИНОВЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2693629C2 |
| НОВЫЕ ФОСФАТНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2617682C2 |
| НОВЫЕ ИНДОЛИЗИНОВЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2013 |
|
RU2646223C2 |
| НОВЫЕ ИНДОЛЬНЫЕ И ПИРРОЛЬНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2693404C2 |
| НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ ФАМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2018 |
|
RU2808689C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ КАРБОНУКЛЕОЗИДА, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕ ПРОТИВОРАКОВЫХ АГЕНТОВ | 2017 |
|
RU2712944C1 |
| ПРОИЗВОДНЫЕ 8-КАРБАМОИЛ-2-(2,3-ДИЗАМЕЩЕННОГО ПИРИД-6-ИЛ)-1,2,3,4-ТЕТРАГИДРОИЗОХИНОЛИНА В КАЧЕСТВЕ ИНДУЦИРУЮЩИХ АПОПТОЗ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ РАКА | 2012 |
|
RU2625315C2 |
| АНТИТЕЛА К В7-Н3 И КОНЪЮГАТЫ АНТИТЕЛА И ЛЕКАРСТВЕННОГО СРЕДСТВА | 2017 |
|
RU2764651C2 |
| СОСТАВ ИНГИБИТОРА BCL-2 НА ОСНОВЕ ЦИКЛОДЕКСТРИНА | 2019 |
|
RU2804366C2 |
Изобретение относится к области органической химии, а именно к гетероциклическому соединению общей формулы (I) или к его энантиомеру, диастереоизомеру, его соли присоединения с фармацевтически приемлемой кислотой, где Het представляет собой 5,6,7,8-тетрагидроиндолизин, индолизин, 1,2-диметил-1H-пиррол; Т представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу или алкил(C1-C4)-NR1R2 группу, R1 и R2 представляют собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу, или R1 и R2 вместе с атомом азота, несущим их, образуют гетероциклоалкильную группу, которая представляет собой морфолин или пиперазин, R3 представляет собой линейную или разветвленную (C1-С6)алкильную группу, арильную группу или гетероарильную группу, которая представляет собой пиррольную группу или пирроло[2,3-b]пиридинильную группу, R4 представляет собой арильную или линейную или разветвленную (С1-С6)алкильную группу, R5 представляет собой атом водорода, R7 представляет собой группу R'7, R'7-CO-, R'7-O-СО-, NR'7R''7-CO-, R'7-SO2-, где R'7 и R''7 представляют собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, которая необязательно замещена 1-2 группами, выбранными из: (i) гетероарильной группы, необязательно замещенной пиразин-2-ильной группой, (ii) арильной группы, арилокси группы, ариламино группы или арилтио группы, где арил и арилокси группы, необязательно замещены одним или двумя атомами галогена, или группой, выбранной из: метильной группы, [2-(морфолин-4-ил)этил]амино группы, [2-(диметиламино)этил]амино группы, [2-(диметиламино)этокси] группы, диметиламинометил группы, морфолинил-СН2 группы, (4-метилпиперазин-1-ил)-СН2 группы, трифторметокси группы; метокси группы; циано группы или (4-метилпиперазин-1-ил) группы; (iii) фенилкарбамоильной группы, (iv) циклоалкила, (v) гетероциклоалкила, (vi) бензилокси группы, (vii) -NH2 или гидрокси; линейную или разветвленную (С2-С6)алкенильную группу, которая замещена арильной группой, где арильная группа необязательно замещена одним или двумя атомами галогена или метокси группой, трифторметильную группу, циклоалкил, гетероциклоалкил; арильную группу; (4-метилпиперазин-1-ил)фенильную группу, или гетероарил, р=р'=0, q=1 или 2 и q'=1, при этом также предполагается, что: "арил" означает фенильную или нафтильную группу, "гетероарил" означает любую моно- или бициклическую группу, состоящую из 5-10 кольцевых членов, содержащую по меньшей мере один ароматический фрагмент, и содержащую от 1 до 4 гетероатомов, выбранных из кислорода, серы и азота, "циклоалкил" означает любую моно- или бициклическую, неароматическую, карбоциклическую группу, содержащую от 3 до 10 кольцевых членов, которая может включать конденсированные или мостиковые кольцевые системы, "гетероциклоалкил" означает любую моно- или бициклическую, неароматическую, карбоциклическую группу, состоящую из 4-10 кольцевых членов, и содержащую от 1 до 2 гетероатомов, выбранных из кислорода, серы, SO, SO2 и азота, причем арильные, гетероарильные, циклоалкильные и гетероциклоалкильные группы, определенные таким образом, и алкильные, алкенильные группы могут быть замещены 1-3 группами, выбранными из: линейной или разветвленной (С1-С6)алкильной группы; линейной или разветвленной (С2-С6)алкинильной группы; линейного или разветвленного (С1-С6)алкокси; гидроксила; оксо; циано; -COOR'; -NR'R''; R'CONR''-; NR'R''CO-; трифторметила; трифторметокси; галогена; арила; гетероарила; при этом предполагается, что R' и R'' независимо друг от друга представляют собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу. Также изобретение относится к конкретным соединениям, способу получения соединения формулы (I), фармацевтической композиции на основе соединения формулы (I), применению композиции и соединения формулы (I). Технический результат: получены новые гетероциклические соединения, ингибирующие апоптическую активность белков семейства Bcl-2, полезные при лечении злокачественных новообразований, аутоиммунных заболеваний и заболеваний иммунной системы. 13 н. и 15 з.п. ф-лы, 1 табл., 817 пр.
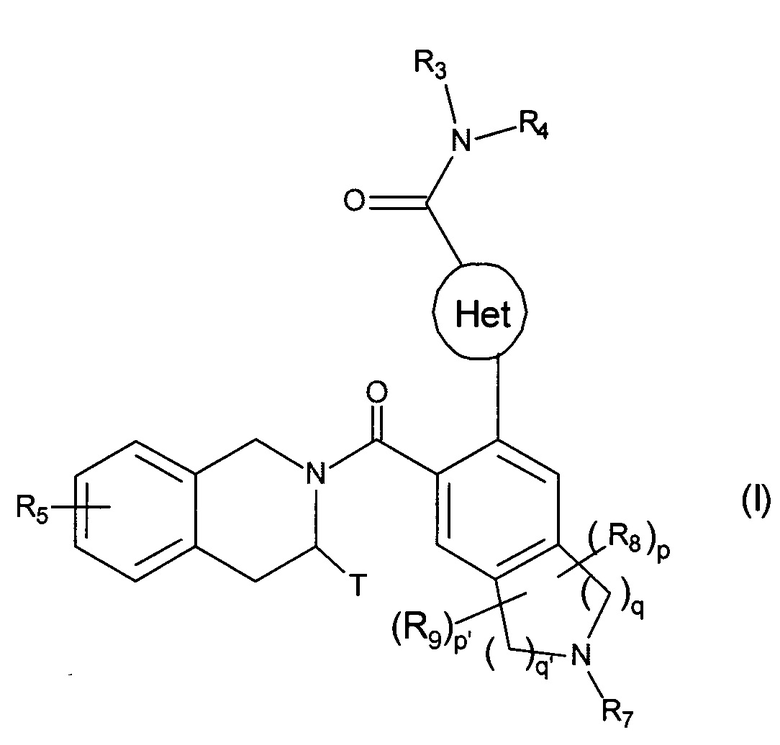
1. Соединение формулы (I):
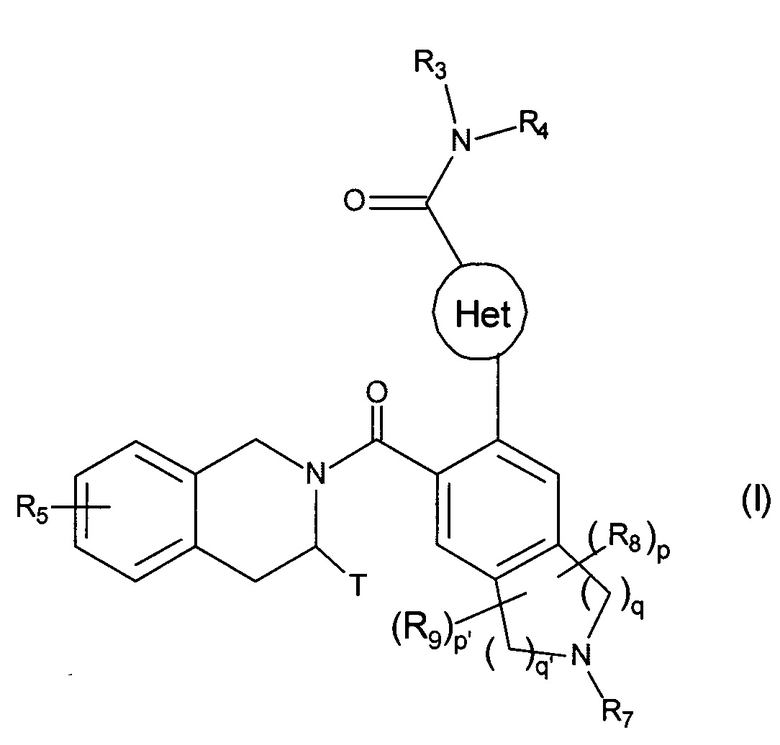
в которой:
 Het представляет собой одну из следующих групп: 5,6,7,8-тетрагидроиндолизин, индолизин или 1,2-диметил-1H-пиррол,
Het представляет собой одну из следующих групп: 5,6,7,8-тетрагидроиндолизин, индолизин или 1,2-диметил-1H-пиррол,
 Т представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу или алкил(C1-C4)-NR1R2 группу,
Т представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу или алкил(C1-C4)-NR1R2 группу,
 R1 и R2 независимо друг от друга представляют собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
R1 и R2 независимо друг от друга представляют собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
или R1 и R2 вместе с атомом азота, несущим их, образуют гетероциклоалкильную группу, которая представляет собой морфолин или пиперазин,
 R3 представляет собой линейную или разветвленную (C1-С6)алкильную группу, арильную группу или гетероарильную группу, которая представляет собой пиррольную группу или пирроло[2,3-b]пиридинильную группу,
R3 представляет собой линейную или разветвленную (C1-С6)алкильную группу, арильную группу или гетероарильную группу, которая представляет собой пиррольную группу или пирроло[2,3-b]пиридинильную группу,
 R4 представляет собой арильную или линейную или разветвленную (С1-С6)алкильную группу,
R4 представляет собой арильную или линейную или разветвленную (С1-С6)алкильную группу,
 R5 представляет собой атом водорода,
R5 представляет собой атом водорода,
 R7 представляет собой группу, выбранную из R'7, R'7-CO-, R'7-O-СО-, NR'7R''7-CO-, R'7-SO2-, где R'7 и R''7 независимо друг от друга представляют собой:
R7 представляет собой группу, выбранную из R'7, R'7-CO-, R'7-O-СО-, NR'7R''7-CO-, R'7-SO2-, где R'7 и R''7 независимо друг от друга представляют собой:
атом водорода,
линейную или разветвленную (С1-С6)алкильную группу, которая необязательно замещена одной или двумя группами, выбранными из:
(i) гетероарильной группы, необязательно замещенной пиразин-2-ильной группой,
(ii) арильной группы, арилокси группы, ариламино группы или арилтио группы, где арил и арилокси группы, необязательно замещены одним или двумя атомами галогена, или группой, выбранной из: метильной группы, [2-(морфолин-4-ил)этил]амино группы, [2-(диметиламино)этил]амино группы, [2-(диметиламино)этокси] группы, диметиламинометил группы, морфолинил-СН2 группы, (4-метилпиперазин-1-ил)-СН2 группы, трифторметокси группы; метокси группы; циано группы или (4-метилпиперазин-1-ил) группы;
(iii) фенилкарбамоильной группы,
(iv) циклоалкила,
(v) гетероциклоалкила,
(vi) бензилокси группы,
(vii) -NH2 или гидрокси,
- линейную или разветвленную (С2-С6)алкенильную группу, которая замещена арильной группой, где арильная группа необязательно замещена одним или двумя атомами галогена или метокси группой,
- трифторметильную группу,
- циклоалкил,
- гетероциклоалкил,
- арильную группу,
- (4-метилпиперазин-1-ил)фенильную группу, или гетероарил,
 р=р'=0,
р=р'=0,
 q=1 или 2 и q'=1, при этом также предполагается, что:
q=1 или 2 и q'=1, при этом также предполагается, что:
- "арил" означает фенильную или нафтильную группу,
- "гетероарил" означает любую моно- или бициклическую группу, состоящую из 5-10 кольцевых членов, содержащую по меньшей мере один ароматический фрагмент, и содержащую от 1 до 4 гетероатомов, выбранных из кислорода, серы и азота,
- "циклоалкил" означает любую моно- или бициклическую, неароматическую, карбоциклическую группу, содержащую от 3 до 10 кольцевых членов, которая может включать конденсированные или мостиковые кольцевые системы,
- "гетероциклоалкил" означает любую моно- или бициклическую, неароматическую, карбоциклическую группу, состоящую из 4-10 кольцевых членов, и содержащую от 1 до 2 гетероатомов, выбранных из кислорода, серы, SO, SO2 и азота,
причем арильные, гетероарильные, циклоалкильные и гетероциклоалкильные группы, определенные таким образом, и алкильные, алкенильные группы могут быть замещены 1-3 группами, выбранными из: линейной или разветвленной (С1-С6)алкильной группы; линейной или разветвленной (С2-С6)алкинильной группы; линейного или разветвленного (С1-С6)алкокси; гидроксила; оксо; циано; -COOR'; -NR'R''; R'CONR''-; NR'R''CO-; трифторметила; трифторметокси; галогена; арила; гетероарила; при этом предполагается, что R' и R'' независимо друг от друга представляют собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
его энантиомеры и диастереоизомеры, и его соли присоединения с фармацевтически приемлемой кислотой.
2. Соединение формулы (I) по п. 1, в которой q=1 и q'=1.
3. Соединение формулы (I) по п. 1, в которой q=2 и q'=1.
4. Соединение формулы (I) по п. 1, в которой Т представляет собой атом водорода, метильную группу, (морфолин-4-ил)метильную группу, 3-(морфолин-4-ил)пропильную группу, диметиламинометильную группу, или (4-метилпиперазин-1-ил)метильную группу.
5. Соединение формулы (I) по п. 1, в которой R3 представляет собой группу, выбранную из фенила, метила, этила, пропила, бутила, 1-метил-1H-пирроло[2,3-b]пиридина или 5-циано-1,2-диметил-1H-пиррола.
6. Соединение формулы (I) по п. 1, в которой R4 представляет собой фенильную или 4-гидроксифенильную группу.
7. Соединение формулы (I) по п. 1, в которой R7 представляет собой группу R'7-CO- или R'7-O-CO-.
8. Соединение формулы (I) по п. 1, в которой R'7 представляет собой арил, циклоалкил или алкил.
9. Соединение формулы (I) по п. 1, в которой R'7 представляет собой нафталиновую, фенильную или индольную группу.
10. Соединение формулы (I) по п. 9, в которой фенильная группа замещена группой, выбранной из: алкила, циано, алкинила, галогена, алкокси или -NR'R''.
11. Соединение формулы (I) по п. 10, в которой фенильная группа замещена группой, выбранной из: метила, этила, метокси, хлора, брома, циано или этинила.
12. Соединение формулы (I):
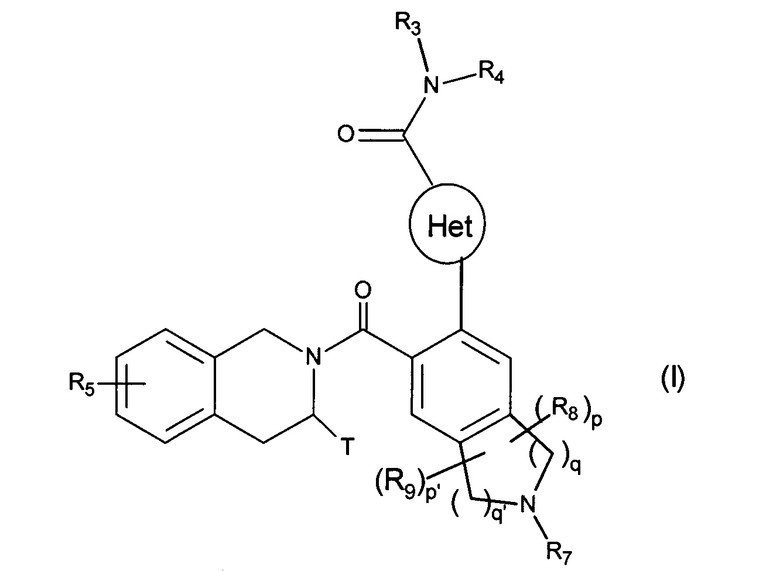
в которой Het, Т, R3-R5, R8-R9, p, p', q, q' определены в пп. 1-6, и R7 представляет собой группу, выбранную из R'7-CO- и R'7-O-CO-, где R'7 представляет собой фенильную группу, которая замещена группой, выбранной из: 2-диметиламиноэтиламина, 2-диметиламиноэтокси, 2-(диметиламино)этил(метил)амина или диметилкарбамоилэтила, его энантиомеры и диастереоизомеры, и его соли присоединения с фармацевтически приемлемой кислотой.
13. Соединение формулы (I) по п. 1 или 12, которое представляет собой
 N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид;
N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид;
 Фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
Фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 Гидрохлорид фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата;
Гидрохлорид фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата;
 Гидрохлорид фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата;
Гидрохлорид фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата;
 Гидрохлорид 4-метилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата;
Гидрохлорид 4-метилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилата;
 2-Метилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
2-Метилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-Метоксифенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-Метоксифенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-Хлорфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-Хлорфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-Этилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-Этилфенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-Цианофенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-Цианофенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 2-Метоксифенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
2-Метоксифенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-Метилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-Метилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-Хлорфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-Хлорфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-Цианофенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-Цианофенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-Цианофенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-Цианофенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-{[2-(Диметиламино)этил]амино}фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-{[2-(Диметиламино)этил]амино}фенил 6-{1-[(4-гидроксифенил)(метил)карбамоил]-5,6,7,8-тетрагидроиндолизин-3-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 Фенил 6-{4-[(4-гидроксифенил)(пропил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
Фенил 6-{4-[(4-гидроксифенил)(пропил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 Фенил 6-{4-[бутил(4-гидроксифенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
Фенил 6-{4-[бутил(4-гидроксифенил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
Фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-[(4-метилпиперазин-1-ил)метил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 N-Бутил-N-(4-гидроксифенил)-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид;
N-Бутил-N-(4-гидроксифенил)-1,2-диметил-5-{7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-фенилацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-1H-пиррол-3-карбоксамид;
 3-[2-(Диметиламино)этокси]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
3-[2-(Диметиламино)этокси]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-{[2-(Диметиламино)этил](метил)амино}фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-{[2-(Диметиламино)этил](метил)амино}фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-Этинилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил] -1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-Этинилфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил] -1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 Нафталин-2-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
Нафталин-2-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 1H-Индол-5-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
1H-Индол-5-ил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 3-[2-(Диметилкарбамоил)этил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
3-[2-(Диметилкарбамоил)этил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-Бромфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
4-Бромфенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3S)-3-(морфолин-4-илметил)-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат;
 4-[2-(Диметилкарбамоил)этил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат; или
4-[2-(Диметилкарбамоил)этил]фенил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат; или
 Циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат.
Циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-[3-(морфолин-4-ил)пропил]-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат.
14. Соединение, которое выбрано из следующего списка:
 N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[4-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[4-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
 N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-{4-[(4-метилпиперазин-1-ил)метил]фенил}ацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-(2-{4-[(4-метилпиперазин-1-ил)метил]фенил}ацетил)-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
 N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[4-(морфолин-4-илметил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[4-(морфолин-4-илметил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
 3-[2-(2-{4-[(Диметиламино)метил]фенил}ацетил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
3-[2-(2-{4-[(Диметиламино)метил]фенил}ацетил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
 3-[2-(2-{4-[2-(Диметиламино)этокси]фенил}ацетил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
3-[2-(2-{4-[2-(Диметиламино)этокси]фенил}ацетил)-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-6-ил]-N-(4-гидроксифенил)-N-метил-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
 N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[3-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
N-(4-Гидроксифенил)-N-метил-3-{7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-2-{2-[3-(4-метилпиперазин-1-ил)фенил]ацетил}-1,2,3,4-тетрагидроизохинолин-6-ил}-5,6,7,8-тетрагидроиндолизин-1-карбоксамид,
 (1r,4r)-4-{[(трет-Бутокси)карбонил]амино}циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат.
(1r,4r)-4-{[(трет-Бутокси)карбонил]амино}циклогексил 6-{4-[(4-гидроксифенил)(метил)карбамоил]-1,5-диметил-1H-пиррол-2-ил}-7-[(3R)-3-метил-1,2,3,4-тетрагидроизохинолин-2-карбонил]-1,2,3,4-тетрагидроизохинолин-2-карбоксилат.
15. Способ получения соединения формулы (I) по п. 1, который отличается тем, что в качестве исходного вещества применяют соединение формулы (II):
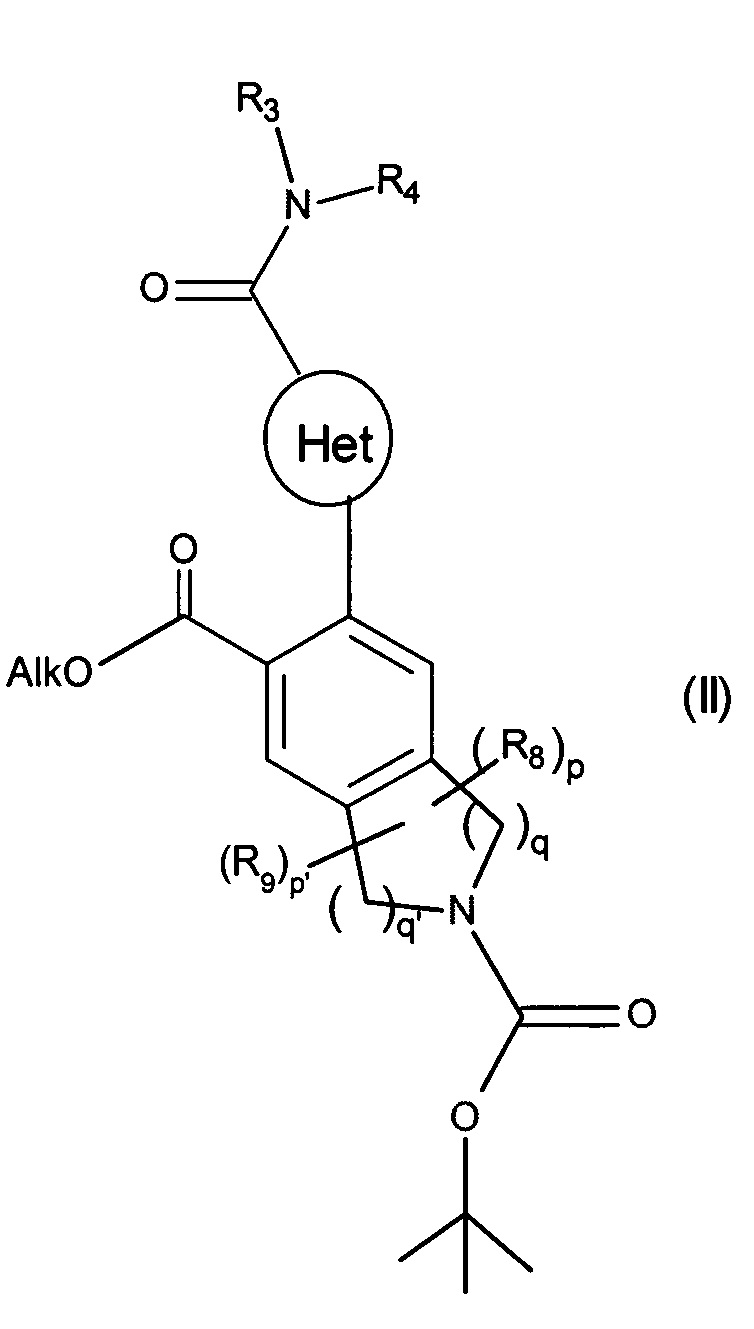
в которой Het, R3, R4, R8, R9, р, р', q и q' являются такими, как определено для формулы (I), и Alk представляет собой линейную или разветвленную (C1-С6) алкильную группу,
причем сложноэфирную группу соединения формулы (II) гидролизуют с получением соответствующей карбоновой кислоты, которую затем подвергают пептидному сочетанию с соединением формулы (III):
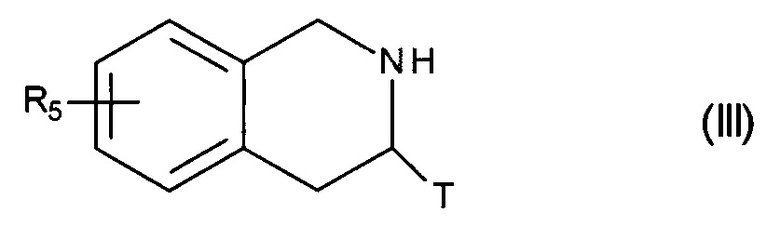
в которой R5 и Т являются такими, как определено для формулы (I), с получением соединения формулы (IV):
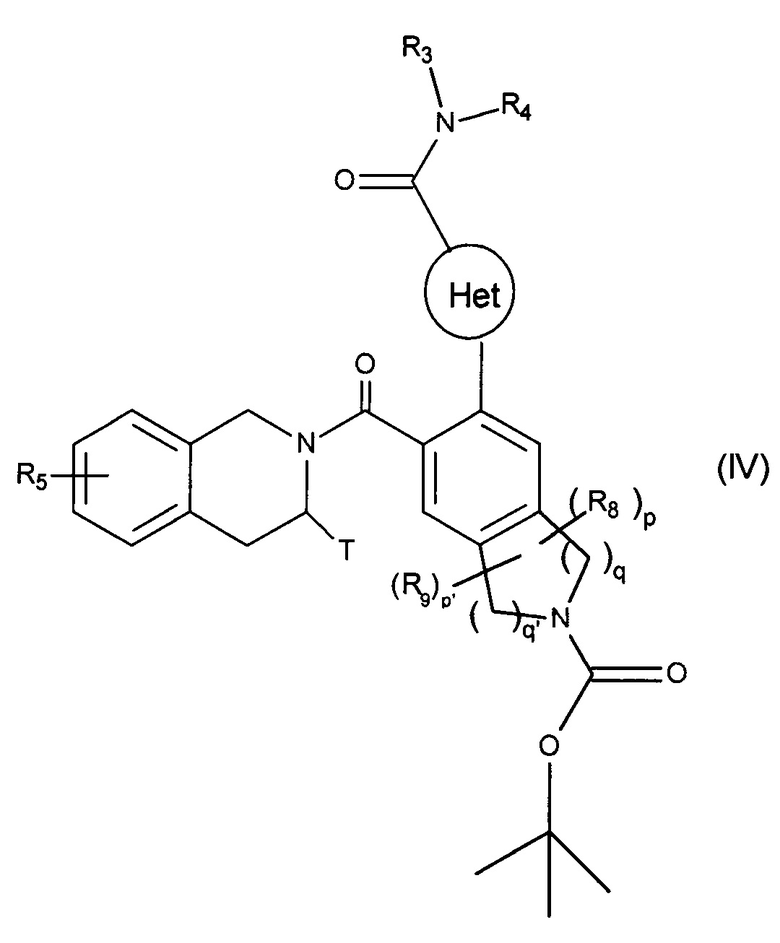
в которой Het, R3, R4, R5, R8, R9, Т, р, р', q и q' являются такими, как определено для формулы (I),
с соединения формулы (IV) снимают защиту и подвергают реакции ацилирования или сульфонилирования с получением соединения формулы (I).
16. Способ по п. 15 получения соединения формулы (I), в которой одна из групп R3 и R4 замещена гидрокси группой, отличающийся тем, что амин NHR3R4 подвергают реакции, защищающей гидрокси группу, заблаговременно перед сочетанием с карбоновой кислотой, образованной из соединения формулы (V), или с соответствующим производным таковой кислоты, где полученную в результате защищенную группу затем подвергают реакции снятия защиты на последней стадии способа.
17. Фармацевтическая композиция ингибирующая антиапоптотическую активность белков семейства Bcl-2, содержащая эффективное количество соединения формулы (I) по любому из пп. 1-14 или его соль присоединения с фармацевтически приемлемой кислотой в комбинации с одним или несколькими фармацевтически приемлемыми наполнителями.
18. Фармацевтическая композиция по п. 17 для применения в качестве проапоптотических агентов.
19. Фармацевтическая композиция по п. 17 для применения для лечения злокачественных новообразований и аутоиммунных заболеваний и заболеваний иммунной системы.
20. Фармацевтическая композиция по п. 17 для применения для лечения рака мочевого пузыря, головного мозга, молочной железы и матки, хронических лимфоидных лейкозов, рака ободочной кишки, пищевода и печени, лимфобластных лейкозов, неходжкинских лимфом, меланом, злокачественных заболеваний крови, миелом, рака яичников, немелкоклеточного рака легкого, рака предстательной железы и мелкоклеточного рака легкого.
21. Применение фармацевтической композиции по п. 17 для изготовления лекарственных средств в качестве проапоптотических агентов.
22. Применение фармацевтической композиции по п. 17 для изготовления лекарственных средств для лечения злокачественных новообразований и аутоиммунных заболеваний и заболеваний иммунной системы.
23. Применение фармацевтической композиции по п. 17 для изготовления лекарственных средств для лечения рака мочевого пузыря, головного мозга, молочной железы и матки, хронических лимфоидных лейкозов, рака ободочной кишки, пищевода и печени, лимфобластных лейкозов, неходжкинских лимфом, меланом, злокачественных заболеваний крови, миелом, рака яичников, немелкоклеточного рака легкого, рака предстательной железы и мелкоклеточного рака легкого.
24. Применение соединения формулы (I) по любому из пп. 1-14, или его соли присоединения с фармацевтически приемлемой кислотой, для изготовления лекарственных средств для лечения рака мочевого пузыря, головного мозга, молочной железы и матки, хронических лимфоидных лейкозов, рака ободочной кишки, пищевода и печени, лимфобластных лейкозов, неходжкинских лимфом, меланом, злокачественных заболеваний крови, миелом, рака яичников, немелкоклеточного рака легкого, рака предстательной железы и мелкоклеточного рака легкого.
25. Фармацевтическая комбинация соединения формулы (I) по любому из пп. 1-14 с противоопухолевым средством, выбранным из генотоксичных средств, митотических ядов, антиметаболитов, ингибиторов протеасом, ингибиторов киназ и антител.
26. Фармацевтическая композиция, содержащая фармацевтическую комбинацию по п. 25 в комбинации с одним или несколькими фармацевтически приемлемыми наполнителями.
27. Применение фармацевтической комбинации по п. 25 для изготовления лекарственных средств для лечения злокачественных новообразований.
28. Применение соединения формулы (I) по любому из пп. 1-14 для изготовления лекарственных средств для лечения злокачественных новообразований в комбинации с радиотерапией.
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| RU 2007128987 A, 27.03.2009. | |||
Авторы
Даты
2019-05-27—Публикация
2014-07-22—Подача