Изобретение относится к медицине, а именно к лабораторной диагностике методами цитохимической экспертизы сукцинатдегидрогеназы (СДГ)* (*Сукциндегидрогеназа - фермент класса оксидоредуктаз (выявляется в лейкоцитах в виде гранул синего цвета) катализирует одну из главных реакций цикла трикарбоновых к-т, является одной из составных частей системы, обеспечивающей в аэробных условиях трансмембранный перенос ионов Na+ в органах.), и может быть использовано для определения оптимального криопротектора на доклиническом этапе криогемотрансфузионной** (** Криогемотрансфузии - трансфузии компонентов крови, смешанных с криопротекторами.) терапии и предупреждения посттрансфузионных осложнений криопротекторного генеза. Для осуществления способа у больного до начала трансфузионной терапии получают порцию венозной крови, делят на равные части в пробирки, в одной из которых контрольная проба крови (КП) не содержит криопротектора, в другие добавляют по одной равной дозе тестируемых криопротекторорв - опытные пробы (ОП), капли ОП и КП наносят в объеме 4 мкл на предметные стекла, из них делают тонкие мазки, высушивают на воздухе, готовят препараты по методике Нахласа в модификации Р.П. Нарциссова*** (*** Справочник по клиническим лабораторным методам исследования под ред. Е.А. Кост. М.: "Медицина", 1975 г.; справочник "Лабораторные методы исследования в клинике" под ред. проф. В.В. Меньшикова. М.: "Медицина", 1987 г.), лейкоциты микроскопируют в проходящем свете, проводят сравнительное исследование среднего цитохимического коэффициента (СЦК) сегментоядерных (с/я) нейтрофилов и лимфоцитов с гранулами синего цвета СДГ ОП и КП. О пригодности тестируемых криопротекторов к использованию (ПКИ) в планируемых криогемотрансфузиях судят по значениям СЦК ОП и СЦК КП. При равности значений СЦК ОП и СЦК КП тестируемый криопротектор оценивают как оптимальный для конкретного больного и пригодный к использованию (ПКИ); при значениях СЦК ОП, отличных от СЦК КП, делают заключение как о непригодном к использованию (НКИ) криопротекторе. Способ прост и доступен врачу по клинической лабораторной диагностике современного онкогематологического центра. Использование предложенного способа позволяет определить in vitro - оптимальный криопротектор на доклиническом этапе и исключить по жизненным показаниям инфузию непригодного для конкретного больного криопротектора. Изобретение относится к медицине, а именно к лабораторной диагностике методам цитохимической экспертизы СДГ, и может быть использовано для определения оптимального персонифицированного криопротектора на доклиническом этапе криогемотрансфузионной терапии и предупреждения постгрансфузионных осложнений криопротекторного генеза. Уровень техники.
В современной клинической медицине посттрансфузионные реакции и осложнения рассматривают как один из универсальных механизмов патогенеза различных заболеваний, характеризующихся накоплением в тканях организма избытка токсических продуктов обмена веществ или клеточного реагирования, маркерами которых служат качественные и полуколичественные характеристики определенных цитохимических ферментативных реакций в лейкоцитах крови до и после смешивания с криопротекторами. Эти процессы могут развиваться как по типу яркой многосимптомной реакции, так и по варианту скрытно развивающихся симптомов посттрансфузионных осложнений (Цитохимия замороженной клетки / Обозная Э.И., Пушкарь Н.С., Маркова О.П., Панков Е.Я.- Киев: Наук. Думка, 1981. -176 с). Поэтому возникает проблема выявления ранних признаков вредного влияния токсичных криопротекторов на клеточном уровне и эффективного предупреждения посттрансфузионных осложнений протекторного генеза.
Известные методы биологического и биохимического исследования сыворотки крови (определение концентрации молекул средней массы, продуктов перекисного окисления липидов, билирубина и т.д.) имеют ряд недостатков:
- необходимость вводить криопротектор или гемоконсервант на его основе в периферическую вену больного, то есть производить инвазивную манипуляцию, которая может быть сопряжена с техническими трудностями, осложнениями технического характера или непереносимостью субъектом лекарственного препарата;
- необходимость использования лабораторных животных и специальной биохимической лаборатории, оснащенной сложным оборудованием и реактивами, что делает анализы не всегда доступными и дорогими как для лечебно-профилактических учреждений, так и для пациентов.
Эти недостатки ограничивают количество и частоту необходимых исследований.
На основании предложенных в литературе лабораторных модификаций для оценки полноценности ядерных клеток крови на этапах низкотемпературного консервирования и прогнозирования предполагаемых результатов криогемотрансфузионной терапии широко используются технологии качественной и полуколичественной оценки цитохимических показателей активаторов жизненно важных клеточных ферментов в периферической крови доноров или больных.
Известен метод цитохимического выявления СДГ для оценки в организме больного нормальных и патологических процессов (Углеводы и углеводный обмен: Материалы Второй Всесоюз. конф. по пробл. «Химия и обмен углеводов», 24-27 янв. 1961 г. М.: Изд-во АН СССР, 1962. - С. 157-163).
За прототип предлагаемого изобретения выбран способ, позволяющий выявить криочувствительность СДГ в лейкоцитах донорской крови после экспозиции с криопротектором ПЭО-400 (Цитохимия замороженной клетки / Обозная Э.И., Пушкарь Н.С., Маркова О.П., Панков Е.Я. - Киев: Наук. Думка, 1981. - 176 с; Архагов Ю.Ф. Изменение морфологии и функционально-метаболической активности лейкоцитов в процессе хранения донорской крови и под влиянием различных лучей: Автореф. дис. … канд. мед. наук. М., 2003. - 155 с). Основным недостатком способа-прототипа является отсутствие сравнительных исследований СЦК лейкоцитов на СДГ в мазках проб венозной крови, смешанных с 15% раствором гексаметиленбистетраоксиэтилмочевины (15% ГМБТОЭМ), 3,3% раствором глицерола (3,3% Гл), 10% раствором диметилсульфоксида (10% ДМСО), гемоконсервантом Тромбокриодмац (ТКД) или гемоконсервантом на основе 55% раствора диметилацетамида (ДМАЦ) с 5% раствором гидроксиэтилкрахмал (ГЭК) (55% ДМАЦ+5% ГЭК), со значениями СЦК КП. Вместе с тем, выбор оптимального персонифицированного криопротектора на этапе, предшествующем криогемотрансфузионной терапии, очень важен для больного, так как позволяет снизить риск посттрансфузионных осложнений криопротекторного генеза.
Целью изобретения является устранение отмеченного недостатка и создание такого способа, который бы позволял индивидуально подобрать in vitro для конкретного больного оптимальный персонифицированный криопротектор или гемоконсервант на его основе на этапе, предшествующем плановой трансфузии криоконсервированного компонента крови.
Раскрытие изобретения.
Техническим результатом изобретения является доступность, простота определения оптимального криопротектора на доклиническом этапе криогемотрансфузионной терапии.
Технический результат в заявляемом способе определения оптимального персонифицированного криопротектора по содержанию сукцинатдегидрогеназы в лейкоцитах консервированной крови достигается тем, что, как и в способе-прототипе, анализ содержания СДГ в лейкоцитах осуществляют по методике Нахласа в модификации Р.П. Нарциссова***.
Новым в способе является то, что диагностику оптимального криопротектора проводят путем сравнительных исследований СЦК ОП на СДГ с 15% ГМБТОЭМ, 3,3% Гл, 10% ДМСО, гемоконсервантом ТКД или комбинированным гемоконсервантом 55% ДМАЦ с 5% ГЭК, со значениями СЦК КП. При этом: об оптимальности криопротектора судят в случаях равенства значений СЦК ОП и КП; о принадлежности ОП к препаратам с высоким клиническим риском и непригодными для криогемотрансфузии судят при значениях СЦК ОП, отличных от СЦК КП.
Необходимое оборудование:
1. Предметные стекла,
2. Пробирки для крови на 20 мл с винтовой герметичной пробкой.
3. Световой микроскоп с проходящим светом,
4. Набор тест-доз различных криопротекторов или гемоконсервантов на их основе, разрешенных к клиническому применению МЗ России,
5. Набор реагентов для цитохимического определения гликогена в лейкоцитах. Заявляемый способ имеет основное преимущество в сравнении с прототипом - определение оптимального криопротектора путем сравнительных исследований значений СЦК ОП ауто-крови на СДГ, смешанных с тест-дозами 15% ГМБТОЭМ, 3,3% Гл, ТКД, 10% ДМСО или 55% ДМАЦ +5% ГЭК, со значениями СЦК КП.
Заявляемый способ осуществляют следующим образом. У обследуемого натощак до начала внутривенных трансфузий криоконсервированных компонентов крови (криогемотрансфузионной терапии) готовят в пробирках «линейку» из тест-доз с 15% ГМБТОЭМ, 3,3% глицерола, гемоконсервантом ТКД, 10% ДМСО или комбинированным гемоконсервантом на основе 55% ДМАЦ и 5% ГЭК по 1,5 мл в каждой; эксфузируют 25 мл аутологичной венозной крови на стабилизирующем растворе и фасуют с помощью дозаторной пипетки в 6 помеченных маркером пробирок по 4,0 мл в каждую; затем в пробирку №1 вносят 0,25 мл тест-дозы 15% ГМБТОЭМ, в пробирку №2 - 0,25 мл тест-дозы 3,3% Гл, в пробирку №3 - 0,25 мл тест-дозы ТКД, в пробирку №4 - 0,25 мл 10% ДМСО, в пробирку №5 - 0,25 мл гемоконсерванта на основе 55% ДМАЦ +5% ГЭК, в пробирку №6 с контрольной пробой крови (КП) криопротектор не вносят; компоненты в пробирках №№1-6 герметизируют пробками, перемешивают на шейкере при температуре плюс 37°С в течение 4 ч; из каждой пробирки биопробы с тестируемыми криопротекторами раскапывают с помощью дозаторной пипетки на чистые предметные стекла, готовят 6 тонких мазков, высушивают на воздухе, фиксируют 60% раствором ацетона, насыщенном трилоном Б при комнатной температуре 30 с. Промывают стекла в двух порциях дистиллированной воды по 5 с и высушивают на воздухе. Инкубируют в инкубационной среде при температуре плюс 37°С 60 мин. Инкубационный раствор готовят по методике Нахласа с соавт. (в модификации Р.П. Нарциссова***). Для этого готовят растворы А и В. Раствор А включает 540 мг сукцината натрия, 10 мл дистиллированной воды и 10 мл фосфатного буфере с рН 7,2. Для приготовления раствора В 20 мг нитротетразоля фиолетового растворяют в 3 каплях диметилформамида и 10 мл дистиллированной воды. Растворы А и В смешивают, фильтруют, затем добавляют 13 мг трилона Б, измеряют рН, добавляют 10 мл дистиллированной воды. Инкубация стекол в рабочем растворе идет в термостате при температуре плюс 37°С в течение 60 мин. Затем стекла промывают проточной водой 1 мин, ополаскивают дистиллированной водой 3-5 с. Докрашивают красителем Романовского в течение 5-10 мин. Смывают краску в проточной воде. Высушивают на воздухе. Окрашенные мазки микроскопируют в проходящем свете, проводят сравнительное исследование СДГ в сегментоядерных нейтрофилах и лимфоцитах с гранулами синего цвета СДГ ОП и КП по Каплоу Л. (1955) в модификации Астальди и Верга (1957). О пригодности тестируемых криопротекторов к использованию (ПКИ) в планируемых криогемотрансфузиях судят по значениям СЦК ОП и СЦК КП; при равности значений СЦК ОП и СЦК КП тестируемый криопротектор оценивают как оптимальный для конкретного больного и пригодный к использованию; при значениях СЦК ОП, отличных от СЦК КП, делают заключение как о непригодном к использованию криопротекторе.
Необходимое оборудование: предметные стекла, пробирки для крови на 5 и 20 мл с винтовой герметичной пробкой, световой микроскоп с проходящим светом, набор тест-доз различных криопротекторов или гемоконсервантов на их основе, разрешенных к клиническому применению МЗ России, набор реагентов для цитохимического определения гликогена в лейкоцитах in vitro диагностики фирмы Диахим-ЦитоСтейн-ПАС (Россия).
В качестве иллюстрации работоспособности заявляемого способа диагностики оптимального криопротектора по содержанию сукцинатдегидрогеназы в лейкоцитах консервированной крови приводим 3 опыта (Табл. 1), которые подтверждают практическое применение данного способа.
Опыт №1. Результаты исследования крови донора П-ва показывают, что из числа исследованных тест-доз криопротекторов оптимальным является комбинированный криопротектор, включающий 55% раствор ДМАЦ +5% раствор ГЭК (СЦК с/я нейтрофилов и лимфоцитов ОП равны СЦК КП - 0,78 и 0,67 соответственно). Заключение: ПКИ является комбинированный криопротектор, включающий 55% раствор ДМАЦ +5% раствор ГЭК, а НКИ являются 15% ГМБТОЭМ, 3,3% Глицерол, ТКД и 10% ДМСО, СЦК которых отличаются от таковых КП и сопряжены с рисками посттрансфузионных осложнений.
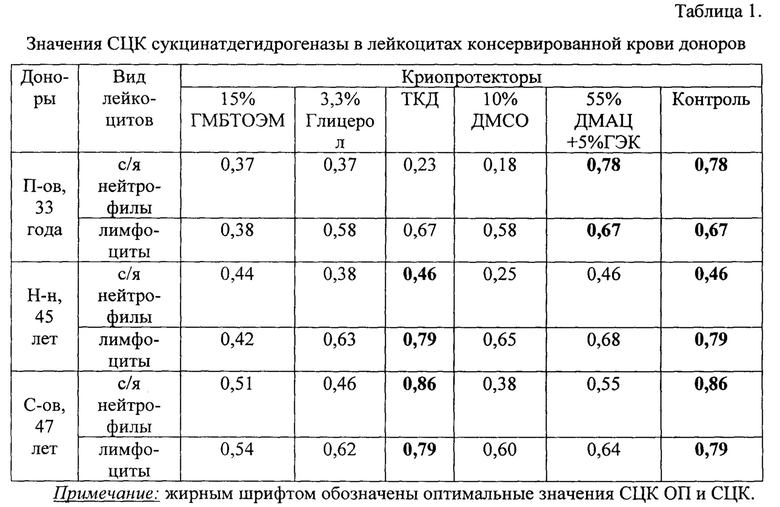
Опыт №2. Результаты исследования крови донора Н-н показывают, что из числа исследованных тест-доз криопротекторов оптимальным является криопротектор ТКД, у которого СЦК с/я нейтрофилов в ОП и КП составляет 0,46, а СЦК лимфоцитов - 0,79 соответственно. Заключение: ПКИ является криопротектор ТКД, а НКИ являются: 15% ГМБТОЭМ, 3,3% Глицерол, 10% ДМСО и комбинированный криопротектор, включающий 55% раствор ДМАЦ +5% раствор ГЭК, которые несут риски посттрансфузионных осложнений.
Опыт №3. Результаты исследования крови донора С-ва показывают, что из числа исследованных тест-доз криопротекторов оптимальным является ТКД (СЦК с/я нейтрофилов в ОП и КП составляет 0,86, лимфоцитов - 0,79 соответственно. Заключение: ПКИ является криопротектор ТКД, а НКИ являются 3,3% Глицерол, 15% ГМБТОЭМ, 10% ДМСО, комбинированный криопротектор на основе 55% ДМАЦ и 5% ГЭК, которые несут риски посттрансфузионных осложнений.
Представленные примеры иллюстрируют применимость предлагаемого способа определения оптимального криопротектора по цитохимическому показателю содержания СДГ в лейкоцитах консервированной крови. Способ дешев и может быть внедрен в практику гематологического центра, использующего трансфузии криоконсервированных компонентов крови или костного мозга.
Таким образом, благодаря использованию более чувствительного способа определения оптимального криопротектора по содержанию сукцинатдегидрогеназы в лейкоцитах консервированной ауто-крови удается оценить эффективность и снизить риски криопротекторного генеза на этапе планируемой криогемотрансфузионной терапии.
Предлагаемое изобретение отвечает критериям «новизна» и «изобретательский уровень», так как проведенные патентно-информационные исследования не выявили источников патентной и научно-технической литературы, которые бы порочили новизну предлагаемого способа, равно как и известных способов с существенными признаками предлагаемого технического решения. Техническим результатом использования является возможность проведения индивидуального скрининга криопротекторов на доклиническом этапе их применения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ подбора оптимального криопротектора по содержанию гликогена в лейкоцитах консервированной крови | 2018 |
|
RU2686107C1 |
| Способ выявления эффективного криопротектора по цитохимическому показателю содержания лейкоцитарной щелочной фосфатазы аутокрови | 2018 |
|
RU2676674C1 |
| Способ определения персонифицированного криопротектора по лейкоцитарной кислой фосфатазе консервированной крови | 2017 |
|
RU2689334C1 |
| Способ определения оптимального моноэндоцеллюлярного криоконсерванта для хранения клеток при -80 С | 2016 |
|
RU2624243C1 |
| Способ прогнозирования течения хронического гепатита С 1 генотипа у нелеченных больных с высокой вирусной нагрузкой | 2017 |
|
RU2657586C1 |
| СПОСОБ ВЫЯВЛЕНИЯ НАРУШЕНИЯ ФУНКЦИИ ФАГОЦИТОВ ПРИ РАЗВИТИИ РЕЦИДИВИРУЮЩИХ ИНФЕКЦИОННЫХ ПРОЦЕССОВ | 2007 |
|
RU2362997C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВИРУЮЩЕГО ТЕЧЕНИЯ АЦЕТОНЕМИЧЕСКОЙ РВОТЫ У ДЕТЕЙ | 2011 |
|
RU2481576C1 |
| Способ определения сенсибилизации организма к миокардиальному антигену при заболеваниях сердца | 1989 |
|
SU1718824A1 |
| Способ прогнозирования течения язвенной болезни | 1990 |
|
SU1772762A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ МИТОХОНДРИАЛЬНЫХ ЗАБОЛЕВАНИЙ У ДЕТЕЙ С НЕДИФФЕРЕНЦИРОВАННЫМИ ФОРМАМИ ЗАДЕРЖКИ НЕРВНО-ПСИХИЧЕСКОГО РАЗВИТИЯ (ВАРИАНТЫ) | 2008 |
|
RU2366959C1 |
Изобретение относится к медицине, а именно к лабораторной диагностике. Способ определения оптимального криопротектора по цитохимическому показателю содержания сукцинатдегидрогеназы в лейкоцитах аутокрови заключается в том, что у больного до начала криогемотрансфузионной терапии получают порцию венозной крови, делят на равные части в пробирки, в одной из которых контрольная проба крови (КП) не содержит криопротектора, в другие добавляют по одной равной дозе тестируемых криопротекторов - опытные пробы (ОП), капли ОП и КП наносят в объеме 4 мкл на предметные стекла, из них делают тонкие мазки, высушивают на воздухе, готовят препараты по методике Нахласа в модификации Р.П. Нарциссова, лейкоциты микроскопируют в проходящем свете, проводят сравнительное исследование среднего цитохимического коэффициента (СЦК) сегментоядерных нейтрофилов и лимфоцитов с гранулами синего цвета СДГ ОП и КП; при равности значений СЦК ОП и СЦК КП тестируемый криопротектор оценивают как оптимальный для конкретного больного и пригодный к использованию; при значениях СЦК ОП, отличных от СЦК КП, делают заключение как о непригодном к использованию криопротекторе. 3 пр., 1 табл.
Способ определения оптимального криопротектора по цитохимическому показателю содержания сукцинатдегидрогеназы в лейкоцитах аутокрови, отличающийся тем, что у больного до начала криогемотрансфузионной терапии получают порцию венозной крови, делят на равные части в пробирки, в одной из которых контрольная проба крови (КП) не содержит криопротектора, в другие добавляют по одной равной дозе тестируемых криопротекторов - опытные пробы (ОП), капли ОП и КП наносят в объеме 4 мкл на предметные стекла, из них делают тонкие мазки, высушивают на воздухе, готовят препараты по методике Нахласа в модификации Р.П. Нарциссова, лейкоциты микроскопируют в проходящем свете, проводят сравнительное исследование среднего цитохимического коэффициента (СЦК) сегментоядерных нейтрофилов и лимфоцитов с гранулами синего цвета СДГ ОП и КП; о пригодности тестируемых криопротекторов к использованию (ПКИ) в планируемых криогемотрансфузиях судят по значениям СЦК ОП и СЦК КП; при равности значений СЦК ОП и СЦК КП тестируемый криопротектор оценивают как оптимальный для конкретного больного и пригодный к использованию; при значениях СЦК ОП, отличных от СЦК КП, делают заключение как о непригодном к использованию криопротекторе.
| СПОСОБ ПОДБОРА КРИОПРОТЕКТОРОВ ДЛЯ КРИОКОНСЕРВАЦИИ БИОЛОГИЧЕСКИХ ОБРАЗЦОВ (ВАРИАНТЫ) | 2002 |
|
RU2236466C2 |
| А.А.Костяев и др | |||
| Зависимость кристаллогенных свойств плазмы донорской крови от температуры замораживания и вида криопротектора / МЕДИЦИНА ЭКСТРЕМАЛЬНЫХ СИТУАЦИЙ, 2013, N 1(43), стр | |||
| Огнетушитель | 0 |
|
SU91A1 |
| Большой толковый словарь русского языка | |||
| Санкт-Петербург "НОРИНТ", 2000, стр | |||
| Автоматический огнетушитель со спринклером | 1924 |
|
SU1172A1 |
Авторы
Даты
2019-05-27—Публикация
2017-12-05—Подача