Изобретение относится к медицине, а именно к лабораторной диагностике, и может найти применение в онкологической, гематологической, хирургической практике и криомедицине с целью определения персонифицированного (соотносящегося с конкретным человеком) криопротектора для живых клеток по содержанию лейкоцитарной кислой фасфатазы (ЛКФ)* (* ЛКФ включает ряд изоферментов, которые ускоряют распад органических эфиров фосфорной кислоты в кислой среде.) консервированной крови и предупреждения развития посттрансфузионных осложнений протекторного генеза. Для осуществления способа у пациента до начала компонентной трансфузионной терапии эксфузируют порцию свежей ауто-крови, стабилизируют раствором цитрата натрия, делят в пробирки на равные части, в контрольной пробе (КП) добавки криопротекторов исключают, в опытные пробы (ОП) добавляют по одной равной дозе тестируемых криопротекторов, перемешивают при плюс 37°С в течение 4 ч, капли приготовленных биологических жидкостей (ПБЖ) из ОП и КП наносят в объеме 4 мкл на предметные стекла, делают 2-3 мазка, высушивают на воздухе, фиксируют в 10% спирт-формалиновой смеси 10 мин, промывают в проточной воде 1-2 мин и высушивают, готовят рабочий раствор с рН 5,2-5,4; инкубируют в рабочем растворе вертикально в термостате при температуре плюс 37°С 2-3 часа, стекла промывают в проточной воде, высушивают, лейкоциты окрашивают на кислую фосфатазу по методике азосочетания Берстона в модификации Ю.Ф. Руденса, И.М. Буйкиса**, микроскопируют в проходящем свете, производят подсчет содержания ЛКФ в сегментоядерных (с/я) нейтрофилах и лимфоцитах с подсчетом среднего цитохимического коэффициента (СЦК) по Кэплоу Л. (1955) в модификации Астальди и Верга (1957)** (** Определение уровня ЛКФ в крови имеет важное значение для диагностики состояния здоровья (Березов Т.Т., Коровкин Б.Ф. Биологическая химия: Учебник. 3-е изд., перераб. и доп. - Учеб. лит. Для студентов мед. вузов. - М.: Медицина, 1998. - С. 704).); при совпадении значений показателей СЦК ОП и СЦК КП тестируемый криопротектор оценивают как оптимальный для конкретного больного и пригодным к использованию; при значениях СЦК ОП, отличных от СЦК КП, делают заключение как о непригодном к использованию криопротекторе. Способ прост и доступен врачу по цитохимическим методам диагностики.
Уровень техники.
В современной клинической медицине постгрансфузионные реакции и осложнения рассматривают как один из универсальных механизмов патогенеза различных заболеваний, характеризующихся накоплением в тканях организма избытка токсических продуктов клеточного реагирования, маркерами которых служат качественные и полуколичественные характеристики определенных цитохимических ферментативных реакций в лейкоцитах крови до и после смешивания с криопротекторами. Эти процессы могут развиваться как по типу яркой реакции «на кончике иглы», так и скрытно развивающихся симптомов посттрансфузионных осложнений (Цитохимия замороженной клетки / Обозная Э.И., Пушкарь Н.С., Маркова О.П., Панков Е.Я.- Киев: Наук. Думка, 1981. - 176 с). Поэтому возникает проблема раннего выявления маркеров вредного влияния токсичных криопротекторов на организм пациентов для эффективного предупреждения посттрансфузионных осложнений протекторного генеза.
Известные методы биологического и биохимического исследования сыворотки крови (определение концентрации молекул средней массы, продуктов перекисного окисления липидов, билирубина и т.д.) имеют ряд недостатков:
- необходимость вводить криопротектор или гемоконсервант на его основе в периферическую вену больного, то есть производить инвазивную манипуляцию, которая может быть сопряжена с техническими трудностями, осложнениями технического характера или непереносимостью субъектом лекарственного препарата;
- необходимость использования лабораторных технологий и специальной биохимической лаборатории, оснащенной сложным оборудованием и реактивами, что делает анализы не всегда доступными и дорогими как для лечебно-профилактических учреждений, так и для пациентов.
Эти недостатки ограничивают количество и частоту необходимых исследований.
На основании предложенных в литературе лабораторных модификаций для оценки полноценности ядерных клеток крови на этапах низкотемпературного консервирования и прогнозирования предполагаемых результатов криогемотрансфузионной терапии широко используются технологии качественной и полуколичественной оценки цитохимических показателей активаторов жизненно важных клеточных ферментов в периферической крови доноров или больных (Березов Т.Т., Коровкин Б.Ф. Биологическая химия: Учебник. 3-е изд., перераб. и доп. - Учеб. лит. Для студентов мед. вузов. - М.: Медицина, 1998. - С. 704).
Исследованиями в уровне техники не обнаружено источников информации, раскрывающих способ определения персонифицированного криопротектора по лейкоцитарной кислой фосфатазе (ЛКФ) консервированной крови.
Целью изобретения является создание такого цитохимического способа, который бы позволял определить in vitro для конкретного пациента качественный криопротектор или гемоконсервант на его основе на этапе, предшествующем плановой трансфзии криоконсервированного компонента ауто-крови.
Раскрытие изобретения.
Техническим результатом изобретения является доступность, простота определения персонифицированного качественного криопротектора на доклиническом этапе криогемотрансфузионной терапии.
Технический результат в заявляемом способе определения персонифицированного качественного криопротектора осуществляется по содержанию ЛКФ в консервированной ауто-крови с помощью методики азосочетания Берстона в модификации Ю.Ф. Руденса и И.М. Буйкиса.
Новым в предлагаемом способе является то, что определение персонифицированного криопротектора проводят путем сравнительных исследований СЦК ОП на ЛКФ с 15% Гексаметиленбистетраоксиэтилмочевина (ГМБТОЭМ), 3,3% Глицерола (Гл), 10% Диметилсульфоксид (ДМСО), гемоконсервантом Тромбокриодмац (ТКД) или комбинированным гемоконсервантом на основе Инфукола, содержащего гидроксиэтилкрахмал (ГЭК), и 8% Диметилацетамид (ДМАЦ), со значениями СЦК КП. Пригодным к использованию (ПКИ) из числа тестируемых определяют криопротектор, у которого значения СЦК для с/я нейтрофилов и лимфоцитов ОП совпадают таковыми КП. Способ прост и доступен врачу клинической лабораторной диагностики.
Необходимое оборудование:
1. Предметные стекла,
2. Пробирки для крови на 20 мл с винтовой герметичной пробкой.
3. Световой микроскоп с проходящим светом,
4. Набор тест-доз различных криопротекторов или гемоконсервантов на их основе, разрешенных к клиническому применению МЗ России,
5. Система счетверенных контейнеров с интегрированным лейкоцитарным фильтром для получения лейкофильтрованных компонентов крови Leukotrap WB с пробоотборником для лабораторных исследований,
6. Набор реагентов для цитохимического определения ЛКФ.
Заявляемый способ осуществляют следующим образом. У пациента натощак до начала внутривенных трансфузий криоконсервированных компонентов крови (криогемотрансфузионной терапии) готовят в пробирках «линейку» с тест-дозами 15% ГМБТОЭМ, 3,3% глицерола, гемоконсерванта ТКД, 10% ДМСО или комбинированного гемоконсерванта на основе Инфукола, содержащего гидроксиэтилкрахмал (ГЭК), и 8% Диметилацетамида (ДМАЦ) по 1,5 мл в каждой; в пробоотборник эксфузируют 25 мл ауто-крови без консерванта, стабилизируют раствором цитрата натрия, эксфузат фасуют с помощью дозаторной пипетки в 6 меченных маркером пробирок по 4,0 мл в каждую; в пробирку №1 вносят 0,25 мл тест-дозы 15% ГМБТОЭМ, в пробирку №2 - 0,25 мл тест-дозы 3,3% Гл, в пробирку №3 - 0,25 мл тест-дозы ТКД, в пробирку №4 - 0,25 мл 10% ДМСО, в пробирку №5 - 0,25 мл гемоконсерванта на основе 55% ДМАЦ +5% ГЭК, в пробирку №6 с контрольной пробой крови (КП) криопротекторы не вносят; ПБЖ в пробирках №№1 - 6 герметизируют винтовыми пробками, перемешивают на шейкере при температуре плюс 37°С в течение 2-3 ч; капли приготовленных биологических жидкостей (ПБЖ) из ОП и КП наносят в объеме 4 мкл на предметные стекла с помощью дозаторных пипеток, делают 2-3 мазка, высушивают на воздухе, фиксируют в 10% спирт-формалиновой смеси 10 мин, промывают в проточной воде 1-2 мин и высушивают, готовят рабочий раствор с рН 5,2-5,4; инкубируют в рабочем растворе вертикально в термостате при температуре плюс 37°С 2-3 часа, стекла промывают в проточной воде, высушивают, лейкоциты окрашивают на кислую фосфатазу по методике азосочетания Берстона в модификации Ю.Ф. Руденса, И.М. Буйкиса**, микроскопируют в проходящем свете, производят подсчет содержания ЛКФ в сегментоядерных (с/я) нейтрофилах и лимфоцитах с подсчетом среднего цитохимического коэффициента (СЦК) по Кэплоу Л. (1955) в модификации Астальди и Верга (1957)**; при совпадении значений показателей СЦК ОП и СЦК КП тестируемый криопротектор оценивают как оптимальный для конкретного больного и пригодным к использованию; при значениях СЦК ОП, отличных от СЦК КП, делают заключение как о непригодном к использованию криопротекторе. Необходимое оборудование: чистые обезжиренные предметные стекла, пробирки для крови на 5 и 20 мл с винтовой герметичной пробкой, световой микроскоп с проходящим светом, набор тест-доз из различных криопротекторов или гемоконсервантов, разрешенных к клиническому применению МЗ России, набор реагентов для цитохимического определения КФ в лейкоцитах in vitro диагностики фирмы Диахим-ЦитоСтейн-ПАС (Россия).
В качестве иллюстрации работоспособности заявляемого способа отбора качественного криопротектора по содержанию показателей СЦК ЛКФ в ауто-крови приводим 3 примера (Табл. 1), которые подтверждают практическое применение данного способа.
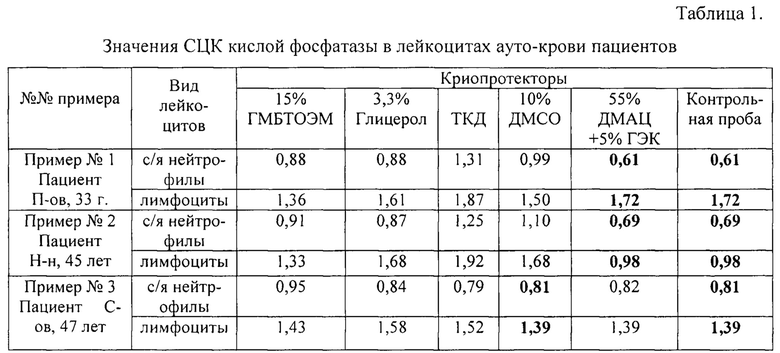
Примечание: жирным шрифтом обозначены оптимальные значения СЦК ОП и СЦК КП.
Пример №1. По результатам исследований ауто-крови пациента П-ва признан оптимальным и ПКИ комбинированный криопротектор на основе 55% ДМАЦ и 5% ГЭК, у которого значения СЦК КФ для лейкоцитов совпадают с таковыми КП (соответственно, 0,61 и 1,72).
Пример №2. Результаты исследования крови донора Н-н показывают, что оптимальным и ПКИ является комбинированный криопротектор, содержащий 55% ДМАЦ + 5% ГЭК, у которого СЦК для с/я нейтрофилов и лимфоцитов аналогичен СЦК КЩ соответственно, 0,69 и 0,98).
Пример №3. Результаты исследования крови донора С-ва показывают, что из числа исследованных тест-доз криопротекторов ПКИ является 10% ДМСО, у которого СЦК для с/я нейтрофилов и лимфоцитов аналогичен СЦК КП (соответственно, 0,81 и 1,39). Представленные примеры иллюстрируют применимость предлагаемого способа определения персонифицированного криопротектора по содержанию ЛКФ в консервированной ауто-крови пациента. Способ дешев и может быть внедрен в практику центра, использующего трансфузии криоконсервированных компонентов крови.
Таким образом, благодаря использованию более чувствительного способа определения персонифицированного криопротектора по содержанию ЛКФ в ауто-крови удается оценить эффективность и снизить риски планируемой криогемотрансфузионной терапии протекторного генеза.
Предлагаемое изобретение отвечает критериям «новизна» и «изобретательский уровень», так как проведенные патентно-информационные исследования не выявили источников патентной и научно-технической литературы, которые бы порочили новизну предлагаемого способа, равно как и известных способов с существенными признаками предлагаемого технического решения. Техническим результатом использования является возможность проведения индивидуального скрининга криопротекторов на доклиническом этапе их применения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выявления эффективного криопротектора по цитохимическому показателю содержания лейкоцитарной щелочной фосфатазы аутокрови | 2018 |
|
RU2676674C1 |
| Способ определения оптимального криопротектора по цитохимическому показателю содержания сукцинатдегидрогеназы в лейкоцитах ауто-крови | 2017 |
|
RU2689328C1 |
| Способ подбора оптимального криопротектора по содержанию гликогена в лейкоцитах консервированной крови | 2018 |
|
RU2686107C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ШЕЙКИ МАТКИ | 2012 |
|
RU2488823C1 |
| СПОСОБ ВЫЯВЛЕНИЯ НАРУШЕНИЯ ФУНКЦИИ ФАГОЦИТОВ ПРИ РАЗВИТИИ РЕЦИДИВИРУЮЩИХ ИНФЕКЦИОННЫХ ПРОЦЕССОВ | 2007 |
|
RU2362997C2 |
| СПОСОБ ОЦЕНКИ ВНУТРИКЛЕТОЧНОГО МЕТАБОЛИЗМА НЕЙТРОФИЛОВ У РАБОТНИКОВ НЕФТЕХИМИЧЕСКОГО И ХИМИЧЕСКОГО ПРОИЗВОДСТВА | 2011 |
|
RU2473086C1 |
| Способ диагностики неспецифического воспалительного заболевания легких | 1978 |
|
SU859861A1 |
| Способ дифференциальной диагностики бронхитов,бронхопневмоний и пневмоний | 1980 |
|
SU1046649A1 |
| Способ определения тканевой несовместимости при пересадке сердца | 1981 |
|
SU1140760A1 |
| Способ прогнозирования течения острых респираторных заболеваний у детей раннего возраста | 1980 |
|
SU942697A1 |
Изобретение относится к медицине, а именно к лабораторной диагностике. Способ определения персонифицированного криопротектора по лейкоцитарной кислой фосфатазе (ЛКФ) консервированной крови заключается в том, что у пациента до начала компонентной трансфузионной терапии эксфузируют порцию свежей аутокрови, стабилизируют раствором цитрата натрия, делят в пробирки на равные части, в контрольной пробе (КП) добавки криопротекторов исключают, в опытные пробы (ОП) добавляют по одной равной дозе тестируемых криопротекторов, перемешивают при плюс 37°С в течение 4 ч, капли приготовленных биологических жидкостей из ОП и КП наносят в объеме 4 мкл на предметные стекла, делают 2-3 мазка, высушивают на воздухе, фиксируют в 10% спирт-формалиновой смеси, лейкоциты окрашивают на кислую фосфатазу по методике азосочетания Берстона в модификации Ю.Ф. Руденса, И.М. Буйкиса, микроскопируют в проходящем свете, производят подсчет содержания ЛКФ в сегментоядерных (с/я) нейтрофилах и лимфоцитах с подсчетом среднего цитохимического коэффициента (СЦК); при совпадении значений показателей СЦК ОП и СЦК КП тестируемый криопротектор оценивают как оптимальный для конкретного больного и пригодным к использованию; при значениях СЦК ОП, отличных от СЦК КП, делают заключение как о непригодном к использованию криопротекторе. 1 табл., 3 пр.
Способ определения персонифицированного криопротектора по лейкоцитарной кислой фосфатазе (ЛКФ) консервированной крови, заключающийся в том, что у пациента до начала компонентной трансфузионной терапии эксфузируют порцию свежей аутокрови, стабилизируют раствором цитрата натрия, делят в пробирки на равные части, в контрольной пробе (КП) добавки криопротекторов исключают, в опытные пробы (ОП) добавляют по одной равной дозе тестируемых криопротекторов, перемешивают при плюс 37°С в течение 4 ч, капли приготовленных биологических жидкостей из ОП и КП наносят в объеме 4 мкл на предметные стекла, делают 2-3 мазка, высушивают на воздухе, фиксируют в 10% спирт-формалиновой смеси, лейкоциты окрашивают на кислую фосфатазу по методике азосочетания Берстона в модификации Ю.Ф. Руденса, И.М. Буйкиса, микроскопируют в проходящем свете, производят подсчет содержания ЛКФ в сегментоядерных (с/я) нейтрофилах и лимфоцитах с подсчетом среднего цитохимического коэффициента (СЦК) по Кэплоу Л. (1955) в модификации Астальди и Верга (1957); при совпадении значений показателей СЦК ОП и СЦК КП тестируемый криопротектор оценивают как оптимальный для конкретного больного и пригодным к использованию; при значениях СЦК ОП, отличных от СЦК КП, делают заключение как о непригодном к использованию криопротекторе.
| СПОСОБ ПОДОГРЕВА ВОДЫ ДЛЯ ОТОПЛЕНИЯ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2336466C2 |
| А.А.Костяев и др | |||
| Зависимость кристаллогенных свойств плазмы донорской крови от температуры замораживания и вида криопротектора / Медицина экстремальных ситуаций, 2013, N 1(43), стр | |||
| Огнетушитель | 0 |
|
SU91A1 |
| СПОСОБ КРИОКОНСЕРВАЦИИ МУЛЬТИПОТЕНТНЫХ МЕЗЕНХИМАЛЬНЫХ СТРОМАЛЬНЫХ КЛЕТОК | 2010 |
|
RU2433173C1 |
Авторы
Даты
2019-05-27—Публикация
2017-12-13—Подача