Изобретение относится к области органической химии, а именно к способу получения С-гидроксиметилимидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксана.
С-Гидроксиметилимидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксан является эффективным ингибитором агрегации тромбоцитов (IC50 0,4 мкМ) [А.А. Алексеев, диссертация на соискание ученой степени кандидата фармацевтических наук, Москва 2015 г], превосходящим по доза-зависимому ингибированию агрегации тромбоцитов ряд известных соединений, демонстрирующих выраженный антиагрегационный эффект [Патент RU №2396271, 2009 г.], наиболее активным из которых является Arg-Gly-Gly-Asp-Trp (IC50 6,3 мкМ).
Известен способ получения имидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксанов конденсацией 3,5-дибром-фенилендиамина-1,2 с карбоновыми кислотами или их хлорангидридами, нитрованием 4,6-дибромбензимидазолов, азидированием 4,6-дибром-5,7-динитробензимидазолов и термоциклизацией 4,6-диазидо-5,7-динитробензимидазолов [В.Л. Королев, В.В. Топоров, Н.Л. Меркулова, В.Д. Даниленко, В.П. Ившин, Т.С. Пивина. Синтез имидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксанов. //Изв.АН. Сер. хим. 2017, 1250-1255]..
Способ получения С-гидроксиметилимидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксана в литературе не описан.
Способ включает конденсацию 3.5-дибром-фенилендиамина-1.2 с гликолевой кислотой, нитрование 2-гидроксиметил-4,6-дибромбензимидазола смесью серной и азотной кислот, азидирование 2-гидроксиметил-4,6-дибром-5,7-динитробензимидазола и термоциклизацию 2-гидроксиметил-4,6-диазидо-5,7-динитробензимидазола. Из-за потенциально высокой чувствительности к механическим воздействиям 2-гидроксиметил-4,6-диазидо-5,7-динитробензимидазола это соединение после реакции азидирования осаждают водой из ДМФА и термоциклизуют без предварительной очистки и сушки.
В связи с тем, что данные, подтверждающие строение синтезированных соединений в литературе не представлены, мы дополнительно подтвердили структуру полученных веществ методами физико-химического анализа.
Брутто-состав веществ подтвержден данными элементного анализа. Температура плавления определена на микроскопном столике «Boetius».
Строение синтезированных соединений подтверждено методами ИК-, ЯМР 1Н, 13С- и масс-спектроскопии высокого разрешения.
ИК-спектры регистрировали на приборе «Vector 22» в прессовке KBr. Спектры ЯМР 1Н и 13С записаны на приборе «Bruker AM-300», химические сдвиги измеряли относительно сигнала растворителя (ДМСО-d6, δН 2.5 м.д., δс 39.5 м.д.). Масс-спектры высокого разрешения регистрировали на приборе “Q Exactive” с ионизацией электрораспылением (ESI-MS) в положительной моде; напряжение на капилляре – 3500 В, диапазон сканирования масс 90-900 Да.
Предлагаемый способ получения С-гидроксиметилимидазо [4,5-e]бензо[1,2-c;3,4-c’]дифуроксана иллюстрируется следующими примерами.
Пример 1. Получение 2-гидроксиметил-4,6-дибромбензимидазола.
1.00 г (3.76 ммолей ) 3.5-дибром-фенилендиамина-1.2 и 2.0 г (26.30 ммолей) гликолевой кислоты нагревали при 120 oС 2 ч., охлаждали до 20 oС, добавляли 10% водный р-р NaOH до слабощелочной реакции, выпавший осадок отфильтровывали, промывали водой, сушили. Получали 1.06 г продукта (выход 92 %). т.пл. 234-236°С (С2Н5ОН/H2O).
Найдено % С 31,68; Н 2,16; N 8,91; Br 51,93 С8H6N2Br2O
Вычислено % С 31,41; Н 1,98; N 9,16; Br 52,23
m/z [M+Н]+найдено/вычислено 306.1907/306.8894
ИК (см-1, KBr) 3382, 3072, 2930, 2878, 1607, 1571, 1496, 1467, 1439, 1414, 1350, 1319, 1227, 1184, 1116, 1089, 960, 852, 783, 739, 619
Спектр ЯМР 1Н (δ, м.д.): 4,85 (с, 2Н, СН2); 7,72 (с, 1Н, СН); 7,80 (с, 1Н, СН). Спектр ЯМР 13С (δ, м.д.) 60.2 (-CH2-OH), 112.7, 115.4, 119.1, 131.7, 138.8, 139.5 (-С=); 160.9 (-C –CH2-).
Пример 2. Получение 2-гидроксиметил-4,6-дибром-5,7-динитробензимидазола
К 1.11 г (3.63 ммолям) 2-гидроксиметил-4.6-дибромбензимидазола в 7 мл Н2SO4 (d=1.84 г/см3) при 0-5 oС и перемешивании прикапывали 1 мл HNO3 (d=1.50 г/см3), повышали температуру до 90-95 оС, перемешивали 3 ч, охлаждали до 20 oС, выливали в лёд, осадок отфильтровывали, нагревали 1,5 часа при кипячении в 40 мл 10% соляной кислоты, охлаждали до 4оС, осадок отфильтровывали, промывали водой, сушили.
Получали 1,04 г продукта (выход 73 %). т.пл. 265-267°С (С2Н5ОН/H2O).
Найдено % С 23,98; Н 1,16; N 13,91; Br 40,03 С8H4N4Br2O5
Вычислено % С 24,27; Н 1,02; N 14,15; Br 40,36
m/z [M+Н]+найдено/вычислено 396.8602/396.8601
ИК (см-1, KBr) 3208, 2984, 2934, 1615, 1553, 1518, 1445, 1401, 1361, 1340, 1311, 1283, 1201, 1160, 1063, 1038, 991, 907, 873, 822, 809, 772, 743, 712, 654, 619
Спектр ЯМР 1Н (δ, м.д.): 4,80 (с, СН2). Спектр ЯМР 13С (δ, м.д.) 57.3 (-CH2-OH), 99.5, 105.4, 131.8, 136.1, 140.3, 146.1 (-С=); 162.7 (-C –CH2-).
Пример 3. Получение С-гидроксиметилимидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксана
1.00 г (2.53 ммоля) 2-гидроксиметил-4,6-дибром-5,7-динитробензимидазола и 0.45 г (6.92 ммоля) NaN3 в 3 мл ДМФА перемешивали при 20 oС 10 ч. , добавляли 60 мл воды, выпавший осадок отфильтровывали, переносили в 3 мл АсОН, нагревали 2 ч при 100 oС, охлаждали до 20 oС, выпавший осадок отфильтровывали, промывали водой, нагревали 0.5 ч при 100 oС в 5 мл воды, охлаждали до 20 oС, отфильтровывали, сушили.
Получали 0,48 г продукта (выход 72 %). т.пл. 185°С разл.
Найдено % С 36,17; Н 1,78; N 31,63 С8H4N6O5
Вычислено % С 36,37; Н 1,53; N 31,81
m/z [M+Н]+найдено/вычислено 265.0316/265.0308
ИК (см-1, KBr) 3150, 2921, 1649, 1557, 1521, 1465, 1447, 1342, 1306, 1282, 1214, 1078, 994, 970, 924, 812, 744, 654
Спектр ЯМР 1Н (δ, м.д.): 4.59 с, 4.66 с, 4.70 с (СН2)) в соотношении 0,17:1,00:0,50. Спектр ЯМР 13С (δ, м.д.) 56.5, 56.9, 57.0 (-CH2-OH); 101.4, 103.8, 105.2 (С=N(O)O); 125.3, 128.2, 128.9 (=C-N=C, =C-NH-C); 137.4, 141.5 (C=NO); 156.9, 157.1 (С-CH2-).
ЯМР-спектры С-гидроксиметилимидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксана приведены для смеси таутомеров [Н.Л. Меркулова, В.М. Даниленко, В.Л. Королев, Т.С. Пивина, В.П. Ившин. Исследование таутомерии имидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксанов методами хромато-масс-, ЯМР-спектроскопии и квантовой химии. //Тез. докл. Всероссийской научной конференции с международным участием «Современные проблемы органической химии», Новосибирск, 5-9 июня, 2017, 232; В.Л. Королев, В.В. Топоров, Н.Л. Меркулова, В.Д. Даниленко, В.П. Ившин, Т.С. Пивина. Синтез имидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксанов. //Изв.АН. Сер. хим. 2017, 1250-1255; В.Л. Королев, В.В. Топоров, Н.Л. Меркулова, В.Д. Даниленко, В.П. Ившин, Т.С. Пивина. Синтез N-замещенных [имидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксанов. //Изв.АН. Сер. хим. 2017, 2126-2130; Investigation of the tautomerism of imidazo[4,5-e]benzo[1,2-c;3,4-c’]difuroxan derivatives by computational and experimental methods, Natalia L. Merkulova, Vjacheslav L. Korolev, Vitalii M. Danilenko, Ivan D. Nesterov, Tatyana S. Pivina, In Proc. of the 21-th Seminar “New Trends in Research of Energetic Materials”, NTREM 2018, Pardubice, the Czech Republic, April 17-20, 2018, 861-867] С-гидроксиметилимидазо [4,5-e]бензо[1,2-c;3,4-c’]дифуроксана.
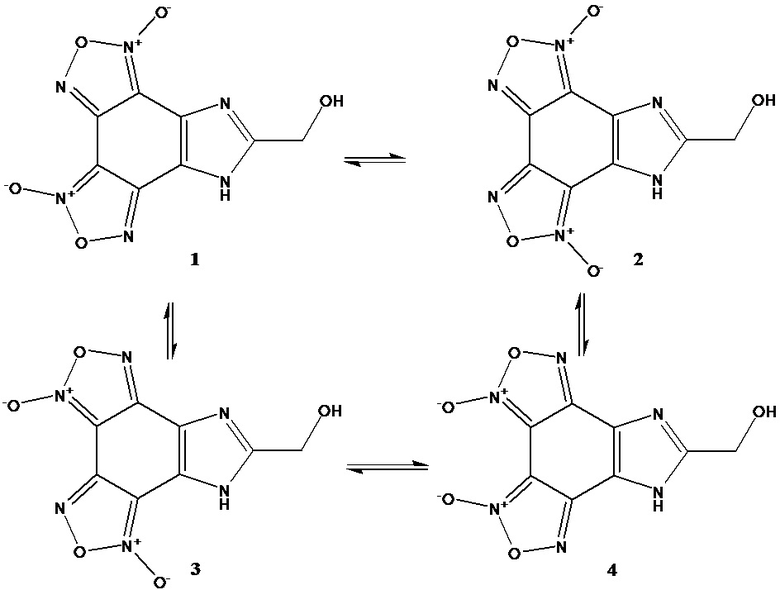
В спектре ЯМР1Н С-гидроксиметилимидазо [4,5-e]бензо[1,2-c;3,4-c’]дифуроксана регистрируются три сигнала (Спектр ЯМР 1Н (δ, м.д.): 4.59 с, 4.66 с, 4.70 с (СН2)) в соотношении 0,17:1,00:0,50. Регистрация трех, а не четырех сигналов, отвечающих всем представленным таутомерным формам (1-4) С-гидроксиметилимидазо [4,5-e]бензо[1,2-c;3,4-c’]дифуроксана вероятно связана со слиянием (вырождением) сигналов изомеров 1 и 3 вследствие легкости миграции NH протона имидазольного цикла [Г.Н. Тен, Т.Г. Бурова, В.И. Баранов. О механизме процесса переноса протона в имидазоле.//Журн. структ. хим. 2007, 674-685].
Спектр ЯМР 13С (δ, м.д.) 56.5, 56.9, 57.0 (-CH2-OH); 101.4, 103.8, 105.2 (С=N(O)O); 125.3, 128.2, 128.9 (=C-N=C, =C-NH-C); 137.4, 141.5 (C=NO); 156.9, 157.1 (С-CH2-). Низкая интенсивность, а также уширение сигналов в спектрах ЯМР 13С С-гидроксиметилимидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксана приводит к уменьшению количества сигналов ароматических атомов углерода.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения N-цианметилимидазо[4,5-e]бензо[1,2-c;3,4-c']дифуроксана | 2019 |
|
RU2707296C1 |
| Способ получения N-карбэтоксиметил-С-метилимидазо[4,5-e]бензо[1,2-c;3,4-c']дифуроксана | 2020 |
|
RU2725631C1 |
| Способ получения N-аллилимидазо[4,5-e]бензо[1,2-c;3,4-c']дифуроксана | 2019 |
|
RU2718905C1 |
| Способ получения C-нитроимидазо[4,5-e]бензо[1,2-c;3,4-c']дифуроксана | 2018 |
|
RU2675159C1 |
| Способ получения C-нитроимидазо[4,5-e]бензо[1,2-c;3,4-c']дифуроксана | 2019 |
|
RU2700931C1 |
| Способ получения N-карбэтоксиметилимидазо[4,5-e]бензо[1,2-c;3,4-c′]дифуроксана | 2017 |
|
RU2663846C1 |
| N-КАРБОКСИМЕТИЛИМИДАЗО[4,5-е]БЕНЗО[1,2-с;3,4-с']ДИФУРОКСАН | 2014 |
|
RU2544547C1 |
| Способ получения N-карбэтоксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с']дифуроксана | 2016 |
|
RU2618230C1 |
| N-КАРБ(ГЛУТАМИНИЛ)ОКСИМЕТИЛИМИДАЗО[4,5-Е]БЕНЗО[1,2-С;3,4-С']ДИФУРОКСАН, ИНГИБИРУЮЩИЙ АГРЕГАЦИЮ ТРОМБОЦИТОВ | 2012 |
|
RU2502739C9 |
| N-КАРБ(АРГИНИЛ)ОКСИМЕТИЛИМИДАЗО[4,5-е]БЕНЗО[1,2-с;3,4-с']ДИФУРОКСАН, ИНГИБИРУЮЩИЙ АГРЕГАЦИЮ ТРОМБОЦИТОВ | 2014 |
|
RU2549355C1 |
Изобретение относится к области органической химии, а именно к способу получения С-гидроксиметилимидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксана конденсацией 3,5-дибромфенилендиамина-1,2 с гликолевой кислотой, нитрованием 2-гидроксиметил-4,6-дибромбензимидазола смесью серной и азотной кислот, азидированием 2-гидроксиметил-4,6-дибром-5,7-динитробензимидазола и термоциклизацией 2-гидроксиметил-4,6-диазидо-5,7-динитробензимидазола. Технический результат - разработан способ получения нового соединения, которое может найти применение в медицине в качестве средства, ингибирующего агрегацию тромбоцитов. 3 пр.
Способ получения С-гидроксиметилимидазо[4,5-e]бензо[1,2-c;3,4-c’]дифуроксана конденсацией 3,5-дибромфенилендиамина-1,2 с гликолевой кислотой, нитрованием 2-гидроксиметил-4,6-дибромбензимидазола смесью серной и азотной кислот, азидированием 2-гидроксиметил-4,6-дибром-5,7-динитробензимидазола и термоциклизацией 2-гидроксиметил-4,6-диазидо-5,7-динитробензимидазола.
| КОРОЛЕВ В.Л | |||
| и др., Изв | |||
| А | |||
| Н | |||
| Серия хим | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Фрикционная передача | 1923 |
|
SU1250A1 |
| N-КАРБОКСИМЕТИЛИМИДАЗО[4,5-е]БЕНЗО[1,2-с;3,4-с']ДИФУРОКСАН | 2014 |
|
RU2544547C1 |
| US 7145016 B1, 05.12.2006 | |||
| RU 2002134671 A, 27.06.2004. | |||
Авторы
Даты
2019-06-26—Публикация
2019-03-31—Подача