Изобретение относится к области органической химии, а именно к разработке нового способа получения промежуточного продукта при синтезе ряда биологически активных соединений.
N-карбэтоксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксан-промежуточный продукт при синтезе ряда биологически активных соединений [В.П. Ившин, В.В. Топоров, В.Л. Королев, А.В. Корманов, Состояние исследований и современные достижения в химии органических соединений - NO-доноров, МАТЕРИАЛЫ ПЯТОЙ МЕЖДУНАРОДНОЙ НАУЧНОЙ ШКОЛЫ «НАУКА И ИННОВАЦИИ - 2010», ISS "SI-2010": Материалы пятого международного научного семинара «Фундаментальные исследования и инновации» и Всероссийского молодежного научного семинара «Наука и инновации 2010», Йошкар-Ола, 18-24 июля 2010 г., с. 396-402].
Кроме того, из N-карбэтоксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксана синтезируют N-карбоксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксан [Патент RU №2544547, 2014 г.],
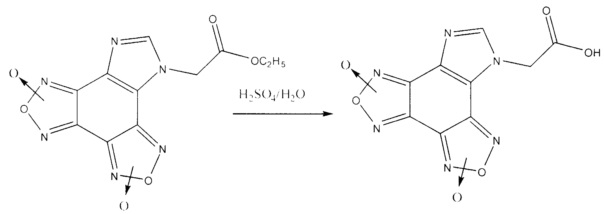
из которого, в свою очередь получают, ряд доз-зависимых ингибиторов агрегации тромбоцитов: N-карб(глутаминил)оксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксан [Патент RU №2502739, 2012 г.], N-карб(аргинил)оксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксан [Патент RU №2549355, 2014 г.], гетеромерные пептиды на основе имидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксана [Патент RU №2550223 2014 г.; Разработка новых антиагрегационных гетеромерных пептидов с имидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксановым фрагментом / А.А. Алексеев, М.И. Брылев, В.Л. Королев, Д.С. Лоторев, А.Ю. Лизунов, Л.А. Павлова, В.П. Ившин, О.Ю. Домашева // Бутлеровские сообщения. - 2014. - Т. 38. №4. - С. 16-19].
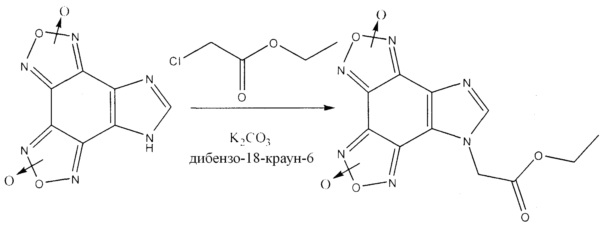
Известен способ получения N-карбэтоксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксана [В.П. Ившин, В.В. Топоров, В.Л. Королев, А.В. Корманов, Состояние исследований и современные достижения в химии органических соединений - NO-доноров, МАТЕРИАЛЫ ПЯТОЙ МЕЖДУНАРОДНОЙ НАУЧНОЙ ШКОЛЫ «НАУКА И ИННОВАЦИИ - 2010», ISS "SI-2010": Материалы пятого международного научного семинара «Фундаментальные исследования и инновации» и Всероссийского молодежного научного семинара «Наука и инновации 2010», Йошкар-Ола, 18-24 июля 2010 г., с.396-402; В.В. Топоров, В.Л. Королев, В.П. Ившин, В.М. Даниленко. Исследование поведения имидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксанов в реакциях нитрования, алкилирования и кислотного гидролиза. // Тез. докл. XVIII Менделеевского съезда по общей и прикладной химии, Москва, 23-28 сентября, 2007, 462]с выходом 47% алкилированием имидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксана этиловым эфиром хлоруксусной кислоты в условиях межфазного катализа (среда: ацетон, триэтиламин, диметилсульфоксид; гетерогенная фаза: карбонат калия; катализатор: дибензо-18-краун-6) и выделением продукта известными способами.
Задачей предлагаемого изобретения является повышение выхода целевого продукта.
Поставленная задача решается способом получения N-карбэтоксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с’] дифуроксана, отличающимся тем, что алкилирование имидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксана проводят этиловым эфиром бромуксусной кислоты.
Способ осуществляют в условиях межфазного катализа (среда: ацетон, триэтиламин, диметилсульфоксид; гетерогенная фаза: карбонат калия; катализатор: дибензо-18-краун-6) с выделением продукта известными способами. Выход продукта составляет 84%.
Предлагаемый способ позволяет повысить выход целевого продукта на 37%.
Предлагаемый способ получения N-карбэтоксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксана иллюстрируется следующим примером.
Пример. К 0,80 г (3,42 ммоль) имидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксана в 40 мл ацетона при перемешивании добавляли 0,16 мл триэтиламина, 1,00 мл (8,98 ммоль) этилового эфира бромуксусной кислоты, 3,20 мл диметилсульфоксида, 1,60 г (1 1,59 ммоль) карбоната калия и каталитическое количество дибензо-1 8-краун-6. Реакционную смесь перемешивали в течение 12 ч. при 20°C, разбавляли водой до начала выпадения осадка, упаривали при пониженном давлении при комнатной температуре, осадок отфильтровывали, промывали водой, сушили. Получали 0,92 г продукта (выход 84%). т.пл. 170-173°C (C2H5OH). Температура плавления пробы смешения полученного продукта с заведомым образцом, полученным по описанию, приведенному в работе [В.В. Топоров, В.Л. Королев, В.П. Ившин, В.М. Даниленко. Исследование поведения имидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксанов в реакциях нитрования, алкилирования и кислотного гидролиза. // Тез. докл. XVIII Менделеевского съезда по общей и прикладной химии, Москва, 23-28 сентября, 2007, 462] депрессии не дает.
В связи с тем, что данные, подтверждающие строение синтезированного соединения в литературе не представлены, мы дополнительно подтвердили структуру полученного продукта методами физико-химического анализа.
Брутто-состав вещества подтвержден данными элементного анализа. Температура плавления определена на микроскопном столике «Boetius».
Строение синтезированного соединения подтверждено методами ИК-, ЯМР 1Н, 13С- и хромато-масс-спектроскопии.
ИК-спектры регистрировали на приборе «Vector 22» в прессовке KBr. Спектры ЯМР 1Н и 13С записаны на приборе «BrukerAM-300», химические сдвиги измеряли относительно сигнала растворителя (ДМСО-d6, δH 2.5 м.д., δC 39.5 м.д.).
Хромато-масс-спектрометрический анализ проводили на приборе Waters MSD SQD - ESI с УФ- и масс-спектрометрическими детекторами: длина волны 220 нм, температура пробоотборника 15°C, температура термостата колонок 40°C. MSD - параметры: температура источника 130°C, температура газа 400°C, напряжение на капилляре 3 kV; колонка WatersAcquity 1,7 μm 2.1⋅50 mm. Градиент от 5 до 100% В за 4 мин (А: 0.1% муравьиной кислоты в воде; В: 0.1% муравьиной кислоты в ацетонитриле.
Найдено % С 41,12; Н 2,70; N 26,48 C11H8N6O6
Вычислено % С 41,25; Н 2,50; N 26,25
Масс-спектр [MS (ES)] m/z 321 [М+Н]+
ИК (см-1, KBr) 3126, 3003, 1746 и 1726 (vC-=O), 1663, 1649, 1593, 1560, 1409, 1379, 1248, 1061, 1017, 989, 974, 960, 871, 808, 638
ЯМР-спектры приведены для смеси 4-х изомеров в соотношении 0,08:0,4:0,5:1,0 1:0,5:0,4:0,08 (по данным ЯМР 1Н). Спектр ЯМР 1Н (δ, м.д., J/Гц): 1,24 (т, 3H, СН3, 3J=6,99); 4,21 (м, 2Н, СН2); 5,44 с, 5,46 с (2Н, СН2); 8.34 с, 8,37 с, 8,46 с, 8,49 с (1Н, CH). Спектр ЯМР 13С (δ, м.д.) 14,06 (СН3); 48,37, 49,17 (СН2С=O); 61,92, 62,09 (СН2СН3); 101,17, 101,74, 103,45, 103,93, 105,39, 106,59 (C=N(O)O и =CNCH2); (C=N(O)O); 116,89, 119,29, 119,74, 121,80, 127,74; 129,11; 130,30; 131,50 (CN=CH и =CNCH2); 141,46; 141.63; 143,46; 143,66; 144,35; 146,34; 146,52; 147,22 (СН и C=NO); 167,01; 167.92 (С=O).
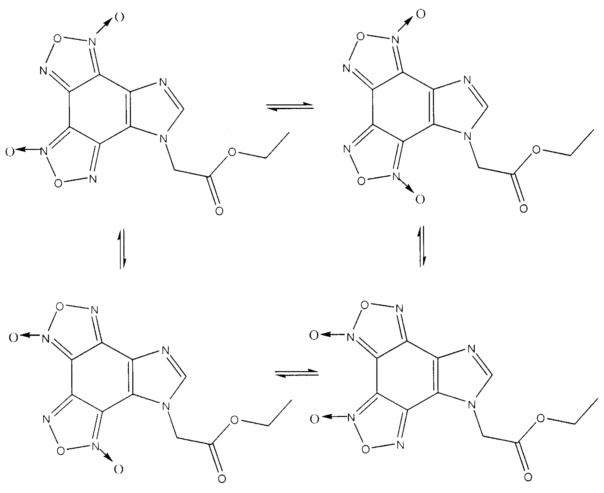
Фуроксановое кольцо в молекуле производных бензофуроксана обладает способностью таутомеризоваться в свою вторую форму, содержащую N-оксидную группу на другой стороне цикла у атома азота [Хмельницкий Л.И., Новиков С.С, Годовикова Т.Н. Химия фуроксанов. Реакции и применение. - М.: Наука. 1983, 311 с.]. Эта изомеризация обратима и в растворах устанавливается равновесие между обоими таутомерами. Для N-карбэтоксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксана теоретически возможно существование четырех таутомерных форм. Их существование в растворе ДМСО-d6 при 36°C подтверждается методом спектроскопии ЯМР 1Н. Сигнал протона имидазольного цикла проявляется в виде четырех синглетов различной интенсивности, соответствующих различным таутомерным формам. Интегральное отношение интенсивности сигналов отвечает мольному соотношению таутомеров в смеси.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения N-карбэтоксиметилимидазо[4,5-e]бензо[1,2-c;3,4-c′]дифуроксана | 2017 |
|
RU2663846C1 |
| Способ получения N-карбэтоксиметил-С-метилимидазо[4,5-e]бензо[1,2-c;3,4-c']дифуроксана | 2020 |
|
RU2725631C1 |
| Способ получения N-аллилимидазо[4,5-e]бензо[1,2-c;3,4-c']дифуроксана | 2019 |
|
RU2718905C1 |
| Способ получения N-цианметилимидазо[4,5-e]бензо[1,2-c;3,4-c']дифуроксана | 2019 |
|
RU2707296C1 |
| Способ получения C-нитроимидазо[4,5-e]бензо[1,2-c;3,4-c']дифуроксана | 2018 |
|
RU2675159C1 |
| Способ получения C-нитроимидазо[4,5-e]бензо[1,2-c;3,4-c']дифуроксана | 2019 |
|
RU2700931C1 |
| N-КАРБОКСИМЕТИЛИМИДАЗО[4,5-е]БЕНЗО[1,2-с;3,4-с']ДИФУРОКСАН | 2014 |
|
RU2544547C1 |
| Способ получения С-гидроксиметилимидазо[4,5-e]бензо[1,2-c;3,4-c']дифуроксана | 2019 |
|
RU2692680C1 |
| ГЕТЕРОМЕРНЫЕ ПЕПТИДЫ НА ОСНОВЕ ИМИДАЗО[4,5-е]БЕНЗО[1,2-с;3,4-с']ДИФУРОКСАНА, ИНГИБИРУЮЩИЕ АГРЕГАЦИЮ ТРОМБОЦИТОВ | 2014 |
|
RU2550223C1 |
| N-КАРБ(ГЛУТАМИНИЛ)ОКСИМЕТИЛИМИДАЗО[4,5-Е]БЕНЗО[1,2-С;3,4-С']ДИФУРОКСАН, ИНГИБИРУЮЩИЙ АГРЕГАЦИЮ ТРОМБОЦИТОВ | 2012 |
|
RU2502739C9 |
Изобретение относится к способу получения N-карбэтоксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксана, отличающемуся тем, что алкилирование имидазо[4,5-е]бензо[1,2-с;3,4-с’]дифуроксана проводят этиловым эфиром бромуксусной кислоты. Технический результат: новый способ позволяет повысить выход целевого продукта.
Способ получения N-карбэтоксиметилимидазо[4,5-е]бензо[1,2-с;3,4-с']дифуроксана, отличающийся тем, что алкилирование имидазо[4,5-е]бензо[1,2-с;3,4-с']дифуроксана проводят этиловым эфиром бромуксусной кислоты.
| N-КАРБОКСИМЕТИЛИМИДАЗО[4,5-е]БЕНЗО[1,2-с;3,4-с']ДИФУРОКСАН | 2014 |
|
RU2544547C1 |
| В.В | |||
| Топоров, В.Л | |||
| Королев, В.П | |||
| Ившин, В.М | |||
| Даниленко | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| // Тез | |||
| докл | |||
| XVIII Менделеевского съезда по общей и прикладной химии, Москва, 23-28 сентября, 2007, 462. | |||
Авторы
Даты
2017-05-03—Публикация
2016-06-02—Подача