Изобретение относится к медицине и касается создания новой противоопухолевой композиции, которая представляет собой комплекс, состоящий из известного фармацевтического препарата цисплатина и ингибитора 6-фосфоглюконатдегидрогеназы (Physcion). Изобретение может быть использовано для производства в последующем лекарственного препарата, который может найти применение в медицине, ветеринарии, биологии, при этом наиболее эффективно может быть использована в области лечения онкологических заболеваний.
На дату подачи заявки в мире существует задача повышения эффективности химической терапии злокачественных новообразований. Недостаточная эффективность терапии обусловлена преимущественно тем, что к большинству используемых в химиотерапии фармацевтических препаратов возникает лекарственная устойчивость (то есть способность сохранять жизнедеятельность, включая размножение, несмотря на контакт с химиопрепаратами) в опухолевых клетках. Одним из таких выявленных заявителем противоопухолевых (снижающий рост и развитие опухолевых клеток) фармацевтических препаратов является широко известный цисплатин, действие которого было открыто Б. Розенбергом в начале 1960-х годов при наблюдении влияния электрического тока на рост бактерий и направлено на нарушение функций ДНК, вызванном химическим повреждением её оснований (Cisplatin in cancer therapy: molecular mechanisms of action, Eur J Pharmacol, 2014) (Цисплатин в терапии рака: молекулярные механизмы действия, Eur J Pharmacol, 2014) [1].
Заявителем проведен анализ существующего уровня техники. Из исследованного заявителем уровня техники выявлено, что одним из наиболее действенных способов для повышения эффективности химической терапии злокачественных образований является создание композиции, состоящей из противоопухолевого фармацевтического препарата и вещества, ингибирующего метаболизм клетки, которая (композиция) способствовала бы увеличению чувствительности (то есть способности реагировать на терапию) опухолевых клеток к химиопрепарату цисплатину.
Цисплатин, являясь хорошо известным по литературным источникам лекарственным средством, обладающий достаточно высокой клинической активностью в отношении таких опухолей, как рак молочной железы, яичников, шейки матки, легких и поджелудочной железы, в свободном состоянии имеет существенный недостаток, связанный с развивающейся к нему у опухолевых клетках устойчивостью и в связи с этим нецелесообразностью продолжения терапии при его использовании по назначению (Cisplatin Resistance: A Cellular Self-Defense Mechanism Resulting from Multiple Epigenetic and Genetic Changes, Pharmacol Rev. 2012) (Устойчивость к цисплатину: клеточный механизм защиты, возникающий в результате множественных эпигенетических и генетических изменений, Pharmacol Rev. 2012) [2].
Далее в выявленном заявителем источнике (Cisplatin in cancer therapy: molecular mechanisms of action, Eur J Pharmacol, 2014) (Цисплатин в терапии рака: молекулярные механизмы действия, Eur J Pharmacol, 2014) [3] описан механизм действия цисплатина, как противоопухолевого средства. Способ действия цисплатина связан с его способностью сшивать пуриновые основания ДНК, тем самым нарушая механизмы репарации (восстановления) ДНК и впоследствии вызывая апоптоз (гибель) в опухолевых клетках.
Заявителем выявлен источник, свидетельствующий, что у большинства опухолевых клеток возникает лекарственная устойчивость к цисплатину (Molecular mechanisms of cisplatin resistance, Oncogene 2012) (Молекулярные механизмы устойчивости к цисплатину, Oncogene. 2012) [4].
Чтобы преодолеть лекарственную устойчивость к цисплатину и повысить эффективность его использования по назначению, его смешивают с другими химиопрепаратами, являющимися цитотоксическими (вызывающими некроз больных и здоровых клеток, то есть массовый патологический процесс, выражающийся в местной гибели ткани в живом организме в результате какого-либо экзо- или эндогенного её повреждения) и цитостатическими (вызывающими апоптоз, то есть не патологическую гибель больных и здоровых клеток) (Classical chemotherapy: mechanisms, toxicities and the therapeutic window. Cancer Biol.Ther. 2003) (Классическая химиотерапия: механизмы, токсичность и терапевтическое окно. Cancer Biol.Ther. 2003) [5].
Из исследованного уровня техники заявителем выявлен источник (Effective combination chemotherapy with paclitaxel and cisplatin with or without human granulocyte colony-stimulating factor and/or erythropoietin in patients with advanced gastric cancer, Br J Cancer. 2002) (Эффективная комбинированная химиотерапия с паклитакселом и цисплатином с или без колониестимулирующего фактора гранулоцитов человека и / или эритропоэтина у пациентов с распространенным раком желудка, Br J Cancer. 2002) [6].
Сущностью известного технического решения является композиция двух химиопрепаратов цисплатина и паклитаксела, активная для пациентов с поздними стадиями рака желудка. Частота ответа (эффективность) на лечение составляла 44%, включая 11% полных ремиссий, средний интервал без прогрессирования заболевания составлял 7 месяцев и общую выживаемость около 11,2 месяца.
Недостатком известного технического решения является развитие ярко выраженной токсичности в ответ на терапию, включая развитие лейкоцитопении у 39 пациентов (87% исследуемых), достигшей 3 или 4 степени у пяти (11%) и двух (4%) пациентов, нейтропении в 39 случаях (87%), достигшей 3 или 4 степени у 10 (22%) и пяти пациентов (11%) соответственно. При этом у последних пяти пациентов (11%) развилась инфекция, причем одному из них потребовалась госпитализация для внутривенного введения антибиотиков. Анемия наблюдалась у 69% пациентов и достигла 3 степени у двух пациентов (4%). Двадцать два пациента (49%) получали эритропоэтин, потому что их уровень гемоглобина упал ниже 12,0 мг/дл-1 во время химиотерапии, при этом в процессе проведения терапии наблюдались желудочно-кишечные расстройства, которые были наиболее часто встречающейся реакцией на проводимую терапию. Тошнота и рвота возникали у 21 пациента (47%), диарея была отмечена у девяти пациентов (20%), запор возник у пяти пациентов, а стоматит 1 или 2 степени у четырех. У двадцати двух пациентов (49%) развилась периферическая невропатия, в том числе у 6 (13%) были тяжелые симптомы. У двух пациентов (4%) развились анафилактические реакции, несмотря на адекватную премедикацию. Алопеция была отмечена у 30 пациентов (67%), 16 из которых имели полное выпадение волос. Об астении сообщили 19 (42%) пациентов. Временно нарушенные функции печени и почек наблюдались у одного (2%) и 10 (22%) пациентов соответственно. Лечение было прекращено преждевременно у двух пациентов из-за анафилаксии, у четырех пациентов из-за периферической невропатии 3-й степени (после шести-десяти курсов лечения), в одном случае из-за интеркуррентного кровотечения в верхнем отделе желудочно-кишечного тракта.
Из исследованного уровня техники заявителем выявлен источник (Epirubicin, Cisplatin, 5-FU combination chemotherapy in sorafenib-refractory metastatic hepatocellular carcinoma, World J Gastroenterol. 2014) (Эпирубицин, Цисплатин, комбинированная химиотерапия 5-FU при метастатической гепатоцеллюлярной карциноме сорафениб, World J Gastroenterol. 2014) [7]. Сущностью известного технического решения является композиция трех химиопрепаратов - цисплатина, эпирубицина и 5-фторурацила, которая показывает умеренную активность у отдельных пациентов с гепатоцеллюлярной карциномой в качестве лечения второй линии (то есть препараты, назначаемые в качестве дополнительного лечения при неэффективности основной схемы терапии). Терапия показала многообещающий клинический результат у отдельных пациентов, даже с прогрессирующей стадией заболевания. Кроме того, все токсические эффекты были управляемыми, и пациенты хорошо переносили режим на протяжении всех циклов лечения.
Недостатком известного технического решения является то, что несмотря на то, что некоторые отобранные пациенты продемонстрировали чувствительность к терапии, общее увеличение выживаемости было минимальным для всех пациентов. К тому же в ответ на терапию наблюдалось развитие нейтропении 3-4 степени у 53,9% пациентов и астении у 26,4% исследуемых.
Из исследованного уровня техники заявителем выявлен источник (Cisplatin and 5-fluorouracil chemotherapy in advanced or recurrent squamous cell carcinoma of the head and neck, Cancer 1987) (Химиотерапия цисплатином и 5-фторурацилом при запущенном или рецидивирующем плоскоклеточном раке головы и шеи, Cancer 1987) [8]. Сущностью известного технического решения является композиция двух химиопрепаратов цисплатина и 5-фторурацила, использование которой приводит к тому, что все исследуемые пациенты с раком головы и шеи, кроме одного, показали явные признаки опухолевого ответа (эффективность лечения) даже после начального цикла химиотерапии.
Недостатком известного технического решения является то, что безрецидивная (отсутствие повторного проявления заболевания) выживаемость была низкой: только 5 из 26 пациентов в группе остались живы и не имели заболеваний от 8 до 28 месяцев после начальной терапии.
Из исследованного уровня техники заявителем выявлен источник (Combination of Gemcitabine and Cisplatin as First-Line Therapy in Advanced Non-Small-Cell Lung Cancer, Cancer Res Treat. 2004) (Комбинация гемцитабина и цисплатина в качестве терапии первой линии при распространенном немелкоклеточном раке легкого, Cancer Res Treat. 2004) [9].
Сущностью известного технического решения является композиция двух химиопрепаратов цисплатина и гемцитабина, которая показывает высокую частоту ответа пациентов (эффективность) с карциномой легкого, равную 53,6%, а у 9,7% пациентов была достигнута стабилизация.
Недостатком известного технического решения является то, что появлялись побочные токсичные реакции в организме в ответ на терапию, которые заключаются в развитии тромбоцитопении у 55,2% исследуемых и анемии у 46,6%. Наиболее распространенными негематологическими (не связанный с клетками крови) токсическими эффектами были усталость (42,4%) и невропатия (25,2%). Неожиданно наблюдался зуд в 5,1% исследованной группы.
Сравнение эффективности использования известных комбинаций с монотерапией (терапией одним препаратом) цисплатином показало достоверное увеличение чувствительности опухолей к терапии. Однако указанные выше недостатки ограничивают более широкое применение цисплатина в виде композиции с другими химиопрепаратами в клинической практике.
Учитывая вышеизложенное, представляется возможным сделать вывод, о том, что на дату представления настоящих заявочных материалов в указанной области техники существует насущная необходимость разработки новых наиболее эффективных композиций цисплатина с другими типами препаратов, а именно молекулярно-нацеленными (таргетными) препаратами, то есть препаратами, оказывающими минимальные побочные токсичные эффекты (An overview of targeted cancer therapy. Biomedicine (Taipei).2015) (Обзор таргетной терапии рака. Биомедицина (Тайбэй). 2015) [10].
На дату подачу заявки заявителем выявлены технические решения, направленные на поиск альтернативных препаратов для композиции с применением (использованием) цисплатина.
Заявителем из существующего уровня техники выявлен источник (Combined cisplatin and aurora inhibitor treatment increase neuroblastoma cell death but surviving cells overproduce BDNF, Biol Open. 2016) (Комбинированное лечение ингибиторами цисплатина и Авроры увеличивает гибель клеток нейробластомы, но выжившие клетки перепроизводят BDNF, Biol Open. 2016) [11], в котором описано, что ингибитор мозгового нейротрофического фактора (BDNF) в комбинации с цисплатином увеличивает чувствительность клеток нейробластомы к цисплатину.
Сущностью препарата является композиция, содержащая химиопрепарат цисплатин и ингибитор Aurora, блокирующий мозговой нейротрофический фактор (BDNF), который является одним из маркёров (то есть специфической молекулой) лекарственной устойчивости опухолевых клеток к цисплатину, поскольку концентрация BDNF резко увеличивается при монотерапии цисплатином. Показано, что выживаемость клеток нейробластомы после 24-часовой обработки цисплатином составляла 43 и 22% после обработки с помощью композиции ингибитора Aurora + цисплатин, тогда как ингибитор Aurora оказался менее эффективным.
Недостатком известного технического решения является то, что комбинированное лечение вызывало парадоксальное увеличение нейротрофического фактора (BDNF) в выживших клетках нейробластомы, в результате чего клетки становились менее чувствительными к терапии с цисплатином.
В связи с этим представляется возможность сделать логический вывод, о том, что комбинированное лечение цисплатином и ингибитором Aurora увеличивает гибель клеток нейробластомы и при этом одновременно индуцирует перепроизводство BDNF в выживших клетках по неизвестному для разработчиков описанной комбинации механизму.
Заявителем также выявлен источник (BI2536, a potent and selective inhibitor of polo-like kinase 1, in combination with cisplatin exerts synergistic effects on gastric cancer cells) (BI2536, мощный и селективный ингибитор киназы 1 в сочетании с цисплатином оказывает синергетическое действие на клетки рака желудка) [12], в котором описывается повышение противоопухолевой эффективности цисплатина в комбинации с ингибитором BI2536.
Сущностью известного технического решения является композиция, содержащая химиопрепарат цисплатин и ингибитор киназы PLK1 (BI2536). PLK1 был идентифицирован как мишень, которая обладает способностью повышать чувствительность клеток рака желудка к традиционным химиотерапевтическим препаратам при лечении рака (A fine-needle aspirate-based vulnerability assay identifies polo-like kinase 1 as a mediator of gemcitabine resistance in pancreatic cancer. Mol Cancer Ther. 2010) (Анализ чувствительности к аспирату определяет, что киназа 1 является медиатором устойчивости к гемцитабину при раке поджелудочной железы. Mol Cancer Ther. 2010) [13].
В известном техническом решении показано, что BI2536 усиливает индуцированное цисплатином ингибирующее (подавляющее) действие на жизнеспособность (способность расти и размножаться) и инвазию клеток рака желудка, что может обеспечить более широкую перспективу улучшения химиотерапевтической чувствительности раковых клеток к цисплатину.
Недостатком известного технического решения является то, что у известного ингибитора (BI2536) отсутствует противоопухолевый эффект, что ограничивает клиническое применение ингибитора BI2536 в терапии.
Заявителем также выявлено изобретение по патенту № 2196604 «Полипептид, являющийся аналогом рецепторсвязывающего фрагмента эпидермального фактора роста с 21-й по 31-ю аминокислоту, его конъюгат с доксорубицином и фармацевтическая композиция на его основе», сущностью которого является фармацевтическая композиция, обладающая противоопухолевым действием, содержащая конъюгат доксорубицина с векторной молекулой в эффективном количестве и подходящий для внутривенного введения фармацевтический носитель, отличающаяся тем, что в качестве конъюгата доксорубицина она содержит его конъюгат с полипептидом формулы MYIEALDSYAC.
Недостатком известного технического решения является то, что в случае нековалентной иммобилизации доксорубицина с пептидными фрагментами эпидермального фактора роста нет гарантии его целенаправленной доставки к опухолевым клеткам-мишеням, чем повышается неспецифическая токсичность препарата.
Заявителем также выявлено изобретение по патенту № PH12018501339 «Комбинированная терапия».
Сущностью известного технического решения является комбинация лекарственных препаратов гемцитабин- [фенилбензокси-L-аланинил)] фосфата (химическое название: 2'-дезокси-2 ', 2'-дифтор-D-цитидин-5'-O- [фенил ( бензокси-L-аланинил)] фосфат) (NUC-1031) и противоракового агента на основе платины, выбранный из цисплатина, пикоплатина, липоплатина и триплатина. Известные комбинации эффективны при лечении рака желчных путей и мочевого пузыря.
Таким образом, основываясь на исследованном уровне техники, представляется возможным сделать логический вывод о том, что в мире существует насущная необходимость в разработках новых композиций цисплатина с молекулярно-нацеленными противоопухолевыми нетоксичными препаратами, итогом которых было бы повышение чувствительности опухолевых клеток к химиопрепарату цисплатин и снижение их (опухолевых клеток) жизнеспособности.
Заявителем выявлен патент № US2016017432 «Фармацевтическая композиция для лечения рака мочевого пузыря, содержащая ингибиторы s100a9 и EGFR и цисплатин, как активные ингредиенты».
Сущностью известного технического решения является способ прогнозирования вероятности рецидива или метастазирования рака мочевого пузыря (MIBC). В соответствии с настоящим изобретением можно точно прогнозировать исход после химиотерапии у пациента с MIBC, предоставлять информацию о чувствительности к цисплатину у пациента с MIBC и повышать чувствительность к цисплатину путем одновременного введения ингибиторов S100A9 и EGFR вместе с обычным цисплатином.
Заявителем выявлен патент № RU 2295517 «Производные дикарбоновых кислот, ингибиторы метастазов и средства, повышающие химиотерапевтическую активность противоопухолевых препаратов, способ усиления эффективности цитостатиков, способ ингибирования процесса метастазирования».
Сущностью известного технического решения состоит в применении дикарбоновых кислот в качестве ингибиторов метастазов и средств, повышающих химиотерапевтическую активность противоопухолевых препаратов. Изобретение относится к способу усиления эффективности цитостатиков в цитостатической химиотерапии опухолей. Способ осуществляют за счет воздействия на опухоль комбинацией известного цитостатика и производных дикарбоновых кислот. Технический результат - усиление противоопухолевой и антиметастатической активности известных цитостатиков за счет применения производных дикарбоновых кислот.
Наиболее подходящим кандидатом для разработки новых композиций цисплатина с новым таргетным препаратом, по мнению заявителя, является ингибитор 6-фосфоглюконатдегидрогеназы (Physcion) окислительного пентозофосфатного клеточного пути. Ингибитор Physcion (C16H12O5, 1,8-дигидрокси-3-метокси-6-метилантрахинон, эмодин-3-метиловый эфир) является органическим гидрофобным (водоотталкивающим) соединением и представляет собой жёлтый порошок, полученный из коркового пигмента лишайников в роду Caloplaca (Effects of chrysophanol, parietin, and nepodin of Rumex crispus on barley and cucumber powdery mildews. Crop Protection, 2004) (Влияние хризофанола, париетина и неподина Rumex crispus на мучнистые росы ячменя и огурца. Crop Protection, 2004) [14].
Преимуществом ингибитора Physcion, по сравнению с приведенными выше аналогами, является наличие собственной противоопухолевой активности. При этом заявителем выявлен источник констатирующий наличие собственной противоопухолевой активности ингибитора Physcion (6-phosphogluconate dehydrogenase links oxidative PPP, lipogenesis and tumor growth by inhibiting LKB1-AMPK signaling, Nat Cell Biol. 2015) (6-фосфоглюконатдегидрогеназа связывает окислительный PPP, липогенез и рост опухоли путем ингибирования передачи сигналов LKB1-AMPK, Nat Cell Biol. 2015) [15].
Сущностью известного технического решения является то, что окислительный пентозофосфатный путь (ПФП) способствует росту опухоли, и было обнаружено, что подавление третьего фермента пентозофосфатного пути, 6-фосфоглюконатдегидрогеназы, ингибитором Physcion снижает пролиферацию (размножение) клеток и рост опухолей.
Кроме того показано, что снижение пролиферации и роста опухолей у ксенотрансплантатов (то есть трансплантат из живой ткани, который берется у животных одного вида и пересаживается представителям другого вида) голых мышей под действием ингибитора Physcion происходит без явной токсичности. Однако в силу гидрофобности препарата Physcion есть проблема подбора оптимального, наименее токсичного для опухолевых клеток, растворителя ингибитора. При этом в понятие гидрофобность (от греч. hydor-вода и phobos-боязнь, страх) входит физическое свойство молекулы, или отдельного ее участка, который стремится избежать контакта с водой. Сама молекула в этом случае называется гидрофобной. Гидрофобные молекулы не поляризованы и не способны образовывать водородные связи, поэтому вода отталкивает такие молекулы, предпочитая образовывать связи внутри себя, т.е. с гидрофильными молекулами.
Из исследованного уровня техники заявителем выявлено, что механизм действия ингибитора Physcion на опухолевые клетки основан на его способности селективно ингибировать ключевой фермент пентозофосфатного пути, 6-фосфоглюконатдегидрогеназу, тем самым снижая липогенез и биосинтез РНК в опухолевых клетках и повышая в них уровень активных форм кислорода (АФК), что ведёт к ослаблению пролиферации клеток и рост опухолей, что приводит к серьезным перестройкам в клеточном метаболизме клеток, и в конечном итоге к программируемой гибели клетки (апоптозу) (6-phosphogluconate dehydrogenase links oxidative PPP, lipogenesis and tumor growth by inhibiting LKB1-AMPK signaling, Nat Cell Biol. 2015) (6-фосфоглюконатдегидрогеназа связывает окислительный PPP, липогенез и рост опухоли путем ингибирования передачи сигналов LKB1-AMPK, Nat Cell Biol. 2015) [15].
Из исследованного уровня техники заявителем выявлен источник (Идентификация новых молекулярно-биологических маркеров чувствительности к цисплатину среди эволюционно консервативных генов, Гапонова А.В., 2017) [16].
Сущностью известного технического решения является то, что ген PGD, который кодирует фермент 6-фосфоглюконатдегидрогеназу пентозофосфатного клеточного пути, вносит вклад в регуляцию чувствительности клеток к цисплатину.
Наиболее близким по сущности к заявленному техническому решению, выбранным заявителем в качестве прототипа, является композиция, описанная в статье (Inhibition of 6-phosphogluconate Dehydrogenase Reverses Cisplatin Resistance in Ovarian and Lung Cancer, Front Pharmacol. 2017) (Ингибирование 6-фосфоглюконатдегидрогеназы обращает резистентность к цисплатину при раке яичников и легких, Front Pharmacol. 2017) [17]. Сущностью известного технического решения является фармацевтическая композиция, содержащая препарат цисплатин с ингибитором Physcion, обладающая противоопухолевым действием и повышающая чувствительность клеточных линий рака легкого и яичников к цисплатину.
Недостатком известного технического решения является то, что не выполнен тест на жизнеспособность клеточных линий рака легкого и яичников под действием композиции цисплатина с ингибитором Physcion, не описаны действующие концентрации компонентов композиции. Также не охарактеризован используемый в эксперименте растворитель для ингибитора Physcion, в связи с чем не представляется возможным сделать однозначный вывод о цитотоксическом действии растворённого ингибитора.
Таким образом, анализ исследованного уровня техники позволяет сделать логический вывод о том, что ингибитор Physcion обладает собственной противоопухолевой активностью, не является токсичным для организма, что делает его (ингибитор Physcion) наиболее подходящим кандидатом для использования в композиции с цисплатином для повышения чувствительности опухолевых клеток к терапии.
При этом следует отметить, что заявителем не выявлены технические решения, обладающие совокупностью существенных признаков заявленного технического решения, обеспечивающих достижение заявленных технических результатов, а именно - направленных на получение композиции ингибитора Physcion и цисплатина, обладающей противоопухолевым действием на жизнеспособность клеточных линий рака легких и поджелудочной железы к цисплатину, с использованием нейтрального растворителя ингибитора Physcion, без применения дополнительного сложного дорогостоящего оборудования.
При этом заявителем из исследованного на дату представления заявочных материалов уровня техники не выявлены технические решения, совпадающие с совокупностью признаков, приведенных в независимом пункте формулы заявленного изобретения, что подтверждает соответствие заявленного технического решения условию патентоспособности «новизна».
Кроме того, заявленное техническое решение позволяет одновременно разрешить казалось бы неразрешимые на дату подачи заявки противоречия, а именно:
- обеспечить получение заявленной композиции с высокой эффективностью в отношении опухолевых клеток;
- исключить использование токсичных компонентов на всех этапах формирования заявленной композиции;
- исключить использование дополнительного сложного дорогостоящего оборудования.
Основываясь на изложенном, представляется возможным сделать вывод о том, что заявленное техническое решение соответствует условию патентоспособности «изобретательский уровень», предъявляемому к изобретениям, так как достигнутые технические результаты не являются очевидными для специалиста в данной области техники.
Задачей заявленного технического решения является устранение недостатков прототипа, а именно - разработка композиции цисплатина с ингибитором Physcion, разбавленном в нейтральном для опухолевых клеток растворителе с эффективной противоопухолевой концентрацией компонентов композиции (цисплатина и ингибитора Physcion).
Техническим результатом заявленного технического решения является противоопухолевая композиция цисплатина с ингибитором Physcion, растворённым в нейтральном для опухолевых клеток растворителе этилацетате, не содержащая токсичных компонентов на всех этапах ее формирования и без использования дополнительного сложного дорогостоящего оборудования, что обеспечивает реализацию поставленных задач.
Сущностью заявленного технического решения является противоопухолевая композиция, состоящая из цисплатина и ингибитора 6-фосфоглюконатдегидрогеназы Physcion, характеризующаяся тем, что дополнительно содержит растворитель этилацетат в соотношениях:
- цисплатин 1-128 мкМ : Physcion 25 мкМ : этилацетат 0,5%,
- цисплатин 1-128 мкМ : Physcion 50 мкМ : этилацетат 1%,
- цисплатин 1-128 мкМ : Physcion 150 мкМ : этилацетат 3%,
с обеспечением возможности повышения чувствительности опухолевой клеточной линии карциномы легкого до 2,2 раза и опухолевой клеточной линии рака поджелудочной железы до 1,6 раза по сравнению с монотерапией цисплатином.
Заявленное техническое решение иллюстрируется Фиг. 1 - Фиг. 3.
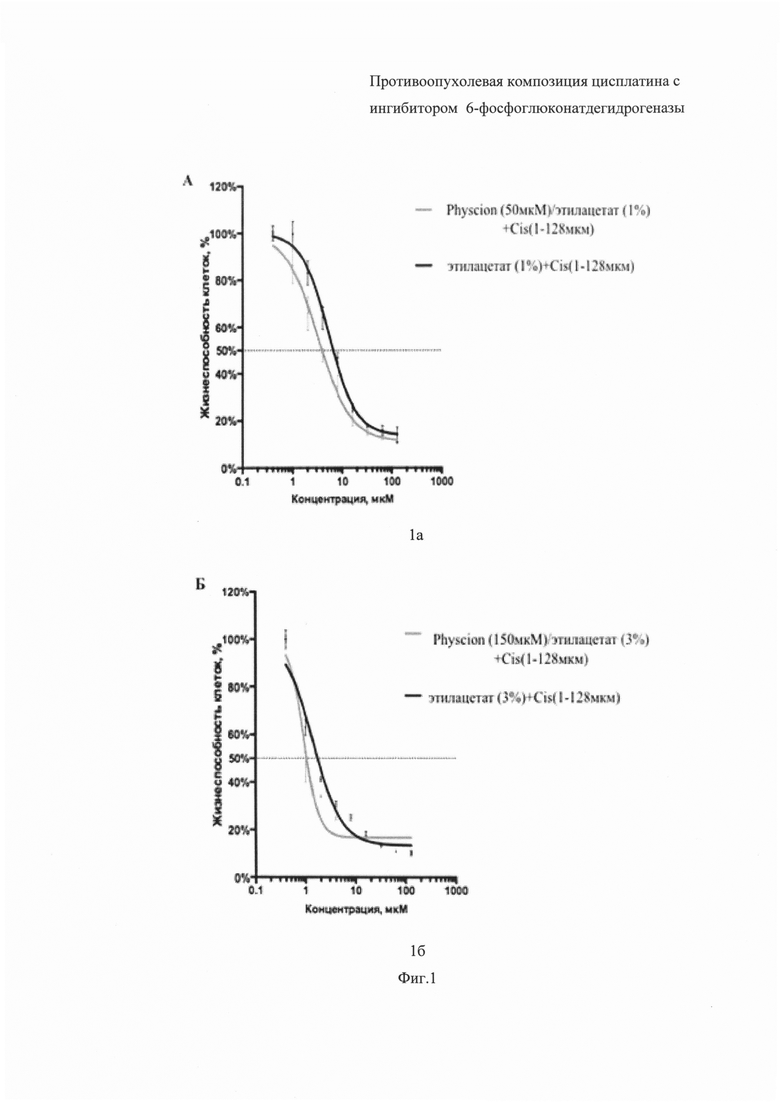
На Фиг. 1 приведены графики, отражающие кривые жизнеспособности (IC50) для клеточной линии рака поджелудочной железы AsPC-1 в эксперименте:
– График 1а:
- для цисплатина (Cis) (1-128 мкМ) в комбинации с Physcion 50 мкМ, растворённом в этилацетате (1%) (зеленая линия),
- для цисплатина (Cis) (1-128 мкМ), растворённом в этилацетате (1%) - без Physcion (черная линия);
– График 1б:
- для цисплатина (Cis) (1-128 мкМ) в комбинации с Physcion 150 мкМ, растворённом в этилацетате (3%) (зеленая линия),
- для цисплатина (Cis) (1-128 мкМ), растворённом в этилацетате (3%) - без Physcion (черная линия).
Из графиков 1а и 1б видно, что при использовании комбинации препаратов цисплатин (Cis) при концентрации (1-128 мкМ) и ингибитора Physcion при концентрациях 50 мкМ и 150 мкМ соответственно (зеленая линия) наблюдается значительное повышение противоопухолевого эффекта заявленной композиции, которое выражается в уменьшении значений IC50 от 6.541 мкМ до 3.901 мкМ и от 1.733 мкМ до 1.051 мкМ соответственно для клеточной линии рака поджелудочной железы AsPC-1 по сравнению с монотерапией цисплатином (черная линия). Это видно из того, что зеленая линия на кривых 1а и 1б смещена влево относительно черной линии, что говорит об уменьшении жизнеспособности клеточной линии AsPC-1 под действием заявленной комбинации цисплатин - Physcion.
Кроме того, также показано отсутствие влияния растворителя этилацетата при действии комбинации цисплатин - Physcion (черная линия), так как она (черная линия) не пересекается с зеленой линией.
При этом следует акцентировать внимание на том, что экспериментально выявлено, что комбинации, содержащие цисплатин (Cis) (1-128 мкМ)/ингибитор Physcion 50 мкМ/этилацетат 1% и цисплатин (Cis) (1-128 мкМ)/ингибитор Physcion 150 мкМ/этилацетат 3% соответственно, являются оптимальными при терапии клеточной линии рака поджелудочной железы AsPC-1. Концентрация менее Physcion 50 мкМ/этилацетат 1% не показала противоопухолевого эффекта, а концентрации выше Physcion 150 мкМ/ этилацетат 3% в эксперименте оказывали в целом токсическое действие на клеточную линию AsPC-1, что нецелесообразно вследствие того, что эта концентрация способна оказать токсическое воздействии на здоровые ткани.
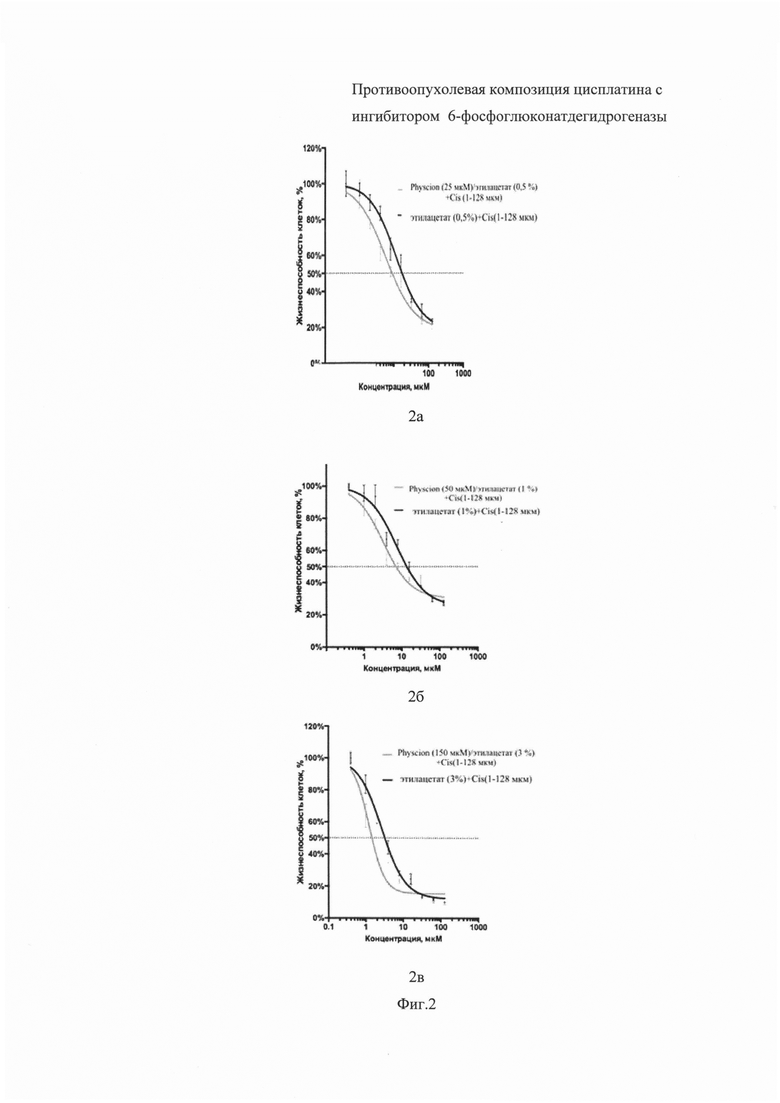
На Фиг. 2 приведены графики, отражающие кривые жизнеспособности (IC50) на клеточной линии карциномы лёгкого Н1299:
– График 2а:
- для цисплатина (Cis) (1-128 мкМ) в комбинации с Physcion 25 мкМ, растворённом в этилацетате (0,5%) (зеленая линия),
- для цисплатина (Cis) (1-128 мкМ), растворённом в этилацетате (0,5%) - без Physcion (черная линия);
– График 2б:
- для цисплатина (Cis) (1-128 мкМ) в комбинации с Physcion 50 мкМ, растворённом в этилацетате (1%) (зеленая линия),
- для цисплатина (Cis) (1-128 мкМ), растворённом в этилацетате (1%) - без Physcion (черная линия);
– График 2в:
- для цисплатина (Cis) (1-128 мкМ) в комбинации с Physcion 150 мкМ, растворённом в этилацетате (3%) (зеленая линия),
- для цисплатина (Cis) (1-128 мкМ), растворённом в этилацетате (3%) - без Physcion (черная линия).
Таким образом экспериментально доказано, что при использовании комбинации препаратов цисплатин (Cis) при концентрации (1-128 мкМ) и ингибитора Physcion при его концентрациях 25 мкМ, 50 мкМ и 150 мкМ (зеленая линия) наблюдается значительное повышение противоопухолевого эффекта, которое выражается в уменьшении значений IC50 от 17.28 мкМ до 8.91 мкМ , от 13.7 мкМ до 7.08 мкМ и от 3.266 мкМ до 1.471 мкМ соответственно для клеточной линии карциномы лёгкого Н1299 по сравнению с монотерапией цисплатином (черная линия). Это видно из того, что зеленая линия на кривых 2а, 2б и 2в смещена влево относительно черной линии, что говорит об уменьшении жизнеспособности клеточной линии Н1299 под действием комбинации цисплатин - Physcion. Кроме того, также показано отсутствие влияния растворителя этилацетата при действии комбинации цисплатин - Physcion (черная линия), так как она (черная линия) не пересекается с зеленой линией.
При этом следует акцентировать внимание на том, что экспериментально выявлено, что комбинации, содержащие цисплатин (Cis) (1-128 мкМ)/ингибитор Physcion 25 мкМ/этилацетат 0.5%, цисплатин (Cis) (1-128 мкМ)/ингибитор Physcion 50 мкМ/этилацетат 1% и цисплатин (Cis) (1-128 мкМ)/ингибитор Physcion 150 мкМ/ этилацетат 3% соответственно являются оптимальными при терапии клеточной линии карциномы лёгкого Н1299. Концентрация менее Physcion 25 мкМ/этилацетат 0.5% не показала противоопухолевого эффекта, а концентрации выше Physcion 150 мкМ/ этилацетат 3% в эксперименте оказывали в целом токсическое действие на клеточную линию Н1299, что нецелесообразно вследствие того, что эта концентрация способна оказать токсическое воздействии на здоровые ткани.
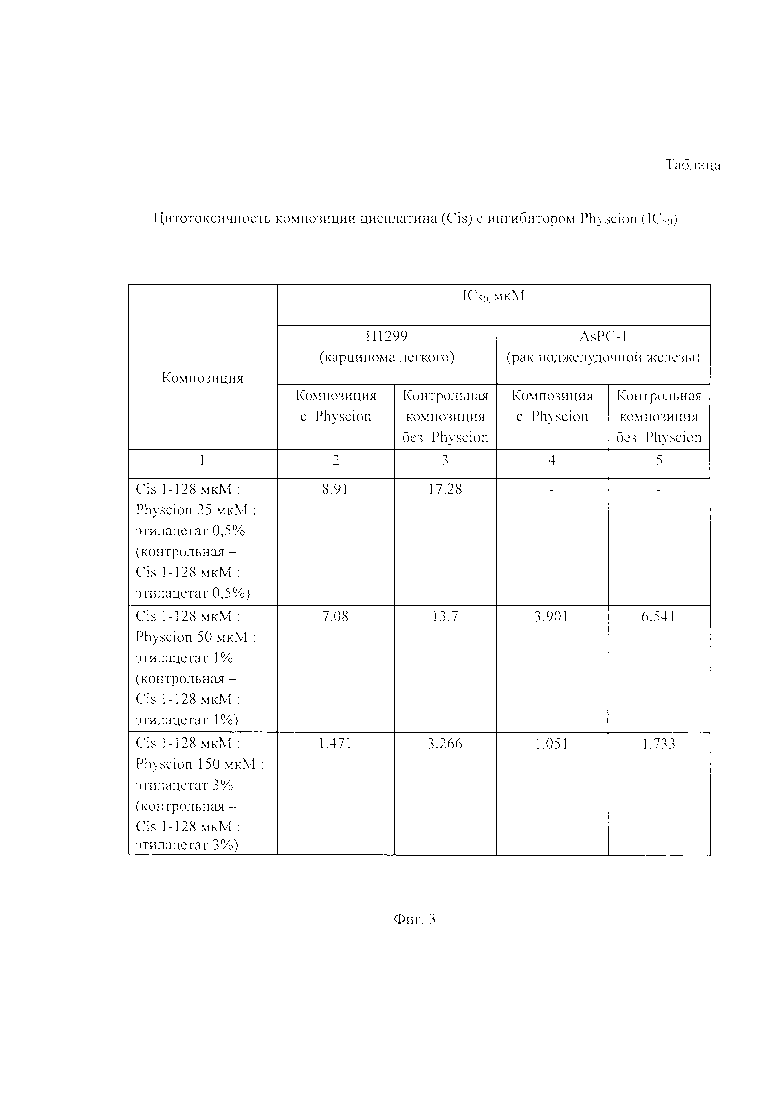
На Фиг.3 представлена сводная Таблица цитотоксичности композиции цисплатина с ингибитором Physcion (IC50), в которой представлены итоговые цифровые показатели, представленные на Фиг.1 и Фиг.2 соответственно.
Таким образом, основываясь на представленной выше информации, представляется возможным сделать логическое умозаключение о том, что при использовании заявленной комбинации препаратов цисплатин и ингибитора Physcion в отношении клеточных линий карциномы лёгкого Н1299 и рака поджелудочной железы AsPC-1, наблюдается снижение значений IC50 комбинации по сравнению с монотерапией цисплатином, что говорит о повышении чувствительности опухолевых клеточных линий Н1299 и AsPC-1 к препарату цисплатин, который, как известно, является базовым препаратом противоопухолевой терапии, что нашло экспериментальное подтверждение заявителем.
Заявленную композицию с применением ингибитора Physcion и химиопрепарата цисплатина получают в последовательности, приведенной ниже, которая указана сначала в целом, а затем более детально в описании примера конкретного выполнения:
- Первая стадия – растворение ингибитора Physcion в растворителе (этилацетат).
- Вторая стадия – приготовление комбинации ингибитора Physcion и цисплатина.
Полученную на второй стадии композицию изучают на цитотоксичность, используя линии опухолевых клеток.
Далее заявителем представлено описание примера конкретной реализации заявленного технического решения более подробно.
Первая стадия – растворение ингибитора Physcion в растворителе (этилацетат).
Этап 1. Разбавление ингибитора Physcion.
Берут навеску 1,4 мг сухого очищенного препарата Physcion («Fresenius Kabi», USA) и растворяют в 1 мл этилацетата в микропробирке типа эппендорф. Растворение проводят путём нагревания ингибитора Physcion при 65-75 °С на водяной бане в течение 30-40 мин до полного растворения вещества, при этом следует акцентировать внимание на том, что указанный диапазон выявлен заявителем в эксперименте и отклонение от указанного температурного диапазона менее 65 °С не приводит к полному растворению препарата Physcion, а нагрев более 75 °С приводит к его более интенсивному испарению, что не желательно.
В результате выполнения указанных действий получают стоковый (начальный) раствор ингибитора Physcion с концентрацией в 5 мМ, который далее разбавляется до меньшей, необходимой экспериментальной концентрации.
В отношении приведенного в Примере 1 режима разбавления ингибитора Physcion следует пояснить, следующее:
- время 30-40 минут является оптимальным, поскольку заявителем экспериментально установлено, что времени менее 30 минут недостаточно для полного растворения ингибитора в растворителе, а более 40 минут процесс вести нецелесообразно, так как композиция полностью формируется в течение указанного времени;
- а температура 65-75 °С является оптимальной, так как заявителем экспериментально установлено, что ниже 65 °С процесс замедляется и ингибитор выпадает в осадок, а выше 75 °С могут начаться деструктивные процессы;
Этап 2. Приготовление раствора ингибитора Physcion в заданных концентрациях.
Из стокового раствора ингибитора Physcion (5 мМ) готовят рабочие концентрации ингибитора (25 мкМ, 50 мкМ и 150 мкМ) путём разбавления стокового раствора в питательной среде RPMI-1640 («Панэко» Россия): для приготовления 25 мкМ, 50 мкМ и 150 мкМ раствора ингибитора стоковый раствор Physcion (5 мМ) разбавляют в питательной среде в соотношении Physcion: RPMI= 1:60, 1:30, 1:9 соответственно.
В результате выполнения указанных операций получают растворы ингибитора Physcion с требуемыми концентрациями 25 мкМ, 50 мкМ и 150 мкМ соответственно.
Вторая стадия - приготовление комбинации ингибитора Physcion и цисплатина.
Этап 3. Приготовление комбинации ингибитора Physcion и цисплатина.
Исходная стоковая концентрация раствора препарата цисплатин («Fresenius Kabi» США) равна 3,3 мМ. Для приготовления комбинации используется диапазон концентраций цисплатина 1-128 мкМ, к каждой из которых добавляют определённую концентрацию ингибитора Physcion (25 мкМ, 50 мкМ или 150 мкМ). Изначально готовят стоковый раствор объёмом 500 мкл, содержащий 128 мкМ цисплатина, необходимую концентрацию Physcion (25 мкМ, 50 мкМ или 150 мкМ) и питательную среду RPMI-1640. Далее стоковую комбинацию разводят в 2 раза, путём отбора 250 мкл стокового раствора и его разбавления в 250 мкл раствора Physcion (25 мкМ, 50 мкМ или 150 мкМ) с питательной средой RPMI-1640, тем самым данная комбинация содержит цисплатин (64 мкМ) и Physcion (25 мкМ, 50 мкМ или 150 мкМ). Далее эту комбинацию, содержащую 64 мкМ цисплатина, по такому же принципу вновь разбавляют в 2 раза, в результате получают комбинацию, содержащую 32 мкМ цисплатина и Physcion (25 мкМ, 50 мкМ или 150 мкМ). Данный процесс повторяют до тех пор, пока концентрация цисплатина в комбинации достигнет 1 мкМ. Готовые комбинации композиции быстро и интенсивно перемешивают в течение 5 мин при температуре плюс 25 - 28 °С и скорости вращения не менее 700 об/мин.
В результате выполнения указанных операций получают целевой продукт - заявленную композицию, состоящую из химиопрепарата цисплатин 1-128 мкМ : Physcion 25 мкМ, цисплатин 1-128 мкМ : Physcion 50 мкМ, цисплатин 1-128 мкМ : Physcion 150 мкМ.
В отношении приведенного в Этапе 3 режима получения заявленной композиции следует пояснить, что:
- время 5 минут является оптимальным, поскольку заявителем экспериментально установлено, что времени менее 5 минут недостаточно для формирования композиции, а более 5 минут процесс вести нецелесообразно, так как композиция полностью формируется в течение указанного времени;
- температура 25-28 °С является оптимальной, так как заявителем экспериментально установлено, что ниже 25 °С процесс замедляется, а выше 28 °С могут начаться деструктивные процессы;
- заявителем экспериментально установлено, что скорость вращения платформы термошейкера должна быть не менее 700 об/мин, поскольку меньшая скорость недостаточна для формирования композиции, а большая не целесообразна.
Этап 4. Исследование цитотоксичности комплексов цисплатина с ингибитором Physcion (IC50) с помощью МТТ-теста, предназначенное для экспериментального подтверждения эффективности использования заявленной композиции при использовании по назначению.
Как было описано ранее, из уровня техники заявителем выявлено, что ингибитор Physcion, использованный в заявленном техническом решении, показал свою безопасность и выраженную противоопухолевую эффективность в экспериментальных исследованиях.
Механизм действия ингибитора Physcion на опухолевые клетки основан на его способности ингибировать фермент 6-фосфоглюконатдегидрогеназу, которая является ключевым ферментом окислительного пентозофосфатного клеточного пути и концентрация которой резко возрастает в опухолевых клетках, что приводит к серьезным метаболическим перестройкам в опухолевой клетке, а именно: снижается липогенез, биосинтез РНК, повышается уровень активных форм кислорода (АФК), что ведёт к ослаблению пролиферации клеток и роста опухолей, и, в конечном итоге, к программируемой гибели опухолевых клеток (апоптозу).
В заявленном техническом решении комплексы цисплатина и ингибитора Physcion исследованы на цитотоксичность с помощью МТТ-теста. Тест на цитотоксичность – один из методов, используемых в лабораторной практике доклинических испытаний фармацевтических субстанций по стандартам GLP (англ. Good Laboratory Practice — Надлежащая лабораторная практика). Национальным аналогом GLP в РФ является стандарт ГОСТ 33044-2014.
Цитотоксичность заявленного комплекса исследована заявителем на двух линиях клеток злокачественных новообразований:
- Н1299 (карцинома легкого);
- AsPC-1 (рак поджелудочной железы).
Для сравнения заявителем исследована цитотоксичность промышленного цисплатина с растворителем ингибитора Physcion – этилацетатом (контрольные композиции).
Реактив МТТ представляет собой тетразолиевый краситель 3-(4,5-диметилтиазол-2-ил)-2,5-дифенил-тетразолиум бромид. Метод основан на том, что дегидрогеназы митохондрий только метаболически активных клеток восстанавливают МТТ в пурпурно-окрашенные кристаллы формазана. Эксперименты проводят, используя культуры клеток Н1299 (карцинома легкого), AsPC-1 (рак поджелудочной железы), полученные из American Type Culture Collection (Manassas, Virginia, USA). Культивируют клетки, используя среду RPMI-1640 («Панэко» Россия) с добавлением 10% FBS (Gibco, USA), 2мM L-глутамина, 10 е.б.а./мл пенициллина и 10 мкг/мл стрептомицина (Панэко). Культивирование клеток производят во влажной атмосфере (5% СО2, 37 °С).
Для определения цитотоксической активности исследуемых композиций клетки пассируют (100 мкл/лунку) в 96-ти луночные планшеты с плотностью 2000 клеток/лунку. В лунки помещают по 30 мкл растворов исследуемых композиций, последовательно увеличивая их концентрацию. Лунки, не содержащие исследуемых препаратов, служат негативным контролем. Инкубацию проводят 72 часа. Для проведения МТТ-теста к культивируемым клеткам добавляют раствор МТТ (Панэко) в концентрации 500 мкг/мл. Затем клетки культивируют еще 3 часа при 37 °С. Полученные кристаллы формазана растворяют в 0,1 мл DMSO (ДМСО, диметилсульфоксида) при встряхивании в течение 10 мин. Далее измеряют оптическую плотность полученных окрашенных растворов на мультискане Tecan Infinite M200 PRO (Tecan Trading AG, Switzerland) при длине волны 555 нм. Все эксперименты проводят трижды, и среднюю величину относительного ингибирования роста клеток высчитывают по формуле:
D=(1-(A-B)/(C-B))x100, где:
A – интенсивность поглощения тестируемых субстанций в заданной концентрации;
B – интенсивность поглощения в лунках, не содержащих клеток;
C – оптическая плотность клеток в отсутствие тестируемых препаратов;
D – относительное ингибирование, %.
Используя зависимость доза/эффект, определяют концентрацию полумаксимального ингибирования IC50 (нМ), которая указывает на концентрацию композиции, при которой выживает 50% клеток.
Таким образом, чем меньше концентрация композиции, при которой выживает 50% клеток (IC50), и, соответственно, 50% клеток гибнет, тем сильнее его токсичное действие, т.е. выше цитотоксичность по отношению к опухолевым клеткам.
Результаты приведены на Фиг. 1, Фиг. 2, Фиг. 3.
На Фиг. 1 (1а, 1б) приведены кривые жизнеспособности (IC50) для клеточной линии рака поджелудочной железы AsPC-1.
Из анализа Фиг.1а (композиция Cis 1-128 мкМ : Physcion 50 мкМ : этилацетат 1%) видно, что для клеточной линии рака поджелудочной железы AsPC-1 средняя концентрация полумаксимального ингибирования (IC50) составила 3.901 мкМ (зеленая линия).
При этом для контрольной композиции без Physcion концентрация полумаксимального ингибирования (IC50) составила 6.541 мкМ (черная линия).
Из указанного следует, что чувствительность клеточной линии рака поджелудочной железы AsPC-1 при воздействии композиции Cis 1-128 мкМ : Physcion 50 мкМ : этилацетат 1% увеличилась в 1.4 раза по сравнению с контрольной композицией без Physcion.
Из анализа Фиг.1б (композиция Cis 1-128 мкМ : Physcion 150 мкМ : этилацетат 3%) видно, что для клеточной линии рака поджелудочной железы AsPC-1 средняя концентрация полумаксимального ингибирования (IC50) составила 1.051 мкМ (зеленая линия).
При этом для контрольной композиции без Physcion концентрация полумаксимального ингибирования (IC50) составила 1.733 мкМ (черная линия), что является доказательством снижения жизнеспособности клеток клеточной линии рака поджелудочной железы AsPC-1.
Из указанного следует, что чувствительность клеточной линии рака поджелудочной железы AsPC-1 при воздействии композиции Cis 1-128 мкМ : Physcion 150 мкМ : этилацетат 3% увеличилась в 1.6 раза по сравнению с контрольной композицией без Physcion.
На Фиг. 2 (2а, 2б, 2в) приведены кривые жизнеспособности (IC50) на клеточной линии карциномы лёгкого Н1299.
Из анализа Фиг.2а (композиция Cis 1-128 мкМ : Physcion 25 мкМ : этилацетат 0,5%) видно, что для клеточной линии карциномы лёгкого Н1299 средняя концентрация полумаксимального ингибирования (IC50) составила 8.91 мкМ (зеленая линия).
При этом для контрольной композиции без Physcion концентрация полумаксимального ингибирования (IC50) составила 17.28 мкМ (черная линия) что является доказательством снижения жизнеспособности клеток клеточной линии карциномы лёгкого Н1299.
Из указанного следует, что чувствительность клеточной линии карциномы лёгкого Н1299 при воздействии композиции Cis 1-128 мкМ : Physcion 25 мкМ : этилацетат 0,5% увеличилась в 1.9 раза по сравнению с контрольной композицией без Physcion.
Из анализа Фиг.2б (композиция Cis 1-128 мкМ : Physcion 50 мкМ : этилацетат 1%) видно, что для клеточной линии карциномы лёгкого Н1299 средняя концентрация полумаксимального ингибирования (IC50) составила 7,08 мкМ (зеленая линия).
При этом для контрольной композиции без Physcion концентрация полумаксимального ингибирования (IC50) составила 13,7 мкМ (черная линия) что является доказательством снижения жизнеспособности клеток клеточной линии карциномы лёгкого Н1299.
Из указанного следует, что чувствительность клеточной линии карциномы лёгкого Н1299 при воздействии композиции Cis 1-128 мкМ : Physcion 50 мкМ : этилацетат 1% увеличилась в 1.9 раза по сравнению с контрольной композицией без Physcion.
Из анализа Фиг.2в (композиция Cis 1-128 мкМ : Physcion 150 мкМ : этилацетат 3%) видно, что для клеточной линии карциномы лёгкого Н1299 средняя концентрация полумаксимального ингибирования (IC50) составила 1.471 мкМ (зеленая линия).
При этом для контрольной композиции без Physcion концентрация полумаксимального ингибирования (IC50) составила 3.266 мкМ (черная линия) что является доказательством снижения жизнеспособности клеток клеточной линии карциномы лёгкого Н1299.
Из указанного следует, что чувствительность клеточной линии карциномы лёгкого Н1299 при воздействии композиции Cis 1-128 мкМ : Physcion 150 мкМ : этилацетат 3% увеличилась в 2,2 раза по сравнению с контрольной композицией без Physcion.
Описанные выше результаты приведены также в сводной Таблице на Фиг. 3:
- в первом столбце приведен перечень исследованных композиций – композиции цисплатина и ингибитора Physcion, приготовленные по Примеру 3, и контрольные композиции цисплатина с растворителем ингибитора Physcion – этилацетатом без Physcion, взятые для сравнения.
- во втором и третьем столбцах приведены данные о цитотоксичности композиций (IC50) в отношении опухолевых клеток Н1299 (карцинома легкого): второй столбец – композиции с Physcion, третий столбец - контрольные композиции без Physcion;
- в четвертом и пятом столбцах приведены данные о цитотоксичности препаратов (IC50) в отношении опухолевых клеток AsPC-1 (рак поджелудочной железы): четвертый столбец – композиции с Physcion, пятый столбец - контрольные композиции без Physcion.
Из представленных в Таблице (Фиг. 3) экспериментальных данных значений IC50 (концентрации, при которой выживает 50% клеток) следует, что композиция цисплатина и ингибитора Physcion повышает чувствительность клеточных линий карциномы легкого Н1299 и рака поджелудочной железы AsPC-1 по сравнению с монотерапией цисплатином.
Эти данные показывают усиление цитотоксичности композиции цисплатина с ингибитором Physcion в отношении опухолевых клеток карциномы легкого Н1299 до 2.2 раза, а в отношении опухолевых клеток рака поджелудочной железы AsPC-1 до 1.6 раза, что является доказательством высокой эффективности использования заявленной композиции по назначению.
Из вышеизложенного представляется возможным сделать логический вывод о том, что в результате проведенных экспериментов заявителем получена композиция цисплатина с ингибитором Physcion, обладающая противоопухолевым эффектом относительно клеточных линий карциномы легкого и рака поджелудочной железы и значительно повышающая чувствительность данных опухолевых клеточных линий к цисплатину по сравнению с монотерапией цисплатином при использовании по назначению.
Метод оценки цитотоксичности (МТТ-тест) выявил разницу цитотоксичности композиций цисплатина с ингибитором Physcion в сравнении с промышленным цисплатином («Fresenius Kabi» США) в отношении опухолевых клеток Н1299 (карцинома легкого) до 2.2 раза, AsPC-1 (рак поджелудочной железы) до 1.6 раза. Полученные данные указывают на эффективность применения заявленного технического решения по назначению в медицине.
Таким образом, заявителем решена поставленная задача и достигнут заявленный технический результат, а именно – сформирована композиция цисплатина с ингибитором Physcion, растворенном в нетоксичном для опухолевых клеток растворителе, не содержащая токсичных компонентов на всех этапах ее формирования, снижающая жизнеспособность опухолевых клеток к цисплатину, которая получена без использования дополнительного сложного дорогостоящего оборудования.
В результате реализации заявленного технического решения представляется возможным сделать общий вывод, что заявителем одновременно решены ряд задач, представленных далее более детально:
- получена новая фармацевтическая композиция цисплатина с таргетным противоопухолевым препаратом Physcion;
- показано усиление токсического воздействия заявленной композиции в отношении опухолевых клеток Н1299 (карцинома легкого) до 2.2 раза, AsPC-1 (рак поджелудочной железы) до 1.6 раза по сравнению с промышленным цисплатином («Fresenius Kabi» США). Это указывает на возможность потенциального применения заявленной композиции для разработки и производства лекарственного препарата, наиболее эффективного против карциномы легкого и рака поджелудочной железы;
- исключено использование токсичных компонентов на всех этапах формирования заявленной композиции;
- исключено использование дополнительного сложного дорогостоящего оборудования.
Заявленное техническое решение соответствует критерию «новизна», предъявляемому к изобретениям, так как из исследованного уровня техники не выявлены технические решения, обладающие заявленной совокупностью отличительных признаков, обеспечивающих достижение заявленных результатов.
Заявленное техническое решение соответствует критерию «изобретательский уровень», предъявляемому к изобретениям, так как заявителем получена, по мнению заявителя, принципиально новая композиция с неизвестными до даты представления заявки концентрациями составляющих компонентов, один из компонентов которого является таргетным противоопухолевым ингибитором, повышающим чувствительность к химиопрепарату цисплатин, что обеспечивает значительное превосходство заявленного технического решения над возможностями известных композиций на дату представления заявленного технического решения.
Заявленное техническое решение соответствует критерию «промышленная применимость», предъявляемому к изобретениям, так как может быть реализовано на любом специализированном предприятии с использованием стандартного оборудования, известных отечественных материалов и технологий.
Использованные источники:
1. Cisplatin in cancer therapy: molecular mechanisms of action, Eur J Pharmacol, 2014. (Цисплатин в терапии рака: молекулярные механизмы действия, Eur J Pharmacol, 2014).
2. Cisplatin Resistance: A Cellular Self-Defense Mechanism Resulting from Multiple Epigenetic and Genetic Changes, Pharmacol Rev. 2012. (Устойчивость к цисплатину: клеточный механизм защиты, возникающий в результате множественных эпигенетических и генетических изменений, Pharmacol Rev. 2012).
3. Cisplatin in cancer therapy: molecular mechanisms of action, Eur J Pharmacol, 2014. (Цисплатин в терапии рака: молекулярные механизмы действия, Eur J Pharmacol, 2014).
4. Molecular mechanisms of cisplatin resistance, Oncogene 2012. (Молекулярные механизмы устойчивости к цисплатину, Oncogene. 2012).
5. Classical chemotherapy: mechanisms, toxicities and the therapeutic window. Cancer Biol.Ther. 2003. (Классическая химиотерапия: механизмы, токсичность и терапевтическое окно. Cancer Biol.Ther. 2003).
6. Effective combination chemotherapy with paclitaxel and cisplatin with or without human granulocyte colony-stimulating factor and/or erythropoietin in patients with advanced gastric cancer, Br J Cancer. 2002. (Эффективная комбинированная химиотерапия с паклитакселом и цисплатином с или без колониестимулирующего фактора гранулоцитов человека и / или эритропоэтина у пациентов с распространенным раком желудка, Br J Cancer. 2002).
7. Epirubicin, Cisplatin, 5-FU combination chemotherapy in sorafenib-refractory metastatic hepatocellular carcinoma, World J Gastroenterol. 2014. (Эпирубицин, Цисплатин, комбинированная химиотерапия 5-FU при метастатической гепатоцеллюлярной карциноме сорафениб, World J Gastroenterol. 2014).
8. Cisplatin and 5-fluorouracil chemotherapy in advanced or recurrent squamous cell carcinoma of the head and neck, Cancer 1987. (Химиотерапия цисплатином и 5-фторурацилом при запущенном или рецидивирующем плоскоклеточном раке головы и шеи, Cancer 1987).
9. Combination of Gemcitabine and Cisplatin as First-Line Therapy in Advanced Non-Small-Cell Lung Cancer, Cancer Res Treat. 2004. (Комбинация гемцитабина и цисплатина в качестве терапии первой линии при распространенном немелкоклеточном раке легкого, Cancer Res Treat. 2004).
10. An overview of targeted cancer therapy. Biomedicine (Taipei).2015. (Обзор таргетной терапии рака. Биомедицина (Тайбэй) .2015).
11. Combined cisplatin and aurora inhibitor treatment increase neuroblastoma cell death but surviving cells overproduce BDNF, Biol Open. 2016. (Комбинированное лечение ингибиторами цисплатина и Авроры увеличивает гибель клеток нейробластомы, но выжившие клетки перепроизводят BDNF, Biol Open. 2016).
12. BI2536, a potent and selective inhibitor of polo-like kinase 1, in combination with cisplatin exerts synergistic effects on gastric cancer cells. (BI2536, мощный и селективный ингибитор киназы 1 в сочетании с цисплатином оказывает синергетическое действие на клетки рака желудка).
13. A fine-needle aspirate-based vulnerability assay identifies polo-like kinase 1 as a mediator of gemcitabine resistance in pancreatic cancer. Mol Cancer Ther. 2010. (Анализ чувствительности к аспирату определяет, что киназа 1 является медиатором устойчивости к гемцитабину при раке поджелудочной железы. Mol Cancer Ther. 2010).
14. Effects of chrysophanol, parietin, and nepodin of Rumex crispus on barley and cucumber powdery mildews. Crop Protection, 2004. (Влияние хризофанола, париетина и неподина Rumex crispus на мучнистые росы ячменя и огурца. Crop Protection, 2004).
15. 6-phosphogluconate dehydrogenase links oxidative PPP, lipogenesis and tumor growth by inhibiting LKB1-AMPK signaling, Nat Cell Biol. 2015. (6-фосфоглюконатдегидрогеназа связывает окислительный PPP, липогенез и рост опухоли путем ингибирования передачи сигналов LKB1-AMPK, Nat Cell Biol. 2015).
16. Идентификация новых молекулярно-биологических маркеров чувствительности к цисплатину среди эволюционно консервативных генов, Гапонова А.В., 2017.
Inhibition of 6-phosphogluconate Dehydrogenase Reverses Cisplatin Resistance in Ovarian and Lung Cancer, Front Pharmacol. 2017 (Ингибирование 6-фосфоглюконатдегидрогеназы обращает резистентность к цисплатину при раке яичников и легких, Front Pharmacol. 2017).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ СОЛИДНЫХ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ МЛЕКОПИТАЮЩИХ | 2024 |
|
RU2841088C2 |
| Натрий-кобальт-полигалактуронат, обладающий противоопухолевой активностью | 2023 |
|
RU2794885C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ХЕМОСЕНСИБИЛИЗАЦИИ ОПУХОЛЕЙ, УСТОЙЧИВЫХ К ПРОТИВОРАКОВЫМ СРЕДСТВАМ | 2007 |
|
RU2396974C2 |
| Применение полиакрилата золота в качестве ингибитора роста клеток меланомы человека | 2018 |
|
RU2708626C1 |
| ПРОТИВОРАКОВАЯ ТЕРАПИЯ, НАПРАВЛЕННАЯ ПРОТИВ РАКОВЫХ СТВОЛОВЫХ КЛЕТОК И ФОРМ РАКА, УСТОЙЧИВЫХ К ЛЕЧЕНИЮ ЛЕКАРСТВЕННЫМИ ПРЕПАРАТАМИ | 2010 |
|
RU2568834C2 |
| 17АЛЬФА-БЕНЗОАТ КОРТЕКСОЛОНА ДЛЯ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ ОПУХОЛЕЙ | 2015 |
|
RU2712752C2 |
| 17A,21-ДИЭФИРЫ КОРТЕКСОЛОНА ДЛЯ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ ОПУХОЛЕЙ | 2015 |
|
RU2712950C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ПРОТИВООПУХОЛЕВЫМ АЛКАЛОИДОМ | 2011 |
|
RU2605335C2 |
| 17A,21-ДИЭФИРЫ КОРТЕКСОЛОНА ДЛЯ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ ОПУХОЛЕЙ | 2015 |
|
RU2821529C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ПРОТИВООПУХОЛЕВЫМ АЛКАЛОИДОМ | 2018 |
|
RU2767664C2 |
Изобретение относится к химико-фармацевтической промышленности и представляет собой противоопухолевую композицию, состоящую из цисплатина и ингибитора 6-фосфоглюконатдегидрогеназы Physcion, отличающуюся тем, что она дополнительно содержит растворитель этилацетат в соотношениях: ицисплатин 1-128 мкМ : Physcion 25 мкМ : этилацетат 0,5%; цисплатин 1-128 мкМ : Physcion 50 мкМ : этилацетат 1%; цисплатин 1-128 мкМ : Physcion 150 мкМ : этилацетат 3%, с обеспечением возможности повышения чувствительности опухолевой клеточной линии карциномы легкого до 2,2 раза и опухолевой клеточной линии рака поджелудочной железы до 1,6 раза по сравнению с монотерапией цисплатином. Изобретение позволяет получить противоопухолевую композицию цисплатина с ингибитором Physcion, растворённым в нейтральном для опухолевых клеток растворителе этилацетате, не содержащую токсичных компонентов на всех этапах ее формирования и без использования дополнительного сложного дорогостоящего оборудования. 3 ил., 1 табл.
Противоопухолевая композиция, состоящая из цисплатина и ингибитора 6-фосфоглюконатдегидрогеназы Physcion, отличающаяся тем, что дополнительно содержит растворитель этилацетат в соотношениях:
- цисплатин 1-128 мкМ : Physcion 25 мкМ : этилацетат 0,5%,
- цисплатин 1-128 мкМ : Physcion 50 мкМ : этилацетат 1%,
- цисплатин 1-128 мкМ : Physcion 150 мкМ : этилацетат 3%,
с обеспечением возможности повышения чувствительности опухолевой клеточной линии карциномы легкого до 2,2 раза и опухолевой клеточной линии рака поджелудочной железы до 1,6 раза по сравнению с монотерапией цисплатином.
Авторы
Даты
2019-07-01—Публикация
2019-03-15—Подача